JP5254202B2 - 粒子の状態を分析するマイクロ流体装置、その作製方法、および分析方法 - Google Patents
粒子の状態を分析するマイクロ流体装置、その作製方法、および分析方法 Download PDFInfo
- Publication number
- JP5254202B2 JP5254202B2 JP2009501390A JP2009501390A JP5254202B2 JP 5254202 B2 JP5254202 B2 JP 5254202B2 JP 2009501390 A JP2009501390 A JP 2009501390A JP 2009501390 A JP2009501390 A JP 2009501390A JP 5254202 B2 JP5254202 B2 JP 5254202B2
- Authority
- JP
- Japan
- Prior art keywords
- opening
- recess
- flow path
- microfluidic device
- base substrate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/48707—Physical analysis of biological material of liquid biological material by electrical means
- G01N33/48728—Investigating individual cells, e.g. by patch clamp, voltage clamp
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Physical Or Chemical Processes And Apparatus (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Automatic Analysis And Handling Materials Therefor (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Micromachines (AREA)
Description
離するため多層整列とボンディングを必要とする。そのようなデバイスの製作は、特に配列が望まれる場合、困難を強いる。更に製作変更は、チップ基板全体が一般的にエッチング除去される必要があるので一層長くなり得る。パッチ開口は、直径が2ミクロン未満であるが、対応するダイアフラムを収容すべく普通1×1mm2のチップ領域がエッチングさ
れなければならない。この要件によって一層低密度の配列になる。
)に延びるパッチ流路を配置することを備えることによって、パッチ開口は、壁の垂直面内に配置される。水平方向パッチ開口手段を提供することによって、流体構造は水平方向に配置可能であり、従って特に試験チャンバ配列を含めるべくデバイスが拡大される場合、流体分配が問題になる垂直組立構造に関連する難点を排除する。
。流路は、第1開口と第2開口、たとえば第1口と第2口を含む。第1開口は、充填部材の第1側壁に配置される。第2開口は、充填部材の第2側壁に配置される。更に第1側壁は、第2側壁に対して対向関係に配置される。第1側壁と第2側壁のうちの少なくとも一部分は、凹部を区画形成する一対の対向側壁に対して少なくとも実質的に垂直である。
成される。流路の周縁壁は、第1開口に隣接する一部分を備える。この部分は、周縁壁のサイズが幅に関して第1開口に向かって減少するように長さ方向に延びる円錐形である。幾つかの実施形態に従ってこの部分は、先端を区画形成する。
に適する。実施形態によっては、各々の外形は、完全に円形である。パッチ・クランプ装置における丸いか円形の開口の利点は、試料生命体のパッチ・クランプがパッチ開口に作用する吸引によって働く場合、高いシール電気抵抗を獲得する可能性である。丸い開口は、約ギガオームのシール抵抗を提供できることが知られている。従って背景のノイズ信号を減らすので一層正確なパッチ・クランプ測定値を取得できるようにする。更に本発明が数ミクロンからミクロン以下のレベル範囲の寸法の開口を製作する能力を提供するので、デバイスは、たとえば細菌、ウイルス、タンパク質およびDNA分子などの細胞以外の多くの種類の生体試料を伴う適用で使用可能である。デバイス製作の観点から狭いエッチングだけが必要とされ、基板を貫通してエッチングしなくてもよいので、平面型パッチ・クランプ法と違って関連する段階が少数のため、簡単な変更になる。従って製作における時間を節約する。当業者には更に、本発明のデバイスが、キャッピング層を用いることによって、マイクロ流体の入口流路と出口流路およびポート、更に大規模平行試験に適した高密度配列を達成する拡張性を含むデバイスの便利なパッケージングを可能にすることは明白であろう。何故なら流路を含むデバイスの壁部分は、小スペースを取るべく形成可能であり、これらの壁部分に形成される流路の外形が、既存の平面型パッチ・クランプにおいて用いられるダイアフラムと違ってリソグラフィによって区画形成され得るからである。
て区画形成される。所望の構成に依存して凹部は、ベース基板の全長/全幅(すなわち一方の縁または、側面から別の縁または側面)におよび得る(たとえば水平方向、対角線上などに)。凹部は更に、ベース基板の1つの縁付近に、あるいは必要であればベース基板の中心付近に位置し得る。そのような凹部の位置は、凹部を含むベース基板の壁部分、一般的には表面に他の物質の蒸着を可能にする。たとえば凹部がベース基板の全面または全長(たとえば末端から末端)に及ぶことが望まれる特定の実施形態において、凹部は、一般的に対向関係にある一対の側壁によって限られる。実施形態によっては凹部の末端は、水平方向開口、たとえば水平方向口である。幾つかの実施形態において凹部は、ベース基板の縁に一端を含み、前記末端は開口を含み得るが、別の末端は、縁と異なるベース基板内の位置で終結する(たとえば中央部分で)。そのような実施形態において凹部は、一対の対向側壁、1つの底壁と、2つの対向側壁を接続する更に別の側壁とによって限られる。前記付加的側壁に対して対向関係に配置され得る凹部の各々の他端は、開口を含むか、開口を区画形成する。実施形態によっては凹部の末端は、ベース基板内に完全に含められる。そのような実施形態において凹部は、二対の対向側壁と1つの底壁を含み得る。幾つかの実施形態において凹部は、2つより多い末端を含む。そのような実施形態において凹部は、一般的に分枝を含む。
部材の2つの側壁に含められ、前記側壁は、互いに対向関係に配置される。用語「対向関係」は、たとえば流路軸など凹部と流路のうちの少なくとも1つを通って流れ得る物質の方向を指す。従って第1開口と第2開口が同じ方を向かない限り、充填部材の2つの側壁は、互いに対して任意の角度で配置され得る。第1側壁と第2側壁は、たとえば互いに対して0°よりも大きく90°未満の範囲内の角度で傾斜され得る。
字形、三角形、直方形、正方形、五角形、六角形、七角形、八角形か任意の他の多角形の任意の適切な断面形であり得る。実施形態によっては、流路の外形は、流路の全長にわたって同じ形状である。他の実施形態において流路の外形は、たとえば徐々に、または段階的に形状を変化させる。第1開口と第2開口は、同様に任意の形状であり得る領域を区画形成する。たとえば第1開口と第2開口などの流路の任意の開口は、たとえば円形、半円形、卵形、V字かU字形、三角形、直方形、正方形か任意の多角形の形状を備える領域を区画形成する。幾つかの実施形態において流路の第1開口と第2開口のうちの少なくとも1つは、少なくとも実質的に円形か少なくとも実質的に楕円形の領域を区画形成する。実施形態によっては、流路は、第1開口と第2開口のうちの1つか両方と同じ断面形を有する。幾つかの実施形態において第1開口か第2開口によって区画形成される領域は、流路の断面の外形と類似の寸法を備える。幾つかの実施形態において第1開口か第2開口によって区画形成される領域は、幅に関して、約0.1ミクロン〜約10ミクロンの範囲内で選択される最大サイズからなる。実施形態によっては、第1開口と第2開口の両方によって区画形成される領域の幅の最大値は、約0.1ミクロン〜約10ミクロンの範囲内にある。
な用語「ガラス」は、広く無結晶性固体材料を指す。熱力学に関する無結晶性固体材料は、サブクール液体に相当する。従ってガラスは、物質を溶融し、その後融点以下に急速冷却することによって得られる。そうすることによって結晶構造は形成されない。用語「ガラス」は、具体的には二酸化ケイ素、炭酸ナトリウム、炭酸カリウム、二酸化マンガンおよび固体化した金属酸化物の群から選択される溶融無機材料を指す。セラミックス例には限定されないが、ケイ酸物セラミックス、酸化物セラミックス、炭化物セラミックスまたは窒化物セラミックスが含まれる。
たとえば約0.5ミクロン以上で、約15ミクロン以下、約50ミクロン以下、または約250ミクロン以下の範囲内にあり得る。たとえば水平凹部の深さは、約0ミクロンよりも大きく約25ミクロン以下の範囲内、または約0ミクロンよりも大きく約500ミクロン以下の範囲内、または約0ミクロンよりも大きく約250ミクロンあるいは約100ミクロン以下の範囲内にあり得る。
は、ベース基板の側壁部分の凹部に配置され得る。そのような水平凹部は更に、充填部材に存在する流路の第1開口を含み得る。補助流路の第1開口は、幾つかの実施形態において充填部材に存在する流路の第1開口のすぐ近くに位置し得る。2つの流路の2つの開口は、たとえば互いに並び得る。
流路のシステムを含み得る。試験すべき化合物の濃度勾配の形成はたとえば、マイクロ流体装置がパッチ・クランプ装置として使用されるべき実施形態において望まれ得る。そのような実施形態において濃度勾配の生成は、用量反応曲線の記録、たとえば各々の化合物のIC50値を含むKDかKI値の測定に役立ち得る。
)。更に別の例示的実施例として表面は、たとえばNaOHと、KOHと、HF,HNO3およびエタノールの混合物と、NH4Fを含有する「緩衝化」HF溶液とを用いることによって、あるいは反応性イオンエッチングを用いるイオン衝撃によってエッチングされ得る(たとえばカオ(Cao),M.ら、J.Phys.Chem.B(2006)vol.110,no.26,p.13072-13075を参照)。
える。充填は、たとえば成長工程を含む蒸着工程を用いることによって実施され得る。実施形態によっては凹部の充填は、ベース基板を充填材によって覆うことによって達成される。従って凹部が同時に充填される。適切な蒸着工程例には、限定されないがプラズマ化学気相成長法、誘導結合プラズマ化学気相成長法(ICP−CVD)、低温化学蒸着、火炎加水分解蒸着(FHC)、物理蒸着(スパッタリング)、エピタキシか被覆が含まれる。適切な被覆工程例には、限定されないが回転被覆か浸漬被覆が含まれる。
めて平滑な充填部材(たとえばガラス)表面が形成可能である。平滑面は、特定の適用、具体的には繊細な細胞膜が機械的に損傷する危険性を最小限にするパッチ・クランプ法に望ましくあり得る。平滑表面は更に、細胞膜によって堅いシールを形成するのに有益である。湿式エッチングは、たとえば金属水酸化物などのブレンステッド塩基かブレンステッド酸を用いることによって実施され得る。例示的実施例として充填材がチタン酸化物である場合、硝酸/フッ化水素酸混合物、塩酸または濃硫酸を用いることによって前記チタン酸化物を除去し得る。適切な金属水酸化物例には、限定されないが、水酸化ナトリウム、NaOH、水酸化カリウム、KOH、水酸化リチウム、LiOHおよび水酸化カルシウム、Ca(OH)2が含まれる。湿式エッチングを用いることによって充填部材の一部分を正確に除去することは、たとえばエッチング溶液中に基板表面を浸漬し、更に数秒内にそれを除去することによって達成可能である。
ように本発明の方法のこの実施形態は、充填材だけが除去されるのでベース基板の材料として用いられ得る様々な物質の湿式エッチングを可能にする。これは各々平滑流路開口を備える平滑面の形成を可能にする。
えば研磨作用、腐食、電気化学的工程と動力学などの幾つかの因子を伴うと考えられる。
成される凹部の寸法を変化させることによって、異なる寸法の流路を単一デバイス内で得ることが可能である。従って単一デバイスは、異なるサイズの細胞/生体分子を分析すべく用いることが可能である。更に流路は、製作中に自己整合する流路の能力のため区画部材において容易に形成可能である。平滑な酸化物表面が保持されるので、側壁の粗さが減り、ウエハ・ボンディングが容易に実施されることができる。
徴に従って、あるいは本発明の他の側面に従うと共に流体チャンバを含む実施形態に従ってデバイスの第1流体チャンバ内に生命体を導入することを含む。
体は、本発明に従う方法において破断され得る。従って内部に含まれる輸送構造の電気特性にアクセス可能になり得る。これに関して細胞中の輸送構造例には、限定されないが細胞膜に位置する以下構造:陰イオンチャネル、陽イオンチャネル、陰イオン輸送体(陰イオン交換輸送体を含む)、陽イオン輸送体(陽イオン交換輸送体を含む)、受容体タンパク質と結合タンパク質の何れかが含まれる。第1電気信号の測定は、生命体を含有する試料溶液の基準電位を測定することを含み得る。前記電位は、生物センサの上面に存在する基準電極から測定される。前記基準電極は、試料溶液と接触する。例示的実施例として細胞のイオンチャネル、細胞膜部分、細胞小器官、細胞小器官部分または精子を通過する電流が検出および定量され得る。更に別の例示的実施例として細胞由来の小胞開口分泌は、たとえばデルニック(Dernick)らによって開示されるプロトコル(Nature Methods(2005)vol.2,no.9,p.699-708)と類似のパッチ電流測定を用いることによって測定され得る。
入される。例示的実施例として開口は、第1流体チャンバの方を向く第1開口であり得る(上記参照)。第1開口が凹面に含まれる実施形態において(上記参照)、凹面は、生命体の配置に役立ち得る。第1開口が凸面に含まれる実施形態において生命体の配置と固定は、マイクロピペットを用いる従来式のパッチ・クランプ法のようであり得る(図7C参照)。
び病原体などの特定の種類の生命体をろ過および捕捉すべく用いられることが可能である。ろ過適用では、入口開口の直径は、サブミクロン範囲内であることが可能である。吸引力の適用によって、開口径より小さな生命体が開口に入り、その後流路を通って第2流体チャンバ内に移動するが、大きな粒子は、第1流体チャンバ内に捕捉されたままである。
テル・ア・ゴー・ゴー・チャネル(hERG)を測定する計算方法(ミュー(Miu),P.,ら.J.A.L.A.(2006)vol.11,no.4,p.195-202)などの任意の自動化データ解析手法が採用され
得る。自動化データ分析手法の更に適した実施例は、アスミルド(Asmild)らによって簡潔に示される(Receptors and Channels(2003)vol.9,no.1,p.49-58)。
光検出の使用を含み得る。
特異的結合のためだけではなく、使用され得るチャンバのサイズが小さいためでもあり得
る(同上)。従って状況によっては、これらの著者(同上)によって記載されるように本発明に従うデバイスに基づく自動化装置で採用される任意のプロトコルの性能を評価および最適化することが望ましくなり得る。
本発明は、非限定的実施例と添付の図面と併せて考慮されると、詳細な説明に準拠して一層よく理解されるだろう。
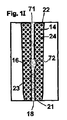
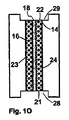
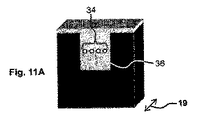
体装置の全表面を覆う。流路18が位置する白色で図示される凹部14は、デバイスの一側面上に配置され、右方に示された方位にある。充填部材16の第1側壁は、ベース基板12の、同様に白色で図示される壁部分(27)を区画形成する。
上壁の一側面にわたると共に水平凹部まで広がる。ベース基板上に充填材を蒸着することによって、空隙を備えた充填部材が形成される。充填材を変形または、リフローすることによって形成された流路は、ベース基板の一側面で水平凹部まで達する。この水平凹部を充填する充填部材の各々一部分を除去することによって、流路の第1開口が形成される。他方側面で水平凹部が乾式エッチングを手段としてマイクロ流体装置に形成される。従って流路の第2開口が形成される。得られたマイクロ流体装置は、第1開口に隣接するテーパ部分を備えた流路を含み得る。テーパ部分は、周縁壁のサイズが幅に関して減少することによって長さ方向に延びる円錐形であり得る。そのようなデバイスは、たとえばテーパ部分に、あるいはテーパ部分内など、流路内に生命体を配置および固定すべく用いられ得る。
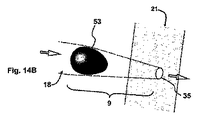
路開口35は、充填部材の側壁によって区画形成される各々のマイクロ流体装置の側壁部分としての第1側壁21内に含められる。第1側壁21は、少なくとも実質的に平面である。図7Cに示すデバイスにおいて流路開口35は、三次元的に構築されるマイクロ流体装置の第1側壁21に含められる。流路開口35に隣接する第1側壁21の表面は、流路開口35を取り囲む突起部33を区画形成するように皿形である。従って流路開口35は、第1側壁21によって区画形成される平面とは、異なる平面に位置する。
:150NaCl,2.8KCl,10CaCl2,1MgCl2,10HEPESおよび2mg/mlのブドウ糖、pH7.2(310mOsm)で下塗りされた。他の溶液は、第1流体
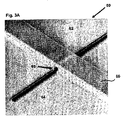
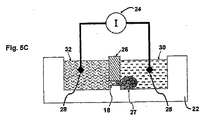
チャンバと第2流体チャンバ(標準パッチ・クランプ法の「バス溶液」と「ピペット溶液」に対応する)において従来式パッチ・クランプ測定と同じ方法で首尾よく使用された。電気抵抗(Ropen)は、パッチ・クランプ増幅器(EPC10,HEKA)に接続されたAg/AgCl電極を介して2つのチャンバにわたって測定された。図4Aに示すように得られたマイクロ流体装置では、測定値は、マイクロ流路配列に基づくRopen=L/σπr2とよく一致した(Lは長さ、rは半径)。
C12細胞で試験された。細胞は、5μg/mlのカルセイン−AM(インビトロゲン(Invitrogen))の蛍光色素と37°Cで15分間インキュベートされた。その後トリプシン処理され、遠沈され(4°Cで5分間1000rpm)、浴チャンバ内に導入する
前に電解質に再懸濁された。細胞がパッチ開口の及ぶ範囲の50μm内に認められたとき
、細胞は、手動式シリンジによって記録チャンバに約25kPaの吸引を適用することによって、再配置および捕捉された。吸引圧がマイクロ流体装置の製作方法(用いられる材料を含めて)に依存して変化し得ることを留意する。
図9Bと図9Cは、図4A(図9B)および図4B(図9C)(容量補償無し)に示すような工程に基づき製作されたデバイスからのマイクロ流体装置の典型的なSEM画像と典型的な電気的記録を示す。デバイスは、シリコンか(図9B)図4Aに示される最終段階中に成長した薄いSiO2絶縁体(約0.35ミクロン)を備えたシリコンからなるベース基板から形成された。特に電流の大きさ(同じ電圧刺激下で)は、容量スパイクのため有意に異なる。そのような大きな容量スパイクは、電解質とシリコン基板の間の電荷結合から生じる。分布容量の推定が困難なため、容量スパイクを電子的に除去することは失敗した。極厚の誘電体層を蒸着することによって容量結合が排除されるが、パッチ開口を詰まらせる。他方では高温は、ガラスをリフローさせることによって、パッチ開口を変形させるので、酸化物層を熱的に成長させる試みはうまくいかない。
験で得られるものよりも小さいか大きな寸法の凹部が必要となり得ることが指摘されるべきである。プラズマ化学気相成長法(PECVD)を用いることによってトレンチ内に低圧(0.33kPa(2.5Torr))でドープ二酸化ケイ素(PSG)を充填した(図13A)。次にウエハは、必要な流路の最終断面に依存して異なるタイミングで1100°C〜1200°Cの範囲内の加熱処理を受けた(図13B)。ウエハ表面は、次に化学機械的平坦化(CMP)によって平坦化されるか、ウエハ表面上の過剰PSGをエッチングし、次いで貯蔵器をマスキングおよびエッチングすることによって平坦化される(図13C)。そのような流路は更に、たとえば電極、相互コネクトおよび貯蔵器のような他のデバイス構成要素を製作するための始動ウエハとしても用いることが可能である。本発明は更に、複数の垂直に自己整列した流路を製作することも可能である。たとえば第1流路の構築後、一番上の酸化物を部分的に除去でき得るので第2流路が上方に製作される。
得る。従って一般的にそのような側部流路の幅は、デバイスの製作中にたとえば充填材などの物質の蒸着がそれらを充填できないように十分に大きく設計される。更にこれらの側部流路の最終断面は総じて、適用吸引が効果的になるべく、周縁壁を備える流路の断面(本実施例においてパッチ開口として使用される)より大きい。50ミクロンの距離は、上限よりはむしろ実施例を示すことに留意する。具体的には図4Bに示すように得られたマイクロ流体装置が使用される場合、50ミクロンよりずっと遠くにある細胞を引付けることが可能である。
(Pi・Vi)/Ti=(Pf・Vf)/Tf…(式1)
式1は、空隙の初期容積Viと、空隙の最終容積Vfを含む。
(Pi・Ai)/Ti=(Pf・Af)/Tf…(式2)
または式3
Af=(Pi/Pf)・(Tf/Ti)・Ai…(式3)
に至る。
適合性であるので既存のシリコン鋳物工場で実行可能である。流路製作費は、電子ビーム・リソグラフィ、ウエハ・ボンディング、レーザ光源、ポリマーなどのような特殊ではないツール/工程が使用されるので低い。本発明は更に、複数の自己整合流路を水平方向と縦方向の両方に製作すべく用いることも可能である。
Claims (28)
- ベース基板(12)、充填部材(16)、および流路(18)を備えるマイクロ流体装置であって、
前記ベース基板(12)の内部は、2つの対向側壁(23,24)と1つの底壁によって区画形成される凹部(14)を備え、
前記充填部材(16)は、前記凹部(14)を充填する充填部を有し、
前記流路(18)は、前記充填部内に形成され
前記流路(18)は第1開口(35)と第2開口を備え、
前記第1開口(35)は、前記充填部材(16)の第1側壁(21)に配置され、
前記第2開口は、前記充填部材(16)の第2側壁(22)に配置され、
前記第1側壁(21)は、前記第2側壁(22)に対して対向関係に配置され、
前記第1側壁(21)と前記第2側壁(22)のうちの少なくとも一方は、前記対向側壁(23,24)に対して垂直であり、
前記第1開口(35)と前記第2開口のうちの少なくとも一方は、円形、または楕円形の領域を区画形成し、
前記流路(18)は周縁壁によって区画形成され、
前記流路(18)の少なくとも一部分における前記周縁壁の断面は、円形、または楕円形の外形を備え、
前記流路(18)の周縁壁は、前記第1開口(35)に隣接する円錐部(9)を有し、
前記円錐部(9)は長さ方向に延び、
前記円錐部(9)において前記周縁壁の幅は、前記第1開口(35)に向かって減少し、
前記第1開口(35)を第1主開口(35)とし、前記第2開口を第2主開口とすると、
前記マイクロ流体装置は更に補助流路(69)を備え、
前記補助流路(69)は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記第1側壁(21)に配置される
ことを特徴とする、マイクロ流体装置。 - 前記流路(18)は、前記充填部材(16)内において水平方向に延びる、
請求項1記載のマイクロ流体装置。 - 前記流路(18)の長さ方向は、前記第1側壁(21)と前記第2側壁(22)のうちの少なくとも一方に対して、垂直である、
請求項1または2記載のマイクロ流体装置。 - 前記第1側壁(21)は、前記ベース基板(12)の壁部分を区画形成する、
請求項1〜3何れか一項記載のマイクロ流体装置。 - 前記ベース基板(12)の前記壁部分は、前記ベース基板(12)の側壁に設けられる、
請求項4記載のマイクロ流体装置。 - 前記ベース基板(12)の前記壁部分は、前記ベース基板(12)の水平凹部(28,29)内に設けられる、
請求項4または5記載のマイクロ流体装置。 - 前記ベース基板(12)の前記壁部分は、水平凹部(28)を備える、
請求項4または5記載のマイクロ流体装置。 - 前記水平凹部(28)は、前記第1開口(35)を備える、
請求項7記載のマイクロ流体装置。 - 前記充填部材(16)によって充填される前記凹部(14)を主凹部(14)と称し、
前記水平凹部(28,29)の少なくとも一部分は、前記主凹部(14)に対して垂直に延びる、
請求項6〜8何れか一項記載のマイクロ流体装置。 - 前記水平凹部(28,29)は周縁壁と入口を備えることによって、流体チャンバ(30,32,62,64)を区画形成する、
請求項6〜9何れか一項記載のマイクロ流体装置。 - 前記マイクロ流体装置は、前記ベース基板(12)の互いに対向する2つの側面上に第1水平凹部(28)と第2水平凹部(29)を備え、
前記第1水平凹部(28)は、前記第1側壁(21)の少なくとも一部を備え、
前記第2水平凹部(29)は、前記第2側壁(22)の少なくとも一部を備え、
前記第1水平凹部(28)は、第1流体チャンバ(30,62)を区画形成し、
前記第2水平凹部(29)は、第2流体チャンバ(32,64)を区画形成し、
前記第1流体チャンバ(30,62)は、前記流路(18)を通じて前記第2流体チャンバ(32,64)に流体連通する、
請求項6〜10何れか一項記載のマイクロ流体装置。 - 前記ベース基板(12)は、前記第1流体チャンバ(30,62)と前記第2流体チャンバ(32,64)を一体的に区画形成する、
請求項11記載のマイクロ流体装置。 - 前記マイクロ流体装置は更に、
前記第1流体チャンバ(30,62)に配置される検出電極(28)と、
前記第2流体チャンバ(32,64)に配置される基準電極(28)と
を備える、
請求項11または12記載のマイクロ流体装置。 - 前記マイクロ流体装置は更に、
前記検出電極(28)と前記基準電極(28)にそれぞれ通信する電気生理学測定回路システムを備える、
請求項13記載のマイクロ流体装置。 - 前記充填部材(16)は、前記ベース基板(12)の全表面を区画形成する、
請求項1〜14何れか一項記載のマイクロ流体装置。 - 前記ベース基板(12)は、前記充填部材(16)の材料よりも変形しにくい材料からなる、
請求項1〜15何れか一項記載のマイクロ流体装置。 - 前記ベース基板(12)の前記材料は、高温と減圧のうちの少なくとも一方の条件下で、前記充填部材(16)の前記材料よりも変形しにくい、
請求項16記載のマイクロ流体装置。 - 前記マイクロ流体装置は更に、
(i)前記ベース基板(12)内に区画形成される複数の凹部(14)であって、前記充填部材(16)は、それぞれ凹部(14)のうちの少なくとも一部分を充填する充填部をそれぞれ有することと;
(ii)それぞれ前記充填部内にそれぞれ対応するように配置される複数の流路(48,58)であって、それぞれ前記流路(48,58)は、前記第1側壁(21)に設けられる第1開口(35)と、前記第2側壁(22)に設けられる第2開口とを有することとを備える、
請求項1〜17何れか一項記載のマイクロ流体装置。 - 前記第1側壁(21)のそれぞれ前記第1開口(35)に対応する部分は、共通平面を区画形成すべく整列される、
請求項18記載のマイクロ流体装置。 - 前記第1側壁(21)のそれぞれ前記第1開口(35)に対応する部分は、前記ベース基板(12)の壁部分を区画形成し、
前記ベース基板(12)の前記壁部分は、前記ベース基板(12)の水平凹部(28)内に設けられる、
請求項19記載のマイクロ流体装置。 - 前記第1側壁(21)のそれぞれ前記第1開口(35)に対応する部分は、前記ベース基板(12)の複数の壁部分を区画形成し、
複数の前記壁部分は、それぞれ水平凹部(28)内に設けられるように、複数の水平凹部(28)を区画形成する、
請求項19記載のマイクロ流体装置。 - ベース基板(12)、充填部材(16)、および流路(18)を備えるマイクロ流体装置であって、
前記ベース基板(12)は凹部(14)を備え、前記凹部(14)は2つの対向側壁(23,24)と1つの底壁を備え、
前記充填部材(16)の一部は、前記凹部(14)内に設けられる充填部を有し、
前記流路(18)は、前記充填部内に区画形成され、
前記流路(18)は、第1開口(35)と第2開口を備え、
前記第1開口(35)は、前記充填部材(16)の第1側壁(21)に配置され、
前記第2開口は、前記充填部材(16)の第2側壁(22)に配置され、
前記第1側壁(21)は、前記第2側壁(22)に対して対向関係に配置され、
前記流路(18)は、周縁壁によって区画形成され、
前記流路(18)の少なくとも一部分における前記周縁壁の断面は、円形、または楕円形の外形を備え、
前記周縁壁は、前記第1開口(35)に隣接する円錐部(9)を備え、
前記円錐部(9)は長さ方向に延び、
前記円錐部(9)において前記周縁壁の幅は、前記第1開口(35)に向かって減少し、
前記第1開口(35)を第1主開口(35)とし、前記第2開口を第2主開口とすると、
前記マイクロ流体装置は更に補助流路(69)を備え、
前記補助流路(69)は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記第1側壁(21)に配置される
ことを特徴とする、マイクロ流体装置。 - 前記第1側壁(21)と前記第2側壁(22)のうちの少なくとも一方は、前記対向側壁(23,24)に対して垂直である、
請求項22記載のマイクロ流体装置。 - 第1流体チャンバ(30,62)と第2流体チャンバ(32,64)を有するマイクロ流体装置であって、
前記第1流体チャンバ(30,62)は、試験されるべき粒子を含有し、
前記第2流体チャンバ(32,64)は、区画部材によって前記第1流体チャンバ(30,62)から流体連通不能に区画され、
前記区画部材はベース基板(12)、充填部材(16)、および流路(18)を備え、
前記ベース基板(12)の内部は、凹部(14)を備え、
前記充填部材(16)は、前記凹部(14)を充填する充填部を有し、
前記流路(18)は、前記充填部に区画形成され
前記流路(18)は第1開口(35)と第2開口を備え、
前記第1開口(35)は、前記充填部材(16)の第1側壁(21)に配置され、
前記第2開口は、前記充填部材(16)の第2側壁(22)に配置され、
前記第1側壁(21)は、前記第2側壁(22)に対して対向関係に配置され、
前記第1側壁(21)と前記第2側壁(22)のうちの少なくとも一方は、前記凹部(14)を区画形成する一対の対向側壁(23,24)に対して垂直であり、
前記流路(18)は周縁壁によって区画形成され、
前記流路(18)の少なくとも一部分における前記周縁壁の断面は、円形、または楕円形の外形を備え、
前記流路の前記周縁壁は、前記第1開口に隣接する円錐部を有し、
前記円錐部は長さ方向に延び、前記円錐部において前記周縁壁の幅は前記第1開口に向かって減少し、
前記第1開口(35)を第1主開口(35)とし、前記第2開口を第2主開口とすると、
前記区画部材は更に補助流路を備え、
前記補助流路は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記第1側壁(21)に配置される
ことを特徴とする、マイクロ流体装置。 - 第1流体チャンバ(30,62)と第2流体チャンバ(32,64)を備えるマイクロ流体装置であって、
前記第1流体チャンバ(30,62)は、試験されるべき粒子を含有し、
前記第2流体チャンバ(32,64)は、区画部材を用いることによって前記第1流体チャンバ(30,62)から流体連通不能に区画され、
前記区画部材はベース基板(12)、充填部材(16)、および流路(18)を備え、
前記ベース基板(12)の内部は、区画形成される凹部(14)を備え、
前記充填部材(16)の一部は、前記凹部(14)を充填する充填部を有し、
前記流路(18)は、前記充填部内に区画形成され
前記流路(18)は第1開口(35)と第2開口を備え、
前記第1開口(35)は、前記充填部材(16)の第1側壁(21)に配置され、
前記第2開口は、前記充填部材(16)の第2側壁(22)に配置され、
前記第1側壁(21)は、前記第2側壁(22)に対して対向関係に配置され、
前記流路(18)は、周縁壁によって区画形成され、
前記流路(18)の少なくとも一部分における前記周縁壁の断面は、円形、または楕円形の外形を備え、
前記周縁壁は、前記第1開口(35)に隣接する円錐部(9)を備え、
前記円錐部(9)は長さ方向に延び、
前記円錐部(9)において前記周縁壁の幅は、前記第1開口(35)に向かって減少し、
前記第1開口(35)を第1主開口(35)とし、前記第2開口を第2主開口とすると、
前記区画部材は更に補助流路を備え、
前記補助流路は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記第1側壁(21)に配置される
ことを特徴とする、マイクロ流体装置。 - マイクロ流体装置の作製方法であって、前記作製方法は、
ベース基板(12)を提供することと;
前記ベース基板(12)の表面に凹部(14)を形成することであって、前記凹部は、前記ベース基板の少なくとも一側面まで広がるように開口することと;
前記凹部(14)を充填材(16)によって充填することであって、前記充填材(16)は前記凹部(14)を充填する充填部を有することと;
空隙が前記凹部に沿って延びるように配置されるように、前記充填部内に前記空隙を形成することであって、前記凹部は、前記空隙が前記凹部の開口側面に隣接する末端を備えるように、前記ベース基板の少なくとも一側面まで広がるように開口することと;
前記凹部(14)における前記充填材(16)に、前記充填材(16)の変形条件を作用させることによって、前記充填部内に前記空隙から流路(18)を形成することと
を備え、
前記流路は、前記開口側面に隣接する円錐部を備える周縁壁を有し、
前記円錐部は長さ方向に延び、前記円錐部において前記周縁壁の幅は前記開口側面に向かって減少し、
前記作製方法は更に補助流路(69)を形成することを備え、
前記補助流路(69)は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記開口側面に配置される
ことを特徴とする、マイクロ流体装置の作製方法。 - マイクロ流体装置の作製方法であって、前記作製方法は、
ベース基板(12)を提供することと;
前記ベース基板(12)の第1表面に第1凹部(14)を形成することであって、前記第1凹部は、前記ベース基板の少なくとも一側面まで広がるように開口することと;
前記ベース基板(12)の第2表面に第2凹部(28,29)を形成することであって、前記第2表面は前記第1表面とは異なることと;
前記第1凹部(14)を充填材(16)によって充填することであって、前記第1凹部(14)を充填する前記充填材(16)の部分を充填部と称することと;
前記充填部内に空隙を形成することであって、前記空隙は前記第1凹部に沿って延び、前記空隙は、前記凹部の開口側面に隣接する末端を備えることと;
前記第1凹部(14)において前記充填材(16)に、前記充填材の変形条件を作用させることによって、前記充填部に前記空隙から流路(18)を形成することと
を備え、
前記流路は周縁壁を有し、
前記流路は、前記開口側面に隣接する円錐部において終結し、
前記円錐部は長さ方向に延び、前記円錐部において前記周縁壁の幅は前記開口側面に向かって減少し、
前記作製方法は更に補助流路を形成することを備え、
前記補助流路は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記開口側面に配置される
ことを特徴とする、マイクロ流体装置の作製方法。 - マイクロ流体装置の作製方法であって、前記作製方法は、
ベース基板(12)を提供することと;
凹部(14)が前記ベース基板(12)の少なくとも一側面内まで広がり且つ開口するように、前記ベース基板(12)の表面に前記凹部(14)を形成することと;
前記ベース基板(12)を充填材(16)によって覆うことであって、前記凹部(14)を充填する前記充填材(16)の部分を充填部と称することと;
前記充填部内に空隙を形成することであって、前記空隙が前記凹部に沿って広がり、前記空隙は、前記凹部の開口側面に隣接する末端を備えることと;
前記凹部(14)において前記充填材(16)に、前記充填材(16)の変形条件を作用させることによって、前記充填部内に前記空隙から流路(18)を形成することと
を備え、
前記流路は周縁壁を備え、
前記流路は、前記開口側面に隣接する円錐部において終結し、
前記円錐部は長さ方向に延び、前記円錐部において前記周縁壁の幅は前記開口側面に向かって減少し、
前記作製方法は更に補助流路を形成することを備え、
前記補助流路は第1補助開口と第2補助開口を備え、
前記第1補助開口は前記開口側面に配置される
ことを特徴とする、マイクロ流体装置の作製方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/SG2006/000071 WO2007108773A1 (en) | 2006-03-23 | 2006-03-23 | Device for analyzing the status of a particle |
| SGPCT/SG2006/000071 | 2006-03-23 | ||
| PCT/SG2007/000080 WO2007108779A1 (en) | 2006-03-23 | 2007-03-23 | Microfluidic device for analyzing the status of a particle |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2009530638A JP2009530638A (ja) | 2009-08-27 |
| JP2009530638A5 JP2009530638A5 (ja) | 2010-05-13 |
| JP5254202B2 true JP5254202B2 (ja) | 2013-08-07 |
Family
ID=38522731
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009501390A Expired - Fee Related JP5254202B2 (ja) | 2006-03-23 | 2007-03-23 | 粒子の状態を分析するマイクロ流体装置、その作製方法、および分析方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20100015008A1 (ja) |
| EP (1) | EP2008093A4 (ja) |
| JP (1) | JP5254202B2 (ja) |
| AU (1) | AU2007227782A1 (ja) |
| WO (2) | WO2007108773A1 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8454811B2 (en) * | 2008-07-14 | 2013-06-04 | Octrolix Bv | Microfluidic system |
| EP2490013A1 (en) | 2009-10-13 | 2012-08-22 | Panasonic Corporation | Measuring device |
| CN101905859B (zh) * | 2010-04-16 | 2011-11-16 | 东南大学 | 正压热成型制备圆片级均匀尺寸玻璃微腔的方法 |
| CN101817498B (zh) * | 2010-04-16 | 2011-11-16 | 东南大学 | 低污染高成品率圆片级均匀尺寸玻璃微腔的制备方法 |
| EP2565261A4 (en) * | 2010-04-27 | 2017-08-16 | Panasonic Intellectual Property Management Co., Ltd. | Measuring device |
| JP5768055B2 (ja) * | 2010-09-30 | 2015-08-26 | 株式会社フジクラ | 基体 |
| US20160281147A1 (en) * | 2015-03-26 | 2016-09-29 | Xagenic Inc. | Ultrasensitive diagnostic device using electrocatalytic fluid displacement (efd) for visual readout |
| US9679897B1 (en) * | 2016-04-04 | 2017-06-13 | International Business Machines Corporation | High density nanofluidic structure with precisely controlled nano-channel dimensions |
| WO2018183744A1 (en) | 2017-03-29 | 2018-10-04 | The Research Foundation For The State University Of New York | Microfluidic device and methods |
| CN110254914B (zh) * | 2019-07-23 | 2021-03-02 | 重庆医药高等专科学校 | 一种蛙电生理实验标本盒 |
| CN110514461B (zh) * | 2019-08-29 | 2021-10-08 | 上海华力微电子有限公司 | 一种化学机械研磨机台缺陷检测方法 |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2502621C3 (de) * | 1975-01-23 | 1978-09-14 | Kernforschungsanlage Juelich Gmbh, 5170 Juelich | Messung elastischer und dielektrischer Eigenschaften der Membran lebender Zellen |
| AU5281690A (en) * | 1989-02-21 | 1990-09-26 | Lam Research Corporation | Novel glass deposition viscoelastic flow process |
| SE470347B (sv) * | 1990-05-10 | 1994-01-31 | Pharmacia Lkb Biotech | Mikrostruktur för vätskeflödessystem och förfarande för tillverkning av ett sådant system |
| JP3199398B2 (ja) * | 1991-07-22 | 2001-08-20 | オリンパス光学工業株式会社 | 生体組織分析装置 |
| US5278103A (en) * | 1993-02-26 | 1994-01-11 | Lsi Logic Corporation | Method for the controlled formation of voids in doped glass dielectric films |
| EP1178315A1 (de) * | 2000-07-31 | 2002-02-06 | Albrecht Dr.med. Priv.Doz. Lepple-Wienhues | Verfahren und Vorrichtung zur Untersuchung von Zellen mit Hilfe der Patch Clamp-Methode |
| US7270730B2 (en) * | 2000-08-04 | 2007-09-18 | Essen Instruments, Inc. | High-throughput electrophysiological measurement system |
| DE10130218A1 (de) * | 2001-06-22 | 2003-01-09 | Infineon Technologies Ag | Vorrichtung für ein Patch-Clamping von Vesikeln und Verfahren zu deren Herstellung |
| DE10203686A1 (de) * | 2002-01-31 | 2003-08-07 | Bayer Ag | Verfahren zur Durchführung von elektrischen Messungen an biologischen Membrankörpern |
| WO2003069381A2 (en) * | 2002-02-12 | 2003-08-21 | Unaxis Balzers Limited | Optical component comprising submicron hollow spaces |
| US20030180965A1 (en) * | 2002-03-25 | 2003-09-25 | Levent Yobas | Micro-fluidic device and method of manufacturing and using the same |
| DE60311973T2 (de) * | 2002-04-17 | 2007-10-31 | Sophion Bioscience A/S | Substrat und verfahren zum messen elektrophysiologischer eigenschaften von zellmembranen |
| AU2003254105B2 (en) * | 2002-07-26 | 2006-05-04 | Applied Biosystems, Llc. | Valve assembly for microfluidic devices, and method for opening and closing same |
| US7214348B2 (en) * | 2002-07-26 | 2007-05-08 | Applera Corporation | Microfluidic size-exclusion devices, systems, and methods |
| JP2004166693A (ja) * | 2002-10-28 | 2004-06-17 | Matsushita Electric Ind Co Ltd | 細胞の固定化方法 |
| US7309467B2 (en) * | 2003-06-24 | 2007-12-18 | Hewlett-Packard Development Company, L.P. | Fluidic MEMS device |
| EP1547676A1 (en) * | 2003-12-24 | 2005-06-29 | Corning Incorporated | Porous membrane microstructure devices and methods of manufacture |
| US20060003145A1 (en) * | 2004-02-04 | 2006-01-05 | Hansen Carl L | Ultra-smooth microfabricated pores on a planar substrate for integrated patch-clamping |
| US7471866B2 (en) * | 2004-06-29 | 2008-12-30 | Her Majesty The Queen In Right Of Canada As Represented By The Minister Of Industry, Through The Communications Research Centre Canada | Waveguiding structures with embedded microchannels and method for fabrication thereof |
| US7223157B2 (en) * | 2005-08-30 | 2007-05-29 | United Microelectronics Corp. | Chemical-mechanical polishing apparatus and method of conditioning polishing pad |
| EP2021790A4 (en) * | 2006-05-31 | 2011-09-07 | Agency Science Tech & Res | TRANSPARENT MICROFLUIDIC DEVICE |
-
2006
- 2006-03-23 WO PCT/SG2006/000071 patent/WO2007108773A1/en active Application Filing
-
2007
- 2007-03-23 JP JP2009501390A patent/JP5254202B2/ja not_active Expired - Fee Related
- 2007-03-23 US US12/294,205 patent/US20100015008A1/en not_active Abandoned
- 2007-03-23 WO PCT/SG2007/000080 patent/WO2007108779A1/en active Application Filing
- 2007-03-23 AU AU2007227782A patent/AU2007227782A1/en not_active Abandoned
- 2007-03-23 EP EP07716167A patent/EP2008093A4/en not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007108779A1 (en) | 2007-09-27 |
| JP2009530638A (ja) | 2009-08-27 |
| US20100015008A1 (en) | 2010-01-21 |
| AU2007227782A1 (en) | 2007-09-27 |
| EP2008093A1 (en) | 2008-12-31 |
| WO2007108779A8 (en) | 2008-01-31 |
| EP2008093A4 (en) | 2010-09-08 |
| WO2007108773A1 (en) | 2007-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5254202B2 (ja) | 粒子の状態を分析するマイクロ流体装置、その作製方法、および分析方法 | |
| JP7045418B2 (ja) | 腫瘍細胞を検出するための装置 | |
| US20100055673A1 (en) | Transparent microfluidic device | |
| US8581605B2 (en) | Nanopore platforms for ion channel recordings and single molecule detection and analysis | |
| US7201836B2 (en) | Multiaperture sample positioning and analysis system | |
| JP3191355U (ja) | 疾患を検出するためのマイクロデバイス | |
| US7708873B2 (en) | Induced-charge electro-osmotic microfluidic devices | |
| US20160040232A1 (en) | Methods and compositions for detecting non-hematopoietic cells from a blood sample | |
| US20060240543A1 (en) | Microwell arrays with nanoholes | |
| US11971405B2 (en) | Nanosensors and methods of making and using nanosensors | |
| US10730042B2 (en) | Biological detection system | |
| US7390650B2 (en) | System and method for obtaining and maintaining high-resistance seals in patch clamp recordings | |
| JP2007527540A (ja) | 細胞の体積変化を測定するための方法及び装置 | |
| JP4351073B2 (ja) | 細胞膜組織の電気生理的な特性を測定するための基質と方法 | |
| Ong et al. | Microfluidic integration of substantially round glass capillaries for lateral patch clamping on chip | |
| Burham et al. | Electrochemically etched nanoporous silicon membrane for separation of biological molecules in mixture | |
| US9399789B2 (en) | Base body and method of manufacturing base body | |
| JP2021505163A (ja) | 細胞とのインタフェースのためのナノ構造プラットフォーム及び対応する製造方法 | |
| CN1774629B (zh) | 微观流体系统及与其相关的膜片、设备和方法 | |
| Gunning et al. | Dense arrays of micro-needles for recording and electrical stimulation of neural activity in acute brain slices | |
| US20040005696A1 (en) | Substrate and method for measuring the electro-physiological properties of cell membranes | |
| Takahashi et al. | Nanopipette Fabrication Guidelines for SICM Nanoscale Imaging | |
| US10627327B2 (en) | Membrane vesicle recovery device, membrane vesicle recovery method, and membrane vesicle analysis method | |
| Yazbeck | Development of nanoparticle blockage based nanopore devices for biosensing and controlled chemical releasing | |
| Bruhn | Nanopore-Based Methods for Characterizing Single Proteins. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100323 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100323 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111226 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20120119 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120131 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120427 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120828 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121226 |
|
| A911 | Transfer of reconsideration by examiner before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20130213 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130326 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130417 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160426 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |