JP5116092B2 - プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 - Google Patents
プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 Download PDFInfo
- Publication number
- JP5116092B2 JP5116092B2 JP2007532549A JP2007532549A JP5116092B2 JP 5116092 B2 JP5116092 B2 JP 5116092B2 JP 2007532549 A JP2007532549 A JP 2007532549A JP 2007532549 A JP2007532549 A JP 2007532549A JP 5116092 B2 JP5116092 B2 JP 5116092B2
- Authority
- JP
- Japan
- Prior art keywords
- aliphatic
- substituted
- optionally substituted
- compound
- optionally
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 C*N1CCOCC1 Chemical compound C*N1CCOCC1 0.000 description 5
- WMFUPWQKKKBMQC-CALCHBBNSA-N CC(C)NC(Nc(cc1)ccc1Nc(nc1N)n[n]1-c1ccnc(N(C[C@H]2C)C[C@H](C)N2C(C)=O)c1)=O Chemical compound CC(C)NC(Nc(cc1)ccc1Nc(nc1N)n[n]1-c1ccnc(N(C[C@H]2C)C[C@H](C)N2C(C)=O)c1)=O WMFUPWQKKKBMQC-CALCHBBNSA-N 0.000 description 1
- MYNSYCVCAPTGHA-UHFFFAOYSA-N CC(Nc(cc1)ccc1Nc(nc1N)n[n]1-c1cc(Cl)ncc1)=O Chemical compound CC(Nc(cc1)ccc1Nc(nc1N)n[n]1-c1cc(Cl)ncc1)=O MYNSYCVCAPTGHA-UHFFFAOYSA-N 0.000 description 1
- VPKIAULJSDXMHU-UHFFFAOYSA-N CCOC(N(CC1)CCN1c(cc1)ccc1N/C(/Oc1ccccc1)=N/C#N)=O Chemical compound CCOC(N(CC1)CCN1c(cc1)ccc1N/C(/Oc1ccccc1)=N/C#N)=O VPKIAULJSDXMHU-UHFFFAOYSA-N 0.000 description 1
- QFHLZUDZRHUNHP-UHFFFAOYSA-N CCOC(N(CC1)CCN1c(cc1)ccc1Nc(nc1N)n[n]1-c1ccnc(Cl)c1)=O Chemical compound CCOC(N(CC1)CCN1c(cc1)ccc1Nc(nc1N)n[n]1-c1ccnc(Cl)c1)=O QFHLZUDZRHUNHP-UHFFFAOYSA-N 0.000 description 1
- NBZMFUYTOVYXGL-BGYRXZFFSA-N CCOC(N(CC1)CCN1c(cc1)ccc1Nc(nc1N)n[n]1-c1ccnc(N(C[C@H]2C)C[C@H](C)N2C(C)=O)c1)=O Chemical compound CCOC(N(CC1)CCN1c(cc1)ccc1Nc(nc1N)n[n]1-c1ccnc(N(C[C@H]2C)C[C@H](C)N2C(C)=O)c1)=O NBZMFUYTOVYXGL-BGYRXZFFSA-N 0.000 description 1
- PAMIQIKDUOTOBW-UHFFFAOYSA-N CN1CCCCC1 Chemical compound CN1CCCCC1 PAMIQIKDUOTOBW-UHFFFAOYSA-N 0.000 description 1
- JOFRAPLLCNYMLE-OKILXGFUSA-N C[C@H](CN(C[C@@H]1C)c2cc(-[n]3nc(Nc(cc4)ccc4N)nc3N)ccn2)N1C(C)=O Chemical compound C[C@H](CN(C[C@@H]1C)c2cc(-[n]3nc(Nc(cc4)ccc4N)nc3N)ccn2)N1C(C)=O JOFRAPLLCNYMLE-OKILXGFUSA-N 0.000 description 1
- APOJIILNJVLCQE-KNVOCYPGSA-N C[C@H]1O[C@@H](C)CN(C)C1 Chemical compound C[C@H]1O[C@@H](C)CN(C)C1 APOJIILNJVLCQE-KNVOCYPGSA-N 0.000 description 1
- YCFQPRVUXPTFON-UHFFFAOYSA-N NNc1ccnc(Cl)c1 Chemical compound NNc1ccnc(Cl)c1 YCFQPRVUXPTFON-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
Description
本発明は、Janusキナーゼ(JAK)の阻害剤として有用な化合物に関係する。また、本発明は、Aurora−2キナーゼ、Flt3キナーゼ、GSK−3キナーゼおよびKDRの阻害剤として有用な化合物にも関係する。更に、本発明は、この発明の化合物を含む薬学的に受容可能な組成物、および様々な障害の治療においてそれらの組成物を使用する方法も提供する。
Janusキナーゼ(JAK)は、JAK1、JAK2、JAK3およびTYK2からなる一群のチロシンキナーゼである。JAKは、サイトカインシグナル伝達系において非常に重要な役割を果たしている。JAKファミリーに属するキナーゼの下流基質は、シグナル伝達物質および転写活性化剤(STAT)タンパク質を含む。JAK/STATシグナル伝達系は、アレルギー反応および喘息などの多くの異常な免疫応答、移植片拒絶反応、慢性関節リウマチ、筋萎縮性側索硬化症および多発性硬化症などの自己免疫疾患、更には白血病およびリンパ腫などの充実性悪性疾患および血液悪性疾患などの媒介にかかわり合っている。また、JAK2は骨髄増殖性障害にもかかわり合っており、この骨髄増殖性障害は、真性赤血球増加症、本態性血小板血症、慢性特発性骨髄線維症、骨髄線維症を伴う骨髄様化生、慢性骨髄性白血病、慢性骨髄単球性白血病、慢性好酸球性白血病、好酸球増多症候群および全身性マスト細胞疾患を含む。
今や、本発明の化合物およびそれらの化合物の薬学的に受容可能な組成物は、プロテインキナーゼの阻害剤として有効であることが判明している。特定の実施態様においては、これらの化合物およびそれらの化合物の薬学的に受容可能な組成物は、GSK−3、JAK−2、JAK−3、Flt3、KDRまたはAurora−2プロテインキナーゼの阻害剤として有効である。好適な実施態様においては、これらの化合物および薬学的に受容可能な組成物は、JAK−2またはJAK−3の阻害剤である。これらの化合物は、一般式I:
(定義および一般的な専門用語)
本明細書で使用する場合、別に示されていない限り、以下の定義が適用される。本発明の目的上、化学元素は、元素の周期表、CASバージョン、Handbook of Chemistry and Physics、第75版により特定されている。更に、有機化学の一般的な原理は、「Organic Chemistry」、Thomas Sorrell、University Science Books、Sausalito:1999;「March’s Advanced Organic Chemistry」、第5版、編集:Smith,M.B.およびMarch,J.、John Wiley & Sons、New York:2001;「Encyclopedia of Organic Transformations」;編集:Richard C. Larock、John Wiley & Sons、New York:1999;「Encyclopedia of Reagents for Organic Synthesis」編集:Leo A.Paquette、John Wiley & Sons New York:1995;T.W.Greene & P.G.M.Wutz、「Protective Groups in Organic Synthesis」、第3版、John Wiley & Sons,Inc.(1999)(およびもっと初期の版)で説明されており、これをもって、これらの参考文献の内容全体が参照により本明細書に組み入れられる。
本発明は、式I:
Rの各出現は、水素、または場合によってJもしくはJ’で置換されたC1−6脂肪族基から独立して選択され;そして
R’は、水素、または場合によって三つまでのJもしくはJ’の出現で置換されたC1−8脂肪族基、場合によって三つまでのJの出現で置換されたC6−10アリール、場合によって三つまでのJの出現で置換された5〜10個の環原子を有するヘテロアリール環、または場合によって三つまでのJもしくはJ’の出現で置換された3〜10個の環原子を有するヘテロシクリル環から選択される基から独立して選択され、あるいは、RおよびR’が一体となって、窒素、酸素もしくはイオウから独立して選択される0〜3個のヘテロ原子を有する5〜8員のシクロアルキル、ヘテロシクリル、アリール、またはヘテロアリール環を形成しており、ここで、各環は、場合により、かつ、独立して、三つまでのJの出現で置換されており;
各R’’の出現は、水素、または場合によって三つまでのJもしくはJ’の出現で置換されたC1−8脂肪族基、場合によって三つまでのJの出現で置換されたC6−10アリール、場合によって三つまでのJの出現で置換された5〜10個の環原子を有するヘテロアリール環、または場合によって三つまでのJもしくはJ’の出現で置換された3〜10個の環原子を有するヘテロシクリル環から選択される基から独立して選択され、あるいは、RおよびR’’が一体となって、窒素、酸素もしくはイオウから独立して選択される0〜3個のヘテロ原子を有する5〜8員のシクロアルキル、ヘテロシクリル、アリール、またはヘテロアリール環を形成しており、ここで、各環は、場合により、かつ、独立して、三つまでのJの出現で置換されており;
各Jの出現は:ハロゲン;−RO;−ORO;−SRO;1,2−メチレンジオキシ;1,2−エチレンジオキシ;場合によってROで置換されたフェニル(Ph);場合によってROで置換された−O(Ph);場合によってROで置換された−(CH2)1−2(Ph);場合によってROで置換された−CH=CH(Ph);−NO2;−CN;−N(RO)2;−NROC(O)RO;−NROC(S)RO;−NROC(O)N(RO)2;−NROC(S)N(RO)2;−NROCO2RO;−NRONROC(O)RO;−NRONROC(O)N(RO)2;−NRONROCO2RO;−C(O)C(O)RO;−C(O)C(O)ORO、−C(O)C(O)N(RO)2、−C(O)CH2C(O)RO;−CO2RO;−C(O)RO;−C(S)RO;−C(S)ORO、−C(O)N(RO)2;−C(S)N(RO)2;−C(=NH)−N(RO)2、−OC(O)N(RO)2;−OC(O)RO;−C(O)N(ORO)RO;−C(NORO)RO;−S(O)2RO;−S(O)3RO;−SO2N(RO)2;−S(O)RO;−NROSO2N(RO)2;−NROSO2RO;−N(ORO)RO;−C(=NH)−N(RO)2;C(=NORO)RO;(CH2)0−2NHC(O)RO;−P(O)2RO;−PO(RO)2;−OPO(RO)2;または−P(O)(H)(ORO);から選択され;
ここで、それぞれ独立したROの出現は、水素、場合によって置換されたC1−6脂肪族基、場合によって置換された5〜6員のヘテロアリールもしくはヘテロ環式環、場合によって置換されたフェニル(Ph);場合によって置換された−O(Ph);場合によって置換された−(CH2)1−2(Ph);場合によって置換された−CH=CH(Ph);から選択されるか、または、同じ置換基または異なる置換基での二つの独立したROの出現は、各RO基が結合されている一つまたは複数の原子と共に一体となって、窒素、酸素もしくはイオウから独立して選択される0〜3個のヘテロ原子を有する5〜8員のヘテロシクリル、アリールもしくはヘテロアリール環または3〜8員のシクロアルキル環を形成しており;
ここで、ROの脂肪族基に対する置換基は、場合によって置換されたヘテロアリール、場合によって置換された、ヘテロ環式基、NH2、NH(C1−6脂肪族)、N(C1−6脂肪族)2、ハロゲン、C1−6脂肪族基、OH、O(C1−6脂肪族)、NO2、CN、CO2H、CO2(C1−6脂肪族)、O(ハロC1−6脂肪族)またはハロ(C1−6脂肪族)であり、ここで、ROのこれらの各C1−6脂肪族基は置換されておらず;
ここで、ROのフェニル、ヘテロアリールまたはヘテロ環式基に対する置換基は、C1−6脂肪族基、NH2、NH(C1−4脂肪族)、N(C1−6脂肪族)2、ハロゲン、C1−6脂肪族基、OH、O(C1−6脂肪族)、NO2、CN、CO2H、CO2(C1−6脂肪族)、O(ハロC1−6脂肪族)またはハロ(C1−6脂肪族)であり、ここで、ROのこれらの各C1−6脂肪族基は置換されておらず;
各J’の出現は、=O、=S、=NNHR*、=NN(R*)2、=NNHC(O)R*、=NNHCO2(アルキル)、=NNHSO2(アルキル)または=NR*から独立して選択され、ここで、各R*は水素または場合によって置換されたC1−6脂肪族基から独立して選択され;またここで、R*の脂肪族基は、場合によってNH2、NH(C1−4脂肪族)、N(C1−4脂肪族)2、ハロゲン、C1−4脂肪族基、OH、O(C1−4脂肪族)、NO2、CN、CO2H、CO2(C1−4脂肪族)、O(ハロC1−4脂肪族)またはハロ(C1−4脂肪族)で置換されており、更にここで、R*の各C1−4脂肪族基は置換されていない。
本発明の化合物は、一般的に、当業者にとって既知の類似の化合物のための方法により、ならびに以下の一般的スキームおよび以下の調製実施例で示されている如き方法により調製することができる。本発明の化合物を調製するためのプロセスは、それらのスキームおよび実施例で説明されている。これらのスキームの可変記号は、本明細書において本化合物(例えば式I)に関して定義されている通りであり、または、それらの化合物を参照することにより容易に認識することができる。
本発明の化合物への別な一般的経路がスキーム3に描かれている。スキーム3では特定の試薬が描かれているが、当業者であれば、ここで描かれている合成を実施するために他の工程および試薬も使用できることが認識されよう。以下のスキーム4および5は、この一般的スキームを更に詳しく描いている。
(薬学的に受容可能な組成物)
上で検討されているように、本発明はプロテインキナーゼの阻害剤である化合物を提供し、それ故、本化合物は、これらに限定するものではないが、アレルギー性疾患、増殖性疾患、自己免疫疾患、臓器移植と関連性のある状態、炎症性疾患、免疫学的に媒介された疾患、ウイルス性疾患または破壊性骨疾患(例えば骨吸収性障害など)を含む疾患、障害および状態の治療に有用である。従って、本発明の別の側面においては、薬学的に受容可能な組成物が提供され、ここで、これらの組成物は、本明細書で開述されている通りのいずれかの化合物を含み、場合によっては、薬学的に受容可能な担体、アジュバントまたはビヒクルも含む。特定の実施態様においては、これらの組成物は、場合によって、更に一つまたはそれ以上付加的な治療薬も含む。
更に別の側面においては、アレルギー性疾患、増殖性疾患、自己免疫疾患、臓器移植と関連性のある状態、炎症性疾患、免疫学的に媒介された疾患、ウイルス性疾患または破壊性骨疾患(例えば骨吸収性障害など)を治療するための方法、またはそれらの疾患の重症度を低減するための方法が提供され、その方法は、それらを必要としている被検者に対して有効量の本化合物または本化合物を含有する薬学的に受容可能な組成物を投与する工程を含む。本発明の特定の実施態様においては、本化合物または薬学的に受容可能な組成物の「有効量」は、興味対象の疾患、障害または状態を治療するのに有効な量、またはそれらの疾患の重症度を低減するのに有効な量である。本化合物および組成物は、本発明の方法により、興味対象の疾患、障害もしくは状態の治療または重症度の低減にとって効果的なあらゆる量およびあらゆる投与経路を用いて投与されてよい。必要とされる正確な量は、被検者の種、年齢および一般的な状態、その感染症の重症度、特定の作用物質、および作用物質の投与様式などに依存して、被検者毎に様々に変わるであろう。本発明の化合物は、好適には、投与しやすく、且つ、投薬量の均一性を保ちやすい投薬単位形態で調合される。本明細書で使用する場合、「投薬単位形態」という表現は、治療されるべき患者にとって適切な作用物質の物理的に個別の単位を表す。しかし、本発明の化合物および組成物の一日の合計使用量は、理にかなった医学的判定の範囲内において、担当医師により決定されることが理解されよう。個々の患者または生物体に対する特定の有効な用量レベルは様々なファクターに依存し、それらのファクターは、治療されるべき障害およびその障害の重症度;使用される特定の化合物の活性;使用される特定の組成物;患者の年齢、体重、一般的な健康状態、性別および食生活;使用される特定の化合物の投与時間、投与経路および排出速度;治療の継続期間;用いられる特定の化合物と組み合わせて使用される薬剤または同時的に使用される薬剤、ならびに医療技術分野において広く知られているファクターなどを含む。本明細書で使用する場合、「患者」という用語は、動物、好適には哺乳動物、最も好適にはヒトを意味する。
以下の例は、尿素を形成するための典型的な実施例である:
DMSO−d6中におけるNMR:
本発明の特定の化合物に対する分析データは、以下の如くにして収集され、記録された:プロトンNMRデータは、Bruker AMX 500装置および適切な溶媒を用いて収集された。LC/MS法は、適切な勾配を用いる1.0ml/分の流量でのHypersil BDS C18、5ミクロン、2.1×50mmカラムを使用した。質量分析計のサンプルは、エレクトロスプレーイオン化を用いて単一MSモードで運転されるMicroMass ZQまたはQuattro II質量分析計で分析された。サンプルは、フローインジェクション(FIA)またはクロマトグラフィーを用いて質量分析計に導入された。質量分析計によるすべての分析での移動相はアセトニトリル−水混合物(幾つかのケースにおいてはTFA)で構成された。以下の表2は、本発明の特定の化合物に対する例証的なLC質量スペクトルデータ(LC/MS)、保持時間(RT)および1H−NMRデータを示しており、ここで、表2の化合物番号は表1に示されている化合物に対応している(空欄は試験を実施しなかったことを示している)。
放射分析法によるフィルター結合アッセイを用いて、種々の化合物がFLT−3活性を阻害する能力をスクリーニングした。このアッセイは、基質ポリ(Glu,Tyr)4:1(pE4Y)への33Pの取り込みをモニタリングするものである。反応は、100mMのHEPES(pH7.5)、10mMのMgCl2、25mMのNaCl、1mMのDTT、0.01%のBSAおよび2.5%のDMSOを含有する溶液中で実施された。このアッセイにおける最終的な基質濃度は、90μMのATPおよび0.5mg/mLのpE4Y(両方ともSigma Chemicals,St Louis,MOから入手)であった。化合物の最終濃度は、一般的に、0.01μMから5μMまでの間である。典型的には、12ポイントの滴定を、10mMのDMSO原液から試験化合物の段階希釈液を調製することにより実施した。反応は室温で実施された。溶液1は、100mMのHEPES(pH7.5)、10mMのMgCl2、25mMのNaCl、1mg/mlのpE4Yおよび180μMのATP(それぞれの反応で、0.3μCiの[γ−33P]ATPを含有)を含んでいる。溶液2は、100mMのHEPES(pH7.5)、10mMのMgCl2、25mMのNaCl、2mMのDTT、0.02%のBSAおよび3nMのFLT−3を含んでいる。このアッセイは、それぞれ50μLの溶液1および2.5mLの試験化合物を混合することにより、96ウェルプレートで実行された。反応は、溶液2を用いて開始された。室温における20分間のインキュベーション後、反応は0.4mMのATPを含有する50μLの20%TCAを用いて停止された。この後、すべての反応体積をフィルタープレートに移し、TOMTEC(Hamden,CT)から入手可能なHarvester9600により5%のTCAで洗った。pE4yに取り込まれた33Pの量は、Packard TopCount Microplate Scintillation Counter(Meriden,CT)により分析された。データは、IC50またはKiを得るべく、Prismソフトウェアを用いて適合化された。
種々の化合物が、標準的な結合酵素アッセイ(Foxら(1998)Protein Sci 7、2249)を用いて、Aurora−2を阻害する能力について以下の仕方でスクリーニングされる。0.1MのHEPES 7.5、10mMのMgCl2、1mMのDTT、25mMのNaCl、2.5mMのホスホエノールピルビン酸、300mMのNADH、30mg/mlのピルビン酸キナーゼ、10mg/mlの乳酸デヒドロゲナーゼ、40mMのATPおよび800μMのペプチド(LRRASLG、American Peptide,Sunnyvale,CA)を含有するアッセイ用のストック緩衝溶液に、最終濃度が30μMになるまで、本発明の化合物のDMSO溶液を加える。結果として生じた混合物を30℃で10分間インキュベートする。反応は、このアッセイにおける最終濃度が70nMになるように10μLのAurora−2ストック溶液を加えることによって開始された。反応速度は、BioRad Ultramarkプレート読み取り装置(Hercules,CA)を用い、30℃において、5分間の読み取り時間にわたって340nmでの吸光度をモニタリングすることにより得られる。Ki値は、阻害剤濃度の関数として、その速度データから決定される。
標準的な結合酵素アッセイ(Foxら、Protein Sci.、(1998)7、2249)を用いて、KDRを阻害する能力について種々の化合物をスクリーニングした。アッセイは、200mMのHEPES 7.5、10mMのMgCl2、25mMのNaCl、1mMのDTTおよび1.5%のDMSOの混合物中において実施された。このアッセイにおける最終的な基質濃度は300μMのATP(Sigma Chemicals)および10μMのポリE4Y(Sigma)であった。アッセイは、37℃および30nMのKDRにおいて実施された。結合酵素系の成分の最終濃度は、2.5mMのホスホエノールピルビン酸、200μMのNADH、30μg/MLのピルビン酸キナーゼおよび10μg/mlの乳酸デヒドロゲナーゼであった。アッセイ用のストック緩衝溶液は、ATPおよび興味対象の試験化合物を除き、上でリストアップされているすべての試薬を含めて調製された。177μlのストック溶液を96ウェルのプレートに入れ、その後、試験化合物を含有する3μlの2mM DMSO原液を加えた(最終的な化合物の濃度、30μM)。このプレートを37℃で約10分間プレインキュベートし、20μlのATP(最終濃度、300μM)を加えることにより反応を開始させた。反応速度は、37℃において、5分間の読み取り時間にわたり、Molecular Devicesプレート読み取り装置(Sunnyvale,CA)を用いて得られた。試験化合物を伴わずにアッセイ用の混合物およびDMSOを含有した標準ウェルと比べて50%より大きい阻害率を示した化合物に対しては、IC50値を決定すべく滴定を行い、IC50値を決定した。
以下に示されているアッセイを用いて、JAKを阻害する能力について種々の化合物をスクリーニングした。反応は、100mMのHEPES(pH7.4)、1mMのDTT、10mMのMgCl2、25mMのNaClおよび0.01%のBSAを含有するキナーゼ緩衝液中において実施された。
これらのアッセイは、JAK−2酵素を使用し、ポリ(Glu)4Tyrの最終濃度が15μMであり、ATPの最終濃度が12μMであった点を除き、実施例25において上で説明されている通りに行われた。
Claims (21)
- 式I:
AはNまたはCR1であり;
R1はH、ハロゲンまたはC1−6アルキルであり;
RXは:
RYは:
Rの各出現は、水素、または場合によってJもしくはJ’で置換されたC1−6脂肪族基から独立して選択され;そして
R’は、水素、または場合によって三つまでのJもしくはJ’の出現で置換されたC1−8脂肪族、場合によって三つまでのJの出現で置換されたC6−10アリール、場合によって三つまでのJの出現で置換された5〜10個の環原子を有するヘテロアリール環、または場合によって三つまでのJもしくはJ’の出現で置換された3〜10個の環原子を有するヘテロシクリル環から選択される基から独立して選択され、あるいは、RおよびR’が一体となって、窒素、酸素もしくはイオウから独立して選択される0〜3個のヘテロ原子を有する5〜8員のシクロアルキル、ヘテロシクリル、アリール、またはヘテロアリール環を形成しており、ここで、各環は、場合により、かつ、独立して、三つまでのJの出現で置換されており;
各R’’の出現は、水素、または場合によって三つまでのJもしくはJ’の出現で置換されたC1−8脂肪族、場合によって三つまでのJの出現で置換されたC6−10アリール、場合によって三つまでのJの出現で置換された5〜10個の環原子を有するヘテロアリール環、または場合によって三つまでのJもしくはJ’の出現で置換された3〜10個の環原子を有するヘテロシクリル環から選択される基から独立して選択され、あるいは、RおよびR’’が一体となって、窒素、酸素もしくはイオウから独立して選択される0〜3個のヘテロ原子を有する5〜8員のシクロアルキル、ヘテロシクリル、アリール、またはヘテロアリール環を形成しており、ここで、各環は、場合により、かつ、独立して、三つまでのJの出現で置換されており;
各Jの出現は:ハロゲン;−RO;−ORO;−SRO;1,2−メチレンジオキシ;1,2−エチレンジオキシ;場合によってROで置換されたフェニル(Ph);場合によってROで置換された−O(Ph);場合によってROで置換された−(CH2)1−2(Ph);場合によってROで置換された−CH=CH(Ph);−NO2;−CN;−N(RO)2;−NROC(O)RO;−NROC(S)RO;−NROC(O)N(RO)2;−NROC(S)N(RO)2;−NROCO2RO;−NRONROC(O)RO;−NRONROC(O)N(RO)2;−NRONROCO2RO;−C(O)C(O)RO;−C(O)C(O)ORO、−C(O)C(O)N(RO)2、−C(O)CH2C(O)RO;−CO2RO;−C(O)RO;−C(S)RO;−C(S)ORO、−C(O)N(RO)2;−C(S)N(RO)2;−C(=NH)−N(RO)2、−OC(O)N(RO)2;−OC(O)RO;−C(O)N(ORO)RO;−C(NORO)RO;−S(O)2RO;−S(O)3RO;−SO2N(RO)2;−S(O)RO;−NROSO2N(RO)2;−NROSO2RO;−N(ORO)RO;−C(=NH)−N(RO)2;C(=NORO)RO;(CH2)0−2NHC(O)RO;−P(O)2RO;−PO(RO)2;−OPO(RO)2;または−P(O)(H)(ORO);から独立して選択され;
ここで、それぞれ独立したROの出現は、水素、場合によって置換されたC1−6脂肪族、場合によって置換された5〜6員のヘテロアリールもしくはヘテロ環式環、場合によって置換されたフェニル(Ph);場合によって置換された−O(Ph);場合によって置換された−(CH2)1−2(Ph);場合によって置換された−CH=CH(Ph);から選択されるか、または、同じ置換基または異なる置換基での二つの独立したROの出現は、各RO基が結合されている一つまたは複数の原子と共に一体となって、窒素、酸素もしくはイオウから独立して選択される0〜3個のヘテロ原子を有する5〜8員のヘテロシクリル、アリールもしくはヘテロアリール環または3〜8員のシクロアルキル環を形成しており;
ここで、ROの脂肪族基に対する置換基は、場合によって置換されたヘテロアリール、場合によって置換された、ヘテロ環式基、NH2、NH(C1−6脂肪族)、N(C1−6脂肪族)2、ハロゲン、C1−6脂肪族、OH、O(C1−6脂肪族)、NO2、CN、CO2H、CO2(C1−6脂肪族)、O(ハロC1−6脂肪族)またはハロ(C1−6脂肪族)であり、ここで、ROの該各C1−6脂肪族基は置換されておらず;
ここで、ROのフェニル、ヘテロアリールまたはヘテロ環式基に対する置換基は、C1−6脂肪族、NH2、NH(C1−4脂肪族)、N(C1−6脂肪族)2、ハロゲン、C1−6脂肪族、OH、O(C1−6脂肪族)、NO2、CN、CO2H、CO2(C1−6脂肪族)、O(ハロC1−6脂肪族)またはハロ(C1−6脂肪族)であり、ここで、ROの該各C1−6脂肪族基は置換されておらず;
各J’の出現は、=O、=S、=NNHR*、=NN(R*)2、=NNHC(O)R*、=NNHCO2(アルキル)、=NNHSO2(アルキル)または=NR*から独立して選択され、ここで、各R*は水素または場合によって置換されたC1−6脂肪族から独立して選択され;ここで、R*の脂肪族基は、場合によってNH2、NH(C1−4脂肪族)、N(C1−4脂肪族)2、ハロゲン、C1−4脂肪族、OH、O(C1−4脂肪族)、NO2、CN、CO2H、CO2(C1−4脂肪族)、O(ハロC1−4脂肪族)またはハロ(C1−4脂肪族)で置換されており、ここで、R*の該各C1−4脂肪族基は置換されていない、
式Iの化合物または該化合物の薬学的に受容可能な塩。 - AがNである、請求項1〜3のいずれか一項に記載の化合物。
- AがCHである、請求項1〜3のいずれか一項に記載の化合物。
- R’がC1−6脂肪族、フェニルまたは5〜8員のヘテロアリール基であり、ここで、R’が場合によって一個までのJの出現で置換されている、請求項1〜3のいずれか一項に記載の化合物。
- R’がC1−6脂肪族基またはフェニルであり、ここで、R’が場合によって一個までのJの出現で置換されており、Jが−COORO、−ORO、ROまたは−CF3であり、ROがC1−3脂肪族基である、請求項6記載の化合物。
- R’がメチル、エチル、プロピル、イソプロピル、−CH2−イソプロピル、ブチル、t−ブチル、−CH2−t−ブチルまたはシクロヘキシルであり、R’が場合によって−COORO、−OROまたはROで置換されている、請求項7記載の化合物。
- Rが水素またはメチルである、請求項1〜3のいずれか一項に記載の化合物。
- 各R’’がC1−6脂肪族基、フェニルまたは5〜8員のヘテロ環式基から独立して選択され、各R’’が、場合によって、かつ、独立して、一個までのJの出現で置換されている、請求項1〜3のいずれか一項に記載の化合物。
- 各R’’がC1−6脂肪族基またはフェニルから独立して選択され、各R’’が、場合によって、かつ、独立して、一個までのJの出現で置換されており、各Jがハロゲン、−CF3、−CN、−COORO、−COROまたは−OROから独立して選択され、各ROがC1−3脂肪族基である、請求項10記載の化合物。
- 各R’’がメチル、エチル、プロピル、イソプロピル、−CH2−イソプロピル、ブチル、t−ブチルまたは−CH2−t−ブチルであり、各R’’が場合によって−CN、−COOROまたは−OROで置換されている、請求項11記載の化合物。
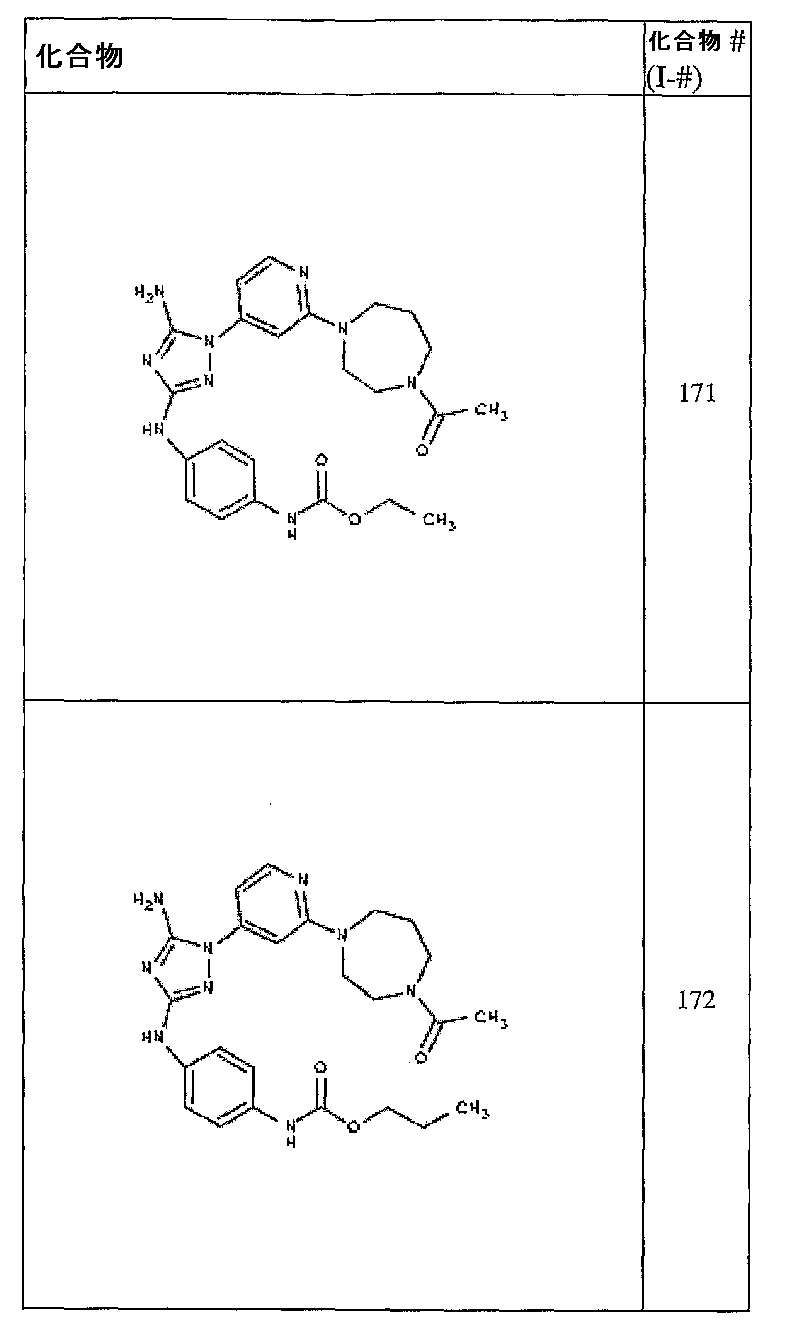
- 表1の化合物のうちの一つから選択される化合物。
- 請求項1〜13のいずれか一項に記載の化合物および薬学的に受容可能な担体、アジュバントまたはビヒクルを含む医薬組成物。
- 化学療法薬もしくは抗増殖剤、抗炎症剤、免疫調節剤もしくは免疫抑制剤、神経栄養因子、心臓血管疾患を治療するための薬剤、糖尿病を治療するための薬剤、または免疫不全障害を治療するための薬剤から選択される付加的な治療薬をさらに含む、請求項14記載の医薬組成物。
- 前記治療薬が免疫調節剤または免疫抑制剤である、請求項15記載の医薬組成物。
- 生物学的サンプルにおけるJAK2またはJAK3キナーゼ活性を阻害する方法であって、該方法は、該生物学的サンプルと請求項1〜13のいずれか一項に記載の化合物とを接触させる工程を包含する、キナーゼ活性の阻害方法。
- 患者における、アレルギー、喘息、自己免疫疾患、移植片拒絶反応、(AML、ルー・ゲーリグ病)、多発性硬化症(MS)、充実性悪性疾患、血液悪性疾患または骨髄増殖性障害から選択される疾患状態を治療するため、または前記疾患状態の重症度を低減するための医薬組成物であって、該組成物は、請求項1〜13のいずれか一項に記載の化合物を含有する、医薬組成物。
- 化学療法薬もしくは抗増殖剤、抗炎症剤、免疫調節剤もしくは免疫抑制剤、または神経栄養因子から選択される付加的な治療薬を含有し、ここで、該付加的な治療薬が、治療されている該疾患にとって適切である、請求項18記載の医薬組成物。
- 前記疾患または障害が、アレルギー反応もしくはI型過敏反応、喘息、筋萎縮性側索硬化症(AML、ルー・ゲーリグ病)、多発性硬化症(MS)、移植片拒絶反応、移植片対宿主病、慢性関節リウマチ、白血病、リンパ腫、真性赤血球増加症、本態性血小板血症、慢性特発性骨髄線維症、骨髄線維症を伴う骨髄様化生、慢性骨髄性白血病、慢性骨髄単球性白血病、慢性好酸球性白血病、好酸球増多症候群、または全身性マスト細胞疾患である、請求項18記載の医薬組成物。
- JAK2またはJAK3キナーゼ活性を阻害するための組成物であって、該組成物は、請求項1〜13のいずれか一項に記載の化合物を含む、組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US61090204P | 2004-09-17 | 2004-09-17 | |
| US60/610,902 | 2004-09-17 | ||
| PCT/US2005/033333 WO2006034116A1 (en) | 2004-09-17 | 2005-09-19 | Diaminotriazole compounds useful as protein kinase inhibitors |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008222676A Division JP2009019048A (ja) | 2004-09-17 | 2008-08-29 | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2008513488A JP2008513488A (ja) | 2008-05-01 |
| JP2008513488A5 JP2008513488A5 (ja) | 2008-10-16 |
| JP5116092B2 true JP5116092B2 (ja) | 2013-01-09 |
Family
ID=35583429
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007532549A Expired - Fee Related JP5116092B2 (ja) | 2004-09-17 | 2005-09-19 | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 |
| JP2008222676A Withdrawn JP2009019048A (ja) | 2004-09-17 | 2008-08-29 | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 |
| JP2013024247A Pending JP2013082756A (ja) | 2004-09-17 | 2013-02-12 | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008222676A Withdrawn JP2009019048A (ja) | 2004-09-17 | 2008-08-29 | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 |
| JP2013024247A Pending JP2013082756A (ja) | 2004-09-17 | 2013-02-12 | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 |
Country Status (22)
| Country | Link |
|---|---|
| US (1) | US7329652B2 (ja) |
| EP (1) | EP1791830B1 (ja) |
| JP (3) | JP5116092B2 (ja) |
| KR (1) | KR20070057955A (ja) |
| CN (1) | CN101039933B (ja) |
| AT (1) | ATE493401T1 (ja) |
| AU (1) | AU2005286968A1 (ja) |
| CA (1) | CA2580610C (ja) |
| CY (1) | CY1112253T1 (ja) |
| DE (1) | DE602005025655D1 (ja) |
| DK (1) | DK1791830T3 (ja) |
| ES (1) | ES2359007T3 (ja) |
| IL (1) | IL181987A0 (ja) |
| MX (1) | MX2007003154A (ja) |
| NO (1) | NO20071915L (ja) |
| NZ (1) | NZ580450A (ja) |
| PL (1) | PL1791830T3 (ja) |
| PT (1) | PT1791830E (ja) |
| RU (1) | RU2443700C2 (ja) |
| SI (1) | SI1791830T1 (ja) |
| WO (1) | WO2006034116A1 (ja) |
| ZA (1) | ZA200702645B (ja) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008042639A1 (en) * | 2006-10-02 | 2008-04-10 | Irm Llc | Compounds and compositions as protein kinase inhibitors |
| WO2008083357A1 (en) * | 2006-12-29 | 2008-07-10 | Rigel Pharmaceuticals, Inc. | Bridged bicyclic aryl and bridged bicyclic heteroaryl substituted triazoles useful as axl inhibitors |
| US9650391B2 (en) * | 2006-12-29 | 2017-05-16 | Rigel Pharmaceuticals Inc. | N3-heteroaryl substituted triazoles and N5-heteroaryl substituted triazoles useful as Axl inhibitors |
| CN110551105B (zh) | 2006-12-29 | 2022-10-18 | 里格尔制药公司 | 用作axl抑制剂的取代三唑 |
| AU2014200824B2 (en) * | 2006-12-29 | 2016-12-15 | Rigel Pharmaceuticals, Inc. | Substituted triazoles useful as Axl inhibitors |
| SI2078010T1 (sl) * | 2006-12-29 | 2014-06-30 | Rigel Pharmaceuticals, Inc., | Policiklični heteroaril substituirani triazoli uporabni kot inhibitorji AXL |
| US7872000B2 (en) | 2006-12-29 | 2011-01-18 | Rigel Pharmaceuticals, Inc. | Bicyclic aryl and bicyclic heteroaryl substituted triazoles useful as Axl inhibitors |
| AU2016259396B2 (en) * | 2006-12-29 | 2018-11-08 | Rigel Pharmaceuticals, Inc. | Substituted triazoles useful as Axl inhibitors |
| KR20100021452A (ko) * | 2007-06-15 | 2010-02-24 | 아이알엠 엘엘씨 | 단백질 키나제 억제제 및 그의 사용 방법 |
| JO2784B1 (en) * | 2007-10-18 | 2014-03-15 | شركة جانسين فارماسوتيكا ان. في | 5,3,1 - Triazole substitute derivative |
| AU2008313776B2 (en) * | 2007-10-18 | 2013-12-05 | Janssen Pharmaceutica Nv | Trisubstituted 1,2,4-triazoles |
| SI2205592T1 (sl) * | 2007-10-26 | 2013-09-30 | Rigel Pharmaceuticals, Inc. | Triazoli substituirani s policikličnim arilom in triazoli substituirani s policikličnim heteroarilom uporabni kot Axl inhibitorji |
| US8778974B2 (en) * | 2008-03-19 | 2014-07-15 | Janssen Pharmaceutica Nv | Trisubstituted 1,2,4 triazoles |
| BRPI0912196A2 (pt) * | 2008-05-09 | 2015-10-06 | Janssen Pharmaceutica Nv | pirazóis trissubstituídos como moduladores do receptor de acetilcolina. |
| SI2328888T1 (sl) | 2008-07-09 | 2013-03-29 | Rigel Pharmaceuticals, Inc. | Premoščeni biciklični heteroaril substituirani triazoli, uporabni kot inhibitorji Axl |
| EP2387395B1 (en) | 2009-01-16 | 2014-10-15 | Rigel Pharmaceuticals, Inc. | Axl inhibitors for use in combination therapy for preventing, treating or managing metastatic cancer |
| CN102414207B (zh) * | 2009-06-09 | 2015-09-30 | 埃科特莱茵药品有限公司 | 氟化氨基三唑衍生物 |
| TW201204360A (en) | 2010-04-20 | 2012-02-01 | Ab Science | Treatment of multiple sclerosis with MASITINIB |
| CN106986863B (zh) | 2012-04-24 | 2019-12-31 | 沃泰克斯药物股份有限公司 | Dna-pk抑制剂 |
| WO2014013014A1 (en) | 2012-07-18 | 2014-01-23 | Fundació Privada Centre De Regulació Genòmica (Crg) | Jak inhibitors for activation of epidermal stem cell populations |
| CN105246883B (zh) | 2013-03-12 | 2017-07-21 | 沃泰克斯药物股份有限公司 | Dna‑pk抑制剂 |
| PL3424920T3 (pl) | 2013-10-17 | 2020-11-16 | Vertex Pharmaceuticals Incorporated | Kokryształy (S)-N-metylo-8-(1-((2'-metylo-4’,6'-dideutero-[4,5'-bipirymidyn]-6-ylo)amino)propan-2-ylo)chinolino-4-karboksyamidu i ich deuterowane pochodne jako inhibitory DNA-PK |
| WO2018041989A1 (en) | 2016-09-02 | 2018-03-08 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for diagnosing and treating refractory celiac disease type 2 |
| US11110108B2 (en) | 2016-09-27 | 2021-09-07 | Vertex Pharmaceuticals Incorporated | Method for treating cancer using a combination of DNA-damaging agents and DNA-PK inhibitors |
| WO2020188015A1 (en) | 2019-03-21 | 2020-09-24 | Onxeo | A dbait molecule in combination with kinase inhibitor for the treatment of cancer |
| US20220177978A1 (en) | 2019-04-02 | 2022-06-09 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods of predicting and preventing cancer in patients having premalignant lesions |
| EP3955920A1 (en) | 2019-04-16 | 2022-02-23 | Institut National de la Santé et de la Recherche Médicale (INSERM) | Use of jak inhibitors for the treatment of painful conditions involving nav1.7 channels |
| KR102133595B1 (ko) | 2019-05-31 | 2020-07-13 | 에이치케이이노엔 주식회사 | 단백질 키나제 억제제로서의 헤테로고리 화합물 |
| KR102112336B1 (ko) | 2019-08-12 | 2020-05-18 | 에이치케이이노엔 주식회사 | 단백질 키나제 억제제로서의 헤테로고리 화합물 |
| WO2021089791A1 (en) | 2019-11-08 | 2021-05-14 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for the treatment of cancers that have acquired resistance to kinase inhibitors |
| WO2021148581A1 (en) | 2020-01-22 | 2021-07-29 | Onxeo | Novel dbait molecule and its use |
| WO2023222565A1 (en) | 2022-05-16 | 2023-11-23 | Institut National de la Santé et de la Recherche Médicale | Methods for assessing the exhaustion of hematopoietic stems cells induced by chronic inflammation |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5637592A (en) * | 1994-07-12 | 1997-06-10 | Janssen Pharmaceutica N.V. | Acyl derivatives of azolones |
| GB9622363D0 (en) * | 1996-10-28 | 1997-01-08 | Celltech Therapeutics Ltd | Chemical compounds |
| KR20000075615A (ko) * | 1997-02-19 | 2000-12-26 | 벌렉스 래보라토리즈, 인크. | Nos 억제제로서의 n-헤테로시클릭 유도체 |
| RU2340611C2 (ru) * | 2000-09-15 | 2008-12-10 | Вертекс Фармасьютикалз Инкорпорейтед | Производные пиразола, используемые в качестве ингибиторов протеинкиназы |
| AU2003299472A1 (en) * | 2002-05-06 | 2004-07-22 | Vertex Pharmaceuticals Incorporated | Thiadiazoles or oxadiazoles and their use as inhibitors of JAK kinase |
| AR042052A1 (es) * | 2002-11-15 | 2005-06-08 | Vertex Pharma | Diaminotriazoles utiles como inhibidores de proteinquinasas |
| WO2004052280A2 (en) * | 2002-12-10 | 2004-06-24 | Imclone Systems Incorporated | Anti-angiogenic compounds and their use in cancer treatment |
| DE602004025258D1 (de) * | 2003-08-06 | 2010-03-11 | Vertex Pharma | Aminotriazol-verbindungen als proteinkinase-hemmer |
-
2005
- 2005-09-19 KR KR1020077008732A patent/KR20070057955A/ko not_active Application Discontinuation
- 2005-09-19 US US11/230,221 patent/US7329652B2/en not_active Expired - Fee Related
- 2005-09-19 ZA ZA200702645A patent/ZA200702645B/xx unknown
- 2005-09-19 AT AT05799808T patent/ATE493401T1/de active
- 2005-09-19 NZ NZ580450A patent/NZ580450A/en not_active IP Right Cessation
- 2005-09-19 AU AU2005286968A patent/AU2005286968A1/en not_active Abandoned
- 2005-09-19 EP EP05799808A patent/EP1791830B1/en active Active
- 2005-09-19 RU RU2007114293/04A patent/RU2443700C2/ru not_active IP Right Cessation
- 2005-09-19 SI SI200531255T patent/SI1791830T1/sl unknown
- 2005-09-19 DK DK05799808.0T patent/DK1791830T3/da active
- 2005-09-19 ES ES05799808T patent/ES2359007T3/es active Active
- 2005-09-19 PL PL05799808T patent/PL1791830T3/pl unknown
- 2005-09-19 WO PCT/US2005/033333 patent/WO2006034116A1/en active Application Filing
- 2005-09-19 JP JP2007532549A patent/JP5116092B2/ja not_active Expired - Fee Related
- 2005-09-19 CN CN2005800353178A patent/CN101039933B/zh not_active Expired - Fee Related
- 2005-09-19 DE DE602005025655T patent/DE602005025655D1/de active Active
- 2005-09-19 PT PT05799808T patent/PT1791830E/pt unknown
- 2005-09-19 MX MX2007003154A patent/MX2007003154A/es active IP Right Grant
- 2005-09-19 CA CA2580610A patent/CA2580610C/en not_active Expired - Fee Related
-
2007
- 2007-03-18 IL IL181987A patent/IL181987A0/en unknown
- 2007-04-16 NO NO20071915A patent/NO20071915L/no not_active Application Discontinuation
-
2008
- 2008-08-29 JP JP2008222676A patent/JP2009019048A/ja not_active Withdrawn
-
2011
- 2011-03-24 CY CY20111100321T patent/CY1112253T1/el unknown
-
2013
- 2013-02-12 JP JP2013024247A patent/JP2013082756A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| SI1791830T1 (sl) | 2011-05-31 |
| JP2013082756A (ja) | 2013-05-09 |
| RU2007114293A (ru) | 2008-10-27 |
| KR20070057955A (ko) | 2007-06-07 |
| CN101039933A (zh) | 2007-09-19 |
| CY1112253T1 (el) | 2015-12-09 |
| CN101039933B (zh) | 2012-06-06 |
| PL1791830T3 (pl) | 2011-05-31 |
| JP2009019048A (ja) | 2009-01-29 |
| NO20071915L (no) | 2007-05-18 |
| DE602005025655D1 (de) | 2011-02-10 |
| AU2005286968A1 (en) | 2006-03-30 |
| IL181987A0 (en) | 2007-07-04 |
| US7329652B2 (en) | 2008-02-12 |
| ZA200702645B (en) | 2008-08-27 |
| WO2006034116A1 (en) | 2006-03-30 |
| CA2580610C (en) | 2013-07-09 |
| RU2443700C2 (ru) | 2012-02-27 |
| NZ580450A (en) | 2011-06-30 |
| EP1791830B1 (en) | 2010-12-29 |
| ES2359007T3 (es) | 2011-05-17 |
| MX2007003154A (es) | 2007-05-15 |
| ATE493401T1 (de) | 2011-01-15 |
| PT1791830E (pt) | 2011-04-04 |
| US20060063756A1 (en) | 2006-03-23 |
| DK1791830T3 (da) | 2011-04-18 |
| JP2008513488A (ja) | 2008-05-01 |
| EP1791830A1 (en) | 2007-06-06 |
| CA2580610A1 (en) | 2006-03-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5116092B2 (ja) | プロテインキナーゼの阻害剤として有用なジアミノトリアゾール化合物 | |
| JP2008513488A5 (ja) | ||
| US8741912B2 (en) | Deazapurines useful as inhibitors of Janus kinases | |
| JP5227032B2 (ja) | プロテインキナーゼの阻害剤として有用なピロロピリミジン | |
| EP1485376B1 (en) | Compositions useful as inhibitors of protein kinases | |
| US7091343B2 (en) | Compositions useful as inhibitors of protein kinases | |
| EP1485380B1 (en) | Azolylaminoazines as inhibitors of protein kinases | |
| EP1485381B1 (en) | Azolylaminoazine as inhibitors of protein kinases | |
| AU2007207533B8 (en) | Azaindoles useful as inhibitors of Janus kinases | |
| EP1931674B1 (en) | Deazapurines useful as inhibitors of janus kinases | |
| US20060122185A1 (en) | Bicyclic inhibitors of Rho kinase | |
| US20040192696A1 (en) | Compositions useful as inhibitors of protein kinases | |
| JP2008528705A5 (ja) | ||
| US20150344481A1 (en) | Novel substituted imidazoles as casein kinase 1 d/e inhibitors | |
| AU2012205127B2 (en) | Diaminotriazole Compounds Useful as Protein Kinase Inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080829 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080829 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111215 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120314 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120322 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120413 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120420 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120514 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120521 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120615 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121011 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121012 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151026 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |