JP4818726B2 - 炎症性腸疾患の治療 - Google Patents
炎症性腸疾患の治療 Download PDFInfo
- Publication number
- JP4818726B2 JP4818726B2 JP2005501247A JP2005501247A JP4818726B2 JP 4818726 B2 JP4818726 B2 JP 4818726B2 JP 2005501247 A JP2005501247 A JP 2005501247A JP 2005501247 A JP2005501247 A JP 2005501247A JP 4818726 B2 JP4818726 B2 JP 4818726B2
- Authority
- JP
- Japan
- Prior art keywords
- colitis
- rats
- treatment
- inflammatory bowel
- bowel disease
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Oncology (AREA)
- Genetics & Genomics (AREA)
- Communicable Diseases (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本発明は、炎症性腸疾患の治療に関し、特に、G タンパク質結合レセプターの活性を調節する能力を有する新規環状ペプチドおよびペプチド疑似(peptidomimetic)化合物によるその症状の治療に関する。該化合物は、好ましくは、C5a レセプターのアンタゴニストとして作用し、多形核白血球およびマクロファージ上のC5aレセプターに対し作用する。
本明細書で引用する引用文献(特許または特許出願を含む)は全て引用により本明細書に含める。何れかの引用文献が従来技術を構成するとは認めがたい。引用文献の考察には著者の主張が述べられており、出願人は、該引用文献の正確さおよび適切さを変更する権利を留保する。多くの従来技術の刊行物を本明細書で引用しているが、これらの引用文献が、オーストラリアまたは何れか他の国において通常の一般的な知識の一部を形成するとは認めがたいことは明かであろう。
IBDにおける補体関与の知識が欠如しているため、我々は、大腸炎の動物モデルにおける特定の補体インヒビターの可能性ある抑制効果を試験した。我々は、C5a レセプターの特定のインヒビターは、ラットにおいて、トリニトロベンゼンスルホン酸(TNBS)-誘発大腸炎での損傷の徴候を改善できることをこの度初めて示す。このモデルは、IBDの病因を調査するのに広範囲に使用されている(Morris et al, 1989)。我々は、C3aおよびC5aの両方によるアンタゴニストに対する強力な保護効果を発見した。それは、IBDの仲介物としての補体に関する大きな役割であって従来明かとされていない該役割を示唆している。
a)G タンパク質-結合レセプターのアンタゴニストであり、
b)実質的にアゴニスト活性はなく、そして
c)式 Iの環状ペプチドまたはペプチド疑似化合物である、
化合物である、
ここで、AはH、アルキル、アリール、NH2、NH-アルキル、N(アルキル)2、NH-アリール、NH-アシル、NH-ベンゾイル、NHSO3、NHSO2-アルキル、NHSO2-アリール、OH、O-アルキル、またはO-アリールであり;
Bはアルキル、アリール、フェニル、ベンジル、ナフチルまたはインドール基、またはL-フェニルアラニンまたはL-フェニルグリシンのようなD-またはL-アミノ酸の側鎖であるが、グリシン、D-フェニルアラニン、L-ホモフェニルアラニン、L-トリプトファン、L-ホモトリプトファン、L-チロシン、またはL-ホモチロシンの側鎖ではなく;
Cはグリシン、アラニン、ロイシン、バリン、プロリン、ヒドロキシプロリン、またはチオプロリンのようなD-、L-またはホモ-アミノの側鎖のような小さな置換基であるが、 好ましくは、イソロイシン、フェニルアラニン、またはシクロヘキシルアラニンのような大きな(bulky)置換基ではなく、;
Dは、D-ロイシン、D-ホモロイシン、D-シクロヘキシルアラニン、D-ホモシクロヘキシルアラニン、D-バリン、D-ノルロイシン、D-ホモ-ノルロイシン、D-フェニルアラニン、D-テトラヒドロイソキノリン、D-グルタミン、D-グルタミン酸、またはD-チロシンのような中性D-アミノ酸の側鎖であるが、好ましくは、グリシンまたはD-アラニンの側鎖のような小さな置換基、D-トリプトファンのような大きな平面的(bulky planar)側鎖、またはD-アルギニンまたはD-リシンのような大きな荷電性(bulky charged)側鎖ではなく;
Eは、L-フェニルアラニン、L-トリプトファンおよびL-ホモトリプトファンからなる群から選択されるアミノ酸の側鎖のような大きな置換基であるか、またはL-1-ナフチルまたはL-3-ベンゾチエニルアラニンであるが、D-トリプトファン、L-N-メチルトリプトファン、L-ホモフェニルアラニン、L-2-ナフチルL-テトラヒドロイソキノリン、L-シクロヘキシルアラニン、D-ロイシン、L-フルオレニルアラニン、またはL-ヒスチジンの側鎖ではなく;
FはL-アルギニン、L-ホモアルギニン、L-シトルリン、またはL-カナバニンの側鎖、またはそれらのバイオイソスター(bioisostere)であり、すなわち、末端グアニジンまたは尿素基が保持されている側鎖であるが、炭素バックボーンは、異なる構造を有する基で置換され、それによって側鎖は、親基と同じ方法で標的タンパク質と全体的に反応し;そして
Xは-(CH2)nNH-または(CH2)n-S-(ここでnは1から4、好ましくは、2または3の整数である);-(CH2)2O-;-(CH2)3O-;-(CH2)3-;-(CH2)4-;-CH2COCHRNH-;または-CH2CHCOCHRNH-(ここで、Rは通常または通常でないアミノ酸の側鎖である)である。
図1は8日間にわたる死亡率への影響を示す。pre = 治療前; post = 治療後
図2は摂食量への影響を示す。摂食した食物の量を24h[A]または8日[B]の何れかの後、測定した。データは平均±SEM(n = 4-12)を示す。*P < 0.05 薬物-処置ラット対大腸炎対照。pre = 治療前; post = 治療後
図3は体重への影響を示す。TNBS 投与後の体重の変化を[A]24hまたは[B]8日の何れかの後、測定した。データは平均±SEM(n = 4-12)を示す。*P < 0.05 薬物-処置ラット対大腸炎対照。 pre = 治療前; post = 治療後.
図4は臨床的な肉眼によるスコアを要約したものである。大腸は、[A]24hまたは[B]8日の何れかにおいて、0-13のスケールで肉眼により損傷をスコアした。データは平均±SEM(n = 4-12)を示す。*P < 0.05 薬物-処置ラット対大腸炎対照。 pre = 治療前; post = 治療後.
図5は大腸ミエロペルオキシダーゼ(MPO)レベルへの影響を示す。ラットの大腸におけるMPOのレベルを[A]24hまたは[B]8日の何れかで測定した。データは平均±SEM (n = 4-12)を示す。*P < 0.05 薬物-処置ラット対大腸炎対照。 pre = 治療前; post = 治療後
図6は24hおよび8日の研究における大腸浮腫レベルへの影響を示す。[A]24h;[B]8日。データは平均± SEM (n = 4-12)を示す。*P < 0.05 薬物-処置ラット対大腸炎対照。 pre = 治療前; post = 治療後.
図7は8日後の血清および大腸のTNF-αレベルへの影響を示す。データは平均±SEM(n = 4-12)を示す。[A]血清;[B]大腸組織。*P < 0.05 薬物-処置ラット対大腸炎対照。 pre = 治療前; post = 治療後.
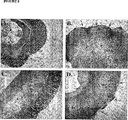
図8はヘマトキシリンおよびエオシンで染色した8日の研究におけるラットの大腸の切片を示す(x 40倍)。画像は各研究対象群のうちの典型および代表的なものである。
[A]未処置の上皮および粘膜層(ML)を有する、生理食塩水注射し偽処置した(sham-operated)ラット;
[B]炎症性細胞(IC)浸潤、浮腫(E)、およびML構造の完全破壊(矢印で示す)を含む、広範囲の損傷を有するTNBS薬物-フリーの大腸炎対照ラット;
[C]IC浸潤およびEを有するが、MLは未処置である、TNBS C5aアンタゴニスト(10 mg/kg/日、経口)処置後ラット;および
[D]IC浸潤、E、広範囲の出血(H)およびMLの糜爛(矢印で示す)を有するTNBSプレドニゾロン(1 mg/kg/日、SC)処置後ラット
この発明は、本明細書に記載の特定の材料および方法に限られるものでないことは明らかに理解される。これらは、変化し得るためである。また、本明細書で使用する用語は特定の実施態様のみを記載することを意図していることが理解され、本発明の範囲を限定することを目的とするものではなく、それは、特許請求の範囲によってのみ制限される。
Cit シトルリン
dCha D-シクロヘキシルアミン
DPhe D-フェニルアラニン
IBD 炎症性腸疾患
ip 腹腔内
iv 静脈内
LPS リポ多糖類
MPO ミエロペルオキシダーゼ
PMN 多形核顆粒球
PMSF フェニルメチルスルホニルフルオリド
Pr 経直腸的
sc 皮下的
TNBS トリニトロベンゼンスルホン酸
TNF-α 腫瘍壊死因子-α
本明細書では、通常、一文字表記および三文字表記のコードを用い、アミノ酸を表す。
ペプチド合成
式 Iの環状ペプチド化合物は、先の我々の出願、出願番号PCT/AU98/00490およびPCT/AU02/01427に詳細に記載する方法により調製される。他の合成方法は、オーストラリア仮出願番号2003902743に記載している。これらの明細書の開示は全て引用により本明細書に含める。本発明は、化合物 AcF-[OPdChaWR] (PMX53)(その相当する直鎖状ペプチドはAc-Phe-Orn-Pro-dCha-Trp-Argである)に関して特に開示しているが、本発明はその化合物に限定しないことが明らかに理解されるだろう。
ヒトC5aレセプターアンタゴニストAcF-[OPdChaWR](AcPhe[Orn-Pro-D-シクロヘキシルアラニン-Trp-Arg])を上記のように合成し、逆相HPLCで精製し、そして質量分析およびプロトンNMR分光法で十分に特性解析した。C5aアンタゴニストを経口投与用にオリーブオイル中(10 mg/mL)に調製し、およびSC投与用に30% ポリエチレングリコール溶液中(0.6 mg/mL)に調製した。C3aアンタゴニストSB 290157(Ph2CHCH2OCH2CO-Arg-OH)は先に詳細に記載している(Ames at al, 2001)。それを合成し、逆相HPLCで精製し、質量分光法およびNMR分光法で特性解析した。それを、IP注射用に50% プロピレングリコール溶液中(30 mg/kg)に調製した。グルココルチコステロイド、プレドニゾロン(Sigma、U.S.A.)をSC投与用に30% ポリエチレングリコール溶液中に調製した。TNF-αインヒビターインフリキシマブ(Remicade(登録商標))をIV投与用の指示書通りに滅菌生理食塩水中(3 mg/mL)に調製した。TNBS-誘発大腸炎を有するラットにおけるプロピレングリコールまたはポリエチレングリコールでは、抗-炎症性効果は観察されなかった。
アッセイは、50 mM HEPES、1 mM CaCl2、5 mM MgCl2、0.5% ウシ血清アルブミン、0.1% バシトラシンおよび100 μM フェニルメチルスルホニルフルオリド(PMSF)の緩衝液を用い、先に記載した(Sanderson et al, 1995)ように単離した新しいヒトPMNで行う。4℃で行ったアッセイでは、緩衝液、非標識ヒト組み換えC5a (Sigma)またはペプチド、Hunter/Bolton標識125I-C5a(〜20pM)(New England Nuclear, MA)およびPMN(0.2 x 106)を、最終体積200μL/ウェルのMillipore Multiscreenアッセイプレート(HV 0.45)に連続的に加える。4℃で60分間のインキュベーション後、サンプルを濾過し、プレートを緩衝液で一度洗浄する。フィルターを乾燥させ、穴を開け、LKBガンマカウンターでカウントする。非特異的な結合は、全結合の10-15%を典型的に生ずる1mM ペプチドまたは100 nM C5aの包含により評価した。
細胞は、先に記載(Sanderson et al, 1995)のように単離し、サイトカラシン Bと共にインキュベーションする(5μg/mL、15分間、37℃)。0.15% ゼラチンおよびペプチドを含むハンクス平衡塩溶液を96ウェルプレートに追加し(全体積100 μL/ウェル)、その後、25μL 細胞(4x106/mL)を加える。C5aに対抗する、それぞれのペプチドの能力を評価するために、それぞれのペプチドと共に細胞を5分間37℃でインキュベーションし、その後、C5a (100 nM)を添加し、更に5分間インキュベーションする。次いで、リン酸ナトリウム50 μL(0.1M、pH 6.8)を各ウェルに添加し、そのプレートを室温に冷却し、等量のジメトキシベンジジン (5.7 mg/mL)およびH2O2(0.51%)の新しい混合物25 μLを各ウェルに添加する。反応は、2%アジドナトリウムを加え10分で終了する。吸光度は、コントロール値(ペプチドなし)で校正したBioscan 450プレートリーダーで、450 nmで測定し、非線形回帰により分析する。
炎症性腸疾患に対するPMX53の効果
IBDにおける補体関与の知識が現在、欠如しているため、我々はラットのトリニトロベンゼンスルホン酸(TNBS)-誘発大腸炎におけるPMX53(AcF-[OPdChaWR])よる可能な抑制効果を試験することを目的とした。比較のため、我々はまた、C3aアンタゴニスト SB 290157 (Ames et, 2001)、コルチコステロイドプレドニゾロン、およびTNF-α抗体インフリキシマブの効率を試験した。
(a) PMX53 (オリーブオイル中、10mg/kg、経口),
(b) PMX53 (30% ポリエチレングリコール中、0.3mg/kg、皮下的)、
(c) C3a アンタゴニスト (30 mg/kg、1日2回(bid)、IP)、
(d) プレドニゾロン (80% ポリエチレングリコール中、1mg/kg、皮下的)、
(e) PMX53 (オリーブオイル中、10mg/kg、経口)、およびプレドニゾロン (80% ポリエチレングリコール中、1mg/kg、皮下的)の組合せ、および
(f) インフリキシマブ (生理食塩水中、1mg/kg、静脈内)。
(a) PMX53 (オリーブオイル中、10mg/kg、経口、誘発前および誘発後の両方)、
(b) PMX53 (30% ポリエチレングリコール中、0.3mg/kg、皮下的、誘発前のみ)、
(c) PMX53 (オリーブオイル中、1mg/kg、経口、誘発後のみ)、
(d) プレドニゾロン (80% ポリエチレングリコール中、1mg/kg、皮下的、誘発前および誘発後の両方)、
(e) PMX53 (オリーブオイル中、10mg/kg、経口)およびプレドニゾロン (80% ポリエチレングリコール中、1mg/kg、皮下的)(誘発前のみ)の組合せ、および
(f) インフリキシマブ (生理食塩水中、1mg/kg、静脈内、誘発前のみ)。
潰瘍化 下痢 癒着
0-損傷なし 0-なし 0-なし
1-病巣の充血 1-軽い 1-軽い
2-充血および腸の肥大化 2-酷い 2-酷い
3-1部位での潰瘍化
4-2部位での潰瘍化
5->1cmの潰瘍化
6-10->2cmの潰瘍化;
1 cm増える毎にスコアが増す。
図 1に示すように、薬物-フリーのラットにおける大腸炎の誘発により、TNBS 投与後最初の2日で、死亡率は高くなり、39%となった。プレドニゾロン後処置を除くすべての薬物治療により、薬物-フリーの大腸炎対照ラット(n = 13)と比較すると死亡率(n = 8-16)は低下した。死亡なしは、偽処置した動物(n = 4)で記録した。誘発前(10 mg/kg/日 経口および0.3 mg/kg/日 SC)または誘発後24時間後(1または10 mg/kg/日 経口)の何れかにC5aアンタゴニストで処置したラットでは、生存率は改善し、死亡率は20%以下となった。コルチコステロイドプレドニゾロン(1 mg/kg/日 SC)で前処置したラットでは、死亡率は同様に減少し、11%となった;しかしながら、プレドニゾロンによる後処置では、死亡率の減少において有意な効果はなかった。インフリキシマブ前処置(3 mg/kg IV)により、死亡率は20%に減少し、それは、C5a アンタゴニスト(10mg/kg 経口または0.3mg/kg SC)またはプレドニゾロン前処置ほどは効果はなかった。C5a アンタゴニスト (10 mg/kg/日 経口)およびプレドニゾロン (1 mg/kg/日 SC)の組合せにより前治療したラットでは、または0.3mg/kg SCのC5a アンタゴニストで前処置したラットでは死亡は見られなかった。
薬物治療24時間後、薬物-フリーの大腸炎対照ラットと比較すると食べ物の消費で有意な改善は見られなかった。8日後、プレドニゾロン後処置ラットを除く全ての薬物-処置ラットは、薬物-フリーの大腸炎対照ラットよりも食べ物を顕著に多く食べた。図 2Aに示すように、大腸炎誘発により、24時間後、偽処置したラットと比較すると全てのTNBS-投与ラットで食べ物の消費が減少した。24時間を超えると、薬物治療により摂取が顕著に改善することはなかった。
体重減少における顕著な減少は、薬物-フリーの大腸炎対照ラットと比較すると薬物治療後24時間後では、見られなかった。8日後、C5a アンタゴニストで処置したラットのみが、薬物-フリーの大腸炎対照ラットと比較すると顕著に体重が重かった。TNBSを受けた全てのラットで、図3Aに示すように、偽処置したラットと比較すると誘発後24時間で相当に体重減少した。薬物治療は、24時間を超えるとこの体重減少に顕著に影響を与えることはなかった。
大腸は、先に確立されたスコアリングシステム(Bobin-Dubigeon et al, 2001)を用い、ブラインド法で、独立した観察者により、出血および潰瘍化の徴候を肉眼で検査した。24時間後、インフリキシマブを除く全ての薬物治療により、薬物-フリーの大腸炎対照ラットと比較すると肉眼によるスコアに顕著な改善が得られた。8日後、プレドニゾロン後処置を除く全ての薬物治療により、薬物-フリーの大腸炎対照ラットと比較すると肉眼によるスコアに顕著な改善が得られた。偽処置した動物では肉眼で明らかな損傷は見られなかった。
24時間後、C5a アンタゴニストまたはC5a アンタゴニストおよびプレドニゾロンの組合せの何れかで処置したラットのみが、薬物-フリーの大腸炎対照ラットと比較すると大腸 MPO レベルで有意な改善があった。8日後、プレドニゾロン後処置を除く全ての薬物治療により、薬物-フリーの大腸炎対照ラットと比較すると大腸MPOレベルにおいて有意な改善があった。図 5Aに示すように、薬物-フリーのラットの大腸におけるMPOのレベルは、24時間で、偽処置したラットよりも実質的に高くなった。この酵素のレベルは、24時間後、全ての薬物-処置ラットにおいて減少し、C5a アンタゴニスト(10 mg/kg/日 経口または0.3 mg/kg/日 SC)またはC5a アンタゴニスト (10 mg/kg/日 経口)およびプレドニゾロン (1 mg/kg/日 SC)の組合せの何れかで前処置したラットで有意な改善があった(P < 0.05)。
乾燥重量に対する湿重量の比により測定される大腸の浮腫は、24時間または8日の何れかで測定した。その結果を図 6に示す。24時間および8日の両方の後、C5a アンタゴニスト、またはC5a アンタゴニストおよびプレドニゾロンの組合せの何れかで処置したラットのみで、薬物-フリーの大腸炎対照ラットと比較すると、大腸の乾燥重量に対する湿重量の比において有意な改善があった。図 6Aに示すように、TNBS-投与したラットの大腸の乾燥重量に対する湿重量の比は、24時間後、偽処置したラットと比較すると相当に増大し、これは浮腫を示す。この時点において、C5a アンタゴニスト (10 mg/kg/日 経口または0.3 mg/kg/日 SC)またはC5a アンタゴニスト (10 mg/kg/日 経口)およびプレドニゾロン (1 mg/kg/日 SC)の組合せで前処置したラットのみで、大腸炎対照ラットと比較すると乾燥重量に対する湿重量の比に有意な減少があった(P < 0.05)。C3a アンタゴニストは顕著な効果を有していなかった。
次いで、8日後、血清または大腸組織の何れかのTNF-αレベルを測定した。その結果を図 7に示す。薬物-フリーの大腸炎対照動物においてTNF-αの血清レベルが増加し、全ての薬物治療によりこれらのレベルは顕著に減少した。プレドニゾロン後処置を除く全ての薬物治療により、薬物-フリーの大腸炎対照ラットと比較すると大腸のTNF-αレベルは顕著に改善した。血清TNF-αおよび大腸組織TNF-αのレベルは24時間後、偽処置したラットと比較するとTNBS-処置ラットでは増加しなかった。図 7Aに示すように、8日後、大腸炎対照ラットの血清TNF-αレベルは、偽処置したラットと比較すると増加した。全ての薬物-処置ラットは、偽処置したラットに類似の血清TNF-αレベルを有しており、これらのレベルは大腸炎対照レベルと比較すると有意に減少した(P < 0.05)。図 7Bに示す大腸組織ホモジネートTNF-αレベルはまた、偽処置した動物と比較すると薬物-フリーのラットにおいて増加した。全ての薬物-処置ラットでは、顕著な低下はなかった(P > 0.05)プレドニゾロン後処置ラット(1 mg/kg/日 SC)を除いて、大腸炎対照ラットと比較するとこのサイトカインの組織レベルは顕著に低下した(P < 0.05)。
大腸の染色した切片を、ブラインド法で、独立した観察者により病状の徴候について試験した。TNBS投与後24時間で、大腸の切片では急性の炎症の徴候が見られた。軽いケースでは、腸の粘膜下組織層に浮腫があり、主に好中球による粘膜および粘膜下組織中への浸潤があった。より酷いケースでは、大腸の粘膜の細胞のネクローシス、およびより酷い浮腫および炎症性細胞の浸潤があった。この短時間の時間枠では、薬物-フリーの大腸炎対照ラットと比較すると薬物-処置ラットの大腸の切片で注目すべき改善は見られなかった。
動物モデルにおける更なる研究
PMX205: ヒドロ桂皮酸-[OPdChaWR]
PMX73: AcF-[OPdPheWR]
PMX201: AcF-[OPdChaWCitrulline]
これらの化合物を、8日研究において、0.3、1、3および10 mg/kg/日、後処置で投与する。
臨床的効力の評価
動物モデルにおいて有効であることが判った化合物のヒトにおける臨床的効力を、標準的な臨床的試験方法を用い測定する。
環状ペプチドには、薬物候補としての環状ペプチドを超える幾つかの重要な利点がある(Fairlie et al 1995, Fairlie et al, 1998, Tyndall and Fairlie, 2001)。この明細書に記載の環状化合物は、ヒトの血液または血漿、ヒトまたはラットの胃液中、またはペプシン、トリプシンおよびキモトリプシンのような消化酵素の存在下での、37℃で少なくとも数時間のタンパク質分解に対して安定である。対照的に、L-アミノ酸からなる短い直鎖状ペプチドは、これらの条件下で直ちに分解され数分以内にコンポーネントのアミノ酸となる。第二の利点は環状および非ペプチド性分子により形成される束縛された単一のコンホメーションにあり、これは、レセプター結合に必要な構造以外に溶液中で複数の構造となるのに十分にフレキシブルである非環状または直鎖状のペプチドとは対照的である。第三に本発明で記載される化合物のような環状化合物は、通常、より脂質可溶性であり、あまり経口的に投与され得ない非環式ペプチドよりも、薬物として、より薬理学的に生物利用可能である。第四に、環状分子の血漿半減期は、通常、ペプチドよりも長くなる。
Ames RS, Lee D, Foley JJ, Jurewicz AJ, Tornetta MA, Bautsch W, Settmacher B, Klos A, Erhard KF, Cousins RD, Sulpizio AC, Hieble JP, McCafferty G, Ward KW, Adams JL, Bondinell WE, Underwood DC, Osborn RR, Badger AM, Sarau HM. J Immunol. 2001,166(10):6341-8.
Fairlie, D. P., Wong, A. K.; West, M. W. Curr. Med. Chem., 1998, 5, 29-62.
Fairlie, D.P., Abbenante, G. and March, D. Curr. Med. Chem., 1995 2 672-705.
Gerard, C and Gerard, N.P. Ann. Rev. Immunol., 1994 12 775-808.
German, A.J., Hall, E.J., and Day, M.J. J Vet Intern Med. 2003 Jan-Feb;17(1):8-20.
Konteatis, Z.D., Siciliano, S.J., Van Riper, G., Molineaux, C.J., Pandya, S., Fischer, P., Rosen, H., Mumford, R.A., and Springer, M.S. J. Immunol., 1994 153 4200-4204.
Mollnes TE, Brekke OL, Fung M, Fure H, Christiansen D, Bergseth G, Videm V, Lappegard KT, Kohl J, Lambris JD. Blood. 2002 Sep 1;100(5):1869-77.
Morris GP, Beck PL, Herridge MS, Depew WT, Szewczuk MR, Wallace JL. Gastroenterol. 1989;96:795-803.
Nielsen OH, Rask-Madsen J. Scand J Gastroenterol Suppl. 1996;31:149-159.
Sanderson, S.D., Kirnarsky, L., Sherman, S.A., Vogen, S.M., Prakesh, O., Ember, J.A., Finch, A.M. and Taylor, S.M. J. Med. Chem., 1995 38 3669-3675.
Tams, T.R. Vet Clin North Am Small Anim Pract., 1993 23:569-86.
Tyndall, J. D. A.; Fairlie, D. P. Curr. Med. Chem. 2001, 8, 893-907.
Claims (11)
- AcPhe[Orn-Pro-D-シクロヘキシルアラニン-Trp-Arg]を含む炎症性腸疾患を治療するための医薬組成物。
- 炎症性腸疾患の治療用の1以上の他の薬剤と共に使用される、請求項1記載の医薬組成物。
- 他の薬剤がインフリキシマブであるか、またはC3aのインヒビターである、請求項2の医薬組成物。
- 治療が、炎症性腸疾患の急性の再発の予防または緩和である、請求項1から3の何れか1項記載の医薬組成物。
- 治療が、炎症性腸疾患の原発性の発生の予防または緩和である、請求項1から3の何れか1項記載の医薬組成物。
- 炎症性腸疾患が、潰瘍性大腸炎、クローン病、リンパ球性−形質球性類腸炎、腹腔の疾患、コラーゲン性大腸炎、リンパ球性大腸炎およびエオシン好性の全腸炎、不定型大腸炎、感染性大腸炎、偽膜性大腸炎(壊死性大腸炎)、および虚血性炎症性腸疾患からなる群から選択される、請求項1から5の何れか1項記載の医薬組成物。
- 炎症性腸疾患が潰瘍性大腸炎である、請求項1から5の何れか1項記載の医薬組成物。
- 炎症性腸疾患がクローン病である、請求項1から5の何れか1項記載の医薬組成物。
- 炎症性腸疾患が全腸炎、イヌ科の形質細胞性−リンパ球性大腸炎、プロトセカ属性大腸炎、および組織球潰瘍性大腸炎からなる群から選択される、請求項1から5の何れか1項記載の医薬組成物。
- 腸溶性カプセルでまたは経直腸的に投与される、請求項1から7の何れか1項記載の医薬組成物。
- 炎症性腸疾患の治療用の医薬の製造における、AcPhe[Orn-Pro-D-シクロヘキシルアラニン-Trp-Arg]の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2002952084 | 2002-10-16 | ||
| AU2002952084A AU2002952084A0 (en) | 2002-10-16 | 2002-10-16 | Treatment of inflammatory bowel disease |
| AU2003902452A AU2003902452A0 (en) | 2003-05-20 | 2003-05-20 | Treatment of inflammatory bowel disease |
| AU2003902452 | 2003-05-20 | ||
| PCT/AU2003/001365 WO2004035078A1 (en) | 2002-10-16 | 2003-10-15 | Treatment of inflammatory bowel disease |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2006505621A JP2006505621A (ja) | 2006-02-16 |
| JP2006505621A5 JP2006505621A5 (ja) | 2006-11-24 |
| JP4818726B2 true JP4818726B2 (ja) | 2011-11-16 |
Family
ID=32108554
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005501247A Expired - Fee Related JP4818726B2 (ja) | 2002-10-16 | 2003-10-15 | 炎症性腸疾患の治療 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US7410945B2 (ja) |
| EP (1) | EP1558277B1 (ja) |
| JP (1) | JP4818726B2 (ja) |
| AT (1) | ATE509632T1 (ja) |
| CA (1) | CA2542507C (ja) |
| WO (1) | WO2004035078A1 (ja) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AUPS160602A0 (en) * | 2002-04-08 | 2002-05-16 | University Of Queensland, The | Therapeutic method |
| AU2002952086A0 (en) * | 2002-10-16 | 2002-11-07 | The University Of Queensland | Treatment of osteoarthritis |
| JP4818726B2 (ja) * | 2002-10-16 | 2011-11-16 | プロミクス・プロプライエタリー・リミテッド | 炎症性腸疾患の治療 |
| US7885748B2 (en) * | 2006-09-13 | 2011-02-08 | Gm Global Technology Operations, Inc. | Virtual accelerometer |
| RU2465272C2 (ru) | 2007-09-10 | 2012-10-27 | КалсиМедика, Инк. | Соединения, моделирующие внутриклеточный кальций |
| WO2009052489A2 (en) * | 2007-10-19 | 2009-04-23 | Alba Therapeutics Corporation | Novel inhibitors of mammalian tight junction opening |
| SG157299A1 (en) * | 2008-05-09 | 2009-12-29 | Agency Science Tech & Res | Diagnosis and treatment of kawasaki disease |
| AU2009288245B2 (en) * | 2008-08-27 | 2012-12-20 | Calcimedica, Inc. | Compounds that modulate intracellular calcium |
| US8524763B2 (en) * | 2008-09-22 | 2013-09-03 | Calcimedica, Inc. | Inhibitors of store operated calcium release |
| EP2477982A4 (en) | 2009-09-16 | 2013-04-03 | Calcimedica Inc | COMPOUNDS THAT MODULATE INTRACELLULAR CALCIUM |
| WO2019075319A1 (en) * | 2017-10-12 | 2019-04-18 | Board Of Regents, The University Of Texas System | COMPOSITIONS AND METHODS FOR TREATING PAIN IN WOMEN |
| CN116115582B (zh) * | 2022-11-10 | 2024-04-16 | 重庆大学 | 前药封装的工程化益生菌及其制备方法与应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11507215A (ja) * | 1995-06-05 | 1999-06-29 | ノバルティス・アクチエンゲゼルシャフト | アゴニスト活性を実質的にもたないC5a受容体アンタゴニストおよび製造方法 |
| WO2002004993A2 (en) * | 2000-07-10 | 2002-01-17 | Intel Corporation | Micromechanical diffraction phase grating |
| JP2002508767A (ja) * | 1997-06-25 | 2002-03-19 | ザ・ユニバーシティ・オブ・クイーンズランド | C5a受容体およびGタンパク質結合受容体の環状アゴニストおよびアンタゴニスト |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5807824A (en) * | 1993-12-06 | 1998-09-15 | Ciba-Geigy Corporation | C5A receptor antagonists having substantially no agonist activity |
| EP0749488A1 (en) * | 1994-03-03 | 1996-12-27 | Genentech, Inc. | Anti-il-8 monoclonal antibodies for treatment of inflammatory disorders |
| US5614370A (en) * | 1994-03-18 | 1997-03-25 | Merck & Co., Inc. | Assay to identify human C5a antagonists and agonists |
| SE9701219D0 (sv) * | 1997-04-04 | 1997-04-04 | Astra Pharma Prod | New compounds |
| AUPR833401A0 (en) * | 2001-10-17 | 2001-11-08 | University Of Queensland, The | G protein-coupled receptor antagonists |
| AUPS160602A0 (en) * | 2002-04-08 | 2002-05-16 | University Of Queensland, The | Therapeutic method |
| JP4818726B2 (ja) * | 2002-10-16 | 2011-11-16 | プロミクス・プロプライエタリー・リミテッド | 炎症性腸疾患の治療 |
| AU2002952086A0 (en) * | 2002-10-16 | 2002-11-07 | The University Of Queensland | Treatment of osteoarthritis |
| AU2003902586A0 (en) * | 2003-05-26 | 2003-06-12 | The University Of Queensland | Treatment of burns |
| US7910945B2 (en) * | 2006-06-30 | 2011-03-22 | Cree, Inc. | Nickel tin bonding system with barrier layer for semiconductor wafers and devices |
-
2003
- 2003-10-15 JP JP2005501247A patent/JP4818726B2/ja not_active Expired - Fee Related
- 2003-10-15 EP EP03750165A patent/EP1558277B1/en not_active Expired - Lifetime
- 2003-10-15 AT AT03750165T patent/ATE509632T1/de not_active IP Right Cessation
- 2003-10-15 CA CA2542507A patent/CA2542507C/en not_active Expired - Fee Related
- 2003-10-15 WO PCT/AU2003/001365 patent/WO2004035078A1/en active Application Filing
- 2003-10-15 US US10/531,564 patent/US7410945B2/en not_active Expired - Fee Related
-
2008
- 2008-06-23 US US12/144,266 patent/US20090004264A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11507215A (ja) * | 1995-06-05 | 1999-06-29 | ノバルティス・アクチエンゲゼルシャフト | アゴニスト活性を実質的にもたないC5a受容体アンタゴニストおよび製造方法 |
| JP2002508767A (ja) * | 1997-06-25 | 2002-03-19 | ザ・ユニバーシティ・オブ・クイーンズランド | C5a受容体およびGタンパク質結合受容体の環状アゴニストおよびアンタゴニスト |
| WO2002004993A2 (en) * | 2000-07-10 | 2002-01-17 | Intel Corporation | Micromechanical diffraction phase grating |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2004035078A1 (en) | 2004-04-29 |
| US20090004264A1 (en) | 2009-01-01 |
| US7410945B2 (en) | 2008-08-12 |
| ATE509632T1 (de) | 2011-06-15 |
| JP2006505621A (ja) | 2006-02-16 |
| CA2542507C (en) | 2013-04-16 |
| EP1558277A1 (en) | 2005-08-03 |
| CA2542507A1 (en) | 2004-04-29 |
| EP1558277B1 (en) | 2011-05-18 |
| EP1558277A4 (en) | 2009-07-29 |
| US20060135411A1 (en) | 2006-06-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20090004264A1 (en) | Methods for treating and ameliorating the symptons of inflammatory bowel diseases | |
| US9376381B2 (en) | High penetration prodrug compositions of peptides and peptide-related compounds | |
| US7579432B2 (en) | Cyclic peptides as G-protein-coupled receptor antagonists | |
| RU2627065C2 (ru) | Пролекарственные композиции с высокой степенью проникновения на основе пептидов и родственных пептидам соединений | |
| US20100267639A1 (en) | Treatment of osteoarthritis | |
| US20030114514A1 (en) | Pharmaceutical compositions containing anti-beta 1 integrin compounds and uses | |
| JP2011241214A (ja) | 線維症の処置におけるC5a受容体アンタゴニストの使用 | |
| KR20070036033A (ko) | 보체 C5a 수용체 조절제를 이용한 신경계 증상의치료방법 | |
| KR20170102005A (ko) | 폴리믹신 유도체 및 이의 용도 | |
| WO2001056994A1 (en) | Integrin antagonists | |
| JP2002528388A (ja) | 環改変された環状ペプチドアナログ | |
| EP2358740A1 (en) | Cyclic peptides and uses thereof | |
| JP2006528208A (ja) | コンプリメント5a受容体阻害剤を使用する出血ショックの処置 | |
| AU2003269602B2 (en) | Treatment of inflammatory bowel disease | |
| AU2003269602A1 (en) | Treatment of inflammatory bowel disease | |
| US20070021329A1 (en) | Treatment of hypersensitivity conditions | |
| ES2366538T3 (es) | Tratamiento de la enfermedad inflamatoria intestinal. | |
| JP2006528209A (ja) | 火傷に対する二次的な全身的損傷の処置方法 | |
| AU2003266862B2 (en) | Treatment of hypersensitivity conditions | |
| TW202317598A (zh) | 具有抗微生物活性的胜肽 | |
| AU2003266862A1 (en) | Treatment of hypersensitivity conditions | |
| AU2004241673A1 (en) | Method of treatment of systemic injury secondary to burns |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060929 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060929 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091222 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100323 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100330 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100622 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101207 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20110127 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110209 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110222 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110606 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110809 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110831 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140909 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |