JP4666190B2 - レジスト材料及びパターン形成方法 - Google Patents
レジスト材料及びパターン形成方法 Download PDFInfo
- Publication number
- JP4666190B2 JP4666190B2 JP2008279231A JP2008279231A JP4666190B2 JP 4666190 B2 JP4666190 B2 JP 4666190B2 JP 2008279231 A JP2008279231 A JP 2008279231A JP 2008279231 A JP2008279231 A JP 2008279231A JP 4666190 B2 JP4666190 B2 JP 4666190B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- atom
- carbon atoms
- hydrogen atom
- branched
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC(C)(C(C)(*)C1(F)F)OC1(C(F)(F)F)OC(*)=O Chemical compound CC(C)(C(C)(*)C1(F)F)OC1(C(F)(F)F)OC(*)=O 0.000 description 4
- BFWRATBLEKZUPB-UHFFFAOYSA-N CC1(C)C2(C)[I](C)CC1CC2 Chemical compound CC1(C)C2(C)[I](C)CC1CC2 BFWRATBLEKZUPB-UHFFFAOYSA-N 0.000 description 1
- BDYRLGDOHAHCIJ-UHFFFAOYSA-N C[I]1C(C2)C(C3CC4CC3)C4C2C1 Chemical compound C[I]1C(C2)C(C3CC4CC3)C4C2C1 BDYRLGDOHAHCIJ-UHFFFAOYSA-N 0.000 description 1
- KKXNZEHOOCSAJT-UHFFFAOYSA-N C[I]1C(C2)C(CCC3)C3C2C1 Chemical compound C[I]1C(C2)C(CCC3)C3C2C1 KKXNZEHOOCSAJT-UHFFFAOYSA-N 0.000 description 1
- WUKXIXOFXAASEC-UHFFFAOYSA-N C[I]1C(CC2)CC2C1 Chemical compound C[I]1C(CC2)CC2C1 WUKXIXOFXAASEC-UHFFFAOYSA-N 0.000 description 1
Landscapes
- Photosensitive Polymer And Photoresist Processing (AREA)
- Exposure And Positioning Against Photoresist Photosensitive Materials (AREA)
- Materials For Photolithography (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
請求項1:
(A)下記一般式(1)で表される繰り返し単位を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
請求項2:
(A)下記一般式(2)で表される繰り返し単位を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
請求項3:
(A)下記一般式(3)で表される繰り返し単位を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
請求項4:
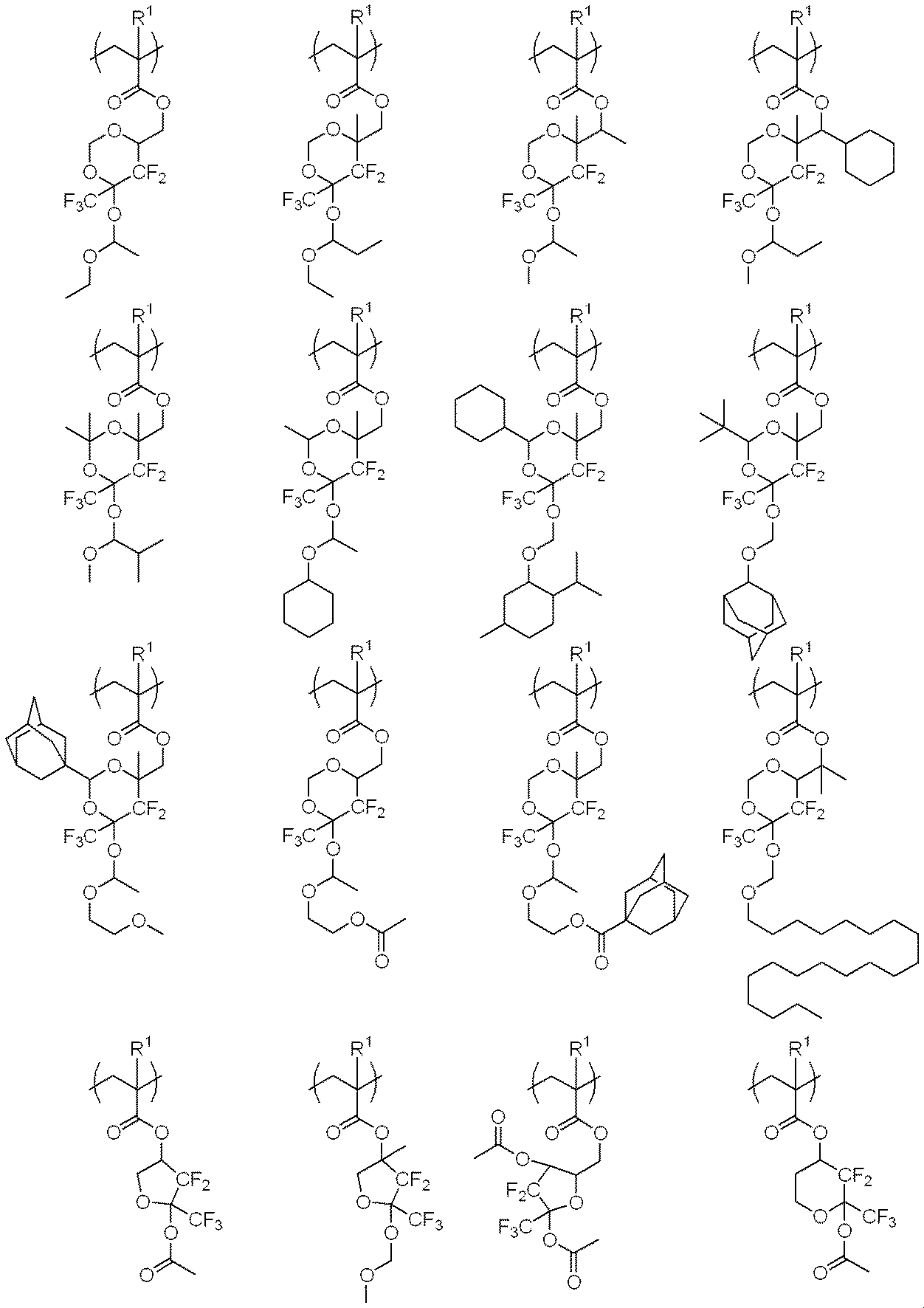
(A)請求項1,2又は3記載の繰り返し単位に加えて、下記一般式(4a)〜(4f)で表される繰り返し単位のうちの1つ又は2つ以上を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
請求項5:
更に、(E)塩基性化合物を含有することを特徴とする請求項1乃至4のいずれか1項記載のレジスト材料。
請求項6:
更に、(F)溶解制御剤を含有することを特徴とする請求項1乃至5のいずれか1項記載のレジスト材料。
請求項7:
(1)請求項1乃至6のいずれか1項に記載のレジスト材料を基板上に塗布する工程と、(2)加熱処理後、フォトマスクを介して高エネルギー線で露光する工程と、(3)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
請求項8:
(1)請求項1乃至6のいずれか1項に記載のレジスト材料を基板上に塗布する工程と、(2)加熱処理後、投影レンズとウエハーの間に液体を挿入させ、フォトマスクを介して高エネルギー線で露光する工程と、(3)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
請求項9:
(1)請求項1乃至6のいずれか1項に記載のレジスト材料を基板上に塗布する工程と、(2)フォトレジスト膜の上に保護膜層を形成する工程と、(3)加熱処理後、投影レンズとウエハーの間に液体を挿入させ、フォトマスクを介して高エネルギー線で露光する工程と、(4)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
請求項10:
前記露光工程において、投影レンズと基板の間に挿入する液体が水であることを特徴とする請求項8又は9記載のパターン形成方法。
請求項11:
露光光源として波長180〜250nmの範囲の高エネルギー線を用いることを特徴とする請求項8乃至10のいずれか1項記載のパターン形成方法。
請求項12:
(1)請求項1乃至6のいずれか1項に記載のレジスト材料をマスクブランクス上に塗布する工程と、(2)加熱処理後、真空中電子ビームで露光する工程と、(3)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
本発明のレジスト用添加剤として用いる高分子化合物は、下記一般式(1)〜(3)で表されるいずれかの繰り返し単位を含むことを特徴とする。
酸不安定基としては種々のものを用いることができるが、具体的には下記一般式(L1)〜(L4)で示される基、炭素数4〜20、好ましくは4〜15の三級アルキル基、各アルキル基がそれぞれ炭素数1〜6のトリアルキルシリル基、炭素数4〜20のオキソアルキル基等を挙げることができる。
RL03は炭素数1〜18、好ましくは炭素数1〜10の酸素原子等のヘテロ原子を有してもよい一価の炭化水素基を示し、直鎖状、分岐状又は環状のアルキル基、これらの水素原子の一部が水酸基、アルコキシ基、オキソ基、アミノ基、アルキルアミノ基等に置換されたものを挙げることができ、具体的には、直鎖状、分岐状又は環状のアルキル基としては上記RL01、RL02と同様のものが例示でき、置換アルキル基としては下記の基等が例示できる。
RL07〜RL16において、炭素数1〜15の一価の炭化水素基としては、具体的にはメチル基、エチル基、プロピル基、イソプロピル基、n−ブチル基、sec−ブチル基、tert−ブチル基、tert−アミル基、n−ペンチル基、n−ヘキシル基、n−オクチル基、n−ノニル基、n−デシル基、シクロペンチル基、シクロヘキシル基、シクロペンチルメチル基、シクロペンチルエチル基、シクロペンチルブチル基、シクロヘキシルメチル基、シクロヘキシルエチル基、シクロヘキシルブチル基等の直鎖状、分岐状又は環状のアルキル基、これらの水素原子の一部が水酸基、アルコキシ基、カルボキシ基、アルコキシカルボニル基、オキソ基、アミノ基、アルキルアミノ基、シアノ基、メルカプト基、アルキルチオ基、スルホ基等に置換されたもの等が例示できる。
RL07〜RL16は互いに結合してこれらが結合する炭素原子と共に環を形成していてもよく(例えば、RL07とRL08、RL07とRL09、RL08とRL10、RL09とRL10、RL11とRL12、RL13とRL14等)、その場合には環の形成に関与する基は炭素数1〜15の二価の炭化水素基を示し、具体的には上記一価の炭化水素基で例示したものから水素原子を1個除いたもの等が例示できる。また、RL07〜RL16は隣接する炭素に結合するもの同士で何も介さずに結合し、二重結合を形成してもよい(例えば、RL07とRL09、RL09とRL15、RL13とRL15等)。
R20の炭素数1〜15の2価の有機基としては、既に例示したアルキル基中の1個の水素原子を引き抜いた形式のもの(例えば、メチレン基やエチレン基)が用いられるほか、下記式で例示される基等も用いることができる。
本発明のレジスト用添加剤として用いる高分子化合物は、上記式(1)〜(3)で表されるいずれかの繰り返し単位を必須単位として含むことを特徴とする。これらの繰り返し単位に対応する重合性単量体化合物は、化合物の構造に応じて最適な方法を選択して製造するのが好ましい。一例として、対応するヘミアセタール化合物のO−アルキル化もしくはO−アシル化反応による製造法を例示するが、製造法はこの方法に限定されない。以下、下記一般式に示すヘミアセタール化合物よりアセタール化合物(1’)の合成を例に詳しく説明する。
反応には塩基もしくは遷移金属の塩を添加することが、反応率を高めるために好ましい。
反応に用いる塩基としては、ピリジン、トリエチルアミン、ジイソプロピルエチルアミン、4−ジメチルアミノピリジン、イミダゾール等のアミン類、ナトリウムメトキシド、ナトリウムエトキシド、カリウムt−ブトキシド等のアルコキシ金属類、炭酸ナトリウム、炭酸カリウム、炭酸セシウム等の炭酸塩類、水酸化ナトリウム、水酸化カリウム、テトラメチルアンモニウムヒドロキシド等の水酸化物類、水素化ナトリウム、水素化カリウム等の金属水素化物類、ブチルリチウム、エチルマグネシウムブロミド等の有機金属類、リチウムジイソプロピルアミド等の金属アミド類の中から反応条件により選択して単独又は混合して用いることができる。塩基の使用量はヘミアセタール化合物1モルに対し、0.3〜20モル、特に0.8〜10モルとすることが望ましい。
以下では、上記式(1)〜(3)及び(4a)〜(4f)で表される繰り返し単位を含む高分子化合物を高分子化合物(P1)とよぶことにする。
一般式(1)〜(3)の単位に対応するモノマーの総モル数をU11、
一般式(4a)〜(4f)の単位に対応するモノマーの総モル数をU12、
一般式(8a)〜(8e),(9a)〜(9e),(10a)〜(10c),(11a)〜(11c)の単位に対応するモノマーの総モル数をU13、
U11+U12+U13=U1
とした場合、
0<U11/U1<1、より好ましくは0.1≦U11/U1≦0.7、更に好ましくは0.2≦U11/U1≦0.6、
0≦U12/U1<1、より好ましくは0.3≦U12/U1≦0.9、更に好ましくは0.4≦U12/U1A≦0.8、
0≦U13/U1<1、より好ましくは0≦U13/U1≦0.5、更に好ましくは0≦U13/U1≦0.3
である。但し、U1≦100モル%である。
本発明のレジスト材料において、高分子化合物(P1)は一般式(1)〜(3)のいずれかの繰り返し単位内に含フッ素ヘミアセタールの水酸基が保護された構造を含み、樹脂の構造の選択により撥水性、滑水性、脂溶性、酸分解性、加水分解性、アルカリ溶解性など各種性能の調整が可能である。
次に、本発明のレジスト材料を用いたパターン形成方法について説明する。本発明におけるパターン形成方法では公知のリソグラフィー技術を用いることができるが、少なくとも基板上にフォトレジスト膜を形成する工程と、高エネルギー線を露光する工程と、現像液を用いて現像する工程を含むことが好ましい。
1H−NMR(300MHz,DMSO−d6中),モル比67:33のジアテレオマー混合物:δ=1.11(0.99H,d,J=6.9Hz),1.12(0.99H,d,J=7.1Hz),1.14(4.02H,d,J=6.9Hz),1.66−1.70(3H,m),1.85−1.90(3H,m),2.70(0.33H,qq,J=7.1,6.9Hz),2.74(0.67H,sep,J=6.9Hz),4.65(0.67H,br.d,J=11.1Hz),4.68(0.33H,dd,J=9.8,1.5Hz),4.79(0.33H,br.d,J=9.8Hz),4.85(0.67H,dd,J=11.1,2.7Hz),5.80(0.67H,m),5.82(0.33H,m),6.08(0.67H,m),6.09(0.33H,m)ppm。
19F−NMR(283MHz,DMSO−d6中),モル比67:33のジアテレオマー混合物:δ=−124.32(0.67F,dq,J=250,17Hz),−119.75(0.33F,dqd,J=246,17,4Hz),−110.80(0.33F,d,J=246Hz),−109.49(0.67F,d,J=250Hz),−80.19(0.67F,d,J=17Hz),−79.92(0.33F,d,J=17Hz)ppm。
IR(薄膜):ν=2966,2935,2877,1779,1727,1639,1469,1452,1386,1371,1336,1301,1282,1216,1155,1110,1087,1039,1004,946,927cm-1。
1H−NMR(600MHz,DMSO−d6中),モル比65:35のジアテレオマー混合物:δ=0.89(1.05H,d,J=6.4Hz),0.90(1.05H,d,J=6.4Hz),0.92(1.95H,d,J=6.4Hz),0.92(1.95H,d,J=6.4Hz),1.66(1.05H,br.d,J=3.7Hz),1.68(1.95H,br.d,J=3.2Hz),1.86(1.95H,m),1.87(1.05H,m),1.90−2.05(1H,m),2.31(0.35H,dd,J=15.6,7.3Hz),2.36(0.65H,dd,J=15.5,6.8Hz),2.37(0.35Hz,dd,J=15.6,6.4Hz),2.40(0.65H,dd,J=15.5,6.9Hz),4.63(0.65H,br.d,J=11.0Hz),4.66(0.35H,dd,J=10.1,1.0Hz),4.77(0.35H,br.d,J=10.1Hz),4.83(0.65H,dd,J=11.0,2.3Hz),5.78(0.65H,m),5.81(0.35H,m),6.06(0.65H,m),6.08(0.35H,m)ppm。
19F−NMR(565MHz,DMSO−d6中),モル比65:35のジアテレオマー混合物:δ=−124.06(0.65F,dq,J=249,16Hz),−119.57(0.35F,dqd,J=246,17,3Hz),−110.46(0.35F,d,J=246Hz),−108.98(0.65F,d,J=249Hz),−79.90(0.65F,d,J=16Hz),−79.57(0.35F,d,J=18Hz)ppm。
IR(薄膜):ν=2969,2881,2848,1727,1639,1473,1452,1388,1367,1328,1303,1284,1207,1159,1103,1066,1010,970,946cm-1。
1H−NMR(600MHz,DMSO−d6中),モル比33:32:19:16のジアテレオマー4種混合物:δ=0.80−0.90(6H,m),1.61−1.71(3H,m),1.84−1.95(4H,m),3.20(0.16H,s),3.26(0.19H,s),3.30(0.33H,s),3.34(0.32H,s),4.35−4.80(2H,m),5.72−5.82(1H,m),6.05−6.10(1H,m)ppm。
19F−NMR(565MHz,DMSO−d6中),モル比33:32:19:16のジアテレオマー4種混合物:δ=−124.63(0.33F,dq,J=243,19Hz),−124.30(0.32F,dq,J=236,18Hz),−121.63(0.32F,d,J=236Hz),−121.49(0.16F,d,J=241Hz),−120.52(0.16F,dq,J=241,17Hz),−119.38(0.19F,dq,J=245,21Hz),116.83(0.19F,d,J=245Hz),−114.83(0.33F,d,J=243Hz),−79.00(0.19F,d,J=21Hz),−78.76(0.33F,d,J=20Hz),−78.29(0.16F,d,J=18Hz),−78.23(0.32F,d,J=20Hz)ppm。
窒素雰囲気下のフラスコに23.41gのMonomer1、77.11gのMonomer6、3.75gの2,2’−アゾビス(イソ酪酸)ジメチル、100.1gのメチルエチルケトンを投入して単量体溶液を調製し、溶液温度を20〜25℃とした。窒素雰囲気下の別のフラスコに50.1gのメチルエチルケトンを投入し、撹拌しながら80℃まで加熱した後、上記単量体溶液を4時間かけて滴下した。滴下終了後、重合液の温度を80℃に保ったまま2時間撹拌を続け、熟成終了後に室温まで冷却した。フラスコに200gのトルエンを投入後、エバポレーターを用いて反応混合物の総重量が250gになるまで濃縮を行った。この濃縮液を1,500gのヘキサン中に滴下し、析出した共重合体を分離後、600gのヘキサンで洗浄し、白色固体を分離した。白色固体を50℃で20時間真空乾燥させることにより目的の高分子化合物(Polymer2)69.3gを得た。樹脂の組成を1H−NMRで分析した結果、共重合体中のMonomer1とMonomer6の組成比は19/81モル%であった。
表1〜5に示す組成で上述の重合性単量体(Monomer1〜13)を仕込み、Polymer2の合成と同様の処方を用いてPolymer1〜19の合成を行った。
窒素雰囲気下のフラスコに100.0gのMonomer6、3.91gの2,2’−アゾビス(イソ酪酸)ジメチル、100.0gのイソプロピルアルコールを投入して単量体溶液を調製し、溶液温度を20〜25℃とした。窒素雰囲気下の別のフラスコに50.0gのイソプロピルアルコールを投入し、撹拌しながら80℃まで加熱した後、上記単量体溶液を4時間かけて滴下した。滴下終了後、重合液の温度を80℃に保ったまま3時間撹拌を続け、熟成終了後に室温まで冷却した。得られた重合液を2,000gの水中に滴下し、析出した共重合体を濾別した。得られた共重合体を600gのヘキサン/イソプロピルエーテル(9/1)混合溶液で4回洗浄し、白色固体を分離した。白色固体を50℃で20時間真空乾燥させることにより目的の高分子化合物(比較Polymer1)92.8gを得た。得られた共重合体のGPC測定を行った結果、重量平均分子量(Mw)はポリスチレン換算で7,800、分散度(Mw/Mn)は1.6であった。
下記Resist Polymerを5g、上記Polymer8〜19及び比較Polymer1を0.25g、PAG1を0.25g、Quencher1を0.05g用い、これらを75gのプロピレングリコールモノエチルエーテルアセテート(PGMEA)に溶解させ、0.2μmサイズのポリプロピレンフィルターで濾過し、レジスト溶液を作製した。また、比較例として、上記Polymer8〜19、比較Polymer1を添加しないレジスト溶液も調製した。
Claims (12)
- (A)下記一般式(1)で表される繰り返し単位を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
- (A)下記一般式(2)で表される繰り返し単位を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
- (A)下記一般式(3)で表される繰り返し単位を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
- (A)請求項1,2又は3記載の繰り返し単位に加えて、下記一般式(4a)〜(4f)で表される繰り返し単位のうちの1つ又は2つ以上を有する高分子化合物、(B)ラクトン環及び/又は水酸基及び/又は無水マレイン酸由来の骨格を有し、酸の作用によりアルカリ現像液に可溶となる高分子化合物、(C)高エネルギー線の露光により酸を発生する化合物、(D)有機溶剤を含有することを特徴とするレジスト材料。
- 更に、(E)塩基性化合物を含有することを特徴とする請求項1乃至4のいずれか1項記載のレジスト材料。
- 更に、(F)溶解制御剤を含有することを特徴とする請求項1乃至5のいずれか1項記載のレジスト材料。
- (1)請求項1乃至6のいずれか1項に記載のレジスト材料を基板上に塗布する工程と、(2)加熱処理後、フォトマスクを介して高エネルギー線で露光する工程と、(3)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
- (1)請求項1乃至6のいずれか1項に記載のレジスト材料を基板上に塗布する工程と、(2)加熱処理後、投影レンズとウエハーの間に液体を挿入させ、フォトマスクを介して高エネルギー線で露光する工程と、(3)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
- (1)請求項1乃至6のいずれか1項に記載のレジスト材料を基板上に塗布する工程と、(2)フォトレジスト膜の上に保護膜層を形成する工程と、(3)加熱処理後、投影レンズとウエハーの間に液体を挿入させ、フォトマスクを介して高エネルギー線で露光する工程と、(4)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
- 前記露光工程において、投影レンズと基板の間に挿入する液体が水であることを特徴とする請求項8又は9記載のパターン形成方法。
- 露光光源として波長180〜250nmの範囲の高エネルギー線を用いることを特徴とする請求項8乃至10のいずれか1項記載のパターン形成方法。
- (1)請求項1乃至6のいずれか1項に記載のレジスト材料をマスクブランクス上に塗布する工程と、(2)加熱処理後、真空中電子ビームで露光する工程と、(3)現像液を用いて現像する工程を含むことを特徴とするパターン形成方法。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008279231A JP4666190B2 (ja) | 2008-10-30 | 2008-10-30 | レジスト材料及びパターン形成方法 |
| US12/608,556 US8431323B2 (en) | 2008-10-30 | 2009-10-29 | Fluorinated monomer of cyclic acetal structure, polymer, resist protective coating composition, resist composition, and patterning process |
| KR1020090103378A KR101438844B1 (ko) | 2008-10-30 | 2009-10-29 | 환상 아세탈 구조를 갖는 불소 함유 단량체, 고분자 화합물, 레지스트 보호막 재료, 레지스트 재료, 및 패턴 형성 방법 |
| TW098136701A TWI424994B (zh) | 2008-10-30 | 2009-10-29 | 具有環狀縮醛構造之含氟單體、高分子化合物、光阻保護膜材料、光阻材料、圖型之形成方法 |
| US13/847,667 US8933251B2 (en) | 2008-10-30 | 2013-03-20 | Fluorinated monomer of cyclic acetal structure, polymer, resist protective coating composition, resist composition, and patterning process |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008279231A JP4666190B2 (ja) | 2008-10-30 | 2008-10-30 | レジスト材料及びパターン形成方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010107695A JP2010107695A (ja) | 2010-05-13 |
| JP4666190B2 true JP4666190B2 (ja) | 2011-04-06 |
Family
ID=42297202
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008279231A Active JP4666190B2 (ja) | 2008-10-30 | 2008-10-30 | レジスト材料及びパターン形成方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4666190B2 (ja) |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5216032B2 (ja) | 2010-02-02 | 2013-06-19 | 信越化学工業株式会社 | 新規スルホニウム塩、高分子化合物、高分子化合物の製造方法、レジスト材料及びパターン形成方法 |
| JP5387605B2 (ja) * | 2010-04-07 | 2014-01-15 | 信越化学工業株式会社 | 含フッ素単量体、高分子化合物、レジスト材料及びパターン形成方法 |
| JP5246220B2 (ja) | 2010-08-23 | 2013-07-24 | 信越化学工業株式会社 | スルホニウム塩、レジスト材料及びパターン形成方法 |
| JP5609815B2 (ja) | 2010-08-26 | 2014-10-22 | 信越化学工業株式会社 | ポジ型化学増幅レジスト材料及びパターン形成方法 |
| US8597869B2 (en) | 2010-10-25 | 2013-12-03 | Shin-Etsu Chemical Co., Ltd. | Sulfonium salt, resist composition, and patterning process |
| JP5454458B2 (ja) | 2010-11-25 | 2014-03-26 | 信越化学工業株式会社 | ポジ型レジスト材料及びパターン形成方法 |
| EP2472320A2 (en) * | 2010-12-30 | 2012-07-04 | Rohm and Haas Electronic Materials LLC | Compositions comprising base-reactive component and processes for photolithography |
| JP5527236B2 (ja) | 2011-01-31 | 2014-06-18 | 信越化学工業株式会社 | ポジ型化学増幅レジスト材料、パターン形成方法及び酸分解性ケトエステル化合物 |
| JP5491450B2 (ja) | 2011-05-30 | 2014-05-14 | 信越化学工業株式会社 | 高分子化合物、化学増幅レジスト材料、該化学増幅レジスト材料を用いたパターン形成方法。 |
| JP5678864B2 (ja) | 2011-10-26 | 2015-03-04 | 信越化学工業株式会社 | ArF液浸露光用化学増幅ポジ型レジスト材料及びパターン形成方法 |
| JP5699943B2 (ja) | 2012-01-13 | 2015-04-15 | 信越化学工業株式会社 | パターン形成方法及びレジスト材料 |
| JP5668710B2 (ja) | 2012-02-27 | 2015-02-12 | 信越化学工業株式会社 | 高分子化合物及びそれを含んだレジスト材料並びにパターン形成方法、該高分子化合物の製造方法 |
| JP2013173855A (ja) | 2012-02-27 | 2013-09-05 | Shin-Etsu Chemical Co Ltd | 高分子化合物の製造方法、該製造方法によって製造された高分子化合物及びそれを含んだレジスト材料並びにパターン形成方法 |
| JP6020347B2 (ja) | 2012-06-04 | 2016-11-02 | 信越化学工業株式会社 | 高分子化合物、レジスト材料及びパターン形成方法 |
| JP5783137B2 (ja) | 2012-06-15 | 2015-09-24 | 信越化学工業株式会社 | スルホニウム塩、高分子化合物、レジスト材料及びパターン形成方法 |
| JP6213016B2 (ja) * | 2012-08-01 | 2017-10-18 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP5790631B2 (ja) | 2012-12-10 | 2015-10-07 | 信越化学工業株式会社 | スルホニウム塩及び高分子化合物、レジスト材料及びパターン形成方法、並びに該高分子化合物の製造方法 |
| JP5815576B2 (ja) | 2013-01-11 | 2015-11-17 | 信越化学工業株式会社 | パターン形成方法 |
| JP5815575B2 (ja) | 2013-01-11 | 2015-11-17 | 信越化学工業株式会社 | パターン形成方法 |
| JP5812030B2 (ja) | 2013-03-13 | 2015-11-11 | 信越化学工業株式会社 | スルホニウム塩及び高分子化合物、レジスト材料及びパターン形成方法 |
| US9164384B2 (en) | 2013-04-26 | 2015-10-20 | Shin-Etsu Chemical Co., Ltd. | Patterning process and resist composition |
| JP5904180B2 (ja) | 2013-09-11 | 2016-04-13 | 信越化学工業株式会社 | スルホニウム塩、化学増幅型レジスト組成物、及びパターン形成方法 |
| JP6206311B2 (ja) | 2014-04-22 | 2017-10-04 | 信越化学工業株式会社 | 光酸発生剤、化学増幅型レジスト材料及びパターン形成方法 |
| JP6125468B2 (ja) | 2014-07-04 | 2017-05-10 | 信越化学工業株式会社 | 光酸発生剤、化学増幅型レジスト材料及びパターン形成方法 |
| JP6217561B2 (ja) | 2014-08-21 | 2017-10-25 | 信越化学工業株式会社 | 新規オニウム塩化合物及びレジスト組成物並びにパターン形成方法 |
| JP6394481B2 (ja) | 2015-04-28 | 2018-09-26 | 信越化学工業株式会社 | レジスト組成物及びパターン形成方法 |
| JP6346129B2 (ja) | 2015-08-05 | 2018-06-20 | 信越化学工業株式会社 | 化合物、高分子化合物、レジスト組成物、及びパターン形成方法 |
| JP6714533B2 (ja) | 2017-03-22 | 2020-06-24 | 信越化学工業株式会社 | スルホニウム塩、レジスト組成物、及びパターン形成方法 |
| JP7344108B2 (ja) | 2019-01-08 | 2023-09-13 | 信越化学工業株式会社 | レジスト組成物、及びパターン形成方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004182796A (ja) * | 2002-11-29 | 2004-07-02 | Tokyo Ohka Kogyo Co Ltd | 高分子化合物、該高分子化合物を含むレジスト組成物および溶解制御剤 |
| JP2006124314A (ja) * | 2004-10-28 | 2006-05-18 | Shin Etsu Chem Co Ltd | 含フッ素重合性化合物、その製造方法、この化合物から得られる高分子化合物、レジスト材料及びこれを用いたパターン形成方法 |
| JP2007249192A (ja) * | 2006-02-15 | 2007-09-27 | Sumitomo Chemical Co Ltd | フォトレジスト組成物 |
| JP2008107806A (ja) * | 2006-09-25 | 2008-05-08 | Fujifilm Corp | レジスト組成物、該レジスト組成物に用いられる樹脂、該樹脂の合成に用いられる化合物及び該レジスト組成物を用いたパターン形成方法 |
| JP2008203452A (ja) * | 2007-02-19 | 2008-09-04 | Shin Etsu Chem Co Ltd | レジスト材料及びこれを用いたパターン形成方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2007119804A1 (ja) * | 2006-04-13 | 2009-08-27 | 旭硝子株式会社 | 液浸露光用レジスト組成物 |
| WO2008032716A1 (fr) * | 2006-09-12 | 2008-03-20 | Asahi Glass Company, Limited | Matériau de résist pour une lithographie et procédé de formation d'un motif de résist |
-
2008
- 2008-10-30 JP JP2008279231A patent/JP4666190B2/ja active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004182796A (ja) * | 2002-11-29 | 2004-07-02 | Tokyo Ohka Kogyo Co Ltd | 高分子化合物、該高分子化合物を含むレジスト組成物および溶解制御剤 |
| JP2006124314A (ja) * | 2004-10-28 | 2006-05-18 | Shin Etsu Chem Co Ltd | 含フッ素重合性化合物、その製造方法、この化合物から得られる高分子化合物、レジスト材料及びこれを用いたパターン形成方法 |
| JP2007249192A (ja) * | 2006-02-15 | 2007-09-27 | Sumitomo Chemical Co Ltd | フォトレジスト組成物 |
| JP2008107806A (ja) * | 2006-09-25 | 2008-05-08 | Fujifilm Corp | レジスト組成物、該レジスト組成物に用いられる樹脂、該樹脂の合成に用いられる化合物及び該レジスト組成物を用いたパターン形成方法 |
| JP2008203452A (ja) * | 2007-02-19 | 2008-09-04 | Shin Etsu Chem Co Ltd | レジスト材料及びこれを用いたパターン形成方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010107695A (ja) | 2010-05-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4666190B2 (ja) | レジスト材料及びパターン形成方法 | |
| JP4748331B2 (ja) | レジスト材料及びパターン形成方法 | |
| JP5170456B2 (ja) | レジスト材料及びパターン形成方法 | |
| JP5375811B2 (ja) | 高分子化合物、レジスト材料、及びパターン形成方法 | |
| JP5131488B2 (ja) | 含フッ素単量体及び含フッ素高分子化合物 | |
| KR101438844B1 (ko) | 환상 아세탈 구조를 갖는 불소 함유 단량체, 고분자 화합물, 레지스트 보호막 재료, 레지스트 재료, 및 패턴 형성 방법 | |
| JP5282781B2 (ja) | レジスト材料及びパターン形成方法 | |
| JP4614092B2 (ja) | フッ素アルコール化合物の製造方法 | |
| JP4858714B2 (ja) | 高分子化合物、レジスト材料、及びパターン形成方法 | |
| JP5387605B2 (ja) | 含フッ素単量体、高分子化合物、レジスト材料及びパターン形成方法 | |
| JP5510176B2 (ja) | レジスト材料及びパターン形成方法 | |
| KR20130016113A (ko) | ArF 액침 노광용 화학 증폭 포지티브형 레지스트 재료 및 패턴 형성 방법 | |
| JP5403128B2 (ja) | レジスト材料及びパターン形成方法 | |
| JP4743452B2 (ja) | 高分子化合物、レジスト保護膜材料、及びパターン形成方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101026 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20101215 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20101228 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140121 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4666190 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |