JP4595178B2 - アミン化合物、中間体、製造法および光学分割剤 - Google Patents
アミン化合物、中間体、製造法および光学分割剤 Download PDFInfo
- Publication number
- JP4595178B2 JP4595178B2 JP2000224998A JP2000224998A JP4595178B2 JP 4595178 B2 JP4595178 B2 JP 4595178B2 JP 2000224998 A JP2000224998 A JP 2000224998A JP 2000224998 A JP2000224998 A JP 2000224998A JP 4595178 B2 JP4595178 B2 JP 4595178B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- methylbenzylamine
- benzyloxybenzyl
- general formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
【発明の属する技術分野】
本発明は、アミン化合物、中間体、製造法および光学分割剤に関する。
【0002】
【従来の技術および発明が解決しようとする課題】
光学活性なα−フェニルエチルアミン、α−ナフチルエチルアミン等の光学活性第1級アミン化合物は、カルボン酸基を有する化合物の光学分割剤として知られている。
本発明者らは、これらの光学活性アミン化合物の誘導体を種々合成し検討した結果、窒素原子にベンジルオキシベンジル基という特定の置換基を有する光学活性第2級アミン化合物が、光学分割剤として優れていることを見い出し本発明に至った。
【0003】
【課題を解決するための手段】
すなわち本発明は、一般式(1)
(式中、*印は不斉炭素原子を表し、R1は、炭素数1〜4のアルキル基または置換基を有していてもよいアラルキル基を表し、R2は、3−ベンジルオキシフェニル基または4−ベンジルオキシフェニル基を表し、Aはアリール基を表わす。ここでアリール基は、炭素数1〜4の低級アルキル基、炭素数1〜4の低級アルコキシ基、ニトロ基またはハロゲン原子で置換されていてもよい。)
で示されるラセミまたは光学活性アミン化合物、中間体、製造法および光学分割剤を提供するものである。
【0004】
【発明の実施の形態】
以下本発明について、詳細に説明する。
一般式(1)で示されるラセミまたは光学活性アミン化合物[以下、アミン化合物(1)という。]において、Aは、低級アルキル基、低級アルコキシ基、ニトロ基、ハロゲン原子が置換していてもよいアリール基であり、アリール基の具体例としては、フェニル基、ナフチル基等が挙げられる。
低級アルキル基は、炭素数1〜4の低級アルキル基であり、具体的にはメチル基、エチル基、n−プロピル基、イソプロピル基、t−ブチル基等が挙げられる。
低級アルコキシ基は、炭素数1〜4の低級アルコキシ基で、具体的にはメトキシ基、エトキシ基、n−プロポキシ基、イソプロポキシ基、t−ブトキシ基等が挙げられる。
ハロゲン原子は、フッ素、塩素、臭素およびヨウ素原子が挙げられる。
置換基Aとして具体的には、フェニル基、ナフチル基、4−メチルフェニル基、4−エチルフェニル基、4−プロピルフェニル基、4−イソプロピルフェニル基、4−t−ブチルフェニル基、2,5−ジメチルフェニル基、2,4,6−トリメチルフェニル基、2−フルオロフェニル基、3−フルオロフェニル基、4−フルオロフェニル基、2−クロロフェニル基、3−クロロフェニル基、4−クロロフェニル基、2,4−ジクロロフェニル基、2,3−ジクロロフェニル基、4−ブロモフェニル基、2−メトキシフェニル基、4−メトキシフェニル基、2−エトキシフェニル基、2−プロポキシフェニル基、3,4−ジメトキシフェニル基、2−メトキシ−5フルオロフェニル基等が挙げられる。特に好ましくは、フェニル基、2,4−ジクロロフェニル基が挙げられる。
【0005】
アミン化合物(1)において、R1は、低級アルキル基または置換基を有していてもよいアラルキル基である。
ここで、R1における低級アルキル基は、前記Aにおける低級アルキル基と同様のものが挙げられ、好ましくは、メチル基が挙げられる。
また、R1における置換基を有していてもよいアラルキル基としては、芳香環に低級アルキル基、低級アルコキシ基、ニトロ基またはハロゲン原子が置換していてもよいベンジル基、フェニルエチル基等が挙げられる。
R1におけるアラルキル基の芳香環に置換していてもよい低級アルキル基、低級アルコキシ基およびハロゲン原子は、前記Aにおける低級アルキル基、低級アルコキシ基およびハロゲン原子と同様のものが挙げられる。
R1における置換基を有していてもよいアラルキル基として、具体的には、ベンジル基、4−メチルベンジル基、3−メトキシベンジル基、4−クロロベンジル基、2−フェニルエチル基等を挙げることができる。
アミン化合物(1)において、R2は、3−ベンジルオキシフェニル基または4−ベンジルオキシフェニル基である。
【0006】
かかるアミン化合物(1)の具体例としては、N−(3−ベンジルオキシベンジル)−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−α−エチルベンジルアミン、N−(3−ベンジルオキシベンジル)−α−プロピルベンジルアミン、N−(3−ベンジルオキシベンジル)−α−イソプロピルベンジルアミン、N−(3−ベンジルオキシベンジル)−α,4−ジメチルベンジルアミン、N−(3−ベンジルオキシベンジル)−α,2,5−トリメチルベンジルアミン、N−(3−ベンジルオキシベンジル)−α,2,4,6−テトラメチルベンジルアミン、N−(3−ベンジルオキシベンジル)−α−メチル−4−イソプロピルベンジルアミン、N−(3−ベンジルオキシベンジル)−2−フルオロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−3−フルオロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−4−フルオロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−4−ブロモ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−2−クロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−3−クロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−4−クロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−2,3−ジクロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−2−メトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−4−メトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−2−エトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−3,4−ジメトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−5−フルオロ−2−メトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−α,β−ジフェニルエチルアミン、N−(3−ベンジルオキシベンジル)−1−フェニル−2−(p−トリル)エチルアミン、N−(3−ベンジルオキシベンジル)−α−フェニル−β−(3−メトキシフェニル)エチルアミン、N−(3−ベンジルオキシベンジル)−α−フェニル−β−(4−クロロフェニル)エチルアミン、N−(3−ベンジルオキシベンジル)−α,γ−ジフェニルプロピルアミン、N−(3−ベンジルオキシベンジル)−α−メチル−1−ナフチルアミン、N−(3−ベンジルオキシベンジル)−α−メチル−2−ナフチルメチルアミン、N−(4−ベンジルオキシベンジル)−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α−エチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α−プロピルベンジルアミン、N−(4−ベンジルオキシベンジル)−α−イソプロピルベンジルアミン、N−(4−ベンジルオキシベンジル)−α,4−ジメチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α,2,5−トリメチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α,2,4,6−テトラメチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α−メチル−4−イソプロピルベンジルアミン、N−(4−ベンジルオキシベンジル)−2−フルオロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−3−フルオロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−4−フルオロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−4−ブロモ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−2−クロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−3−クロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−4−クロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−2,3−ジクロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−2−メトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−4−メトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−2−エトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−3,4−ジメトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−5−フルオロ−2−メトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α,β−ジフェニルエチルアミン、N−(4−ベンジルオキシベンジル)−1−フェニル−2−(p−トリル)エチルアミン、N−(4−ベンジルオキシベンジル)−α−フェニル−β−(3−メトキシフェニル)エチルアミン、N−(4−ベンジルオキシベンジル)−α−フェニル−β−(4−クロロフェニル)エチルアミン、N−(4−ベンジルオキシベンジル)−α,γ−ジフェニルプロピルアミン、N−(4−ベンジルオキシベンジル)−α−メチル−1−ナフチルアミン、N−(4−ベンジルオキシベンジル)−α−メチル−2−ナフチルメチルアミン等のラセミまたは光学活性体が挙げられ、好ましくは、N−(3−ベンジルオキシベンジル)−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミンが挙げられる。
【0007】
本発明のアミン化合物(1)は、例えば一般式(2)
(式中、*印は不斉炭素原子を表し、R1は、炭素数1〜4のアルキル基または置換基を有していてもよいアラルキル基を表し、Aはアリール基を表わす。ここでアリール基は、炭素数1〜4の低級アルキル基、炭素数1〜4の低級アルコキシ基、ニトロ基またはハロゲン原子で置換されていてもよい。)
で示されるラセミまたは光学活性アミン[以下、アミン(2)という。]と一般式(3)
(式中、R2は、3−ベンジルオキシフェニル基または4−ベンジルオキシフェニル基を表す。)
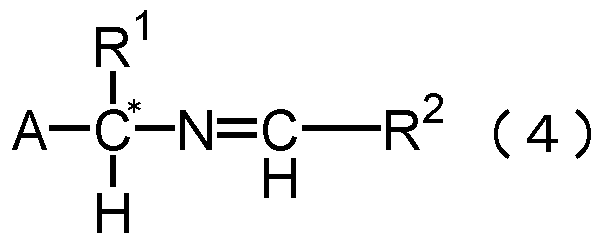
で示されるベンジルオキシベンズアルデヒド類[以下、ベンジルオキシベンズアルデヒド類(3)という。]とを反応させ、一般式(4)
(式中、*印、R1、R2、Aは前記と同じ意味を表す。)
で示されるイミン化合物[以下、イミン化合物(4)という。]を得、次いで該化合物を還元することにより得ることができる。
【0008】
また、アミン化合物(1)の塩としては、例えば、塩酸、硫酸、硝酸等の鉱酸と該アミン化合物との塩が挙げられる。
【0009】
アミン(2)とベンジルオキシベンズアルデヒド類(3)とを反応させてイミン化合物(4)を得る反応において、アミン(2)としては、例えば、α−メチルベンジルアミン、1−(1−ナフチル)エチルアミン、α、4−ジメチルベンジルアミン、4−イソプロピル−α−メチルベンジルアミン、4−ニトロ−α−メチルベンジルアミン、4−ブロモ−α−メチルベンジルアミン、α−エチルベンジルアミン、α−イソプロピルベンジルアミン、1−フェニル−2−(p−トリル)エチルアミン等のラセミまたは光学活性体が挙げられ、これらは公知化合物であり容易に入手できる。
また、ベンジルオキシベンズアルデヒド類(3)としては、3−ベンジルオキシベンズアルデヒド、4−ベンジルオキシベンズアルデヒドが挙げられる。
【0010】
上記反応には、通常、溶媒が用いられ、用いられる溶媒としては、例えば、メタノール、エタノール、イソプロピルアルコール等のアルコール類、ジエチルエーテル、t−ブチルメチルエーテル、n−ブチルエーテル、テトラヒドロフラン等のエーテル類、ベンゼン、トルエン、キシレン等の芳香族炭化水素類、クロロホルム、ジクロルメタン、ジクロルエタン、クロルベンゼン等のハロゲン化炭化水素類等を例示することができる。
溶媒は、上記の1種を単独で使用しても、2種以上を混合して使用してもよい。
【0011】
反応温度は、通常、0℃〜200℃であり、好ましくは0℃〜150℃の範囲である。
反応時間は、通常、0.5〜30時間、好ましくは0.5〜10時間で充分目的を達することができる。
ここで得られたイミン化合物(4)は、単離することもできるが、単離することなく次の反応に用いることができる。
【0012】
イミン化合物(4)の具体例としては、例えば、
N−(3−ベンジルオキシベンジリデン)−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α−エチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α−プロピルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α−イソプロピルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α,4−ジメチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α,2,5−トリメチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α,2,4,6−テトラメチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α−メチル−4−イソプロピルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−2−フルオロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−3−フルオロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−4−フルオロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−4−ブロモ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−2−クロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−3−クロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−4−クロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−2,3−ジクロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−2,4−ジクロロ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−2−メトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−4−メトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−2−エトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−3,4−ジメトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−5−フルオロ−2−メトキシ−α−メチルベンジルアミン、N−(3−ベンジルオキシベンジリデン)−α,β−ジフェニルエチルアミン、N−(3−ベンジルオキシベンジリデン)−1−フェニル−2−(p−トリル)エチルアミン、N−(3−ベンジルオキシベンジリデン)−α−フェニル−β−(3−メトキシフェニル)エチルアミン、N−(3−ベンジルオキシベンジリデン)−α−フェニル−β−(4−クロロフェニル)エチルアミン、N−(3−ベンジルオキシベンジリデン)−α,γ−ジフェニルプロピルアミン、N−(3−ベンジルオキシベンジリデン)−α−メチル−1−ナフチルアミン、N−(3−ベンジルオキシベンジリデン)−α−メチル−2−ナフチルメチルアミン、N−(4−ベンジルオキシベンジリデン)−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α−エチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α−プロピルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α−イソプロピルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α,4−ジメチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α,2,5−トリメチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α,2,4,6−テトラメチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α−メチル−4−イソプロピルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−2−フルオロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−3−フルオロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−4−フルオロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−4−ブロモ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−2−クロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−3−クロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−4−クロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−2,3−ジクロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−2,4−ジクロロ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−2−メトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−4−メトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−2−エトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−3,4−ジメトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−5−フルオロ−2−メトキシ−α−メチルベンジルアミン、N−(4−ベンジルオキシベンジリデン)−α,β−ジフェニルエチルアミン、N−(4−ベンジルオキシベンジリデン)−1−フェニル−2−(p−トリル)エチルアミン、N−(4−ベンジルオキシベンジリデン)−α−フェニル−β−(3−メトキシフェニル)エチルアミン、N−(4−ベンジルオキシベンジリデン)−α−フェニル−β−(4−クロロフェニル)エチルアミン、N−(4−ベンジルオキシベンジリデン)−α,γ−ジフェニルプロピルアミン、N−(4−ベンジルオキシベンジリデン)−α−メチル−1−ナフチルアミン、N−(4−ベンジルオキシベンジリデン)−α−メチル−2−ナフチルメチルアミン
等のラセミまたは光学活性体を挙げることができる。
【0013】
次に、イミン化合物(4)を還元し、アミン化合物(1)を得る還元方法において、還元剤としては、通常、金属水素化物等の還元剤を用いる方法または還元触媒を用いて接触還元する方法等が挙げられる。
【0014】
還元剤を用いる方法において、金属水素化物としては、例えば、水素化リチウムアルミニウム、水素化ホウ素ナトリウム、ボラン等が挙げられる。ボランとしては、ジボラン、ボラン−THF、ボラン−スルフィド錯体、ボランアミン錯体等が挙げられる。
これらの還元剤の使用量は、水素化リチウムアルミニウムまたは水素化ホウ素ナトリウムを用いる場合、イミン化合物(4)に対して通常0.25〜5モル倍程度、好ましくは0.25〜2モル倍程度の範囲である。
ボランを用いる場合、ボランの使用量はイミン化合物(4)に対して、ホウ素基準で通常、0.3〜5モル倍程度、好ましくは0.3〜3モル倍程度の範囲である。
【0015】
この反応では通常溶媒が用いられ、用いられる溶媒としては、還元反応に不活性な溶媒が挙げられ、かかる溶媒としては、ジエチルエーテル、t−ブチルメチルエーテル、n−ブチルエーテル、テトラヒドロフラン等のエーテル類、ベンゼン、トルエン、キシレン等の芳香族炭化水素類、クロロホルム、ジクロルメタン、ジクロルエタン、クロルベンゼン等のハロゲン化炭化水素類、等を例示できる。
また、還元剤として水素化ホウ素ナトリウム等を使用する場合には、上記溶媒の他に、メタノール、エタノール、イソプロピルアルコール等の低級アルコール類も用いることができる。
溶媒は、上記の1種を単独で使用しても、2種以上を混合して使用してもよく、使用量は特に限定されない。
【0016】
反応温度は、通常、−50℃〜100℃程度、好ましくは−20℃〜100℃程度の範囲である。反応時間は特に限定されない。
反応終了後、水、酢酸または鉱酸で分解した後に塩基性とし、次いで中性ないし弱塩基性下に分液した有機層を濃縮すれば、アミン化合物(1)が得られ、必要に応じて、再結晶、シリカゲル等を用いたカラムクロマトグラフィー等によって精製することもできる。
【0017】
接触水添による方法において、還元触媒としてはラネーニッケル、パラジウム−炭素、二酸化白金、白金黒、等が挙げられる。
これら触媒の使用量は、通常、イミン化合物(4)に対して0.1〜100重量%、好ましくは0.5〜50重量%程度である。
この反応に用いられる溶媒としては、通常、還元反応に不活性な溶媒が用いられ、かかる溶媒としては例えば、メタノール、エタノール、イソプロピルアルコール等のアルコール類、ジエチルエーテル、t−ブチルメチルエーテル、n−ブチルエーテル、テトラヒドロフラン等のエーテル類、酢酸エチル等のエステル類、ベンゼン、トルエン、キシレン等の芳香族炭化水素類、水等を例示できる。
溶媒は、上記の1種を単独で使用しても、2種以上を混合して使用してもよく、使用量は特に限定されない。
反応温度は、通常、−30℃〜150℃、好ましくは−10℃〜100℃程度の範囲である。
反応圧力は、通常、0〜10MPa、好ましくは0〜5MPa程度である。反応時間は、特に限定されない。
【0018】
反応終了後、触媒を濾過して除き、濾液を濃縮すれば本発明化合物であるアミン化合物(1)が得られ、必要に応じて再結晶、シリカゲル等を用いたカラムクロマトグラフィーによって精製することもできる。
【0019】
【発明の効果】
本発明の光学活性アミン化合物(1)は、カルボン酸の光学分割剤として優れた性能を示す。
また、本発明の光学活性アミン化合物(1)は、対応する光学活性アミン(2)から容易に製造しうるので、この点でも工業的に有利である。
【0020】
【実施例】
以下に実施例を示し、本発明をより具体的に説明するが、本発明はこれらの実施例に限定されるものではない。
なお、以下の実施例において化学純度はガスクロマトグラフィーにより測定し、光学純度は、高速液体クロマトグラフィーにより測定した。
【0021】
実施例1
(S)−α−メチルベンジルアミン27.19g(0.224mol)と3−ベンジルオキシベンズアルデヒド50.00g(0.236mol)をエタノール600ml中室温で8時間攪拌した。原料アミンの消失を確認後、水素化ホウ素ナトリウム8.15g(0.215mol)を室温で添加し、30℃〜35℃で8時間攪拌した。
反応後、室温下で10%塩酸185.00gを加えた。その後、減圧濃縮し、残渣を水700mlに溶解後ジエチルエーテル500mlで洗浄した。
得られた水層を20%水酸化ナトリウム水溶液でpH>10とし、トルエン500mlで水層から抽出後、水250mlで洗浄した後減圧濃縮することにより、54.71g(0.172mol)の(S)−N−(3−ベンジルオキシベンジル)−α−メチルベンジルアミンが得られた。(収率77.4%、純度99.5%。)
NMRスペクトルデータ(δppm、CDCl3)
1.34 (d) 2H;1.54 (s) 1H;3.61 (q) 2H;3.79 (q) 1H;5.06 (s) 2H;6.83〜7.46 (m) 14H;
【0022】
実施例2
実施例1において、3−ベンジルオキシベンズアルデヒドに代えて4−ベンジルオキシベンズアルデヒドを用いる以外は実施例1に準じて行った。
(S)−N−(4−ベンジルオキシベンジル)−α−メチルベンジルアミン57.3g(0.181mol)が得られた。(収率80.4%、純度99.3%。)
NMRスペクトルデータ(δppm、CDCl3)
1.34 (d) 2H;1.48 (s) 1H;3.55 (q) 2H;3.78 (q) 1H;5.05 (s) 2H;6.90〜7.45 (m) 14H;
【0023】
実施例3
45℃でラセミ体の3,3,3−トリフルオロ−2−ヒドロキシ−2−メチルプロピオン酸159mg(1.01mmol)をt−ブチルメチルエーテル1.48gに溶解し、この溶液に、同温で(S)−N−(3−ベンジルオキシベンジル)―α―メチルベンジルアミン172mg(0.54mmol)をあらかじめt−ブチルメチルエーテル1.48gに溶解した溶液を加え、攪拌して混合した。 結晶の析出を確認後、攪拌しながら0.5時間かけて徐々に35℃まで冷却した。
析出した結晶を濾別し、t−ブチルメチルエーテル2.96gで洗浄後乾燥し、光学純度95%eeの(R)−3,3,3−トリフルオロ−2−ヒドロキシ−2−メチルプロピオン酸の(S)−N−(3−ベンジルオキシベンジル)―α―メチルベンジルアミン塩61mg(収率13%)を得た。融点131〜132℃、比旋光度[α]D 25=−5.8゜(c=0.59、メタノール)。
【0024】
実施例4
(R)−2,4−ジクロロ−α−メチルベンジルアミン7.48g(0.0394mol)と3−ベンジルオキシベンズアルデヒド10.03g(0.0473mol)をt−ブチルメチルエーテル50mlとメタノール10mlの混合溶媒中室温で5時間攪拌した。原料アミンの消失を確認後、メタノール20mlを添加し、水素化ホウ素ナトリウム2.63g(0.0695mol)を室温で徐々に添加し、室温で13時間攪拌した。
反応後、室温下で36%塩酸13mlと水10mlを加え、減圧濃縮した。
得られた液状の濃縮物に、t−ブチルメチルエーテル25mlを加えて攪拌後静置して固体を析出させた後、ろ過により析出物を分離除去した。
得られたろ液に、水酸化ナトリウム21.35gを水200mlに溶解したものを加えて塩基性とし、t−ブチルメチルエーテル500mlで抽出した。
得られた抽出液を減圧濃縮することにより、14.51g(0.0376mol)の粗製(R)−N−(3−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミンが得られた。(収率95.5%、純度80.8%。)得られた粗製(R)−N−(3−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミン14.51gに36%塩酸4ml、t−ブチルメチルエーテル30mlを加えた後、室温で2日間静置して結晶を析出させた。
ろ過により結晶を分離後、得られた結晶をt−ブチルメチルエーテル25mlで洗浄し、水酸化ナトリウム1.84gを水50mlに溶解したものを加えて塩基性とした後、t−ブチルメチルエーテル300mlで抽出した。
得られた抽出液を減圧濃縮することにより、5.62g(0.0145mol)の精製(R)−N−(3−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミンが得られた。(収率37.0%、純度99.8%。)
NMRスペクトルデータ(δppm、CDCl3)
1.30 (d) 3H;1.57 (s) 1H;3.57 (d) 2H;4.27 (q) 1H;5.05 (s) 2H;7.20〜7.58 (m) 12H;
【0025】
実施例5
(R)−2,4−ジクロロ−α−メチルベンジルアミン7.34g(0.0386mol)と4−ベンジルオキシベンズアルデヒド9.73g(0.0458mol)をt−ブチルメチルエーテル50mlとメタノール20mlの混合溶媒中室温で9時間攪拌した。原料アミンの消失を確認後、水素化ホウ素ナトリウム1.75g(0.0463mol)を室温で添加し、室温で5時間攪拌した。
反応後、室温下で36%塩酸13mlと水30mlを加えたところ、結晶が析出したため、ろ過により結晶を分離した。
得られた結晶をt−ブチルメチルエーテル25mlで洗浄した後、水酸化ナトリウム2.93gを水100mlに溶解したものを加えて塩基性とし、t−ブチルメチルエーテル900mlで抽出した。
得られた抽出液を減圧濃縮することにより、12.53g(0.0324mol)の(R)−N−(4−ベンジルオキシベンジル)−2,4−ジクロロ−α−メチルベンジルアミンが得られた。(収率84.0%、純度99.4%。)
NMRスペクトルデータ(δppm、CDCl3)
1.30 (d) 3H;1.63 (s) 1H;3.52 (s) 2H;4.27 (q) 1H;5.04 (s) 2H;6.88〜7.58 (m) 12H;
【0026】
実施例6
(S)−α−メチルベンジルアミン0.12g(0.97mmol)と3−ベンジルオキシベンズアルデヒド0.25g(1.19mmol)をt−ブチルメチルエーテル4ml中室温で3日間攪拌した後、減圧濃縮することにより、0.35g(1.12mmol)の(S)−N−(3−ベンジルオキシベンジリデン)−α−メチルベンジルアミンが得られた。(収率115%、純度85%。)
NMRスペクトルデータ(δppm、CDCl3)
1.58 (d) 3H;4.54 (q) 1H;5.10 (s) 2H;7.04〜7.50 (m) 14H;8.33 (s) 1H;
【0027】
実施例7
(S)−α−メチルベンジルアミン0.11g(0.93mmol)と4−ベンジルオキシベンズアルデヒド0.26g(1.23mmol)をt−ブチルメチルエーテル4ml中室温で3日間攪拌した後、減圧濃縮することにより得られた残渣をn−ヘキサン5mlで洗浄後ろ過乾燥することにより、0.24g(0.77mmol)の(S)−N−(4−ベンジルオキシベンジリデン)−α−メチルベンジルアミンが得られた。(収率83%、純度90%。)
NMRスペクトルデータ(δppm、CDCl3)
1.57 (d) 3H;4.50 (q) 1H;5.08 (s) 2H;6.97〜7.84 (m) 14H;8.29 (s) 1H;
【0028】
実施例8
(R)−2,4−ジクロロ−α−メチルベンジルアミン0.19g(1.02mmol)と3−ベンジルオキシベンズアルデヒド0.25g(1.19mmol)をt−ブチルメチルエーテル4ml中室温で3日間攪拌した後、減圧濃縮することにより、0.43g(1.11mmol)の(R)−N−(3−ベンジルオキシベンジリデン)−2,4−ジクロロ−α−メチルベンジルアミンが得られた。(収率109%、純度90%。)
NMRスペクトルデータ(δppm、CDCl3)
1.51 (d) 3H;4.92 (q) 1H;5.10 (s) 2H;7.02〜7.74 (m) 12H;8.35 (s) 1H;
【0029】
実施例9
(R)−2,4−ジクロロ−α−メチルベンジルアミン0.23g(1.22mmol)と4−ベンジルオキシベンズアルデヒド0.26g(1.23mmol)をt−ブチルメチルエーテル4ml中室温で3日間攪拌した後、減圧濃縮することにより、0.47g(1.23mmol)の(R)−N−(4−ベンジルオキシベンジリデン)−2,4−ジクロロ−α−メチルベンジルアミンが得られた。(収率100%、純度98%。)
NMRスペクトルデータ(δppm、CDCl3)
1.49 (d) 3H;4.88 (q) 1H;5.09 (s) 2H;6.98〜7.74 (m) 12H;8.31 (s) 1H;
Claims (7)
- 一般式(1)において、Aが2,4−ジクロロフェニル基である請求項1記載のラセミまたは光学活性アミン化合物あるいはその塩。
- 一般式(4)において、Aが2,4−ジハロフェニル基である請求項5記載のラセミまたは光学活性イミン化合物あるいはその塩。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000224998A JP4595178B2 (ja) | 1999-08-04 | 2000-07-26 | アミン化合物、中間体、製造法および光学分割剤 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP11-221065 | 1999-08-04 | ||
| JP22106599 | 1999-08-04 | ||
| JP2000224998A JP4595178B2 (ja) | 1999-08-04 | 2000-07-26 | アミン化合物、中間体、製造法および光学分割剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2001106661A JP2001106661A (ja) | 2001-04-17 |
| JP4595178B2 true JP4595178B2 (ja) | 2010-12-08 |
Family
ID=26524060
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000224998A Expired - Fee Related JP4595178B2 (ja) | 1999-08-04 | 2000-07-26 | アミン化合物、中間体、製造法および光学分割剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4595178B2 (ja) |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE122005000033I1 (de) * | 1994-10-21 | 2005-09-29 | Nps Pharma Inc | Kalzium-Rezeptor aktive Verbindungen. |
| JPH11180930A (ja) * | 1997-12-22 | 1999-07-06 | Sumitomo Chem Co Ltd | 光学活性trans−シクロブタンジカルボン酸類の製造方法 |
-
2000
- 2000-07-26 JP JP2000224998A patent/JP4595178B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2001106661A (ja) | 2001-04-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6770761B2 (en) | Process for preparation of 2-amino-6 (alkyl) amino-4,5,6,7-tetrahydrobenzothiazoles | |
| CN114206847B (zh) | 杂环亚基乙酰胺衍生物的制造方法 | |
| TWI306092B (en) | Process for preparation of phenethylamine derivatives | |
| US9944599B2 (en) | Processes for the preparation of beta-aminosulfone compounds | |
| US10370329B2 (en) | Process for the enantiomeric resolution of apremilast intermediates | |
| EP2146719B1 (en) | Process for making galantamine | |
| JP4045722B2 (ja) | アミン化合物、中間体、製造法および光学分割剤 | |
| JP4170990B2 (ja) | 光学的に活性であるセリン誘導体の製造方法 | |
| JP2013528581A (ja) | キラルなβ−アミノカルボキサミド誘導体の製造方法 | |
| EP0773921A1 (en) | Process for the preparation of a substituted 2.5-diamino-3-hydroxyhexane | |
| US6653507B2 (en) | Process for producing optically active 3,3,3-trifluoro-2-hydroxy-2-methylpropionic acid, and salt thereof | |
| JP4595178B2 (ja) | アミン化合物、中間体、製造法および光学分割剤 | |
| JP2012514005A (ja) | (2−アミノ)テトラヒドロカルバゾール−プロパン酸の合成 | |
| JP4406482B2 (ja) | 光学活性2−アミノシクロヘキサノール誘導体の製造法 | |
| JP2007332129A (ja) | 光学活性な4−アミノ−3−置換フェニルブタン酸の製造方法 | |
| JP2677115B2 (ja) | イミン化合物およびその製造方法 | |
| JP2004504261A (ja) | 水素化第一アミンの製造 | |
| WO2024028999A1 (ja) | N-[4-メチルアミノベンゾイル]-l-グルタミン酸ジエチルエステルの製造方法 | |
| JP2003171354A (ja) | 光学活性アミン化合物又はその塩の製造方法 | |
| JPWO2004065368A1 (ja) | トランドラプリル合成中間体の製造方法 | |
| JP4339074B2 (ja) | 光学活性な1,2−ビス(3,5−ジメチルフェニル)−1,2−エタンジアミンの製造方法 | |
| JP2011026201A (ja) | 光学活性ピロリル−コハク酸イミド誘導体の立体選択的な製造方法 | |
| WO2010004580A2 (en) | Process for preparing indole derivatives | |
| JP2011079782A (ja) | 光学活性1−アミノ−2−プロパノール及びその中間体、並びに、それらの製造方法 | |
| JP2003261524A (ja) | アミノ化合物類ならびにその立体選択的製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070614 |
|
| RD05 | Notification of revocation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7425 Effective date: 20080128 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100526 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100601 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100723 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100824 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100906 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131001 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |