JP4420653B2 - ニッケル・水素蓄電池 - Google Patents
ニッケル・水素蓄電池 Download PDFInfo
- Publication number
- JP4420653B2 JP4420653B2 JP2003379498A JP2003379498A JP4420653B2 JP 4420653 B2 JP4420653 B2 JP 4420653B2 JP 2003379498 A JP2003379498 A JP 2003379498A JP 2003379498 A JP2003379498 A JP 2003379498A JP 4420653 B2 JP4420653 B2 JP 4420653B2
- Authority
- JP
- Japan
- Prior art keywords
- hydrogen storage
- nickel
- electrode
- storage alloy
- positive electrode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Description
実施例1においては、負極活物質の水素吸蔵合金として、希土類元素のLaの他にMgとNiとを含み、組成式La0.7Mg0.3Ni3.4で表わされ、平均粒径が60μmになった水素吸蔵合金粉末を用いるようにした。なお、この水素吸蔵合金においては、希土類元素のLaと、Mgとの合計量に対するMgのモル比、Mg/(La+Mg)が0.3になっている。
比較例1においては、負極活物質の水素吸蔵合金として、希土類元素のLaの他にMgとNiとAlとCoとを含み、組成式La0.83Mg0.17Ni3.03Al0.17Co0.1で表わされ、平均粒径が60μmになった水素吸蔵合金粉末を用いるようにし、それ以外は、上記の実施例1の場合と同様にして、比較例1のニッケル・水素蓄電池を作製した。なお、この比較例1において用いた水素吸蔵合金においては、希土類元素のLaと、Mgとの合計量に対するMgのモル比、Mg/(La+Mg)が0.17になっている。
比較例2においては、負極として、上記の実施例1の場合と同様に、組成式La0.7Mg0.3Ni3.4で表わされ、平均粒径が60μmになった水素吸蔵合金粉末を用いて作製した水素吸蔵合金電極を用いるようにした。
比較例3においては、負極活物質の水素吸蔵合金として、上記の比較例1と同じ、組成式La0.83Mg0.17Ni3.03Al0.17Co0.1で表わされ、平均粒径が60μmになった水素吸蔵合金粉末を用いるようにし、また正極としては、上記の比較例2と同様にして作製した非焼結式のニッケル極を用いるようにし、それ以外は、上記の実施例1の場合と同様にして、比較例2のニッケル・水素蓄電池を作製した。
実験例1においては、上記の実施例1の場合と同じ、組成式La0.7Mg0.3Ni3.4で表わされ、平均粒径が60μmになった水素吸蔵合金粉末を用い、この水素吸蔵合金粉末100重量部に対して、結着剤のポリテトラフルオロエチレン5重量部と少量の水とを加え、これらを混合させてペーストを調製し、このペーストを圧延し、所定の寸法に切断し、これをニッケルメッシュで包み込み、加圧成形して負極として使用する水素吸蔵合金極を作製した。
実験例2においては、組成式La0.7Mg0.3Ni3.3で表わされ、平均粒径が60μmになった水素吸蔵合金粉末を用いるようにし、それ以外は、上記の実験例1の場合と同様にして、実験例2の試験セルを作製した。なお、上記の水素吸蔵合金粉末についても、Cu−Kα線をX線源とするX線回折測定装置(リガク社製:RINT2000)を用い、上記の実施例1の場合と同様にして、2θ=31°〜33°の範囲に現れる最強ピーク強度(IA)と、2θ=40°〜44°の範囲に現れる最強ピーク強度(IB)との強度比(IA/IB)を求めたところ、強度比IA/IBは0.127であり、CaCu5型とは異なる結晶構造を有していた。
活性化率P2(%)=(Dc/Da)×100
活性化率P3(%)=(Dd/Da)×100
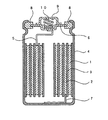
2 負極
3 セパレータ
4 電池缶
5 正極リード
6 正極蓋
7 負極リード
8 絶縁パッキン
9 正極外部端子
10 コイルスプリング
20 試験セル容器
21 作用極
22 対極
23 参照極
24 アルカリ電解液
Claims (1)
- 正極と、水素吸蔵合金を用いた負極と、アルカリ電解液とを備えた密閉型のニッケル・水素蓄電池において、上記の正極として焼結式のニッケル極を用いると共に、上記の水素吸蔵合金として、少なくとも希土類元素とマグネシウムとニッケルとを含み、Cu−Kα線をX線源とするX線回折測定において2θ=31°〜33°の範囲に現れる最強ピーク強度(IA)と、2θ=40°〜44°の範囲に現れる最強ピーク強度(IB)との強度比(IA/IB)が0.1以上であり、上記の希土類元素とマグネシウムとの合計量に対するマグネシウムのモル比が0.3以上であり、かつ、希土類元素とマグネシウムとの合計量に対する他の元素のモル比が3.3より大きいものを用いたことを特徴とするニッケル・水素蓄電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003379498A JP4420653B2 (ja) | 2003-11-10 | 2003-11-10 | ニッケル・水素蓄電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003379498A JP4420653B2 (ja) | 2003-11-10 | 2003-11-10 | ニッケル・水素蓄電池 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2005142104A JP2005142104A (ja) | 2005-06-02 |
| JP2005142104A5 JP2005142104A5 (ja) | 2008-07-17 |
| JP4420653B2 true JP4420653B2 (ja) | 2010-02-24 |
Family
ID=34689540
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003379498A Expired - Fee Related JP4420653B2 (ja) | 2003-11-10 | 2003-11-10 | ニッケル・水素蓄電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4420653B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105349841B (zh) * | 2014-08-19 | 2019-09-06 | 株式会社杰士汤浅国际 | 贮氢合金及其制造方法 |
-
2003
- 2003-11-10 JP JP2003379498A patent/JP4420653B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2005142104A (ja) | 2005-06-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5743780B2 (ja) | 円筒型ニッケル−水素蓄電池 | |
| JP2011233423A (ja) | アルカリ蓄電池 | |
| JP2012156101A (ja) | アルカリ蓄電池用水素吸蔵合金電極及びそれを用いたアルカリ蓄電池 | |
| JP4958411B2 (ja) | 水素吸蔵合金電極及びアルカリ蓄電池 | |
| JP5252920B2 (ja) | アルカリ蓄電池 | |
| JP5322392B2 (ja) | 水素吸蔵合金電極およびその製造方法ならびにアルカリ蓄電池 | |
| JP4342186B2 (ja) | アルカリ蓄電池 | |
| JP5717125B2 (ja) | アルカリ蓄電池 | |
| JP5512176B2 (ja) | アルカリ蓄電池およびアルカリ蓄電池システム | |
| JP3381264B2 (ja) | 水素吸蔵合金電極 | |
| JP6024295B2 (ja) | アルカリ蓄電池 | |
| JP2012134134A (ja) | アルカリ蓄電池 | |
| JP4420767B2 (ja) | ニッケル・水素蓄電池 | |
| JP4420653B2 (ja) | ニッケル・水素蓄電池 | |
| JP5147235B2 (ja) | ニッケル水素蓄電池 | |
| JP2005226084A (ja) | アルカリ蓄電池用水素吸蔵合金、アルカリ蓄電池及びアルカリ蓄電池の製造方法 | |
| JP4989033B2 (ja) | アルカリ蓄電池用水素吸蔵合金及びニッケル・水素蓄電池 | |
| JP2018070931A (ja) | 負極材料および電池 | |
| JP2013196991A (ja) | アルカリ蓄電池 | |
| JPH11162459A (ja) | ニッケル水素二次電池 | |
| JP4420641B2 (ja) | アルカリ蓄電池用水素吸蔵合金及びアルカリ蓄電池 | |
| JP3895985B2 (ja) | ニッケル・水素蓄電池 | |
| JP4115367B2 (ja) | アルカリ蓄電池用水素吸蔵合金及びその製造方法並びにアルカリ蓄電池 | |
| JP3895984B2 (ja) | ニッケル・水素蓄電池 | |
| JP2563638B2 (ja) | 水素吸蔵合金電極 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060728 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080529 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20080613 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080624 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080806 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20091104 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20091201 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121211 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121211 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131211 Year of fee payment: 4 |
|
| LAPS | Cancellation because of no payment of annual fees |