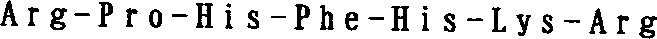JP4210330B2 - ヒアルロン酸レセプター結合剤、およびその使用方法 - Google Patents
ヒアルロン酸レセプター結合剤、およびその使用方法 Download PDFInfo
- Publication number
- JP4210330B2 JP4210330B2 JP52393097A JP52393097A JP4210330B2 JP 4210330 B2 JP4210330 B2 JP 4210330B2 JP 52393097 A JP52393097 A JP 52393097A JP 52393097 A JP52393097 A JP 52393097A JP 4210330 B2 JP4210330 B2 JP 4210330B2
- Authority
- JP
- Japan
- Prior art keywords
- cac
- amino acids
- letter code
- hyaluronic acid
- pip2
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/42—Proteins; Polypeptides; Degradation products thereof; Derivatives thereof, e.g. albumin, gelatin or zein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/117—Esters of phosphoric acids with cycloaliphatic alcohols
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70585—CD44
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Description
この発明は、レセプターが介在する治療によって治療可能な疾患や異常を治療するために好適な新規な結合剤、および治療が必要な哺乳動物の各部位のレセプターに結合するように該結合剤を使用する方法に関する。本発明は、例えば、ヒト悪性腫瘍の治療に使用できる。
発明の背景
Hyal Pharmaceutical Corporationを譲受人とする米国特許出願第07/675,908号明細書および同様にHyal Pharmaceutical Corporationを譲受人とするPCT特許出願PCT/CA90/00306、公開番号第WO91/04058号公報(これから米国特許出願第07/675、908が国内段階として出願されている)には、少なくとも約10mgのヒアルロン酸(HA)を投与して、人体の治療が必要な部位に有効量の薬剤及び/又は治療薬を運び、瘢痕組織を始めとする治療が必要な部位の組織を全ての膜を介して治療すべき細胞の送り込むようにする使用法が開示されている。
上記PCT出願明細書の第25頁第17行には、薬剤及び/又は治療剤と少なくとも約200mgのヒアルロン酸(例えば、ヒアルロン酸ナトリウム)を併用した場合の効果について記載がある。即ち、薬剤及び/又は治療剤投与時の副作用(胃腸障害、神経異常、抑欝などが通常認められる副作用である)が、例えば、NSAID(非ステロイド系抗炎症剤)等を単独投与した場合、通常許容されている適正投与量以上で投与されたときでも抑制できることが記載されている。同様にHyal Pharmaceutical Corporationを譲受人とする米国特許出願第08/486,328号明細書、同第08/520,591号明細書、およびPCT出願第PCT/CA95/00477号明細書には、ヒアルロン酸類の使用によって、ヒアルロン酸に対して高い親和性を示す細胞表面レセプターを発現する組織および細胞の細胞活性の調節について開示している。これら細胞表面レセプターは、ヒアルロナンを結合する付着分子ICAM−1、付着分子CD44及び付着分子HARLEC[ヒアルロン酸(ヒアルロナン−Hyaluronan)レセプター肝臓内皮細胞)、および調節分子RHAMM(HA介在運動性を対象とするレセプター−Receptor for HA Mediated Motility)を有する。HARLECは肝臓内皮細胞に発現し、(その細胞表面に産生し、かつ付着する)。有効量のある形のヒアルロン酸を投与して、細胞表面レセプターに結合した場合、人体内において、ヒアルロン酸に対して高い親和性を示す細胞表面レセプターを発現する組織及び/又は細胞(例えば、付着細胞または調節細胞)の細胞活性を調節することができる。
薬剤及び/又は治療剤を輸送するためにヒアルロン酸を使用できる理由の一つは、その細胞表面レセプターに対する選択的結合である。
人体は、少なくとも1028の異なるアミノ酸の組合せを有する。例えば、“Identification of Recognition Sequences of Adhesion Molecules Using PhageDisplay Technology”、O’Neil、Karyn T.、et al;Methods in Enzymology、Vol.245、(1994)、370−386を参照。ある種のヒアルロン酸、例えばヒアルロン酸ナトリウム(HA)を誘因体として人体に送り込むと、全体で少なくとも1028の組み合せからわずか2つのアミノ酸の組み合せがHAに結合する。この2つの組み合せはHAに対する特異性が高い。
1.最初の組み合せのアミノ酸配列は次の通りである。
下線部はHA結合タンパク質(Rhamm、ICAM−1、CD44、HARLECなど)の基本的アミノ酸モチーフである。下線部は結合部分である。
2.アミノ酸結合部分の第2系列は第2アミノ酸配列に存在する。即ち、
このアミノ酸の結合部分は小さく、結合対象部分は細胞核である。この小さな結合部分は、細胞核に転座するただ一つのHAレセプターであるHA結合タンパク質Rhammにも結合する。
各アルファベットは以下の表に示す異なるアミノ酸を表す。
上記モチーフがHA結合部分になることを示す証拠は、The EMBO Journal、Vol.13、No.2(1994)、pp.286−296に発表された論文“Identification of a common hualuronan binding motif in the hyaluronan binding proteins RHAMM、CD44 and link protein”にある。この論文(写しを添付してある)の内容は、本明細書で従来例として使用する。
本発明者は、試験を通じて、別な分子、即ちPIP−2(ホスファチジルイノシトール−4,5−ビスホスフェートであり、このうちのホスホイノシトール−4,5−ビスホスフェートが活性部分である)がこれら同じ部分に特異的に結合することを見いだした。PIP2の構造式は次の通りである。
上記式のうちの下記の部分が活性部分である。
よく知られているように、RhammはHAに結合する。本発明者は、試験によって、RhammはPIP2にも結合することを見いだした。PIP2を過剰に使用した場合、HAを置換する。Rhammは、腫瘍形成、再狭窄や他の修復例に対して“upregulated”になる点で、きわめて重要なレセプターである。HAは、(Rhammを始めとする)表面細胞レセプターに選択的に結合する能力があるため、薬剤を疾患部位や異常部位に輸送するために使用するのにすぐれたものである。このように、PIP2はHAを単独で使用して、あるいは薬剤及び/又は治療剤と併用して、治療してきた同じ異常や疾患を治療するために使用できる。PIP2は小さな分子であるため、PIP2、あるいはPIP2、HAに似た化合物、即ちHAやPIP2の類似体、同族体、誘導体、錯体なども有効にかつより簡単に使用できるはずである。これら化合物は、新規な、合成または精製天然化合物である。なお、天然に産生するものは、未精製状態である。
即ち、本発明の目的は新規な結合剤を提供することである。
本発明の別な目的は、治療を必要とする、例えば、悪性腫瘍や再狭窄の治療を必要とする哺乳類の体内部位にあるレセプターと結合するレセプター介在治療によって治療可能な疾患や異常を治療するために上記の新規結合剤を使用する治療方法を提供することである。
当業者ならば、以下の発明の要約および実施例の詳細な説明から、本発明の上記以外の目的を理解できるはずである。
発明の要約
本発明は、第1に、(ヒアルロナン、薬学上許容できるヒアルロナンの塩または他の形のヒアルロン酸類以外の)、有効量の結合剤と併用して、有効量の薬剤及び/又は治療剤を投与するレセプター介在治療によって治療可能な、あるいは予防可能な疾患及び/又は異常を治療及び/又は予防する新規な方法を提供するものである。この結合剤は、薬剤及び/又は治療剤と混合して投与する。疾患部位または異常部位に到達すると、以下の結合部分からなる群から選択される少なくとも一つの部分で上記部位に結合する。
(a)RSHKTRSHH
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}、あるいは
{別コード}
(b)RPHFHKR
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}、あるいは
{別コード}
このような結合剤の一つは、PIP2の活性部分、ホスホイノシトール−4,5−ビスホスフェートである。新規な結合剤は、ヒアルロナンも結合する上記部分に結合するため、本発明は、ヒアルロナンが有効な、任意のレセプター介在治療にも適用可能である。このように、本発明はヒアルロナンの使用方法と同様にして、再狭窄の予防や他の治療にも使用できる。即ち、本発明は以下の公開、未公開公報に記載されている治療や予防治療に使用できる。まず、1995年12月1日にカナダ特許庁に出願され、“所定投与量の薬剤および治療剤の標的”を発明の名称とするカナダ特許出願第2,164,260号明細書、および1996年3月29日に出願され、“所定投与量の薬剤、治療剤およびその他のグリコサミノグリカン類(GAGS)の標的”を発明の名称とするカナダ特許出願第2,173,037号明細書を挙げる。さらに、以下のものがある。
いずれも従来例として本明細書で使用するものである。なお、各明細書記載の各形態のヒアルロナンを例えば本明細書に開示する他の結合剤で置換することができ、同様に使用することができる。
いくつかの用途を説明するために、一例として、PCT/CA90/00306(国際公開第WO91/04058)から次の記載を引用する。
(i)第17頁第3行〜第18頁第16行に次の記載がある。
本出願人は、疾患や異常を治療するために、症例に応じて、治療上有効な非毒性量の薬剤及び/又は治療剤を使用した、あるいは配合した併合製剤および製剤組成が疾患や異常を治療するために、治療すべき個々の細胞に細胞膜を介して治療されるべき部位において、(瘢痕組織を含む)組織への製剤の浸透を促進するのに十分な量のヒアルロン酸及び/又はその塩(例えば、ナトリウム塩)及び/又はヒアルロン酸の同族体、類似体、誘導体、錯体、エステル、フラグメント及び/又はサブユニットとともに投与するか、これらに担持した形で哺乳類に投与できることを見いだした。詳しくは、これら併合製剤または製剤組成は、必要に応じて、治療上有効な非毒性量の疾患や異常を治療する薬剤及び/又は治療剤、例えば遊離ラジカルスカベンジャー(例えば、アスコルビン酸(ビタミンC))、(単核細胞症治療用の)ビタミンC、抗癌剤、化学療法剤、避妊クリームDelfenTMに存在するノノキシノール−9[ノニルフェノキシポリエトキシエタノール]などのノニオン系表面活性剤、アニオン系表面活性剤(例えば、塩化セチルピリジニウム)やカチオン系表面活性剤(例えば、塩化ベンザルコニウム)などの抗ウィルス剤、非ステロイド系抗炎症剤(NSAID)、例えば、インドメタシン、ナプロキセンおよび(ToradolTMの商標で市販されている)ケトラックのトロメタミン塩およびステロイド系抗炎症剤、抗真菌剤、解毒剤(例えば、直腸浣腸剤)、鎮痛剤、気管支拡張剤、抗菌剤、抗生物質、血管虚血治療剤(例えば、糖尿病治療剤、バージャー病治療剤)、抗体単クローン剤、育毛を対象とする局所投与用ミノキシジル、利尿剤(例えば、LasixTMの商標で市販されている(フロセミド))、免疫抑制剤(例えば、シクロスポリン)、リンホカイン(例えば、インターロイキン−2などやα−and−β−インターフェロンなど)を利用したり、配合するものである。このような併合製剤や製剤組成物を罹患している患者に投与した場合、疾患や異常に予期しない程の改善がみられる。
これら製剤組成物はさまざまな方法で投与できる。即ち、静脈投与、動脈投与、腹腔投与、胸膜腔投与、経皮投与、皮膚への(局所)投与、直腸投与、経口投与、(例えば、腫瘍、膿瘍などの患部への)直接注射投与、患者の皮膚へ貼った絆創膏への投与などの投与方法が利用できる。ヒアルロン酸及びその塩、および製剤は別々に投与することも可能であるが、疾患や異常を治療するためには、好ましくは同一部位(ある部位では静脈投与、そして他の部位ではピギーバック方式投与)に、十分な量で、しかも連続的か断続的(好ましくは共存的に、より好ましくは同時に)に投与するのがよい。
(ii)第25頁、第18行から第26行、第14行には次の記載がある。
このように、また発明の別な態様によれば、(n−メチルグルカミンに溶解した)インドメタシンなどのNSAIDや他のNSAIDを200mg以上のヒアルロン酸とともに、体重1kgにつき1〜2mgの量でNSAID(例えば、インドメタシンとNMG)を投与すると、(必要に応じて)大量にインドメタシンを投与した場合でも、胃腸障害、神経異常や抑欝などの重大な毒性副作用が生じない。ヒアルロン酸量をこれより抑えると、通常の副作用が再発する恐れがある。さらに、認められた反応は、NSAID(例えば、IndocidTM)をヒアルロン酸と併用した場合によりすぐれたものになり、全身の静脈により投与しても、併用が病変組織を“標的”にすることを明らかに示している。このように、腫瘍性の病気に罹患した患者に、他の薬剤(例えば、アスコルビン酸[ビタミンC]、フロレチンや抗癌剤など)に加えて、50〜200mgのNSAID−ヒアルロン酸(ヒアルロン酸ナトリウム)(例えば、インドメタシンおよびヒアルロン酸)を投与すると、疼痛がただちに劇的に消える。この後少しの時間がたつと、腫瘍部が消散、再吸収され、肺機能や肝機能に、これら臓器に腫瘍が残存していても、改善が認められることになる。このように、ヒアルロン酸(その塩など)とともに投与されたNSAID(またはステロイド系抗炎症剤)によって活性が増大したマクロファージの作用によって死滅した腫瘍、腫瘍遺残や腫瘍毒素が体外に排出されることになる。即ち、本出願人は、NSAIDをヒアルロン酸(ヒアルロン酸ナトリウム)と併用すると、マクロファージ機能を阻害するプロスタグランジンシンセターゼの酵素作用による産生を阻止することによって、マクロファージを脱阻害するとみている。このように、ヒアルロン酸(塩などの形で)はNSAIDの活性を強化するだけでなく、プロスタグランジン合成抑制剤の使用に伴う副作用や毒性を低減するものである。
化学療法剤として使用するのに好適な薬剤を例示すれば、ノバントロン(ミトキサントロン)、メソトレキサート、5−FU(5−フルオウラシル)、カルボプラチン、経口投与用メチルCCNU、およびミトマイシンCがある。
(iii)第26頁、第32行〜第37には次の記載がある。
ヒアルロン酸およびその塩は異なる投与量、即ち体重70kgに対して10〜1,000mgの投与量で使用でき、最適投与量は体重70kgに対して50〜350mgである。毒性がないため、ヒアルロン酸を過剰量(例えば、体重70kgに対して3,000mg)で使用しても、副作用は認められない。
(iv)第29頁、第27行から第33頁、第31行には次の記載がある。
本発明に使用するのに好適なある一つの形のヒアルロン酸及び/又はその塩(例えば、ナトリウム塩)、およびヒアルロン酸の同族体、類似体、誘導体、錯体、エステル、フラグメント及びサブユニット、好ましくはヒアルロン酸およびその塩は、Sterivet Laboratories Limited製のフラクションである。このようなフラクションの一つは、ヒアルロン酸ナトリウム20mg/mlの15mlバイアル(300mg/バイアル−Lot2F3)である。ヒアルロン酸ナトリウムフラクションは2%溶液で、平均分子量は約225,000である。フラクションはまた水q.s.を含み、これは、注射組成物とするには、U.S.P.に従って三回蒸留し、殺菌する。ヒアルロン酸及び/又はその塩のバイアルは、バイアルの内容物と反応しないブチルストッパーで密封したタイプ1ホウケイ酸ガラスバイアルに担持してもよい。
ヒアルロン酸及び/又はその塩(例えば、ナトリウム塩)、およびヒアルロン酸の同族体、類似体、誘導体、錯体、エステル、フラグメント及びサブユニット、好ましくはヒアルロン酸およびその塩のフラクションは、下記の特性をもつヒアルロン酸及び/又はその塩からなるものである。
以下に示す特性のうち少なくとも一つの特性を示す、天然源から得られたヒアルロン酸の実質的にピロゲンを含まない、精製フラクション。
i)150,000〜225,000の分子量、
ii)硫酸化ムコ多糖類が全重量基準で約1.25%未満、
iii)タンパク質が全重量基準で約0.6%未満、
iv)鉄分が全重量基準で約150ppm未満、
v)鉛分が全重量基準で約15ppm未満、
vi)グルコサミンが0.0025%未満、
vii)グルクロン酸が0.025%未満、
viii)N−アセチルグルコサミンが0.025%未満、
ix)アミノ酸が0.0025%未満、
x)257nmにおけるUV消衰係数が約0.275未満、
xi)280nmにおけるUV消衰係数が約0.25未満、および
xii)7.3〜7.9の範囲にあるpH。
好ましくは、ヒアルロン酸を水と混合する。また、ヒアルロン酸フラクションの平均分子量が150,000〜225,000の範囲にあるのが好ましい。より好ましくは、ヒアルロン酸のフラクションが下記に示す特性のうち少なくとも一つの特性を有する。
i)硫酸化ムコ多糖類が全重量基準で約1%未満、
ii)タンパク質が全重量基準で約0.4%未満、
iii)鉄分が全重量基準で約100ppm未満、
iv)鉛分が全重量基準で約10ppm未満、
v)グルコサミンが0.00166%未満、
vi)グルクロン酸が0.0166%未満、
vii)N−アセチルグルコサミンが0.0166%未満、
viii)アミノ酸が0.00166%未満、
x)257nmにおけるUV消衰係数が約0.23未満、
xi)280nmにおけるUV消衰係数が約0.19未満、および
xii)7.5〜7.7の範囲にあるpH。
他の形のヒアルロン酸及び/又はその塩、およびヒアルロン酸の同族体、類似体、誘導体、錯体、エステル、フラグメントおよびサブユニットについては、他の製造メーカー、例えば既に言及した先行文献に記載されている各メーカーから入手可能である。さらに、本発明では、以下の具体的特性をもつ、LifeCoreTM Biomedical、Inc.製のヒアルロン酸ナトリウムを使用するのが有利である。
特性 特性値など
外観 白色ないしクリーム色の粒子
臭気 知覚できるほどの臭気はない
平均粘度 <750,000ダルトン
分子量
UV/Vis走査、190〜820nm 基準走査対応
OD、260nm <0.250D単位
ヒアルロニダーゼ感受性 陽性反応
IR走査 基準走査対応
pH、10mg/g溶液 6.2〜7.8
水 最大8%
タンパク質 <0.3mcg/mgNa
Hy
アセテート <10.0mcg/mgNaHy
重金属、最大ppm
As Cd Cr Co Cu Fe Pb Hg Ni
2.0 5.0 5.0 10.0 10.0 25.0 10.O 10.0 5.0
微生物による生物学的負荷 認められず
内毒素 <0.07EU/mgNaHy
生物学的安全性試験 ウサギによる眼球毒性試験をパス
以下の各文献には、ヒアルロン酸、ヒアルロン酸源、およびヒアルロン酸の製造方法および回収方法が記載されている。
米国特許第4,141,973号には、以下の特性を示す(ナトリウム塩を含む)ヒアルロン酸フラクションが記載されている。
(a)平均分子量が約750,000以上、好ましくは約1,200,000以上である。即ち、限界粘度数が約1,400cm3/g以上、好ましくは2,000cm3/g以上である。
(b)タンパク質含量が0.5重量%未満である。
(c)ヒアルロン酸ナトリウム1%溶液の紫外線吸光度が波長257nmで3.0未満、好ましくは波長280nmで2.0未満である。
(d)ヒアルロン酸ナトリウムの1%生理学的緩衝液の動粘度が約1,000cS以上、好ましくは約10,000cS以上である。
(e)220nmで測定した場合、ヒアルロン酸ナトリウムの0.1〜0.2%生理学的緩衝液のモル旋光度が−11×103degree−cm2/モル(二糖類)未満である。
(f)生理学的緩衝液に溶解したヒアルロン酸ナトリウムの1%溶液1mlを硝子液に注入して、存在する硝子液のほぼ半分を置き換えた場合、ヨザル眼球の硝子液および前房の有意味な細胞浸潤が生じない、房水フレアがない、硝子液に濁りやフレアがない、角膜、水晶体、虹彩、網膜および絨毛膜に対して病理学的変化がない。このHUAが
(g)無菌で、ピロゲンを含まず、そして
(h)非抗原性である。
カナダ特許第1,205,031号(従来例として米国特許第4,141,973号に言及)には、平均分子量が50,000〜100,000、250,000〜350,000および500,000〜730,000のヒアルロン酸ナトリウム、およびその製造方法が記載されている。
高分子量ヒアルロン酸(またはその塩か他の形のヒアルロン酸)を使用する場合、筋肉内凝固を起こさずに投与を可能にするために、希釈する必要がある。
(vi)第33頁、第37行から第35頁、第30行には次の記載がある。
このように、本出願人がヒアルロン酸(およびヒアルロン酸ナトリウム及び/又は他の形のヒアルロン酸)を薬剤及び/又は治療剤と併用して、異常や疾患を治療した場合に、全く予期しない結果が得られた。
具体例
1.適用例
癌、マクロファージの活性増大
薬品および薬剤
遊離ラジカルスカベンジャー、スーパーオキシドジムスターゼ、アスコルビン酸(ビタミンC)、抗癌剤、NSAID、化学療法剤、解毒剤(例えば、コレスチラミン)
1A.適用例
脳外傷患者(DMSO)における脳腫ちょうの抑制
薬品および薬剤
ジメチルスルホキシド
2.適用例
育毛、局所投与による増毛
薬品および薬剤
ミノキシジル−併用
3.適用例
ヘルペス、粘膜潰瘍、帯状泡疹
薬品および薬剤
ノニオン系表面活性剤(ノノキシノール−9など)、アニオン系表面性剤(塩化セチルピリジニウムなど)、カチオン系表面活性剤(塩化ベンザルコニウムなど)
4.適用例
腎不全、心不全、高血圧、浮腫
薬品および薬剤
利尿剤−フロセミド
5.適用例
感染症、アクネ、単核細胞症
薬品および薬剤
抗生物質、抗菌剤、殺菌剤、etc.アスコルビン酸、ヒアルロン酸
6.適用例
移植
薬品および薬剤
シクロスポリン
7.適用例
炎症、腫瘍破壊物の除去
薬品および薬剤
非ステロイド系抗炎症剤、NSAID(毒素、遺残など)、ジクロフェナク
適用例
副作用の抑制
薬品および薬剤
インドメタシン、ピロキシカム
適用例
(背中の痛みなどの)疼痛除去
薬品および薬剤
イブプロフェン、ケトロラックのトロメタミン塩、ナプロキセン
8.適用例
解毒
薬品および薬剤
浣腸剤、解毒剤、腹膜透析
9.適用例
気管支拡張
薬品および薬剤
ベクロメタゾンジプロピオネートなどの気管支拡張剤、クロモグリク酸ナトリウム(ただし、適用例は気管支拡張剤としてだけではない。)
10.適用例
血管虚血
薬品および薬剤
トレンタールなどの適当な薬剤と併用して、糖尿病、バージャー病などにおける四肢の治療に使用
11.適用例
HIV(AIDS)
薬品および薬剤
DMSO、ビタミンC、(インドメタシン、ナプロキセン、ケトラックトロメサタンなどの)NSAID、インターフェロン、VibramycinTM、(ドキシサイクロン)、テトラサイクリン
12.適用例
糖尿病
薬品および薬剤
インシュリン
13.適用例
閉経後
薬品および薬剤
エストロゲン代替物
14.適用例
局所予防
薬品および薬剤
代謝拮抗剤(インフェクション−スルホンアミドなど)
15.適用例
腫ちょうの抑制
薬品および薬剤
DMSO
16.適用例
高血圧、心臓
薬品および薬剤
カルシウムチャネルブロッカー(インサフィシャンシーニフェジピンなど)、β−ブロッカー(アテノール、プロパノールなど)
17.適用例
プロスタグランジン合成抑制
薬品および薬剤
アセチルサリチル酸
18.適用例
(移植を目的として)組織を灌流する灌流液による組織酸素供給の強化
薬品および薬剤
灌流剤
即ち、本発明は、別な態様によれば、レセプター介在治療によって治療することができ、かつ(ヒアルロナン以外の形の)結合剤を有効な量で投与することからなる疾患や異常を治療する方法であって、上記結合剤が、
(a)RSHKTRSHH
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}、あるいは
{別コード}
(b)RPHFHKR
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}、あるいは
{別コード}
から選択される少なくとも一つの結合部分で疾患部位または異常部位に結合することによって、上記レセプターの機能を抑制する疾患または異常の治療方法を提供するものである。
この態様によれば、例えば、再狭窄を予防するために、この結合剤を有効な量で投与すると、狭窄部位に平滑筋細胞が移動したり、白血球細胞(マクロファージ)が侵潤することがなくなる。
治療上有効な量と考えられる結合剤の量は、体重1kgにつき結合剤(例えば、PIP2)約0.1〜約1.5mgである。好ましくは、治療を受ける患者の体重1kgにつき結合剤(例えば、PIP2)を約0.2〜1mgを投与できる。この量を上記範囲外にしても有効であるが、好ましくは、細胞や人体のいずれに対しても毒性を示さない量で結合剤を投与する必要がある。にもかかわらず、使用する量では結合剤が毒性がないと考えられる場合でも、患者個々にとって有効な量で結合剤を投与した場合に細胞が死ぬことがある。投与は必要な期間続ける。
上記のPIP2は、本発明の目的を満足するもので、投与する場合には、体重1kgにつき約0.1〜約1.5mg、特に0.2〜1mgの適正量で使用する。PIP2の薬効(例えば、治療効果)を増強するために、例えば、グルクロン酸や他の適当な非毒性・親水性剤にPIP2を結合するなどして、変性すると、PIP2の脂肪可溶性を低く抑えることができる。反応生成物は、PIP2と親水性剤とから調製することができる。
また、PIP2結合分子はそれ自体が変性して、ホスフェートをサルフェート、カーボネート、ナイトレート、サルファイト、ナイトライトなどの他の部位によって置換することができる。
また、目的のレセプターへの結合を達成するために、イノシトール環全体を必要とするものではない。つまり、ヒドロキシルラジカルが結合する4つの炭素原子からなる、椅子形構造部分のみが上記結合に必要と考えられる。換言すれば、下記の式で表される椅子形構造を構成するこれら4つの炭素原子を含む別な分子が好適である。即ち、次の構造式の化合物が好適である。
ただし、R1とR2は、分子の残りの部分とともに、(PIP2と同様に)閉環を形成するか、あるいは結合することなく、閉環分子を形成するブリッジを形成し、そしてR1とR2はそれぞれ低級アルキルか他の適当な置換基である。
さらに、体内に自然に存在するHAに結合して、HAがレセプターを刺激することを阻止する結合剤として、下記の右旋形結合部分(アミノ酸配列)
(a)RSHKTRSHH
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}
(b)RPHFHKR
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}
を使用することができる。これらの作用機序は、上記の右旋形が分割できないことによる。このように、右旋形アミノ酸配列は、大きな結合部分および小さな結合部分両者の結合モチーフに結合するために使用できる。
上記の、
(a)RSHKTRSHH
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}
(b)RPHFHKR
{アミノ酸の一文字コード}、あるいは
{アミノ酸の三文字コード}
それぞれに対するアンチセンスペプチド、および上記で説明した右旋形アンチセンスペプチドもまた好適である。これれらは、当業者ならば簡単かつ容易に同定できるはずである。また、これらは公知方法によって調製でき、これについても、当業者ならば理解できるはずである。従って、PIP2模擬体や(ヒアルロナンの形を取らない)他のヒアルロナン模擬体も好適である。アンチセンスペプチドは次の通りである。
(a)については、アンチセンスペプチドはASVFWSSVV(別コードで示せば、GCG-AGC-GTG-TTC-TGG-TCC-AGC-GTG-GTG)であり、
(b)については、アンチセンスペプチドはAGVKVFA(別コードで示せば、GCC-GGG-GTG-AAG-GTG-TTC-GCC)である。
アンチセンスペプチドは、当業者者にとっては公知な方法によって製造でき、簡単に同定できる。以下の文献が参考になる。
(i)“Identification of Recognition Sequences of Adhesion Molecules Using Phage Display Technology”、Methods inEnzymology、Vol.245、p.370、および
(ii)“Molecular Cloning of a Novel Hyaluronan Receptor that Mediates Tumour Cell Motility”、The Journal of Cell Biology、Vol.117、1992、p.1343。
これらアンチセンスペプチドの使用量は前記と同じで、体重1kgにつき約0.1〜約1.5mgである。この量を上記範囲外にしても有効であるが、上記と同様に好ましくは、細胞や人体のいずれに対しても毒性を示さない量でアンチセンスペプチドを投与する必要がある。にもかかわらず、使用する量ではアンチセンスペプチドが毒性がないと考えられる場合でも、患者個々にとって有効な量で投与した場合に細胞が死ぬことがある。投与は必要な期間続ける。
【図面の簡単な説明】
図1
(1)ビオチニル化ヒアルロナン単独、(2)PIP2を5ug/ml、(3)PIP2を50ug/ml、(4)PIP2を250ug/ml、および(5)未標識ヒアルロナンを100ug/ml存在させた状態で、ビオチニル化ヒアルロナンプローブにアミノ酸配列RSHKTRSHHを含むファージを結合した。これら結果から、PIP2により、上記配列へのヒアルロナンの結合が有効に抑制できることがわかる。また、未標識ヒアルロナンのこの配列に対するビオチニル化ヒアルロナンに拮抗する能力により、ヒアルロナンとこの配列との間の相互作用の特異性が確認できる。
図2
PIP2の、RHAMMへのヒアルロナンの結合を抑制する能力。(a)ビオチニル化ヒアルロナンはRHAMMに結合する(この細部および対照については、Yang等の論文“Identification of a commonlink protein”、(The EMBO Journal、Vol.13、No.2、pp.286−296、1994を参照。この文献の内容は従来例として本開示に記載してある)。(b)250ug/mlのPIP2は、本質的に、ヒアルロナンからRHAMMに結合する能力を奪うものである。図1に示した配列RSHKTRSHHは基本アミノ酸(7つの介在アミノ酸)基本アミノ酸のヒアルロナン結合モチーフ(細部については、上記のYang等の論文を参照)を有し、これがPIP2に結合するため、PIP2が、ヒアルロナンがRHAMMにおいて結合する同じモチーフに結合する。
図3
トランスブロット評価における3H−PIP2のRHAMMへの結合。3H−PIP2はRHAMMに結合し、これは未標識PIP2に拮抗する。
図4
細胞質および細胞核に局在化したRhamm。
図5
細胞核、そして程度は小さいが細胞質に存在するFITC−HA。
実施例の詳細な説明
手順
図1
ストレプタビジン被覆ビーズで捕捉したビオチニル化ヒアルロナンに暴露することによって配列RSHKTRSHHを有するバクテリオファージを単離した。次に、これらバクテリオファージを5〜250ugのPIP2の存在下でビオチニル化ヒアルロナンに、あるいは100ugの未標識外因性ヒアルロナンに暴露した。これらの異なる条件下においてビオチニル化ヒアルロナンプローブで捕捉したバクテリオファージを寒天プレートに面線接種し、37℃で48時間培養した。培養プレートを次に写真撮影した。
図2
Yang,B.、Yang.B.L.、Savani,R.C.およびTurley,E.A.がThe EMBO Journal13、286−296(1994)に詳しく記述しているように、E.Coli菌に形質変換したRHAMMv2cDNAを使用して、RHAMM変異体2を合成した。RHAMMタンパク質をSDS−PAGE(上記文献を参照)中で電気泳動させ、酢酸ニトロセルロースにトランスブロットした。次に、ビオチニル化ヒアルロナンを膜培養し、結合したビオチニル化ヒアルロナンを上記文献記載の化学発光によって検出した。同じではあるが別なブロットにおいて、ビオチニル化ヒアルロナンをPIP2(250ug/ml)と混合し、混合物を次にRHAMMを有する膜で培養した。上記と同様にして、結合ビオチニル化ヒアルロナンを化学発光により検出した。
図3
SDS−PAGEで分離し、かつ上記のようにしてニトロセルロース膜にトランスブロットしたRHAMMで、トリチウム標識化PIP2(Amersham、50uCl/10ml)を培養した。放射線標識化PIP2をRHAMMで1時間培養し、洗浄し、KODAKの放射能写真フィルムに一月露光した。Bioradデンシトメーターを使用して、フィルム走査した。ブロットを洗剤で洗浄し、多クローン抗RHAMM抗体を使用して、RHAMMについて再プローブして、放射線標識化バンドがRHAMMタンパク質に一致するかどうかをチェックした。
PIP2疑似体投与量の決定
ヒアルロナンに拮抗する投与量範囲は5−250ug/10ml。ラットの血液容量は約15mlで、ラットの平均体重は250gである。
従って、ラットに対するPIP2の使用量は体重基準で25〜375ug/250gまたは100〜1,500ug/kgまたは0.1〜1.5mg/kgである。
当業者にとっては公知な方法で、有効量の変更アデノウイルス組み込み遺伝子治療剤(例えば、GMCSF−髄コロニー刺激因子における成長の頭文字)を投与を目的として調製する。この変更アデノウイルスは、投与されると、免疫システムを腫瘍に引き付ける作用をもつ。本発明では、従来より知られている方法で投与するのではなく、本発明のアンチセンスペプチドでアデノウイルス組み込み遺伝子治療剤を変更して、表面に変更“ウイルスコート”したものを患者に投与する。なお、当業者ならば、公知方法によってこれを簡単に実施できるはずである。
乳癌、膵臓癌、結腸癌では、HA(ヒアルロナン)レセプターが増大する。換言すれば、過度に表現される。転移の場合、RHAMM表現(HAレセプター表現)が大きく表れる。即ち、上記のようにアンチセンスペプチド(結合部分の鏡像)をオーバーコートとして組み込んで(そして特に上記のアンチセンスペプチド(b)を組み込んで)変更したアデノウイルスを投与すると、癌性腫瘍のRHAMMに結合し、アデノウイルスが正確に細胞核に到達する。このため、腫瘍の核がアデノウイルスによって変更され(遺伝子が設計通りに有効に複製される)、腫瘍が免疫システムによって破壊されることになる。これは、RHAMMを表現する細胞では、ヒアルロナンが細胞に到達し、RHAMMに結合し、約15分後、ヒアルロナンが細胞核に浸透することによる。アンチセンスペプチド、例えばアンチセンスペプチドは、従って、細胞に正確に浸透し、細胞核に浸透する。この作用機序を図4および図5に示す。特に、図5では、FITC−HA(ヒアルロナン)が細胞核および細胞質に存在している。同じことは、上記のアンチセンスペプチドについてもいえる。この点については、“Nuclear Localization Signals Direct Nuclear Proteins to the Nucleus”、The Molecular Biology of the Cell、3rd edition、pp.563−564(B.Alvertz、D.Brag、J.Lewis、M.Raff、K.Roberts、J.O.Watosn)が参考になる。
発明の範囲から逸脱せずに、上記実施例では多くの変更が可能である。従って、ここで開示したものはすべて発明を説明するためのもので、発明を制限するものではない。
Claims (2)
- 再狭窄の治療又は予防のための有効量の薬剤及び/又は治療薬および有効量のホスファチジルイノシトール−4,5−ビスホスフェート(以下、PIP2と略記する)とを含む再狭窄の治療又は予防のための薬剤組成物であって、PIP2は該薬剤及び/又は治療薬と混合され、かつ、疾患部位又は異常部位にて、下記の結合部分群の少なくとも1つと結合する結合剤として機能することを特徴とするもの:
(a)RSHKTRSHH
{アミノ酸の一文字コード}あるいは
{アミノ酸の三文字コード}あるいは
CGC−TCG−CAC−AAG−ACC−AGG−TCG−CAC−CACでコード化されるもの、
(b)RPHFHKR
{アミノ酸の一文字コード}あるいは
{アミノ酸の三文字コード}あるいは
CGG−CCC−CAC−TTC−CAC−AAG−CGGでコード化されるもの。 - 有効量のホスファチジルイノシトール−4,5−ビスホスフェート(以下、PIP2と略記する)を含む再狭窄の治療又は予防のための薬剤組成物であって、PIP2は疾患部位又は異常部位にて、下記の結合部分群の少なくとも1つと結合する結合剤として機能することを特徴とするもの:
(a)RSHKTRSHH
{アミノ酸の一文字コード}あるいは
{アミノ酸の三文字コード}あるいは
CGC−TCG−CAC−AAG−ACC−AGG−TCG−CAC−CACでコード化されるもの、
(b)RPHFHKR
{アミノ酸の一文字コード}あるいは
{アミノ酸の三文字コード}あるいは
CGG−CCC−CAC−TTC−CAC−AAG−CGGでコード化されるもの。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA2,166,155 | 1995-12-27 | ||
| CA002166155A CA2166155C (en) | 1995-12-27 | 1995-12-27 | Agents binding to hyaluronic acid binding domains and the use thereof |
| PCT/CA1996/000870 WO1997024111A2 (en) | 1995-12-27 | 1996-12-23 | Novel hyaluronic acid receptors binding agents and the use thereof |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2000506502A JP2000506502A (ja) | 2000-05-30 |
| JP2000506502A5 JP2000506502A5 (ja) | 2004-11-04 |
| JP4210330B2 true JP4210330B2 (ja) | 2009-01-14 |
Family
ID=4157242
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP52393097A Expired - Fee Related JP4210330B2 (ja) | 1995-12-27 | 1996-12-23 | ヒアルロン酸レセプター結合剤、およびその使用方法 |
Country Status (15)
| Country | Link |
|---|---|
| EP (1) | EP0874624B1 (ja) |
| JP (1) | JP4210330B2 (ja) |
| KR (1) | KR100476782B1 (ja) |
| AT (1) | ATE255411T1 (ja) |
| AU (1) | AU725478B2 (ja) |
| BR (1) | BR9612355A (ja) |
| CA (1) | CA2166155C (ja) |
| DE (1) | DE69630974T2 (ja) |
| ES (1) | ES2211996T3 (ja) |
| HU (1) | HU226598B1 (ja) |
| IL (1) | IL124828A0 (ja) |
| NO (1) | NO982935L (ja) |
| PL (1) | PL327542A1 (ja) |
| WO (1) | WO1997024111A2 (ja) |
| ZA (1) | ZA9610840B (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2237051A1 (en) * | 1997-12-19 | 1999-06-19 | Eva A. Turley | Enhanced affinity hyaluronan binding peptides |
| SE0101854L (sv) * | 2001-05-28 | 2002-11-29 | Bioneris Ab | Användning av en förening med en negativt laddad region av grupper för behandling av restenos. |
| WO2004060404A1 (ja) * | 2002-12-27 | 2004-07-22 | Chugai Seiyaku Kabushiki Kaisha | 薬物担体 |
| EP1896386B1 (en) * | 2005-06-08 | 2012-09-05 | Cangene Corporation | Hyaluronic acid binding peptides enhance host defense against pathogenic bacteria |
| AU2011261107B2 (en) | 2010-05-31 | 2016-04-14 | London Health Sciences Centre Research Inc. | RHAMM binding peptides |
| KR101383941B1 (ko) | 2012-03-09 | 2014-04-10 | 동아에스티 주식회사 | 피록시캄 또는 약제학적으로 허용되는 그의 염과 히알루론산 또는 약제학적으로 허용되는 그의 염의 안정한 액상 조성물 및 그 제조방법 |
| AU2013347797A1 (en) | 2012-11-25 | 2015-07-02 | The Regents Of The University Of California | Peptides that stimulate subcutaneous adipogenesis |
| US10844102B2 (en) | 2014-05-28 | 2020-11-24 | The Regents Of The University Of California | Peptides, compositions, and methods for stimulating subcutaneous adipogenesis |
| EP3271383A4 (en) | 2015-03-20 | 2019-06-12 | London Health Sciences Centre Research Inc. | GASED PEPTIDES AND USES THEREOF |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA1340994C (en) * | 1989-09-21 | 2000-05-16 | Rudolf Edgar Dr. Falk | Treatment of conditions and disease |
| WO1996006622A1 (en) * | 1991-07-03 | 1996-03-07 | Hyal Pharmaceutical Corporation | Hyaluronic acid and derivatives for modulation of cellular activity |
| CA2122551A1 (en) * | 1994-04-29 | 1995-10-30 | Rudolf Edgar Falk | Clearing of atherosclerosis |
| GB9207949D0 (en) * | 1992-04-09 | 1992-05-27 | Univ Manitoba | Molecular cloning of a novel hyaluronan receptor that mediates tumor cell motility |
-
1995
- 1995-12-27 CA CA002166155A patent/CA2166155C/en not_active Expired - Lifetime
-
1996
- 1996-12-23 IL IL12482896A patent/IL124828A0/xx not_active IP Right Cessation
- 1996-12-23 BR BR9612355-9A patent/BR9612355A/pt not_active Application Discontinuation
- 1996-12-23 HU HU9902059A patent/HU226598B1/hu not_active IP Right Cessation
- 1996-12-23 WO PCT/CA1996/000870 patent/WO1997024111A2/en not_active Application Discontinuation
- 1996-12-23 ZA ZA9610840A patent/ZA9610840B/xx unknown
- 1996-12-23 JP JP52393097A patent/JP4210330B2/ja not_active Expired - Fee Related
- 1996-12-23 AT AT96941564T patent/ATE255411T1/de not_active IP Right Cessation
- 1996-12-23 EP EP96941564A patent/EP0874624B1/en not_active Expired - Lifetime
- 1996-12-23 KR KR10-1998-0704359A patent/KR100476782B1/ko not_active IP Right Cessation
- 1996-12-23 ES ES96941564T patent/ES2211996T3/es not_active Expired - Lifetime
- 1996-12-23 AU AU10912/97A patent/AU725478B2/en not_active Ceased
- 1996-12-23 DE DE69630974T patent/DE69630974T2/de not_active Expired - Lifetime
- 1996-12-23 PL PL96327542A patent/PL327542A1/xx unknown
-
1998
- 1998-06-24 NO NO982935A patent/NO982935L/no unknown
Also Published As
| Publication number | Publication date |
|---|---|
| KR100476782B1 (ko) | 2005-07-18 |
| EP0874624B1 (en) | 2003-12-03 |
| NO982935D0 (no) | 1998-06-24 |
| BR9612355A (pt) | 1999-12-28 |
| HU226598B1 (hu) | 2009-04-28 |
| IL124828A0 (en) | 1999-01-26 |
| EP0874624A2 (en) | 1998-11-04 |
| WO1997024111A3 (en) | 1997-10-02 |
| HUP9902059A3 (en) | 2000-07-28 |
| AU725478B2 (en) | 2000-10-12 |
| ES2211996T3 (es) | 2004-07-16 |
| NO982935L (no) | 1998-08-27 |
| AU1091297A (en) | 1997-07-28 |
| KR19990072058A (ko) | 1999-09-27 |
| ZA9610840B (en) | 1997-06-27 |
| WO1997024111A2 (en) | 1997-07-10 |
| ATE255411T1 (de) | 2003-12-15 |
| HUP9902059A2 (hu) | 2000-04-28 |
| JP2000506502A (ja) | 2000-05-30 |
| CA2166155C (en) | 2008-02-05 |
| PL327542A1 (en) | 1998-12-21 |
| DE69630974T2 (de) | 2004-10-28 |
| CA2166155A1 (en) | 1997-06-28 |
| DE69630974D1 (de) | 2004-01-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2146139C1 (ru) | Лечение состояний и заболеваний, комбинации и композиции, предназначенные для лечения, способ повышения активности макрофагов и комбинации для его осуществления | |
| US5614506A (en) | Use of hyaluronic acid and forms to prevent arterial restenosis | |
| CA2122519C (en) | Cancer treatment and metastasis prevention | |
| US6475795B1 (en) | Use of hyaluronan in gene therapy | |
| JPH10504828A (ja) | 細胞活性調整のためのヒアルロン酸およびその誘導体 | |
| TW200831113A (en) | Pharmaceutical agent having long-lasting effect of treating arthritic disorders | |
| US5674857A (en) | Use of hyaluronic acid to repair ischemia reperfusion damage | |
| JP4210330B2 (ja) | ヒアルロン酸レセプター結合剤、およびその使用方法 | |
| AU694113B2 (en) | Compositions, for inhibition, control and regression of angiogenesis, containing hyaluronic acid and NSAID | |
| US5834444A (en) | Hyaluronic acid and salts thereof inhibit arterial restenosis | |
| JP2003089647A (ja) | 関節性疾患治療剤 | |
| CA2175282A1 (en) | Use of forms of hyaluronic acid (ha) for the treatment of cancer | |
| WO1999002151A1 (en) | Paclitaxel compositions containing hyaluronic acid of a molecular weight of less than 750.000 da | |
| JPH10506884A (ja) | マクロファージ浸潤に関連する病気あるいは容体、特に脳卒中、心筋梗塞の治療 | |
| HU227067B1 (en) | Use of hyaluronic acid for preparing pharmaceutical compositions to prevent arterial restenosis | |
| JP3811500B2 (ja) | 動脈硬化の除去のためのヒアルロン酸を含む薬剤組成物 | |
| JP2000513707A (ja) | 投与薬剤の目標化、治療薬および他のグリコサミノグリカン(gags) | |
| CA2166154A1 (en) | Binding agents and the use thereof | |
| CZ288292B6 (en) | Compound therapeutic preparations intended for treatment of diseases or states of tissues comprising insufficiently perfused tissues and pathological tissues of human being |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20031205 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20031205 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080219 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080501 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080616 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080814 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080930 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081027 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111031 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121031 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131031 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |