JP3746381B2 - 化学発光酵素免疫測定方法 - Google Patents
化学発光酵素免疫測定方法 Download PDFInfo
- Publication number
- JP3746381B2 JP3746381B2 JP24440498A JP24440498A JP3746381B2 JP 3746381 B2 JP3746381 B2 JP 3746381B2 JP 24440498 A JP24440498 A JP 24440498A JP 24440498 A JP24440498 A JP 24440498A JP 3746381 B2 JP3746381 B2 JP 3746381B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- chemiluminescent
- immunoassay method
- enzyme immunoassay
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Landscapes
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
【発明の属する技術分野】
本発明は、化学発光反応を利用する酵素免疫測定方法に関するものであり、更に詳しくは、ペルオキシダーゼ酵素を標識物質として用い、特定の新規化学発光試薬を用いる抗原又は抗体の免疫学的測定方法に関するものである。
【0002】
【従来の技術】
酵素免疫測定方法は、標識物質に放射性同位元素を使用しないので良好な測定環境を保持することが可能であり、人体に対して危険性の少ない免疫測定方法として開発され、種々の物質の測定系に利用されている。この酵素免疫測定方法において使用される酵素としては、ぺルオキシダーゼ、アルカリホスファターゼ、β−ガラクトシダーゼ及びグルコースオキシダーゼ等を挙げることができる。これらの酵素を用いた酵素標識抗体又は抗原の酵素活性を検出する方法としては、過酸化水素/o−フェニレンジアミン、4−ニトロフェニル−ホスフェ−ト、2−ニトロフェニル−β−ガラクトシド等の酵素基質の酵素による分解反応に伴い生成する発色性物質の発色量を測定して酵素活性を定量し、この酵素活性と相関性を有する抗体又は抗原の量を定量する比色法が一般的である。
【0003】
しかしながら、臨床化学分析においては、その測定対象が生体試料(主として血清、尿等)であり、その測定値は病態の診断又は経過観察等に用いられることが多く、そのために、より高感度及び高精度な測定が求められているが、比色法によりこの要求を完全に満足させることは難しい。
【0004】
そこで、この要求を満たすことを目的として蛍光法が提案されている。蛍光法とは、標識に用いた酵素の触媒活性により、4−ヒドロキシフェニル酢酸、4−メチルウムベリフェリル−β−ガラクトシド、4−メチルウムベリフェリル−ホスフェート等の蛍光基質を分解して蛍光を発生させた後、この蛍光強度を測定して酵素活性を定量し、この酵素活性と相関性を有する抗体又は抗原の量を定量する方法である。しかし、蛍光法では、励起光の散乱が存在するため前記の要求を満たすには充分とは云い難い。また、比色法及び蛍光法では、キセノンランプ等の光源が必要であり、光源からの光に由来する迷走現象や溶媒に由来するラマン光が原因となり、バックグラウンドのレベルを上昇させてしまうので、比色法及び蛍光法による測定の高感度化は原理的に困難である。
【0005】
近年、比色法及び蛍光法を上回る高感度な酵素免疫測定方法として、化学発光酵素免疫測定方法(CLEIA)が開発され注目されている。CLEIAは、酵素の触媒活性によって化学発光性物質が中間体を経て励起状態となり、この状態から基底状態に戻る際に放出される発光量を測定して酵素活性を定量し、この酵素活性と相関性を有する抗体又は抗原の量を定量する方法であり、化学反応により化学発光性物質を発光させるため光源が不要であり、光源に起因するバックグラウンドの上昇等がないため測定の高感度化が可能である。CLEIAに用いられる酵素としては、ぺルオキシダーゼ、アルカリホスファターゼ、β−ガラクトシダーゼ、グルコースオキシダーゼ、デヒドロゲナーゼ等が挙げられる。これらのなかで、取り扱い易さ、入手し易さ等の点でぺルオキシダーゼが好適に用いられる。酵素にペルオキシダーゼ、化学発光性物質にルミノール、発光増強剤にp−ヨードフェノールを各々用いる化学発光系が開発され、種々の物質が化学発光反応により免疫学的に高感度に定量することが可能になっている。
【0006】
しかしながら、ペルオキシダーゼ酵素を標識物質とするCLEIAにおいては、測定対象物質の低濃度領域での定量性を更に高める必要性が生じるケースが多く、ペルオキシダーゼ酵素を標識物質とするCLEIAの更なる高感度化が望まれていた。
【0007】
【発明が解決しようとする課題】
従って、本発明は、前記事情に鑑み、測定対象物質をより高感度で測定可能な化学発光反応による新規な免疫測定系を利用した酵素免疫測定方法を提供することを課題とする。
【0008】
【課題を解決するための手段】
そこで、本発明者らは、前記課題を解決するために鋭意検討を行なった結果、化学発光性物質として、N,N’−ジ置換−9,9’−ビスアクリジニウム塩類をN,N−ジ置換カルボン酸アミド化合物の存在下において光照射により反応させる際に、その反応時及び/又は反応後にアミノアルコール化合物を添加することにより得られる化学発光試薬を用い、さらに、発光増強剤として特定のフェノール系化合物を用いる化学発光系が、化学発光性物質にルミノールを用いる系より高感度に測定対象物質を免疫学的に定量することが可能なことを見い出し、これらの知見に基づいて本発明に到達した。
【0009】
すなわち、本発明は、ペルオキシダーゼ酵素標識した抗体若しくは抗原を試料中の測定すべき抗原若しくは抗体又はそれらの凝集物と混合し、抗原抗体反応によりペルオキシダーゼ酵素標識−抗原抗体錯体からなる免疫複合体を形成させ、必要により、該免疫複合体を不溶性担体に固定化した抗体若しくは抗原と反応させて該不溶性担体上に捕捉した後、これに、N,N’−ジ置換−9,9’−ビスアクリジニウム塩類をN,N−ジ置換カルボン酸アミド化合物の存在下において光照射により反応させる際に、その反応時及び/又は反応後にアミノアルコール化合物を添加することにより得られる化学発光試薬を添加し、水素受容体の存在下において化学発光させ、その発光強度を測定することにより試料中の抗原又は抗体の量を定量することを特徴とする化学発光酵素免疫測定方法に関するものである。
【0010】
【発明の実施の形態】
以下、本発明につき更に詳しく説明する。
本発明の化学発光酵素免疫測定方法は、抗原抗体反応により測定すべき抗原若しくは抗体をペルオキシダーゼ酵素標識した免疫複合体として捕捉する免疫反応段階と、生成した該免疫複合体をその分子中に存在する標識酵素を用いる化学発光反応により測定する化学発光反応段階とからなる。
【0011】
免疫反応段階を構成する抗原抗体反応の方法は任意であり、前記化学発光試薬を用いることができるものであれば、いずれの方法も採用することができる。
例えば、
▲1▼不溶性担体に結合した抗体に試料中の測定すべき抗原を捕捉させた後にペルオキシダーゼ酵素標識抗体を反応させるサンドイッチ法、
▲2▼サンドイッチ法において、不溶性担体に結合した抗体と異なる動物種に由来する抗体を用い、生成したサンドイッチ錯体に対して、さらにこの抗体に対する標識第二抗体を反応させる二抗体法、
▲3▼不溶性担体に結合した抗体に試料中の測定すべき抗原をペルオキシダーゼ酵素標識抗原の存在下で反応させる競合法、
▲4▼測定すべき抗原又は抗体を含有する試料にこれらと特異的に反応する標識した抗体又は抗原を作用させて凝集沈殿させた後、遠心分離して分離した免疫複合体中の標識物質を検出する凝集沈殿法、
▲5▼不溶性担体に結合した抗原に試料中の測定すべき抗体をペルオキシダーゼ酵素標識抗ヒトガンマグロブリン抗体を作用させる抗体検出法、さらに、
▲6▼ビオチン標識抗体及びペルオキシダーゼ酵素標識アビジンを反応させるビチオン−アビジン法等
を非限定的に用いることができる。
【0012】
本発明の化学発光酵素免疫測定方法に用いられる不溶性担体としては、例えば、ポリスチレン、ポリエチレン、ポリプロピレン、ポリエステル、ポリアクリロニトリル、フッ素樹脂、架橋デキストラン、ポリサッカライド等の高分子化合物、その他、ガラス、金属、磁性粒子及びこれらの組み合わせ等が挙げられる。また、不溶性担体の形状としては、例えば、トレイ状、球状、繊維状、棒状、盤状、容器状、セル、マイクロプレート、試験管等の種々の形状で用いることができる。さらに、これら不溶性担体への抗原又は抗体の固定化方法は任意であるが、物理的吸着法、共有結合法、イオン結合法等を用いることができる。
【0013】
また、本発明の化学発光酵素免疫測定方法において用いられる抗体類は、モノクローナル抗体及びポリクローナル抗体のいずれを使うことも可能であり、その形態としては全抗体又はF(ab’)2 、Fab等の断片を用いることができる。また、抗体の起源は任意であるが、マウス、ラット、兎、羊、山羊、鶏等に由来する抗体が好適に用いられる。
【0014】
本発明の化学発光酵素免疫測定方法の後段を構成する化学発光反応段階は、N,N’−ジ置換−9,9’−ビスアクリジニウム塩類をN,N−ジ置換カルボン酸アミド化合物の存在下において光照射により反応させる際にその反応時及び/又は反応後にアミノアルコールを添加して得られる化学発光試薬を用い、更に所望により発光増強剤の存在下に水素受容体を作用させて不溶性担体上に捕捉された標識物質であるペルオキシダーゼ酵素の活性を測定するものであり、その測定方順は任意であるが、一般に、化学発光性物質及び発光増強剤を含有する測定試薬をペルオキシダーゼ酵素標識抗体又は抗原を免疫学的に捕捉した不溶性担体に添加し、特定塩基性pH領域において過酸化水素水溶液を添加して化学発光反応させ、その化学発光量を発光測定装置で測定する方法等が行なわれている。
【0015】
次に、本発明の化学発光酵素免疫測定方法に用いられる化学発光試薬について説明する。
前記化学発光試薬は、N,N’−ジ置換−9,9’−ビスアクリジニウム塩類をN,N−ジ置換カルボン酸アミド化合物の存在下において光照射により反応させる際に、その反応時及び/又は反応後に特定のアミノアルコール化合物を添加することにより得られる化学発光性物質を含有する反応混合物である。
前記N,N’−ジ置換−9,9’−ビスアクリジニウム塩類は、下記一般式(1)
【0016】
【化4】
で表わすことができる。
【0017】
前記一般式(1)において、R1 及びR2 は、アルキル基、アリール基及びハロゲン化アリール基からなる群より選択され、互いに同一でも又は異なるものでもよい。また、アルキル基としては炭素数1〜14の直鎖状又は分岐状のものを挙げることができ、特に、炭素数1〜10のものが好ましく、具体的には、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、ペンチル基、イソペンチル基、ヘキシル基、イソヘキシル基等を例示することができる。アリール基は炭素数6〜20のものであり、アリール基には炭素数1〜14のアルキル基が結合したものでもよい。具体的にはフェニル基、トリール基、キシリル基等を例示することができる。R3 、R4 、R5 及びR6 は、水素原子、アルキル基、アリール基、アルコキシ基、アリーロキシ基及びハロゲン原子からなる群より選択され、互いに同一でも又は異なるものでもよい。アルキル基は炭素数1〜14の直鎖状又は分岐状のものであり、特に、炭素数1〜10のものが好ましく、具体的には、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、ペンチル基、イソペンチル基等を例示することができる。アリール基は炭素数6〜20であり、アリール基には炭素数1〜14のアルキル基が結合したものでもよい。具体的には、フェニル基、トリール基、キシリル基等を例示することができる。アルコキシ基は炭素数1〜14の直鎖状又は分岐状アルキル基を有し、また、アリーロキシ基は、炭素数6〜20のアリール基を有する。
【0018】
前記式(1)において、Xはn価の陰イオンであり、nは1又は2である。陰イオン(対イオン)としては、具体的には硝酸イオン、ハロゲンイオン、リン酸イオン、硫酸イオン、スルホン酸イオン等が挙げられる。
【0019】
前記N,N’−ジ置換−9,9’−ビスアクリジニウム塩類の具体例としては、N,N’−ジメチル−9,9’−ビスアクリジニウム塩、N,N’−ジエチル−9,9’−ビスアクリジニウム塩、N,N’−ジプロピル−9,9’−ビスアクリジニウム塩、N,N’−ジイソプロピル−9,9’−ビスアクリジニウム塩、N,N’−ジフェニル−9,9’−ビスアクリジニウム塩、N,N’−ジ−m−クロロフェニル−9,9’−ビスアクリジニウム塩などが挙げられ、特に、N,N’−ジメチル−9,9’−ビスアクリジニウムジナイトレート(ルシゲニン)が好適である。
前記N,N−ジ置換カルボン酸アミド化合物は、下記一般式(2)
【0020】
【化5】
で表わすことができる。
【0021】
前記一般式(2)において、R1 は、炭素数1〜10のアルキル基、炭素数2〜10のアルケニル基及び炭素数6〜20のアリール基からなる群より選択され、アリール基はアルキル基、ハロゲン、ニトロ基、水酸基及びアミノ基等で置換されていてもよく、R2 は、メチル基及びエチル基からなる群より選択され、R3 は、炭素数1〜10のアルキル基、炭素数2〜10のアルケニル基及び炭素数6〜20のアリール基からなる群より選択され、アリール基はアルキル基、ハロゲン原子、ニトロ基、水酸基及びアミノ基等で置換されていてもよい。R1 及びR3 のアルキル基としては、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基等の直鎖状又は分岐状のものを挙げることができる。また、R1 及びR3 は互いに結合して、それぞれが結合しているカルボニル基の炭素原子及びアミド基の窒素原子と共に環を形成していてもよい。
【0022】
前記N,N−ジ置換カルボン酸アミド化合物の具体例としては、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N,N−ジメチルアクリルアミド、N,N−ジメチルプロピオンアミド、N,N−ジメチルベンズアミド、N−メチル−2−ピロリドン等が非限定的に挙げられる。
また、化学発光試薬の製造に用いられる原料の一つであるアミノアルコール化合物は、下記一般式(3)
【0023】
【化6】
で表わすことができる。
前記一般式(3)において、Rは炭素数1〜5の二価の脂肪族炭化水素基であり、mは1〜3の整数である。
その具体的な例としては、モノエタノールアミン、ジエタノールアミン、トリエタノールアミン、モノイソプロパノールアミン、ジイソプロパノールアミン、トリイソプロパノールアミン等を非限定的に挙げることができる。
【0024】
前記アミノアルコール化合物の添加は、発光反応時において、ブランク値を低下させる効果及びペルオキシダーゼの高濃度領域における発光強度を上昇させる効果を有し、また、化学発光試薬の保存時において、その発光性能の低下を防ぐ保存安定性を改善する効果等を有し、化学発光試薬の感度や安定性等の性能の向上に寄与する処が大きい。
【0025】
前記化学発光試薬の製造に用いられる光照射用の光線としては、波長領域が約290〜800nmの範囲の紫外可視部が用いられ、特に、約400〜800nmの範囲の可視光が望ましい。これらの光源としては、高圧水銀灯、低圧水銀灯、殺菌灯、蛍光灯及び白熱電灯等を非限定的に用いることができ、特に、白熱電灯が好ましく用いられる。この光照射により得られる化学発光試薬は、光源を用いずに自然光の下で製造した化学発光試薬に較べて、同じ原料ルシゲニン濃度で製造し同量で使用した場合に短時間で非常に高い発光強度を示すことと、この反応を光遮断下に実施した場合にはペルオキシダーゼ濃度依存性を有する化学発光試薬が得られないことから、化学発光性化合物の生成には光照射が重要な役割を担っていることが認められる。
【0026】
前記N,N’−ジ置換−9,9’−ビスアクリジニウム塩類は、pH8付近では過酸化水素ともペルオキシダーゼ存在下の過酸化水素とも顕著な発光反応は起こさないが、これはN,N’−ジ置換−9,9’−ビスアクリジニウムカチオンが対イオン、特に硝酸イオンと安定な塩を形成しているためと考えられる。しかし、N,N−ジ置換カルボン酸アミド化合物等の極性の高い化合物の存在下で光照射を行なうことにより、N,N’−ジ置換−9,9’−ビスアクリジニウムカチオンへの対アニオンからの電荷移動が促進され、イオン性の高い塩類からラジカル性を有する電荷移動錯体に変化し、この錯体がN,N−ジ置換カルボン酸アミド化合物の配位若しくは溶媒和によって安定化され、この安定化されたビラジカル性化合物が過酸化水素の酵素分解により生成する活性酸素と反応して、励起状態のジオキセタン構造を経て発光するのでペルオキシダーゼ濃度に依存した発光強度が得られるものと考えられる。この光照射による反応において、アミノアルコール化合物の添加は、N,N’−ジ置換−9,9’−ビスアクリジニウムカチオンへの電荷移動に関与してその反応を促進し、発光反応時のブランク値を高める副生成物の生成を抑え、且つ生成するビラジカルを更に安定化する作用を有するものと考えられる。
【0027】
前記N,N’−ジ置換−9,9’−ビスアクリジニウム塩類、N,N−ジ置換カルボン酸アミド化合物及びアミノアルコール化合物の混合モル比は、N,N’−ジ置換−9,9’−ビスアクリジニウム塩類に対してN,N−ジ置換カルボン酸アミド化合物を1〜1万倍モル、アミノアルコール化合物を1〜1万倍モルの量でそれぞれ用いることができ、さらに、同種及び/又は異種のN,N−ジ置換カルボン酸アミド化合物及び/又はその他の溶媒を反応溶媒として用いることもできる。
【0028】
光照射反応の反応温度は用いられる溶媒の有無及び種類によって異なるが、一般的に−10〜+150℃、好ましくは0〜120℃、特に好ましくは20〜90℃の範囲の温度である。反応時間は1分〜一昼夜、好ましくは10分〜15時間、特に好ましくは30分〜10時間の範囲の時間で行なうことができる。
【0029】
前記化学発光試薬は、pH7.5〜13の塩基性条件下において、過剰の過酸化水素の存在下、ペルオキシダーゼの濃度に依存した量で発光する。この発光は、フェノール性化合物等の発光促進剤によって増強することが認められる。このようなフェノール性化合物としては、p−ヒドロキシ桂皮酸、p−フェニルフェノール、p−(4−クロロフェニル)フェノール、p−(4−ブロモフェニル)フェノール、p−(4−ヨードフェニル)フェノール、p−ヨードフェノール、p−ブロモフェノール、p−クロロフェノール、2,4−ジクロロフェノール、p−クマル酸、6−ヒドロキシベンゾチアゾール、2−ナフトール、ホタルルシフェリン等が非限定的に挙げられる。
【0030】
前記化学発光試薬の濃度は、10-8〜1M、好ましくは10-6〜10-2M、さらに好ましくは10-4〜10-2Mの範囲の濃度で用いられ、その使用量は10〜500μl、好ましくは50〜300μlの範囲で用いるのが望ましい。また、発光促進剤は、化学発光試薬の量の0.01〜100倍モル、好ましくは0.1〜10倍モルの範囲で用い、その濃度は10-6〜1M、好ましくは10-4〜10-2Mの範囲で用いるのが望ましい。
【0031】
化学発光反応に用いられる水素受容体としては、ペルオキシダーゼ酵素の基質となり得るものであれば特に限定されるものではないが、有機過酸化物、無機過酸化物等が任意に用いられ、特に、過酸化水素が好ましい。この水素受容体の使用量は化学発光試薬に対して充分に過剰な量で用いることが必要であり、その使用量は化学発光試薬に対して3〜1万倍モル、好ましくは10〜1000倍モルの範囲で用いるのが望ましい。
【0032】
また、ペルオキシダーゼを標識物質として抗体、核酸等を標識して種々の物質を定量する場合には、特に限定されるものではないが、ペルオキシダーゼとして、西洋ワサビペルオキシダーゼ(HRP)が好ましく用いられる。
【0033】
化学発光反応に用いる塩基性緩衝液としては、トリス緩衝液、リン酸緩衝液、ほう酸緩衝液、炭酸緩衝液、グリシン−水酸化ナトリウム緩衝液等を任意に用いることができる。これらの緩衝液の濃度は1mM〜1Mの範囲で用いるのが望ましい。また、反応時に界面活性剤、キレート剤等の添加剤を任意に用いることができる。
【0034】
本発明の化学発光酵素免疫測定方法における化学発光反応の発光量の測定は発光光度計を用いて測定することができる。その際に、発光量測定の開始点及び積算時間は任意であるが、発光量が安定し且つ発光量の濃度依存性の高い時間を選択するのが望ましい。例えば、測定開始点は試薬混合後0〜1時間、好ましくは0〜30分、特に好ましくは0〜15分であり、測定の積算時間は1秒〜1分、好ましくは1〜30秒、特に好ましくは1〜10秒である。
【0035】
【実施例】
以下、参考例と共に実施例及び比較例を示し、本発明を具体的に説明する。もっとも本発明は実施例等により限定されるものではない。
尚、参考例及び実施例中の%は重量%を意味する。
【0036】
[参考例1]
化学発光試薬の調製
ルシゲニンを1.5mg試験管に採り、これにN,N−ジメチルアセトアミドを1ml加えて溶解させた後、30℃の温度の水浴中で250Wのコピーランプを7時間照射してから、トリエタノールアミン0.5mlを添加し混合することにより化学発光試薬を得た。次に、この化学発光試薬を8×10-4Mのp−ヨードフェノール75mMトリス塩酸緩衝液(pH8.0) 溶液で500倍に希釈することにより化学発光試薬溶液を調製した。
【0037】
[参考例2]
不溶性担体固定化ポリクローナル抗体の製造
抗原に特異的反応性を有する兎等の動物由来のポリクローナル抗体を10mMリン酸緩衝生理食塩水(pH7.4) (PBS)に10mg/mlの濃度で溶解した溶液を、白色マイクロプレート(ラボシステム社)の各ウェルに0.1mlずつ加え、37℃の温度で1時間放置した後、PBSで洗浄してから、1%ウシ血清アルブミン(BSA)水溶液を0.3mlずつ加えて37℃の温度で1時間放置してポストコーティング処理を実施してポリクローナル抗体固定化白色マイクロプレートを得た。
【0038】
[参考例3]
ペルオキシダーゼ酵素標識モノクローナル抗体の製造
抗原に特異的反応性を有するマウス由来等のモノクローナル抗体を10mMリン酸緩衝生理食塩水(PBS)(pH7.4) に1.0mg/mlの濃度で溶解した溶液1mlに、N−(m−マレイミド安息香酸)−N−サクシンイミドエステル(MBS)の10mg/mlの濃度のジメチルホルムアミド溶液0.1mlを添加し、25℃の温度で30分間反応させた。次いで、この反応混合液をセファデックスG−25を充填したカラムを用い、0.1Mリン酸緩衝液(pH6.0) でゲル濾過を行ない、マレイミド化モノクローナル抗体と未反応MBSとを分離した。
一方、ペルオキシダーゼ酵素としてホースラディッシュ・ペルオキシダーゼ(HRP)の1.0mg/mlのPBS溶液に、N−サクシンイミジル−3−(2−ピリジルチオ)プロピオネート(SPDP)の10mg/mlの濃度のエタノール溶液を添加し、25℃の温度で30分間反応させた。
次いで、この反応混合液をセファデックスG−25を充填したカラムを用い、10mM酢酸緩衝液(pH4.5) でゲル濾過して精製、ピリジルジスルフィド化HRPを含有する画分を採取し、これをコロジオンバック中において氷冷下に約10倍に濃縮した。次に、これに0.1Mジチオスレイトールを含有する0.1M酢酸緩衝生理食塩水(pH4.5) 1mlを添加して、25℃の温度で30分間撹拌してHRP分子中に導入したピリジルジスルフィド基を還元した後、この反応混合液をセファデックスG−25を充填したカラムを用いてゲル濾過し、チオール化HRPを含有する画分を得た。
次に、マレイミド化モノクローナル抗体とチオール化HRPとを混合し、コロジオンバックを用いて氷冷下に4mg/mlの蛋白質濃度まで濃縮し、4℃で一昼夜放置した後、ウルトロゲルAcA44(SEPRACOR社)を充填したカラムを用いてゲル濾過し、ペルオキシダーゼ酵素標識モノクローナル抗体を得た。
【0039】
[実施例1]
同時サンドイッチ法CLEIAによるα−フェトプロテイン(AFP)の測定兎抗ヒトAFPポリクローナル抗体を固定化した白色マイクロプレートに、精製したヒトAFP(標準物質)を0〜800ng/mlの範囲で含有する2%BSA含有PBS溶液(pH7.4) 50μlとペルオキシダーゼ酵素標識マウス抗ヒトAFPモノクローナル抗体を約3μg/mlの濃度で含有する2%BSA含有PBS溶液(pH7.4) 100μlとを加え、37℃の温度で1時間インキュベートした。次に、ウェル内の溶液を吸引除去した後、ウェル内を生理食塩水で洗浄してから、各ウェルに75mMトリス塩酸緩衝液(pH8.0) 100μlを加え、これに参考例1で調製した化学発光試薬溶液100μl及び0.0017%過酸化水素を含む75mMトリス塩酸緩衝液(pH8.0) 50μlを順次注入して発光させた後、この発光量をルミノメーター(ダイアヤトロン社製ルミナスCT−9000D)で0〜5秒間積算して測定し、この値を標準物質濃度に対してプロットすることにより、図1に示される濃度依存性の良い検量線を得た。この検量線を用いて血清検体中のヒトAFPを0.01ng/mlの濃度まで測定することが可能であった。
【0040】
[実施例2]
同時サンドイッチ法CLEIAによるプロラクチン(PRL)の測定
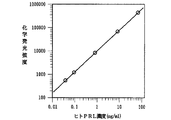
兎抗ヒトPRLポリクローナル抗体を固定化した白色マイクロプレートに、精製したヒトPRL(標準物質)を0〜200ng/mlの範囲で含有する2%BSA含有PBS溶液(pH7.4) 50μlとペルオキシダーゼ酵素標識マウス抗ヒトPRLモノクローナル抗体を約2μg/mlの濃度で含有する2%BSA含有PBS溶液(pH7.4) 100μlとを加え、37℃の温度で1時間インキュベートした。次いで、ウェル内の溶液を吸引除去し、ウェル内を生理食塩水で洗浄してから、各ウェルに75mMトリス塩酸緩衝液(pH8.0) 100μlを加え、これに参考例1で調製した化学発光試薬溶液100μl及び0.0017%過酸化水素を含む75mMトリス塩酸緩衝液(pH8.0) 50μlを順次注入して発光させた後、この発光量をルミノメーター(ダイアヤトロン社製ルミナスCT−9000D)で0〜5秒間積算して測定し、この値を標準物質濃度に対してプロットすることにより、図2に示される濃度依存性の良い検量線を得た。この検量線を用いて血清検体中のヒトプロラクチンを0.01ng/mlの濃度まで測定することが可能であった。
【0041】
[実施例3]
同時サンドイッチ法CLEIAによるヒト絨毛性ゴナドトロピンβ鎖(βhCG)の測定
兎抗ヒトhCGポリクローナル抗体を固定化した白色マイクロプレートに、精製したβhCG(標準物質)を0〜200mIU/mlの範囲で含有する2%BSA含有PBS溶液(pH7.4) 50μlとペルオキシダーゼ酵素標識マウス抗βhCGモノクローナル抗体を約2μg/mlの濃度で含有する2%BSA含有PBS溶液(pH7.4) 100μlとを加え、37℃の温度で1時間インキュベートした。次に、ウェル内の溶液を吸引除去した後、ウェル内を生理食塩水で洗浄してから、各ウェルに75mMトリス塩酸緩衝液(pH8.0) 100μlを加え、これに参考例1で調製した化学発光試薬溶液100μl及び0.0017%過酸化水素を含む75mMトリス塩酸緩衝液(pH8.0) 50μlを順次注入して発光させた後、この発光量をルミノメーター(ダイアヤトロン社製ルミナスCT−9000D)で0〜5秒間積算して測定し、この値を標準物質濃度に対してプロットすることにより、図3に示される濃度依存性の良い検量線を得た。この検量線を用いて血清検体中のβhCGを0.01mIU/mlの濃度まで測定することが可能であった。
【0042】
[比較例1]
ルミノールを用いる同時サンドイッチ法CLEIAによるα−フェトプロティ ン(AFP)の測定
兎抗ヒトAFPポリクローナル抗体を固定化した白色マイクロプレートに、精製したヒトAFP(標準物質)を0〜800ng/mの範囲で含有する2%BSA含有PBS溶液(pH7.4) 50μlとペルオキシダーゼ酵素標識マウス抗ヒトAFPモノクローナル抗体を約3μg/mlの濃度で含有する2%BSA含有PBS溶液(pH7.4) 100μlとを加え、37℃の温度で1時間インキュベートした。次に、ウェル内の溶液を吸引除去した後、ウェル内を生理食塩水で洗浄してから、各ウェルにp−ヨードフェノールを10-3Mの濃度で含有する0.1Mトリス塩酸緩衝液(pH8.4) 100μlを加え、これにルミノールを5.6×10-5Mの濃度で含有する0.1Mトリス塩酸緩衝液(pH8.4) 100μl、及び0.0034%過酸化水素の0.1Mトリス塩酸緩衝液(pH8.4) 50μlを注入して発光させ、この発光量をルミノメーター(ダイアヤトロン社製ルミナスCT−9000D)で0〜5秒間積算して測定し、この値を標準物質濃度に対してプロットすることにより、図4に示される濃度依存性を有する検量線を得た。この検量線を用いて血清検体中のヒトAFPを2.0ng/mlの濃度まで測定することが可能であった。
【0043】
【発明の効果】
本発明の化学発光酵素免疫測定方法によれば、入手が容易であり取り扱いも比較的に容易なペルオキシダーゼ酵素を標識物質として用い、安価で入手が容易であるルシゲニン等を出発原料とし、且つ容易に製造できる新規化学発光試薬を用いる化学発光反応により測定対象物質である種々の抗原又は抗体類を免疫学的に高感度に測定することができる。
【図面の簡単な説明】
【図1】 実施例1記載の反応系を用いて化学発光させた化学発光量をヒトαAFP(標準物質)の濃度の関数としてプロットして作成したヒトαAFP測定用の検量線である。
【図2】 実施例2記載の反応系を用いて化学発光させた化学発光量をヒトプロラクチン(標準物質)の濃度の関数としてプロットして作成したヒトプロラクチン測定用の検量線である。
【図3】 実施例3記載の反応系を用いて化学発光させた化学発光量をβhCG(標準物質)の濃度の関数としてプロットして作成したβhCG測定用の検量線である。
【図4】 比較例1記載の反応系を用いて化学発光させた化学発光量をヒトαAFP(標準物質)の濃度の関数としてプロットして作成したヒトαAFP測定用の検量線である。
Claims (10)
- ペルオキシダーゼ酵素標識した抗体若しくは抗原を試料中の測定すべき抗原若しくは抗体又はこれらの凝集物と混合し、抗原抗体反応によりペルオキシダーゼ酵素標識−抗原抗体錯体からなる免疫複合体を形成させた後、これに
N,N’−ジ置換−9,9’−ビスアクリジニウム塩類をN,N−ジ置換
カルボン酸アミド化合物の存在下において光照射により反応させる際に、
その反応時及び/又は反応後アミノアルコール化合物を添加することによ
り得られる化学発光試薬
を添加し、水素受容体の存在下において化学発光させ、その発光強度を測定することにより試料中の抗原又は抗体の量を測定することを特徴とする化学発光酵素免疫測定方法。 - 前記N,N−ジ置換カルボン酸アミド化合物が、下記一般式(2)
で表わされる化合物である請求項1又は2に記載の化学発光酵素免疫測定方法。 - 前記N,N’−ジ置換−9,9’−ビスアクリジニウム塩類が、N,N’−ジメチル−9,9’−ビスアクリジニウムジナイトレート(ルシゲニン)である請求項1ないし3のいずれかの1項に記載の化学発光酵素免疫測定方法。
- 前記N,N−ジ置換カルボン酸アミド化合物が、N,N−ジメチルホルムアミド又はN,N−ジメチルアセトアミドである請求項1ないし4のいずれかの1項に記載の化学発光酵素免疫測定方法。
- 前記アミノアルコール化合物が、モノエタノールアミン、ジエタノールアミン及びトリエタノールアミンからなる群より選択される少なくとも一種の化合物である請求項1ないし6のいずれかの1項に記載の化学発光酵素免疫測定方法。
- 前記水素受容体が、過酸化水素又は過酸化水素源である請求項1ないし7のいずれかの1項に記載の化学発光酵素免疫測定方法。
- 前記化学発光反応を行なう際に、さらに、発光増強剤を含有させてなる請求項1ないし8のいずれかの1項に記載の化学発光酵素免疫測定方法。
- 前記発光増強剤が、フェノール性化合物である請求項9に記載の化学発光酵素免疫測定方法。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP24440498A JP3746381B2 (ja) | 1998-08-14 | 1998-08-14 | 化学発光酵素免疫測定方法 |
| US09/529,546 US6395503B1 (en) | 1998-08-14 | 1999-08-13 | Chemiluminescent reagents and chemiluminescence analysis methods with the use of the same |
| CA002306752A CA2306752C (en) | 1998-08-14 | 1999-08-13 | Chemiluminescent reagent and chemiluminescent analysis using the same |
| PCT/JP1999/004401 WO2000009626A1 (en) | 1998-08-14 | 1999-08-13 | Chemiluminescent reagents and chemiluminescence analysis methods with the use of the same |
| EP99937071A EP1038939B1 (en) | 1998-08-14 | 1999-08-13 | Chemiluminescent reagents and chemiluminescence analysis methods with the use of the same |
| DE69933850T DE69933850T2 (de) | 1998-08-14 | 1999-08-13 | Chemilumineszenzmittel und chemilumineszenzanalyseverfahren mit deren verwendung |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP24440498A JP3746381B2 (ja) | 1998-08-14 | 1998-08-14 | 化学発光酵素免疫測定方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2000065831A JP2000065831A (ja) | 2000-03-03 |
| JP3746381B2 true JP3746381B2 (ja) | 2006-02-15 |
Family
ID=17118173
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP24440498A Expired - Fee Related JP3746381B2 (ja) | 1998-08-14 | 1998-08-14 | 化学発光酵素免疫測定方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3746381B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2025070747A1 (ja) * | 2023-09-29 | 2025-04-03 | 富士フイルム株式会社 | 被検試料に含まれる抗原の測定方法、およびヒト絨毛性ゴナドトロピン又はエストラジオールの測定キット |
-
1998
- 1998-08-14 JP JP24440498A patent/JP3746381B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2000065831A (ja) | 2000-03-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US5424194A (en) | 4-(cyanomethylthio)phenol enhanced peroxidase assays | |
| BRPI1008760B1 (pt) | método de ensaio e kit para um analito em uma amostra e sistema para realizar o método de ensaio | |
| US6395503B1 (en) | Chemiluminescent reagents and chemiluminescence analysis methods with the use of the same | |
| EP0321487B1 (en) | Enhanced luminescent assay | |
| US4835101A (en) | Luminescent analyses with enhanced storage stability | |
| JP3819612B2 (ja) | β−hCGの免疫学的測定方法 | |
| JP3746381B2 (ja) | 化学発光酵素免疫測定方法 | |
| JP4177498B2 (ja) | 酵素免疫測定法 | |
| JP3792899B2 (ja) | 化学発光酵素免疫測定方法 | |
| JP3815905B2 (ja) | 酵素免疫測定法 | |
| JP4028645B2 (ja) | 化学発光酵素免疫測定方法 | |
| EP0480361A2 (en) | Quantitation by chemiluminescence using photosenstive substance | |
| JP3815897B2 (ja) | プロラクチンの免疫学的測定方法 | |
| JP4286357B2 (ja) | 化学発光酵素免疫測定方法 | |
| JP3792886B2 (ja) | 化学発光酵素免疫測定方法 | |
| JP3865515B2 (ja) | α−フェトプロテインの免疫学的測定方法 | |
| JP3745112B2 (ja) | 化学発光酵素免疫測定方法 | |
| JP3776229B2 (ja) | 化学発光試薬及びその製造方法 | |
| JP2660932B2 (ja) | パーオキシダーゼ活性の化学発光測定法 | |
| JP3749636B2 (ja) | メダラシンの免疫学的測定方法 | |
| JPH051995A (ja) | 金属ポルフインを用いる新規測定法 | |
| CN108414736A (zh) | 一种利用化学发光增强子修饰的抗体检测目标物的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20050809 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050929 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20051025 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20051122 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20091202 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101202 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111202 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111202 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121202 Year of fee payment: 7 |
|
| LAPS | Cancellation because of no payment of annual fees |