JP3607043B2 - リチウム含有複合窒化物の製造方法 - Google Patents
リチウム含有複合窒化物の製造方法 Download PDFInfo
- Publication number
- JP3607043B2 JP3607043B2 JP15398497A JP15398497A JP3607043B2 JP 3607043 B2 JP3607043 B2 JP 3607043B2 JP 15398497 A JP15398497 A JP 15398497A JP 15398497 A JP15398497 A JP 15398497A JP 3607043 B2 JP3607043 B2 JP 3607043B2
- Authority
- JP
- Japan
- Prior art keywords
- lithium
- cobalt
- composite nitride
- nitride
- transition element
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Landscapes
- Inorganic Compounds Of Heavy Metals (AREA)
- Compounds Of Iron (AREA)
Description
【0001】
【発明の属する技術分野】
本発明は、リチウム含有複合窒化物の製造方法に関するものである。
【0002】
【従来の技術】
リチウム含有複合窒化物は、窒化リチウム(Li3N)を基本構造とし、その構造中のリチウムの一部を他元素で置換した化合物である。リチウム含有複合窒化物としては、一般式Li3−x−yMxN(式中MはTi、V、Cr、Mn、Fe、Co、Ni、およびCuからなる群より選ばれた少なくとも一種の遷移元素を表し、xおよびyは0<x≦0.8、0≦y≦2−xの範囲で示される実数を表す。)で表されるものである。これらの化合物は、結晶中に遷移元素を導入したことにより、窒化リチウムと同様に優れたリチウムイオン伝導性を有していると同時に電子伝導性も有するといった特徴を持ち、広い分野での応用が期待されている。ここで、xは遷移元素による置換割合を表す。また、yは非化学量論組成をとりうる範囲を表すが、化学量論組成であるy=0の組成が一般的である。
【0003】
このようなリチウム含有複合窒化物は、一般的には、金属リチウムを窒素と反応させることにより合成して得た窒化リチウムを出発原料に用い、これに遷移元素粉末または遷移元素の窒化物粉末を混合し、窒素雰囲気中または窒素ー水素混合雰囲気中で焼成することにより合成される(西島ら、Solid State Ionics 83(1996)107−111)。
【0004】
【発明が解決しようとする課題】
従来の合成方法では、不純物の混入が避けられず、またリチウムと遷移元素の組成比の正確な制御が困難であった。
【0005】
【課題を解決するための手段】
本発明は、リチウム、遷移元素M(MはTi、V、Cr、Mn、Fe、Co、Ni、およびCuからなる群より選ばれた少なくとも一種の遷移元素を示す)、およびリチウムと遷移元素Mとの合金からなる群より選ばれ、所定量のリチウムおよび遷移元素Mを含む原料を、窒素を含む雰囲気中で加熱処理することにより、一般式Li3−x−yMxN(式中、xおよびyは各々0<x≦0.8、0≦y≦2−xの範囲で示される実数を表す)で表されるリチウム含有複合窒化物を合成する。
ここで、合金とは、二種以上の金属からなる固溶体、共晶体、および金属間化合物の三種の状態の少なくとも一種を指すものとする。
【0006】
【発明の実施の形態】
本発明に用いるリチウム−遷移元素M合金のLi/Mのモル比は、目的とする窒化物と同じか、またはリチウム過剰(過剰量は15%以下)とすることが好ましい。
反応温度については、20℃以上、600℃以下の範囲内の温度であることが実用上好ましい。これは、反応温度が20℃未満では反応速度が遅く、600℃を超える温度ではリチウムの蒸発や昇華による組成の変化が大きくなる可能性があるためである。
反応時間については、反応速度およびリチウムの昇華等を考慮すると、6時間以上、50時間以下であることが好ましい。
【0007】
反応の雰囲気は、窒素雰囲気だけでなく、不活性ガスと窒素の混合雰囲気及び水素と窒素の混合雰囲気を用いることができる。ただし、いずれの場合も雰囲気中の水分量は露点−20℃以下、酸素分圧は1%以下であることが好ましい。水分量、酸素分圧のいずれか一方でも前記条件を満たさない場合には、不純物である酸化リチウム、水酸化リチウムの生成が著しく増加し、不純物抑制の効果が得られない。
【0008】
従来の合成法では、遷移元素Mの固溶が進み難いだけでなく、反応温度が700℃以上と比較的高いのでリチウムの昇華の影響を受けやすく、両者の影響で合成物の組成の正確な制御が困難であった。また、高い反応温度では副反応が起こりやすく、活物質中に微量の未反応物や副反応生成物等の不純物が混入しやすい。さらに、このような合成物に含まれる不純物の除去は極めて困難であった。
本発明の合成方法によると、微量の不純物成分の生成を抑制することができ、また、合成される材料組成を正確に制御することができ、かつ合成の再現性を大幅に向上させることができる。
【0009】
【実施例】
以下、本発明の実施例を詳細に説明するが、本発明はこれら実施例に限定されるものではない。
《実施例1》
本実施例では、遷移元素Mとしてコバルトを用いた例について説明する。
本実施例において、材料の混合、焼成、分析等の作業行程は、全て窒素雰囲気中で行った。また、雰囲気中の水分量は露点−60℃、酸素分圧は50ppmであった。
リチウム−コバルト複合窒化物は次のようにして合成した。
まず、所定組成比のリチウム−コバルト合金を銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し、窒素と反応させた。反応後、得られた黒灰色の化合物を粉砕しリチウム−コバルト複合窒化物粉末を得た。
リチウム−コバルト比については、Li/Coのモル比が2.9/0.1、2.8/0.2、2.6/0.4、2.4/0.6、2.2/0.8、2.1/0.9、2.0/1.0、1.9/1.1のそれぞれについて合成を行った。
いずれの場合にも、出発原料であるリチウム−コバルト合金のLi/Coモル比は目的とする窒化物と同じか、またはリチウム過剰(過剰量は15%以下)とすることが好ましい。本実施例においては、目的組成と同じとした。
【0010】
合成した各サンプルについて、それぞれCuのKα線を用いた粉末X線回折測定を行った。代表的なX線回折パターンとして図1にLi/Coのモル比が2.6/0.4のパターンを示した。他のいずれのサンプルでも窒化リチウム(Li3N)と同じ六方晶に基づく回折パターンが現れていた。しかし、Li/Coのモル比が1.9/1.1のものでは、金属Coに基づく回折ピークが見られ、Coが固溶しきれていないことを示していた。
なお、X線回折パターンに現れているシリコンの回折ピークは、内部標準として混合したものである。
【0011】
《比較例1》
比較のために、従来法による合成法として、窒化リチウム(Li3N)とコバルト粉末を出発原料として用い、リチウム−コバルト複合窒化物を合成した。
まず、所定組成比の窒化リチウムとコバルト粉末を銅製の容器に入れ、窒素雰囲気中、700℃で8時間保持し反応させた。反応後、得られた黒灰色の化合物を粉砕しリチウム−コバルト複合窒化物粉末を得た。
リチウム−コバルト比については、Li/Coのモル比が2.9/0.1、2.8/0.2、2.6/0.4、2.4/0.6、2.2/0.8、2.1/0.9、2.0/1.0、1.9/1.1のそれぞれについて合成を行った。
いずれの場合にも、出発原料の混合比は目的組成と同じとした。
【0012】
合成した各サンプルのそれぞれについて粉末X線回折測定を行った。代表的なX線回折パターンとして図2にLi/Coのモル比が2.6/0.4のパターンを示す。いずれも結晶系は窒化リチウム(Li3N)と同じ六方晶であったが、酸化リチウムと考えられる不純物のピークが現れており、単一相を得ることができなかった。特に、Li/Coのモル比が2.2/0.8以下のコバルト置換量の大きなサンプルでは、金属Coに基づく回折ピークが見られ、従来の合成法ではCo固溶量の限界値も小さいことがわかった。なお、X線回折パターンに現れているシリコンのピークは、内部標準として混合したものである。
【0013】
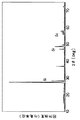
図3は実施例1および比較例1により得られた各サンプルの格子定数cをCo置換割合xに対してプロットして示す。実施例と比較し、比較例により合成した窒化物は、同じ仕込み組成でも格子定数が異なり、いずれの組成でもc軸が大きくなっている。これは、Co固溶量が少なくなっていることを表している。従来例の700℃で焼成する場合は、リチウムの昇華の影響は見られないものの、Coが固溶し難く、Co固溶量の制御も困難であると考えられる。特に、コバルト置換割合が0.8以上の場合には、格子定数変化が無く、これ以上の固溶が進んでいないと考えられる。
【0014】
《実施例2》
本実施例では、遷移元素MとしてTi、V、Cr、Mn、Fe、Ni、Cuの各元素を用いた。
まず、Li/Mのモル比が2.6/0.4であるリチウム−M合金粉末を銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し、窒素と反応させた。反応後、得られた黒灰色の化合物を粉砕しリチウム−Ti複合窒化物、リチウム−V複合窒化物、リチウム−Cr複合窒化物、リチウム−Mn複合窒化物、リチウム−Fe複合窒化物、リチウム−Ni複合窒化物、リチウム−Cu複合窒化物を得た。
いずれの場合にも、出発原料であるリチウム−M合金のLi/Mのモル比は、目的とする窒化物と同じとした。
【0015】
《比較例2》
置換元素をTi、V、Cr、Mn、Fe、Ni、Cuとした以外は比較例1と同様の方法でLi/Mのモル比が2.6/0.4の仕込み組成比のサンプルを合成した。
【0016】
実施例2および比較例2で合成した各サンプルについて粉末X線回折測定を行ったところ、いずれの置換元素を用いた場合でも、本発明の合成法によると、窒化リチウムと同様の六方晶系の結晶構造を有する化合物が不純物のない単一相で合成できていた。一方、従来例の比較例2によるサンプルは、いずれも酸化リチウムに基づく回折ピークが見られ、単一相は得られなかった。
以上のように、置換元素MがTi、V、Cr、Mn、Fe、Ni、Cuのいずれの場合も本発明の方法で合成することにより、従来法で合成した場合よりも不純物の少ないリチウム含有複合窒化物を得ることができた。
【0017】
《実施例3》
本実施例では、遷移元素Mをコバルトとし、リチウム、コバルト、リチウムーコバルト合金を出発原料として用いた場合について説明する。
なお、本実施例での材料混合、焼成、分析等の作業行程は全て窒素雰囲気中で行った。また、雰囲気中の水分量は露点−60℃、酸素分圧は50ppmであった。
リチウムーコバルト複合窒化物は次のようにして合成した。
まず、所定量のリチウムとコバルト粉末を銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し反応させた。反応後、得られた黒灰色の化合物を粉砕し、リチウムーコバルト複合窒化物粉末を得た。
【0018】
つぎに、リチウムとCo3Liを目的の組成比となるように混合し、銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し反応させた。反応後、得られた黒灰色の化合物を粉砕し、リチウムーコバルト複合窒化物粉末を得た。
いずれの場合も、リチウムーコバルト比についてはLi/Coモル比が2.6/0.4となるように合成を行った。また、出発原料であるリチウムーコバルト合金のLi/Coモル比は目的とする窒化物と同じか、またはリチウム過剰(過剰量は15%以下)とすることが好ましい。本実施例においては目的組成と同じとした。
また、反応温度については20℃以上、600℃以下の範囲の温度であることが実用上好ましい。これは、反応温度が20℃未満では反応速度が遅く、600℃を超える温度ではリチウムの昇華による組成の変化が大きくなる可能性があるためである。
【0019】
反応時間については本実施例では24時間としたが、反応速度およびリチウムの昇華等を考慮すると6時間以上、50時間以下であることが好ましい。
また、反応の雰囲気を窒素雰囲気としたが、不活性ガスと窒素の混合雰囲気、または水素と窒素の混合雰囲気中でもよい。ただし、いずれの場合も雰囲気中の水分量は露点−20℃以下、酸素分圧は1%以下であることが好ましい。水分量、酸素分圧のいずれか一方でも前記条件を満たさない場合には、不純物である酸化リチウム、水酸化リチウムの生成が著しく増加し、本発明の合成法による不純物抑制の効果が得られない。
【0020】
合成した各サンプルについてそれぞれ粉末X線回折測定を行った。図4にリチウムとコバルト粉末を用いて合成したサンプルの粉末X線回折パターンを、図5にリチウムとCo3Liを用いて合成したサンプルの粉末X線回折パターンをそれぞれ示す。いずれの場合も実施例1の図1と同様の回折パターンが得られ、六方晶に基づく回折パターンが現れていた。また、いずれのサンプルも図1と同様に酸化リチウムによると思われるピークは見られなかった。
さらに、X線回折パターンより各サンプルの格子定数cを求めたところ、いずれも、実施例1のLi/Co=2.6/0.4の比で合成した場合と同等の値であった。
従って、本実施例で合成したサンプルは、いずれも、実施例1の場合と同等のリチウムーコバルト複合窒化物が合成できていると考えられる。
本実施例では、出発原料としてリチウムとコバルトを用いた場合、およびリチウムとCo3Liを用いた場合について説明したが、Co3Li以外のリチウムーコバルト合金とリチウムの組み合わせ、および、リチウムーコバルト合金とコバルトの組み合わせでも同様にリチウムーコバルト複合窒化物を合成することができる。
【0021】
【発明の効果】
以上のように本発明によれば、不純物の生成を抑制し、組成が正確に制御されたリチウム含有複合窒化物を得ることができる。
【図面の簡単な説明】
【図1】本発明の一実施例により得たリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【図2】比較例のリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【図3】実施例および比較例のリチウム−コバルト複合窒化物の格子定数cとコバルト置換割合の関係を示す図である。
【図4】本発明の他の実施例により得たリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【図5】本発明の他の実施例により得たリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【発明の属する技術分野】
本発明は、リチウム含有複合窒化物の製造方法に関するものである。
【0002】
【従来の技術】
リチウム含有複合窒化物は、窒化リチウム(Li3N)を基本構造とし、その構造中のリチウムの一部を他元素で置換した化合物である。リチウム含有複合窒化物としては、一般式Li3−x−yMxN(式中MはTi、V、Cr、Mn、Fe、Co、Ni、およびCuからなる群より選ばれた少なくとも一種の遷移元素を表し、xおよびyは0<x≦0.8、0≦y≦2−xの範囲で示される実数を表す。)で表されるものである。これらの化合物は、結晶中に遷移元素を導入したことにより、窒化リチウムと同様に優れたリチウムイオン伝導性を有していると同時に電子伝導性も有するといった特徴を持ち、広い分野での応用が期待されている。ここで、xは遷移元素による置換割合を表す。また、yは非化学量論組成をとりうる範囲を表すが、化学量論組成であるy=0の組成が一般的である。
【0003】
このようなリチウム含有複合窒化物は、一般的には、金属リチウムを窒素と反応させることにより合成して得た窒化リチウムを出発原料に用い、これに遷移元素粉末または遷移元素の窒化物粉末を混合し、窒素雰囲気中または窒素ー水素混合雰囲気中で焼成することにより合成される(西島ら、Solid State Ionics 83(1996)107−111)。
【0004】
【発明が解決しようとする課題】
従来の合成方法では、不純物の混入が避けられず、またリチウムと遷移元素の組成比の正確な制御が困難であった。
【0005】
【課題を解決するための手段】
本発明は、リチウム、遷移元素M(MはTi、V、Cr、Mn、Fe、Co、Ni、およびCuからなる群より選ばれた少なくとも一種の遷移元素を示す)、およびリチウムと遷移元素Mとの合金からなる群より選ばれ、所定量のリチウムおよび遷移元素Mを含む原料を、窒素を含む雰囲気中で加熱処理することにより、一般式Li3−x−yMxN(式中、xおよびyは各々0<x≦0.8、0≦y≦2−xの範囲で示される実数を表す)で表されるリチウム含有複合窒化物を合成する。
ここで、合金とは、二種以上の金属からなる固溶体、共晶体、および金属間化合物の三種の状態の少なくとも一種を指すものとする。
【0006】
【発明の実施の形態】
本発明に用いるリチウム−遷移元素M合金のLi/Mのモル比は、目的とする窒化物と同じか、またはリチウム過剰(過剰量は15%以下)とすることが好ましい。
反応温度については、20℃以上、600℃以下の範囲内の温度であることが実用上好ましい。これは、反応温度が20℃未満では反応速度が遅く、600℃を超える温度ではリチウムの蒸発や昇華による組成の変化が大きくなる可能性があるためである。
反応時間については、反応速度およびリチウムの昇華等を考慮すると、6時間以上、50時間以下であることが好ましい。
【0007】
反応の雰囲気は、窒素雰囲気だけでなく、不活性ガスと窒素の混合雰囲気及び水素と窒素の混合雰囲気を用いることができる。ただし、いずれの場合も雰囲気中の水分量は露点−20℃以下、酸素分圧は1%以下であることが好ましい。水分量、酸素分圧のいずれか一方でも前記条件を満たさない場合には、不純物である酸化リチウム、水酸化リチウムの生成が著しく増加し、不純物抑制の効果が得られない。
【0008】
従来の合成法では、遷移元素Mの固溶が進み難いだけでなく、反応温度が700℃以上と比較的高いのでリチウムの昇華の影響を受けやすく、両者の影響で合成物の組成の正確な制御が困難であった。また、高い反応温度では副反応が起こりやすく、活物質中に微量の未反応物や副反応生成物等の不純物が混入しやすい。さらに、このような合成物に含まれる不純物の除去は極めて困難であった。
本発明の合成方法によると、微量の不純物成分の生成を抑制することができ、また、合成される材料組成を正確に制御することができ、かつ合成の再現性を大幅に向上させることができる。
【0009】
【実施例】
以下、本発明の実施例を詳細に説明するが、本発明はこれら実施例に限定されるものではない。
《実施例1》
本実施例では、遷移元素Mとしてコバルトを用いた例について説明する。
本実施例において、材料の混合、焼成、分析等の作業行程は、全て窒素雰囲気中で行った。また、雰囲気中の水分量は露点−60℃、酸素分圧は50ppmであった。
リチウム−コバルト複合窒化物は次のようにして合成した。
まず、所定組成比のリチウム−コバルト合金を銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し、窒素と反応させた。反応後、得られた黒灰色の化合物を粉砕しリチウム−コバルト複合窒化物粉末を得た。
リチウム−コバルト比については、Li/Coのモル比が2.9/0.1、2.8/0.2、2.6/0.4、2.4/0.6、2.2/0.8、2.1/0.9、2.0/1.0、1.9/1.1のそれぞれについて合成を行った。
いずれの場合にも、出発原料であるリチウム−コバルト合金のLi/Coモル比は目的とする窒化物と同じか、またはリチウム過剰(過剰量は15%以下)とすることが好ましい。本実施例においては、目的組成と同じとした。
【0010】
合成した各サンプルについて、それぞれCuのKα線を用いた粉末X線回折測定を行った。代表的なX線回折パターンとして図1にLi/Coのモル比が2.6/0.4のパターンを示した。他のいずれのサンプルでも窒化リチウム(Li3N)と同じ六方晶に基づく回折パターンが現れていた。しかし、Li/Coのモル比が1.9/1.1のものでは、金属Coに基づく回折ピークが見られ、Coが固溶しきれていないことを示していた。
なお、X線回折パターンに現れているシリコンの回折ピークは、内部標準として混合したものである。
【0011】
《比較例1》
比較のために、従来法による合成法として、窒化リチウム(Li3N)とコバルト粉末を出発原料として用い、リチウム−コバルト複合窒化物を合成した。
まず、所定組成比の窒化リチウムとコバルト粉末を銅製の容器に入れ、窒素雰囲気中、700℃で8時間保持し反応させた。反応後、得られた黒灰色の化合物を粉砕しリチウム−コバルト複合窒化物粉末を得た。
リチウム−コバルト比については、Li/Coのモル比が2.9/0.1、2.8/0.2、2.6/0.4、2.4/0.6、2.2/0.8、2.1/0.9、2.0/1.0、1.9/1.1のそれぞれについて合成を行った。
いずれの場合にも、出発原料の混合比は目的組成と同じとした。
【0012】
合成した各サンプルのそれぞれについて粉末X線回折測定を行った。代表的なX線回折パターンとして図2にLi/Coのモル比が2.6/0.4のパターンを示す。いずれも結晶系は窒化リチウム(Li3N)と同じ六方晶であったが、酸化リチウムと考えられる不純物のピークが現れており、単一相を得ることができなかった。特に、Li/Coのモル比が2.2/0.8以下のコバルト置換量の大きなサンプルでは、金属Coに基づく回折ピークが見られ、従来の合成法ではCo固溶量の限界値も小さいことがわかった。なお、X線回折パターンに現れているシリコンのピークは、内部標準として混合したものである。
【0013】
図3は実施例1および比較例1により得られた各サンプルの格子定数cをCo置換割合xに対してプロットして示す。実施例と比較し、比較例により合成した窒化物は、同じ仕込み組成でも格子定数が異なり、いずれの組成でもc軸が大きくなっている。これは、Co固溶量が少なくなっていることを表している。従来例の700℃で焼成する場合は、リチウムの昇華の影響は見られないものの、Coが固溶し難く、Co固溶量の制御も困難であると考えられる。特に、コバルト置換割合が0.8以上の場合には、格子定数変化が無く、これ以上の固溶が進んでいないと考えられる。
【0014】
《実施例2》
本実施例では、遷移元素MとしてTi、V、Cr、Mn、Fe、Ni、Cuの各元素を用いた。
まず、Li/Mのモル比が2.6/0.4であるリチウム−M合金粉末を銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し、窒素と反応させた。反応後、得られた黒灰色の化合物を粉砕しリチウム−Ti複合窒化物、リチウム−V複合窒化物、リチウム−Cr複合窒化物、リチウム−Mn複合窒化物、リチウム−Fe複合窒化物、リチウム−Ni複合窒化物、リチウム−Cu複合窒化物を得た。
いずれの場合にも、出発原料であるリチウム−M合金のLi/Mのモル比は、目的とする窒化物と同じとした。
【0015】
《比較例2》
置換元素をTi、V、Cr、Mn、Fe、Ni、Cuとした以外は比較例1と同様の方法でLi/Mのモル比が2.6/0.4の仕込み組成比のサンプルを合成した。
【0016】
実施例2および比較例2で合成した各サンプルについて粉末X線回折測定を行ったところ、いずれの置換元素を用いた場合でも、本発明の合成法によると、窒化リチウムと同様の六方晶系の結晶構造を有する化合物が不純物のない単一相で合成できていた。一方、従来例の比較例2によるサンプルは、いずれも酸化リチウムに基づく回折ピークが見られ、単一相は得られなかった。
以上のように、置換元素MがTi、V、Cr、Mn、Fe、Ni、Cuのいずれの場合も本発明の方法で合成することにより、従来法で合成した場合よりも不純物の少ないリチウム含有複合窒化物を得ることができた。
【0017】
《実施例3》
本実施例では、遷移元素Mをコバルトとし、リチウム、コバルト、リチウムーコバルト合金を出発原料として用いた場合について説明する。
なお、本実施例での材料混合、焼成、分析等の作業行程は全て窒素雰囲気中で行った。また、雰囲気中の水分量は露点−60℃、酸素分圧は50ppmであった。
リチウムーコバルト複合窒化物は次のようにして合成した。
まず、所定量のリチウムとコバルト粉末を銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し反応させた。反応後、得られた黒灰色の化合物を粉砕し、リチウムーコバルト複合窒化物粉末を得た。
【0018】
つぎに、リチウムとCo3Liを目的の組成比となるように混合し、銅製の容器に入れ、窒素雰囲気中、300℃で24時間保持し反応させた。反応後、得られた黒灰色の化合物を粉砕し、リチウムーコバルト複合窒化物粉末を得た。
いずれの場合も、リチウムーコバルト比についてはLi/Coモル比が2.6/0.4となるように合成を行った。また、出発原料であるリチウムーコバルト合金のLi/Coモル比は目的とする窒化物と同じか、またはリチウム過剰(過剰量は15%以下)とすることが好ましい。本実施例においては目的組成と同じとした。
また、反応温度については20℃以上、600℃以下の範囲の温度であることが実用上好ましい。これは、反応温度が20℃未満では反応速度が遅く、600℃を超える温度ではリチウムの昇華による組成の変化が大きくなる可能性があるためである。
【0019】
反応時間については本実施例では24時間としたが、反応速度およびリチウムの昇華等を考慮すると6時間以上、50時間以下であることが好ましい。
また、反応の雰囲気を窒素雰囲気としたが、不活性ガスと窒素の混合雰囲気、または水素と窒素の混合雰囲気中でもよい。ただし、いずれの場合も雰囲気中の水分量は露点−20℃以下、酸素分圧は1%以下であることが好ましい。水分量、酸素分圧のいずれか一方でも前記条件を満たさない場合には、不純物である酸化リチウム、水酸化リチウムの生成が著しく増加し、本発明の合成法による不純物抑制の効果が得られない。
【0020】
合成した各サンプルについてそれぞれ粉末X線回折測定を行った。図4にリチウムとコバルト粉末を用いて合成したサンプルの粉末X線回折パターンを、図5にリチウムとCo3Liを用いて合成したサンプルの粉末X線回折パターンをそれぞれ示す。いずれの場合も実施例1の図1と同様の回折パターンが得られ、六方晶に基づく回折パターンが現れていた。また、いずれのサンプルも図1と同様に酸化リチウムによると思われるピークは見られなかった。
さらに、X線回折パターンより各サンプルの格子定数cを求めたところ、いずれも、実施例1のLi/Co=2.6/0.4の比で合成した場合と同等の値であった。
従って、本実施例で合成したサンプルは、いずれも、実施例1の場合と同等のリチウムーコバルト複合窒化物が合成できていると考えられる。
本実施例では、出発原料としてリチウムとコバルトを用いた場合、およびリチウムとCo3Liを用いた場合について説明したが、Co3Li以外のリチウムーコバルト合金とリチウムの組み合わせ、および、リチウムーコバルト合金とコバルトの組み合わせでも同様にリチウムーコバルト複合窒化物を合成することができる。
【0021】
【発明の効果】
以上のように本発明によれば、不純物の生成を抑制し、組成が正確に制御されたリチウム含有複合窒化物を得ることができる。
【図面の簡単な説明】
【図1】本発明の一実施例により得たリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【図2】比較例のリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【図3】実施例および比較例のリチウム−コバルト複合窒化物の格子定数cとコバルト置換割合の関係を示す図である。
【図4】本発明の他の実施例により得たリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
【図5】本発明の他の実施例により得たリチウム−コバルト複合窒化物のX線回折パターンを示す図である。
Claims (2)
- リチウム、遷移元素M(MはTi、V、Cr、Mn、Fe、Co、Ni、およびCuからなる群より選ばれた少なくとも一種の遷移元素を示す)、およびリチウムと遷移元素Mとの合金からなる群より選ばれ、所定量のリチウムおよび遷移元素Mを含む原料を、窒素を含む雰囲気中で加熱処理して一般式Li3−x−yMxN(式中、xおよびyは各々0<x≦0.8、0≦y≦2−xの範囲で示される実数を表す)で表されるリチウム含有複合窒化物を得ることを特徴とするリチウム含有複合窒化物の製造方法。
- 前記加熱温度が、20℃以上、600℃以下の範囲である請求項1記載のリチウム含有複合窒化物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP15398497A JP3607043B2 (ja) | 1997-06-11 | 1997-06-11 | リチウム含有複合窒化物の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP15398497A JP3607043B2 (ja) | 1997-06-11 | 1997-06-11 | リチウム含有複合窒化物の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPH111308A JPH111308A (ja) | 1999-01-06 |
| JP3607043B2 true JP3607043B2 (ja) | 2005-01-05 |
Family
ID=15574375
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP15398497A Expired - Fee Related JP3607043B2 (ja) | 1997-06-11 | 1997-06-11 | リチウム含有複合窒化物の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3607043B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4840778B2 (ja) * | 2007-03-19 | 2011-12-21 | 国立大学法人大阪大学 | 蛍光体の製造方法、蛍光体、並びに蛍光体含有組成物、発光装置、画像表示装置及び照明装置 |
| KR102738331B1 (ko) * | 2020-04-16 | 2024-12-03 | 후루카와 기카이 긴조쿠 가부시키가이샤 | 질화리튬 제조장치 및 질화리튬의 제조방법 |
-
1997
- 1997-06-11 JP JP15398497A patent/JP3607043B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JPH111308A (ja) | 1999-01-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Takada et al. | Preparation and crystal structure refinement of Li4Mn5O12 by the Rietveld method | |
| KR100589031B1 (ko) | 캐소드 흡장 조성물, 이의 제조 방법 및 이를 포함하는 재충전식 리튬 전지 | |
| Paulsen et al. | Studies of the layered manganese bronzes, Na2/3 [Mn1− xMx] O2 with M= Co, Ni, Li, and Li2/3 [Mn1− xMx] O2 prepared by ion-exchange | |
| US5858324A (en) | Lithium based compounds useful as electrodes and method for preparing same | |
| US5393622A (en) | Process for production of positive electrode active material | |
| Rørmark et al. | Oxygen stoichiometry and structural properties of La 1− x A x MnO 3±δ (A= Ca or Sr and 0≤ x≤ 1) | |
| US5240794A (en) | Electrochemical cell | |
| Nishijima et al. | Li deintercalation and structural change in the lithium transition metal nitride Li3FeN2 | |
| Massarotti et al. | Stability of LiMn2O4 and new high temperature phases in air, O2 and N2 | |
| JP2007123255A (ja) | リチウム・遷移金属複合酸化物及びその製造方法並びにそれを用いてなるリチウム電池 | |
| Xia et al. | Studies on Li Mn O spinel system (obtained from melt-impregnation method) as a cathode for 4 V lithium batteries Part II. Optimum spinel from γ-MnOOH | |
| Thackeray et al. | Review–from LiMn2O4 to partially-disordered Li2MnNiO4: the evolution of lithiated-spinel cathodes for Li-ion batteries | |
| Scheer et al. | Oxide complexes formed in the systems platinum metals: alkali carbonates: oxygen | |
| EP3341991A1 (en) | High tap density lithium positive electrode active material, intermediate and process of preparation | |
| Croguennec et al. | Preparation, physical and structural characterization of LiMnO2 samples with variable cationic disorder | |
| Alcantara et al. | X-ray diffraction, 57Fe Mössbauer and step potential electrochemical spectroscopy study of LiFeyCo1− yO2 compounds | |
| JP5069007B2 (ja) | リチウム・遷移金属複合酸化物の製造方法 | |
| Fey et al. | A new preparation method for a novel high voltage cathode material: LiNiVO4 | |
| JP3707744B2 (ja) | リチウム複合酸化物の製造方法 | |
| JP5657970B2 (ja) | リチウム・遷移金属複合酸化物及びそれを用いてなるリチウム電池 | |
| Zinkevich | Constitution of the Sr–Ni–O system | |
| JP3607043B2 (ja) | リチウム含有複合窒化物の製造方法 | |
| Feng et al. | Synthesis of lithium manganese oxides from layered manganese oxides by hydrothermal soft chemical process | |
| JP4066102B2 (ja) | リチウムマンガン複合酸化物の製造方法 | |
| Simada et al. | Solid-state reactions in the system Cu—Sb—O; Formation of a new copper (I) antimony oxide |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20040827 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20040916 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20041006 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |