JP2020077576A - リチウムイオン二次電池 - Google Patents
リチウムイオン二次電池 Download PDFInfo
- Publication number
- JP2020077576A JP2020077576A JP2018211482A JP2018211482A JP2020077576A JP 2020077576 A JP2020077576 A JP 2020077576A JP 2018211482 A JP2018211482 A JP 2018211482A JP 2018211482 A JP2018211482 A JP 2018211482A JP 2020077576 A JP2020077576 A JP 2020077576A
- Authority
- JP
- Japan
- Prior art keywords
- positive electrode
- negative electrode
- battery
- ion secondary
- secondary battery
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
Description
[リチウムイオン二次電池の全体構成]
最初に、本発明の一実施形態に係るリチウムイオン二次電池の全体構成について図面を参照しながら説明する。図1は、本発明の一実施形態に係るリチウムイオン二次電池を示す概略断面図である。このようなリチウムイオン二次電池は、積層型リチウムイオン二次電池と呼ばれる。なお、図1には積層型セルの構成を示すが、本発明のリチウムイオン二次電池は、正極・負極・セパレータを重ねて層状に巻いた捲回型であってもよい。
[リチウムイオン二次電池用負極]
負極12は、負極集電体12Aの片面に負極合材層12Bが設けられた構成を有する。ここで、負極合材層12Bは、負極活物質、導電助材、水分散性バインダを含む。負極合材層12B内でのこれらの物質は、電池内に注入された電解液と接触している。
(負極活物質)
負極活物質としては、金属リチウム、リチウム含有合金、リチウムとの合金化が可能な金属もしくは合金、リチウムイオンのドープ・脱ドープが可能な酸化物、リチウムイオンのドープ・脱ドープが可能な遷移金属窒素化物、および、リチウムイオンのドープ・脱ドープが可能な炭素材料からなる群から選ばれた少なくとも1種(単独で用いてもよいし、これらの2種以上を含む混合物を用いてもよい)を用いることができる。これらの中でもリチウムイオンをドープ・脱ドープすることが可能な炭素材料が好ましい。このような炭素材料としては、カーボンブラック、活性炭、黒鉛材料(人造黒鉛、天然黒鉛)、非晶質炭素材料、等が挙げられる。前記炭素材料の形態は、繊維状、球状、ポテト状、フレーク状いずれの形態であってもよい。また、その粒径も特に限定されないが、通常5〜50μm、好ましくは20〜30μm程度である。
これらの炭素材料は、1種類で使用してもよく、2種類以上混合して使用してもよい。
負極合材層は、導電助材を含むことが好ましい。本発明で用いる導電助材としては、公知の導電助材を使用することができる。公知の導電助材としては、導電性を有する炭素材料であれば特に限定されるものではないが、グラファイト、カーボンブラック、導電性炭素繊維(カーボンナノチューブ、カーボンナノファイバー、カーボンファイバー)、フラーレン等を単独で、もしくは2種類以上を併せて使用することができる。市販のカーボンブラックとしては、例えば、トーカブラック#4300、#4400、#4500、#5500等(東海カーボン社製、ファーネスブラック)、プリンテックスL等(デグサ社製、ファーネスブラック)、Raven7000、5750、5250、5000ULTRAIII、5000ULTRA等、Conductex SC ULTRA、Conductex 975ULTRA等、PUER BLACK100、115、205等(コロンビヤン社製、ファーネスブラック)、#2350、#2400B、#2600B、#30050B、#3030B、#3230B、#3350B、#3400B、#5400B等(三菱化学社製、ファーネスブラック)、MONARCH1400、1300、900、VulcanXC−72R、BlackPearls2000、LITX−50、LITX−200等(キャボット社製、ファーネスブラック)、Ensaco250G、Ensaco260G、Ensaco350G、SuperP−Li(TIMCAL社製)、ケッチェンブラックEC−300J、EC−600JD(アクゾ社製)、デンカブラック、デンカブラックHS−100、FX−35(電気化学工業社製、アセチレンブラック)等、グラファイトとしては例えば人造黒鉛や燐片状黒鉛、塊状黒鉛、土状黒鉛などの天然黒鉛が挙げられるが、これらに限定されるものではない。
上記水分散性バインダとして、スチレンブタジエンゴム(SBR)、アクリロニトリル-ブタジエンゴム、アクリロニトリル-ブタジエン-スチレンゴム、カルボキシメチルセルロース(CMC)、およびヒドロキシプロピルメチルセルロース、ポリビニルアルコール、ヒドロキシプロピルセルロース、ジアセチルセルロースから選ばれる1種もしくは2種以上を組み合わせて用いることができる。特に、上記負極バインダとしてスチレンブタジエンゴムおよびカルボキシメチルセルロースを適宜混合したものを用いることが望ましい。
本実施形態に係る負極合材層には、上記各成分に加えて、その他の適当な成分が含まれていてもよい。例えば、負極合材層が合剤スラリーから形成される場合、負極合材層には、その合剤スラリー由来の各種配合成分が含まれることがある。そのような合剤スラリー由来の各種配合成分の例として、増粘剤、並びに、界面活性剤、分散剤、濡れ剤、消泡剤などその他の添加剤が挙げられる。
(負極合材層の形成方法)
本実施形態のリチウムイオン二次電池用負極が備える合材層は、上述した負極活物質、導電助材、水分散性バインダを含む負極合材スラリーを集電体の表面に塗布して、乾燥することによって製造することができる。合材スラリーに含まれる溶媒は水を使用することが好ましいが、必要に応じて、例えば、集電体への塗工性向上のために、水と相溶する液状媒体を使用しても良い。水と相溶する液状媒体としては、アルコール類、グリコール類、セロソルブ類、アミノアルコール類、アミン類、ケトン類、カルボン酸アミド類、リン酸アミド類、スルホキシド類、カルボン酸エステル類、リン酸エステル類、エーテル類、ニトリル類等が挙げられ、水と相溶する範囲で使用しても良い。
合材層の製造方法においては、集電体上に上記合剤スラリーを塗布乾燥後、金型プレスやロールプレスなどを用い、加圧処理により活物質層の空隙率を低くする工程を有することが好ましい。
正極活物質は、リチウムの吸蔵放出が可能な材料であれば特に限定されず、リチウムイオン二次電池に通常用いられる正極活物質でありうる。具体的には、リチウム(Li)とニッケル(Ni)とを構成金属元素とする酸化物のほか、リチウム及びニッケル以外に他の少なくとも一種の金属元素(すなわち、LiとNi以外の遷移金属元素及び/又は典型金属元素)を、原子数換算でニッケルと同程度またはニッケルよりも少ない割合で構成金属元素として含む酸化物をも包含する意味である。上記LiおよびNi以外の金属元素は、例えば、Co,Mn,Al,Cr,Fe,V,Mg,Ca,Na,Ti,Zr,Nb,Mo,W,Cu,Zn,Ga,In,Sn,LaおよびCeからなる群から選択される一種または二種以上の金属元素であり得る。これらの正極活物質は、単独で用いても複数を混合して用いてもよい。
電極合材層中の正極活物質の含有量は、通常10wt%以上、好ましくは30wt%以上、更に好ましくは50wt%以上であり、特に好ましくは70wt%以上である。また、通常99.9wt%以下、好ましくは99wt%以下である。
セパレータとしては、例えば、ポリエチレン(PE)、ポリプロピレン(PP)、ポリエステル、セルロース、ポリアミド等の樹脂からなる微多孔膜や多孔質の平板、更には不織布を挙げることができる。好適例として、一種または二種以上のポリオレフィン樹脂を主体に構成された単層または多層構造の多孔性樹脂シートが挙げられる。セパレータの厚みは、例えば15μm〜30μmとすることができる。好ましい一態様では、ポリエチレン等の熱可塑性樹脂からなる多孔性樹脂層を備えた、シャットダウン機能を有するセパレータである。この態様によれば、セパレータの温度が熱可塑性樹脂の軟化点に達すると樹脂が融解して細孔が目詰まりすることにより電流を遮断することができる。
電解液としては、例えば、通常リチウムイオン二次電池で用いられるものであることが好ましく、具体的には、有機溶媒に支持塩(リチウム塩)が溶解した形態を有する。ここで、リチウム塩として、例えば、六フッ化リン酸リチウム(LiPF6)、四フッ化ホウ酸リチウム(LiBF4)、過塩素酸リチウム(LiClO4)、六フッ化ヒ酸リチウム(LiAsF6)、六フッ化タンタル酸リチウム(LiTaF6)、四塩化アルミニウム酸リチウム(LiAlCl4)、リチウムデカクロロデカホウ素酸(Li2B10Cl10)等の無機酸陰イオン塩、トリフルオロメタンスルホン酸リチウム(LiCF3SO3)、リチウムビス(トリフルオロメタンスルホニル)イミド(Li(CF3SO2)2N)、リチウムビス(ペンタフルオロエタンスルホニル)イミド(Li(C2F5SO2)2N)等の有機酸陰イオン塩の中から選ばれる、少なくとも1種類のリチウム塩等を挙げることができる。その中でも、六フッ化リン酸リチウム(LiPF6)が好ましい。
ここで、実施形態において電解液には、添加剤としてメタンジスルホニルジフルオリド(以下、スルホン化合物と記載する。)が含まれる。スルホン化合物の含有量は、任意に設定可能であるが、中でも0.01重量%以上10重量%以下であるのが好ましい。電解液において高い化学的安定性が得られるからである。詳細には、0.01重量%よりも少ないと、電解液の化学的安定性が十分かつ安定に得られない可能性があり、10重量%よりも多いと、電気化学デバイスの主要な電気的性能(例えば電池における容量特性など)が十分に得られない可能性があるからである。
負極作製
1.スラリー調製
スラリー調製は5Lのプラネタリーディスパを用いた。
天然黒鉛960gと、Super−P(導電性カーボン、BET比表面積62m2/g)10gに、1%CMC(CMCを純水で溶解させた)を450g加え30分間混合した。次いで、1%−CMC水溶液300gを加えて30分間混練した後、更に、1%−CMC250gを加えて30分間混練した。その後、バインダとなるSBR(40%乳化液)50gを加えて30分間混合した後、真空脱泡30分間を行った。こうして固形分濃度45%のスラリーを調製した。
スラリー塗工にはダイコーターを用いた。乾燥後の塗布重量が11.0mg/cm2になるように、上記スラリーを銅箔(厚み10μm)の片面に塗布し乾燥した。次いで、反対面(未塗工面)に、同様に塗布重量が11.0mg/cm2になるように、上記スラリーを銅箔に塗布し乾燥した。こうして得た両面塗工(22.0mg/cm2)した負極ロールを、真空乾燥オーブンで120℃、12時間乾燥し、電極を得た。
小型プレス機を用いた。上下ロールのギャップ(隙間)を調整し、上記負極をプレス密度が1.45±0.05g/cm3になるように圧縮した。
電極塗布面積(表面:58mm×372mm、裏面:58mm×431mm)とタブ溶接余白が得られるように電極をスリットし、負極A−1を得た。
1.スラリー調製
スラリー調製は5Lのプラネタリーディスパを用いた。NCM523(Umicore社製、組成式 LiNi0.5Co0.2Mn0.3O2)920gと、Super−P(TIMCAL社製導電性カーボン)20g、KS−6(TIMREX社製鱗片状黒鉛)20gを10分間混合した後、N−メチルピロリドン(NMP)を100g加え更に20分間混合した。
スラリー塗工にはダイコーターを用いた。乾燥後の塗布重量が19.0mg/cm2になるように、上記スラリーをアルミ箔(厚み20μm、幅200mm)の片面に塗布し乾燥した。次いで、反対面(未塗工面)に、同様に塗布重量が19.0mg/cm2になるように、上記スラリーをアルミ箔に塗布し乾燥した。
こうして得た両面塗工(38.0mg/cm2)した正極ロールを、真空乾燥オーブンで130℃、12時間乾燥した。
35トンプレス機を用いた。上下ロールのギャップ(隙間)を調整し、上記正極をプレス密度が2.9±0.05g/cm3になるように圧縮した。
電極塗布面積(表面:56mm×334mm、裏:56mm×408mm)とタブ溶接余白が得られるように電極をスリットし正極C−1を得た。
捲回型電池(設計容量1Ah)
1.捲回
セパレータには、前記多孔質耐熱層付セパレータ(60.5mm×450mm)を用いた。
負極A−1(表面/裏面)とセパレータ(多孔質絶縁層が正極C−1と接するように配置)と正極C−1(裏面/表面)とセパレータ(多孔質絶縁層が正極C−1と接するように配置)を重ねて捲回した後プレス成型した。次いで、正極C−1の余白部分にアルミニウム製タブを超音波接合機で接合し、負極A−1の余白部分にニッケル製タブを超音波接合機で接合した。これをラミネートシートで挟み込み、3辺を加熱シールした。
非水溶媒としてエチレンカーボネート(以下、EC)とジメチルカーボネート(以下、DMC)とメチルエチルカーボネート(EMC)とを混合し、混合溶媒を作成した。電解液の作製にあたっては、電解液中に含まれるLiPF6を、最終的に得られる非水電解液中における電解質濃度が1モル/リットルとなるように溶解させて作成した。比較例の電解液として無添加の電解液を作成した。また、上記の混合溶媒にスルホン化合物を添加し、実施例の非水電解液を作成した。スルホン化合物の添加量(すなわち、最終的な非水電解液の全量に対する含有量)は、0.5質量%とした試料1、1.0質量%とした試料2、1.5質量%とした試料3を作成した。試料1〜試料3は実施例の電解液である。また、最終的な非水電解液において、EC、DMC及びEMCの質量比は、EC:DMC:EMC=30:35:35(質量比)となるように調整した。比較例の電池として無添加の電解液で作製した電池を電池0とし、実施例の電池として試料1〜3で作製した電池を電池1〜電池3とする。
電解液注液前に、上記を真空乾燥機にて、70℃×12h減圧乾燥した。電解液(1mol−LiPF6、EC/DEC=3/7(vol.比)、添加剤VC 1.0質量%)4.7±0.1gを注液した後、真空引きしながら加熱シールした。
3.エージング処理
電解液注液後の電池0〜3を40℃の雰囲気温度下で12h保持した。次いで、40℃雰囲気温度下で0.05Cで3.0Vまで定電流充電し、0.1Cで3.4Vまで定電流充電し、0.24Cで3.7Vまで定電流充電し、40℃雰囲気温度下で、24h休止した。その後、40℃雰囲気温度下で0.5Cで4.2Vまで定電流定電圧充電(0.5C−CCCV)し、30分間休止した後、3.0Vまで0.5Cで定電流放電(0.5C−CC)した。更に、0.5C−CCCVで4.2Vの充電と、0.5C−CCで3.7Vの放電を行い、3.7Vまで充電した。そして、40℃雰囲気温度下で7日間保存した。こうして電池0〜3を得た。
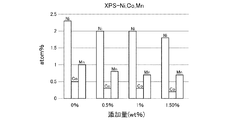
リチウムイオン二次電池の負極や正極表面の電子状態は、1〜10nm程度の検出深さを持つX線光電子分光法(X-ray photoelectron spectroscopy、以下、「XPS」と称する。)を用いて分析ができる。正極材の劣化は、電解液に接している活物質表面や、表面の結晶構造がダメージを受けることで進行する。正極活物質表面では、充電過程のたびに電解液が少しずつ酸化され、活物質表面に金属が溶出してしまうからである。活物質表面はリチウムイオンおよび電子の伝導に直接関わるため、その劣化は電池の容量低下や出力低下の原因となる。そこで、XPS測定では、負極や正極の表面に付着した元素の原子組成百分率(atom%)を検出し、負極表面や正極表面の状態を観測する。
作製した電池を充電すると、負極表面においてスルホン化合物が電気化学反応し、SEIと呼ばれる安定被膜が形成される。保存後の電池1〜3では、0.1atom%程度のS原子が検出された。ここで、スルホン化合物の添加量が増加しても、負極表面において検出されるS原子の原子組成百分率はあまり変化しないことが分かる。
次に、電池0〜3の保存前後における直流抵抗DCIR及び交流抵抗EIS-Z"を測定した。図5は、電池0〜3の保存前後における直流抵抗DCIR及び交流抵抗EIS-Z"を、電池0を基準に規格化した表である。尚、規格化とは、各電池の値を電池0の値で除し、電池0を100としたときの相対値を示す。
(直流抵抗DCIR)
直流抵抗の測定にあっては、以下の方法で充放電を行った後、25℃にて初期の電池抵抗を測定した。
まず、SOC(State of Charge)50%から放電レート0.2CでCC10s放電を行い、充電レート0.2CでCC−CV10s充電を行った。
次に、放電レート1CでCC10s放電を行い、放電レート2CでCC−CV10s充電を行った。
次に、放電レート2CでCC10s放電を行い、充電レート2CでCC−CV10s充電を行った。
次に、放電レート5CでCC10s放電を行い、充電レート5CでCC−CV10s充電を行った。こうして各電池0〜3を得た。
なお、CC10s放電とは、定電流(Constant Current)にて10秒間放電することを意味する。CC−CV10s充電とは、定電流定電圧(Constant Current - Constant Voltage)にて10秒間充電することを意味する。
各充放電休止電流と各充放電休止電圧とから直流抵抗を求め、得られた直流抵抗を、電池の初期の電池抵抗とした。また、電池を60℃で1週間保管した後、上記の方法により、保存後の電池抵抗を求め、保存前後の直流抵抗を図5のDCIR欄に示した。各電池の値は、電池0を基準に規格化したものである。
交流抵抗の測定にあっては、電池0〜3の交流インピーダンスを以下の方法によって測定した。電池のSOCを50%に調整し、25℃におけるBode-Plotを測定した(BioLogic社、VSP-300)。
周波数を0.1Hzから6MHzまで変化させ、虚数部の抵抗値と応答周波数からBode-Plotを求めた。さらに、Bode-Plotにより、10Hzにおける抵抗値を抽出した。また、電池を60℃で1週間保管した後、上記の方法により、保存後のEISを求め、保存前後の交流抵抗を図5のEIS-Z"(10Hz)欄に示した。各電池の値は、電池0を基準に規格化したものである。尚、EIS-Z"(10Hz)は、主に正極に由来する抵抗値として表される。
10 電池素子
11 正極
12 負極
13 セパレータ
21 正極リード
22 負極リード
Claims (3)
- リチウムイオンを吸蔵及び放出可能な正極及び負極と、セパレータと、電解液と、これら電池要素群を収容するケースと、を有するリチウムイオン二次電池であって、
前記ケースへの収容前電解液中にヘキサフルオロリン酸リチウムとメタンジスルホニルジフルオリド(以下、スルホン化合物)とを有し、
X線光電子分光法(以下、XPS)により、前記ケース内に前記電池要素群を収容し所定期間保存後のリチウムイオン二次電池の正極表面から検出される硫黄原子の原子組成百分率(以下、Satom%)を、前記所定期間保存後のリチウムイオン二次電池の負極表面から検出されるSatom%で除した値が2以上であることを特徴とするリチウムイオン二次電池。 - 請求項1に記載のリチウムイオン二次電池において、
前記除した値が3以上であることを特徴とするリチウムイオン二次電池。 - 請求項1または2に記載のリチウムイオン二次電池において、
前記正極の正極活物質は、LiNiaCobMncO2(ただし式中、0<a<1、0<b<1、0<c<1であり、a+b+c=1を満たす)であることを特徴とするリチウムイオン二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018211482A JP2020077576A (ja) | 2018-11-09 | 2018-11-09 | リチウムイオン二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018211482A JP2020077576A (ja) | 2018-11-09 | 2018-11-09 | リチウムイオン二次電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2020077576A true JP2020077576A (ja) | 2020-05-21 |
Family
ID=70724300
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018211482A Pending JP2020077576A (ja) | 2018-11-09 | 2018-11-09 | リチウムイオン二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2020077576A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112299387A (zh) * | 2019-08-02 | 2021-02-02 | 惠州比亚迪实业有限公司 | 再生磷酸铁锂正极材料及其制备方法 |
| EP4210142A4 (en) * | 2020-09-03 | 2025-06-18 | Central Glass Co Ltd | NON-AQUEOUS ELECTROLYTE AND NON-AQUEOUS ELECTROLYTE BATTERY |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006049112A (ja) * | 2004-08-05 | 2006-02-16 | Mitsubishi Chemicals Corp | 非水系電解液及び非水系電解液電池 |
| JP2009054407A (ja) * | 2007-08-27 | 2009-03-12 | Sony Corp | 電解液および二次電池 |
| JP2009054408A (ja) * | 2007-08-27 | 2009-03-12 | Sony Corp | 電解液および二次電池 |
| WO2017102557A1 (en) * | 2015-12-17 | 2017-06-22 | Basf Se | Cyanoalkyl sulfonylfluorides for electrolyte compositions for high energy lithium-ion batteries |
-
2018
- 2018-11-09 JP JP2018211482A patent/JP2020077576A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006049112A (ja) * | 2004-08-05 | 2006-02-16 | Mitsubishi Chemicals Corp | 非水系電解液及び非水系電解液電池 |
| JP2009054407A (ja) * | 2007-08-27 | 2009-03-12 | Sony Corp | 電解液および二次電池 |
| JP2009054408A (ja) * | 2007-08-27 | 2009-03-12 | Sony Corp | 電解液および二次電池 |
| WO2017102557A1 (en) * | 2015-12-17 | 2017-06-22 | Basf Se | Cyanoalkyl sulfonylfluorides for electrolyte compositions for high energy lithium-ion batteries |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112299387A (zh) * | 2019-08-02 | 2021-02-02 | 惠州比亚迪实业有限公司 | 再生磷酸铁锂正极材料及其制备方法 |
| CN112299387B (zh) * | 2019-08-02 | 2022-05-13 | 惠州比亚迪实业有限公司 | 再生磷酸铁锂正极材料及其制备方法 |
| EP4210142A4 (en) * | 2020-09-03 | 2025-06-18 | Central Glass Co Ltd | NON-AQUEOUS ELECTROLYTE AND NON-AQUEOUS ELECTROLYTE BATTERY |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6705384B2 (ja) | リチウム二次電池 | |
| US9991561B2 (en) | Lithium ion secondary battery | |
| US9401529B2 (en) | Nonaqueous electrolytic solution and battery including a heteropolyacid and/or a heteropolyacid compound | |
| JP7276957B2 (ja) | リチウムイオン二次電池 | |
| US20090169992A1 (en) | Lithium Secondary Battery Using Ionic Liquid | |
| WO2017047280A1 (ja) | リチウム二次電池及びその製造方法 | |
| KR102525619B1 (ko) | 리튬 이차 전지 | |
| CN111640975A (zh) | 用于锂离子电化学电池的电解质组合物 | |
| KR20180083274A (ko) | 비수전해액 및 이를 포함하는 리튬 이차전지 | |
| JP7110350B2 (ja) | ホウ酸リチウム化合物、リチウム二次電池用添加剤、リチウム二次電池用非水電解液、リチウム二次電池前駆体、並びに、リチウム二次電池及びその製造方法 | |
| KR102230038B1 (ko) | 리튬 이차 전지 | |
| CN112204773A (zh) | 锂二次电池 | |
| JP2012084426A (ja) | 非水電解質二次電池 | |
| JP5435622B2 (ja) | フィルム外装型非水系電解質二次電池 | |
| JPWO2019235469A1 (ja) | 還元型グラフェン系材料 | |
| JP7428346B2 (ja) | リチウム二次電池、及びリチウム二次電池の製造方法 | |
| JP7413635B2 (ja) | リン酸ホウ素リチウム化合物、リチウム二次電池用添加剤、リチウム二次電池用非水電解液、リチウム二次電池前駆体、リチウム二次電池の製造方法、及びリチウム二次電池 | |
| JP7276956B2 (ja) | リチウムイオン二次電池 | |
| JPWO2016098428A1 (ja) | リチウムイオン二次電池 | |
| JP2020077576A (ja) | リチウムイオン二次電池 | |
| JP7510496B2 (ja) | リチウム二次電池 | |
| JP7346799B2 (ja) | リン酸ホウ素リチウム化合物、リチウム二次電池用添加剤、リチウム二次電池用非水電解液、リチウム二次電池前駆体、リチウム二次電池の製造方法、及びリチウム二次電池 | |
| JP2020077575A (ja) | リチウムイオン二次電池 | |
| JP5573875B2 (ja) | 非水電解質溶液およびリチウムイオン二次電池 | |
| US10944098B2 (en) | Negative electrode active material particle, negative electrode, lithium-ion secondary battery, and production method of negative electrode active material particle |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20190521 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210804 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220622 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220705 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20230110 |