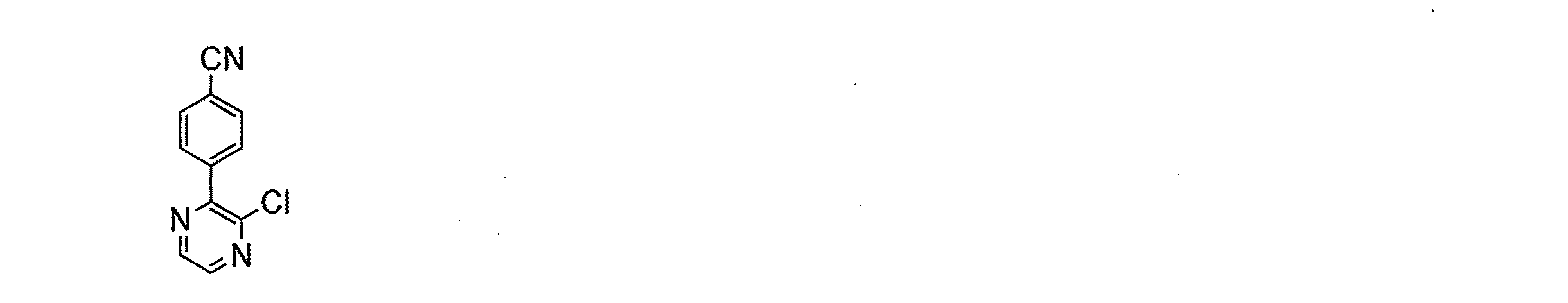JP2018522047A - Rorガンマモジュレータとしての新規化合物 - Google Patents
Rorガンマモジュレータとしての新規化合物 Download PDFInfo
- Publication number
- JP2018522047A JP2018522047A JP2018505705A JP2018505705A JP2018522047A JP 2018522047 A JP2018522047 A JP 2018522047A JP 2018505705 A JP2018505705 A JP 2018505705A JP 2018505705 A JP2018505705 A JP 2018505705A JP 2018522047 A JP2018522047 A JP 2018522047A
- Authority
- JP
- Japan
- Prior art keywords
- phenyl
- pyrazin
- acetamide
- mmol
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 CCC(*)(CCC(*C)CC1)CCC1c(cc1)ccc1NC(CC(C)=CC=C(C(C(*)(*)*)(F)F)C=C)=O Chemical compound CCC(*)(CCC(*C)CC1)CCC1c(cc1)ccc1NC(CC(C)=CC=C(C(C(*)(*)*)(F)F)C=C)=O 0.000 description 9
- DUHDRIZGITYNJL-KRHMZKEVSA-N CC(/C=C(/c(cc1)ccc1F)\Nc(cc1)ccc1N)=N Chemical compound CC(/C=C(/c(cc1)ccc1F)\Nc(cc1)ccc1N)=N DUHDRIZGITYNJL-KRHMZKEVSA-N 0.000 description 1
- CQMIHGACFASYRE-ISLYRVAYSA-N CC(C)(C)N/C(/c(cc1)ccc1F)=C(\C[NH-])/c(cc1)ccc1[N+]([O-])=O Chemical compound CC(C)(C)N/C(/c(cc1)ccc1F)=C(\C[NH-])/c(cc1)ccc1[N+]([O-])=O CQMIHGACFASYRE-ISLYRVAYSA-N 0.000 description 1
- ZVLJSRKWSWVGML-UHFFFAOYSA-N CC(CN(CC1)C(C)=O)N1c1c(-c(cc2)ccc2[N+]([O-])=O)nccn1 Chemical compound CC(CN(CC1)C(C)=O)N1c1c(-c(cc2)ccc2[N+]([O-])=O)nccn1 ZVLJSRKWSWVGML-UHFFFAOYSA-N 0.000 description 1
- AHQSDTAPZOQQBJ-UHFFFAOYSA-N CC(N1C)=NC=CC1=O Chemical compound CC(N1C)=NC=CC1=O AHQSDTAPZOQQBJ-UHFFFAOYSA-N 0.000 description 1
- JRKKMADZCUSKCM-UHFFFAOYSA-N CC(c1ccccc1)Nc1c(-c(cc2)ccc2N)nccn1 Chemical compound CC(c1ccccc1)Nc1c(-c(cc2)ccc2N)nccn1 JRKKMADZCUSKCM-UHFFFAOYSA-N 0.000 description 1
- LRVLJQUHFDTIOM-UHFFFAOYSA-O CCc(cccc1)c1-c1nccnc1-c(cc1)ccc1NC(Cc1ccc(C(C(C)=O)(F)[FH+])cc1)=O Chemical compound CCc(cccc1)c1-c1nccnc1-c(cc1)ccc1NC(Cc1ccc(C(C(C)=O)(F)[FH+])cc1)=O LRVLJQUHFDTIOM-UHFFFAOYSA-O 0.000 description 1
- GVWBPHVZYDHZIC-LJQANCHMSA-N CCc(cccc1)c1-c1nccnc1-c(cc1)ccc1NC(Cc1ccc(C([C@@H](C)O)(F)F)cc1)=O Chemical compound CCc(cccc1)c1-c1nccnc1-c(cc1)ccc1NC(Cc1ccc(C([C@@H](C)O)(F)F)cc1)=O GVWBPHVZYDHZIC-LJQANCHMSA-N 0.000 description 1
- QUWKGGLGFZEZFC-ZDUSSCGKSA-N C[C@@H](c1ccccc1)Oc1c(-c(cc2)ccc2[N+]([O-])=O)nccn1 Chemical compound C[C@@H](c1ccccc1)Oc1c(-c(cc2)ccc2[N+]([O-])=O)nccn1 QUWKGGLGFZEZFC-ZDUSSCGKSA-N 0.000 description 1
- PAZCIXSXNBHIAR-OCAPTIKFSA-N C[C@H](C1)O[C@@H](C)CN1c(nccn1)c1Cl Chemical compound C[C@H](C1)O[C@@H](C)CN1c(nccn1)c1Cl PAZCIXSXNBHIAR-OCAPTIKFSA-N 0.000 description 1
- CUBRZZYLOXCVDX-CYBMUJFWSA-N C[C@H](c1ccccc1)Oc1c(-c(cc2)ccc2N)nccn1 Chemical compound C[C@H](c1ccccc1)Oc1c(-c(cc2)ccc2N)nccn1 CUBRZZYLOXCVDX-CYBMUJFWSA-N 0.000 description 1
- YOUAHOATOIGQBC-UHFFFAOYSA-N Cc(cc1)cc(F)c1-c1c(-c(cc2)ccc2[N+]([O-])=O)nccn1 Chemical compound Cc(cc1)cc(F)c1-c1c(-c(cc2)ccc2[N+]([O-])=O)nccn1 YOUAHOATOIGQBC-UHFFFAOYSA-N 0.000 description 1
- OXQOBQJCDNLAPO-UHFFFAOYSA-O Cc1c(C)[nH+]ccn1 Chemical compound Cc1c(C)[nH+]ccn1 OXQOBQJCDNLAPO-UHFFFAOYSA-O 0.000 description 1
- JJQYJIVOKJBWCC-UHFFFAOYSA-N Cc1c(CCOc2c(C)nccn2)[s]cn1 Chemical compound Cc1c(CCOc2c(C)nccn2)[s]cn1 JJQYJIVOKJBWCC-UHFFFAOYSA-N 0.000 description 1
- WFCZXOVIIMDURM-UHFFFAOYSA-N Cc1c(NC(CO)c2ccccc2)nccn1 Chemical compound Cc1c(NC(CO)c2ccccc2)nccn1 WFCZXOVIIMDURM-UHFFFAOYSA-N 0.000 description 1
- MEYNOHOGQKIZTF-UHFFFAOYSA-N Fc(c(F)c1)ccc1-c(nccn1)c1Cl Chemical compound Fc(c(F)c1)ccc1-c(nccn1)c1Cl MEYNOHOGQKIZTF-UHFFFAOYSA-N 0.000 description 1
- WTKFVAIAKJEADU-LPEIPFDXSA-N N=C(C(F)(F)F)/C=C(/c(cccc1)c1Cl)\Nc(cc1)ccc1[N+]([O-])=O Chemical compound N=C(C(F)(F)F)/C=C(/c(cccc1)c1Cl)\Nc(cc1)ccc1[N+]([O-])=O WTKFVAIAKJEADU-LPEIPFDXSA-N 0.000 description 1
- YUKAYUILIHUSNJ-UHFFFAOYSA-N Nc(cc1)ccc1-c(nccc1)c1-c(cc1)ccc1Cl Chemical compound Nc(cc1)ccc1-c(nccc1)c1-c(cc1)ccc1Cl YUKAYUILIHUSNJ-UHFFFAOYSA-N 0.000 description 1
- YLIDLVYOBVFZBE-UHFFFAOYSA-N Nc(cc1)ccc1-c(nccc1)c1-c(cc1)ccc1F Chemical compound Nc(cc1)ccc1-c(nccc1)c1-c(cc1)ccc1F YLIDLVYOBVFZBE-UHFFFAOYSA-N 0.000 description 1
- VWOPHBPFLVPPPW-UHFFFAOYSA-N [O-][N+](c(cc1)ccc1-c1c(-c2ccncc2)nccn1)=O Chemical compound [O-][N+](c(cc1)ccc1-c1c(-c2ccncc2)nccn1)=O VWOPHBPFLVPPPW-UHFFFAOYSA-N 0.000 description 1
- ZOWCWTCXUNDANA-UHFFFAOYSA-N [O-][N+](c(cc1)ccc1-c1ccncc1-c(cc1)ccc1Cl)=O Chemical compound [O-][N+](c(cc1)ccc1-c1ccncc1-c(cc1)ccc1Cl)=O ZOWCWTCXUNDANA-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P23/00—Anaesthetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/36—Radicals substituted by singly-bound nitrogen atoms
- C07D213/40—Acylated substituent nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/12—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/26—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/34—One oxygen atom
- C07D239/36—One oxygen atom as doubly bound oxygen atom or as unsubstituted hydroxy radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/42—One nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/12—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/14—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D241/18—Oxygen or sulfur atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/14—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D241/20—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Rheumatology (AREA)
- Pulmonology (AREA)
- Pain & Pain Management (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Anesthesiology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Transplantation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pyridine Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
Description
本出願は、2015年8月3日出願のインド仮出願第2930/MUM/2015号の利益を請求し、これは、その全体が参照によって本明細書に組み込まれる。
本特許出願は、レチノイド関連オーファン受容体ガンマt(RORγt)モジュレータとして有用であり得る新規化合物を対象とする。
本出願は、RORγt受容体のモジュレータである化合物を対象とする。
またはその互変異性体、その立体異性体もしくはその薬学的に許容される塩に関する
[式中、
環Aは、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
Lは、存在しないか、またはy*−X−(CRxRy)t−*zであり;Xは、O、NRx1及び
x、y及びzのそれぞれは、結合点を表し;
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R3の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R5の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRa及びRbはそれぞれ、水素及びC1〜8アルキルから独立に選択され;
同じでも、または異なってもよいRx及びRyはそれぞれ、水素、C1〜8アルキル及びヒドロキシC1〜8アルキルから独立に選択されるか;またはRx及びRyは、それらが結合している炭素原子と一緒に、3〜6員シクロアルキル環を形成しており;
Rx1は、水素またはC1〜8アルキルから選択され;
「n」は、0、1、2または3であり;
「m」は、0、1、または2であり;
「p」は、0、1、または2であり;
「q」は、0、1、2または3であり、
「t」は、0、1、2または3である]。
環Aが、
環Bが、シクロヘキシル、フェニル、6−オキソ−1,6−ジヒドロピリジニル、ピペリジニル、ピペラジニル、モルホリニル、イソオキサゾリル、ピラゾリル、チアゾリル、ピリジニルまたはピリミジニルであり;
Lが、存在しないか、または
R1が、ヒドロキシル、メチルまたはメトキシであり;
R2が、シアノ、F、Cl、メチル、エチル、メトキシ、メトキシエチル、トリフルオロメチル、シクロプロピル、C(O)メチル、C(O)シクロプロピルまたはオキセタン−3−イルであり;
R3が、メチル、tert−ブチルまたはトリフルオロメチルであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「n」が、0、1または2であり;
「m」が、0または1であり;
「p」が、0または1であり;
「q」が、0である、式(I)の化合物を提供する。
Lが、存在しないか、または
R1が、ヒドロキシル、メチルまたはメトキシであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「p」が、0または1であり;
「q」が、0である、式(I)の化合物を提供する。
[式中、
環Aは、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
x及びyのそれぞれは、結合点を表し;
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R3の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRa及びRbはそれぞれ、水素及びC1〜8アルキルから独立に選択され;
「n」は、0、1、2または3であり;
「m」は、0、1または2であり;
「p」は、0、1または2である]。
環Aが、
環Bが、フェニル、6−オキソ−1,6−ジヒドロピリジニル、ピペリジニル、ピペラジニル、モルホリニル、ピラゾリル、ピリジニルまたはピリミジニルであり;
R1が、ヒドロキシル、メチルまたはメトキシであり;
R2が、シアノ、F、Cl、メチル、エチル、メトキシ、メトキシエチル、トリフルオロメチル、C(O)メチル、C(O)シクロプロピルまたはオキセタン−3−イルであり;
R3が、メチル、tert−ブチルまたはトリフルオロメチルであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「n」が、0、1または2であり;
「m」が、0または1であり;
「p」が、0または1である、式(II)の化合物を提供する。
R1が、ヒドロキシル、メチルまたはメトキシであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「p」が、0または1である、式(II)の化合物を提供する。
[式中、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
Xは、−O−、−NRx1−及び
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRa及びRbはそれぞれ、水素及びC1〜8アルキルから独立に選択され;
同じでも、または異なってもよいRx及びRyはそれぞれ、水素、C1〜8アルキル及びヒドロキシC1〜8アルキルから独立に選択されるか;またはRx及びRyは、それらが結合している炭素原子と一緒に、3〜6員シクロアルキル環を形成しており;
Rx1は、水素またはC1〜8アルキルから選択され;
「n」は、0、1、2または3であり;
「p」は、0、1または2であり;
「t」は、0、1、2または3である]。
環Bが、シクロヘキシル、フェニル、ピペラジニル、イソオキサゾリルまたはチアゾリルであり;
Xが、−O−、−NH−、−N(CH3)−または
R1が、ヒドロキシル、メチルまたはメトキシであり;
R2が、F、Cl、メチルまたはシクロプロピルであり;
R4が、Fであり;
Raが、水素であり;Rbが、水素またはメチルであり;
Rxが、水素であり;Ryが、水素、メチルまたはヒドロキシメチルであるか;またはRx及びRyが一緒に、シクロプロピル環を形成しており;
「n」が、0、1または2であり;
「p」が、0または1であり;
「t」が、0、1または2である、式(III)の化合物を提供する。
R1が、ヒドロキシル、メチルまたはメトキシであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「p」が、0または1である、式(III)の化合物を提供する。
「ハロゲン」または「ハロ」という用語は、フッ素(フルオロ)、塩素(クロロ)、臭素(ブロモ)、またはヨウ素(ヨード)を意味する。
本発明の化合物は典型的には、医薬組成物の形態で投与される。本明細書に記載の医薬組成物は、1つまたは複数の本明細書に記載の化合物及び1つまたは複数の薬学的に許容される添加剤を含む。典型的には、薬学的に許容される添加剤は、規制当局によって承認されているか、または一般に、ヒトまたは動物使用について安全であると考えられている。薬学的に許容される添加剤には、これらだけに限定されないが、担体、希釈剤、流動促進剤及び滑沢剤、防腐剤、緩衝剤、キレート化剤、ポリマー、ゲル化剤、増粘剤、溶媒などが包含される。
本発明の化合物は、レチノイド関連オーファン受容体ガンマ、殊にレチノイド関連オーファン受容体ガンマt(RORγt)の作用を阻害する、すなわち、RORγtの作用を防止、阻害、または抑制し、かつ/またはRORγt調節効果を誘発し得るので、殊に有用である。したがって、本発明の化合物は、RORガンマ活性、及び殊にRORγtの阻害が有利である状態の処置において有用である。
一般式(Ia)、(Ib)及び(II)のもの、中間体ならびに特定の例を包含する本明細書に記載の化合物は、スキーム1〜14において図示するとおりの合成方法によって調製される。さらに、具体的な酸、塩基、試薬、カップリング試薬、溶媒などが記載される次のスキームでは、他の適切な酸、塩基、試薬、カップリング試薬、溶媒などが使用されてもよく、かつそれらが本発明の範囲内に包含され得ることは理解される。反応条件、例えば、温度、反応時間、またはそれらの組合せの変更は、本発明の一部と想定される。この一般反応順序を使用して得られる化合物は、不十分な純度のものであることがある。これらの化合物は、当業者に公知の有機化合物を精製するための方法のいずれか、例えば、種々の溶媒が適切な比で使用される結晶化またはシリカゲルもしくはアルミナカラムクロマトグラフィーを使用して精製され得る。すべての考えられる幾何異性体及び立体異性体が、本発明の範囲内と想定される。
別段に述べない限り、後処理は、括弧内に示されている有機相と水相との間での反応混合物の分配、層の分離、及び硫酸ナトリウム上での有機層の乾燥、濾過、及び溶媒の蒸発を含む。精製は、別段に記載しない限り、一般に、移動相として適切な極性の酢酸エチル/石油エーテル混合物を使用するシリカゲルクロマトグラフィー技術による精製を包含する。異なる溶離液系の使用は、括弧内に示される。
中間体1
4−[3−(4−クロロフェニル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、2:1)中で、室温で、炭酸ナトリウム一水和物(513mg、4.14mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(50mg、0.06mmol)を使用して、ステップ1中間体(310mg、1.38mmol)を4−アミノフェニルボロン酸ピナコールエステル(302mg、1.38mmol)と反応させることによって、標題化合物を調製して、生成物270mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.42 (s, 2H), 6.46 (d, J=8.4 Hz, 2H), 7.09 (d, J=8.4 Hz, 2H), 7.38−7.47 (m, 4H), 8.51 (s, 1H), 8.57 (s, 1H); APCI−MS (m/z) 282 (M+H)+。
[4−(1,1−ジフルオロプロピル)フェニル]酢酸
ジクロロメタン(20mL)中のステップ3中間体(1.42g、5.25mmol)の撹拌溶液に0℃で、トリフルオロ酢酸(10mL)を添加し、混合物を1時間にわたって、室温で撹拌した。反応混合物中の溶媒を蒸発させ、得られた残渣をシリカゲルカラムクロマトグラフィーによって精製して、所望の生成物491mgを得た;1H NMR (300 MHz, DMSO−d6) δ 0.90 (t, J=6.0 Hz, 3H), 2.11−2.28 (m, 2H), 3.63 (s, 2H), 7.33 (d, J=8.4 Hz, 2H), 7.42 (d, J=8.4 Hz, 2H), 12.42 (br s, 1H); APCI−MS (m/z) 213 (M−H)−。
4−(1,1−ジフルオロ−2−オキソプロピル)フェニル]酢酸
中間体2のステップ4において記載した手順のとおりに、ジクロロメタン(10mL)中で、ステップ5中間体(501mg、1.76mmol)をトリフルオロ酢酸(10mL)と反応させることによって標題化合物を調製して、生成物379mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.36 (s, 3H), 3.66 (s, 2H), 7.43 (d, J=7.8 Hz, 2H), 7.52 (d, J=8.4 Hz, 2H), 12.22 (br s, 1H)。
4−[3−(3−クロロフェニル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO(15mL)及び水(5.0mL)の混合物中で、室温で、炭酸ナトリウム一水和物(412mg、3.33mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(36mg、0.05mmol)を使用して、ステップ1中間体(250mg、1.11mmol)を4−アミノフェニルボロン酸ピナコールエステル(243mg、1.11mmol)と反応させることによって、標題化合物を調製して、生成物273mgを得た。生成物を、特徴づけることなく、さらに使用した。
4−[3−(4−フルオロフェニル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、1,4−ジオキサン及び水の混合物(15mL、2:1)中で、80℃で、2M炭酸ナトリウム溶液(2.9mL、5.99mmol)を使用して、ビス(ジベンジリデン)アセトンパラジウム(0)(276mg、0.23mmol)の存在下で、ステップ1中間体(503mg、2.39mmol)を4−アミノフェニルボロン酸ピナコールエステル(787mg、3.59mmol)と反応させることによって、標題化合物を調製して、生成物321mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.38 (s, 2H), 6.44 (d, J=9.0 Hz, 2H), 7.06 (d, J=8.4 Hz, 2H), 7.17 (t, J=9.0 Hz, 2H), 7.44 (t, J=8.1 Hz, 2H), 7.46−7.61 (m, 2H)。
4−[3−(3,4−ジフルオロフェニル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(15mL、3:1)中で、室温で、炭酸ナトリウム一水和物(409mg、3.33mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(40mg、0.05mmol)を使用して、ステップ1中間体(250mg、1.10mmol)を4−アミノフェニルボロン酸ピナコールエステル(290mg、1.10mmol)と反応させることによって、標題化合物を調製して、生成物256mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.44 (s, 2H), 6.48 (d, J=8.4 Hz, 2H), 7.09 (d, J=8.4 Hz, 2H), 7.20−7.26 (m, 1H), 7.40−7.50 (m, 2H), 8.54 (s, 1H), 8.60 (s, 1H)。
4−[3−(4,4−ジフルオロピペリジン−1−イル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、テトラキス(トリフェニルホスフィン)パラジウム(0)(247mg、0.21mmol)の存在下で、1,4−ジオキサン及び水の混合物(10mL、2:1)中で、80℃で、炭酸ナトリウム一水和物(796mg、6.42mmol)を使用して、ステップ1中間体(500mg、2.14mmol)を4−アミノフェニルボロン酸ピナコールエステル(703mg、3.21mmol)と反応させることによって、標題化合物を調製して、生成物316mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.90−2.12 (m, 4H), 3.18−3.26 (m, 4H), 5.46 (s, 2H), 6.62 (d, J=8.4 Hz, 2H), 7.68 (d, J=8.1 Hz, 2H), 8.02 (d, J=1.8 Hz, 1H), 8.13 (d, J=2.4 Hz, 1H)。
4−[3−(モルホリン−4−イル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(15mL、3:1)中で、室温で、炭酸ナトリウム一水和物(879mg、7.09mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(86mg、0.11mmol)を使用して、ステップ1中間体(500mg、2.36mmol)を4−アミノフェニルボロン酸ピナコールエステル(518mg、2.36mmol)と反応させることによって、標題化合物を調製して、生成物150mgを得た;1H NMR (300 MHz, DMSO−d6) δ 3.05 (t, J=4.8 Hz, 4H), 3.63 (t, J=4.8 Hz, 4H), 5.45 (s, 2H), 6.62 (d, J=8.4 Hz, 2H), 7.68 (d, J=8.4 Hz, 1H), 8.02 (d, J=2.4 Hz, 1H), 8.11 (d, J=2.4 Hz, 1H)。
4−[1−tert−ブチル−5−(4−フルオロフェニル)−1H−ピラゾール−4−イル]アニリン
エタノール及び水の混合物(1:1、10mL)中のステップ3中間体(306mg、0.90mmol)及び塩化アンモニウム(482mg、9.01mmol)の懸濁液に70℃で、鉄粉(151mg、2.70mmol)を添加し、得られた混合物を100℃で1時間にわたって撹拌した。反応混合物を室温に冷却し、飽和NaHCO3水溶液に注ぎ入れ、酢酸エチル(50mL×2)で抽出した。有機層を十分に乾燥させ、濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーによって精製して、標題化合物210mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.35 (s, 9H), 4.89 (s, 2H), 6.31 (d, J=8.1 Hz, 2H), 6.66 (d, J=7.8 Hz, 2H), 7.24 (t, J=8.7 Hz, 2H), 7.38 (t, J=8.1 Hz, 2H), 7.54 (s, 1H)。
[4−(1,1−ジフルオロ−2−メトキシエチル)フェニル]酢酸
中間体3のステップ1において記載した手順のとおりに、DMSO(10mL)中で、銅粉末(903mg、14.2mmol)を使用して、1−ブロモ−4−ヨードベンゼン(1.0g、3.55mmol)をブロモジフルオロ酢酸エチル(1.43g、7.06mmol)と反応させることによって、標題化合物を調製して、生成物623mgを得た;1H NMR (300 MHz, CDCl3) δ 1.30 (t, J=7.2 Hz, 3H), 4.29 (q, J=7.2 Hz, 2H), 7.47 (d, J=8.4 Hz, 2H), 7.59 (d, J=8.4 Hz, 2H)。
エタノール(4.0mL)中のステップ1中間体(206mg、0.73mmol)の撹拌溶液に−10℃で、塩化カルシウム(25mg、0.22mmol)を、続いて、ホウ水素化ナトリウム(70mg、1.84mmol)を添加した。得られた混合物を室温で2時間にわたって撹拌した。反応混合物を飽和NaHCO3水溶液(10mL)でクエンチし、酢酸エチル(40mL×2)で抽出した。合わせた有機層をブライン(50mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。粗製の化合物をシリカゲルカラムクロマトグラフィーによって精製して、標題生成物176mgを得た;1H NMR (300 MHz, CDCl3) δ 3.95 (t, J=13.2 Hz, 2H), 7.40 (d, J=8.4 Hz, 2H), 7.58 (d, J=8.1 Hz, 2H)。
無水DMF(20mL)中のステップ2中間体(170mg、0.71mmol)の撹拌溶液に、水素化ナトリウム(60%w/w、37mg、0.93mmol)を0℃で添加した。15分後に、ヨウ化メチル(68μL、1.07mmol)を添加し、混合物を室温で2時間にわたって撹拌した。反応混合物を水(30mL)でクエンチし、酢酸エチル(2×50mL)で抽出した。合わせた有機層をブライン(100mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーによって精製して、標題生成物141mgを得た;1H NMR (300 MHz, CDCl3) δ 3.42 (s, 3H), 3.78 (t, J=12.6 Hz, 2H), 7.39 (d, J=8.1 Hz, 2H), 7.56 (d, J=8.4 Hz, 2H)。
中間体2のステップ3において記載した手順のとおりに、トルエン(10mL)中で、n−ブチルリチウム(1.51mL、2.41mmol)、トリ−tert−ブチルホスホニウムテトラフルオロボラート(58mg、0.20mmol)、ビス(ジベンジリデン)アセトンパラジウム(0)(58mg、0.10mmol)及びジシクロヘキシルアミン(782μL、2.41mmol)の存在下で、ステップ3中間体(506mg、2.01mmol)を酢酸tert−ブチル(272μL、2.01mmol)と反応させることによって、標題化合物を調製して、生成物398mgを得た;1H NMR (300 MHz, CDCl3) δ 1.44 (s, 9H), 3.43 (s, 3H), 3.55 (s, 3H), 3.79 (t, J=13.2 Hz, 2H), 7.36 (d, J=13.8 Hz, 2H), 7.46 (d, J=8.4 Hz, 2H); ESI−MS (m/z) 283 (M−H)−。
中間体2のステップ4において記載した手順のとおりに、ジクロロメタン(6.0mL)中で、ステップ4中間体(386mg、1.38mmol)をトリフルオロ酢酸(3.0mL)と反応させることによって、標題化合物を調製して、生成物161mgを得た;1H NMR (300 MHz, DMSO−d6) δ 3.31 (s, 3H), 3.62 (s, 2H), 3.86 (t, J=14.1 Hz, 2H), 7.35 (d, J=7.8 Hz, 2H), 7.46 (d, J=8.1 Hz, 2H), 12.41 (br s, 1H)。
4−[3−(2−クロロフェニル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、1:1)中で、鉄粉(75mg、1.34mmol)及び塩化アンモニウム(240mg、4.49mmol)を使用して、ステップ2中間体(140mg、0.44mmol)を還元することによって、標題化合物を調製して、生成物110mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.36 (s, 2H), 6.36 (d, J=7.8 Hz, 2H), 7.02 (d, J=8.4 Hz, 2H), 7.42 (br s, 4H), 8.53 (s, 1H), 8.65 (s, 1H)。
4−[3−(4−クロロ−2−フルオロフェニル)ピラジン−2−イル]アニリン
4−[3−(2,4−ジフルオロフェニル)ピラジン−2−イル]アニリン
4−[3−(4−クロロフェニル)ピリジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール(15mL)及び水(3.0mL)の混合物中で、鉄粉(198mg、3.54mmol)及び塩化アンモニウム(379mg、7.08mmol)を使用して、ステップ2中間体(220mg、0.70mmol)を還元することによって、標題化合物を調製して、生成物178mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.25 (br s, 2H), 6.41 (d, J=8.4 Hz, 2H), 6.97 (d, J=8.1 Hz, 2H), 7.21 (d, J=8.4 Hz, 2H), 7.30−7.41 (m, 3H), 7.70 (d, J=6.3 Hz, 1H), 8.58 (d, J=4.5 Hz, 1H)。
4−[3−(2−フルオロフェニル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、4:1)中で、鉄粉(177mg、3.16mmol)及び塩化アンモニウム(565mg、10.56mmol)を使用して、ステップ1中間体(312mg、1.05mmol)を還元することによって、標題化合物を調製して、生成物211mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.38 (s, 2H), 6.40 (d, J=8.4 Hz, 2H), 7.04−7.17 (m, 3H), 7.29 (t, J=7.2 Hz, 1H), 7.42−7.57 (m, 2H), 8.55 (s, 1H), 8.64 (d, J=2.1 Hz, 1H); APCI−MS (m/z) 266 (M+H)+。
4−{3−[4−(トリフルオロメチル)フェニル]ピラジン−2−イル}アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、4:1)中で、鉄粉(167mg、3.00mmol)及び塩化アンモニウム(536mg、10.02mmol)を使用して、ステップ1中間体(346mg、1.00mmol)を還元することによって、標題化合物を調製して、生成物241mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.42 (s, 2H), 6.44 (d, J=8.4 Hz, 2H), 7.05 (d, J=7.8 Hz, 2H), 7.62 (d, J=8.1 Hz, 2H), 7.71 (d, J=8.4 Hz, 2H), 8.56 (s, 1H), 8.61 (s, 1H); APCI−MS (m/z) 316 (M+H)+。
4−[3−(4−メチルフェニル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、4:1)中で、鉄粉(139mg、2.49mmol)及び塩化アンモニウム(445mg、8.32mmol)を使用して、ステップ1中間体(240mg、0.83mmol)を還元することによって、標題化合物を調製して、生成物176mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.31 (s, 3H), 5.37 (s, 2H), 6.44 (d, J=7.8 Hz, 2H), 7.08 (d, J=7.8 Hz, 2H), 7.14 (d, J=8.7 Hz, 2H), 7.31 (d, J=7.8 Hz, 2H), 8.51 (d, J=9.0 Hz, 2H)。
4−[3−(4−フルオロフェニル)ピリジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(218mg、3.91mmol)及び塩化アンモニウム(418mg、7.81mmol)を使用して、ステップ1中間体(230mg、0.78mmol)を還元することによって、標題化合物を調製して、生成物164mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.22 (s, 2H), 6.39 (d, J=8.7 Hz, 2H), 6.96 (d, J=7.8 Hz, 2H), 7.13−7.24 (m, 4H), 7.29−7.33 (m, 1H), 7.69 (d, J=7.2 Hz, 1H), 8.55 (s, 1H)。
4−(3−フェニルピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、4:1)中で、鉄粉(206mg、3.68mmol)及び塩化アンモニウム(657mg、12.29mmol)を使用して、ステップ1中間体(341mg、1.22mmol)を還元することによって、標題化合物を調製して、生成物219mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.39 (s, 2H), 6.44 (d, J=8.4 Hz, 2H), 7.08 (d, J=8.7 Hz, 2H), 7.33−7.42 (m, 5H), 8.52 (s, 1H), 8.57 (s, 1H)。
4−[3−(4−アミノフェニル)ピラジン−2−イル]ベンゾニトリル
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、3:1)中で、鉄粉(279mg、4.99mmol)及び塩化アンモニウム(890mg、16.64mmol)を使用して、ステップ2中間体(503mg、1.66mmol)を還元することによって、標題化合物を調製して、生成物313mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.42 (s, 2H), 6.45 (d, J=8.1 Hz, 2H), 7.06 (d, J=8.4 Hz, 2H), 7.59 (d, J=7.8 Hz, 2H), 7.80 (d, J=8.1 Hz, 2H), 8.55 (s, 1H), 8.62 (s, 1H)。
4−[3−(ピリジン−4−イル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(200mg、3.69mmol)及び塩化アンモニウム(384mg、7.18mmol)を使用して、ステップ1中間体(200mg、0.71mmol)を還元することによって、標題化合物を調製して、生成物132mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.48 (s, 2H), 6.47 (d, J=8.1 Hz, 2H), 7.09 (d, J=8.1 Hz, 2H), 7.40 (d, J=5.7 Hz, 2H), 8.54−8.65 (m, 4H)。
4−[5−(4−フルオロフェニル)−3−メチル−1H−ピラゾール−1−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、4:1)中で、鉄粉(125mg、2.23mmol)及び塩化アンモニウム(408mg、7.43mmol)を使用して、ステップ2中間体(221mg、0.74mmol)を還元することによって、標題化合物を調製して、生成物151mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.20 (s, 3H), 5.27 (s, 2H), 6.33 (s, 1H), 6.48 (d, J=9.0 Hz, 2H), 6.82 (d, J=9.0 Hz, 2H), 7.10−7.21 (m, 4H); ESI−MS (m/z) 268 (M+H)+。
4−[3−(1−メチル−1H−ピラゾール−4−イル)ピラジン−2−イル]アニリン
中間体1のステップ1において記載した手順のとおりに、1,4ジオキサン(2.3mL)中で、90℃で、2M炭酸ナトリウム溶液(1.2mL、2.31mmol)及びテトラキス(トリフェニルホスフィン)パラジウム(0)(89mg、0.07mmol)を使用して、ステップ1中間体(150mg、0.77mmol)を4−アミノフェニルボロン酸ピナコールエステル(203mg、0.92mmol)と反応させることによって、標題化合物を調製して、生成物86mgを得た;1H NMR (300 MHz, DMSO−d6) δ 3.78 (s, 3H), 5.43 (s, 2H), 6.60 (d, J=8.4 Hz, 2H), 7.17 (t, J=8.1 Hz, 3H), 7.74 (s, 1H), 8.41 (d, J=9.3 Hz, 2H)。
1−{4−[3−(4−アミノフェニル)ピラジン−2−イル]ピペラジン−1−イル}エタノン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(85mg、1.52mmol)及び塩化アンモニウム(163mg、3.05mmol)を使用して、ステップ2中間体(100mg、0.30mmol)を還元することによって、標題化合物を調製して、生成物87mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.98 (s, 3H), 3.06 (br s, 4H), 3.47 (br s, 4H), 5.46 (s, 2H), 6.62 (d, J=8.4 Hz, 2H), 7.70 (d, J=8.4 Hz, 2H), 8.03 (s, 1H), 8.12 (s, 1H); ESI−MS (m/z) 298 (M+H)+。
5−[3−(4−アミノフェニル)ピラジン−2−イル]−1−メチルピリジン−2(1H)−オン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(145mg、2.59mmol)及び塩化アンモニウム(278mg、5.19mmol)を使用して、ステップ2中間体(160mg、0.51mmol)を還元することによって、標題化合物を調製して、生成物93mgを得た;1H NMR (300 MHz, CDCl3) δ 3.44−3.58 (m, 3H), 6.38−6.42 (m, 1H), 7.04 (d, J=7.5 Hz, 1H), 7.14 (d, J=8.7 Hz, 1H), 7.26 (s, 1H), 7.42 (d, J=8.1 Hz, 2H), 7.50−7.53 (m, 1H), 7.78 (br s, 1H), 8.45−8.56 (m, 2H)。
4−[3−(4−クロロフェニル)ピラジン−2−イル]−2−フルオロアニリン
4−[3−(4−メトキシフェニル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、3:1)中で、鉄粉(151mg、2.70mmol)及び塩化アンモニウム(482mg、9.13mmol)を使用して、ステップ1中間体(277mg、0.90mmol)を還元することによって、標題化合物を調製して、生成物199mgを得た;1H NMR (300 MHz, DMSO−d6) δ δ 3.76 (s, 3H), 5.37 (s, 2H), 6.45 (d, J=8.7 Hz, 2H), 6.89 (d, J=8.1 Hz, 2H), 7.10 (d, J=8.1 Hz, 2H), 7.37 (d, J=8.7 Hz, 2H), 8.49 (d, J=10.2 Hz, 2H)。
4−[5−(4−フルオロフェニル)−3−(トリフルオロメチル)−1H−ピラゾール−1−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、3:1)中で、鉄粉(266mg、4.77mmol)及び塩化アンモニウム(850mg、15.90mmol)を使用して、ステップ2中間体(511mg、1.59mmol)を還元することによって、標題化合物を調製して、生成物314mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.48 (s, 2H), 6.53 (d, J=8.4Hz, 2H), 6.95 (d, J=8.7 Hz, 2H), 7.10 (s, 1H), 7.21−7.26 (m, 2H), 7.30−7.33 (m, 2H)。
4−[5−(2−クロロフェニル)−3−(トリフルオロメチル)−1H−ピラゾール−1−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、3:1)中で、鉄粉(323mg、5.79mmol)及び塩化アンモニウム(1.33g、19.32mmol)を使用して、ステップ2中間体(709mg、1.93mmol)を還元することによって、標題化合物を調製して、生成物412mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.38 (s, 2H), 6.44 (d, J=8.7 Hz, 2H), 6.88 (d, J=8.7 Hz, 2H), 7.03 (s, 1H), 7.40−7.51 (m, 4H); APCI−MS (m/z) 338 (M+H)+。
4−[3−(2−クロロフェニル)ピリジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、3:1)中で、鉄粉(165mg、2.96mmol)及び塩化アンモニウム(316mg、5.92mmol)を使用して、ステップ1中間体(184mg、0.59mmol)を還元することによって、標題化合物を調製して、生成物127mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.17 (s, 2H), 6.31 (d, J=8.4 Hz, 2H), 6.94 (d, J=7.8 Hz, 2H), 7.23−7.32 (m, 4H), 7.40−7.43 (m, 1H), 7.60 (d, J=7.5 Hz, 1H), 8.58 (s, 1H)。
4−[3−(2−メチルフェニル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、1:1)中で、鉄粉(128mg、2.29mmol)及び塩化アンモニウム(410mg、7.65mmol)を使用して、ステップ1中間体(223mg、0.76mmol)を還元することによって、標題化合物を調製して、生成物153mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.89 (s, 3H), 5.36 (s, 2H), 6.36 (d, J=8.4 Hz, 2H), 7.03 (d, J=8.1 Hz, 2H), 7.20−7.27 (m, 4H), 8.52 (s, 1H), 8.61 (s, 1H); APCI−MS (m/z) 262 (M+H)+。
4−[3−(4−メチルピペラジン−1−イル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(186mg、3.34mmol)及び塩化アンモニウム(358mg、6.68mmol)を使用して、ステップ2中間体(200mg、0.66mmol)を還元することによって、標題化合物を調製して、生成物129mgを得た;1H NMR (300 MHz, CDCl3) δ 2.41 (s, 4H), 2.60 (s, 4H), 3.34 (s, 3H), 3.85 (br s, 2H), 6.73 (d, J=8.7 Hz, 2H), 7.74 (d, J=7.8 Hz, 2H), 8.01 (s, 1H), 8.12 (s, 1H); APCI−MS (m/z) 270 (M+H)+。
4−[3−(4−エチルピペラジン−1−イル)ピラジン−2−イル]アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(169mg、3.03mmol)及び塩化アンモニウム(324mg、6.06mmol)を使用して、ステップ2中間体(190mg、0.60mmol)を還元することによって、標題化合物を調製して、生成物108mgを得た;1H NMR (300 MHz, CDCl3) δ 1.13 (t, J=6.9 Hz, 3H), 2.48−2.57 (m, 6H), 3.30 (s, 4H), 3.83 (br s, 2H), 6.72 (d, J=7.8 Hz, 2H), 7.73 (d, J=8.4 Hz, 2H), 7.98 (s, 1H), 8.09 (s, 1H); APCI−MS (m/z) 285 (M+H)+。
4−(2−(4−クロロフェニル)ピリジン−3−イル)アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、室温で、炭酸ナトリウム(238mg、2.27mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(28mg、0.04mmol)を使用して、ステップ1中間体(203mg、0.76mmol)を4−アミノフェニルボロン酸ピナコールエステル(264mg、0.91mmol)と反応させることによって、標題化合物を調製して、生成物137mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.20 (s, 2H), 6.48 (d, J=8.1 Hz, 2H), 7.81 (d, J=8.1 Hz, 2H), 7.32 (s, 4H), 7.38−7.42 (m, 1H), 7.72 (d, J=7.2 Hz, 1H), 8.56 (s, 1H); APCI−MS (m/z) 281 (M+H)+。
4−(4−(4−クロロフェニル)ピリジン−3−イル)アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、室温で、炭酸ナトリウム(294mg、2.80mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(34mg、0.05mmol)を使用して、ステップ1中間体(251mg、0.93mmol)を4−アミノフェニルボロン酸ピナコールエステル(326mg、1.12mmol)と反応させることによって、標題化合物を調製して、生成物123mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.20 (s, 2H), 6.47 (d, J=8.4 Hz, 2H), 6.79 (d, J=7.8 Hz, 2H), 7.20 (t, J=8.4 Hz, 2H), 7.33−7.41 (m, 3H), 8.51 (s, 2H)。
4−(3−((2S,6R)−2,6−ジメチルモルホリノ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(190mg、3.42mmol)及び塩化アンモニウム(366mg、6.84mmol)を使用して、ステップ2中間体(215mg、0.68mmol)を還元することによって、標題化合物を調製して、生成物137mgを得た;1H NMR (300 MHz, CDCl3) δ 1.11 (d, J=6.3 Hz, 6H), 2.45 (t, J=12.3 Hz, 2H), 3.48 (d, J=12.3 Hz, 4H), 3.68 (br s, 2H), 6.85 (d, J=7.8 Hz, 2H), 7.80 (d, J=7.8 Hz, 2H), 8.03 (s, 1H), 8.11 (s, 1H); APCI−MS (m/z) 285 (M+H)+。
4−(5−(2,4−ジクロロフェニル)−3−メチル−1H−ピラゾール−1−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、4:1)中で、鉄粉(238mg、4.27mmol)及び塩化アンモニウム(761mg、714.2mmol)を使用して、ステップ2中間体(496mg、1.42mmol)を還元することによって、標題化合物を調製して、生成物210mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.25 (s, 3H), 5.21 (s, 2H), 6.30 (s, 1H), 6.43 (d, J=8.7 Hz, 2H), 6.79 (d, J=8.7 Hz, 2H), 7.32 (d, J=7.8 Hz, 1H), 7.38−7.43 (m, 1H), 7.67 (d, J=9.9 Hz, 1H); ESI−MS (m/z) 318 (M+H)+。
4−(3−(2−クロロ−4−フルオロフェニル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(50mL、5:1)中で、鉄粉(559mg、10.0mmol)及び塩化アンモニウム(1.8g、33.36mmol)を使用して、ステップ1中間体(1.1g、3.34mmol)を還元することによって、標題化合物を調製して、生成物732mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.40 (s, 2H), 6.42 (d, J=8.4 Hz, 2H), 7.03 (d, J=8.4 Hz, 2H), 7.33 (t, J=5.7 Hz, 1H), 7.43−7.53 (m, 2H), 8.54 (s, 1H), 8.67 (s, 1H)。
4−(3−(2−エチルフェニル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(60mL、5:1)中で、鉄粉(658mg、11.8mmol)及び塩化アンモニウム(2.1g、39.3mmol)を使用して、ステップ1中間体(1.2g、3.93mmol)を還元することによって、標題化合物を調製して、生成物790mgを得た;1H NMR (300 MHz, DMSO−d6) δ 0.84 (t, J=7.5 Hz, 3H), 2.26 (q, J=7.5 Hz, 2H), 5.35 (s, 2H), 6.36 (d, J=7.8 Hz, 2H), 7.05 (d, J=8.4 Hz, 2H), 7.17−7.34 (m, 4H), 8.51 (s, 1H), 8.61 (s, 1H); APCI−MS (m/z) 276 (M+H)+。
4−(3−(4−(2−メトキシエチル)ピペラジン−1−イル)ピラジン−2−イル)アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(12mL、3:1)中で、炭酸カリウム(161mg、1.17mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II).ジクロロメタン複合体(16mg、0.02mmol)を使用して、ステップ1中間体(100mg、0.39mmol)を4−アミノフェニルボロン酸ピナコールエステル(102mg、0.46mmol)と反応させることによって、標題化合物を調製して、生成物98mgを得た;1H NMR (300 MHz, CDCl3) δ 2.19−2.23 (m, 2H), 2.64−2.72 (m, 6H), 3.32−3.36 (m, 7H), 3.60 (br s, 2H), 6.74 (d, J=8.4 Hz, 2H), 7.75 (d, J=8.4 Hz, 2H), 7.99 (s, 1H), 8.10 (s, 1H)。
1−(4−(3−(4−アミノフェニル)ピラジン−2−イル)−3−メチルピペラジン−1−イル)エタノン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(164mg、2.93mmol)及び塩化アンモニウム(313mg、5.86mmol)を使用して、ステップ2中間体(200mg、0.59mmol)を還元することによって、標題化合物を調製して、生成物147mgを得た;1H NMR (300 MHz, CDCl3) δ 0.96, 1.02 (d, J=6.3 Hz, 3H,回転異性体), 2.04, 2.10 (s, 3H,回転異性体), 2.92−2.96 (m, 2H), 3.07−3.15 (m, 2H), 3.28−3.39 (m, 2H), 3.65−3.72 (m, 1H), 3.82−4.09 (m, 2H), 6.85 (d, J=7.8 Hz, 2H), 7.78 (d, J=5.4 Hz, 2H), 8.04 (s, 1H), 8.13 (s, 1H); APCI−MS (m/z) 312 (M+H)+。
4−(3−(ピリミジン−5−イル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(150mg、2.69mmol)及び塩化アンモニウム(287mg、5.37mmol)を使用して、ステップ2中間体(150mg、0.54mmol)を還元することによって、標題化合物を調製して、生成物97mgを得た;1H NMR (300 MHz, CDCl3) δ 3.23 (br s, 2H), 6.71 (d, J=7.8 Hz, 2H), 7.25 (d, J=7.2 Hz, 2H), 8.60 (d, J=12.9 Hz, 2H), 8.85 (s, 2H), 9.15 (s, 1H); APCI−MS (m/z) 250 (M+H)+。
4−(3−(4−フルオロ−2−メチルフェニル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(194mg、3.47mmol)及び塩化アンモニウム(372mg、6.95mmol)を使用して、ステップ1中間体(215mg、0.69mmol)を還元することによって、標題化合物を調製して、生成物163mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.90 (s, 3H), 5.38 (s, 2H), 6.40 (d, J=8.4 Hz, 2H), 7.00−7.10 (m, 4H), 7.21−7.26 (m, 1H), 8.53 (s 1H), 8.63 (s, 1H); ESI−MS (m/z) 280 (M+H)+。
4−(3−(4−クロロフェニル)ピリジン−4−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、3:1)中で、鉄粉(119mg、2.13mmol)及び塩化アンモニウム(380mg、7.11mmol)を使用して、ステップ2中間体(221mg、0.71mmol)を還元することによって、標題化合物を調製して、生成物113mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.28 (s, 2H), 6.43 (d, J=8.1 Hz, 2H), 6.79 (d, J=8.1 Hz, 2H), 7.16 (d, J=8.4 Hz, 2H), 7.31−7.38 (m, 3H), 8.42 (s, 1H), 8.49 (d, J=5.4 Hz, 1H); APCI−MS (m/z) 281 (M+H)+。
4−(3−(2,4−ジメチルフェニル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(24mL、5:1)中で、鉄粉(265mg、4.75mmol)及び塩化アンモニウム(508mg、9.5mmol)を使用して、ステップ1中間体(290mg、0.95mmol)を還元することによって、標題化合物を調製して、生成物243mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.92 (s, 3H), 2.33 (s, 3H), 3.75 (br s, 2H), 6.53 (d, J=8.1 Hz, 2H), 6.96 (s, 1H), 7.02 (d, J=8.1 Hz, 1H), 7.15 (d, J=7.8 Hz, 1H), 7.20−7.27 (m, 2H), 8.49 (s, 1H), 8.55 (s, 1H); APCI−MS (m/z) 276 (M+H)+。
4−(3−(2−フルオロ−4−メチルフェニル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(262mg、4.69mmol)及び塩化アンモニウム(501mg、9.38mmol)を使用して、ステップ1中間体(290mg、0.94mmol)を還元することによって、標題化合物を調製して、生成物163mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.34 (s, 3H), 5.36 (s, 2H), 6.42 (d, J=8.1 Hz, 2H), 6.96 (d, J=11.1 Hz, 1H), 7.05−7.10 (m, 3H), 7.41 (t, J=7.8 Hz, 1H), 8.53 (s, 1H), 8.61 (s, 1H); ESI−MS (m/z) 280 (M+H)+。
2−(4−アミノフェニル)−3−(2−クロロ−4−フルオロフェニル)ピリミジン−4(3H)−オン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(73mg、1.30mmol)及び塩化アンモニウム(234mg、4.37mmol)を使用して、ステップ2中間体(151mg、0.44mmol)を還元することによって、標題化合物を調製して、生成物102mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.59 (s, 2H), 6.34 (d, J=7.2 Hz, 2H), 6.43 (d, J=6.3 Hz, 1H), 6.99 (d, J=8.4 Hz, 2H), 7.28−7.32 (m, 1H), 7.50−7.63 (m, 2H), 8.05 (d, J=6.3 Hz, 1H); APCI−MS (m/z) 316 (M+H)+。
4−(3−(2,4−ジクロロフェニル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(177mg、3.18mmol)及び塩化アンモニウム(339mg、6.36mmol)を使用して、ステップ1中間体(220mg、0.64mmol)を還元することによって、標題化合物を調製して、生成物162mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.41 (s, 2H), 6.42 (d, J=8.7 Hz, 2H), 7.03 (d, J=7.8 Hz, 2H), 7.51 (s, 2H), 7.64 (s, 1H), 8.55 (s, 1H), 8.68 (s, 1H); APCI−MS (m/z) 316 (M+H)+。
(4−(3−(4−アミノフェニル)ピラジン−2−イル)ピペラジン−1−イル)(シクロプロピル)メタノン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(16mL、3:1)中で、炭酸カリウム(389mg、2.81mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II).ジクロロメタン複合体(77mg、0.09mmol)を使用して、ステップ1中間体(250mg、0.93mmol)を4−アミノフェニルボロン酸ピナコールエステル(246mg、1.13mmol)と反応させることによって、標題化合物を調製して、生成物198mgを得た;1H NMR (300 MHz, DMSO−d6) δ 0.68−0.72 (m, 4H), 1.95−1.99 (m, 1H), 3.07−3.12 (m, 4H), 3.51−3.55 (m, 2H), 3.70−3.74 (m, 2H), 5.46 (s, 2H), 6.62 (d, J=6.9 Hz, 2H), 7.71 (d, J=6.9 Hz, 2H), 8.02 (s, 1H), 8.12 (s, 1H); APCI−MS (m/z) 324 (M+H)+。
3−(4−アミノフェニル)−N−(4−クロロフェニル)−N−メチルピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、炭酸ナトリウム(254mg、2.39mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(59mg、0.08mmol)を使用して、ステップ2中間体(203mg、0.78mmol)を4−アミノフェニルボロン酸(280mg、0.96mmol)と反応させることによって、標題化合物を調製して、生成物143mgを得た;1H NMR (300 MHz, DMSO−d6) δ 3.22 (s, 3H), 5.40 (br s, 2H), 6.43 (d, J=8.1 Hz, 2H), 6.70 (d, J=8.4 Hz, 2H), 7.10 (d, J=8.7 Hz, 2H), 7.40 (d, J=8.4 Hz, 2H), 8.23 (s, 1H), 8.38 (s, 1H); APCI−MS (m/z) 311 (M+H)+。
3−(4−アミノフェニル)−N−ベンジル−N−メチルピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、3:1)中で、炭酸ナトリウム(452mg、4.27mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(52mg、0.07mmol)を使用して、ステップ2中間体(333mg、1.42mmol)を4−アミノフェニルボロン酸ピナコールエステル(498mg、1.71mmol)と反応させることによって、標題化合物を調製して、生成物270mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.59 (s, 3H), 4.38 (s, 2H), 5.41 (s, 2H), 6.60 (d, J=8.4 Hz, 2H), 7.10 (d, J=7.2 Hz, 2H), 7.22−7.28 (m, 3H), 7.53 (d, J=8.1 Hz, 2H), 7.96 (s, 1H), 8.03 (s, 1H)。
3−(4−アミノフェニル)−N−ベンジルピラジン−2−アミン
3−(4−アミノフェニル)−N−(1−フェニルエチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、炭酸ナトリウム(280mg、2.64mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(63mg、0.08mmol)を使用して、ステップ1中間体(206mg、0.88mmol)を4−アミノフェニルボロン酸ピナコールエステル(308mg、1.06mmol)と反応させることによって、標題化合物を調製して、生成物105mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.44 (d, J=5.4 Hz, 3H), 5.11−5.12 (m, 1H), 5.55 (s, 2H), 6.06−6.10 (m, 1H), 6.67 (d, J=7.8 Hz, 2H), 7.19−7.41 (m, 6H), 7.72 (s, 1H), 7.77 (s, 1H)。
(R)−3−(4−アミノフェニル)−N−(1−フェニルエチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、炭酸ナトリウム(370mg、3.49mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(71mg、0.09mmol)を使用して、ステップ1中間体(232mg、0.99mmol)を4−アミノフェニルボロン酸ピナコールエステル(435mg、1.49mmol)と反応させることによって、標題化合物を調製して、生成物210mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.45 (d, J=6.6 Hz, 3H), 5.12−5.18 (m, 1H), 5.46 (s, 2H), 6.09 (d, J=6.9 Hz, 1H), 6.67 (d, J=8.1 Hz, 2H), 7.18 (d, J=7.2 Hz, 1H), 7.28 (t, J=7.2 Hz, 2H), 7.34−7.44 (m, 4H), 7.72 (s, 1H), 7.77 (s, 1H); APCI−MS (m/z) 291 (M+H)+。
(R)−3−(4−アミノフェニル)−N−メチル−N−(1−フェニルエチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、3:1)中で、炭酸ナトリウム(388mg、3.65mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(44mg、0.06mmol)を使用して、ステップ2中間体(302mg、1.22mmol)を4−アミノフェニルボロン酸ピナコールエステル(530mg、1.82mmol)と反応させることによって、標題化合物を調製して、生成物183mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.42 (d, J=6.9 Hz, 3H), 2.38 (s, 3H), 5.22−5.26 (m, 1H), 5.36 (s, 2H), 6.60 (d, J=8.4 Hz, 2H), 7.12 (d, J=5.7 Hz, 2H), 7.19−7.28 (m, 3H), 7.48 (d, J=8.4 Hz, 2H), 7.95 (s, 1H), 8.02 (s, 1H); APCI−MS (m/z) 305 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−フェニルエチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、炭酸ナトリウム(340mg、3.20mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(38mg、0.05mmol)を使用して、ステップ1中間体(250mg、1.07mmol)を4−アミノフェニルボロン酸ピナコールエステル(374mg、1.28mmol)と反応させることによって、標題化合物を調製して、生成物190mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.45 (d, J=6.6 Hz, 3H), 5.12−5.16 (m, 1H), 5.45 (s, 2H), 6.12 (d, J=6.9 Hz, 1H), 6.67 (d, J=8.7 Hz, 2H), 7.19 (d, J=7.8 Hz, 1H), 7.28 (t, J=8.7 Hz, 2H), 7.35−7.44 (m, 3H), 7.72 (s, 1H), 7.78 (s, 1H); APCI−MS (m/z) 291 (M+H)+。
(S)−3−(4−アミノフェニル)−N−メチル−N−(1−フェニルエチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、3:1)中で、炭酸ナトリウム(388mg、3.65mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(44mg、0.06mmol)を使用して、ステップ2中間体(302mg、1.22mmol)を4−アミノフェニルボロン酸ピナコールエステル(425mg、1.46mmol)と反応させることによって、標題化合物を調製して、生成物230mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.42 (d, J=6.9 Hz, 3H), 2.38 (s, 3H), 5.22−5.28 (m, 1H), 5.37 (s, 2H), 6.60 (d, J=8.1 Hz, 2H), 7.12 (d, J=6.9 Hz, 2H), 7.20−7.28 (m, 3H), 7.50 (d, J=8.4 Hz, 2H), 7.95 (s, 1H), 8.02 (s, 1H); ESI−MS (m/z) 305 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−(4−クロロフェニル)エチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(10mL、4:1)中で、炭酸ナトリウム(300mg、2.83mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(67mg、0.09mmol)を使用して、ステップ1中間体(253mg、0.94mmol)を4−アミノフェニルボロン酸ピナコールエステル(330mg、1.13mmol)と反応させることによって、標題化合物を調製して、生成物162mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.43 (d, J=6.9 Hz, 3H), 5.08−5.12 (m, 1H), 5.45 (s, 2H), 6.24 (d, J=6.9 Hz, 1H), 6.65 (d, J=8.4 Hz, 2H), 7.18 (d, J=7.8 Hz, 1H), 7.32 (d, J=8.7 Hz, 2H), 7.43 (d, J=8.7 Hz, 2H), 7.73 (d, J=7.5 Hz, 2H), 8.31 (s, 1H); APCI−MS (m/z) 325 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−(3−クロロフェニル)エチル)ピラジン−2−アミン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(48mg、0.85mmol)及び塩化アンモニウム(152mg、2.85mmol)を使用して、ステップ1中間体(101mg、0.28mmol)を還元することによって、標題化合物を調製して、生成物79mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.42 (d, J=6.6 Hz, 3H), 5.08−5.12 (m, 1H), 5.44 (s, 2H), 6.28−6.33 (m, 1H), 6.65−7.69 (m, 2H), 7.21−7.32 (m, 3H), 7.41−7.45 (m, 3H), 7.74 (d, J=7.8 Hz, 2H)。
(S)−3−(4−アミノフェニル)−N−(1−(4−クロロフェニル)エチル)−N−メチルピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO(10mL)中で、炭酸ナトリウム(381mg、3.60mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(43mg、0.06mmol)を使用して、ステップ1中間体(341mg、1.20mmol)を4−アミノフェニルボロン酸ピナコールエステル(422mg、1.45mmol)と反応させることによって、標題化合物を調製して、生成物162mgを得た 1H NMR (300 MHz, DMSO−d6) δ 1.40 (d, J=6.9 Hz, 3H), 2.36 (s, 3H), 5.25−5.28 (m, 1H), 5.36 (s, 2H), 6.58 (d, J=7.8 Hz, 2H), 7.14 (d, J=7.8 Hz, 2H), 7.32 (d, J=7.8 Hz, 2H), 7.46 (d, J=7.8 Hz, 2H), 7.95 (s, 1H), 8.02 (s, 1H); APCI−MS (m/z) 338 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−(2−クロロフェニル)エチル)ピラジン−2−アミン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(90mg、1.62mmol)及び塩化アンモニウム(290mg、5.41mmol)を使用して、ステップ1中間体(192mg、0.54mmol)を還元することによって、標題化合物を調製して、生成物140mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.43 (d, J=6.9 Hz, 3H), 5.37−5.45 (m, 1H), 5.47 (s, 2H), 6.33 (d, J=6.9 Hz, 1H), 6.68 (d, J=8.4 Hz, 2H), 7.19−7.26 (m, 2H), 7.38 (d, J=7.8 Hz, 2H), 7.46 (d, J=8.4 Hz, 2H), 7.73 (d, J=5.1 Hz, 2H); APCI−MS (m/z) 325 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−(4−フルオロ−2−メチルフェニル)エチル)ピラジン−2−アミン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(86mg、1.54mmol)及び塩化アンモニウム(275mg、5.14mmol)を使用して、ステップ1中間体(181mg、0.51mmol)を還元することによって、標題化合物を調製して、生成物130mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.37 (d, J=6.6 Hz, 3H), 2.38 (s, 3H), 5.18−5.22 (m, 1H), 5.47 (s, 2H), 6.16 (d, J=7.8 Hz, 1H), 6.64 (d, J=8.4 Hz, 2H), 6.91−6.95 (m, 2H), 7.39 (d, J=8.1 Hz, 3H), 7.69 (s, 1H), 7.75 (s, 1H); APCI−MS (m/z) 323 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−(2,4−ジメチルフェニル)エチル)ピラジン−2−アミン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(100mg、1.80mmol)及び塩化アンモニウム(320mg、5.99mmol)を使用して、ステップ1中間体(209mg、0.60mmol)を還元することによって、標題化合物を調製して、生成物140mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.37 (d, J=6.6 Hz, 3H), 2.19 (s, 3H), 2.33 (s, 3H), 5.20−5.24 (m, 1H), 5.56 (br s, 2H), 5.97−6.02 (m, 1H), 6.67 (d, J=8.4 Hz, 2H), 6.92 (s, 2H), 7.23 (d, J=7.8 Hz, 1H), 7.38 (d, J=8.1 Hz, 2H), 7.70 (s, 1H), 7.78 (s, 1H); APCI−MS (m/z) 319 (M+H)+。
(S)−3−(4−アミノフェニル)−N−(1−(2−クロロ−4−フルオロフェニル)エチル)ピラジン−2−アミン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(44mg、0.79mmol)及び塩化アンモニウム(140mg、2.63mmol)を使用して、ステップ1中間体(98mg、0.26mmol)を還元することによって、標題化合物を調製して、生成物62mgを得た。生成物をそのまま、特徴づけることなく、次のステップに入れた。
3−(4−アミノフェニル)−N−(シクロヘキシルメチル)ピラジン−2−アミン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(62mg、1.10mmol)及び塩化アンモニウム(197mg、3.68mmol)を使用して、ステップ1中間体(115mg、0.37mmol)を還元することによって、標題化合物を調製して、生成物84mgを得た;1H NMR (300 MHz, DMSO−d6) δ 0.88−0.93 (m, 3H), 1.12−1.18 (m, 3H), 1.60−1.76 (m, 5H), 3.12 (t, J=5.7 Hz, 2H), 5.42 (s, 2H), 6.02−6.06 (m, 1H), 6.64 (d, J=8.4 Hz, 2H), 7.33 (d, J=9.0 Hz, 2H), 7.69 (s, 1H), 7.82 (s, 1H); ESI−MS (m/z) 283 (M+H)+。
(S)−3−(4−アミノ−3−フルオロフェニル)−N−(1−(2−クロロフェニル)エチル)ピラジン−2−アミン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(8.0mL、3:1)中で、炭酸ナトリウム(180mg、1.69mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(46mg、0.06mmol)を使用して、ステップ1中間体(151mg、0.56mmol)を4−アミノ−3−フルオロフェニルボロン酸ピナコールエステル(160mg、0.68mmol)と反応させることによって、標題化合物を調製して、生成物159mgを得た;1H NMR (300 MHz DMSO−d6) δ 1.43 (d, J=6.6 Hz, 3H), 3.94 (s, 1H), 5.38−5.42 (m, 1H), 5.51 (s, 2H), 6.60 (d, J=6.6 Hz, 1H), 6.83−6.91 (m, 1H), 7.19−7.25 (m, 2H), 7.36−7.41 (m, 2H), 7.46 (d, J=5.7 Hz, 1H), 7.72−7.78 (m, 2H); ESI−MS (m/z) 343 (M+H)+。
(S)−3−(4−アミノ−2−フルオロフェニル)−N−(1−(2−クロロフェニル)エチル)ピラジン−2−アミン
4−(3−(ベンジルオキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(49mg、0.87mmol)及び塩化アンモニウム(155mg、2.89mmol)を使用して、ステップ1中間体(89mg、0.29mmol)を還元することによって、標題化合物を調製して、生成物72mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.46 (s, 2H), 5.53 (s, 2H), 6.58 (d, J=8.1 Hz, 2H), 7.36−7.41 (m, 3H), 7.43−7.48 (m, 2H), 7.85 (d, J=8.4 Hz, 2H), 8.01 (s, 1H), 8.20 (s, 1H); APCI−MS (m/z) 278 (M+H)+。
4−(3−(1−フェニルエトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(99mg、1.76mmol)及び塩化アンモニウム(315mg、5.88mmol)を使用して、ステップ1中間体(189mg、0.59mmol)を還元することによって、標題化合物を調製して、生成物141mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.63 (d, J=6.3 Hz, 3H), 5.67 (br s, 2H), 6.25 (d, J=6.3 Hz, 1H), 6.64 (d, J=8.7 Hz, 2H), 7.24−7.43 (m, 5H), 7.92 (d, J=8.4 Hz, 3H), 8.14 (s, 1H); APCI−MS (m/z) 292 (M+H)+。
4−(3−((2−クロロ−4−フルオロベンジル)オキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(116mg、2.08mmol)及び塩化アンモニウム(370mg、6.92mmol)を使用して、ステップ1中間体(249mg、0.69mmol)を還元することによって、標題化合物を調製して、生成物120mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.49 (s, 2H), 5.58 (br s, 2H), 6.58 (d, J=8.1 Hz, 2H), 7.25−7.29 (m, 1H), 7.56 (d, J=8.7 Hz, 1H), 7.64 (t, J=8.1 Hz, 1H), 7.82 (d, J=8.1 Hz, 2H), 8.03 (s, 1H), 8.23 (s, 1H); APCI−MS (m/z) 330 (M+H)+。
(R)−4−(3−(1−フェニルエトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(118mg、2.10mmol)及び塩化アンモニウム(374mg、70.0mmol)を使用して、ステップ1中間体(204mg、0.70mmol)を還元することによって、標題化合物を調製して、生成物142mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.64 (d, J=6.3 Hz, 3H), 5.56 (br s, 2H), 6.25 (d, J=6.9 Hz, 1H), 6.63 (d, J=8.4 Hz, 2H), 7.24−7.44 (m, 5H), 7.89−7.93 (m, 3H), 8.14 (s, 1H); APCI−MS (m/z) 292 (M+H)+。
(S)−4−(3−(1−フェニルエトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(69mg、1.23mmol)及び塩化アンモニウム(220mg、4.11mmol)を使用して、ステップ1中間体(120mg、0.41mmol)を還元することによって、標題化合物を調製して、生成物87mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.63 (d, J=6.3 Hz, 3H), 5.56 (s, 2H), 6.23−6.27 (m, 1H), 6.63 (d, J=9.0 Hz, 2H), 7.26 (d, J=6.9 Hz, 1H), 7.34 (t, J=7.2 Hz, 2H), 7.42 (d, J=7.2 Hz, 2H), 7.89−7.93 (m, 3H), 8.14 (s, 1H); APCI−MS (m/z) 292 (M+H)+。
4−(3−(1−(2−シクロプロピルフェニル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(92mg、1.65mmol)及び塩化アンモニウム(296mg、5.53mmol)を使用して、ステップ1中間体(200mg、0.55mmol)を還元することによって、標題化合物を調製して、生成物140mgを得た;1H NMR (300 MHz, DMSO−d6) δ 0.60−0.64 (m, 1H), 0.74−0.78 (m, 1H), 0.90−0.95 (m, 2H), 1.64 (d, J=6.3 Hz, 3H), 2.11−2.15 (m, 1H), 5.55 (s, 2H), 6.64 (d, J=8.7 Hz, 2H), 6.72−6.76 (m, 1H), 7.01−7.05 (m, 1H), 7.11−7.17 (m, 2H), 7.34−7.38 (m, 1H), 7.89−7.96 (m, 3H), 8.12 (s, 1H); APCI−MS (m/z) 332 (M+H)+。
4−(3−(1−フェニルシクロプロポキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(36mg、0.64mmol)及び塩化アンモニウム(116mg、2.16mmol)を使用して、ステップ1中間体(72mg、0.22mmol)を還元することによって、標題化合物を調製して、生成物65mgを得た。生成物をそのまま、特徴づけることなく、次のステップに入れた。
(R)−4−(3−(1−(2−クロロフェニル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(25mL、5:1)中で、鉄粉(172mg、3.08mmol)及び塩化アンモニウム(550mg、10.28mmol)を使用して、ステップ1中間体(366mg、1.03mmol)を還元することによって、標題化合物を調製して、生成物230mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.64 (d, J=6.3 Hz, 3H), 5.58 (s, 2H), 6.45−6.50 (m, 1H), 6.64 (d, J=8.7 Hz, 2H), 7.29−7.32 (m, 2H), 7.43−7.47 (m, 2H), 7.90−7.95 (m, 3H), 8.15 (s, 1H)。
(S)−4−(3−(1−(2−クロロフェニル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(185mg、3.30mmol)及び塩化アンモニウム(589mg、11.01mmol)を使用して、ステップ1中間体(392mg、1.10mmol)を還元することによって、標題化合物を調製して、生成物246mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.64 (d, J=6.3 Hz, 3H), 5.57 (s, 2H), 6.44−6.48 (m, 1H), 6.64 (d, J=8.4 Hz, 2H), 7.28−7.32 (m, 2H), 7.42−7.46 (m, 2H), 7.89−7.95 (m, 3H), 8.14 (s, 1H)。
4−(3−(2−クロロフェノキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(129mg、2.30mmol)及び塩化アンモニウム(247mg、4.61mmol)を使用して、ステップ1中間体(151mg、0.46mmol)を還元することによって、標題化合物を調製して、生成物89mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.62 (s, 2H), 6.66 (d, J=8.1 Hz, 2H), 7.29−7.33 (m, 1H), 7.39−7.43 (m, 2H), 7.61 (d, J=8.1 Hz, 1H), 7.90−7.97 (m, 3H), 8.35 (s, 1H); APCI−MS (m/z) 298 (M+H)+。
(R)−4−(3−(1−(2−クロロ−4−メチルフェニル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(85mg、1.52mmol)及び塩化アンモニウム(272mg、5.08mmol)を使用して、ステップ1中間体(188mg、0.51mmol)を還元することによって、標題化合物を調製して、生成物140mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.61 (d, J=6.3 Hz, 3H), 2.25 (s, 3H), 5.55 (s, 2H), 6.41−6.45 (m, 1H), 6.63 (d, J=6.9 Hz, 2H), 7.12 (d, J=8.4 Hz, 1H), 7.26−7.34 (m, 2H), 7.87−7.91 (m, 3H), 8.13 (s, 1H); APCI−MS (m/z) 340 (M+H)+。
4−(3−((3,5−ジメチルイソオキサゾール−4−イル)メトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(52mg、0.94mmol)及び塩化アンモニウム(167mg、3.13mmol)を使用して、ステップ1中間体(102mg、0.31mmol)を還元することによって、標題化合物を調製して、生成物56mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.23 (s, 3H), 2.43 (s, 3H), 5.27 (s, 2H), 5.53 (s, 2H), 6.57 (d, J=8.1 Hz, 2H), 7.79 (d, J=8.7 Hz, 2H), 8.03 (s, 1H), 8.21 (s, 1H)。
4−(3−(2−(3,5−ジメチルイソオキサゾール−4−イル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(70mg、1.24mmol)及び塩化アンモニウム(221mg、4.14mmol)を使用して、ステップ1中間体(141mg、0.41mmol)を還元することによって、標題化合物を調製して、生成物121mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.14 (s, 3H), 2.24 (s, 3H), 2.83 (t, J=6.6 Hz, 2H), 4.45 (t, J=6.6 Hz, 2H), 5.53 (s, 2H), 6.58 (d, J=8.1 Hz, 2H), 7.71 (d, J=8.4 Hz, 2H), 7.97 (s, 1H), 8.16 (s, 1H); ESI−MS (m/z) 311 (M+H)+。
4−(3−((2−クロロベンジル)オキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(49mg、0.88mmol)及び塩化アンモニウム(158mg、2.95mmol)を使用して、ステップ1中間体(101mg、0.29mmol)を還元することによって、標題化合物を調製して、生成物78mgを得た;1H NMR (300 MHz, DMSO−d6) δ 5.52 (s, 4H), 6.58 (d, J=7.8 Hz, 2H), 7.37−7.41 (m, 2H), 7.53−7.57 (m, 2H), 7.83 (d, J=8.4 Hz, 2H), 8.02 (s, 1H), 8.22 (s, 1H); ESI−MS (m/z) 312 (M+H)+。
4−(3−(2−(4−メチルチアゾール−5−イル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(18mL、5:1)中で、鉄粉(73mg、1.31mmol)及び塩化アンモニウム(141mg、2.63mmol)を使用して、ステップ2中間体(90mg、0.26mmol)を還元することによって、標題化合物を調製して、生成物56mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.32 (s, 3H), 3.31 (t, J=6.3 Hz, 2H), 4.54 (t, J=6.3 Hz, 2H), 5.53 (s, 2H), 6.56 (d, J=8.7 Hz, 2H), 7.73 (d, J=9.0 Hz, 2H), 7.98 (s, 1H), 8.18 (s, 1H), 8.84 (s, 1H); ESI−MS (m/z) 313 (M+H)+。
4−(3−(シクロヘキシルメトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(70mg、1.26mmol)及び塩化アンモニウム(225mg、4.21mmol)を使用して、ステップ1中間体(132mg、0.42mmol)を還元することによって、標題化合物を調製して、生成物103mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.00−1.24 (m, 5H), 1.68−1.81 (m, 5H), 3.15−3.21 (m, 1H), 4.16 (d, J=3.9 Hz, 2H), 5.51 (s, 2H), 6.61 (d, J=8.7 Hz, 2H), 7.83 (d, J=7.2 Hz, 2H), 7.96 (s, 1H), 8.15 (s, 1H); ESI−MS (m/z) 282 (M−H)−。
4−(3−(3−(ベンジルオキシ)アゼチジン−1−イル)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(10mL、5:1)中で、鉄粉(97mg、1.72mmol)及び塩化アンモニウム(308mg、5.76mmol)を使用して、ステップ1中間体(209mg、0.57mmol)を還元することによって、標題化合物を調製して、生成物161mgを得た;1H NMR (300 MHz, DMSO−d6) δ 3.32−3.57 (m, 2H), 3.86−3.91 (m, 2H), 4.34−4.37 (m, 1H), 4.38 (s, 2H), 5.40 (s, 2H), 6.61 (d, J=8.4 Hz, 2H), 7.28−7.32 (m, 7H), 7.96 (s, 2H); ESI−MS (m/z) 333 (M+H)+。
2−((3−(4−アミノフェニル)ピラジン−2−イル)アミノ)−2−フェニルエタノール
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(12mL、3:1)中で、80℃で、炭酸ナトリウム(255mg、2.40mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II).ジクロロメタン複合体(65mg、0.08mmol)を使用して、ステップ1中間体(200mg、0.80mmol)を4−アミノフェニルボロン酸ピナコールエステル(210mg、0.96mmol)と反応させることによって、標題化合物を調製して、生成物127mgを得た;1H NMR (300 MHz, DMSO−d6) δ 3.34−3.42 (m, 1H), 3.56−3.62 (m, 1H), 4.80−4.84 (m, 1H), 5.43 (s, 2H), 5.56−5.58 (m, 1H), 6.01 (br s, 1H), 6.62 (d, J=8.4 Hz, 2H), 7.29 (d, J=8.7 Hz, 2H), 7.32−7.36 (m, 5H), 7.75 (s, 1H), 7.86 (s, 1H)。
(R)−4−(3−(1−(2,4−ジメチルフェニル)エトキシ)ピラジン−2−イル)アニリン
中間体9のステップ4において記載した手順のとおりに、エタノール及び水の混合物(12mL、5:1)中で、鉄粉(56mg、1.00mmol)及び塩化アンモニウム(180mg、3.34mmol)を使用して、ステップ1中間体(117mg、0.33mmol)を還元することによって、標題化合物を調製して、生成物72mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.58 (d, J=6.3 Hz, 3H), 2.20 (s, 3H), 2.35 (s, 3H), 5.52 (s, 2H), 6.33−6.37 (m, 1H), 6.63 (d, J=8.1 Hz, 2H), 6.93−6.99 (m, 2H), 7.21−7.27 (m, 2H), 7.90 (s, 1H), 7.92 (s, 1H), 8.10 (s, 1H)。
4−(3−(4−(オキセタン−3−イル)ピペラジン−1−イル)ピラジン−2−イル)アニリン
中間体1のステップ1において記載した手順のとおりに、DMSO及び水の混合物(12mL、3:1)中で、80℃で、炭酸カリウム(415mg、3.00mmol)及び[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(82mg、0.10mmol)を使用して、ステップ3中間体(255mg、1.00mmol)を4−アミノフェニルボロン酸ピナコールエステル(263mg、1.20mmol)と反応させることによって、標題化合物を調製して、生成物123mgを得た;1H NMR (300 MHz, DMSO−d6) δ 2.28−2.32 (m, 3H), 3.08−3.12 (m, 4H), 3.37−3.46 (m, 2H), 4.41 (t, J=5.7 Hz, 2H), 4.52 (t, J=6.3 Hz, 2H), 5.42 (br s, 2H), 6.60 (d, J=8.7 Hz, 2H), 7.65 (d, J=8.1 Hz, 2H), 8.01 (s, 1H), 8.09 (s, 1H); ESI−MS (m/z) 312 (M+H)+。
N−(4−(3−(4−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド(実施例1)の調製
N−(4−(3−(4−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド(実施例2)の調製
メタノール(5.0mL)中のステップ1中間体(134mg、0.27mmol)の撹拌溶液に、0℃で、ホウ水素化ナトリウム(125mg、0.32mmol)を添加した。反応混合物を0℃で、1時間にわたって撹拌した。混合物を塩化アンモニウム水溶液(20mL)でクエンチし、水(20mL)に注ぎ入れ、酢酸エチル(70mL×2)で抽出した。合わせた有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。得られた粗製の物質をシリカゲルカラムクロマトグラフィーによって精製して、生成物64mgを得た;1H NMR (300 MHz, DMSO−d6) δ 1.07 (d, J=5.7 Hz, 3H), 3.70 (s, 2H), 3.99−4.06 (m, 1H), 5.51 (d, J=6.0 Hz, 1H), 7.34 (d, J=8.1 Hz, 3H), 7.39−7.45 (m, 7H), 7.56 (d, J=8.1 Hz, 2H), 8.67 (d, J=3.9 Hz, 2H), 10.34 (s, 1H); ESI−MS (m/z) 494 (M+H)+。
(S)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2−エチルフェニル)ピラジン−2−イル)フェニル)アセトアミド(実施例52)の調製
THF(3.0mL)、メタノール(1.0mL)及び水(1.0mL)の混合物中のステップ3中間体(96mg、0.13mmol)の撹拌溶液に、水酸化リチウム一水和物(16mg、0.38mmol)を添加し、混合物を室温で30分間にわたって撹拌した。反応混合物を飽和塩化アンモニウム水溶液(10mL)でクエンチし、生成物を酢酸エチル(2×20mL)中で抽出した。合わせた有機層を水(20mL)及びブライン(10mL)で洗浄した。有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。得られた残渣をフラッシュシリカゲルカラムクロマトグラフィーによって精製して、標題生成物38mgを得た;1H NMR (300 MHz, DMSO−d6) δ 0.85 (t, J=7.2 Hz, 3H), 1.05 (d, J=6.3 Hz, 3H), 2.26 (q, J=7.2 Hz, 2H), 3.67 (s, 2H), 4.02−4.05 (m, 1H), 5.49 (d, J=6.0 Hz, 1H), 7.16−7.34 (m, 6H), 7.39−7.49 (m, 6H), 8.66 (s, 1H), 8.72 (s, 1H), 10.27 (s, 1H); APCI−MS (m/z) 488 (M+H)+;キラルHPLC純度:97.34%。
THF(3.0mL)、メタノール(1.0mL)及び水(1.0mL)の混合物中のステップ3中間体(105mg、0.14mmol)の撹拌溶液に、水酸化リチウム一水和物(17mg、0.40mmol)を添加し、混合物を室温で30分間にわたって撹拌した。反応混合物を飽和塩化アンモニウム水溶液(10mL)でクエンチし、生成物を酢酸エチル(2×20mL)中で抽出した。合わせた有機層を水(20mL)及びブライン(10mL)で洗浄した。有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。得られた残渣をフラッシュシリカゲルカラムクロマトグラフィーによって精製して、標題生成物48mgを固体として得た;1H NMR (300 MHz, DMSO−d6) δ 0.84 (t, J=7.8 Hz, 3H), 1.06 (d, J=6.3 Hz, 3H), 2.26 (q, J=7.8 Hz, 2H), 3.67 (s, 2H), 4.01−4.05 (m, 1H), 5.50 (d, J=6.0 Hz, 1H), 7.14−7.34 (m, 6H), 7.40−7.49 (m, 6H), 8.66 (s, 1H), 8.73 (s, 1H), 10.28 (s, 1H); APCI−MS (m/z) 488 (M+H)+;キラルHPLC純度:95.86%。
バイオアッセイ
JBC 2011,286,26:22707−10;及びDrug Metabolism and Disposition 2009,37,10:2069−78において記載されているとおりに、TR−FRETアッセイ(LanthaScreen(商標)、Invitrogen of Carlsbad、CAから入手可能)を使用して、本明細書に記載の化合物をRORガンマモジュレータ活性についてスクリーニングした。
このアッセイは、RORガンマへのアゴニストの結合が、リガンド結合性ドメイン内のへリックス12の周囲で配座変化を引き起こして、共活性化因子ペプチドについて、より高い親和性をもたらすという原理に基づく。RORガンマは構成的に活性であるので、このアッセイにおいて使用されるフルオレセイン−D22共活性化因子ペプチドは、リガンドの非存在下で動員される。共活性化因子ペプチドの結合は、TR−FRETシグナルの増大をもたらす一方で、アンタゴニストの結合は、共活性化因子ペプチドの動員を低下させて、化合物を含まない対照と比較してTR−FRETシグナルの低下をもたらす。このアッセイを、2ステップ手順、すなわち、化合物を用いるプレインキュベーションステップ、続く、抗GST標識テルビウム(Tb)及びアクセプターとしてのフルオレセイン標識フルオロフォアを添加しての検出ステップを使用して行った。
Claims (56)
- 式(I)の化合物
[式中、
環Aは、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
Lは、存在しないか、またはy*−X−(CRxRy)t−*zであり;Xは、O、NRx1及び
x、y及びzのそれぞれは、結合点を表し;
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R3の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R5の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRa及びRbはそれぞれ、水素及びC1〜8アルキルから独立に選択され;
同じでも、または異なってもよいRx及びRyはそれぞれ、水素、C1〜8アルキル及びヒドロキシC1〜8アルキルから独立に選択されるか;またはRx及びRyは、それらが結合している炭素原子と一緒に、3〜6員シクロアルキル環を形成しており;
Rx1は、水素またはC1〜8アルキルから選択され;
「n」は、0、1、2または3であり;
「m」は、0、1または2であり;
「p」は、0、1または2であり;
「q」は、0、1、2または3であり、
「t」は、0、1、2または3である]。 - 環Bが、シクロヘキシル、フェニル、6−オキソ−1,6−ジヒドロピリジニル、ピペリジニル、ピペラジニル、モルホリニル、イソオキサゾリル、ピラゾリル、チアゾリル、ピリジニルまたはピリミジニルである、請求項1に記載の化合物。
- Lが存在しない、請求項1または2に記載の化合物。
- R1が、ヒドロキシル、メチルまたはメトキシである、請求項1〜4のいずれか1項に記載の化合物。
- 「n」が、0である、請求項1〜5のいずれか1項に記載の化合物。
- 各R2が独立に、シアノ、F、Cl、メチル、エチル、メトキシ、メトキシエチル、トリフルオロメチル、シクロプロピル、C(O)メチル、C(O)シクロプロピルまたはオキセタン−3−イルであり、「n」が、1または2である、請求項1〜5のいずれか1項に記載の化合物。
- 「m」が、0である、請求項1〜7のいずれか1項に記載の化合物。
- R3が、メチル、tert−ブチルまたはトリフルオロメチルであり、「m」が、1である、請求項1〜7のいずれか1項に記載の化合物。
- 「p」が、0である、請求項1〜9のいずれか1項に記載の化合物。
- R4が、Fであり、pが、1である、請求項1〜9のいずれか1項に記載の化合物。
- Ra及びRbの一方が、水素であり、他方が、水素またはメチルである、請求項1〜11のいずれか1項に記載の化合物。
- Ra及びRbが、水素である、請求項1〜12のいずれか1項に記載の化合物。
- Raが、水素であり、Rbが、メチルである、請求項1〜12のいずれか1項に記載の化合物。
- R1が、メチルであり;Raが、水素であり、Rbが、水素である、請求項1〜12のいずれか1項に記載の化合物。
- R1が、ヒドロキシルであり;Raが、水素であり、Rbが、メチルである、請求項1〜12のいずれか1項に記載の化合物。
-
- 環Aが、
環Bが、シクロヘキシル、フェニル、6−オキソ−1,6−ジヒドロピリジニル、ピペリジニル、ピペラジニル、モルホリニル、イソオキサゾリル、ピラゾリル、チアゾリル、ピリジニルまたはピリミジニルであり;
Lが、存在しないか、または
R1が、ヒドロキシル、メチルまたはメトキシであり;
R2が、シアノ、F、Cl、メチル、エチル、メトキシ、メトキシエチル、トリフルオロメチル、シクロプロピル、C(O)メチル、C(O)シクロプロピルまたはオキセタン−3−イルであり;
R3が、メチル、tert−ブチルまたはトリフルオロメチルであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「n」が、0、1または2であり;
「m」が、0または1であり;
「p」が、0または1であり;
「q」が、0である、請求項1に記載の化合物。 -
Lが、存在しないか、または
R1が、ヒドロキシル、メチルまたはメトキシであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「p」が、0または1であり;
「q」が、0である、請求項1に記載の化合物。 - 式(II)の化合物
[式中、
環Aは、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
x及びyのそれぞれは、結合点を表し;
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R3の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRa及びRbはそれぞれ、水素及びC1〜8アルキルから独立に選択され;
「n」は、0、1、2または3であり;
「m」は、0、1または2であり;
「p」は、0、1または2である]。 - 環Bが、フェニル、6−オキソ−1,6−ジヒドロピリジン−3−イル、ピペリジニル、ピペラジニル、モルホリニル、ピラゾリル、ピリジニルまたはピリミジニルである、請求項21に記載の化合物。
- R2が、シアノ、F、Cl、メチル、エチル、メトキシ、メトキシエチル、トリフルオロメチル、C(O)メチル、C(O)シクロプロピルまたはオキセタン−3−イルであり、「n」が、1または2である、請求項21または22に記載の化合物。
- R3が、メチル、tert−ブチルまたはトリフルオロメチルであり、「m」が、1である、請求項21〜23のいずれか1項に記載の化合物。
-
-
R1が、ヒドロキシル、メチルまたはメトキシであり;
R4が、Fであり;
Raが、水素であり;
Rbが、水素またはメチルであり;
「p」が、0または1である、請求項21に記載の化合物。 - 式(III)の化合物
[式中、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
Xは、−O−、−NRx1−及び
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRa及びRbはそれぞれ、水素及びC1〜8アルキルから独立に選択され;
同じでも、または異なってもよいRx及びRyはそれぞれ、水素、C1〜8アルキル及びヒドロキシC1〜8アルキルから独立に選択されるか;またはRx及びRyは、それらが結合している炭素原子と一緒に、3〜6員シクロアルキル環を形成しており;
Rx1は、水素またはC1〜8アルキルから選択され;
「n」は、0、1、2または3であり;
「p」は、0、1または2であり;
「t」は、0、1、2または3である]。 - 環Bが、シクロヘキシル、フェニル、ピペラジニル、イソオキサゾリルまたはチアゾリルである、請求項27に記載の化合物。
- 下記から選択される化合物:
N−(4−(3−(4−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(4−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(4−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−メトキシエチル)フェニル)アセトアミド;
N−(4−(3−(3−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(2−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(4−クロロ−2−フルオロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(4−クロロフェニル)ピリジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(4−フルオロフェニル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(3,4−ジフルオロフェニル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(2,4−ジフルオロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(2−フルオロフェニル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−(トリフルオロメチル)フェニル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(p−トリル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−フルオロフェニル)ピリジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−フェニルピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(4−シアノフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(ピリジン−4−イル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(4,4−ジフルオロピペリジン−1−イル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−モルホリノピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(5−(4−フルオロフェニル)−3−メチル−1H−ピラゾール−1−イル)フェニル)アセトアミド;
N−(4−(1−(tert−ブチル)−5−(4−フルオロフェニル)−1H−ピラゾール−4−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(1−(tert−ブチル)−5−(4−フルオロフェニル)−1H−ピラゾール−4−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(1−メチル−1H−ピラゾール−4−イル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(4−アセチルピペラジン−1−イル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(1−メチル−6−オキソ−1,6−ジヒドロピリジン−3−イル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(4−クロロフェニル)ピラジン−2−イル)−2−フルオロフェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−メトキシフェニル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(5−(4−フルオロフェニル)−3−(トリフルオロメチル)−1H−ピラゾール−1−イル)フェニル)アセトアミド;
N−(4−(5−(2−クロロフェニル)−3−(トリフルオロメチル)−1H−ピラゾール−1−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(2−クロロフェニル)ピリジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(o−トリル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−メチルピペラジン−1−イル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−エチルピペラジン−1−イル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(2−(4−クロロフェニル)ピリジン−3−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(4−(4−クロロフェニル)ピリジン−3−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((2S,6R)−2,6−ジメチルモルホリノ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(2−クロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(5−(2,4−ジクロロフェニル)−3−メチル−1H−ピラゾール−1−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(2−クロロ−4−フルオロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2−エチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−(2−メトキシエチル)ピペラジン−1−イル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(4−アセチル−2−メチルピペラジン−1−イル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(ピリミジン−5−イル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−フルオロ−2−メチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(2−クロロ−4−フルオロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(4−クロロフェニル)ピリジン−4−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(2,4−ジメチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(2−フルオロ−4−メチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(1−(2−クロロ−4−フルオロフェニル)−6−オキソ−1,6−ジヒドロピリミジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(2,4−ジクロロフェニル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2,4−ジメチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
(S)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2−エチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
(R)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2−エチルフェニル)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(4−(シクロプロパンカルボニル)ピペラジン−1−イル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−((4−クロロフェニル)(メチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(ベンジル(メチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(ベンジルアミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((1−フェニルエチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
(R)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((1−フェニルエチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
(R)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(メチル(1−フェニルエチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
(S)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((1−フェニルエチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
(S)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(メチル(1−フェニルエチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
(S)−N−(4−(3−((1−(4−クロロフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
(S)−N−(4−(3−((1−(3−クロロフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
(S)−N−(4−(3−((1−(4−クロロフェニル)エチル)(メチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
(S)−N−(4−(3−((1−(2−クロロフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
(S)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((1−(4−フルオロ−2−メチルフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(((S)−1−(2−クロロフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
(S)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((1−(2,4−ジメチルフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
(S)−N−(4−(3−((1−(2−クロロ−4−フルオロフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−((シクロヘキシルメチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(((S)−1−(4−クロロフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(((S)−1−(2−クロロフェニル)エチル)アミノ)ピラジン−2−イル)−2−フルオロフェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(((S)−1−(2−クロロフェニル)エチル)アミノ)ピラジン−2−イル)−3−フルオロフェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(ベンジルオキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(1−フェニルエトキシ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−((2−クロロ−4−フルオロベンジル)オキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−(ベンジルオキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
(R)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(1−フェニルエトキシ)ピラジン−2−イル)フェニル)アセトアミド;
(S)−2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(1−フェニルエトキシ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(1−(2−シクロプロピルフェニル)エトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(1−フェニルシクロプロポキシ)ピラジン−2−イル)フェニル)アセトアミド;
(R)−N−(4−(3−(1−(2−クロロフェニル)エトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−((R)−1−(2−クロロフェニル)エトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
(S)−N−(4−(3−(1−(2−クロロフェニル)エトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−((S)−1−(2−クロロフェニル)エトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(2−クロロフェノキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
N−(4−(3−((R)−1−(2−クロロ−4−メチルフェニル)エトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((3,5−ジメチルイソオキサゾール−4−イル)メトキシ)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2−(3,5−ジメチルイソオキサゾール−4−イル)エトキシ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−((2−クロロベンジル)オキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(2−(4−メチルチアゾール−5−イル)エトキシ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(シクロヘキシルメトキシ)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
N−(4−(3−(3−(ベンジルオキシ)アゼチジン−1−イル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−(((S)−1−(2,4−ジメチルフェニル)エチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
N−(4−(3−(4−(シクロプロパンカルボニル)ピペラジン−1−イル)ピラジン−2−イル)フェニル)−2−(4−(1,1−ジフルオロプロピル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−((2−ヒドロキシ−1−フェニルエチル)アミノ)ピラジン−2−イル)フェニル)アセトアミド;
2−(4−(1,1−ジフルオロ−2−ヒドロキシプロピル)フェニル)−N−(4−(3−((R)−1−(2,4−ジメチルフェニル)エトキシ)ピラジン−2−イル)フェニル)アセトアミドまたは
2−(4−(1,1−ジフルオロプロピル)フェニル)−N−(4−(3−(4−(オキセタン−3−イル)ピペラジン−1−イル)ピラジン−2−イル)フェニル)アセトアミド及び
その薬学的に許容される塩。 - 請求項1〜37のいずれか1項に記載の化合物及び薬学的に許容される添加剤を含む医薬組成物。
- 前記薬学的に許容される添加剤が、担体または希釈剤である、請求項38に記載の医薬組成物。
- 請求項1〜37のいずれか1項に記載の化合物の有効量を投与することを含む、対象においてRORγt媒介性疾患、障害、症候群、または状態を処置する方法。
- 前記疾患、障害、症候群または状態が、炎症性または自己免疫疾患である、請求項40に記載の方法。
- 前記炎症性または自己免疫疾患が、関節リウマチ、乾癬、慢性閉塞性肺疾患(COPD)、喘息、多発性硬化症、大腸炎、潰瘍性大腸炎及び炎症性腸疾患からなる群から選択される、請求項41に記載の方法。
- 前記疾患、障害、症候群または状態が、疼痛、慢性疼痛、急性疼痛、炎症性疼痛、関節炎疼痛、神経障害性疼痛、術後疼痛、外科手術上の疼痛、内臓疼痛、歯痛、月経前疼痛、中枢性疼痛、癌性疼痛、火傷、片頭痛もしくは群発性頭痛、神経損傷、神経炎、神経痛、中毒、虚血性損傷、間質性膀胱炎、ウイルス、寄生虫もしくは細菌感染、外傷後損傷による疼痛、または過敏性腸症候群と関連する疼痛である、請求項40に記載の方法。
- 前記疾患、障害、症候群または状態が、慢性閉塞性肺疾患(COPD)、喘息、気管支痙攣、または咳である、請求項40に記載の方法。
- それを必要とする対象に、請求項1〜37のいずれか1項に記載の化合物を投与することを含む、慢性閉塞性肺疾患(COPD)、喘息、咳、疼痛、炎症性疼痛、慢性疼痛、急性疼痛、関節炎、変形性関節症、多発性硬化症、関節リウマチ、大腸炎、潰瘍性大腸炎、乾癬及び炎症性腸疾患からなる群から選択される疾患、障害、症候群または状態を処置する方法。
- 式(Ia)の化合物
(i)式(1)の化合物を、式(2)の化合物と反応させて、式(Ia)の化合物を得ること
[式中、
環Aは、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
Lは、存在しないか、y*−X−(CRxRy)t−*zであり;Xは、O、NRx1及び
x、y及びzのそれぞれは、結合点を表し;
R1は、ヒドロキシル、C1〜8アルキル及びC1〜8アルコキシから選択され;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R3の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R5の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
同じでも、または異なってもよいRx及びRyはそれぞれ、水素、C1〜8アルキル及びヒドロキシC1〜8アルキルから独立に選択されるか;またはRx及びRyは、それらが結合している炭素原子と一緒に、3〜6員シクロアルキル環を形成しており;
Rx1は、水素またはC1〜8アルキルから選択され;
「n」は、0、1、2または3であり;
「m」は、0、1または2であり;
「p」は、0、1または2であり;
「q」は、0、1、2または3であり、
「t」は、0、1、2または3である]。 - カップリング剤の存在下で、式(1)の化合物を式(2)の化合物と反応させる、請求項46に記載のプロセス。
- 前記カップリング剤が、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド(EDCI)、プロピルホスホン酸無水物(T3P)、N,N’−ジシクロヘキシルカルボジイミド(DCC)及び(1−[ビス(ジメチルアミノ)メチレン]−1H−1,2,3−トリアゾロ[4,5−b]ピリジニウム3−オキシドヘキサフルオロホスファート)(HATU)またはそれらの組合せから選択される、請求項47に記載のプロセス。
- 塩基の存在下で、式(1)の化合物を式(2)の化合物と反応させる、請求項46に記載のプロセス。
- 前記塩基が、Et3N、DIPEA、ピリジンまたはDMAPから選択される、請求項49に記載のプロセス。
- 式(Ib)の化合物
(i)式(1)の化合物を式(3)の化合物と反応させて、式(4)の化合物を得ること;及び
[式中、
環Aは、
環Bは、C3〜6シクロアルキル、C6〜14アリール、3〜15員ヘテロシクリル及び5〜14員ヘテロアリールから選択され;
Lは、存在しないか、またはy*−X−(CRxRy)t−*zであり;Xは、O、NRx1及び
x、y及びzのそれぞれは、結合点を表し;
R2の各出現は、シアノ、ハロゲン、ヒドロキシル、C1〜8アルキル、C1〜8アルコキシ、C1〜8アルコキシC1〜8アルキル、ハロC1〜8アルキル、ハロC1〜8アルコキシ、ヒドロキシC1〜8アルキル、C(O)C1〜8アルキル、C3〜6シクロアルキル、C(O)C3〜6シクロアルキル及び3〜15員複素環式環から独立に選択され;
R3の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R4の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
R5の各出現は、ハロゲン、シアノ、C1〜8アルキル;ハロC1〜8アルキル及びC3〜6シクロアルキルから独立に選択され;
Rbは、C1〜8アルキルであり;
同じでも、または異なってもよいRx及びRyはそれぞれ、水素、C1〜8アルキル及びヒドロキシC1〜8アルキルから独立に選択されるか;またはRx及びRyは、それらが結合している炭素原子と一緒に、3〜6員シクロアルキル環を形成しており;
Rx1は、水素またはC1〜8アルキルから選択され;
「n」は、0、1、2または3であり;
「m」は、0、1または2であり;
「p」は、0、1または2であり;
「q」は、0、1、2または3であり、
「t」は、0、1、2または3である]。 - カップリング剤の存在下で、式(1)の化合物を式(3)の化合物と反応させる、請求項51に記載のプロセス。
- 前記カップリング剤が、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド(EDCI)、プロピルホスホン酸無水物(T3P)、N,N’−ジシクロヘキシルカルボジイミド(DCC)及び(1−[ビス(ジメチルアミノ)メチレン]−1H−1,2,3−トリアゾロ[4,5−b]ピリジニウム3−オキシドヘキサフルオロホスファート)(HATU)またはそれらの組合せから選択される、請求項52に記載のプロセス。
- 塩基の存在下で、式(1)の化合物を式(3)の化合物と反応させる、請求項51に記載のプロセス。
- 前記塩基が、Et3N、DIPEA、ピリジンまたはDMAPから選択される、請求項54に記載のプロセス。
- 式(4)の化合物の還元を、ホウ水素化ナトリウムを使用して実施する、請求項51に記載のプロセス。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN2930MU2015 | 2015-08-03 | ||
| IN2930/MUM/2015 | 2015-08-03 | ||
| PCT/IB2016/054639 WO2017021879A1 (en) | 2015-08-03 | 2016-08-02 | Novel compounds as ror gamma modulators |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018522047A true JP2018522047A (ja) | 2018-08-09 |
| JP6661749B2 JP6661749B2 (ja) | 2020-03-11 |
Family
ID=56799510
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018505705A Expired - Fee Related JP6661749B2 (ja) | 2015-08-03 | 2016-08-02 | Rorガンマモジュレータとしての新規化合物 |
Country Status (26)
| Country | Link |
|---|---|
| US (3) | US9975887B2 (ja) |
| EP (2) | EP3686187A1 (ja) |
| JP (1) | JP6661749B2 (ja) |
| KR (1) | KR102229608B1 (ja) |
| CN (1) | CN108026050B (ja) |
| AU (1) | AU2016303540B2 (ja) |
| BR (1) | BR112018001469B1 (ja) |
| CA (1) | CA2993304C (ja) |
| CL (1) | CL2018000289A1 (ja) |
| CY (1) | CY1122916T1 (ja) |
| DK (1) | DK3331863T3 (ja) |
| EA (1) | EA034201B1 (ja) |
| ES (1) | ES2791496T3 (ja) |
| HU (1) | HUE048902T2 (ja) |
| IL (1) | IL256805B (ja) |
| MX (2) | MX2018001464A (ja) |
| MY (1) | MY198809A (ja) |
| NZ (1) | NZ739228A (ja) |
| PE (1) | PE20180686A1 (ja) |
| PH (1) | PH12018500251B1 (ja) |
| PL (1) | PL3331863T3 (ja) |
| PT (1) | PT3331863T (ja) |
| SI (1) | SI3331863T1 (ja) |
| UA (1) | UA122148C2 (ja) |
| WO (1) | WO2017021879A1 (ja) |
| ZA (1) | ZA201800506B (ja) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6484228B2 (ja) | 2013-06-13 | 2019-03-13 | モービルアイ ビジョン テクノロジーズ リミテッド | 視覚強化ナビゲーション |
| TW201718536A (zh) | 2015-08-03 | 2017-06-01 | 必治妥美雅史谷比公司 | 可作為TNFα調節劑之雜環化合物 |
| GB201513742D0 (en) | 2015-08-03 | 2015-09-16 | Heptares Therapeutics Ltd | Muscarinic agonists |
| KR20180052635A (ko) | 2015-09-18 | 2018-05-18 | 가켄 세이야쿠 가부시키가이샤 | 바이아릴 유도체 및 이를 포함하는 약제 |
| WO2018042342A1 (en) * | 2016-08-30 | 2018-03-08 | Glenmark Pharmaceuticals S.A. | 1,2,3-benzotriazole derivatives as ror gamma t modulators |
| AR110481A1 (es) | 2016-12-05 | 2019-04-03 | Lead Pharma Holding Bv | MODULADORES DE ROR g (RORg) |
| WO2018193297A1 (en) | 2017-04-21 | 2018-10-25 | Cadila Healthcare Limited | Novel compounds as ror-gamma modulators |
| CN107805242A (zh) * | 2017-10-31 | 2018-03-16 | 长春海谱润斯科技有限公司 | 一种吡嗪联嘧啶衍生物及其有机发光器件 |
| WO2019119207A1 (en) | 2017-12-18 | 2019-06-27 | Merck Sharp & Dohme Corp. | Purine inhibitors of human phosphatidylinositol 3-kinase delta |
| CN112566901A (zh) * | 2018-06-18 | 2021-03-26 | 詹森药业有限公司 | 作为RORγt的调节剂的苯基取代的吡唑类 |
| WO2019244001A1 (en) * | 2018-06-18 | 2019-12-26 | Janssen Pharmaceutica Nv | 6-aminopyridin-3-yl pyrazoles as modulators of roryt |
| MX2022004383A (es) | 2019-10-11 | 2022-09-07 | Glenmark Specialty Sa | Composicion de polvo seco inhalable contra enfermedades pulmonares. |
| AR120598A1 (es) * | 2019-12-02 | 2022-02-23 | Fmc Corp | Proceso para la síntesis de un 2-(5-isoxazolil)-fenol |
| WO2022049534A1 (en) | 2020-09-03 | 2022-03-10 | Glenmark Specialty S.A. | Polymorphic forms of a rorγ inhibiting compound and processes for its preparation |
| TW202404957A (zh) * | 2022-06-29 | 2024-02-01 | 大陸商上海翰森生物醫藥科技有限公司 | 雜環類衍生物抑制劑、其製備方法和應用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012158784A2 (en) * | 2011-05-16 | 2012-11-22 | Theodore Mark Kamenecka | Modulators of the nuclear hormone receptor ror |
| WO2013029338A1 (en) * | 2011-09-01 | 2013-03-07 | Glaxo Group Limited | Novel compounds |
| WO2013171729A2 (en) * | 2013-01-08 | 2013-11-21 | Glenmark Pharmaceuticals S.A. | Aryl and heteroaryl amide compounds as rorgamat modulator |
| WO2014125426A1 (en) * | 2013-02-15 | 2014-08-21 | Aurigene Discovery Technologies Limited | Trisubstituted heterocyclic derivatives as ror gamma modulators |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU5636900A (en) * | 1999-06-30 | 2001-01-31 | Merck & Co., Inc. | Src kinase inhibitor compounds |
| SI2324008T1 (sl) * | 2008-07-24 | 2012-08-31 | Nerviano Medical Sciences Srl | 3,4-diarilpirazoli kot protein-kinazni inhibitorji |
| US8377970B2 (en) * | 2009-10-08 | 2013-02-19 | Rhizen Pharmaceuticals Sa | Modulators of calcium release-activated calcium channel |
| US8993612B2 (en) * | 2009-10-08 | 2015-03-31 | Rhizen Pharmaceuticals Sa | Modulators of calcium release-activated calcium channel and methods for treatment of non-small cell lung cancer |
| WO2012028100A1 (en) | 2010-09-01 | 2012-03-08 | Glaxo Group Limited | Novel compounds |
| WO2012027965A1 (en) | 2010-09-01 | 2012-03-08 | Glaxo Group Limited | Novel compounds |
| AU2011326071A1 (en) | 2010-11-08 | 2013-05-23 | Lycera Corporation | N- sulfonylated tetrahydroquinolines and related bicyclic compounds inhibition of RORy activity and the treatment of diseases |
| WO2012100734A1 (en) | 2011-01-24 | 2012-08-02 | Glaxo Group Limited | Compounds useful as retinoid-related orphan receptor gamma modulators |
| WO2012100732A1 (en) | 2011-01-24 | 2012-08-02 | Glaxo Group Limited | Retinoid-related orphan receptor gamma modulators, composition containing them and uses thereof |
| EP2511263A1 (en) | 2011-04-14 | 2012-10-17 | Phenex Pharmaceuticals AG | Pyrrolo sulfonamide compounds for modulation of orphan nuclear receptor RAR-related orphan receptor-gamma (RORgamma, NR1F3) activity and for the treatment of chronic inflammatory and autoimmune diseases |
| WO2015008234A1 (en) | 2013-07-17 | 2015-01-22 | Glenmark Pharmaceuticals S.A. | Bicyclic heterocyclic compounds as ror gamma modulators |
| PE20161399A1 (es) * | 2014-04-16 | 2017-01-14 | Glenmark Phamaceuticals S A | Compuestos de aril y heteroaril eter como moduladores de ror gamma |
| TW201718536A (zh) | 2015-08-03 | 2017-06-01 | 必治妥美雅史谷比公司 | 可作為TNFα調節劑之雜環化合物 |
| GB201513742D0 (en) | 2015-08-03 | 2015-09-16 | Heptares Therapeutics Ltd | Muscarinic agonists |
| AR105556A1 (es) | 2015-08-03 | 2017-10-18 | Hoffmann La Roche | Derivados de etinilo |
-
2016
- 2016-08-02 CA CA2993304A patent/CA2993304C/en active Active
- 2016-08-02 PT PT167568062T patent/PT3331863T/pt unknown
- 2016-08-02 AU AU2016303540A patent/AU2016303540B2/en not_active Ceased
- 2016-08-02 BR BR112018001469-9A patent/BR112018001469B1/pt not_active IP Right Cessation
- 2016-08-02 EA EA201890072A patent/EA034201B1/ru unknown
- 2016-08-02 PH PH1/2018/500251A patent/PH12018500251B1/en unknown
- 2016-08-02 NZ NZ73922816A patent/NZ739228A/en not_active IP Right Cessation
- 2016-08-02 EP EP20160567.2A patent/EP3686187A1/en not_active Withdrawn
- 2016-08-02 US US15/318,513 patent/US9975887B2/en active Active
- 2016-08-02 MY MYPI2018700273A patent/MY198809A/en unknown
- 2016-08-02 MX MX2018001464A patent/MX2018001464A/es active IP Right Grant
- 2016-08-02 ES ES16756806T patent/ES2791496T3/es active Active
- 2016-08-02 CN CN201680052651.2A patent/CN108026050B/zh not_active Expired - Fee Related
- 2016-08-02 JP JP2018505705A patent/JP6661749B2/ja not_active Expired - Fee Related
- 2016-08-02 PL PL16756806T patent/PL3331863T3/pl unknown
- 2016-08-02 HU HUE16756806A patent/HUE048902T2/hu unknown
- 2016-08-02 EP EP16756806.2A patent/EP3331863B1/en active Active
- 2016-08-02 MX MX2020001361A patent/MX386111B/es unknown
- 2016-08-02 DK DK16756806.2T patent/DK3331863T3/da active
- 2016-08-02 PE PE2018000176A patent/PE20180686A1/es unknown
- 2016-08-02 WO PCT/IB2016/054639 patent/WO2017021879A1/en not_active Ceased
- 2016-08-02 KR KR1020187006237A patent/KR102229608B1/ko not_active Expired - Fee Related
- 2016-08-02 UA UAA201800444A patent/UA122148C2/uk unknown
- 2016-08-02 SI SI201630747T patent/SI3331863T1/sl unknown
-
2018
- 2018-01-09 IL IL256805A patent/IL256805B/en active IP Right Grant
- 2018-01-24 ZA ZA2018/00506A patent/ZA201800506B/en unknown
- 2018-02-01 CL CL2018000289A patent/CL2018000289A1/es unknown
- 2018-04-18 US US15/956,168 patent/US10344024B2/en active Active
-
2019
- 2019-05-03 US US16/402,948 patent/US10988467B2/en not_active Expired - Fee Related
-
2020
- 2020-05-15 CY CY20201100450T patent/CY1122916T1/el unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012158784A2 (en) * | 2011-05-16 | 2012-11-22 | Theodore Mark Kamenecka | Modulators of the nuclear hormone receptor ror |
| WO2013029338A1 (en) * | 2011-09-01 | 2013-03-07 | Glaxo Group Limited | Novel compounds |
| WO2013171729A2 (en) * | 2013-01-08 | 2013-11-21 | Glenmark Pharmaceuticals S.A. | Aryl and heteroaryl amide compounds as rorgamat modulator |
| WO2014125426A1 (en) * | 2013-02-15 | 2014-08-21 | Aurigene Discovery Technologies Limited | Trisubstituted heterocyclic derivatives as ror gamma modulators |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6661749B2 (ja) | Rorガンマモジュレータとしての新規化合物 | |
| KR102727059B1 (ko) | 설포닐우레아와 관련 화합물 및 그 용도 | |
| ES2777123T3 (es) | Pirazol para el tratamiento de trastornos autoinmunes | |
| TWI583681B (zh) | 胺基嘧啶基化合物 | |
| CN108368116B (zh) | Janus激酶抑制剂、其组合物及用途 | |
| CN105566321B (zh) | 杂芳化合物及其在药物中的应用 | |
| JP2020502103A (ja) | Cftr増強物質としての二環式ヘテロアリール誘導体 | |
| CN105916859A (zh) | 杂环化合物 | |
| JP2017516850A (ja) | Jak阻害剤である5−クロロ−2−ジフルオロメトキシフェニルピラゾロピリミジン化合物 | |
| CN107108599A (zh) | 作为Rorγt调节剂的三氟甲基醇 | |
| CN120584106A (zh) | Nlrp3炎性小体抑制剂 | |
| CN121127471A (zh) | 作为nlrp3抑制剂的吡唑并嘧啶衍生物 | |
| KR20170008852A (ko) | 신규 화합물 | |
| WO2017051319A1 (en) | Aryl and heteroaryl ether compounds as ror gamma modulators | |
| HK1254692B (en) | Novel compounds as ror gamma modulators | |
| RU2795512C2 (ru) | Сульфонилмочевины и родственные соединения и их применение | |
| KR102948713B1 (ko) | 설포닐우레아와 관련 화합물 및 그 용도 | |
| BR112017017610B1 (pt) | Composto de fórmula (ii) ou um sal ou solvato farmaceuticamente a c e i t á v e i s d o m e s m o , u s o d o c o m p o s t o o u d o s a l o u s o l v a t o farmaceuticamente aceitáveis e composição farmacêutica | |
| HK1258764B (en) | Janus kinases inhibitors, compositions thereof and use thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180403 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190315 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200108 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200120 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200212 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6661749 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |