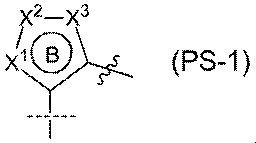JP2017095366A - 新規ビアリールアミド誘導体 - Google Patents
新規ビアリールアミド誘導体 Download PDFInfo
- Publication number
- JP2017095366A JP2017095366A JP2015226136A JP2015226136A JP2017095366A JP 2017095366 A JP2017095366 A JP 2017095366A JP 2015226136 A JP2015226136 A JP 2015226136A JP 2015226136 A JP2015226136 A JP 2015226136A JP 2017095366 A JP2017095366 A JP 2017095366A
- Authority
- JP
- Japan
- Prior art keywords
- group
- alkyl group
- ring
- halogenated
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Landscapes
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
【課題】本発明は、PDE2A選択的阻害作用を有する化合物、及びそれを含有してなる医薬組成物を提供する。【解決手段】本発明は、次の一般式(I)【化1】[式中、pは0〜6の整数を示し;qは、1〜5の整数を示し;X1は、C−H、N、又はOを示し;X2は、N、又はN−R4bを示し;X3は、N−R4a、C−R4b、又はC−Hを示し;環Aは単環式ヘテロアリール環等を示し;環Qはベンゼン環等を示し;R1、R2a、R2b、及びR3はアルキル基等を示す。]で表される化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物、及びこれらを含有してなる医薬組成物に関する。【選択図】なし
Description
本発明は、ホスホジエステラーゼ2A(以下、「PDE2A」と記す。)阻害作用を有する化合物、とりわけ、下記式(I)で表されるビアリールアミド構造を持つことを特徴とする化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物、及び、それらを有効成分として含有することを特徴とする医薬組成物に関する。
ホスホジエステラーゼ(PDE、環状ヌクレオチドホスホジエステラーゼ)は、21種の異なる遺伝子でコードされる酵素のスーパーファミリーである。これまで、アミノ酸配列の相同性、生化学的性質、阻害薬による特徴付け等の構造的/機能的特性により11種類が哺乳動物において同定されている(非特許文献1、及び2参照)。
細胞シグナルカスケードにおけるPDEの役割は、環状ヌクレオチドである環状アデノシン一リン酸(adenosine 3’,5’−cyclic monophosphate:cAMP)及び/又は環状グアノシン一リン酸(guanosine 3’,5’−cyclic monophosphate:cGMP)のホスホジエステル結合を加水分解すること、即ち、3’−エステル結合の加水分解を選択的に触媒し、不活性な5’−一リン酸を形成することで、代謝的に不活性化することである。
11種類のPDEファミリーは基質特異性に基づき、cAMP特異的PDE(PDE4、7、8)、cGMP特異的PDE(PDE5、6、9)、及び二重基質PDE(PDE1、2、3、10、11)の3つに分類される(非特許文献3、及び4参照)。
cAMP及びcGMPは、Gタンパク質結合受容体(GPCR、G Protein Cuppled Receptor)を介した細胞内情報伝達における重要なセカンドメッセンジャーであるため、PDEは、広範な生理学的機序に関与し、生物の恒常性において重要な役割を果たす。具体的には、炎症促進性メディエータの産生および作用、イオンチャネル機能、筋弛緩、学習および記憶形成、分化、アポトーシス、脂質生成、グリコーゲン分解ならびに糖新生等の種々の生理学的プロセスの制御に関わっている。とりわけ、神経細胞においては、神経細胞の分化及び生存とともに神経伝達の制御に重要な役割を果たしている(非特許文献5参照)。
cAMP及びcGMPによるこれらのプロセスの制御は、プロテインキナーゼA(PKA)及びプロテインキナーゼG(PKG)の活性化を伴い、転写因子、イオンチャネル及び受容体を含めた多様な生理的プロセスを制御している様々な基質がリン酸化される。cAMP及びcGMPの細胞内濃度は、細胞外からのシグナルに応答して変動し、cAMP及びcGMPの合成に関与する酵素(アデニルシクラーゼ(AC)およびグアニルシクラーゼ(GC))と、それら酵素の加水分解に関与するPDEとのバランスによって調節されている(非特許文献6参照)。
PDE2Aは、一次アミノ酸配列及び独特な酵素活性に基づいてファミリーが特定されており、PDE2A1、PDE2A2、及びPDE2A3等の複数のPDE2Aアイソフォームが報告されている。ヒトPDE2A3配列は、1997年に単離がされている(非特許文献7参照)。
PDE2Aは、cAMP又はcGMPの両方を代謝することができ、とりわけcGMPに対して、より高い親和性を有する二重基質酵素である。PDE2Aは、脳で高度に発現されており、又、多くの他の組織でも発現している事から、広範囲の機能と有用性を有している(非特許文献8参照)。更に、PDE2Aは、神経発達、学習及び記憶、プロラクチン及びアルドステロン分泌、骨細胞分化及び骨吸収、免疫学的反応、血管新生、炎症性細胞輸送、心収縮、血小板凝集、女性の性的興奮障害、骨関節炎痛、悪性黒色腫、及び低酸素性肺血管収縮、等の潜在的な治療可能性が示されている(特許文献1、及び2参照。非特許文献9〜24参照)。
PDE2Aを阻害する事で、統合失調症における認知記憶、社会的認知、及び作業記憶などの認知能力の欠損が改善され、認知機能が高まることが、複数の認知能力の前臨床モデルにおいて示されている(非特許文献25参照)。更に、PDE2Aの阻害は、老化及びアルツハイマー病において発症する認知障害も改善することが示されている(非特許文献26、及び27参照)。又、PDE2Aを阻害する事で、不安及びうつ病の前臨床モデルにおいて有効性を示すことも報告されている(非特許文献28、29、及び30参照)。
また、血管透過性の増大は、PDE2活性の増加に起因していることが示されている。内皮にあるPDE2及びPDE3は、偏頭痛に関連して、cGMPの濃度を検知するセンサー、又は内皮透過性を制御するスイッチとして作動している(非特許文献31、及び32参照)。
認知障害におけるPDE2阻害の役割は、Brandonらによって報告されている。PDE2阻害剤の1つであるBAY60−7550(CAS No.439083-90-6)の生化学プロファイル及び挙動プロファイルにおいて、当該化合物が他のPDEアイソフォームにて著しい有効性を示し、クリアランスが高く、又脳透過性が限られていた事が報告されている(非特許文献33参照)。
細胞シグナルカスケードにおけるPDEの役割は、環状ヌクレオチドである環状アデノシン一リン酸(adenosine 3’,5’−cyclic monophosphate:cAMP)及び/又は環状グアノシン一リン酸(guanosine 3’,5’−cyclic monophosphate:cGMP)のホスホジエステル結合を加水分解すること、即ち、3’−エステル結合の加水分解を選択的に触媒し、不活性な5’−一リン酸を形成することで、代謝的に不活性化することである。
11種類のPDEファミリーは基質特異性に基づき、cAMP特異的PDE(PDE4、7、8)、cGMP特異的PDE(PDE5、6、9)、及び二重基質PDE(PDE1、2、3、10、11)の3つに分類される(非特許文献3、及び4参照)。
cAMP及びcGMPは、Gタンパク質結合受容体(GPCR、G Protein Cuppled Receptor)を介した細胞内情報伝達における重要なセカンドメッセンジャーであるため、PDEは、広範な生理学的機序に関与し、生物の恒常性において重要な役割を果たす。具体的には、炎症促進性メディエータの産生および作用、イオンチャネル機能、筋弛緩、学習および記憶形成、分化、アポトーシス、脂質生成、グリコーゲン分解ならびに糖新生等の種々の生理学的プロセスの制御に関わっている。とりわけ、神経細胞においては、神経細胞の分化及び生存とともに神経伝達の制御に重要な役割を果たしている(非特許文献5参照)。
cAMP及びcGMPによるこれらのプロセスの制御は、プロテインキナーゼA(PKA)及びプロテインキナーゼG(PKG)の活性化を伴い、転写因子、イオンチャネル及び受容体を含めた多様な生理的プロセスを制御している様々な基質がリン酸化される。cAMP及びcGMPの細胞内濃度は、細胞外からのシグナルに応答して変動し、cAMP及びcGMPの合成に関与する酵素(アデニルシクラーゼ(AC)およびグアニルシクラーゼ(GC))と、それら酵素の加水分解に関与するPDEとのバランスによって調節されている(非特許文献6参照)。
PDE2Aは、一次アミノ酸配列及び独特な酵素活性に基づいてファミリーが特定されており、PDE2A1、PDE2A2、及びPDE2A3等の複数のPDE2Aアイソフォームが報告されている。ヒトPDE2A3配列は、1997年に単離がされている(非特許文献7参照)。
PDE2Aは、cAMP又はcGMPの両方を代謝することができ、とりわけcGMPに対して、より高い親和性を有する二重基質酵素である。PDE2Aは、脳で高度に発現されており、又、多くの他の組織でも発現している事から、広範囲の機能と有用性を有している(非特許文献8参照)。更に、PDE2Aは、神経発達、学習及び記憶、プロラクチン及びアルドステロン分泌、骨細胞分化及び骨吸収、免疫学的反応、血管新生、炎症性細胞輸送、心収縮、血小板凝集、女性の性的興奮障害、骨関節炎痛、悪性黒色腫、及び低酸素性肺血管収縮、等の潜在的な治療可能性が示されている(特許文献1、及び2参照。非特許文献9〜24参照)。
PDE2Aを阻害する事で、統合失調症における認知記憶、社会的認知、及び作業記憶などの認知能力の欠損が改善され、認知機能が高まることが、複数の認知能力の前臨床モデルにおいて示されている(非特許文献25参照)。更に、PDE2Aの阻害は、老化及びアルツハイマー病において発症する認知障害も改善することが示されている(非特許文献26、及び27参照)。又、PDE2Aを阻害する事で、不安及びうつ病の前臨床モデルにおいて有効性を示すことも報告されている(非特許文献28、29、及び30参照)。
また、血管透過性の増大は、PDE2活性の増加に起因していることが示されている。内皮にあるPDE2及びPDE3は、偏頭痛に関連して、cGMPの濃度を検知するセンサー、又は内皮透過性を制御するスイッチとして作動している(非特許文献31、及び32参照)。
認知障害におけるPDE2阻害の役割は、Brandonらによって報告されている。PDE2阻害剤の1つであるBAY60−7550(CAS No.439083-90-6)の生化学プロファイル及び挙動プロファイルにおいて、当該化合物が他のPDEアイソフォームにて著しい有効性を示し、クリアランスが高く、又脳透過性が限られていた事が報告されている(非特許文献33参照)。
PDE2A阻害剤について、以下のような報告がある。例えば、PDE2A阻害剤として、国際公開第2012/114222号パンフレット(特許文献1)にはイミダゾ[5,1−f][1,2,4]トリアジン誘導体が、また国際公開第2013/161913号パンフレット(特許文献2)には2−オキソ−2,3−ジヒドロピリド[2,3−b]ピラジン−4(1H)−カルボキサミド誘導体などの化合物が開示されており、これらの文献にはPDE2A阻害剤が、精神障害(例えば、統合失調症(妄想型、解体型、緊張型、鑑別不能型、及び残遺型、等)、統合失調症様障害、統合失調感情障害(妄想型又は抑うつ型)、妄想性障害、物質誘導性精神障害(アルコール、アンフェタミン、大麻、コカイン、幻覚剤、肥満症、吸入剤、オピオイド、またはフェンシクリジンによって誘発された精神病)、妄想型人格障害、統合失調型の人格障害、等)、運動障害(例えば、ハンチントン病、ドーパミンアゴニスト治療に伴う異常運動症(ジスキネジア)、パーキンソン病、不穏下肢症候群、及び本態性振戦、等)、不安障害(例えば、強迫性障害、恐慌性障害、広場恐怖症、特定恐怖症、社会恐怖症、対人恐怖、心的外傷後ストレス障害、急性ストレス障害、及び全般性不安障害、等)、認知症(老年認知症、アルツハイマー病、多発脳梗塞性認知症、アルコール性認知症又は他の薬物関連認知症、頭蓋内腫瘍又は脳外傷に関連する認知症、ハンチントン病又はパーキンソン病に関連する認知症、エイズ関連認知症、前頭側頭型認知症、せん妄、及び健忘障害、等)、気分障害(気分エピソード)(例えば、大うつ病エピソード(軽度、中等度、または重度型)、躁病エピソード、混合性エピソード、または軽躁病エピソード、非定型うつ病エピソード、メランコリー型うつ病エピソード、緊張病性うつ病エピソード、産後発症気分エピソード、脳卒中後うつ病、季節性うつ病、大うつ病性障害、気分変調性障害/気分変調症、小うつ病性障害、月経前不快気分障害、統合失調症後うつ病性障害、精神障害に併発する大うつ病性障害、双極性障害(I型及びII型を含む。)、気分循環性障害、等)、神経変性障害(例えば、偏頭痛、てんかん、パーキンソン病、ハンチントン病、脳外傷に関連する神経変性、脳卒中に関連する神経変性、脳梗塞に関連する神経変性、低血糖誘発性神経変性、てんかん発作に関連する神経変性、神経毒中毒に関連する神経変性、多系統委縮症、及び線条体中型有棘ニューロンの神経変性、等)、睡眠障害(過眠症、概日リズム睡眠障害、不眠症、睡眠時異常行動、及び睡眠遮断、等)、摂食障害(食欲不振症、過食症、気晴らし食い障害、過食、及び氷食症、等)、薬物依存症、小児精神障害(注意欠陥障害、注意欠陥/多動性障害、行為障害、及び自閉症、等)、精神薄弱(ダウン症候群及び脆弱X症候群を含む。)、精神遅滞、学習障害(読字障害、算数障害、及び書字表出障害を含む。)、偏執傾向、肥満症、メタボリック症候群、インスリン非依存性糖尿病(NIDDM)、耐糖能障害、肺炎、変形性関節症、等の治療剤又は予防剤として使用できることも開示されている。
これらの知見によれば、PDE2A阻害剤は、神経内のcAMP及び/又はcGMPレベルを上昇させることにより、精神障害および神経変性障害、特に統合失調症やアルツハイマー病、うつ病、不安障害、及び行動障害等に対する治療及び/又は予防において、有用な治療薬としての可能性が期待される。
これらの知見によれば、PDE2A阻害剤は、神経内のcAMP及び/又はcGMPレベルを上昇させることにより、精神障害および神経変性障害、特に統合失調症やアルツハイマー病、うつ病、不安障害、及び行動障害等に対する治療及び/又は予防において、有用な治療薬としての可能性が期待される。
国際公開第2014/133046号パンフレット(特許文献3)に、PDE10阻害剤として、N−脂環式又はN−アリール−4−ヘテロアリールピラゾール−5−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2002/088097号パンフレット(特許文献4)に、プロテインキナーゼ阻害剤として、4,5’−ジ−1H−1,2,3−トリアゾール−5−カルボキサミド誘導体が開示されているが、本明細書中の化合物とは異なる。
国際公開第2014/064134号パンフレット(特許文献5)に、SKY阻害剤として、N−脂肪族基又はN−脂環式−3−ヘテロアリールピラゾール−4−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2010/111059号パンフレット(特許文献6)に、P2X3受容体拮抗剤として、1−アリール−3−ヘテロアリールピラゾール−4−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2007/052843号パンフレット(特許文献7)に、FXR阻害剤として、N−アリール−5−ヘテロアリールピラゾール−4−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2015/060368号パンフレット(特許文献8)に、PDE2A阻害剤として、N−アリールアルキル−2−アリール−チアゾール-4−カルボン酸アミド構造やN−アリールアルキル−ピリミジン−4−又はピラジン−2−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2002/088097号パンフレット(特許文献4)に、プロテインキナーゼ阻害剤として、4,5’−ジ−1H−1,2,3−トリアゾール−5−カルボキサミド誘導体が開示されているが、本明細書中の化合物とは異なる。
国際公開第2014/064134号パンフレット(特許文献5)に、SKY阻害剤として、N−脂肪族基又はN−脂環式−3−ヘテロアリールピラゾール−4−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2010/111059号パンフレット(特許文献6)に、P2X3受容体拮抗剤として、1−アリール−3−ヘテロアリールピラゾール−4−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2007/052843号パンフレット(特許文献7)に、FXR阻害剤として、N−アリール−5−ヘテロアリールピラゾール−4−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
国際公開第2015/060368号パンフレット(特許文献8)に、PDE2A阻害剤として、N−アリールアルキル−2−アリール−チアゾール-4−カルボン酸アミド構造やN−アリールアルキル−ピリミジン−4−又はピラジン−2−カルボン酸アミド構造を有する化合物が開示されているが、本明細書中の化合物とは異なる。
5−ヘテロアリール−1H−1,2,3−トリアゾール−4−カルボキサミド誘導体として、1−(2−クロロフェニル)−N−[1−(2−フラニル)エチル]−5−(2−ピリジニル)−1H−1,2,3−トリアゾール−4−カルボキサミド(CAS登録番号:1396856-78-2)、N−[1−(2−フラニル)エチル]−1−(2−メトキシフェニル)−5−(2−ピリジニル)−1H−1,2,3−トリアゾール−4−カルボキサミド(CAS登録番号:1396855-06-3)、1−(2−メトキシフェニル)−5−(2−ピリジニル)−N−[1−(2−チエニル)プロピル]−1H−1,2,3−トリアゾール−4−カルボキサミド(CAS登録番号:1396765-00-6)、1−(2−クロロフェニル)−5−(2−ピリジニル)−N−[1−(3−ピリジニル)エチル]−1H−1,2,3−トリアゾール−4−カルボキサミド(CAS登録番号:1396757-75-7)、及び1−(2−クロロフェニル)−5−(2−ピリジニル)−N−[1−(2−チエニル)プロピル]−1H−1,2,3−トリアゾール−4−カルボキサミド(CAS登録番号:1396708-53-4)等の化合物が開示されているが、何れの化合物も本明細書中の化合物とは異なる。
さて、医薬品開発においては、目的とする薬理活性のみでなく、吸収、分布、代謝、排泄等の各種の面で厳しいクライテリアを満たすことが要求される。例えば、薬物相互作用、脱感受性ないし耐性、経口投与時の消化管吸収、小腸内への移行速度、吸収速度と初回通過効果、臓器バリアー、蛋白結合、薬物代謝酵素の誘導や阻害、排泄経路や体内クリアランス、適用方法(適用部位、方法、目的)等において種々の検討課題が要求されており、医薬品としては目的とする薬理活性のみでなく、各種の厳しいクライテリアを満たすものが望まれてきている。
Essayan D M., J Allergy Clin Immunol, 108, p671-680, 2001.
Francis S H., Prog Nucleic Acid Res Mol Biol., 65, p1-52, 2001.
Soderling S H., Proc Natl Acad USA, 96(12), p7071-7076, 1999.
Chappie T A., Journal of Medicinal Chemistry, 55, p7299-7331, 2012.
Menniti F S., Nat Rev Drug Discov, 5(8), p660-670, 2006.
Houslay M D., Cir Res, 100(7), p950-966, 2007.
Rosman G J., Gene, 191(1),p89-95, 1997.
J.A.Beavo, et. al., Rev.Physico.Biochem.Pharm., 135, p67-104,1999.
W.C.G. van Staveren, et. al., Brain Res., 888, p275, 2001.
J. O’Donnell, et. al., J. Pharm. Exp. Ther., 302, p249 ,2002.
M.O. Velardez, et. al., Eur. J. Endo., 143, 279 (2000)
N. Gallo-Payet, et. al., Endo., 140, 3594, 1999.
C. Allardt-Lamberg, et. al., Biochem. Pharm., 59, 1133, 2000.
S. Wakabayashi, et. al., J. Bone, Miner. Res., 17, 249,2002.
M.D. Houslay, et. al., Cell. Signal., 8, 97, 1996.
T. Keravis, et. al., J.Vasc. Res., 37, 235, 2000.
S.L. Wolda, et. al., J. Histochem. Cytochem., 47, 895, 1999.
R. Fischmeister, et. al., J. Clin. Invest., 99, 2710, 1997.
P. Donzeau-Gouge, et al., J. Physiol., 533, 329 ,2001.
D.J. Paterson, et. Al., Card. Res., 52, 446 ,2001.
R.J. Haslam, et. Al., Biochem. J., 323, 371, 1997.
M.Plummer et, al., Bioorganic & Medicinal Chemistry Letters, 23 (11), p3438-3442 及び p3443-3447,2013.
H. Morita, et al., Oncology Reports, 29, 1275-1284,2013.
J. Haynes, et. al., J. Pharm. Exp. Ther., 276, 752,1996.
Boess et al., Neuropharmacology, 47 (7),p1081-92, 2004.
Domek-Lopacinska and Strosznajder, Brain Research, 1216, p68-77, 2008.
Annerieke S.R. Sierksma, et. al., Neuropharmacology., 64,p124-136, 2013.
Masood et al., JPET 331 (2),p690-699, 2009.
Masood et al., JPET 326 (2),p369-379, 2008.
Reierson et al., Neurosci. Lett., 466 (3), p149-53, 2009.
Surapisitchat et al, Circulation Research,101, p811-818, 2007.
Duran et al., Cardiovascular Res.,87, p254-261, 2010.
Brandon, et. al., Annual Reports in Medicinal Chemistry, 42, p4-5, 2007.
現在、アルツハイマー病、統合失調症、アルツハイマー病又は統合失調症を伴う認知障害の薬物療法において、種々の治療薬が利用可能となっている。しかし一方で、薬剤に起因する副作用により、患者の治療満足度が低い状況であり、既存薬に比して、より良い薬剤プロファイルを有する新たな治療薬の開発が求められている。
PDE2A阻害剤は、前述の通り統合失調症、アルツハイマー病、統合失調症又はアルツハイマー病に伴う認知障害、うつ病、不安障害、及び行動障害、等の有用な治療薬として期待されているが、現時点では臨床開発が進行している段階であって、当該分野からの治療薬の上市には至っていない。
PDE2A阻害作用を有する化合物の報告例は複数あるが、前記の医薬品開発上の総合的課題は常にある。より具体的には、例えば、溶解性がよくないこと、代謝安定性が低く経口投与による全身曝露が困難であること、吸収性や持続性等の薬物動態が良好ではないこと、あるいは不整脈を起こす危険性があるhERG(human ether−a−go−go related gene)チャネルの阻害活性を示すこと、薬物代謝酵素(例えば、シトクロムP450等)の誘導あるいは阻害活性を示すことや高い蛋白結合率を示すなど、有用性や安全性の課題がある。これらの問題を可能な限り多く解決し、且つ有効性の高い化合物を見出すことが求められている。
本発明は、安全性が高く、有効性に優れたPDE2A阻害剤として有用な新規な化合物、を提供する。
PDE2A阻害剤は、前述の通り統合失調症、アルツハイマー病、統合失調症又はアルツハイマー病に伴う認知障害、うつ病、不安障害、及び行動障害、等の有用な治療薬として期待されているが、現時点では臨床開発が進行している段階であって、当該分野からの治療薬の上市には至っていない。
PDE2A阻害作用を有する化合物の報告例は複数あるが、前記の医薬品開発上の総合的課題は常にある。より具体的には、例えば、溶解性がよくないこと、代謝安定性が低く経口投与による全身曝露が困難であること、吸収性や持続性等の薬物動態が良好ではないこと、あるいは不整脈を起こす危険性があるhERG(human ether−a−go−go related gene)チャネルの阻害活性を示すこと、薬物代謝酵素(例えば、シトクロムP450等)の誘導あるいは阻害活性を示すことや高い蛋白結合率を示すなど、有用性や安全性の課題がある。これらの問題を可能な限り多く解決し、且つ有効性の高い化合物を見出すことが求められている。
本発明は、安全性が高く、有効性に優れたPDE2A阻害剤として有用な新規な化合物、を提供する。
本発明者らは、上記の課題を解決すべく、安全性が高く、及び/又は有効性に優れたPDE2A選択的阻害剤を得るべく、鋭意研究を重ねてきた結果、下記一般式(I)で表されるビアリールアミド構造を持つことを特徴とする化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物が、PDE2A選択的阻害作用を有することを見出した。本発明の化合物は、PDE2A選択的阻害作用を有し、統合失調症、アルツハイマー病、統合失調症又はアルツハイマー病に伴う認知障害、うつ病、不安障害、及び行動障害、等の改善作用を有する医薬の有効成分として有用である。
本発明の下記一般式(I)で表されるビアリールアミド構造を持つ化合物は、ピラゾール環の5位、又はトリアゾール環の5位カルボキサミド構造を有し、当該カルボキサミド構造が結合する炭素原子に隣接する窒素原子が置換された窒素原子であること、また、イソオキサゾール環の4位、又はピラゾール環の4位にカルボキサミド構造を有し、当該カルボキサミド構造が結合する炭素原子に隣接する原子が炭素原子であることを特徴とするものである。さらに、当該カルボキサミド構造が結合する炭素原子に隣接する反対側の炭素原子に窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個含有する、5〜14員のヘテロアリール環が結合している(但し、5〜14員のヘテロアリール環は、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する)ことを特徴とするものである。
そして、本発明の化合物がこのような特徴を有することにより、カルボキサミド構造に結合するアルキル鎖は必ずしも極性を有する官能基を有する必要がないことも本発明の化合物の特徴である。
即ち、本発明は、下記一般式(I)
そして、本発明の化合物がこのような特徴を有することにより、カルボキサミド構造に結合するアルキル鎖は必ずしも極性を有する官能基を有する必要がないことも本発明の化合物の特徴である。
即ち、本発明は、下記一般式(I)
[式(I)中、pは、0〜6の整数であり;qは、1〜5の整数であり;
環Qは、ベンゼン環、又は単環式ヘテロアリール環を表わし;
環Aは、窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個含有する、5〜14員のヘテロアリール環(但し、当該5〜14員のヘテロアリール環は、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する)を表わし;
次の部分構造式(PS−1)で表わされる環B:
環Qは、ベンゼン環、又は単環式ヘテロアリール環を表わし;
環Aは、窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個含有する、5〜14員のヘテロアリール環(但し、当該5〜14員のヘテロアリール環は、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する)を表わし;
次の部分構造式(PS−1)で表わされる環B:
は、次の式(PS−1−1):
次の式(PS−1−2):
次の式(PS−1−3):
又は次の式(PS−1−4):
から選択され;
R1は、各々独立して、ハロゲン原子、水酸基、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、及び−CONRARB(ここに、−NRARB、および−CONRARAにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表し;
R2a及びR2bは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環、及び環状エーテル環は、各々、−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよく(但し、R2a及びR2bが、同時に水素原子を表わすことはない);
R1は、各々独立して、ハロゲン原子、水酸基、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、及び−CONRARB(ここに、−NRARB、および−CONRARAにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表し;
R2a及びR2bは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環、及び環状エーテル環は、各々、−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよく(但し、R2a及びR2bが、同時に水素原子を表わすことはない);
R3は、各々独立して、水酸基、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、カルボキシ基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)、及びオキソ基からなる群から選らばれる基を表わすか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい;
R4aは、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4aにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく);
R4bは、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4bにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく)]で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物に関する。
また、本発明は、前記一般式(I)で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物、及び製薬上許容される担体を含有する医薬組成物に関する。
さらに、本発明は、前記一般式(I)で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物を有効成分とする、PDE2Aが関与する疾患の予防及び/又は治療剤に関する。
また、本発明は、本発明は、前記一般式(I)で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物を有効成分とする、PDE2A阻害剤に関する。
R4aは、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4aにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく);
R4bは、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4bにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく)]で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物に関する。
また、本発明は、前記一般式(I)で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物、及び製薬上許容される担体を含有する医薬組成物に関する。
さらに、本発明は、前記一般式(I)で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物を有効成分とする、PDE2Aが関与する疾患の予防及び/又は治療剤に関する。
また、本発明は、本発明は、前記一般式(I)で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物を有効成分とする、PDE2A阻害剤に関する。
本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物(以下、「本発明の化合物」ともいう。)は、PDE2A選択的阻害作用を有する化合物であり、統合失調症、アルツハイマー病、統合失調症又はアルツハイマー病に伴う認知障害、うつ病、不安障害、及び行動障害、等の改善作用を有している。また、本発明の化合物を有効成分として含有する医薬組成物は、経口投与可能であり、PDE2A阻害剤や、PDE2Aが関与する疾患、とりわけ統合失調症、アルツハイマー病、統合失調症又はアルツハイマー病に伴う認知障害、うつ病、不安障害、及び行動障害、等の予防及び/又は治療剤として期待される。更に、本発明の化合物は、溶解性が良好であること、代謝安定性が高いこと、優れた経口吸収性をもつこと、あるいはhERGチャネルの阻害作用が少ないこと、などの少なくとも一つ以上の特徴も有することから有用性が高い。
本発明は、以下の態様に示される下記一般式(I)で表されるビアリールアミド構造を持つことを特徴とする化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物、並びにそれらを有効成分として含有することを特徴とする医薬組成物、それらの医薬用途、及びPDE2A阻害剤に関する。
本発明の態様をより詳細に説明すれば、以下のとおりである。
[1]下記の一般式(I):
[1]下記の一般式(I):
[式(I)中、pは、0〜6の整数であり;qは、1〜5の整数であり;
環Qは、ベンゼン環、又は単環式ヘテロアリール環を表わし;
環Aは、窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個含有する、5〜14員のヘテロアリール環(但し、当該5〜14員のヘテロアリール環は、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する)を表わし;からなる群から選らばれるヘテロアリール環を表わし;
次の部分構造式(PS−1)で表わされる環B:
環Qは、ベンゼン環、又は単環式ヘテロアリール環を表わし;
環Aは、窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個含有する、5〜14員のヘテロアリール環(但し、当該5〜14員のヘテロアリール環は、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する)を表わし;からなる群から選らばれるヘテロアリール環を表わし;
次の部分構造式(PS−1)で表わされる環B:
は、次の式(PS−1−1):
次の式(PS−1−2):
次の式(PS−1−3):
又は次の式(PS−1−4):
から選択され;
R1は、各々独立して、ハロゲン原子、水酸基、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、及び−CONRARB(ここに、−NRARB、および−CONRARAにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表し;
R2a及びR2bは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環、及び環状エーテル環は、各々、−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよく(但し、R2a及びR2bが、同時に水素原子を表わすことはない);
R1は、各々独立して、ハロゲン原子、水酸基、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、及び−CONRARB(ここに、−NRARB、および−CONRARAにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表し;
R2a及びR2bは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、R2a及びR2bにおけるC1〜6アルキル基は、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環、及び環状エーテル環は、各々、−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよく(但し、R2a及びR2bが、同時に水素原子を表わすことはない);
R3は、各々独立して、水酸基、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、カルボキシ基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)、及びオキソ基からなる群から選らばれる基を表し;環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい;
R4aは、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4aにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく);
R4bは、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4bにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく)]で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物。
R4aは、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4aにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく);
R4bは、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基を表わし(R4bにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよく)]で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物。
[2]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−1)で表されるピラゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[3]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−2)で表されるトリアゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[4]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−3)で表されるイソオキサゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[5]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−4)で表されるピラゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[6]pが、p=0〜3である、前記[1]から[5]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[7]pが、p=0〜1である、前記[1]から[6]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。。
[3]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−2)で表されるトリアゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[4]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−3)で表されるイソオキサゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[5]環Bの前記部分構造式(PS−1)で表される環が、前記式(PS−1−4)で表されるピラゾール環である、前記[1]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[6]pが、p=0〜3である、前記[1]から[5]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[7]pが、p=0〜1である、前記[1]から[6]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。。
[8]qが、q=1〜3である、前記[1]から[7]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[9]qが、q=1〜2である、前記[1]から[8]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[10]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[1]から[9]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[11]環Qが、ベンゼン環である、前記[10]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[12]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[1]から[11]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[13]環Aが、チアゾール環、オキサゾール環、イソオキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[1]から[12]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[14]環Aが形成する基が、チアゾール−2−イル、オキサゾール−2−イル、イソオキサゾール−3−イル、1H−トリアゾール−4−イル、ピリジン−2−イル、ピリミジン−2−イル、ピリミジン−4−イル、ピラジン−2−イル、キノリン−2−イル、又はイソキノリン−3−イルである、前記[13]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[9]qが、q=1〜2である、前記[1]から[8]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[10]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[1]から[9]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[11]環Qが、ベンゼン環である、前記[10]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[12]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[1]から[11]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[13]環Aが、チアゾール環、オキサゾール環、イソオキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[1]から[12]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[14]環Aが形成する基が、チアゾール−2−イル、オキサゾール−2−イル、イソオキサゾール−3−イル、1H−トリアゾール−4−イル、ピリジン−2−イル、ピリミジン−2−イル、ピリミジン−4−イル、ピラジン−2−イル、キノリン−2−イル、又はイソキノリン−3−イルである、前記[13]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[15]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[1]から[14]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[16]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[1]から[15]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[17]R1が、シアノ基、メチル基、及びトリフルオロメチル基からなる群から選ばれる基を表す、前記[1]から[16]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[18]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[1]から[17]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[19]R2a及びR2bは、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[1]から[18]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[20]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、又はメトキシメチル基であり、R2a及びR2bにより形成される環が、シクロプロパン環、又はオキセタン環である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)前記[1]から[19]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[16]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[1]から[15]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[17]R1が、シアノ基、メチル基、及びトリフルオロメチル基からなる群から選ばれる基を表す、前記[1]から[16]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[18]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[1]から[17]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[19]R2a及びR2bは、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[1]から[18]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[20]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、又はメトキシメチル基であり、R2a及びR2bにより形成される環が、シクロプロパン環、又はオキセタン環である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)前記[1]から[19]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[21]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[1]から[20]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[22]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環(当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい)を形成する、前記[1]から[21]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[23]R3が、フッ素原子、臭素原子、及びトリフルオロメトキシ基からなる群から選ばれる基であるか、環Q上の2個のR3(q=2又はq>2)が一緒になって形成する3〜8員エーテル環が、2,2−ジフルオロジオソラン環である、前記[1]から[22]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[22]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環(当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい)を形成する、前記[1]から[21]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[23]R3が、フッ素原子、臭素原子、及びトリフルオロメトキシ基からなる群から選ばれる基であるか、環Q上の2個のR3(q=2又はq>2)が一緒になって形成する3〜8員エーテル環が、2,2−ジフルオロジオソラン環である、前記[1]から[22]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[24]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[1]から[23]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[25]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[1]から[24]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[26]R4aが、メチル基、エチル基、2,2,2−トリフルオロエチル基、2−メトキシエチル基、又はシクロプロピルメチル基である、前記[1]から[25]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[27]R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[1]から[26]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[28]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[1]から[27]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[29]R4bが、水素原子、又はメチル基である、前記[1]から[28]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[25]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[1]から[24]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[26]R4aが、メチル基、エチル基、2,2,2−トリフルオロエチル基、2−メトキシエチル基、又はシクロプロピルメチル基である、前記[1]から[25]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[27]R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[1]から[26]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[28]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[1]から[27]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[29]R4bが、水素原子、又はメチル基である、前記[1]から[28]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[30]pが0〜3の整数であり;qが1〜3の整数であり;環Qがベンゼン環又は6員ヘテロアリール環であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基であるか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)基であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)であり;R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[1]から[29]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[31]pが0〜1の整数であり;qが1〜2の整数であり;環Qが、ベンゼン環であり;環Aが、チアゾール環、オキサゾール環、イソオキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環(当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい)を形成するものであり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[1]から[30]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[31]pが0〜1の整数であり;qが1〜2の整数であり;環Qが、ベンゼン環であり;環Aが、チアゾール環、オキサゾール環、イソオキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環(当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい)を形成するものであり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[1]から[30]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[32]下記式(I−a):
[式(I−a)中、p、q、環A、環Q、R1、R2a、R2b、R3、及びR4aは前記[1]中の定義と同じである]で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[33]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[32]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[33]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[32]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[34]pが、p=0〜3の整数である、前記[32]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[35]pが、p=0〜1の整数である、前記[32]又は[33]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[36]qが、q=1〜3の整数である、前記[32]から[35]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[37]qが、q=1〜2の整数である、前記[32]から[36]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[38]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[32]から[37]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[39]環Qが、ベンゼン環である、前記[32]から[38]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[35]pが、p=0〜1の整数である、前記[32]又は[33]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[36]qが、q=1〜3の整数である、前記[32]から[35]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[37]qが、q=1〜2の整数である、前記[32]から[36]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[38]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[32]から[37]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[39]環Qが、ベンゼン環である、前記[32]から[38]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[40]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[32]から[39]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[41]環Aが、チアゾール環、オキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[32]から[40]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[42]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[32]から[41]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[43]環Aが形成する基が、チアゾール−2−イル、オキサゾール−2−イル、1H−トリアゾール−4−イル、ピリジン−2−イル、ピリミジン−2−イル、ピリミジン−4−イル、ピラジン−2−イル、キノリン−2−イル、又はイソキノリン−3−イルである、前記[32]から[42]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[41]環Aが、チアゾール環、オキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[32]から[40]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[42]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[32]から[41]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[43]環Aが形成する基が、チアゾール−2−イル、オキサゾール−2−イル、1H−トリアゾール−4−イル、ピリジン−2−イル、ピリミジン−2−イル、ピリミジン−4−イル、ピラジン−2−イル、キノリン−2−イル、又はイソキノリン−3−イルである、前記[32]から[42]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[44]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[32]から[43]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[45]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[32]から[44]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物
[45]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[32]から[44]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物
[46]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[32]から[45]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[47]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[32]から[46]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[47]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[32]から[46]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[48]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[32]から[47]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[49]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[32]から[48]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[50]R3が、フッ素原子、臭素原子、及びトリフルオロメトキシ基からなる群から選ばれる基である、前記[32]から[49]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[49]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[32]から[48]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[50]R3が、フッ素原子、臭素原子、及びトリフルオロメトキシ基からなる群から選ばれる基である、前記[32]から[49]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[51]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[32]から[50]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[52]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[32]から[51]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[52]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[32]から[51]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[53]pがp=0〜3の整数であり;qが1〜3の整数であり;環Qがベンゼン環、又は6員ヘテロアリール環であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[32]から[52]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[54]pが0〜1の整数であり;qが1〜2の整数であり;環Qがベンゼン環であり;環Aが、チアゾール環、オキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよいであり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[32]から[53]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[55]下記式(I−aa):
[式(I−aa)中、p、q、環A、R1、R2a、R2b、R3、及びR4aは、前記[2]中の定義と同じであり;Q1、Q2、Q3、Q4、及びQ5は、各々独立して、NまたはC−Hを表す]で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[56]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[55]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[56]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[55]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[57]pが、p=0〜3の整数、又はp=0〜1の整数である、前記[55]又は[56]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[58]qが、q=1〜3の整数である、前記[55]から[57]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[59]qが、q=1〜2の整数である、前記[55]から[58]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[58]qが、q=1〜3の整数である、前記[55]から[57]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[59]qが、q=1〜2の整数である、前記[55]から[58]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[60]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)である、前記[55]から[59]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[61]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[55]から[60]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[61]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[55]から[60]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[62]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[55]から[61]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[63]環Aが、チアゾール環、オキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[55]から[62]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[64]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[55]から[63]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[63]環Aが、チアゾール環、オキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[55]から[62]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[64]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[55]から[63]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[65]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[55]から[64]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[66]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[55]から[65]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[66]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[55]から[65]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[67]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[55]から[66]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[68]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[55]から[67]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[68]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[55]から[67]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[69]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[55]から[68]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[70]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[55]から[69]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[70]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[55]から[69]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[71]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[55]から[70]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[72]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[55]から[71]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[72]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[55]から[71]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[73]前記[55]の一般式(I−aa)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1)又は部分構造式(PS−2−2):
[部分構造式(PS−2−1)、及び部分構造式(PS−2−2)において、Q1、Q2、Q4、及びQ5は、各々独立して、NまたはC−Hを表し、R3は前記してきた定義と同じである。]
を表わす、前記[55]から[72]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[74]前記の一般式(I−aa)における次の部分構造式(PS−2):
を表わす、前記[55]から[72]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[74]前記の一般式(I−aa)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1):
[部分構造式(PS−2−1−1)及び部分構造式(PS−2−2−1)において、R3は、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す。]
で表される、前記[55]から[73]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[75]前記の一般式(I−aa)における前記の部分構造式(PS−2)で表される基が、4−ブロモフェニル基、4−(トリフルオロメチル)フェニル基、3−フルオロ−4−(トリフルオロメトキシ)フェニル基、又は2,2−ジフルオロベンゾ[d][1,3]ジオキソニル基である、前記[73]又は[74]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。。
で表される、前記[55]から[73]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[75]前記の一般式(I−aa)における前記の部分構造式(PS−2)で表される基が、4−ブロモフェニル基、4−(トリフルオロメチル)フェニル基、3−フルオロ−4−(トリフルオロメトキシ)フェニル基、又は2,2−ジフルオロベンゾ[d][1,3]ジオキソニル基である、前記[73]又は[74]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。。
[76]pが0〜3の整数であり;qが1〜3の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1)又は部分構造式(PS−2−2)であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[55]から[75]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[77]pが0〜1の整数であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、チアゾール環、オキサゾール環、1H−トリアゾール環、ピリジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよいであり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[55]から[76]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[78]下記式(I−b):
[78]下記式(I−b):
[式(I−b)中、p、q、環A、環Q、R1、R2a、R2b、R3、及びR4aは前記の[1]での定義と同じである。]
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[79]環Aが、トリアゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[78]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[80]pが、p=0〜3の整数、又はp=0である、前記[78]又は[79]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[80]pが、p=0〜3の整数、又はp=0である、前記[78]又は[79]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[81]qが、q=1〜3の整数である、前記[78]から[80]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[82]qが、q=1〜2の整数である、前記[78]から[81]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[82]qが、q=1〜2の整数である、前記[78]から[81]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[83]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[78]から[82]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[84]環Qが、ベンゼン環である、前記[78]から[83]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[84]環Qが、ベンゼン環である、前記[78]から[83]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[85]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[78]から[84]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[86]環Aが、ピリジン環、又はピラジン環である、前記[78]から[85]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[87]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[78]から[86]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[88]環Aが形成する基が、ピリジン−2−イル、又はピラジン−2−イルである、前記[78]から[87]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[86]環Aが、ピリジン環、又はピラジン環である、前記[78]から[85]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[87]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[78]から[86]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[88]環Aが形成する基が、ピリジン−2−イル、又はピラジン−2−イルである、前記[78]から[87]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[89]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[78]から[88]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[90]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[78]から[89]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[90]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[78]から[89]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[91]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[78]から[90]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[92]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[78]から[91]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[93]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、又はメトキシメチル基である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[78]から[92]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[92]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[78]から[91]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[93]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、又はメトキシメチル基である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[78]から[92]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[94]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[78]から[93]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[95]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[78]から[94]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[96]R3が、フッ素原子、及びトリフルオロメトキシ基からなる群から選ばれる基である、前記[78]から[95]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[95]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[78]から[94]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[96]R3が、フッ素原子、及びトリフルオロメトキシ基からなる群から選ばれる基である、前記[78]から[95]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[97]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[78]から[96]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[98]R4aが、C1〜6アルキル基である、前記[78]から[97]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[99]R4aが、メチル基である、前記[78]から[98]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[98]R4aが、C1〜6アルキル基である、前記[78]から[97]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[99]R4aが、メチル基である、前記[78]から[98]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[100]pが0〜3の整数であり;qが1〜3の整数であり;環Qが、ベンゼン環、又は6員ヘテロアリール環であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[78]から[99]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[101]pが0であり;qが1〜2の整数であり;環Qがベンゼン環であり;環Aがピリジン環、又はピラジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4aが、C1〜6アルキル基、前記[78]から[100]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物である。
[101]pが0であり;qが1〜2の整数であり;環Qがベンゼン環であり;環Aがピリジン環、又はピラジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4aが、C1〜6アルキル基、前記[78]から[100]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物である。
[102]下記式(I−bb):
[式(I−bb)中、p、q、環A、R1、R2a、R2b、R3、及びR4aは前記の[78]での定義と同じであり;Q1、Q2、Q3、Q4、及びQ5は、各々独立して、NまたはC−Hを表す]で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[103]環Aが、トリアゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[102]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[103]環Aが、トリアゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[102]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[104]pが、p=0〜3の整数、又はp=0である、前記[102]又は[103]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[105]qが、q=1〜3の整数である、前記[102]から[104]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[106]qが、q=1〜2の整数である、前記[102]から[105]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[105]qが、q=1〜3の整数である、前記[102]から[104]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[106]qが、q=1〜2の整数である、前記[102]から[105]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[107]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)である、前記[102]から[106]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[108]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[102]から[107]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[108]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[102]から[107]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[109]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[102]から[108]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[110]環Aが、ピリジン環、又はピラジン環である、前記[102]から[109]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[111]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[102]から[110]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[110]環Aが、ピリジン環、又はピラジン環である、前記[102]から[109]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[111]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[102]から[110]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[112]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[102]から[111]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[113]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[102]から[112]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[113]R1が、各々独立して、シアノ基、C1〜6アルキル基、及びハロゲン化C1〜6アルキル基からなる群から選らばれる基を表す、前記[102]から[112]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[114]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[102]から[113]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[115]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[102]から[114]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[115]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[102]から[114]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[116]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[102]から[115]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[117]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[102]から[116]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[117]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[102]から[116]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[118]R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[102]から[117]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[119]R4aが、C1〜6アルキル基である、前記[102]から[118]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[119]R4aが、C1〜6アルキル基である、前記[102]から[118]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[120]前記[102]の一般式(I−bb)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1)又は部分構造式(PS−2−2):
[部分構造式(PS−2−1)、及び部分構造式(PS−2−2)において、Q1、Q2、Q4、及びQ5は、各々独立して、NまたはC−Hを表し、R3は、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい。]
を表わされる、前記[102]から[119]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[121]前記[102]の一般式(I−bb)における次の部分構造式(PS−2):
を表わされる、前記[102]から[119]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[121]前記[102]の一般式(I−bb)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1):
[部分構造式(PS−2−1−1)及び部分構造式(PS−2−2−1)において、R3は、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す。]
で表される、前記[102]から[120]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[122]前記[102]の一般式(I−bb)における前記の部分構造式(PS−2)で表される基が、4−(トリフルオロメチル)フェニル基、又は3−フルオロ−4−(トリフルオロメトキシ)フェニル基である、前記[102]から[121]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される、前記[102]から[120]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[122]前記[102]の一般式(I−bb)における前記の部分構造式(PS−2)で表される基が、4−(トリフルオロメチル)フェニル基、又は3−フルオロ−4−(トリフルオロメトキシ)フェニル基である、前記[102]から[121]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[123]pが0〜3の整数であり;qが1〜3の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1)又は部分構造式(PS−2−2)であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4aが、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4aにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[102]から[122]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[124]pが0であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、ピリジン環、又はピラジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4aが、C1〜6アルキル基である、前記[102]から[123]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[125]下記式(I−c):
[124]pが0であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、ピリジン環、又はピラジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4aが、C1〜6アルキル基である、前記[102]から[123]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[125]下記式(I−c):
[式(I−c)中、p、q、環A、環Q、R1、R2a、R2b、R3、及びR4bは前記[1]での定義と同じである。]
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[126]環Aが、イソオキサゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[125]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[126]環Aが、イソオキサゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[125]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[127]pが、p=0〜3の整数、又はp=0〜1の整数である、前記[125]又は[126]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和。
[128]qが、q=1〜3の整数である、前記[125]から[127]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[129]qが、q=1〜2の整数である、前記[125]から[128]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[130]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[125]から[129]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[131]環Qが、ベンゼン環である、前記[125]から[130]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[128]qが、q=1〜3の整数である、前記[125]から[127]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[129]qが、q=1〜2の整数である、前記[125]から[128]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[130]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[125]から[129]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[131]環Qが、ベンゼン環である、前記[125]から[130]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[132]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[125]から[131]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[133]環Aが、イソオキサゾール環、又はピリジン環である、前記[125]から[132]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[134]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[125]から[133]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[135]環Aが形成する基が、イソオキサゾール−3−イル、又はピリミジン−2−イル等である、前記[134]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[133]環Aが、イソオキサゾール環、又はピリジン環である、前記[125]から[132]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[134]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[125]から[133]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[135]環Aが形成する基が、イソオキサゾール−3−イル、又はピリミジン−2−イル等である、前記[134]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[136]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[125]から[135]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[137]R1が、各々独立して、C1〜6アルキル基を表す、前記[125]から[136]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[138]R1が、メチル基等である、前記[125]から[137]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[137]R1が、各々独立して、C1〜6アルキル基を表す、前記[125]から[136]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[138]R1が、メチル基等である、前記[125]から[137]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[139]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[125]から[138]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[140]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[125]から[139]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[141]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、又はメトキシメチル基であり、R2a及びR2bにより形成される環状エーテル環が、オキセタン環である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[125]から[140]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[140]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[125]から[139]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[141]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、又はメトキシメチル基であり、R2a及びR2bにより形成される環状エーテル環が、オキセタン環である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[125]から[140]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[142]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[125]から[141]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[143]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい、前記[125]から[142]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[144]R3が、フッ素原子、及びトリフルオロメトキシ基からなる群から選ばれる基であるか、環Q上の2個のR3(q=2又はq>2)が一緒になって2,2−ジフルオロジオソラン環を形成している、前記[125]から[143]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[143]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい、前記[125]から[142]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[144]R3が、フッ素原子、及びトリフルオロメトキシ基からなる群から選ばれる基であるか、環Q上の2個のR3(q=2又はq>2)が一緒になって2,2−ジフルオロジオソラン環を形成している、前記[125]から[143]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[145]R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[125]から[144]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[146]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[125]から[145]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[146]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[125]から[145]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[147]pが0〜3の整数であり;qが1〜3の整数であり;環Qが、ベンゼン環、又は6員ヘテロアリール環であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[125]から[146]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[148]pが0〜1の整数であり;qが1〜2の整数であり;環Qが、ベンゼン環であり;環Aが、イソオキサゾール環、又はピリジン環であり;R1が、各々独立して、C1〜6アルキル基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい基であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[125]から[147]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[148]pが0〜1の整数であり;qが1〜2の整数であり;環Qが、ベンゼン環であり;環Aが、イソオキサゾール環、又はピリジン環であり;R1が、各々独立して、C1〜6アルキル基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい基であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[125]から[147]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[149]下記式(I−cc):
[式(I−cc)中、p、q、環A、R1、R2a、R2b、R3、及びR4bは前記[78]での定義と同じであり;Q1、Q2、Q3、Q4、及びQ5は、各々独立して、NまたはC−Hを表す。]
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[150]環Aが、イソオキサゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[149]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[150]環Aが、イソオキサゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[149]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[151]pが、p=0〜3の整数、又はp=0〜1の整数である、前記[149]又は[150]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[152]qが、q=1〜3の整数である、前記[149]から[151]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[153]qが、q=1〜2の整数である、前記[149]から[152]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[154]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)である、前記[149]から[153]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[155]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[149]から[154]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[152]qが、q=1〜3の整数である、前記[149]から[151]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[153]qが、q=1〜2の整数である、前記[149]から[152]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[154]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)である、前記[149]から[153]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[155]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[149]から[154]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[156]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[149]から[155]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[157]環Aが、イソオキサゾール環、又はピリジン環である、前記[149]から[156]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[158]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[149]から[157]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[157]環Aが、イソオキサゾール環、又はピリジン環である、前記[149]から[156]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[158]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[149]から[157]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[159]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[149]から[158]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[160]R1が、各々独立して、C1〜6アルキル基を表す、前記[149]から[159]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[160]R1が、各々独立して、C1〜6アルキル基を表す、前記[149]から[159]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[161]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[149]から[160]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[162]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[149]から[161]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[162]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[149]から[161]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[163]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[149]から[162]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[164]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい、前記[149]から[163]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[164]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい、前記[149]から[163]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[165]R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[149]から[164]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[166]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[149]から[165]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[166]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[149]から[165]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[167]前記[149]の一般式(I−cc)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1)又は部分構造式(PS−2−2):
[部分構造式(PS−2−1)、及び部分構造式(PS−2−2)において、Q1、Q2、Q4、及びQ5は、各々独立して、NまたはC−Hを表し、R3は、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい。]
で表わさせれる基である、前記[149]から[166]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[168]前記の一般式(I−cc)における次の部分構造式(PS−2):
で表わさせれる基である、前記[149]から[166]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[168]前記の一般式(I−cc)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1):
[部分構造式(PS−2−1−1)および部分構造式(PS−2−2−1)において、R3は、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよい。]
で表される、前記[149]から[167]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[169]前記[149]の一般式(I−cc)における前記の部分構造式(PS−2)で表される基が、4−(トリフルオロメチル)フェニル基、3−フルオロ−4−(トリフルオロメトキシ)フェニル基、又は2,2−ジフルオロベンゾ[d][1,3]ジオキソニル基である、前記[149]から[168]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される、前記[149]から[167]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[169]前記[149]の一般式(I−cc)における前記の部分構造式(PS−2)で表される基が、4−(トリフルオロメチル)フェニル基、3−フルオロ−4−(トリフルオロメトキシ)フェニル基、又は2,2−ジフルオロベンゾ[d][1,3]ジオキソニル基である、前記[149]から[168]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[170]pが0〜3の整数であり;qが1〜3の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1)又は部分構造式(PS−2−2)であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[149]から[169]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[171]pが0〜1の整数であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、イソオキサゾール環、又はピリジン環であり;R1が、各々独立して、C1〜6アルキル基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよいであり;R4bが、水素原子、又はC1〜6アルキル基である、前記[149]から[170]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[171]pが0〜1の整数であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、イソオキサゾール環、又はピリジン環であり;R1が、各々独立して、C1〜6アルキル基であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々が結合する際にさらに酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、又はR2a及びR2bによって形成される環状エーテル環は、各々、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子で1〜3個置換されていてもよいであり;R4bが、水素原子、又はC1〜6アルキル基である、前記[149]から[170]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[172]下記式(I−d):
[式(I−d)中、p、q、環A、環Q、R1、R2a、R2b、R3、及びR4bは前記[1]での定義と同じである。]
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[173]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[172]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[173]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[172]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[174]pが、p=0〜3の整数、又はp=0である、前記[172]又は[173]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[175]qが、q=1〜3の整数である、前記[172]から[174]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[176]qが、q=1〜2の整数である、前記[172]から[175]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[175]qが、q=1〜3の整数である、前記[172]から[174]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[176]qが、q=1〜2の整数である、前記[172]から[175]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[177]環Qが、ベンゼン環、又は6員ヘテロアリール環である、前記[172]から[176]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[178]環Qが、ベンゼン環である、前記[172]から[177]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[178]環Qが、ベンゼン環である、前記[172]から[177]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[179]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[172]から[178]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[180]環Aが、チアゾール環、又はピリジン環である、前記[172]から[179]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[181]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[172]から[180]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[182]環Aが形成する基が、チアゾール−2−イル、又はピリジン−2−イル等である、前記[172]から[181]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[180]環Aが、チアゾール環、又はピリジン環である、前記[172]から[179]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[181]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[172]から[180]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[182]環Aが形成する基が、チアゾール−2−イル、又はピリジン−2−イル等である、前記[172]から[181]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[183]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[172]から[182]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[184]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[172]から[183]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[185]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[172]から[184]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[186]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、及びメトキシメチル基からなる群から選ばれる基である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[172]から[185]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[185]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい、前記[172]から[184]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[186]R2a及びR2bが、水素原子、メチル基、1−ヒドロキシ−1−メチル−エチル基、及びメトキシメチル基からなる群から選ばれる基である(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[172]から[185]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[187]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[172]から[186]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[188]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[172]から[187]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[189]R3が、各々独立して、フッ素原子、及びトリフルオロメトキシ基からなる群から選ばれるきである、前記[172]から[188]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[188]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[172]から[187]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[189]R3が、各々独立して、フッ素原子、及びトリフルオロメトキシ基からなる群から選ばれるきである、前記[172]から[188]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[190]R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[172]から[189]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[191]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[172]から[190]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[191]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[172]から[190]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[192]pが0〜3の整数であり;qが1〜3の整数であり;環Qが、ベンゼン環、又は6員ヘテロアリール環であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよいであり;R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[172]から[191]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[193]pが0であり;qが1〜2の整数であり;環Qが、ベンゼン環であり;環Aが、チアゾール環、又はピリジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[172]から[192]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[193]pが0であり;qが1〜2の整数であり;環Qが、ベンゼン環であり;環Aが、チアゾール環、又はピリジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[172]から[192]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[194]下記式(I−dd):
[式(I−dd)中、p、q、環A、R1、R2a、R2b、R3、及びR4bは前記[172]での定義と同じであり;Q1、Q2、Q3、Q4、及びQ5は、各々独立して、NまたはC−Hを表す。]
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[195]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[194]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[195]環Aが、ピラゾール環と結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[194]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[196]pが、p=0〜3の整数、又はp=0である、前記[194]又は[195]に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[197]qが、q=1〜3の整数である、前記[194]から[196]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[198]qが、q=1〜2の整数である、前記[194]から[197]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[197]qが、q=1〜3の整数である、前記[194]から[196]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[198]qが、q=1〜2の整数である、前記[194]から[197]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[199]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)である、前記[194]から[198]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[200]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[194]から[199]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[200]Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)である、前記[194]から[199]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[201]環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環である、前記[194]から[200]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[202]環Aが、チアゾール環、又はピリジン環である、前記[194]から[201]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[203]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[194]から[202]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[202]環Aが、チアゾール環、又はピリジン環である、前記[194]から[201]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[203]環Aが、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する、前記[194]から[202]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[204]R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[194]から[203]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[205]R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)、前記[194]から[204]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[206]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基である、前記[194]から[205]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[206]R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基である、前記[194]から[205]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[207]R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい、前記[194]から[206]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[208]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[194]から[207]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[208]R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す、前記[194]から[207]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[209]R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)、前記[194]から[208]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[210]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[194]から[209]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[210]R4bが、水素原子、又はC1〜6アルキル基を表す、前記[194]から[209]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[211]前記[194]の一般式(I−dd)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1)又は部分構造式(PS−2−2):
[部分構造式(PS−2−1)、及び部分構造式(PS−2−2)において、Q1、Q2、Q4、及びQ5は、各々独立して、NまたはC−Hを表し、R3は、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい。]
で表わされる、前記[194]から[210]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[212]前記[194]の一般式(I−dd)における次の部分構造式(PS−2):
で表わされる、前記[194]から[210]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[212]前記[194]の一般式(I−dd)における次の部分構造式(PS−2):
が、次の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1):
[部分構造式(PS−2−1−1)および部分構造式(PS−2−2−1)において、R3は、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表す。]
で表される、前記[194]から[211]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[213]前記[194]の一般式(I−dd)における前記の部分構造式(PS−2)で表される基が、4−(トリフルオロメチル)フェニル基、又は3−フルオロ−4−(トリフルオロメトキシ)フェニル基である、前記[194]から[212]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
で表される、前記[194]から[211]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[213]前記[194]の一般式(I−dd)における前記の部分構造式(PS−2)で表される基が、4−(トリフルオロメチル)フェニル基、又は3−フルオロ−4−(トリフルオロメトキシ)フェニル基である、前記[194]から[212]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[214]pが0〜3の整数であり;qが1〜3の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)、(Q1=Q2=Q3=Q4=C−H、Q5=N)、又は(Q2=N、Q1=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1)又は部分構造式(PS−2−2)であり;環Aが、チアゾール環、オキサゾール環、1H−イミダゾール環、イソチアゾール環、イソオキサゾール環、1H−ピラゾール環、チアジアゾール環、オキサジアゾール環、1H−トリアゾール環、ピリジン環、ピリダジン環、ピリミジン環、ピラジン環、キノリン環、又はイソキノリン環であり;R1が、各々独立して、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基を表すであり;R2a及びR2bが、各々独立して、水素原子、C1〜6アルキル基、又はC3〜8シクロアルキル基を表わすか、R2a及びR2bにおけるC1〜6アルキル基が、各々結合することにより、隣接する炭素原子と共にC3〜8シクロアルキル環を形成するか、又はR2a及びR2bにおけるC1〜6アルキル基の各々が結合する際にさらに酸素原子を含んで、隣接する炭素原子と共に環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、C3〜8シクロアルキル基、又はR2a及びR2bによって形成されるC3〜8シクロアルキル環および環状エーテル環は、各々、−OH、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい(但し、R2a及びR2bが、同時に水素原子を表わすことはない)であり;R3が、各々独立して、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、及び−SO2NRARB(ここに、前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)を表わす)からなる群から選らばれる基を表すか、環Q上の2個のR3(q=2又はq>2)がそれぞれ独立してC1〜6アルキル基及び/又は−O−(C1〜6アルキル基)であって、当該2個のR3基が隣接位に置換している場合は、当該各R3が結合することにより、隣接する原子と共に3〜8員エーテル環を形成してもよく、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、及びオキソ基からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R4bが、水素原子、C1〜6アルキル基、又はハロゲン化C1〜6アルキル基を表す(R4bにおける、当該C1〜6アルキル基、又はハロゲン化C1〜6アルキル基は、ハロゲン原子、−O−(C1〜6アルキル基)、及びC3〜8シクロアルキル基からなる群から選らばれる基で1〜3個置換されていてもよい)である、前記[194]から[213]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[215]pが0であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、チアゾール環、又はピリジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[194]から[214]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[215]pが0であり;qが1〜2の整数であり;Q1、Q2、Q3、及びQ4の組み合わせが、(Q1=Q2=Q3=Q4=Q5=C−H)であり;部分構造式(PS−2)が、前記の部分構造式(PS−2−1−1)、又は部分構造式(PS−2−2−1)であり;環Aが、チアゾール環、又はピリジン環であり;R2a及びR2bが、各々独立して、水素原子、又はC1〜6アルキル基を表わし;R2a及びR2bにおける当該C1〜6アルキル基は、−OH、C1〜6アルキル基、及び−O−(C1〜6アルキル基)からなる群から選らばれる基で1〜3個置換されていてもよい基であり;R3が、各々独立して、ハロゲン原子、及び−O−(ハロゲン化C1〜6アルキル基)からなる群から選らばれる基であり;R4bが、水素原子、又はC1〜6アルキル基である、前記[194]から[214]のいずれか1項に記載の化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[216]以下に記載される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物、或いはそれらの光学異性体。(なお、以下に表される化合物の名称は、ChemBioDraw(登録商標) Ultra 14(CambridgeSoft)の化合物名称命名プログラムに従って得られる英語名称に基づくものである。)
(1) 1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(2) (R)−N−(1−(4−ブロモフェニル)エチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(3) N−(1−(4−ブロモフェニル)シクロプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(4) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(5) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(6) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(7) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(8) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(9) 1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−1H−ピラゾール−5−カルボキサミド;
(10) (R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(1) 1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(2) (R)−N−(1−(4−ブロモフェニル)エチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(3) N−(1−(4−ブロモフェニル)シクロプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(4) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(5) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(6) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(7) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(8) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(9) 1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−1H−ピラゾール−5−カルボキサミド;
(10) (R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(11) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(12) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(13) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(14) 1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(15) 1−メチル−4−(2−メチルピリミジン−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(16) 1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(17) (R)−1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(18) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(19) 4−(4−シアノチアゾール−2−イル)−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(20) (R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(12) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(13) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(14) 1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(15) 1−メチル−4−(2−メチルピリミジン−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(16) 1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(17) (R)−1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(18) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(19) 4−(4−シアノチアゾール−2−イル)−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(20) (R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(21) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミド;
(22) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミド;
(23) 1−メチル−4−(ピリミジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(24) (R)−1−メチル−4−(キノリン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(25) (R)−1−エチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(26)(S)−1−エチル−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(27) 1−エチル−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(28) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(29) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(30) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(22) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミド;
(23) 1−メチル−4−(ピリミジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(24) (R)−1−メチル−4−(キノリン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(25) (R)−1−エチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(26)(S)−1−エチル−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(27) 1−エチル−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(28) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(29) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(30) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(31) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
(32) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
(33) (S)−1−(シクロプロピルメチル)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(34) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミド;
(35) (R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(36) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(37) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(38) (R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(39) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(40) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(32) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
(33) (S)−1−(シクロプロピルメチル)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(34) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミド;
(35) (R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(36) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(37) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(38) (R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(39) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(40) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(41) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(42) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(43) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(44) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(45) (R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(46) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(47) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(48) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(49) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(50) (S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(42) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(43) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(44) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(45) (R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(46) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(47) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(48) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(49) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(50) (S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(51) 3’,5−ジメチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(52) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(53) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(54) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(55) 3’,5−ジメチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(56) (R)−5−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(57) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(58) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(59) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(60)(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(52) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(53) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(54) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(55) 3’,5−ジメチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(56) (R)−5−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(57) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(58) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(59) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(60)(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(61) (S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(62) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(63) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(64) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(65) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(66) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(67) 3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
(68) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(69) 1−メチル−3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
(70) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(71) 1−メチル−3−(チアゾール−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド、又は
(72) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(チアゾール−2−イル)−1H−ピラゾール−4−カルボキサミド。
(62) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(63) N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(64) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(65) (S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(66) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(67) 3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
(68) (S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(69) 1−メチル−3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
(70) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(71) 1−メチル−3−(チアゾール−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド、又は
(72) N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(チアゾール−2−イル)−1H−ピラゾール−4−カルボキサミド。
[217]前記[1]から[216]のいずれか一項に記載された化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物の少なくともひとつの化合物、及び製薬上許容される担体を含有する医薬組成物。
[218]医薬組成物が、PDE2Aが関与する疾患の予防及び/又は治療のためのものである、前記[217]に記載の医薬組成物。
[219]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症、からなる群から選択される少なくとも1つの疾患である、前記[217]又は[218]に記載の医薬組成物。
[220]医薬組成物が、さらに他の予防及び/又は治療薬(他の薬剤)の有効成分を含有してなる、[217]から[219]のいずれか一項に記載の医薬組成物。
[221]医薬組成物が、他の予防及び/又は治療薬(他の薬剤)と併用して使用されるものである、[217]から[219]のいずれか一項に記載の医薬組成物。
[222]他の予防及び/又は治療薬(他の薬剤)が、(1)非定型抗精神病薬、(2)定型抗精神病薬、(3)選択的セロトニン再取り込み阻害薬(SSRI)、(4)選択的セロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)、(5)選択的ノルアドレナリン・ドーパミン再取り込み阻害薬(NDRI)、(6)ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA)、(7)セロトニン・ノルアドレナリン・ドパミン三重モノアミン再取り込み阻害剤、(8)双極性障害治療薬、(9)てんかん治療薬、(10)多発性硬化症治療薬、(11)ハンチントン病治療薬、(12)トリアゾロピリジン系抗うつ薬(SARI)、(13)四環系抗うつ薬、(14)三環系抗うつ薬、(15)その他抗うつ薬、(16)α7ニコチン受容体作動薬、(17)α7ニコチン受容体活性調節薬、(18)α7ニコチン受容体部分調節薬、(19)PDE阻害薬、(20)NK2拮抗薬、(21)NK3拮抗薬、(22)ムスカリン型M1アセチルコリン受容体活性調節薬、(23)ムスカリン型M2アセチルコリン受容体活性調節薬、(24)アデノシン受容体調節薬、(25)ムスカリン型M4アセチルコリン受容体活性調節薬、(26)ムスカリン型M5アセチルコリン受容体活性調節薬、(27)アデノシン受容体調節薬、(28)グリシントランスポーター1(GlyT1)阻害薬、(29)グルタミン酸増強薬、(30)NMDA受容体阻害薬、(31)代謝性グルタミン酸受容体調節薬(mGlu)、(32)抗不安薬、(33)睡眠導入剤、(34)βアミロイドワクチン、(35)βアミロイド分解酵素等、(36)脳機能賦活薬、(37)カンナビノイド調節薬、(38)コリンエステラーゼ阻害薬、(39)MAO−B阻害剤、(40)パーキンソン病治療薬、(41)糖尿病治療薬、(42)抗肥満薬、(43)コレステロール低下薬等の高脂血症治療薬、(44)降圧剤、(45)非ステロイド性抗炎症薬、(46)疾患修飾性抗リウマチ薬、(47)抗サイトカイン薬、(48)ステロイド薬、(49)性ホルモンまたはその誘導体、及び(50)副甲状腺ホルモン(PTH)からなる群より選択される薬剤の1種以上である、[220]又は[221]に記載の医薬組成物。
[218]医薬組成物が、PDE2Aが関与する疾患の予防及び/又は治療のためのものである、前記[217]に記載の医薬組成物。
[219]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症、からなる群から選択される少なくとも1つの疾患である、前記[217]又は[218]に記載の医薬組成物。
[220]医薬組成物が、さらに他の予防及び/又は治療薬(他の薬剤)の有効成分を含有してなる、[217]から[219]のいずれか一項に記載の医薬組成物。
[221]医薬組成物が、他の予防及び/又は治療薬(他の薬剤)と併用して使用されるものである、[217]から[219]のいずれか一項に記載の医薬組成物。
[222]他の予防及び/又は治療薬(他の薬剤)が、(1)非定型抗精神病薬、(2)定型抗精神病薬、(3)選択的セロトニン再取り込み阻害薬(SSRI)、(4)選択的セロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)、(5)選択的ノルアドレナリン・ドーパミン再取り込み阻害薬(NDRI)、(6)ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA)、(7)セロトニン・ノルアドレナリン・ドパミン三重モノアミン再取り込み阻害剤、(8)双極性障害治療薬、(9)てんかん治療薬、(10)多発性硬化症治療薬、(11)ハンチントン病治療薬、(12)トリアゾロピリジン系抗うつ薬(SARI)、(13)四環系抗うつ薬、(14)三環系抗うつ薬、(15)その他抗うつ薬、(16)α7ニコチン受容体作動薬、(17)α7ニコチン受容体活性調節薬、(18)α7ニコチン受容体部分調節薬、(19)PDE阻害薬、(20)NK2拮抗薬、(21)NK3拮抗薬、(22)ムスカリン型M1アセチルコリン受容体活性調節薬、(23)ムスカリン型M2アセチルコリン受容体活性調節薬、(24)アデノシン受容体調節薬、(25)ムスカリン型M4アセチルコリン受容体活性調節薬、(26)ムスカリン型M5アセチルコリン受容体活性調節薬、(27)アデノシン受容体調節薬、(28)グリシントランスポーター1(GlyT1)阻害薬、(29)グルタミン酸増強薬、(30)NMDA受容体阻害薬、(31)代謝性グルタミン酸受容体調節薬(mGlu)、(32)抗不安薬、(33)睡眠導入剤、(34)βアミロイドワクチン、(35)βアミロイド分解酵素等、(36)脳機能賦活薬、(37)カンナビノイド調節薬、(38)コリンエステラーゼ阻害薬、(39)MAO−B阻害剤、(40)パーキンソン病治療薬、(41)糖尿病治療薬、(42)抗肥満薬、(43)コレステロール低下薬等の高脂血症治療薬、(44)降圧剤、(45)非ステロイド性抗炎症薬、(46)疾患修飾性抗リウマチ薬、(47)抗サイトカイン薬、(48)ステロイド薬、(49)性ホルモンまたはその誘導体、及び(50)副甲状腺ホルモン(PTH)からなる群より選択される薬剤の1種以上である、[220]又は[221]に記載の医薬組成物。
[223]前記[1]から[216]のいずれか一項に記載された化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物の少なくともひとつの化合物を含有してなる、PDE2Aが関与する疾患の予防及び/又は治療剤。
[224]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[223]に記載の予防及び/又は治療剤。
[225]PDE2Aが関与する疾患の予防及び/又は治療剤が、さらに他の予防及び/又は治療薬(他の薬剤)の有効成分を含有してなる、[223]又は[224]に記載のPDE2Aが関与する疾患の予防及び/又は治療剤。
[226]PDE2Aが関与する疾患の予防及び/又は治療剤が、他の予防及び/又は治療薬(他の薬剤)と併用して使用されるものである、[223]又は[224]に記載のPDE2Aが関与する疾患の予防及び/又は治療剤。
[227]他の予防及び/又は治療薬(他の薬剤)が、前記[222]に記載の予防及び/又は治療薬(薬剤)である、前記[225]又は[226]に記載のPDE2Aが関与する疾患の予防及び/又は治療剤。
[224]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[223]に記載の予防及び/又は治療剤。
[225]PDE2Aが関与する疾患の予防及び/又は治療剤が、さらに他の予防及び/又は治療薬(他の薬剤)の有効成分を含有してなる、[223]又は[224]に記載のPDE2Aが関与する疾患の予防及び/又は治療剤。
[226]PDE2Aが関与する疾患の予防及び/又は治療剤が、他の予防及び/又は治療薬(他の薬剤)と併用して使用されるものである、[223]又は[224]に記載のPDE2Aが関与する疾患の予防及び/又は治療剤。
[227]他の予防及び/又は治療薬(他の薬剤)が、前記[222]に記載の予防及び/又は治療薬(薬剤)である、前記[225]又は[226]に記載のPDE2Aが関与する疾患の予防及び/又は治療剤。
[228]前記[1]から[216]のいずれか一項に記載された化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物の少なくともひとつの化合物を含有してなるPDE2A阻害剤。
[229]PDE2Aが関与する疾患の予防及び/又は治療のための医薬組成物を製造するための、前記[1]から[216]のいずれか一項に記載された化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物の使用。
[230]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[229]に記載の使用。
[230]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[229]に記載の使用。
[231]PDE2Aが関与する疾患の予防及び/又は治療のための医薬組成物の有効成分として使用するための、前記[1]から[216]のいずれか一項に記載された化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物。
[232]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[231]に記載の化合物若しくは薬学的に許容できるその塩、又はそれらの溶媒和物。
[232]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[231]に記載の化合物若しくは薬学的に許容できるその塩、又はそれらの溶媒和物。
[233]PDE2Aが関与する疾患の患者に、治療に有効な量の前記[1]から[216]のいずれか一項に記載された化合物若しくはその製薬学的に許容される塩、又はそれらの溶媒和物を投与することを含む、PDE2Aが関与する疾患を治療する方法。
[234]治療に有効な量が、PDE2Aを阻害するのに有効な量である前記[233]に記載の方法。
[235]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[233]又は[234]に記載の方法。
[234]治療に有効な量が、PDE2Aを阻害するのに有効な量である前記[233]に記載の方法。
[235]PDE2Aが関与する疾患が、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[233]又は[234]に記載の方法。
[236]PDE2Aが関与する疾患が、(1)統合失調症(妄想型、解体型、緊張型、鑑別不能型、又は残遺型)、(2)統合失調症様障害、(3)統合失調感情障害(妄想型又は抑うつ型)、(4)妄想性障害、(5)物質誘導性精神障害、(6)妄想型人格障害、(7)統合失調型の人格障害、(8)ハンチントン病、(9)ドーパミンアゴニスト療法に伴う異常運動症(ジスキネジア)、(10)パーキンソン病、(11)不穏下肢症候群、(12)本態性振戦、(13)恐慌性障害、(14)広場恐怖症、(15)特定恐怖症、(16)社会恐怖症、(17)強迫性障害、(18)心的外傷後ストレス障害、(19)急性ストレス障害、(20)全般性不安障害、(21)食欲不振症、(22)過食症、(23)気晴らし食い障害、(24)氷食症、(25)過眠症、(26)概日リズム睡眠障害、(27)不眠症、(28)睡眠時異常行動、(29)睡眠遮断、(30)大うつ病エピソード(軽度、中等度、又は重度型)、(31)躁病エピソード、(32)混合性エピソード、(33)軽躁病エピソード、(34)非定型うつ病、(35)メランコリー型うつ病、(36)緊張病性うつ病、(37)季節性うつ病、(38)産後発症気分エピソード、(39)脳卒中後うつ病、(40)大うつ病性障害、(41)気分変調性障害、(42)気分変調症、(43)小うつ病性障害、(44)月経前不快気分障害、(45)統合失調症後うつ病性障害、(46)妄想性障害又は統合失調症等の精神障害に併発する大うつ病性障害、(47)双極性障害(I型及びII型)、(48)気分循環性障害、(49)偏頭痛、(50)てんかん、(51)ハンチントン病、(52)脳外傷に関連する神経変性、(53)脳卒中に関連する神経変性、(54)脳梗塞に関連する神経変性、(55)低血糖誘発性神経変性、(56)てんかん発作に関連する神経変性、(57)神経毒中毒に関連する神経変性、(58)多系統委縮症、(59)線条体中型有棘ニューロンの神経変性、(60)加齢性認知低下、(61)アルツハイマー病、(62)統合失調症又はアルツハイマー病に伴う認知症、(63)多発脳梗塞性認知症、(64)アルコール性認知症又は他の薬物関連認知症、(65)頭蓋内腫瘍又は脳外傷に関連する認知症、(66)ハンチントン病又はパーキンソン病に関連する認知症、(67)エイズ関連認知症、(68)前頭側頭型認知症、(69)せん妄、(70)健忘障害、(71)心的外傷後ストレス障害、(72)精神遅滞、(73)読字障害、(74)算数障害、(75)書字表出障害、(76)注意欠陥障害、(77)注意欠陥/多動性障害(ADHA)、(78)行為障害、(79)自閉症、(80)薬物依存症、(81)トゥーレット症候群、(82)チック障害、(83)精神薄弱(ダウン症候群及び脆弱X症候群を含む。)、(84)肥満、(85)メタボリック症候群、(86)インスリン非依存性糖尿病、(87)耐糖能障害、(89)肺炎、及び(90)変形性関節症からなる群から選択される少なくとも1つの疾患である、前記[217]から[222]のいずれか一項に記載の医薬組成物、[223]若しくは[227]に記載の予防及び/又は治療剤、前記[229]若しくは[230]に記載の使用、前記[231]若しくは[232]に記載の化合物若しくは製薬学的に許容されるその塩、若しくはそれらの溶媒和物、又は前記[233]から[235]のいずれか一項に記載の方法。
次に、本発明の化合物について具体的に説明する。
本発明の化合物に関する説明において、例えば「C1〜6」とは、構成炭素原子数が1から6であることを示し、特に断らない限り、直鎖、分枝鎖または環状の基の総炭素原子数を表わす。
本発明の化合物に関する説明において、例えば「C1〜6」とは、構成炭素原子数が1から6であることを示し、特に断らない限り、直鎖、分枝鎖または環状の基の総炭素原子数を表わす。
本明細書中、特に断りのない限り、「ハロゲン原子」としては、例えば、フッ素原子、塩素原子、臭素原子、及びヨウ素原子等が挙げられる。
本明細書中、特に断りのない限り、「ハロゲン化C1〜6アルキル基」等における「ハロゲン化」とは、置換基として1〜5個の前記「ハロゲン原子」を有することを意味する。
本明細書中、特に断りのない限り、「ハロゲン化C1〜6アルキル基」等における「ハロゲン化」とは、置換基として1〜5個の前記「ハロゲン原子」を有することを意味する。
本明細書中、特に断りのない限り、「C1〜6アルキル基」としては、例えば、メチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、sec−ブチル、tert−ブチル、ペンチル、イソペンチル、ネオペンチル、ヘキシル等が挙げられる。
本明細書中、特に断りのない限り、「ハロゲン化C1〜6アルキル基」とは、前記「C1〜6アルキル基」が数個の、好ましくは1〜5個のハロゲン原子で任意に置換されている基を意味し、例えば、フルオロメチル、ジフルオロメチル、トリフルオロメチル、2,2,2−トリフルオロエチル、1,1,2,2−テトラフルオロエチル、ペンタフルオロエチル等が挙げられる。
本明細書中、特に断りのない限り、「−O−C1〜6アルキル基」とは、前記した「C1〜6アルキル基」が酸素原子に結合したアルコキシ基を表し、例えば、メトキシ基、エトキシ基などが挙げられる。
本明細書中、特に断りのない限り、「−O−ハロゲン化C1〜6アルキル基」とは、前記した「ハロゲン化C1〜6アルキル基」が酸素原子に結合したハロゲン化アルコキシ基を表し、例えば、フルオロメトキシ基、ジフルオロメトキシ基、トリフルオロメトキシ基、2,2,2−トリフルオロエトキシ基、1,1,2,2−テトラフルオロエトキシ基、ペンタフルオロエトキシ基等が挙げられる。
本明細書中、特に断りのない限り、「−C(O)−(C1〜6アルキル基)」とは、前記した「C1〜6アルキル基」にカルボニル基(−CO−)が結合したアルキルカルボニル基であり、例えば、アセチル基、エチルカルボニル基、プロピルカルボニル基、イソプロピルカルボニル基、ブチルカルボニル基、イソブチルカルボニル基、sec−ブチルカルボニル基、tert−ブチルカルボニル基、ペンチルカルボニル基、イソペンチルカルボニル基、ネオペンチルカルボニル基、ヘキシルカルボニル基等が挙げられる。
本明細書中、特に断りのない限り、「−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]」とは、「C1〜6アルキル基」にスルフィド基(n=0のとき)、スルフィニル基(n=1のとき)、又はスルホニル基(n=2のとき)が結合したアルキルチオ基(n=0のとき)、アルキルスルフィニル基(n=1のとき)、又はアルキルスルホニル基(n=2のとき)であり、例えば、メチルチオ基、エチルチオ基、プロピルチオ基、イソプロピルチオ基、ブチルチオ基、メチルスルフィニル基、エチルスルフィニル基、プロピルスルフィニル基、イソプロピルスルフィニル基、ブチルスルフィニル基、メチルスルホニル基、エチルスルホニル基、プロピルスルホニル基、イソプロピルスルホニル基、ブチルスルホニル基などが挙げられる。
本明細書中、特に断りのない限り、「−O−C1〜6アルキル基」とは、前記した「C1〜6アルキル基」が酸素原子に結合したアルコキシ基を表し、例えば、メトキシ基、エトキシ基などが挙げられる。
本明細書中、特に断りのない限り、「−O−ハロゲン化C1〜6アルキル基」とは、前記した「ハロゲン化C1〜6アルキル基」が酸素原子に結合したハロゲン化アルコキシ基を表し、例えば、フルオロメトキシ基、ジフルオロメトキシ基、トリフルオロメトキシ基、2,2,2−トリフルオロエトキシ基、1,1,2,2−テトラフルオロエトキシ基、ペンタフルオロエトキシ基等が挙げられる。
本明細書中、特に断りのない限り、「−C(O)−(C1〜6アルキル基)」とは、前記した「C1〜6アルキル基」にカルボニル基(−CO−)が結合したアルキルカルボニル基であり、例えば、アセチル基、エチルカルボニル基、プロピルカルボニル基、イソプロピルカルボニル基、ブチルカルボニル基、イソブチルカルボニル基、sec−ブチルカルボニル基、tert−ブチルカルボニル基、ペンチルカルボニル基、イソペンチルカルボニル基、ネオペンチルカルボニル基、ヘキシルカルボニル基等が挙げられる。
本明細書中、特に断りのない限り、「−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]」とは、「C1〜6アルキル基」にスルフィド基(n=0のとき)、スルフィニル基(n=1のとき)、又はスルホニル基(n=2のとき)が結合したアルキルチオ基(n=0のとき)、アルキルスルフィニル基(n=1のとき)、又はアルキルスルホニル基(n=2のとき)であり、例えば、メチルチオ基、エチルチオ基、プロピルチオ基、イソプロピルチオ基、ブチルチオ基、メチルスルフィニル基、エチルスルフィニル基、プロピルスルフィニル基、イソプロピルスルフィニル基、ブチルスルフィニル基、メチルスルホニル基、エチルスルホニル基、プロピルスルホニル基、イソプロピルスルホニル基、ブチルスルホニル基などが挙げられる。
本明細書中、特に断りのない限り、「C3〜8シクロアルキル基」としては、炭素数3〜8の単環式又は多環式の飽和又は不飽和のシクロアルキル基が挙げられ、例えば、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、シクロヘプチルおよびシクロオクチル等が挙げられる。
本明細書中、特に断りのない限り、「−O−(C3〜8シクロアルキル基)」とは、前記した「C3〜8シクロアルキル基」が酸素原子に結合したシクロアルコキシ基を表し、例えば、シクロプロピルオキシ、シクロブチルオキシ、シクロペンチルオキシ、シクロヘキシルオキシ、シクロヘプチルオキシ、シクロオクチルオキシ等が挙げられる。
本明細書中、特に断りのない限り、「−O−(C3〜8シクロアルキル基)」とは、前記した「C3〜8シクロアルキル基」が酸素原子に結合したシクロアルコキシ基を表し、例えば、シクロプロピルオキシ、シクロブチルオキシ、シクロペンチルオキシ、シクロヘキシルオキシ、シクロヘプチルオキシ、シクロオクチルオキシ等が挙げられる。
本明細書中、特に断りのない限り、「環状エーテル基」とは、環中に1個又は2個の酸素原子(但し、酸素原子は連続して結合していない。)、及び2〜7個、好ましくは2〜6個の炭素原子を有する、3〜8員の単環式又は多環式の飽和又は不飽和の環状エーテル化合物から環上の任意の水素原子を除いてできる1価の基を意味し、このような「環状エーテル基」としては、例えば、オキシラニル、オキセタニル、テトラヒドロフラニル、テトラヒドロピラニル、オキセパニル、オキソカニル、ジオキサニル等が挙げられる。
本明細書中、特に断りのない限り、「3〜8員エーテル環」とは、前記した環状エーテル基を形成している環状エーテル環における、員数が3〜8のものであって、例えば、オキシラン、オキセタン、テトラヒドロフラン、1,3−ジオキソラン、テトラヒドロピラン、1,4−ジオキサン、オキセパン、1,4−ジオキセパン、オキソカン等が挙げられる。
本発明において、2個の基が一緒になって、隣接する原子と共に「C3〜8シクロアルキル環」又はさらに酸素原子が加わって「環状エーテル環」を形成する場合の「C3〜8シクロアルキル環」や「環状エーテル環」は、前記の「シクロアルキル基」や「環状エーテル基」で形成されている環を意味するものである。このようにして形成された「C3〜8シクロアルキル基」、「環状エーテル基」、「環状アルキル環」若しくは「環状エーテル環」の炭素原子は、任意に−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選ばれる基で数個、好ましくは1〜3個置換されていてもよい。
本明細書中、特に断りのない限り、「3〜8員エーテル環」とは、前記した環状エーテル基を形成している環状エーテル環における、員数が3〜8のものであって、例えば、オキシラン、オキセタン、テトラヒドロフラン、1,3−ジオキソラン、テトラヒドロピラン、1,4−ジオキサン、オキセパン、1,4−ジオキセパン、オキソカン等が挙げられる。
本発明において、2個の基が一緒になって、隣接する原子と共に「C3〜8シクロアルキル環」又はさらに酸素原子が加わって「環状エーテル環」を形成する場合の「C3〜8シクロアルキル環」や「環状エーテル環」は、前記の「シクロアルキル基」や「環状エーテル基」で形成されている環を意味するものである。このようにして形成された「C3〜8シクロアルキル基」、「環状エーテル基」、「環状アルキル環」若しくは「環状エーテル環」の炭素原子は、任意に−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基からなる群から選ばれる基で数個、好ましくは1〜3個置換されていてもよい。
本明細書中、特に断りのない限り、「C2〜6アルケニル基」としては、例えば、ビニル、アリル、イソプロペニル、ブテニル、ペンテニル、及びヘキセニル等が挙げられる。
本明細書中、特に断りのない限り、「C6〜14アリール基」としては、例えば、フェニル、1−ナフチル、2−ナフチル、2−,3−,4−ビフェニルアンスリル、フェナンスリル、アセナフチル、インダニル、インデニル、および1,2,3,4−テトラヒドロナフチル等が挙げられる。
本明細書中、特に断りのない限り、「C7〜20アラルキル基」としては、例えば、ベンジル、フェネチル、ジフェニルメチル、トリチル、ビフェニルメチル、ナフチルメチル、インダニルメチル、1,2,3,4−テトラヒドロナフタレン−1−イルメチル、等が挙げられる。
本明細書中、特に断りのない限り、「C6〜14アリール基」としては、例えば、フェニル、1−ナフチル、2−ナフチル、2−,3−,4−ビフェニルアンスリル、フェナンスリル、アセナフチル、インダニル、インデニル、および1,2,3,4−テトラヒドロナフチル等が挙げられる。
本明細書中、特に断りのない限り、「C7〜20アラルキル基」としては、例えば、ベンジル、フェネチル、ジフェニルメチル、トリチル、ビフェニルメチル、ナフチルメチル、インダニルメチル、1,2,3,4−テトラヒドロナフタレン−1−イルメチル、等が挙げられる。
本明細書中、特に断りのない限り、前記「ヘテロアリール環」とは、窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個、好ましくは1〜3個含有する、単環式、多環式又は縮合環式(但し、多環式又は縮合環式の場合には部分的に水素化されていてもよい)のヘテロアリール環を意味する。
本明細書中、特に断りのない限り、前記「ヘテロアリール環」としては、例えば、「単環式ヘテロアリール環」、「縮環式ヘテロアリール環」、「部分的に水素化された縮環式ヘテロアリール環」が挙げられる。
本明細書中、特に断りのない限り、前記「単環式ヘテロアリール環」としては、前記したヘテロアリール環の単環式のものであって、環員数が5〜8、さらには5〜7のものが好ましく(「5〜7員ヘテロアリール環」)、例えば、ピロール、フラン、チオフェン、イミダゾール、オキサゾール、チアゾール、ピラゾール、イソオキサゾール、イソチアゾール、トリアゾール、オキサジアゾール、チアジアゾール、フラザン、チアトリアゾール、オキサトリアゾール、テトラゾール、テトラゾール、ピリジン、ピリダジン、ピリミジン、ピラジン、トリアジン、テトラジン、ジアゼピン、オキサゼピン等が挙げられる。又、このうち、環員数6のものを「6員ヘテロアリール環」と言い、ピリジン、ピリダジン、ピリミジン、ピラジン、トリアジン、テトラジン等が挙げられる。
本明細書中、特に断りのない限り、前記「ヘテロアリール環」としては、例えば、「単環式ヘテロアリール環」、「縮環式ヘテロアリール環」、「部分的に水素化された縮環式ヘテロアリール環」が挙げられる。
本明細書中、特に断りのない限り、前記「単環式ヘテロアリール環」としては、前記したヘテロアリール環の単環式のものであって、環員数が5〜8、さらには5〜7のものが好ましく(「5〜7員ヘテロアリール環」)、例えば、ピロール、フラン、チオフェン、イミダゾール、オキサゾール、チアゾール、ピラゾール、イソオキサゾール、イソチアゾール、トリアゾール、オキサジアゾール、チアジアゾール、フラザン、チアトリアゾール、オキサトリアゾール、テトラゾール、テトラゾール、ピリジン、ピリダジン、ピリミジン、ピラジン、トリアジン、テトラジン、ジアゼピン、オキサゼピン等が挙げられる。又、このうち、環員数6のものを「6員ヘテロアリール環」と言い、ピリジン、ピリダジン、ピリミジン、ピラジン、トリアジン、テトラジン等が挙げられる。
本明細書中、特に断りのない限り、前記「縮環式ヘテロアリール環」としては、環員数8〜14のものが好ましく、即ち、「8〜14員縮環式ヘテロアリール環」としては、例えば、下記式(chA−1)ないし式(chA−11):
[前記式(chA−1)ないし式(chA−11)中、Xは、N−H、O、又はSから選らばれ;Aは、C−H又はNから選らばれる]の群の中から選ばれる環等が挙げられる。
本発明の一般式(I)で表される化合物において、環Aのヘテロアリール基は、「単環式ヘテロアリール環」又は「縮環式ヘテロアリール環」から選ばれ、特に、「単環式5〜14員のヘテロアリール環」又は「縮環式5〜14員のヘテロアリール環」が好ましい。ここで、環Bと結合している環Aのヘテロアリール環の炭素原子の隣接位(α位)が必ず窒素原子である。また、環Qがヘテロアリール基である場合にも、環Qのヘテロアリール基は、前記したヘテロアリール環の任意位置で隣接する炭素原子と結合することができる。好ましい結合位置としては、隣接する炭素原子と結合している環Qのヘテロアリール環の炭素原子の隣接位(α位)に環Qのヘテロアリール環の窒素原子などのヘテロ原子がくる位置が挙げられる。
本明細書中、特に断りのない限り、前記「5〜14員のヘテロアリール環」としては、例えば、ピロール、フラン、チオフェン、イミダゾール、オキサゾール、チアゾール、ピラゾール、イソオキサゾール、イソチアゾール、トリアゾール、オキサジアゾール、チアジアゾール、フラザン、チアトリアゾール、オキサトリアゾール、テトラゾール、テトラゾール、ピリジン、ピリダジン、ピリミジン、ピラジン、トリアジン、テトラジン、ジアゼピン、オキサゼピン、キノリン、イソキノリン等が挙げられる。
本発明の一般式(I)で表される化合物において、環Aのヘテロアリール基は、「単環式ヘテロアリール環」又は「縮環式ヘテロアリール環」から選ばれ、特に、「単環式5〜14員のヘテロアリール環」又は「縮環式5〜14員のヘテロアリール環」が好ましい。ここで、環Bと結合している環Aのヘテロアリール環の炭素原子の隣接位(α位)が必ず窒素原子である。また、環Qがヘテロアリール基である場合にも、環Qのヘテロアリール基は、前記したヘテロアリール環の任意位置で隣接する炭素原子と結合することができる。好ましい結合位置としては、隣接する炭素原子と結合している環Qのヘテロアリール環の炭素原子の隣接位(α位)に環Qのヘテロアリール環の窒素原子などのヘテロ原子がくる位置が挙げられる。
本明細書中、特に断りのない限り、前記「5〜14員のヘテロアリール環」としては、例えば、ピロール、フラン、チオフェン、イミダゾール、オキサゾール、チアゾール、ピラゾール、イソオキサゾール、イソチアゾール、トリアゾール、オキサジアゾール、チアジアゾール、フラザン、チアトリアゾール、オキサトリアゾール、テトラゾール、テトラゾール、ピリジン、ピリダジン、ピリミジン、ピラジン、トリアジン、テトラジン、ジアゼピン、オキサゼピン、キノリン、イソキノリン等が挙げられる。
本明細書中、特に断りのない限り、「−NRARB基」とは、「アミノ基」の窒素原子上の二つの水素原子がRAおよびRBに置換された基を意味する。すなわち、「−NRARB基」とは、「アミノ基」の窒素原子上の二つの水素原子が、水素原子であるか、又は各々独立して、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)等から任意に選ばれる基に置換されている基を意味する。また、「−CONRARB」及び「−SO2NRARB」における「−NRARB基」についても同様である。
また、「オキソ基」は、カルボニル基(−CO−)の酸素原子部分からなる基である。
なお、本明細書中で使用されるその他の化学用語は、当業者が通常使用している意味で使用されている。
また、「オキソ基」は、カルボニル基(−CO−)の酸素原子部分からなる基である。
なお、本明細書中で使用されるその他の化学用語は、当業者が通常使用している意味で使用されている。
本発明の化合物の好ましい態様については、前記の[1]から[216]の項に具体的に記載してきたとおりである。本発明の化合物の名称は、ChemBioDraw(登録商標) Ultra 14(CambridgeSoft)の化合物名称命名プログラムに従って得られる英語名称に基づくものであるが、これに拘束されるものではない。
本発明の好ましい化合物としては、以下の化合物を例示することができるが、これに限定されるものではない。
1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−N−(1−(4−ブロモフェニル)エチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(4−ブロモフェニル)シクロプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタンー3−イル)−1H−ピラゾール−5−カルボキサミド;
本発明の好ましい化合物としては、以下の化合物を例示することができるが、これに限定されるものではない。
1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−N−(1−(4−ブロモフェニル)エチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(4−ブロモフェニル)シクロプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタンー3−イル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(2−メチルピリミジン−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
4−(4−シアノチアゾール−2−イル)−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(2−メチルピリミジン−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
4−(4−シアノチアゾール−2−イル)−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(ピリミジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(キノリン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−エチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(S)−1−エチル−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−エチル−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
1−メチル−4−(ピリミジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(キノリン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−エチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
(S)−1−エチル−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
1−エチル−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミド;
(S)−1−(シクロプロピルメチル)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミド;
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミド;
(R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
3’,5−ジメチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
3’,5−ジメチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(R)−5−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
3’,5−ジメチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
3’,5−ジメチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミド;
(R)−5−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
1−メチル−3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
1−メチル−3−(チアゾール−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド、又は
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(チアゾール−2−イル)−1H−ピラゾール−4−カルボキサミド。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
1−メチル−3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド;
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボキサミド;
1−メチル−3−(チアゾール−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−4−カルボキサミド、又は
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(チアゾール−2−イル)−1H−ピラゾール−4−カルボキサミド。
本発明の化合物には、次の式で例示されるように数種の互変異性体が存在し得る。これらの互変異性体も本発明の化合物の範囲に包含される。これらの互変異性体の存在比は、化合物が固体状態であるか、もしくは液体に溶解している状態であるかに応じて、その存在比は変化し得る。
なお、本明細書における任意の構造式における任意の特定の互変異性体の記載は、その型に限定されることを意図しておらず、互変異性体セット全体の代表であることを意図するものである。
例えば、後述する実施例1の化合物において、1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドと記載した化合物名であれば、その互変異性体の1つである、1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルビミディクアシド、も当該実施例1の化合物に包含される化合物である。
例えば、後述する実施例1の化合物において、1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドと記載した化合物名であれば、その互変異性体の1つである、1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルビミディクアシド、も当該実施例1の化合物に包含される化合物である。
本明細書中、特に断りのない限り、環状基に可変置換基が置換している場合、該可変置換基は環状基の特定の炭素原子に結合されていない事を意味する。例えば、下記式Aにおける可変置換基Rxは、該式Aにおける炭素原子i、ii、またはiiiの何れかに置換する事ができ、下記式Bにおける可変置換基Ryは、該式Bにおける炭素原子iv、またはvの何れかに置換する事ができ、下記式Cにおける可変置換基Rzは、該式Cにおける炭素原子viまたはviii、並びにNH基の水素原子に置き換わり(Vii)の何れかに置換する事ができる事を意味する。
本明細書中、特に断りのない限り、「式(I)の化合物」、「式(I)で表される化合物」等と記載している場合、「式(I−a)の化合物」、「式(I−aa)の化合物」、「式(I−b)の化合物」、及び「式(I−bb)の化合物」等の、「式(I)の化合物」の下位概念にあたる化合物にも言及するものとする。
以上の全ての態様において、「化合物」の文言を用いるとき、「その製薬学的に許容される塩」についても言及するものとする。
以上の全ての態様において、「化合物」の文言を用いるとき、「その製薬学的に許容される塩」についても言及するものとする。
本発明の化合物は、置換基の種類によって、酸付加塩を形成する場合や塩基との塩を形成する場合がある。かかる塩としては、製薬学的に許容しうる塩であれば特に限定されないが、例えば、金属塩、アンモニウム塩、有機塩基との塩、無機酸との塩、有機酸との塩、塩基性、又は酸性アミノ酸との塩などが挙げられる。
本発明中の化合物が酸性である場合には、無機又は有機の塩基から塩を形成する場合がある。かかる塩としては、製薬学的に許容しうる塩であれば特に限定されなく、無機又は有機の塩基を包含する製薬学的に許容しうる非毒性の塩基から調製された塩を表す。無機塩基から得られる塩としては、アルミニウム塩、アンモニウム塩、カルシウム塩、銅塩、鉄(III)塩、鉄(II)塩、リチウム塩、マグネシウム塩、マンガン(III)塩、マンガン(II)塩、バリウム塩、カリウム塩、ナトリウム塩、セシウム塩及び亜鉛塩、等が挙げられる(一塩の他、二塩等も含む。)。
本発明中の化合物が酸性である場合には、無機又は有機の塩基から塩を形成する場合がある。かかる塩としては、製薬学的に許容しうる塩であれば特に限定されなく、無機又は有機の塩基を包含する製薬学的に許容しうる非毒性の塩基から調製された塩を表す。無機塩基から得られる塩としては、アルミニウム塩、アンモニウム塩、カルシウム塩、銅塩、鉄(III)塩、鉄(II)塩、リチウム塩、マグネシウム塩、マンガン(III)塩、マンガン(II)塩、バリウム塩、カリウム塩、ナトリウム塩、セシウム塩及び亜鉛塩、等が挙げられる(一塩の他、二塩等も含む。)。
有機塩基から得られる塩としては、例えば、メチルアミン、エチルアミン、t−ブチルアミン、t−オクチルアミン、シクロヘキシルアミン、エタノールアミン、エチレンジアミン、ジエチルアミン、ジシクロヘキシルアミン、ジベンジルアミン、ジエタノールアミン、N,N'−ジベンジルエチレンジアミン、トリメチルアミン、トリエチルアミン、トリエタノールアミン、ピペリジン、モルホリン、ピリジン、ピコリン、2,6−ルチジン、リシン、アルギニン、オルニチン、N−メチルグルカミン、グルコサミン、フェニルグリシンアルキルエステル、グアニジン、等との塩が挙げられる。
本発明中の化合物が塩基性である場合には、無機酸及び有機酸から塩を形成する場合がある。かかる酸としては、例えば、塩酸、臭化水素酸、硝酸、硫酸、リン酸、酢酸、乳酸、マンデル酸、コハク酸、フマル酸、マレイン酸、リンゴ酸、酒石酸、クエン酸、安息香酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸、p−トルエンスルホン酸、グルタミン酸、カンファースルホン酸、クエン酸、グルコン酸、イセチオン酸、粘液酸、パモ酸、パントテン酸、よう化水素酸、ギ酸、トリフルオロ酢酸、プロピオン酸、酪酸、吉草酸、エナント酸、カプリン酸、ミリスチン酸、パルミチン酸、ステアリン酸、ソルビン酸、シュウ酸、マロン酸、フタル酸、桂皮酸、グリコール酸、ピルビン酸、オキシル酸、サリチル酸、N−アセチルシステイン、アスパラギン酸、等が挙げられる。かかる塩としては、製薬学的に許容しうる塩であれば特に限定されない。
本発明中の化合物が塩基性である場合には、無機酸及び有機酸から塩を形成する場合がある。かかる酸としては、例えば、塩酸、臭化水素酸、硝酸、硫酸、リン酸、酢酸、乳酸、マンデル酸、コハク酸、フマル酸、マレイン酸、リンゴ酸、酒石酸、クエン酸、安息香酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸、p−トルエンスルホン酸、グルタミン酸、カンファースルホン酸、クエン酸、グルコン酸、イセチオン酸、粘液酸、パモ酸、パントテン酸、よう化水素酸、ギ酸、トリフルオロ酢酸、プロピオン酸、酪酸、吉草酸、エナント酸、カプリン酸、ミリスチン酸、パルミチン酸、ステアリン酸、ソルビン酸、シュウ酸、マロン酸、フタル酸、桂皮酸、グリコール酸、ピルビン酸、オキシル酸、サリチル酸、N−アセチルシステイン、アスパラギン酸、等が挙げられる。かかる塩としては、製薬学的に許容しうる塩であれば特に限定されない。
前記塩は、常法に従い、例えば、本発明中の化合物と適量の酸又は塩基を含む溶液を混合することにより目的の塩を形成させた後に分別濾取するか、若しくは、当該混合溶媒を留去することにより得ることができる。また、本発明の化合物又は其の塩は、水、エタノール、グリセロール等の溶媒と溶媒和物を形成しうる。
塩に関する総説として、Handbook of Pharmaceutical Salts:Properties,Selection,and Use、Stahl&Wermuth(Wiley−VCH、2002)が出版されており、本書に詳細な記載がなされている。前記塩は、当該総説を参照して製造することができる。
塩に関する総説として、Handbook of Pharmaceutical Salts:Properties,Selection,and Use、Stahl&Wermuth(Wiley−VCH、2002)が出版されており、本書に詳細な記載がなされている。前記塩は、当該総説を参照して製造することができる。
本発明の化合物は、非溶媒和形態、若しくは溶媒和形態で存在することができる。本明細書において、「溶媒和物」は、本発明の化合物と1種又は複数の薬学的に許容される溶媒分子(例えば、水、エタノール等)を含む分子複合体を意味する。前記溶媒分子が水である場合、特に「水和物」と言う。
本発明の化合物に関する記載においては、塩、溶媒和物、及びその塩の溶媒和物に関する記載を包含する。
本発明の化合物に関する記載においては、塩、溶媒和物、及びその塩の溶媒和物に関する記載を包含する。
本発明の化合物の「プロドラッグ」も本発明の化合物に包含される。「プロドラッグ」とは、例えば、目的とする薬理活性を殆どもしくは全く示さない可能性のある、本発明の化合物のある種の誘導体を、身体内又は身体上に投与した時、例えば、加水分解等により目的とする薬理活性を有する、本発明の化合物に変換される場合、投与前の化合物のことを「プロドラッグ」と呼ぶ。
本発明の化合物の「プロドラッグ」は、例えば、本発明の化合物に存在する適切な官能基を、文献公知の方法、例えば、Design of Prodrugs、H.Bundgaard(Elsevier、1985)に記載されている方法に準じることで製造することができる。
本発明の化合物の「プロドラッグ」は、例えば、本発明の化合物に存在する適切な官能基を、文献公知の方法、例えば、Design of Prodrugs、H.Bundgaard(Elsevier、1985)に記載されている方法に準じることで製造することができる。
本発明の化合物が、幾何異性体、配置異性体、互変異性体、光学異性体、立体異性体、位置異性体、及び回転異性体、等の異性体を有する場合、いずれか一方の異性体及び各異性体の混合物も本発明の化合物に包含される。更に、本発明の化合物に光学異性体が存在する場合、ラセミ体から分割された光学異性体も本発明の化合物に包含される。
本発明の化合物に、1つまたは複数の不斉炭素原子が有る場合には、2種以上の立体異性体が存在できる。例えば、本発明の化合物の式(I)のR2a及びR2bにおいて、R2a及びR2bの組み合わせが、水素原子及びC1〜6アルキル基の場合(下記式(I−x))には、光学異性体が存在する。
本発明の化合物に、1つまたは複数の不斉炭素原子が有る場合には、2種以上の立体異性体が存在できる。例えば、本発明の化合物の式(I)のR2a及びR2bにおいて、R2a及びR2bの組み合わせが、水素原子及びC1〜6アルキル基の場合(下記式(I−x))には、光学異性体が存在する。
即ち、本明細書中、特に断りが無い限り、一般式(I−x)には(R)体(下記の一般式(I−x−R))、及び(S)体(下記の一般式(I−x−S))の両異性体が含まれる事を意味する。
なお、本明細書において、*マークが有る化合物(例えば、下記の一般式(I−x’))は、(R)体、又は(S)体のいずれかの立体配置を有している化合物、又は当該化合物が少なくとも過剰に含有されている化合物を意味する。また、立体配置を太線で表すこともある。
本発明の化合物に、「C2〜6アルケニル基」などの不飽和結合が含まれる場合、幾何異性体(シス/トランス、またはZ/E)が存在できる。
構造異性体が低いエネルギー障壁により相互変換可能である場合には、互変異性が生じ得る。互変異性としては、例えば、イミノ基、ケト基、又はオキシム基を有する化合物における、プロトン互変異性の形態が挙げられる。
本発明の化合物に、幾何異性体、配置異性体、立体異性体、及び配座異性体等が存在する場合には、公知の手段により各々を単離することができる。
構造異性体が低いエネルギー障壁により相互変換可能である場合には、互変異性が生じ得る。互変異性としては、例えば、イミノ基、ケト基、又はオキシム基を有する化合物における、プロトン互変異性の形態が挙げられる。
本発明の化合物に、幾何異性体、配置異性体、立体異性体、及び配座異性体等が存在する場合には、公知の手段により各々を単離することができる。
本発明の化合物が光学活性体である場合には、対応するラセミ体から通常の光学分割手段により、(+)体又は(−)体[D体又はL体]に分離できる。
本発明の化合物に、光学異性体、立体異性体、位置異性体、回転異性体、及び互変異性体がある場合には、自体公知の合成手法、分離手法により各々の異性体を単一の化合物として得ることができる。分離手法としては、例えば、分別再結晶法、ジアステレオマー法、及びキラルカラム法、等の光学分割法が挙げられる。以下、各分割法について詳述する。
分別再結晶法:ラセミ体に対して光学分割剤をイオン結合させ、結晶性のジアステレオマーを得た後、其の結晶性のジアステレオマーを分別再結晶法によって分離し、所望により光学分割剤の除去工程を経て、光学的に純粋な化合物を得る方法である。光学分割剤は、例えば、(+)−マンデル酸、(−)−マンデル酸、(+)−酒石酸、(−)−酒石酸、(+)−1−フェネチルアミン、(−)−1−フェネチルアミン、シンコニン、(−)−シンコニジン、及びブルシン等が挙げられる。
ジアステレオマー法:ラセミ体の混合物に光学分割剤を共有結合させ、ジアステレオマーの混合物を得、次に、通常の分離手段(例えば、分別再結晶、シリカゲルカラムクロマトグラフィー、及びHPLC等)により光学的に純粋なジアステレオマーへ分離し、その後、化学反応(加水分解反応等)による光学分割剤の除去工程を経て、光学的に純粋な光学異性体を得る反応である。
例えば、本発明の化合物が水酸基又はアミノ基(1級、2級)を有する場合には、当該化合物と光学活性有機酸(例えば、α−メトキシ−α−(トリフルオロメチル)フェニル酢酸、及び(−)−メントキシ酢酸等)との縮合反応により、各々からエステル体又はアミド体のジアステレオマーが得られる。又、本発明の化合物がカルボキシ基を有する場合、当該化合物と光学活性アミン又は光学活性アルコールとの縮合反応により、各々からアミド体又はエステル体のジアステレオマーが得られる。縮合反応により得られたジアステレオマーを分離し、各ジアステレオマーを酸又は塩基による加水分解反応に付すことで、元の化合物の光学的に純粋な光学異性体へ変換される。
分別再結晶法:ラセミ体に対して光学分割剤をイオン結合させ、結晶性のジアステレオマーを得た後、其の結晶性のジアステレオマーを分別再結晶法によって分離し、所望により光学分割剤の除去工程を経て、光学的に純粋な化合物を得る方法である。光学分割剤は、例えば、(+)−マンデル酸、(−)−マンデル酸、(+)−酒石酸、(−)−酒石酸、(+)−1−フェネチルアミン、(−)−1−フェネチルアミン、シンコニン、(−)−シンコニジン、及びブルシン等が挙げられる。
ジアステレオマー法:ラセミ体の混合物に光学分割剤を共有結合させ、ジアステレオマーの混合物を得、次に、通常の分離手段(例えば、分別再結晶、シリカゲルカラムクロマトグラフィー、及びHPLC等)により光学的に純粋なジアステレオマーへ分離し、その後、化学反応(加水分解反応等)による光学分割剤の除去工程を経て、光学的に純粋な光学異性体を得る反応である。
例えば、本発明の化合物が水酸基又はアミノ基(1級、2級)を有する場合には、当該化合物と光学活性有機酸(例えば、α−メトキシ−α−(トリフルオロメチル)フェニル酢酸、及び(−)−メントキシ酢酸等)との縮合反応により、各々からエステル体又はアミド体のジアステレオマーが得られる。又、本発明の化合物がカルボキシ基を有する場合、当該化合物と光学活性アミン又は光学活性アルコールとの縮合反応により、各々からアミド体又はエステル体のジアステレオマーが得られる。縮合反応により得られたジアステレオマーを分離し、各ジアステレオマーを酸又は塩基による加水分解反応に付すことで、元の化合物の光学的に純粋な光学異性体へ変換される。
キラルカラム法:ラセミ体又は其の塩をキラルカラム(光学異性体分離用カラム)によるクロマトグラフィーに付すことで、直接光学分割する方法である。
例えば、高速液体クロマトグラフィー(HPLC)の場合には、キラルカラム(例えば、ダイセル社製CHIRALシリーズ等)に光学異性体の混合物を添加し、溶出溶媒(水、種々の緩衝液(例えば、リン酸緩衝液)、及び有機溶媒(例えば、エタノール、メタノール、イソプロパノール、アセトニトリル、トリフルオロ酢酸、及びジエチルアミン等)等の単独溶媒、又は其れらの混合溶媒)を用いて展開することで、光学異性体の分離が可能である。又、例えば、ガスクロマトグラフィーの場合、キラルカラム(例えば、CP−Chirasil−DeX CB(ジーエルサイエンス社製)等)を使用して、光学異性体の分離が可能である。
例えば、高速液体クロマトグラフィー(HPLC)の場合には、キラルカラム(例えば、ダイセル社製CHIRALシリーズ等)に光学異性体の混合物を添加し、溶出溶媒(水、種々の緩衝液(例えば、リン酸緩衝液)、及び有機溶媒(例えば、エタノール、メタノール、イソプロパノール、アセトニトリル、トリフルオロ酢酸、及びジエチルアミン等)等の単独溶媒、又は其れらの混合溶媒)を用いて展開することで、光学異性体の分離が可能である。又、例えば、ガスクロマトグラフィーの場合、キラルカラム(例えば、CP−Chirasil−DeX CB(ジーエルサイエンス社製)等)を使用して、光学異性体の分離が可能である。
本発明の化合物が光学活性体である場合には、光学異性体の一方を選択的に合成する不斉合成により合成することができる。光学活性な化合物は、(1)ラセミ化合物をエナンチオ選択的に反応させ光学活性体に導く不斉合成反応、(2)天然に存在する光学活性化合物(糖、アミノ酸等)からジアステレオ選択的に合成する方法、により合成する事ができる。
本発明の化合物は、結晶であってもよく、結晶形が単一であっても結晶形混合物であっても本発明の化合物に包含される。また、本発明の化合物の結晶に、結晶多形がある場合には、いずれの結晶型も本発明の化合物に包含される。
本発明の化合物は、薬学的に許容され得る共結晶又は共結晶塩であってもよい。ここで、共結晶又は共結晶塩とは、各々が異なる物理的特性(例えば、構造、融点、融解熱、吸湿性、溶解性および安定性等)を持つ、室温で二種又はそれ以上の独特な固体から構成される結晶性物質を意味する。共結晶又は共結晶塩は、自体公知の共結晶化法に従い製造することができる。
本発明の化合物には、同位元素(例えば、水素の同位体、2H及び3H等、炭素の同位体、11C、13C、及び14C等、塩素の同位体、36Cl等、フッ素の同位体、18F等、ヨウ素の同位体、123I及び125I等、窒素の同位体、13N及び15N等、酸素の同位体、15O、17O、及び18O等、リンの同位体、32P等、並びに硫黄の同位体、35S等)で標識、又は置換された化合物も包含される。
本発明の化合物のうち、ある種の同位元素(例えば、11C、18F、15O、及び13N等の陽電子放出同位元素)で標識又は置換された化合物は、例えば、陽電子断層法(Positron Emission Tomography;PET)において使用するトレーサー(PETトレーサー)として用いることができ、医療診断等の分野において有用である。
また、本発明の化合物のうち、ある種の同位元素で標識又は置換された化合物は、薬物及び/又は基質の組織分布研究において有用である。例えば、3H及び14Cは、それらによる標識または置換が容易であり、かつ検出手段が容易である点から、該研究目的において有用である。
本発明の化合物のうち、2H(あるいはDまたは重水素と表記する場合がある。)で標識または置換された化合物(D化化合物、重水素化化合物)は、安定性が高くなることが期待され、活性化合物自体として有用である。例えば、代謝を受ける位置の水素原子を2Hに置換した化合物が挙げられ、化合物の性質にほとんど影響を与えずに、代謝反応速度を低下させることができる。また、代謝酵素と不可逆的に結合する位置を2Hに置換した化合物は、その代謝酵素の作用を阻害することを抑制し、併用時の薬物相互作用を軽減することができる。
本発明の化合物のうち、同位体標識された化合物は、当業者に知られている通常の技法によって、又は後述の実施例に記載する合成方法に類似する方法によって得る事ができる。また、非標識化合物の代わりに、得られた同位体標識化合物を薬理実験に用いる事ができる。
本発明の化合物のうち、ある種の同位元素(例えば、11C、18F、15O、及び13N等の陽電子放出同位元素)で標識又は置換された化合物は、例えば、陽電子断層法(Positron Emission Tomography;PET)において使用するトレーサー(PETトレーサー)として用いることができ、医療診断等の分野において有用である。
また、本発明の化合物のうち、ある種の同位元素で標識又は置換された化合物は、薬物及び/又は基質の組織分布研究において有用である。例えば、3H及び14Cは、それらによる標識または置換が容易であり、かつ検出手段が容易である点から、該研究目的において有用である。
本発明の化合物のうち、2H(あるいはDまたは重水素と表記する場合がある。)で標識または置換された化合物(D化化合物、重水素化化合物)は、安定性が高くなることが期待され、活性化合物自体として有用である。例えば、代謝を受ける位置の水素原子を2Hに置換した化合物が挙げられ、化合物の性質にほとんど影響を与えずに、代謝反応速度を低下させることができる。また、代謝酵素と不可逆的に結合する位置を2Hに置換した化合物は、その代謝酵素の作用を阻害することを抑制し、併用時の薬物相互作用を軽減することができる。
本発明の化合物のうち、同位体標識された化合物は、当業者に知られている通常の技法によって、又は後述の実施例に記載する合成方法に類似する方法によって得る事ができる。また、非標識化合物の代わりに、得られた同位体標識化合物を薬理実験に用いる事ができる。
[本発明の化合物の製造方法]
以下に、本発明の式(I)で表される化合物の製造方法について説明する。本発明の化合物である式(I)で表される化合物、その塩及びそれらの溶媒和物は、市販化合物または市販化合物から文献公知の製造方法により容易に得ることが出来る化合物を出発原料もしくは合成中間体として、既知の一般的化学的な製造方法を組み合わせることで容易に製造することが可能であり、以下に示す代表的な製造方法に従い製造することができる。また、本発明は以下に説明する製造方法に、何ら限定されるものではない。
以下に、本発明の式(I)で表される化合物の製造方法について説明する。本発明の化合物である式(I)で表される化合物、その塩及びそれらの溶媒和物は、市販化合物または市販化合物から文献公知の製造方法により容易に得ることが出来る化合物を出発原料もしくは合成中間体として、既知の一般的化学的な製造方法を組み合わせることで容易に製造することが可能であり、以下に示す代表的な製造方法に従い製造することができる。また、本発明は以下に説明する製造方法に、何ら限定されるものではない。
下記の製造方法の各々の式中における、m、Z、R1、R2b、R3a、R3b、R4、R5a、R5b、及び環Bの定義は、特に断らない限り、前記態様に記載された一般式(I)の各々の定義と同一である。
製造方法中におけるMの定義は、特に断らない限り、リチウム、ナトリウム、カリウム等の金属である。製造方法中におけるRA又はRBの定義は、特に断らない限り、C1〜6アルキル基、C6〜14アリール基またはベンジル基である。
製造方法中におけるMの定義は、特に断らない限り、リチウム、ナトリウム、カリウム等の金属である。製造方法中におけるRA又はRBの定義は、特に断らない限り、C1〜6アルキル基、C6〜14アリール基またはベンジル基である。
本発明の製造方法中の各工程の各式は、塩を形成していても良く、当該塩としては、前述した式(I)の塩と同様のものが挙げられる。
本発明の製造方法の各工程の原料化合物は、反応液のままか粗製物として次の反応に用いることも可能である。又、常法に従って反応混合物から単離することも可能であり、それ自体が公知の手段、例えば、抽出、濃縮、中和、濾過、蒸留、再結晶、クロマトグラフィー等の分離手段により容易に精製が可能である。
上記の再結晶で用いられる溶媒は、例えば、水、メタノール、エタノール、2−プロパノール、ブタノール、ジエチルエーテル、テトラヒドロフラン、1,4−ジオキサン、n−ヘキサン、シクロヘキサン、ヘプタン、ベンゼン、トルエン、キシレン、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、1,3−ジメチル−2−イミダゾリジノン、クロロホルム、塩化メチレン、1,2−ジクロロエタン、アセトニトリル、アセトン、ジフェニルケトン、酢酸メチル、酢酸エチル、ジメチルスルホキシド、酢酸、トリフルオロ酢酸、メタンスルホン酸、等が挙げられる。これらの溶媒は、単独で用いることも可能であり、二種以上の溶媒を適当な割合、例えば、1:1〜1:10の割合で混合して用いることも可能である。また、式中の化合物が市販されている場合には市販品をそのまま用いることも可能であり、自体公知の方法、またはそれに準じた方法にて製造したものを用いることも可能である。
上記の再結晶で用いられる溶媒は、例えば、水、メタノール、エタノール、2−プロパノール、ブタノール、ジエチルエーテル、テトラヒドロフラン、1,4−ジオキサン、n−ヘキサン、シクロヘキサン、ヘプタン、ベンゼン、トルエン、キシレン、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、1,3−ジメチル−2−イミダゾリジノン、クロロホルム、塩化メチレン、1,2−ジクロロエタン、アセトニトリル、アセトン、ジフェニルケトン、酢酸メチル、酢酸エチル、ジメチルスルホキシド、酢酸、トリフルオロ酢酸、メタンスルホン酸、等が挙げられる。これらの溶媒は、単独で用いることも可能であり、二種以上の溶媒を適当な割合、例えば、1:1〜1:10の割合で混合して用いることも可能である。また、式中の化合物が市販されている場合には市販品をそのまま用いることも可能であり、自体公知の方法、またはそれに準じた方法にて製造したものを用いることも可能である。
本発明の製造方法の各工程の各式に、変換可能な官能基(カルボキシ基、アミノ基、水酸基、カルボニル基、メルカプト基、−C(O)−O−C1〜6アルキル基、−C(O)−O−C6〜14アリール基、−C(O)−O−C7〜20アラルキル基、スルホ基、ハロゲン原子等)を含む場合には、これらの官能基を自体公知の方法またはそれに準ずる方法によって変換することにより種々の化合物を製造することができる。
前記の変換反応において、化合物が遊離の状態で得られる場合には、常法に従って塩に変換してもよく、また塩として得られる場合には、常法に従って遊離体またはその他の塩に変換することもできる。
前記の変換反応において、化合物が遊離の状態で得られる場合には、常法に従って塩に変換してもよく、また塩として得られる場合には、常法に従って遊離体またはその他の塩に変換することもできる。
これらの官能基の変換は、例えば、ラーロック(Richard C.Larock)らの、コンプリヘンシブ・オルガニック・トランスフォーメーション(Comprehensive Organic Transformations)、第2版、1999年10月刊、ウィリー ビーシーエッチ(Wiley−VCH)社、の成書に記載の方法等に準じて行う事ができる。
本発明の製造方法の各工程の各式に、置換基として水酸基、アミノ基、カルボキシ基、チオール基等の反応性基がある場合には、各反応工程においてこれらの基を適宜保護し、適当な段階で当該保護基を除去することもできる。
保護基の導入及び除去の方法は、保護される基又は保護基の種類により適宜行われるが、例えば、グリーン(Greene)らの『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)』の成書に記載の方法により行うことができる。
保護基の導入及び除去の方法は、保護される基又は保護基の種類により適宜行われるが、例えば、グリーン(Greene)らの『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)』の成書に記載の方法により行うことができる。
本発明の製造方法の各工程の反応温度は、特に断らない限り、−78℃から溶媒が還流する温度の範囲であれば、限定されない。又、反応時間は、特に断らない限り、反応が十分に進行する時間であれば、限定されない。
前記反応温度における、「−78℃から溶媒が還流する温度の範囲」の意味する処は、−78℃から反応に用いる溶媒(又は混合溶媒)が還流する温度迄の範囲内の温度を意味する。例えば、溶媒にメタノールを用いる場合、「−78℃から溶媒が還流する温度で」とは、−78℃からメタノールが還流する温度迄の範囲内の温度を意味する。また、同様に「−78℃から反応溶液が還流する温度で」とは、−78℃から反応溶液が還流する温度迄の範囲内の任意の温度を意味する。
前記反応温度における、「−78℃から溶媒が還流する温度の範囲」の意味する処は、−78℃から反応に用いる溶媒(又は混合溶媒)が還流する温度迄の範囲内の温度を意味する。例えば、溶媒にメタノールを用いる場合、「−78℃から溶媒が還流する温度で」とは、−78℃からメタノールが還流する温度迄の範囲内の温度を意味する。また、同様に「−78℃から反応溶液が還流する温度で」とは、−78℃から反応溶液が還流する温度迄の範囲内の任意の温度を意味する。
本明細書の製造方法中、特に断らない限り、「室温」とは、実験室、研究室等の温度の意味であり、1〜30℃の範囲の温度を意味する。
本発明の製造方法の各工程の反応は、無溶媒、又は反応前に原料化合物を適当な反応に関与しない溶媒に溶解又は懸濁して行うことができる。
前記、反応に関与しない溶媒としては、例えば、水、シクロヘキサン、ヘキサン、ベンゼン、クロロベンゼン、トルエン、キシレン、メタノール、エタノール、1−プロパノール、2−プロパノール、tert−ブチルアルコール、N,N−ジメチルホルムアミド(DMF)、N,N−ジメチルアセトアミド、ヘキサメチルホスホリックトリアミド、1,3‐ジメチル‐2‐イミダゾリジノン、ジメチルスルホキシド、アセトニトリル、プロピオニトリル、ジエチルエーテル、ジイソプロピルエーテル、ジフェニルエーテル、テトラヒドロフラン、1,4−ジオキサン、1,2−ジメトキシエタン、酢酸メチル、酢酸エチル、酢酸ブチル、アセトン、メチルエチルケトン、ジクロロメタン、クロロホルム、四塩化炭素、1,2−ジクロロエタン、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン、ルチジン、無水酢酸、ギ酸、酢酸、プロピオン酸、トリフルオロ酢酸、メタンスルホン酸、塩酸、硫酸、等が挙げられる。これらの溶媒は、単独で用いることも可能であり、又は反応条件により適宜選択し二種以上の溶媒を適宜の割合で混合して用いることも可能である。これらの溶媒は、反応条件に応じて適宜選択される。
本明細書の製造方法中、特に断らない限り、「反応に関与しない溶媒」と記載した場合、使用する溶媒は、一種の溶媒を単独で用いてもよく、または反応条件により適宜選択し二種以上の溶媒を適宜の割合で混合して用いてもよいことを意味する。
前記、反応に関与しない溶媒としては、例えば、水、シクロヘキサン、ヘキサン、ベンゼン、クロロベンゼン、トルエン、キシレン、メタノール、エタノール、1−プロパノール、2−プロパノール、tert−ブチルアルコール、N,N−ジメチルホルムアミド(DMF)、N,N−ジメチルアセトアミド、ヘキサメチルホスホリックトリアミド、1,3‐ジメチル‐2‐イミダゾリジノン、ジメチルスルホキシド、アセトニトリル、プロピオニトリル、ジエチルエーテル、ジイソプロピルエーテル、ジフェニルエーテル、テトラヒドロフラン、1,4−ジオキサン、1,2−ジメトキシエタン、酢酸メチル、酢酸エチル、酢酸ブチル、アセトン、メチルエチルケトン、ジクロロメタン、クロロホルム、四塩化炭素、1,2−ジクロロエタン、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン、ルチジン、無水酢酸、ギ酸、酢酸、プロピオン酸、トリフルオロ酢酸、メタンスルホン酸、塩酸、硫酸、等が挙げられる。これらの溶媒は、単独で用いることも可能であり、又は反応条件により適宜選択し二種以上の溶媒を適宜の割合で混合して用いることも可能である。これらの溶媒は、反応条件に応じて適宜選択される。
本明細書の製造方法中、特に断らない限り、「反応に関与しない溶媒」と記載した場合、使用する溶媒は、一種の溶媒を単独で用いてもよく、または反応条件により適宜選択し二種以上の溶媒を適宜の割合で混合して用いてもよいことを意味する。
本発明の製造方法の各工程で用いられる塩基(又は脱酸剤)としては、例えば、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化マグネシウム、炭酸リチウム、炭酸ナトリウム、炭酸カリウム、炭酸セシウム、炭酸カルシウム、炭酸水素ナトリウム、リン酸三カリウム、酢酸ナトリウム、フッ化セシウム、トリエチルアミン、N,N−ジイソプロピルエチルアミン、トリブチルアミン、シクロヘキシルジメチルアミン、ピリジン、ルチジン、4−ジメチルアミノピリジン(DMAP)、N,N−ジメチルアニリン、N−メチルピペリジン、N−メチルピロリジン、N−メチルモルホリン、1,5−ジアザビシクロ[4.3.0]−5−ノネン、1,4−ジアザビシクロ[2.2.2]オクタン、1,8−ジアザビシクロ[5.4.0]−7−ウンデセン(DBU)、イミダゾール、ナトリウムメトキシド、ナトリウムエトキシド、カリウムtert−ブトキシド、ナトリウムtert−ブトキシド、水素化ナトリウム、水素化カリウム、ナトリウムアミド、リチウムジイソプロピルアミド、リチウムヘキサメチルジシラジド、メチルリチウム、n−ブチルリチウム、sec−ブチルリチウム、tert−ブチルリチウム、等が挙げられる。但し、上記に記載したものに必ずしも限定されるわけではない。これらの塩基は、反応条件に応じて適宜選択される。
本発明の製造方法の各工程で用いられる酸、又は酸触媒は、例えば、塩酸、硫酸、硝酸、臭化水素酸、リン酸、酢酸、トリフルオロ酢酸、シュウ酸、フタル酸、フマル酸、酒石酸、マレイン酸、クエン酸、コハク酸、メタンスルホン酸、p−トルエンスルホン酸、10−カンファースルホン酸、三フッ化ホウ素エーテル錯体、ヨウ化亜鉛、無水塩化アルミニウム、無水塩化亜鉛、無水塩化鉄、等が挙げられる。但し、上記に記載したものに必ずしも限定されるわけではない。これらの酸又は酸触媒は、反応条件に応じて適宜選択される。
本発明の式(I)で表される化合物は、式(CA)で表されるカルボン酸誘導体[L=OHの場合:カルボン酸、式(CA−A);L=OMの場合:カルボン酸塩、式(CA−M);L=Xの場合:酸ハライド、式(CA−H)]と式(AM)で表わされるアミンの縮合反応から得ることができる。
以下に、式(CA)および式(AM)および式(I)で表される化合物の製造方法を示す。
[製造方法A]
式(CA)で表わされるカルボン酸誘導体[L=OHの場合:カルボン酸、式(CA);L=OMの場合:カルボン酸塩、式(CA−M);L=Xの場合:酸ハライド、式(CA−H)]の製造方法:
式(CA)で表わされるカルボン酸誘導体[L=OHの場合:カルボン酸、式(CA);L=OMの場合:カルボン酸塩、式(CA−M);L=Xの場合:酸ハライド、式(CA−H)]の製造方法:
<工程1>
<W=ボロン酸エステルの場合>
式(A−1)で表される化合物[式(A−1)で表わされる化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば『ザ・ジャーナル・オブ・オーガニック・ケミストリー(The Journal of Organic Chemistry)、60、7508‐2665、1995年』に記載された方法に準じて、ビス(ピナコラート)ジボロン、ビス(ネオペンチルグリコラート)ジボロン等のジボロンエステル存在下、酢酸パラジウム(II)、テトラキストリフェニルホスフィンパラジウム、トリス(ジベンジリデンアセトン)ジパラジウム、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)−ジクロロメタンコンプレックスなどのパラジウム触媒の存在下、トリフェニルホスフィン、トリス(tert−ブチル)ホスフィン、トリス(o−トリル)ホスフィン、2−ジシクロヘキシルホスフィノ−2’,6’−ジメトキシビフェニル等のホスフィン系試薬、およびトリエチルアミン、N,N−ジイソプロピルエチルアミン、炭酸カリウム、酢酸カリウム等の有機または無機塩基存在下または非存在下、またはホスフィン系試薬の替わりにテトラメチルアンモニウムクロリド、テトラブチルアンモニウムクロリド等存在下または非存在下、トルエン、N,N−ジメチルホルムアミド、ジメチルスルホキシド、1,4−ジオキサン等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるボロン酸エステルを製造することができる。
<W=ボロン酸エステルの場合>
式(A−1)で表される化合物[式(A−1)で表わされる化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば『ザ・ジャーナル・オブ・オーガニック・ケミストリー(The Journal of Organic Chemistry)、60、7508‐2665、1995年』に記載された方法に準じて、ビス(ピナコラート)ジボロン、ビス(ネオペンチルグリコラート)ジボロン等のジボロンエステル存在下、酢酸パラジウム(II)、テトラキストリフェニルホスフィンパラジウム、トリス(ジベンジリデンアセトン)ジパラジウム、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)−ジクロロメタンコンプレックスなどのパラジウム触媒の存在下、トリフェニルホスフィン、トリス(tert−ブチル)ホスフィン、トリス(o−トリル)ホスフィン、2−ジシクロヘキシルホスフィノ−2’,6’−ジメトキシビフェニル等のホスフィン系試薬、およびトリエチルアミン、N,N−ジイソプロピルエチルアミン、炭酸カリウム、酢酸カリウム等の有機または無機塩基存在下または非存在下、またはホスフィン系試薬の替わりにテトラメチルアンモニウムクロリド、テトラブチルアンモニウムクロリド等存在下または非存在下、トルエン、N,N−ジメチルホルムアミド、ジメチルスルホキシド、1,4−ジオキサン等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるボロン酸エステルを製造することができる。
<W=ボロン酸の場合>
式(A−1)で表される化合物を用い、文献公知の方法、例えば『ケミッシェ・ベリヒテ(Chemische Berichte)、42、3090、1909年』に記載された方法に準じて、トルエン、テトラヒドロフラン、1,4−ジオキサン等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、n−ブチルリチウム、sec−ブチルリチウム等のアルキルリチウム、イソプロピルマグネシウムクロリド等のグリニャール(Grignard)試薬、または金属マグネシウムの存在下、トリメチルボレート、トリイソプロピルボレート等のトリアルキルボレートを加え、−78℃から室温で反応を行った後、塩酸、硫酸等の酸を加え、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるボロン酸を製造することができる。
式(A−1)で表される化合物を用い、文献公知の方法、例えば『ケミッシェ・ベリヒテ(Chemische Berichte)、42、3090、1909年』に記載された方法に準じて、トルエン、テトラヒドロフラン、1,4−ジオキサン等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、n−ブチルリチウム、sec−ブチルリチウム等のアルキルリチウム、イソプロピルマグネシウムクロリド等のグリニャール(Grignard)試薬、または金属マグネシウムの存在下、トリメチルボレート、トリイソプロピルボレート等のトリアルキルボレートを加え、−78℃から室温で反応を行った後、塩酸、硫酸等の酸を加え、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるボロン酸を製造することができる。
<W=トリフルオロボレート塩の場合>
式(A−1)で表されるボロン酸エステルまたはボロン酸を用い、文献公知の方法、例えば『ケミカル・レビューズ(Chemical Reviews)、108、288‐325、2008年』に記載された方法に準じて、ジフッ化水素カリウム(KHF2)存在下、メタノール、エタノール、水等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるトリフルオロボレート塩を製造することができる。
式(A−1)で表されるボロン酸エステルまたはボロン酸を用い、文献公知の方法、例えば『ケミカル・レビューズ(Chemical Reviews)、108、288‐325、2008年』に記載された方法に準じて、ジフッ化水素カリウム(KHF2)存在下、メタノール、エタノール、水等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるトリフルオロボレート塩を製造することができる。
<W=ボロン酸 N−メチルイミノ二酢酸(MIDA)エステルの場合>
式(A−1)で表されるボロン酸を用い、文献公知の方法、例えば『ジャーナル・オブ・オルガノメタリック ケミストリー(Journal of Organometallic Chemistry)、307(1)、p1−6、1986年』に記載された方法に準じて、N−メチルイミノ二酢酸(MIDA)の存在下、ベンゼン、トルエン、キシレンまたはジメチルスルホキシド等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるボロン酸 N−メチルイミノ二酢酸(MIDA)エステルを製造することができる。
式(A−1)で表されるボロン酸を用い、文献公知の方法、例えば『ジャーナル・オブ・オルガノメタリック ケミストリー(Journal of Organometallic Chemistry)、307(1)、p1−6、1986年』に記載された方法に準じて、N−メチルイミノ二酢酸(MIDA)の存在下、ベンゼン、トルエン、キシレンまたはジメチルスルホキシド等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−2)で表されるボロン酸 N−メチルイミノ二酢酸(MIDA)エステルを製造することができる。
<工程2>
<製造方法A><工程1>で得られた式(A−2)で表わされる化合物と、式(A−3)で表わされる化合物[式(A−3)で表わされる化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば 『実験化学講座 第5版 18 有機化合物の合成 VI −金属を用いる有機合成−、327‐352頁、2004年、丸善』、および『ジャーナル・オブ・メディシナル・ケミストリー(Journal of Medicinal Chemistry)、48(20)、p6326‐6339、2005年』に記載された方法に準じて、酢酸パラジウム(II)(Pd(OAc)2)、テトラキストリフェニルホスフィンパラジウム(Pd(PPh3)4)、トリス(ジベンジリデンアセトン)ジパラジウム((dba)3Pd2)、ビス(ジベンジリデンアセトン)パラジウム((dba)2Pd)、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(Pd(dppf)Cl2)等のパラジウム触媒、トリフェニルホスフィン、トリス(tert−ブチル)ホスフィン、トリス(o−トリル)ホスフィン、2−ジシクロヘキシルホスフィノ−2’,6’−ジメトキシビフェニル、2−ジシクロヘキシルホスフィノ−2’,4’,6’−トリイソプロピルビフェニル等のホスフィン系試薬、およびトリエチルアミン、N,N−ジイソプロピルエチルアミン、リン酸カリウム、炭酸カリウム、炭酸セシウム等の有機または無機塩基存在下、トルエン、キシレン、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、ジメトキシエタン、アセトニトリル(アセトニトリル/水)、ジオキサン(ジオキサン/水)、テトラヒドロフラン(テトラヒドロフラン/水)等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−4)で表される化合物を製造することができる。またはホスフィン系試薬の替わりにテトラメチルアンモニウムクロリド、テトラブチルアンモニウムクロリド等を用いて、同様の方法にて製造することができる。
<製造方法A><工程1>で得られた式(A−2)で表わされる化合物と、式(A−3)で表わされる化合物[式(A−3)で表わされる化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば 『実験化学講座 第5版 18 有機化合物の合成 VI −金属を用いる有機合成−、327‐352頁、2004年、丸善』、および『ジャーナル・オブ・メディシナル・ケミストリー(Journal of Medicinal Chemistry)、48(20)、p6326‐6339、2005年』に記載された方法に準じて、酢酸パラジウム(II)(Pd(OAc)2)、テトラキストリフェニルホスフィンパラジウム(Pd(PPh3)4)、トリス(ジベンジリデンアセトン)ジパラジウム((dba)3Pd2)、ビス(ジベンジリデンアセトン)パラジウム((dba)2Pd)、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)(Pd(dppf)Cl2)等のパラジウム触媒、トリフェニルホスフィン、トリス(tert−ブチル)ホスフィン、トリス(o−トリル)ホスフィン、2−ジシクロヘキシルホスフィノ−2’,6’−ジメトキシビフェニル、2−ジシクロヘキシルホスフィノ−2’,4’,6’−トリイソプロピルビフェニル等のホスフィン系試薬、およびトリエチルアミン、N,N−ジイソプロピルエチルアミン、リン酸カリウム、炭酸カリウム、炭酸セシウム等の有機または無機塩基存在下、トルエン、キシレン、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、ジメトキシエタン、アセトニトリル(アセトニトリル/水)、ジオキサン(ジオキサン/水)、テトラヒドロフラン(テトラヒドロフラン/水)等の反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(A−4)で表される化合物を製造することができる。またはホスフィン系試薬の替わりにテトラメチルアンモニウムクロリド、テトラブチルアンモニウムクロリド等を用いて、同様の方法にて製造することができる。
<工程3>
<RA=C1〜6アルキル基(例えば、メチル、エチル基等)、C6〜14アリール基(例えば、フェニル基等)の場合>
<製造方法A><工程2>で得られた式(A−4)で表される化合物を用い、文献公知の方法、例えば『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、1−43頁、1992年、丸善』などに記載された方法に準じて、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等の塩基存在下、水およびメタノール、エタノール、2−プロパノール、N,N−ジメチルホルムアミド、1,4−ジオキサン、テトラヒドロフラン等の反応に不活性な溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、反応後の後処理工程の違いにより、式(CA−A)もしくは式(CA−M)で表わされる化合物を製造することができる。
<RA=C1〜6アルキル基(例えば、メチル、エチル基等)、C6〜14アリール基(例えば、フェニル基等)の場合>
<製造方法A><工程2>で得られた式(A−4)で表される化合物を用い、文献公知の方法、例えば『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、1−43頁、1992年、丸善』などに記載された方法に準じて、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等の塩基存在下、水およびメタノール、エタノール、2−プロパノール、N,N−ジメチルホルムアミド、1,4−ジオキサン、テトラヒドロフラン等の反応に不活性な溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、反応後の後処理工程の違いにより、式(CA−A)もしくは式(CA−M)で表わされる化合物を製造することができる。
<RA=tert−ブチル基の場合>
<製造方法A><工程2>で得られた式(A−4)で表される化合物を用い、塩酸、トリフルオロ酢酸等の酸を反応させることで、式(CA−A)で表わされる化合物を製造することができる。
<製造方法A><工程2>で得られた式(A−4)で表される化合物を用い、塩酸、トリフルオロ酢酸等の酸を反応させることで、式(CA−A)で表わされる化合物を製造することができる。
<RA=C7〜20アラルキル基(例えば、ベンジル基等)の場合>
<製造方法A><工程2>で得られた式(A−4)で表される化合物を用い、文献公知の方法、例えば『実験化学講座 第4版 26 有機合成VIII 不斉合成・還元・糖・標識化合物、159−266頁、1992年、丸善』等に記載された方法に準じて、パラジウム−炭素(Pd−C)、ラネーニッケル(Raney−Ni)、酸化白金(Pt2O)等の触媒存在下、水素ガス雰囲気下にて、メタノール、エタノール、2−プロパノール等のアルコール系溶媒、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等のエーテル系溶媒、酢酸エチル、酢酸メチル等の極性溶媒など反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(CA)で表される化合物を製造することができる。
<製造方法A><工程2>で得られた式(A−4)で表される化合物を用い、文献公知の方法、例えば『実験化学講座 第4版 26 有機合成VIII 不斉合成・還元・糖・標識化合物、159−266頁、1992年、丸善』等に記載された方法に準じて、パラジウム−炭素(Pd−C)、ラネーニッケル(Raney−Ni)、酸化白金(Pt2O)等の触媒存在下、水素ガス雰囲気下にて、メタノール、エタノール、2−プロパノール等のアルコール系溶媒、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等のエーテル系溶媒、酢酸エチル、酢酸メチル等の極性溶媒など反応に関与しない溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(CA)で表される化合物を製造することができる。
<工程4>
<製造方法A><工程3>で得られた式(CA−A)で表される化合物又は式(CA−M)で表される化合物を用い、文献公知の方法、例えば『ジャーナル・オブ・ザ・アメリカン・ケミカル・ソサエティ(Journal of the American Chemical Society)、109(24)、p7488−7494、1987年』等に記載された方法に準じて、トリエチルアミン、N,N−ジイソプロピルエチルアミン、N,N−ジメチルアミノピリジン等の塩基の存在もしくは非存在下、塩化チオニル、塩化オキサリル、塩化ホスホリル、塩化スルフリル、三塩化リン、五塩化リン、三臭化リン等のハロゲン化剤と、ジオキサン、テトラヒドロフラン、ベンゼン、トルエン、ジクロロメタン、1,2−ジクロロエタン、クロロホルム等の反応に不活性な溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(CA−H)で表される化合物を製造することができる。
<製造方法A><工程3>で得られた式(CA−A)で表される化合物又は式(CA−M)で表される化合物を用い、文献公知の方法、例えば『ジャーナル・オブ・ザ・アメリカン・ケミカル・ソサエティ(Journal of the American Chemical Society)、109(24)、p7488−7494、1987年』等に記載された方法に準じて、トリエチルアミン、N,N−ジイソプロピルエチルアミン、N,N−ジメチルアミノピリジン等の塩基の存在もしくは非存在下、塩化チオニル、塩化オキサリル、塩化ホスホリル、塩化スルフリル、三塩化リン、五塩化リン、三臭化リン等のハロゲン化剤と、ジオキサン、テトラヒドロフラン、ベンゼン、トルエン、ジクロロメタン、1,2−ジクロロエタン、クロロホルム等の反応に不活性な溶媒、もしくはこれらの混合溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(CA−H)で表される化合物を製造することができる。
[製造方法B]
式(CA−1)[式(CA)において、環Bが式(PS−1−1)で表わされるピラゾール環、及び環Aが2−オキサゾール環又は2−チアゾール環の場合]の合成:
式(CA−1)[式(CA)において、環Bが式(PS−1−1)で表わされるピラゾール環、及び環Aが2−オキサゾール環又は2−チアゾール環の場合]の合成:
<工程1>
式(B−1)で表される化合物、および式(B−2)で表される化合物[式(B−1)および式(B−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば『ストラテジック アプリケイションズ オブ ネームド リアクションズ イン オルガニック シンセシズ(Strategic Applications of Named Reactions in Organic Synthesis)、Elsevier Academic Press、2005、p438−439、Stille Cross−Coupling』等に記載された方法に準じて、テトラキストリフェニルホスフィンパラジウム(Pd(PPh3)4)等のパラジウム触媒存在下、フッ化セシウム、炭酸リチウム等の塩基の存在下または非存在下、トルエン、N,N−ジメチルホルムアミド、ジメチルスルホキシド、1,4−ジオキサン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で、室温から溶媒が還流する温度で反応を行うことにより、式(B−3)で表される化合物を製造することができる。
式(B−1)で表される化合物、および式(B−2)で表される化合物[式(B−1)および式(B−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば『ストラテジック アプリケイションズ オブ ネームド リアクションズ イン オルガニック シンセシズ(Strategic Applications of Named Reactions in Organic Synthesis)、Elsevier Academic Press、2005、p438−439、Stille Cross−Coupling』等に記載された方法に準じて、テトラキストリフェニルホスフィンパラジウム(Pd(PPh3)4)等のパラジウム触媒存在下、フッ化セシウム、炭酸リチウム等の塩基の存在下または非存在下、トルエン、N,N−ジメチルホルムアミド、ジメチルスルホキシド、1,4−ジオキサン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で、室温から溶媒が還流する温度で反応を行うことにより、式(B−3)で表される化合物を製造することができる。
<工程2>
<製造方法B><工程1>で得られる式(B−3)で表される化合物を用い、<製造方法A><工程3>と同様な方法により、式(CA−A2)または式(CA−M2)で表される化合物を製造することができる。
<製造方法B><工程1>で得られる式(B−3)で表される化合物を用い、<製造方法A><工程3>と同様な方法により、式(CA−A2)または式(CA−M2)で表される化合物を製造することができる。
<工程3>
<製造方法B><工程2>で得られる式(CA−A2)または式(CA−M2)で表される化合物を用い、<製造方法A><工程4>と同様な方法により、式(CA−H2)で表される化合物を製造することができる。
<製造方法B><工程2>で得られる式(CA−A2)または式(CA−M2)で表される化合物を用い、<製造方法A><工程4>と同様な方法により、式(CA−H2)で表される化合物を製造することができる。
[製造方法C]
式(CA−A3)、式(CA−M3)、および式(CA−H3)、[式(CA)において、環Bが式(PS−1−4)で表わされるピラゾール環、及び環Aが2−ピリジン環の場合]の合成:
式(CA−A3)、式(CA−M3)、および式(CA−H3)、[式(CA)において、環Bが式(PS−1−4)で表わされるピラゾール環、及び環Aが2−ピリジン環の場合]の合成:
<工程1>
式(C−1)で表される化合物、および式(C−2)で表される化合物[式(C−1)および式(C−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、<製造方法B><工程1>と同様な方法により、式(C−3)で表される化合物を製造することができる。
式(C−1)で表される化合物、および式(C−2)で表される化合物[式(C−1)および式(C−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、<製造方法B><工程1>と同様な方法により、式(C−3)で表される化合物を製造することができる。
<工程2>
<製造方法C><工程1>で得られる式(C−3)で表される化合物を用い、<製造方法A><工程3>と同様な方法により、式(CA−A3)または式(CA−M3)で表される化合物を製造することができる。
<製造方法C><工程1>で得られる式(C−3)で表される化合物を用い、<製造方法A><工程3>と同様な方法により、式(CA−A3)または式(CA−M3)で表される化合物を製造することができる。
<工程3>
<製造方法C><工程2>で得られる式(CA−A3)または式(CA−M3)で表される化合物を用い、<製造方法A><工程4>と同様な方法により、式(CA−H2)で表される化合物を製造することができる。
<製造方法C><工程2>で得られる式(CA−A3)または式(CA−M3)で表される化合物を用い、<製造方法A><工程4>と同様な方法により、式(CA−H2)で表される化合物を製造することができる。
[製造方法D]
[製造方法C]における、式(C−3)で表わされる化合物の別途合成:
[製造方法C]における、式(C−3)で表わされる化合物の別途合成:
<工程1>
式(D−1)で表される化合物および式(D−2)で表される化合物[式(D−1)で表される化合物および式(D−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『オルガニックレターズ、17(17)、p4144−4147、2015年』等に記載された方法に準じて、水素化ナトリウム、カリウムt−ブトキシド等の塩基の存在下、ジエチルエーテル、テトラヒドロフラン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で反応を行い、式(D−3)で表される化合物を製造することができる。
<工程2>
[製造方法D]<工程3>で得られる式(D−3)で表される化合物を用いて、文献公知の方法、例えば、『ヘテロサイクルズ、85(8)、p1913−1923、2012年』等に記載された方法に準じて、テトラヒドロフラン、トルエン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、N,N−ジメチルホルムアミドジメチルアセタールジエチルエーテルを室温から溶媒が還流する温度で反応させ、溶媒を留去した後、エタノール等の溶媒中、ヒドラジン一水和物を室温で反応させることで、式(D−4)で表される化合物を製造することができる。
式(D−1)で表される化合物および式(D−2)で表される化合物[式(D−1)で表される化合物および式(D−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『オルガニックレターズ、17(17)、p4144−4147、2015年』等に記載された方法に準じて、水素化ナトリウム、カリウムt−ブトキシド等の塩基の存在下、ジエチルエーテル、テトラヒドロフラン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で反応を行い、式(D−3)で表される化合物を製造することができる。
<工程2>
[製造方法D]<工程3>で得られる式(D−3)で表される化合物を用いて、文献公知の方法、例えば、『ヘテロサイクルズ、85(8)、p1913−1923、2012年』等に記載された方法に準じて、テトラヒドロフラン、トルエン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、N,N−ジメチルホルムアミドジメチルアセタールジエチルエーテルを室温から溶媒が還流する温度で反応させ、溶媒を留去した後、エタノール等の溶媒中、ヒドラジン一水和物を室温で反応させることで、式(D−4)で表される化合物を製造することができる。
<工程3>
[製造方法D]<工程2>で得られる式(D−4)で表される化合物、及び式(D−5)で表される化合物[式(D−5)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『バイオオルガニック アンド メディシナル ケミストリー レターズ、18(5)、p1702−1707、2008年』等に記載された方法に準じて、トリエチルアミン、ピリジン、水素化ナトリウム、水酸化ナトリウム、炭酸カリウム等の塩基の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N‐ジメチルホルムアミド等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で置換反応を行い、式(C−3)で表される化合物を製造することができる。
[製造方法D]<工程2>で得られる式(D−4)で表される化合物、及び式(D−5)で表される化合物[式(D−5)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『バイオオルガニック アンド メディシナル ケミストリー レターズ、18(5)、p1702−1707、2008年』等に記載された方法に準じて、トリエチルアミン、ピリジン、水素化ナトリウム、水酸化ナトリウム、炭酸カリウム等の塩基の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N‐ジメチルホルムアミド等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で置換反応を行い、式(C−3)で表される化合物を製造することができる。
[製造方法E]
式(CA−A5)、式(CA−M5)および式(CA−H5)[式(CA)において、環Bが式(PS−1−2)のトリアゾール環で、R4a=メチルの場合]の合成:
式(CA−A5)、式(CA−M5)および式(CA−H5)[式(CA)において、環Bが式(PS−1−2)のトリアゾール環で、R4a=メチルの場合]の合成:
<工程1>
式(E−1)で表される化合物[式(E−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]およびトリメチルシリルメチルアジドを用い、文献公知の方法、例えば、『国際公開2012/062687号パンフレット』等に記載された方法に準じて、ベンゼン、トルエン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で反応を行い、式(E−2)で表される化合物を製造することができる。
式(E−1)で表される化合物[式(E−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]およびトリメチルシリルメチルアジドを用い、文献公知の方法、例えば、『国際公開2012/062687号パンフレット』等に記載された方法に準じて、ベンゼン、トルエン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で反応を行い、式(E−2)で表される化合物を製造することができる。
<工程2>
[製造方法E]<工程1>で得られる式(E−2)で表される化合物を用い、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、トリメルシリル基を脱保護する事により、式(E−3)で表される化合物を製造することができる。
[製造方法E]<工程1>で得られる式(E−2)で表される化合物を用い、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、トリメルシリル基を脱保護する事により、式(E−3)で表される化合物を製造することができる。
<工程3>
[製造方法E]<工程2>で得られる式(E−3)で表される化合物を用い、[製造方法A]<工程3>と同様な方法により、式(CA−A5)または式(CA−M5)で表される化合物を製造することができる。
[製造方法E]<工程2>で得られる式(E−3)で表される化合物を用い、[製造方法A]<工程3>と同様な方法により、式(CA−A5)または式(CA−M5)で表される化合物を製造することができる。
<工程4>
[製造方法E]<工程3>で得られる式(CA−A5)または式(CA−M5)で表される化合物を用い、[製造方法A]<工程4>と同様な方法により、式(CA−H5)で表される化合物を製造することができる。
[製造方法E]<工程3>で得られる式(CA−A5)または式(CA−M5)で表される化合物を用い、[製造方法A]<工程4>と同様な方法により、式(CA−H5)で表される化合物を製造することができる。
[製造方法F]
式(CA−A6)、式(CA−M6)および式(CA−H6)[式(CA)において、環Bが式(PS−1−2)のトリアゾール環で、R4a≠メチルの場合]の合成:
式(CA−A6)、式(CA−M6)および式(CA−H6)[式(CA)において、環Bが式(PS−1−2)のトリアゾール環で、R4a≠メチルの場合]の合成:
<工程1>
式(E−1)で表される化合物および式(F−1)で表される化合物[式(F−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『ジャーナル オブ オルガニック ケミストリー、74(11)、p4318−4323、2009年』等に記載された方法に準じて、ベンゼン、トルエン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で反応を行い、式(E−2)で表される化合物を製造することができる。
式(E−1)で表される化合物および式(F−1)で表される化合物[式(F−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『ジャーナル オブ オルガニック ケミストリー、74(11)、p4318−4323、2009年』等に記載された方法に準じて、ベンゼン、トルエン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で0℃から溶媒が還流する温度で反応を行い、式(E−2)で表される化合物を製造することができる。
<工程2>
[製造方法F]<工程2>で得られる式(F−2)で表される化合物を用い、[製造方法A]<工程3>と同様な方法により、式(CA−A6)または式(CA−M6)で表される化合物を製造することができる。
[製造方法F]<工程2>で得られる式(F−2)で表される化合物を用い、[製造方法A]<工程3>と同様な方法により、式(CA−A6)または式(CA−M6)で表される化合物を製造することができる。
<工程3>
[製造方法F]<工程2>で得られる式(CA−A6)または式(CA−M6)で表される化合物を用い、[製造方法A]<工程4>と同様な方法により、式(CA−H6)で表される化合物を製造することができる。
[製造方法F]<工程2>で得られる式(CA−A6)または式(CA−M6)で表される化合物を用い、[製造方法A]<工程4>と同様な方法により、式(CA−H6)で表される化合物を製造することができる。
[製造方法G]
式(I−a−1)[式(I−a)において、環Aがトリアゾール環の場合]の合成:
式(I−a−1)[式(I−a)において、環Aがトリアゾール環の場合]の合成:
<工程1>
式(G−1)で表される化合物[式(G−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]およびトリメチルシリルアセチレンを用い、文献公知の方法、例えば、例えば『ストラテジック アプリケイションズ オブ ネームド リアクションズ イン オルガニック シンセシズ(Strategic Applications of Named Reactions in Organic Synthesis)、Elsevier Academic Press、2005、p424−425、Sonogasira Cross−Cupling』等に記載された方法に準じて、ヨウ化銅(CuI)、ビス(トリフェニルホスフィン)パラジウム(II)ジクロリド(Pd(PPh3)2Cl2)およびトリエチルアミン等の塩基の存在下、ベンゼン、N、N−ジメチルホルムアミド、酢酸エチル、アセトニトリル等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で室温から溶媒が還流する温度で反応を行い、式(G−2)で表される化合物を製造することができる。
<工程2>
[製造方法G]<工程1>で得られる式(G−2)で表される化合物を用い、[製造方法A]<工程3>と同様な方法により、式(G−3)で表される化合物を製造することができる。
式(G−1)で表される化合物[式(G−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]およびトリメチルシリルアセチレンを用い、文献公知の方法、例えば、例えば『ストラテジック アプリケイションズ オブ ネームド リアクションズ イン オルガニック シンセシズ(Strategic Applications of Named Reactions in Organic Synthesis)、Elsevier Academic Press、2005、p424−425、Sonogasira Cross−Cupling』等に記載された方法に準じて、ヨウ化銅(CuI)、ビス(トリフェニルホスフィン)パラジウム(II)ジクロリド(Pd(PPh3)2Cl2)およびトリエチルアミン等の塩基の存在下、ベンゼン、N、N−ジメチルホルムアミド、酢酸エチル、アセトニトリル等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中で室温から溶媒が還流する温度で反応を行い、式(G−2)で表される化合物を製造することができる。
<工程2>
[製造方法G]<工程1>で得られる式(G−2)で表される化合物を用い、[製造方法A]<工程3>と同様な方法により、式(G−3)で表される化合物を製造することができる。
<工程3>
[製造方法G]<工程2>で得られる式(G−3)で表される化合物および式(AM)で表わされるアミン[式(AM)で表されるアミンは、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、191−309頁、1992年、丸善』等に記載された方法に準じて、1,3−ジシクロヘキシルカルボジイミド(DCC)、1−エチル−3−(3’−ジメチルアミノプロピル)カルボジイミド塩酸塩(WSC・HCl)、1−ヒドロキシベンゾトリアゾール(HOBT)、ベンゾトリアゾール−1−イロキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェイト(BOP試薬)、ビス(2−オキソ−3−オキサゾリジニル)ホスフィニッククロリド(BOP−Cl)、2−クロロ−1,3−ジメチルイミダゾリニウムヘキサフルオロホスフェイト(CIP)、4−(4,6−ジメトキシ−1,3,5−トリアジン−2−イル)−4−メチルモルホリニウムクロリド(DMTMM)、ポリリン酸(PPA)、2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート メタンアミニウム(HATU)等の縮合剤の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N−ジメチルホルムアミド、メタノール、エタノール、2−プロパノール等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン等の塩基の存在下または非存在下、0℃から溶媒が還流する温度で反応を行い、式(G−4)で表される化合物を製造することができる。
<工程4>
[製造方法G]<工程3>で得られる式(G−4)で表される化合物を用い、[製造方法E]<工程1>と同様な方法により、式(I−a−1)で表される化合物を製造することができる。
[製造方法G]<工程2>で得られる式(G−3)で表される化合物および式(AM)で表わされるアミン[式(AM)で表されるアミンは、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、191−309頁、1992年、丸善』等に記載された方法に準じて、1,3−ジシクロヘキシルカルボジイミド(DCC)、1−エチル−3−(3’−ジメチルアミノプロピル)カルボジイミド塩酸塩(WSC・HCl)、1−ヒドロキシベンゾトリアゾール(HOBT)、ベンゾトリアゾール−1−イロキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェイト(BOP試薬)、ビス(2−オキソ−3−オキサゾリジニル)ホスフィニッククロリド(BOP−Cl)、2−クロロ−1,3−ジメチルイミダゾリニウムヘキサフルオロホスフェイト(CIP)、4−(4,6−ジメトキシ−1,3,5−トリアジン−2−イル)−4−メチルモルホリニウムクロリド(DMTMM)、ポリリン酸(PPA)、2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート メタンアミニウム(HATU)等の縮合剤の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N−ジメチルホルムアミド、メタノール、エタノール、2−プロパノール等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン等の塩基の存在下または非存在下、0℃から溶媒が還流する温度で反応を行い、式(G−4)で表される化合物を製造することができる。
<工程4>
[製造方法G]<工程3>で得られる式(G−4)で表される化合物を用い、[製造方法E]<工程1>と同様な方法により、式(I−a−1)で表される化合物を製造することができる。
[製造方法H]
式(AM−1)[式(AM)において、R2aおよびR2bでC3〜8シクロアルキル環を形成する場合]の合成:
式(AM−1)[式(AM)において、R2aおよびR2bでC3〜8シクロアルキル環を形成する場合]の合成:
<工程1>
文献公知の方法、例えば、『ジャーナル・オブ・メディシナル ケミストリー、58(15)、p5900−5915、2015年』等に記載された方法に準じて、ジエチルエーテル、テトラヒドルフラン、1,2−ジメトキシエタン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、−78度にて、n−ブチルリチウムを用いて式(H−2)で表される化合物[式(H−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]をリチオ化した後、式(H−1)で表される化合物[式(H−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を反応させる事により、式(H−3)で表される化合物を製造することができる。
<工程2>
[製造方法H]<工程2>で得られる式(H−3)で表される化合物を用い、文献公知の方法、例えば、『ジャーナル・オブ・メディシナル ケミストリー、58(15)、p5900−5915、2015年』等に記載された方法に準じて、アジ化ナトリウムを反応させる事で、式(H−4)で表される化合物を製造することができる。
<工程3>
[製造方法H]<工程3>で得られる式(H−4)で表される化合物を用い、文献公知の方法、例えば、『実験化学講座 第4版 26 有機合成VIII 不斉合成・還元・糖・標識化合物、159−266頁、1992年、丸善』等に記載された方法に準じて、水素化リチウムアルミニウム(LAH)等の還元剤存在下、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等の反応に関与しない溶媒中、0℃から溶媒が還流する温度で反応を行い、式(AM−1)で表される化合物を製造することができる。
文献公知の方法、例えば、『ジャーナル・オブ・メディシナル ケミストリー、58(15)、p5900−5915、2015年』等に記載された方法に準じて、ジエチルエーテル、テトラヒドルフラン、1,2−ジメトキシエタン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、−78度にて、n−ブチルリチウムを用いて式(H−2)で表される化合物[式(H−2)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]をリチオ化した後、式(H−1)で表される化合物[式(H−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を反応させる事により、式(H−3)で表される化合物を製造することができる。
<工程2>
[製造方法H]<工程2>で得られる式(H−3)で表される化合物を用い、文献公知の方法、例えば、『ジャーナル・オブ・メディシナル ケミストリー、58(15)、p5900−5915、2015年』等に記載された方法に準じて、アジ化ナトリウムを反応させる事で、式(H−4)で表される化合物を製造することができる。
<工程3>
[製造方法H]<工程3>で得られる式(H−4)で表される化合物を用い、文献公知の方法、例えば、『実験化学講座 第4版 26 有機合成VIII 不斉合成・還元・糖・標識化合物、159−266頁、1992年、丸善』等に記載された方法に準じて、水素化リチウムアルミニウム(LAH)等の還元剤存在下、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等の反応に関与しない溶媒中、0℃から溶媒が還流する温度で反応を行い、式(AM−1)で表される化合物を製造することができる。
[製造方法J]
式(AM−2)[式(AM)において、R2aおよびR2bでオキセタン環、テトラヒドロピラン環等を形成する場合]の合成:
式(AM−2)[式(AM)において、R2aおよびR2bでオキセタン環、テトラヒドロピラン環等を形成する場合]の合成:
<工程1>
式(J−1)で表される化合物[式(J−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]および2−メチル−2−プロパンスルフィンアミドを用い、文献公知の方法、例えば、『オルガニックレターズ(Organic Letters)、12(5)、1116−1119頁、2010年』等に記載された方法に準じて、オルトチタン酸 テトラエチル等のルイス酸存在下、テトラヒドロフラン等の反応に関与しない溶媒中、0℃から溶媒が還流する温度で反応を行い、式(J−2)で表される化合物を製造することができる。
<工程2>
[製造方法J]<工程1>で得られる式(J−2)で表される化合物および[製造方法H]<工程1>に記載された方法に準じて調整される式(H−2−L)で表わされるリチオ化合物を用い、文献公知の方法、例えば、『オルガニックレターズ(Organic Letters)、12(5)、1116−1119頁、2010年』等に記載された方法に準じて、テトラヒドロフラン等の反応に関与しない溶媒中、−78℃から室温で反応を行い、式(J−3)で表される化合物を製造することができる。
<工程3>
[製造方法J]<工程2>で得られる式(J−3)で表される化合物を用いて、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、2−メチル−2−プロパンスルフィニル基を脱保護する事により、式(AM−2)で表される化合物を製造することができる。
式(J−1)で表される化合物[式(J−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]および2−メチル−2−プロパンスルフィンアミドを用い、文献公知の方法、例えば、『オルガニックレターズ(Organic Letters)、12(5)、1116−1119頁、2010年』等に記載された方法に準じて、オルトチタン酸 テトラエチル等のルイス酸存在下、テトラヒドロフラン等の反応に関与しない溶媒中、0℃から溶媒が還流する温度で反応を行い、式(J−2)で表される化合物を製造することができる。
<工程2>
[製造方法J]<工程1>で得られる式(J−2)で表される化合物および[製造方法H]<工程1>に記載された方法に準じて調整される式(H−2−L)で表わされるリチオ化合物を用い、文献公知の方法、例えば、『オルガニックレターズ(Organic Letters)、12(5)、1116−1119頁、2010年』等に記載された方法に準じて、テトラヒドロフラン等の反応に関与しない溶媒中、−78℃から室温で反応を行い、式(J−3)で表される化合物を製造することができる。
<工程3>
[製造方法J]<工程2>で得られる式(J−3)で表される化合物を用いて、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、2−メチル−2−プロパンスルフィニル基を脱保護する事により、式(AM−2)で表される化合物を製造することができる。
[製造方法K]
式(AM−3)[式(AM)において、R2a=H、およびR2b=で1−ヒドロキシ−1−メチル−エチル基の場合]の合成:
式(AM−3)[式(AM)において、R2a=H、およびR2b=で1−ヒドロキシ−1−メチル−エチル基の場合]の合成:
<工程1>
式(K−1)で表される化合物[式(K−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、1−82頁、1992年、丸善』等に記載された方法に準じて、塩酸、硫酸、塩化チオニル、塩化アセチル等の酸性試薬存在下、メタノール、エタノール、2−プロパノール等の溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(K−2)で表される化合物を製造することができる。
<工程2>
[製造方法K]<工程1>で得られる式(K−2)で表される化合物を用い、文献公知の方法、例えば、『実験化学講座 第4版 25、有機合成VII、有機金属試薬による合成、13−19頁、59−72頁、1992年、丸善』等に記載された方法に準じて、大過剰のメチルマグネシウムブロミド等のグリニア試薬の存在下、ジエチルエーテル、1,4−ジオキサン、テトラヒドロフラン、1,2−ジメトキシエタン、ベンゼン、トルエン、キシレン等の反応に関与しない溶媒中、−78度から溶媒が還流する温度で反応を行い、式(J−2)で表される化合物を製造することができる。
式(K−1)で表される化合物[式(K−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、1−82頁、1992年、丸善』等に記載された方法に準じて、塩酸、硫酸、塩化チオニル、塩化アセチル等の酸性試薬存在下、メタノール、エタノール、2−プロパノール等の溶媒を用いて、0℃から溶媒が還流する温度で反応を行い、式(K−2)で表される化合物を製造することができる。
<工程2>
[製造方法K]<工程1>で得られる式(K−2)で表される化合物を用い、文献公知の方法、例えば、『実験化学講座 第4版 25、有機合成VII、有機金属試薬による合成、13−19頁、59−72頁、1992年、丸善』等に記載された方法に準じて、大過剰のメチルマグネシウムブロミド等のグリニア試薬の存在下、ジエチルエーテル、1,4−ジオキサン、テトラヒドロフラン、1,2−ジメトキシエタン、ベンゼン、トルエン、キシレン等の反応に関与しない溶媒中、−78度から溶媒が還流する温度で反応を行い、式(J−2)で表される化合物を製造することができる。
[製造方法L]
式(AM−3−C)[式(AM−3)の光学活性体]の合成:
式(AM−3−C)[式(AM−3)の光学活性体]の合成:
<工程1>
式(L−1)で表される化合物[式(L−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]および光学活性な2−メチル−2−プロパンスルフィンアミドを用い、文献公知の方法、例えば、『国際公開2012/063207号パンフレット』等に記載された方法に準じて、トルエン等の反応に関与しない溶媒中、室温から溶媒が還流する温度で反応を行い、式(L−2)で表される化合物を製造することができる。
<工程2>
[製造方法L]<工程1>で得られる式(L−2)で表される化合物および式(L−3)で表される化合物[式(L−3)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『ジャーナル・オブ・ザ・アメリカン・ケミカル・ソサエティ(Journal of the American Chemical Society)、127(4)、p1092−1093、2005年』等等に記載された方法に準じて、ビス(アセトニトリル)(1,5−シクロオクタジエン)ロジウム(I)テトラフルオロボレート等のロジウム触媒およびトリエチルアミン等の塩基存在下、1,4−ジオキサン等の反応に関与しない溶媒中、室温から溶媒が還流する温度で反応を行い、式(L−4)で表される化合物を製造することができる。
式(L−1)で表される化合物[式(L−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]および光学活性な2−メチル−2−プロパンスルフィンアミドを用い、文献公知の方法、例えば、『国際公開2012/063207号パンフレット』等に記載された方法に準じて、トルエン等の反応に関与しない溶媒中、室温から溶媒が還流する温度で反応を行い、式(L−2)で表される化合物を製造することができる。
<工程2>
[製造方法L]<工程1>で得られる式(L−2)で表される化合物および式(L−3)で表される化合物[式(L−3)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]を用い、文献公知の方法、例えば、『ジャーナル・オブ・ザ・アメリカン・ケミカル・ソサエティ(Journal of the American Chemical Society)、127(4)、p1092−1093、2005年』等等に記載された方法に準じて、ビス(アセトニトリル)(1,5−シクロオクタジエン)ロジウム(I)テトラフルオロボレート等のロジウム触媒およびトリエチルアミン等の塩基存在下、1,4−ジオキサン等の反応に関与しない溶媒中、室温から溶媒が還流する温度で反応を行い、式(L−4)で表される化合物を製造することができる。
<工程3>
[製造方法L]<工程2>で得られる式(L−4)で表される化合物を用いて、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、2−メチル−2−プロパンスルフィニル基を脱保護する事により、式(K−2−C)で表される化合物を製造することができる。
<工程4>
[製造方法L]<工程3>で得られる式(K−2−C)で表される化合物を用い、[製造方法K]<工程2>と同様な方法により、式(AM−3−C)で表される化合物を製造することができる。
[製造方法L]<工程2>で得られる式(L−4)で表される化合物を用いて、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、2−メチル−2−プロパンスルフィニル基を脱保護する事により、式(K−2−C)で表される化合物を製造することができる。
<工程4>
[製造方法L]<工程3>で得られる式(K−2−C)で表される化合物を用い、[製造方法K]<工程2>と同様な方法により、式(AM−3−C)で表される化合物を製造することができる。
[製造方法M]
式(AM−4)および式(AM−4−C)[式(AM)において、R2a=H、およびR2b=でメトキシメチル基の場合の光学活性体]の合成:
式(AM−4)および式(AM−4−C)[式(AM)において、R2a=H、およびR2b=でメトキシメチル基の場合の光学活性体]の合成:
<工程1>
式(M−1)で表される化合物[式(M−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]およびヒドロキシルアミン塩酸塩を用い、文献公知の方法、例えば、『ジャーナル オブ オルガニック ケミストリー(Journal of Organic Chemistry)、75(18)、p6271−6274頁、2010年』等に記載された方法に準じて、ピリジン、N,N−ジイソプロピルエチルアミン、炭酸ナトリウム、炭酸カリウム、炭酸水素ナトリウム等の塩基存在下又は非存在下、メタノール、エタノール、水等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、0度から溶媒が還流する温度で反応を行い、式(M−2)の化合物を製造することができる。
<工程2>
[製造方法M]<工程1>で得られる式(M−2)で表される化合物を用い、文献公知の方法、例えば、『実験化学講座 第4版 26 有機合成VIII 不斉合成・還元・糖・標識化合物、159−266頁、1992年、丸善』等に記載された方法に準じて、パラジウム−炭素(Pd−C)、ラネーニッケル(Raney−Ni)、酸化白金(PtO2)等の触媒存在下、水素ガス雰囲気下にて、メタノール、エタノール、2−プロパノール、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン、酢酸エチル、酢酸メチル等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、0度から溶媒が還流する温度で反応を行い、式(AM−4)の化合物を製造することができる。
<工程3>
[製造方法M]<工程2>で得られる式(AM−4)で表される化合物を用い、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、アミノ基を保護することにより、式(M−3)で表される化合物を製造することができる。
<工程4>
[製造方法M]<工程3>で得られる式(M−3)で表される化合物を用い、前記記載のキラルカラム法を用いることにより、式(M−4)で表される化合物を製造することができる。
<工程5>
[製造方法M]<工程4>で得られる式(M−4)で表される化合物を用い、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、保護基P1を脱保護する事により、式(AM−4−C)で表される化合物を製造することができる。
式(M−1)で表される化合物[式(M−1)で表される化合物は、市販化合物、または市販化合物から文献公知の製造方法により製造できる化合物である]およびヒドロキシルアミン塩酸塩を用い、文献公知の方法、例えば、『ジャーナル オブ オルガニック ケミストリー(Journal of Organic Chemistry)、75(18)、p6271−6274頁、2010年』等に記載された方法に準じて、ピリジン、N,N−ジイソプロピルエチルアミン、炭酸ナトリウム、炭酸カリウム、炭酸水素ナトリウム等の塩基存在下又は非存在下、メタノール、エタノール、水等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、0度から溶媒が還流する温度で反応を行い、式(M−2)の化合物を製造することができる。
<工程2>
[製造方法M]<工程1>で得られる式(M−2)で表される化合物を用い、文献公知の方法、例えば、『実験化学講座 第4版 26 有機合成VIII 不斉合成・還元・糖・標識化合物、159−266頁、1992年、丸善』等に記載された方法に準じて、パラジウム−炭素(Pd−C)、ラネーニッケル(Raney−Ni)、酸化白金(PtO2)等の触媒存在下、水素ガス雰囲気下にて、メタノール、エタノール、2−プロパノール、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン、酢酸エチル、酢酸メチル等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、0度から溶媒が還流する温度で反応を行い、式(AM−4)の化合物を製造することができる。
<工程3>
[製造方法M]<工程2>で得られる式(AM−4)で表される化合物を用い、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、アミノ基を保護することにより、式(M−3)で表される化合物を製造することができる。
<工程4>
[製造方法M]<工程3>で得られる式(M−3)で表される化合物を用い、前記記載のキラルカラム法を用いることにより、式(M−4)で表される化合物を製造することができる。
<工程5>
[製造方法M]<工程4>で得られる式(M−4)で表される化合物を用い、文献公知の方法、例えば、『プロテクティブ・グループス・イン・オーガニック・シンセシス(Protective Groups in Organic Synthesis 4thEdition) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)、グリーン(Greene)ら』の成書に記載された方法に準じて、保護基P1を脱保護する事により、式(AM−4−C)で表される化合物を製造することができる。
<製造方法N>
式(I)の合成:式(CA−A)、式(CA−M)または式(CA−H)で表わされるカルボン酸誘導体と、式(AM)で表わされるアミンとの縮合反応。
式(I)の合成:式(CA−A)、式(CA−M)または式(CA−H)で表わされるカルボン酸誘導体と、式(AM)で表わされるアミンとの縮合反応。
<工程1>
式(CA−M)で表わされるカルボン酸塩および式(AM)で表わされるアミンを用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、191−309ページ、1992年、丸善』等に記載された方法に準じて、2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート メタンアミニウム(HATU)等の縮合剤の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N−ジメチルホルムアミド、メタノール、エタノール、2−プロパノール等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、N,N−ジイソプロピルエチルアミン、トリエチルアミン、ピリジン等の塩基存在下または非存在下、0℃から溶媒が還流する温度で反応させることにより、式(I)で表わされる化合物を製造することができる。
式(CA−M)で表わされるカルボン酸塩および式(AM)で表わされるアミンを用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、191−309ページ、1992年、丸善』等に記載された方法に準じて、2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート メタンアミニウム(HATU)等の縮合剤の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N−ジメチルホルムアミド、メタノール、エタノール、2−プロパノール等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、N,N−ジイソプロピルエチルアミン、トリエチルアミン、ピリジン等の塩基存在下または非存在下、0℃から溶媒が還流する温度で反応させることにより、式(I)で表わされる化合物を製造することができる。
<工程2>
式(CA−A)で表わされるカルボン酸および式(AM)で表わされるアミンを用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、191−309頁、1992年、丸善』等に記載された方法に準じて、1,3−ジシクロヘキシルカルボジイミド(DCC)、1−エチル−3−(3’−ジメチルアミノプロピル)カルボジイミド塩酸塩(WSC・HCl)、1−ヒドロキシベンゾトリアゾール(HOBT)、ベンゾトリアゾール−1−イロキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェイト(BOP試薬)、ビス(2−オキソ−3−オキサゾリジニル)ホスフィニッククロリド(BOP−Cl)、2−クロロ−1,3−ジメチルイミダゾリニウムヘキサフルオロホスフェイト(CIP)、4−(4,6−ジメトキシ−1,3,5−トリアジン−2−イル)−4−メチルモルホリニウムクロリド(DMTMM)、ポリリン酸(PPA)、2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート メタンアミニウム(HATU)等の縮合剤の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N−ジメチルホルムアミド、メタノール、エタノール、2−プロパノール等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン等の塩基存在下または非存在下、0℃から溶媒が還流する温度で反応させることにより、式(I)で表される化合物を製造することができる。
式(CA−A)で表わされるカルボン酸および式(AM)で表わされるアミンを用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV 酸・アミノ酸・ペプチド、191−309頁、1992年、丸善』等に記載された方法に準じて、1,3−ジシクロヘキシルカルボジイミド(DCC)、1−エチル−3−(3’−ジメチルアミノプロピル)カルボジイミド塩酸塩(WSC・HCl)、1−ヒドロキシベンゾトリアゾール(HOBT)、ベンゾトリアゾール−1−イロキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェイト(BOP試薬)、ビス(2−オキソ−3−オキサゾリジニル)ホスフィニッククロリド(BOP−Cl)、2−クロロ−1,3−ジメチルイミダゾリニウムヘキサフルオロホスフェイト(CIP)、4−(4,6−ジメトキシ−1,3,5−トリアジン−2−イル)−4−メチルモルホリニウムクロリド(DMTMM)、ポリリン酸(PPA)、2−(1H−7−アザベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート メタンアミニウム(HATU)等の縮合剤の存在下、ジクロロメタン、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、N,N−ジメチルホルムアミド、メタノール、エタノール、2−プロパノール等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン等の塩基存在下または非存在下、0℃から溶媒が還流する温度で反応させることにより、式(I)で表される化合物を製造することができる。
<工程3>
式(CA−H)で表わされる酸ハライドおよび式(AM)で表わされるアミンを用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV酸・アミノ酸・ペプチド、144−146頁、1992年、丸善』等に記載された方法に準じて、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン、4−ジメチルアミノピリジン等の塩基の存在下、ジクロロメタン、クロロホルム、1,2−ジクロロエタン、ジエチルエーテル、テトラドロフラン、1,4−ジオキサン、トルエン、ベンゼン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、0℃から溶媒が還流する温度で反応させることにより、式(I)で表わされる化合物を同様に製造することができる。
式(CA−H)で表わされる酸ハライドおよび式(AM)で表わされるアミンを用いて、文献公知の方法、例えば、『実験化学講座 第4版 22 有機合成IV酸・アミノ酸・ペプチド、144−146頁、1992年、丸善』等に記載された方法に準じて、トリエチルアミン、N,N−ジイソプロピルエチルアミン、ピリジン、4−ジメチルアミノピリジン等の塩基の存在下、ジクロロメタン、クロロホルム、1,2−ジクロロエタン、ジエチルエーテル、テトラドロフラン、1,4−ジオキサン、トルエン、ベンゼン等の反応に関与しない溶媒又はこれらの溶媒の混合溶媒中、0℃から溶媒が還流する温度で反応させることにより、式(I)で表わされる化合物を同様に製造することができる。
本発明の一般式(I)で表わされる化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物は、後述する薬理実験例1(ヒトPDE2A阻害作用)において、優れたPDE2A阻害活性を有する。本発明の化合物におけるPDE2A阻害作用は、PDE2A阻害作用を適宜選択した方法、例えば、後述の薬理実験例1(ヒト由来PDE2A阻害作用)で測定した場合、IC50値で、1000nM以下が好ましく、より好ましくは100nM以下である化合物を用いることが好ましい。
また、本発明の一般式(I)で表わされる化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物は、PDE2Aに対して非常に選択性が高く、選択的PDE2A阻害剤である。
本明細書において特に断りが無い限り、「選択的PDE2A阻害剤」とは、PDE1又はPDE3〜11阻害活性と比して、大幅にPDE2A阻害活性を有する化合物を意味する。一実施形態において、「選択的PDE2A阻害剤」とは、好ましくは、他の任意のPDE酵素(例えば、PDE1A、3A、4A、4B、5A、6、7A、7B、8A、9A、10Aおよび11A)阻害に関して、その化合物が有するIC50値の約1/1000以下であるPDE2A阻害活性を有する化合物である。言い換えると、該化合物は、他の任意のPDE酵素を阻害する場合に必要とされるIC50値の約1/1000以下でPDE2A活性を同程度阻害する。
また、本発明の一般式(I)で表わされる化合物若しくはそれらの製薬学的に許容される塩、又はそれらの溶媒和物は、PDE2Aに対して非常に選択性が高く、選択的PDE2A阻害剤である。
本明細書において特に断りが無い限り、「選択的PDE2A阻害剤」とは、PDE1又はPDE3〜11阻害活性と比して、大幅にPDE2A阻害活性を有する化合物を意味する。一実施形態において、「選択的PDE2A阻害剤」とは、好ましくは、他の任意のPDE酵素(例えば、PDE1A、3A、4A、4B、5A、6、7A、7B、8A、9A、10Aおよび11A)阻害に関して、その化合物が有するIC50値の約1/1000以下であるPDE2A阻害活性を有する化合物である。言い換えると、該化合物は、他の任意のPDE酵素を阻害する場合に必要とされるIC50値の約1/1000以下でPDE2A活性を同程度阻害する。
本発明の本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物は、PDE2A阻害活性を有しており、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療に有効である。さらに本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物のいくつかの化合物は、安全性も高くPDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療に有効である。
次に本発明の医薬組成物について説明する。本発明の医薬組成物は、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の少なくともひとつを有効成分として含有するものである。
即ち、本発明の医薬組成物は、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の少なくともひとつ、及び製薬上許容される担体を含有してなるものである。本発明の医薬組成物は、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療に有効である。
即ち、本発明の医薬組成物は、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の少なくともひとつ、及び製薬上許容される担体を含有してなるものである。本発明の医薬組成物は、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療に有効である。
また、本発明は、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物を含有してなる、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防剤及び/又は治療剤に関する。
本発明は、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療のための医薬組成物を製造するための、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の使用(USE)に関する。
さらに、本発明は、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療のための医薬組成物に使用するための、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物に関する。
また、本発明は、PDE2Aが関与する疾患若しくはPDE2A受容体が関与する疾患の患者、又はPDE2Aが関与する疾患若しくはPDE2A受容体が関与する疾患になりそうな患者に、治療又は予防に有効な量の本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物を含有する医薬組成物を投与することを含む、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防方法及び/又は治療方法に関する。
本発明は、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療のための医薬組成物を製造するための、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の使用(USE)に関する。
さらに、本発明は、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防及び/又は治療のための医薬組成物に使用するための、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物に関する。
また、本発明は、PDE2Aが関与する疾患若しくはPDE2A受容体が関与する疾患の患者、又はPDE2Aが関与する疾患若しくはPDE2A受容体が関与する疾患になりそうな患者に、治療又は予防に有効な量の本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物を含有する医薬組成物を投与することを含む、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患の予防方法及び/又は治療方法に関する。
PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患としては、例えば、(1)統合失調症(妄想型、解体型、緊張型、鑑別不能型、又は残遺型)、(2)統合失調症様障害、(3)統合失調感情障害(妄想型又は抑うつ型)、(4)妄想性障害、(5)物質誘導性精神障害、(6)妄想型人格障害、(7)統合失調型の人格障害、(8)ハンチントン病、(9)ドーパミンアゴニスト療法に伴う異常運動症(ジスキネジア)、(10)パーキンソン病、(11)不穏下肢症候群、(12)本態性振戦、(13)恐慌性障害、(14)広場恐怖症、(15)特定恐怖症、(16)社会恐怖症、(17)強迫性障害、(18)心的外傷後ストレス障害、(19)急性ストレス障害、(20)全般性不安障害、(21)食欲不振症、(22)過食症、(23)気晴らし食い障害、(24)氷食症、(25)過眠症、(26)概日リズム睡眠障害、(27)不眠症、(28)睡眠時異常行動、(29)睡眠遮断、(30)大うつ病エピソード(軽度、中等度、又は重度型)、(31)躁病エピソード、(32)混合性エピソード、(33)軽躁病エピソード、(34)非定型うつ病、(35)メランコリー型うつ病、(36)緊張病性うつ病、(37)季節性うつ病、(38)産後発症気分エピソード、(39)脳卒中後うつ病、(40)大うつ病性障害、(41)気分変調性障害、(42)気分変調症、(43)小うつ病性障害、(44)月経前不快気分障害、(45)統合失調症後うつ病性障害、(46)妄想性障害又は統合失調症等の精神障害に併発する大うつ病性障害、(47)双極性障害(I型及びII型)、(48)気分循環性障害、(49)偏頭痛、(50)てんかん、(51)ハンチントン病、(52)脳外傷に関連する神経変性、(53)脳卒中に関連する神経変性、(54)脳梗塞に関連する神経変性、(55)低血糖誘発性神経変性、(56)てんかん発作に関連する神経変性、(57)神経毒中毒に関連する神経変性、(58)多系統委縮症、(59)線条体中型有棘ニューロンの神経変性、(60)加齢性認知低下、(61)アルツハイマー病、(62)統合失調症又はアルツハイマー病に伴う認知症、(63)多発脳梗塞性認知症、(64)アルコール性認知症又は他の薬物関連認知症、(65)頭蓋内腫瘍又は脳外傷に関連する認知症、(66)ハンチントン病又はパーキンソン病に関連する認知症、(67)エイズ関連認知症、(68)前頭側頭型認知症、(69)せん妄、(70)健忘障害、(71)心的外傷後ストレス障害、(72)精神遅滞、(73)読字障害、(74)算数障害、(75)書字表出障害、(76)注意欠陥障害、(77)注意欠陥/多動性障害(ADHA)、(78)行為障害、(79)自閉症、(80)薬物依存症、(81)トゥーレット症候群、(82)チック障害、(83)精神薄弱(ダウン症候群及び脆弱X症候群を含む。)、(84)肥満、(85)メタボリック症候群、(86)インスリン非依存性糖尿病、(87)耐糖能障害、(89)肺炎、及び(90)変形性関節症等が挙げられる。
これらの疾患の中でも、PDE2Aが関与する疾患又はPDE2A受容体が関与する疾患として特に精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症等が挙げられる。
本発明に従って治療することのできる「精神障害」としては、例えば、(1)統合失調症(妄想型、解体型、緊張型、鑑別不能型、又は残遺型)、(2)統合失調症様障害、(3)統合失調感情障害(妄想型又は抑うつ型)、(4)妄想性障害、(5)物質誘導性精神障害(例えば、アルコール、アンフェタミン、大麻、コカイン、幻覚剤、吸入剤、オピオイド、またはフェンシクリジンによって誘発された精神病)、(6)妄想型人格障害、及び(7)統合失調型の人格障害、等が挙げられる。但し、これらに限定されるものではない。
本明細書中、特に断りのない限り、「統合失調症」又は「統合失調症様障害」の症状としては、例えば、(1)陽性症状、陰性症状、及び其れに関連する妄想及び/又は幻覚症状、(2)解体した会話(頻繁に脱線したり、支離滅裂な会話)、(3)感情の平板化(感情表現の幅と強さの著しい低下)、(4)アロギー(会話の内容と量の低下)、(5)アンヘドニア(快感能力の消失/減退)、(6)不相応な情動、(7)不快気分(例えば、抑うつ、不安、または怒り等)、(8)意欲低下、(9)非社会性(社会的交流から喜びを得る能力の欠如)、及び(10)認知機能障害の一部等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「運動障害」としては、例えば、(1)ハンチントン病、(2)ドーパミンアゴニスト療法に伴う異常運動症(ジスキネジア)、(3)パーキンソン病、(4)不穏下肢症候群(Restless Legs Syndrome:RLS)、及び(5)本態性振戦、等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「不安障害」としては、例えば、(1)恐慌性障害、(2)広場恐怖症、(3)特定恐怖症、(4)社会恐怖症、(5)強迫性障害、(6)心的外傷後ストレス障害、(7)急性ストレス障害、及び(8)全般性不安障害、等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「摂食障害」としては、例えば、(1)食欲不振症、(2)過食症、(3)気晴らし食い障害、及び(4)氷食症、等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「睡眠障害」としては、例えば、(1)過眠症、(2)概日リズム睡眠障害、(3)不眠症、(4)睡眠時異常行動、及び(5)睡眠遮断、等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「睡眠障害」としては、例えば、(1)過眠症、(2)概日リズム睡眠障害、(3)不眠症、(4)睡眠時異常行動、及び(5)睡眠遮断、等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「気分障害(気分エピソード)」としては、例えば、(1)大うつ病エピソード(軽度、中等度、又は重度型)、躁病エピソード、混合性エピソード、軽躁病エピソード、(2)非定型うつ病、(3)メランコリー型うつ病、(4)緊張病性うつ病、(5)季節性うつ病、(6)産後発症気分エピソード、(7)脳卒中後うつ病、(8)大うつ病性障害、(9)気分変調性障害/気分変調症、(10)小うつ病性障害、(11)月経前不快気分障害、(12)統合失調症後うつ病性障害、(13)妄想性障害又は統合失調症等の精神障害に併発する大うつ病性障害、(14)双極性障害(I型及びII型)、及び(15)気分循環性障害、等が挙げられる。但し、これらに限定されるものではない。
本明細書中、特に断りのない限り、「神経変性障害」は、中枢神経系におけるニューロンの機能不全、及び/又はニューロン死に起因する神経機能障害または状態を意味する。神経変性障害の治療には、当該障害での危機的状態にあるニューロンの機能不全及び/又はニューロン死を防ぐか、且つ/又は危機的状態にあるニューロンの機能不全、又はニューロン死に起因する機能喪失を補う為に、損傷している若しくは正常に働いているニューロンの機能を高められる薬剤を投与すること、等が挙げられる。
本発明に従って治療することのできる「神経変性障害」としては、例えば、(1)偏頭痛、(2)てんかん、(3)パーキンソン病、(4)ハンチントン病、(5)認知症、(6)脳外傷に関連する神経変性、(7)脳卒中に関連する神経変性、(8)脳梗塞に関連する神経変性、(9)低血糖誘発性神経変性、(10)てんかん発作に関連する神経変性、(11)神経毒中毒に関連する神経変性、(12)多系統委縮症、及び(13)線条体中型有棘ニューロンの神経変性、等が挙げられる。但し、これらに限定されるものではない。
本明細書中、特に断りのない限り、「神経毒中毒」とは、神経毒による中毒を指す。神経毒は、神経死、即ち神経学的損傷を引き起こしうる任意の化学物質または物質である。神経毒の例としてアルコールが挙げられる。アルコールが妊婦によって乱用された場合、新生児は胎児性アルコール症候群であるアルコール中毒および神経学的損傷を生じうる。他の神経毒の例としては、カイニン酸、ドウモイ酸、およびアクロメリン酸、ある種の農薬(例えば、ジクロロジフェニルトリクロロエタン(Dichloro diphenyl trichloroethane:DDT)等)、ある種の殺虫剤(例えば、有機リン酸類等)、揮発性有機溶媒(例えば、トルエン等)、金属(例えば、鉛、水銀、ヒ素、リン、およびアルミニウム等)、兵器として用いられるある種の化学物質(例えば、枯れ葉剤であるエージェントオレンジまたは神経ガス等)、および神経毒性抗腫瘍剤等が挙げられる。但し、これらに限定されるものではない。
本明細書中、特に断りのない限り、「注意および/または認知の欠如を含む障害」における、「注意および/または認知の欠如」は、同じ年齢の他の個体と比較して特定の個体において、記憶、知力、または学習および論理能力などの1種または複数の認知的機能が正常以下であることを意味する。また、「注意および/または認知の欠如」は、例えば、加齢性認知低下で起こるような1種または複数の認知的局面の任意の特定の個体における機能の低下を意味する。
本発明に従って治療することのできる「注意および/または認知の欠如を含む障害」としては、例えば、(1)認知症(例えば、加齢性認知低下、アルツハイマー病、統合失調症又はアルツハイマー病に伴う認知症、多発脳梗塞性認知症、アルコール性認知症又は他の薬物関連認知症、頭蓋内腫瘍又は脳外傷に関連する認知症、ハンチントン病又はパーキンソン病に関連する認知症、エイズ関連認知症、及び前頭側頭型認知症、等)、(2)せん妄、(3)健忘障害、(4)心的外傷後ストレス障害(PTSD)、(5)精神遅滞、(6)学習障害(例えば、読字障害、算数障害、及び書字表出障害、等)、等が挙げられる。但し、これらに限定されるものではない。
本発明に従って治療することのできる「小児精神障害」としては、例えば、(1)注意欠陥障害、(2)注意欠陥/多動性障害(ADHA)、(3)行為障害、および(4)自閉症、等が挙げられる。但し、これらに限定されるものではない。
本明細書中、特に断りのない限り、「薬物依存症」は薬物に対する異常な欲望を意味し、一般に所望の薬物を摂取しようとする衝動強迫のような動機的障害、及び強度の薬物切望のエピソードを特徴とする。例えば、麻薬、アルコール、アンフェタミン、コカイン、ニコチン、又はアヘン等の嗜癖が挙げられる。
本発明に従って治療することのできる「他の障害」としては、例えば、(1)トゥーレット症候群、(2)チック障害、及び(3)精神薄弱(ダウン症候群及び脆弱X症候群を含む。)、等が挙げられる。但し、これらに限定されるものではない。
本明細書中、特に断りのない限り、「疾患を治療する」にあるような「治療する」とは、疾患(1つ若しくは複数)の進行を、回復させる、緩和する、又は抑制することを意味する。又、本明細書中、特に断りのない限り、「治療する」は、患者の症状に応じて、疾患の発症又はその疾患に関連する任意の症状の発症を予防することを包含する、疾患の予防並びに発症前に疾患又はその任意の症状の重症度を低減することも包含する。本明細書では、特に断りのない限り、「治療する」は、任意の疾患の再発を予防又は改善することも含むものとする。
本発明は、本発明の一般式(I)で表される化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の1つ以上を含有してなるPDE2A阻害剤に関する。
本発明のPDE2A阻害剤は選択性があり、インビボだけでなくインビトロにおいても有用である。
本発明のPDE2A阻害剤は選択性があり、インビボだけでなくインビトロにおいても有用である。
[本発明の予防・治療剤の製剤化]
本発明の医薬組成物又は予防剤若しくは治療剤は、医薬製剤として経口又は非経口で投与される。
本発明の医薬製剤は、有効成分として本発明の一般式(I)で表される化合物の少なくとも一つ以上を含んでおり、さらに製薬上許容される担体と組み合わせて製造することができる。より詳細には、賦形剤(例;乳糖、白糖、マンニット、結晶セルロース、ケイ酸、トウモロコシデンプン、バレイショデンプン)、結合剤(例;セルロース類(ヒドロキシプロピルセルロース(HPC)、ヒドロキシプロピルメチルセルロース(HPMC))、結晶セルロース、糖類(乳糖、マンニット、白糖、ソルビトール、エリスリトール、キシリトール、)、デンプン類(トウモロコシデンプン、バレイショデンプン)、α化デンプン、デキストリン、ポリビニルピロリドン(PVP)、マクロゴール、ポリビニルアルコール(PVA))、滑沢剤(例;ステアリン酸マグネシウム、ステアリン酸カルシウム、タルク、カルボキシメチルセルロース)、崩壊剤(例;デンプン類(トウモロコシデンプン、バレイショデンプン)、カルボキシメチルスターチナトリウム、カルメロース、カルメロースカルシウム、クロスカルメロースナトリウム、クロスポピドン)、被膜剤(例;セルロース類(ヒドロキシプロピルセルロース(HPC)、ヒドロキシプロピルメチルセルロース(HPMC)、アミノアルキルメタクリレートコポリマーE、メタクリル酸コポリマーLD)、可塑剤(例;クエン酸トリエチル、マクロゴール)、隠蔽剤(例;酸化チタン)、着色剤、香味剤、防腐剤(例;塩化ベンザルコニウム、パラオキシ安息香酸エステル)、等張化剤(例;グリセリン、塩化ナトリウム、塩化カルシウム、マンニトール、ブドウ糖)、pH調節剤(例;水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、塩酸、硫酸、リン酸緩衝液などの緩衝液)、安定化剤(例;糖、糖アルコール、キサンタンガム)、分散剤、酸化防止剤(例;アスコルビン酸、ブチルヒドロキシアニソール(BHA)、没食子酸プロピル、dl−α−トコフェロール)、緩衝剤、保存剤(例;パラベン、ベンジルアルコール、塩化ベンザルコニウム)、芳香剤(例;バニリン、l−メントール、ローズ油)、溶解補助剤(例;ポリオキシエチレン硬化ヒマシ油、ポリソルベート80、ポリエチレングリコール、リン脂質コレステロール、トリエタノールアミン)、吸収促進剤(例;グリコール酸ナトリウム、エデト酸ナトリウム、カプリン酸ナトリウム、アシルカルニチン類、リモネン)、ゲル化剤、懸濁化剤、又は乳化剤などを適宜選択して使用して、一般的に用いられる適当なこれらの添加剤と、本発明の化合物と適宜組み合わせて、必要に応じて適当な溶媒を用いることにより、種々の剤形とすることが出来る。
本発明の医薬組成物又は予防剤若しくは治療剤は、医薬製剤として経口又は非経口で投与される。
本発明の医薬製剤は、有効成分として本発明の一般式(I)で表される化合物の少なくとも一つ以上を含んでおり、さらに製薬上許容される担体と組み合わせて製造することができる。より詳細には、賦形剤(例;乳糖、白糖、マンニット、結晶セルロース、ケイ酸、トウモロコシデンプン、バレイショデンプン)、結合剤(例;セルロース類(ヒドロキシプロピルセルロース(HPC)、ヒドロキシプロピルメチルセルロース(HPMC))、結晶セルロース、糖類(乳糖、マンニット、白糖、ソルビトール、エリスリトール、キシリトール、)、デンプン類(トウモロコシデンプン、バレイショデンプン)、α化デンプン、デキストリン、ポリビニルピロリドン(PVP)、マクロゴール、ポリビニルアルコール(PVA))、滑沢剤(例;ステアリン酸マグネシウム、ステアリン酸カルシウム、タルク、カルボキシメチルセルロース)、崩壊剤(例;デンプン類(トウモロコシデンプン、バレイショデンプン)、カルボキシメチルスターチナトリウム、カルメロース、カルメロースカルシウム、クロスカルメロースナトリウム、クロスポピドン)、被膜剤(例;セルロース類(ヒドロキシプロピルセルロース(HPC)、ヒドロキシプロピルメチルセルロース(HPMC)、アミノアルキルメタクリレートコポリマーE、メタクリル酸コポリマーLD)、可塑剤(例;クエン酸トリエチル、マクロゴール)、隠蔽剤(例;酸化チタン)、着色剤、香味剤、防腐剤(例;塩化ベンザルコニウム、パラオキシ安息香酸エステル)、等張化剤(例;グリセリン、塩化ナトリウム、塩化カルシウム、マンニトール、ブドウ糖)、pH調節剤(例;水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、塩酸、硫酸、リン酸緩衝液などの緩衝液)、安定化剤(例;糖、糖アルコール、キサンタンガム)、分散剤、酸化防止剤(例;アスコルビン酸、ブチルヒドロキシアニソール(BHA)、没食子酸プロピル、dl−α−トコフェロール)、緩衝剤、保存剤(例;パラベン、ベンジルアルコール、塩化ベンザルコニウム)、芳香剤(例;バニリン、l−メントール、ローズ油)、溶解補助剤(例;ポリオキシエチレン硬化ヒマシ油、ポリソルベート80、ポリエチレングリコール、リン脂質コレステロール、トリエタノールアミン)、吸収促進剤(例;グリコール酸ナトリウム、エデト酸ナトリウム、カプリン酸ナトリウム、アシルカルニチン類、リモネン)、ゲル化剤、懸濁化剤、又は乳化剤などを適宜選択して使用して、一般的に用いられる適当なこれらの添加剤と、本発明の化合物と適宜組み合わせて、必要に応じて適当な溶媒を用いることにより、種々の剤形とすることが出来る。
本発明の医薬製剤の剤形としては、例えば、錠剤、カプセル剤、顆粒剤、散剤、丸剤、エアゾール剤、吸入剤、軟膏剤、貼付剤、坐剤、注射剤、トローチ剤、液剤、酒精剤、懸濁剤、エキス剤、エリキシル剤等があげられる。また、経口、皮下投与、筋肉内投与、鼻腔内投与、経皮投与、静脈内投与、動脈内投与、神経周囲投与、硬膜外投与、硬膜下腔内投与、脳室内投与、直腸内投与、吸入等により患者に投与し得る。
本発明の医薬製剤は、通常のカテーテル技法または注入(infusion)を用いることを含む、注射による非経口投与用に製剤化することができる。注射用製剤は、保存剤を添加して、例えばアンプルまたは多回投与容器で、単位投与形態として提供することができる。これらの製剤は、油性又は水性ビヒクル中の懸濁剤、液剤、またはエマルションなどの形態をとることができ、懸濁化剤、安定化剤、及び/又は分散剤などの製剤化剤を含有することができる。あるいは活性成分は、使用前に、適切なビヒクル、たとえば滅菌発熱物質除去水で再構成するための粉末形態であることもできる。
製品溶液が必要とされる場合、製品溶液は患者への経口または非経口投与に必要とされる強度の溶液を生じるのに充分な量で、水(または他の水性媒質)に単離包接複合体を溶解することによって製造できる。これらの化合物は、口腔内で活性成分が放出されるように設計されている、迅速分散投与形態(fddf)に製剤化することができる。これらの製剤は多くの場合、急速溶解性ゼラチンをベースとしたマトリクスを用いて製剤化されている。これらの投与形態はよく知られており、広範な薬物を送達するために用いることができる。ほとんどの迅速分散投与形態は、担体または構造形成剤としてゼラチンを利用する。典型的に、ゼラチンは、包装から取り出すときに破損を防ぐ充分な強度を投与形態に付与するために用いられるが、ひとたび口に入れると、ゼラチンはその投与形態が即時分解することを可能にする。あるいは、同じ効果を得るために、種々のデンプンが用いられる。
本発明の化合物はまた、たとえば通常の坐剤基剤、たとえばカカオバターまたは他のグリセリドなどを含有する、坐剤または停留浣腸などの直腸組成物に製剤化することもできる。
鼻腔内投与または吸入による投与の場合、本発明の化合物は、患者によって圧搾されるか、もしくはポンプで送り出されるポンプスプレー容器から溶液または懸濁液の形態で、または適切な噴射剤、たとえば、ジクロロジフルオロメタン、トリクロロフルオロメタン、ジクロロテトラフルオロエタン、二酸化炭素、もしくは他の適切なガスを用いて、加圧式容器もしくはネブライザからエアロゾルスプレー形(aerosol spray presentation)として、好都合に送達される。加圧式エアロゾルの場合、投与単位は、計量された量を送達する弁を提供することによって決定することができる。加圧式容器またはネブライザは、活性化合物の溶液または懸濁液を含有することができる。吸入器または注入器で用いるカプセル剤およびカートリッジ剤(たとえば、ゼラチンから製造される)は、本発明の化合物とラクトースまたはデンプンなどの適切な粉末基剤との混合粉末を含有させて製剤化することができる。
平均的成人において上述の状態を治療するためのエアロゾル製剤は、好ましくはエアロゾルの各計量用量または「1吹き(puff)」が本発明の化合物約20mgから約1000mgを含有するように設定される。エアロゾルによる総日用量は、約100mgから約10mgの範囲内となる。投与は1日数回、たとえば2、3、4、または8回、たとえば各回1、2、または3用量の投与であることができる。
本発明の医薬組成物中の本発明の化合物の含量は、剤形、本発明の化合物の投与量等により異なるが、例えば、組成物全量に対して、約0.01−100重量%、好ましくは0.1−95重量%である。
本発明の化合物の投与量は、投与対象、投与ルート(経口、非経口、直腸、または口腔等)、対象疾患、症状等によっても異なるが、例えば、統合失調症の患者(成人、体重約60kg)に経口投与する場合、通常1回量として約0.1〜約20mg/kg体重、好ましくは約0.2〜10mg/kg体重、さらに好ましくは約0.5〜約10mg/kg体重であり、この量を1日1回〜数回(例えば3回)投与するのが望ましい。
[本発明の化合物を含有する併用剤]
本発明の化合物や本発明の医薬組成物は、医療現場で行われている一般的な方法で、他の予防及び/又は治療薬(他の薬物又は薬剤)と併用することも可能である。本発明の化合物と併用しうる他の予防及び/又は治療薬(薬剤)としては、例えば、(A)精神疾患、特に統合失調症、もしくは双極性障害、強迫性障害、大うつ病、パーキンソン病、ハンチントン病、アルツハイマー病、認知機能障害や記憶障害の治療薬、(B)統合失調症と併発し易い疾患の治療薬等が挙げられる。
本発明の化合物や本発明の医薬組成物は、医療現場で行われている一般的な方法で、他の予防及び/又は治療薬(他の薬物又は薬剤)と併用することも可能である。本発明の化合物と併用しうる他の予防及び/又は治療薬(薬剤)としては、例えば、(A)精神疾患、特に統合失調症、もしくは双極性障害、強迫性障害、大うつ病、パーキンソン病、ハンチントン病、アルツハイマー病、認知機能障害や記憶障害の治療薬、(B)統合失調症と併発し易い疾患の治療薬等が挙げられる。
前記(A)の薬剤としては、例えば、(1)非定型抗精神病薬[具体的には、オランザピン、クエチアピン、クロザピン、ジプラシドン、リスペリドン、パリペリドン、ペロスピロン、ブロナンセリン、ルラシドン、アリピプラゾール、セルチンドール、アミスルプリド、イロペリドン、ビフェプルノックス、アセナピン、メルペロン、ブレクスピプラゾール、ゾテピン等]、(2)定型抗精神病薬[具体的には、クロルプロマジン、プクロルペラジン、ペルフェナジン、レボメプロマジン、フルフェナジン、チオリダジン、プロペリシアジン、スピペロン、モペロン、ハロペリドール、チミペロン、ブロムペリドール、ピモジド、フロロピパミド、スルピリド、チアプリド、スルトプリド、ネモナプリド、オキシペルチン等]、(3)選択的セロトニン再取り込み阻害薬(SSRI)[具体的には、エスシタロプラム、シタロプラム、パロキセチン、セルトラリン、フルボキサミン、フルオキセチン等]、(4)選択的セロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)[具体的には、ミルナシプラン、デュロキセチン、ベンラファキシン、ネファゾドン等]、(5)選択的ノルアドレナリン・ドーパミン再取り込み阻害薬(NDRI)[具体的には、ブプロピオン等]、(6)ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA)[具体的には、ミルタザピン等]、(7)セロトニン・ノルアドレナリン・ドパミン三重モノアミン再取り込み阻害剤、(8)双極性障害治療薬[具体的には、リチウム、バルプロ酸等]、(9)てんかん治療薬[具体的には、フェニトイン、フェノバルビタール、カルバマゼピン、バルプロ酸、エトスクシミド、ガバペンチン、ソルフェトン、フェルバトール等]、(10)多発性硬化症治療薬[具体的には、トルテロジン、オキシブチニン、オキシコドン、インターフェロンβ−1b、インターフェロンβ−1a、アザチオプリン、メトトレキサート、ガラティラメル等]、(11)ハンチントン病治療薬[具体的には、テトラベナジン等]、(12)トリアゾロピリジン系抗うつ薬(SARI)[具体的には、トラゾドン等]、(13)四環系抗うつ薬[具体的には、セチプチリン、ミアンセリン、マプロチリン等]、(14)三環系抗うつ薬[具体的には、アミトリプチリン、トリミプラミン、イミプラミン、デシプラミン、ノルトリプチリン、クロミプラミン、ロフェプラミン、アモキサピン、ドスレピン等]、(15)その他抗うつ薬[具体的には、NS−2359、Lu AA21004、DOV21947等]、(16)α7ニコチン受容体作動薬、(17)α7ニコチン受容体活性調節薬、(18)α7ニコチン受容体部分調節薬[具体的には、SSR−180711、PNU−120596等]、(19)PDE阻害薬[PDE1阻害薬、PDE4阻害薬、PDE5阻害薬、PDE7阻害薬、PDE9阻害薬、PDE10阻害薬等]、(20)NK2拮抗薬、(21)NK3拮抗薬、(22)ムスカリン型M1アセチルコリン受容体活性調節薬、(23)ムスカリン型M2アセチルコリン受容体活性調節薬、(24)アデノシン受容体調節薬、(25)ムスカリン型M4アセチルコリン受容体活性調節薬、(26)ムスカリン型M5アセチルコリン受容体活性調節薬、(27)アデノシン受容体調節薬、(28)グリシントランスポーター1(GlyT1)阻害薬[具体的には、ALX5407、SSR504734等]、(29)グルタミン酸増強薬[具体的には、アンパカイン]、(30)NMDA受容体阻害薬[具体的には、塩酸メマンチン等]、(31)代謝性グルタミン酸受容体調節薬(mGlu)[具体的には、CDPPB、MPEP等]、(32)抗不安薬((i)ベンゾジアゼピン系抗不安薬[具体的には、クロルジアゼポキシド、ジアゼパム、オキサゾラム、メダゼパム、クロキサゾラム、ロラゼパム、クロラゼプ酸二カリウム、プラゼパム、ブロマゼパム、フルジアゼパム、メキサゾラム、アルプラゾラム、フルトプラゼパム、フルタゾラム、ロフラゼプ酸エチル等]、(ii)チエノジアゼピン系抗不安薬[具体的には、エチゾラム、クロチアゼパム等]、(iii)セロトニン5−HT1A作動薬[具体的には、タンドスピロン等])、(33)睡眠導入剤((i)ベンゾジアゼピン系睡眠導入剤[具体的には、ニトラゼパム、エスタゾラム、塩酸フルラゼパム、ニメタゼパム、フルラゼパム、ハロキサゾラム、フルニトラゼパム、塩酸リルマザポン、ロルメタゼパム、トリアゾラム等]、(ii)チエノジアゼピン系眠導入剤[具体的には、ブロチゾラム等]、(iii)非ベンゾジアゼピン系睡眠導入剤[具体的には、ゾルピデム等]、(iv)メラトニン受容体作動薬[具体的には、ラメルテオン等])、(v)シクロピロロン系眠導入剤[具体的には、ゾピクロン等]、(34)βアミロイドワクチン、(35)βアミロイド分解酵素等、(36)脳機能賦活薬[具体的には、アニラセタム、ニセルゴリン等]、(37)カンナビノイド調節薬、(38)コリンエステラーゼ阻害薬[具体的には、塩酸ドネペジル、リバスチグミン、臭化水素酸ガランタミン、タクリン、等]、(39)MAO−B阻害剤[具体的には、ラサリジン、セレギリン等]、(40)パーキンソン病治療薬((i)ドーパミン受容体作動薬[具体的には、レボドパ、塩酸アマンタジン、メシル酸ブロモクリプチン、メシル酸ペルゴリド、カベルゴリン、塩酸タリペキソール、塩酸プラミペキソール水和物、塩酸セレギリン、塩酸ロピニロール等]、(ii)モノアミン酸化酵素阻害薬[具体的には、デプレニル、セルジリン(セレギリン)、レマセミド,リルゾール等]、(iii)抗コリン剤[具体的には、トリヘキシフェニジル、プロフェナミン、ビペリデン、プロシクリジン、ベンズトロピン、塩酸ピロヘプチン、塩酸メチキセン、塩酸マザチコール等]、(iv)COMT阻害剤[具体的には、トルカポン、エンタカポン等]、(v)筋萎縮性側索硬化症治療薬[具体的には、リルゾール等、神経栄養因子等]、(vi)アポトーシス阻害薬[具体的には、CPI−1189、IDN−6556、CEP−1347等]、(vii)神経分化・再生促進剤[具体的には、レテプリニム(Leteprinim]、キサリプローデン(Xaliproden;SR−57746−A]、SB−216763等])等が挙げられる。
また、前記(B)の薬剤としては、例えば、(41)糖尿病治療薬((i)PPARγ作用薬(作動薬、阻害薬)[具体的には、ピオグリタゾン、ロシグリタゾン、トログリタゾン、シグリタゾン、ダルグリタゾン、エングリタゾン、ネトグリタゾン等]、(ii)インスリン分泌促進薬[(a)スルホニル尿素剤(具体的には、トルブタミド、アセトヘキサミド、クロルプロパミド、グリベンクラミド、グリクラジド、グリピジド、グリメピリド、グリペンチド、グリキドン、グリソラミド、トラザミド等)、(b)非スルホニル尿素剤等]、(iii)速効型インスリン分泌促進剤(具体的には、ナテグリニド、ミチグリニド、レパグリニド等)、(iv)αグルコシダーゼ阻害薬[具体的には、アカルボース、ボグリボース、ミグリトール、カミグリボース、アジポシン、エミグリテート、プラジミシン−Q、サルボスタチン等]、(v)インスリン抵抗性改善薬[具体的には、(a)PPARγ作用薬、(b)PTP−1B阻害薬、(c)DPP−4阻害薬[具体的には、シタグリプチン、ビルダグリプチン、アログリプチン、サクサグリプチン、NVP−DPP−728等]、(d)GLP−1及びGLP−1作動薬[具体的には、エキセナチド、リラグルチド等]、(e)11β−HSD阻害薬等、(f)GPR40作動薬、(g)GPR119作動薬、(h)GPR120作動薬]、(vi)肝糖新生抑制剤[具体的には、グルカゴン拮抗薬等]、(vii)ビグアナイド剤[具体的には、メトホルミン、ブホルミン、フェンホルミン等]、(viii)インスリンまたはインスリン誘導体[具体的には、インスリン亜鉛懸濁液、インスリンリスプロ、インスリンアスパルト、レギュラーインスリン、NPHインスリン、インスリングラルギン、インスリンデテミル、混合型インスリン等]、(ix)α2拮抗薬[具体的には、ミダグリゾール、イサグリドール、デリグリドール、イダゾキサン、エファロキサン等])、(42)抗肥満薬((i)アドレナリンβ3受容体作動薬[具体的には、KRP−204、TRK−380/TAC−301等]、(ii)CB−1受容体拮抗薬[具体的には、リモナバン、SR−147778、BAY−65−2520等]、(iii)ニューロペプチドY(NPY)受容体拮抗薬[具体的には、S−2367等]、(iv)摂食抑制薬[モノアミン再取り込み阻害剤[具体的には、シブトラミン、マジンドール等]]、(v)リパーゼ阻害薬[具体的には、オルリスタット、セチリスタット等]、(vi)ペプチドYY(PYY)受容体拮抗薬、(vii)毛様体神経栄養因子および誘導体[具体的には、アキソキン]等)、(43)コレステロール低下薬等の高脂血症治療薬((i)ω3脂肪酸類[具体的には、イコサペント酸エチル(EPA−E製剤、例えば、製品名:エパデール(登録商標)等)、ドコサヘキサエン酸(DHA)、イコサペント酸エチルおよびドコサヘキサエン酸エチルの混合製剤(例えば、製品名:ロバザTM、オマコール(登録商標)等)等]、(ii)HMG−CoA還元酵素阻害剤[具体的には、アトルバスタチン、シンバスタチン、ピタバスタチン、イタバスタチン、フルバスタチン、ロバスタチン、プラバスタチン、リバスタチン、ロスバスタチン等](iii)HMG−CoA合成酵素阻害剤、(iv)コレステロール吸収阻害剤[具体的には、エゼチミブ]、(v)アシル−CoA・コレステロールアシル転移酵素(ACAT)阻害剤、(vi)CETP阻害剤、(vii)スクアレン合成酵素阻害剤、(viii)抗酸化剤[具体的には、プロブコール等]、(ix)PPARα作動薬[具体的には、クロフィブラート、エトフィブラート、フェノフィブラート、ベザフィブラート、シプロフィブラート、ゲムフィブロジル、KRP−101等]、(x)PPARδ作動薬、(xi)LXR作動薬、(xii)FXR作動薬[具体的には、INT−747等]、(xiii)MTTP阻害剤、(xiv)スクアレンエポシダーゼ阻害剤等)、(44)降圧剤((i)利尿剤[具体的には、トリクロルメチアジド、ヒドロクロロチアジド、メフルシド、インダパミド、メチクラン、クロルタリドン、トリパミド、フロセミド、トラセミド、ブメタニド、エタクリン酸、スピロノラクトン、トリアムテレン、エプレレノン等]、(ii)カルシウム受容体拮抗薬[具体的には、アムロジピン、フェロジピン、ニカルジピン、ニフェジピン、ニモジピン、ニトレンジピン、ニルバジピン、アラニジピン、アゼルニジピン、マニジピン、バルニジピン、エホニジピン、シルニジピン、ベニジピン、ジルチアゼム等]、(iii)アンジオテンシン変換酵素阻害薬(ACEI)[具体的には、カプトプリル、リシノプリル、エナラプリル、デラプリル、ペリンドプリル、ベナゼプリル、トランドラプリル、キナプリル、アラセプリル、イミダプリル、テモカプリル、シラザプリル等]、(iv)アンジオテンシン受容体拮抗薬(ARB)[具体的には、ロサルタン、オルメサルタン、テルミサルタン、バルサルタン、カンデサルタンシレキセチル、イルベサルタン等]、(v)直接的レニン阻害薬[具体的には、アリスキレン等]、(vi)α受容体遮断薬[具体的には、トラゾリン、フェントラミン、ドキサゾシン、プラゾシン、ブナゾシン、テラゾシン、ウラピジル等]、(vii)β受容体遮断薬[具体的には、ボピンドロール、ピンドロール、チモロール、ジクロロイソプレナリン、アルプレノロール、カルテオロール、インデノロール、ブニトロロール、ペンブトロール、プロプラノロール、ナドロール、ニプラジロール、チリソロール、アセブトロール、セリプロロール、メトプロロール、アテノロール、ビソプロロール、ベタキソロール、プラクトロール、ベバントロール、ブトキサミン、カルベジロール、アモスラロール、アロチノロール、ラベタロール等]、(viii)α1β遮断薬[具体的には、カルベジロール、ラベタロール、アロチノロール、ベバントロール等]、(ix)α2受容体刺激薬[具体的には、クロニジン、メチルドパ、グアンファシン等])、(45)非ステロイド性抗炎症薬[具体的には、メロキシカム、テオキシカム、インドメタシン、イブプロフェン、セレコキシブ、ロフェコキシブ、アスピリン、インドメタシン等]、(46)疾患修飾性抗リウマチ薬(DMARDs)、(47)抗サイトカイン薬[具体的には、TNF阻害薬、MAPキナーゼ阻害薬]、(48)ステロイド薬[具体的には、デキサメサゾン、ヘキセストロール、酢酸コルチゾン等]、(49)性ホルモンまたはその誘導体[具体的には、プロゲステロン、エストラジオール、安息香酸エストラジオール等]、(50)副甲状腺ホルモン(PTH)等が挙げられる。
前記してきた疾患に対して、本発明の医薬と既存薬剤とを併用することにより、既存薬剤の投薬量を下げることが可能であり、既存薬剤の副作用を軽減することが可能となる。もちろん、当該薬剤を用いた併用方法は、前記疾患に限定されるものではなく、且つ併用される薬剤は前記に例示した化合物に限定されない。
本発明の医薬製剤と併用薬剤の投与形態は、特に限定されず、投与に際して、本発明の医薬製剤と併用薬剤とが組み合わされていればよい。このような投与形態としては、例えば、
(1)本発明の医薬製剤の有効成分と併用薬剤の有効成分とを同時に製剤化して得られる単一の製剤としての投与、
(2)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の同一投与経路での同時投与、
(3)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の同一投与経路での時間差をおいての投与、
(4)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の異なる投与経路での同時投与、
(5)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の異なる投与経路での時間差をおいての投与(例えば、本発明の医薬製剤-併用薬剤の順序での投与、あるいはその逆の順序での投与)などが用いられる。
また、本発明の医薬製剤と併用薬剤とを別々に製剤化して、これらを組合せて投与するためのキットとすることもできる。
本明細書では、これらの投与形態又はキットされた形態をまとめて、本発明の併用剤という。
(1)本発明の医薬製剤の有効成分と併用薬剤の有効成分とを同時に製剤化して得られる単一の製剤としての投与、
(2)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の同一投与経路での同時投与、
(3)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の同一投与経路での時間差をおいての投与、
(4)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の異なる投与経路での同時投与、
(5)本発明の医薬製剤と併用薬剤とを別々に製剤化して得られる2種の製剤の異なる投与経路での時間差をおいての投与(例えば、本発明の医薬製剤-併用薬剤の順序での投与、あるいはその逆の順序での投与)などが用いられる。
また、本発明の医薬製剤と併用薬剤とを別々に製剤化して、これらを組合せて投与するためのキットとすることもできる。
本明細書では、これらの投与形態又はキットされた形態をまとめて、本発明の併用剤という。
本発明の併用剤を投与するに際しては、前記したいずれの投与形態を採用することもできる。例えば、本発明の併用剤と本発明の医薬製剤とを同時期に投与してもよいが、併用剤の投与の後、本発明の医薬製剤を投与してもよいし、本発明の医薬製剤の投与後、併用剤を投与してもよい。時間差をおいて投与する場合、時間差は投与する有効成分、剤形、及び投与方法により異なるが、例えば、本発明の併用剤を先に投与する場合、併用剤を投与した後1分〜3日以内、好ましくは10分〜1日以内、より好ましくは15分〜1時間以内に本発明の医薬製剤を投与する方法が挙げられる。本発明の医薬製剤を先に投与する場合、本発明の化合物を投与した後、1分〜1日以内、好ましくは10分〜6時間以内、より好ましくは15分〜1時間以内に本発明の併用剤を投与する方法が挙げられる。
本発明の併用剤は、副作用が問題とならなければ、どのような量を設定することも可能である。本発明の併用剤の有効成分としての一日投与量は、投与対象、投与ルート、対象疾患、症状等によっても異なるが、例えば、統合失調症の患者(成人、体重約60kg)に経口投与する場合、通常1回量として約0.1〜約20mg/kg体重、好ましくは約0.2〜10mg/kg体重、さらに好ましくは約0.5〜約10mg/kg体重であり、この量を1日1回〜数回(例えば3回)投与するのが望ましい。
本発明の化合物が本発明の併用剤と組み合せて使用される場合には、お互いの剤の量は、それらの剤の反対効果を考えて安全な範囲内で低減できる。
本発明の化合物が本発明の併用剤と組み合せて使用される場合には、お互いの剤の量は、それらの剤の反対効果を考えて安全な範囲内で低減できる。
本発明の併用剤は、毒性が低く、例えば、本発明の化合物、又は(及び)上記併用薬物を公知の方法に従って、薬理学的に許容される担体と混合して医薬製剤、例えば、錠剤(糖衣錠、フイルムコーティング錠を含む。)、散剤、顆粒剤、カプセル剤、(ソフトカプセルを含む。)、液剤、注射剤、坐剤、徐放剤などとすることができ、それらは、経口的、又は非経口的に安全に投与することができる。
本発明の併用剤の製造に用いられてもよい薬理学的に許容される担体としては、上記した本発明の医薬組成物に使用されるものと同様のものを使用することができる。
本発明の併用剤の製造に用いられてもよい薬理学的に許容される担体としては、上記した本発明の医薬組成物に使用されるものと同様のものを使用することができる。
本発明の併用剤における本発明の化合物と併用薬物との配合比は、投与対象、投与ルート、疾患などにより適宜選択することができる。上記併用薬物は、2種以上を適宜の割合で組み合せて用いてもよい。
併用薬物の投与量は、臨床上用いられている用量を基準として適宜選択することができる。また、本発明の化合物と併用薬物の配合比は、投与対象、投与ルート、対象疾患、症状、組み合わせ等により適宜選択することができる。例えば、投与対象がヒトである場合、本発明の化合物1重量部に対し、併用薬物を0.01〜100重量部用いればよい。例えば、本発明の併用剤における本発明の化合物の含有量は、製剤の形態によって相違するが、通常製剤全体に対して約0.01〜99.9重量%の範囲であり、好ましくは約0.1〜50重量%の範囲であり、さらに好ましくは約0.5〜20重量%程度の範囲である。
本発明の併用剤における併用薬物の含有量は、製剤の形態によって相違するが、通常製剤全体に対して約0.01〜99.9重量%の範囲であり、好ましくは約0.1〜50重量%の範囲であり、さらに好ましくは約0.5〜20重量%の範囲である。
本発明の併用剤における担体などの添加剤の含有量は、製剤の形態によって相違するが、通常製剤全体に対して約1〜99.99重量%の範囲であり、好ましくは約10〜90重量%の範囲である。
本発明の化合物、及び併用薬物をそれぞれ別々に製剤化する場合も同様の含有量でよい。
上記したように投与量は種々の条件で変動するので、上記投与量より少ない量で十分な場合もあり、また範囲を超えて投与する必要がある場合もある
本発明の併用剤における担体などの添加剤の含有量は、製剤の形態によって相違するが、通常製剤全体に対して約1〜99.99重量%の範囲であり、好ましくは約10〜90重量%の範囲である。
本発明の化合物、及び併用薬物をそれぞれ別々に製剤化する場合も同様の含有量でよい。
上記したように投与量は種々の条件で変動するので、上記投与量より少ない量で十分な場合もあり、また範囲を超えて投与する必要がある場合もある
本発明の化合物は、単回または多回投与のいずれかで、単独でまたは薬学的に許容できる担体と組み合わせて投与することができる。適切な医薬担体には、不活性固体希釈剤または充填剤、滅菌水溶液、および種々の有機溶媒が包含される。それにより形成される医薬組成物は次いで、錠剤、粉剤、ロゼンジ、液体調剤、シロップ剤、注射液などの様々な投与形態で容易に投与することができる。これらの医薬組成物は、香味剤、結合剤、賦形剤などの追加成分を場合により含有できる。したがって、本発明の化合物は、経口、口腔、鼻腔、非経口(たとえば、静脈内、筋内、または皮下)、経皮(たとえば、パッチ)、もしくは直腸投与用に、または吸入もしくは注入(insufflation)による投与に適した形態で製剤化することができる。
[薬理実験例]
以下に実験例を挙げて、本発明を具体的に説明するが、本発明はこれらによって何ら限定されるものではない。以下の薬理実施例1ないし10は、本発明の化合物の有効性を試験する方法を提供する。
以下に実験例を挙げて、本発明を具体的に説明するが、本発明はこれらによって何ら限定されるものではない。以下の薬理実施例1ないし10は、本発明の化合物の有効性を試験する方法を提供する。
(薬理実験例1):in vitroでの化合物評価(酵素阻害活性評価:ヒトPDE2A阻害作用)
IMAP TR−FRET Phosphodiersterase Evaluation Assay Kit(モレキュラーデバイス)を用いて測定した。384ウェルプレート(Corning)に希釈した各濃度の被検化合物10μL、及び1×IMAP Reaction Buffer containing 0.1%BSA(kit添付の5×より作成、10mM Tris−HCl、pH=7.2、10mM MgCl2、0.05%NaN3、及び0.1% BSA)で400ng/mLに希釈したPDE2A酵素(BPSバイオサイエンス)5μLを加え、5分間室温にてプレインキュベーションした。1×IMAP Reaction Buffer containing 0.1%BSAで400nMに希釈したキット添付のcGMP基質の5μLを加えて60分間室温にて反応させた。さらにキット添付のIMAP TR−FRET Binding solution 60μLを添加して4時間以上放置したのち、EnVision2100(PerkinElmer)にて励起波長340nmでTerbiumの蛍光強度(Emission=490nm)及びTR−FRET(Emission=520nm)を測定することによって、産生された5’−GMPの量を算出した。被検化合物の代わりに溶媒を添加したウェルのカウントを0%、PDE2A酵素を加えていないウェルのカウントを100%として各被検化合物の阻害活性を算出した。
IMAP TR−FRET Phosphodiersterase Evaluation Assay Kit(モレキュラーデバイス)を用いて測定した。384ウェルプレート(Corning)に希釈した各濃度の被検化合物10μL、及び1×IMAP Reaction Buffer containing 0.1%BSA(kit添付の5×より作成、10mM Tris−HCl、pH=7.2、10mM MgCl2、0.05%NaN3、及び0.1% BSA)で400ng/mLに希釈したPDE2A酵素(BPSバイオサイエンス)5μLを加え、5分間室温にてプレインキュベーションした。1×IMAP Reaction Buffer containing 0.1%BSAで400nMに希釈したキット添付のcGMP基質の5μLを加えて60分間室温にて反応させた。さらにキット添付のIMAP TR−FRET Binding solution 60μLを添加して4時間以上放置したのち、EnVision2100(PerkinElmer)にて励起波長340nmでTerbiumの蛍光強度(Emission=490nm)及びTR−FRET(Emission=520nm)を測定することによって、産生された5’−GMPの量を算出した。被検化合物の代わりに溶媒を添加したウェルのカウントを0%、PDE2A酵素を加えていないウェルのカウントを100%として各被検化合物の阻害活性を算出した。
被検化合物のPDE2A阻害活性はIC50値で表し、IC50値が100〜1000nmol/Lの本発明の化合物を「+」として、IC50値が100nmol/L未満の化合物を「++」として、次の表1に示した。
この結果、本発明の化合物は極めて良好なPDE2A阻害活性を示すことが確認された。
次に示す薬理実験例2(被験化合物をラットに経口投与することによる新奇物体認識機能に関する実験)により、精神障害及び神経変性障害治療薬としての有効性をインビボ試験として示される。
次に示す薬理実験例2(被験化合物をラットに経口投与することによる新奇物体認識機能に関する実験)により、精神障害及び神経変性障害治療薬としての有効性をインビボ試験として示される。
(薬理実験例2):ラット新奇物体認識試験
(動物)
雄性Sprague−Dawleyラットを購入し、飼育施設に到着後、動物を少なくとも一週間の馴化期間をおいて実験に使用する。動物は、温度と湿度をコントロールした実験室で、12時間明暗サイクル下で飼育し、食餌と水を自由摂取させる。
(動物)
雄性Sprague−Dawleyラットを購入し、飼育施設に到着後、動物を少なくとも一週間の馴化期間をおいて実験に使用する。動物は、温度と湿度をコントロールした実験室で、12時間明暗サイクル下で飼育し、食餌と水を自由摂取させる。
(薬物投与)
被験化合物は、0.5w/v%メチルセルロース400溶液 (和光純薬工業株式会社、日本)に懸濁し、経口投与(p.o.)する。ラットに対して被験化合物は5mL/kg体重の容量で投与する。
被験化合物は、0.5w/v%メチルセルロース400溶液 (和光純薬工業株式会社、日本)に懸濁し、経口投与(p.o.)する。ラットに対して被験化合物は5mL/kg体重の容量で投与する。
(ラット新奇物体認識試験における作用)
ラットにおける被験化合物の新奇物体認識機能に対する亢進作用について試験を行う。試験開始前日、雄性Sprague−Dawleyラットを、飼育ケージ内で測定を実施する部屋に1時間以上馴化させる。馴化後、ラットを試験装置(幅60cmx奥行き60cmx高さ35cmの蓋なしの灰色のポリ塩化ビニル製の箱)に対して10分間馴化させる。翌日、ラットを同様に飼育ケージ内で測定を実施する部屋に1時間以上馴化させる。馴化後、動物に溶媒又は被験化合物のいずれかを経口投与し、すぐに飼育ケージに戻す。被験化合物の投与一定時間後に、再び動物を飼育ケージより取り出し、獲得試行として試験装置に同じ形をした物体を2つ置き、3分間それぞれの物体に対する探索時間を計測する。獲得試行の48時間後、測定装置内に獲得試行時と同じ物体と異なる形の新しい物体を1つずつ置き、保持試行を実施する。それぞれの物体に対する探索時間を3分間計測し、各物体に対する探索時間の合計に対して、新しく変えた物体に対する探索時間の割合を認識指標(Recognition Index)として算出する。溶媒のみを投与した群(溶媒群)と被験化合物を投与した群における認識指標を比較することで、ラット新奇物体認識機能に対する被験化合物の作用を評価する。認識指標(Recognition Index)は平均値と平均値の標準誤差として表す。統計解析は、溶媒群と被験化合物を投与した群の比較についてDunnett’s test (p<0.05で有意差あり)を用いて解析を行う。
ラットにおける被験化合物の新奇物体認識機能に対する亢進作用について試験を行う。試験開始前日、雄性Sprague−Dawleyラットを、飼育ケージ内で測定を実施する部屋に1時間以上馴化させる。馴化後、ラットを試験装置(幅60cmx奥行き60cmx高さ35cmの蓋なしの灰色のポリ塩化ビニル製の箱)に対して10分間馴化させる。翌日、ラットを同様に飼育ケージ内で測定を実施する部屋に1時間以上馴化させる。馴化後、動物に溶媒又は被験化合物のいずれかを経口投与し、すぐに飼育ケージに戻す。被験化合物の投与一定時間後に、再び動物を飼育ケージより取り出し、獲得試行として試験装置に同じ形をした物体を2つ置き、3分間それぞれの物体に対する探索時間を計測する。獲得試行の48時間後、測定装置内に獲得試行時と同じ物体と異なる形の新しい物体を1つずつ置き、保持試行を実施する。それぞれの物体に対する探索時間を3分間計測し、各物体に対する探索時間の合計に対して、新しく変えた物体に対する探索時間の割合を認識指標(Recognition Index)として算出する。溶媒のみを投与した群(溶媒群)と被験化合物を投与した群における認識指標を比較することで、ラット新奇物体認識機能に対する被験化合物の作用を評価する。認識指標(Recognition Index)は平均値と平均値の標準誤差として表す。統計解析は、溶媒群と被験化合物を投与した群の比較についてDunnett’s test (p<0.05で有意差あり)を用いて解析を行う。
(薬理実験例3):溶解性試験
(1)DMSO析出溶解性(Kinetic Solubility)
本発明の化合物の10mMのジメチルスルホキシド(DMSO)溶液を最終濃度100μMとなるように50mMリン酸緩衝液(pH7.4)に添加する。その溶液を室温で1.5時間、600rpmにて撹拌しながらインキュベーションした後、フィルタープレート(MultiScreenHTS−PCFフィルタープレート(MerckMillipore))でろ過し、プレートリーダー(Powerscan HT(大日本製薬))を用いて、ろ液の吸光度を最大吸収波長で測定する。同時に、試験化合物の既知濃度(1、3、10、30、100μM)を添加したDMSO溶液を検量線標準溶液として各々の標準溶液吸光度を測定し、検量線を作成する。ろ液および標準溶液の吸光度値より化合物の溶解度(μM)を算出する。
(2)結晶溶解性(Thermodynamic Solubility)
本発明の化合物を1mg/mLとなるように溶媒(例えば、水、緩衝液)に添加する。その溶液を25℃または37℃で24時間1000rpmにて撹拌しながらインキュベーションした後、フィルタープレートでろ過する。ろ液をHPLCにて分析し、最大吸収波長にてピークを検出し、ピーク面積を測定する。同様に試験化合物の既知濃度(例えば、0.01、0.03、0.1、0.3、1、3、10μg/mL)を添加した溶液(例えば、DMSO溶液、1,4−ジオキサン溶液、メタノール溶液)を検量線標準溶液として各々のピーク面積を測定し、検量線のピーク面積より化合物の溶解度(μg/mL)を算出する。
(1)DMSO析出溶解性(Kinetic Solubility)
本発明の化合物の10mMのジメチルスルホキシド(DMSO)溶液を最終濃度100μMとなるように50mMリン酸緩衝液(pH7.4)に添加する。その溶液を室温で1.5時間、600rpmにて撹拌しながらインキュベーションした後、フィルタープレート(MultiScreenHTS−PCFフィルタープレート(MerckMillipore))でろ過し、プレートリーダー(Powerscan HT(大日本製薬))を用いて、ろ液の吸光度を最大吸収波長で測定する。同時に、試験化合物の既知濃度(1、3、10、30、100μM)を添加したDMSO溶液を検量線標準溶液として各々の標準溶液吸光度を測定し、検量線を作成する。ろ液および標準溶液の吸光度値より化合物の溶解度(μM)を算出する。
(2)結晶溶解性(Thermodynamic Solubility)
本発明の化合物を1mg/mLとなるように溶媒(例えば、水、緩衝液)に添加する。その溶液を25℃または37℃で24時間1000rpmにて撹拌しながらインキュベーションした後、フィルタープレートでろ過する。ろ液をHPLCにて分析し、最大吸収波長にてピークを検出し、ピーク面積を測定する。同様に試験化合物の既知濃度(例えば、0.01、0.03、0.1、0.3、1、3、10μg/mL)を添加した溶液(例えば、DMSO溶液、1,4−ジオキサン溶液、メタノール溶液)を検量線標準溶液として各々のピーク面積を測定し、検量線のピーク面積より化合物の溶解度(μg/mL)を算出する。
(薬理実験例4):代謝安定性試験
(1)代謝安定性試験1
本発明の化合物の10mMのDMSO溶液を最終濃度1μMとなるように肝ミクロソーム溶液(ヒト、ラット、マウス、イヌまたはサル;XenoTech)、NADPH生成溶液(β−NADP、Glucose−6−Phosphate、G−6−PDH(Y)、MgCl2を含む水)に添加する。その溶液を37℃で20分間インキュベートした後、アセトニトリルで反応停止する。反応液をフィルタープレート(MultiScreenHTS−HVプレート(MerckMillipore))で遠心ろ過し、高速液体クロマトグラム/マススペクトロメトリーを用いて、ろ液中の試験化合物を測定する。同様に反応時間0分のサンプルをコントロールとして測定し、各時点における残存率(%)を算出し、100−残存率(%)より代謝率(%)を算出する。
(2)代謝安定性試験2
本発明の化合物の10mMのDMSO溶液を最終濃度1μMとなるように肝細胞懸濁液(ヒト;GIBCO、ラット、イヌ、サル;XenoTech)に添加する。その溶液を37℃で5、15、30、45、60、120分間インキュベートした後、アセトニトリルで反応停止する。反応液をフィルタープレート(MultiScreenHTS−HVプレート(MerckMillipore))で遠心ろ過し、高速液体クロマトグラム/マススペクトロメトリーを用いて、ろ液中の試験化合物を測定する。同様に反応時間0分のサンプルをコントロールとして測定し、肝細胞反応サンプルとコントロールの比より、各時点における残存率(%)を算出する。反応時間を横軸、残存率を縦軸としてプロットし、その傾きからクリアランス(μL/106cells/min)を算出する。
(1)代謝安定性試験1
本発明の化合物の10mMのDMSO溶液を最終濃度1μMとなるように肝ミクロソーム溶液(ヒト、ラット、マウス、イヌまたはサル;XenoTech)、NADPH生成溶液(β−NADP、Glucose−6−Phosphate、G−6−PDH(Y)、MgCl2を含む水)に添加する。その溶液を37℃で20分間インキュベートした後、アセトニトリルで反応停止する。反応液をフィルタープレート(MultiScreenHTS−HVプレート(MerckMillipore))で遠心ろ過し、高速液体クロマトグラム/マススペクトロメトリーを用いて、ろ液中の試験化合物を測定する。同様に反応時間0分のサンプルをコントロールとして測定し、各時点における残存率(%)を算出し、100−残存率(%)より代謝率(%)を算出する。
(2)代謝安定性試験2
本発明の化合物の10mMのDMSO溶液を最終濃度1μMとなるように肝細胞懸濁液(ヒト;GIBCO、ラット、イヌ、サル;XenoTech)に添加する。その溶液を37℃で5、15、30、45、60、120分間インキュベートした後、アセトニトリルで反応停止する。反応液をフィルタープレート(MultiScreenHTS−HVプレート(MerckMillipore))で遠心ろ過し、高速液体クロマトグラム/マススペクトロメトリーを用いて、ろ液中の試験化合物を測定する。同様に反応時間0分のサンプルをコントロールとして測定し、肝細胞反応サンプルとコントロールの比より、各時点における残存率(%)を算出する。反応時間を横軸、残存率を縦軸としてプロットし、その傾きからクリアランス(μL/106cells/min)を算出する。
(薬理実験例5):パッチクランプ法によるhERG阻害試験
hERG(human ether−a−go−go related gene)チャネルに対する作用を全自動パッチクランプシステム(QPatch HT(Sophion Bioscience))を用いて測定する。細胞(CHO hERG DUO(B’SYS))のhERG IKr電流を確認するため、膜電位を−80mVに保持し、−50mV、0.02秒間および20mV、4.8秒間の脱分極パルスに続く−50mV、5秒間の再分極パルスを15秒に1回の頻度で与える。試験化合物のhERGチャネルに対する作用は、再分極パルスによって誘導されるテール電流の変化によって確認する。測定は室温で行う。hERGチャネル阻害率は、試験化合物添加前のテール電流ピーク値に対する添加後4分のテール電流の減少率(抑制率)として算出する。
この抑制率を算出することにより、薬物によるQT延長とそれに続く致死的な副作用(心室頻拍や突然死など)を誘発する可能性が示される。
hERG(human ether−a−go−go related gene)チャネルに対する作用を全自動パッチクランプシステム(QPatch HT(Sophion Bioscience))を用いて測定する。細胞(CHO hERG DUO(B’SYS))のhERG IKr電流を確認するため、膜電位を−80mVに保持し、−50mV、0.02秒間および20mV、4.8秒間の脱分極パルスに続く−50mV、5秒間の再分極パルスを15秒に1回の頻度で与える。試験化合物のhERGチャネルに対する作用は、再分極パルスによって誘導されるテール電流の変化によって確認する。測定は室温で行う。hERGチャネル阻害率は、試験化合物添加前のテール電流ピーク値に対する添加後4分のテール電流の減少率(抑制率)として算出する。
この抑制率を算出することにより、薬物によるQT延長とそれに続く致死的な副作用(心室頻拍や突然死など)を誘発する可能性が示される。
(薬理実験例6):ファーマコキネティクス(PK)試験
(1)ラットカセットPK試験
本発明の化合物を6から10週齢の雄性Crl:CD(SD)ラットに、0.1から0.3mg/kg(投与溶媒は、DMSO:Dimethylacetamide:PEG400:生理食塩水=1.2:2.8:4:2、1mL/kg)で静脈内投与した後、0.25、0.5、1、2、4、6時間後に頸静脈より採血、あるいは1mg/kg(投与溶媒は、DMSO:Tween80:蒸留水=1:1:8、10mL/kg)で経口単回投与した後、0.5、1、2、4時間後に頚静脈より採血する。血液を遠心分離(3000rpm、15分間、4℃)して得られた血漿を用いて、高速液体クロマトグラム/マススペクトロメトリーにて、血漿中の試験化合物を測定する。同様に試験化合物の既知濃度を添加した標準溶液を測定し、作成した検量線より血漿中濃度(μg/mL)を算出し、最高血漿中濃度をCmax(μg/mL)とする。
(2)PK試験
本発明の化合物を動物(約6から8週齢の雄性Crl:CD(SD)ラット、もしくは、約1から3カ年齢の雄性ビーグル犬、もしくは、約6から7カ年齢の雄性カニクイザル)に1mg/kg(投与溶媒は、Dimethylacetamide:PEG400:蒸留水=4:4:2、0.1から1mL/kg)で静脈内投与あるいは1から3mg/kg(投与溶媒は、40% PEG400、2から5mL/kg)で経口投与した後、0.083、0.25、0.5、1、2,4、8、24時間後にラットは頚静脈より、イヌおよびサルは上腕橈側皮静脈より採血する。血液を遠心分離(3000rpm、15分間、4℃)して得られた血漿を用いて、高速液体クロマトグラム/マススペクトロメトリーにて、血漿中の試験化合物を測定する。同様に試験化合物の既知濃度を添加した標準溶液を測定し、作成した検量線より血漿中濃度(μg/mL)を算出し、最高血漿中濃度をCmax(μg/mL)とする。
(1)ラットカセットPK試験
本発明の化合物を6から10週齢の雄性Crl:CD(SD)ラットに、0.1から0.3mg/kg(投与溶媒は、DMSO:Dimethylacetamide:PEG400:生理食塩水=1.2:2.8:4:2、1mL/kg)で静脈内投与した後、0.25、0.5、1、2、4、6時間後に頸静脈より採血、あるいは1mg/kg(投与溶媒は、DMSO:Tween80:蒸留水=1:1:8、10mL/kg)で経口単回投与した後、0.5、1、2、4時間後に頚静脈より採血する。血液を遠心分離(3000rpm、15分間、4℃)して得られた血漿を用いて、高速液体クロマトグラム/マススペクトロメトリーにて、血漿中の試験化合物を測定する。同様に試験化合物の既知濃度を添加した標準溶液を測定し、作成した検量線より血漿中濃度(μg/mL)を算出し、最高血漿中濃度をCmax(μg/mL)とする。
(2)PK試験
本発明の化合物を動物(約6から8週齢の雄性Crl:CD(SD)ラット、もしくは、約1から3カ年齢の雄性ビーグル犬、もしくは、約6から7カ年齢の雄性カニクイザル)に1mg/kg(投与溶媒は、Dimethylacetamide:PEG400:蒸留水=4:4:2、0.1から1mL/kg)で静脈内投与あるいは1から3mg/kg(投与溶媒は、40% PEG400、2から5mL/kg)で経口投与した後、0.083、0.25、0.5、1、2,4、8、24時間後にラットは頚静脈より、イヌおよびサルは上腕橈側皮静脈より採血する。血液を遠心分離(3000rpm、15分間、4℃)して得られた血漿を用いて、高速液体クロマトグラム/マススペクトロメトリーにて、血漿中の試験化合物を測定する。同様に試験化合物の既知濃度を添加した標準溶液を測定し、作成した検量線より血漿中濃度(μg/mL)を算出し、最高血漿中濃度をCmax(μg/mL)とする。
(薬理実験例7):タンパク結合試験
本発明の化合物の10mMのDMSO溶液を最終濃度10μMとなるように正常血漿(ヒト、ラット、イヌ、サル)に添加する。簡易平衡透析装置(HTD96b Complete Unit(HTDialysis))にて37℃で4時間透析した後、透析膜の内側(血漿側)溶液および外側(PBS側)溶液中の試験化合物濃度を、高速液体クロマトグラム/マススペクトロメトリーを用いて測定する。PBS側と血漿側の比から非結合分率(%)を算出し、100−非結合分率(%)より蛋白結合率(%)を算出する。
本発明の化合物の10mMのDMSO溶液を最終濃度10μMとなるように正常血漿(ヒト、ラット、イヌ、サル)に添加する。簡易平衡透析装置(HTD96b Complete Unit(HTDialysis))にて37℃で4時間透析した後、透析膜の内側(血漿側)溶液および外側(PBS側)溶液中の試験化合物濃度を、高速液体クロマトグラム/マススペクトロメトリーを用いて測定する。PBS側と血漿側の比から非結合分率(%)を算出し、100−非結合分率(%)より蛋白結合率(%)を算出する。
(薬理実験例8):ファーマコキネティクス試験における各種パラメータの算出
ラット、イヌ、サルの各動物種におけるPK試験(前記薬理実験例6)によって得られた血漿中濃度の時間推移についてモデル非依存的解析を行い、全身クリアランスCLtot(L/hr/kg)、定常状態における分布容積Vdss(L/kg)、血漿中濃度―時間曲線下面積AUC(μg・hr/mL)、半減期T1/2(hr)を算出する。また、静脈内投与時のAUCと経口投与時のAUCを比較してバイオアベイラビリティを算出する。
ラット、イヌ、サルの各動物種におけるPK試験(前記薬理実験例6)によって得られた血漿中濃度の時間推移についてモデル非依存的解析を行い、全身クリアランスCLtot(L/hr/kg)、定常状態における分布容積Vdss(L/kg)、血漿中濃度―時間曲線下面積AUC(μg・hr/mL)、半減期T1/2(hr)を算出する。また、静脈内投与時のAUCと経口投与時のAUCを比較してバイオアベイラビリティを算出する。
(薬理実験例9):ヒトにおける薬物動態パラメータの予測
前記薬理実験例6または8等に記載の方法にて得られた、動物のファーマコキネティクス試験における各種パラメータ、インビトロ試験における代謝安定性、タンパク結合率などのパラメータを用い、アロメトリックスケーリングによる方法またはIVIVE(in vitro/in vivo extrapolation)法などの当業者に知られた方法により、ヒトにおける薬物動態パラメータを予測する。
前記薬理実験例6または8等に記載の方法にて得られた、動物のファーマコキネティクス試験における各種パラメータ、インビトロ試験における代謝安定性、タンパク結合率などのパラメータを用い、アロメトリックスケーリングによる方法またはIVIVE(in vitro/in vivo extrapolation)法などの当業者に知られた方法により、ヒトにおける薬物動態パラメータを予測する。
(薬理実験例10):安全性試験
本発明の化合物をマウスまたはラットに単回で経口投与し、死亡例は認められず、目立った行動異常も観察されないことにより、本発明の化合物の安全性が示される。
本発明の化合物をマウスまたはラットに単回で経口投与し、死亡例は認められず、目立った行動異常も観察されないことにより、本発明の化合物の安全性が示される。
以上の結果より、本発明の化合物は、優れた選択的PDE2A阻害剤作用を有することが示され、精神障害、運動障害、不安障害、摂食障害、睡眠障害、気分障害、神経変性障害、注意および/または認知の欠如を含む障害、小児精神障害、薬物依存症、他の障害、肥満、メタボリック症候群、インスリン非依存性糖尿病、耐糖能障害、肺炎、及び変形性関節症、等の疾患の予防及び/または治療剤に用いることが期待される。
本発明の化合物は、以下に示す各種疾患に対して有望な予防、あるいは治療効果がを示すことが期待される。具体的には、(1)統合失調症(妄想型、解体型、緊張型、鑑別不能型、又は残遺型)、(2)統合失調症様障害、(3)統合失調感情障害(妄想型又は抑うつ型)、(4)妄想性障害、(5)物質誘導性精神障害、(6)妄想型人格障害、(7)統合失調型の人格障害、(8)ハンチントン病、(9)ドーパミンアゴニスト療法に伴う異常運動症(ジスキネジア)、(10)パーキンソン病、(11)不穏下肢症候群、(12)本態性振戦、(13)恐慌性障害、(14)広場恐怖症、(15)特定恐怖症、(16)社会恐怖症、(17)強迫性障害、(18)心的外傷後ストレス障害、(19)急性ストレス障害、(20)全般性不安障害、(21)食欲不振症、(22)過食症、(23)気晴らし食い障害、(24)氷食症、(25)過眠症、(26)概日リズム睡眠障害、(27)不眠症、(28)睡眠時異常行動、(29)睡眠遮断、(30)大うつ病エピソード(軽度、中等度、又は重度型)、(31)躁病エピソード、(32)混合性エピソード、(33)軽躁病エピソード、(34)非定型うつ病、(35)メランコリー型うつ病、(36)緊張病性うつ病、(37)季節性うつ病、(38)産後発症気分エピソード、(39)脳卒中後うつ病、(40)大うつ病性障害、(41)気分変調性障害、(42)気分変調症、(43)小うつ病性障害、(44)月経前不快気分障害、(45)統合失調症後うつ病性障害、(46)妄想性障害又は統合失調症等の精神障害に併発する大うつ病性障害、(47)双極性障害(I型及びII型)、(48)気分循環性障害、(49)偏頭痛、(50)てんかん、(51)ハンチントン病、(52)脳外傷に関連する神経変性、(53)脳卒中に関連する神経変性、(54)脳梗塞に関連する神経変性、(55)低血糖誘発性神経変性、(56)てんかん発作に関連する神経変性、(57)神経毒中毒に関連する神経変性、(58)多系統委縮症、(59)線条体中型有棘ニューロンの神経変性、(60)加齢性認知低下、(61)アルツハイマー病、(62)統合失調症又はアルツハイマー病に伴う認知症、(63)多発脳梗塞性認知症、(64)アルコール性認知症又は他の薬物関連認知症、(65)頭蓋内腫瘍又は脳外傷に関連する認知症、(66)ハンチントン病又はパーキンソン病に関連する認知症、(67)エイズ関連認知症、(68)前頭側頭型認知症、(69)せん妄、(70)健忘障害、(71)心的外傷後ストレス障害、(72)精神遅滞、(73)読字障害、(74)算数障害、(75)書字表出障害、(76)注意欠陥障害、(77)注意欠陥/多動性障害(ADHA)、(78)行為障害、(79)自閉症、(80)薬物依存症、(81)トゥーレット症候群、(82)チック障害、(83)精神薄弱(ダウン症候群及び脆弱X症候群を含む。)、(84)肥満、(85)メタボリック症候群、(86)インスリン非依存性糖尿病、(87)耐糖能障害、(89)肺炎、及び(90)変形性関節症、等に対して有望な治療効果が期待できる。
次に、本発明をさらに詳細に説明するために実施例、試験例をあげるが、これらの例は単なる例示であって、本発明を限定するものではなく、また本発明の範囲を逸脱しない範囲で変化させてもよい。
核磁気共鳴スペクトル(NMR)の測定には、JEOL JNM−ECX400 FT−NMR(日本電子)、JEOL JNM−ECX300 FT−NMR(日本電子)、Bruker Avance III 400MHz NMR(ブルカー)を用いた。
液体クロマトグラフィー−質量分析スペクトル(LC−Mass)は以下の方法で測定した。Waters AQUITY UPLCシステムおよびCAPCELL Pakカラム(2.0mm×50mm、3μm)(資生堂)を用い、メタノール:0.05%トリフルオロ酢酸水溶液=5:95(0分)〜95:5(1.0分)〜95:5(1.6分)〜5:95(2.0分)の移動相およびグラジエント条件を用いた。分取系には化合物によりより適宜変更したグラジエント条件を用いた。
超臨界流体液体クロマトグラフィー(SFC)による光学分割はWaters SFC Prep15 Fraction Lynx Systemおよび対応するキラルカラムを用いて実施した。光学純度分析はWaters SFC UPC2および対応するキラルカラムを用いて実施した。
液体クロマトグラフィー−質量分析スペクトル(LC−Mass)は以下の方法で測定した。Waters AQUITY UPLCシステムおよびCAPCELL Pakカラム(2.0mm×50mm、3μm)(資生堂)を用い、メタノール:0.05%トリフルオロ酢酸水溶液=5:95(0分)〜95:5(1.0分)〜95:5(1.6分)〜5:95(2.0分)の移動相およびグラジエント条件を用いた。分取系には化合物によりより適宜変更したグラジエント条件を用いた。
超臨界流体液体クロマトグラフィー(SFC)による光学分割はWaters SFC Prep15 Fraction Lynx Systemおよび対応するキラルカラムを用いて実施した。光学純度分析はWaters SFC UPC2および対応するキラルカラムを用いて実施した。
1H−NMRデータ中、NMRシグナルのパターンで、sはシングレット、dはダブレット、tはトリプレット、qはカルテット、mはマルチプレット、brはブロード、Jはカップリング定数、Hzはヘルツ、CDCl3は重クロロホルム、DMSO−d6は重ジメチルスルホキシドを意味する。1H−NMRデータ中、水酸基(OH)、アミノ基(NH2)、カルボキシル基(COOH)のプロトン等、ブロードバンドであるため確認ができないシグナルについては、データに記載していない。
LC−Massデータ中、Mは分子量、RTは保持時間、[M+H]+はプロトンが付加した分子イオンピークを意味する。
実施例中の「室温」は、通常約0℃から約35℃の温度を示すものとする。
実施例中の「室温」は、通常約0℃から約35℃の温度を示すものとする。
1−メチル−4−(6−メチルピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622992−94−2)(33mg)および1−[4−(トリフルオロメトキシ)フェニル]エチルアミン(CAS番号123195−23−3)(34mg)のN−メチル−2−ピロリドン(0.50ml)溶液に、プロピルホスホン酸無水物(≧50%酢酸エチル溶液、0.13ml)、N,N−ジイソプロピルエチルアミン(26μl)を順次加え、室温で15時間撹拌した。反応液をHPLCを用いて分取精製を行い、標記化合物(27.7mg)を得た。
1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622992−94−2)(33mg)および1−[4−(トリフルオロメトキシ)フェニル]エチルアミン(CAS番号123195−23−3)(34mg)のN−メチル−2−ピロリドン(0.50ml)溶液に、プロピルホスホン酸無水物(≧50%酢酸エチル溶液、0.13ml)、N,N−ジイソプロピルエチルアミン(26μl)を順次加え、室温で15時間撹拌した。反応液をHPLCを用いて分取精製を行い、標記化合物(27.7mg)を得た。
(R)−N−(1−(4−ブロモフェニル)エチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、(R)−(+)−1−(4−ブロモフェニル)エチルアミン(CAS番号45791−36−4)(33mg)を用いて標記化合物(31mg)を得た。
実施例1と同様の方法により、(R)−(+)−1−(4−ブロモフェニル)エチルアミン(CAS番号45791−36−4)(33mg)を用いて標記化合物(31mg)を得た。
N−(1−(4−ブロモフェニル)シクロプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、1−(4−ブロモフェニル)シクロプロパン−1−アミン 塩酸塩(CAS番号345965−54−0)(35mg)を用いて標記化合物(16mg)を得た。
実施例1と同様の方法により、1−(4−ブロモフェニル)シクロプロパン−1−アミン 塩酸塩(CAS番号345965−54−0)(35mg)を用いて標記化合物(16mg)を得た。
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
メチル 2−アミノ−(4−(トリフルオロメトキシ)フェニル)アセテート 塩酸塩の製造
4−(トリフルオロメトキシ)−DL−フェニルグリシン(CAS番号261952−24−3)(500mg)のメタノール(4.5mL)懸濁液に塩化チオニル(0.47mL)をゆっくり加え、70℃で3時間加熱した。反応液にトルエンを加え、減圧下で濃縮した。生じた析出物をろ取し、標記化合物(540mg)を白色固体として得た。
<工程2>
1−アミノ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロパン−2−オールの製造
メチルマグネシウムブロミド (3mol/L、エーテル溶液)(17.5mL)とトルエン(10mL)の混合液に、氷冷下で前記の<工程1>で得た化合物(3.0g)を30分かけて徐々に加えた後、同温で1時間撹拌した。反応液に飽和塩化アンモニウム水溶液(10mL)を加え反応停止し、25%アンモニア水(20mL)を加えた後、酢酸エチル(200mL)で抽出した。有機層を分液し、セライトを用いてろ過した。水槽を酢酸エチル(150mL)で2回抽出した。有機層を合わせ、水(50mL)、飽和食塩水(50mL)で順次洗浄し、硫酸ナトリウムで乾燥した後に濃縮し、標記粗化合物(2.5g)を黄色油状物として得た。
<工程3>
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(110mg)を用いて標記化合物(44mg)を無色油状物として得た。
<工程1>
メチル 2−アミノ−(4−(トリフルオロメトキシ)フェニル)アセテート 塩酸塩の製造
4−(トリフルオロメトキシ)−DL−フェニルグリシン(CAS番号261952−24−3)(500mg)のメタノール(4.5mL)懸濁液に塩化チオニル(0.47mL)をゆっくり加え、70℃で3時間加熱した。反応液にトルエンを加え、減圧下で濃縮した。生じた析出物をろ取し、標記化合物(540mg)を白色固体として得た。
<工程2>
1−アミノ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロパン−2−オールの製造
メチルマグネシウムブロミド (3mol/L、エーテル溶液)(17.5mL)とトルエン(10mL)の混合液に、氷冷下で前記の<工程1>で得た化合物(3.0g)を30分かけて徐々に加えた後、同温で1時間撹拌した。反応液に飽和塩化アンモニウム水溶液(10mL)を加え反応停止し、25%アンモニア水(20mL)を加えた後、酢酸エチル(200mL)で抽出した。有機層を分液し、セライトを用いてろ過した。水槽を酢酸エチル(150mL)で2回抽出した。有機層を合わせ、水(50mL)、飽和食塩水(50mL)で順次洗浄し、硫酸ナトリウムで乾燥した後に濃縮し、標記粗化合物(2.5g)を黄色油状物として得た。
<工程3>
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(110mg)を用いて標記化合物(44mg)を無色油状物として得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
エチル (S)−2−(((S)−tert−ブチルスルフィニル)アミノ)−2−(4−(トリフルオロメトキシ)フェニル)アセテートの製造
(S,E)−エチル 2−((tert−ブチルスルフィニル)イミノ)アセテート(CAS番号1255940−61−4)(2.99g)、4−トリフリオロメトキシフェニルボロン酸(2g)の1,4−ジオキサン(40ml)溶液に、ビス(アセトニトリル)(1,5−シクロオクタジエン)ロジウム(I)テトラフルオフロボレート(CAS番号 32679−02−0)(0.37g)を室温で加え、80℃で6時間撹拌した。得られた反応液を濃縮後、シリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−50:50)にて精製し、標記化合物(1.69g)を褐色油状物として得た。
<工程2>
エチル (S)−2−アミノ−2−(4−(トリフルオロメトキシ)フェニル)アセテート塩酸塩の製造
前記の<工程1>で得られた化合物(1.6g)のシクロペンチルメチルエーテル溶液(16ml)に、4規定塩酸―シクロペンチルメチルエーテル溶液(10.89ml)を室温で加え、室温で30分撹拌した。得られた反応液を濃縮後、ヘプタン(15ml)を加えた。17時間後、析出した固体をろ取し、シクロペンチルメチルエーテル/ヘプタン混合溶液(1:2、20ml)で洗浄することで標記化合物(1.15g)を橙色個体として得た。
<工程3>
(S)−1−アミノ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロパノールの製造
氷冷下、3Mメチルマグネシウムブロミドのジエチルエーテル溶液(6.12ml)に前記の<工程2>で得られた化合物(1.1g)を2回に分割して加え、室温で1時間撹拌した。反応液を塩化アンモニウム水溶液(25ml)でクエンチし、25%アンモニア水溶液(10ml)を加え、酢酸エチル(80ml、50mlx2)で抽出した。得られた有機層を飽和食塩水(20ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(910mg)を黄色固体として得た。
<工程4>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造合成
実施例1と同様の方法により、前記の<工程3>で得た化合物(60mg)を用いて標記化合物(15mg)を得た。
<工程1>
エチル (S)−2−(((S)−tert−ブチルスルフィニル)アミノ)−2−(4−(トリフルオロメトキシ)フェニル)アセテートの製造
(S,E)−エチル 2−((tert−ブチルスルフィニル)イミノ)アセテート(CAS番号1255940−61−4)(2.99g)、4−トリフリオロメトキシフェニルボロン酸(2g)の1,4−ジオキサン(40ml)溶液に、ビス(アセトニトリル)(1,5−シクロオクタジエン)ロジウム(I)テトラフルオフロボレート(CAS番号 32679−02−0)(0.37g)を室温で加え、80℃で6時間撹拌した。得られた反応液を濃縮後、シリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−50:50)にて精製し、標記化合物(1.69g)を褐色油状物として得た。
<工程2>
エチル (S)−2−アミノ−2−(4−(トリフルオロメトキシ)フェニル)アセテート塩酸塩の製造
前記の<工程1>で得られた化合物(1.6g)のシクロペンチルメチルエーテル溶液(16ml)に、4規定塩酸―シクロペンチルメチルエーテル溶液(10.89ml)を室温で加え、室温で30分撹拌した。得られた反応液を濃縮後、ヘプタン(15ml)を加えた。17時間後、析出した固体をろ取し、シクロペンチルメチルエーテル/ヘプタン混合溶液(1:2、20ml)で洗浄することで標記化合物(1.15g)を橙色個体として得た。
<工程3>
(S)−1−アミノ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロパノールの製造
氷冷下、3Mメチルマグネシウムブロミドのジエチルエーテル溶液(6.12ml)に前記の<工程2>で得られた化合物(1.1g)を2回に分割して加え、室温で1時間撹拌した。反応液を塩化アンモニウム水溶液(25ml)でクエンチし、25%アンモニア水溶液(10ml)を加え、酢酸エチル(80ml、50mlx2)で抽出した。得られた有機層を飽和食塩水(20ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(910mg)を黄色固体として得た。
<工程4>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造合成
実施例1と同様の方法により、前記の<工程3>で得た化合物(60mg)を用いて標記化合物(15mg)を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
エチル (S)−2−(((S)−tert−ブチルスルフィニル)アミノ)−2−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)アセテートの製造
(S,E)−エチル 2−((tert−ブチルスルフィニル)イミノ)アセテート(CAS番号1255940−61−4)(1.93g)、3−フルオロ−4−トリフルオロメトキシフェニルボロン酸(1.40g)の1,4−ジオキサン溶液(40ml)にビス(アセトニトリル)(1,5−シクロオクタジエン)ロジウム(I)テトラフルオフロボレート(0.24g)を室温で加え、80℃で12時間撹拌した。得られた反応液を濃縮後、シリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−50:50)にて精製し、標記化合物(1.40g)を褐色油状物として得た。
<工程2>
エチル (S)−2−アミノ−2−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)アセテート塩酸塩の製造
前記の<工程1>で得られた化合物(1.40g)のシクロペンチルメチルエーテル溶液(14.0ml)に、4規定塩酸―シクロペンチルメチルエーテル溶液(9.08ml)を室温で加え、室温で1時間撹拌した。得られた反応液を濃縮後、ヘプタン(15ml)を加えた。析出した固体をろ取し、ヘプタンで洗浄することで標記化合物(1.08g)をベージュ色固体として得た。
<工程3>
(S)−1−アミノ−2−メチル−1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)プロパノールの製造
氷冷下、3Mメチルマグネシウムブロミドのジエチルエーテル溶液(5.25ml)に前記の<工程2>で得られた化合物(1.0g)を20分かけて加え、室温で1.5時間撹拌した。反応液を塩化アンモニウム水溶液でクエンチし、25%アンモニア水溶液を加え、酢酸エチルで抽出した。得られた有機層を飽和食塩水で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(834mg)を黄色固体として得た。
<工程4>
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程3>で得た化合物(36.9mg)を用いて標記化合物(40.5mg)を得た。
<工程1>
エチル (S)−2−(((S)−tert−ブチルスルフィニル)アミノ)−2−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)アセテートの製造
(S,E)−エチル 2−((tert−ブチルスルフィニル)イミノ)アセテート(CAS番号1255940−61−4)(1.93g)、3−フルオロ−4−トリフルオロメトキシフェニルボロン酸(1.40g)の1,4−ジオキサン溶液(40ml)にビス(アセトニトリル)(1,5−シクロオクタジエン)ロジウム(I)テトラフルオフロボレート(0.24g)を室温で加え、80℃で12時間撹拌した。得られた反応液を濃縮後、シリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−50:50)にて精製し、標記化合物(1.40g)を褐色油状物として得た。
<工程2>
エチル (S)−2−アミノ−2−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)アセテート塩酸塩の製造
前記の<工程1>で得られた化合物(1.40g)のシクロペンチルメチルエーテル溶液(14.0ml)に、4規定塩酸―シクロペンチルメチルエーテル溶液(9.08ml)を室温で加え、室温で1時間撹拌した。得られた反応液を濃縮後、ヘプタン(15ml)を加えた。析出した固体をろ取し、ヘプタンで洗浄することで標記化合物(1.08g)をベージュ色固体として得た。
<工程3>
(S)−1−アミノ−2−メチル−1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)プロパノールの製造
氷冷下、3Mメチルマグネシウムブロミドのジエチルエーテル溶液(5.25ml)に前記の<工程2>で得られた化合物(1.0g)を20分かけて加え、室温で1.5時間撹拌した。反応液を塩化アンモニウム水溶液でクエンチし、25%アンモニア水溶液を加え、酢酸エチルで抽出した。得られた有機層を飽和食塩水で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(834mg)を黄色固体として得た。
<工程4>
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程3>で得た化合物(36.9mg)を用いて標記化合物(40.5mg)を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−オンの製造
N−メトキシ−N−メチル−2−メトキシアセトアミド(CAS番号132289−57−7)(75g)と4−ブロモ−2−フルオロ−1−(トリフルオロメトキシ)ベンゼン(58g)のテトラヒドロフラン(600mL)溶液に、窒素雰囲気下、−78℃で n−ブチルリチウム(2.5モル/L、テトラヒドロフラン溶液)(290mL)を滴下し、室温で2時間撹拌した。反応液を飽和塩化アンモニウム水(100mL)を加えて反応停止した。溶媒留去した後、酢酸エチル(1L)で2回抽出した。有機層を合わせ、飽和食塩水(500mL)で洗浄し、硫酸マグネシウムで乾燥した後、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;石油エーテル:酢酸エチル=95:5)で精製し、標記化合物(50g)を褐色油状物として得た。
<工程2>
1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−オン オキシムの製造
前記の<工程1>で得た化合物(49g)と塩化ヒドロキシルアンモニウム(67g)のエタノール(400mL)懸濁液を室温で終夜撹拌した。エタノールを留去し、残渣を酢酸エチル(400mL)で希釈した。有機層を1規定塩酸(100mL)、飽和重層水(100mL)で順次洗浄した後、硫酸マグネシウムで乾燥し、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;石油エーテル:酢酸エチル=95:5)で精製し、標記粗化合物(50g)を無色油状物として得た。
<工程1>
1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−オンの製造
N−メトキシ−N−メチル−2−メトキシアセトアミド(CAS番号132289−57−7)(75g)と4−ブロモ−2−フルオロ−1−(トリフルオロメトキシ)ベンゼン(58g)のテトラヒドロフラン(600mL)溶液に、窒素雰囲気下、−78℃で n−ブチルリチウム(2.5モル/L、テトラヒドロフラン溶液)(290mL)を滴下し、室温で2時間撹拌した。反応液を飽和塩化アンモニウム水(100mL)を加えて反応停止した。溶媒留去した後、酢酸エチル(1L)で2回抽出した。有機層を合わせ、飽和食塩水(500mL)で洗浄し、硫酸マグネシウムで乾燥した後、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;石油エーテル:酢酸エチル=95:5)で精製し、標記化合物(50g)を褐色油状物として得た。
<工程2>
1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−オン オキシムの製造
前記の<工程1>で得た化合物(49g)と塩化ヒドロキシルアンモニウム(67g)のエタノール(400mL)懸濁液を室温で終夜撹拌した。エタノールを留去し、残渣を酢酸エチル(400mL)で希釈した。有機層を1規定塩酸(100mL)、飽和重層水(100mL)で順次洗浄した後、硫酸マグネシウムで乾燥し、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;石油エーテル:酢酸エチル=95:5)で精製し、標記粗化合物(50g)を無色油状物として得た。
<工程3>
tert−ブチル (1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)カルバメートの製造
前記の<工程2>で得た化合物(50g)と二炭酸ジ−tert−ブチル(CAS番号:24424-99-5)(81g)のメタノール(1L)溶液にパラジウム/炭素(Pd10%)(20g)を加え、水素雰囲気化室温で4時間撹拌した。触媒をろ別し、ろ液を減圧濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;石油エーテル:酢酸エチル=90:10)で精製し、標記化合物(35g)を白色固体として得た。
<工程4>
1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−アミン 塩酸塩の製造
前記の<工程3>で得た化合物(5.0g)に塩化水素(4モル/L酢酸エチル溶液、50ml)を加え、室温で2時間撹拌した。反応液を濃縮し、残渣にイソプロピルエーテルを加え析出物をろ取し、イソプロピルエーテルで洗浄した。得られた析出物を減圧乾燥し、標記化合物(3.8g)を白色固体として得た。
<工程5>
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程4>で得た化合物(48mg)を用いて標記化合物(54mg)を得た。
tert−ブチル (1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)カルバメートの製造
前記の<工程2>で得た化合物(50g)と二炭酸ジ−tert−ブチル(CAS番号:24424-99-5)(81g)のメタノール(1L)溶液にパラジウム/炭素(Pd10%)(20g)を加え、水素雰囲気化室温で4時間撹拌した。触媒をろ別し、ろ液を減圧濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;石油エーテル:酢酸エチル=90:10)で精製し、標記化合物(35g)を白色固体として得た。
<工程4>
1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−アミン 塩酸塩の製造
前記の<工程3>で得た化合物(5.0g)に塩化水素(4モル/L酢酸エチル溶液、50ml)を加え、室温で2時間撹拌した。反応液を濃縮し、残渣にイソプロピルエーテルを加え析出物をろ取し、イソプロピルエーテルで洗浄した。得られた析出物を減圧乾燥し、標記化合物(3.8g)を白色固体として得た。
<工程5>
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程4>で得た化合物(48mg)を用いて標記化合物(54mg)を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
tert−ブチル (S)−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)カルバメートの分離
前記の実施例7の<工程3>で得た化合物(10g)を、SFC(カラム:(R,R)−Whelk−O1直径20mmx250mm,5μm、移動相:10%2−プロパノール/CO2、流速:70g/min、温度:35℃)を用いて光学分割を行うことで、標記化合物(4.2g,97.3%ee)を第一分画として得た。光学純度はHPLC(カラム:(株)ダイセル化学工業性 CHIRALCEL AD−H 直径4.6mmx250mm、移動相:5%エタノール/ヘキサン、流速:1.0mL/min、温度:40℃)により測定した(保持時間:4.4分)。
<工程2>
(S)−1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−アミン塩酸塩の製造
前記の実施例7の<工程3>で得た化合物(1g)の酢酸エチル(10ml)溶液に、0℃で塩化水素(酢酸エチル溶液、40mL)を加え、室温で2時間撹拌した。反応液を濃縮し、標記化合物(0.82g)を黄色固体として得た。
<工程3>
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(15mg)を用いて標記化合物(19mg)を得た。
<工程1>
tert−ブチル (S)−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)カルバメートの分離
前記の実施例7の<工程3>で得た化合物(10g)を、SFC(カラム:(R,R)−Whelk−O1直径20mmx250mm,5μm、移動相:10%2−プロパノール/CO2、流速:70g/min、温度:35℃)を用いて光学分割を行うことで、標記化合物(4.2g,97.3%ee)を第一分画として得た。光学純度はHPLC(カラム:(株)ダイセル化学工業性 CHIRALCEL AD−H 直径4.6mmx250mm、移動相:5%エタノール/ヘキサン、流速:1.0mL/min、温度:40℃)により測定した(保持時間:4.4分)。
<工程2>
(S)−1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエタン−1−アミン塩酸塩の製造
前記の実施例7の<工程3>で得た化合物(1g)の酢酸エチル(10ml)溶液に、0℃で塩化水素(酢酸エチル溶液、40mL)を加え、室温で2時間撹拌した。反応液を濃縮し、標記化合物(0.82g)を黄色固体として得た。
<工程3>
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(6−メチルピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(15mg)を用いて標記化合物(19mg)を得た。
1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
2−メチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)プロパン−2−スルフィンアミドの製造
1−ブロモ−4−(トリフルオロメトキシ)ベンゼン(620mg)のテトラヒドロフラン(10mL)溶液に、ドライアイス―アセトン浴冷下でn−ブチルリチウム(1.6Mヘキサン溶液、1.5mL)を10分かけて滴下し、同温で1時間撹拌した。反応液にドライアイス―アセトン浴冷下で、2−メチル−N−(オキセタン−3−イリデン)プロパン−2−スルフィンアミド(CAS番号1158098−73−7)(300mg)のテトラヒドロフラン(2mL)溶液を加え、同温で30分撹拌した後、室温で45分撹拌した。反応液に飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を硫酸ナトリウムで乾燥し、減圧下で濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;n−ヘプタン:酢酸エチル=100:0−50:50)で精製し、標記化合物(520mg)を淡黄色油状物として得た。
<工程1>
2−メチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)プロパン−2−スルフィンアミドの製造
1−ブロモ−4−(トリフルオロメトキシ)ベンゼン(620mg)のテトラヒドロフラン(10mL)溶液に、ドライアイス―アセトン浴冷下でn−ブチルリチウム(1.6Mヘキサン溶液、1.5mL)を10分かけて滴下し、同温で1時間撹拌した。反応液にドライアイス―アセトン浴冷下で、2−メチル−N−(オキセタン−3−イリデン)プロパン−2−スルフィンアミド(CAS番号1158098−73−7)(300mg)のテトラヒドロフラン(2mL)溶液を加え、同温で30分撹拌した後、室温で45分撹拌した。反応液に飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を硫酸ナトリウムで乾燥し、減圧下で濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;n−ヘプタン:酢酸エチル=100:0−50:50)で精製し、標記化合物(520mg)を淡黄色油状物として得た。
<工程2>
3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−アミン 塩酸塩の製造
前記の<工程1>で得た化合物(670mg)のメタノール(2.2mL)溶液に、氷冷下で塩化水素 (約4規定1,4−ジオキサン溶液、0.74mL)を加え、同温で30分撹拌した。同温でジイソプロピルエーテル(25mL)を加え、15分撹拌した。析出物をろ取し、ジイソプロピルエーテルで洗浄し、標記化合物(340mg)を淡褐色固体として得た。
<工程3>
1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(32mg)を用いて標記化合物(4.3mg)を得た。
3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−アミン 塩酸塩の製造
前記の<工程1>で得た化合物(670mg)のメタノール(2.2mL)溶液に、氷冷下で塩化水素 (約4規定1,4−ジオキサン溶液、0.74mL)を加え、同温で30分撹拌した。同温でジイソプロピルエーテル(25mL)を加え、15分撹拌した。析出物をろ取し、ジイソプロピルエーテルで洗浄し、標記化合物(340mg)を淡褐色固体として得た。
<工程3>
1−メチル−4−(6−メチルピリジン−2−イル)−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(32mg)を用いて標記化合物(4.3mg)を得た。
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1368131−71−8)(30mg)および(1R)−1−[4−(トリフルオロメトキシ)フェニル]エタン−1−アミン(CAS番号1209050−26−9)(30mg)を用いて標記化合物(12mg)を得た。
実施例1と同様の方法により、1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1368131−71−8)(30mg)および(1R)−1−[4−(トリフルオロメトキシ)フェニル]エタン−1−アミン(CAS番号1209050−26−9)(30mg)を用いて標記化合物(12mg)を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例10と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例10と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例10と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例10と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例10と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例10と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、1−メチル−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622993−01−4)(41mg)を用いて標記化合物(29mg)を得た。
実施例1と同様の方法により、1−メチル−4−(6−(トリフルオロメチル)ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622993−01−4)(41mg)を用いて標記化合物(29mg)を得た。
1−メチル−4−(2−メチルピリミジン−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、1−メチル−4−(2−メチルピリミジン−4−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622993−28−5 )(33mg)を用いて標記化合物(35mg)を得た。
実施例1と同様の方法により、1−メチル−4−(2−メチルピリミジン−4−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622993−28−5 )(33mg)を用いて標記化合物(35mg)を得た。
1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622992−93−1 )(33mg)を用いて標記化合物(24mg)を得た。
実施例1と同様の方法により、1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボン酸(CAS番号1622992−93−1 )(33mg)を用いて標記化合物(24mg)を得た。
(R)−1−メチル−4−(5−メチルピラジン−2−イル)−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例16と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例16と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(5−メチルピラジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例16と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例16と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
4−(4−シアノチアゾール−2−イル)−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、4−(4−シアノチアゾール−2−イル)−1−メチル−1H−ピラゾール−5−カルボン酸(CAS番号1622994−03−9)(35mg)を用いて標記化合物(19mg)を得た。
実施例1と同様の方法により、4−(4−シアノチアゾール−2−イル)−1−メチル−1H−ピラゾール−5−カルボン酸(CAS番号1622994−03−9)(35mg)を用いて標記化合物(19mg)を得た。
(R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボン酸の製造
4−ブロモ−1−メチル−1H−ピラゾロ−5−カルボン酸エチルエステル(CAS番号1328640−39−6)(200mg)のトルエン(2mL)溶液に4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン(148μL)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(78.6mg)、2−ジシクロヘキシルホスフィノ−2’ ,6’−ジメトキシビフェニル(70.5mg)、トリエチルアミン(359μL)を加え100℃で1時間撹拌した。室温に冷却後、炭酸カリウム(356mg)の水(0.4mL)−エタノール(1.6mL)の混合溶液を加えさらに3−ブロモイソキノリン(179mg)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(78.6mg)、2−ジシクロヘキシルホスフィノ−2’ ,6’−ジメトキシビフェニル(70.5mg)を加え100℃で1時間撹拌した。冷却した反応液をセライトろ過しセライトを酢酸エチル、水で順次洗浄した。得られた溶液を酢酸エチルで抽出後、水、飽和食塩水で洗浄し、硫酸ナトリウムで乾燥、ろ過、濃縮した。得られた残渣にエタノール(2.4mL)および1N−NaOH(2.6mL)を加え室温で1時間撹拌した。反応液を水および酢酸エチルで希釈後、酢酸エチルで抽出した。水層を1N−HClによって中和し酢酸エチルで3回抽出した。合わせた有機層を飽和食塩水で洗浄、硫酸ナトリウムで乾燥、ろ過、濃縮することで標記化合物(59.6mg)を得た。
<工程1>
4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボン酸の製造
4−ブロモ−1−メチル−1H−ピラゾロ−5−カルボン酸エチルエステル(CAS番号1328640−39−6)(200mg)のトルエン(2mL)溶液に4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン(148μL)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(78.6mg)、2−ジシクロヘキシルホスフィノ−2’ ,6’−ジメトキシビフェニル(70.5mg)、トリエチルアミン(359μL)を加え100℃で1時間撹拌した。室温に冷却後、炭酸カリウム(356mg)の水(0.4mL)−エタノール(1.6mL)の混合溶液を加えさらに3−ブロモイソキノリン(179mg)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(78.6mg)、2−ジシクロヘキシルホスフィノ−2’ ,6’−ジメトキシビフェニル(70.5mg)を加え100℃で1時間撹拌した。冷却した反応液をセライトろ過しセライトを酢酸エチル、水で順次洗浄した。得られた溶液を酢酸エチルで抽出後、水、飽和食塩水で洗浄し、硫酸ナトリウムで乾燥、ろ過、濃縮した。得られた残渣にエタノール(2.4mL)および1N−NaOH(2.6mL)を加え室温で1時間撹拌した。反応液を水および酢酸エチルで希釈後、酢酸エチルで抽出した。水層を1N−HClによって中和し酢酸エチルで3回抽出した。合わせた有機層を飽和食塩水で洗浄、硫酸ナトリウムで乾燥、ろ過、濃縮することで標記化合物(59.6mg)を得た。
<工程2>
(R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程1>で得た化合物(19mg)を用いて標記化合物(8.6mg)を得た。
(R)−4−(イソキノリン−3−イル)−1−メチル−N−(1−(4−トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程1>で得た化合物(19mg)を用いて標記化合物(8.6mg)を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(イソキノリン−3−イル)−1−メチル−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
1−メチル−4−(ピリミジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(R)−1−メチル−4−(キノリン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(R)−1−エチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−1−エチル−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
1−エチル−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例20と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
メチル 1−(2−メトキシエチル)−1H−ピラゾール−5−カルボキシレートの製造
1−(2−メトキシエチル)−1H−ピラゾール−5−カルボン酸(CAS番号936249−31−9)(200mg)のトルエン−メタノール溶液(2:1、2ml)にトリメチルシリルジアゾメタン(ca.10%ヘキサン溶液)(3.92ml)を加えて室温で1時間撹拌した。反応液を濃縮することで、標記化合物(230mg)を無色油状物として得た。
<工程2>
メチル 4−ブロモ−1−(2−メトキシエチル)−1H−ピラゾール−5−カルボキシレートの製造
前記の<工程1>で得られた化合物(200mg)のN,N−ジメチルホルムアミド溶液(3ml)にN−ブルモスクシンイミド(213mg)を室温で加え、18時間撹拌した。反応液を水(30ml)で希釈し、酢酸エチル(50mlx2)で抽出した。得られた有機層をチオ硫酸ナトリウム水溶液(10ml)、水(50mlx2)、飽和食塩水(20ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(300mg)を無色油状物として得た。
<工程1>
メチル 1−(2−メトキシエチル)−1H−ピラゾール−5−カルボキシレートの製造
1−(2−メトキシエチル)−1H−ピラゾール−5−カルボン酸(CAS番号936249−31−9)(200mg)のトルエン−メタノール溶液(2:1、2ml)にトリメチルシリルジアゾメタン(ca.10%ヘキサン溶液)(3.92ml)を加えて室温で1時間撹拌した。反応液を濃縮することで、標記化合物(230mg)を無色油状物として得た。
<工程2>
メチル 4−ブロモ−1−(2−メトキシエチル)−1H−ピラゾール−5−カルボキシレートの製造
前記の<工程1>で得られた化合物(200mg)のN,N−ジメチルホルムアミド溶液(3ml)にN−ブルモスクシンイミド(213mg)を室温で加え、18時間撹拌した。反応液を水(30ml)で希釈し、酢酸エチル(50mlx2)で抽出した。得られた有機層をチオ硫酸ナトリウム水溶液(10ml)、水(50mlx2)、飽和食塩水(20ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(300mg)を無色油状物として得た。
<工程3>
1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸の製造
前記の<工程2>で得られた化合物(150mg)、4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン(CAS番号25015−63−8)(0.09ml)、トリス(ジベンジリデンアセトン)ジパラジウム(26mg)、2−ジシクロヘキシルホスフィノ−2’,6’−ジメトキシビフェニル(CAS番号657408−07−6)(23mg)、トリエチルアミン(0.24ml)の1,4−ジオキサン溶液(9ml)を1時間加熱還流した。反応液を室温まで冷却した後、2−クロロピリジン(65mg)、炭酸カリウム(236mg)、水(3ml)を加えて、17時間加熱還流した。反応液を室温まで冷却した後、1規定水酸化ナトリウム水溶液(2.85ml)を加えて、80℃で2時間加熱撹拌した。反応液を0.4規定水酸化ナトリウム水溶液(50ml)で逆抽出した後、水層を酢酸エチル(20ml)で洗浄した。水層がpH4になるまで1規定塩酸水溶液を加え、酢酸エチル(30mlx5)で抽出した。得られた有機層を水(50ml)、飽和食塩水(20ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(150mg)を黄色個体として得た。
<工程4>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程4>で得た化合物(30mg)を用いて標記化合物(3.2mg)を得た。
1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸の製造
前記の<工程2>で得られた化合物(150mg)、4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン(CAS番号25015−63−8)(0.09ml)、トリス(ジベンジリデンアセトン)ジパラジウム(26mg)、2−ジシクロヘキシルホスフィノ−2’,6’−ジメトキシビフェニル(CAS番号657408−07−6)(23mg)、トリエチルアミン(0.24ml)の1,4−ジオキサン溶液(9ml)を1時間加熱還流した。反応液を室温まで冷却した後、2−クロロピリジン(65mg)、炭酸カリウム(236mg)、水(3ml)を加えて、17時間加熱還流した。反応液を室温まで冷却した後、1規定水酸化ナトリウム水溶液(2.85ml)を加えて、80℃で2時間加熱撹拌した。反応液を0.4規定水酸化ナトリウム水溶液(50ml)で逆抽出した後、水層を酢酸エチル(20ml)で洗浄した。水層がpH4になるまで1規定塩酸水溶液を加え、酢酸エチル(30mlx5)で抽出した。得られた有機層を水(50ml)、飽和食塩水(20ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(150mg)を黄色個体として得た。
<工程4>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程4>で得た化合物(30mg)を用いて標記化合物(3.2mg)を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例28と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例28と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−(2−メトキシエチル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例28と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例28と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
メチル 4−ブロモ−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−3−カルボキシレートの製造
メチル 4−ブロモ−1H−ピラゾール−3−カルボキシレート(CAS番号81190−89−8)(600mg)のN,N―ジメチルスルホキシド溶液(3ml)に炭酸カリウム(890mg)を加えて室温で10分撹拌した。反応液に2,2,2−トリフルオロメチルトリフルオロメタンスルホネート(0.84ml)を加えて、さらに18時間撹拌した。反応液をカラムクロマトグラフィーにて精製することで、標記化合物(230mg)を得た。
<工程2>
4−(ピリジン−2−イル)―1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボン酸の製造
前記の<工程1>で得られた化合物(200mg)のトルエン溶液(3.0ml)に、2−(トリブチルスタンニル)ピリジン(CAS番号:17997−47−6)(0.29ml)、テトラキストリフェニルホスフィンパラジウム(161mg)を加え、マイクロウェーブを用いて180℃で1時間加熱撹拌した。反応液を濃縮し、残渣にエタノール(3.0mL)と1規定水酸化ナトリウム水溶液(3.0mL)を加え、60℃で1時間撹拌した。酢酸エチル(15mL)を加え分液し、有機層を1規定水酸化ナトリウム水溶液で抽出した。水層を酢酸エチルで洗浄した後、pH4になるまで1規定塩酸を加え、酢酸エチル(20mL)で3回抽出した。有機層を飽和食塩水で洗浄し、硫酸ナトリウムで乾燥した後、ろ過、濃縮することで標記粗化合物(40mg)を得た。
<工程3>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(20mg)を用いて標記化合物(4.3mg)を得た。
<工程1>
メチル 4−ブロモ−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−3−カルボキシレートの製造
メチル 4−ブロモ−1H−ピラゾール−3−カルボキシレート(CAS番号81190−89−8)(600mg)のN,N―ジメチルスルホキシド溶液(3ml)に炭酸カリウム(890mg)を加えて室温で10分撹拌した。反応液に2,2,2−トリフルオロメチルトリフルオロメタンスルホネート(0.84ml)を加えて、さらに18時間撹拌した。反応液をカラムクロマトグラフィーにて精製することで、標記化合物(230mg)を得た。
<工程2>
4−(ピリジン−2−イル)―1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボン酸の製造
前記の<工程1>で得られた化合物(200mg)のトルエン溶液(3.0ml)に、2−(トリブチルスタンニル)ピリジン(CAS番号:17997−47−6)(0.29ml)、テトラキストリフェニルホスフィンパラジウム(161mg)を加え、マイクロウェーブを用いて180℃で1時間加熱撹拌した。反応液を濃縮し、残渣にエタノール(3.0mL)と1規定水酸化ナトリウム水溶液(3.0mL)を加え、60℃で1時間撹拌した。酢酸エチル(15mL)を加え分液し、有機層を1規定水酸化ナトリウム水溶液で抽出した。水層を酢酸エチルで洗浄した後、pH4になるまで1規定塩酸を加え、酢酸エチル(20mL)で3回抽出した。有機層を飽和食塩水で洗浄し、硫酸ナトリウムで乾燥した後、ろ過、濃縮することで標記粗化合物(40mg)を得た。
<工程3>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(20mg)を用いて標記化合物(4.3mg)を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1−(2,2,2−トリフルオロエチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例31と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例31と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−1−(シクロプロピルメチル)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例31と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例31と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
エチル1−メチル−4−(オキサゾル−2−イル)−1H−ピラゾール−5−カルボキシレートの製造合成
エチル 4ブロモ−1−メチル−1H−ピラゾール−5−カルボキシレート(CAS番号1328640−39−6)(120mg)、2−(トリブチルスタンニル)オキサゾール(CAS番号145214−05−7)(277mg)のN,N−ジメチルホルムアミド溶液(2ml)にテトラキストリフェニルホスフィンパラジウム(178mg)、ヨウ化銅(I)(29mg)、フッ化セシウム(235mg)を加えて3回脱気した後窒素置換し、100℃で20時間加熱撹拌した。反応液を塩化アンモニウム水溶液(3ml)でクエンチ後、酢酸エチル(5ml)を加えてセライトろ過した。得られた溶液を酢酸エチル(15mlx2)で抽出、水(15mlx2)、飽和食塩水(10ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮した。得られた組成生物をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−80:20)にて精製し、標記化合物(100mg)を無色油状物として得た。
<工程1>
エチル1−メチル−4−(オキサゾル−2−イル)−1H−ピラゾール−5−カルボキシレートの製造合成
エチル 4ブロモ−1−メチル−1H−ピラゾール−5−カルボキシレート(CAS番号1328640−39−6)(120mg)、2−(トリブチルスタンニル)オキサゾール(CAS番号145214−05−7)(277mg)のN,N−ジメチルホルムアミド溶液(2ml)にテトラキストリフェニルホスフィンパラジウム(178mg)、ヨウ化銅(I)(29mg)、フッ化セシウム(235mg)を加えて3回脱気した後窒素置換し、100℃で20時間加熱撹拌した。反応液を塩化アンモニウム水溶液(3ml)でクエンチ後、酢酸エチル(5ml)を加えてセライトろ過した。得られた溶液を酢酸エチル(15mlx2)で抽出、水(15mlx2)、飽和食塩水(10ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮した。得られた組成生物をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−80:20)にて精製し、標記化合物(100mg)を無色油状物として得た。
<工程2>
リチウム1−メチル−4−(オキサゾル−2−イル)−1H−ピラゾール−5−カルボキシレートの製造
前記の<工程1>で得られた化合物(50mg)のメタノール溶液(4ml)に水酸化リチウム(6mg)を加えて、室温で16時間撹拌した。反応液を濃縮することで標記化合物(60mg)を白色固体として得た。
<工程3>
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(40mg)を用いて標記化合物(4.9mg)を得た。
リチウム1−メチル−4−(オキサゾル−2−イル)−1H−ピラゾール−5−カルボキシレートの製造
前記の<工程1>で得られた化合物(50mg)のメタノール溶液(4ml)に水酸化リチウム(6mg)を加えて、室温で16時間撹拌した。反応液を濃縮することで標記化合物(60mg)を白色固体として得た。
<工程3>
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(オキサゾール−2−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(40mg)を用いて標記化合物(4.9mg)を得た。
(R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
<工程1>
エチル 1−メチル−4−((トリメチルシリル)エチニル)−1H−ピラゾール−5−カルボキシレートの製造
エチル 4−ヨード−1−メチル−1H−ピラゾール−5−カルボン酸(CAS番号1354705−42−2)(300mg)のジエチルアミン溶液(5ml)にトリメチルシリルアセチレン(0.3ml)、ビス(トリフェニルホスフィン)パラジウム(II)ジクロリド(75.2mg)、ヨウ化銅(I)(20.4mg)を加えて60℃で1時間加熱撹拌した。反応液を水で希釈し、酢酸エチルで抽出した。得られた有機層を水、飽和食塩水で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮した。得られた粗成績体をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10)にて精製し、標記化合物(110mg)を黄色固体として得た。
<工程2>
4−エチニル−1−メチル−1H−ピラゾール−5−カルボン酸の製造
前記の<工程1>で得られた化合物(100mg)のテトラヒドロフラン−水混合溶液(4:1、 2.5ml)に、水酸化リチウム(9.57mg)を加えて室温で18時間撹拌した。反応溶液のpHが1になるまで1規定塩酸を加え、酢酸エチル(20mlx3)で抽出した。得られた有機層を飽和食塩水(10ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(50mg)を茶色固体として得た。
<工程1>
エチル 1−メチル−4−((トリメチルシリル)エチニル)−1H−ピラゾール−5−カルボキシレートの製造
エチル 4−ヨード−1−メチル−1H−ピラゾール−5−カルボン酸(CAS番号1354705−42−2)(300mg)のジエチルアミン溶液(5ml)にトリメチルシリルアセチレン(0.3ml)、ビス(トリフェニルホスフィン)パラジウム(II)ジクロリド(75.2mg)、ヨウ化銅(I)(20.4mg)を加えて60℃で1時間加熱撹拌した。反応液を水で希釈し、酢酸エチルで抽出した。得られた有機層を水、飽和食塩水で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮した。得られた粗成績体をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10)にて精製し、標記化合物(110mg)を黄色固体として得た。
<工程2>
4−エチニル−1−メチル−1H−ピラゾール−5−カルボン酸の製造
前記の<工程1>で得られた化合物(100mg)のテトラヒドロフラン−水混合溶液(4:1、 2.5ml)に、水酸化リチウム(9.57mg)を加えて室温で18時間撹拌した。反応溶液のpHが1になるまで1規定塩酸を加え、酢酸エチル(20mlx3)で抽出した。得られた有機層を飽和食塩水(10ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮することで標記化合物(50mg)を茶色固体として得た。
<工程3>
(R)−4−エチニル−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例10と同様の方法により、1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸の代わりに前記の<工程2>で得られた化合物(25mg)を用いることで、標記化合物(45mg)を得た。
<工程4>
(R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
前記の<工程3>で得られた化合物(40mg)、トリメチルシリルアジド(0.03ml)のn−ブタノール−水混合溶液(10:3、1.3ml)硫酸銅5水和物(14.81mg)、L−アスコルビン酸ナトリウム(70.5mg)を室温で加え、10分撹拌した。その後、テトラブチルアンモニウムフルオリドのテトラヒドロフラン溶液(0.18ml)を加え、室温にて30分撹拌した。反応液を水(15ml)で希釈し、酢酸エチル(20mlx2)で抽出した。得られた有機層を水(15ml)、飽和食塩水(10ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮した。得られた粗成績体をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−60:40)にて精製し、標記化合物(31mg)を黄色油状物として得た。
(R)−4−エチニル−1−メチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
実施例10と同様の方法により、1−メチル−4−(ピリジン−2−イル)−1H−ピラゾール−5−カルボン酸の代わりに前記の<工程2>で得られた化合物(25mg)を用いることで、標記化合物(45mg)を得た。
<工程4>
(R)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾール−5−カルボキサミドの製造
前記の<工程3>で得られた化合物(40mg)、トリメチルシリルアジド(0.03ml)のn−ブタノール−水混合溶液(10:3、1.3ml)硫酸銅5水和物(14.81mg)、L−アスコルビン酸ナトリウム(70.5mg)を室温で加え、10分撹拌した。その後、テトラブチルアンモニウムフルオリドのテトラヒドロフラン溶液(0.18ml)を加え、室温にて30分撹拌した。反応液を水(15ml)で希釈し、酢酸エチル(20mlx2)で抽出した。得られた有機層を水(15ml)、飽和食塩水(10ml)で洗浄し、硫酸ナトリウムで乾燥後、ろ過、濃縮した。得られた粗成績体をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−60:40)にて精製し、標記化合物(31mg)を黄色油状物として得た。
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例35と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例35と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(1−メチル−1H−1,2,3−トリアゾール−4−イル)−1H−ピラゾール−5−カルボキサミドの製造
実施例35と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例35と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
<工程1>
1−メチル−4−(ピリジン−2−イル−1H−1,2,3−トリアゾール−5−カルボン酸の製造
エチル 5−(ピリジン−2−イル)−3−((トリメチルシリル)メチル)−3H−1,2,3−トリアゾール−4−カルボキシレート(CAS番号1374672−88−4)(400mg)のメタノール(5mL)溶液に炭酸カリウム(363mg)を加え、室温で2時間撹拌した。水酸化リチウム一水和物(55mg)と水(1mL)を加え、室温で1時間撹拌した。水(50mL)を加えろ過し、ろ液に1規定塩酸を加えてpH3〜4に調整した。
水層を酢酸エチル(50mL)で2回抽出し、有機層を合わせ、飽和食塩水(100mL)で2回洗浄し、硫酸ナトリウムで乾燥した。有機層をろ過、濃縮し、標記化合物(150mg)を白色固体として得た。
<工程2>
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程1>で得た化合物(30mg)を用いて標記化合物(38mg)を得た。
<工程1>
1−メチル−4−(ピリジン−2−イル−1H−1,2,3−トリアゾール−5−カルボン酸の製造
エチル 5−(ピリジン−2−イル)−3−((トリメチルシリル)メチル)−3H−1,2,3−トリアゾール−4−カルボキシレート(CAS番号1374672−88−4)(400mg)のメタノール(5mL)溶液に炭酸カリウム(363mg)を加え、室温で2時間撹拌した。水酸化リチウム一水和物(55mg)と水(1mL)を加え、室温で1時間撹拌した。水(50mL)を加えろ過し、ろ液に1規定塩酸を加えてpH3〜4に調整した。
水層を酢酸エチル(50mL)で2回抽出し、有機層を合わせ、飽和食塩水(100mL)で2回洗浄し、硫酸ナトリウムで乾燥した。有機層をろ過、濃縮し、標記化合物(150mg)を白色固体として得た。
<工程2>
(R)−1−メチル−4−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程1>で得た化合物(30mg)を用いて標記化合物(38mg)を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−4−(ピリジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例38と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
<工程1>
エチル 3−(ピラジン−2−イル)プロピオレートの製造
臭化亜鉛(2.6g)のテトラヒドロフラン(20ml)溶液にトリエチルアミン(6.5ml)、2−ヨードピラジン(0.95ml),プロピオン酸エチル(1.5ml)とテトラキス(トリフェニルホスフィン)パラジウム(0)(340mg)を加え、室温で18時間撹拌した。反応液をジエチルエーテル(20ml)で希釈し、有機層を飽和塩化アンモニウム水溶液(30ml)、飽和食塩水で順次洗浄し、硫酸ナトリウムで乾燥し、ろ過した。有機層を減圧濃縮し、得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−40:60)で精製し、標記粗化合物(560mg)を橙色油状物として得た。
<工程2>
エチル 4−(ピラジン−2−イル)−1−((トリメチルシリル)メチル)−1H−1,2,3−トリアゾール−5−カルボキシレートの製造
前記の<工程1>で得た化合物(560mg)のトルエン(11ml)溶液にトリメチルシリルメチルアジド(CAS番号87576−94−1)(490mg)を加え、85℃で16時間加熱した。反応液をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−80:20)で精製し、標記化合物(300mg)を黄色油状物として得た。
<工程1>
エチル 3−(ピラジン−2−イル)プロピオレートの製造
臭化亜鉛(2.6g)のテトラヒドロフラン(20ml)溶液にトリエチルアミン(6.5ml)、2−ヨードピラジン(0.95ml),プロピオン酸エチル(1.5ml)とテトラキス(トリフェニルホスフィン)パラジウム(0)(340mg)を加え、室温で18時間撹拌した。反応液をジエチルエーテル(20ml)で希釈し、有機層を飽和塩化アンモニウム水溶液(30ml)、飽和食塩水で順次洗浄し、硫酸ナトリウムで乾燥し、ろ過した。有機層を減圧濃縮し、得られた粗生成物をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−40:60)で精製し、標記粗化合物(560mg)を橙色油状物として得た。
<工程2>
エチル 4−(ピラジン−2−イル)−1−((トリメチルシリル)メチル)−1H−1,2,3−トリアゾール−5−カルボキシレートの製造
前記の<工程1>で得た化合物(560mg)のトルエン(11ml)溶液にトリメチルシリルメチルアジド(CAS番号87576−94−1)(490mg)を加え、85℃で16時間加熱した。反応液をシリカゲルカラムクロマトグラフィー(移動相;ヘプタン:酢酸エチル=90:10−80:20)で精製し、標記化合物(300mg)を黄色油状物として得た。
<工程3>
1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボン酸の製造
前記の<工程2>で得た化合物(250mg)のメタノール(8.2mL)溶液に炭酸カリウム(140mg)を加え、室温で5時間撹拌した。水層を酢酸エチル(10mL)で3回抽出し、有機層を合わせ、飽和食塩水で洗浄し、硫酸ナトリウムで乾燥した。ろ過、濃縮し、標記租化合物(90mg)を褐色固体として得た。
<工程4>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程3>で得た化合物(20mg)を用いて標記化合物(18mg)を得た。
1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボン酸の製造
前記の<工程2>で得た化合物(250mg)のメタノール(8.2mL)溶液に炭酸カリウム(140mg)を加え、室温で5時間撹拌した。水層を酢酸エチル(10mL)で3回抽出し、有機層を合わせ、飽和食塩水で洗浄し、硫酸ナトリウムで乾燥した。ろ過、濃縮し、標記租化合物(90mg)を褐色固体として得た。
<工程4>
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程3>で得た化合物(20mg)を用いて標記化合物(18mg)を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−1−メチル−4−(ピラジン−2−イル)−1H−1,2,3−トリアゾール−5−カルボキサミドの製造
前記の実施例43の<工程3>で得た化合物(20mg)を用いて、実施例1)と同様の方法により標記化合物(18mg)を得た。
前記の実施例43の<工程3>で得た化合物(20mg)を用いて、実施例1)と同様の方法により標記化合物(18mg)を得た。
(R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミドの製造
<工程1>
3−メチル−5−(ピリジン−2−イル)イソキサゾール−4−カルボン酸の製造
5−(5−ブロモ−ピリジン−2−イル)−3−メチル−イソキサゾール−4−カルボン酸(CAS番号1299607−70−7)(400mg)のエタノール溶液(5ml)にパラジウム−炭素(100mg)、トリエチルアミン(0.39ml)を加え、反応容器を水素置換した後、2時間撹拌した。反応液をセライトろ過した後、濃縮することで標記粗化合物(570mg)を褐色固体として得た。
<工程2>
(R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程1>で得た化合物(30mg)を用いて標記化合物(31.7mg)を得た。
<工程1>
3−メチル−5−(ピリジン−2−イル)イソキサゾール−4−カルボン酸の製造
5−(5−ブロモ−ピリジン−2−イル)−3−メチル−イソキサゾール−4−カルボン酸(CAS番号1299607−70−7)(400mg)のエタノール溶液(5ml)にパラジウム−炭素(100mg)、トリエチルアミン(0.39ml)を加え、反応容器を水素置換した後、2時間撹拌した。反応液をセライトろ過した後、濃縮することで標記粗化合物(570mg)を褐色固体として得た。
<工程2>
(R)−3−メチル−5−(ピリジン−2−イル)−N−(1−4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程1>で得た化合物(30mg)を用いて標記化合物(31.7mg)を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−3−メチル−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例45と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
3’,5−ジメチル−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミドの製造
3−メチル−5−(5−メチルイソキサゾール−3−イル)イソキサゾール−4−カルボン酸(CAS番号849066−63−3)(31mg)を用いて、実施例1と同様の方法により標記化合物(28mg)を得た。
3−メチル−5−(5−メチルイソキサゾール−3−イル)イソキサゾール−4−カルボン酸(CAS番号849066−63−3)(31mg)を用いて、実施例1と同様の方法により標記化合物(28mg)を得た。
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミドの製造
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミドの製造
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3’,5−ジメチル−[3,5’−ビイソオキサゾール]−4’−カルボキサミドの製造
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
3’,5−ジメチル−N−(3−(4−(トリフルオロメトキシ)フェニル)オキセタン−3−イル)−[3,5’−ビイソオキサゾール]−4’−カルボキサミドの製造
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例51と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(R)−5−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)イソオキサゾール−4−カルボキサミドの製造
5−ピリジン−2−イルイソキサゾール−4−カルボン酸(CAS番号954230−71−8)(25mg)を用いて、実施例1と同様の方法により標記化合物(24mg)を得た。
5−ピリジン−2−イルイソキサゾール−4−カルボン酸(CAS番号954230−71−8)(25mg)を用いて、実施例1と同様の方法により標記化合物(24mg)を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(2,2−ジフルオロベンゾ[d][1,3]ジオキソル−5−イル)−2−ヒドロキシ−2−メチルプロピル)−5−(ピリジン−2−イル)イソオキサゾール−4−カルボキサミドの製造
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例56と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
1−メチル−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボン酸(CAS番号1152510−81−0)(20mg)を用いて、実施例1と同様の方法により標記化合物(15mg)を得た。
1−メチル−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボン酸(CAS番号1152510−81−0)(20mg)を用いて、実施例1と同様の方法により標記化合物(15mg)を得た。
N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−ヒドロキシ−2−メチルプロピル)−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例62と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
(S)−N−(2−ヒドロキシ−2−メチル−1−(4−(トリフルオロメトキシ)フェニル)プロピル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボン酸(CAS番号1152510−81−0)(25mg)を用いて、実施例1と同様の方法により標記化合物(25mg)を得た。
1−メチル−3−(ピリジン−2−イル)−1H−ピラゾール−4−カルボン酸(CAS番号1152510−81−0)(25mg)を用いて、実施例1と同様の方法により標記化合物(25mg)を得た。
1−メチル−3−(ピリジン−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例68と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例68と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(ピリジン−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例68と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
実施例68と同様の方法もしくは、これに準ずる方法で標記化合物を得た。
1−メチル−3−(チアゾ−ル−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾ−ル−4−カルボキサミドの製造
<工程1>
エチル 1−メチル−3−(チアゾル−2−イル)−1H−ピラゾール−4−カルボキシレートの製造
エチル 3−ヨード−1−メチル−1H−ピラゾール−4−カルボキシレート(235mg)、2−トリブチルスタンニルチアゾール(CAS番号121359−48−6)(314mg)、フッ化セシウム(255mg)、テトラキス(トリフェエニルホスフィン)パラジウム(0)(194mg)のN,N−ジメトルホルムアミド溶液(3ml)を100℃で1。5時間加熱撹拌した。反応液をシリカゲルカラムクロマトグラフィー(移動相;n−ヘキサン:酢酸エチル=80:20−50:50)で精製し、標記粗化合物(150mg)を茶色油状物として得た。
<工程2>
リチウム 1−メチル−3−(チアゾル−2−イル)−1H−ピラゾール−4−カルボキシレートの製造
前記の<工程1>で得られた化合物(150mg)、水酸化リチウム−1水和物(32mg)のメタノール−水混合溶液(4:1、2.5ml)を60度で17時間加熱撹拌した。反応液を濃縮することで、標記粗化合物(164mg)を黄色固体として得た。
<工程3>
1−メチル−3−(チアゾ−ル−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(45mg)を用いて標記化合物(3.0mg)を得た。
<工程1>
エチル 1−メチル−3−(チアゾル−2−イル)−1H−ピラゾール−4−カルボキシレートの製造
エチル 3−ヨード−1−メチル−1H−ピラゾール−4−カルボキシレート(235mg)、2−トリブチルスタンニルチアゾール(CAS番号121359−48−6)(314mg)、フッ化セシウム(255mg)、テトラキス(トリフェエニルホスフィン)パラジウム(0)(194mg)のN,N−ジメトルホルムアミド溶液(3ml)を100℃で1。5時間加熱撹拌した。反応液をシリカゲルカラムクロマトグラフィー(移動相;n−ヘキサン:酢酸エチル=80:20−50:50)で精製し、標記粗化合物(150mg)を茶色油状物として得た。
<工程2>
リチウム 1−メチル−3−(チアゾル−2−イル)−1H−ピラゾール−4−カルボキシレートの製造
前記の<工程1>で得られた化合物(150mg)、水酸化リチウム−1水和物(32mg)のメタノール−水混合溶液(4:1、2.5ml)を60度で17時間加熱撹拌した。反応液を濃縮することで、標記粗化合物(164mg)を黄色固体として得た。
<工程3>
1−メチル−3−(チアゾ−ル−2−イル)−N−(1−(4−(トリフルオロメトキシ)フェニル)エチル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例1と同様の方法により、前記の<工程2>で得た化合物(45mg)を用いて標記化合物(3.0mg)を得た。
N−(1−(3−フルオロ−4−(トリフルオロメトキシ)フェニル)−2−メトキシエチル)−1−メチル−3−(チアゾ−ル−2−イル)−1H−ピラゾ−ル−4−カルボキサミドの製造
実施例7と同様の方法により、前記の実施例71の<工程2>で得た化合物(33mg)を用いて標記化合物(3.2mg)を得た。
実施例7と同様の方法により、前記の実施例71の<工程2>で得た化合物(33mg)を用いて標記化合物(3.2mg)を得た。
前記してきた各実施例で製造した化合物の化学構造式を以下に示す。また、これらの化合物の1H−NMRデータ(無印:400MHz NMR、*印:300MHz NMR。溶媒は表中に記載のとおりである。)を次の表2に示し、LC−Massデータ(各表中のRTはクロマトグラフィーの保持時間(分)を示す。)を以下の表3及び表4に示す。
前記してきた各実施例において製造された新規な中間体化合物の化学構造を次に示す。
なお、これらの中間体化合物については、例えば、(実施例1)<工程1>で得られた化合物を(実施例1−1)のように表記した。
なお、これらの中間体化合物については、例えば、(実施例1)<工程1>で得られた化合物を(実施例1−1)のように表記した。
前記してきた中間体化合物の1H−NMRデータ(無印:400MHz NMR、*印:300MHz NMR。溶媒は表中に記載のとおりである。)を次の表5に示し、LC−Massデータ(各表中のRTはクロマトグラフィーの保持時間(分)を示す。)を以下の表6に示す。
これらの中間体化合物は、本発明の化合物を製造する上で有用な化合物であり、有用な最終化合物を製造する上で有用な中間体化合物である。
本発明の化合物若しくはその塩又はそれらの溶媒和物は、PDE2A阻害活性を有し、それを含有する医薬組成物はPDE2A受容体が関与する各種の疾患の予防及び/又は治療のための医薬として有用であり、産業上の利用可能性を有している。
Claims (10)
- 下記の一般式(I):
[式(I)中、pは、0〜6の整数であり;qは、1〜5の整数であり;
環Qは、ベンゼン環、又は単環式ヘテロアリール環を表わし;
環Aは、窒素原子、硫黄原子、及び酸素原子からなる群から選ばれるヘテロ原子を1〜5個含有する、5〜14員のヘテロアリール環(但し、当該5〜14員のヘテロアリール環は、環Bと結合している炭素原子の隣接位(α位)に必ず窒素原子を有する)を表わし;次の部分構造式(PS−1)で表わされる環B:
は、次の式(PS−1−1):
次の式(PS−1−2):
次の式(PS−1−3):
、又は次の式(PS−1−4):
から選択され);R1は、各々独立して、ハロゲン原子、水酸基、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、又は−CONRARB(−NRARB、および−CONRARAにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)から選ばれる基を表わす)から選らばれる基を表し;R2a及びR2bは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、又はC3〜8シクロアルキル基から選らばれる基を表わし;R2a及びR2bにおけるC1〜6アルキル基は、各々が結合することにより、C3〜8シクロアルキル環を形成してもよく;R2a及びR2bにおけるC1〜6アルキル基は、各々が結合する際に酸素原子を含んで、環状エーテル環を形成してもよく;R2a及びR2bにおける当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、C3〜8シクロアルキル基、又はR3a及びR3bによって形成されるC3〜8シクロアルキル環、及び環状エーテル環は、各々、−OH、ハロゲン原子、−CN、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基から選らばれる基で1〜3個置換されていてもよく(但し、R2a及びR2bが、同時に水素原子を表わすことはない);R3は、各々独立して、水酸基、ハロゲン原子、シアノ基、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、カルボキシ基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、−O−(C3〜8シクロアルキル基)、−C(O)−(C1〜6アルキル基)、−S(O)n−(C1〜6アルキル基)[但し、n=0〜2]、−NRARB、−CONRARB、−SO2NRARB(前記−NRARB、−CONRARA、および−SO2NRARBにおけるRAおよびRBは、各々独立して、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−C(O)−(C1〜6アルキル基)、又は−S(O)2−(C1〜6アルキル基)から選ばれる基を表わす)、又はオキソ基から選らばれる基を表し;環Q上のR3(q=2又はq>2)が隣接位に置換する場合は、当該各R3が結合することにより、3〜8員エーテル環を形成してもよく(但し、結合する各R3の組み合わせは、−O−(C1〜6アルキル基)および(C1〜6アルキル基)、又は−O−(C1〜6アルキル基)および−O−(C1〜6アルキル基)である)、当該3〜8員エーテル環は、ハロゲン原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、−O−(C1〜6アルキル基)、−O−(ハロゲン化C1〜6アルキル基)、及びオキソ基から選らばれる基で1〜3個置換されていてもよい;R4aは、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基から選らばれる基を表わし(R4aにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、又はC3〜8シクロアルキル基から選らばれる基で1〜3個置換されていてもよく);R4bは、水素原子、C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基から選らばれる基を表わし(R4bにおける、当該C1〜6アルキル基、ハロゲン化C1〜6アルキル基、又はC3〜8シクロアルキル基は、−OH、ハロゲン原子、−O−(C1〜6アルキル基)、又はC3〜8シクロアルキル基から選らばれる基で1〜3個置換されていてもよく)]
で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。 - 請求項1に記載の化合物若しくは製薬学的に許容されるその塩、又はそれらの溶媒和物の少なくとも1つ、及び製薬学上許容される担体を含有する医薬組成物。
- さらに他の予防及び/又は治療薬を含有してなる、請求項2に記載の医薬組成物。
- 他の予防及び/又は治療薬と併用して使用される、請求項2に記載の医薬組成物。
- 請求項3又は4に記載の他の予防及び/又は治療薬が、(1)非定型抗精神病薬、(2)定型抗精神病薬、(3)選択的セロトニン再取り込み阻害薬(SSRI)、(4)選択的セロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)、(5)選択的ノルアドレナリン・ドーパミン再取り込み阻害薬(NDRI)、(6)ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA)、(7)セロトニン・ノルアドレナリン・ドパミン三重モノアミン再取り込み阻害剤、(8)双極性障害治療薬、(9)てんかん治療薬、(10)多発性硬化症治療薬、(11)ハンチントン病治療薬、(12)トリアゾロピリジン系抗うつ薬(SARI)、(13)四環系抗うつ薬、(14)三環系抗うつ薬、(15)その他抗うつ薬、(16)α7ニコチン受容体作動薬、(17)α7ニコチン受容体活性調節薬、(18)α7ニコチン受容体部分調節薬、(19)PDE阻害薬、(20)NK2拮抗薬、(21)NK3拮抗薬、(22)ムスカリン型M1アセチルコリン受容体活性調節薬、(23)ムスカリン型M2アセチルコリン受容体活性調節薬、(24)アデノシン受容体調節薬、(25)ムスカリン型M4アセチルコリン受容体活性調節薬、(26)ムスカリン型M5アセチルコリン受容体活性調節薬、(27)アデノシン受容体調節薬、(28)グリシントランスポーター1(GlyT1)阻害薬、(29)グルタミン酸増強薬、(30)NMDA受容体阻害薬]、(31)代謝性グルタミン酸受容体調節薬(mGlu)、(32)抗不安薬((i)ベンゾジアゼピン系抗不安薬、(ii)チエノジアゼピン系抗不安薬、(iii)セロトニン5−HT1A作動薬)、(33)睡眠導入剤((i)ベンゾジアゼピン系睡眠導入剤、(ii)チエノジアゼピン系眠導入剤、(iii)非ベンゾジアゼピン系睡眠導入剤、(iv)メラトニン受容体作動薬)、(v)シクロピロロン系眠導入剤)、(34)βアミロイドワクチン、(35)βアミロイド分解酵素等、(36)脳機能賦活薬、(37)カンナビノイド調節薬、(38)コリンエステラーゼ阻害薬、(39)MAO−B阻害剤、(40)パーキンソン病治療薬((i)ドーパミン受容体作動薬、(ii)モノアミン酸化酵素阻害薬、(iii)抗コリン剤、(iv)COMT阻害剤、(v)筋萎縮性側索硬化症治療薬、(vi)アポトーシス阻害薬、(vii)神経分化・再生促進剤)、(41)糖尿病治療薬((i)PPARγ作用薬(作動薬、阻害薬)、(ii)インスリン分泌促進薬、(iii)速効型インスリン分泌促進剤、(iv)αグルコシダーゼ阻害薬、(v)インスリン抵抗性改善薬、(vi)肝糖新生抑制剤、(vii)ビグアナイド剤、(viii)インスリンまたはインスリン誘導体、(ix)α2拮抗薬)、(42)抗肥満薬((i)アドレナリンβ3受容体作動薬、(ii)CB−1受容体拮抗薬、(iii)ニューロペプチドY(NPY)受容体拮抗薬、(iv)摂食抑制薬、(v)リパーゼ阻害薬、(vi)ペプチドYY(PYY)受容体拮抗薬、(vii)毛様体神経栄養因子および誘導体)、(43)コレステロール低下薬等の高脂血症治療薬((i)ω3脂肪酸類、(ii)HMG−CoA還元酵素阻害剤、(iii)HMG−CoA合成酵素阻害剤、(iv)コレステロール吸収阻害剤、(v)アシル−CoA・コレステロールアシル転移酵素(ACAT)阻害剤、(vi)CETP阻害剤、(vii)スクアレン合成酵素阻害剤、(viii)抗酸化剤、(ix)PPARα作動薬、(x)PPARδ作動薬、(xi)LXR作動薬、(xii)FXR作動薬、(xiii)MTTP阻害剤、(xiv)スクアレンエポシダーゼ阻害剤等)、(44)降圧剤((i)利尿剤、(ii)カルシウム受容体拮抗薬、(iii)アンジオテンシン変換酵素阻害薬(ACEI)、(iv)アンジオテンシン受容体拮抗薬(ARB)、(v)直接的レニン阻害薬、(vi)α受容体遮断薬、(vii)β受容体遮断薬、(viii)α1β遮断薬、(ix)α2受容体刺激薬)、(45)非ステロイド性抗炎症薬、(46)疾患修飾性抗リウマチ薬(DMARDs)、(47)抗サイトカイン薬、(48)ステロイド薬、(49)性ホルモンまたはその誘導体及び(50)副甲状腺ホルモン(PTH)からなる群より選択される薬剤の1種以上である、請求項3又は4に記載の医薬組成物。
- 請求項1に記載の化合物若しくは製薬学的に許容されるその塩又はそれらの溶媒和物の少なくとも1つを有効成分として含有する、PDE2Aが関与する疾患の予防及び/又は治療剤。
- さらに他の予防及び/又は治療薬を含有してなる、請求項6に記載の予防及び/又は治療剤。
- 他の予防及び/又は治療薬と併用して使用される、請求項6に記載の予防及び/又は治療剤。
- 請求項7又は8に記載の他の予防及び/又は治療薬が、(1)非定型抗精神病薬、(2)定型抗精神病薬、(3)選択的セロトニン再取り込み阻害薬(SSRI)、(4)選択的セロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)、(5)選択的ノルアドレナリン・ドーパミン再取り込み阻害薬(NDRI)、(6)ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA)、(7)セロトニン・ノルアドレナリン・ドパミン三重モノアミン再取り込み阻害剤、(8)双極性障害治療薬、(9)てんかん治療薬、(10)多発性硬化症治療薬、(11)ハンチントン病治療薬、(12)トリアゾロピリジン系抗うつ薬(SARI)、(13)四環系抗うつ薬、(14)三環系抗うつ薬、(15)その他抗うつ薬、(16)α7ニコチン受容体作動薬、(17)α7ニコチン受容体活性調節薬、(18)α7ニコチン受容体部分調節薬、(19)PDE阻害薬、(20)NK2拮抗薬、(21)NK3拮抗薬、(22)ムスカリン型M1アセチルコリン受容体活性調節薬、(23)ムスカリン型M2アセチルコリン受容体活性調節薬、(24)アデノシン受容体調節薬、(25)ムスカリン型M4アセチルコリン受容体活性調節薬、(26)ムスカリン型M5アセチルコリン受容体活性調節薬、(27)アデノシン受容体調節薬、(28)グリシントランスポーター1(GlyT1)阻害薬、(29)グルタミン酸増強薬、(30)NMDA受容体阻害薬]、(31)代謝性グルタミン酸受容体調節薬(mGlu)、(32)抗不安薬((i)ベンゾジアゼピン系抗不安薬、(ii)チエノジアゼピン系抗不安薬、(iii)セロトニン5−HT1A作動薬)、(33)睡眠導入剤((i)ベンゾジアゼピン系睡眠導入剤、(ii)チエノジアゼピン系眠導入剤、(iii)非ベンゾジアゼピン系睡眠導入剤、(iv)メラトニン受容体作動薬)、(v)シクロピロロン系眠導入剤)、(34)βアミロイドワクチン、(35)βアミロイド分解酵素等、(36)脳機能賦活薬、(37)カンナビノイド調節薬、(38)コリンエステラーゼ阻害薬、(39)MAO−B阻害剤、(40)パーキンソン病治療薬((i)ドーパミン受容体作動薬、(ii)モノアミン酸化酵素阻害薬、(iii)抗コリン剤、(iv)COMT阻害剤、(v)筋萎縮性側索硬化症治療薬、(vi)アポトーシス阻害薬、(vii)神経分化・再生促進剤)、(41)糖尿病治療薬((i)PPARγ作用薬(作動薬、阻害薬)、(ii)インスリン分泌促進薬、(iii)速効型インスリン分泌促進剤、(iv)αグルコシダーゼ阻害薬、(v)インスリン抵抗性改善薬、(vi)肝糖新生抑制剤、(vii)ビグアナイド剤、(viii)インスリンまたはインスリン誘導体、(ix)α2拮抗薬)、(42)抗肥満薬((i)アドレナリンβ3受容体作動薬、(ii)CB−1受容体拮抗薬、(iii)ニューロペプチドY(NPY)受容体拮抗薬、(iv)摂食抑制薬、(v)リパーゼ阻害薬、(vi)ペプチドYY(PYY)受容体拮抗薬、(vii)毛様体神経栄養因子および誘導体)、(43)コレステロール低下薬等の高脂血症治療薬((i)ω3脂肪酸類、(ii)HMG−CoA還元酵素阻害剤、(iii)HMG−CoA合成酵素阻害剤、(iv)コレステロール吸収阻害剤、(v)アシル−CoA・コレステロールアシル転移酵素(ACAT)阻害剤、(vi)CETP阻害剤、(vii)スクアレン合成酵素阻害剤、(viii)抗酸化剤、(ix)PPARα作動薬、(x)PPARδ作動薬、(xi)LXR作動薬、(xii)FXR作動薬、(xiii)MTTP阻害剤、(xiv)スクアレンエポシダーゼ阻害剤等)、(44)降圧剤((i)利尿剤、(ii)カルシウム受容体拮抗薬、(iii)アンジオテンシン変換酵素阻害薬(ACEI)、(iv)アンジオテンシン受容体拮抗薬(ARB)、(v)直接的レニン阻害薬、(vi)α受容体遮断薬、(vii)β受容体遮断薬、(viii)α1β遮断薬、(ix)α2受容体刺激薬)、(45)非ステロイド性抗炎症薬、(46)疾患修飾性抗リウマチ薬(DMARDs)、(47)抗サイトカイン薬、(48)ステロイド薬、(49)性ホルモンまたはその誘導体及び(50)副甲状腺ホルモン(PTH)からなる群より選択される薬剤の1種以上である、請求項6又は7に記載の予防及び/又は治療剤。
- 請求項1に記載の化合物若しくは製薬学的に許容されるその塩又はそれらの溶媒和物の1つ以上を含有してなるPDE2A阻害剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015226136A JP2017095366A (ja) | 2015-11-18 | 2015-11-18 | 新規ビアリールアミド誘導体 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015226136A JP2017095366A (ja) | 2015-11-18 | 2015-11-18 | 新規ビアリールアミド誘導体 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017095366A true JP2017095366A (ja) | 2017-06-01 |
Family
ID=58803685
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015226136A Pending JP2017095366A (ja) | 2015-11-18 | 2015-11-18 | 新規ビアリールアミド誘導体 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2017095366A (ja) |
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018534279A (ja) * | 2015-10-13 | 2018-11-22 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | ピラゾロ[1,5−a]ピリミジン−3−カルボキシアミドの環状エーテル誘導体 |
| WO2019126099A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Isoxazole n-linked carbamoyl cyclohexyl acids as lpa antagonists |
| WO2019126086A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Cyclohexyl acid isoxazole azines as lpa antagonists |
| WO2019126087A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Cyclohexyl acid isoxazole azoles as lpa antagonists |
| WO2019133770A3 (en) * | 2017-12-29 | 2019-08-15 | Biomarin Pharmaceutical Inc. | Glycolate oxidase inhibitors for the treatment of disease |
| WO2019161877A1 (en) | 2018-02-20 | 2019-08-29 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers |
| WO2020060915A1 (en) | 2018-09-18 | 2020-03-26 | Bristol-Myers Squibb Company | Cyclopentyl acids as lpa antagonists |
| WO2020257139A1 (en) | 2019-06-18 | 2020-12-24 | Bristol-Myers Squibb Company | Cyclobutyl carboxylic acids as lpa antagonists |
| WO2021023617A1 (en) | 2019-08-02 | 2021-02-11 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers |
| WO2021023616A1 (en) | 2019-08-02 | 2021-02-11 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers for use in epilepsy or seizures |
| US11434199B2 (en) | 2018-02-20 | 2022-09-06 | H. Lundbeck A/S | Alcohol derivatives as KV7 potassium channel openers |
| US11548849B2 (en) | 2019-08-02 | 2023-01-10 | H. Lundbeck A/S | Alcohol derivatives as KV7 potassium channel openers |
| RU2805308C2 (ru) * | 2017-12-29 | 2023-10-13 | Байомарин Фармасьютикал Инк. | Ингибиторы гликолатоксидазы для лечения заболеваний |
-
2015
- 2015-11-18 JP JP2015226136A patent/JP2017095366A/ja active Pending
Cited By (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10875867B2 (en) | 2015-10-13 | 2020-12-29 | Boehringer Ingelheim International Gmbh | Cyclic ether derivatives of pyrazolo[1,5-a]pyrimidine-3-carboxyamide |
| US12351584B2 (en) | 2015-10-13 | 2025-07-08 | Boehringer Ingelheim International Gmbh | Cyclic ether derivatives of pyrazolo[1,5-a]pyrimidine-3-carboxyamide |
| US11691977B2 (en) | 2015-10-13 | 2023-07-04 | Boehringer Ingelheim International Gmbh | Cyclic ether derivatives of pyrazolo[1,5-A]pyrimidine-3-carboxyamide |
| US10479794B2 (en) | 2015-10-13 | 2019-11-19 | Boehringer Ingelheim International Gmbh | Cyclic ether derivatives of pyrazolo[1,5-a]pyrimidine-3-carboxyamide |
| JP2018534279A (ja) * | 2015-10-13 | 2018-11-22 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | ピラゾロ[1,5−a]ピリミジン−3−カルボキシアミドの環状エーテル誘導体 |
| WO2019126099A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Isoxazole n-linked carbamoyl cyclohexyl acids as lpa antagonists |
| WO2019126086A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Cyclohexyl acid isoxazole azines as lpa antagonists |
| WO2019126087A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Cyclohexyl acid isoxazole azoles as lpa antagonists |
| JP2021509401A (ja) * | 2017-12-29 | 2021-03-25 | ビオマリン プハルマセウトイカル インコーポレイテッド | 疾患の治療のためのグルコール酸オキシダーゼ阻害剤 |
| WO2019133770A3 (en) * | 2017-12-29 | 2019-08-15 | Biomarin Pharmaceutical Inc. | Glycolate oxidase inhibitors for the treatment of disease |
| RU2805308C2 (ru) * | 2017-12-29 | 2023-10-13 | Байомарин Фармасьютикал Инк. | Ингибиторы гликолатоксидазы для лечения заболеваний |
| US11384055B2 (en) | 2017-12-29 | 2022-07-12 | Biomarin Pharmaceutical Inc. | Glycolate oxidase inhibitors for the treatment of disease |
| JP7344878B2 (ja) | 2017-12-29 | 2023-09-14 | ビオマリン プハルマセウトイカル インコーポレイテッド | 疾患の治療のためのグルコール酸オキシダーゼ阻害剤 |
| EP4241843A2 (en) | 2018-02-20 | 2023-09-13 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers |
| US12258305B2 (en) | 2018-02-20 | 2025-03-25 | H. Lundbeck A/S | Alcohol derivatives as Kv7 potassium channel openers |
| US11434199B2 (en) | 2018-02-20 | 2022-09-06 | H. Lundbeck A/S | Alcohol derivatives as KV7 potassium channel openers |
| WO2019161877A1 (en) | 2018-02-20 | 2019-08-29 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers |
| WO2020060915A1 (en) | 2018-09-18 | 2020-03-26 | Bristol-Myers Squibb Company | Cyclopentyl acids as lpa antagonists |
| WO2020257139A1 (en) | 2019-06-18 | 2020-12-24 | Bristol-Myers Squibb Company | Cyclobutyl carboxylic acids as lpa antagonists |
| US11548849B2 (en) | 2019-08-02 | 2023-01-10 | H. Lundbeck A/S | Alcohol derivatives as KV7 potassium channel openers |
| EP4461725A2 (en) | 2019-08-02 | 2024-11-13 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers |
| WO2021023616A1 (en) | 2019-08-02 | 2021-02-11 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers for use in epilepsy or seizures |
| WO2021023617A1 (en) | 2019-08-02 | 2021-02-11 | H. Lundbeck A/S | Alcohol derivatives as kv7 potassium channel openers |
| US12508239B2 (en) | 2019-08-02 | 2025-12-30 | H. Lundbeck A/S | Alcohol derivatives as Kv7 potassium channel openers for use in epilepsy or seizures |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7033764B2 (ja) | Cdk阻害剤としての置換型ヘテロシクリル誘導体 | |
| JP2017095366A (ja) | 新規ビアリールアミド誘導体 | |
| EP2963037B1 (en) | Novel pyrazole derivative | |
| CA2785923C (en) | Therapeutic compounds and related methods of use | |
| JP6466335B2 (ja) | ROR−γ−Tのメチレン連結キノリニルモジュレーター | |
| JP5641664B2 (ja) | イミダゾ[1,2−b]ピリダジン誘導体およびPDE10阻害剤としてのそれらの使用 | |
| JP6662846B2 (ja) | 6,7−ジヒドロピラゾロ[1,5−a]ピラジン−4(5H)−オン化合物およびMGLUR2受容体の負のアロステリック調節因子としてのそれらの使用 | |
| CN106795165B (zh) | 咪唑并哒嗪化合物 | |
| CN107614499A (zh) | 吡啶并[3,4‑d]嘧啶衍生物及其药学上可允许的盐 | |
| JP6689856B2 (ja) | 6,7−ジヒドロピラゾロ[1,5−a]ピラジン−4(5H)−オン化合物およびMGLUR2受容体の負のアロステリック調節因子としてのそれらの使用 | |
| CN104302634A (zh) | 用于抑制abl1、abl2和bcr-abl1的活性的苯甲酰胺衍生物 | |
| CN107141309A (zh) | 杂芳基化合物及其使用方法 | |
| WO2016084866A1 (ja) | 新規ジアザビシクロ誘導体 | |
| TW201302730A (zh) | 吡唑化合物 | |
| CN105121439A (zh) | 作为pde4亚型抑制剂用于治疗cns和其他病症的氮杂苯并咪唑化合物 | |
| JP6786566B2 (ja) | ヘテロアリール化合物及びその使用方法 | |
| WO2016088813A1 (ja) | 新規ジアザビシクロ[2.2.2]オクタン誘導体 | |
| JP2021528398A (ja) | RORγTのモジュレーターとしての6−アミノピリジン−3−イルピラゾール | |
| US20190177327A1 (en) | Substituted methyl pyrazolopyrimidinone and methyl imidazopyrazinone compounds as pde1 inhibitors | |
| JP6977038B2 (ja) | Gsk−3阻害剤 | |
| US10981916B2 (en) | Substituted pyrazolopyrimidinone compounds as PDE2 inhibitors | |
| JP6745594B2 (ja) | ピラゾール誘導体の塩の結晶 | |
| US20240190824A1 (en) | Inhibitors of trek (twik related k+ channels) channel function | |
| JP2017206566A (ja) | イオンチャネルモジュレーターとしての縮合複素環式化合物 | |
| JP2017075116A (ja) | 新規縮合複素環化合物 |