JP2016502995A - 鼻腔内予防接種投薬レジメン - Google Patents
鼻腔内予防接種投薬レジメン Download PDFInfo
- Publication number
- JP2016502995A JP2016502995A JP2015547071A JP2015547071A JP2016502995A JP 2016502995 A JP2016502995 A JP 2016502995A JP 2015547071 A JP2015547071 A JP 2015547071A JP 2015547071 A JP2015547071 A JP 2015547071A JP 2016502995 A JP2016502995 A JP 2016502995A
- Authority
- JP
- Japan
- Prior art keywords
- vaccine
- vaccine composition
- antigens
- containers
- intranasal administration
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 238000002255 vaccination Methods 0.000 title claims abstract description 65
- 229960005486 vaccine Drugs 0.000 claims abstract description 562
- 239000000203 mixture Substances 0.000 claims abstract description 544
- 229940124856 vaccine component Drugs 0.000 claims abstract description 86
- 230000003053 immunization Effects 0.000 claims abstract description 60
- 238000002649 immunization Methods 0.000 claims abstract description 53
- 238000004519 manufacturing process Methods 0.000 claims abstract description 6
- 239000000427 antigen Substances 0.000 claims description 289
- 102000036639 antigens Human genes 0.000 claims description 289
- 108091007433 antigens Proteins 0.000 claims description 289
- 230000028993 immune response Effects 0.000 claims description 109
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims description 83
- 235000014113 dietary fatty acids Nutrition 0.000 claims description 62
- 239000000194 fatty acid Substances 0.000 claims description 62
- 229930195729 fatty acid Natural products 0.000 claims description 62
- 150000004665 fatty acids Chemical class 0.000 claims description 62
- 241000700605 Viruses Species 0.000 claims description 60
- 238000000034 method Methods 0.000 claims description 54
- 239000002671 adjuvant Substances 0.000 claims description 48
- 241000342334 Human metapneumovirus Species 0.000 claims description 32
- 206010013023 diphtheria Diseases 0.000 claims description 32
- 241000894006 Bacteria Species 0.000 claims description 31
- 238000007911 parenteral administration Methods 0.000 claims description 28
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 claims description 20
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 claims description 20
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 claims description 20
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 claims description 20
- 239000005642 Oleic acid Substances 0.000 claims description 20
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 claims description 20
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 claims description 20
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 claims description 20
- RZRNAYUHWVFMIP-KTKRTIGZSA-N 1-oleoylglycerol Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(O)CO RZRNAYUHWVFMIP-KTKRTIGZSA-N 0.000 claims description 18
- RZRNAYUHWVFMIP-HXUWFJFHSA-N glycerol monolinoleate Natural products CCCCCCCCC=CCCCCCCCC(=O)OC[C@H](O)CO RZRNAYUHWVFMIP-HXUWFJFHSA-N 0.000 claims description 18
- 208000037797 influenza A Diseases 0.000 claims description 18
- 201000006082 Chickenpox Diseases 0.000 claims description 17
- 241001263478 Norovirus Species 0.000 claims description 17
- 201000005702 Pertussis Diseases 0.000 claims description 17
- 208000000474 Poliomyelitis Diseases 0.000 claims description 17
- 206010043376 Tetanus Diseases 0.000 claims description 17
- 206010046980 Varicella Diseases 0.000 claims description 17
- 208000037798 influenza B Diseases 0.000 claims description 17
- 201000008827 tuberculosis Diseases 0.000 claims description 17
- 241000193738 Bacillus anthracis Species 0.000 claims description 16
- 241000588832 Bordetella pertussis Species 0.000 claims description 16
- 206010008342 Cervix carcinoma Diseases 0.000 claims description 16
- 241000711573 Coronaviridae Species 0.000 claims description 16
- 241000701022 Cytomegalovirus Species 0.000 claims description 16
- 241000709661 Enterovirus Species 0.000 claims description 16
- 241000588724 Escherichia coli Species 0.000 claims description 16
- 208000009889 Herpes Simplex Diseases 0.000 claims description 16
- 208000007514 Herpes zoster Diseases 0.000 claims description 16
- 201000005505 Measles Diseases 0.000 claims description 16
- 208000005647 Mumps Diseases 0.000 claims description 16
- 241000588652 Neisseria gonorrhoeae Species 0.000 claims description 16
- 241000150452 Orthohantavirus Species 0.000 claims description 16
- 208000002606 Paramyxoviridae Infections Diseases 0.000 claims description 16
- 241000589517 Pseudomonas aeruginosa Species 0.000 claims description 16
- 241000702670 Rotavirus Species 0.000 claims description 16
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 claims description 16
- 201000010881 cervical cancer Diseases 0.000 claims description 16
- 239000004615 ingredient Substances 0.000 claims description 16
- 208000010805 mumps infectious disease Diseases 0.000 claims description 16
- 201000005404 rubella Diseases 0.000 claims description 16
- 241000606768 Haemophilus influenzae Species 0.000 claims description 15
- 241000187479 Mycobacterium tuberculosis Species 0.000 claims description 15
- 229940065181 bacillus anthracis Drugs 0.000 claims description 15
- 241000606161 Chlamydia Species 0.000 claims description 14
- 241000194017 Streptococcus Species 0.000 claims description 14
- 208000005252 hepatitis A Diseases 0.000 claims description 14
- 201000001371 inclusion conjunctivitis Diseases 0.000 claims description 14
- 206010044325 trachoma Diseases 0.000 claims description 14
- 206010020751 Hypersensitivity Diseases 0.000 claims description 12
- 230000007815 allergy Effects 0.000 claims description 12
- 241000282412 Homo Species 0.000 claims description 11
- 230000004044 response Effects 0.000 claims description 11
- 208000006877 Insect Bites and Stings Diseases 0.000 claims description 10
- 241001465754 Metazoa Species 0.000 claims description 10
- 239000013566 allergen Substances 0.000 claims description 10
- 229960004784 allergens Drugs 0.000 claims description 10
- 239000002537 cosmetic Substances 0.000 claims description 10
- 230000007613 environmental effect Effects 0.000 claims description 10
- 235000013305 food Nutrition 0.000 claims description 10
- 239000004816 latex Substances 0.000 claims description 10
- 229920000126 latex Polymers 0.000 claims description 10
- 229910052759 nickel Inorganic materials 0.000 claims description 10
- 150000002194 fatty esters Chemical class 0.000 claims description 8
- 241000238711 Pyroglyphidae Species 0.000 claims description 5
- 229940046533 house dust mites Drugs 0.000 claims description 5
- 241000606153 Chlamydia trachomatis Species 0.000 claims description 2
- 229940038705 chlamydia trachomatis Drugs 0.000 claims description 2
- 241000580858 Simian-Human immunodeficiency virus Species 0.000 claims 7
- 206010022000 influenza Diseases 0.000 description 31
- 235000011187 glycerol Nutrition 0.000 description 25
- 229960005150 glycerol Drugs 0.000 description 25
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 18
- 201000010099 disease Diseases 0.000 description 17
- 241000701806 Human papillomavirus Species 0.000 description 11
- 210000000987 immune system Anatomy 0.000 description 11
- 229960003971 influenza vaccine Drugs 0.000 description 11
- 241000725303 Human immunodeficiency virus Species 0.000 description 10
- 241000725643 Respiratory syncytial virus Species 0.000 description 10
- 201000003176 Severe Acute Respiratory Syndrome Diseases 0.000 description 10
- 210000002966 serum Anatomy 0.000 description 9
- 125000004432 carbon atom Chemical group C* 0.000 description 8
- 210000002850 nasal mucosa Anatomy 0.000 description 8
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 7
- 229940047650 haemophilus influenzae Drugs 0.000 description 7
- 230000002265 prevention Effects 0.000 description 7
- WWZKQHOCKIZLMA-UHFFFAOYSA-N Caprylic acid Natural products CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 6
- -1 alkynyl carboxylic acids Chemical class 0.000 description 6
- 230000008901 benefit Effects 0.000 description 6
- 238000002347 injection Methods 0.000 description 6
- 239000007924 injection Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 229940124590 live attenuated vaccine Drugs 0.000 description 5
- 229940023012 live-attenuated vaccine Drugs 0.000 description 5
- 210000001331 nose Anatomy 0.000 description 5
- 230000037452 priming Effects 0.000 description 5
- 125000003342 alkenyl group Chemical group 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- MBMBGCFOFBJSGT-KUBAVDMBSA-N all-cis-docosa-4,7,10,13,16,19-hexaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCC(O)=O MBMBGCFOFBJSGT-KUBAVDMBSA-N 0.000 description 4
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 4
- 230000003466 anti-cipated effect Effects 0.000 description 4
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 4
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 4
- UKMSUNONTOPOIO-UHFFFAOYSA-N docosanoic acid Chemical compound CCCCCCCCCCCCCCCCCCCCCC(O)=O UKMSUNONTOPOIO-UHFFFAOYSA-N 0.000 description 4
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 4
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 4
- VKOBVWXKNCXXDE-UHFFFAOYSA-N icosanoic acid Chemical compound CCCCCCCCCCCCCCCCCCCC(O)=O VKOBVWXKNCXXDE-UHFFFAOYSA-N 0.000 description 4
- 229940031551 inactivated vaccine Drugs 0.000 description 4
- SECPZKHBENQXJG-FPLPWBNLSA-N palmitoleic acid Chemical compound CCCCCC\C=C/CCCCCCCC(O)=O SECPZKHBENQXJG-FPLPWBNLSA-N 0.000 description 4
- 239000004094 surface-active agent Substances 0.000 description 4
- LDVVTQMJQSCDMK-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl formate Chemical compound OCC(CO)OC=O LDVVTQMJQSCDMK-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 125000002015 acyclic group Chemical group 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 235000006708 antioxidants Nutrition 0.000 description 3
- 230000001580 bacterial effect Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 229960004279 formaldehyde Drugs 0.000 description 3
- VZCCETWTMQHEPK-QNEBEIHSSA-N gamma-linolenic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/CCCCC(O)=O VZCCETWTMQHEPK-QNEBEIHSSA-N 0.000 description 3
- 235000020664 gamma-linolenic acid Nutrition 0.000 description 3
- 230000036039 immunity Effects 0.000 description 3
- 230000002163 immunogen Effects 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 210000004877 mucosa Anatomy 0.000 description 3
- 229920001983 poloxamer Polymers 0.000 description 3
- 235000018102 proteins Nutrition 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 230000001932 seasonal effect Effects 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 230000003612 virological effect Effects 0.000 description 3
- GWHCXVQVJPWHRF-KTKRTIGZSA-N (15Z)-tetracosenoic acid Chemical compound CCCCCCCC\C=C/CCCCCCCCCCCCCC(O)=O GWHCXVQVJPWHRF-KTKRTIGZSA-N 0.000 description 2
- DRHZYJAUECRAJM-DWSYSWFDSA-N (2s,3s,4s,5r,6r)-6-[[(3s,4s,4ar,6ar,6bs,8r,8ar,12as,14ar,14br)-8a-[(2s,3r,4s,5r,6r)-3-[(2s,3r,4s,5r,6s)-5-[(2s,3r,4s,5r)-4-[(2s,3r,4r)-3,4-dihydroxy-4-(hydroxymethyl)oxolan-2-yl]oxy-3,5-dihydroxyoxan-2-yl]oxy-3,4-dihydroxy-6-methyloxan-2-yl]oxy-5-[(3s,5s, Chemical compound O([C@H]1[C@H](O)[C@H](O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O1)O)O[C@H]1CC[C@]2(C)[C@H]3CC=C4[C@@H]5CC(C)(C)CC[C@@]5([C@@H](C[C@@]4(C)[C@]3(C)CC[C@H]2[C@@]1(C=O)C)O)C(=O)O[C@@H]1O[C@H](C)[C@@H]([C@@H]([C@H]1O[C@H]1[C@@H]([C@H](O)[C@@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@](O)(CO)CO3)O)[C@H](O)CO2)O)[C@H](C)O1)O)O)OC(=O)C[C@@H](O)C[C@H](OC(=O)C[C@@H](O)C[C@@H]([C@@H](C)CC)O[C@H]1[C@@H]([C@@H](O)[C@H](CO)O1)O)[C@@H](C)CC)C(O)=O)[C@@H]1OC[C@@H](O)[C@H](O)[C@H]1O DRHZYJAUECRAJM-DWSYSWFDSA-N 0.000 description 2
- HOBAELRKJCKHQD-UHFFFAOYSA-N (8Z,11Z,14Z)-8,11,14-eicosatrienoic acid Natural products CCCCCC=CCC=CCC=CCCCCCCC(O)=O HOBAELRKJCKHQD-UHFFFAOYSA-N 0.000 description 2
- TWJNQYPJQDRXPH-UHFFFAOYSA-N 2-cyanobenzohydrazide Chemical compound NNC(=O)C1=CC=CC=C1C#N TWJNQYPJQDRXPH-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 235000021357 Behenic acid Nutrition 0.000 description 2
- DPUOLQHDNGRHBS-UHFFFAOYSA-N Brassidinsaeure Natural products CCCCCCCCC=CCCCCCCCCCCCC(O)=O DPUOLQHDNGRHBS-UHFFFAOYSA-N 0.000 description 2
- 239000005635 Caprylic acid (CAS 124-07-2) Substances 0.000 description 2
- 102000009016 Cholera Toxin Human genes 0.000 description 2
- 108010049048 Cholera Toxin Proteins 0.000 description 2
- 235000021298 Dihomo-γ-linolenic acid Nutrition 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- URXZXNYJPAJJOQ-UHFFFAOYSA-N Erucic acid Natural products CCCCCCC=CCCCCCCCCCCCC(O)=O URXZXNYJPAJJOQ-UHFFFAOYSA-N 0.000 description 2
- OPGOLNDOMSBSCW-CLNHMMGSSA-N Fursultiamine hydrochloride Chemical compound Cl.C1CCOC1CSSC(\CCO)=C(/C)N(C=O)CC1=CN=C(C)N=C1N OPGOLNDOMSBSCW-CLNHMMGSSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 239000005639 Lauric acid Substances 0.000 description 2
- 235000021353 Lignoceric acid Nutrition 0.000 description 2
- CQXMAMUUWHYSIY-UHFFFAOYSA-N Lignoceric acid Natural products CCCCCCCCCCCCCCCCCCCCCCCC(=O)OCCC1=CC=C(O)C=C1 CQXMAMUUWHYSIY-UHFFFAOYSA-N 0.000 description 2
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 235000021360 Myristic acid Nutrition 0.000 description 2
- TUNFSRHWOTWDNC-UHFFFAOYSA-N Myristic acid Natural products CCCCCCCCCCCCCC(O)=O TUNFSRHWOTWDNC-UHFFFAOYSA-N 0.000 description 2
- XJXROGWVRIJYMO-SJDLZYGOSA-N Nervonic acid Natural products O=C(O)[C@@H](/C=C/CCCCCCCC)CCCCCCCCCCCC XJXROGWVRIJYMO-SJDLZYGOSA-N 0.000 description 2
- 235000021314 Palmitic acid Nutrition 0.000 description 2
- 235000021319 Palmitoleic acid Nutrition 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- FHICGHSMIPIAPL-HDYAAECPSA-N [2-[3-[6-[3-[(5R,6aS,6bR,12aR)-10-[6-[2-[2-[4,5-dihydroxy-3-(3,4,5-trihydroxyoxan-2-yl)oxyoxan-2-yl]ethoxy]ethyl]-3,4,5-trihydroxyoxan-2-yl]oxy-5-hydroxy-2,2,6a,6b,9,9,12a-heptamethyl-1,3,4,5,6,6a,7,8,8a,10,11,12,13,14b-tetradecahydropicene-4a-carbonyl]peroxypropyl]-5-[[5-[8-[3,5-dihydroxy-4-(3,4,5-trihydroxyoxan-2-yl)oxyoxan-2-yl]octoxy]-3,4-dihydroxy-6-methyloxan-2-yl]methoxy]-3,4-dihydroxyoxan-2-yl]propoxymethyl]-5-hydroxy-3-[(6S)-6-hydroxy-2,6-dimethylocta-2,7-dienoyl]oxy-6-methyloxan-4-yl] (2E,6S)-6-hydroxy-2-(hydroxymethyl)-6-methylocta-2,7-dienoate Chemical compound C=C[C@@](C)(O)CCC=C(C)C(=O)OC1C(OC(=O)C(\CO)=C\CC[C@](C)(O)C=C)C(O)C(C)OC1COCCCC1C(O)C(O)C(OCC2C(C(O)C(OCCCCCCCCC3C(C(OC4C(C(O)C(O)CO4)O)C(O)CO3)O)C(C)O2)O)C(CCCOOC(=O)C23C(CC(C)(C)CC2)C=2[C@@]([C@]4(C)CCC5C(C)(C)C(OC6C(C(O)C(O)C(CCOCCC7C(C(O)C(O)CO7)OC7C(C(O)C(O)CO7)O)O6)O)CC[C@]5(C)C4CC=2)(C)C[C@H]3O)O1 FHICGHSMIPIAPL-HDYAAECPSA-N 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- JAZBEHYOTPTENJ-JLNKQSITSA-N all-cis-5,8,11,14,17-icosapentaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O JAZBEHYOTPTENJ-JLNKQSITSA-N 0.000 description 2
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 2
- 239000002518 antifoaming agent Substances 0.000 description 2
- 230000003078 antioxidant effect Effects 0.000 description 2
- 235000021342 arachidonic acid Nutrition 0.000 description 2
- 229940114079 arachidonic acid Drugs 0.000 description 2
- OGBUMNBNEWYMNJ-UHFFFAOYSA-N batilol Chemical class CCCCCCCCCCCCCCCCCCOCC(O)CO OGBUMNBNEWYMNJ-UHFFFAOYSA-N 0.000 description 2
- 229940116226 behenic acid Drugs 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- GONOPSZTUGRENK-UHFFFAOYSA-N benzyl(trichloro)silane Chemical compound Cl[Si](Cl)(Cl)CC1=CC=CC=C1 GONOPSZTUGRENK-UHFFFAOYSA-N 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 230000003139 buffering effect Effects 0.000 description 2
- 239000002738 chelating agent Substances 0.000 description 2
- SECPZKHBENQXJG-UHFFFAOYSA-N cis-palmitoleic acid Natural products CCCCCCC=CCCCCCCCC(O)=O SECPZKHBENQXJG-UHFFFAOYSA-N 0.000 description 2
- GWHCXVQVJPWHRF-UHFFFAOYSA-N cis-tetracosenoic acid Natural products CCCCCCCCC=CCCCCCCCCCCCCCC(O)=O GWHCXVQVJPWHRF-UHFFFAOYSA-N 0.000 description 2
- HABLENUWIZGESP-UHFFFAOYSA-N decanoic acid Chemical compound CCCCCCCCCC(O)=O.CCCCCCCCCC(O)=O HABLENUWIZGESP-UHFFFAOYSA-N 0.000 description 2
- HOBAELRKJCKHQD-QNEBEIHSSA-N dihomo-γ-linolenic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/CCCCCCC(O)=O HOBAELRKJCKHQD-QNEBEIHSSA-N 0.000 description 2
- 235000020669 docosahexaenoic acid Nutrition 0.000 description 2
- 229940090949 docosahexaenoic acid Drugs 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 235000020673 eicosapentaenoic acid Nutrition 0.000 description 2
- 229960005135 eicosapentaenoic acid Drugs 0.000 description 2
- JAZBEHYOTPTENJ-UHFFFAOYSA-N eicosapentaenoic acid Natural products CCC=CCC=CCC=CCC=CCC=CCCCC(O)=O JAZBEHYOTPTENJ-UHFFFAOYSA-N 0.000 description 2
- DPUOLQHDNGRHBS-KTKRTIGZSA-N erucic acid Chemical compound CCCCCCCC\C=C/CCCCCCCCCCCC(O)=O DPUOLQHDNGRHBS-KTKRTIGZSA-N 0.000 description 2
- HQPMKSGTIOYHJT-UHFFFAOYSA-N ethane-1,2-diol;propane-1,2-diol Chemical compound OCCO.CC(O)CO HQPMKSGTIOYHJT-UHFFFAOYSA-N 0.000 description 2
- FARYTWBWLZAXNK-WAYWQWQTSA-N ethyl (z)-3-(methylamino)but-2-enoate Chemical compound CCOC(=O)\C=C(\C)NC FARYTWBWLZAXNK-WAYWQWQTSA-N 0.000 description 2
- VZCCETWTMQHEPK-UHFFFAOYSA-N gamma-Linolensaeure Natural products CCCCCC=CCC=CCC=CCCCCC(O)=O VZCCETWTMQHEPK-UHFFFAOYSA-N 0.000 description 2
- 229960002733 gamolenic acid Drugs 0.000 description 2
- 208000006454 hepatitis Diseases 0.000 description 2
- 231100000283 hepatitis Toxicity 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 235000020778 linoleic acid Nutrition 0.000 description 2
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 2
- 229960004488 linolenic acid Drugs 0.000 description 2
- 230000016379 mucosal immune response Effects 0.000 description 2
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 2
- FUZZWVXGSFPDMH-UHFFFAOYSA-N n-hexanoic acid Natural products CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- 229960002446 octanoic acid Drugs 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 229920001993 poloxamer 188 Polymers 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000003252 repetitive effect Effects 0.000 description 2
- 210000002345 respiratory system Anatomy 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- JIWBIWFOSCKQMA-UHFFFAOYSA-N stearidonic acid Natural products CCC=CCC=CCC=CCC=CCCCCC(O)=O JIWBIWFOSCKQMA-UHFFFAOYSA-N 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 241000712461 unidentified influenza virus Species 0.000 description 2
- YYGNTYWPHWGJRM-UHFFFAOYSA-N (6E,10E,14E,18E)-2,6,10,15,19,23-hexamethyltetracosa-2,6,10,14,18,22-hexaene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC=C(C)CCC=C(C)CCC=C(C)C YYGNTYWPHWGJRM-UHFFFAOYSA-N 0.000 description 1
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 description 1
- 244000283070 Abies balsamea Species 0.000 description 1
- 235000007173 Abies balsamea Nutrition 0.000 description 1
- 241000238876 Acari Species 0.000 description 1
- 241000208140 Acer Species 0.000 description 1
- 206010001742 Allergy to animal Diseases 0.000 description 1
- 244000036975 Ambrosia artemisiifolia Species 0.000 description 1
- 235000003129 Ambrosia artemisiifolia var elatior Nutrition 0.000 description 1
- 229930183010 Amphotericin Natural products 0.000 description 1
- QGGFZZLFKABGNL-UHFFFAOYSA-N Amphotericin A Natural products OC1C(N)C(O)C(C)OC1OC1C=CC=CC=CC=CCCC=CC=CC(C)C(O)C(C)C(C)OC(=O)CC(O)CC(O)CCC(O)C(O)CC(O)CC(O)(CC(O)C2C(O)=O)OC2C1 QGGFZZLFKABGNL-UHFFFAOYSA-N 0.000 description 1
- 241000283084 Balaenoptera musculus Species 0.000 description 1
- 235000018185 Betula X alpestris Nutrition 0.000 description 1
- 235000018212 Betula X uliginosa Nutrition 0.000 description 1
- 241000219495 Betulaceae Species 0.000 description 1
- 108010071134 CRM197 (non-toxic variant of diphtheria toxin) Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000726768 Carpinus Species 0.000 description 1
- 235000001543 Corylus americana Nutrition 0.000 description 1
- 240000007582 Corylus avellana Species 0.000 description 1
- 235000007466 Corylus avellana Nutrition 0.000 description 1
- 229940046168 CpG oligodeoxynucleotide Drugs 0.000 description 1
- 208000001840 Dandruff Diseases 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 102100020715 Fms-related tyrosine kinase 3 ligand protein Human genes 0.000 description 1
- 101710162577 Fms-related tyrosine kinase 3 ligand protein Proteins 0.000 description 1
- 208000004262 Food Hypersensitivity Diseases 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 101710154606 Hemagglutinin Proteins 0.000 description 1
- 101000669447 Homo sapiens Toll-like receptor 4 Proteins 0.000 description 1
- 241000721662 Juniperus Species 0.000 description 1
- 241000209082 Lolium Species 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 241000588650 Neisseria meningitidis Species 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 240000007817 Olea europaea Species 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 101710093908 Outer capsid protein VP4 Proteins 0.000 description 1
- 101710135467 Outer capsid protein sigma-1 Proteins 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 1
- 244000134552 Plantago ovata Species 0.000 description 1
- 235000003421 Plantago ovata Nutrition 0.000 description 1
- 244000268528 Platanus occidentalis Species 0.000 description 1
- 235000006485 Platanus occidentalis Nutrition 0.000 description 1
- 208000035109 Pneumococcal Infections Diseases 0.000 description 1
- 206010035734 Pneumonia staphylococcal Diseases 0.000 description 1
- 241000209504 Poaceae Species 0.000 description 1
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 108010093965 Polymyxin B Proteins 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 241000219000 Populus Species 0.000 description 1
- 101710176177 Protein A56 Proteins 0.000 description 1
- 239000009223 Psyllium Substances 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 208000037656 Respiratory Sounds Diseases 0.000 description 1
- 241000124033 Salix Species 0.000 description 1
- 206010048908 Seasonal allergy Diseases 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- BHEOSNUKNHRBNM-UHFFFAOYSA-N Tetramethylsqualene Natural products CC(=C)C(C)CCC(=C)C(C)CCC(C)=CCCC=C(C)CCC(C)C(=C)CCC(C)C(C)=C BHEOSNUKNHRBNM-UHFFFAOYSA-N 0.000 description 1
- 240000007313 Tilia cordata Species 0.000 description 1
- 102100039360 Toll-like receptor 4 Human genes 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 244000098338 Triticum aestivum Species 0.000 description 1
- 244000274883 Urtica dioica Species 0.000 description 1
- 235000009108 Urtica dioica Nutrition 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 206010047924 Wheezing Diseases 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- ILRRQNADMUWWFW-UHFFFAOYSA-K aluminium phosphate Chemical compound O1[Al]2OP1(=O)O2 ILRRQNADMUWWFW-UHFFFAOYSA-K 0.000 description 1
- 229940047712 aluminum hydroxyphosphate Drugs 0.000 description 1
- 229940009444 amphotericin Drugs 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 235000003484 annual ragweed Nutrition 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000005875 antibody response Effects 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 244000052616 bacterial pathogen Species 0.000 description 1
- UREZNYTWGJKWBI-UHFFFAOYSA-M benzethonium chloride Chemical compound [Cl-].C1=CC(C(C)(C)CC(C)(C)C)=CC=C1OCCOCC[N+](C)(C)CC1=CC=CC=C1 UREZNYTWGJKWBI-UHFFFAOYSA-M 0.000 description 1
- 229960001950 benzethonium chloride Drugs 0.000 description 1
- VEZXCJBBBCKRPI-UHFFFAOYSA-N beta-propiolactone Chemical compound O=C1CCO1 VEZXCJBBBCKRPI-UHFFFAOYSA-N 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 229960001506 brilliant green Drugs 0.000 description 1
- 235000006263 bur ragweed Nutrition 0.000 description 1
- 150000001733 carboxylic acid esters Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- CYDMQBQPVICBEU-UHFFFAOYSA-N chlorotetracycline Natural products C1=CC(Cl)=C2C(O)(C)C3CC4C(N(C)C)C(O)=C(C(N)=O)C(=O)C4(O)C(O)=C3C(=O)C2=C1O CYDMQBQPVICBEU-UHFFFAOYSA-N 0.000 description 1
- CYDMQBQPVICBEU-XRNKAMNCSA-N chlortetracycline Chemical compound C1=CC(Cl)=C2[C@](O)(C)[C@H]3C[C@H]4[C@H](N(C)C)C(O)=C(C(N)=O)C(=O)[C@@]4(O)C(O)=C3C(=O)C2=C1O CYDMQBQPVICBEU-XRNKAMNCSA-N 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 229940001442 combination vaccine Drugs 0.000 description 1
- 235000003488 common ragweed Nutrition 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N dodecahydrosqualene Natural products CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000005183 environmental health Effects 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 235000020932 food allergy Nutrition 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 239000000185 hemagglutinin Substances 0.000 description 1
- 208000002672 hepatitis B Diseases 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 230000000937 inactivator Effects 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 235000021374 legumes Nutrition 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229960001226 live attenuated influenza Drugs 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 235000011147 magnesium chloride Nutrition 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- RUAIJHHRCIHFEV-UHFFFAOYSA-N methyl 4-amino-5-chlorothiophene-2-carboxylate Chemical compound COC(=O)C1=CC(N)=C(Cl)S1 RUAIJHHRCIHFEV-UHFFFAOYSA-N 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- NJTGANWAUPEOAX-UHFFFAOYSA-N molport-023-220-454 Chemical compound OCC(O)CO.OCC(O)CO NJTGANWAUPEOAX-UHFFFAOYSA-N 0.000 description 1
- 229910000402 monopotassium phosphate Inorganic materials 0.000 description 1
- 235000019796 monopotassium phosphate Nutrition 0.000 description 1
- 239000002539 nanocarrier Substances 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 235000014571 nuts Nutrition 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 230000003071 parasitic effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 229960003742 phenol Drugs 0.000 description 1
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 1
- 229960005323 phenoxyethanol Drugs 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- PJNZPQUBCPKICU-UHFFFAOYSA-N phosphoric acid;potassium Chemical compound [K].OP(O)(O)=O PJNZPQUBCPKICU-UHFFFAOYSA-N 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229960000502 poloxamer Drugs 0.000 description 1
- 229920000024 polymyxin B Polymers 0.000 description 1
- 229960005266 polymyxin b Drugs 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- GRLPQNLYRHEGIJ-UHFFFAOYSA-J potassium aluminium sulfate Chemical compound [Al+3].[K+].[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O GRLPQNLYRHEGIJ-UHFFFAOYSA-J 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 229960000380 propiolactone Drugs 0.000 description 1
- 235000004252 protein component Nutrition 0.000 description 1
- 229940070687 psyllium Drugs 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 235000009736 ragweed Nutrition 0.000 description 1
- 235000014102 seafood Nutrition 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 229940031439 squalene Drugs 0.000 description 1
- TUHBEKDERLKLEC-UHFFFAOYSA-N squalene Natural products CC(=CCCC(=CCCC(=CCCC=C(/C)CCC=C(/C)CC=C(C)C)C)C)C TUHBEKDERLKLEC-UHFFFAOYSA-N 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 238000012549 training Methods 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229960000172 trivalent influenza vaccine Drugs 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 239000000277 virosome Substances 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/145—Orthomyxoviridae, e.g. influenza virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/39—Medicinal preparations containing antigens or antibodies characterised by the immunostimulating additives, e.g. chemical adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
- A61P31/06—Antibacterial agents for tuberculosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5252—Virus inactivated (killed)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
- A61K2039/541—Mucosal route
- A61K2039/543—Mucosal route intranasal
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55566—Emulsions, e.g. Freund's adjuvant, MF59
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16111—Influenzavirus A, i.e. influenza A virus
- C12N2760/16134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16211—Influenzavirus B, i.e. influenza B virus
- C12N2760/16234—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
Description
本発明は、ヒトの免疫化における使用のためのワクチンの投与についての新規の投与レジメンを可能にする。本発明は、医学的に訓練された人員によるワクチンの投与なしに、予防接種を可能にする。
大抵のワクチン組成物は注射によって非経口投与される。近年、鼻または口腔内の粘膜表面を介しての投与などの、ワクチンについての他の送達経路が研究されている。大抵のタイプのワクチンについて、例えばプライム用量および1回または複数回のブースト用量として、ワクチンを2回以上投与することによって、よりよい免疫化が達成されることが公知であり、ここで、ブースト用量はプライム用量よりも時間的に後である。
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、および
(c)任意で、使用説明書
を含むワクチンキットであって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの体積のワクチン組成物を含有する、ワクチンキットに関する。
(a)(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネントであって、容器の1つが鼻腔内投与用のワクチン組成物を含有し、別のまたは同じ容器がアジュバントを含有する、第1ワクチンコンポーネント、
(b)任意で、1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネントであって、容器の1つが鼻腔内投与用のワクチン組成物を含有し、別のまたは同じ容器がアジュバントを含有する、第2ワクチンコンポーネント、および
(c)任意で、使用説明書
を含むワクチンキットであって、
ワクチン組成物を含む容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの体積のワクチン組成物を含有する、ワクチンキットを提供する。
(図2)血清中のインフルエンザ特異的IgG2aを示す。平均値および誤差(SEM)を示す。第3用量後にグループA〜Cにおいて有意差を見ることができなかったが、第1用量後、グループBは、プライム時に非経口注射を受けたグループ(グループAおよびC)と比較して、有意により低い血清IgG2a力価を示した。
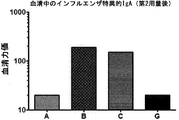
(図3)血清中のインフルエンザ特異的IgAを示す。第2用量後のIgA力価中央値を示す(第42日)。
(図4)血清中のインフルエンザ特異的IgAを示す。IgA力価中央値を示す。
本発明は、
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、および
(c)任意で、使用説明書
を含むワクチンキットであって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチンキットを提供する。
(a)(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネントであって、容器の1つが鼻腔内投与用のワクチン組成物を含有し、別のまたは同じ容器がアジュバントを含有する、第1ワクチンコンポーネント、
(b)任意で、1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネントであって、容器の1つが鼻腔内投与用のワクチン組成物を含有し、別のまたは同じ容器がアジュバントを含有する、第2ワクチンコンポーネント、および
(c)任意で、使用説明書
を含むワクチンキットであって、
ワクチン組成物を含む容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチンキットを提供する。
ウイルスに対する抗原:
(i)インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、ヒト乳頭腫ウイルス(HPV)、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する抗原、またはそれらの混合物、
(ii)ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する抗原、またはそれらの混合物。
細菌に対する抗原:
(i)肺炎球菌(Pneumococci)および/もしくは髄膜炎菌(Meningococci)に対する抗原、またはそれらの混合物、
(ii)ヘモフィルスインフルエンザ(Haemophilus influenzae)b、炭疽菌(Bacillus anthracis)、トラコーマクラミジア(Chlamydia trachomatis)、緑膿菌(Pseudomonas aeruginosa)、結核菌(Mycobacterium tuberculosis)、ジフテリア(Diphtheria)、大腸菌(Escherichia coli)、群連鎖球菌(Group Streptococcus)、淋菌(Neisseria gonorrhoeae)および/もしくは百日咳菌(Bordetella pertussis)に対する抗原、またはそれらの混合物。あるいは、
他の抗原:
(i)ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌および/もしくは水痘に対する抗原、またはそれらの混合物、あるいは
それらの混合物。
アレルギーに対する抗原:
(i)イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物。
ウイルス群1に関連付けられる疾患:
インフルエンザA型、
インフルエンザB型、
呼吸器合胞体ウイルス(RSV)、
ヒトメタニューモウイルス(hMPV)、
ヒト乳頭腫ウイルス(HPV)、
ロタウイルス、
ノロウイルス、
ヒト免疫不全ウイルス(HIV)、
単純ヘルペス、
パラインフルエンザウイルス(OIV)。
ウイルス群2に関連付けられる疾患:
ライノウイルス、
重症急性呼吸器症候群(SARS)、
コロナウイルス、
帯状疱疹/水痘、
A〜E型肝炎、
ハンタウイルス、
サイトメガロウイルス。
細菌群1に関連付けられる疾患:
肺炎球菌、
髄膜炎菌。
細菌群2に関連付けられる疾患:
ヘモフィルスインフルエンザb(Hib)
炭疽菌、
トラコーマクラミジア、
緑膿菌、
結核菌、
ジフテリア、
大腸菌、
群連鎖球菌、
淋菌、
百日咳菌。
GSK製のAS01、AS02、AS03、AS04
Novartis製のMF59
CRM197(タンパク質結合のために使用される)
Nanobio製のNanostat
ImmuneDesign/Medimmune製のGLA(TLR-4アゴニスト)
Hemispherex Biopharma製のAmpligen
Nasvax製のVaxisome
Isconova製のMatrix-M(サポニン誘導体)
CSL製のIscomatrix(サポニン誘導体)
GSK(以前はID Biomedical)製のプロテオソームアジュバント
Incellart製のNanocarriers
Agenus製のQS21 Stimulon
Intercell製のIC31
Mucosis製のBacerium-Like Particle (BLP) aka Mimopath technology
Eisai製のE6020
3M Drug Delivery Systems製のResequimod
DNAアジュバント:Flt3リガンドまたはCpGオリゴデオキシヌクレオチド(oligodeoxunucleotide)
ミシガン大学(James R Baker博士)からのW085EC
Walter Reed製のInvaplex
Finlay Institute製のAFCol
コレラ毒素(CT)または易熱性毒素(LT)-誘導体および変異体。
上述したように、新規のレジメンは多くのタイプの予防接種において使用され得る。以下においてインフルエンザ予防接種を例として用いるが、本発明はそれに限定されない。
(a)第1ワクチンコンポーネントの使用によるワクチン組成物の投与であって、第1ワクチンコンポーネントが、各容器がワクチン組成物を含む1つまたは複数の容器の第1セットを含む、投与、
(b)任意で、第2ワクチンコンポーネントの使用によるワクチン組成物の投与であって、第2ワクチンコンポーネントが、各容器がワクチン組成物を含む1つまたは複数の容器の第2セットを含む、投与
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、投与レジメンに関する。
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、デバイスに関する。
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
の使用であって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用に関する。
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
の使用であって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用に関する。
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
を投与する段階を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、方法に関する。
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチンに関する。
− ヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
− ワクチン組成物の投与における使用のためのデバイス。
− ヒトを免疫化するための:(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネントの使用であって、第1および第2容器のセットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用。
− ヒトを鼻腔内的に免疫化するためのワクチンの製造のための:(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネントの使用であって、容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用。
− 予防接種の必要があるヒトを処置する方法。
− 鼻腔内投与用に処方されたワクチン。
この実験は、プライム用量が非経口的および鼻腔内的の両方で与えられ、第1ブースト用量が鼻腔内に与えられる、レジメンに関する。鼻腔内に与えられる用量は、2つ以上の容器に、例えば2つの容器に分割してもよく、各容器の内容物を鼻孔へ投与する。
マウス(Balb/c、雌性、7〜9週齢、1群当たりn=8(陰性対照群においてn=4))は予防接種スケジュールに従い、それらに第0日、第21日および第42日に予防接種し、第61日に屠殺した。予防接種の用量および体積は以下の通りであった:経鼻(i.n.):2x5μl(各鼻孔中に5μl)中、1.5または0.5μg HA、2% Endocine(商標)。研究において使用したEndocine(商標)アジュバントは、ワクチン組成物中20mg/mlの最終濃度で等モル量のグリセロールモノオレエートおよびオレイン酸を含む。皮下(s.c):50μl中1.5または0.5μg HA(右後脚中)。試験物質は、スプリットインフルエンザA型/カリフォルニア/07/2009 (H1N1)抗原およびEndocine(商標)アジュバント(Eurocine Vaccines AB製)であった。陰性対照は食塩水(塩化ナトリウム)0.9%であった。血液サンプルおよび鼻洗浄サンプルを第1日、第19日、第40日および第61日に採取した。
1.
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、および
(c)任意で、使用説明書
を含むワクチンキットであって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチンキット。
2.容器の第1セットが4個までの容器を有する、態様1記載のキット。
3.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様1または2記載のキット。
4.第2ワクチンコンポーネントがキット中に含まれる、前述の態様のいずれかに記載のキット。
5.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載のキット。
6.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のキット。
7.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様6記載のキット。
8.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のキット。
9.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様8記載のキット。
10.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のキット。
11.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様10記載のキット。
12.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のキット。
13.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のキット。
14.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様12または13記載のキット。
15.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様12〜14のいずれか1つに記載のキット。
16.ワクチン組成物が30種類までの異なる抗原を含有する、態様12〜15のいずれか1つに記載のキット。
17.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様12〜16のいずれか1つに記載のキット。
18.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様12〜17のいずれか1つに記載のキット。
19.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様12〜18のいずれか1つに記載のキット。
20.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様12〜19のいずれか1つに記載のキット。
21.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様12〜20のいずれか1つに記載のキット。
22.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様12〜21のいずれか1つに記載のキット。
23.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様12〜22のいずれか1つに記載のキット。
24.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載のキット。
25.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載のキット。
26.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のキット。
27.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のキット。
28.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載のキット。
29.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載のキット。
30.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様29記載のキット。
31.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様29または30記載のキット。
32.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載のキット。
33.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載のキット。
34.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様33記載のキット。
35.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載のキット。
36.鼻への自己投与による予防接種用の前述の態様のいずれかに記載の容器のセット。
37.ヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメンであって:
(a)第1ワクチンコンポーネントの使用によるワクチン組成物の投与であって、第1ワクチンコンポーネントが、各容器がワクチン組成物を含む1つまたは複数の容器の第1セットを含む、投与、
(b)任意で、第2ワクチンコンポーネントの使用によるワクチン組成物の投与であって、第2ワクチンコンポーネントが、各容器がワクチン組成物を含む1つまたは複数の容器の第2セットを含む、投与
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、投与レジメン。
38.容器の第1セットが4個までの容器を有する、態様37記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
39.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様37または38記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
40.第2ワクチンコンポーネントが、ヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン中に含まれる、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
41.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
42.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
43.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様42記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
44.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
45.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様44記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
46.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
47.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様46記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
48.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
49.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
50.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様48または49記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
51.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様48〜50のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
52.ワクチン組成物が30種類までの異なる抗原を含有する、態様48〜51のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
53.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様48〜52のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
54.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様48〜53のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
55.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様48〜53のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
56.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様48〜55のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
57.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様48〜56のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
58.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様48〜57のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
59.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様48〜58のいずれか1つに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
60.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
61.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
62.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
63.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
64.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
65.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
66.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様65記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
67.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様65または66記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
68.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
69.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
70.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様69記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
71.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載のヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメン。
72.ワクチン組成物の投与における使用のためのデバイスであって:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、デバイス。
73.容器の第1セットが4個までの容器を有する、態様72記載のデバイス。
74.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様72または73記載のデバイス。
75.第2ワクチンコンポーネントがデバイス中に含まれる、前述の態様のいずれかに記載のデバイス。
76.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載のデバイス。
77.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のデバイス。
78.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様77記載のデバイス。
79.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のデバイス。
80.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様79記載のデバイス。
81.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のデバイス。
82.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様81記載のデバイス。
83.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のデバイス。
84.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のデバイス。
85.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様83または84記載のデバイス。
86.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様83〜85のいずれか1つに記載のデバイス。
87.ワクチン組成物が30種類までの異なる抗原を含有する、態様83〜86のいずれか1つに記載のデバイス。
88.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様83〜87のいずれか1つに記載のデバイス。
89.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様83〜88のいずれか1つに記載のデバイス。
90.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様83〜89のいずれか1つに記載のデバイス。
91.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様83〜90のいずれか1つに記載のデバイス。
92.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様83〜91のいずれか1つに記載のデバイス。
93.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様83〜92のいずれか1つに記載のデバイス。
94.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様83〜93のいずれか1つに記載のデバイス。
95.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載のデバイス。
96.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載のデバイス。
97.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のデバイス。
98.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のデバイス。
99.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載のデバイス。
100.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載のデバイス。
101.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様100記載のデバイス。
102.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様100または101記載のデバイス。
103.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載のデバイス。
104.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載のデバイス。
105.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様104記載のデバイス。
106.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載のデバイス。
107.ヒトを免疫化するための:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
の使用であって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用。
108.容器の第1セットが4個までの容器を有する、態様107記載の使用。
109.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様107または108記載の使用。
110.第2ワクチンコンポーネントが使用中に含まれる、前述の態様のいずれかに記載の使用。
111.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載の使用。
112.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の使用。
113.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様112記載の使用。
114.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の使用。
115.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様114記載のキット。
116.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の使用。
117.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様116記載の使用。
118.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載の使用。
119.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載の使用。
120.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様118または119記載の使用。
121.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様118〜120のいずれか1つに記載の使用。
122.ワクチン組成物が30種類までの異なる抗原を含有する、態様118〜121のいずれか1つに記載の使用。
123.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様118〜122のいずれか1つに記載の使用。
124.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様118〜123のいずれか1つに記載の使用。
125.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様118〜124のいずれか1つに記載の使用。
126.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様118〜125のいずれか1つに記載の使用。
127.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様118〜126のいずれか1つに記載の使用。
128.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様118〜127のいずれか1つに記載の使用。
129.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様118〜128のいずれか1つに記載の使用。
130.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載の使用。
131.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載の使用。
132.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載の使用。
133.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載の使用。
134.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載の使用。
135.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載の使用。
136.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様135記載の使用。
137.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様135または136記載の使用。
138.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載の使用。
139.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載の使用。
140.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様139記載の使用。
141.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載の使用。
142.ヒトを鼻腔内的に免疫化するためのワクチンの製造のための:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
の使用であって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用。
143.容器の第1セットが4個までの容器を有する、態様142記載の使用。
144.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様132または133記載の使用。
145.第2ワクチンコンポーネントが使用中に含まれる、前述の態様のいずれかに記載の使用。
146.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載の使用。
147.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の使用。
148.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様147記載の使用。
149.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の使用。
150.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様149記載の使用。
151.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の使用。
152.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様151記載の使用。
153.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載の使用。
154.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載の使用。
155.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様153または154記載の使用。
156.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様153〜155のいずれか1つに記載の使用。
157.ワクチン組成物が30種類までの異なる抗原を含有する、態様153〜156のいずれか1つに記載の使用。
158.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様153〜157のいずれか1つに記載の使用。
159.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様153〜158のいずれか1つに記載の使用。
160.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様153〜159のいずれか1つに記載の使用。
161.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様153〜160のいずれか1つに記載の使用。
162.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様153〜161のいずれか1つに記載の使用。
163.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様153〜162のいずれか1つに記載の使用。
164.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様153〜163のいずれか1つに記載の使用。
165.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載の使用。
166.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載の使用。
167.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載の使用。
168.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載の使用。
169.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載の使用。
170.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載の使用。
171.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様170記載の使用。
172.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様170または171記載の使用。
173.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載の使用。
174.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載の使用。
175.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様174記載の使用。
176.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載の使用。
177.予防接種の必要があるヒトを処置する方法であって、
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
を投与する段階を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、方法。
178.容器の第1セットが4個までの容器を有する、態様177記載の方法。
179.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様177または178記載の方法。
180.第2ワクチンコンポーネントが方法中に含まれる、前述の態様のいずれかに記載の方法。
181.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載の方法。
182.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の方法。
183.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様182記載の方法。
184.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の方法。
185.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様184記載の方法。
186.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載の方法。
187.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様186記載の方法。
188.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載の方法。
189.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載の方法。
190.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様188または189記載の方法。
191.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様188〜190のいずれか1つに記載の方法。
192.ワクチン組成物が30種類までの異なる抗原を含有する、態様188〜191のいずれか1つに記載の方法。
193.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様188〜192のいずれか1つに記載の方法。
194.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様188〜193のいずれか1つに記載の方法。
195.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様188〜194のいずれか1つに記載の方法。
196.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様188〜195のいずれか1つに記載の方法。
197.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様188〜196のいずれか1つに記載の方法。
198.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様188〜197のいずれか1つに記載の方法。
199.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様188〜198のいずれか1つに記載の方法。
200.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載の方法。
201.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載の方法。
202.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載の方法。
203.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載の方法。
204.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載の方法。
205.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載の方法。
206.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様205記載の方法。
207.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様205または206記載の方法。
208.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載の方法。
209.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載の方法。
210.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様209記載の方法。
211.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載の方法。
212.鼻腔内投与用に処方されたワクチンであって、
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチン。
213.容器の第1セットが4個までの容器を有する、態様212記載のワクチン。
214.第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、態様212または213記載のワクチン。
215.第2ワクチンコンポーネントがワクチン中に含まれる、前述の態様のいずれかに記載のワクチン。
216.容器の第2セットが8個までの容器を有する、前述の態様のいずれかに記載のワクチン。
217.容器の第1セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のワクチン。
218.容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様217記載のワクチン。
219.容器の第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のワクチン。
220.容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様219記載のワクチン。
221.容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前述の態様のいずれかに記載のワクチン。
222.容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、態様221記載のワクチン。
223.第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のワクチン。
224.第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前述の態様のいずれかに記載のワクチン。
225.1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、態様223または224記載のワクチン。
226.1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、態様223〜225のいずれか1つに記載のワクチン。
227.ワクチン組成物が30種類までの異なる抗原を含有する、態様223〜226のいずれか1つに記載のワクチン。
228.第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、態様223〜227のいずれか1つに記載のワクチン。
229.1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様223〜228のいずれか1つに記載のワクチン。
230.1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様223〜229のいずれか1つに記載のワクチン。
231.1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様223〜230のいずれか1つに記載のワクチン。
232.1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様223〜231のいずれか1つに記載のワクチン。
233.1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、態様223〜232のいずれか1つに記載のワクチン。
234.1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、態様223〜233のいずれか1つに記載のワクチン。
235.各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前述の態様のいずれかに記載のワクチン。
236.鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前述の態様のいずれかに記載のワクチン。
237.容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のワクチン。
238.容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前述の態様のいずれかに記載のワクチン。
239.鼻腔内投与用のワクチン組成物がアジュバントを含有する、前述の態様のいずれかに記載のワクチン。
240.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前述の態様のいずれかに記載のワクチン。
241.ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、態様240記載のワクチン。
242.ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、態様240または241記載のワクチン。
243.鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前述の態様のいずれかに記載のワクチン。
244.鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前述の態様のいずれかに記載のワクチン。
245.ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、態様244記載のワクチン。
246.鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前述の態様のいずれかに記載のワクチン。
Claims (96)
- (a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント、および
(c)任意で、使用説明書
を含むワクチンキットであって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチンキット。 - 容器の第1セットが4個までの容器を有する、請求項1記載のキット。
- 第1ワクチンコンポーネントが非経口投与用のワクチン組成物をさらに含有する、請求項1または2記載のキット。
- 第2ワクチンコンポーネントがキット中に含まれる、前記請求項のいずれか一項記載のキット。
- 容器の第2セットが8個までの容器を有する、前記請求項のいずれか一項記載のキット。
- 容器の第1セット中のワクチン組成物が同じ成分で構成されている、前記請求項のいずれか一項記載のキット。
- 容器の第1セット中のワクチン組成物中の個々の成分の濃度および量が同じである、請求項6記載のキット。
- 容器の第2セット中のワクチン組成物が同じ成分で構成されている、前記請求項のいずれか一項記載のキット。
- 容器の第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、請求項8記載のキット。
- 容器の第1および第2セット中のワクチン組成物が同じ成分で構成されている、前記請求項のいずれか一項記載のキット。
- 容器の第1および第2セット中のワクチン組成物中の個々の成分の濃度および量が同じである、請求項10記載のキット。
- 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、前記請求項のいずれか一項記載のキット。
- 第1コンポーネント中の非経口投与用のワクチン組成物が1種または複数種の抗原を含有する、前記請求項のいずれか一項記載のキット。
- 1種または複数種の抗原が、不活性化細菌もしくはウイルスの、全体またはそれらの一部に由来する、請求項12または13記載のキット。
- 1種または複数種の抗原が、細菌および/またはウイルスの1つまたは複数の株に由来する、請求項12〜14のいずれか一項記載のキット。
- ワクチン組成物が30種類までの異なる抗原を含有する、請求項12〜15のいずれか一項記載のキット。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項12〜16のいずれか一項記載のキット。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項12〜17のいずれか一項記載のキット。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項12〜18のいずれか一項記載のキット。
- 1種または複数種の抗原が、肺炎球菌(Pneumococci)および/もしくは髄膜炎菌(Meningococci)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項12〜19のいずれか一項記載のキット。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb(Haemophilus influenza b)、炭疽菌(Bacillus anthracis)、トラコーマクラミジア(Chlamydia trachomatis)、緑膿菌(Pseudomonas aeruginosa)、結核菌(Mycobacterium tuberculosis)、ジフテリア(Diphtheria)、大腸菌(Escherichia coli)、群連鎖球菌(Group Streptococcus)、淋菌(Neisseria gonorrhoeae)および/もしくは百日咳菌(Bordetella pertussis)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項12〜20のいずれか一項記載のキット。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項12〜21のいずれか一項記載のキット。
- 1種または複数種の抗原が、イエダニ、花粉および他の環境アレルゲン、食物、虫刺され、ラテックス、化粧品、動物および/もしくはニッケルに起因するアレルギーに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項12〜22のいずれか一項記載のキット。
- 各容器中の鼻腔内投与用のワクチン組成物の体積が約50μl〜約250μlである、前記請求項のいずれか一項記載のキット。
- 鼻腔内投与用のワクチン組成物を含有する各容器が、予防接種用量の50%または100%を含有する、前記請求項のいずれか一項記載のキット。
- 容器の第1セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前記請求項のいずれか一項記載のキット。
- 容器の第2セットが2つの容器であり、各々が同じワクチン組成物を同じ体積で含有する、前記請求項のいずれか一項記載のキット。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載のキット。
- 鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪酸とのモノエステル、
(ii)脂肪酸、
(iii)脂肪酸の組み合わせ、
(iv)それらの混合物
のうちの1つまたは複数を含有する、前記請求項のいずれか一項記載のキット。 - ワクチン組成物が、5〜40 mg/mlの濃度でグリセロールと脂肪酸とのモノエステルを含有する、請求項29記載のキット。
- ワクチン組成物が、2〜40 mg/mlの総濃度で脂肪酸または脂肪酸の組み合わせを含有する、請求項29または30記載のキット。
- 鼻腔内投与用のワクチン組成物が:
(i)グリセロールと脂肪エステルとのモノエステル、および
(ii)脂肪酸
を含有する、前記請求項のいずれか一項記載のキット。 - 鼻腔内投与用のワクチン組成物が:
(i)グリセロールモノオレエート、および
(ii)オレイン酸
を含有する、前記請求項のいずれか一項記載のキット。 - ワクチン組成物中において、グリセロールモノオレエートの濃度が2.5〜20 mg/mlであり、オレイン酸の濃度が2.5〜20 mg/mlである、請求項33記載のキット。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載のキット。
- 鼻への自己投与による予防接種用の前記請求項のいずれか一項記載の容器のセット。
- ヒトの免疫化における使用のためのワクチン組成物の鼻腔内投与についての投与レジメンであって:
(a)第1ワクチンコンポーネントの使用によるワクチン組成物の投与であって、第1ワクチンコンポーネントが、各容器がワクチン組成物を含む1つまたは複数の容器の第1セットを含む、投与
(b)任意で、第2ワクチンコンポーネントの使用によるワクチン組成物の投与であって、第2ワクチンコンポーネントが、各容器がワクチン組成物を含む1つまたは複数の容器の第2セットを含む、投与
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、投与レジメン。 - 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、請求項37記載の投与レジメン。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項38のいずれか一項記載の投与レジメン。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項38〜39のいずれか一項記載の投与レジメン。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項38〜40のいずれか一項記載の投与レジメン。
- 1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項38〜41のいずれか一項記載の投与レジメン。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項38〜42のいずれか一項記載の投与レジメン。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項39〜43のいずれか一項記載の投与レジメン。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載の投与レジメン。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載の投与レジメン。
- ワクチン組成物の投与における使用のためのデバイスであって:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、デバイス。 - 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、請求項47記載のデバイス。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項48のいずれか一項記載のデバイス。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項48〜49のいずれか一項記載のデバイス。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項48〜50のいずれか一項記載のデバイス。
- 1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項48〜51のいずれか一項記載のデバイス。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項48〜52のいずれか一項記載のデバイス。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項48〜53のいずれか一項記載のデバイス。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載のデバイス。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載のデバイス。
- ヒトを免疫化するための:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
の使用であって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用。 - 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、請求項56記載の使用。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項58のいずれか一項記載の使用。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項58〜59のいずれか一項記載の使用。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項58〜60のいずれか一項記載の使用。
- 1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項58〜61のいずれか一項記載の使用。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項58〜62のいずれか一項記載の使用。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項58〜63のいずれか一項記載の使用。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載の使用。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載の使用。
- ヒトを鼻腔内的に免疫化するためのワクチンの製造のための:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
の使用であって、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、使用。 - 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、請求項67記載の使用。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項68のいずれか一項記載の使用。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項68〜69のいずれか一項記載の使用。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項68〜70のいずれか一項記載の使用。
- 1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項68〜71のいずれか一項記載の使用。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項68〜72のいずれか一項記載の使用。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項68〜73のいずれか一項記載の使用。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載の使用。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載の使用。
- 予防接種の必要があるヒトを処置する方法であって:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
を投与する段階を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、方法。 - 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、請求項77記載の方法。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項78のいずれか一項記載の方法。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項78〜79のいずれか一項記載の方法。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項78〜80のいずれか一項記載の方法。
- 1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項78〜81のいずれか一項記載の方法。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項78〜82のいずれか一項記載の方法。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項78〜83のいずれか一項記載の方法。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載の方法。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載の方法。
- 鼻腔内投与用に処方されたワクチンであって:
(a)各容器が鼻腔内投与用のワクチン組成物を含有する(i)1つまたは複数の容器の第1セットを含む、第1ワクチンコンポーネント、
(b)任意で、各容器が鼻腔内投与用のワクチン組成物を含有する1つまたは複数の容器の第2セットを含む、第2ワクチンコンポーネント
を含み、
容器の第1および第2セットの各容器が、約5マイクロリットル〜約400マイクロリットルの総体積のワクチン組成物を含有する、ワクチン。 - 第1および第2コンポーネント中の鼻腔内投与用のワクチン組成物が1種または複数種の抗原を含有する、請求項87記載のワクチン。
- 第1および第2コンポーネントのワクチン組成物が同じ抗原を含有する、請求項88のいずれか一項記載のワクチン。
- 1種または複数種の抗原が、インフルエンザA型、インフルエンザB型、RSV、ヒトメタニューモウイルス(hMPV)、HPV、ロタウイルス、ノロウイルス、HIV、単純ヘルペス、および/もしくはパラインフルエンザウイルス(OIV)に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項88〜89のいずれか一項記載のワクチン。
- 1種または複数種の抗原が、ライノウイルス、SARS、コロナウイルス、帯状疱疹/水痘、A〜E型肝炎、ハンタウイルス、および/もしくはサイトメガロウイルスに対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項88〜90のいずれか一項記載のワクチン。
- 1種または複数種の抗原が、肺炎球菌および/もしくは髄膜炎菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項88〜91のいずれか一項記載のワクチン。
- 1種または複数種の抗原が、ヘモフィルスインフルエンザb、炭疽菌、トラコーマクラミジア、緑膿菌、結核菌、ジフテリア、大腸菌、群連鎖球菌、淋菌および/もしくは百日咳菌に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項88〜92のいずれか一項記載のワクチン。
- 1種または複数種の抗原が、ジフテリア、破傷風、百日咳、ポリオ、麻疹、ムンプス、風疹、子宮頸癌、結核および/もしくは水痘に対する免疫応答を誘導する抗原、またはそれらの混合物である、請求項86〜93のいずれか一項記載のワクチン。
- 鼻腔内投与用のワクチン組成物がアジュバントを含有する、前記請求項のいずれか一項記載のワクチン。
- 鼻腔内投与用のワクチン組成物が自己投与によって与えられる、前記請求項のいずれか一項記載のワクチン。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DKPA201270788 | 2012-12-17 | ||
| DKPA201270788 | 2012-12-17 | ||
| PCT/EP2013/076905 WO2014095866A1 (en) | 2012-12-17 | 2013-12-17 | Intranasal vaccination dosage regimen |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018135426A Division JP2018172434A (ja) | 2012-12-17 | 2018-07-19 | 鼻腔内予防接種投薬レジメン |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016502995A true JP2016502995A (ja) | 2016-02-01 |
| JP2016502995A5 JP2016502995A5 (ja) | 2016-12-01 |
Family
ID=49880734
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015547071A Ceased JP2016502995A (ja) | 2012-12-17 | 2013-12-17 | 鼻腔内予防接種投薬レジメン |
| JP2018135426A Pending JP2018172434A (ja) | 2012-12-17 | 2018-07-19 | 鼻腔内予防接種投薬レジメン |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018135426A Pending JP2018172434A (ja) | 2012-12-17 | 2018-07-19 | 鼻腔内予防接種投薬レジメン |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9700614B2 (ja) |
| EP (1) | EP2931309A1 (ja) |
| JP (2) | JP2016502995A (ja) |
| AU (1) | AU2013361781B2 (ja) |
| HK (1) | HK1215546A1 (ja) |
| PH (1) | PH12015501459A1 (ja) |
| WO (1) | WO2014095866A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101858840B1 (ko) * | 2016-01-15 | 2018-05-16 | 단국대학교 천안캠퍼스 산학협력단 | 집먼지진드기 유래 알레르겐에 의한 과민반응 면역조절제 |
| CA3133718A1 (en) * | 2019-03-20 | 2020-09-24 | Advagene Biopharma Co., Ltd. | Method of modulating mucosal immunogenicity |
| WO2024030938A1 (en) * | 2022-08-02 | 2024-02-08 | Yale University | Compositions, kits, and methods of immunizing against viral infections |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002542203A (ja) * | 1999-04-19 | 2002-12-10 | スミスクライン ビーチャム バイオロジカルズ ソシエテ アノニム | ワクチン |
| JP2004527524A (ja) * | 2001-04-05 | 2004-09-09 | カイロン コーポレイション | 非経口初回抗原刺激後の粘膜追加免疫 |
| JP2009514840A (ja) * | 2005-11-04 | 2009-04-09 | ノバルティス ヴァクシンズ アンド ダイアグノスティクス エスアールエル | インフルエンザワクチンによってプライム(priming)/ブースト(boosting)するための投与経路 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7964200B2 (en) | 2005-05-18 | 2011-06-21 | Children's Hospital & Research Center At Oakland | Methods and compositions for immunizing against Chlamydia infection |
| US8535683B2 (en) | 2006-03-22 | 2013-09-17 | Abbott Biologicals B.V. | Intranasal or inhalational administration of virosomes |
| EP1998814A4 (en) | 2006-05-11 | 2010-06-16 | Novavax Inc | NEW VACCINES AGAINST INFLUENZA M2 |
| GB0905570D0 (en) | 2009-03-31 | 2009-05-13 | Novartis Ag | Combined vaccines |
| US8658180B2 (en) | 2008-08-15 | 2014-02-25 | Mark A. Miller | Vaccines against influenza virus |
| EA201171032A1 (ru) | 2009-02-10 | 2012-02-28 | Новартис Аг | Схемы лечения с помощью вакцины против гриппа, связанного с пандемическими штаммами |
| CN103154021A (zh) | 2010-08-16 | 2013-06-12 | 威斯特解剖及生物研究所 | 通用甲型流感疫苗 |
| CA2810597A1 (en) | 2010-09-30 | 2012-04-05 | Eurocine Vaccines Ab | Improved vaccine compositions |
-
2013
- 2013-12-17 AU AU2013361781A patent/AU2013361781B2/en not_active Ceased
- 2013-12-17 EP EP13811884.9A patent/EP2931309A1/en not_active Withdrawn
- 2013-12-17 JP JP2015547071A patent/JP2016502995A/ja not_active Ceased
- 2013-12-17 WO PCT/EP2013/076905 patent/WO2014095866A1/en active Application Filing
- 2013-12-17 US US14/650,831 patent/US9700614B2/en active Active
-
2015
- 2015-06-24 PH PH12015501459A patent/PH12015501459A1/en unknown
-
2016
- 2016-03-29 HK HK16103564.2A patent/HK1215546A1/zh unknown
-
2018
- 2018-07-19 JP JP2018135426A patent/JP2018172434A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002542203A (ja) * | 1999-04-19 | 2002-12-10 | スミスクライン ビーチャム バイオロジカルズ ソシエテ アノニム | ワクチン |
| JP2004527524A (ja) * | 2001-04-05 | 2004-09-09 | カイロン コーポレイション | 非経口初回抗原刺激後の粘膜追加免疫 |
| JP2009514840A (ja) * | 2005-11-04 | 2009-04-09 | ノバルティス ヴァクシンズ アンド ダイアグノスティクス エスアールエル | インフルエンザワクチンによってプライム(priming)/ブースト(boosting)するための投与経路 |
Non-Patent Citations (1)
| Title |
|---|
| PETERSSON, P. ET AL.: "The Eurocine L3 adjuvants with subunit influenza antigens induce protective immunity in mice after i", VACCINE, vol. 28, no. 39, JPN5013010932, 7 September 2010 (2010-09-07), pages 6491 - 7, XP027267112, ISSN: 0003762114 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2931309A1 (en) | 2015-10-21 |
| JP2018172434A (ja) | 2018-11-08 |
| US20160184424A1 (en) | 2016-06-30 |
| PH12015501459A1 (en) | 2015-09-21 |
| HK1215546A1 (zh) | 2016-09-02 |
| AU2013361781A1 (en) | 2015-07-02 |
| AU2013361781B2 (en) | 2017-06-29 |
| WO2014095866A1 (en) | 2014-06-26 |
| US9700614B2 (en) | 2017-07-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210393772A1 (en) | Adjuvant and vaccine compositions | |
| Bonanni et al. | Vaccine evolution | |
| Kocourkova et al. | Vaccine ingredients: components that influence vaccine efficacy | |
| AU2013360890B2 (en) | Vaccine composition for use in immuno-compromised populations | |
| JP5712126B2 (ja) | 遅延型追加刺激免疫処置に対する迅速な応答 | |
| JP2018172434A (ja) | 鼻腔内予防接種投薬レジメン | |
| BE1022008B1 (fr) | Compositions immunogenes combinees | |
| CN101123982B (zh) | 脂质和一氧化二氮组合作为用于增强疫苗功效的佐剂 | |
| JP6802790B2 (ja) | アジュバント組成物及び関連方法 | |
| JP2016222704A (ja) | 改善されたワクチン組成物 | |
| US11707521B2 (en) | Mucosal adjuvant | |
| CN116139266B (zh) | 长链不饱和脂肪酸在制备用于灭活疫苗的免疫增强剂中的用途 | |
| Arora et al. | MBBS, MD Fellowship (IVF &Reproductive Medicine) Milann Fertility Centre Bengaluru India | |
| WO2016105274A1 (en) | A rabies composition comprising pika adjuvant |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150818 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161012 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20161012 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170803 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171025 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20171211 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180220 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180322 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180822 |
|
| A045 | Written measure of dismissal of application [lapsed due to lack of payment] |
Free format text: JAPANESE INTERMEDIATE CODE: A045 Effective date: 20191121 |