JP2016166319A - 熱消去性インク組成物及びその製造方法 - Google Patents
熱消去性インク組成物及びその製造方法 Download PDFInfo
- Publication number
- JP2016166319A JP2016166319A JP2015084537A JP2015084537A JP2016166319A JP 2016166319 A JP2016166319 A JP 2016166319A JP 2015084537 A JP2015084537 A JP 2015084537A JP 2015084537 A JP2015084537 A JP 2015084537A JP 2016166319 A JP2016166319 A JP 2016166319A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- dye
- ink composition
- dispersion
- reaction medium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000000976 ink Substances 0.000 title claims abstract description 64
- 239000000203 mixture Substances 0.000 title claims abstract description 60
- 238000004519 manufacturing process Methods 0.000 title claims description 10
- -1 fatty acid ester compound Chemical class 0.000 claims abstract description 78
- 239000012429 reaction media Substances 0.000 claims abstract description 53
- 150000001875 compounds Chemical class 0.000 claims abstract description 43
- 239000002612 dispersion medium Substances 0.000 claims abstract description 43
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 claims abstract description 16
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 15
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 9
- 239000006185 dispersion Substances 0.000 claims description 41
- 239000002270 dispersing agent Substances 0.000 claims description 9
- 150000002894 organic compounds Chemical class 0.000 claims description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 7
- 238000002844 melting Methods 0.000 claims description 5
- 230000008018 melting Effects 0.000 claims description 5
- 238000002156 mixing Methods 0.000 claims description 5
- 239000011550 stock solution Substances 0.000 claims description 4
- 238000011161 development Methods 0.000 claims description 3
- 238000004040 coloring Methods 0.000 claims description 2
- 239000013078 crystal Substances 0.000 claims description 2
- 150000002576 ketones Chemical class 0.000 claims 1
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 abstract description 7
- 235000014113 dietary fatty acids Nutrition 0.000 abstract description 5
- 229930195729 fatty acid Natural products 0.000 abstract description 5
- 239000000194 fatty acid Substances 0.000 abstract description 5
- 239000000975 dye Substances 0.000 description 55
- 239000007788 liquid Substances 0.000 description 18
- 125000004432 carbon atom Chemical group C* 0.000 description 15
- 235000013824 polyphenols Nutrition 0.000 description 12
- QWVGKYWNOKOFNN-UHFFFAOYSA-N o-cresol Chemical compound CC1=CC=CC=C1O QWVGKYWNOKOFNN-UHFFFAOYSA-N 0.000 description 10
- 125000000217 alkyl group Chemical group 0.000 description 9
- 238000010586 diagram Methods 0.000 description 5
- 238000010438 heat treatment Methods 0.000 description 5
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 5
- CJPNOLIZCWDHJK-UHFFFAOYSA-N 2-Pentadecanone Chemical compound CCCCCCCCCCCCCC(C)=O CJPNOLIZCWDHJK-UHFFFAOYSA-N 0.000 description 4
- 229920000858 Cyclodextrin Polymers 0.000 description 4
- KRHYYFGTRYWZRS-UHFFFAOYSA-N Fluorane Chemical class F KRHYYFGTRYWZRS-UHFFFAOYSA-N 0.000 description 4
- 229910000040 hydrogen fluoride Inorganic materials 0.000 description 4
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 4
- QNSFPYSRPPFJGJ-UHFFFAOYSA-N spiro[2-benzofuran-3,5'-chromeno[2,3-d]pyrimidine]-1-one Chemical compound C12=CC=CC=C2OC2=NC=NC=C2C11OC(=O)C2=CC=CC=C21 QNSFPYSRPPFJGJ-UHFFFAOYSA-N 0.000 description 4
- VOZKAJLKRJDJLL-UHFFFAOYSA-N 2,4-diaminotoluene Chemical compound CC1=CC=C(N)C=C1N VOZKAJLKRJDJLL-UHFFFAOYSA-N 0.000 description 3
- 125000004203 4-hydroxyphenyl group Chemical group [H]OC1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 3
- ZAJNGDIORYACQU-UHFFFAOYSA-N decan-2-one Chemical compound CCCCCCCCC(C)=O ZAJNGDIORYACQU-UHFFFAOYSA-N 0.000 description 3
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 3
- 150000003839 salts Chemical class 0.000 description 3
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 2
- BBMCTIGTTCKYKF-UHFFFAOYSA-N 1-heptanol Chemical compound CCCCCCCO BBMCTIGTTCKYKF-UHFFFAOYSA-N 0.000 description 2
- LSKONYYRONEBKA-UHFFFAOYSA-N 2-Dodecanone Chemical compound CCCCCCCCCCC(C)=O LSKONYYRONEBKA-UHFFFAOYSA-N 0.000 description 2
- IEDKVDCIEARIIU-UHFFFAOYSA-N 2-Nonadecanone Chemical compound CCCCCCCCCCCCCCCCCC(C)=O IEDKVDCIEARIIU-UHFFFAOYSA-N 0.000 description 2
- POQLVOYRGNFGRM-UHFFFAOYSA-N 2-Tetradecanone Chemical compound CCCCCCCCCCCCC(C)=O POQLVOYRGNFGRM-UHFFFAOYSA-N 0.000 description 2
- XJLDYKIEURAVBW-UHFFFAOYSA-N 3-decanone Chemical compound CCCCCCCC(=O)CC XJLDYKIEURAVBW-UHFFFAOYSA-N 0.000 description 2
- OHKTUDSKDILFJC-UHFFFAOYSA-N 4-[(4-hydroxy-3,5-dimethylphenyl)-(4-hydroxyphenyl)methyl]-2,6-dimethylphenol Chemical compound CC1=C(O)C(C)=CC(C(C=2C=CC(O)=CC=2)C=2C=C(C)C(O)=C(C)C=2)=C1 OHKTUDSKDILFJC-UHFFFAOYSA-N 0.000 description 2
- WXYSZTISEJBRHW-UHFFFAOYSA-N 4-[2-[4-[1,1-bis(4-hydroxyphenyl)ethyl]phenyl]propan-2-yl]phenol Chemical compound C=1C=C(C(C)(C=2C=CC(O)=CC=2)C=2C=CC(O)=CC=2)C=CC=1C(C)(C)C1=CC=C(O)C=C1 WXYSZTISEJBRHW-UHFFFAOYSA-N 0.000 description 2
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical class OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 2
- VOWWYDCFAISREI-UHFFFAOYSA-N Bisphenol AP Chemical compound C=1C=C(O)C=CC=1C(C=1C=CC(O)=CC=1)(C)C1=CC=CC=C1 VOWWYDCFAISREI-UHFFFAOYSA-N 0.000 description 2
- IPAJDLMMTVZVPP-UHFFFAOYSA-N Crystal violet lactone Chemical compound C1=CC(N(C)C)=CC=C1C1(C=2C=CC(=CC=2)N(C)C)C2=CC=C(N(C)C)C=C2C(=O)O1 IPAJDLMMTVZVPP-UHFFFAOYSA-N 0.000 description 2
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 2
- XCXKZBWAKKPFCJ-UHFFFAOYSA-N Hexadecan-2-one Chemical compound CCCCCCCCCCCCCCC(C)=O XCXKZBWAKKPFCJ-UHFFFAOYSA-N 0.000 description 2
- LTMXHUUHBSCKEK-UHFFFAOYSA-N Hexadecan-3-one Chemical compound CCCCCCCCCCCCCC(=O)CC LTMXHUUHBSCKEK-UHFFFAOYSA-N 0.000 description 2
- AMQJEAYHLZJPGS-UHFFFAOYSA-N N-Pentanol Chemical compound CCCCCO AMQJEAYHLZJPGS-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 150000007933 aliphatic carboxylic acids Chemical class 0.000 description 2
- LLEMOWNGBBNAJR-UHFFFAOYSA-N biphenyl-2-ol Chemical compound OC1=CC=CC=C1C1=CC=CC=C1 LLEMOWNGBBNAJR-UHFFFAOYSA-N 0.000 description 2
- 150000001733 carboxylic acid esters Chemical class 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- WTJKUFMLQFLJOT-UHFFFAOYSA-N heptadecan-9-one Chemical compound CCCCCCCCC(=O)CCCCCCCC WTJKUFMLQFLJOT-UHFFFAOYSA-N 0.000 description 2
- PQYGSSYFJIJDFK-UHFFFAOYSA-N heptyl ketone Chemical compound CCCCCCCC(=O)CCCCCCC PQYGSSYFJIJDFK-UHFFFAOYSA-N 0.000 description 2
- GARHHHWGJIXLDK-UHFFFAOYSA-N icosan-2-one Chemical compound CCCCCCCCCCCCCCCCCCC(C)=O GARHHHWGJIXLDK-UHFFFAOYSA-N 0.000 description 2
- 150000002596 lactones Chemical group 0.000 description 2
- 238000000034 method Methods 0.000 description 2
- PJLJQAWUAPNCJC-UHFFFAOYSA-N octadecan-2-one Chemical compound CCCCCCCCCCCCCCCCC(C)=O PJLJQAWUAPNCJC-UHFFFAOYSA-N 0.000 description 2
- DMCJFWXGXUEHFD-UHFFFAOYSA-N pentatriacontan-18-one Chemical compound CCCCCCCCCCCCCCCCCC(=O)CCCCCCCCCCCCCCCCC DMCJFWXGXUEHFD-UHFFFAOYSA-N 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- VARQGBHBYZTYLJ-UHFFFAOYSA-N tricosan-12-one Chemical compound CCCCCCCCCCCC(=O)CCCCCCCCCCC VARQGBHBYZTYLJ-UHFFFAOYSA-N 0.000 description 2
- CYIFVRUOHKNECG-UHFFFAOYSA-N tridecan-2-one Chemical compound CCCCCCCCCCCC(C)=O CYIFVRUOHKNECG-UHFFFAOYSA-N 0.000 description 2
- VMPHSYLJUKZBJJ-UHFFFAOYSA-N trilaurin Chemical compound CCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCC)COC(=O)CCCCCCCCCCC VMPHSYLJUKZBJJ-UHFFFAOYSA-N 0.000 description 2
- DUXYWXYOBMKGIN-UHFFFAOYSA-N trimyristin Chemical compound CCCCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCCCC)COC(=O)CCCCCCCCCCCCC DUXYWXYOBMKGIN-UHFFFAOYSA-N 0.000 description 2
- DCXXMTOCNZCJGO-UHFFFAOYSA-N tristearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCCCCCCCC)COC(=O)CCCCCCCCCCCCCCCCC DCXXMTOCNZCJGO-UHFFFAOYSA-N 0.000 description 2
- KYWIYKKSMDLRDC-UHFFFAOYSA-N undecan-2-one Chemical compound CCCCCCCCCC(C)=O KYWIYKKSMDLRDC-UHFFFAOYSA-N 0.000 description 2
- YNMZZHPSYMOGCI-UHFFFAOYSA-N undecan-3-one Chemical compound CCCCCCCCC(=O)CC YNMZZHPSYMOGCI-UHFFFAOYSA-N 0.000 description 2
- NBSLHMOSERBUOV-UHFFFAOYSA-N undecan-4-one Chemical compound CCCCCCCC(=O)CCC NBSLHMOSERBUOV-UHFFFAOYSA-N 0.000 description 2
- LIZLYZVAYZQVPG-UHFFFAOYSA-N (3-bromo-2-fluorophenyl)methanol Chemical compound OCC1=CC=CC(Br)=C1F LIZLYZVAYZQVPG-UHFFFAOYSA-N 0.000 description 1
- BZQDHZSCEMOENZ-UHFFFAOYSA-N (4-hydroxyphenyl) 2-methylbutanoate Chemical compound CCC(C)C(=O)OC1=CC=C(O)C=C1 BZQDHZSCEMOENZ-UHFFFAOYSA-N 0.000 description 1
- NKJOXAZJBOMXID-UHFFFAOYSA-N 1,1'-Oxybisoctane Chemical compound CCCCCCCCOCCCCCCCC NKJOXAZJBOMXID-UHFFFAOYSA-N 0.000 description 1
- HCNHNBLSNVSJTJ-UHFFFAOYSA-N 1,1-Bis(4-hydroxyphenyl)ethane Chemical compound C=1C=C(O)C=CC=1C(C)C1=CC=C(O)C=C1 HCNHNBLSNVSJTJ-UHFFFAOYSA-N 0.000 description 1
- GDDPLWAEEWIQKZ-UHFFFAOYSA-N 1,1-diethoxydecane Chemical compound CCCCCCCCCC(OCC)OCC GDDPLWAEEWIQKZ-UHFFFAOYSA-N 0.000 description 1
- ZQNOIYUMSNPIGA-UHFFFAOYSA-N 1,1-diethoxyundecane Chemical compound CCCCCCCCCCC(OCC)OCC ZQNOIYUMSNPIGA-UHFFFAOYSA-N 0.000 description 1
- TYJRTUKWJFOYFK-UHFFFAOYSA-N 1,1-dimethoxytridecane Chemical compound CCCCCCCCCCCCC(OC)OC TYJRTUKWJFOYFK-UHFFFAOYSA-N 0.000 description 1
- FBJUQTUWWCVIDH-UHFFFAOYSA-N 1,1-dimethoxyundecane Chemical compound CCCCCCCCCCC(OC)OC FBJUQTUWWCVIDH-UHFFFAOYSA-N 0.000 description 1
- MQESVSITPLILCO-UHFFFAOYSA-N 1-(4-butylphenyl)ethanone Chemical compound CCCCC1=CC=C(C(C)=O)C=C1 MQESVSITPLILCO-UHFFFAOYSA-N 0.000 description 1
- UQBRZOXCKKBKDU-UHFFFAOYSA-N 1-(4-heptylphenyl)ethanone Chemical compound CCCCCCCC1=CC=C(C(C)=O)C=C1 UQBRZOXCKKBKDU-UHFFFAOYSA-N 0.000 description 1
- WWBVHJKFJZBRSO-UHFFFAOYSA-N 1-(4-hexylphenyl)ethanone Chemical compound CCCCCCC1=CC=C(C(C)=O)C=C1 WWBVHJKFJZBRSO-UHFFFAOYSA-N 0.000 description 1
- PWRSUUUQEQAMEV-UHFFFAOYSA-N 1-(4-nonylphenyl)ethanone Chemical compound CCCCCCCCCC1=CC=C(C(C)=O)C=C1 PWRSUUUQEQAMEV-UHFFFAOYSA-N 0.000 description 1
- AQNYEAINONORRY-UHFFFAOYSA-N 1-(4-tert-butylphenyl)propan-1-one Chemical compound CCC(=O)C1=CC=C(C(C)(C)C)C=C1 AQNYEAINONORRY-UHFFFAOYSA-N 0.000 description 1
- KEAGRYYGYWZVPC-UHFFFAOYSA-N 1-[4-(2-methylpropyl)phenyl]ethanone Chemical compound CC(C)CC1=CC=C(C(C)=O)C=C1 KEAGRYYGYWZVPC-UHFFFAOYSA-N 0.000 description 1
- LTSWUFKUZPPYEG-UHFFFAOYSA-N 1-decoxydecane Chemical compound CCCCCCCCCCOCCCCCCCCCC LTSWUFKUZPPYEG-UHFFFAOYSA-N 0.000 description 1
- CMCBDXRRFKYBDG-UHFFFAOYSA-N 1-dodecoxydodecane Chemical compound CCCCCCCCCCCCOCCCCCCCCCCCC CMCBDXRRFKYBDG-UHFFFAOYSA-N 0.000 description 1
- UJEGHEMJVNQWOJ-UHFFFAOYSA-N 1-heptoxyheptane Chemical compound CCCCCCCOCCCCCCC UJEGHEMJVNQWOJ-UHFFFAOYSA-N 0.000 description 1
- FDCJDKXCCYFOCV-UHFFFAOYSA-N 1-hexadecoxyhexadecane Chemical compound CCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCC FDCJDKXCCYFOCV-UHFFFAOYSA-N 0.000 description 1
- BPIUIOXAFBGMNB-UHFFFAOYSA-N 1-hexoxyhexane Chemical compound CCCCCCOCCCCCC BPIUIOXAFBGMNB-UHFFFAOYSA-N 0.000 description 1
- QQLIGMASAVJVON-UHFFFAOYSA-N 1-naphthalen-1-ylethanone Chemical compound C1=CC=C2C(C(=O)C)=CC=CC2=C1 QQLIGMASAVJVON-UHFFFAOYSA-N 0.000 description 1
- DKZRLCHWDNEKRH-UHFFFAOYSA-N 1-nonoxynonane Chemical compound CCCCCCCCCOCCCCCCCCC DKZRLCHWDNEKRH-UHFFFAOYSA-N 0.000 description 1
- HBXWUCXDUUJDRB-UHFFFAOYSA-N 1-octadecoxyoctadecane Chemical compound CCCCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCCCC HBXWUCXDUUJDRB-UHFFFAOYSA-N 0.000 description 1
- YGUGZXZLWIADHU-UHFFFAOYSA-N 1-pentadecoxypentadecane Chemical compound CCCCCCCCCCCCCCCOCCCCCCCCCCCCCCC YGUGZXZLWIADHU-UHFFFAOYSA-N 0.000 description 1
- AOPDRZXCEAKHHW-UHFFFAOYSA-N 1-pentoxypentane Chemical compound CCCCCOCCCCC AOPDRZXCEAKHHW-UHFFFAOYSA-N 0.000 description 1
- DYQAZJQDLPPHNB-UHFFFAOYSA-N 1-phenyl-2-hexanone Chemical compound CCCCC(=O)CC1=CC=CC=C1 DYQAZJQDLPPHNB-UHFFFAOYSA-N 0.000 description 1
- QQXJNLYVPPBERR-UHFFFAOYSA-N 1-phenyldecan-1-one Chemical compound CCCCCCCCCC(=O)C1=CC=CC=C1 QQXJNLYVPPBERR-UHFFFAOYSA-N 0.000 description 1
- VUXIOSYYRVXOOT-UHFFFAOYSA-N 1-phenylheptadecan-1-one Chemical compound CCCCCCCCCCCCCCCCC(=O)C1=CC=CC=C1 VUXIOSYYRVXOOT-UHFFFAOYSA-N 0.000 description 1
- IIOLAWJMOGLOIB-UHFFFAOYSA-N 1-phenylhexadecan-1-one Chemical compound CCCCCCCCCCCCCCCC(=O)C1=CC=CC=C1 IIOLAWJMOGLOIB-UHFFFAOYSA-N 0.000 description 1
- MAHPVQDVMLWUAG-UHFFFAOYSA-N 1-phenylhexan-1-one Chemical compound CCCCCC(=O)C1=CC=CC=C1 MAHPVQDVMLWUAG-UHFFFAOYSA-N 0.000 description 1
- DBLXXVQTWJFJFI-UHFFFAOYSA-N 1-phenyloctadecan-1-one Chemical compound CCCCCCCCCCCCCCCCCC(=O)C1=CC=CC=C1 DBLXXVQTWJFJFI-UHFFFAOYSA-N 0.000 description 1
- UDEVCZRUNOLVLU-UHFFFAOYSA-N 1-phenyloctan-1-one Chemical compound CCCCCCCC(=O)C1=CC=CC=C1 UDEVCZRUNOLVLU-UHFFFAOYSA-N 0.000 description 1
- SDNCECLJQYEDRK-UHFFFAOYSA-N 1-phenylpentadecan-1-one Chemical compound CCCCCCCCCCCCCCC(=O)C1=CC=CC=C1 SDNCECLJQYEDRK-UHFFFAOYSA-N 0.000 description 1
- LXUIUVLDNRQBQJ-UHFFFAOYSA-N 1-phenyltetradecan-1-one Chemical compound CCCCCCCCCCCCCC(=O)C1=CC=CC=C1 LXUIUVLDNRQBQJ-UHFFFAOYSA-N 0.000 description 1
- ZZNDQCACFUJAKJ-UHFFFAOYSA-N 1-phenyltridecan-1-one Chemical compound CCCCCCCCCCCCC(=O)C1=CC=CC=C1 ZZNDQCACFUJAKJ-UHFFFAOYSA-N 0.000 description 1
- LHJBFOGCFZHBAJ-UHFFFAOYSA-N 1-phenylundecan-1-one Chemical compound CCCCCCCCCCC(=O)C1=CC=CC=C1 LHJBFOGCFZHBAJ-UHFFFAOYSA-N 0.000 description 1
- HANWHVWXFQSQGJ-UHFFFAOYSA-N 1-tetradecoxytetradecane Chemical compound CCCCCCCCCCCCCCOCCCCCCCCCCCCCC HANWHVWXFQSQGJ-UHFFFAOYSA-N 0.000 description 1
- CSHOPPGMNYULAD-UHFFFAOYSA-N 1-tridecoxytridecane Chemical compound CCCCCCCCCCCCCOCCCCCCCCCCCCC CSHOPPGMNYULAD-UHFFFAOYSA-N 0.000 description 1
- TXYKVMGAIGVXFY-UHFFFAOYSA-N 1-undecoxyundecane Chemical compound CCCCCCCCCCCOCCCCCCCCCCC TXYKVMGAIGVXFY-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- VQWGCFKMUFNLIK-UHFFFAOYSA-N 2-[2-(4-dodecoxy-3-methoxyphenyl)ethenyl]quinoline Chemical compound C1=C(OC)C(OCCCCCCCCCCCC)=CC=C1C=CC1=CC=C(C=CC=C2)C2=N1 VQWGCFKMUFNLIK-UHFFFAOYSA-N 0.000 description 1
- XSAYZAUNJMRRIR-UHFFFAOYSA-N 2-acetylnaphthalene Chemical compound C1=CC=CC2=CC(C(=O)C)=CC=C21 XSAYZAUNJMRRIR-UHFFFAOYSA-N 0.000 description 1
- UXGVMFHEKMGWMA-UHFFFAOYSA-N 2-benzofuran Chemical compound C1=CC=CC2=COC=C21 UXGVMFHEKMGWMA-UHFFFAOYSA-N 0.000 description 1
- CBMGWFGJZMYIKU-UHFFFAOYSA-N 2-cyclohexyl-4,6-bis[(2-hydroxy-5-methylphenyl)methyl]phenol Chemical compound CC1=CC=C(O)C(CC=2C=C(C(O)=C(CC=3C(=CC=C(C)C=3)O)C=2)C2CCCCC2)=C1 CBMGWFGJZMYIKU-UHFFFAOYSA-N 0.000 description 1
- TUBNHXBTFDDYPI-UHFFFAOYSA-N 2-cyclohexyl-4-[(5-cyclohexyl-4-hydroxy-2-methylphenyl)-(4-hydroxyphenyl)methyl]-5-methylphenol Chemical compound CC1=CC(O)=C(C2CCCCC2)C=C1C(C=1C(=CC(O)=C(C2CCCCC2)C=1)C)C1=CC=C(O)C=C1 TUBNHXBTFDDYPI-UHFFFAOYSA-N 0.000 description 1
- CYEJMVLDXAUOPN-UHFFFAOYSA-N 2-dodecylphenol Chemical group CCCCCCCCCCCCC1=CC=CC=C1O CYEJMVLDXAUOPN-UHFFFAOYSA-N 0.000 description 1
- HSMPBMPAFKENTP-UHFFFAOYSA-N 2-ethyl-4-(3-ethyl-4-hydroxyphenyl)sulfanylphenol Chemical compound C1=C(O)C(CC)=CC(SC=2C=C(CC)C(O)=CC=2)=C1 HSMPBMPAFKENTP-UHFFFAOYSA-N 0.000 description 1
- WWIMLMKKVDHIRI-UHFFFAOYSA-N 2-hexyl-4-(3-hexyl-4-hydroxyphenyl)sulfanylphenol Chemical compound C1=C(O)C(CCCCCC)=CC(SC=2C=C(CCCCCC)C(O)=CC=2)=C1 WWIMLMKKVDHIRI-UHFFFAOYSA-N 0.000 description 1
- JADYBWICRJWGBW-UHFFFAOYSA-N 2-hydroxy-3-(tetradecanoyloxy)propyl tetradecanoate Chemical compound CCCCCCCCCCCCCC(=O)OCC(O)COC(=O)CCCCCCCCCCCCC JADYBWICRJWGBW-UHFFFAOYSA-N 0.000 description 1
- DUIOKRXOKLLURE-UHFFFAOYSA-N 2-octylphenol Chemical group CCCCCCCCC1=CC=CC=C1O DUIOKRXOKLLURE-UHFFFAOYSA-N 0.000 description 1
- XHALKWMTKWHQLO-UHFFFAOYSA-N 2-tert-butyl-4-(3-tert-butyl-4-hydroxyphenyl)sulfanylphenol Chemical compound C1=C(O)C(C(C)(C)C)=CC(SC=2C=C(C(O)=CC=2)C(C)(C)C)=C1 XHALKWMTKWHQLO-UHFFFAOYSA-N 0.000 description 1
- GRIKUIPJBHJPPN-UHFFFAOYSA-N 3',6'-dimethoxyspiro[2-benzofuran-3,9'-xanthene]-1-one Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(OC)C=C1OC1=CC(OC)=CC=C21 GRIKUIPJBHJPPN-UHFFFAOYSA-N 0.000 description 1
- YMTYZTXUZLQUSF-UHFFFAOYSA-N 3,3'-Dimethylbisphenol A Chemical compound C1=C(O)C(C)=CC(C(C)(C)C=2C=C(C)C(O)=CC=2)=C1 YMTYZTXUZLQUSF-UHFFFAOYSA-N 0.000 description 1
- JZEPXWWZAJGALH-UHFFFAOYSA-N 3,3-bis(1-butyl-2-methylindol-3-yl)-2-benzofuran-1-one Chemical compound C1=CC=C2C(C3(C4=CC=CC=C4C(=O)O3)C3=C(C)N(C4=CC=CC=C43)CCCC)=C(C)N(CCCC)C2=C1 JZEPXWWZAJGALH-UHFFFAOYSA-N 0.000 description 1
- XBCTUDRVBSOUQD-UHFFFAOYSA-N 3-(1h-indol-2-yl)-3-phenyl-2-benzofuran-1-one Chemical class C12=CC=CC=C2C(=O)OC1(C=1NC2=CC=CC=C2C=1)C1=CC=CC=C1 XBCTUDRVBSOUQD-UHFFFAOYSA-N 0.000 description 1
- UYMBCDOGDVGEFA-UHFFFAOYSA-N 3-(1h-indol-2-yl)-3h-2-benzofuran-1-one Chemical class C12=CC=CC=C2C(=O)OC1C1=CC2=CC=CC=C2N1 UYMBCDOGDVGEFA-UHFFFAOYSA-N 0.000 description 1
- HOUWRQXIBSGOHF-UHFFFAOYSA-N 3-[4-(diethylamino)phenyl]-3-(1-ethyl-2-methylindol-3-yl)-2-benzofuran-1-one Chemical compound C1=CC(N(CC)CC)=CC=C1C1(C=2C3=CC=CC=C3N(CC)C=2C)C2=CC=CC=C2C(=O)O1 HOUWRQXIBSGOHF-UHFFFAOYSA-N 0.000 description 1
- BJEMXPVDXFSROA-UHFFFAOYSA-N 3-butylbenzene-1,2-diol Chemical group CCCCC1=CC=CC(O)=C1O BJEMXPVDXFSROA-UHFFFAOYSA-N 0.000 description 1
- SVAPVDMWXJVISW-UHFFFAOYSA-N 3h-2-benzofuran-1-one;benzylbenzene Chemical class C1=CC=C2C(=O)OCC2=C1.C=1C=CC=CC=1CC1=CC=CC=C1 SVAPVDMWXJVISW-UHFFFAOYSA-N 0.000 description 1
- ZGZVGZCIFZBNCN-UHFFFAOYSA-N 4,4'-(2-Methylpropylidene)bisphenol Chemical compound C=1C=C(O)C=CC=1C(C(C)C)C1=CC=C(O)C=C1 ZGZVGZCIFZBNCN-UHFFFAOYSA-N 0.000 description 1
- VWGKEVWFBOUAND-UHFFFAOYSA-N 4,4'-thiodiphenol Chemical compound C1=CC(O)=CC=C1SC1=CC=C(O)C=C1 VWGKEVWFBOUAND-UHFFFAOYSA-N 0.000 description 1
- NMWKWBPNKPGATC-UHFFFAOYSA-N 4,5,6,7-tetrachloro-2-benzofuran-1(3H)-one Chemical compound ClC1=C(Cl)C(Cl)=C2COC(=O)C2=C1Cl NMWKWBPNKPGATC-UHFFFAOYSA-N 0.000 description 1
- QFHQFVJGMQSORR-UHFFFAOYSA-N 4,5,6,7-tetrachloro-3-[4-(diethylamino)-2-ethoxyphenyl]-3-(1-ethyl-2-methylindol-3-yl)-2-benzofuran-1-one Chemical compound CCOC1=CC(N(CC)CC)=CC=C1C1(C=2C3=CC=CC=C3N(CC)C=2C)C(C(Cl)=C(Cl)C(Cl)=C2Cl)=C2C(=O)O1 QFHQFVJGMQSORR-UHFFFAOYSA-N 0.000 description 1
- KXNGHSFCHPSAOV-UHFFFAOYSA-N 4,6-bis[(4-hydroxyphenyl)methyl]benzene-1,3-diol Chemical compound C1=CC(O)=CC=C1CC1=CC(CC=2C=CC(O)=CC=2)=C(O)C=C1O KXNGHSFCHPSAOV-UHFFFAOYSA-N 0.000 description 1
- VBWOZLRBXCGUHD-UHFFFAOYSA-N 4-(4-hydroxy-3,5-dipropylphenyl)sulfanyl-2,6-dipropylphenol Chemical compound CCCC1=C(O)C(CCC)=CC(SC=2C=C(CCC)C(O)=C(CCC)C=2)=C1 VBWOZLRBXCGUHD-UHFFFAOYSA-N 0.000 description 1
- IBNFPRMKLZDANU-UHFFFAOYSA-N 4-(4-hydroxy-3-methylphenyl)sulfanyl-2-methylphenol Chemical compound C1=C(O)C(C)=CC(SC=2C=C(C)C(O)=CC=2)=C1 IBNFPRMKLZDANU-UHFFFAOYSA-N 0.000 description 1
- OQOWCTSSBAKQTR-UHFFFAOYSA-N 4-(4-hydroxy-3-pentylphenyl)sulfanyl-2-pentylphenol Chemical compound C1=C(O)C(CCCCC)=CC(SC=2C=C(CCCCC)C(O)=CC=2)=C1 OQOWCTSSBAKQTR-UHFFFAOYSA-N 0.000 description 1
- PSVHQRAAAHMGSH-UHFFFAOYSA-N 4-(4-hydroxy-3-propylphenyl)sulfanyl-2-propylphenol Chemical compound C1=C(O)C(CCC)=CC(SC=2C=C(CCC)C(O)=CC=2)=C1 PSVHQRAAAHMGSH-UHFFFAOYSA-N 0.000 description 1
- WJWLOPSPRRVVLR-UHFFFAOYSA-N 4-[(2-hydroxyphenyl)-(4-hydroxy-2,3,5-triphenylphenyl)methyl]-2,3,6-triphenylphenol Chemical compound OC1=CC=CC=C1C(C=1C(=C(C=2C=CC=CC=2)C(O)=C(C=2C=CC=CC=2)C=1)C=1C=CC=CC=1)C1=CC(C=2C=CC=CC=2)=C(O)C(C=2C=CC=CC=2)=C1C1=CC=CC=C1 WJWLOPSPRRVVLR-UHFFFAOYSA-N 0.000 description 1
- SRKIZOFXPUNFBI-UHFFFAOYSA-N 4-[(4-hydroxy-3,5-dimethylphenyl)-(4-hydroxy-3-methoxyphenyl)methyl]-2,6-dimethylphenol Chemical compound C1=C(O)C(OC)=CC(C(C=2C=C(C)C(O)=C(C)C=2)C=2C=C(C)C(O)=C(C)C=2)=C1 SRKIZOFXPUNFBI-UHFFFAOYSA-N 0.000 description 1
- OXJMWJCOJFLNJE-UHFFFAOYSA-N 4-[(4-hydroxy-3-methylphenyl)-(4-hydroxyphenyl)methyl]-2-methylphenol Chemical compound C1=C(O)C(C)=CC(C(C=2C=CC(O)=CC=2)C=2C=C(C)C(O)=CC=2)=C1 OXJMWJCOJFLNJE-UHFFFAOYSA-N 0.000 description 1
- RSSGMIIGVQRGDS-UHFFFAOYSA-N 4-[(4-hydroxyphenyl)-phenylmethyl]phenol Chemical compound C1=CC(O)=CC=C1C(C=1C=CC(O)=CC=1)C1=CC=CC=C1 RSSGMIIGVQRGDS-UHFFFAOYSA-N 0.000 description 1
- ICYDRUIZSPKQOH-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)decyl]phenol Chemical compound C=1C=C(O)C=CC=1C(CCCCCCCCC)C1=CC=C(O)C=C1 ICYDRUIZSPKQOH-UHFFFAOYSA-N 0.000 description 1
- YMZDMPPYBDUSMI-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)dodecyl]phenol Chemical compound C=1C=C(O)C=CC=1C(CCCCCCCCCCC)C1=CC=C(O)C=C1 YMZDMPPYBDUSMI-UHFFFAOYSA-N 0.000 description 1
- CZCLTCVIZZPPBW-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)heptyl]phenol Chemical compound C=1C=C(O)C=CC=1C(CCCCCC)C1=CC=C(O)C=C1 CZCLTCVIZZPPBW-UHFFFAOYSA-N 0.000 description 1
- WKGVDZYQWLBSQC-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)hexyl]phenol Chemical compound C=1C=C(O)C=CC=1C(CCCCC)C1=CC=C(O)C=C1 WKGVDZYQWLBSQC-UHFFFAOYSA-N 0.000 description 1
- OUKOUEHLRVEKCJ-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)nonyl]phenol Chemical compound C=1C=C(O)C=CC=1C(CCCCCCCC)C1=CC=C(O)C=C1 OUKOUEHLRVEKCJ-UHFFFAOYSA-N 0.000 description 1
- VHLLJTHDWPAQEM-UHFFFAOYSA-N 4-[2-(4-hydroxyphenyl)-4-methylpentan-2-yl]phenol Chemical compound C=1C=C(O)C=CC=1C(C)(CC(C)C)C1=CC=C(O)C=C1 VHLLJTHDWPAQEM-UHFFFAOYSA-N 0.000 description 1
- XHQYAMKBTLODDV-UHFFFAOYSA-N 4-[2-(4-hydroxyphenyl)heptan-2-yl]phenol Chemical compound C=1C=C(O)C=CC=1C(C)(CCCCC)C1=CC=C(O)C=C1 XHQYAMKBTLODDV-UHFFFAOYSA-N 0.000 description 1
- UWFUILMHBCVIMK-UHFFFAOYSA-N 4-[bis(4-hydroxy-3,5-dimethylphenyl)methyl]benzene-1,2-diol Chemical compound CC1=C(O)C(C)=CC(C(C=2C=C(O)C(O)=CC=2)C=2C=C(C)C(O)=C(C)C=2)=C1 UWFUILMHBCVIMK-UHFFFAOYSA-N 0.000 description 1
- GZFGOTFRPZRKDS-UHFFFAOYSA-N 4-bromophenol Chemical compound OC1=CC=C(Br)C=C1 GZFGOTFRPZRKDS-UHFFFAOYSA-N 0.000 description 1
- TTWBMGNNEJOEOJ-UHFFFAOYSA-N 4-chloro-n-fluorocyclohexan-1-amine Chemical compound FNC1CCC(Cl)CC1 TTWBMGNNEJOEOJ-UHFFFAOYSA-N 0.000 description 1
- WXNZTHHGJRFXKQ-UHFFFAOYSA-N 4-chlorophenol Chemical compound OC1=CC=C(Cl)C=C1 WXNZTHHGJRFXKQ-UHFFFAOYSA-N 0.000 description 1
- ZBCATMYQYDCTIZ-UHFFFAOYSA-N 4-methylcatechol Chemical compound CC1=CC=C(O)C(O)=C1 ZBCATMYQYDCTIZ-UHFFFAOYSA-N 0.000 description 1
- NTDQQZYCCIDJRK-UHFFFAOYSA-N 4-octylphenol Chemical compound CCCCCCCCC1=CC=C(O)C=C1 NTDQQZYCCIDJRK-UHFFFAOYSA-N 0.000 description 1
- SKVLHBJJOXTLKQ-UHFFFAOYSA-N 7,7-bis[4-(diethylamino)-2-ethoxyphenyl]furo[3,4-b]pyridin-5-one Chemical compound CCOC1=CC(N(CC)CC)=CC=C1C1(C=2C(=CC(=CC=2)N(CC)CC)OCC)C2=NC=CC=C2C(=O)O1 SKVLHBJJOXTLKQ-UHFFFAOYSA-N 0.000 description 1
- CATPNSYLEMYNJK-UHFFFAOYSA-N 7-[2-ethoxy-4-(n-ethylanilino)phenyl]-7-(1-ethyl-2-methylindol-3-yl)furo[3,4-b]pyridin-5-one Chemical compound C=1C=C(C2(C3=NC=CC=C3C(=O)O2)C=2C3=CC=CC=C3N(CC)C=2C)C(OCC)=CC=1N(CC)C1=CC=CC=C1 CATPNSYLEMYNJK-UHFFFAOYSA-N 0.000 description 1
- HTVITOHKHWFJKO-UHFFFAOYSA-N Bisphenol B Chemical compound C=1C=C(O)C=CC=1C(C)(CC)C1=CC=C(O)C=C1 HTVITOHKHWFJKO-UHFFFAOYSA-N 0.000 description 1
- 239000007848 Bronsted acid Substances 0.000 description 1
- QFOHBWFCKVYLES-UHFFFAOYSA-N Butylparaben Chemical compound CCCCOC(=O)C1=CC=C(O)C=C1 QFOHBWFCKVYLES-UHFFFAOYSA-N 0.000 description 1
- 0 CC(*N)(c1ccccc1)c1ccccc1 Chemical compound CC(*N)(c1ccccc1)c1ccccc1 0.000 description 1
- AJUWUYJULVYGRA-UHFFFAOYSA-N Dodecanal dimethyl acetal Chemical compound CCCCCCCCCCCC(OC)OC AJUWUYJULVYGRA-UHFFFAOYSA-N 0.000 description 1
- RPWFJAMTCNSJKK-UHFFFAOYSA-N Dodecyl gallate Chemical compound CCCCCCCCCCCCOC(=O)C1=CC(O)=C(O)C(O)=C1 RPWFJAMTCNSJKK-UHFFFAOYSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- VUVUIDMZOWHIIJ-UHFFFAOYSA-N Heneicosan-2-one Chemical compound CCCCCCCCCCCCCCCCCCCC(C)=O VUVUIDMZOWHIIJ-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- HSGQXSBXGSRINJ-UHFFFAOYSA-N Nonyl octanoate Chemical compound CCCCCCCCCOC(=O)CCCCCCC HSGQXSBXGSRINJ-UHFFFAOYSA-N 0.000 description 1
- IGFHQQFPSIBGKE-UHFFFAOYSA-N Nonylphenol Chemical group CCCCCCCCCC1=CC=C(O)C=C1 IGFHQQFPSIBGKE-UHFFFAOYSA-N 0.000 description 1
- AAAIZLQILBFRTJ-UHFFFAOYSA-N Pentadecyl acetate Chemical compound CCCCCCCCCCCCCCCOC(C)=O AAAIZLQILBFRTJ-UHFFFAOYSA-N 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- AMNPXXIGUOKIPP-UHFFFAOYSA-N [4-(carbamothioylamino)phenyl]thiourea Chemical compound NC(=S)NC1=CC=C(NC(N)=S)C=C1 AMNPXXIGUOKIPP-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000000862 absorption spectrum Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 229940116224 behenate Drugs 0.000 description 1
- VHNFAQLOVBWGGB-UHFFFAOYSA-N benzhydrylbenzene;3h-2-benzofuran-1-one Chemical class C1=CC=C2C(=O)OCC2=C1.C1=CC=CC=C1C(C=1C=CC=CC=1)C1=CC=CC=C1 VHNFAQLOVBWGGB-UHFFFAOYSA-N 0.000 description 1
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 1
- ZFVMWEVVKGLCIJ-UHFFFAOYSA-N bisphenol AF Chemical compound C1=CC(O)=CC=C1C(C(F)(F)F)(C(F)(F)F)C1=CC=C(O)C=C1 ZFVMWEVVKGLCIJ-UHFFFAOYSA-N 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 229940114081 cinnamate Drugs 0.000 description 1
- 239000000084 colloidal system Substances 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- VYDIMQRLNMMJBW-UHFFFAOYSA-N cyclopentyl(phenyl)methanone Chemical compound C=1C=CC=CC=1C(=O)C1CCCC1 VYDIMQRLNMMJBW-UHFFFAOYSA-N 0.000 description 1
- MKJDUHZPLQYUCB-UHFFFAOYSA-N decan-4-one Chemical compound CCCCCCC(=O)CCC MKJDUHZPLQYUCB-UHFFFAOYSA-N 0.000 description 1
- INSRQEMEVAMETL-UHFFFAOYSA-N decane-1,1-diol Chemical compound CCCCCCCCCC(O)O INSRQEMEVAMETL-UHFFFAOYSA-N 0.000 description 1
- 229940028820 didecyl ether Drugs 0.000 description 1
- GHKVUVOPHDYRJC-UHFFFAOYSA-N didodecyl hexanedioate Chemical compound CCCCCCCCCCCCOC(=O)CCCCC(=O)OCCCCCCCCCCCC GHKVUVOPHDYRJC-UHFFFAOYSA-N 0.000 description 1
- RQIKFACUZHNEDV-UHFFFAOYSA-N dihexadecyl hexanedioate Chemical compound CCCCCCCCCCCCCCCCOC(=O)CCCCC(=O)OCCCCCCCCCCCCCCCC RQIKFACUZHNEDV-UHFFFAOYSA-N 0.000 description 1
- GYFBKUFUJKHFLZ-UHFFFAOYSA-N dioctadecyl hexanedioate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)CCCCC(=O)OCCCCCCCCCCCCCCCCCC GYFBKUFUJKHFLZ-UHFFFAOYSA-N 0.000 description 1
- CZZYITDELCSZES-UHFFFAOYSA-N diphenylmethane Chemical compound C=1C=CC=CC=1CC1=CC=CC=C1 CZZYITDELCSZES-UHFFFAOYSA-N 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- QZQPCVVMCYMSFX-UHFFFAOYSA-N ditetradecyl hexanedioate Chemical compound CCCCCCCCCCCCCCOC(=O)CCCCC(=O)OCCCCCCCCCCCCCC QZQPCVVMCYMSFX-UHFFFAOYSA-N 0.000 description 1
- TWBHLKOHVHGYGC-UHFFFAOYSA-N docosan-2-one Chemical compound CCCCCCCCCCCCCCCCCCCCC(C)=O TWBHLKOHVHGYGC-UHFFFAOYSA-N 0.000 description 1
- PERIHWAPLOBAJM-UHFFFAOYSA-N dodecan-3-one Chemical compound CCCCCCCCCC(=O)CC PERIHWAPLOBAJM-UHFFFAOYSA-N 0.000 description 1
- AVQSOIZWTINZLU-UHFFFAOYSA-N dodecan-4-one Chemical compound CCCCCCCCC(=O)CCC AVQSOIZWTINZLU-UHFFFAOYSA-N 0.000 description 1
- DOXYUCZSYSEALW-UHFFFAOYSA-N dodecan-5-one Chemical compound CCCCCCCC(=O)CCCC DOXYUCZSYSEALW-UHFFFAOYSA-N 0.000 description 1
- 229940080643 dodecyl gallate Drugs 0.000 description 1
- 235000010386 dodecyl gallate Nutrition 0.000 description 1
- 239000000555 dodecyl gallate Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 125000000219 ethylidene group Chemical group [H]C(=[*])C([H])([H])[H] 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- UHUSDOQQWJGJQS-UHFFFAOYSA-N glycerol 1,2-dioctadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(CO)OC(=O)CCCCCCCCCCCCCCCCC UHUSDOQQWJGJQS-UHFFFAOYSA-N 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- MPLLSYWBBPPERF-UHFFFAOYSA-N heptyl decanoate Chemical compound CCCCCCCCCC(=O)OCCCCCCC MPLLSYWBBPPERF-UHFFFAOYSA-N 0.000 description 1
- RLVQDVJFVFDINC-UHFFFAOYSA-N heptyl hexadecanoate Chemical compound CCCCCCCCCCCCCCCC(=O)OCCCCCCC RLVQDVJFVFDINC-UHFFFAOYSA-N 0.000 description 1
- MFCQPVRHCQCFBB-UHFFFAOYSA-N heptyl tetradecanoate Chemical compound CCCCCCCCCCCCCC(=O)OCCCCCCC MFCQPVRHCQCFBB-UHFFFAOYSA-N 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 1
- ZEZOYRQXQABJSR-UHFFFAOYSA-N icosan-10-one Chemical compound CCCCCCCCCCC(=O)CCCCCCCCC ZEZOYRQXQABJSR-UHFFFAOYSA-N 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- POULHZVOKOAJMA-UHFFFAOYSA-N methyl undecanoic acid Natural products CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229940105132 myristate Drugs 0.000 description 1
- FIIGZGVXXBOCPL-UHFFFAOYSA-N n-fluoro-3-methylcyclohexan-1-amine Chemical compound CC1CCCC(NF)C1 FIIGZGVXXBOCPL-UHFFFAOYSA-N 0.000 description 1
- BKIMMITUMNQMOS-UHFFFAOYSA-N nonane Chemical compound CCCCCCCCC BKIMMITUMNQMOS-UHFFFAOYSA-N 0.000 description 1
- PFUPABFCHVRLLY-UHFFFAOYSA-N nonanophenone Chemical compound CCCCCCCCC(=O)C1=CC=CC=C1 PFUPABFCHVRLLY-UHFFFAOYSA-N 0.000 description 1
- JZHKSJXMXQZMCR-UHFFFAOYSA-N nonyl decanoate Chemical compound CCCCCCCCCOC(=O)CCCCCCCCC JZHKSJXMXQZMCR-UHFFFAOYSA-N 0.000 description 1
- RXKFMSCHUQBPQZ-UHFFFAOYSA-N nonyl docosanoate Chemical compound CCCCCCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCC RXKFMSCHUQBPQZ-UHFFFAOYSA-N 0.000 description 1
- LZFVXMOMDUCLJV-UHFFFAOYSA-N nonyl dodecanoate Chemical compound CCCCCCCCCCCC(=O)OCCCCCCCCC LZFVXMOMDUCLJV-UHFFFAOYSA-N 0.000 description 1
- YPVZSWAJJTUWSN-UHFFFAOYSA-N nonyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCC YPVZSWAJJTUWSN-UHFFFAOYSA-N 0.000 description 1
- SDPZWRKQPQDSQW-UHFFFAOYSA-N nonyl palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OCCCCCCCCC SDPZWRKQPQDSQW-UHFFFAOYSA-N 0.000 description 1
- DBUPMBVQCHHADZ-UHFFFAOYSA-N nonyl tetradecanoate Chemical compound CCCCCCCCCCCCCC(=O)OCCCCCCCCC DBUPMBVQCHHADZ-UHFFFAOYSA-N 0.000 description 1
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical group CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- RIKCMEDSBFQFAL-UHFFFAOYSA-N octyl 4-hydroxybenzoate Chemical compound CCCCCCCCOC(=O)C1=CC=C(O)C=C1 RIKCMEDSBFQFAL-UHFFFAOYSA-N 0.000 description 1
- 235000010292 orthophenyl phenol Nutrition 0.000 description 1
- GARQDIVXKVBJFP-UHFFFAOYSA-N p-Octylacetophenone Chemical compound CCCCCCCCC1=CC=C(C(C)=O)C=C1 GARQDIVXKVBJFP-UHFFFAOYSA-N 0.000 description 1
- BLUCLILBMXJZEJ-UHFFFAOYSA-N pentadecyl butyrate Chemical compound CCCCCCCCCCCCCCCOC(=O)CCC BLUCLILBMXJZEJ-UHFFFAOYSA-N 0.000 description 1
- IZLXNLCCESMPCA-UHFFFAOYSA-N pentadecyl decanoate Chemical compound CCCCCCCCCCCCCCCOC(=O)CCCCCCCCC IZLXNLCCESMPCA-UHFFFAOYSA-N 0.000 description 1
- CNUKXAPRIPMHEX-UHFFFAOYSA-N pentadecyl docosanoate Chemical compound CCCCCCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCCCCCC CNUKXAPRIPMHEX-UHFFFAOYSA-N 0.000 description 1
- XRONBWIVNVRBIF-UHFFFAOYSA-N pentadecyl dodecanoate Chemical compound CCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCC XRONBWIVNVRBIF-UHFFFAOYSA-N 0.000 description 1
- ZJJQVISBZSCPCM-UHFFFAOYSA-N pentadecyl hexadecanoate Chemical compound CCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCCCC ZJJQVISBZSCPCM-UHFFFAOYSA-N 0.000 description 1
- YYYQIRQULKVEKH-UHFFFAOYSA-N pentadecyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCCCCCC YYYQIRQULKVEKH-UHFFFAOYSA-N 0.000 description 1
- IKYYXKWKFNBGJA-UHFFFAOYSA-N pentadecyl octanoate Chemical compound CCCCCCCCCCCCCCCOC(=O)CCCCCCC IKYYXKWKFNBGJA-UHFFFAOYSA-N 0.000 description 1
- PQWBDPUBNMEITD-UHFFFAOYSA-N pentyl dodecanoate Chemical compound CCCCCCCCCCCC(=O)OCCCCC PQWBDPUBNMEITD-UHFFFAOYSA-N 0.000 description 1
- YGDMPMKCHSXJJF-UHFFFAOYSA-N pentyl hexadecanoate Chemical compound CCCCCCCCCCCCCCCC(=O)OCCCCC YGDMPMKCHSXJJF-UHFFFAOYSA-N 0.000 description 1
- QPXYWTUZRZEUAK-UHFFFAOYSA-N pentyl tetradecanoate Chemical compound CCCCCCCCCCCCCC(=O)OCCCCC QPXYWTUZRZEUAK-UHFFFAOYSA-N 0.000 description 1
- 150000003014 phosphoric acid esters Chemical class 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 229960001755 resorcinol Drugs 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 125000003003 spiro group Chemical group 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- ZDIXOWNDGFVYNK-UHFFFAOYSA-N tridecan-3-one Chemical compound CCCCCCCCCCC(=O)CC ZDIXOWNDGFVYNK-UHFFFAOYSA-N 0.000 description 1
- AAEAAZAPXYHUIW-UHFFFAOYSA-N tridecyl butyrate Chemical compound CCCCCCCCCCCCCOC(=O)CCC AAEAAZAPXYHUIW-UHFFFAOYSA-N 0.000 description 1
- JFOWPZXGNKSOTH-UHFFFAOYSA-N tridecyl decanoate Chemical compound CCCCCCCCCCCCCOC(=O)CCCCCCCCC JFOWPZXGNKSOTH-UHFFFAOYSA-N 0.000 description 1
- VBCBSDJKFLGBIX-UHFFFAOYSA-N tridecyl docosanoate Chemical compound CCCCCCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCCCC VBCBSDJKFLGBIX-UHFFFAOYSA-N 0.000 description 1
- INJZMNQWJIWOEA-UHFFFAOYSA-N tridecyl dodecanoate Chemical compound CCCCCCCCCCCCCOC(=O)CCCCCCCCCCC INJZMNQWJIWOEA-UHFFFAOYSA-N 0.000 description 1
- QEIJVPZRDAHCHE-UHFFFAOYSA-N tridecyl hexadecanoate Chemical compound CCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCCCC QEIJVPZRDAHCHE-UHFFFAOYSA-N 0.000 description 1
- GKAVWWCJCPVMNR-UHFFFAOYSA-N tridecyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCCCC GKAVWWCJCPVMNR-UHFFFAOYSA-N 0.000 description 1
- CTWLAMKOJQOQLN-UHFFFAOYSA-N tridecyl tetradecanoate Chemical compound CCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCC CTWLAMKOJQOQLN-UHFFFAOYSA-N 0.000 description 1
- 229940113164 trimyristin Drugs 0.000 description 1
- WENNKWXPAWNIOO-UHFFFAOYSA-N undecan-5-one Chemical compound CCCCCCC(=O)CCCC WENNKWXPAWNIOO-UHFFFAOYSA-N 0.000 description 1
- ZBUPFBRWKJDEAX-UHFFFAOYSA-N undecyl decanoate Chemical compound CCCCCCCCCCCOC(=O)CCCCCCCCC ZBUPFBRWKJDEAX-UHFFFAOYSA-N 0.000 description 1
- JHDNXONYKMEEBK-UHFFFAOYSA-N undecyl dodecanoate Chemical compound CCCCCCCCCCCOC(=O)CCCCCCCCCCC JHDNXONYKMEEBK-UHFFFAOYSA-N 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- NCSMRDAYUUPTTK-UHFFFAOYSA-N undecyl hexadecanoate Chemical compound CCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCC NCSMRDAYUUPTTK-UHFFFAOYSA-N 0.000 description 1
- MRXRZUAPYOLFFW-UHFFFAOYSA-N undecyl octanoate Chemical compound CCCCCCCCCCCOC(=O)CCCCCCC MRXRZUAPYOLFFW-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Inks, Pencil-Leads, Or Crayons (AREA)
Abstract
【課題】紙面上に描かれた筆跡等を昇温によって容易に消去できるとともに、インク組成物自体は昇温させても消色し難い熱消去性インク組成物を提供する。【解決手段】本発明の熱消去性インク組成物は、顕色剤(例えばビスフェノールA等のフェノール性の水酸基を有する化合物)によって発色状態とされたロイコ染料と、前記ロイコ染料に接触して、温度に応じて、前記ロイコ染料の発色状態を消色状態とする反応媒体(例えば脂肪酸エステル化合物)と、前記ロイコ染料と前記反応媒体とを独立した分散質として分散させ、紙面上で消失する水系の分散媒とを含む。【選択図】図3
Description
本発明は熱消去性インク組成物及びその製造方法に関する。
従来より、昇温により消去することのできる熱消去性インク組成物が知られている(例えば、特許文献1参照)。この熱消去性インク組成物は、顕色剤によって発色状態とされた染料と、昇温により所定の温度で染料の発色状態を消色状態とする反応媒体との混合物が分散媒に分散されている。このため、紙面上に描かれた筆跡等は、擦過による摩擦熱によって容易に消去することができる。
しかし、上記従来の熱消去性インク組成物では、インク組成物自体も昇温によって色が消去するため、車の中や窓際等、温度が高くなる環境に置かれた場合、インク組成物自体が消色してしまい、筆記できなくなるという問題があった。本発明は、上記従来の実情に鑑みてなされたものであり、紙面上に描かれた筆跡等を昇温によって容易に消去できるとともに、インク組成物自体は昇温させても消色し難い熱消去性インク組成物を提供することを解決すべき課題としている。
上記従来の熱消去性インク組成物が昇温によって消色する原因は、発色状態の染料が昇温下で反応媒体と接触するためであると考えられる。本発明者らは、発色状態の染料と反応媒体とを分散媒の中で独立した分散質として分散させておけば、染料と反応媒体との接触が阻止され、消色現象を防げるのではないかと考え、鋭意研究を行った結果、本発明を完成した。
すなわち、本発明の熱消去性インク組成物は、顕色剤によって発色状態とされた染料と、前記染料に接触して、温度に応じて、前記染料の発色状態を消色状態とする反応媒体と、前記染料と前記反応媒体とを独立した分散質として分散させ、紙面上で消失する分散媒とを含む。
本発明の熱消去性インク組成物では、顕色剤によって発色状態とされた染料と、発色状態とされた染料に接触して、温度に応じて、発色状態を消色状態とする反応媒体とが、独立した分散質として分散媒中に分散している。分散媒中の分散質どうしは表面電荷によって互いに反発するため、インク組成物の温度が高くなっても、発色状態の染料と反応媒体とが接触することはなく、発色状態の染料の色が消えることはない。
一方、本発明の熱消去性インク組成物によって描かれた筆跡等は、紙面上の分散媒が蒸発したり紙に吸収されたりして消失し、紙面上に残された発色状態の染料と反応媒体とが接触する状態となる。このため、擦過やドライヤー等によって紙面を昇温させれば、両者が反応して、発色状態の染料は消色状態になる。
したがって、本発明の熱消去性インク組成物によれば、紙等に描かれた筆跡等を昇温によって消去できるにもかかわらず、インク組成物自体は昇温によっても色が消え難くなる。
一方、本発明の熱消去性インク組成物によって描かれた筆跡等は、紙面上の分散媒が蒸発したり紙に吸収されたりして消失し、紙面上に残された発色状態の染料と反応媒体とが接触する状態となる。このため、擦過やドライヤー等によって紙面を昇温させれば、両者が反応して、発色状態の染料は消色状態になる。
したがって、本発明の熱消去性インク組成物によれば、紙等に描かれた筆跡等を昇温によって消去できるにもかかわらず、インク組成物自体は昇温によっても色が消え難くなる。
本発明の熱消去性インク組成物に用いられる顕色剤は電子受容性化合物を含み、染料は電子供与性呈色有機化合物を含むことが好ましい。電子受容性化合物としてはブレンステッド酸やルイス酸を用いることができる。この中でもフェノール性水酸基を有する化合物が特に好適である。また、電子供与性呈色有機化合物は電子受容性化合物である顕色剤から電子を受け取り発色するものであれば特に限定はない。ロイコ染料は、ラクトン環が顕色剤によって開環して鋭敏に発色するため、電子供与性呈色有機化合物として特に好適である。
本発明の熱消去性インク組成物に用いられる反応媒体は、溶融状態において顕色剤と接触することにより染料を消色状態とし、融点においてヒステリシスが得られる有機化合物が好ましい。ここで、「融点においてヒステリシスが得られる」とは、結晶状態から溶融状態へ変化する温度と、溶融状態から結晶状へ変化する温度とが異なることを指し、前者の温度が後者の温度より高い。前者は凡そ60℃以下であり、硬質な物質をインクに当接させてこれを人が擦ることにより生じる摩擦熱でインクに含まれる反応媒体は結晶状態から溶融状態に変態する。他方、後者の温度は室温より充分低く設定される。熱によって消去された箇所が、冷却によって再発色することを防ぐためである。
融点においてヒステリシスが得られる化合物からなる反応媒体が結晶状態において、当該反応媒体と顕色剤により発色状態となった染料が接触した時、顕色剤と染料との結合状態は維持された状態である。他方、反応媒体が溶融状態となると、顕色剤及び/又は染料との結合状態が溶融状態の反応媒体中において分離され、もって、消色状態となる。
このような反応媒体として、例えば、アルコール化合物、エステル化合物、ケトン化合物、エーテル化合物、酸アミド化合物が挙げられる。
染料と反応媒体の混合比はモル濃度比で1:0.5〜1:10であることが好ましい。より好ましくは1:1.5〜1:10である。
また、分散媒は水を含むことが好ましい。分散媒に水が含まれていれば、顕色剤によって発色状態とされた染料や反応媒体を溶解することなく分散させることができる。また、本発明の熱消去性インク組成物によって筆記した場合、筆跡から水分が蒸発して紙面に固着し易くなる。
融点においてヒステリシスが得られる化合物からなる反応媒体が結晶状態において、当該反応媒体と顕色剤により発色状態となった染料が接触した時、顕色剤と染料との結合状態は維持された状態である。他方、反応媒体が溶融状態となると、顕色剤及び/又は染料との結合状態が溶融状態の反応媒体中において分離され、もって、消色状態となる。
このような反応媒体として、例えば、アルコール化合物、エステル化合物、ケトン化合物、エーテル化合物、酸アミド化合物が挙げられる。
染料と反応媒体の混合比はモル濃度比で1:0.5〜1:10であることが好ましい。より好ましくは1:1.5〜1:10である。
また、分散媒は水を含むことが好ましい。分散媒に水が含まれていれば、顕色剤によって発色状態とされた染料や反応媒体を溶解することなく分散させることができる。また、本発明の熱消去性インク組成物によって筆記した場合、筆跡から水分が蒸発して紙面に固着し易くなる。
本発明の熱消去性インク組成物は、次のようにして製造することができる。
すなわち、本発明の第1の局面の熱消去性インク組成物の製造方法は、紙面上で消失する分散媒へ、顕色剤によって発色状態とされた染料を分散させて第1の分散液を準備する第1のステップと、前記分散媒へ、染料に接触して、温度に応じて、前記染料の発色状態を消色状態とする反応媒体を分散させて第2の分散液を準備する第2のステップと、前記第1の分散液と前記第2の分散液とを混合する第3のステップと、を含む方法である。
本発明者の試験結果によれば、発色状態とされた染料が分散された第1の分散液と、反応媒体が分散された第2の分散液とを混合すれば、第1と第2の分散液において共通した分散媒中に染料と反応媒体とが独立した分散質として分散された状態となる。この分散状態は反応媒体の融点より高い温度となっても維持されるので、インクが高い温度環境にさらされても、消色することがない。
なお、分散媒は、溶融状態の反応媒体を溶解しないものとする。
すなわち、本発明の第1の局面の熱消去性インク組成物の製造方法は、紙面上で消失する分散媒へ、顕色剤によって発色状態とされた染料を分散させて第1の分散液を準備する第1のステップと、前記分散媒へ、染料に接触して、温度に応じて、前記染料の発色状態を消色状態とする反応媒体を分散させて第2の分散液を準備する第2のステップと、前記第1の分散液と前記第2の分散液とを混合する第3のステップと、を含む方法である。
本発明者の試験結果によれば、発色状態とされた染料が分散された第1の分散液と、反応媒体が分散された第2の分散液とを混合すれば、第1と第2の分散液において共通した分散媒中に染料と反応媒体とが独立した分散質として分散された状態となる。この分散状態は反応媒体の融点より高い温度となっても維持されるので、インクが高い温度環境にさらされても、消色することがない。
なお、分散媒は、溶融状態の反応媒体を溶解しないものとする。
本発明の熱消去性インク組成物の製造方法において、
第1のステップは、前記顕色剤はフェノール性水酸基を有する化合物を含み、前記染料はロイコ染料を含み、これらを結合させて発色状態としたインク原液を準備するステップと、
前記分散媒は水を含み、包接化合物を形成可能な化合物(例えばシクロデキストリン)を第1の分散剤として、前記インク原液を前記分散媒へ分散させるステップとを含み、
前記第2のステップは、前記反応媒体はアルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種を含み、包接化合物を形成可能な化合物(例えばシクロデキストリン)を第2の分散剤として、該アルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種を前記分散媒へ分散させるステップを含むことが好ましい。
第1のステップは、前記顕色剤はフェノール性水酸基を有する化合物を含み、前記染料はロイコ染料を含み、これらを結合させて発色状態としたインク原液を準備するステップと、
前記分散媒は水を含み、包接化合物を形成可能な化合物(例えばシクロデキストリン)を第1の分散剤として、前記インク原液を前記分散媒へ分散させるステップとを含み、
前記第2のステップは、前記反応媒体はアルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種を含み、包接化合物を形成可能な化合物(例えばシクロデキストリン)を第2の分散剤として、該アルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種を前記分散媒へ分散させるステップを含むことが好ましい。
本発明の熱消去性インク組成物の製造方法においては、第3のステップにおいて、反応媒体が結晶を維持する温度で第1の分散液と前記第2の分散液とが混合されることが好ましい。混合液中において、とくにその撹拌時において、溶解した反応媒体が染料に接触する状態を確実に避けるためである。
本発明の熱消去性インク組成物は、次のようにしても製造することができる。
すなわち、本発明の第2の局面の熱消去性インク組成物の製造方法は、顕色剤によって発色状態とされた染料と、発色状態を消色状態とする反応媒体と、をグレンミル及び/又はボールミルを用いて紙面上で消失する分散媒へ分散させる方法である。
顕色剤によって発色状態とされた染料と、発色状態を消色状態とする反応媒体と、をグレンミルやボールミルを用いて分散させれば、染料や反応媒体が粉砕されるときの摩擦熱が分散媒へ散逸するため、発色した染料を反応媒体によって消色するために必要な温度まで上がることはない。また、染料や反応媒体が粉砕されたと同時に、分散媒の中に独立した分散質として分散していく。このため、本発明の熱消去性インク組成物をワンステップで製造することができる。
すなわち、本発明の第2の局面の熱消去性インク組成物の製造方法は、顕色剤によって発色状態とされた染料と、発色状態を消色状態とする反応媒体と、をグレンミル及び/又はボールミルを用いて紙面上で消失する分散媒へ分散させる方法である。
顕色剤によって発色状態とされた染料と、発色状態を消色状態とする反応媒体と、をグレンミルやボールミルを用いて分散させれば、染料や反応媒体が粉砕されるときの摩擦熱が分散媒へ散逸するため、発色した染料を反応媒体によって消色するために必要な温度まで上がることはない。また、染料や反応媒体が粉砕されたと同時に、分散媒の中に独立した分散質として分散していく。このため、本発明の熱消去性インク組成物をワンステップで製造することができる。
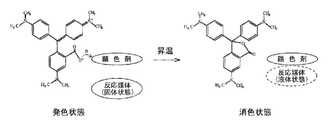
まず、従来から知られた熱消去性インク組成物の原理を説明する。図1はロイコ染料として3,3-Bis(p-dimethylaminophenyl)-6-dimethylaminophthalide(クリスタルバイオレットラクトン)を用いた場合の熱消去性インク組成物の原理を示す図である。熱消去性インク組成物内において、ロイコ染料は顕色剤(例えばビスフェノールA)に電子を供与してラクトン環が開環した複合体構造をとなっている(図1左側)。この構造においてはπ電子の共鳴構造が長くなるため、吸収スペクトルは長波長側に移動して発色する。また、共存する反応媒体が固体状態であれば、発色状態の染料とには作用し得ないため、消色状態になることはない。このインクによって紙面上に描かれた筆跡等は、擦過等によって温度を高くすると、反応媒体が溶融状態となり、反応媒体によって染料と顕色剤との結合が切れて、π電子の共鳴構造が短くなり、消色状態となる(図1右側)。
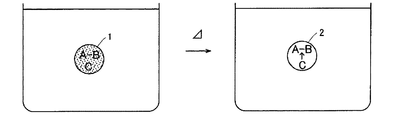
このような消色現象は、従来の熱消去性インク組成物自体の温度を高くしても起こりうる。従来の熱消去性インク組成物では、図2の左側の図に示すように、顕色剤Bによって発色状態とされた染料Aと、昇温により所定の温度で染料の発色状態を消色状態とする反応媒体Cとが混合状態で分散質1として分散されている。このため、この熱消去性インク組成物自体を所定の温度以上にした場合、図2の右側の図に示すように、反応媒体Cが溶融し、顕色剤Bや染料Aに作用して染料Aが消色状態となった分散質2となるからである。
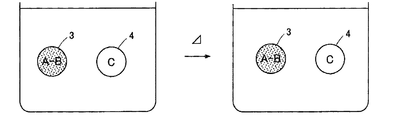
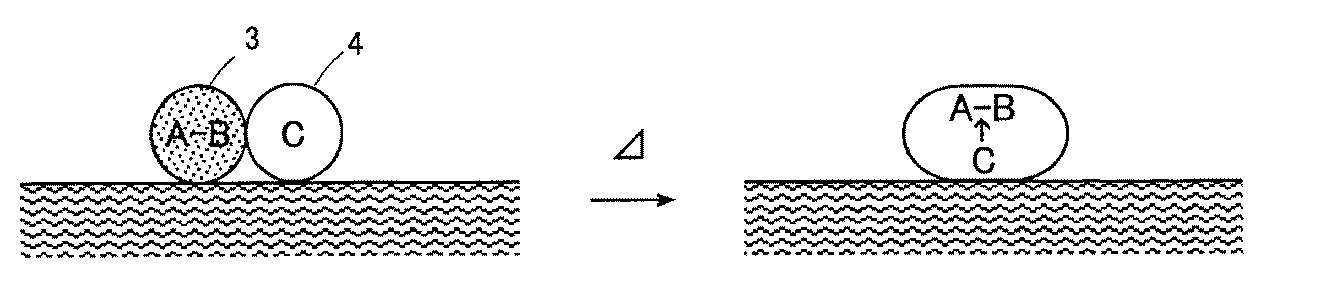
これに対して、本発明の熱消去性インク組成物では、図3に示すように、顕色剤Bによって発色状態とされた染料Aと、反応媒体Cとがそれぞれ独立した分散質3及び分散質4として分散媒に分散されている(図3左図)。このため、この分散状態を保ったままで所定の温度以上にしても、反応媒体Cは発色した染料Aとは接触することはなく、発色状態の染料Aの色が消えることはない(図3右図)。
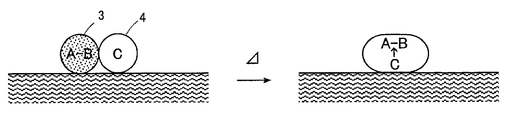
一方、本発明の熱消去性インク組成物を用いたボールペン等によって紙面上に記載された場合は、分散媒は蒸発したり、紙に吸収されたりするため、紙面上には図4に示すように、顕色剤で発色した染料からなる分散質3と、反応媒体からなる分散質4とが接触する状態で残留する。そして、擦過やドライヤー等によって加熱されると、反応媒体からなる分散質4が溶融して顕色剤で発色した染料からなる分散質3を消色する。
一方、本発明の熱消去性インク組成物を用いたボールペン等によって紙面上に記載された場合は、分散媒は蒸発したり、紙に吸収されたりするため、紙面上には図4に示すように、顕色剤で発色した染料からなる分散質3と、反応媒体からなる分散質4とが接触する状態で残留する。そして、擦過やドライヤー等によって加熱されると、反応媒体からなる分散質4が溶融して顕色剤で発色した染料からなる分散質3を消色する。
分散質3及び分散質4を独立した状態で分散媒に分散させるためには、分散質3を分散媒に分散させた第1の分散液と、分散質4を分散媒に分散させた第2の分散液とを混合すればよい。こうであれば、分散質3と分散質4とが、表面荷電によって反発し、お互い位接触することが防止される。また、第1の分散液や第2の分散液を調製する場合に、分散剤を用いることが好ましい。こうであれば、分散質3や分散質4を分散媒中に容易に分散させることができる。また、それらの分散質表面に吸着した分散剤による保護コロイドとしての効果や表面荷電による斥力によって分散質3と分散質4との接触が防止される。
第1及び第2の分散液に用いられる分散剤は、選択される分散媒及び分散質に応じて任意に選択できる。
第1の分散液の分散媒と第2の分散液の分散媒とは紙面上で消失し、第1の分散液と第2の分散液とを混合したときに相手方の分散状態に干渉しないものであれば、任意に選択可能である。
ここに、紙面上で消失するとは、筆記具から分離して紙面上に乗せられたとき紙面への吸収や蒸発等により、紙面上に存在しなくなることを指し、その結果、第1及び第2の分散液の媒質は相互に接触可能となる。なお、紙面とは、筆記対象となる媒体であり、その材質は必ずしも紙に限定されるものでない。
第1の分散液の分散媒が第2の分散液の分散状態に干渉しないとは、第1の分散液の分散媒が第2の分散液の分散質を溶解させたり、凝縮させたりせず、また第2の分散媒とも化学反応を起こさないことをいう。従って、第1及び第2の分散液の分散媒は同一若しくは同種とすることが好ましいが、勿論、上記の機能を有する分散媒であれば、第1の分散液と第2の分散液において異種を採用できる。
実施例では第1の分散媒と第2の分散媒としてともに水を採用している。
第1及び第2の分散液に用いられる分散剤は、選択される分散媒及び分散質に応じて任意に選択できる。
第1の分散液の分散媒と第2の分散液の分散媒とは紙面上で消失し、第1の分散液と第2の分散液とを混合したときに相手方の分散状態に干渉しないものであれば、任意に選択可能である。
ここに、紙面上で消失するとは、筆記具から分離して紙面上に乗せられたとき紙面への吸収や蒸発等により、紙面上に存在しなくなることを指し、その結果、第1及び第2の分散液の媒質は相互に接触可能となる。なお、紙面とは、筆記対象となる媒体であり、その材質は必ずしも紙に限定されるものでない。
第1の分散液の分散媒が第2の分散液の分散状態に干渉しないとは、第1の分散液の分散媒が第2の分散液の分散質を溶解させたり、凝縮させたりせず、また第2の分散媒とも化学反応を起こさないことをいう。従って、第1及び第2の分散液の分散媒は同一若しくは同種とすることが好ましいが、勿論、上記の機能を有する分散媒であれば、第1の分散液と第2の分散液において異種を採用できる。
実施例では第1の分散媒と第2の分散媒としてともに水を採用している。
本発明の用いる顕色剤、染料、及び反応媒体としては、従来使用されていた以下の化合物(例えば特開2008-076787に記載の化合物)を用いることができる。
顕色剤としては、フェノール性水酸基を有する化合物(例えば、モノフェノール化合物、ポリフェノール化合物)や、さらにその置換基としてアルキル基、アリール基、アシル基、アルコキシカルボニル基、カルボキシ基及びそのエステル又はアミド基、ハロゲン基等が結合したフェノール性水酸基を有する化合物が挙げられる。フェノール性水酸基を有する化合物は、ビス型、トリス型フェノールであってもよく、フェノール−アルデヒド縮合樹脂でもよい。さらには、フェノール性水酸基を有する化合物の金属塩であってもよい。
顕色剤としては、フェノール性水酸基を有する化合物(例えば、モノフェノール化合物、ポリフェノール化合物)や、さらにその置換基としてアルキル基、アリール基、アシル基、アルコキシカルボニル基、カルボキシ基及びそのエステル又はアミド基、ハロゲン基等が結合したフェノール性水酸基を有する化合物が挙げられる。フェノール性水酸基を有する化合物は、ビス型、トリス型フェノールであってもよく、フェノール−アルデヒド縮合樹脂でもよい。さらには、フェノール性水酸基を有する化合物の金属塩であってもよい。
以下に具体例を挙げる。
フェノール、o−クレゾール、ターシャリーブチルカテコール、ノニルフェノール、n−オクチルフェノール、n−ドデシルフェノール、n−ステアリルフェノール、p−クロロフェノール、p−ブロモフェノール、o−フェニルフェノール、p−ヒドロキシ安息香酸n−ブチル、p−ヒドロキシ安息香酸n−オクチル、レゾルシン、没食子酸ドデシル、2,2−ビス(4−ヒドロキシフェニル)プロパン、4,4−ジヒドロキシジフェニルスルホン、1,1−ビス(4−ヒドロキシフェニル)エタン、2,2−ビス(4−ヒドロキシ−3−メチルフェニル)プロパン、ビス(4−ヒドロキシフェニル)スルフィド、1−フェニル−1,1−ビス(4−ヒドロキシフェニル)エタン、1,1−ビス(4−ヒドロキシフェニル)−3−メチルブタン、1,1−ビス(4−ヒドロキシフェニル)−2−メチルプロパン、1,1−ビス(4−ヒドロキシフェニル)n−ヘキサン、1,1−ビス(4−ヒドロキシフェニル)n−ヘプタン、1,1−ビス(4−ヒドロキシフェニル)n−オクタン、1,1−ビス(4−ヒドロキシフェニル)n−ノナン、1,1−ビス(4−ヒドロキシフェニル)n−デカン、1,1−ビス(4−ヒドロキシフェニル)n−ドデカン、2,2−ビス(4−ヒドロキシフェニル)ブタン、2,2−ビス(4−ヒドロキシフェニル)エチルプロピオネート、2,2−ビス(4−ヒドロキシフェニル)−4−メチルペンタン、2,2−ビス(4−ヒドロキシフェニル)ヘキサフルオロプロパン、2,2−ビス(4−ヒドロキシフェニル)n−ヘプタン、2,2−ビス(4−ヒドロキシフェニル)n−ノナン等がある。
フェノール、o−クレゾール、ターシャリーブチルカテコール、ノニルフェノール、n−オクチルフェノール、n−ドデシルフェノール、n−ステアリルフェノール、p−クロロフェノール、p−ブロモフェノール、o−フェニルフェノール、p−ヒドロキシ安息香酸n−ブチル、p−ヒドロキシ安息香酸n−オクチル、レゾルシン、没食子酸ドデシル、2,2−ビス(4−ヒドロキシフェニル)プロパン、4,4−ジヒドロキシジフェニルスルホン、1,1−ビス(4−ヒドロキシフェニル)エタン、2,2−ビス(4−ヒドロキシ−3−メチルフェニル)プロパン、ビス(4−ヒドロキシフェニル)スルフィド、1−フェニル−1,1−ビス(4−ヒドロキシフェニル)エタン、1,1−ビス(4−ヒドロキシフェニル)−3−メチルブタン、1,1−ビス(4−ヒドロキシフェニル)−2−メチルプロパン、1,1−ビス(4−ヒドロキシフェニル)n−ヘキサン、1,1−ビス(4−ヒドロキシフェニル)n−ヘプタン、1,1−ビス(4−ヒドロキシフェニル)n−オクタン、1,1−ビス(4−ヒドロキシフェニル)n−ノナン、1,1−ビス(4−ヒドロキシフェニル)n−デカン、1,1−ビス(4−ヒドロキシフェニル)n−ドデカン、2,2−ビス(4−ヒドロキシフェニル)ブタン、2,2−ビス(4−ヒドロキシフェニル)エチルプロピオネート、2,2−ビス(4−ヒドロキシフェニル)−4−メチルペンタン、2,2−ビス(4−ヒドロキシフェニル)ヘキサフルオロプロパン、2,2−ビス(4−ヒドロキシフェニル)n−ヘプタン、2,2−ビス(4−ヒドロキシフェニル)n−ノナン等がある。
なお、前記フェノール性水酸基を有する化合物として、少なくとも3以上のベンゼン環を有し、且つ、分子量が250以上、好ましくは分子量が250乃至500のフェノール性水酸基を有する化合物、又は、一般式(C6H2R1R2OH)2S(式中、R1は炭素数1乃至8のアルキル基を示し、R2は水素又は炭素数1乃至8のアルキル基を示す。)で示されるフェノール性水酸基を有する化合物を用いると、消色状態から発色状態に移行する際の変色感度をより鋭敏にすることができるため、好適である。
前述した少なくとも3以上のベンゼン環を有し、且つ、分子量が250以上のフェノール性水酸基を有する化合物としては、
4,4′,4″−メチリデントリスフェノール、2,6−ビス〔(2−ヒドロキシ−5−メチルフェノール)メチル〕−4−メチルフェノール、4,4′−〔1−[4−[1−(4−ヒドロキシフェニル)−1−メチルエチル]フェニル]エチリデン〕ビスフェノール、 4,4′,4″−エチリデントリス〔2−メチルフェノール〕、4,4′−〔(2−ヒドロキシフェニル)メチレン〕ビス[2,3,6−トリフェニルフェノール]、2,2−メチレンビス[6−[(2−ヒドロキシ−5−メチルフェニル)メチル]−4−メチルフェノール]、 2,4,6−トリス(4−ヒドロキシフェニルメチル)1,3−ベンゼンジオール、4,4′,4″−エチリデントリスフェノール、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2−メチルフェノール]、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2,6−ジメチルフェノール]、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2−メチルフェノール]、4,4′−[(4−ヒドロキシフェニル]メチレン]ビス[2,6−ジメチルフェノール]、4,4′−[(4−ヒドロキシ−3−メトキシフェニル)メチレン]ビス[2,6−ジメチルフェノール]、2,4−ビス[(5−メチル−2−ヒドロキシフェニル)メチル]−6−シクロヘキシルフェノール、4,4′−[1−[4−[1−(4−ヒドロキシ−3−メチルフェノール)−1−メチルエチル]フェニル]エチリデン]ビス[2−メチルフェノール]、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2−シクロヘキシル−5−メチルフェノール]、4,6−ビス[(4−ヒドロキシフェニル)メチル]1,3−ベンゼンジオール、4,4′−[(3,4−ジ−ヒドロキシフェニル)メチレン]ビス[2,6−ジメチルフェノール]、4,4′−(1−フェニルエチリデン)ビスフェノール、5,5′−(1−メチルエチリデン)ビス[1−フェニル−2−オール]、
4,4′,4″−メチリデントリスフェノール、4,4′−[1−[4−[1−(4−ヒドロキシフェニル)−1−メチルエチル]フェニル]エチリデン]ビスフェノール、4,4′−(フェニルメチレン)ビスフェノール、4,4′−[1,4−フェニレンビス(1−メチルエチリデン)]ビス[2−メチルフェノール]、5,5′−(1,1−シクロヘキシリデン)ビス−[1−ビフェニル−2−オール]等が挙げられる。
前述した少なくとも3以上のベンゼン環を有し、且つ、分子量が250以上のフェノール性水酸基を有する化合物としては、
4,4′,4″−メチリデントリスフェノール、2,6−ビス〔(2−ヒドロキシ−5−メチルフェノール)メチル〕−4−メチルフェノール、4,4′−〔1−[4−[1−(4−ヒドロキシフェニル)−1−メチルエチル]フェニル]エチリデン〕ビスフェノール、 4,4′,4″−エチリデントリス〔2−メチルフェノール〕、4,4′−〔(2−ヒドロキシフェニル)メチレン〕ビス[2,3,6−トリフェニルフェノール]、2,2−メチレンビス[6−[(2−ヒドロキシ−5−メチルフェニル)メチル]−4−メチルフェノール]、 2,4,6−トリス(4−ヒドロキシフェニルメチル)1,3−ベンゼンジオール、4,4′,4″−エチリデントリスフェノール、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2−メチルフェノール]、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2,6−ジメチルフェノール]、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2−メチルフェノール]、4,4′−[(4−ヒドロキシフェニル]メチレン]ビス[2,6−ジメチルフェノール]、4,4′−[(4−ヒドロキシ−3−メトキシフェニル)メチレン]ビス[2,6−ジメチルフェノール]、2,4−ビス[(5−メチル−2−ヒドロキシフェニル)メチル]−6−シクロヘキシルフェノール、4,4′−[1−[4−[1−(4−ヒドロキシ−3−メチルフェノール)−1−メチルエチル]フェニル]エチリデン]ビス[2−メチルフェノール]、4,4′−[(4−ヒドロキシフェニル)メチレン]ビス[2−シクロヘキシル−5−メチルフェノール]、4,6−ビス[(4−ヒドロキシフェニル)メチル]1,3−ベンゼンジオール、4,4′−[(3,4−ジ−ヒドロキシフェニル)メチレン]ビス[2,6−ジメチルフェノール]、4,4′−(1−フェニルエチリデン)ビスフェノール、5,5′−(1−メチルエチリデン)ビス[1−フェニル−2−オール]、
4,4′,4″−メチリデントリスフェノール、4,4′−[1−[4−[1−(4−ヒドロキシフェニル)−1−メチルエチル]フェニル]エチリデン]ビスフェノール、4,4′−(フェニルメチレン)ビスフェノール、4,4′−[1,4−フェニレンビス(1−メチルエチリデン)]ビス[2−メチルフェノール]、5,5′−(1,1−シクロヘキシリデン)ビス−[1−ビフェニル−2−オール]等が挙げられる。
前記一般式(C6H2R1R2OH)2Sで示されるフェノール性水酸基を有する化合物としては、
ビス(3−メチル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−ジメチル−4−ヒドロキシフェニル)、ビス(3−エチル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−ジエチル−4−ヒドロキシフェニル)スルフィド、ビス(3−プロピル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−ジプロピル−4−ヒドロキシフェニル)スルフィド、ビス(3−t−ブチル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−t−ブチル−4−ヒドロキシフェニル)スルフィド、ビス(3−ペンチル−4−ヒドロキシフェニル)スルフィド、ビス(3−ヘキシル−4−ヒドロキシフェニル)スルフィド、ビス(3−ヘプチル−4−ヒドキシフェニル)スルフィド、ビス(5−オクチル−2−ヒドロキシフェニル)スルフィド等が挙げられる。
ビス(3−メチル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−ジメチル−4−ヒドロキシフェニル)、ビス(3−エチル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−ジエチル−4−ヒドロキシフェニル)スルフィド、ビス(3−プロピル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−ジプロピル−4−ヒドロキシフェニル)スルフィド、ビス(3−t−ブチル−4−ヒドロキシフェニル)スルフィド、ビス(3,5−t−ブチル−4−ヒドロキシフェニル)スルフィド、ビス(3−ペンチル−4−ヒドロキシフェニル)スルフィド、ビス(3−ヘキシル−4−ヒドロキシフェニル)スルフィド、ビス(3−ヘプチル−4−ヒドキシフェニル)スルフィド、ビス(5−オクチル−2−ヒドロキシフェニル)スルフィド等が挙げられる。
前記フェノール性水酸基を有する化合物が最も有効な熱変色特性を発現させることができるが、芳香族カルボン酸及び炭素数2〜5の脂肪族カルボン酸、カルボン酸金属塩、酸性リン酸エステル及びそれらの金属塩、1、2、3−トリアゾール及びその誘導体から選ばれる化合物等であってもよい。
染料としては、ロイコ染料を好適に用いることができる。ロイコ染料としては、トリフェニルメタンフタリド化合物、ジフェニルメタンフタリド化合物、フェニルインドリルフタリド化合物、インドリルフタリド化合物、ジフェニルメタンアザフタリド化合物、フェニルインドリルアザフタリド化合物、フルオラン化合物、スチリノキノリン化合物、ジアザローダミンラクトン化合物等が挙げられ、以下にこれらの化合物を例示する。
3,3−ビス(p−ジメチルアミノフェニル)−6−ジメチルアミノフタリド、3−(4−ジエチルアミノフェニル)−3−(1−エチル−2−メチルインドール−3−イル)フタリド、3,3−ビス(1−n−ブチル−2−メチルインドール−3−イル)フタリド、3,3−ビス(2−エトキシ−4−ジエチルアミノフェニル)−4−アザフタリド、3−〔2−エトキシ−4−(N−エチルアニリノ)フェニル〕−3−(1−エチル−2−メチルインドール−3−イル)−4−アザフタリド、3,6−ジフェニルアミノフルオラン、3,6−ジメトキシフルオラン、3,6−ジ−n−ブトキシフルオラン、2−メチル−6−(N−エチル−N−p−トリルアミノ)フルオラン、3−クロロ−6−シクロヘキシルアミノフルオラン、2−メチル−6−シクロヘキシルアミノフルオラン、2−(2−クロロアニリノ)−6−ジ−n−ブチルアミノフルオラン、2−(3−トリフルオロメチルアニリノ)−6−ジエチルアミノフルオラン、2−(N−メチルアニリノ)−6−(N−エチル−N−p−トリルアミノ)フルオラン、1,3−ジメチル−6−ジエチルアミノフルオラン、2−クロロ−3−メチル−6−ジエチルアミノフルオラン、2−アニリノ−3−メチル−6−ジエチルアミノフルオラン、2−アニリノ−3−メチル−6−ジ−n−ブチルアミノフルオラン、2−キシリジノ−3−メチル−6−ジエチルアミノフルオラン、1,2−ベンツ−6−ジエチルアミノフルオラン、1,2−ベンツ−6−(N−エチル−N−イソブチルアミノ)フルオラン、1,2−ベンツ−6−(N−エチル−N−イソアミルアミノ)フルオラン、2−(3−メトキシ−4−ドデコキシスチリル)キノリン、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジエチルアミノ)−8−(ジエチルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(ジ−n−ブチルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(ジエチルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(N−エチル−N−i−アミルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(ジ−n−ブチルアミノ)−4−フェニル、3−(2−メトキシ−4−ジメチルアミノフェニル)−3−(1−ブチル−2−メチルインドール−3−イル)−4,5,6,7−テトラクロロフタリド、3−(2−エトキシ−4−ジエチルアミノフェニル)−3−(1−エチル−2−メチルインドール−3−イル)−4,5,6,7−テトラクロロフタリド、3−(2−エトキシ−4−ジエチルアミノフェニル)−3−(1−ペンチル−2−メチルインドール−3−イル)−4,5,6,7−テトラクロロフタリド等を挙げることができる。更には、蛍光性の黄色〜赤色の発色を発現させるのに有効な、ピリジン系、キナゾリン系、ビスキナゾリン系化合物等を挙げることができる。
3,3−ビス(p−ジメチルアミノフェニル)−6−ジメチルアミノフタリド、3−(4−ジエチルアミノフェニル)−3−(1−エチル−2−メチルインドール−3−イル)フタリド、3,3−ビス(1−n−ブチル−2−メチルインドール−3−イル)フタリド、3,3−ビス(2−エトキシ−4−ジエチルアミノフェニル)−4−アザフタリド、3−〔2−エトキシ−4−(N−エチルアニリノ)フェニル〕−3−(1−エチル−2−メチルインドール−3−イル)−4−アザフタリド、3,6−ジフェニルアミノフルオラン、3,6−ジメトキシフルオラン、3,6−ジ−n−ブトキシフルオラン、2−メチル−6−(N−エチル−N−p−トリルアミノ)フルオラン、3−クロロ−6−シクロヘキシルアミノフルオラン、2−メチル−6−シクロヘキシルアミノフルオラン、2−(2−クロロアニリノ)−6−ジ−n−ブチルアミノフルオラン、2−(3−トリフルオロメチルアニリノ)−6−ジエチルアミノフルオラン、2−(N−メチルアニリノ)−6−(N−エチル−N−p−トリルアミノ)フルオラン、1,3−ジメチル−6−ジエチルアミノフルオラン、2−クロロ−3−メチル−6−ジエチルアミノフルオラン、2−アニリノ−3−メチル−6−ジエチルアミノフルオラン、2−アニリノ−3−メチル−6−ジ−n−ブチルアミノフルオラン、2−キシリジノ−3−メチル−6−ジエチルアミノフルオラン、1,2−ベンツ−6−ジエチルアミノフルオラン、1,2−ベンツ−6−(N−エチル−N−イソブチルアミノ)フルオラン、1,2−ベンツ−6−(N−エチル−N−イソアミルアミノ)フルオラン、2−(3−メトキシ−4−ドデコキシスチリル)キノリン、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジエチルアミノ)−8−(ジエチルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(ジ−n−ブチルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(ジエチルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(N−エチル−N−i−アミルアミノ)−4−メチル−、スピロ〔5H−(1)ベンゾピラノ(2,3−d)ピリミジン−5,1′(3′H)イソベンゾフラン〕−3′−オン,2−(ジ−n−ブチルアミノ)−8−(ジ−n−ブチルアミノ)−4−フェニル、3−(2−メトキシ−4−ジメチルアミノフェニル)−3−(1−ブチル−2−メチルインドール−3−イル)−4,5,6,7−テトラクロロフタリド、3−(2−エトキシ−4−ジエチルアミノフェニル)−3−(1−エチル−2−メチルインドール−3−イル)−4,5,6,7−テトラクロロフタリド、3−(2−エトキシ−4−ジエチルアミノフェニル)−3−(1−ペンチル−2−メチルインドール−3−イル)−4,5,6,7−テトラクロロフタリド等を挙げることができる。更には、蛍光性の黄色〜赤色の発色を発現させるのに有効な、ピリジン系、キナゾリン系、ビスキナゾリン系化合物等を挙げることができる。
また、反応媒体としては、染料に接触して、温度に応じて、染料の発色状態を消色状態とするものであればよい。例えば、アルコール化合物、エステル化合物、ケトン化合物、エーテル化合物、酸アミド化合物が挙げられる。その中でも、色濃度−温度の関係においてヒステリシスが得られる結晶性有機化合物であることが好ましい。こうであれば消去された箇所が冷却によって再発色することを防止することができる。
このような大きなヒステリシス特性を示す化合物としてカルボン酸エステル化合物が挙げられる。例えば、分子中に置換芳香族環を含むカルボン酸エステル、無置換芳香族環を含むカルボン酸と炭素数10以上の脂肪族アルコールのエステル、分子中にシクロヘキシル基を含むカルボン酸エステル、炭素数6以上の脂肪酸と無置換芳香族アルコール又はフェノールのエステル、炭素数8以上の脂肪酸と分岐脂肪族アルコール又はエステル、ジカルボン酸と芳香族アルコール又は分岐脂肪族アルコールのエステル、ケイ皮酸ジベンジル、ステアリン酸ヘプチル、アジピン酸ジデシル、アジピン酸ジラウリル、アジピン酸ジミリスチル、アジピン酸ジセチル、アジピン酸ジステアリル、トリラウリン、トリミリスチン、トリステアリン、ジミリスチン、ジステアリン等が用いられる。
このような大きなヒステリシス特性を示す化合物としてカルボン酸エステル化合物が挙げられる。例えば、分子中に置換芳香族環を含むカルボン酸エステル、無置換芳香族環を含むカルボン酸と炭素数10以上の脂肪族アルコールのエステル、分子中にシクロヘキシル基を含むカルボン酸エステル、炭素数6以上の脂肪酸と無置換芳香族アルコール又はフェノールのエステル、炭素数8以上の脂肪酸と分岐脂肪族アルコール又はエステル、ジカルボン酸と芳香族アルコール又は分岐脂肪族アルコールのエステル、ケイ皮酸ジベンジル、ステアリン酸ヘプチル、アジピン酸ジデシル、アジピン酸ジラウリル、アジピン酸ジミリスチル、アジピン酸ジセチル、アジピン酸ジステアリル、トリラウリン、トリミリスチン、トリステアリン、ジミリスチン、ジステアリン等が用いられる。
また、炭素数9以上の奇数の脂肪族一価アルコールと炭素数が偶数の脂肪族カルボン酸から得られる脂肪酸エステル化合物、n−ペンチルアルコール又はn−ヘプチルアルコールと炭素数10乃至16の偶数の脂肪族カルボン酸より得られる総炭素数17乃至23の脂肪酸エステル化合物も有効である。
具体的には、酢酸n−ペンタデシル、酪酸n−トリデシル、酪酸n−ペンタデシル、カプロン酸n−ウンデシル、カプロン酸n−トリデシル、カプロン酸n−ペンタデシル、カプリル酸n−ノニル、カプリル酸n−ウンデシル、カプリル酸n−トリデシル、カプリル酸n−ペンタデシル、カプリン酸n−ヘプチル、カプリン酸n−ノニル、カプリン酸n−ウンデシル、カプリン酸n−トリデシル、カプリン酸n−ペンタデシル、ラウリン酸n−ペンチル、ラウリン酸n−ヘプチル、ラウリン酸n−ノニル、ラウリン酸n−ウンデシル、ラウリン酸n−トリデシル、ラウリン酸n−ペンタデシル、ミリスチン酸n−ペンチル、ミリスチン酸n−ヘプチル、ミリスチン酸n−ノニル、ミリスチン酸n−ウンデシル、ミリスチン酸n−トリデシル、ミリスチン酸n−ペンタデシル、パルミチン酸n−ペンチル、パルミチン酸n−ヘプチル、パルミチン酸n−ノニル、パルミチン酸n−ウンデシル、パルミチン酸n−トリデシル、パルミチン酸n−ペンタデシル、ステアリン酸n−ノニル、ステアリン酸n−ウンデシル、ステアリン酸n−トリデシル、ステアリン酸n−ペンタデシル、エイコサン酸n−ノニル、エイコサン酸n−ウンデシル、エイコサン酸n−トリデシル、エイコサン酸n−ペンタデシル、ベヘニン酸n−ノニル、ベヘニン酸n−ウンデシル、ベヘニン酸n−トリデシル、ベヘニン酸n−ペンタデシル等が挙げられる。
具体的には、酢酸n−ペンタデシル、酪酸n−トリデシル、酪酸n−ペンタデシル、カプロン酸n−ウンデシル、カプロン酸n−トリデシル、カプロン酸n−ペンタデシル、カプリル酸n−ノニル、カプリル酸n−ウンデシル、カプリル酸n−トリデシル、カプリル酸n−ペンタデシル、カプリン酸n−ヘプチル、カプリン酸n−ノニル、カプリン酸n−ウンデシル、カプリン酸n−トリデシル、カプリン酸n−ペンタデシル、ラウリン酸n−ペンチル、ラウリン酸n−ヘプチル、ラウリン酸n−ノニル、ラウリン酸n−ウンデシル、ラウリン酸n−トリデシル、ラウリン酸n−ペンタデシル、ミリスチン酸n−ペンチル、ミリスチン酸n−ヘプチル、ミリスチン酸n−ノニル、ミリスチン酸n−ウンデシル、ミリスチン酸n−トリデシル、ミリスチン酸n−ペンタデシル、パルミチン酸n−ペンチル、パルミチン酸n−ヘプチル、パルミチン酸n−ノニル、パルミチン酸n−ウンデシル、パルミチン酸n−トリデシル、パルミチン酸n−ペンタデシル、ステアリン酸n−ノニル、ステアリン酸n−ウンデシル、ステアリン酸n−トリデシル、ステアリン酸n−ペンタデシル、エイコサン酸n−ノニル、エイコサン酸n−ウンデシル、エイコサン酸n−トリデシル、エイコサン酸n−ペンタデシル、ベヘニン酸n−ノニル、ベヘニン酸n−ウンデシル、ベヘニン酸n−トリデシル、ベヘニン酸n−ペンタデシル等が挙げられる。
また、ケトン化合物としては、総炭素数が10以上の脂肪族ケトン化合物が有効であり、2−デカノン、3−デカノン、4−デカノン、2−ウンデカノン、3−ウンデカノン、4−ウンデカノン、5−ウンデカノン、2−ドデカノン、3−ドデカノン、4−ドデカノン、5−ドデカノン、2−トリデカノン、3−トリデカノン、2−テトラデカノン、2−ペンタデカノン、8−ペンタデカノン、2−ヘキサデカノン、3−ヘキサデカノン、9−ヘプタデカノン、2−ペンタデカノン、2−オクタデカノン、2−ノナデカノン、10−ノナダカノン、2−エイコサノン、11−エイコサノン、2−ヘンエイコサノン、2-ドコサノン、ラウロン、ステアロン等が挙げられる。
また、総炭素数が12乃至24のアリールアルキルケトン、例えば、n−オクタデカノフェノン、n−ヘプタデカノフェノン、n−ヘキサデカノフェノン、n−ペンタデカノフェノン、n−テトラデカノフェノン、4−n−ドデカアセトフェノン、n−トリデカノフェノン、4−n−ウンデカノアセトフェノン、n−ラウロフェノン、4−n−デカノアセトフェノン、n−ウンデカノフェノン、4−n−ノニルアセトフェノン、n−デカノフェノン、4−n−オクチルアセトフェノン、n−ノナノフェノン、4−n−ヘプチルアセトフェノン、n−オクタノフェノン、4−n−ヘキシルアセトフェノン、4−n−シクロヘキシルアセトフェノン、4−tert−ブチルプロピオフェノン、n−ヘプタフェノン、4−n−ペンチルアセトフェノン、シクロヘキシルフェニルケトン、ベンジル−n−ブチルケトン、4−n−ブチルアセトフェノン、n−ヘキサノフェノン、4−イソブチルアセトフェノン、1−アセトナフトン、2−アセトナフトン、シクロペンチルフェニルケトン等が挙げられる。
また、総炭素数が12乃至24のアリールアルキルケトン、例えば、n−オクタデカノフェノン、n−ヘプタデカノフェノン、n−ヘキサデカノフェノン、n−ペンタデカノフェノン、n−テトラデカノフェノン、4−n−ドデカアセトフェノン、n−トリデカノフェノン、4−n−ウンデカノアセトフェノン、n−ラウロフェノン、4−n−デカノアセトフェノン、n−ウンデカノフェノン、4−n−ノニルアセトフェノン、n−デカノフェノン、4−n−オクチルアセトフェノン、n−ノナノフェノン、4−n−ヘプチルアセトフェノン、n−オクタノフェノン、4−n−ヘキシルアセトフェノン、4−n−シクロヘキシルアセトフェノン、4−tert−ブチルプロピオフェノン、n−ヘプタフェノン、4−n−ペンチルアセトフェノン、シクロヘキシルフェニルケトン、ベンジル−n−ブチルケトン、4−n−ブチルアセトフェノン、n−ヘキサノフェノン、4−イソブチルアセトフェノン、1−アセトナフトン、2−アセトナフトン、シクロペンチルフェニルケトン等が挙げられる。
また、エーテル化合物としては、総炭素数10以上の脂肪族エーテル化合物が有効であり、ジペンチルエーテル、ジヘキシルエーテル、ジヘプチルエーテル、ジオクチルエーテル、ジノニルエーテル、ジデシルエーテル、ジウンデシルエーテル、ジドデシルエーテル、ジトリデシルエーテル、ジテトラデシルエーテル、ジペンタデシルエーテル、ジヘキサデシルエーテル、ジオクタデシルエーテル、デカンジオールジメチルエーテル、ウンデカンジオールジメチルエーテル、ドデカンジオールジメチルエーテル、トリデカンジオールジメチルエーテル、デカンジオールジエチルエーテル、ウンデカンジオールジエチルエーテル等が挙げられる。
更に、反応媒体としてより好適には、特開2006−137886号公報に記載される下記一般式(1)や、特開2006−188660号公報に記載される下記一般式(2)で示される化合物が用いられる。
〔式中、R1は水素原子又はメチル基を示し、mは0〜2の整数を示し、X1、X2のいずれか一方は−(CH2)nOCOR2又は−(CH2)nCOOR2、他方は水素原子を示し、nは0〜2の整数を示し、R2は炭素数4以上のアルキル基又はアルケニル基を示し、Y1及びY2は水素原子、炭素数1〜4のアルキル基、メトキシ基、又は、ハロゲンを示し、r及びpは1〜3の整数を示す。〕
〔式中、Rは炭素数8以上のアルキル基又はアルケニル基を示す。〕
前記式(1)で示される化合物のうち、R1が水素原子の場合、より広いヒステリシス幅を有する可逆熱変色性組成物が得られるため好適であり、更にR1が水素原子であり、且つ、mが0の場合がより好適である。
また、前記式(2)中のRは炭素数8以上のアルキル基又はアルケニル基を示すが、好ましくは炭素数10〜24のアルキル基、更に好ましくは炭素数12〜22のアルキル基である。
また、前記式(2)中のRは炭素数8以上のアルキル基又はアルケニル基を示すが、好ましくは炭素数10〜24のアルキル基、更に好ましくは炭素数12〜22のアルキル基である。
以下、本願発明の熱消去性インク組成物を具体的に記載した実施例について説明する。
(実施例1)
実施例1の熱消去性インク組成物は以下の方法によって製造する。
1)第1分散液の調製(第1のステップ)
ロイコ染料としてPSD-150(日本曹達株式会社製)を5gと、顕色剤としてビスフェノールA5gを混合機で粉砕混合した後、第1の分散剤としてシクロデキストリン1gを水300mlに溶解した液の中に投入し、撹拌混合することにより、黒色に発色した第1の分散液を調製する。
2)第2分散液の調製(第2のステップ)
反応媒体としてMARK-Ao50(n- octadecyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate)3g粉砕して得た粉体を、分散剤としてシクロデキストリン0.5gを水300mlに溶解した液の中に投入し、撹拌混合することにより第2の分散液を調製する。
3)第3のステップ
上記のようにして得られた第1の分散液300mlと、第2の分散液100mlとを混合撹拌して実施例1の熱消去性インク組成物を得る。
(実施例1)
実施例1の熱消去性インク組成物は以下の方法によって製造する。
1)第1分散液の調製(第1のステップ)
ロイコ染料としてPSD-150(日本曹達株式会社製)を5gと、顕色剤としてビスフェノールA5gを混合機で粉砕混合した後、第1の分散剤としてシクロデキストリン1gを水300mlに溶解した液の中に投入し、撹拌混合することにより、黒色に発色した第1の分散液を調製する。
反応媒体としてMARK-Ao50(n- octadecyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate)3g粉砕して得た粉体を、分散剤としてシクロデキストリン0.5gを水300mlに溶解した液の中に投入し、撹拌混合することにより第2の分散液を調製する。
3)第3のステップ
上記のようにして得られた第1の分散液300mlと、第2の分散液100mlとを混合撹拌して実施例1の熱消去性インク組成物を得る。
<評 価>
上記のようにし得られた熱消去性インク組成物をボールペン用の軸体に注入し、ボールペン本体に装着してボールペンとした。このボールペンを恒温槽内に載置し、70℃で5時間の加熱し、加熱前後における色の変化を目視により判定する。その結果、加熱前後における色の変化は認められない。
その後、当該ボールペンを用いて汎用のコピー紙に文字を書き、その後、文字を摩擦することにより、文字の色が消失する。
上記のようにし得られた熱消去性インク組成物をボールペン用の軸体に注入し、ボールペン本体に装着してボールペンとした。このボールペンを恒温槽内に載置し、70℃で5時間の加熱し、加熱前後における色の変化を目視により判定する。その結果、加熱前後における色の変化は認められない。
その後、当該ボールペンを用いて汎用のコピー紙に文字を書き、その後、文字を摩擦することにより、文字の色が消失する。
この発明は上記発明の実施の態様及び実施例の説明に何ら限定されるものではない。特許請求の範囲を逸脱せず、当業者が容易に想到できる範囲で種々の変形態様もこの発明に含まれる。
3,4…分散質
Claims (11)
- 顕色剤によって発色状態とされた染料と、
前記染料に接触して、温度に応じて、前記染料の発色状態を消色状態とする反応媒体と、
前記染料と前記反応媒体とを独立した分散質として分散させ、紙面上で消失する分散媒と、を含む熱消去性インク組成物。 - 前記顕色剤は電子受容性化合物を含み、前記染料は電子供与性呈色有機化合物を含む、請求項1に記載の熱消去性インク組成物。
- 前記電子供与性呈色有機化合物はロイコ染料であり、前記電子受容性化合物はフェノール性水酸基を有する化合物である、請求項2に記載の熱消去性インク組成物。
- 前記反応媒体は、溶融状態において前記顕色剤と接触することにより前記染料を消色状態とし、融点においてヒステリシスが得られる有機化合物である、請求項1から3の何れかに記載の熱消去性インク組成物。
- 前記結晶性有機化合物はアルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種である、請求項4に記載の熱消去性インク組成物。
- 前記染料と前記反応媒体の混合比はモル濃度比で1:0.5〜1:10である、請求項1〜5の何れかに記載の熱消去性インク組成物。
- 前記分散媒は水を含む、請求項1〜6の何れかに記載の熱消去性インク組成物。
- 紙面上で消失する分散媒へ、顕色剤によって発色状態とされた染料を分散させて第1の分散液を準備する第1のステップと、
前記分散媒へ、染料に接触して、温度に応じて、前記染料の発色状態を消色状態とする反応媒体を分散させて第2の分散液を準備する第2のステップと、
前記第1の分散液と前記第2の分散液とを混合する第3のステップと、
を含む熱消去性インク組成物の製造方法。 - 前記第1のステップは、
前記顕色剤はフェノール性水酸基を有する化合物を含み、前記染料はロイコ染料を含み、これらを結合させて発色状態としたインク原液を準備するステップと、
前記分散媒は水を含み、包接化合物を形成可能な化合物を第1の分散剤として、前記インク原液を前記分散媒へ分散させるステップと
を含み、
前記第2のステップは、
前記反応媒体はアルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種を含み、包接化合物を形成可能な化合物を第2の分散剤として、該アルコール化合物、エステル化合物、ケトン化合物、エーテル化合物及び酸アミド化合物の少なくとも1種を前記分散媒へ分散させるステップ、
を含む、請求項8に記載の熱消去性インク組成物の製造方法。 - 前記第3のステップにおいて、前記反応媒体が結晶を維持する温度で前記第1の分散液と前記第2の分散液とが混合される、請求項8又は9に記載の熱消去性インク組成物の製造方法。
- 顕色剤によって発色状態とされた染料と、発色状態を消色状態とする反応媒体と、をグレンミル及び/又はボールミルを用いて紙面上で消失する分散媒へ分散させる熱消去性インク組成物の製造方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015043470 | 2015-03-05 | ||
| JP2015043470 | 2015-03-05 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2016166319A true JP2016166319A (ja) | 2016-09-15 |
Family
ID=56898359
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015084537A Pending JP2016166319A (ja) | 2015-03-05 | 2015-04-16 | 熱消去性インク組成物及びその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2016166319A (ja) |
-
2015
- 2015-04-16 JP JP2015084537A patent/JP2016166319A/ja active Pending
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220275215A1 (en) | Compound for Use in Colour Change Compositions | |
| JP5276800B2 (ja) | 固形筆記体、固形筆記体セット | |
| JP2009166310A (ja) | 固形筆記体及びそれを用いた固形筆記体セット | |
| WO2014178373A1 (ja) | 固形筆記体 | |
| JP4093940B2 (ja) | 感温変色性色彩記憶性液状組成物 | |
| JP5638445B2 (ja) | 固形筆記体及びそれを用いた固形筆記体セット | |
| JP5926420B2 (ja) | 複合式筆記具 | |
| JP4707408B2 (ja) | 可逆熱変色性記録材及びそれを用いた可逆熱変色性表示体 | |
| JP2008217393A (ja) | 可逆熱変色性ic磁気表示カード | |
| JP4460845B2 (ja) | 可逆熱変色性マイクロカプセル顔料 | |
| JP4851159B2 (ja) | 可逆熱変色性マイクロカプセル顔料 | |
| JP6027424B2 (ja) | 固形筆記体 | |
| JP2016166319A (ja) | 熱消去性インク組成物及びその製造方法 | |
| JP2017170664A (ja) | 偽造防止媒体 | |
| JP2014235395A (ja) | 可逆熱変色性ラベル | |
| JP2014213543A (ja) | 可逆熱変色性印刷物 | |
| JP2012183690A (ja) | ボールペンレフィル及びそれを用いたボールペン | |
| JP2011126285A (ja) | 可逆熱変色性記録材及びそれを用いた可逆熱変色性表示体 | |
| JP2006263921A (ja) | 熱変色性筆記具セット | |
| JP6616108B2 (ja) | 消去性インク組成物及びその製造方法並びにその定着液 | |
| JP6800299B2 (ja) | 温度インジケーター | |
| JP5745261B2 (ja) | 複合式筆記具 | |
| JP5955666B2 (ja) | 描画セット及びそれを用いた描画方法 | |
| JP2014080453A (ja) | 固形筆記体及びそれを用いた固形筆記体セット | |
| JP4575574B2 (ja) | 可逆熱変色性マイクロカプセル顔料 |