JP2015046292A - 負極及び二次電池 - Google Patents
負極及び二次電池 Download PDFInfo
- Publication number
- JP2015046292A JP2015046292A JP2013176650A JP2013176650A JP2015046292A JP 2015046292 A JP2015046292 A JP 2015046292A JP 2013176650 A JP2013176650 A JP 2013176650A JP 2013176650 A JP2013176650 A JP 2013176650A JP 2015046292 A JP2015046292 A JP 2015046292A
- Authority
- JP
- Japan
- Prior art keywords
- negative electrode
- secondary battery
- liti
- charge
- active material
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
【課題】充放電効率を向上させることができる負極及び当該負極を備える二次電池を提供する。
【解決手段】スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有し、かつ、前記LiTi2O4と前記Na2Ti6O13の合計量に対する前記Na2Ti6O13の割合が10〜30質量%であることを特徴とする負極を提供する。
【選択図】図1
【解決手段】スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有し、かつ、前記LiTi2O4と前記Na2Ti6O13の合計量に対する前記Na2Ti6O13の割合が10〜30質量%であることを特徴とする負極を提供する。
【選択図】図1
Description
本発明は、負極及び当該負極を用いた二次電池に関する。
近年、パソコン、ビデオカメラ、携帯電話等の情報関連機器や通信機器等の急速な普及に伴い、その電源として利用される電池の開発が重要視されている。また、自動車産業界においても、電気自動車やハイブリッド自動車用の高出力且つ高容量の電池の開発が進められている。各種電池の中でも、エネルギー密度と出力が高いことから、リチウム電池が注目されている。そして、電池の性能向上のための活物質に関する研究が進められている(例えば、特許文献1〜5)。
例えば、特許文献1には、スピネル型構造のLiTi2O4を活物質として用いた負極と、Li2MnO3またはLiMnO2を活物質として用いた正極と、非水電解液とからなる非水電解液リチウム二次電池が記載されている。
例えば、特許文献1には、スピネル型構造のLiTi2O4を活物質として用いた負極と、Li2MnO3またはLiMnO2を活物質として用いた正極と、非水電解液とからなる非水電解液リチウム二次電池が記載されている。
しかし、スピネル型構造を有するLiTi2O4は充放電効率が低いという問題があった。
本発明は上記実情を鑑みて成し遂げられたものであり、本発明の目的は、充放電効率を向上させることができる負極及び当該負極を備える二次電池を提供することである。
本発明は上記実情を鑑みて成し遂げられたものであり、本発明の目的は、充放電効率を向上させることができる負極及び当該負極を備える二次電池を提供することである。
本発明の負極は、スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有し、かつ、前記LiTi2O4と前記Na2Ti6O13の合計量に対する前記Na2Ti6O13の割合が10〜30質量%であることを特徴とする。
負極において、上記LiTi2O4と、上記Na2Ti6O13とを組み合わせて用い、さらにLiTi2O4とNa2Ti6O13の比率を上記範囲とすることによって、Na2Ti6O13を用いない場合と比較して、負極の充放電効率を向上させることができる。
負極において、上記LiTi2O4と、上記Na2Ti6O13とを組み合わせて用い、さらにLiTi2O4とNa2Ti6O13の比率を上記範囲とすることによって、Na2Ti6O13を用いない場合と比較して、負極の充放電効率を向上させることができる。
本発明の二次電池は、正極、負極、及び前記正極と前記負極との間に介在する電解質層を備える二次電池であって、
前記負極が本発明の負極であることを特徴とする。
前記負極が本発明の負極であることを特徴とする。
本発明の二次電池は、リチウム二次電池又はナトリウム二次電池であることが好ましい。
本発明の負極は充放電効率に優れており、二次電池の充放電効率を向上させることができる。
本発明の負極は、スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有し、かつ、前記LiTi2O4と前記Na2Ti6O13の合計量に対する前記Na2Ti6O13の割合が10〜30質量%であることを特徴とする。
上述したように、負極活物質として用いられているスピネル型構造を有するLiTi2O4は、充放電効率が低いという問題があった。これは、スピネル型構造を有するLiTi2O4は単相での合成が難しく、TiO2やラムスデライト型構造を有するLiTi2O4等の不純物相の除去が困難なためであると考えられる。上記不純物相は、スピネル型構造を有するLiTi2O4とは充放電電位域が異なるため、上記不純物相に取り込まれたLiが脱離されず、Liが消費される副反応等が生じ、充放電効率が低くなると考えられる。なお、本発明において、充放電電位域とは、二次電池が、過充電、過放電にならない電位領域のことをいう。
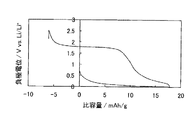
一方、本発明者は、図1に示すように、Na2Ti6O13はLiを吸蔵(挿入)することができ、さらには、驚くべきことに、吸蔵したLiのみならず、Naも放出し、充放電効率が100%を超えることを見出した(後述の参考実験例1)。すなわち、Na2Ti6O13は、吸蔵させたLi量よりも放出されるLi及びNaの合計量が多くなるため、Na2Ti6O13を負極に含有させることで、充電容量に対する放電容量の割合を高くすることが可能である。また、本発明者は、スピネル型構造を有するLiTi2O4が、Na2Ti6O13の充放電電位域と同じ充放電電位域で使用することができることを見出した。なお、スピネル型構造を有するLiTi2O4の充放電電位域は、具体的には、1.0〜2.0V(vs.Li/Li+)であり、Na2Ti6O13の充放電電位域は、具体的には、1.3〜1.5V(vs.Li/Li+)である。
本発明者は、上記知見から、本発明を完成させるに至った。
すなわち、スピネル型構造を有するLiTi2O4と、適量のNa2Ti6O13とを負極に含有させることによって、Na2Ti6O13が有効に機能し、二次電池の充放電効率を向上させることができる。
一方、本発明者は、図1に示すように、Na2Ti6O13はLiを吸蔵(挿入)することができ、さらには、驚くべきことに、吸蔵したLiのみならず、Naも放出し、充放電効率が100%を超えることを見出した(後述の参考実験例1)。すなわち、Na2Ti6O13は、吸蔵させたLi量よりも放出されるLi及びNaの合計量が多くなるため、Na2Ti6O13を負極に含有させることで、充電容量に対する放電容量の割合を高くすることが可能である。また、本発明者は、スピネル型構造を有するLiTi2O4が、Na2Ti6O13の充放電電位域と同じ充放電電位域で使用することができることを見出した。なお、スピネル型構造を有するLiTi2O4の充放電電位域は、具体的には、1.0〜2.0V(vs.Li/Li+)であり、Na2Ti6O13の充放電電位域は、具体的には、1.3〜1.5V(vs.Li/Li+)である。
本発明者は、上記知見から、本発明を完成させるに至った。
すなわち、スピネル型構造を有するLiTi2O4と、適量のNa2Ti6O13とを負極に含有させることによって、Na2Ti6O13が有効に機能し、二次電池の充放電効率を向上させることができる。
[負極]
本発明の負極は、少なくとも、スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有する。
本発明の負極の充放電電位域は、特に限定されないが、上記LiTi2O4及びNa2Ti6O13の充放電電位域の観点から、0.1〜2.0V(vs.Li/Li+)、特に1.0〜2.0V(vs.Li/Li+)の充放電電位域で使用することが好ましい。
本発明の負極は、少なくとも、スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有する。
本発明の負極の充放電電位域は、特に限定されないが、上記LiTi2O4及びNa2Ti6O13の充放電電位域の観点から、0.1〜2.0V(vs.Li/Li+)、特に1.0〜2.0V(vs.Li/Li+)の充放電電位域で使用することが好ましい。
スピネル型構造を有するLiTi2O4は、金属イオンを吸蔵、放出する負極活物質として機能するものである。スピネル型構造を有するLiTi2O4の製造方法は、特に限定されず、従来公知の方法を用いることができる。
Na2Ti6O13の製造方法は、特に限定されず、例えば、原料として、ナトリウム化合物及びチタン化合物を、Na2Ti6O13の化学組成となるように秤量、混合し、大気雰囲気下、焼成することによって製造することができる。
ナトリウム化合物としては、ナトリウムを含有するものであれば特に制限されず、例えば、Na2O、Na2O2等の酸化物、Na2CO3、NaNO3等の塩類、NaOHなどの水酸化物等が挙げられる。
チタン化合物としては、三価のチタンを含むものであれば特に限定されず、例えば、Ti2O3等の酸化物等が挙げられる。
原料を混合する方法は特に限定されず、例えば、乳鉢、ボールミル、メカノケミカル法等が挙げられる。
焼成温度は、例えば、650〜950℃とすることができる。
焼成時間は、少なくとも3時間以上であれば特に限定されず、例えば、3〜24時間とすることができる。
なお、ナトリウム化合物としてNa2CO3を用いる場合は、Na2CO3をNaO2とCO2とに分解させるため、上記焼成をする前に、原料を所定時間、大気雰囲気下、仮焼成してもよい。
仮焼成温度は、例えば、300〜500℃とすることができる。
仮焼成時間は、例えば、1〜24時間とすることができる。
ナトリウム化合物としては、ナトリウムを含有するものであれば特に制限されず、例えば、Na2O、Na2O2等の酸化物、Na2CO3、NaNO3等の塩類、NaOHなどの水酸化物等が挙げられる。
チタン化合物としては、三価のチタンを含むものであれば特に限定されず、例えば、Ti2O3等の酸化物等が挙げられる。
原料を混合する方法は特に限定されず、例えば、乳鉢、ボールミル、メカノケミカル法等が挙げられる。
焼成温度は、例えば、650〜950℃とすることができる。
焼成時間は、少なくとも3時間以上であれば特に限定されず、例えば、3〜24時間とすることができる。
なお、ナトリウム化合物としてNa2CO3を用いる場合は、Na2CO3をNaO2とCO2とに分解させるため、上記焼成をする前に、原料を所定時間、大気雰囲気下、仮焼成してもよい。
仮焼成温度は、例えば、300〜500℃とすることができる。
仮焼成時間は、例えば、1〜24時間とすることができる。
本発明の負極は、LiTi2O4とNa2Ti6O13の合計量に対して10〜30質量%のNa2Ti6O13を含有する。Na2Ti6O13の含有率が30質量%を超えると、充放電効率の向上効果を得ることができず、さらには、充電容量及び放電容量も低くなってしまう。また、Na2Ti6O13の含有率が10質量%未満だと、Na2Ti6O13の添加による、充放電効率向上効果を充分に得られないおそれがある。
本発明の負極は、典型的には、負極活物質層を備え、該負極活物質層が、上記LiTi2O4と上記Na2Ti6O13を含有し、且つ、LiTi2O4とNa2Ti6O13の合計量に対するNa2Ti6O13の割合が10〜30質量%である。また、本発明の負極は、負極活物質層のみからなるものであってもよいが、負極活物質層に加え、負極集電体を備えていてもよい。
負極活物質層は、必要に応じ、上記LiTi2O4と上記Na2Ti6O13に加え、導電材、結着剤等のその他成分を含有する。
その他成分を含有する場合、負極活物質層における、上記LiTi2O4及び上記Na2Ti6O13の合計量の割合は、例えば、85質量%以上とすることが好ましく、特に90質量%以上とすることが好ましい。
その他成分を含有する場合、負極活物質層における、上記LiTi2O4及び上記Na2Ti6O13の合計量の割合は、例えば、85質量%以上とすることが好ましく、特に90質量%以上とすることが好ましい。
導電材としては、負極活物質層の導電性を向上させることができるものであれば特に限定されず、例えば、アセチレンブラック、ケッチェンブラック等のカーボン材料等を挙げることができる。また、負極活物質層における導電材の含有割合は、導電材の種類によって異なるものであるが、負極活物質層の総質量を100質量%としたとき、通常、1〜30質量%である。
結着剤としては、例えば、ポリフッ化ビニリデン(PVdF)、ポリテトラフルオロエチレン(PTFE)、スチレンブタジエンゴム−カルボキシメチルセルロース(SBR−CMC)、ポリアクリル酸、ポリイミド、ポリアミック酸、ポリアミドイミド等を挙げることができる。また、負極活物質層における結着剤の含有割合は、負極活物質等を固定化できる程度であれば良く、より少ないことが好ましい。結着剤の含有割合は、負極活物質層の総質量を100質量%としたとき、通常、1〜10質量%である。
負極活物質層の層厚は、特に限定されないが、例えば、10〜100μm、中でも10〜50μmであることが好ましい。
負極活物質層の層厚は、特に限定されないが、例えば、10〜100μm、中でも10〜50μmであることが好ましい。
負極集電体は、上記負極活物質層の集電を行う機能を有するものである。負極集電体の材料は特に限定されないが、負極の充放電電位域における副反応防止の観点から、負極の充放電電位域において伝導金属イオン種と合金化反応を起こさない金属が好ましい。例えば、リチウム二次電池の場合には、3.0V(vs.Li/Li+)以下でLiと合金化反応を起こさない金属が好ましく、ナトリウム二次電池の場合には、3.0V(vs.Li/Li+)以下でNaと合金化反応を起こさない金属が好ましい。
リチウム二次電池、ナトリウム二次電池において使用可能な負極集電体としては、銅、SUS、ニッケル、鉄、チタン等を挙げることができる。負極集電体の形状としては、例えば、箔状、板状、メッシュ状等を挙げることができ、メッシュ状が好ましい。
リチウム二次電池、ナトリウム二次電池において使用可能な負極集電体としては、銅、SUS、ニッケル、鉄、チタン等を挙げることができる。負極集電体の形状としては、例えば、箔状、板状、メッシュ状等を挙げることができ、メッシュ状が好ましい。
負極を製造する方法は、特に限定されない。例えば、LiTi2O4、Na2Ti6O13、さらに必要に応じて、結着剤等のその他の成分を混合した混合物を、分散媒に分散させてスラリーを調製し、該スラリーを負極集電体上に塗布、乾燥、圧延する方法等が挙げられる。
分散媒は、特に限定されず、例えば、N−メチル−2−ピロリドン等が挙げられる。
塗布方法としては、ドクターブレード法、メタルマスク印刷法、静電塗布法、ディップコート法、スプレーコート法、ロールコート法、グラビアコート法、スクリーン印刷法等が挙げられる。
負極は、さらに、負極集電体に接続された負極リードを備えていてもよい。
分散媒は、特に限定されず、例えば、N−メチル−2−ピロリドン等が挙げられる。
塗布方法としては、ドクターブレード法、メタルマスク印刷法、静電塗布法、ディップコート法、スプレーコート法、ロールコート法、グラビアコート法、スクリーン印刷法等が挙げられる。
負極は、さらに、負極集電体に接続された負極リードを備えていてもよい。
[二次電池]
本発明の二次電池は、正極、負極、及び前記正極と前記負極との間に介在する電解質層を備える二次電池であって、前記負極が本発明の負極であることを特徴とする。
二次電池の種類としては、特に限定されず、例えば、金属二次電池(金属イオン二次電池を含む)、金属空気二次電池等が挙げられる。金属二次電池としては、例えば、リチウム二次電池、ナトリウム二次電池、マグネシウム二次電池、カルシウム二次電池等が挙げられ、リチウム二次電池及びナトリウム二次電池が好ましい。
本発明の二次電池は、正極、負極、及び前記正極と前記負極との間に介在する電解質層を備える二次電池であって、前記負極が本発明の負極であることを特徴とする。
二次電池の種類としては、特に限定されず、例えば、金属二次電池(金属イオン二次電池を含む)、金属空気二次電池等が挙げられる。金属二次電池としては、例えば、リチウム二次電池、ナトリウム二次電池、マグネシウム二次電池、カルシウム二次電池等が挙げられ、リチウム二次電池及びナトリウム二次電池が好ましい。
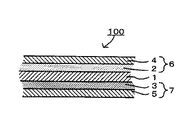
図2は、本発明の二次電池の一例を示す図であって、正極、電解質層及び負極の積層方向に切断した断面の模式図である。なお、本発明の二次電池は、必ずしもこの例のみに限定されない。
二次電池100は、正極活物質層2及び正極集電体4を含む正極6と、負極活物質層3及び負極集電体5を含む負極7と、正極6及び負極7に挟持される電解質層1を備える。
以下、本発明の二次電池の各構成について説明する。
二次電池100は、正極活物質層2及び正極集電体4を含む正極6と、負極活物質層3及び負極集電体5を含む負極7と、正極6及び負極7に挟持される電解質層1を備える。
以下、本発明の二次電池の各構成について説明する。
正極は、少なくとも正極活物質層を備え、通常は、さらに正極集電体を備える。
正極活物質層は、少なくとも正極活物質を含有し、必要に応じ導電材、結着剤等を含有する。
正極活物質としては、充放電時に金属イオンとなって正負極間を移動する金属を含有しており、金属イオンを吸蔵、放出することができるものであれば特に限定されない。
正極活物質の具体例としては、例えば、リチウム二次電池においては、LiCoO2、LiNi1/3Mn1/3Co1/3O2、LiNiPO4、LiCoPO4、LiFePO4、LiMnPO4、LiNiO2、LiMn2O4、LiCoMnO4、Li2NiMn3O8、Li3Fe2(PO4)3等、ナトリウム二次電池においては、Na2CrO4、NaCoPO4、NaMnPO4、Na4Co3(PO4)2P2O7、NaCo1/2Fe1/2O2、Na4[Fe(CN)6]、KFe2(CN)6、NaFeO2、NaNi1/2Mn1/2O2、Na2/3[Ni1/3Mn2/3]O2、Na2(Fe,Mn)PO4F等を用いることができる。
導電材、結着剤は、上述した負極活物質層における導電材、結着剤と同様とすることができる。
正極活物質層の厚さは、特に限定されないが、例えば、10〜250μm、中でも20〜200μmであることが好ましい。
正極集電体は、正極活物質層の集電を行う機能を有するものである。正極集電体の材料としては、例えば、SUS、ニッケル、アルミニウム、鉄、チタン、銅等の金属材料、カーボンファイバー、カーボンペーパー等のカーボン材料、窒化チタン等の高電子伝導性セラミックス材料等が挙げられる。また、正極集電体の形状としては、上述した負極集電体の形状と同様のものを採用することができる。
正極を製造する方法は、特に限定されず、例えば、負極と同様とすることができる。
正極は、さらに、正極集電体に接続された正極リードを備えていてもよい。
正極活物質層は、少なくとも正極活物質を含有し、必要に応じ導電材、結着剤等を含有する。
正極活物質としては、充放電時に金属イオンとなって正負極間を移動する金属を含有しており、金属イオンを吸蔵、放出することができるものであれば特に限定されない。
正極活物質の具体例としては、例えば、リチウム二次電池においては、LiCoO2、LiNi1/3Mn1/3Co1/3O2、LiNiPO4、LiCoPO4、LiFePO4、LiMnPO4、LiNiO2、LiMn2O4、LiCoMnO4、Li2NiMn3O8、Li3Fe2(PO4)3等、ナトリウム二次電池においては、Na2CrO4、NaCoPO4、NaMnPO4、Na4Co3(PO4)2P2O7、NaCo1/2Fe1/2O2、Na4[Fe(CN)6]、KFe2(CN)6、NaFeO2、NaNi1/2Mn1/2O2、Na2/3[Ni1/3Mn2/3]O2、Na2(Fe,Mn)PO4F等を用いることができる。
導電材、結着剤は、上述した負極活物質層における導電材、結着剤と同様とすることができる。
正極活物質層の厚さは、特に限定されないが、例えば、10〜250μm、中でも20〜200μmであることが好ましい。
正極集電体は、正極活物質層の集電を行う機能を有するものである。正極集電体の材料としては、例えば、SUS、ニッケル、アルミニウム、鉄、チタン、銅等の金属材料、カーボンファイバー、カーボンペーパー等のカーボン材料、窒化チタン等の高電子伝導性セラミックス材料等が挙げられる。また、正極集電体の形状としては、上述した負極集電体の形状と同様のものを採用することができる。
正極を製造する方法は、特に限定されず、例えば、負極と同様とすることができる。
正極は、さらに、正極集電体に接続された正極リードを備えていてもよい。
電解質層は、正極及び負極との間に保持され、正極及び負極との間の金属イオンの伝導を可能とする電解質を少なくとも含有する。
電解質としては、金属イオン伝導性を有していればよく、例えば、電解液、ゲル電解質、固体電解質等が挙げられる。これらは、1種類のみを単独で用いてもよいし、2種類以上を組み合わせて用いてもよい。
電解質としては、金属イオン伝導性を有していればよく、例えば、電解液、ゲル電解質、固体電解質等が挙げられる。これらは、1種類のみを単独で用いてもよいし、2種類以上を組み合わせて用いてもよい。
電解液としては、水系電解液、非水系電解液が挙げられる。
水系電解液としては、通常、金属塩及び水を含有したものを用いる。非水系電解液としては、通常、金属塩及び非水溶媒を含有したものを用いる。
金属塩としては、例えば、リチウム二次電池においては、LiPF6、LiBF4、LiClO4、LiAsF6、LiCF3SO3、LiN(SO2CF3)2(Li−TFSI)、LiN(SO2C2F5)2、LiC(SO2CF3)3等のリチウム塩、ナトリウム二次電池においては、NaPF6、NaBF4、NaClO4、NaCF3SO3、(CF3SO2)2NNa、NaN(FSO2)、NaC(CF3SO2)3等のナトリウム塩等を用いることができる。
水系電解液としては、通常、金属塩及び水を含有したものを用いる。非水系電解液としては、通常、金属塩及び非水溶媒を含有したものを用いる。
金属塩としては、例えば、リチウム二次電池においては、LiPF6、LiBF4、LiClO4、LiAsF6、LiCF3SO3、LiN(SO2CF3)2(Li−TFSI)、LiN(SO2C2F5)2、LiC(SO2CF3)3等のリチウム塩、ナトリウム二次電池においては、NaPF6、NaBF4、NaClO4、NaCF3SO3、(CF3SO2)2NNa、NaN(FSO2)、NaC(CF3SO2)3等のナトリウム塩等を用いることができる。
非水溶媒としては、例えば、エチレンカーボネート(EC)、プロピレンカーボネート(PC)、ブチレンカーボネート(BC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、エチルメチルカーボネート(EMC)、γ−ブチロラクトン、スルホラン、アセトニトリル(AcN)、ジメトキシメタン、1,2−ジメトキシエタン(DME)、1,3−ジメトキシプロパン、ジエチルエーテル、テトラエチレングリコールジメチルエーテル(TEGDME)、テトラヒドロフラン、2−メチルテトラヒドロフラン、ジメチルスルホキシド(DMSO)及びこれらの混合物等を挙げることができる。高誘電率、低粘度を確保する観点から、高誘電率、高粘度を有するEC、PC、BC等の環状カーボネート化合物と、低誘電率、低粘度を有するDMC、DEC、EMC等の鎖状カーボネート化合物の混合物が好ましく、EC、DMC、EMCの混合溶媒が特に好ましい。
非水系電解液における金属塩の濃度は、例えば、0.3〜5Mであればよく、0.8〜3Mであることが好ましく、1〜2.5Mであることが特に好ましく、1〜1.5Mであることがさらに好ましい。金属塩濃度が5Mを超えると、電解液の粘度が過度に高められ、ハイレートでの放電容量や低温での放電容量が低下するおそれがある。一方、金属塩の濃度が0.3M未満となると、金属イオンの消費に対して供給が追従できなくなり、ハイレートでの放電容量や低温での放電容量が低下するおそれがある。
非水系電解液における金属塩の濃度は、例えば、0.3〜5Mであればよく、0.8〜3Mであることが好ましく、1〜2.5Mであることが特に好ましく、1〜1.5Mであることがさらに好ましい。金属塩濃度が5Mを超えると、電解液の粘度が過度に高められ、ハイレートでの放電容量や低温での放電容量が低下するおそれがある。一方、金属塩の濃度が0.3M未満となると、金属イオンの消費に対して供給が追従できなくなり、ハイレートでの放電容量や低温での放電容量が低下するおそれがある。
ゲル電解質は、通常、非水系電解液にポリマーを添加してゲル化したものである。
ゲル電解質は、上述した非水系電解液に、ポリエチレンオキシド、ポリプロピレンオキシド、ポリアクリルニトリル、ポリビニリデンフロライド(PVdF)、ポリウレタン、ポリアクリレート、セルロース等のポリマーを添加し、ゲル化することにより得られる。
ゲル電解質は、上述した非水系電解液に、ポリエチレンオキシド、ポリプロピレンオキシド、ポリアクリルニトリル、ポリビニリデンフロライド(PVdF)、ポリウレタン、ポリアクリレート、セルロース等のポリマーを添加し、ゲル化することにより得られる。
固体電解質としては、硫化物固体電解質、酸化物固体電解質等を用いることができる。
硫化物固体電解質としては、具体的には、リチウム二次電池においては、Li2S−P2S5、Li2S−P2S3、Li2S−P2S3−P2S5、Li2S−SiS2、Li2S−Si2S、Li2S−B2S3、Li2S−GeS2、LiI−Li2S−P2S5、LiI−Li2S−SiS2−P2S5、Li2S−SiS2−Li4SiO4、Li2S−SiS2−Li3PO4、Li3PS4−Li4GeS4、Li3.4P0.6Si0.4S4、Li3.25P0.25Ge0.76S4、Li4−xGe1−xPxS4等を例示することができる。
酸化物固体電解質としては、具体的には、リチウム二次電池においては、LiPON(リン酸リチウムオキシナイトライド)、Li1.3Al0.3Ti0.7(PO4)3、La0.51Li0.34TiO0.74、Li3PO4、Li2SiO2、Li2SiO4等、ナトリウム二次電池においては、β−Al2O3、Na3Zr2Si2PO12等を例示することができる。
硫化物固体電解質としては、具体的には、リチウム二次電池においては、Li2S−P2S5、Li2S−P2S3、Li2S−P2S3−P2S5、Li2S−SiS2、Li2S−Si2S、Li2S−B2S3、Li2S−GeS2、LiI−Li2S−P2S5、LiI−Li2S−SiS2−P2S5、Li2S−SiS2−Li4SiO4、Li2S−SiS2−Li3PO4、Li3PS4−Li4GeS4、Li3.4P0.6Si0.4S4、Li3.25P0.25Ge0.76S4、Li4−xGe1−xPxS4等を例示することができる。
酸化物固体電解質としては、具体的には、リチウム二次電池においては、LiPON(リン酸リチウムオキシナイトライド)、Li1.3Al0.3Ti0.7(PO4)3、La0.51Li0.34TiO0.74、Li3PO4、Li2SiO2、Li2SiO4等、ナトリウム二次電池においては、β−Al2O3、Na3Zr2Si2PO12等を例示することができる。
電解質として電解液を用いる場合、正極と負極との間に、絶縁性多孔質体であるセパレータを配置し、該セパレータに電解液を含浸させることで、正極と負極との絶縁を確保することができる。セパレータとしては、多孔質膜であれば特に限定されず、例えば、ポリエチレン(PE)多孔膜、ポリプロピレン(PP)多孔膜等の多孔膜;および樹脂不織布、ガラス繊維不織布等の不織布等を挙げることができる。セパレータは、単層構造であっても良く、積層構造であっても良く、積層する膜の数、材質、膜厚は、特に限定されない。
本発明の二次電池は、正極、電解質層、負極等を収納する電池ケースを備えていてもよい。電池ケースの形状としては、具体的にはコイン型、平板型、円筒型、ラミネート型等を挙げることができる。また、本発明の二次電池は、積層型、捲回型のいずれも採用することができる。
以下に、実施例、比較例、参考実験例を挙げて、本発明をさらに具体的に説明するが、本発明は、これらの実施例のみに限定されるものではない。
[参考実験例1]
LiTi2O4を用いず、Na2Ti6O13、PVdF(株式会社クレハ製)、及びアセチレンブラック(電気化学工業株式会社製)を、Na2Ti6O13:PVdF:アセチレンブラック=85:10:5の質量比で混合したこと以外は、後述する実施例1と同様に負極を作製した。そして、作製した負極を用いて、後述する(評価用セルの作製)と同様に評価用セルを作製した。
そして、負極の電位の上限値を2.5V(vs.Li/Li+)、下限値を0.01V(vs.Li/Li+)に設定し、評価用セルの充放電試験を行った。初回充放電時の充放電曲線を図1に示す。図1に示すように、Na2Ti6O13は充電容量(約18mAh/g)に対する放電容量(約18mAh/g+約6mAh/g=24mAh/g)の割合が高くなる(充放電効率が100%を超える)ことがわかる。これは、Na2Ti6O13は、放電時に、充電時に吸蔵したLiのみならず、Naを放出することができ、充電時の金属イオン吸蔵量よりも放電時の金属イオン放出量が多くなるためであると考えられる。
LiTi2O4を用いず、Na2Ti6O13、PVdF(株式会社クレハ製)、及びアセチレンブラック(電気化学工業株式会社製)を、Na2Ti6O13:PVdF:アセチレンブラック=85:10:5の質量比で混合したこと以外は、後述する実施例1と同様に負極を作製した。そして、作製した負極を用いて、後述する(評価用セルの作製)と同様に評価用セルを作製した。
そして、負極の電位の上限値を2.5V(vs.Li/Li+)、下限値を0.01V(vs.Li/Li+)に設定し、評価用セルの充放電試験を行った。初回充放電時の充放電曲線を図1に示す。図1に示すように、Na2Ti6O13は充電容量(約18mAh/g)に対する放電容量(約18mAh/g+約6mAh/g=24mAh/g)の割合が高くなる(充放電効率が100%を超える)ことがわかる。これは、Na2Ti6O13は、放電時に、充電時に吸蔵したLiのみならず、Naを放出することができ、充電時の金属イオン吸蔵量よりも放電時の金属イオン放出量が多くなるためであると考えられる。
[Na2Ti6O13の合成]
Na2CO3とTi2O3とをNa:Ti=1:3(mol比)となるように混合し、大気雰囲気下450℃で12時間仮焼成した後、さらに、大気雰囲気下850℃で24時間焼成した。
その後、得られた粉末についてX線回折(XRD)測定を行い、Na2Ti6O13が合成されたことを確認した。
Na2CO3とTi2O3とをNa:Ti=1:3(mol比)となるように混合し、大気雰囲気下450℃で12時間仮焼成した後、さらに、大気雰囲気下850℃で24時間焼成した。
その後、得られた粉末についてX線回折(XRD)測定を行い、Na2Ti6O13が合成されたことを確認した。
[負極の作製]
(実施例1)
LiTi2O4とNa2Ti6O13とをLiTi2O4:Na2Ti6O13=9:1(質量比)となるように秤量し、乳鉢を用いて混合した。その後、該混合物、PVdF(株式会社クレハ製)、及びアセチレンブラック(電気化学工業株式会社製)を、混合物:PVdF:アセチレンブラック=85:10:5の質量比で混合し、溶媒N−メチル−2−ピロリドン(和光純薬工業株式会社製)に分散させてスラリーを調製した。該スラリーをドクターブレード法で銅箔(負極集電体)上に塗布して、直径16mmに打ち抜いた後、乾燥、圧延し、負極を得た。
(実施例1)
LiTi2O4とNa2Ti6O13とをLiTi2O4:Na2Ti6O13=9:1(質量比)となるように秤量し、乳鉢を用いて混合した。その後、該混合物、PVdF(株式会社クレハ製)、及びアセチレンブラック(電気化学工業株式会社製)を、混合物:PVdF:アセチレンブラック=85:10:5の質量比で混合し、溶媒N−メチル−2−ピロリドン(和光純薬工業株式会社製)に分散させてスラリーを調製した。該スラリーをドクターブレード法で銅箔(負極集電体)上に塗布して、直径16mmに打ち抜いた後、乾燥、圧延し、負極を得た。
(実施例2)
LiTi2O4:Na2Ti6O13=8:2(質量比)としたこと以外は実施例1と同様に負極を作製した。
LiTi2O4:Na2Ti6O13=8:2(質量比)としたこと以外は実施例1と同様に負極を作製した。
(実施例3)
LiTi2O4:Na2Ti6O13=7:3(質量比)としたこと以外は実施例1と同様に負極を作製した。
LiTi2O4:Na2Ti6O13=7:3(質量比)としたこと以外は実施例1と同様に負極を作製した。
(比較例1)
Na2Ti6O13を用いず、LiTi2O4、PVdF、及びアセチレンブラックを、LiTi2O4:PVdF:アセチレンブラック=85:10:5の質量比で混合したこと以外は、実施例1と同様に負極を作製した。
Na2Ti6O13を用いず、LiTi2O4、PVdF、及びアセチレンブラックを、LiTi2O4:PVdF:アセチレンブラック=85:10:5の質量比で混合したこと以外は、実施例1と同様に負極を作製した。
(比較例2)
LiTi2O4:Na2Ti6O13=6:4(質量比)としたこと以外は、実施例1と同様に負極を作製した。
LiTi2O4:Na2Ti6O13=6:4(質量比)としたこと以外は、実施例1と同様に負極を作製した。
(比較例3)
LiTi2O4:Na2Ti6O13=5:5(質量比)としたこと以外は、実施例1と同様に負極を作製した。
LiTi2O4:Na2Ti6O13=5:5(質量比)としたこと以外は、実施例1と同様に負極を作製した。
[負極の評価]
(評価用セルの作製)
上記にて作製した負極を用いて、以下のようにして評価用セルを作製した。
箔状のリチウム金属(本城金属株式会社製)をローラーで平滑化し、直径19mmに打抜いて対極を得た。
EC、DMC及びEMCをEC:DMC:EMC=3:4:3(体積比)で混合した混合溶媒に、リチウム塩(LiPF6)を1Mの濃度になるように溶解し、非水系電解液を調製した。
セパレータとして、ポリプロピレンからなる多孔質膜を準備した。
上記負極、対極、電解質及びセパレータと、2032型コインセルを用いてリチウム二次電池(コイン型)を作製した。
(評価用セルの作製)
上記にて作製した負極を用いて、以下のようにして評価用セルを作製した。
箔状のリチウム金属(本城金属株式会社製)をローラーで平滑化し、直径19mmに打抜いて対極を得た。
EC、DMC及びEMCをEC:DMC:EMC=3:4:3(体積比)で混合した混合溶媒に、リチウム塩(LiPF6)を1Mの濃度になるように溶解し、非水系電解液を調製した。
セパレータとして、ポリプロピレンからなる多孔質膜を準備した。
上記負極、対極、電解質及びセパレータと、2032型コインセルを用いてリチウム二次電池(コイン型)を作製した。
(充放電試験)
負極の電位の上限値を2.0V(vs.Li/Li+)、下限値を0.1V(vs.Li/Li+)に設定し、実施例1〜3、比較例1〜3で作製した負極の充放電試験を行った。
まず、25℃環境下で電流値0.025mA/cm2にて、負極電位が下限値0.1V(vs.Li/Li+)に達するまで充電した。
その後、10分間の休止後、25℃環境下で電流値0.025mA/cm2にて、負極電位が上限値2.0V(vs.Li/Li+)に達するまで放電した。
上記充電時の総通電量から負極活物質の単位質量当たりの初回充電容量(mAh/g)を算出した。また、上記放電時の総通電量から負極活物質の単位質量当たりの初回放電容量(mAh/g)を算出した。
そして、算出した初回放電容量と初回充電容量から、初回充電容量に対する初回放電容量の割合(初回充放電効率)を算出した。結果を表1に示す。
負極の電位の上限値を2.0V(vs.Li/Li+)、下限値を0.1V(vs.Li/Li+)に設定し、実施例1〜3、比較例1〜3で作製した負極の充放電試験を行った。
まず、25℃環境下で電流値0.025mA/cm2にて、負極電位が下限値0.1V(vs.Li/Li+)に達するまで充電した。
その後、10分間の休止後、25℃環境下で電流値0.025mA/cm2にて、負極電位が上限値2.0V(vs.Li/Li+)に達するまで放電した。
上記充電時の総通電量から負極活物質の単位質量当たりの初回充電容量(mAh/g)を算出した。また、上記放電時の総通電量から負極活物質の単位質量当たりの初回放電容量(mAh/g)を算出した。
そして、算出した初回放電容量と初回充電容量から、初回充電容量に対する初回放電容量の割合(初回充放電効率)を算出した。結果を表1に示す。
[評価結果]
表1に示すように、実施例1〜3の初回充放電効率は、比較例1と比較して向上した。一方、比較例2〜3の初回充放電効率は、比較例1と比較して減少した。また、実施例1〜3では、100mAh/g以上の充放電容量を保持しているのに対して、比較例2〜3では、充電容量及び放電容量共に、100mAh/gを大きく下回った。
以上の結果から、スピネル型構造を有するLiTi2O4に、Na2Ti6O13を、LiTi2O4とNa2Ti6O13の合計量に対するNa2Ti6O13の割合が10〜30質量%となるように添加することで、充放電容量100mAh/g以上を維持しつつ、充放電効率を向上させることができることがわかる。
表1に示すように、実施例1〜3の初回充放電効率は、比較例1と比較して向上した。一方、比較例2〜3の初回充放電効率は、比較例1と比較して減少した。また、実施例1〜3では、100mAh/g以上の充放電容量を保持しているのに対して、比較例2〜3では、充電容量及び放電容量共に、100mAh/gを大きく下回った。
以上の結果から、スピネル型構造を有するLiTi2O4に、Na2Ti6O13を、LiTi2O4とNa2Ti6O13の合計量に対するNa2Ti6O13の割合が10〜30質量%となるように添加することで、充放電容量100mAh/g以上を維持しつつ、充放電効率を向上させることができることがわかる。
1 電解質層
2 正極活物質層
3 負極活物質層
4 正極集電体
5 負極集電体
6 正極
7 負極
100 二次電池
2 正極活物質層
3 負極活物質層
4 正極集電体
5 負極集電体
6 正極
7 負極
100 二次電池
Claims (3)
- スピネル型構造を有するLiTi2O4と、Na2Ti6O13とを含有し、かつ、前記LiTi2O4と前記Na2Ti6O13の合計量に対する前記Na2Ti6O13の割合が10〜30質量%であることを特徴とする負極。
- 正極、負極、及び前記正極と前記負極との間に介在する電解質層を備える二次電池であって、
前記負極が請求項1に記載の負極であることを特徴とする二次電池。 - リチウム二次電池又はナトリウム二次電池である、請求項2に記載の二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013176650A JP2015046292A (ja) | 2013-08-28 | 2013-08-28 | 負極及び二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013176650A JP2015046292A (ja) | 2013-08-28 | 2013-08-28 | 負極及び二次電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2015046292A true JP2015046292A (ja) | 2015-03-12 |
Family
ID=52671642
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013176650A Pending JP2015046292A (ja) | 2013-08-28 | 2013-08-28 | 負極及び二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2015046292A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN120073090A (zh) * | 2025-03-18 | 2025-05-30 | 浙江古越电源有限公司 | 一种高能量充电效率快的密闭阀控式动力电池 |
-
2013
- 2013-08-28 JP JP2013176650A patent/JP2015046292A/ja active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN120073090A (zh) * | 2025-03-18 | 2025-05-30 | 浙江古越电源有限公司 | 一种高能量充电效率快的密闭阀控式动力电池 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5527385B2 (ja) | 正極活物質およびハイブリッドイオン電池 | |
| KR101497330B1 (ko) | 황-리튬 이온 전지용 전극 조립체 및 이를 포함하는 황-리튬 이온 전지 | |
| CA3040031C (en) | Battery module for starting a power equipment | |
| US20130252104A1 (en) | Positive electrode for lithium ion secondary battery and lithium ion secondary battery including positive electrode | |
| US20200335789A1 (en) | Method for suppressing thermal runaway caused by internal short circuit | |
| KR20170024862A (ko) | 유무기 복합 고체 전지 | |
| CN110556521A (zh) | 硅阳极材料 | |
| JP2020123460A (ja) | プレドープ材、プレドープ材を含む正極、並びに、その正極を備えた非水電解質二次電池の製造方法、及び、金属酸化物の製造方法 | |
| JP7640271B2 (ja) | 焼結材料及びその製造方法並びに固体電池の製造方法 | |
| US20140011083A1 (en) | Electrode for non-aqueous electrolyte secondary batteries and non-aqueous electrolyte secondary battery including the same | |
| JP2011192561A (ja) | 非水電解液二次電池の製造方法 | |
| CN107768722B (zh) | 锂离子电池和锂离子电池的制造方法 | |
| KR102036665B1 (ko) | 음극, 이의 제조방법 및 이를 포함하는 리튬 이차전지 | |
| WO2023120622A1 (ja) | 二次電池用正極およびその製造方法、ならびに二次電池 | |
| KR101116551B1 (ko) | 리튬 이차전지용 음극 및 이를 포함하는 리튬 이차 전지 | |
| CN115702509B (zh) | 电极和锂离子二次电池 | |
| JP2014110228A (ja) | 非水蓄電デバイス用電解液及びリチウムイオン二次電池 | |
| JP5831426B2 (ja) | リチウムイオン電池用負極活物質、リチウムイオン電池、及び、リチウムイオン電池の使用方法 | |
| JP7271891B2 (ja) | リチウムイオン二次電池用正極活物質、リチウムイオン二次電池用正極活物質の製造方法 | |
| JP5333658B2 (ja) | 電池用活物質および電池 | |
| JP2015046292A (ja) | 負極及び二次電池 | |
| US20220149384A1 (en) | Current collector, conductive layer forming paste, electrode, and energy storage device | |
| KR102207523B1 (ko) | 리튬 이차전지 | |
| JP2021106074A (ja) | 負極活物質 | |
| JP2014017157A (ja) | リチウム二次電池用正極活物質、リチウム二次電池用正極活物質の製造方法、及びリチウム二次電池 |