JP2013510079A - ポリシルアルキレンシロキサンの製造プロセス - Google Patents
ポリシルアルキレンシロキサンの製造プロセス Download PDFInfo
- Publication number
- JP2013510079A JP2013510079A JP2012535874A JP2012535874A JP2013510079A JP 2013510079 A JP2013510079 A JP 2013510079A JP 2012535874 A JP2012535874 A JP 2012535874A JP 2012535874 A JP2012535874 A JP 2012535874A JP 2013510079 A JP2013510079 A JP 2013510079A
- Authority
- JP
- Japan
- Prior art keywords
- acid
- ring
- siloxane monomer
- carbon atoms
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 238000004519 manufacturing process Methods 0.000 title abstract description 8
- 239000000178 monomer Substances 0.000 claims abstract description 79
- 239000000203 mixture Substances 0.000 claims abstract description 64
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 claims abstract description 60
- 238000000034 method Methods 0.000 claims abstract description 50
- 238000007151 ring opening polymerisation reaction Methods 0.000 claims abstract description 46
- 125000004122 cyclic group Chemical group 0.000 claims abstract description 24
- -1 siloxanes Chemical class 0.000 claims abstract description 17
- 230000002378 acidificating effect Effects 0.000 claims abstract description 15
- 239000002685 polymerization catalyst Substances 0.000 claims abstract description 15
- 238000002844 melting Methods 0.000 claims abstract description 7
- 230000008018 melting Effects 0.000 claims abstract description 7
- 230000008569 process Effects 0.000 claims description 38
- 125000004432 carbon atom Chemical group C* 0.000 claims description 35
- 239000003054 catalyst Substances 0.000 claims description 28
- 229920000642 polymer Polymers 0.000 claims description 20
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 claims description 20
- 239000002904 solvent Substances 0.000 claims description 18
- 125000001183 hydrocarbyl group Chemical group 0.000 claims description 13
- BKJGWMLFLSBAHC-UHFFFAOYSA-N 2,2,4,4,6,6,8,8-octamethyl-1,5,2,4,6,8-dioxatetrasilocane Chemical group C[Si]1(C)C[Si](C)(C)O[Si](C)(C)C[Si](C)(C)O1 BKJGWMLFLSBAHC-UHFFFAOYSA-N 0.000 claims description 12
- 238000002360 preparation method Methods 0.000 claims description 11
- 125000005843 halogen group Chemical group 0.000 claims description 10
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 8
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 8
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 claims description 8
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 claims description 8
- 238000007142 ring opening reaction Methods 0.000 claims description 8
- 239000002253 acid Substances 0.000 claims description 7
- 125000002947 alkylene group Chemical group 0.000 claims description 7
- 125000003118 aryl group Chemical group 0.000 claims description 7
- 229910052757 nitrogen Inorganic materials 0.000 claims description 6
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 6
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 6
- 239000004215 Carbon black (E152) Substances 0.000 claims description 5
- 150000007513 acids Chemical class 0.000 claims description 5
- 150000002148 esters Chemical class 0.000 claims description 5
- 229930195733 hydrocarbon Natural products 0.000 claims description 5
- 125000001424 substituent group Chemical group 0.000 claims description 5
- 229910052717 sulfur Inorganic materials 0.000 claims description 5
- 125000004434 sulfur atom Chemical group 0.000 claims description 5
- 125000004429 atom Chemical group 0.000 claims description 4
- QWPPOHNGKGFGJK-UHFFFAOYSA-N hypochlorous acid Chemical compound ClO QWPPOHNGKGFGJK-UHFFFAOYSA-N 0.000 claims description 4
- VUQUOGPMUUJORT-UHFFFAOYSA-N methyl 4-methylbenzenesulfonate Chemical compound COS(=O)(=O)C1=CC=C(C)C=C1 VUQUOGPMUUJORT-UHFFFAOYSA-N 0.000 claims description 4
- OIRDBPQYVWXNSJ-UHFFFAOYSA-N methyl trifluoromethansulfonate Chemical compound COS(=O)(=O)C(F)(F)F OIRDBPQYVWXNSJ-UHFFFAOYSA-N 0.000 claims description 4
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 claims description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 claims description 4
- 239000004721 Polyphenylene oxide Substances 0.000 claims description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 3
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 claims description 3
- 125000005003 perfluorobutyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 claims description 3
- 229920000570 polyether Polymers 0.000 claims description 3
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 claims description 3
- 239000011964 heteropoly acid Substances 0.000 claims 3
- 150000003457 sulfones Chemical class 0.000 claims 3
- 238000006116 polymerization reaction Methods 0.000 abstract description 11
- 239000007858 starting material Substances 0.000 abstract description 5
- 239000000543 intermediate Substances 0.000 abstract description 4
- 238000000746 purification Methods 0.000 abstract 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 24
- 238000006243 chemical reaction Methods 0.000 description 19
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 18
- 239000000047 product Substances 0.000 description 15
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 12
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 229910052786 argon Inorganic materials 0.000 description 6
- 229920001577 copolymer Polymers 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 5
- IALUUOKJPBOFJL-UHFFFAOYSA-N potassium oxidosilane Chemical class [K+].[SiH3][O-] IALUUOKJPBOFJL-UHFFFAOYSA-N 0.000 description 5
- 125000000217 alkyl group Chemical group 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 239000000460 chlorine Substances 0.000 description 4
- 229910052801 chlorine Inorganic materials 0.000 description 4
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 4
- 238000004821 distillation Methods 0.000 description 4
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical compound CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 4
- 238000001542 size-exclusion chromatography Methods 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- MFGOFGRYDNHJTA-UHFFFAOYSA-N 2-amino-1-(2-fluorophenyl)ethanol Chemical compound NCC(O)C1=CC=CC=C1F MFGOFGRYDNHJTA-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- HUCVOHYBFXVBRW-UHFFFAOYSA-M caesium hydroxide Inorganic materials [OH-].[Cs+] HUCVOHYBFXVBRW-UHFFFAOYSA-M 0.000 description 3
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 3
- 125000001309 chloro group Chemical group Cl* 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 238000006459 hydrosilylation reaction Methods 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical group [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 235000011054 acetic acid Nutrition 0.000 description 2
- 239000003929 acidic solution Substances 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 2
- 125000003710 aryl alkyl group Chemical group 0.000 description 2
- VTDZAHJRMRMQNP-UHFFFAOYSA-N chloro-[[chloro(dimethyl)silyl]methyl]-dimethylsilane Chemical compound C[Si](C)(Cl)C[Si](C)(C)Cl VTDZAHJRMRMQNP-UHFFFAOYSA-N 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical compound CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 238000005227 gel permeation chromatography Methods 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 2
- 150000002678 macrocyclic compounds Chemical class 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 2
- GKTNLYAAZKKMTQ-UHFFFAOYSA-N n-[bis(dimethylamino)phosphinimyl]-n-methylmethanamine Chemical compound CN(C)P(=N)(N(C)C)N(C)C GKTNLYAAZKKMTQ-UHFFFAOYSA-N 0.000 description 2
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 2
- 229960002446 octanoic acid Drugs 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 239000011574 phosphorus Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- CPRMKOQKXYSDML-UHFFFAOYSA-M rubidium hydroxide Chemical compound [OH-].[Rb+] CPRMKOQKXYSDML-UHFFFAOYSA-M 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 239000005051 trimethylchlorosilane Substances 0.000 description 2
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 2
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 2
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 1
- FRPZMMHWLSIFAZ-UHFFFAOYSA-N 10-undecenoic acid Chemical compound OC(=O)CCCCCCCCC=C FRPZMMHWLSIFAZ-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 239000005632 Capric acid (CAS 334-48-5) Substances 0.000 description 1
- 239000005635 Caprylic acid (CAS 124-07-2) Substances 0.000 description 1
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 1
- 239000005046 Chlorosilane Substances 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical group NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 238000005684 Liebig rearrangement reaction Methods 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 229920002845 Poly(methacrylic acid) Polymers 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 1
- YYQRGCZGSFRBAM-UHFFFAOYSA-N Triclofos Chemical compound OP(O)(=O)OCC(Cl)(Cl)Cl YYQRGCZGSFRBAM-UHFFFAOYSA-N 0.000 description 1
- NTSNXSJENBZFSF-UHFFFAOYSA-N [Na+].[SiH3][O-] Chemical compound [Na+].[SiH3][O-] NTSNXSJENBZFSF-UHFFFAOYSA-N 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- OBETXYAYXDNJHR-UHFFFAOYSA-N alpha-ethylcaproic acid Natural products CCCCC(CC)C(O)=O OBETXYAYXDNJHR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 238000000149 argon plasma sintering Methods 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- UXJHQBVRZUANLK-UHFFFAOYSA-N azanylidyne(dichloro)-$l^{5}-phosphane Chemical compound ClP(Cl)#N UXJHQBVRZUANLK-UHFFFAOYSA-N 0.000 description 1
- ZSTLPJLUQNQBDQ-UHFFFAOYSA-N azanylidyne(dihydroxy)-$l^{5}-phosphane Chemical class OP(O)#N ZSTLPJLUQNQBDQ-UHFFFAOYSA-N 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- KHAVLLBUVKBTBG-UHFFFAOYSA-N caproleic acid Natural products OC(=O)CCCCCCCC=C KHAVLLBUVKBTBG-UHFFFAOYSA-N 0.000 description 1
- 235000011089 carbon dioxide Nutrition 0.000 description 1
- 238000012656 cationic ring opening polymerization Methods 0.000 description 1
- OUKMJYHQZXBWNQ-UHFFFAOYSA-N cesium oxidosilane Chemical compound [Cs+].[SiH3][O-] OUKMJYHQZXBWNQ-UHFFFAOYSA-N 0.000 description 1
- 238000012668 chain scission Methods 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- KOPOQZFJUQMUML-UHFFFAOYSA-N chlorosilane Chemical compound Cl[SiH3] KOPOQZFJUQMUML-UHFFFAOYSA-N 0.000 description 1
- 239000007859 condensation product Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229920001795 coordination polymer Polymers 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 150000001923 cyclic compounds Chemical class 0.000 description 1
- 238000000113 differential scanning calorimetry Methods 0.000 description 1
- YWEUIGNSBFLMFL-UHFFFAOYSA-N diphosphonate Chemical compound O=P(=O)OP(=O)=O YWEUIGNSBFLMFL-UHFFFAOYSA-N 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229920006158 high molecular weight polymer Polymers 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229920000592 inorganic polymer Polymers 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- KBJKWYZQIJZAOZ-UHFFFAOYSA-N lithium;oxidosilane Chemical compound [Li+].[SiH3][O-] KBJKWYZQIJZAOZ-UHFFFAOYSA-N 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- HMMGMWAXVFQUOA-UHFFFAOYSA-N octamethylcyclotetrasiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O1 HMMGMWAXVFQUOA-UHFFFAOYSA-N 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 235000021313 oleic acid Nutrition 0.000 description 1
- 125000000962 organic group Chemical group 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 125000005375 organosiloxane group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- ITMJUULNSKIGHA-UHFFFAOYSA-N oxidosilane rubidium(1+) Chemical compound [Rb+].[SiH3][O-] ITMJUULNSKIGHA-UHFFFAOYSA-N 0.000 description 1
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 1
- DLYUQMMRRRQYAE-UHFFFAOYSA-N phosphorus pentoxide Inorganic materials O1P(O2)(=O)OP3(=O)OP1(=O)OP2(=O)O3 DLYUQMMRRRQYAE-UHFFFAOYSA-N 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 239000012264 purified product Substances 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- UOULCEYHQNCFFH-UHFFFAOYSA-M sodium;hydroxymethanesulfonate Chemical compound [Na+].OCS([O-])(=O)=O UOULCEYHQNCFFH-UHFFFAOYSA-M 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000007155 step growth polymerization reaction Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- NBRKLOOSMBRFMH-UHFFFAOYSA-N tert-butyl chloride Chemical compound CC(C)(C)Cl NBRKLOOSMBRFMH-UHFFFAOYSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000005622 tetraalkylammonium hydroxides Chemical class 0.000 description 1
- TUNFSRHWOTWDNC-HKGQFRNVSA-N tetradecanoic acid Chemical compound CCCCCCCCCCCCC[14C](O)=O TUNFSRHWOTWDNC-HKGQFRNVSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- ZDHXKXAHOVTTAH-UHFFFAOYSA-N trichlorosilane Chemical compound Cl[SiH](Cl)Cl ZDHXKXAHOVTTAH-UHFFFAOYSA-N 0.000 description 1
- 229960001147 triclofos Drugs 0.000 description 1
- 125000000725 trifluoropropyl group Chemical group [H]C([H])(*)C([H])([H])C(F)(F)F 0.000 description 1
- GYIODRUWWNNGPI-UHFFFAOYSA-N trimethyl(trimethylsilylmethyl)silane Chemical compound C[Si](C)(C)C[Si](C)(C)C GYIODRUWWNNGPI-UHFFFAOYSA-N 0.000 description 1
- ODKIUNOEAXCLRI-UHFFFAOYSA-N tris(methylsilyl) phosphate Chemical compound C[SiH2]OP(=O)(O[SiH2]C)O[SiH2]C ODKIUNOEAXCLRI-UHFFFAOYSA-N 0.000 description 1
- 229960002703 undecylenic acid Drugs 0.000 description 1
- 229940005605 valeric acid Drugs 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L83/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon only; Compositions of derivatives of such polymers
- C08L83/04—Polysiloxanes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0834—Compounds having one or more O-Si linkage
- C07F7/0838—Compounds with one or more Si-O-Si sequences
- C07F7/0872—Preparation and treatment thereof
- C07F7/0874—Reactions involving a bond of the Si-O-Si linkage
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/20—Polysiloxanes containing silicon bound to unsaturated aliphatic groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/48—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule in which at least two but not all the silicon atoms are connected by linkages other than oxygen atoms
- C08G77/485—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule in which at least two but not all the silicon atoms are connected by linkages other than oxygen atoms containing less than 25 silicon atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/48—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule in which at least two but not all the silicon atoms are connected by linkages other than oxygen atoms
- C08G77/50—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule in which at least two but not all the silicon atoms are connected by linkages other than oxygen atoms by carbon linkages
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Silicon Polymers (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Description
a)シロキサンモノマー及び線状オリゴマーの混合物を形成する、酸性又は塩基性開環重合触媒の存在下での、以下の構造の環状モノマーの開環重合を行うステップと、
(i)1〜14個の炭素原子を有する線状又は分岐アルキレン基、及び、
(ii)6〜20個の炭素原子を有する芳香族基
から選択され、各Rは同じ又は異なり、H、OH、1〜18個の炭素原子を有する炭化水素基、1〜18個の炭素原子を有する置換炭化水素基又は最大18個の炭素原子を有する炭化水素オキシ基であり、nは1〜6の整数である)
b)任意に適切な溶媒を用いてステップ(a)において調製された線状オリゴマーを除去するステップと、
c)前記溶媒が存在する場合には除去するステップと、
を具えるプロセスによって得られる、シロキサンモノマー混合物が提供される。
a)シロキサンモノマー及び線状オリゴマーの混合物を形成する、酸性又は塩基性開環重合触媒の存在下での、以下の構造の環状モノマーの開環重合を行うステップと、
(i)1〜14個の炭素原子を有する線状又は分岐アルキレン基、及び、
(ii)6〜20個の炭素原子を有する芳香族基
から選択され、各Rは同じ又は異なり、H、OH、1〜18個の炭素原子を有する炭化水素基、1〜18個の炭素原子を有する置換炭化水素基又は最大18個の炭素原子を有する炭化水素オキシ基であり、nは1〜6の整数である)
b)任意に、適切な溶媒を用いてステップ(a)において調製された線状オリゴマーを除去するステップと、
c)前記溶媒が存在する場合には除去するステップと、
を具える、シロキサンモノマー混合物を得るための方法が提供される。
本発明に従って用いられる環状モノマーは、以下の一般構造を有する。
(i)1〜14個の炭素原子を有する線状又は分岐アルキレン基、及び
(ii)6〜20個の炭素原子を有する芳香族基
から選択される。)
あるいは、各Xは1〜6個の炭素原子を有する線状又は分岐アルキレン基である。一般的には、Xはメチレン基又はエチレン基である。線状又は分岐アルキレン基はある程度の置換を含有することができる。
Z1−PCl2=N(−PCl2=N)n−PCl2−O
を有する有機ケイ素基を含有する酸素含有クロロホスファゼンを含むことができる。式中、Z1は酸素によってリンに結合した有機ケイ素基、塩素原子又はヒドロキシル基を表し、nは0又は1〜8の整数を表す。前記触媒は、上記及び/又はそれらの互変異性体の縮合生成物を含むこともできる(触媒は、Z1がヒドロキシル基である場合、互変異性体形態で存在する)。塩素原子のすべて又はいくつかはQ基により置き換えることができ、Qはヒドロキシル基、一価有機基、例えばアルコキシ基又はアリールオキシ基、塩素以外のハロゲン原子、有機ケイ素基及びリン含有基を表す。式(I)の酸素含有クロロホスファゼンは好適には塩素原子をQ基により置き換えていないものである。多数のホスファゼン塩基及びそれらの合成経路については文献、例えば、Schwesinger et al,Liebigs Ann.1996年,1055−1081頁に記載されている。
前記シロキサンモノマー混合物を、上述したように同様の酸性又は塩基性開環重合触媒の存在下において、前記混合物の融点範囲内の温度で、開環重合するステップを具える、プロセスを提供する。
a)シロキサンモノマー及び線状オリゴマーの混合物を形成する、酸性又は塩基性開環重合触媒の存在下での、以下の構造の環状モノマーの開環重合を行うステップと、
b)任意に、適切な溶媒を用いてステップ(a)において調製された線状オリゴマーを除去するステップと、
c)前記溶媒が存在する場合には除去し、シロキサンモノマー混合物を調製するステップと、
d)該シロキサンモノマー混合物を、上述した同様の酸性又は塩基性開環重合触媒の存在下で、該シロキサンモノマー混合物の融点範囲内の温度で開環重合するステップと、
を具える、プロセスを提供する。
(環状モノマーの調製)
環状モノマーは、いずれかの適切な調製方法によって調製することができる。1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンの場合、その調製経路についていくつか記載されており、これらのいずれかを用いることができるが、完全を期すため、この一連の実施例においてその調製に用いられる2段階法を以下に示す。
(ビス−(クロロジメチルシリル)−メタンの合成)
40.4g(0.2519mol)[1mol部]のビス−(トリメチルシリル)−メタン(Gelest)、200g(1.84mol)[7.3mol部]のトリメチルクロロシラン(Aldrich)及び4g(0.03mol)[0.12mol部]の塩化アルミニウム(Aldrich)を3口丸底フラスコ中に添加し、57℃、アルゴンブランケット下で撹拌した。形成されたいずれかのテトラメチルシランを反応器から蒸留し、ビス(クロロシラン)を形成した。反応の温度を80℃より低く維持し、調製期間中を通してトリス−クロロシラン又は他の異性体の形成を防止した。48時間後、150gのトリメチルクロロシランを回収した。冷却後、反応混合物を室温で蒸発させ、20mlのアセトンをフラスコ中に添加し、触媒を不活性化した。最終生成物を63℃、20mmHgの減圧下での蒸留により精製した。約95%の純度を約80%の収率とともに得た。
(1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンの合成)
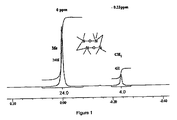
酸化亜鉛(17.5g、0.209mol)(1.6mol部)及び酢酸エチル(54ml)を、滴下漏斗、機械的攪拌器、及び窒素出口を有する還流冷却器を備えた250ml丸底3口フラスコ中に導入した。1時間かけて、40mlの酢酸エチル中の(27g、0.1343mol)(1mol部)のビス−(クロロジメチルシリル)−メタンの溶液を室温でフラスコに添加した。添加が完了した後、撹拌を8時間継続させた。次に得られた混合物を83mlの飽和重炭酸ナトリウム水溶液中に激しい撹拌下で導入した。有機相を無水硫酸ナトリウムを用いて分離及び乾燥させた。得られた乾燥生成物を次に60℃、1mbarの減圧下での蒸留により精製した。約15gの1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンが得られ、これは約40%の収率に対応する。精製した生成物の1HNMR(400Mhz、CDCl3)を図1に示す;δ=0(s、24H)SiCH3;−0.23(s、2H)SiCH2。
[比較例1]
Interrante他により主張されたプロセスに従って、以下のプロセスを用いる1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンの開環重合のための一連の1段階プロセスにより高分子量線状ポリマーを生成することを試みた。重合条件及び結果を以下に表1において記載する。
実施例1
(シロキサンモノマー混合物の調製)
8gの上述のように得られた1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタン(環状モノマー)、及び、8μlのトリフリン酸を、3口丸底フラスコ中に導入し、アルゴンブランケットの下、96時間25℃で撹拌し、シロキサンモノマー及び線状オリゴマーの混合物を調製した。メタノール(クロマトグラフィーグレード)を1体積部の混合物対10体積部のメタノールの量で混合物中に導入した。存在する線状オリゴマーは、メタノールの存在によって沈殿させた後、残ったシロキサンモノマーの混合物を含有する浮遊物から容易に分離した。メタノールを得られた浮遊物から回転蒸発器における蒸発により除去し、シロキサンモノマーの粗混合物を得た。粗混合物を蒸留することによりシロキサンモノマーを精製し、シロキサンモノマーの混合物の98%の収率を得た。精製されたシロキサンモノマーを次にプロトンにより特徴づけ、本発明によるシロキサンモノマー混合物の存在を確認した。
実施例2
(高分子量ポリシルアルキレンシロキサンポリマー(生成物A)の調製)
2gの実施例1において生成されたシロキサンモノマー混合物、及び、2μlのトリフリン酸を3口丸底フラスコ中に導入し、アルゴンブランケット下、4時間25℃で撹拌した。生成物Aを、次に過剰メタノール及び2μLのトリエチルアミンの混合物中に沈殿させることにより回収した。
実施例3
(高分子量ポリシルアルキレンシロキサンポリマー(生成物B)の調製)
4gの上記調製されたシロキサンモノマー混合物、及び、4μlの溶媒(ジクロロメタン)中のトリフリン酸を3口丸底フラスコ中に導入し、アルゴンブランケット下、4時間25℃で撹拌し、生成物Bを生成した。生成物Bを、過剰メタノール及び4μLのトリエチルアミンの混合物中に沈殿させた。
比較例2
実施例3において生成されたメタノール可溶性相を次に蒸発させ、蒸留により精製し、生成物C、すなわち、未反応1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンを得た。1gの実施例3の生成物、及び4μlのトリフリン酸を、その後、生成物Cとともに3口丸底フラスコ中に導入し、アルゴンブランケット下、96時間25℃で撹拌し、生成物Dを得た。しかしながら、このプロセスは、以下の表2において見られるように、高分子量ポリマーを生成することができなかった。これは実施例3において生成されたメタノール可溶性相へのトリエチルアミンの導入が残ったトリフリン酸のようなその中のいずれかの残った酸性種を効率的に中和したためであり得ると考えられる。
Claims (21)
- a)シロキサンモノマー及び線状オリゴマーの混合物を形成する、酸性又は塩基性開環重合触媒の存在下での、以下の構造の環状モノマーの開環重合を行うステップと、
(ここで、Xは、
(i)1〜14個の炭素原子を有する線状又は分岐アルキレン基、及び、
(ii)6〜20個の炭素原子を有する芳香族基
から選択され、各Rは同じ又は異なり、H、OH、1〜18個の炭素原子を有する炭化水素基、1〜18個の炭素原子を有する置換炭化水素基又は最大18個の炭素原子を有する炭化水素オキシ基であり、nは1〜6の整数である)
b)任意に適切な溶媒を用いてステップ(a)において調製された線状オリゴマーを除去するステップと、
c)前記溶媒が存在する場合には除去するステップと、
を具えるプロセスによって得られる、シロキサンモノマー混合物。 - 前記環状モノマーが、1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンであることを特徴とする、請求項1に記載のシロキサンモノマー混合物。
- 前記開環触媒が、ヘテロポリ酸、過塩素酸、硫酸、塩酸、HI、HBr、HClO4、H2SO4、HNO3、H3PO4、パラ−トルエンスルホン酸、トリフルオロ酢酸、ペルフルオロアルケンスルホン酸、メチルトシレート、メチルトリフレート及びシリルエステルトリフルオロメタンスルホン酸、からなる群より選択されることを特徴とする、請求項1又は2に記載のシロキサンモノマー混合物。
- 前記開環触媒がトリフリン酸であることを特徴とする、請求項3に記載のシロキサンモノマー混合物。
- ステップ(a)が15℃〜50℃の温度で行われることを特徴とする、前請求項のいずれかに記載のシロキサンモノマー混合物。
- Xが1〜18個の炭素原子を有する置換炭化水素基であるとき、置換基が、ハロゲン原子、ハロゲン原子含有基、酸素原子、酸素原子含有基、窒素原子、窒素原子含有基、硫黄原子、及び硫黄原子含有基、から選択される、請求項1に記載のシロキサンモノマー混合物。
- Xが1〜18個の炭素原子を有する置換炭化水素基であるとき、前記ハロゲン原子含有基が、クロロメチル、ペルフルオロブチル、トリフルオロエチル、及びノナフルオロへキシルの1つ以上から選択され、前記酸素原子含有基が、(メタ)アクリル、カルボキシル及びポリエーテルの1つ以上から選択される、請求項6に記載のシロキサンモノマー混合物。
- a)シロキサンモノマー及び線状オリゴマーの混合物を形成する、酸性又は塩基性開環重合触媒の存在下での、以下の構造の環状モノマーの開環重合を行うステップと、
(ここで、Xは、
(i)1〜14個の炭素原子を有する線状又は分岐アルキレン基、及び、
(ii)6〜20個の炭素原子を有する芳香族基
から選択され、各Rは同じ又は異なり、H、OH、1〜18個の炭素原子を有する炭化水素基、1〜18個の炭素原子を有する置換炭化水素基又は最大18個の炭素原子を有する炭化水素オキシ基であり、nは1〜6の整数である)
b)任意に、適切な溶媒を用いてステップ(a)において調製された線状オリゴマーを除去するステップと、
c)前記溶媒が存在する場合には除去するステップと、
を具える、シロキサンモノマー混合物を得るための方法。 - 前記環状モノマーが、1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンであることを特徴とする、請求項8に記載の方法。
- 前記開環触媒が、ヘテロポリ酸、過塩素酸、硫酸、塩酸、HI、HBr、HClO4、H2SO4、HNO3、H3PO4、パラ−トルエンスルホン酸、トリフルオロ酢酸、ペルフルオロアルケンスルホン酸、メチルトシレート、メチルトリフレート及びシリルエステルトリフルオロメタンスルホン酸、からなる群より選択されることを特徴とする、請求項8又は9に記載の方法。
- 前記開環触媒がトリフリン酸であることを特徴とする、請求項10に記載の方法。
- ステップ(a)が15℃〜50℃の温度で行われることを特徴とする、請求項8〜11のいずれか1項に記載の方法。
- Xが1〜18個の炭素原子を有する置換炭化水素基であるとき、置換基が、ハロゲン原子、ハロゲン原子含有基、酸素原子、酸素原子含有基、窒素原子、窒素原子含有基、硫黄原子、及び硫黄原子含有基、から選択される、請求項8に記載のシロキサンモノマー混合物。
- Xが1〜18個の炭素原子を有する置換炭化水素基であるとき、前記ハロゲン原子含有基が、クロロメチル、ペルフルオロブチル、トリフルオロエチル、及びノナフルオロへキシルの1つ以上から選択され、前記酸素原子含有基が、(メタ)アクリル、カルボキシル及びポリエーテルの1つ以上から選択される、請求項13に記載のシロキサンモノマー混合物。
- 以下の繰り返し単位を含む高分子量線状ポリシルアルキレンシロキサンポリマーを得るためのプロセスであって、
(ここで、X、R及びnは、請求項8において定義したとおりである。)
a)シロキサンモノマー及び線状オリゴマーの混合物を形成する、酸性又は塩基性開環重合触媒の存在下での、以下の構造の環状モノマーの開環重合を行うステップと、
(ここで、X及びRは前述のとおりであり、nは1〜6の整数である。)
b)任意に、適切な溶媒を用いてステップ(a)において調製された線状オリゴマーを除去するステップと、
c)前記溶媒が存在する場合には除去し、シロキサンモノマー混合物を調製するステップと、
d)該シロキサンモノマー混合物を、上述した同様の酸性又は塩基性開環重合触媒の存在下で、該シロキサンモノマー混合物の融点範囲内の温度で開環重合するステップと、
を具える、プロセス。 - 前記環状モノマーが、1,1,3,3,5,5,7,7−オクタメチル−2,6−ジオキサ−1,3,5,7−テトラシラシクロオクタンであることを特徴とする、請求項16又は17に記載のプロセス。
- 前記開環触媒が、ヘテロポリ酸、過塩素酸、硫酸、塩酸、HI、HBr、HClO4、H2SO4、HNO3、H3PO4、パラ−トルエンスルホン酸、トリフルオロ酢酸、ペルフルオロアルケンスルホン酸、メチルトシレート、メチルトリフレート及びシリルエステルトリフルオロメタンスルホン酸、からなる群より選択されることを特徴とする、請求項16、17又は18に記載のプロセス。
- 前記開環触媒がトリフリン酸であることを特徴とする、請求項19に記載のプロセス。
- ステップ(a)が15℃〜50℃の温度で行われることを特徴とする、請求項17〜20のいずれか1項に記載のプロセス。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP09306051 | 2009-11-03 | ||
| EP09306051.5 | 2009-11-03 | ||
| PCT/EP2010/066661 WO2011054830A1 (en) | 2009-11-03 | 2010-11-02 | A process for the production of polysilalkylenesiloxanes |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013510079A true JP2013510079A (ja) | 2013-03-21 |
| JP2013510079A5 JP2013510079A5 (ja) | 2015-03-12 |
Family
ID=43499983
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012535874A Ceased JP2013510079A (ja) | 2009-11-03 | 2010-11-02 | ポリシルアルキレンシロキサンの製造プロセス |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8586690B2 (ja) |
| EP (1) | EP2496585A1 (ja) |
| JP (1) | JP2013510079A (ja) |
| KR (1) | KR20120080247A (ja) |
| CN (1) | CN102596970B (ja) |
| WO (1) | WO2011054830A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5533906B2 (ja) * | 2011-02-28 | 2014-06-25 | 信越化学工業株式会社 | 付加反応硬化型オルガノポリシルメチレンシロキサンコポリマー組成物 |
| JP5697160B2 (ja) * | 2011-11-10 | 2015-04-08 | 信越化学工業株式会社 | オルガノポリシロキサン組成物及びその硬化物 |
| KR101939234B1 (ko) | 2012-07-23 | 2019-01-16 | 삼성전자 주식회사 | 메모리 장치, 메모리 시스템 및 상기 메모리 장치의 독출 전압의 제어 방법 |
| MY155102A (en) * | 2013-01-09 | 2015-09-07 | Daicel Corp | Curable resin composition, and cured product of same |
| CN104817699A (zh) * | 2015-04-24 | 2015-08-05 | 浙江润禾有机硅新材料有限公司 | 一种乙烯基硅油及其制备方法 |
| CN104788679A (zh) * | 2015-04-24 | 2015-07-22 | 浙江润禾有机硅新材料有限公司 | 含亚烷基结构的乙烯基硅油及其制备方法 |
| EP3153540B8 (en) | 2015-10-09 | 2018-07-25 | Dow Silicones Corporation | Process for preparing linear carbosiloxane polymers |
| TWI705598B (zh) * | 2019-11-29 | 2020-09-21 | 輝能科技股份有限公司 | 電能供應系統與其封裝結構 |
| CN114634525A (zh) * | 2020-12-16 | 2022-06-17 | 江西贝特利新材料有限公司 | 一种四甲基环四硅氧烷的制备方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0465429A (ja) * | 1990-07-06 | 1992-03-02 | Shin Etsu Chem Co Ltd | ポリシルエチレンシロキサン |
| JPH05222066A (ja) * | 1992-02-17 | 1993-08-31 | Shin Etsu Chem Co Ltd | 新規有機ケイ素化合物 |
| JPH05279373A (ja) * | 1992-04-01 | 1993-10-26 | Shin Etsu Chem Co Ltd | 5員環状シルエチレンシロキサンの製造方法 |
| US6080829A (en) * | 1998-06-24 | 2000-06-27 | Medtronic, Inc. | Silalkylenesiloxane copolymer materials and methods for their preparation |
| WO2001030887A1 (fr) * | 1999-10-28 | 2001-05-03 | Japan Science And Technology Corporation | Procede de polymerisation de silalkylenesiloxanes |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2229514C3 (de) | 1972-06-16 | 1979-01-04 | Wacker-Chemie Gmbh, 8000 Muenchen | Verfahren zur Förderung von Kondensations- und/oder Äquilibrierungsreaktionen von Organosiliciumverbindungen |
| DE3428581A1 (de) | 1984-08-02 | 1986-02-13 | Wacker-Chemie GmbH, 8000 München | Verfahren zum stabilisieren von organopolysiloxanen |
| DE3533028A1 (de) | 1985-09-16 | 1987-03-19 | Wacker Chemie Gmbh | Verfahren zum stabilisieren von organopolysiloxanen |
| EP0465262B1 (en) * | 1990-07-06 | 1996-06-05 | Shin-Etsu Chemical Co., Ltd. | Polysilethylenesiloxane |
| EP0465263B1 (en) | 1990-07-06 | 1996-10-09 | Shin-Etsu Chemical Co., Ltd. | Polysilethylenesiloxane |
| GB9103666D0 (en) | 1991-02-21 | 1991-04-10 | Dow Corning Sa | Method of making organopolysiloxanes |
| JPH0770324A (ja) | 1993-09-03 | 1995-03-14 | Toray Dow Corning Silicone Co Ltd | 有機ケイ素重合体の製造方法 |
| GB9703554D0 (en) | 1997-02-20 | 1997-04-09 | Dow Corning | Polymerisation of cyclosiloxanes |
| GB9827069D0 (en) | 1998-12-09 | 1999-02-03 | Dow Corning | Polymerisation catalyst |
-
2010
- 2010-11-02 JP JP2012535874A patent/JP2013510079A/ja not_active Ceased
- 2010-11-02 CN CN201080049875.0A patent/CN102596970B/zh not_active Expired - Fee Related
- 2010-11-02 WO PCT/EP2010/066661 patent/WO2011054830A1/en active Application Filing
- 2010-11-02 KR KR1020127014183A patent/KR20120080247A/ko not_active Application Discontinuation
- 2010-11-02 US US13/505,716 patent/US8586690B2/en not_active Expired - Fee Related
- 2010-11-02 EP EP10771492A patent/EP2496585A1/en not_active Withdrawn
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0465429A (ja) * | 1990-07-06 | 1992-03-02 | Shin Etsu Chem Co Ltd | ポリシルエチレンシロキサン |
| JPH05222066A (ja) * | 1992-02-17 | 1993-08-31 | Shin Etsu Chem Co Ltd | 新規有機ケイ素化合物 |
| JPH05279373A (ja) * | 1992-04-01 | 1993-10-26 | Shin Etsu Chem Co Ltd | 5員環状シルエチレンシロキサンの製造方法 |
| US6080829A (en) * | 1998-06-24 | 2000-06-27 | Medtronic, Inc. | Silalkylenesiloxane copolymer materials and methods for their preparation |
| WO2001030887A1 (fr) * | 1999-10-28 | 2001-05-03 | Japan Science And Technology Corporation | Procede de polymerisation de silalkylenesiloxanes |
Non-Patent Citations (1)
| Title |
|---|
| JPN6014036294; Polymer Preprints 42(1), 2001, 225-226 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102596970A (zh) | 2012-07-18 |
| US20120226010A1 (en) | 2012-09-06 |
| CN102596970B (zh) | 2016-02-10 |
| EP2496585A1 (en) | 2012-09-12 |
| KR20120080247A (ko) | 2012-07-16 |
| US8586690B2 (en) | 2013-11-19 |
| WO2011054830A1 (en) | 2011-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2013510079A (ja) | ポリシルアルキレンシロキサンの製造プロセス | |
| EP2679617B1 (en) | Organopolysiloxane and method of preparation | |
| EP3385268A1 (en) | Linear organopolysiloxane having different functional groups at both terminals, and method for producing same | |
| JPH0297529A (ja) | パーフルオロアルキル基含有オルガノポリシロキサンの製造方法 | |
| EP0465262B1 (en) | Polysilethylenesiloxane | |
| JP5278242B2 (ja) | 分子鎖両末端トリオルガノシロキシ基封鎖オルガノポリシロキサンの製造方法 | |
| EP0252652B1 (en) | Method for preparing vinyl terminated fluorine-containing polydiorganosiloxane | |
| JP4114723B2 (ja) | オルガノシロキサンもしくはポリオルガノシロキサンの製造のための触媒 | |
| US20080167487A1 (en) | Process for Preparing Diorganopolysiloxanes | |
| US5041586A (en) | Method of preparing a silyphosphate mixture, silyphosphate mixture and its use in stabilizing metal silanolates in siloxane polymers | |
| EP0661331B1 (en) | Silicon-containing polymer, process for preparing the same and monomer thereof | |
| JPH0662768B2 (ja) | 窒化塩化リンを含有する組成物,その製法ならびにオルガノ(ポリ)シロキサンの縮合方法および平衡方法 | |
| JP3705333B2 (ja) | シラノール基を有する有機けい素化合物の製造方法 | |
| KR101877599B1 (ko) | 폴리실록산의 제조 방법 | |
| Chojnowski et al. | Synthesis of linear polysiloxanes with electron-donating organophosphorus pendant groups by kinetically controlled ring-opening polymerization | |
| US3274153A (en) | Method of polymerizing hydroxylated organosilicon compounds | |
| JP5716533B2 (ja) | 分子鎖両末端トリオルガノシロキシ基封鎖オルガノポリシロキサンの製造方法 | |
| JP6685386B2 (ja) | (メタ)アクリレート基を有する有機ケイ素化合物およびその製造方法 | |
| EP0693520B1 (en) | Method for the preparation of organopolysiloxanes | |
| JPH07242678A (ja) | 2,4,6,8−テトラメチルシクロテトラシロキサンの製造方法 | |
| JP6978369B2 (ja) | ポリエーテルの製造方法 | |
| US3689455A (en) | Preparation of siloxy-carboranyl polymers | |
| KR20220123422A (ko) | 액체 실리케이트 수지 | |
| JPH0216768B2 (ja) | ||
| JP3057139B2 (ja) | 直鎖状ポリオルガノシロキサン及び製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20131017 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140821 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140826 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141125 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20141202 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141222 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20150121 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150714 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151014 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160315 |
|
| A045 | Written measure of dismissal of application [lapsed due to lack of payment] |
Free format text: JAPANESE INTERMEDIATE CODE: A045 Effective date: 20160726 |