JP2012502654A - チャイニーズハムスター卵巣細胞系 - Google Patents
チャイニーズハムスター卵巣細胞系 Download PDFInfo
- Publication number
- JP2012502654A JP2012502654A JP2011527782A JP2011527782A JP2012502654A JP 2012502654 A JP2012502654 A JP 2012502654A JP 2011527782 A JP2011527782 A JP 2011527782A JP 2011527782 A JP2011527782 A JP 2011527782A JP 2012502654 A JP2012502654 A JP 2012502654A
- Authority
- JP
- Japan
- Prior art keywords
- cho
- gnt1
- cells
- cell line
- protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1048—Glycosyltransferases (2.4)
- C12N9/1051—Hexosyltransferases (2.4.1)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/505—Erythropoietin [EPO]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/555—Interferons [IFN]
- C07K14/57—IFN-gamma
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/005—Glycopeptides, glycoproteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y204/00—Glycosyltransferases (2.4)
- C12Y204/01—Hexosyltransferases (2.4.1)
- C12Y204/0115—N-Acetyllactosaminide beta-1,6-N-acetylglucosaminyl-transferase (2.4.1.150)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
- C12N2510/02—Cells for production
Abstract
本発明者らは、野生型チャイニーズハムスター卵巣細胞と比較して、例えば機能的GnT1の存在下においてタンパク質を高度にシアル化できるチャイニーズハムスター卵巣(CHO)細胞であって、前記CHO細胞はRicinus communisアグルチニンI(RCA−I)を用いた選択によって入手できるCHO細胞を提供する。
Description
[関連出願の相互参照]
2008年9月19日に出願された米国特許出願第61/098,270号明細書および2009年6月3日に出願された米国特許出願第61/183,647号明細書が参照される。上記特許の発明者Songは本願の発明者である。
2008年9月19日に出願された米国特許出願第61/098,270号明細書および2009年6月3日に出願された米国特許出願第61/183,647号明細書が参照される。上記特許の発明者Songは本願の発明者である。
上記の特許出願、そして本出願および上記の特許出願の各々において上記の特許出願の各々の審査手続き中を含めて引用または参照された各文書(「特許出願および論文が引用した文書」)、ならびに上記の特許出願および論文の各々および特許出願および論文が引用した文書のいずれかにおいて引用または言及された任意の製品についての任意の製造業者の取扱説明書またはカタログは、参照することによって本明細書に組み入れられる。さらに、本明細書において引用した全文書、そして本明細書において引用した文書において引用または参照された全文書、ならびに本明細書、または本明細書に組み入れられた任意の文書において引用または言及された任意の製品についての任意の製造業者の取扱説明書またはカタログは、本明細書に参照することによって組み入れられる。本明細書に参照することによって組み入れられた文書またはその中の任意の教示は、本発明の実施において使用することができる。本明細書に参照することによって組み入れられた文書は、先行技術であると認められるものではない。
[発明の分野]
本発明は、バイオテクノロジーおよび分子生物学の分野に関する。本発明は、特に、チャイニーズハムスター卵巣細胞系および組換えタンパク質発現におけるそれらの使用に関する。
本発明は、バイオテクノロジーおよび分子生物学の分野に関する。本発明は、特に、チャイニーズハムスター卵巣細胞系および組換えタンパク質発現におけるそれらの使用に関する。
タンパク質は、様々な診断学、薬理学、農業、栄養、および研究用途において有用である。タンパク質、特には治療用タンパク質の製造には高額の費用を要することを考えると、生産効率またはタンパク質の機能および安定性における小さな増進さえ有益な可能性がある。
タンパク質の機能および安定性、したがってその有用性は、糖タンパク質を形成するためのタンパク質への糖残基の翻訳後付加によって影響を及ぼすことができることである。例えば、糖タンパク質に付着した多糖類への末端シアル酸残基の付加は、一般に血流中のタンパク質の寿命を増加させ、そして特定の場合には、さらに一部の糖タンパク質の溶解性、熱安定性、プロテアーゼ攻撃への耐性、抗原性、および比活性度に影響を及ぼすことができる。例えば、Gu and Wang(1998),Biotechnol.and Bioeng.58(6):642−48;Morell et al.(1968),J.Biol.Chem.243(1):155−59を参照されたい。
例えばチャイニーズハムスター卵巣(CHO)細胞などの細胞系によって生成された組換え糖タンパク質および薬物は、一般には特異的にシアル化されたアイソフォームからなる。低シアル化のアイソフォームは、循環中半減期が短くなるので、このため有効性が低い。
このため、糖タンパク質、特に薬理学的用途に使用される糖タンパク質のシアル酸含量を増加させることは望ましい。実際に、バイオテクノロジー分野における主要な研究の焦点の1つは、組換えタンパク質薬のシアル化を増加させる方法であった。
本発明の第1の態様によると、本発明者らは、野生型チャイニーズハムスター卵巣(CHO)細胞と比較してタンパク質を高シアル化できるチャイニーズハムスター卵巣(CHO)細胞を提供するが、該CHO細胞は、Ricinus communis(ヒマ)のアグルチニンI(RCA−I)を用いた選択によって入手することができる。該CHO細胞は、機能的GnT1の存在下ではより高いシアル化を行ってもよい。
CHO細胞は、GnT1遺伝子内に突然変異を含んでもよい。
GnT1遺伝子における突然変異は、GnT1配列(GenBankアクセッション番号:AF343963)の特定位置で以下の突然変異、(a)1015位でのCからTへのトランジッション、(b)1300位でのGからCへのトランスバージョン、(c)638位でのAからCへのトランスバージョン、(d)784位でのCからGへのトランスバージョン、(e)811位でのTからAへのトランスバージョン、(f)コードされたアミノ酸配列の236位からのフレームシフトを生じさせる706位での挿入、(g)1015位でのCからTへのトランジッション、(h)246位でのGからAへのトランジッション、(i)258位でのGからAへのトランジッション、(j)859位でのAからTへのトランスバージョンの内の1つ以上を含んでもよい。
GnT1遺伝子は、配列番号1に示したGnT1核酸配列を含んでもよい。
CHO細胞は、GnT1配列(GenBankアクセッション番号:AF343963)の特定位置で以下の突然変異:(a)434位でAlaからPro、(b)213位でAsp→Ala、(c)262位でArg →Gly、(d)271位でTrp→Arg、(e)GnT1をコードする核酸配列の706位での挿入の結果として生じる236位からのフレームシフト、(f)339位でのGln→STOP、(g)82位でのTrp→STOP、(h)86位でのTrp→STOP、(i)287位でのLys→STOPの内の1つ以上を含むGnT1タンパク質を発現してもよい。
CHO細胞は、配列番号2に示したGnT1タンパク質を発現してもよい。
CHO細胞は、例えば当該組換えタンパク質などの当該タンパク質をコードする核酸配列を含んでもよい。目的のタンパク質は、エリスロポエチン(EPO)またはインターフェロン−γ(IFN−γ)を含んでもよい。
CHO細胞は、機能的GnT1をコードする核酸配列を含むことができる。目的のタンパク質をコードする核酸配列および機能的GnT1をコードする核酸配列は、1つの発現ベクター内に含まれてもよい。
目的のタンパク質をコードする核酸配列および機能的GnT1をコードする核酸配列は、CHO細胞内に安定的にトランスフェクトしてもよい。
本発明の第2の態様によると、本発明の第1態様によるCHO細胞を含むCHO細胞系が提供される。
CHO細胞系は、JW152細胞系(ATCCにブダペスト条約の下でアクセッション番号PTA−9657として寄託された)、JW80細胞系、JW36細胞系、KFC15002細胞系、KFC15071細胞系、KFC5008細胞系、JW152細胞系、KFC5026細胞系、KFC20011細胞系またはKFC15047細胞系を含んでもよい。
CHO細胞またはCHO細胞系は、懸濁培養に順応させることができる。
本発明者らは、本発明の第3態様によると、本発明の第1または第2態様によるCHO細胞またはCHO細胞系によって発現された組換えタンパク質を提供する。
組換えタンパク質は、エリスロポエチン(EPO)またはインターフェロン−γ(IFN−γ)を含むことができる。
組換えタンパク質は、4以下、3.5以下、3以下、2.5以下もしくは2以下のpKaを含むか、または150より大きい、例えば160より大きい、170より大きい、180より大きい、例えば190より大きい、200より大きい、210より大きい、例えば220より大きい、もしくは230より大きいZ数を含むか、またはその両方を含んでもよい。
本発明の第4の態様として、組換えタンパク質を発現させる方法であって、該タンパク質をコードする核酸を上記に記載したようにCHO細胞内に導入するステップと、該タンパク質を該CHO細胞又はその子孫から発現させるステップと、任意選択により該タンパク質を精製するステップとを含む方法が提供される。
本方法は、機能的GnT1をコードする核酸をCHO細胞内に導入することを含んでもよい。
本方法は、該タンパク質をコードする核酸配列および機能的GnT1をコードする核酸配列を含む発現ベクターを導入することを含んでもよい。
本方法は、目的のタンパク質をコードする核酸配列および機能的GnT1をコードする核酸配列を安定的にトランスフェクトすることを含んでもよい。
本発明者らは、本発明の第5の態様によると、配列番号1に示した配列、または表D1の第2列に記載した突然変異を有するGnT1配列を含む配列を含む核酸、またはその変異体、ホモログ、誘導体もしくはフラグメントを提供する。
本発明は、第6の態様では、配列番号2に示した配列、または表D1の第3列に記載した突然変異を有するGnT1配列を含む配列を含むポリペプチド、またはその変異体、ホモログ、誘導体もしくはフラグメントを提供する。
本発明の第7の態様では、CHO細胞または細胞系を提供する方法であって、該方法は、CHO細胞をRicinus communisのアグルチニンI(RCA−I)の存在下で培養するステップと、該培養を生存する細胞を選択するステップとを含む方法が提供される。
本方法は、CHO細胞をRicinus communisのアグルチニンI(RCA−I)の存在下で培養するステップと、該培養を生存する細胞を選択するステップとを含むことができる。
本方法は、CHO細胞を、0.1μg/mL〜100μg/mL、例えば50μg/mLまで、または20μg/mLまで、例えば10μg/mLもしくは5μg/mLまでの濃度のRCA−Iへ曝露させることを含むことができる。
本方法は、CHO細胞をRCA−Iへ、1時間、数時間(例えば、2、3、4、5、6、7、8、9、10、11、12時間)、一晩から数日間、例えば2日間または3日間、例えば一晩までの期間にわたって曝露させることを含むことができる。
本方法は、凝集試験においてRCA−Iと反応しない細胞を選択することをさらに含むことができる。
本発明の第8の態様によると、本発明者らは、上記に記載した方法によって入手できるCHO細胞またはCHO細胞系を提供する。
本発明の実施は、他に特に指示しない限り、化学、分子生物学、微生物学、組換えDNAおよび免疫学の従来技術を使用するが、これらは当業者の能力の範囲内に含まれる。そのような技術は、文献において説明されている。例えば、J.Sambrook,E.F.Fritsch,and T.Maniatis,1989,Molecular Cloning:A Laboratory Manual,Second Edition,Books 1−3,Cold Spring Harbor Laboratory Press;Ausubel,F.M.et al.(1995 and periodic supplements;Current Protocols in Molecular Biology,ch.9,13,and 16,John Wiley & Sons,New York,N.Y.);B.Roe,J.Crabtree,and A.Kahn,1996,DNA Isolation and Sequencing:Essential Techniques,John Wiley & Sons;J.M.Polak and James O’D.McGee,1990,In Situ Hybridization:Principles and Practice;Oxford University Press;M.J.Gait(Editor),1984,Oligonucleotide Synthesis:A Practical Approach,Irl Press;D.M.J.Lilley and J.E.Dahlberg,1992,Methods of Enzymology:DNA Structure Part A:Synthesis and Physical Analysis of DNA Methods in Enzymology,Academic Press;Using Antibodies:A Laboratory Manual:Portable Protocol NO.I by Edward Harlow,David Lane,Ed Harlow(1999,Cold Spring Harbor Laboratory Press,ISBN 0−87969−544−7);Antibodies:A Laboratory Manual by Ed Harlow(Editor),David Lane(Editor)(1988,Cold Spring Harbor Laboratory Press,ISBN 0−87969−314−2),1855.Handbook of Drug Screening,edited by Ramakrishna Seethala,Prabhavathi B.Fernandes(2001,New York,NY,Marcel Dekker,ISBN 0−8247−0562−9);and Lab Ref:A Handbook of Recipes,Reagents,and Other Reference Tools for Use at the Bench,Edited Jane Roskams and Linda Rodgers,2002,Cold Spring Harbor Laboratory,ISBN 0−87969−630−3を参照されたい。これらの全本文は、各々を参照することによって本明細書に組み入れられる。
<配列表>
配列番号1は、CHO JW152細胞由来のN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)I cDNAの核酸配列である。
配列番号1は、CHO JW152細胞由来のN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)I cDNAの核酸配列である。
配列番号2は、配列番号1によってコードされたN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)Iのアミノ酸配列である。
細胞毒性レクチンであるRCA−Iを用いて、本発明者らは、CHO−K1細胞から新規なCHO変異細胞系であるJW152を単離した。
EPOおよびGnTIのcDNAを用いて安定的にトランスフェクトされたJW152細胞によって生成された組換えEPOは、高度にシアル化されたアイソフォームを含有する。これらの安定的にトランスフェクトされた細胞系の幾つかは、懸濁培養中で順応し、無血清培地中で増殖する。これらの細胞によって生成されたEPOは、IEFアッセイによって分析される。これらの結果は、無血清培地中で生成されたEPOが高シアル化された状態であることを証明した。
これらの結果は、JW152細胞がタンパク質、例えば糖タンパク質薬を含む高シアル化されたタンパク質などを生成するための宿主細胞系になる潜在能力を有することを示唆している。
細胞系JW152は、2008年12月11日にアメリカンタイプカルチャーコレクション(American Type Culture Collection:ATCC、10801 University Boulevard、米合衆国バージニア州マナッサス、VA 20110−2209)に特許手続上の微生物の寄託の国際承認に関するブダペスト条約(the Budapest Treaty on the International Recognition of the Deposit of Microorganisms for the Purposes of Patent Procedure)下の国際寄託番号としてのアクセッション番号PTA−9657を付けて寄託された。
本発明者らは、このため野生型チャイニーズハムスター卵巣(CHO)細胞と比較してタンパク質を高シアル化できるチャイニーズハムスター卵巣(CHO)細胞または細胞系を提供する。
より高いシアル化が可能なCHO細胞は、適切な選択法、例えばRCA−1選択法によって生成することができる。そのような方法は、以下の「CHO細胞およびCHO細胞系」においてさらに詳細に説明される。このため、RCA−Iを使用すると、GnTIの存在下で高シアル化された組換えタンパク質を生成するCHOグリコシル化変異細胞を単離することができる。
そのような選択法は、それゆえ本明細書に記載した方法および組成物に特に含まれる。
本発明者らはこのため、野生型チャイニーズハムスター卵巣細胞と比較してタンパク質を高シアル化できるチャイニーズハムスター卵巣(CHO)細胞または細胞系を提供するが、該CHO細胞はRicinus communisアグルチニンI(RCA−I)を用いた選択によって入手できる。一般に、本発明者らは、RCA−I耐性CHO細胞または細胞系、例えばRCA−I耐性CHO−K1細胞または細胞系を提供する。
遺伝分析により、JW152細胞内の機能異常のN−アセチル−グルコサミニルトランスフェラーゼI(GnTI)遺伝子を明らかにした。変異細胞由来のGnTIのcDNAの分子クローニングにより、早期の終止コドンを生じさせる点突然変異が同定された。結果として、JW152細胞は、447アミノ酸を含有する正常タンパク質ではなく338アミノ酸しか備えていないGnTIタンパク質の短縮(trancated)バージョンしか合成できない。
RCA−Iを使用して、本発明者らは、さらに多くのCHO変異系(約100クローン)を単離している。遺伝分析により、それら全部に機能的GnTI遺伝子が欠如することを証明した。それらの内の多くはGnTI遺伝子のコーディング領域において相違する点突然変異を有し、それらが様々のオリジナルクローンに由来することを示唆している。それでも、それらは全部がGnTIの存在下では組換えタンパク質のシアル化を劇的に改善した。これらのまた別のCHO細胞系由来のGnT1遺伝子における突然変異は、以下の表D1に示した。
したがって、本発明者らは、機能的GnT1の存在下では野生型チャイニーズハムスター卵巣細胞と比較してタンパク質を高シアル化できるチャイニーズハムスター卵巣(CHO)細胞であって、該GnT1遺伝子における突然変異を含むCHO細胞を提供する。本発明者らはさらに、野生型チャイニーズハムスター卵巣細胞と比較してタンパク質を高シアル化できるチャイニーズハムスター卵巣(CHO)細胞または細胞系であって、Ricinus communisアグルチニンI(RCA−I)を用いた選択によって入手でき、GnT1遺伝子における突然変異を含むCHO細胞を提供する。
GnT1遺伝子内の突然変異は、任意の点突然変異、欠失、反転などを含んでもよい。GnT1遺伝子における突然変異は、部分機能的、または非機能的GnT1ポリペプチドをコードしてもよい。GnT1遺伝子における突然変異は、短縮GnT1ポリペプチドをコードしてもよい。
本発明者らは、これらの変異CHO変異系およびクローンの各々を含むCHO細胞および細胞系を提供する。本発明者らは、RCA−I選択法に由来する、および野生型もしくは天然CHO細胞または親細胞と比較して高シアル化できる具体的な細胞系を提供する。本発明者らは、以下でより詳細に説明するように、変異CHO核酸およびそのような細胞または細胞系に含まれるポリペプチド配列を提供する。
CHO細胞または細胞系は、JW152細胞系を含んでもよい。CHO細胞または細胞系は、JW80細胞系を含んでもよい。CHO細胞または細胞系は、JW36細胞系を含んでもよい。CHO細胞または細胞系は、KFC15002細胞系を含んでもよい。CHO細胞または細胞系は、KFC15071細胞系を含んでもよい。CHO細胞または細胞系は、KFC5008細胞系を含んでもよい。CHO細胞または細胞系は、JW152細胞系を含んでもよい。CHO細胞または細胞系は、KFC5026細胞系を含んでもよい。CHO細胞または細胞系は、KFC20011細胞系を含んでもよい。CHO細胞または細胞系は、KFC15047細胞系を含んでもよい。
CHO細胞または細胞系は、目的のタンパク質、例えば異種もしくは組換えタンパク質をコードする核酸によりトランスフェクトされてもよい。そのようなタンパク質は、糖タンパク質を含んでもよい。CHO細胞または細胞系は、機能的GnT1配列、完全長GnT1配列または野生型GnT1配列をコードする核酸によりトランスフェクトまたは共トランスフェクトされてもよい。
上記で言及したように、本発明者らは、核酸自体、例えば変異GnT1遺伝子をコードする核酸、またはそのような核酸のフラグメント、変異体、誘導体もしくはホモログを提供する。変異GnT1遺伝子をコードする核酸、フラグメント、変異体、誘導体またはホモログは、それを含むCHO細胞がそのような核酸を含まないCHO細胞、例えば野生型CHO細胞と比較して、より高いシアル化を行うことができるようにするものでもよい。変異GnT1遺伝子をコードする核酸は、配列番号1に示した配列、またはその変異体、ホモログ、誘導体もしくはフラグメントを含んでもよい。
配列番号1
CHO JW152細胞から単離されたN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)I(Mgat1、GenBank:AF343963)mRNAのコーディング領域。これらの変異細胞では、1015位でのCからTへの点突然変異が同定された(ボールド体で示した):
CHO JW152細胞から単離されたN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)I(Mgat1、GenBank:AF343963)mRNAのコーディング領域。これらの変異細胞では、1015位でのCからTへの点突然変異が同定された(ボールド体で示した):
本発明者らは、変異GnT1ポリペプチド、ならびにそれらのフラグメント、変異体、誘導体およびホモログをさらに提供する。変異GnT1ポリペプチド、フラグメント、変異体、誘導体またはホモログは、そのようなポリペプチドを含んでいないCHO細胞、例えば野生型CHO細胞と比較して、それを含むCHO細胞がより高いシアル化を行うことができるようにするものでもよい。変異GnT1ポリペプチドは、配列番号2に示した配列、またはその変異体、ホモログ、誘導体もしくはフラグメントを含んでもよい。
配列番号2
CHO JW152細胞内の変異遺伝子によってコードされたN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)I(GnTI)タンパク質。点突然変異(C1015T)の結果として、JW152細胞は、447アミノ酸を含有する正常タンパク質ではなく338アミノ酸しか含有していないGnTIの短縮バージョンしか生成しない。ボールド体のC末端部分は、JW152細胞内では翻訳されない。
CHO JW152細胞内の変異遺伝子によってコードされたN−アセチルグルコアミニルトランスフェラーゼ(acetylglucoaminyltransferase)I(GnTI)タンパク質。点突然変異(C1015T)の結果として、JW152細胞は、447アミノ酸を含有する正常タンパク質ではなく338アミノ酸しか含有していないGnTIの短縮バージョンしか生成しない。ボールド体のC末端部分は、JW152細胞内では翻訳されない。
図2に示したJW152−pEIG安定系の幾つかは、懸濁培養中で順応し、無血清培地中で増殖する。無血清培地中で生成されたEPOは、高シアル化された状態であった。本発明者らはこのため、懸濁培養中で順応した、または無血清培地中で増殖する、RCA−I選択に由来する変異CHO細胞および細胞系を提供する。
結論として、本発明者らは、グリコシル化変異細胞をCHO細胞から単離するための新規な方法を開発した。RCA−I処理を生存する全CHO細胞は、極めて類似する特性を有する。第1に、その全ての細胞は、機能的GnTI遺伝子を欠如する。第2に、その全ての細胞が、GnTIの存在下で野生型CHO細胞よりも良好に、その組換えタンパク質をシアル化する。この特徴は、一過性のトランスフェクトされた細胞、および安定的にトランスフェクトされた細胞の両方において同一のままである。
RCA−I、例えばJW152細胞を用いて単離されたCHOグリコシル化変異細胞は、GnTIが存在する限り、高くシアル化された組換え糖タンパク質を生成できる。本方法は、シアル酸含量がその有効性のために重要である組換え糖タンパク質を生成するために使用できる。これらのタンパク質には、EPO、IEF−γ、第VIII因子などが含まれる。
<CHO細胞および細胞系>
本明細書に記載したCHO細胞および細胞系は、任意の適切な手段によって作成されてもよい。例えば、CHO細胞および細胞系は、適切な凝集剤、例えばアグルチニンIを用いる選択によって生成されてもよい。アグルチニンは、任意の適切なアグルチニン、例えばRicinus communisアグルチニンI(RCA−I)を含んでもよい。
本明細書に記載したCHO細胞および細胞系は、任意の適切な手段によって作成されてもよい。例えば、CHO細胞および細胞系は、適切な凝集剤、例えばアグルチニンIを用いる選択によって生成されてもよい。アグルチニンは、任意の適切なアグルチニン、例えばRicinus communisアグルチニンI(RCA−I)を含んでもよい。
本発明者らはこのため、CHO細胞または細胞系を提供する方法であって、Ricinus communisアグルチニンI(RCA−I)の存在下でCHO細胞を培養するステップと、該培養を生存する細胞を選択するステップとを含む方法を提供する。
本明細書に記載したCHO細胞および細胞系は、出発もしくは親細胞をRicinus communisアグルチニンI(RCA−I)で処理するステップと、そのような処理を生存する細胞を選択することとによって作成されてもよい。そのような生存細胞をさらにクローニングし、細胞系を作成してもよい。選択された細胞および細胞系は、本文書に記載したように高いシアル化活性を含んでもよい。選択された細胞および細胞系は、本文書に記載したように、変異GnT1遺伝子およびポリペプチドを含んでもよい。
例えば、本文書に記載したCHO細胞もしくは細胞系は、親細胞系をRicinus communisアグルチニンI(RCA−I)へ適切な期間にわたって適切な濃度で曝露させることによって選択されてもよい。
RCA−1濃度は、0.1μg/mL〜100μg/mL、例えば50μg/mLまでまたは20μg/mLまでの範囲に及んでよい。特定濃度の例には、10μg/mLおよび5μg/mLが含まれる。
培養またはRCA−1への曝露の期間は、1時間、数時間(例えば、2、3、4、5、6、7、8、9、10、11、12時間)、一晩から数日間、例えば2日間もしくは3日間までであってよい。
一般には、この期間および濃度は、多数のCHO細胞を除去するが、RCA−Iに耐性である小さな比率の細胞が生存してコロニーを形成することができるように調整することができる。この範囲内で、濃度ならびに曝露および選択の期間は変動してよいが、一般には、RCA−Iの濃度が高いほど必要な曝露期間は短かくなり、その逆もまた同様である。
選択は、任意の適切な出発細胞または細胞系を対象に実施できるが、これは一般にはCHO細胞または細胞系であろう。任意の公知のCHO細胞または細胞系は、出発点またはCHO−K1を含む親細胞として使用できよう。その他の適切な出発細胞は、CHO(85050302)、CHO(PROTEIN FREE)(00102307)、CHO−K1(85051005)、CHO−K1/SF(93061607)、CHO/dhFr−(94060607)、CHO/dhFr−AC−free(05011002)、RR−CHOKI(92052129)(括弧内はECACCアクセッション番号)を含むことができるが、それらに限定されない。
選択後、生存した細胞を増殖させ、コロニーを形成させるが、その後に採取してもよい。このために許容される時間は変動するが、一般にはコロニーを採取可能なサイズへ増殖させるために十分な長さである。そのような時間の例は、5日間、7日間、9日間、11日間、13日間、1週間、2週間、3週間またはそれ以上である。
採取することは手作業で行えるが、採取はロボット、例えばCLONEPIX(Genetix社、英国ハンプシャー州ニューミルトン)の使用によって自動化することができる。採取されたコロニーを、さらにクローニングし、さらにスクリーニングし、特性解析し、そして培養するなどできる。
選択された細胞を、その後の試験にかけることができる。例えば、選択された細胞は、変異細胞がもはやRCA−Iと反応しないことを確認するためにRCA−Iを用いて凝集試験にかけることができる。
限定されることは意図されない特定の例として、CHO−K1細胞は、例えば6ウエルプレート内で集密まで培養されてよい。培養培地を、無血清DMEMに変更してもよい。Ricinus communisアグルチニンI(RCA−I、EY Laboratories社)を、培地中に添加して10μg/gmLの最終濃度に達してもよい。RCA−Iは、細胞とともに一晩インキュベートされてもよい。RCA−Iを含有する無血清DMEMは、例えば10% FBSを備える新鮮DMEMと取り替えられてよい。9日後、RCA−I処理を生存するCHO細胞のコロニーを、採取して、例えば24ウエルプレート内で培養することができる。
これらの細胞は、変異細胞がもはやRCA−Iと反応しないことを確認するために、また別の試験、例えば凝集試験にかけられてもよい。本発明者らはこのため、CHO細胞もしくは細胞系を提供する方法であって、Ricinus communisアグルチニンI(RCA−I)の存在下でCHO細胞を培養するステップと、該培養から生存し、凝集試験においてRCA−Iと反応しない細胞を選択するステップとを含む方法を提供する。
RCA−Iで選択したCHO細胞およびCHO細胞系は、それらのシアル化挙動について、例えば目的のタンパク質を発現させることと、シアル化度を決定することとによって試験することができる。これは、以下の「シアル化」に記載した方法によって行うことができる。
本発明者らはこのため、CHO細胞もしくは細胞系を提供する方法であって、Ricinus communisアグルチニンI(RCA−I)の存在下でCHO細胞を培養するステップと、該培養を生存する細胞を選択することと、高度のシアル化挙動、例えば発現されたタンパク質の高Z数または低pIを示すそれらの細胞または細胞系を選択するステップとを含む方法を提供する。
そのような選択された細胞内のGnT1遺伝子は、当分野において公知の方法を用いてクローニングおよび配列決定することができる。GnT1遺伝子は、本明細書に記載したように変異GnT1遺伝子を含んでもよい。
本発明者らはこのため、CHO細胞または細胞系を提供する方法であって、Ricinus communisアグルチニンI(RCA−I)の存在下でCHO細胞を培養するステップと、該培養を生存する細胞を選択するステップと、本明細書に記載した変異GnT1遺伝子を含むそれらの細胞または細胞系を選択するステップとを含む方法を提供する。
<変異CHO細胞および細胞系>
本発明者らは、上述したように、RCA−I選択に由来するCHO細胞または細胞系を提供する。そのような細胞系は、JW152細胞系、またはJW80細胞系、JW36細胞系、KFC15002細胞系、KFC15071細胞系、KFC5008細胞系、JW152細胞系、KFC5026細胞系、KFC20011細胞系、またはKFC15047細胞系を含む以下の表D1に記載した細胞系のいずれかを含むことができよう。
本発明者らは、上述したように、RCA−I選択に由来するCHO細胞または細胞系を提供する。そのような細胞系は、JW152細胞系、またはJW80細胞系、JW36細胞系、KFC15002細胞系、KFC15071細胞系、KFC5008細胞系、JW152細胞系、KFC5026細胞系、KFC20011細胞系、またはKFC15047細胞系を含む以下の表D1に記載した細胞系のいずれかを含むことができよう。
<タンパク質発現>
本明細書に記載したCHO細胞は、目的の任意のタンパク質を発現させるための宿主細胞として使用できる。これは当分野において公知の手段によって行うことができる。
本明細書に記載したCHO細胞は、目的の任意のタンパク質を発現させるための宿主細胞として使用できる。これは当分野において公知の手段によって行うことができる。
CHO細胞および細胞系におけるタンパク質発現は前記文献において明確に記載され、当業者であれば、本明細書に記載したCHO細胞および細胞系をタンパク質発現のための宿主として使用する際に、ほとんど困難を有しない。そこで例えば、CHO細胞および細胞系は、当分野において公知の手段によって目的のタンパク質を発現できる発現ベクターによりトランスフェクトすることができる。
CHO細胞および細胞系は、さらに野生型または機能的GnT1、例えばGenBankアクセッション番号AF343963に提示された配列を発現することができる。これは、GnT1をコードする発現ベクターによりCHO細胞および細胞系をトランスフェクトすることによって実施できる。これは、目的のタンパク質をコードする核酸を含有するベクターと同一または相違するベクター上であってよい。
任意の適切なタンパク質は、本明細書に記載したCHO細胞を宿主細胞として使用して発現させることができる。タンパク質は、異種タンパク質を含むことができる。タンパク質は、組換えタンパク質を含むことができる。タンパク質は、操作されたタンパク質を含むことができる。タンパク質は、糖タンパク質を含むことができる。
例には、治療または薬理学的目的の異種タンパク質が含まれる。発現させることのできるタンパク質には、抗EGFR mAb、α−グルコシダーゼ、ラロニダーゼ、Ig−CTLA4融合、N−アセチルガラクトサミン−4−スルファターゼ、黄体化ホルモン、抗VEGF mAb 、第VIII因子、抗lgE mAb、抗CD11a mAb、α−ガラクトシダーゼ、インターフェロン−β、抗TNFα mAb、エリスロポエチン、抗CD52 mAb、第VIII因子、組織プラスミノーゲン活性化因子、抗−HER2 mAb、TNFα受容体融合、第IX因子、卵胞刺激ホルモン、抗CD20 mAb、インターフェロン−β,β−グルコセレブロシダーゼ、デオキシリボヌクレアーゼIなどが含まれる。
例えば、本発明者らは、本明細書に記載したCHO細胞および細胞系を用いたエリスロポエチン(EPO)、インターフェロン−γおよび第VIII因子の発現について記載する。本発明者らはさらに、本明細書に記載したCHO細胞および細胞系から発現されたエリスロポエチン(EPO)、インターフェロン−γおよび第VIII因子の高シアル化形またはアイソフォームについても記載する。
<シアル酸>
用語「シアル酸」は、1ファミリーの炭素数が9個のカルボキシル化された糖の任意のメンバーを意味すると意図されている。
用語「シアル酸」は、1ファミリーの炭素数が9個のカルボキシル化された糖の任意のメンバーを意味すると意図されている。
シアル酸ファミリーの最も一般的なメンバーは、N−アセチルノイラミン酸(2−ケト−5−アセトアミド−3,5−ジデオキシ−D−グリセロ−D−ガラクトノヌロピラノース(galactononulopyranos)−1−オニン酸(onic acid)(Neu5Ac、NeuAc、またはNANAと略記されることが多い)である。該ファミリーの第2メンバーは、N−グリコリル−ノイラミン酸(Neu5GcまたはNeuGc)であり、このときNeuAcのN−アセチル基はヒドロキシル化されている。第3のシアル酸ファミリーメンバーは、2−ケト−3−デオキシ−ノヌロソン酸(KDN)である。17
9−置換シアル酸、例えば9−O−C1−C6−アシル−Neu5Ac、例えば9−O−ラクチル−Neu5Acもしくは9−O−アセチル−Neu5Ac、9−デオキシ−9−フルオロ−Neu5Acおよび9−アジド−9−デオキシ−Neu5Acも、また、含まれる。シアル酸ファミリーの概説については、例えば、Varki;Glycobiology 2 1992;25−40;Sialic Acids:Chemistry,Metabolism and Function,R.Schauer,Ed.を参照されたい。
<シアル化>
タンパク質のシアル化度を、様々な手段、例えばZ数を使用すること、またはタンパク質の等電点を明示することによって測定することができる。
タンパク質のシアル化度を、様々な手段、例えばZ数を使用すること、またはタンパク質の等電点を明示することによって測定することができる。
本発明者らはこのため、本明細書に記載したCHO細胞および細胞系を用いたタンパク質発現を提供するが、そのようなタンパク質発現は、目的のタンパク質の高シアル化形またはアイソフォームを含む。本明細書に記載したCHO細胞および細胞系からのタンパク質発現は、糖タンパク質などのタンパク質、例えばエリスロポエチン(EPO)、インターフェロン−γおよび第VIII因子の生成を可能にするが、これらのタンパク質は高Z数もしくは低pI、またはその両方を有する。
<Z数>
パラメーターのZ数は、糖タンパク質中の炭水化物成分の内のいくつのアンテナが荷電残基、例えばシアル酸を有するかの尺度を提供する。
パラメーターのZ数は、糖タンパク質中の炭水化物成分の内のいくつのアンテナが荷電残基、例えばシアル酸を有するかの尺度を提供する。
Z数を決定するために、炭水化物成分は、上述したようにペプチドから遊離され、所望であれば標識される。この混合物は、次に電荷に基づいて種の分離を許容するイオン交換クロマトグラフィーによって分離される。溶出ピークの可視化は、上記で言及したように標識によるものでもよく、または一部の他の方法、例えば質量分析法によるものでもよい。
クロマトグラムは、次にモノ、ジ、トリおよびテトラ荷電炭水化物種に関連するピークを統合することによって分析される。各種によって表される全炭水化物のパーセンテージは、次に以下の方程式:Z=P’モノ+2P’ジ+3P’トリ+4P’テトラ(式中、Zは、Z数であり、P’モノ、P’ジ、P’トリ、およびP’テトラは、各々モノ、ジ、トリおよびテトラ荷電である全炭水化物のパーセンテージである)にしたがってZ数を計算するために使用できる。
高Z数は、多数のアンテナが荷電残基を有しているため、糖タンパク質は高く荷電され、そしてシアル酸残基の場合には酸性であることを示している。
本明細書に記載したCHO細胞は、高くシアル化されたタンパク質を発現することができる。そこで例えば、CHO細胞は、例えば150より大きい、例えば160より大きい、170より大きい、180より大きい、例えば190より大きい、200より大きい、210より大きい、例えば220より大きい、例えば230より大きいZ数値を備えるタンパク質を発現することができる。
<等電点>
タンパク質の等電点(pI)は、さらにまたタンパク質のシアル化の尺度として使用できる。シアル化度が高いほど、タンパク質はより酸性となり、pIは小さくなる。
タンパク質の等電点(pI)は、さらにまたタンパク質のシアル化の尺度として使用できる。シアル化度が高いほど、タンパク質はより酸性となり、pIは小さくなる。
本明細書に記載したCHO細胞によって発現されたタンパク質は、それらの正常対応物、例えば天然タンパク質、または野生型CHO細胞によって発現された対応タンパク質より有意に小さいpIプロファイルを有する。例えば、本明細書に記載したCHO細胞および細胞系によって発現されたタンパク質は、小さいpI、例えば4.5以下、例えば4.3以下、4.1以下、4.0以下、3.8以下、3.6以下、3.4以下、3.2以下、3.0以下、2.8以下、2.6以下などの小さいpI値を有してもよい。これらのpIは、個別タンパク質分子、またはそれらのバッチもしくは分画のpIでもよい、または発現された多数のタンパク質の平均pIでもよい。
発現されたタンパク質は、当業者には公知である多数の方法を使用してアイソフォームの混合物から単離することができる。例えば、等電点焦点法(isoelectric focussing)、クロマト分画法(chromatofocussing)またはイオン交換クロマトグラフィーを使用すると、pIに基づいてアイソフォームを分離することができる。様々な分画は、シアル酸含量について分析することができ、所望の分画を使用するために選択できる。
<変異GnT1配列>
本発明者らは、変異GnT1アミノ酸配列および変異GnT1核酸配列を含む変異GnT1配列を開示する。
本発明者らは、変異GnT1アミノ酸配列および変異GnT1核酸配列を含む変異GnT1配列を開示する。
例示の変異GnT1アミノ酸配列には、配列番号2に示した配列、ならびに以下の表D1の第3列に示した突然変異を含む配列が含まれる。
例示の変異GnT1核酸配列には、配列番号1に示した配列、ならびに以下の表D1の第2列に示した突然変異を含む配列が含まれる。
表D1は、以下の実施例に記載したように、RCA−Iを用いた選択から単離されたクローンのGnT1配列における突然変異を示している。
対応する突然変異は、各ヌクレオチドおよびアミノ酸突然変異ならびに二次構造/相互作用における可能性のある破壊場所または終止コドン突然変異の場合に結果として生じるアミノ酸の消失を示すことと平行して表示されている。
見いだされた突然変異がPCRの誤差に起因しなかったことを確認するために、最少4つの細菌コロニーが配列決定された。
表D1。RCA−Iスクリーニングからのクローン由来のGnT1突然変異体において見いだされた突然変異の表(以下の実施例10)。GnT1遺伝子において相違する突然変異を備える9個のCHOグリコシル化突然変異体。機能消失をもたらす点突然変異は、4つの細胞系(JW80、JW36、KFC15002、KFC15071)において見いだされた。終止コドンの生成を生じさせる点挿入(point insertion)は、KFC 5008において見いだされた。早期終止コドンをもたらす突然変異は、別の4つの細胞系(JW152、KFC5026、KFC20011、KFC15047)においても見いだされた。
<変異GnT1ポリペプチド>
CHO細胞および細胞系は、変異GnT1ポリペプチドを含んでいる。
CHO細胞および細胞系は、変異GnT1ポリペプチドを含んでいる。
本発明者らはこのため、一般に変異GnT1ポリペプチドをそれらのフラグメント、ホモログ、変異体および誘導体と一緒に提供する。これらのポリペプチド配列は、本明細書に、および特には配列表に開示したポリペプチド配列を含んでもよい。
変異GnT1ポリペプチドは、野生型GnT1配列と比較して1つ以上の変化を含む場合がある。そのような突然変異は、コーディング核酸配列内に導入される終止コドンおよびその結果であるGnT1のmRNAの翻訳の早期終結から生じてもよい。
変異GnT1ポリペプチドは、野生型GnT1ポリペプチドより短くてもよい。変異GnT1ポリペプチドは、野生型GnT1ポリペプチドの短縮バージョンでもよい。変異GnT1ポリペプチドの長さは、野生型配列の90%以下、80%以下、70%以下などであってよい。
例えば、変異GnT1ポリペプチドは、完全長もしくは野生型GnT1ポリペプチドと比較して5、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100またはそれ以上のC末端残基が欠如していてもよい。
変異GnT1ポリペプチドは、例えば配列番号2に提示した配列を含んでもよい。これは、細胞系JW152由来の変異GnT1ポリペプチド配列である。変異GnT1ポリペプチドは、上記の表D1の第3列に提示した突然変異を含むGnT1配列を含んでもよい。
本明細書に開示した変異GnT1ポリペプチド配列は、配列表に提示された特定の配列、またはそのフラグメント、もしくは変異GnT1タンパク質から入手された配列には限定されず、場合によっては、それらが変異GnT1の少なくとも1つの生物学的活性を有することを前提として、任意の起源、例えば関連細胞ホモログ、他の種由来ホモログおよびその変異体もしくは誘導体から入手された相同配列もまた含まれることを理解されたい。
本開示はこのため、配列表に記述されたアミノ酸配列の変異体、ホモログまたは誘導体、および本明細書に開示したヌクレオチド配列によってコードされるアミノ酸配列の変異体、ホモログまたは誘導体を含んでいる。そのような配列は、一般に「変異GnT1配列」と呼ばれる。
変異GnT1ポリペプチドの長さは、対応する野生型配列の90%以下、80%以下、70%以下などであってよい。
例えば、変異GnT1核酸は、5、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100またはそれ以上のC末端残基が欠如する変異GnT1ポリペプチドをコードする可能性がある。
<生物学的活性>
一部の実施形態では、これらの配列は、場合によっては変異GnT1の少なくとも1つの生物学的活性を含んでいる。生物学的活性は、野生型GnT1と比較して、より高くシアル化されたタンパク質を発現する改善された能力を含むことができる。
一部の実施形態では、これらの配列は、場合によっては変異GnT1の少なくとも1つの生物学的活性を含んでいる。生物学的活性は、野生型GnT1と比較して、より高くシアル化されたタンパク質を発現する改善された能力を含むことができる。
<ホモログ>
開示されたポリペプチドには、任意の起源、例えば関連ウイルス/細菌タンパク質、細胞ホモログおよび合成ペプチド、ならびにそれらの変異体または誘導体から入手された相同配列が含まれる。
開示されたポリペプチドには、任意の起源、例えば関連ウイルス/細菌タンパク質、細胞ホモログおよび合成ペプチド、ならびにそれらの変異体または誘導体から入手された相同配列が含まれる。
本文書の状況では、相同配列またはホモログは、場合によっては、例えば本明細書の配列表に示したようにGnT1とともに少なくとも30、例えば50、70、90または100アミノ酸にわたるアミノ酸レベルで少なくとも60、70、80または90%同一である、例えば少なくとも95もしくは98%同一であるアミノ酸配列を含むと理解されている。本文書の状況では、相同配列は、アミノ酸レベルで、GnT1の配列とともに少なくとも15、25、35、50または100、例えば200、300、400または500アミノ酸にわたり少なくとも15、20、25、30、40、50、60、70、80または90%同一である、例えば少なくとも95もしくは98%同一であるアミノ酸配列を含むと理解されている。
相同性は類似性(すなわち、類似の化学的特性/機能を有するアミノ酸残基)に関して考察することもできるが、本文書の状況においては、配列同一性に関して相同性を表現することが可能である。一部の実施形態では、配列同一性は、関連配列の長さの全てに比して、すなわち例えば関連遺伝子の全長または完全長配列に比して決定される。
相同性比較は、目視で、またはより通例では、容易に入手できる配列比較プログラムを用いて実施することができる。これらの市販で入手できるコンピュータープログラムは、2つ以上の配列間の相同性率(%)を計算できる。
相同性率(%)は、隣接配列と比較して計算することができるが、すなわち1つの配列が他の配列とアラインさせられ、1つの配列内の各アミノ酸が他の配列内の対応するアミノ酸と、一度に1残基ずつ直接的に比較される。これは、「ギャップ無し」アラインメントと呼ばれる。典型的には、ギャップ無しアラインメントは、相当に少ない数の残基(例えば、50未満の隣接アミノ酸)にわたってのみ実施される。
これは極めて単純かつ首尾一貫した方法であるが、例えば、他の点で同一対の配列では、1つの挿入もしくは欠失は以下のアミノ酸残基がアラインメントから締め出されることを引き起こすので、そこでグローバルアラインメントが実施される場合は相同性率(%)の大きな減少が生じることを考慮に入れることができない。結果として、大多数の配列比較方法は、全相同性スコアに過度にペナルティを与えることなく可能性のある挿入および欠失を考慮に入れる最適なアラインメントを生じさせるように設計されている。これは、局所相同性を最大化することを試みるために配列アラインメントに「ギャップ」を挿入することによって達成される。
しかし、これらのより複雑な方法はアラインメント内で発生する各ギャップに「ギャップペナルティ」を指定するので、このため同数の同一アミノ酸については、できる限り少ない数のギャップを備える配列アラインメントは、2つの比較された配列間のより高度の関連性を反映して、多数のギャップを備える配列より高いスコアを達成する。典型的には、ギャップの存在に対する相当に高いコストおよび該ギャップ内の各後続残基に対するより小さなペナルティを要求する「アフィンギャップコスト」が使用される。これは、最も一般的に使用されるギャップ・スコアリングシステムである。高ギャップペナルティは、当然ながらより少数のギャップを備える最適化アラインメントを生じさせる。大多数のアラインメントプログラムによって、ギャップペナルティを変更することができる。しかし、配列比較のためにそのようなソフトウェアを使用する場合にはデフォルト値を使用できる。例えばGCG Wisconsin Bestfitパッケージ(以下を参照されたい)を使用した場合は、アミノ酸配列についてのデフォルト・ギャップ・ペナルティは、1つのギャップについては−12および各伸長については−4である。
最高相同性率(%)の計算は、このためギャップペナルティを考慮に入れて、最適アラインメントの生成を最初に必要とする。そのようなアラインメントを実施するための適切なコンピュータープログラムは、GCG Wisconsin Bestfitパッケージ(University of Wisconsin,U.S.A.;Devereux et al.,1984,Nucleic Acids Research 12:387)である。配列比較を実施できる他のソフトウェアの例には、BLASTパッケージ(Ausubel et al.,1999 ibid - Chapter 18を参照されたい)、FASTA(Atschul et al.,1990,J.Mol.Biol.,403−410)およびGENEWORKS比較ツールセットが含まれるがそれらに限定されない。BLASTおよびFASTAはどちらもオフラインおよびオンライン検索のために利用できる(Ausubel et al.,1999 ibid,pages 7−58 to 7−60を参照されたい)。
最終相同性率(%)は同一性によって測定できるが、アラインメントプロセス自体は、典型的には絶対的対比較法(all−or−nothing pair comparison)には基づいていない。その代りに、化学的類似性または進化距離に基づいて各ペアワイズ比較にスコアを指定する目盛り付き類似性スコアマトリックスが一般に使用される。一般に使用されるそのようなマトリックスの例は、BLASTプログラムセットのためのデフォルトマトリックスであるBLOSUM62マトリックスである。GCG Wisconsinプログラムは、一般には公衆デフォルト値または供給された場合はカスタム記号比較表のいずれかを使用する(これ以上の詳細についてはユーザーマニュアルを参照されたい)。GCGパッケージのための公衆デフォルト値、または他のソフトウェアの場合にはデフォルトマトリックス、例えばBLOSUM62を使用できる。
ソフトウェアが最適なアラインメントを生成すると、相同性率(%)、例えば配列同一性率(%)を計算するのが可能である。ソフトウェアは、典型的にはこれを配列比較の一部として実行し、数値結果を生成する。
<変異体および誘導体>
本明細書に記載したアミノ酸配列に関連する用語「変異体」もしくは「誘導体」には、その配列から、またはその配列への1つ(またはそれ以上)のアミノ酸の任意の置換、変化、修飾、置換、欠失または付加が含まれる。例えば、生じたアミノ酸配列は未修飾配列と実質的に同一活性を維持し、例えば配列表に示した変異GnT1ポリペプチドと少なくとも同一の活性を有する。
本明細書に記載したアミノ酸配列に関連する用語「変異体」もしくは「誘導体」には、その配列から、またはその配列への1つ(またはそれ以上)のアミノ酸の任意の置換、変化、修飾、置換、欠失または付加が含まれる。例えば、生じたアミノ酸配列は未修飾配列と実質的に同一活性を維持し、例えば配列表に示した変異GnT1ポリペプチドと少なくとも同一の活性を有する。
実施例に示したアミノ酸配列を有するポリペプチド、またはそれらのフラグメントもしくはホモログは、本明細書に記載した方法および組成物において使用するために修飾されてよい。典型的には、配列の生物学的活性を維持する修飾が行われる。例えば、修飾された配列が未修飾配列の生物学的活性を維持することを前提に、1、2もしくは3〜10、20もしくは30置換のアミノ酸置換が行われてもよい。アミノ酸置換は、例えば治療的に投与されるポリペプチドの血漿中半減期を増加させるために、自然には発生しないアナログの使用を含んでもよい。
変異GnT1の天然変異体は、保存的アミノ酸置換を含む可能性が高い。保存的置換は、例えば以下の表にしたがって規定することができる。第2列の同一ブロック内および第3列の同一線内のアミノ酸は、相互に置換することができる。
<フラグメント>
本明細書に開示され、マーカーとして有用なポリペプチドは、配列表に提示した配列のフラグメントを含む、上記で言及した完全長ポリペプチドおよびそれらの変異体もまた含んでいる。
本明細書に開示され、マーカーとして有用なポリペプチドは、配列表に提示した配列のフラグメントを含む、上記で言及した完全長ポリペプチドおよびそれらの変異体もまた含んでいる。
ポリペプチドは、変異GnT1ポリペプチドの完全長配列のフラグメントもまた含んでいる。そのようなフラグメントは、少なくとも1つのエピトープを含んでもよい。エピトープを同定する方法は、当分野において周知である。フラグメントは、典型的には少なくとも6アミノ酸、例えば少なくとも10、20、30、50または100アミノ酸を含む。
変異GnT1アミノ酸配列由来の、例えば5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、105、110、115、120、125、130、135、140、145または150またはそれ以上の残基からなるフラグメントが含まれる。
変異GnT1タンパク質ならびにそれらの対立遺伝子および種変異系のポリペプチドフラグメントは、保存的置換を含む、1つ以上(例、5、10、15、または20)の置換を含有してもよい。置換、欠失および/または挿入が、例えば相違する種において発生する場合は、配列表に記載された例えば50%、40%または20%未満のアミノ酸残基が変更させられる。
変異GnT1、ならびにフラグメント、ホモログ、変異体および誘導体は、組換え手段によって作成することができる。しかし、それらは例えば固相合成法などの当業者には周知の技術を使用する合成手段によって作成することもできる。タンパク質は、例えば抽出および精製において役立つために、融合タンパク質として生成されてもよい。融合タンパク質パートナーの例には、グルタチオン−S−トランスフェラーゼ(GST)、6xHis、GAL4(DNA結合および/または転写活性化ドメイン)およびβ−ガラクトシダーゼが含まれる。融合タンパク質パートナーと目的のタンパク質配列との間で融合タンパク質配列の除去を許容するために、タンパク質分解的切断部位を含めることも、また便宜的かもしれない。融合タンパク質は、それが当該配列のタンパク質の機能を妨害しない融合タンパク質であってもよい。タンパク質は、動物細胞由来の細胞抽出物の生成によって入手されてもよい。
本明細書に開示した変異GnT1ポリペプチド、変異体、ホモログ、フラグメントおよび誘導体は、実質的に単離された形態にあってよい。そのようなポリペプチドは、該タンパク質の所定の目的を妨害しない担体もしくは希釈液と混合することができ、それでもなお実質的に単離されていると見なせると理解されている。変異GnT1変異体、ホモログ、フラグメントもしくは誘導体は、さらに実質的に精製された形態であってよく、その場合には調製物内にタンパク質を一般には含んでおり、該調製物内のタンパク質の90%超、例えば95%、98%または99%がタンパク質である。
本明細書に開示した変異GnT1ポリペプチド、変異体、ホモログ、フラグメントおよび誘導体は、明示的(revealing)標識を用いて標識することができる。明示的標識は、ポリペプチドなどの検出を可能にする任意の適切な標識であってよい。適切な標識には、放射性同位体、例えば125I、酵素、抗体、ポリヌクレオチドおよびリンカー、例えばビオチンが含まれる。標識されたポリペプチドは、サンプル中のポリペプチドの量を決定するために、診断方法、例えばイムノアッセイにおいて使用できる。ポリペプチドもしくは標識されたポリペプチドは、さらにまた標準プロトコルを用いて動物およびヒトにおける前記ポリペプチドに対する免疫反応性を検出するための血清学的または細胞媒介性免疫アッセイにおいて使用することができる。
本明細書に開示した、任意選択的に標識された変異GnT1ポリペプチド、変異体、ホモログ、フラグメントおよび誘導体は、固相に、例えばイムノアッセイウェルまたはディップスティックの表面に固定することもできる。そのような標識および/または固定化されたポリペプチドは、適切な容器内のキットに適切な試薬、コントロール、取扱説明書などと一緒に包装することができる。そのようなポリペプチドおよびキットは、イムノアッセイによってポリペプチドまたはそれらの対立遺伝子もしくは種変異体に対する抗体の検出方法において使用できる。
イムノアッセイ法は、当分野において周知であり、一般的には、(a)前記タンパク質に対する抗体によって結合可能なエピトープを含むポリペプチドを提供するステップと、(b)抗体−抗原複合体の形成を可能にする条件下で生物学的サンプルを前記ポリペプチドとともにインキュベートするステップと、(c)前記ポリペプチドを含む抗体−抗原複合体が形成されるかどうかを決定するステップとを含む。
本明細書に開示した変異GnT1ポリペプチド、変異体、ホモログ、フラグメントおよび誘導体は、それらが疾患に及ぼす機能を含む細胞機能における対応する遺伝子およびそれらのホモログの役割を試験するために、インビトロまたはインビボ細胞培養システムにおいて使用できる。例えば、切断もしくは修飾されたポリペプチドは、細胞内で発生する正常機能を破壊するために細胞内に導入することができる。ポリペプチドは、組換え発現ベクターからのポリペプチドのインサイチュー発現によって細胞内に導入することができる(以下を参照されたい)。発現ベクターは、任意選択によりポリペプチドの発現を制御するために誘導性プロモーターを有している。
適切な宿主細胞、例えば昆虫細胞または哺乳動物細胞の使用は、組換え発現産物に最適な生物学的活性を授けるための必要に応じて、そのような翻訳後修飾(例、ミリストイル化、グリコシル化、切断、ラピデーション(lapidation)およびチロシン、セリンもしくはトレオニンリン酸化)を提供すると予期される。その中で本明細書に開示した変異GnT1ポリペプチド、変異体、ホモログ、フラグメントおよび誘導体が発現させられるそのような細胞培養システムは、細胞内のポリペプチドの機能を妨害または増強する候補物質を同定するためのアッセイシステムにおいて使用できる。
<変異GnT1核酸>
CHO細胞および細胞系は、変異GnT1核酸を含む。
CHO細胞および細胞系は、変異GnT1核酸を含む。
本発明者らはこのため、一般に変異GnT1核酸をそれらのフラグメント、ホモログ、変異体および誘導体と一緒に提供する。これらの核酸配列は、本明細書に、および特に配列表に開示したポリペプチド配列をコードする可能性がある。
ポリペプチドは、変異GnT1核酸を含んでもよい。変異GnT1核酸は、野生型GnT1配列と比較して1つ以上の点突然変異を含んでもよい。そのような突然変異は、アミノ酸配列への対応する変化を生じさせる、または終止コドンおよびGnT1 mRNAの翻訳の早期終結を導入することができる。
変異GnT1核酸は、終止コドンを生じさせる突然変異を含んでもよく、これは野生型GnT1ポリペプチドより短い変異GnT1ポリペプチドを生じさせる。変異GnT1ポリペプチドの長さは、野生型配列の90%以下、80%以下、70%以下などでもよい。
例えば、変異GnT1核酸は、5、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100またはそれ以上のC末端残基が欠如する変異GnT1ポリペプチドをコードする可能性がある。
変異GnT1核酸は、例えば配列番号1に提示した配列を含んでもよい。これは、細胞系JW152由来の変異GnT1核酸配列である。変異GnT1核酸は、上記の表D1の第2列に提示した突然変異を含むGnT1配列を含んでもよい。
詳細には、本発明者らは、本明細書に開示したGnT1ポリペプチドのいずれかをコードする核酸またはポリヌクレオチドを提供する。そこで、用語「GnT1配列」は、それに応じて解釈されなければならない。しかし、そのような核酸またはポリヌクレオチドは、配列番号1に提示した配列、またはそのような核酸の対応するポリペプチド、およびフラグメント、ホモログ、変異体または誘導体をコードする配列を含んでもよい。上記の用語は、このためこれらの配列に関すると解釈されてもよい。
本文書において使用する用語「ポリヌクレオチド」、「ヌクレオチド」、および核酸は、相互に同義語であることが意図されている。「ポリヌクレオチド」は、一般には、未修飾RNAもしくはDNAまたは修飾RNAもしくはDNAであってよい、任意のポリリボヌクレオチドもしくはポリデオキシリボヌクレオチドを意味している。「ポリヌクレオチド」には、制限なく、一本鎖および二本鎖DNA、一本鎖および二本鎖領域の混合物であるDNA、一本鎖および二本鎖RNA、ならびに一本鎖および二本鎖領域の混合物であるRNA、一本鎖、より典型的には二本鎖または一本鎖および二本鎖領域の混合物であってよいDNAおよびRNAを含むハイブリッド分子が含まれる。さらに、「ポリヌクレオチド」は、RNAもしくはDNAまたはRNAおよびDNAの両方を含む三本鎖領域を意味する。用語「ポリヌクレオチド」には、さらにまた1つ以上の修飾された塩基を含有するDNAまたはRNAおよび安定的または他の理由から修飾された骨格を備えるDNAまたはRNAもまた含まれる。「修飾」塩基には、例えば、トリチル化塩基および例えばイノシンなどの異常塩基が含まれる。DNAおよびRNAには様々な修飾が行われてきた。そこで「ポリヌクレオチド」は、典型的には実際に見いだされる化学的、酵素的または代謝的修飾形、ならびにウイルスおよび細胞に特徴的なDNAおよびRNAの化学形態を含んでいる。「ポリヌクレオチド」は、さらにまたオリゴヌクレオチドと呼ばれることが多い相当に短いポリヌクレオチドを含んでいる。
当業者であれば、多数の相違するポリヌクレオチドおよび核酸は、遺伝コードの縮重の結果として同一ポリペプチドをコードできることを理解できる。さらに、当業者であれば、ルーチン技術を使用して、ポリペプチドがその中で発現させられる任意の特定宿主生物のコドン使用頻度を反映するために本明細書に記載したポリヌクレオチドによってコードされるポリペプチド配列には影響を及ぼさないヌクレオチド置換を行えることが理解されるはずである。
<変異GnT1変異体、誘導体およびホモログ>
本明細書に記載した変異GnT1ポリヌクレオチドは、DNAもしくはRNAを含むことができる。それらは、一本鎖または二本鎖であってよい。それらはさらにまた、それらの内部に合成もしくは修飾ヌクレオチドを含むポリヌクレオチドでもよい。オリゴヌクレオチドへの多数の様々なタイプの修飾は、当分野において公知である。これらは、メチルホスホネートおよびホスホロチオエート骨格、分子の3’および/または5’末端におけるアクリジンもしくはポリリシン鎖の付加を含んでいる。本特許文書のために、本明細書に記載したポリヌクレオチドが当分野において利用できる任意の方法によって修飾できると理解すべきである。そのような修飾は、ポリヌクレオチドのインビボ活性または寿命を増強するために実施できる。
本明細書に記載した変異GnT1ポリヌクレオチドは、DNAもしくはRNAを含むことができる。それらは、一本鎖または二本鎖であってよい。それらはさらにまた、それらの内部に合成もしくは修飾ヌクレオチドを含むポリヌクレオチドでもよい。オリゴヌクレオチドへの多数の様々なタイプの修飾は、当分野において公知である。これらは、メチルホスホネートおよびホスホロチオエート骨格、分子の3’および/または5’末端におけるアクリジンもしくはポリリシン鎖の付加を含んでいる。本特許文書のために、本明細書に記載したポリヌクレオチドが当分野において利用できる任意の方法によって修飾できると理解すべきである。そのような修飾は、ポリヌクレオチドのインビボ活性または寿命を増強するために実施できる。
ポリヌクレオチドが二本鎖の場合は、個別または組み合わせのいずれかの二重鎖の両方の鎖は、本明細書に記載した方法および組成物によって含まれる。ポリヌクレオチドが一本鎖である場合は、そのポリヌクレオチドの相補的配列もまた含まれると理解すべきである。
ヌクレオチド配列に関連する用語「変異体」、「ホモログ」または「誘導体」には、その配列から、またはその配列への1つ(またはそれ以上)のヌクレオチドの任意の置換、変化、修飾、取替え、欠失もしくは付加が含まれる。結果として生じる配列は、CHO細胞内のより高いシアル化を媒介できるポリペプチドをコードしてもよい。
配列同一性に関連して上記で指示したように、「ホモログ」は、例えば、配列表に示した関連配列との少なくとも5%同一性、少なくとも10%同一性、少なくとも15%同一性、少なくとも20%同一性、少なくとも25%同一性、少なくとも30%同一性、少なくとも35%同一性、少なくとも40%同一性、少なくとも45%同一性、少なくとも50%同一性、少なくとも55%同一性、少なくとも60%同一性、少なくとも65%同一性、少なくとも70%同一性、少なくとも75%同一性、少なくとも80%同一性、少なくとも85%同一性、少なくとも90%、または少なくとも95%同一性を有する。
少なくとも95%同一性、例えば少なくとも96%同一性、例えば少なくとも97%同一性、例えば少なくとも98%同一性、例えば少なくとも99%同一性であってよい。ヌクレオチド相同性比較は、上記に記載したように実施できる。使用できる配列比較プログラムは、上記に記載したGCG Wisconsin Bestfitプログラムである。デフォルトのスコアリングマトリックスは、各同一ヌクレオチドに対しては10および各ミスマッチに対しては−9のマッチ値を有する。各ヌクレオチドに対して、デフォルトのギャップ作成ペナルティは−50であり、デフォルトのギャップ伸長ペナルティは−3である。
一部の実施形態では、変異GnT1ポリヌクレオチドは、配列番号1に示した配列に対して少なくとも90%以上の配列同一性を有している。変異GnT1ポリヌクレオチドは、配列番号1に示した配列との60%以上、例えば65%以上、70%以上、75%以上、80%以上、85%以上、90%以上、95%以上、97%以上または98%以上の配列同一性を有していてよい。
<ハイブリダイゼーション>
本発明者らはさらに、本明細書に提示した配列のいずれか、それらの変異体、フラグメントもしくは誘導体、または上記のいずれかの相補体へ選択的にハイブリダイズすることのできる変異GnT1ヌクレオチド配列について記載する。ヌクレオチド配列は、長さが少なくとも15ヌクレオチドの配列、例えば長さが少なくとも20、30、40もしくは50ヌクレオチドの配列である。
本発明者らはさらに、本明細書に提示した配列のいずれか、それらの変異体、フラグメントもしくは誘導体、または上記のいずれかの相補体へ選択的にハイブリダイズすることのできる変異GnT1ヌクレオチド配列について記載する。ヌクレオチド配列は、長さが少なくとも15ヌクレオチドの配列、例えば長さが少なくとも20、30、40もしくは50ヌクレオチドの配列である。
本明細書で使用する用語「ハイブリダイゼーション」は、「それにより核酸鎖が塩基対合により相補鎖と結合するプロセス」ならびにポリメラーゼ連鎖反応テクノロジーにおいて実施されるような増幅プロセスを含むものとする。
本明細書に提示したヌクレオチド配列、またはそれらの相補体へ選択的にハイブリダイズすることのできるポリヌクレオチドは、一般には、少なくとも20、例えば少なくとも25もしくは30、例えば少なくとも40、60もしくは100以上の隣接ヌクレオチドにわたって、本明細書に提示した対応するヌクレオチド配列に対して少なくとも70%、例えば少なくとも80もしくは90%、または少なくとも95%もしくは98%相同である。
用語「選択的にハイブリダイズすることができる」は、プローブとして使用されるポリヌクレオチドが、標的ポリヌクレオチドがバックグラウンドより有意に高いレベルでプローブにハイブリダイズすることが見いだされる条件下で使用されることを意味する。バックグラウンドハイブリダイゼーションは、例えば存在する他のポリヌクレオチドのために、スクリーニングされるcDNAもしくはゲノムDNAライブラリー内で発生する可能性がある。結果的に、バックグラウンドは、プローブとライブラリーの非特異的DNAメンバーとの間の相互作用によって生成されるシグナルの10倍未満、例えば標的DNAを用いて観察される特異的相互作用と同等の強度の100倍未満などであるレベルを付与する。相互作用の強度は、例えば、プローブを例えば32Pで放射標識することによって測定することができる。
ハイブリダイゼーション条件は、Berger and Kimmel(1987,Guide to Molecular Cloning Techniques,Methods in Enzymology,Vol 152,Academic Press,サンディエゴカリフォルニア州)に教示されたように核酸結合複合体の融解温度(Tm)に基づき、以下で説明するように規定された「ストリンジェンシー(厳密性)」を付与する。
最高ストリンジェンシーは、典型的には約Tm−5℃である(プローブのTmより5℃低い)。高ストリンジェンシーはTmより約5℃〜10℃低く、中ストリンジェンシーはTmより約10℃〜20℃低く、低ストリンジェンシーはTmより約20℃〜25℃低い。当業者であれば理解できるように、最高ストリンジェンシーハイブリダイゼーションを使用すると、同一ポリヌクレオチド配列を同定または検出することができるが、中(もしくは低)ストリンジェンシーのハイブリダイゼーションを使用すると、類似もしくは関連するポリヌクレオチド配列を同定または検出することができる。
1つの態様では、本発明者らは、変異GnT1核酸、またはそのフラグメント、ホモログ、変異体もしくは誘導体に、ストリンジェントな条件(例、65℃および0.1×SSC{1×SSC=0.15MのNaCl、0.015MのNa3シトレート(pH 7.0)})下でハイブリダイズすることのできるヌクレオチド配列を開示する。
ポリヌクレオチドが二本鎖である場合は、二重鎖の両方の鎖は、個別に、または組み合わせてのいずれかで本開示に含まれる。ポリヌクレオチドが一本鎖の場合は、そのポリヌクレオチドの相補的配列もまた開示されかつ含まれると理解すべきである。
本明細書に開示された配列と100%相同ではないが、本開示の範囲内に含まれるポリヌクレオチドは、多数の方法で入手できる。本明細書に記載した配列の他の変異体は、例えば、ある範囲の個体、例えば相違する集団由来の個体から作成されたDNAライブラリーを精査することによって入手することができる。さらに、他のウイルス/細菌、または細胞ホモログ、特には哺乳動物細胞(例、ラット、マウス、ウシおよび霊長類細胞)において見いだされる細胞ホモログを入手してもよく、そのようなホモログおよびそれらのフラグメントは、一般には、本明細書に記載の配列表に示した配列に選択的にハイブリダイズすることができる。そのような配列は、他の動物種から作成されたcDNAライブラリーまたは他の動物種由来のゲノムDNAライブラリーを精査することと、中から高ストリンジェンシー条件下で配列番号1の全部または一部を含むプローブを用いてそのようなライブラリーを精査することとによって入手してもよい。類似の検討材料は、変異GnT1の種ホモログおよび対立遺伝子変異体を入手することにも当てはまる。
本明細書に記載したポリヌクレオチドは、プライマー、例えばPCRプライマー、代替増幅反応のためのプライマー、例えば放射性もしくは非放射性標識を用いる従来型手段によって明示的標識を用いて標識されたプローブを生成するために使用されてもよく、またはポリヌクレオチドを、ベクター内にクローニングしてもよい。そのようなプライマー、プローブおよびその他のフラグメントは、長さが少なくとも15、例えば少なくとも20、例えば少なくとも25、30もしくは40ヌクレオチドであり、さらにまた本明細書で使用する用語「ポリヌクレオチド」に含まれる。フラグメントは、長さが500、200、100、50または20ヌクレオチド未満であってもよい。
DNAポリヌクレオチドおよびプローブなどのポリヌクレオチドを、組換え的、合成的、または当業者であれば利用できる任意の手段によって生成することができる。それらを、さらにまた標準技術によってクローニングすることもできる。
一般に、プライマーは、一度に1つのヌクレオチドが所望の核酸配列の段階的製造を含む合成的手段によって生成される。これを実施するための自動化技術を使用する技術は、当分野において容易に利用できる。
より長いポリヌクレオチドは、一般には組換え手段を用いて、例えばPCR(ポリメラーゼ連鎖反応)クローニング技術を使用して生成される。これは、一対の(例えば、約15〜30ヌクレオチドの)プライマーを作成することと、クローニングを所望する1領域の配列をフランキングすることと、該プライマーを動物またはヒト細胞から入手されるmRNAもしくはcDNAと接触させることと、ポリメラーゼ連鎖反応を該所望領域の増幅を発生させる条件下で実施することと、該増幅させたフラグメントを(例えば、アガロースゲル上で該反応混合物を精製することによって)単離することと、該増幅させたDNAを回収することとを含んでいる。プライマーは、適切な制限酵素認識部位を含有するように設計できるので、増幅させたDNAは適切なクローニングベクター内にクローニングすることができる。
〔実施例1〕
〔実施例1〕
<細胞培養>
チャイニーズハムスター卵巣K1(CHO−K1)細胞を、最初はDr.Donald K.MacCallum(University of Michigan Medical Scholl、ミシガン州アナーバー、MI)から入手する。
チャイニーズハムスター卵巣K1(CHO−K1)細胞を、最初はDr.Donald K.MacCallum(University of Michigan Medical Scholl、ミシガン州アナーバー、MI)から入手する。
JW152細胞を含む親および変異CHO細胞は、5%のCO2を備える加湿培養器内で37℃で10%ウシ胎児血清(FBS)が補給されたダルベッコ変法イーグル培地(Dulbecco’s Modified Eagle Media:DMEM)中で培養される。
Lec1.3細胞(Lec1細胞)は、Dr.P.Stanley(Albert Einstein College of Medicine、ニューヨーク州)のご厚意で提供され、プロリン(40 mg/L)(Invitrogen/Gibco社)および10%のFBSが補給されたα−MEM(Gibco社)中で培養される。
〔実施例2〕
〔実施例2〕
<RCA−I耐性CHO細胞の単離>
CHO−K1細胞は、集密になるまで6ウェルプレート内で培養され、その後に培養培地は無血清DMEMに変更される。Ricinus communisアグルチニンI(RCA−I、EY Laboratories社)は、10μg/mLの最終濃度に達するまで培地に加えられ、細胞とともに一晩インキュベートされる。
CHO−K1細胞は、集密になるまで6ウェルプレート内で培養され、その後に培養培地は無血清DMEMに変更される。Ricinus communisアグルチニンI(RCA−I、EY Laboratories社)は、10μg/mLの最終濃度に達するまで培地に加えられ、細胞とともに一晩インキュベートされる。
次にRCA−Iを含有する無血清DMEMは10%のFBSを含む新鮮DMEMと取り替えられる。9日後、RCA−I処理を生残したCHO細胞のコロニーが採取され、24ウェルプレート内で培養される。
これらの細胞は次に、変異細胞がもはやRCA−Iと反応しないことを確認するために、RCA−Iを用いて凝集試験にかけられる。
〔実施例3〕
〔実施例3〕
<発現構築物>
ヒトエリスロポエチン(EPO)に対するコーディング領域および幾つかのグリコシル化関連遺伝子は、pcDNA3.1ベクター(Invitrogen社)内にクローニングされる。
ヒトエリスロポエチン(EPO)に対するコーディング領域および幾つかのグリコシル化関連遺伝子は、pcDNA3.1ベクター(Invitrogen社)内にクローニングされる。
その後に脳心筋炎ウイルス(EMCV)の内部リボソーム侵入部位(IRES)およびチャイニーズハムスターN−アセチルグルコサミニルトランスフェラーゼI(EPO−IRES−GnTI、もしくは略してEIG)に対するコーディング領域が続くヒトEPOのオープンリーディングフレームを含有していたDNAフラグメントもまたpcDNA3.1内にクローニングされる。結果として生じたEPOおよびGnTIの両方を発現するベクターは、pEIGと呼ばれる。効率的翻訳を保証するために、Kozakコンセンサス配列(GCCACC)は、各構築物内の翻訳開始コドンATGの上流に配置される。
〔実施例4〕
〔実施例4〕
<親および変異CHO細胞系における組換えヒトEPOの一過性発現>
特に明示しない限り、EPOを発現する1μgのDNA構築物およびGnTIまたは他のグリコシル化関連遺伝子を発現する1μgのDNA構築物は、製造業者のプロトコルにしたがってリポフェクタミン(Invitrogen社)とともに野生型もしくはJW−152変異細胞内に共トランスフェクトされる。
特に明示しない限り、EPOを発現する1μgのDNA構築物およびGnTIまたは他のグリコシル化関連遺伝子を発現する1μgのDNA構築物は、製造業者のプロトコルにしたがってリポフェクタミン(Invitrogen社)とともに野生型もしくはJW−152変異細胞内に共トランスフェクトされる。
トランスフェクションの2日後、トランスフェクトされた細胞からの馴化培養培地が収集される。各トランスフェクションサンプル中の組換えEPOの濃度は、EPO ELISAキット(Roche社)を使用して標準ELISAによって決定される。
〔実施例5〕
〔実施例5〕
<野生型CHO細胞およびJW−152CHO細胞によって生成されたEPOの等電点焦点(IEF)分析>
様々なサンプルにおけるEPOのシアル化パターンは、IEFおよびその後に以前に記載されたようなウエスタンブロット法によって分析される(Schriebl et al.2007,Electrophoresis 28:2100−7)。IEFについてのpH範囲は、3〜10である。
〔実施例6〕
様々なサンプルにおけるEPOのシアル化パターンは、IEFおよびその後に以前に記載されたようなウエスタンブロット法によって分析される(Schriebl et al.2007,Electrophoresis 28:2100−7)。IEFについてのpH範囲は、3〜10である。
〔実施例6〕
<RCA−I耐性CHO細胞内のGnTI cDNAの分子クローニングおよび配列決定分析>
各細胞系について、1×107細胞をペレットにし、PBS中で洗った。全RNAは、RNAqueousキット(Ambion社)を使用してペレットから抽出される。次にcDNAは、製造業者の推奨にしたがって、モロニー(Moloney)マウス白血病ウイルス(MMLV)逆転写酵素(Promega社)を使用した逆転写を通して合成される。
各細胞系について、1×107細胞をペレットにし、PBS中で洗った。全RNAは、RNAqueousキット(Ambion社)を使用してペレットから抽出される。次にcDNAは、製造業者の推奨にしたがって、モロニー(Moloney)マウス白血病ウイルス(MMLV)逆転写酵素(Promega社)を使用した逆転写を通して合成される。
各細胞系のcDNA由来のGnTIアンプリコンは、PFX(Invitrogen社)を用いるポリメラーゼ連鎖反応(PCR)を通して入手される。これは、続いてpcDNA 3.1発現ベクター内にクローニングされ、そして配列決定される。各変異体系由来の少なくとも4つのクローンが配列決定される。全プラスミド精製は、Promega社からの少量もしくは中量調製キットを使用して実施される。構築物は、Big Dye 3.1(Applied Biosystems社)を用いたサイクルシーケンシング後にABI Prism 3100遺伝分析装置(Applied Biosystems社)を使用して配列決定される。
これらの結果は、上記の表D1に示されている。
〔実施例7〕
〔実施例7〕
<安定的にトランスフェクトされたCHO細胞系の単離>
CHO−K1細胞は、EPOを単独で発現する構築物によりトランスフェクトされるが、変異JW152細胞はEPOおよびGnTIの両方を発現するpEIGによりトランスフェクトされる。トランスフェクトされた細胞は、2週間にわたってG418(0.8mg/mL)を用いて選択される。
CHO−K1細胞は、EPOを単独で発現する構築物によりトランスフェクトされるが、変異JW152細胞はEPOおよびGnTIの両方を発現するpEIGによりトランスフェクトされる。トランスフェクトされた細胞は、2週間にわたってG418(0.8mg/mL)を用いて選択される。
トランスフェクトされたプールから得られる安定的にトランスフェクトされた細胞は、限界希釈法を使用して96ウェル内で培養される。EPOを発現した単一トランスフェクトされた細胞由来の安定的細胞系は、ドットブロット分析を使用して選択され、各細胞系によって発現された組換えEPOのシアル化パターンは、等電焦点法を用いて分析される。
〔実施例8〕
〔実施例8〕
<結果:RCA−I耐性変異CHO細胞系の単離および特性解析>
RCA−Iは、糖タンパク質もしくは糖脂質上のβ結合ガラクトース残基に対して特異的であることが知られている植物レクチンであり、CHO−K1細胞由来のグリコシル化突然変異体を選択するために使用される。大多数のCHO細胞は、一晩のインキュベーション後にRCA−Iによって殺滅される。
RCA−Iは、糖タンパク質もしくは糖脂質上のβ結合ガラクトース残基に対して特異的であることが知られている植物レクチンであり、CHO−K1細胞由来のグリコシル化突然変異体を選択するために使用される。大多数のCHO細胞は、一晩のインキュベーション後にRCA−Iによって殺滅される。
9〜10日後、RCA−I処理を生存した細胞は単一クローンに増殖させられた。これらのクローンは採取され、24ウエルプレート内で培養される。クローンの1つはJW152と命名されている。
この細胞系内の遺伝的欠陥を特性解析するために、JW152細胞は、ヒトEPOを発現するために構築物でトランスフェクトされる。JW152細胞によって生成された組換えEPOは、エンドグリコシダーゼH(Endo H)を用いて処理される。
これらの結果は、図1に示されている。図1は、JW152発現EPOがEndo H処理に対して感受性であることを示しているが、これはEPO分子上で見いだされるグリカン構造(N−グリカン類)が高マンノースタイプであることを示唆している。そこで、グリコシル化経路の初期由来の遺伝子には欠陥があることが疑われる。
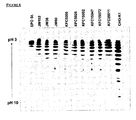
この観察に基づいて、相補性検定が実施される。この検定では、EPO構築物に加えて、JW152細胞は、N−グリコシル化経路上の幾つかの遺伝子により共トランスフェクトされる。これらの遺伝子には、グルコシダーゼI、グルコシダーゼII、マンノシダーゼIA、IB、IC、マンノシダーゼII、GnTIおよびGnTIIが含まれる。これらの共トランスフェクション実験においてJW152細胞によって生成されるEPOサンプルは、等電焦点法(IEF)によって、およびその後にウエスタンブロット法によって分析される。
これらの結果は、図2に示されている。左端のレーン(CHO WT)は、コントロールとしての野生型CHO細胞によって発現されたEPOを示している。CHO−JW152の下のレーンは、JW152細胞によって生成されたEPOを示し、これはEPOの不完全グリコシル化を証明している。残りのレーンは、指示したように様々のグリコシル化関連遺伝子により共トランスフェクトされるJW152細胞系内で生成されたEPOを示している。
試験された遺伝子間で、GnTIだけがJW152細胞内で生成されたEPOのシアル化パターンを回復することができる。これらの結果は、JW152細胞には機能的GnTI遺伝子が欠如することを示唆している。
このIEF/ウエスタンブロットアッセイから行われたまた別の重要な観察では、GnTIの存在下では、JW152細胞は野生型細胞と比較して(野生型細胞によって生成されたEPOを用いた場合と比較して)はるかに良好にEPOをシアル化する。
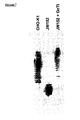
この相違がGnTIを過剰発現することの結果ではなくJW152細胞の固有の特徴に起因することを確認するために、3つのCHO細胞系はGnTI構築物により共トランスフェクトすることによって分析される。馴化培地中の組換えEPOが収集され、IEFによって分析される。
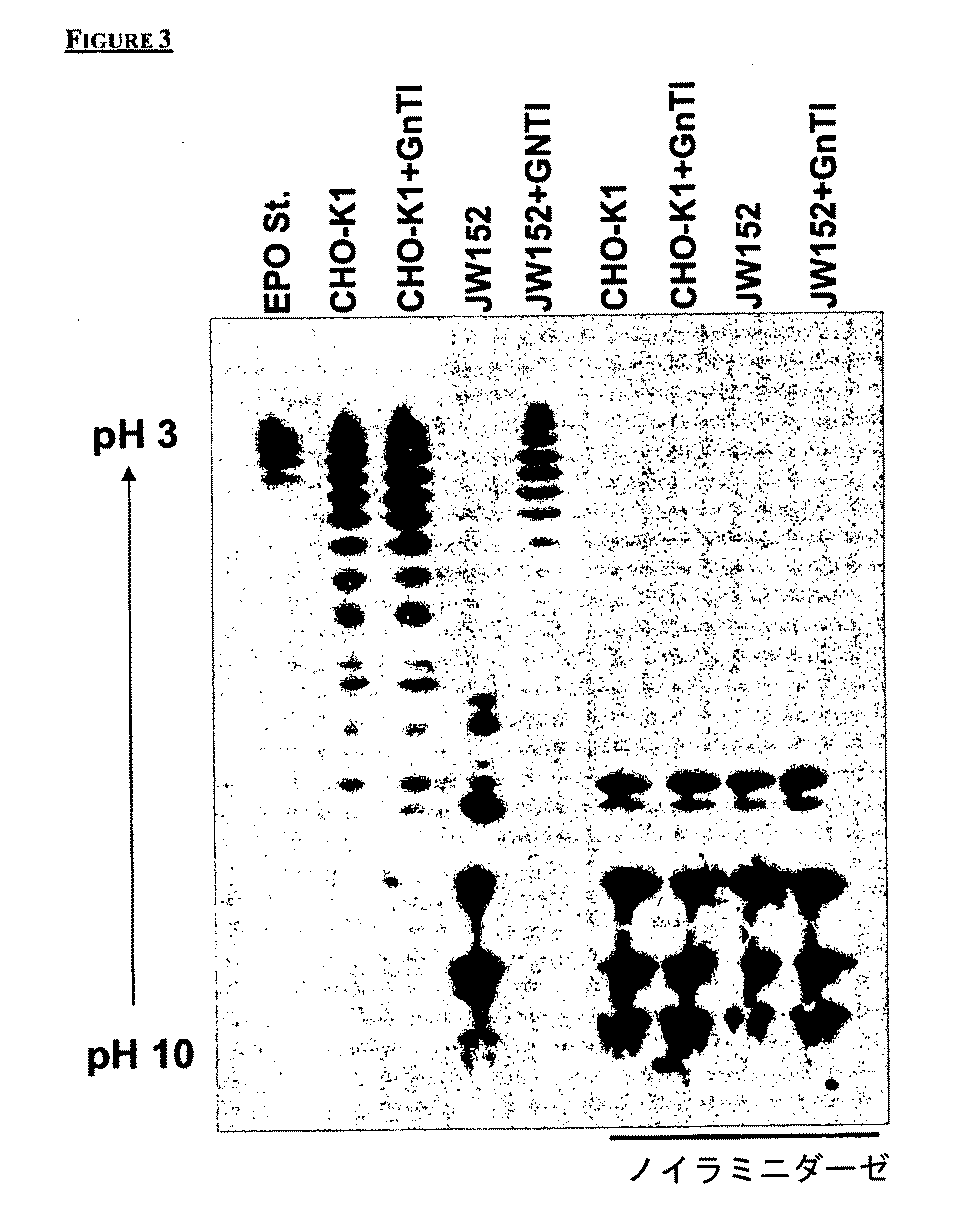
これらの結果は、図3に示されている。GnTIは、野生型CHO細胞におけるEPOのシアル化を改善しなかった(CHO−WTレーンおよびCHO−WT+GnTIレーンを比較する)。GnTIの共発現を伴う、および共発現を伴わないCHO−K1のEPOシアル化パターンは同一であると思われるので、GnTIの過剰発現はCHO−K1+GnT1と表示されたレーンにおいて見られるシアル化の改善の原因ではない。
GnTIは、JW152細胞におけるEPOのシアル化を劇的に改善した(JW152+GnTIレーン)。GnTIの存在下では、JW152細胞はEPOを野生型CHO細胞と比較してはるかに良好にシアル化する(CHO−WTレーンおよびCHO−JW152+GnTIレーンを比較する)。
図3は、GnTIの存在下では、JW152細胞が野生型細胞と比較してはるかに良好に組換えタンパク質をシアル化することを示している。シアル酸を切断するノイラミニダーゼ類を用いたサンプルの処理は、シアル酸の切断後には塩基領域に還元される酸性領域内のEPO帯を生じさせるが、これはEPOのより高いシアル化形が実際にはゲルの酸性領域内に集中することを証明している。
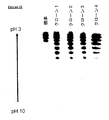
Lec1細胞は、以前にP.Stanleyによって単離されているが、それらにはGnTI活性が欠如することが知られている。Lec1細胞(Lec1)によって生成されたEPOのIEFパターンは、JW152によって生成されたEPOのIEFパターンと類似である。GnTIにより共トランスフェクトされるLec1細胞によって生成されたEPOは、野生型CHO細胞によって生成されたEPOと類似のシアル化パターンを示す。
これは、図4に示されている。そこで、図4は、以前に公表されたGnTI欠陥を有するLec1突然変異体の機能的GnTIの存在下では、EPOの発現もまた高シアル化されることを示している。
〔実施例9〕
〔実施例9〕
<結果:GnTIの存在下でのJW152細胞内の組換えEPOの安定的発現>
図2および図3に提示したデータは、全部が一過性にトランスフェクトされた細胞由来である。安定的にトランスフェクトされた細胞によって生成されたEPOのシアル化パターンを解明するために、JW152細胞はpEIGによりトランスフェクトされ、G418を用いて選択される。
図2および図3に提示したデータは、全部が一過性にトランスフェクトされた細胞由来である。安定的にトランスフェクトされた細胞によって生成されたEPOのシアル化パターンを解明するために、JW152細胞はpEIGによりトランスフェクトされ、G418を用いて選択される。
選択の2週間後、単一クローンが採取され、G418の選択圧下でさらに2週間にわたり24ウェルプレート内で培養される。10個の無作為に採取されたそのような安定的にトランスフェクトされたクローンによって生成されたEPOは、IEFによって分析される。
図10に示したように、様々のクローンによって生成された全EPOサンプルは高くシアル化されている。シアル化パターンは、図3に示した一過性にトランスフェクトされた細胞によって生成されたEPOのシアル化パターンと極めて類似する。
図11に示した結果は、様々の安定的クローンによって生成されたEPOサンプルが全シアル化において相違するが、一般には図10に示したEPOサンプルほど良好にはシアル化されていないことを証明している。
〔実施例10〕
〔実施例10〕
<結果:RCA−I処理を生存した全CHO細胞は、機能異常のGnTI遺伝子を有し、それらはGnTIにより共コトランスフェクトされると全部がそれらのタンパク質をより良好にシアル化する>
RCA−Iは、β−Gal残基に特異的に結合することが知られている。理論的には、これらの細胞がそれらの表面糖タンパク質上の末端糖としてのβ−Galを発現しない限り、それらはRCA−I処理を生き残り、変異クローンとして単離されるはずである。
RCA−Iは、β−Gal残基に特異的に結合することが知られている。理論的には、これらの細胞がそれらの表面糖タンパク質上の末端糖としてのβ−Galを発現しない限り、それらはRCA−I処理を生き残り、変異クローンとして単離されるはずである。
本発明者らは、RCA−Iを用いて100個より多い変異CHOクローンを単離し、それらが様々の遺伝子内に遺伝突然変異を有すると期待した。驚くべきことに、図2に記載した相補性検定が実施されると、RCA−I処理を生存した全クローンは機能異常GnTI遺伝子を有すると確認される。
さらに、図9に示したように、これらのクローン内で生成されたEPOは、GnTIにより共トランスフェクトされると全部が高シアル化される。mRNAは、変異体系の一部から単離され、cDNAに逆転写される。GnTIについてのコーディング領域は、cDNAを鋳型として使用するPCRによって増幅され、pcDNA3.1内にクローニングされる。
シーケンシング分析は、これらの変異体系内のGnTI遺伝子内で9つの相違する点突然変異を明らかにしたが、これはそれらが様々なオリジナル変異体細胞から達したことを示唆している(上記の表D1を参照されたい)。JW152のようなそれらの一部は、早期終止コドンを生じさせる点突然変異を有している。その他は、GnTIコーディング領域内でアミノ酸残基を変化させる突然変異を有している。GnTI遺伝子内に相違する突然変異を各々が備える9つの変異体系は、pEIGによりトランスフェクトされる。全9つの細胞系によって生成されたEPOは、IEFによって分析されると全部が高シアル化されている(データは示していない)。
〔実施例10〕
〔実施例10〕
<JW152およびその他のCHO GnT1突然変異体におけるシアル化パターン>
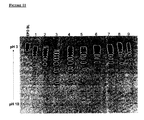
図5に示したように、EPOの不完全シアル化は、CHO野生型と比較して、各々がGnT1機能の消失をもたらすGnT1遺伝子内の相違する突然変異を有する、RCAレクチンを用いて選択された9個のCHOグリコシル化突然変異体において観察される。
図5に示したように、EPOの不完全シアル化は、CHO野生型と比較して、各々がGnT1機能の消失をもたらすGnT1遺伝子内の相違する突然変異を有する、RCAレクチンを用いて選択された9個のCHOグリコシル化突然変異体において観察される。
図6に示したように、各々がGnT1遺伝子内に相違する突然変異を有する9個のCHOグリコシル化突然変異体は、レスキュー後にCHO野生型より優れたシアル化パターンを有する。
図7は、相違する糖タンパク質分子、EPO−Fc、本質的にはエリスロポエチン融合タンパク質の等電焦点法サンプルを用いた実験の結果を示している。この実験は、上記に記載したプロトコルを用いてEPO発現およびIEF分析について、相違するコーディング配列を備える発現ベクターだけを用いて実施された。
左端のレーンは、EPO−Fcコーディング配列を含有する発現ベクターでトランスフェクトされたCHO−K1細胞内でのEPO−Fcの発現を示している。中央のレーンは、EPO−Fcコーディング配列を含有する発現ベクターによりトランスフェクトされたJW152細胞内でのEPO−Fcの発現を示している。右端のレーンは、EPO−Fcコーディング配列を含有する発現ベクターおよび機能的GnTIコーディング配列を含有する発現ベクターにより共トランスフェクトされたJW152細胞内でのEPO−Fcの発現を示している。図7に示したように、レスキューされたJW152細胞による優れたシアル化は、相違するモデルの糖タンパク質を用いた場合さえ維持されている。
これらの結果は、レスキューされたJW152による優れたシアル化が相違するモデルの糖タンパク質を用いた場合でさえ維持されることを証明している。
図12は、付着した培養中の安定的JW152細胞系について観察されたシアル化パターンが懸濁培養中で維持されることを示している。
結論として、本発明者らは、新規なCHOグリコシル化変異細胞を単離するための方法を開発した。CHO細胞を処理するためにRCA−Iが使用される限り、生存細胞はそれらのGnTI遺伝子内に遺伝的欠陥を有することになる。GnTIにより共トランスフェクトされると、これらのRCA−I耐性CHO細胞は、高シアル化されたN−グリカン類を備える組換え糖タンパク質を発現する。
〔実施例11〕
〔実施例11〕
<HPAECクロマトグラム>
図8は、機能的GnTIを共発現するJW152細胞内で発現されたEPO−Fcから切断されたより良好にシアル化されたグリカン類を示しているHPAECクロマトグラムを示している写真である。CHO−K1およびJW152内で一過性に発現され、GnTIにより共トランスフェクトされたEPO−Fcは、プロテインA結合クロマトグラフィーカラムによるアフィニティ精製を用いて精製される。等量のEPO−Fc上のグリカン類は、ペプチド:N−グリコシダーゼF(PNGase F)を用いた処理によって切断され、そしてグリカン類に付着したシアル酸の数にしたがって、高pHアニオン交換クロマトグラフィー(HPAEC)を使用して分離される。
図8は、機能的GnTIを共発現するJW152細胞内で発現されたEPO−Fcから切断されたより良好にシアル化されたグリカン類を示しているHPAECクロマトグラムを示している写真である。CHO−K1およびJW152内で一過性に発現され、GnTIにより共トランスフェクトされたEPO−Fcは、プロテインA結合クロマトグラフィーカラムによるアフィニティ精製を用いて精製される。等量のEPO−Fc上のグリカン類は、ペプチド:N−グリコシダーゼF(PNGase F)を用いた処理によって切断され、そしてグリカン類に付着したシアル酸の数にしたがって、高pHアニオン交換クロマトグラフィー(HPAEC)を使用して分離される。
このクロマトグラムは、CHO−K1サンプルと比較した場合に、4S群におけるJW152サンプルについて明確に高いピークおよび1S群における低いピークを示している。
<参考文献>
Weikert et al.(1999)Engineering Chinese hamster ovary cells to maximize sialic acid content of recombinant glycoproteins.Nature Biotechnology 17:1116.
Weikert et al.(1999)Engineering Chinese hamster ovary cells to maximize sialic acid content of recombinant glycoproteins.Nature Biotechnology 17:1116.
本文書に言及した特許出願および特許の各々、そして上記の特許出願および特許の各々において特許出願および特許の各々の審査手続き中を含めて引用もしくは参照された各文書(「特許出願が引用した文書」)、ならびに特許出願および論文の各々および該特許出願が引用した文書のいずれかにおいて引用もしくは言及された任意の製品についての任意の製造業者の取扱説明書もしくはカタログは、これにより参照して本明細書に組み入れられる。さらに、本明細書において引用した全文書、ならびに本明細書において引用した文書の中で引用もしくは参照された全文書、ならびに本明細書において引用もしくは言及された任意の製品についての任意の製造業者の取扱説明書もしくはカタログは、これにより参照して組み入れられる。
本発明の記載した方法およびシステムの様々な修飾および変形は、当業者には、本発明の範囲および精神から逸脱せずに明白になる。本発明は特定の好ましい実施形態と結び付けて記載してきたが、請求する本発明は、そのような特定の実施形態に過度に限定すべきではないと理解すべきである。実際に、分子生物学または関連分野の当業者には明白である、本発明を実施するための記載した様式の様々な修飾は、請求の範囲内に含まれると意図されている。
ATCC
ブダペストの制限された寄託証明書
特許手続のための微生物寄託の国際承認に関するブダペスト条約
国際書式
規則7.3に準拠して発行された原寄託のケースの受託書および
規則10.2に準拠して発行された生存性に関する陳述書
アメリカン・タイプ・カルチャー・コレクション(ATCC(登録商標))は、特許出願に関連する貴殿の種子/株の寄託を受領しました。以下の情報を特許庁の要件を満たすために提供致します。
科学技術研究庁
Dr.Song Zhiwei 様
20 Biopolis way #06−01
Centros.SG
シンガポール 138668
寄託者:科学技術研究庁
ATCC(登録商標)による種子/株の受託日:2008年12月11日
寄託者による識別参照番号:ATCC(登録商標)特許寄託指定番号
チャイニーズハムスター卵巣細胞 JW152 PTA−9657
ATCC(登録商標)は、以下のように理解しています。
1.これらの種子/株の寄託は、ATCC(登録商標)に、明示的にも黙示的にも、該特許を侵害する許諾を与えるものではなく、これらの種子/株の他者へのATCC(登録商標)からの公開は、明示的にも黙示的にも、前記特許を侵害する許諾を与えるものではありません。
2.前記寄託物が該特許の有効期間中に死滅した、もしくは破損した場合は、それを生存性材料と置換することは貴殿の責任です。さらに、寄託期間中に配布するのに十分な量を供給することもまた貴殿の責任です。ATCC(登録商標)は、本物質を30年間または前記寄託に対する最新の依頼日より5年間のいずれか長い期間に渡り配布および維持します。アメリカ合衆国および多数の他の国々がブダペスト条約の締約国です。
米国特許の発行に先立ち、ATCC(登録商標)は、1回の手数料を考慮して、寄託者もしくは関連特許庁によって指示される場合を除いて、これらの種子/株またはそれらまたはそれらの寄託に関するあらゆる情報を配布しないことに同意します。関連特許の発行後には、我々は、種子/株を公開することに責任を負い、それらは何の制約も受けずに公衆へ配布するために利用可能になります。我々は、寄託日から30年間に渡り該種子/株に対する要請について貴殿にお知らせします。
本寄託は、2009年1月8日に検査され、同日に前記種子/株は生存性でありました。
国際寄託機関:アメリカン・タイプ・カルチャー・コレクション(ATCC(登録商標))、アメリカ合衆国バージニア州マナッサス
ATCC(登録商標)の代表権を有する者の署名
2009年1月9日
ATCC(登録商標)特許寄託 日付
CC:Dr.Khoo Chong Yee
ブダペストの制限された寄託証明書
特許手続のための微生物寄託の国際承認に関するブダペスト条約
国際書式
規則7.3に準拠して発行された原寄託のケースの受託書および
規則10.2に準拠して発行された生存性に関する陳述書
アメリカン・タイプ・カルチャー・コレクション(ATCC(登録商標))は、特許出願に関連する貴殿の種子/株の寄託を受領しました。以下の情報を特許庁の要件を満たすために提供致します。
科学技術研究庁
Dr.Song Zhiwei 様
20 Biopolis way #06−01
Centros.SG
シンガポール 138668
寄託者:科学技術研究庁
ATCC(登録商標)による種子/株の受託日:2008年12月11日
寄託者による識別参照番号:ATCC(登録商標)特許寄託指定番号
チャイニーズハムスター卵巣細胞 JW152 PTA−9657
ATCC(登録商標)は、以下のように理解しています。
1.これらの種子/株の寄託は、ATCC(登録商標)に、明示的にも黙示的にも、該特許を侵害する許諾を与えるものではなく、これらの種子/株の他者へのATCC(登録商標)からの公開は、明示的にも黙示的にも、前記特許を侵害する許諾を与えるものではありません。
2.前記寄託物が該特許の有効期間中に死滅した、もしくは破損した場合は、それを生存性材料と置換することは貴殿の責任です。さらに、寄託期間中に配布するのに十分な量を供給することもまた貴殿の責任です。ATCC(登録商標)は、本物質を30年間または前記寄託に対する最新の依頼日より5年間のいずれか長い期間に渡り配布および維持します。アメリカ合衆国および多数の他の国々がブダペスト条約の締約国です。
米国特許の発行に先立ち、ATCC(登録商標)は、1回の手数料を考慮して、寄託者もしくは関連特許庁によって指示される場合を除いて、これらの種子/株またはそれらまたはそれらの寄託に関するあらゆる情報を配布しないことに同意します。関連特許の発行後には、我々は、種子/株を公開することに責任を負い、それらは何の制約も受けずに公衆へ配布するために利用可能になります。我々は、寄託日から30年間に渡り該種子/株に対する要請について貴殿にお知らせします。
本寄託は、2009年1月8日に検査され、同日に前記種子/株は生存性でありました。
国際寄託機関:アメリカン・タイプ・カルチャー・コレクション(ATCC(登録商標))、アメリカ合衆国バージニア州マナッサス
ATCC(登録商標)の代表権を有する者の署名
2009年1月9日
ATCC(登録商標)特許寄託 日付
CC:Dr.Khoo Chong Yee
Claims (16)
- 例えば機能的GnT1の存在下において、野生型チャイニーズハムスター卵巣(CHO)細胞と比較して、タンパク質をより高シアル化できるチャイニーズハムスター卵巣(CHO)細胞であって、前記CHO細胞は、Ricinus communis(ヒマ)のアグルチニンI(RCA−I)を用いた選択によって入手できるCHO細胞。
- (i)GnT1遺伝子における、例えばGnT1配列(GenBankアクセッション番号:AF343963)の特定位置における、
(a)1015位でのCからTへのトランジッション;
(b)1300位でのGからCへのトランスバージョン;
(c)638位でのAからCへのトランスバージョン;
(d)784位でのCからGへのトランスバージョン;
(e)811位でのTからAへのトランスバージョン;
(f)コードされたアミノ酸配列の236位からのフレームシフトを生じさせる706位での挿入;
(g)1015位でのCからTへのトランジッション;
(h)246位でのGからAへのトランジッション;
(i)258位でのGからAへのトランジッション;
(j)859位でのAからTへのトランスバージョン
から選択される突然変異を含む、または
(ii)GnT1配列(GenBankアクセッション番号:AF343963)の特定位置で以下の:
(a)434位でAlaからProへ;
(b)213位でAsp→Ala;
(c)262位でArg→Gly;
(d)271位でTrp→Arg;
(e)GnT1をコードする核酸配列の706位での挿入の結果として生じる236位からのフレームシフト;
(f)339位でのGln→STOP;
(g)82位でのTrp→STOP;
(h)86位でのTrp→STOP;
(i)287位でのLys→STOPの内の1つ以上の突然変異を含むGnT1タンパク質を発現する、請求項1に記載のCHO細胞。 - 前記GnT1遺伝子は、配列番号1に示したGnT1核酸配列を含む、または配列番号2に示したGnT1タンパク質を発現する、請求項1または2に記載のCHO細胞。
- 前記CHO細胞は:
(a)目的のタンパク質、例えば目的の組換えタンパク質、例えばエリスロポエチン(EPO)もしくはインターフェロン−γ(IFN−γ)をコードする核酸配列;
(b)機能的GnT1をコードする核酸配列;または
(c)例えばCHO細胞内に安定的にトランスフェクトされた、1つの発現ベクター内に含まれた目的のタンパク質をコードする核酸配列および機能的GnT1をコードする核酸配列を含む、請求項1、2または3に記載のCHO細胞。 - 請求項1〜4のいずれかに記載のCHO細胞を含むCHO細胞系。
- JW152細胞系(ATCCにブダペスト条約の下でアクセッション番号PTA−9657として寄託された)、JW80細胞系、JW36細胞系、KFC15002細胞系、KFC15071細胞系、KFC5008細胞系、JW152細胞系、KFC5026細胞系、KFC20011細胞系またはKFC15047細胞系を含むCHO細胞系。
- 懸濁培養に順応させられている、請求項1〜6のいずれかに記載のCHO細胞もしくはCHO細胞系。
- 例えばエリスロポエチン(EPO)もしくはインターフェロン−γ(IFN−γ)を含む、請求項1〜7のいずれかに記載のCHO細胞もしくはCHO細胞系によって発現された組換えタンパク質。
- 4以下、3.5以下、3以下、2.5以下もしくは2以下のpKaまたは150より大きい、例えば160より大きい、170より大きい、180より大きい、例えば190より大きい、200より大きい、210より大きい、例えば220より大きい、もしくは230より大きいZ数、またはその両方を含む、請求項8に記載の組換えタンパク質。
- 組換えタンパク質を発現する方法であって、前記方法は、前記タンパク質をコードする核酸を請求項1〜7のいずれかに記載のCHO細胞内に導入することと、前記タンパク質を該CHO細胞もしくはその子孫から発現することと、前記タンパク質を精製することとを含み、前記方法はさらに、任意で前記タンパク質をコードする核酸配列および機能的GnT1をコードする核酸配列を含む発現ベクターの形態にあるなどの前記CHO細胞内に機能的GnT1をコードする核酸を導入もしくは安定的にトランスフェクトすることを含む方法。
- 配列番号1に示した配列、またはGnT1配列を含む配列を表D1の第2列に記載した突然変異と一緒に含む核酸、またはその変異体、ホモログ、誘導体もしくはフラグメント。
- 配列番号2に示した配列、またはGnT1配列を含む配列を表D1の第3列に記載した突然変異と一緒に含むポリペプチド、またはその変異体、ホモログ、誘導体もしくはフラグメント。
- CHO細胞もしくは細胞系を提供する方法であって、前記方法はRicinus communisアグルチニンI(RCA−I)の存在下でCHO細胞を培養することと、該培養を生残する細胞を選択することとを含み、例えば:
(a)前記CHO細胞は、0.1μg/mL〜100μg/mL、例えば50μg/mLまで、または20μg/mLまで、例えば10μg/mLもしくは5μg/mLまでの濃度のRCA−Iへ曝露される;または
(b)前記CHO細胞は、RCA−Iへ、1時間、数時間(例えば、2、3、4、5、6、7、8、9、10、11、12時間)、一晩から数日間、例えば2日間もしくは3日間、例えば一晩までの期間にわたって曝露される方法。 - 凝集試験においてRCA−Iと反応しない細胞を選択することをさらに含む、請求項13に記載の方法。
- 請求項13または14に記載の方法によって入手可能なCHO細胞もしくはCHO細胞系。
- 実質的に添付図面の図1〜12を参照および図示して上記に記載したCHO細胞、細胞系、組換えタンパク質、方法、核酸またはポリペプチド。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US9827008P | 2008-09-19 | 2008-09-19 | |
| US61/098,270 | 2008-09-19 | ||
| US18364709P | 2009-06-03 | 2009-06-03 | |
| US61/183,647 | 2009-06-03 | ||
| PCT/SG2009/000348 WO2010033085A1 (en) | 2008-09-19 | 2009-09-18 | Chinese hamster ovary cell lines |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2012502654A true JP2012502654A (ja) | 2012-02-02 |
Family
ID=42039751
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011527782A Pending JP2012502654A (ja) | 2008-09-19 | 2009-09-18 | チャイニーズハムスター卵巣細胞系 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US9012176B2 (ja) |
| EP (1) | EP2342320B1 (ja) |
| JP (1) | JP2012502654A (ja) |
| KR (1) | KR20110060913A (ja) |
| CN (2) | CN104450783B (ja) |
| CA (1) | CA2737748A1 (ja) |
| WO (1) | WO2010033085A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SG184051A1 (en) | 2010-03-25 | 2012-10-30 | Agency Science Tech & Res | Method of producing recombinant proteins with mannose- terminated n-glycans |
| ES2733248T3 (es) | 2012-01-11 | 2019-11-28 | Sigma Aldrich Co Llc | Producción de proteínas recombinantes con glicoformas simples |
| CN109370980B (zh) | 2012-05-02 | 2023-05-09 | 生命技术公司 | 高产量瞬时表达系统 |
| EP3322813A1 (en) * | 2015-07-13 | 2018-05-23 | Life Technologies Corporation | System and method for improved transient protein expression in cho cells |
| CN108588127A (zh) * | 2018-04-11 | 2018-09-28 | 上海药明生物技术有限公司 | 一种表达高甘露糖糖型的葡萄糖脑苷脂酶的细胞株及其制备方法和应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7297680B2 (en) * | 1999-04-15 | 2007-11-20 | Crucell Holland B.V. | Compositions of erythropoietin isoforms comprising Lewis-X structures and high sialic acid content |
-
2009
- 2009-09-18 US US13/119,461 patent/US9012176B2/en active Active
- 2009-09-18 JP JP2011527782A patent/JP2012502654A/ja active Pending
- 2009-09-18 CN CN201410587557.XA patent/CN104450783B/zh active Active
- 2009-09-18 WO PCT/SG2009/000348 patent/WO2010033085A1/en active Application Filing
- 2009-09-18 CA CA2737748A patent/CA2737748A1/en not_active Abandoned
- 2009-09-18 CN CN200980146306.5A patent/CN102439140B/zh active Active
- 2009-09-18 KR KR20117007071A patent/KR20110060913A/ko not_active Application Discontinuation
- 2009-09-18 EP EP09814854.7A patent/EP2342320B1/en active Active
-
2015
- 2015-03-03 US US14/636,795 patent/US9273292B2/en active Active
Non-Patent Citations (8)
| Title |
|---|
| JPN6014006592; Biochim. Biophys. Acta Vol. 1425, 1998, p. 441-452 * |
| JPN6014006593; Proc. Natl. Acad. Sci. USA. Vol. 101, No. 52, 2004, p. 18153-18158 * |
| JPN6014006594; J. Biol. Chem. Vol. 277, No. 20, 2002, p. 18182-18190 * |
| JPN6014006595; Methods Enzymol. Vol. 416, 2006, p. 159-182 * |
| JPN6014006596; Glycobiology Vol. 13, No. 1, 2003, p. 43-50 * |
| JPN6014006597; J. Biol. Chem. Vol. 271, No. 44, 1996, p. 27818-27822 * |
| JPN6014006598; Biochemistry Vol. 40, 2001, p. 8765-8772 * |
| JPN6014006599; J. Biol. Chem. Vol. 252, No. 3, 1977, p. 1107-1116 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2342320A1 (en) | 2011-07-13 |
| US9012176B2 (en) | 2015-04-21 |
| KR20110060913A (ko) | 2011-06-08 |
| US20150184135A1 (en) | 2015-07-02 |
| WO2010033085A1 (en) | 2010-03-25 |
| EP2342320A4 (en) | 2012-12-12 |
| US20110177555A1 (en) | 2011-07-21 |
| EP2342320B1 (en) | 2014-11-26 |
| CN104450783A (zh) | 2015-03-25 |
| CN102439140A (zh) | 2012-05-02 |
| CN102439140B (zh) | 2014-12-03 |
| CA2737748A1 (en) | 2010-03-25 |
| CN104450783B (zh) | 2018-08-31 |
| US9273292B2 (en) | 2016-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9273292B2 (en) | Chinese hamster ovary cell lines | |
| Shimozawa et al. | Identification of a new complementation group of the peroxisome biogenesis disorders and PEX14 as the mutated gene | |
| EP1210418A1 (en) | Secreted and transmembrane polypeptides and nucleic acids encoding the same | |
| EP3365452B1 (en) | Expression in mammalian cells with gaussia luciferase signal peptide | |
| JP2004526412A (ja) | 分泌及び膜貫通ポリペプチドとそれをコードする核酸 | |
| CN1317010A (zh) | 编码与感觉转导有关的g-蛋白偶联受体的核酸 | |
| Ishida et al. | Identification and characterization of human Golgi nucleotide sugar transporter SLC35D2, a novel member of the SLC35 nucleotide sugar transporter family | |
| Oldstone et al. | Discriminated selection among viral peptides with the appropriate anchor residues: implications for the size of the cytotoxic T-lymphocyte repertoire and control of viral infection | |
| JP2001505783A (ja) | 分泌ヒトタンパク質 | |
| Pinello et al. | MAR1 links membrane adhesion to membrane merger during cell-cell fusion in Chlamydomonas | |
| Lim et al. | The Golgi CMP-sialic acid transporter: a new CHO mutant provides functional insights | |
| JP2013510574A (ja) | チャイニーズハムスターからのグリコシルトランスフェラーゼおよび関連方法 | |
| JPH0892285A (ja) | ヒトclap蛋白質およびそれをコードするdna | |
| KR20180120751A (ko) | 프레닐화 검정 | |
| US7888117B2 (en) | Human OCT-2 variant peptide chains, nucleic acids, and methods | |
| EP2023962B1 (en) | Human oct-2 variant peptide chains, nucleic acids, and methods | |
| WO1997045535A1 (en) | Recombinant rna 3'-terminal phosphate cyclases and production methods thereof | |
| WO2020116602A1 (ja) | 可溶型mhcクラスii分子の産生誘導組成物、キット、産生細胞および製造方法 | |
| EP2385131A1 (en) | The use of a genetically modified cell line expressing functional asialoglycoprotein receptor in the production of highly sialylated glycoproteins | |
| CA2585822A1 (en) | Breast, rectal, colon and lung tumour marker pro19628 polypeptide and encoding nucleic acid | |
| EP1439228B1 (en) | Sodium-independent transporter transporting small-sized neutral amino acid, gene thereof and method of analyzing transporter function by constructing fused proteins enabling the specification of the function | |
| AU2003204357B2 (en) | Further pro polypeptides and sequences thereof | |
| JP2001503994A (ja) | チロシンリン酸化切断溝関連タンパク質(pstpip) | |
| US20050196797A1 (en) | SMG-1 binding protein and screening method for substances that can regulate the activity thereof | |
| WO2004024913A1 (ja) | 新規タンパク質及びそれをコードするdna |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120801 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140214 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140711 |