JP2012194292A - フォトレジスト組成物 - Google Patents
フォトレジスト組成物 Download PDFInfo
- Publication number
- JP2012194292A JP2012194292A JP2011057313A JP2011057313A JP2012194292A JP 2012194292 A JP2012194292 A JP 2012194292A JP 2011057313 A JP2011057313 A JP 2011057313A JP 2011057313 A JP2011057313 A JP 2011057313A JP 2012194292 A JP2012194292 A JP 2012194292A
- Authority
- JP
- Japan
- Prior art keywords
- group
- carbon atoms
- represented
- hydrocarbon group
- examples
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Abstract
Description
本発明は、フォトレジスト組成物に関する。
化学増幅型のフォトレジスト組成物は、KrFエキシマレーザーやArFエキシマレーザーに代表される遠紫外光等の照射により露光部に酸を生成させ、この酸を触媒とする反応により、露光部と未露光部の現像液に対する溶解速度を変化させ、基板上にレジストパターンを形成させる組成物である(特開昭59−45439号公報参照)。
このような化学増幅型のフォトレジスト組成物に含有される酸発生剤には、露光光に対する透明性に優れると共に、発生する酸の強さ、沸点及びレジスト膜中の拡散距離(以下、「拡散長」ともいう。)が適切であること等の特性が求められる。
上述の特性のうち、適切な酸の強さ、沸点及び拡散長を発揮するためには、イオン性の酸発生剤ではアニオン部分の構造が重要である。例えば、トリフルオロメタンスルホニル構造を有する酸発生剤は、発生する酸が十分強い酸となり、フォトレジストとしての解像性能が高いという特徴がある。また、10−カンファースルホニル構造のような大きな有機基に結合したスルホニル構造を有する酸発生剤は、発生する酸の沸点が十分高いという特徴があるが、有機溶媒の種類によっては溶解性が低いという不都合がある。
一方、より精密な線幅制御を行う場合、例えば、デバイスの設計寸法がサブハーフミクロン以下であるような場合には、上記フォトレジスト組成物には、解像性能が優れているだけでなく、レジストパターン形成後のパターン表面の平滑性に優れていること、すなわち、ナノエッジラフネスの発生が抑制できること、さらには焦点深度(DOF:Depth of Focus)が広いことも要求される。パターン表面の凹凸形状(ナノエッジラフネス)は、その後のエッチング等の処理により被加工基板にレジストパターンを転写する際に基板に転写され、その結果として、被加工基板のパターンの寸法精度が低下してしまうという不都合がある。そこで、上述のような酸発生剤を種々調整することが検討されている。しかし、未だ上記要求を満たすことはできておらず、ナノエッジラフネスの発生を抑制できると共に広い焦点深度を発揮するフォトレジスト組成物が求められている。
本発明は、以上のような事情に基づいてなされたものであり、その目的は、ナノエッジラフネス抑制性及び焦点深度に優れるフォトレジスト組成物を提供することである。
上記課題を解決するためになされた発明は、
[A]下記式(1−1)で表される構造単位(I)を有する重合体(以下、「[A]重合体」ともいう。)、及び
[B]下記式(2)で表される酸発生剤(以下、「[B]酸発生剤」ともいう。)
を含有するフォトレジスト組成物である。
(式(1−1)中、Rは、水素原子又はメチル基である。Raは、1価の有機基である。pは、0〜3の整数である。Raが複数ある場合、複数のRaは同一でも異なっていてもよい。qは、1〜3の整数である。但し、p及びqは、p+q≦5を満たす。)
(式(2)中、R1は、炭素数5〜20の鎖状炭化水素基、炭素数5〜20の脂環式炭化水素基又は炭素数6〜20の芳香族炭化水素基を含み、炭素数14以上の1価の有機基である。この鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。M+は、1価のオニウムカチオンである。)
[A]下記式(1−1)で表される構造単位(I)を有する重合体(以下、「[A]重合体」ともいう。)、及び
[B]下記式(2)で表される酸発生剤(以下、「[B]酸発生剤」ともいう。)
を含有するフォトレジスト組成物である。
本発明のフォトレジスト組成物は、フェノール性水酸基を有する[A]重合体及び[B]酸発生剤を含有し、この[B]酸発生剤が、上記特定範囲の炭素数を有する炭化水素基を含み、かつ構成炭素数が上記所定値以上であることで、ナノエッジラフネス抑制性及び焦点深度に優れる。当該フォトレジスト組成物が、上記構成を有することで、ナノエッジラフネス抑制性に優れる理由については必ずしも明らかではないが、例えば、[B]酸発生剤が、上記特定構造を有することで、発生する酸の嵩高さが増し、[A]重合体を含むレジスト膜中における酸拡散長が十分に短くなること等が考えられる。また、上記酸の酸拡散長が十分に短くなることで、パターン形成の精度が高まり、結果として、当該フォトレジスト組成物の焦点深度が広くなると考えられる。
上記鎖状炭化水素基が分岐状であることが好ましい。上記鎖状炭化水素基が分岐状であることで、[B]酸発生剤の嵩高さが増し、発生する酸の酸拡散長がより短くなると考えられ、その結果、当該フォトレジスト組成物のナノエッジラフネス抑制性及び焦点深度がより向上する。
上記R1が、少なくとも1つのエステル結合を有することが好ましい。上記R1が、少なくとも1つのエステル結合を有することで、[B]酸発生剤の溶媒への溶解性が高まると共に、嵩高い基を有する[B]酸発生剤とフェノール性水酸基を有する[A]重合体との相溶性が増し、レジスト膜中の[B]酸発生剤の分散性が向上し、その結果、当該フォトレジスト組成物のナノエッジラフネス抑制性及び焦点深度がさらに向上する。また、上記R1がエステル結合を有することで、比較的炭素数の多い[B]酸発生剤の合成が容易になる。
上記R1が、下記式(2−1a)で表される有機基であることが好ましい。
(式(2−1a)中、R2及びR3は、それぞれ独立して、少なくとも1つのエステル結合を有し、かつ炭素数5〜20の鎖状炭化水素基、炭素数5〜20の脂環式炭化水素基又は炭素数6〜20の芳香族炭化水素基を含む1価の有機基である。この鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。)
[B]酸発生剤は上記特定の有機基を有することで、嵩高さがさらに高まり、発生する酸の拡散長がさらに短くなると考えられ、その結果、当該フォトレジスト組成物のナノエッジラフネス抑制性及び焦点深度がさらに向上する。
[A]重合体が、下記式(1−2)で表される構造単位(II)をさらに有することが好ましい。
(式(1−2)中、R’は、水素原子又はメチル基である。Rbは、1価の炭化水素基又は酸解離性基を含まない1価のオキシ炭化水素基である。rは、0〜5の整数である。Rbが複数ある場合、複数のRbは同一でも異なっていてもよい。)
当該フォトレジスト組成物は、[A]重合体が構造単位(II)をさらに有することで、ナノエッジラフネス抑制性及び焦点深度がさらに向上する。
[A]重合体が、下記式(1−3)で表される構造単位(III)をさらに有することが好ましい。
(式(1−3)中、R”は、水素原子又はメチル基である。Rcは、酸解離性基を含まない1価の有機基である。sは、0〜3の整数である。Rdは、1価の酸解離性基である。tは、1〜3の整数である。Rc及びRdがそれぞれ複数ある場合、複数のRc及びRdはそれぞれ同一でも異なっていてもよい。但し、s及びtは、s+t≦5を満たす。)
[A]重合体が、酸解離性基を含む構造単位としての構造単位(III)をさらに有することで、当該フォトレジスト組成物は、ポジ型のレジストパターン形成能を向上させることができる。
当該フォトレジスト組成物は、上述の特性を有しているので、ポジ型のフォトレジスト組成物として好適に用いることができ、ナノエッジラフネス抑制性及び焦点深度に優れるポジ型のレジストパターンを形成することができる。
また、当該フォトレジスト組成物は、上述の特性を有しているので、[E]架橋剤をさらに含有することで、ネガ型のフォトレジスト組成物として好適に用いることができ、ナノエッジラフネス抑制性及び焦点深度に優れるネガ型のレジストパターンを形成することができる。
本明細書において、「鎖状炭化水素基」とは、環状構造を含まず、鎖状構造のみで構成された炭化水素基を意味し、直鎖状炭化水素基及び分岐状炭化水素基の双方を含むものとする。「脂環式炭化水素基」とは、環構造としては脂環式構造のみを含み、芳香環構造を含まない炭化水素基を意味する。但し、脂肪族環状炭化水素の構造のみで構成されている必要はなく、その一部に鎖状構造を含んでいてもよい。「芳香族炭化水素基」とは、環構造として、芳香環構造を含む炭化水素基を意味する。但し、芳香環構造のみで構成されている必要はなく、その一部に鎖状構造や脂環式構造を含んでいてもよい。単に「炭化水素基」という場合には、上記鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基が含まれる。
本発明のフォトレジスト組成物によれば、ナノエッジラフネスの発生が抑制されたレジストパターンを形成することができ、また広い焦点深度を発揮することができる。
<フォトレジスト組成物>
当該フォトレジスト組成物は、[A]重合体及び[B]酸発生剤を含有する。また、本発明の効果を損なわない範囲において、任意成分を含有していてもよい。
当該フォトレジスト組成物は、[A]重合体及び[B]酸発生剤を含有する。また、本発明の効果を損なわない範囲において、任意成分を含有していてもよい。
当該フォトレジスト組成物は、ポジ型のフォトレジスト組成物としても、ネガ型のフォトレジスト組成物としても用いることができる。ポジ型のフォトレジスト組成物とする場合には、上記[A]重合体が酸解離性基を含む構造単位を有することが好ましい。当該フォトレジスト組成物は、[A]重合体が酸解離性基を含む構造単位を有すると、[B]酸発生剤から発生する酸により、露光部における酸解離性基が解離して極性基を生じ、現像液に可溶となり、ポジ型のレジストパターンを効果的に形成することができる。ここで、「酸解離性基」とは、例えば、ヒドロキシル基、カルボキシル基等の極性基の水素原子を置換する基であって、酸の存在下で解離する基をいう。かかる酸解離性基を含む構造単位としては、例えば後述する構造単位(III)、構造単位(IV)等が挙げられる。
一方、ネガ型のフォトレジスト組成物とする場合には、当該フォトレジスト組成物は、後述する[E]架橋剤をさらに含有することが好ましい。当該フォトレジスト組成物が[E]架橋剤を含有することで、上記[B]酸発生剤等から発生する酸により、露光部において、フェノール構造を有する[A]重合体の架橋反応が進行し、現像液に不溶又は難溶となって残存し、ネガ型のレジストパターンを効果的に形成することができる。以下、各構成成分について説明する。
<[A]重合体>
[A]重合体は、上記式(1−1)で表される構造単位(I)を有する重合体である。当該フォトレジスト組成物は、[B]酸発生剤から発生する酸の作用により、露光部における[A]重合体の現像液に対する溶解性が変化することで、レジストパターンを形成することができる。
[A]重合体は、上記式(1−1)で表される構造単位(I)を有する重合体である。当該フォトレジスト組成物は、[B]酸発生剤から発生する酸の作用により、露光部における[A]重合体の現像液に対する溶解性が変化することで、レジストパターンを形成することができる。
[構造単位(I)]
構造単位(I)は、上記式(1−1)で表される構造単位である。[A]重合体が構造単位(I)を有することで、ポジ型のフォトレジスト組成物においては、現像液に対する溶解性を調整することにより、ネガ型のフォトレジスト組成物においては、露光部における架橋反応を効率的に進行させることにより、当該フォトレジスト組成物は優れた解像性を発揮することができる。また、レジストパターンの基板への密着性を向上させることができる。
構造単位(I)は、上記式(1−1)で表される構造単位である。[A]重合体が構造単位(I)を有することで、ポジ型のフォトレジスト組成物においては、現像液に対する溶解性を調整することにより、ネガ型のフォトレジスト組成物においては、露光部における架橋反応を効率的に進行させることにより、当該フォトレジスト組成物は優れた解像性を発揮することができる。また、レジストパターンの基板への密着性を向上させることができる。
上記式(1)中、Rは、水素原子又はメチル基である。Raは、1価の有機基である。pは、0〜3の整数である。Raが複数ある場合、複数のRaは同一でも異なっていてもよい。qは、1〜3の整数である。但し、p及びqは、p+q≦5を満たす。
上記Rとしては、水素原子が好ましい。
上記Raで表される1価の有機基としては、例えば、炭素数1〜12の1価の鎖状炭化水素基、炭素数3〜20の1価の脂環式炭化水素基、炭素数6〜20の1価の芳香族炭化水素基、1価の酸素原子含有有機基、1価の窒素原子含有有機基等が上げられる。
上記1価の鎖状炭化水素基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、2−メチルプロピル基、1−メチルプロピル基、t−ブチル基、n−ペンチル基、n−ヘキシル基、n−デシル基等が挙げられる。
上記1価の脂環式炭化水素基としては、例えば、シクロペンチル基、シクロヘキシル基、シクロオクチル基、ノルボルニル基、アダマンチル基等が挙げられる。
上記1価の芳香族炭化水素基としては、例えば、フェニル基、o−トリル基、m−トリル基、p−トリル基、2,4−キシリル基、2,6−キシリル基、3,5−キシリル基、メシチル基、o−クメニル基、m−クメニル基、p−クメニル基、ベンジル基、フェネチル基、1−ナフチル基、2−ナフチル基等が挙げられる。
上記1価の酸素原子含有有機基としては、例えば、
カルボキシル基;
ヒドロキシメチル基、1−ヒドロキシエチル基、2−ヒドロキシエチル基、1−ヒドロキシプロピル基、2−ヒドロキシプロピル基、3−ヒドロキシプロピル基、1−ヒドロキシブチル基、2−ヒドロキシブチル基、3−ヒドロキシブチル基、4−ヒドロキシブチル基等の炭素数1〜8の直鎖状又は分岐状のヒドロキシアルキル基;
3−ヒドロキシシクロペンチル基、4−ヒドロキシシクロヘキシル基等の炭素数3〜8のヒドロキシシクロアルキル基;
メトキシ基、エトキシ基、n−プロポキシ基、i−プロポキシ基、n−ブトキシ基、2−メチルプロポキシ基、1−メチルプロポキシ基、t−ブトキシ基等の炭素数1〜8の直鎖状又は分岐状のアルコキシ基;
シクロペンチルオキシ基、シクロヘキシルオキシ基等のシクロアルキルオキシ基;
カルボキシル基;
ヒドロキシメチル基、1−ヒドロキシエチル基、2−ヒドロキシエチル基、1−ヒドロキシプロピル基、2−ヒドロキシプロピル基、3−ヒドロキシプロピル基、1−ヒドロキシブチル基、2−ヒドロキシブチル基、3−ヒドロキシブチル基、4−ヒドロキシブチル基等の炭素数1〜8の直鎖状又は分岐状のヒドロキシアルキル基;
3−ヒドロキシシクロペンチル基、4−ヒドロキシシクロヘキシル基等の炭素数3〜8のヒドロキシシクロアルキル基;
メトキシ基、エトキシ基、n−プロポキシ基、i−プロポキシ基、n−ブトキシ基、2−メチルプロポキシ基、1−メチルプロポキシ基、t−ブトキシ基等の炭素数1〜8の直鎖状又は分岐状のアルコキシ基;
シクロペンチルオキシ基、シクロヘキシルオキシ基等のシクロアルキルオキシ基;
メトキシカルボニルオキシ基、エトキシカルボニルオキシ基、n−プロポキシカルボニルオキシ基、n−ブトキシカルボニルオキシ基等の炭素数2〜9の直鎖状のアルコキシカルボニルオキシ基;
(1−メトキシエトキシ)メチル基、(1−エトキシエトキシ)メチル基、(1−n−プロポキシエトキシ)メチル基、(1−n−ブトキシエトキシ)メチル基、(1−メトキシプロポキシ)メチル基、(1−エトキシプロポキシ)メチル基等の炭素数3〜11の直鎖状又は分岐状の(1−アルコキシアルコキシ)アルキル基;
(1−シクロペンチルオキシエトキシ)メチル基、(1−シクロヘキシルオキシエトキシ)メチル基等の炭素数5〜11の(1−シクロアルキルオキシアルコキシ)アルキル基;
(1−メトキシエトキシ)メチル基、(1−エトキシエトキシ)メチル基、(1−n−プロポキシエトキシ)メチル基、(1−n−ブトキシエトキシ)メチル基、(1−メトキシプロポキシ)メチル基、(1−エトキシプロポキシ)メチル基等の炭素数3〜11の直鎖状又は分岐状の(1−アルコキシアルコキシ)アルキル基;
(1−シクロペンチルオキシエトキシ)メチル基、(1−シクロヘキシルオキシエトキシ)メチル基等の炭素数5〜11の(1−シクロアルキルオキシアルコキシ)アルキル基;
メトキシカルボニルオキシメチル基、エトキシカルボニルオキシメチル基、n−プロポキシカルボニルオキシメチル基、i−プロポキシカルボニルオキシメチル基、n−ブトキシカルボニルオキシメチル基、t−ブトキシカルボニルオキシメチル基等の炭素数3〜10の直鎖状又は分岐状のアルコキシカルボニルオキシアルキル基;
シクロペンチルオキシカルボニルオキシメチル基、シクロヘキシルオキカルボニルオキシメチル基等の炭素数5〜10のシクロアルキルオキシカルボニルオキシアルキル基等が挙げられる。
シクロペンチルオキシカルボニルオキシメチル基、シクロヘキシルオキカルボニルオキシメチル基等の炭素数5〜10のシクロアルキルオキシカルボニルオキシアルキル基等が挙げられる。
上記1価の窒素原子含有有機基としては、例えば、
シアノ基;
シアノメチル基、1−シアノエチル基、2−シアノエチル基、1−シアノプロピル基、2−シアノプロピル基、3−シアノプロピル基、1−シアノブチル基、2−シアノブチル基、3−シアノブチル基、4−シアノブチル基等の炭素数2〜9の直鎖状又は分岐状のシアノアルキル基;
3−シアノシクロペンチル基、4−シアノシクロヘキシル基等の炭素数4〜9のシアノシクロアルキル基等が挙げられる。
シアノ基;
シアノメチル基、1−シアノエチル基、2−シアノエチル基、1−シアノプロピル基、2−シアノプロピル基、3−シアノプロピル基、1−シアノブチル基、2−シアノブチル基、3−シアノブチル基、4−シアノブチル基等の炭素数2〜9の直鎖状又は分岐状のシアノアルキル基;
3−シアノシクロペンチル基、4−シアノシクロヘキシル基等の炭素数4〜9のシアノシクロアルキル基等が挙げられる。
Raとしては、これらの中で、パターンの矩形性向上の観点から、1価の鎖状炭化水素基が好ましく、メチル基、エチル基、n−プロピル基及びi−プロピル基が好ましい。
上記pとしては、0〜2が好ましく、0又は1がより好ましく、0がさらに好ましい。上記qとしては、1又は2が好ましく、1がより好ましい。
上記構造単位(I)を与える単量体としては、例えば、2−ヒドロキシスチレン、3−ヒドロキシスチレン、4−ヒドロキシスチレン、2−ヒドロキシ−α−メチルスチレン、3−ヒドロキシ−α−メチルスチレン、4−ヒドロキシ−α−メチルスチレン、2−メチル−3−ヒドロキシスチレン、4−メチル−3−ヒドロキシスチレン、5−メチル−3−ヒドロキシスチレン、2−メチル−4−ヒドロキシスチレン、3−メチル−4−ヒドロキシスチレン、3,4−ジヒドロキシスチレン、2,4,6−トリヒドロキシスチレン等が挙げられる。この中で、得られる構造単位(I)のフェノール性水酸基の酸性度の観点から、4−ヒドロキシスチレン及び4−ヒドロキシ−α−メチルスチレンが好ましく、4−ヒドロキシスチレンがさらに好ましい。
上記構造単位(I)の含有割合としては、[A]重合体を構成する全構造単位に対して50〜90モル%が好ましく、60〜85モル%がより好ましく、65〜80モル%がさらに好ましい。構造単位(I)の含有割合が50モル%未満だと、レジストパターンの基板への密着性が低下するおそれがある。また、ネガ型のフォトレジスト組成物の場合には、パターン形成性が低下するおそれがある。逆に、含有割合が90モル%を超えると、現像後のコントラストが低下するおそれがある。[A]重合体は、構造単位(I)を1種又は2種以上有していてもよい。
[A]重合体は、上記構造単位(I)に加えて、上記構造単位(II)をさらに有することが好ましい。当該フォトレジスト組成物によれば、[A]重合体が構造単位(II)をさらに有することで、ナノエッジラフネス抑制性及び焦点深度が向上する。
[構造単位(II)]
構造単位(II)は、上記式(1−2)で表される構造単位である。
構造単位(II)は、上記式(1−2)で表される構造単位である。
上記式(1−2)中、R’は、水素原子又はメチル基である。Rbは、1価の炭化水素基又は酸解離性基を含まない1価のオキシ炭化水素基である。rは、0〜3の整数である。Rbが複数ある場合、複数のRbは同一でも異なっていてもよい。
上記R’としては、水素原子が好ましい。
上記Rbで表される1価の炭化水素基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、t−ブチル基等のアルキル基基;シクロペンチル基、シクロヘキシル基等のシクロアルキル基;フェニル基、ナフチル基、ベンジル基等の芳香族炭化水素基等が挙げられる。
上記Rbで表される酸解離性基を含まない1価のオキシ炭化水素基としては、例えば、メトキシ基、エトキシ基、n−プロポキシ基、i−プロポキシ基、n−ブトキシ基等の1級又は2級のアルコキシ基;シクロペンチルオキシ基、シクロヘキシルオキシ基等のシクロアルキルオキシ基;フェノキシ基、ベンジルオキシ基等のオキシ芳香族炭化水素基等が挙げられる。
上記Rbとしては、この中で、アルキル基及びアルコキシ基が好ましく、メチル基、エチル基、メトキシ基及びエトキシ基がより好ましく、メチル基及びメトキシ基がさらに好ましく、メチル基が特に好ましい。
上記rとしては、0〜2が好ましく、0又は1がより好ましく、0がさらに好ましい。
上記構造単位(II)を与える単量体としては、例えば、スチレン、α−メチルスチレン、2−メチルスチレン、3−メチルスチレン、4−メチルスチレン、2−メトキシスチレン、3−メトキシスチレン、4−メトキシスチレン等が挙げられる。この中で、スチレンが好ましい。
上記構造単位(II)の含有割合としては、ポジ型のフォトレジスト組成物の場合には、[A]重合体を構成する全構造単位に対して、20モル%以下が好ましく、1〜10モル%がより好ましく、2〜8モル%がさらに好ましい。構造単位(II)の含有割合が20モル%を超えると、レジスト膜の現像性が低下するおそれがある。また、ネガ型のフォトレジスト組成物の場合には、[A]重合体を構成する全構造単位に対して、0〜50モル%が好ましく、10〜40モル%がより好ましく、20〜35モル%がさらに好ましい。構造単位(II)の含有割合が50モル%を超えると、パターン形成性が低下するおそれがある。[A]重合体は、構造単位(II)を1種又は2種以上有していてもよい。
当該フォトレジスト組成物がポジ型の場合は、[A]重合体は、酸解離性基を含む構造単位としての構造単位(III)をさらに有することが好ましい。当該フォトレジスト組成物は、[A]重合体が、酸解離性基を含む構造単位として構造単位(III)を有することで、ナノエッジラフネス抑制性及び焦点深度にさらに優れるポジ型のレジストパターンを形成することができる。
[構造単位(III)]
構造単位(III)は、上記式(1−3)で表される構造単位である。
構造単位(III)は、上記式(1−3)で表される構造単位である。
上記式(1−3)中、R”は、水素原子又はメチル基である。Rcは、酸解離性基を含まない1価の有機基である。sは、0〜3の整数である。Rdは、1価の酸解離性基である。tは、1〜3の整数である。Rc及びRdがそれぞれ複数ある場合、複数のRc及びRdはそれぞれ同一でも異なっていてもよい。但し、s及びtは、s+t≦5を満たす。
上記R”としては、水素原子が好ましい。
上記Rcで表される酸解離性基を含まない1価の有機基の例としては、上記式(1−1)のRaで表される1価の有機基において、鎖状炭化水素基、脂環式炭化水素基、芳香族炭化水素基、1価の酸素原子含有有機基のうちのカルボキシル基、ヒドロキシアルキル基、ヒドロキシシクロアルキル基、アルコキシ基及びシクロアルキルオキシ基、並びに1価の窒素原子含有有機基についての例を挙げることができる。
上記Rdで表される1価の酸解離性基としては、例えば、
置換メチル基、1−置換エチル基、1−分岐アルキル基、トリオルガノシリル基、トリオルガノゲルミル基、アルコキシカルボニル基、アシル基、1価の環式酸解離性基等が挙げられる。
置換メチル基、1−置換エチル基、1−分岐アルキル基、トリオルガノシリル基、トリオルガノゲルミル基、アルコキシカルボニル基、アシル基、1価の環式酸解離性基等が挙げられる。
上記置換メチル基としては、例えば、メトキシメチル基、メチルチオメチル基、エトキシメチル基、エチルチオメチル基、メトキシエトキシメチル基、ベンジルオキシメチル基、ベンジルチオメチル基、フェナシル基、ブロモフェナシル基、メトキシフェナシル基、メチルチオフェナシル基、α−メチルフェナシル基、シクロプロピルメチル基、ベンジル基、ジフェニルメチル基、トリフェニルメチル基、ブロモベンジル基、ニトロベンジル基、メトキシベンジル基、メチルチオベンジル基、エトキシベンジル基、エチルチオベンジル基、ピペロニル基、メトキシカルボニルメチル基、エトキシカルボニルメチル基、n−プロポキシカルボニルメチル基、i−プロポキシカルボニルメチル基、n−ブトキシカルボニルメチル基、t−ブトキシカルボニルメチル基等が挙げられる。
上記1−置換エチル基としては、例えば、1−メトキシエチル基、1−メチルチオエチル基、1,1−ジメトキシエチル基、1−エトキシエチル基、1−エチルチオエチル基、1,1−ジエトキシエチル基、1−プロポキシエチル基、1−シクロヘキシルオキシエチル基、1−フェノキシエチル基、1−フェニルチオエチル基、1,1−ジフェノキシエチル基、1−ベンジルオキシエチル基、1−ベンジルチオエチル基、1−シクロプロピルエチル基、1−フェニルエチル基、1,1−ジフェニルエチル基、1−メトキシカルボニルエチル基、1−エトキシカルボニルエチル基、1−n−プロポキシカルボニルエチル基、1−イソプロポキシカルボニルエチル基、1−n−ブトキシカルボニルエチル基、1−t−ブトキシカルボニルエチル基等が挙げられる。
上記1−分岐アルキル基としては、例えば、i−プロピル基、sec−ブチル基、t−ブチル基、1,1−ジメチルプロピル基、1−メチルブチル基、1,1−ジメチルブチル基等が挙げられる。
上記トリオルガノシリル基としては、例えば、トリメチルシリル基、エチルジメチルシリル基、ジエチルメチルシリル基、トリエチルシリル基、ジメチルi−プロピルシリル基、メチルジ−i−プロピルシリル基、トリ−i−プロピルシリル基、t−ブチルジメチルシリル基、ジ−t−ブチルメチルシリル基、トリ−t−ブチルシリル基、ジメチルフェニルシリル基、メチルジフェニルシリル基、トリフェニルシリル基等が挙げられる。
上記トリオルガノゲルミル基としては、例えば、トリメチルゲルミル基、エチルジメチルゲルミル基、ジエチルメチルゲルミル基、トリエチルゲルミル基、ジメチルi−プロピルゲルミル基、メチルジ−i−プロピルゲルミル基、トリ−i−プロピルゲルミル基、t−ブチルジメチルゲルミル基、ジ−t−ブチルメチルゲルミル基、トリ−t−ブチルゲルミル基、ジメチルフェニルゲルミル基、メチルジフェニルゲルミル基、トリフェニルゲルミル基等が挙げられる。
上記アルコキシカルボニル基としては、例えば、メトキシカルボニル基、エトキシカルボニル基、i−プロポキシカルボニル基、t−ブトキシカルボニル基等が挙げられる。
上記アシル基としては、例えば、アセチル基、プロピオニル基、ブチリル基、ヘプタノイル基、ヘキサノイル基、バレリル基、ピバロイル基、イソバレリル基、ラウロイル基、ミリストイル基、パルミトイル基、ステアロイル基、オキサリル基、マロニル基、スクシニル基、グルタリル基、アジポイル基、ピペロイル基、スベロイル基、アゼラオイル基、セバコイル基、アクリロイル基、プロピオロイル基、メタクリロイル基、クロトノイル基、オレオイル基、マレオイル基、フマロイル基、メサコノイル基、カンホロイル基、ベンゾイル基、フタロイル基、イソフタロイル基、テレフタロイル基、ナフトイル基、トルオイル基、ヒドロアトロポイル基、アトロポイル基、シンナモイル基、フロイル基、テノイル基、ニコチノイル基、イソニコチノイル基等が挙げられる。
上記1価の環式酸解離性基としては、例えば、シクロプロピル基、シクロペンチル基、シクロヘキシル基、シクロヘキセニル基、4−メトキシシクロヘキシル基、テトラヒドロフラニル基、テトラヒドロピラニル基、テトラヒドロチオフラニル基、テトラヒドロチオピラニル基、3−ブロモテトラヒドロピラニル基、4−メトキシテトラヒドロピラニル基、4−メトキシテトラヒドロチオピラニル基、3−テトラヒドロチオフェン−1,1−ジオキシド基等が挙げられる。
これらの中でも、t−ブチル基、ベンジル基、1−メトキシエチル基、1−エトキシエチル基、トリメチルシリル基、t−ブトキシカルボニル基、t−ブトキシカルボニルメチル基、テトラヒドロフラニル基、テトラヒドロピラニル基、テトラヒドロチオフラニル基及びテトラヒドロチオピラニル基が好ましく、t−ブチル基がさらに好ましい。
上記構造単位(III)を与える重合性不飽和化合物としては、例えば、4−t−ブトキシスチレン、4−t−ブトキシ−α−メチルスチレン、4−(2−エチル−2−プロポキシ)スチレン、4−(2−エチル−2−プロポキシ)−α−メチルスチレン、4−(1−エトキシエトキシ)スチレン、4−(1−エトキシエトキシ)−α−メチルスチレン、アセトキシスチレン等が挙げられる。この中で、4−t−ブトキシスチレンが好ましい。
上記構造単位(III)の含有割合としては、ポジ型のフォトレジスト組成物の場合、[A]重合体を構成する全構造単位に対して、15〜40モル%が好ましく、17〜35モル%がより好ましく、20〜30モル%がさらに好ましい。構造単位(III)の含有割合が15モル%未満だと、解像度が低下するおそれがある。逆に、含有割合が40モル%を超えると、レジストパターンの基板への密着性が低下するおそれがある。[A]重合体は、構造単位(III)を1種又は2種以上有していてもよい。
当該フォトレジスト組成物がポジ型である場合、[A]重合体は、酸解離性基を含む構造単位として、構造単位(IV)を有していてもよい。
[構造単位(IV)]
構造単位(IV)は、下記式(1−4)で表される構造単位である。
構造単位(IV)は、下記式(1−4)で表される構造単位である。
上記式(1−4)中、RAは、水素原子又はメチル基である。Reは、1価の酸解離性基である。
上記RAとしては、水素原子が好ましい。
上記Reで表される1価の酸解離性基としては、例えば、t−ブチル基、1−メチルシクロペンチル基、1−エチルシクロペンチル基、2−メチルアダマンチル基、2−エチルアダマンチル基等が挙げられる。
上記構造単位(IV)を与える単量体としては、例えば、(メタ)アクリル酸t−ブチル、(メタ)アクリル酸1−メチルシクロペンチル、(メタ)アクリル酸1−エチルシクロペンチル、(メタ)アクリル酸2−メチルアダマンチル、(メタ)アクリル酸2−エチルアダマンチル等が挙げられる。
上記構造単位(IV)の含有割合としては、ポジ型のフォトレジスト組成物の場合、[A]重合体を構成する全構造単位に対して、10〜40モル%が好ましく、10〜30モル%がさらに好ましい。構造単位(IV)の含有割合が10モル%未満だと、解像度が低下する場合がある。逆に、含有割合が40モル%を超えると、ドライエッチング耐性が不十分となる場合がある。[A]重合体は、構造単位(IV)を1種又は2種以上有していてもよい。
また、[A]重合体は、分子鎖間で2価の酸解離性基を介する架橋構造を形成する下記式(1−4−a)で表される構造単位(IV−a)を有することが好ましい。[A]重合体が構造単位(IV−a)を有することで、レジスト膜の現像において、極性基の生成と共に、[A]重合体の分子量が低下するため、ポジ型のフォトレジスト組成物の場合、コントラストを向上させることができる。
上記式(1−4−a)中、RB及びRB’は、それぞれ独立して、水素原子又はメチル基である。Rfは、2価の酸解離性基である。
上記RB及びRB’としては、水素原子が好ましい。
上記Rfで表される2価の酸解離性基としては、例えば、1,1,3,3−テトラメチルプロパンジイル基、1,1,4,4−テトラメチルブタンジイル基、1,1,5,5−テトラメチルペンタンジイル基等が挙げられる。この中で、1,1,4,4−テトラメチルブタンジイル基が好ましい。
上記構造単位(IV−a)を与える単量体としては、例えば、2,4−ジメチルペンタン−2,4−ジアクリレート、2,5−ジメチルヘキサン−2,5−ジアクリレート、2,6−ジメチルヘプタン−2,6−ジアクリレート等が挙げられる。この中で、2,5−ジメチルヘキサン−2,5−ジアクリレートがより好ましい。
上記構造単位(IV−a)の含有割合としては、ポジ型のフォトレジスト組成物の場合、[A]重合体を構成する全構造単位に対して、10モル%以下が好ましく、1〜5モル%がさらに好ましい。構造単位(IV−a)の含有割合が10モル%を超えると、当該フォトレジスト組成物のパターン形成性が低下する場合がある。[A]重合体は、構造単位(IV−a)を1種又は2種以上有していてもよい。
[その他の構造単位]
[A]重合体は、上記構造単位(I)〜(IV)以外にもその他の構造単位を有していてもよい。その他の構造単位としては、例えば、下記単量体に由来する構造単位(V)が挙げられる。
[A]重合体は、上記構造単位(I)〜(IV)以外にもその他の構造単位を有していてもよい。その他の構造単位としては、例えば、下記単量体に由来する構造単位(V)が挙げられる。
(メタ)アクリル酸メチル、(メタ)アクリル酸エチル、(メタ)アクリル酸n−プロピル、(メタ)アクリル酸i−プロピル、(メタ)アクリル酸n−ブチル、(メタ)アクリル酸2−メチルプロピル、(メタ)アクリル酸1−メチルプロピル、(メタ)アクリル酸n−ペンチル、(メタ)アクリル酸ネオペンチル、(メタ)アクリル酸n−ヘキシル、(メタ)アクリル酸2−エチルヘキシル、(メタ)アクリル酸2−ヒドロキシエチル、(メタ)アクリル酸2−ヒドロキシ−n−プロピル、(メタ)アクリル酸3−ヒドロキシ−n−プロピル、(メタ)アクリル酸フェニル、(メタ)アクリル酸ベンジル、(メタ)アクリル酸1−メチル−2−アダマンチル、(メタ)アクリル酸1−エチル−2−アダマンチル、(メタ)アクリル酸8−メチル−8−トリシクロデシル、(メタ)アクリル酸8−エチル−8−トリシクロデシル、(メタ)アクリル酸3−メチル−3−テトラシクロドデセニル、(メタ)アクリル酸3−エチル−3−テトラシクロドデセニル、2,5−ジメチルヘキサン−2,5−ジ(メタ)アクリレート等の(メタ)アクリル酸エステル類;
(メタ)アクリル酸、クロトン酸、マレイン酸、無水マレイン酸、フマル酸、けい皮酸等の不飽和カルボン酸(無水物)類;
(メタ)アクリル酸2−カルボキシエチル、(メタ)アクリル酸2−カルボキシ−n−プロピル、(メタ)アクリル酸3−カルボキシ−n−プロピル等の不飽和カルボン酸のカルボキシアルキルエステル類;
(メタ)アクリロニトリル、α−クロロアクリロニトリル、クロトンニトリル、マレインニトリル、フマロニトリル等の不飽和ニトリル化合物;
(メタ)アクリル酸2−カルボキシエチル、(メタ)アクリル酸2−カルボキシ−n−プロピル、(メタ)アクリル酸3−カルボキシ−n−プロピル等の不飽和カルボン酸のカルボキシアルキルエステル類;
(メタ)アクリロニトリル、α−クロロアクリロニトリル、クロトンニトリル、マレインニトリル、フマロニトリル等の不飽和ニトリル化合物;
(メタ)アクリルアミド、N,N−ジメチル(メタ)アクリルアミド、クロトンアミド、マレインアミド、フマルアミド等の不飽和アミド化合物;
マレイミド、N−フェニルマレイミド、N−シクロヘキシルマレイミド等の不飽和イミド化合物;N−ビニル−ε−カプロラクタム、N−ビニルピロリドン、2−ビニルピリジン、3−ビニルピリジン、4−ビニルピリジン、2−ビニルイミダゾール、4−ビニルイミダゾール等の含窒素ビニル化合物等。
マレイミド、N−フェニルマレイミド、N−シクロヘキシルマレイミド等の不飽和イミド化合物;N−ビニル−ε−カプロラクタム、N−ビニルピロリドン、2−ビニルピリジン、3−ビニルピリジン、4−ビニルピリジン、2−ビニルイミダゾール、4−ビニルイミダゾール等の含窒素ビニル化合物等。
上記構造単位(V)の含有割合としては、[A]重合体を構成する全構造単位に対して、通常、25モル%以下であり、15モル%以下が好ましい。構造単位(V)の含有割合が25モル%を超えると、解像度が低下する場合がある。[A]重合体は、構造単位(V)を1種又は2種以上有していてもよい。
[A]重合体の例としては、例えば、4−ヒドロキシスチレン/4−t−ブトキシスチレン共重合体、4−ヒドロキシスチレン/4−t−ブトキシスチレン/アクリル酸1−メチルシクロペンチル共重合体、4−ヒドロキシスチレン/4−t−ブトキシスチレン/アクリル酸1−エチルシクロペンチル共重合体、4−ヒドロキシスチレン/4−t−ブトキシスチレン/スチレン共重合体、4−ヒドロキシスチレン/アクリル酸t−ブチル/スチレン共重合体、4−ヒドロキシスチレン/アクリル酸1−メチルシクロペンチル/スチレン共重合体、4−ヒドロキシスチレン/アクリル酸1−エチルシクロペンチル/スチレン共重合体、4−ヒドロキシスチレン/4−t−ブトキシスチレン/2,5−ジメチルヘキサン−2,5−ジアクリレート共重合体、4−ヒドロキシスチレン/アクリル酸2−エチルアダマンチル/スチレン共重合体、4−ヒドロキシスチレン/アクリル酸2−エチルアダマンチル共重合体、4−ヒドロキシスチレン/4―(1−エトキシエトキシ)スチレン/4−tert−ブトキシスチレン共重合体、4−ヒドロキシスチレン/4―(1−エトキシエトキシ)スチレン共重合体、4−ヒドロキシスチレン/4―(1−エトキシエトキシ)スチレン/スチレン共重合体、4−ヒドロキシスチレン/4−t−ブトキシスチレン/N,N−ジメチルアクリルアミド共重合体等が挙げられる。この中で、4−ヒドロキシスチレン/4−t−ブトキシスチレン/スチレン共重合体、4−ヒドロキシスチレン/4−t−ブトキシスチレン/2,5−ジメチルヘキサン−2,5−ジアクリレート共重合体及び4−ヒドロキシスチレン/4−t−ブトキシスチレン/N,N−ジメチルアクリルアミド共重合体が好ましい。
<[A]重合体の合成方法>
[A]重合体を合成する方法は特に制限されず、従来公知の方法を用いることができる。例えば、(i)置換又は非置換ヒドロキシスチレンのフェノール性水酸基を保護基で保護した単量体、例えば、ブトキシカルボニルオキシスチレン、ブトキシスチレン、アセトキスチレン、テトラヒドロピラニルオキシスチレン等と、構造単位(I)以外の所定の構造単位に対応する単量体と共に付加重合させた後、酸触媒又は塩基性触媒を作用させることにより、保護基を加水分解して脱離させる方法;(ii)置換又は非置換ヒドロキシスチレンを、構造単位(I)以外の所定の構造単位に対応する単量体と共に付加重合させる方法等が挙げられる。この中で、[A]重合体を効率良く合成できる観点から、(i)の方法が好ましい。
[A]重合体を合成する方法は特に制限されず、従来公知の方法を用いることができる。例えば、(i)置換又は非置換ヒドロキシスチレンのフェノール性水酸基を保護基で保護した単量体、例えば、ブトキシカルボニルオキシスチレン、ブトキシスチレン、アセトキスチレン、テトラヒドロピラニルオキシスチレン等と、構造単位(I)以外の所定の構造単位に対応する単量体と共に付加重合させた後、酸触媒又は塩基性触媒を作用させることにより、保護基を加水分解して脱離させる方法;(ii)置換又は非置換ヒドロキシスチレンを、構造単位(I)以外の所定の構造単位に対応する単量体と共に付加重合させる方法等が挙げられる。この中で、[A]重合体を効率良く合成できる観点から、(i)の方法が好ましい。
上記付加重合としては、例えば、ラジカル重合、アニオン重合、カチオン重合、熱重合等が挙げられるが、アニオン重合又はカチオン重合が、得られる共重合体の分散度(Mw/Mn比)を小さくできる点で好ましい。
上記(i)の方法において加水分解反応に使用される酸触媒としては、例えば、塩酸、硫酸等の無機酸が挙げられる。また、塩基性触媒としては、例えば、トリアルキルアミン等の有機塩基、水酸化ナトリウム等の無機塩基等が挙げられる。
[A]重合体のゲルパーミエーションクロマトグラフィー(GPC)によるポリスチレン換算重量平均分子量(Mw)は特に限定されないが、1,000〜150,000が好ましく、3,000〜100,000がさらに好ましい。また、[A]重合体のMwとGPCによるポリスチレン換算数平均分子量(Mn)との比(Mw/Mn)は、通常、1〜5であり、好ましくは1〜3である。
当該フォトレジスト組成物における[A]重合体の含有量としては、全固形分([F]溶媒以外の成分の合計質量)に対して、通常、70質量%以上であり、80質量%が好ましい。[A]重合体は、1種又は2種以上を用いることができる。
<[B]酸発生剤>
[B]酸発生剤は、上記式(2)で表される酸発生剤である。当該フォトレジスト組成物は、上記[A]重合体に加え、[B]酸発生剤を含有することで、ナノエッジラフネス抑制性及び焦点深度に優れる。
[B]酸発生剤は、上記式(2)で表される酸発生剤である。当該フォトレジスト組成物は、上記[A]重合体に加え、[B]酸発生剤を含有することで、ナノエッジラフネス抑制性及び焦点深度に優れる。
上記式(2)中、R1は、炭素数5〜20の鎖状炭化水素基、炭素数5〜20の脂環式炭化水素基又は炭素数6〜20の芳香族炭化水素基を含み、炭素数14以上の1価の有機基である。この鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。M+は、1価のオニウムカチオンである。
[B]酸発生剤は、スルホネートアニオンにおけるR1で表される1価の有機基が、上記特定範囲の炭素数を有する炭化水素基を含むことに加えて、構成炭素数が14以上である。当該フォトレジスト組成物が、[B]酸発生剤を含有することで、ナノエッジラフネス抑制性に優れる理由については必ずしも明らかではないが、例えば、[B]酸発生剤が、上記特定の炭化水素基を含み、かつ構成炭素数が所定値以上であることで、発生する酸の嵩高さが増し、上記[A]重合体を含むレジスト膜中における酸拡散長が十分に短くなること等が考えられる。また、上記酸の酸拡散長が短くなることで、パターン形成の精度が高まり、結果として、当該フォトレジスト組成物の焦点深度が広くなること等が考えられる。
[B]酸発生剤のR1の炭素数が13以下である場合、又はR1が上記特定の炭化水素基を有さない場合は、得られるフォトレジスト組成物のナノエッジラフネスの発生を低減することが困難であり、また焦点深度も狭くなる。これについても、R1の炭素数が上記所定値より小さい場合、又はR1が上記特定の炭化水素基を有さない場合は、構成される酸発生剤の酸拡散長が十分短くならないためと考えられる。
R1で表される有機基の炭素数の下限としては、15が好ましく、16がより好ましく、18がさらに好ましい。一方、R1の炭素数の上限としては、30が好ましく、25がより好ましく、22がさらに好ましい。
上記R1に含まれる炭素数5〜20の鎖状炭化水素基、炭素数5〜20の脂環式炭化水素基及び炭素数6〜20の芳香族炭化水素基は1価であっても2価以上であってもよいが1価が好ましい。この中で、鎖状炭化水素基及び脂環式炭化水素基が好ましく、脂環式炭化水素基がより好ましい。
上記R1に含まれる炭素数5〜20の鎖状炭化水素基としては、例えば、n−ペンタン、n−ヘキサン、n−ヘプタン、n−オクタン、n−デカン、n−ドデカン、n−ヘキサデカン等の直鎖状炭化水素;
2−メチルブタン、2,2−ジメチルプロパン、2−メチルペンタン、3−メチルペンタン、2,2−ジメチルブタン、2,3−ジメチルブタン、2−エチルブタン、2−メチルヘキサン、3−メチルヘキサン、2,2−ジメチルヘキサン、2,3−ジメチルヘキサン、2,4−ジメチルヘキサン、2,5−ジメチルヘキサン、3,4−ジメチルヘキサン、3−エチルペンタン、2−メチルヘプタン、3−メチルヘプタン、4−メチルヘプタン、2,2−ジメチルヘプタン、2,3−ジメチルヘプタン、3,3−ジメチルヘプタン、4,4−ジメチルヘプタン、3−エチルヘキサン等の分岐状炭化水素の水素原子をm個除いたm価(mは1以上の整数である。)の鎖状炭化水素基等が挙げられる。
2−メチルブタン、2,2−ジメチルプロパン、2−メチルペンタン、3−メチルペンタン、2,2−ジメチルブタン、2,3−ジメチルブタン、2−エチルブタン、2−メチルヘキサン、3−メチルヘキサン、2,2−ジメチルヘキサン、2,3−ジメチルヘキサン、2,4−ジメチルヘキサン、2,5−ジメチルヘキサン、3,4−ジメチルヘキサン、3−エチルペンタン、2−メチルヘプタン、3−メチルヘプタン、4−メチルヘプタン、2,2−ジメチルヘプタン、2,3−ジメチルヘプタン、3,3−ジメチルヘプタン、4,4−ジメチルヘプタン、3−エチルヘキサン等の分岐状炭化水素の水素原子をm個除いたm価(mは1以上の整数である。)の鎖状炭化水素基等が挙げられる。
この中で、分岐状の鎖状炭化水素基が好ましい。ここで、「分岐状の鎖状炭化水素基」とは、直鎖状炭化水素の末端炭素原子のみに結合手を有する「直鎖状の鎖状炭化水素基」以外の鎖状炭化水素基を意味する。R1は分岐状の鎖状炭化水素基を含むことでより嵩高くなり、[B]酸発生剤から発生する酸の拡散長がより短くなると考えられ、当該フォトレジスト組成物のナノエッジラフネス抑制性及び焦点深度がより向上する。
1価の鎖状炭化水素基(mが1の場合)としては、例えば、直鎖状炭化水素基として、1−ペンチル基、1−ヘキシル基、1−オクチル基、1−デシル基等が挙げられ、分岐状炭化水素基として、2−ペンチル基、3−ペンチル基、2−メチル−1−ブチル基、3−メチル−1−ブチル基、2−ヘキシル基、3−ヘキシル基、2−メチル−1−ペンチル基、3−メチル−1−ペンチル基、2−オクチル基、3−オクチル基、4−オクチル基、2−メチル−1−ヘプチル基、3−メチル−1−ヘプチル基、2−エチル−1−ヘキシル基、3−エチル−1−ヘキシル基等が挙げられる。この中で、3−メチル−1−ペンチル基、2−オクチル基及び2−エチル−1−ヘキシル基が好ましく、2−エチル−1−ヘキシル基がより好ましい。
上記R1に含まれる炭素数5〜20の脂環式炭化水素基としては、例えば、シクロペンタン、シクロヘキサン、シクロオクタン、シクロデカン等の単環の脂環式炭化水素;ノルボルナン、アダマンタン、トリシクロデカン、テトラシクロドデカン等の多環の脂環式炭化水素の水素原子をm個除いたm価(mは1以上の整数である。)の脂環式炭化水素基等が挙げられる。
1価の脂環式炭化水素基(mが1の場合)としては、例えば、シクロペンチル基、シクロヘキシル基、シクロオクチル基、シクロデシル基等の単環の脂環式炭化水素基;ノルボルニル基、アダマンチル基等の多環の脂環式炭化水素基等が挙げられる。この中で、シクロペンチル基、シクロヘキシル基、ノルボルニル基及びアダマンチル基が好ましく、シクロヘキシル基及びノルボルニル基がより好ましい。
上記R1に含まれる炭素数6〜20の芳香族炭化水素構造としては、例えば、ベンゼン、ナフタレン、アントラセン、フェナンスレン、トルエン、キシレン、エチルベンゼン等の芳香族炭化水素の水素原子をm個除いたm価(mは1以上の整数である。)の芳香族炭化水素基等が挙げられる。
1価の芳香族炭化水素基(mが1の場合)としては、例えば、フェニル基、ナフチル基、アントラニル基等のアリール基;ベンジル基、フェニルエチル基、フェニルプロピル基等のアラルキル基等が挙げられる。この中で、アリール基が好ましく、フェニル基及びナフチル基がより好ましく、フェニル基がさらに好ましい。
上記R1に含まれる鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基が有していてもよい置換基としては、例えば、
ヒドロキシル基、アルコキシ基、アルキルカルボニル基、アルコキシカルボニル基、アルキルカルボニルオキシ基、チオール基、ハロゲン原子(フッ素原子、塩素原子、臭素原子、ヨウ素原子等)、ヘテロ原子(酸素原子、窒素原子、硫黄原子、リン原子、ケイ素原子等)を有する有機基等が挙げられる。また、上記置換基としては、同一炭素原子に結合する2つの水素原子を置換しカルボニル基を形成する酸素原子(=O)であってもよく、異なる炭素原子に結合する2つの水素原子を置換する2価の官能基であってもよい。この2価の官能基としては、例えば、置換によりラクトンを形成するエステル基、ラクタムを形成するアミド基、スルトンを形成するスルホニルオキシ基、環状ウレタンを形成するウレタン基、環状ウレアを形成するウレア基、環状カーボネートを形成するカーボネート基、環状スルフィドを形成するスルフィド基等が挙げられる。
ヒドロキシル基、アルコキシ基、アルキルカルボニル基、アルコキシカルボニル基、アルキルカルボニルオキシ基、チオール基、ハロゲン原子(フッ素原子、塩素原子、臭素原子、ヨウ素原子等)、ヘテロ原子(酸素原子、窒素原子、硫黄原子、リン原子、ケイ素原子等)を有する有機基等が挙げられる。また、上記置換基としては、同一炭素原子に結合する2つの水素原子を置換しカルボニル基を形成する酸素原子(=O)であってもよく、異なる炭素原子に結合する2つの水素原子を置換する2価の官能基であってもよい。この2価の官能基としては、例えば、置換によりラクトンを形成するエステル基、ラクタムを形成するアミド基、スルトンを形成するスルホニルオキシ基、環状ウレタンを形成するウレタン基、環状ウレアを形成するウレア基、環状カーボネートを形成するカーボネート基、環状スルフィドを形成するスルフィド基等が挙げられる。
上記R1で表される1価の有機基としては、少なくとも1つのエステル結合を有することが好ましい。上記R1が、少なくとも1つのエステル結合を有することで、[B]酸発生剤の溶媒への溶解性が高まると共に、嵩高い基を有する[B]酸発生剤とフェノール性水酸基を有する[A]重合体との相溶性が増し、レジスト膜中の[B]酸発生剤の分散性が向上し、その結果、当該フォトレジスト組成物のナノエッジラフネス抑制性及び焦点深度がさらに向上する。また、上記R1がエステル結合を有することで、比較的炭素数の多い[B]酸発生剤の合成が容易になる。このエステル結合には、ラクトン環を形成するエステル結合も含まれる。上記エステル結合の数は1つでもよく、2つ以上でもよいが、1つ又は2つが好ましく、2つがより好ましい。
上記R1の好ましい例として、上記式(2−1a)で表される有機基が挙げられる。
上記式(2−1a)中、R2及びR3は、それぞれ独立して、少なくとも1つのエステル結合を有し、かつ炭素数5〜20の鎖状炭化水素基、炭素数5〜20の脂環式炭化水素基又は炭素数6〜20の芳香族炭化水素基を含む1価の有機基である。この鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。
上記R2及びR3で表される1価の有機基に含まれる鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基、並びにこの鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基が有していてもよい置換基の例としては、上記R1におけるそれぞれの例が挙げられる。
上記R2及びR3でそれぞれ表される1価の有機基としては、下記式(2−1a−i)〜(2−1a−iv)で表される基が好ましい。
上記式(2−1a−ii)〜(2−1a−iv)中、X1、X2及びX3は、それぞれ独立して、単結合、炭素数1〜10のアルカンジイル基、炭素数3〜30の2価の脂環式炭化水素基又は炭素数6〜30の2価の芳香族炭化水素基である。
上記式(2−1a−i)中、Rxは、エステル結合を含む置換基を有する炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基又は炭素数6〜20の1価の芳香族炭化水素基である。
上記式(2−1a−ii)中、Ryは、炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基又は炭素数6〜20の1価の芳香族炭化水素基である。これらの鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。
上記式(2−1a−iii)中、Yは炭素数5〜10の3価の鎖状炭化水素基である。
上記式(2−1a−iv)中、Zは、メタンジイル基、エタンジイル基、酸素原子又は硫黄原子である。
上記式(2−1a−i)中、Rxは、エステル結合を含む置換基を有する炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基又は炭素数6〜20の1価の芳香族炭化水素基である。
上記式(2−1a−ii)中、Ryは、炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基又は炭素数6〜20の1価の芳香族炭化水素基である。これらの鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。
上記式(2−1a−iii)中、Yは炭素数5〜10の3価の鎖状炭化水素基である。
上記式(2−1a−iv)中、Zは、メタンジイル基、エタンジイル基、酸素原子又は硫黄原子である。
上記X1、X2及びX3で表される炭素数1〜10のアルカンジイル基としては、例えば、メタンジイル基、エタンジイル基、プロパンジイル基、ブタンジイル基、ヘキサンジイル基、オクタンジイル基等が挙げられる。
上記X1、X2及びX3で表される炭素数3〜30の2価の脂環式炭化水素基としては、例えば、シクロペンタンジイル基、シクロヘキサンジイル基、シクロオクタンジイル基、シクロデカンジイル基、シクロペンタンジイルメタンジイル基、シクロヘキサンジイルエタンジイル基等が挙げられる。
上記X1、X2及びX3で表される炭素数6〜30の2価の芳香族炭化水素基としては、例えば、ベンゼンジイル基、ナフタレンジイル基、アントラセンジイル基、ベンゼンジイルメタンジイル基、ナフタレンジイルエタンジイル基等が挙げられる。
上記Rxにおける炭素数5〜20の1価の鎖状炭化水素基、5〜20の1価の脂環式炭化水素基及び炭素数6〜20の1価の芳香族炭化水素基の例としては、上記式(2)のR1に含まれる各1価の炭化水素基(mが1の場合)の例が挙げられる。
上記Rxが有するエステル基を含む置換基としては、例えば、メトキシカルボニル基、エトキシカルボニル基等のアルコキシカルボニル基;シクロペンチルオキシカルボニル基、シクロヘキシルオキシカルボニル基等のシクロアルキルオキシカルボニル基;フェニルオキシカルボニル基、ナフチルオキシカルボニル基等のアリールオキシカルボニル基;メチルカルボニルオキシ基、エチルカルボニルオキシ基等のアルキルカルボニルオキシ基;シクロペンチルカルボニルオキシ基、シクロヘキシルカルボニルオキシ基等のシクロアルキルカルボニルオキシ基;フェニルカルボニルオキシ基、ナフチルカルボニルオキシ基等のアリールカルボニルオキシ基等が挙げられる。、
上記Ryで表される炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基及び炭素数6〜20の1価の芳香族炭化水素基、並びにこれらの炭化水素基が有していてもよい置換基の例としては、上記式(2)のR1におけるそれぞれの例が挙げられる。
上記Yで表される炭素数5〜10の3価の鎖状炭化水素基としては、例えば、ペンタントリイル基、ヘキサントリイル基、オクタントリイル基、デカントリイル基等が挙げられる。
上記Zとしては、メタンジイル基及び酸素原子が好ましく、メタンジイル基がより好ましい。
上記式(2−1a)で表される有機基としては、下記式(2−1−1a)で表される有機基が特に好ましい。
上記式(2−1−1a)中、R2A及びR3Aは、それぞれ独立して、炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基又は炭素数6〜20の1価の芳香族炭化水素基である。これらの鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。
上記R2A及びR3Aで表される炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基及び炭素数6〜20の1価の芳香族炭化水素基、並びにこれらの炭化水素基が有していてもよい置換基の例としては、上記式(2)のR1におけるそれぞれの例が挙げられる。
上記式(2−1−1a)で表される有機基を有する[B]酸発生剤の具体例としては、例えば、下記式で表される化合物等が挙げられる。
上記式中、M+は、1価のオニウムカチオンである。なお、M+で表される1価のオニウムカチオンについては後述する。
この中で、上記R2A及びR3Aが分岐状の炭化水素基、脂環式炭化水素基又はラクトン基である化合物が好ましく、R2A及びR3Aが、2−エチル−1−ヘキシル基、シクロヘキシル基又はノルボルナンラクトン基である化合物がさらに好ましい。
また、上記R1の他の好ましい例として、下記式(2−2a)で表される有機基が挙げられる。
上記式(2−2a)中、REは、それぞれ独立して、炭素数1〜30の1価の有機基である。nは1〜4の整数である。Tは、炭素数5〜20の(n+1)価の脂環式炭化水素基である。REが複数ある場合、複数のREはそれぞれ同一でも異なっていてもよい。但し、式(2−2a)で表される有機基を構成する炭素原子数は14以上である。
上記REで表される炭素数1〜30の1価の有機基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基等のアルキル基;シクロペンチル基、シクロヘキシル基等のシクロアルキル基;フェニル基、ナフチル基等のアリール基、ベンジル基、フェネチル基等のアラルキル基;メトキシ基、エトキシ基、n−プロポキシ基、i−プロポキシ基等のアルコキシ基;シクロペンチルオキシ基、シクロヘキシルオキシ基等のシクロアルキルオキシ基;フェノキシ基、ナフチルオキシ基等のアリールオキシ基;メトキシカルボニル基、エトキシカルボニル基、n−プロポキシカルボニル基等のアルコキシカルボニル基、シクロペンチルオキシカルボニル基、シクロヘキシルオキシカルボニル基等のシクロヘキシルオキシカルボニル基、フェノキシカルボニル基、ナフチルオキシカルボニル基等のアリールオキシカルボニル基等が挙げられる。
上記式(2−2a)で表される有機基の好ましい具体例としては、下記式(2−2a−A)及び(2−2a−B)で表される有機基が挙げられる。
上記式(2−2a−A)及び(2−2a−B)中、R4〜R7は、それぞれ独立して、炭素数1〜30の1価の有機基である。この有機基の水素原子の一部又は全部は置換されていてもよい。また、上記R4とR5及びR6とR7が互いに結合して環状構造を形成していてもよい。m1は、0又は1である。m2は、0〜2の整数である。但し、上記式(2−2a−A)及び(2−2a−B)で表される有機基を構成する炭素数は、それぞれ14以上である。
上記R4〜R7でそれぞれ表される1価の有機基の例としては、上記式(2−2a)のREで表される1価の有機基における例が挙げられる。
上記式(2−2a−A)で表される有機基としては、下記式(2−2−1a−A)で表される有機基が好ましく、上記式(2−2a−B)で表される有機基としては、下記式(2−2−1a−B)で表される有機基が好ましい。
上記式(2−2−1a−A)及び(2−2−1a−B)中、R4A、R5A、R6A及びR7Aは、それぞれ独立して、炭素数1〜20の1価の鎖状炭化水素基、炭素数3〜20の1価の脂環式炭化水素基、炭素数6〜20の1価の芳香族炭化水素基又は炭素数4〜20の1価の複素環基である。この鎖状炭化水素基、脂環式炭化水素基、芳香族炭化水素基及び複素環基の水素原子の一部又は全部は置換されていてもよい。
上記R4A、R5A、R6A及びR7Aで表される炭素数1〜20の1価の鎖状炭化水素基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、t−ブチル基、n−ペンチル基、i−ペンチル基、n−ヘキシル基、i−ヘキシル基、n−ヘプチル基、n−オクチル基、i−オクチル基、n−ノニル基、n−デシル基、2−エチルヘキシル基、及びn−ドデシル基等が挙げられる。
上記R4A、R5A、R6A及びR7Aで表される炭素数3〜20の1価の脂環式炭化水素基としては、例えば、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、ボルニル基、ノルボルニル基、アダマンチル基、カンファニル基等が挙げられる。
上記R4A、R5A、R6A及びR7Aで表されるす炭素数6〜20の1価の芳香族炭化水素基としては、例えば、フェニル基、1−ナフチル基、2−ナフチル基、1−アントリル基、及び1−フェナントリル基等が挙げられる。
上記R4A、R5A、R6A及びR7Aで表される炭素数4〜20の1価の複素環基としては、例えば、フリル基、チエニル基、ピラニル基、ピロリル基、チアントレニル基、ピラゾリル基、イソチアゾリル基、イソオキサゾリル基、ピラジニル基、ピリミジニル基、ピリダジニル基、単環式又は多環式ラクトンに由来する基等が挙げられる。
上記鎖状炭化水素基、脂環式炭化水素基、芳香族炭化水素基及び複素環基が有していてもよい置換基の例としては、上記式(2)のR1における置換基の例が挙げられる。
上記式(2−2a−A)及び(2−2a−B)でそれぞれ表される有機基を有する[B]酸発生剤の具体例としては、下記式で表される化合物が挙げられる。
上記式中、M+は、1価のオニウムカチオンである。
上記R1の他の好ましい例としては、下記式(2−3a)で表される有機基も挙げられる。
上記式(2−3a)中、R8は、炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基又は炭素数6〜20の1価の芳香族炭化水素基である。この鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。Aは、エステル基、アミド基、ウレタン基、ウレア基、カーボネート基又はスルフィド基である。R9はフッ素原子を有していてもよい炭素数1〜10のアルカンジイル基である。
上記R8で表される炭素数5〜20の1価の鎖状炭化水素基、炭素数5〜20の1価の脂環式炭化水素基、炭素数6〜20の1価の芳香族炭化水素基及びこれらの鎖状炭化水素基、脂環式炭化水素基及び芳香族炭化水素基が有していてもよい置換基の例としては、上記式(2)のR1におけるそれぞれの例が挙げられる。
上記Aとしては、エステル基及びアミド基が好ましく、エステル基がより好ましい。
上記R9で表されるフッ素原子を有していてもよい炭素数1〜10のアルカンジイル基としては、メタンジイル基、エタンジイル基、プロパンジイル基、ヘキサンジイル基等のアルカンジイル基;ジフルオロメタンジイル基、ジフルオロエタンジイル基、ジフルオロプロパンジイル基、テトラフルオロエタンジイル基、テトラフルオロプロパンジイル基、ヘキサフルオロプロパンジイル基、オクタフルオロブタンジイル基、パーフルオロオクタンジイル基等のフッ素化アルカンジイル基等が挙げられる。
上記式(2−3a)で表される有機基を有する[B]酸発生剤の具体例としては、例えば、下記式で表される化合物が挙げられる。
上記式中、M+は、1価のオニウムカチオンである。
上記R1の他の好ましい例として、下記式(2−4a)で表される有機基も挙げられる。
上記式(2−4a)中、R10は、1価の有機基である。R11は、2価の有機基である。但し、R10及びR11のいずれかは、炭素数5〜20の鎖状炭化水素基、炭素数5〜20の脂環式炭化水素基又は炭素数6〜20の芳香族炭化水素基を含む。E1及びE2は、それぞれ独立して、エステル基、アミド基、ウレタン基、ウレア基、カーボネート基又はスルフィド基である。R12は、フッ素原子を有していてもよい炭素数1〜10のアルカンジイル基である。
上記R10で表される1価の有機基の例としては、上記式(2−2a)のREで表される1価の有機基の例が挙げられる。また、上記R11で表される2価の有機基の例としては、上記1価の有機基から1個の水素原子を除いた基等が挙げられる。
E1及びE2としては、エステル基及びアミド基が好ましく、エステル基がより好ましい。
上記R12で表されるフッ素原子を有していてもよい炭素数1〜10のアルカンジイル基の例としては、上記R9と同じ例が挙げられる。
上記式(2−4a)で表される有機基を有する[B]酸発生剤の具体例としては、例えば、下記式で表される化合物が挙げられる。
上記式中、M+は、1価のオニウムカチオンである。
上記M+の1価のオニウムカチオンとしては、例えば、O、S、Se、N、P、As、Sb、Cl、Br、I等の原子を有するオニウムカチオンが挙げられる。これらの中でも、S及びIの各原子を有するオニウムカチオンが好ましい。
上記S原子を有するオニウムカチオン(スルホニウムカチオン)の例としては、例えば、下記式(2−A)で表されるカチオンが挙げられる。また、上記I原子を有するオニウムカチオン(ヨードニウムカチオン)の例としては、例えば、下記式(2−B)で表されるカチオンが挙げられる。
上記式(2−A)中、R13a、R13b及びR13cは、それぞれ独立して、炭素数1〜10の直鎖状若しくは分岐状のアルキル基、又は炭素数6〜18の芳香族炭化水素基である。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。また、R13a、R13b及びR13cのいずれか2つが互いに結合して、それらが結合する硫黄原子と共に環状構造を形成していてもよい。
上記式(2−B)中、R14a及びR14bは、それぞれ独立して、炭素数1〜10の直鎖状若しくは分岐状のアルキル基、又は炭素数6〜18の芳香族炭化水素基である。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。また、R14a及びR14bが互いに結合して、それらが結合するヨウ素原子と共に環状構造を形成していてもよい。
上記R13a、R13b、R13c、R14a及びR14bで表される炭素数1〜10の直鎖状若しくは分岐状のアルキル基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、t−ブチル基、n−ペンチル基、i−ペンチル基、n−ヘキシル基、i−ヘキシル基、n−ヘプチル基、n−オクチル基、i−オクチル基、n−ノニル基、n−デシル基、2−エチルヘキシル基等が挙げられる。
上記R13a、R13b、R13c、R14a及びR14bで表される炭素数6〜18の芳香族炭化水素基としては、例えば、フェニル基、1−ナフチル基、2−ナフチル基、1−アントリル基、1−フェナントリル基等が挙げられる。
また、上記アルキル基及び芳香族炭化水素基が有していてもよい置換基としては、上記式(2)のR1においける置換基の例を挙げることができる。
上記式(2−A)で表されるオニウムカチオンの中でも、下記式(2−A−1)又は(2−A−2)でそれぞれ表されるオニウムカチオンが好ましい。
上記式(2−A−1)中、R15a、R15b及びR15cは、それぞれ独立して、水素原子、炭素数1〜12の直鎖状若しくは分岐状のアルキル基、炭素数6〜12の芳香族炭化水素基、−OSO2−RG1、又は−SO2−RG2である。但し、R15a、R15b及びR15cのうちの2個以上が互いに結合して環を形成していてもよい。また、R15a、R15b及びR15cがそれぞれ複数存在する場合、複数のR15a、R15b及びR15cはそれぞれ同一でも異なっていてもよい。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。
RG1及びRG2は、それぞれ独立して、炭素数1〜12の直鎖状若しくは分岐状のアルキル基、炭素数5〜25の脂環式炭化水素基又は炭素数6〜12の芳香族炭化水素基である。上記アルキル基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。j1〜j3は、それぞれ独立して、0〜5の整数である。
RG1及びRG2は、それぞれ独立して、炭素数1〜12の直鎖状若しくは分岐状のアルキル基、炭素数5〜25の脂環式炭化水素基又は炭素数6〜12の芳香族炭化水素基である。上記アルキル基、脂環式炭化水素基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。j1〜j3は、それぞれ独立して、0〜5の整数である。
上記式(2−A−2)中、R16aは水素原子、炭素数1〜8の直鎖状若しくは分岐状のアルキル基、又は炭素数6〜8の芳香族炭化水素基である。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。但し、R16aが複数ある場合、複数のR16aはそれぞれ同一でも異なっていてもよく、複数のR16aが互いに結合して環を形成していてもよい。
R16bは、水素原子、炭素数1〜7の直鎖状若しくは分岐状のアルキル基、又は炭素数6〜7の芳香族炭化水素基である。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。但し、R16bが複数ある場合、複数のR16bはそれぞれは同一でも異なっていてもよく、複数のR16bが互いに結合して環を形成していてもよい。j4は、0〜7の整数である。j5は、0〜6の整数である。j6は、0〜3の整数である。
R16bは、水素原子、炭素数1〜7の直鎖状若しくは分岐状のアルキル基、又は炭素数6〜7の芳香族炭化水素基である。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。但し、R16bが複数ある場合、複数のR16bはそれぞれは同一でも異なっていてもよく、複数のR16bが互いに結合して環を形成していてもよい。j4は、0〜7の整数である。j5は、0〜6の整数である。j6は、0〜3の整数である。
上記R15a、R15b及びR15cで表される炭素数1〜12の直鎖状若しくは分岐状のアルキル基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、t−ブチル基、n−ペンチル基、i−ペンチル基、n−ヘキシル基、i−ヘキシル基、n−ヘプチル基、n−オクチル基、i−オクチル基、n−ノニル基、n−デシル基、2−エチルヘキシル基等が挙げられる。
上記R15a、R15b及びR15cで表される炭素数6〜12の芳香族炭化水素基としては、例えば、フェニル基、ナフチル基等が挙げられる。
上記RG1及びRG2で表される炭素数1〜12の直鎖状若しくは分岐状のアルキル基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、t−ブチル基、n−ペンチル基、i−ペンチル基、n−ヘキシル基、i−ヘキシル基、n−ヘプチル基、n−オクチル基、i−オクチル基、n−ノニル基、n−デシル基、2−エチルヘキシル基等が挙げられる。
上記RG1及びRG2で表される炭素数5〜25の脂環式炭化水素基としては、例えば、シクロペンチル基、シクロヘキシル基、シクロオクチル基、アダマンチル基、ノルボニル基等が挙げられる。
上記RG1及びRG2で表される炭素数6〜12の芳香族炭化水素基としては、例えば、フェニル基、ナフチル基等が挙げられる。
上記R16aで表される炭素数1〜8の直鎖状若しくは分岐状のアルキル基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、t−ブチル基、n−ペンチル基、i−ペンチル基、n−ヘキシル基、i−ヘキシル基、n−ヘプチル基、n−オクチル基、i−オクチル基、2−エチルヘキシル基等が挙げられる。
上記R16aで表される炭素数6〜8の芳香族炭化水素基としては、例えば、フェニル基等が挙げられる。
上記R16bで表される炭素数1〜7の直鎖状若しくは分岐状のアルキル基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、t−ブチル基、n−ペンチル基、i−ペンチル基、n−ヘキシル基、i−ヘキシル基、n−ヘプチル基等が挙げられる。
上記R16bで表される炭素数6〜7の芳香族炭化水素基としては、例えば、フェニル基等が挙げられる。
上記式(2−A−1)及び(2−A−2)におけるアルキル基及び芳香族炭化水素基が有してもよい置換基としては、フッ素、塩素、臭素、ヨウ素等のハロゲン原子、ヒドロキシル基、シアノ基、チオール基、芳香族炭化水素基、アルケニル基、ヘテロ原子(例えば、ハロゲン原子、酸素原子、窒素原子、硫黄原子、リン原子、ケイ素原子等)を含むアルキル基、脂環式炭化水素基等の有機基等が挙げられる。さらに、炭化水素基の同一炭素上の2つの水素原子が1つの酸素原子で置換されたケト基を例示することができる。これらの置換基は、構造上可能な範囲内でいくつ存在していても良い。
上記式(2−A−1)及び(2−A−2)で表されるスルホニウムカチオンの中でも、下記式(i−1)〜(i−13)で表されるものが好ましい。
これらの中で、上記式(i−1)、(i−6)〜(i−13)で表されるカチオンがより好ましい。
また、上記式(2−B)で表されるオニウムカチオンの中でも、下記式(2−B−1)で表されるオニウムカチオンが好ましい。
上記式(2−B−1)中、R17a及びR17bは、それぞれ独立して、水素原子、炭素数1〜12の直鎖状若しくは分岐状のアルキル基、又は炭素数6〜12の芳香族炭化水素基である。上記アルキル基及び芳香族炭化水素基の水素原子の一部又は全部は置換されていてもよい。j7及びj8は、それぞれ独立して、0〜5の整数である。R17a及びR17bが複数ある場合、複数のR17a及びR17bはそれぞれ同一でも異なっていてもよい。また、R17a及びR17bのうちの2個以上が互いに結合して環を形成していてもよい。
上記R17a及びR17bで表される炭素数1〜12の直鎖状若しくは分岐状のアルキル基としては、例えば、メチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、2−メチルプロピル基、1−メチルプロピル基、t−ブチル基等が挙げられる。
上記R17a及びR17bで表される炭素数6〜12の芳香族炭化水素基としては、例えば、フェニル基、ナフチル基等が挙げられる。
上記式(2−B−1)におけるアルキル基及び芳香族炭化水素基が有してもよい置換基としては、上記式(2−A−1)及び(2−A−2)におけるアルキル基及び炭化水素基
の置換基の例を挙げることができる。
の置換基の例を挙げることができる。
上記式(2−B−1)で表されるヨードニウムカチオンの中でも、下記式(ii−1)〜(ii−3)でそれぞれ表されるカチオンが好ましい。
これらの中で、上記式(ii−1)又は(ii−2)で表されるものがより好ましい。
上記M+で表される1価のオニウムカチオンは、例えば、Advances in Polymer Science,Vol.62,p.1−48(1984)に記載されている一般的な方法に準じて製造することができる
[B]酸発生剤の含有量としては、[A]重合体100質量部に対して、0.1〜20質量部であることが好ましく、0.5〜15質量部であることが更に好ましい。[B]酸発生剤の含有量が0.1質量部未満であると、感度及び現像性が低下する場合がある。逆に、20質量部を超えると、露光光に対する透明性、パターン形状、耐熱性等が低下する場合がある。当該フォトレジスト組成物は、[B]酸発生剤を1種又は2種以上含有することができる。
<[C]他の酸発生剤>
当該フォトレジスト組成物は、酸発生剤として上記[B]酸発生剤を含有しているので、必ずしも必要ではないが、[C]他の酸発生剤を含有してもよい。[C]他の酸発生剤としては、酸発生効率、耐熱性等が良好であるという観点から、例えば、オニウム塩、ジアゾメタン化合物、N−スルホニルオキシイミド化合物、スルホン化合物、スルホン酸エステル化合物、ジスルホニルメタン化合物、オキシムスルホネート化合物、ヒドラジンスルホネート化合物等が挙げられる。当該フォトレジスト組成物は、[C]他の酸発生剤を1種又は2種以上含有することができる。
当該フォトレジスト組成物は、酸発生剤として上記[B]酸発生剤を含有しているので、必ずしも必要ではないが、[C]他の酸発生剤を含有してもよい。[C]他の酸発生剤としては、酸発生効率、耐熱性等が良好であるという観点から、例えば、オニウム塩、ジアゾメタン化合物、N−スルホニルオキシイミド化合物、スルホン化合物、スルホン酸エステル化合物、ジスルホニルメタン化合物、オキシムスルホネート化合物、ヒドラジンスルホネート化合物等が挙げられる。当該フォトレジスト組成物は、[C]他の酸発生剤を1種又は2種以上含有することができる。
上記オニウム塩としては、例えば、スルホニウム塩、ヨードニウム塩、ホスホニウム塩、ジアゾニウム塩、ピリジニウム塩等が挙げられる。なお、これらのオニウム塩は、1種又は2種以上用いることができる。
上記スルホニウム塩としては、例えば、トリフェニルスルホニウムトリフルオロメタンスルホネート、トリフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、トリフェニルスルホニウムベンゼンスルホネート、トリフェニルスルホニウムp−トルエンスルホネート、トリフェニルスルホニウム10−カンファースルホネート、トリフェニルスルホニウムn−オクタンスルホネート、トリフェニルスルホニウム4−トリフルオロメチルベンゼンスルホネート、トリフェニルスルホニウムナフタレンスルホネート、トリフェニルスルホニウムパーフルオロベンゼンスルホネート;
(4−t−ブトキシフェニル)ジフェニルスルホニウムトリフルオロメタンスルホネート、(4−t−ブトキシフェニル)ジフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、(4−t−ブトキシフェニル)ジフェニルスルホニウムパーフルオロ−n−オクタンスルホネート、(4−t−ブトキシフェニル)ジフェニルスルホニウム10−カンファースルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウムトリフルオロメタンスルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウムパーフルオロ−n−オクタンスルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウム10−カンファースルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウムn−オクタンスルホネート;
トリス(4−メトキシフェニル)スルホニウムトリフルオロメタンスルホネート、トリス(4−メトキシフェニル)スルホニウムノナフルオロ−n−ブタンスルホネート、トリス(4−メトキシフェニル)スルホニウムパーフルオロ−n−オクタンスルホネート、トリス(4−メトキシフェニル)スルホニウム10−カンファースルホネート;
(4−フルオロフェニル)ジフェニルスルホニウムトリフルオロメタンスルホネート、(4−フルオロフェニル)ジフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、(4−フルオロフェニル)ジフェニルスルホニウム10−カンファースルホネート;
(4−フルオロフェニル)ジフェニルスルホニウムトリフルオロメタンスルホネート、(4−フルオロフェニル)ジフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、(4−フルオロフェニル)ジフェニルスルホニウム10−カンファースルホネート;
トリス(4−フルオロフェニル)スルホニウムトリフルオロメタンスルホネート、トリス(4−フルオロフェニル)スルホニウムノナフルオロ−n−ブタンスルホネート、トリス(4−フルオロフェニル)スルホニウム10―カンファースルホネート、トリス(4−フルオロフェニル)スルホニウムp−トルエンスルホネート、トリス(4−トリフルオロメチルフェニル)スルホニウムトリフルオロメタンスルホネート;
2,4,6−トリメチルフェニルジフェニルスルホニウムトリフルオロメタンスルホネート、2,4,6−トリメチルフェニルジフェニルスルホニウム2,4−ジフルオロベンゼンスルホネート、2,4,6−トリメチルフェニルジフェニルスルホニウム4−トリフルオロメチルベンゼンスルホネート等が挙げられる。
これらの中でも、トリフェニルスルホニウムトリフルオロメタンスルホネート、トリフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、トリフェニルスルホニウム10−カンファースルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウムトリフルオロメタンスルホネート、(4−ヒドロキシフェニル)ジフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、トリス(4−メトキシフェニル)スルホニウムトリフルオロメタンスルホネート、トリス(4−メトキシフェニル)スルホニウムノナフルオロ−n−ブタンスルホネート、(4−フルオロフェニル)ジフェニルスルホニウムトリフルオロメタンスルホネート、(4−フルオロフェニル)ジフェニルスルホニウムノナフルオロ−n−ブタンスルホネート、2,4,6−トリメチルフェニルジフェニルスルホニウムトリフルオロメタンスルホネート、2,4,6−トリメチルフェニルジフェニルスルホニウム2,4−ジフルオロベンゼンスルホネート、2,4,6−トリメチルフェニルジフェニルスルホニウム4−トリフルオロメチルベンゼンスルホネートが好ましい。
上記ヨードニウム塩としては、例えば、ジフェニルヨードニウムトリフルオロメタンスルホネート、ジフェニルヨードニウムノナフルオロ−n−ブタンスルホネート、ジフェニルヨードニウムパーフルオロ−n−オクタンスルホネート、ジフェニルヨードニウム10−カンファースルホネート、ジフェニルヨードニウムn−オクタンスルホネート;
ビス(4−t−ブチルフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−t−ブチルフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−t−ブチルフェニル)ヨードニウムパーフルオロ−n−オクタンスルホネート、ビス(4−t−ブチルフェニル)ヨードニウム10−カンファースルホネート、ビス(4−t−ブチルフェニル)ヨードニウムn−オクタンスルホネート、(4−メトキシフェニル)フェニルヨードニウムトリフルオロメタンスルホネート、(4−メトキシフェニル)フェニルヨードニウムノナフルオロ−n−ブタンスルホネート、(4−メトキシフェニル)フェニルヨードニウムパーフルオロ−n−オクタンスルホネート;
(4−フルオロフェニル)フェニルヨードニウムトリフルオロメタンスルホネート、(4−フルオロフェニル)フェニルヨードニウムノナフルオロ−n−ブタンスルホネート、(4−フルオロフェニル)フェニルヨードニウム10−カンファースルホネート;
ビス(4−フルオロフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−フルオロフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−フルオロフェニル)ヨードニウム10−カンファースルホネート;
ビス(4−フルオロフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−フルオロフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−フルオロフェニル)ヨードニウム10−カンファースルホネート;
ビス(4−クロロフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−クロロフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−クロロフェニル)ヨードニウムパーフルオロ−n−オクタンスルホネート、ビス(4−クロロフェニル)ヨードニウムn−ドデシルベンゼンスルホネート、ビス(4−クロロフェニル)ヨードニウム10−カンファースルホネート、ビス(4−クロロフェニル)ヨードニウムn−オクタンスルホネート、ビス(4−クロロフェニル)ヨードニウム4−トリフルオロメチルベンゼンスルホネート、ビス(4−クロロフェニル)ヨードニウムパーフルオロベンゼンスルホネート;
ビス(4−トリフルオロメチルフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムパーフルオロ−n−オクタンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムn−ドデシルベンゼンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムp−トルエンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムベンゼンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウム10−カンファースルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムn−オクタンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウム4−トリフルオロメチルベンゼンスルホネート、ビス(4−トリフルオロメチルフェニル)ヨードニウムパーフルオロベンゼンスルホネート等が挙げられる。
これらの中でも、ジフェニルヨードニウムトリフルオロメタンスルホネート、ジフェニルヨードニウムノナフルオロ−n−ブタンスルホネート、ジフェニルヨードニウム10−カンファースルホネート、ビス(4−t−ブチルフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−t−ブチルフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−t−ブチルフェニル)ヨードニウム10−カンファースルホネート、(4−フルオロフェニル)フェニルヨードニウムトリフルオロメタンスルホネート、(4−フルオロフェニル)フェニルヨードニウムノナフルオロ−n−ブタンスルホネート、(4−フルオロフェニル)フェニルヨードニウム10−カンファースルホネート、ビス(4−フルオロフェニル)ヨードニウムトリフルオロメタンスルホネート、ビス(4−フルオロフェニル)ヨードニウムノナフルオロ−n−ブタンスルホネート、ビス(4−フルオロフェニル)ヨードニウム10−カンファースルホネート、トリス(4−トリフルオロメチルフェニル)スルホニウムトリフルオロメタンスルホネーが好ましい。上記スルホニウム塩は、1種又は2種以上を用いることができる。
上記ジアゾメタン化合物としては、例えば、ビス(トリフルオロメタンスルホニル)ジアゾメタン、ビス(シクロヘキシルスルホニル)ジアゾメタン、ビス(3,3−ジメチル−1,5−ジオキサスピロ[5.5]ドデカン−8−スルホニル)ジアゾメタン、ビス(1,4−ジオキサスピロ[4.5]デカン−7−スルホニル)ジアゾメタン、ビス(t−ブチルスルホニル)ジアゾメタン等が挙げられる。
これらの中でも、ビス(シクロヘキシルスルホニル)ジアゾメタン、ビス(3,3−ジメチル−1,5−ジオキサスピロ[5.5]ドデカン−8−スルホニル)ジアゾメタン、ビス(1,4−ジオキサスピロ[4.5]デカン−7−スルホニル)ジアゾメタンが好ましい。上記ジアゾメタン化合物は、1種又は2種以上を用いることができる。
上記N−スルホニルオキシイミド化合物としては、例えば、N−(トリフルオロメチルスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(トリフルオロメチルスルホニルオキシ)−7−オキサビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(トリフルオロメチルスルホニルオキシ)ビシクロ[2.2.1]ヘプタン−5,6−オキシ−2,3−ジカルボキシイミド;
N−(10−カンファースルホニルオキシ)スクシンイミド、N−(10−カンファースルホニルオキシ)フタルイミド、N−(10−カンファースルホニルオキシ)−7−オキサビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(10−カンファースルホニルオキシ)ビシクロ[2.2.1]ヘプタン−5,6−オキシ−2,3−ジカルボキシイミド、N−(10−カンファースルホニルオキシ)ナフチルイミド、N−〔(5−メチル−5−カルボキシメチルビシクロ[2.2.1]ヘプタン−2−イル)スルホニルオキシ〕スクシンイミド;
N−(n−オクチルスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(n−オクチルスルホニルオキシ)ビシクロ[2.2.1]ヘプタン−5,6−オキシ−2,3−ジカルボキシイミド、N−(パーフルオロフェニルスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(パーフルオロフェニルスルホニルオキシ)−7−オキサビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(パーフルオロフェニルスルホニルオキシ)ビシクロ[2.2.1]ヘプタン−5,6−オキシ−2,3−ジカルボキシイミド、N−(ノナフルオロ−n−ブチルスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(ノナフルオロ−n−ブチルスルホニルオキシ)−7−オキサビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(ノナフルオロ−n−ブチルスルホニルオキシ)ビシクロ[2.2.1]ヘプタン−5,6−オキシ−2,3−ジカルボキシイミド;
N−(パーフルオロ−n−オクチルスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(パーフルオロ−n−オクチルスルホニルオキシ)−7−オキサビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(パーフルオロ−n−オクチルスルホニルオキシ)ビシクロ[2.2.1]ヘプタン−5,6−オキシ−2,3−ジカルボキシイミド等が挙げられる。
これらの中でも、N−(トリフルオロメチルスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド、N−(10−カンファースルホニルオキシ)スクシンイミド、N−[(5−メチル−5−カルボキシメチルビシクロ[2.2.1]ヘプタン−2−イル)スルホニルオキシ]スクシンイミドが好ましい。上記N−スルホニルオキシイミド化合物は、1種又は2種以上を用いることができる。
上記スルホン化合物としては、例えば、β−ケトスルホン、β−スルホニルスルホンや、これらのα−ジアゾ化合物等が挙げられる。より具体的には、フェナシルフェニルスルホン、メシチルフェナシルスルホン、ビス(フェニルスルホニル)メタン、4−トリスフェナシルスルホン等が挙げられる。上記スルホン化合物は、1種又は2種以上を用いることができる。
上記スルホン酸エステル化合物としては、例えば、アルキルスルホン酸エステル、ハロアルキルスルホン酸エステル、アリールスルホン酸エステル、イミノスルホネート等が挙げられる。より具体的には、ベンゾイントシレート、ピロガロールトリス(トリフルオロメタンスルホネート)、ピロガロールトリス(ノナフルオロブタンスルホネート)、ピロガロールトリス(メタンスルホネート)、ニトロベンジル−9,10−ジエトキシアントラセン−2−スルホネート、α−メチロールベンゾイントシレート、α−メチロールベンゾイントリフルオロメタンスルホネート、α−メチロールベンゾインn−オクタンスルホネート、α−メチロールベンゾインn−ドデカンスルホネート等が挙げられる。上記スルホン酸エステル化合物は、1種又は2種以上を用いることができる。
上記ジスルホニルメタン化合物としては、例えば、下記式(3−1)で表される化合物等が挙げられる。
上記式(3−1)中、R18a及びR18bは、それぞれ独立して、直鎖状若しくは分岐状のアルキル基、シクロアルキル基、アリール基、アラルキル基又はヘテロ原子を有する1価の有機基である。V1及びV2は、それぞれ独立して、水素原子、アリール基、直鎖状若しくは分岐状の1価の鎖状炭化水素基、又はヘテロ原子を有する1価の有機基である。但し、V1及びV2の少なくとも一方はアリール基である。また、V1及びV2は互いに結合して、少なくとも1個の不飽和結合を有する炭素単環構造若しくは炭素多環構造を有する基又は下記式(3−1a)で表される基を形成していてもよい。
上記式(3−1a)中、W1及びW2は、それぞれ独立して、水素原子、ハロゲン原子、直鎖状若しくは分岐状のアルキル基、シクロアルキル基、アリール基、又はアラルキル基である。但し、上記アルキル基、シクロアルキル基、アリール基及びアラルキル基は、互いに結合して、それらが結合する炭素原子と共に炭素単環構造を形成していてもよい。uは2〜10の整数である。
W1及びW2が互いに結合して炭素単環構造を形成する場合、同一の炭素原子に結合しているW1及びW2で炭素単環構造を形成してもよく、異なる炭素原子に結合しているW1及びW2で炭素単環構造を形成してもよい。上記ジスルホニルメタン化合物は、1種又は2種以上を用いることができる。
オキシムスルホネート化合物としては、例えば、下記式(3−2−A)及び式(3−2−B)でそれぞれ表される化合物が挙げられる。
上記式(3−2−A)及び(3−2−B)中、R19a、R19b及びR19cは、それぞれ独立して、1価の有機基である。R20a、R20b及びR20cは、それぞれ独立して、1価の有機基である。
上記R19a、R19b及びR19cで表される1価の有機基としては、例えば、メチル基、エチル基、n―プロピル基、フェニル基、トシル基、トリフルオロメチル基、ペンタフルオロエチル基等が挙げられる。
上記R20a、R20b及びR20cで表される1価の有機基としては、例えば、フェニル基、トシル基、1−ナフチル基等が挙げられる。上記オキシムスルホネート化合物は、1種又は2種以上を用いることができる。
上記ヒドラジンスルホネート化合物としては、例えば、ビス(ベンゼンスルホニル)ヒドラジン、ビス(p−トルエンスルホニル)ヒドラジン、ビス(トリフルオロメタンスルホニル)ヒドラジン、ビス(ペンタフルオロエタンスルホニル)ヒドラジン、ビス(n−プロパンスルホニル)ヒドラジン、ベンゼンスルホニルヒドラジン、p−トルエンスルホニルヒドラジン、トリフルオロメタンスルホニルヒドラジン、ペンタフルオロエタンスルホニルヒドラジン、n−プロパンスルホニルヒドラジン、トリフルオロメタンスルホニル・p−トルエンスルホニルヒドラジン等が挙げられる。上記ヒドラジンスルホネート化合物は、1種又は2種以上を用いることができる。
[C]他の酸発生剤の含有量としては、[A]重合体100質量部に対して、20質量部以下が好ましく、1〜15質量部がより好ましい。[C]他の酸発生剤の含有量が20質量部を超えると、露光光に対する透明性が低下し、パターン形状、耐熱性等が低下するおそれがある。
<[D]酸拡散制御剤>
当該感放射線性樹脂組成物は、[D]酸拡散制御剤を含有することが好ましい。[D]酸拡散制御剤は、露光により[B]酸発生剤等から発生した酸のレジスト膜中における拡散現象を制御し、非露光領域での好ましくない化学反応を抑制する作用を有する。
当該感放射線性樹脂組成物は、[D]酸拡散制御剤を含有することが好ましい。[D]酸拡散制御剤は、露光により[B]酸発生剤等から発生した酸のレジスト膜中における拡散現象を制御し、非露光領域での好ましくない化学反応を抑制する作用を有する。
[D]酸拡散制御剤としては、例えば、含窒素有機化合物又は感光性塩基性化合物が挙げられる。含窒素有機化合物としては、例えば、下記式(4−1)で表される化合物(以下、「含窒素化合物(i)」ともいう。)、同一分子内に窒素原子を2個有する化合物(以下、「含窒素化合物(ii)」ともいう。)、窒素原子を3個以上有するポリアミノ化合物や含窒素重合性化合物の重合体(以下、これらをまとめて「含窒素化合物(iii)」ともいう。)、アミド基含有化合物、ウレア化合物、含窒素複素環化合物等が挙げられる。なお、[D]酸拡散制御剤は、1種又は2種以上を用いることができる。
上記式(4−1)中、R21a、R21b及びR21cは、それぞれ独立して、水素原子、直鎖状若しくは分岐状のアルキル基、シクロアルキル基、アリール基又はアラルキル基である。上記アルキル基、シクロアルキル基、アリール基及びアラルキル基の水素原子の一部又は全部は置換されていてもよい。
含窒素化合物(i)としては、例えば、n−ヘキシルアミン、n−ヘプチルアミン、n−オクチルアミン、n−ノニルアミン、n−デシルアミン、シクロヘキシルアミン等のモノ(シクロ)アルキルアミン類;ジ−n−ブチルアミン、ジ−n−ペンチルアミン、ジ−n−ヘキシルアミン、ジ−n−ヘプチルアミン、ジ−n−オクチルアミン、ジ−n−ノニルアミン、ジ−n−デシルアミン、シクロヘキシルメチルアミン、ジシクロヘキシルアミン等のジ(シクロ)アルキルアミン類;トリエチルアミン、トリ−n−プロピルアミン、トリ−n−ブチルアミン、トリ−n−ペンチルアミン、トリ−n−ヘキシルアミン、トリ−n−ヘプチルアミン、トリ−n−オクチルアミン、トリ−n−ノニルアミン、トリ−n−デシルアミン、シクロヘキシルジメチルアミン、メチルジシクロヘキシルアミン、トリシクロヘキシルアミン等のトリ(シクロ)アルキルアミン類;トリエタノールアミン等の置換アルキルアミン;アニリン、N−メチルアニリン、N,N−ジメチルアニリン、2−メチルアニリン、3−メチルアニリン、4−メチルアニリン、4−ニトロアニリン、ジフェニルアミン、トリフェニルアミン、ナフチルアミン、2,4,6−トリ−tert−ブチル−N−メチルアニリン、N−フェニルジエタノールアミン、2,6−ジイソプロピルアニリン等の芳香族アミン類が挙げられる。
含窒素化合物(ii)としては、例えば、エチレンジアミン、N,N,N’,N’−テトラメチルエチレンジアミン、テトラメチレンジアミン、ヘキサメチレンジアミン、4,4’−ジアミノジフェニルメタン、4,4’−ジアミノジフェニルエーテル、4,4’−ジアミノベンゾフェノン、4,4’−ジアミノジフェニルアミン、2,2−ビス(4−アミノフェニル)プロパン、2−(3−アミノフェニル)−2−(4−アミノフェニル)プロパン、2−(4−アミノフェニル)−2−(3−ヒドロキシフェニル)プロパン、2−(4−アミノフェニル)−2−(4−ヒドロキシフェニル)プロパン、1,4−ビス〔1−(4−アミノフェニル)−1−メチルエチル〕ベンゼン、1,3−ビス〔1−(4−アミノフェニル)−1−メチルエチル〕ベンゼン、ビス(2−ジメチルアミノエチル)エーテル、ビス(2−ジエチルアミノエチル)エーテル、1−(2−ヒドロキシエチル)−2−イミダゾリジノン、2−キノキサリノール、N,N,N’,N’−テトラキス(2−ヒドロキシプロピル)エチレンジアミン、N,N,N’,N”,N”−ペンタメチルジエチレントリアミン等が挙げられる。
含窒素化合物(iii)としては、例えば、ポリエチレンイミン、ポリアリルアミン、2−ジメチルアミノエチルアクリルアミドの重合体等が挙げられる。
アミド基含有化合物としては、例えば、N−t−ブトキシカルボニルジ−n−オクチルアミン、N−t−ブトキシカルボニルジ−n−ノニルアミン、N−t−ブトキシカルボニルジ−n−デシルアミン、N−t−ブトキシカルボニルジシクロヘキシルアミン、N−t−ブトキシカルボニル−1−アダマンチルアミン、N−t−ブトキシカルボニル−2−アダマンチルアミン、N−t−ブトキシカルボニル−N−メチル−1−アダマンチルアミン、(S)−(−)−1−(t−ブトキシカルボニル)−2−ピロリジンメタノール、(R)−(+)−1−(t−ブトキシカルボニル)−2−ピロリジンメタノール、N−t−ブトキシカルボニル−4−ヒドロキシピペリジン、N−t−ブトキシカルボニルピロリジン、N−t−ブトキシカルボニルピペラジン、N,N−ジ−t−ブトキシカルボニル−1−アダマンチルアミン、N,N−ジ−t−ブトキシカルボニル−N−メチル−1−アダマンチルアミン、N−t−ブトキシカルボニル−4,4’−ジアミノジフェニルメタン、N,N’−ジ−t−ブトキシカルボニルヘキサメチレンジアミン、N,N,N’N’−テトラ−t−ブトキシカルボニルヘキサメチレンジアミン、N,N’−ジ−t−ブトキシカルボニル−1,7−ジアミノヘプタン、N,N’−ジ−t−ブトキシカルボニル−1,8−ジアミノオクタン、N,N’−ジ−t−ブトキシカルボニル−1,9−ジアミノノナン、N,N’−ジ−t−ブトキシカルボニル−1,10−ジアミノデカン、N,N’−ジ−t−ブトキシカルボニル−1,12−ジアミノドデカン、N,N’−ジ−t−ブトキシカルボニル−4,4’−ジアミノジフェニルメタン、N−t−ブトキシカルボニルベンズイミダゾール、N−t−ブトキシカルボニル−2−メチルベンズイミダゾール、N−t−ブトキシカルボニル−2−フェニルベンズイミダゾール等のN−t−ブトキシカルボニル基含有アミノ化合物のほか、ホルムアミド、N−メチルホルムアミド、N,N−ジメチルホルムアミド、アセトアミド、N−メチルアセトアミド、N,N−ジメチルアセトアミド、プロピオンアミド、ベンズアミド、ピロリドン、N−メチルピロリドン、N−アセチル−1−アダマンチルアミン、イソシアヌル酸トリス(2−ヒドロキシエチル)等が挙げられる。
ウレア化合物としては、例えば、尿素、メチルウレア、1,1−ジメチルウレア、1,3−ジメチルウレア、1,1,3,3−テトラメチルウレア、1,3−ジフェニルウレア、トリ−n−ブチルチオウレア等が挙げられる。
含窒素複素環化合物としては、例えば、イミダゾール、4−メチルイミダゾール、4−メチル−2−フェニルイミダゾール、ベンズイミダゾール、2−フェニルベンズイミダゾール、1−ベンジル−2−メチルイミダゾール、1−ベンジル−2−メチル−1H−イミダゾール等のイミダゾール類;ピリジン、2−メチルピリジン、4−メチルピリジン、2−エチルピリジン、4−エチルピリジン、2−フェニルピリジン、4−フェニルピリジン、2−メチル−4−フェニルピリジン、ニコチン、ニコチン酸、ニコチン酸アミド、キノリン、4−ヒドロキシキノリン、8−オキシキノリン、アクリジン、2,2’:6’,2”−ターピリジン等のピリジン類;ピペラジン、1−(2−ヒドロキシエチル)ピペラジン等のピペラジン類の他、ピラジン、ピラゾール、ピリダジン、キノザリン、プリン、ピロリジン、ピペリジン、ピペリジンエタノール、3−ピペリジノ−1,2−プロパンジオール、モルホリン、4−メチルモルホリン、1−(4−モルホリニル)エタノール、4−アセチルモルホリン、3−(N−モルホリノ)−1,2−プロパンジオール、1,4−ジメチルピペラジン、1,4−ジアザビシクロ[2.2.2]オクタン等が挙げられる。この中で、イミダゾール類が好ましく、2−フェニルベンズイミダゾールがより好ましい。
上記感光性塩基性化合物は、露光領域では対応する中性の物質に効率よく分解し、未露光部では分解せずにそのまま残る性質を有する成分である。このような感光性塩基性化合物は、非感光性の塩基性化合物に比べて、露光部に発生する酸を有効活用することができるため、感度を向上させることができる。
上記感光性塩基性化合物としては、上記性質を有する限り特に限定されないが、下記式(4−2−A)及び式(4−2−B)で表される化合物が好適に用いられる。
上記式(4−2−A)及び(4−2−B)中、R22a〜R22eは、それぞれ独立して、水素原子、ハロゲン原子、炭素数1〜10のアルキル基、炭素数3〜10の脂環式炭化水素基又は炭素数1〜10のアルコキシ基である。上記アルキル基、脂環式炭化水素基及びアルコキシ基の水素原子の一部又は全部は置換されていてもよい。E−及びG−は、それぞれ独立して、OH−、RD−O−又はRD−COO−である。但し、RDは、1価の有機基である。
上記ハロゲン原子としては、例えば、フッ素原子、塩素原子、臭素原子、ヨウ素原子等が挙げられる。
上記R22a〜R22eで表される炭素数1〜10のアルキル基としては、例えば、メチル基、エチル基、n−ブチル基、t−ブチル基等が挙げられる。
上記R22a〜R22eで表される炭素数3〜10の脂環式炭化水素基としては、例えば、シクロペンチル基、シクロペンテニル基、シクロヘキシル基、シクロヘキセニル基、ノルボルニル基、ノルボルネニル基、アダマンチル基等が挙げられる。
上記アルキル基及び脂環式炭化水素基の置換基としては、例えば、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、アルコキシ基等が挙げられる。
上記R22a〜R22eで表される炭素数1〜10のアルコキシ基としては、例えば、メトキシ基、t−ブトキシ基等が挙げられる。
置換されたアルキル基、脂環式炭化水素基及びアルコキシ基としては、トリフルオロメチル基、トリクロロメチル基、パーフルオロシクロペンチル基、t−ブトキシカルボニルメチルオキシ基等が挙げられる。
上記R22a〜R22eとしては、水素原子又はt−ブチル基が好ましく、水素原子がより好ましい。
上記RDで表される1価の有機基としては、例えば、置換基を有していてもよいアルキル基、置換基を有していてもよいアリール基等が挙げられる。
上記E−及びG−で表されるアニオンは、OH−、CH3COO−、並びに下記式(4−2−a)、式(4−2−b)及び式(4−2−c)でそれぞれ表されるアニオンから選択される少なくとも1種のアニオンであることが好ましい。
上記感光性塩基性化合物としては、トリフェニルスルホニウム化合物(上記式(4−2a)で表される化合物)であって、そのアニオン(E−又はG−)が、OH−、CH3COO−、並びに上記式(4−2−b)及び式(4−2−c)でそれぞれ表されるアニオンから選択される少なくとも1種のアニオンである化合物が好ましい。
[D]酸拡散制御剤の含有量としては、[A]重合体100質量部に対して、15質量部以下が好ましく、0.001〜10質量部がさらに好ましく、0.005〜5質量部が特に好ましい。[D]酸拡散制御剤の含有量が15質量部を超えると、レジストとしての感度や露光部の現像性が低下する場合がある。逆に、含有量が0.001質量部未満だと、プロセス条件によっては、レジストとしてのパターン形状や寸法忠実度が低下する場合がある。
<[E]架橋剤>
当該フォトレジスト組成物が、ネガ型のフォトレジスト組成物である場合、[E]架橋剤をさらに含有することが好ましい。当該フォトレジスト組成物は、[E]架橋剤を含有することにより、電磁波等を照射された際、[B]酸発生剤等から生成する酸の触媒作用により、[E]架橋剤の架橋反応が進行し、[A]重合体の分子相互間及び同一分子内で架橋し、アルカリ現像液に対する溶解性が低い架橋重合体が形成されるため、現像後にネガ型のレジストパターンを形成することができる。
当該フォトレジスト組成物が、ネガ型のフォトレジスト組成物である場合、[E]架橋剤をさらに含有することが好ましい。当該フォトレジスト組成物は、[E]架橋剤を含有することにより、電磁波等を照射された際、[B]酸発生剤等から生成する酸の触媒作用により、[E]架橋剤の架橋反応が進行し、[A]重合体の分子相互間及び同一分子内で架橋し、アルカリ現像液に対する溶解性が低い架橋重合体が形成されるため、現像後にネガ型のレジストパターンを形成することができる。
上記[E]架橋剤としては、[A]重合体を架橋することができ、架橋した重合体がアルカリ現像液に不溶又は難溶となるものであれば、特に限定されない。[E]架橋剤としては、例えば、下記式(5−1)〜(5−5)でそれぞれ表される架橋性官能基を有する化合物等が挙げられる。
上記式(5−1)中、eは1又は2である。Q1は、eが1の場合、単結合、酸素原子、硫黄原子、カルボニルオキシ基又はアミノ基であり、eが2の場合、窒素原子である。Q2は、酸素原子又は硫黄原子である。eは、1又は2である。k1は、0〜3の整数である。k2は、1〜3の整数である。但し、k1及びk2は、1≦k1+k2≦4を満たす。
上記式(5−1)で表される架橋性官能基としては、例えば、グリシジルエーテル基、グリシジルエステル基、グリシジルアミノ基等が挙げられる。
上記式(5−2)中、Q3は、酸素原子、カルボニル基又はカルボニルオキシ基である。R23a及びR23bは、それぞれ独立して、水素原子又は炭素数1〜4のアルキル基である。R23cは、炭素数1〜5のアルキル基、炭素数6〜12のアリール基又は炭素数7〜14のアラルキル基である。fは、1以上の整数である。
上記式(5−2)で表される架橋性官能基としては、例えば、メトキシメチル基、エトキシメチル基、ベンジルオキシメチル基、アセトキシメチル基、ベンゾイルオキシメチル基、ホルミル基、アセチル基等が挙げられる。
上記式(5−3)中、R24a、R24b及びR24cは、それぞれ独立して、水素原子又は炭素数1〜4のアルキル基である。
上記式(5−3)で表される架橋性官能基としては、例えば、ビニル基、イソプロペニル基等が挙げられる。
上記式(5−4)中、R25a及びR25bは、それぞれ独立して、水素原子又は炭素数1〜4のアルキル基である。R26a及びR26bは、それぞれ独立して、炭素数1〜5のアルキル基又は炭素数1〜5のヒドロキシアルキル基である。gは、1以上の整数である。
上記式(5−4)で表される架橋性官能基としては、例えば、ジメチルアミノメチル基、ジエチルアミノメチル基、ジメチロールアミノメチル基、ジエチロールアミノメチル基等が挙げられる。
上記式(5−5)中、R27a及びR27bは、それぞれ独立して、水素原子又は炭素数1〜4のアルキル基である。R28は、酸素原子、硫黄原子及び窒素原子のいずれかの原子を含む2価の基であり、結合している窒素原子と共に3〜8員環の1価の複素環基を形成する。hは、1以上の整数である。
上記式(5−5)で表される架橋性官能基としては、例えばモノホリルメチル基等が挙げられる。
上述の架橋性官能基を有する化合物としては、例えば、ビスフェノールA系エポキシ化合物、ビスフェノールF系エポキシ化合物、ビスフェノールS系エポキシ化合物、ノボラック樹脂系エポキシ化合物、レゾール樹脂系エポキシ化合物、ポリ(ヒドロキシスチレン)系エポキシ化合物、メチロール基含有メラミン化合物、メチロール基含有ベンゾグアナミン化合物、メチロール基含有尿素化合物、メチロール基含有フェノール化合物、アルコキシアルキル基含有メラミン化合物、アルコキシアルキル基含有ベンゾグアナミン化合物、アルコキシアルキル基含有尿素化合物、アルコキシアルキル基含有フェノール化合物、カルボキシルメチル基含有メラミン樹脂、カルボキシルメチル基含有ベンゾグアナミン樹脂、カルボキシルメチル基含有尿素樹脂、カルボキシルメチル基含有フェノール樹脂、カルボキシルメチル基含有メラミン化合物、カルボキシルメチル基含有ベンゾグアナミン化合物、カルボキシルメチル基含有尿素化合物、カルボキシルメチル基含有フェノール化合物等が挙げられる。
これらの架橋性官能基を有する化合物の中でも、メチロール基含有フェノール化合物、メトキシメチル基含有メラミン化合物、メトキシメチル基含有フェノール化合物、メトキシメチル基含有グリコールウリル化合物、メトキシメチル基含有ウレア化合物、又はアセトキシメチル基含有フェノール化合物が好ましく、ヘキサメトキシメチルメラミン等のメトキシメチル基含有メラミン化合物、メトキシメチル基含有グリコールウリル化合物、メトキシメチル基含有ウレア化合物が更に好ましく、1,3−ビス(メトキシメチル)ウレア、1,3,4,6−テトラキス(メトキシメチル)グリコールウリルが特に好ましい。
上記メトキシメチル基含有メラミン化合物としては、例えば、商品名で、CYMEL300、CYMEL301、CYMEL303、CYMEL305(CYTEC Industries社製)等が挙げられる。上記メトキシメチル基含有グリコールウリル化合物としては、商品名で、CYMEL1174(CYTEC Industries社製)、MX−270(三和ケミカル社製)等が挙げられる。上記メトキシメチル基含有ウレア化合物としては、商品名で、MX290(三和ケミカル社製)等が挙げられる。[E]架橋剤は、1種又は2種以上を用いることができる。
[E]架橋剤としては、上述の架橋性官能基を有する重合体も好ましい。このような重合体としては、例えば、[A]重合体の構造単位(I)等が有する酸性基の水素原子を、架橋性官能基で置換した重合体が挙げられる。この重合体の場合、架橋性官能基の導入率は、架橋性官能基の種類や、重合体の種類等に依存し一概には規定することはできないが、全酸性基に対して、5〜60モル%が好ましく、10〜50モル%がさらに好ましく、15〜40モル%が特に好ましい。架橋性官能基の導入率が5モル%未満だと、[E]架橋剤による架橋反応が十分に進行しないため、架橋度が小さくなり、得られるレジストパターンの高さが低下し、蛇行や膨潤等が発生し易くなるおそれがある。逆に、架橋性官能基の導入率が60モル%を超えると、未露光部の現像性が低下するおそれがある。
[E]架橋剤の含有量としては、ネガ型のフォトレジスト組成物の場合、[A]重合体100質量部に対して、0.1〜20質量部が好ましく、1〜15質量部がより好ましく、3〜10質量部がさらに好ましい。[E]架橋剤の含有量が0.1質量部未満だと、レジストパターンにおける架橋度が小さくなり、パターン形成性が低下するおそれがある。逆に、[E]架橋剤の含有量が20質量部を超えると、未露光部における現像性が低下するおそれがある。
<[F]溶媒>
当該フォトレジスト組成物は、通常、[F]溶媒を含有する。[F]溶媒は、少なくとも上記[A]重合体、[B]酸発生剤、及び必要に応じて加えられる任意成分を溶解できれば特に限定されない。
当該フォトレジスト組成物は、通常、[F]溶媒を含有する。[F]溶媒は、少なくとも上記[A]重合体、[B]酸発生剤、及び必要に応じて加えられる任意成分を溶解できれば特に限定されない。
[F]溶媒としては、例えば、
エチレングリコールモノメチルエーテルアセテート、エチレングリコールモノエチルエーテルアセテート、エチレングリコールモノ−n−プロピルエーテルアセテート、エチレングリコールモノ−n−ブチルエーテルアセテート等のエチレングリコールモノアルキルエーテルアセテート類;
プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、プロピレングリコールモノ−n−プロピルエーテル、プロピレングリコールモノ−n−ブチルエーテル等のプロピレングリコールモノアルキルエーテル類;
プロピレングリコールジメチルエーテル、プロピレングリコールジエチルエーテル、プロピレングリコールジ−n−プロピルエーテル、プロピレングリコールジ−n−ブチルエーテル等のプロピレングリコールジアルキルエーテル類;
プロピレングリコールモノメチルエーテルアセテート、プロピレングリコールモノエチルエーテルアセテート、プロピレングリコールモノ−n−プロピルエーテルアセテート、プロピレングリコールモノ−n−ブチルエーテルアセテート等のプロピレングリコールモノアルキルエーテルアセテート類;
エチレングリコールモノメチルエーテルアセテート、エチレングリコールモノエチルエーテルアセテート、エチレングリコールモノ−n−プロピルエーテルアセテート、エチレングリコールモノ−n−ブチルエーテルアセテート等のエチレングリコールモノアルキルエーテルアセテート類;
プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、プロピレングリコールモノ−n−プロピルエーテル、プロピレングリコールモノ−n−ブチルエーテル等のプロピレングリコールモノアルキルエーテル類;
プロピレングリコールジメチルエーテル、プロピレングリコールジエチルエーテル、プロピレングリコールジ−n−プロピルエーテル、プロピレングリコールジ−n−ブチルエーテル等のプロピレングリコールジアルキルエーテル類;
プロピレングリコールモノメチルエーテルアセテート、プロピレングリコールモノエチルエーテルアセテート、プロピレングリコールモノ−n−プロピルエーテルアセテート、プロピレングリコールモノ−n−ブチルエーテルアセテート等のプロピレングリコールモノアルキルエーテルアセテート類;
乳酸メチル、乳酸エチル、乳酸n−プロピル、乳酸i−プロピル等の乳酸エステル類;
ぎ酸n−アミル、ぎ酸i−アミル、酢酸エチル、酢酸n−プロピル、酢酸i−プロピル、酢酸n−ブチル、酢酸i−ブチル、酢酸n−アミル、酢酸i−アミル、プロピオン酸i−プロピル、プロピオン酸n−ブチル、プロピオン酸i−ブチル等の脂肪族カルボン酸エステル類;
ヒドロキシ酢酸エチル、2−ヒドロキシ−2−メチルプロピオン酸エチル、2−ヒドロキシ−3−メチル酪酸メチル、メトキシ酢酸エチル、エトキシ酢酸エチル、3−メトキシプロピオン酸メチル、3−メトキシプロピオン酸エチル、3−エトキシプロピオン酸メチル、3−エトキシプロピオン酸エチル、3−メトキシブチルアセテート、3−メチル−3−メトキシブチルアセテート、3−メチル−3−メトキシブチルプロピオネート、3−メチル−3−メトキシブチルブチレート、アセト酢酸メチル、アセト酢酸エチル、ピルビン酸メチル、ピルビン酸エチル等のエステル類;
トルエン、キシレン等の芳香族炭化水素類;
メチルエチルケトン、2−ペンタノン、2−ヘキサノン、2−ヘプタノン、3−ヘプタノン、4−ヘプタノン、シクロヘキサノン等のケトン類;
N−メチルホルムアミド、N,N−ジメチルホルムアミド、N−メチルアセトアミド、N,N−ジメチルアセトアミド、N−メチルピロリドン等のアミド類;
γ−ブチロラクン等のラクトン類等が挙げられる。[F]溶媒は、1種又は2種以上を用いることができる。
ぎ酸n−アミル、ぎ酸i−アミル、酢酸エチル、酢酸n−プロピル、酢酸i−プロピル、酢酸n−ブチル、酢酸i−ブチル、酢酸n−アミル、酢酸i−アミル、プロピオン酸i−プロピル、プロピオン酸n−ブチル、プロピオン酸i−ブチル等の脂肪族カルボン酸エステル類;
ヒドロキシ酢酸エチル、2−ヒドロキシ−2−メチルプロピオン酸エチル、2−ヒドロキシ−3−メチル酪酸メチル、メトキシ酢酸エチル、エトキシ酢酸エチル、3−メトキシプロピオン酸メチル、3−メトキシプロピオン酸エチル、3−エトキシプロピオン酸メチル、3−エトキシプロピオン酸エチル、3−メトキシブチルアセテート、3−メチル−3−メトキシブチルアセテート、3−メチル−3−メトキシブチルプロピオネート、3−メチル−3−メトキシブチルブチレート、アセト酢酸メチル、アセト酢酸エチル、ピルビン酸メチル、ピルビン酸エチル等のエステル類;
トルエン、キシレン等の芳香族炭化水素類;
メチルエチルケトン、2−ペンタノン、2−ヘキサノン、2−ヘプタノン、3−ヘプタノン、4−ヘプタノン、シクロヘキサノン等のケトン類;
N−メチルホルムアミド、N,N−ジメチルホルムアミド、N−メチルアセトアミド、N,N−ジメチルアセトアミド、N−メチルピロリドン等のアミド類;
γ−ブチロラクン等のラクトン類等が挙げられる。[F]溶媒は、1種又は2種以上を用いることができる。
<[G]添加剤>
当該フォトレジスト組成物は、[G]添加剤として、必要に応じ、界面活性剤、増感剤、染料、顔料、接着助剤、4−ヒドロキシ−4’−メチルカルコン等のハレーション防止剤、形状改良剤、保存安定剤、消泡剤等を含有することができる。
当該フォトレジスト組成物は、[G]添加剤として、必要に応じ、界面活性剤、増感剤、染料、顔料、接着助剤、4−ヒドロキシ−4’−メチルカルコン等のハレーション防止剤、形状改良剤、保存安定剤、消泡剤等を含有することができる。
[界面活性剤]
界面活性剤は、当該フォトレジスト組成物の塗布性やストリエーション、レジストとしての現像性等を改良する作用を有するものである。
界面活性剤は、当該フォトレジスト組成物の塗布性やストリエーション、レジストとしての現像性等を改良する作用を有するものである。
界面活性剤としては、例えば、ポリオキシエチレンラウリルエーテル、ポリオキシエチレンステアリルエーテル、ポリオキシエチレンオレイルエーテル、ポリオキシエチレンn−オクチルフェノールエーテル、ポリオキシエチレンn−ノニルフェノールエーテル、ポリエチレングリコールジラウレート、ポリエチレングリコールジステアレート等が挙げられる。市販品としては、商品名で、例えば、「エフトップEF301」、同EF303、同EF352(以上、トーケムプロダクツ社製)、「メガファック F171」、同F173(以上、大日本インキ化学工業社製)、「フロラードFC430」、同FC431(以上、住友スリーエム社製)、「アサヒガードAG710」、「サーフロンS−382」、同SC101、同SC102、同SC103、同SC104、同SC105、同SC106(以上、旭硝子社製)、「KP341」(信越化学工業社製)、「ポリフローNo.75」、同No.95(以上、共栄社化学社製)等が挙げられる。
界面活性剤の含有量としては、[A]重合体100質量部に対して、通常、2質量部以下である。界面活性剤は、1種又は2種以上を用いることができる。
[増感剤]
増感剤は、[B]酸発生剤及び[C]他の酸発生剤の生成量を増加する作用を示すものであり、当該フォトレジスト組成物の「みかけの感度」を向上させる効果を奏する。増感剤としては、例えば、ローズベンガル類等が挙げられる。増感剤の含有量としては、[A]重合体100質量部に対して、通常、50質量部以下である。
増感剤は、[B]酸発生剤及び[C]他の酸発生剤の生成量を増加する作用を示すものであり、当該フォトレジスト組成物の「みかけの感度」を向上させる効果を奏する。増感剤としては、例えば、ローズベンガル類等が挙げられる。増感剤の含有量としては、[A]重合体100質量部に対して、通常、50質量部以下である。
<フォトレジスト組成物の調製方法>
当該フォトレジスト組成物は、例えば、[A]重合体、[B]酸発生剤、必要に応じて加える任意成分及び[F]溶媒を所定の割合で混合することにより調製できる。当該フォトレジスト組成物は、全固形分濃度が0.1〜50質量%、好ましくは1〜40質量%となるように各成分を溶媒に均一に溶解又は分散させた後、例えば、孔径0.2μm程度のフィルターで濾過することによって調製される。
当該フォトレジスト組成物は、例えば、[A]重合体、[B]酸発生剤、必要に応じて加える任意成分及び[F]溶媒を所定の割合で混合することにより調製できる。当該フォトレジスト組成物は、全固形分濃度が0.1〜50質量%、好ましくは1〜40質量%となるように各成分を溶媒に均一に溶解又は分散させた後、例えば、孔径0.2μm程度のフィルターで濾過することによって調製される。
<レジストパターンの形成方法>
当該フォトレジスト組成物を用いるレジストパターンの形成方法は、(1)レジスト膜形成工程、(2)露光工程及び(3)現像工程を有する。形成されるパターンがポジ型及びネガ型それぞれの場合に分けて以下説明する。
当該フォトレジスト組成物を用いるレジストパターンの形成方法は、(1)レジスト膜形成工程、(2)露光工程及び(3)現像工程を有する。形成されるパターンがポジ型及びネガ型それぞれの場合に分けて以下説明する。
[ポジ型レジストパターン]
以下、ポジ型レジストパターンの形成方法について説明する。
以下、ポジ型レジストパターンの形成方法について説明する。
[(1)レジスト膜形成工程]
本工程では、当該ポジ型のフォトレジスト組成物を基板上に塗布し、レジスト膜を形成する。基板としては、例えば、シリコンウェハー、アルミニウム等で被覆されたウェハー等が挙げられる。塗布方法としては、例えば、回転塗布、流延塗布、ロール塗布等が挙げられる。
本工程では、当該ポジ型のフォトレジスト組成物を基板上に塗布し、レジスト膜を形成する。基板としては、例えば、シリコンウェハー、アルミニウム等で被覆されたウェハー等が挙げられる。塗布方法としては、例えば、回転塗布、流延塗布、ロール塗布等が挙げられる。
当該フォトレジスト組成物を塗布した後、必要に応じて、70〜160℃程度の温度で加熱処理(以下、「プレベーク(PB)」ともいう。)を行ってもよい。
なお、環境雰囲気中に含まれる塩基性不純物等の影響を防止するため、例えば、特開平5−188598号公報等に記載の保護膜を、レジスト被膜上に設けることもできる。
[(2)露光工程]
本工程では、(1)工程で形成したレジスト膜に対し、所定のマスクパターンを介して露光を行う。
[(2)露光工程]
本工程では、(1)工程で形成したレジスト膜に対し、所定のマスクパターンを介して露光を行う。
、露光に使用される電磁波又は荷電粒子線としては、可視光線、紫外線、遠紫外線、X線等の電磁波、電子線、α線等の荷電粒子線等を適宜選択することができるが、ArFエキシマレーザー(波長193nm)又はKrFエキシマレーザー(波長248nm)で代表される遠紫外線が好ましく、特にKrFエキシマレーザー(波長248nm)が好ましい。露光量等の露光条件は、フォトレジスト組成物の配合組成や添加剤の種類等に応じて、適宜選定される。
なお、高精度で微細なレジストパターンを安定して形成するために、露光後に、70〜160℃の温度で30秒以上加熱処理(以下、「ポストエクスポージャーベーク(PEB)」ともいう。)を行なうことが好ましい。PEBの温度が70℃未満であると、基板の種類による感度のばらつきが増大するおそれがある。
[(3)現像工程]
本工程では、(2)工程の露光後に、アルカリ現像液を用いて現像を行い、ポジ型のレジストパターンを形成する。
本工程では、(2)工程の露光後に、アルカリ現像液を用いて現像を行い、ポジ型のレジストパターンを形成する。
アルカリ現像液としては、アルカリ金属水酸化物、アンモニア、モノ−、ジ−又はトリ−アルキルアミン類、モノ−、ジ−又はトリ−アルカノールアミン類、複素環式アミン類、テトラアルキルアンモニウムヒドロキシド類、コリン、1,8−ジアザビシクロ−[5.4.0]−7−ウンデセン、1,5−ジアザビシクロ−[4.3.0]−5−ノネン等のアルカリ性化合物を、通常、1〜10質量%、好ましくは1〜5質量%、特に好ましくは1〜3質量%の濃度となるように溶解させたアルカリ性水溶液が好適に用いられる。また、上記アルカリ現像液には、例えば、メタノールやエタノール等の水溶性有機溶媒や界面活性剤を適宜添加することもできる。
現像工程における処理条件としては、通常、10℃〜50℃で10秒〜200秒、好ましくは15℃〜30℃で15秒〜100秒、特に好ましくは20℃〜25℃で15秒〜90秒である。
[ネガ型レジストパターン]
以下、ネガ型レジストパターンの形成方法について説明する。
以下、ネガ型レジストパターンの形成方法について説明する。
[(1)レジスト膜形成工程]
本工程では、当該ネガ型のフォトレジスト組成物を基板上に塗布し、レジスト膜を形成する。用いる基板及び塗布方法としては、ポジ型の場合と同様である。また、プレベーク(PB)及びレジスト膜上の保護膜の形成についてもポジ型の場合と同様である。
本工程では、当該ネガ型のフォトレジスト組成物を基板上に塗布し、レジスト膜を形成する。用いる基板及び塗布方法としては、ポジ型の場合と同様である。また、プレベーク(PB)及びレジスト膜上の保護膜の形成についてもポジ型の場合と同様である。
[(2)露光工程]
本工程では、(1)工程で形成したレジスト膜に対し、所定のマスクパターンを介して露光を行う。この際、露光により[B]酸発生剤等から発生したスルホン酸等の作用により、[A]重合体中の酸性基が[E]架橋剤と反応して架橋される。このようにして、架橋された[A]重合体を有するレジスト膜の露光部は、アルカリ性の現像液に対する溶解性が低くなる。
本工程では、(1)工程で形成したレジスト膜に対し、所定のマスクパターンを介して露光を行う。この際、露光により[B]酸発生剤等から発生したスルホン酸等の作用により、[A]重合体中の酸性基が[E]架橋剤と反応して架橋される。このようにして、架橋された[A]重合体を有するレジスト膜の露光部は、アルカリ性の現像液に対する溶解性が低くなる。
露光後に加熱処理(PEB)を行うことが好ましい。このPEBにより、レジスト膜中の[E]架橋剤の架橋反応が円滑に進行する。PEBの加熱条件は、フォトレジスト組成物の配合組成によって変わるが、30〜200℃であることが好ましく、50〜170℃であることがさらに好ましい。
[(3)現像工程]
本工程では、(2)工程の露光後に、アルカリ現像液を用いて現像を行い、ネガ型のレジストパターンを形成する。
本工程では、(2)工程の露光後に、アルカリ現像液を用いて現像を行い、ネガ型のレジストパターンを形成する。
アルカリ現像液としては、例えば、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、けい酸ナトリウム、メタけい酸ナトリウム、アンモニア水、エチルアミン、n−プロピルアミン、ジエチルアミン、ジ−n−プロピルアミン、トリエチルアミン、メチルジエチルアミン、エチルジメチルアミン、トリエタノールアミン、テトラメチルアンモニウムヒドロキシド、ピロール、ピペリジン、コリン、1,8−ジアザビシクロ−[5.4.0]−7−ウンデセン、及び1,5−ジアザビシクロ−[4.3.0]−5−ノネン等のアルカリ性化合物からなる群より選択される少なくとも1種を溶解したアルカリ性水溶液が挙げられる。上記アルカリ性水溶液の濃度は、10質量%以下であることが好ましい。アルカリ性水溶液の濃度が10質量%を超えると、非露光部も現像液に溶解してしまうおそれがある。
現像液には、例えば、有機溶媒を添加することもできる。このような有機溶媒としては、例えば、
アセトン、メチルエチルケトン、メチルi−ブチルケトン、シクロペンタノン、シクロヘキサノン、3−メチルシクロペンタノン、2,6−ジメチルシクロヘキサノン等のケトン類;
メチルアルコール、エチルアルコール、n−プロピルアルコール、i−プロピルアルコール、n−ブチルアルコール、t−ブチルアルコール、シクロペンタノール、シクロヘキサノール、1,4−ヘキサンジオール、1,4−ヘキサンジメチロール等のアルコール類;
テトラヒドロフラン、ジオキサン等のエーテル類;
酢酸エチル、酢酸n−ブチル、酢酸i−アミル等のエステル類;
トルエン、キシレン等の芳香族炭化水素類;
フェノール、アセトニルアセトン、ジメチルホルムアミド等が挙げられる。なお、これらの有機溶媒は、1種又は2種以上を用いることができる。
アセトン、メチルエチルケトン、メチルi−ブチルケトン、シクロペンタノン、シクロヘキサノン、3−メチルシクロペンタノン、2,6−ジメチルシクロヘキサノン等のケトン類;
メチルアルコール、エチルアルコール、n−プロピルアルコール、i−プロピルアルコール、n−ブチルアルコール、t−ブチルアルコール、シクロペンタノール、シクロヘキサノール、1,4−ヘキサンジオール、1,4−ヘキサンジメチロール等のアルコール類;
テトラヒドロフラン、ジオキサン等のエーテル類;
酢酸エチル、酢酸n−ブチル、酢酸i−アミル等のエステル類;
トルエン、キシレン等の芳香族炭化水素類;
フェノール、アセトニルアセトン、ジメチルホルムアミド等が挙げられる。なお、これらの有機溶媒は、1種又は2種以上を用いることができる。
上記現像液中の有機溶媒の含有割合は、上記アルカリ性水溶液100体積部に対して、100体積部以下であることが好ましい。有機溶媒の含有割合が100体積部を超えると、現像性が低下して、露光部の現像残りが多くなるおそれがある。また、現像液には、界面活性剤等を適量添加することもできる。なお、現像液で現像した後、水で洗浄して乾燥することが好ましい。
上述の形成方法により、レジスト膜の未露光部が現像液により溶解、除去されることによって、ネガ型のレジストパターンを形成することができる。
以下、本発明を実施例に基づいて具体的に説明するが、本発明はこれらの実施例に限定されるものではない。各種物性値の測定方法を以下に示す。
<重量平均分子量(Mw)、数平均分子量(Mn)>
重合体のMw及びMnは、東ソー株式会社製GPCカラム(G2000HXL 2本、G3000HXL 1本、G4000HXL 1本)を用い、流量1.0mL/分、溶出溶媒テトラヒドロフラン、カラム温度40℃の分析条件で、単分散ポリスチレンを標準とするゲルパーミエーションクロマトグラフィー(GPC)により測定した。
重合体のMw及びMnは、東ソー株式会社製GPCカラム(G2000HXL 2本、G3000HXL 1本、G4000HXL 1本)を用い、流量1.0mL/分、溶出溶媒テトラヒドロフラン、カラム温度40℃の分析条件で、単分散ポリスチレンを標準とするゲルパーミエーションクロマトグラフィー(GPC)により測定した。
<13C−NMR分析>
重合体の13C−NMR分析は、核磁気共鳴装置(日本電子株式会社製「JNM−ECX400」)を使用し、測定した。
重合体の13C−NMR分析は、核磁気共鳴装置(日本電子株式会社製「JNM−ECX400」)を使用し、測定した。
<[A]重合体の合成>
[A]重合体の合成に用いた単量体(下記式(L−1)〜(L−5)でそれぞれ表される化合物(以下、「化合物(L−1)」のように称する。))を以下に表す。
[A]重合体の合成に用いた単量体(下記式(L−1)〜(L−5)でそれぞれ表される化合物(以下、「化合物(L−1)」のように称する。))を以下に表す。
[合成例1](重合体(A−1)の合成)
上記化合物(L−1)117g(72モル%)、化合物(L−2)41g(23モル%)、化合物(L−3)5g(5モル%)、アゾビスイソブチロニトリル(AIBN)6g及びt−ドデシルメルカプタン1gを、プロピレングリコールモノメチルエーテル160gに溶解した後、窒素雰囲気下、反応温度を70℃に保持して、16時間重合反応を行った。重合後、反応溶液を大量のn−ヘキサン中に滴下し、生成重合体を凝固させて精製した。
上記化合物(L−1)117g(72モル%)、化合物(L−2)41g(23モル%)、化合物(L−3)5g(5モル%)、アゾビスイソブチロニトリル(AIBN)6g及びt−ドデシルメルカプタン1gを、プロピレングリコールモノメチルエーテル160gに溶解した後、窒素雰囲気下、反応温度を70℃に保持して、16時間重合反応を行った。重合後、反応溶液を大量のn−ヘキサン中に滴下し、生成重合体を凝固させて精製した。
次いで、この精製して得られた重合体に、プロピレングリコールモノメチルエーテル150gを加えた後、さらにメタノール300g、トリエチルアミン80g及び水15gを加えて、沸点にて還流させながら、8時間加水分解反応を行なった。反応後、溶媒およびトリエチルアミンを減圧留去し、得られた重合体をアセトンに溶解した後、大量の水中に滴下して凝固させ、生成した白色粉末をろ過して、減圧下50℃で一晩乾燥し、重合体(A−1)を得た(94g、収率71%)。
得られた重合体(A−1)は、Mwが16,000、Mw/Mnが1.7であった。また、13C−NMR分析の結果、下記式(A1)で表される構造単位:下記式(A2)で表される構造単位:下記式(A3)で表される構造単位の含有割合比(モル比)は、72:5:23であった。
[合成例2](重合体(A−2)の合成)
上記化合物(L−1)182g(73モル%)、化合物(L−2)66g(24モル%)、化合物(L−4)11g(重合性基基準で3モル%)、AIBN14g及びt−ドデシルメルカプタン11gを、プロピレングリコールモノメチルエーテル240gに溶解した後、窒素雰囲気下、反応温度を70℃に保持して、16時間重合反応を行った。重合後、反応溶液を大量のn−ヘキサン中に滴下して、生成重合体を凝固させて精製し、減圧下50℃で3時間乾燥した。
上記化合物(L−1)182g(73モル%)、化合物(L−2)66g(24モル%)、化合物(L−4)11g(重合性基基準で3モル%)、AIBN14g及びt−ドデシルメルカプタン11gを、プロピレングリコールモノメチルエーテル240gに溶解した後、窒素雰囲気下、反応温度を70℃に保持して、16時間重合反応を行った。重合後、反応溶液を大量のn−ヘキサン中に滴下して、生成重合体を凝固させて精製し、減圧下50℃で3時間乾燥した。
次いで、この精製して得られた重合体190gに、プロピレングリコールモノメチルエーテル150gを加えた後、さらにメタノール300g、トリエチルアミン100g及び水15gを加えて、沸点にて還流させながら、8時間加水分解反応を行なった。反応後、溶媒及びトリエチルアミンを減圧留去し、得られた重合体をアセトンに溶解した後、大量の水中に滴下して凝固させ、生成した白色粉末をろ過して、減圧下50℃で一晩乾燥し、重合体(A−2)を得た(157g、収率74%)。
得られた重合体(A−2)は、Mwが27,000、Mw/Mnが2.6であった。また、13C−NMR分析の結果、下記式(A1)で表される構造単位:下記式(A3)で表される構造単位:下記式(A4a)で表される構造単位の含有割合比(モル比)は、75:22:3であった。
[合成例3](重合体(A−3)の合成)
上記化合物(L−1)114g(69モル%)、化合物(L−2)35g(20モル%)及び化合物(L−5)11g(11モル%)、AIBN6g及びt−ドデシルメルカプタン1gを、プロピレングリコールモノメチルエーテル160gに溶解した後、窒素雰囲気下、反応温度を70℃に保持して、16時間重合反応を行った。重合後、反応溶液を大量のn−ヘキサン中に滴下し、生成重合体を凝固させて精製した。
上記化合物(L−1)114g(69モル%)、化合物(L−2)35g(20モル%)及び化合物(L−5)11g(11モル%)、AIBN6g及びt−ドデシルメルカプタン1gを、プロピレングリコールモノメチルエーテル160gに溶解した後、窒素雰囲気下、反応温度を70℃に保持して、16時間重合反応を行った。重合後、反応溶液を大量のn−ヘキサン中に滴下し、生成重合体を凝固させて精製した。
次いで、この精製して得られた重合体に、プロピレングリコールモノメチルエーテル150gを加えた後、さらにメタノール300g、トリエチルアミン80g及び水15gを加えて、沸点にて還流させながら、8時間加水分解反応を行なった。反応後、溶媒およびトリエチルアミンを減圧留去し、得られた重合体をアセトンに溶解した後、大量の水中に滴下して凝固させ、生成した白色粉末をろ過して、減圧下50℃で一晩乾燥し、重合体(A−3)を得た(94g、収率72%)。
得られた重合体(A−3)は、Mwが14,000、Mw/Mnが1.7であった。また、13C−NMR分析の結果、下記式(A1)で表される構造単位:下記式(A3)で表される構造単位:下記式(A5)で表される構造単位の含有割合比(モル比)が70:20:10であった。
<フォトレジスト組成物の調製>
上記合成例で合成した重合体(A−1)〜(A−3)以外のフォトレジスト組成物を構成する各成分([A]重合体、[B]酸発生剤、[C]他の酸発生剤、[D]酸拡散抑制剤、[E]架橋剤及び[F]溶媒)について以下に示す。
上記合成例で合成した重合体(A−1)〜(A−3)以外のフォトレジスト組成物を構成する各成分([A]重合体、[B]酸発生剤、[C]他の酸発生剤、[D]酸拡散抑制剤、[E]架橋剤及び[F]溶媒)について以下に示す。
[[A]重合体]
(A―4):ヒドロキシスチレン/スチレン共重合体(上記化合物(L−1)と化合物(L−3)とを共重合(重合仕込みモル比=8:2)した後、加水分解して得られる重合体であり、Mw=4,000、Mw/Mn=1.5、上記式(A1)で表される構造単位:上記式(A2)で表される構造単位の含有割合比(モル比)は79:21であった。)
(A―5):ヒドロキシスチレン/スチレン共重合体(上記化合物(L−1)と化合物(L−3)とを共重合(重合仕込みモル比=7:3)した後、加水分解して得られる重合体であり、Mw=4,000、Mw/Mn=1.5、上記式(A1)で表される構造単位:上記式(A2)で表される構造単位の含有割合比(モル比)は68:32であった。)
(A―4):ヒドロキシスチレン/スチレン共重合体(上記化合物(L−1)と化合物(L−3)とを共重合(重合仕込みモル比=8:2)した後、加水分解して得られる重合体であり、Mw=4,000、Mw/Mn=1.5、上記式(A1)で表される構造単位:上記式(A2)で表される構造単位の含有割合比(モル比)は79:21であった。)
(A―5):ヒドロキシスチレン/スチレン共重合体(上記化合物(L−1)と化合物(L−3)とを共重合(重合仕込みモル比=7:3)した後、加水分解して得られる重合体であり、Mw=4,000、Mw/Mn=1.5、上記式(A1)で表される構造単位:上記式(A2)で表される構造単位の含有割合比(モル比)は68:32であった。)
[[B]酸発生剤]
下記式(B−1)〜(B−5)でそれぞれ表される化合物
下記式(B−1)〜(B−5)でそれぞれ表される化合物
[[C]他の酸発生剤]
(C−1)トリフェニルスルホニウム10−カンファースルホネート(下記式(C−1)で表される化合物)
(C−1)トリフェニルスルホニウム10−カンファースルホネート(下記式(C−1)で表される化合物)
(C−2):N−(トリフルオロメタンスルホニルオキシ)ビシクロ[2.2.1]ヘプト−5−エン−2,3−ジカルボキシイミド
(C−3):2,4,6−トリメチルフェニルジフェニルスルホニウム2,4−ジフルオロベンゼンスルホネート
(C−4):トリフェニルスルホニウムp−トルエンスルホネート
(C−5):トリフェニルスルホニウムトリフルオロメタンスルホネート
(C−3):2,4,6−トリメチルフェニルジフェニルスルホニウム2,4−ジフルオロベンゼンスルホネート
(C−4):トリフェニルスルホニウムp−トルエンスルホネート
(C−5):トリフェニルスルホニウムトリフルオロメタンスルホネート
[[D]酸拡散制御剤]
(D−1):2−フェニルベンズイミダゾール
(D−1):2−フェニルベンズイミダゾール
[[E]架橋剤]
(E−1):1,3,4,6−テトラキス(メトキシメチル)グリコールウリル
(E−1):1,3,4,6−テトラキス(メトキシメチル)グリコールウリル
[[F]溶媒]
(F−1):乳酸エチル
(F−2):プロピレングリコールモノメチルエーテルアセテート
(F−1):乳酸エチル
(F−2):プロピレングリコールモノメチルエーテルアセテート
[実施例1]
重合体(A−1)100質量部、酸発生剤(B−5)2質量部、他の酸発生剤(C−2)10質量部、酸拡散制御剤(D−1)0.4質量部、並びに溶媒(F−1)350質量部及び溶媒(F−2)800質量部を混合し、得られた混合溶液を孔径0.2μmのテフロン(登録商標)製メンブレンフィルターでろ過することにより、実施例1に係るポジ型のフォトレジスト組成物(J−1)を調製した。
重合体(A−1)100質量部、酸発生剤(B−5)2質量部、他の酸発生剤(C−2)10質量部、酸拡散制御剤(D−1)0.4質量部、並びに溶媒(F−1)350質量部及び溶媒(F−2)800質量部を混合し、得られた混合溶液を孔径0.2μmのテフロン(登録商標)製メンブレンフィルターでろ過することにより、実施例1に係るポジ型のフォトレジスト組成物(J−1)を調製した。
[実施例2〜14及び比較例1〜4]
表2に示す種類及び配合量の各成分を使用した以外は、実施例1と同様にして、実施例2〜14のフォトレジスト組成物(J−2)〜(J−14)及び比較例1〜4のフォトレジスト組成物(CJ−1)〜(CJ−4)を調製した。表2中の「−」は該当する成分を使用しなかったことを示す。なお、フォトレジスト組成物(J−2)〜(J−11)及び(CJ−1)〜(CJ−3)はポジ型のフォトレジスト組成物であり、フォトレジスト組成物(J−12)〜(J−14)及び(CJ−4)はネガ型のフォトレジスト組成物である。
表2に示す種類及び配合量の各成分を使用した以外は、実施例1と同様にして、実施例2〜14のフォトレジスト組成物(J−2)〜(J−14)及び比較例1〜4のフォトレジスト組成物(CJ−1)〜(CJ−4)を調製した。表2中の「−」は該当する成分を使用しなかったことを示す。なお、フォトレジスト組成物(J−2)〜(J−11)及び(CJ−1)〜(CJ−3)はポジ型のフォトレジスト組成物であり、フォトレジスト組成物(J−12)〜(J−14)及び(CJ−4)はネガ型のフォトレジスト組成物である。
<評価>
上記実施例1〜14のフォトレジスト組成物(J−1)〜(J−14)及び比較例1〜4のフォトレジスト組成物(CJ−1)〜(CJ−4)について、下記方法により、レジストパターンを形成し、感度、ナノエッジラフネス及び焦点深度について評価した。
上記実施例1〜14のフォトレジスト組成物(J−1)〜(J−14)及び比較例1〜4のフォトレジスト組成物(CJ−1)〜(CJ−4)について、下記方法により、レジストパターンを形成し、感度、ナノエッジラフネス及び焦点深度について評価した。
[レジストパターンの形成]
各フォトレジスト組成物をシリコンウエハ上に回転塗布した後、110℃で90秒間PBを行なって、膜厚0.25μmのレジスト膜を形成した。その後、各レジスト膜に、KrFエキシマレーザー照射装置(株式会社ニコン製「NSR−S203B」)を用い、KrFエキシマレーザー(波長248nm)を、マスクパターンを介し露光量を変えて露光したのち、110℃で90秒間PEBを行なった。その後、2.38質量%テトラメチルアンモニウムヒドロキシド水溶液を現像液として用い、23℃で60秒間現像した後、水で30秒間洗浄し、乾燥して、レジストパターンを形成した。
各フォトレジスト組成物をシリコンウエハ上に回転塗布した後、110℃で90秒間PBを行なって、膜厚0.25μmのレジスト膜を形成した。その後、各レジスト膜に、KrFエキシマレーザー照射装置(株式会社ニコン製「NSR−S203B」)を用い、KrFエキシマレーザー(波長248nm)を、マスクパターンを介し露光量を変えて露光したのち、110℃で90秒間PEBを行なった。その後、2.38質量%テトラメチルアンモニウムヒドロキシド水溶液を現像液として用い、23℃で60秒間現像した後、水で30秒間洗浄し、乾燥して、レジストパターンを形成した。
[感度]
線幅160nmのライン部と、隣り合うライン部によって形成される間隔が160nmのスペース部(すなわち、溝)とからなるパターン(いわゆる、ライン・アンド・スペースパターン(1L1S))を1対1の線幅に形成する露光量を最適露光量とし、この最適露光量を感度(単位:mJ/cm2)とした。
線幅160nmのライン部と、隣り合うライン部によって形成される間隔が160nmのスペース部(すなわち、溝)とからなるパターン(いわゆる、ライン・アンド・スペースパターン(1L1S))を1対1の線幅に形成する露光量を最適露光量とし、この最適露光量を感度(単位:mJ/cm2)とした。
[ナノエッジラフネス]
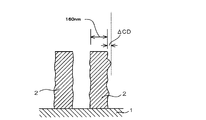
設計線幅160nmのライン・アンド・スペースパターン(1L1S)のラインパターンを、半導体用走査電子顕微鏡(高分解能FEB測長装置、日立製作所社製「S−9220」)にて観察した。観察された形状について、図1及び図2に示すように、シリコンウエハー1上に形成したレジスト被膜のライン部2の横側面2aに沿って生じた凹凸の最も著しい箇所における線幅と、設計線幅160nmとの差「ΔCD」を測定することによりナノエッジラフネス(単位:nm)を評価した。
設計線幅160nmのライン・アンド・スペースパターン(1L1S)のラインパターンを、半導体用走査電子顕微鏡(高分解能FEB測長装置、日立製作所社製「S−9220」)にて観察した。観察された形状について、図1及び図2に示すように、シリコンウエハー1上に形成したレジスト被膜のライン部2の横側面2aに沿って生じた凹凸の最も著しい箇所における線幅と、設計線幅160nmとの差「ΔCD」を測定することによりナノエッジラフネス(単位:nm)を評価した。
[焦点深度(DOF)]
線幅1600nmのライン部と、隣り合うライン部によって形成される間隔が160nmのスペース部(すなわち、溝)とからなるパターン(10ライン1スペースパターン(10L1S))を孤立スペースパターン(ISパターン)とし、このパターンのスペース部が160nmで形成される露光量で焦点深度(DOF(Depth of Focus))(単位:μm)を測定した。焦点深度は0.05μmステップで露光されたISパターンを上記半導体用走査電子顕微鏡にて観察し、スペースが基板まで到達している場合を解像していると判断して測定した。
線幅1600nmのライン部と、隣り合うライン部によって形成される間隔が160nmのスペース部(すなわち、溝)とからなるパターン(10ライン1スペースパターン(10L1S))を孤立スペースパターン(ISパターン)とし、このパターンのスペース部が160nmで形成される露光量で焦点深度(DOF(Depth of Focus))(単位:μm)を測定した。焦点深度は0.05μmステップで露光されたISパターンを上記半導体用走査電子顕微鏡にて観察し、スペースが基板まで到達している場合を解像していると判断して測定した。
得られたこれらの評価結果を下記表3に示す。なお、比較例3における「(*1)」は、レジストパターンを解像できなかったことを示す。
表3の結果から明らかなように、特定の炭化水素基を有し、かつ所定値以上の炭素数を有する酸発生剤(B−1)〜(B−5)を含有する実施例1〜14のフォトレジスト組成物は、構成炭素数が所定値未満の他の酸発生剤のみを含有する比較例1〜4のフォトレジスト組成物に比べて、ナノエッジラフネス抑制性に優れ、かつ焦点深度にも優れることが示された。
本発明によれば、ナノエッジラフネスを抑制することができ、かつ焦点深度にも優れるフォトレジスト組成物を提供することができる。従って、本発明はリソグラフィーによる微細加工に好適である。
1 基材
2 レジストパターン
2a レジストパターンの横側面
2 レジストパターン
2a レジストパターンの横側面
Claims (8)
- [A]下記式(1−1)で表される構造単位(I)を有する重合体、及び
[B]下記式(2)で表される酸発生剤
を含有するフォトレジスト組成物。
- 上記鎖状炭化水素基が分岐状である請求項1に記載のフォトレジスト組成物。
- 上記R1が、少なくとも1つのエステル結合を有する有機基である請求項1又は請求項2に記載のフォトレジスト組成物。
- ポジ型である請求項1から請求項6のいずれか1項に記載のフォトレジスト組成物。
- [E]架橋剤をさらに含有し、ネガ型である請求項1から請求項5のいずれか1項に記載のフォトレジスト組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011057313A JP2012194292A (ja) | 2011-03-15 | 2011-03-15 | フォトレジスト組成物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011057313A JP2012194292A (ja) | 2011-03-15 | 2011-03-15 | フォトレジスト組成物 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2012194292A true JP2012194292A (ja) | 2012-10-11 |
Family
ID=47086269
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011057313A Pending JP2012194292A (ja) | 2011-03-15 | 2011-03-15 | フォトレジスト組成物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2012194292A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018131443A (ja) * | 2012-12-26 | 2018-08-23 | 東京応化工業株式会社 | 化合物 |
| WO2018168252A1 (ja) * | 2017-03-13 | 2018-09-20 | 富士フイルム株式会社 | 感活性光線性又は感放射線性樹脂組成物、レジスト膜、パターン形成方法、及び電子デバイスの製造方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010100604A (ja) * | 2008-09-26 | 2010-05-06 | Fujifilm Corp | 感活性光線性または感放射線性樹脂組成物、及び該感光性組成物を用いたパターン形成方法 |
| JP2010256858A (ja) * | 2009-01-30 | 2010-11-11 | Fujifilm Corp | ネガ型レジストパターン形成方法、それに用いられる現像液及びネガ型化学増幅型レジスト組成物、並びにレジストパターン |
| JP2011013581A (ja) * | 2009-07-03 | 2011-01-20 | Fujifilm Corp | 感活性光線性又は感放射性樹脂組成物及びそれを用いたパターン形成方法 |
| JP2011048142A (ja) * | 2009-08-27 | 2011-03-10 | Sumitomo Chemical Co Ltd | レジスト組成物及びパターン形成方法 |
| WO2011030737A1 (ja) * | 2009-09-11 | 2011-03-17 | Jsr株式会社 | 感放射線性組成物及び新規化合物 |
| JP2012003249A (ja) * | 2010-05-19 | 2012-01-05 | Tokyo Ohka Kogyo Co Ltd | レジスト組成物、レジストパターン形成方法、新規な化合物及び酸発生剤 |
-
2011
- 2011-03-15 JP JP2011057313A patent/JP2012194292A/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010100604A (ja) * | 2008-09-26 | 2010-05-06 | Fujifilm Corp | 感活性光線性または感放射線性樹脂組成物、及び該感光性組成物を用いたパターン形成方法 |
| JP2010256858A (ja) * | 2009-01-30 | 2010-11-11 | Fujifilm Corp | ネガ型レジストパターン形成方法、それに用いられる現像液及びネガ型化学増幅型レジスト組成物、並びにレジストパターン |
| JP2011013581A (ja) * | 2009-07-03 | 2011-01-20 | Fujifilm Corp | 感活性光線性又は感放射性樹脂組成物及びそれを用いたパターン形成方法 |
| JP2011048142A (ja) * | 2009-08-27 | 2011-03-10 | Sumitomo Chemical Co Ltd | レジスト組成物及びパターン形成方法 |
| WO2011030737A1 (ja) * | 2009-09-11 | 2011-03-17 | Jsr株式会社 | 感放射線性組成物及び新規化合物 |
| JP2012003249A (ja) * | 2010-05-19 | 2012-01-05 | Tokyo Ohka Kogyo Co Ltd | レジスト組成物、レジストパターン形成方法、新規な化合物及び酸発生剤 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018131443A (ja) * | 2012-12-26 | 2018-08-23 | 東京応化工業株式会社 | 化合物 |
| WO2018168252A1 (ja) * | 2017-03-13 | 2018-09-20 | 富士フイルム株式会社 | 感活性光線性又は感放射線性樹脂組成物、レジスト膜、パターン形成方法、及び電子デバイスの製造方法 |
| JPWO2018168252A1 (ja) * | 2017-03-13 | 2019-12-19 | 富士フイルム株式会社 | 感活性光線性又は感放射線性樹脂組成物、レジスト膜、パターン形成方法、及び電子デバイスの製造方法 |
| JP7015295B2 (ja) | 2017-03-13 | 2022-02-02 | 富士フイルム株式会社 | 感活性光線性又は感放射線性樹脂組成物、レジスト膜、パターン形成方法、及び電子デバイスの製造方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4103523B2 (ja) | レジスト組成物 | |
| JP4830442B2 (ja) | ポジ型感放射線性樹脂組成物 | |
| JP4544085B2 (ja) | ポジ型感放射線性樹脂組成物 | |
| JP6292059B2 (ja) | 基板の加工方法 | |
| JP4946094B2 (ja) | 新規化合物、それを用いた感放射線性酸発生剤及びポジ型感放射線性樹脂組成物 | |
| JP4910238B2 (ja) | 化学増幅型感放射線性樹脂組成物 | |
| JP4665810B2 (ja) | ポジ型感放射線性樹脂組成物 | |
| JP2009258598A (ja) | 感放射線性組成物及びパターン形成方法 | |
| JP5741289B2 (ja) | フォトレジスト組成物 | |
| JP4774996B2 (ja) | 感放射線性樹脂組成物 | |
| JP2007297284A (ja) | スルホニウム塩化合物および感放射線性樹脂組成物 | |
| JP5761196B2 (ja) | 感放射線性樹脂組成物 | |
| JP4877231B2 (ja) | 感放射線性樹脂組成物 | |
| JP2004302440A (ja) | レジスト組成物 | |
| JP2004054209A (ja) | パターン形成方法および感放射線性樹脂組成物 | |
| JP2016133743A (ja) | レジストパターン形成方法及び基板の加工方法 | |
| JP4360264B2 (ja) | ポジ型感放射線性樹脂組成物 | |
| JP5509660B2 (ja) | 感放射線性樹脂組成物の製造方法 | |
| JP2012194292A (ja) | フォトレジスト組成物 | |
| JP2009223024A (ja) | ポジ型感放射線性樹脂組成物 | |
| JP4924256B2 (ja) | 感放射線性樹脂組成物 | |
| JP4650175B2 (ja) | 感放射線性樹脂組成物及びそれに用いる感放射性の酸発生剤 | |
| JP4045982B2 (ja) | 感放射線性樹脂組成物 | |
| JP4710685B2 (ja) | ポジ型感放射線性樹脂組成物 | |
| JP5392098B2 (ja) | 感放射線性組成物の製造方法及びレジスト膜の膜厚制御方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130808 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140519 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140527 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140930 |