JP2010529167A - 神経変性疾患または血液疾患の治療のための[1,10]−フェナントロリン誘導体 - Google Patents
神経変性疾患または血液疾患の治療のための[1,10]−フェナントロリン誘導体 Download PDFInfo
- Publication number
- JP2010529167A JP2010529167A JP2010511627A JP2010511627A JP2010529167A JP 2010529167 A JP2010529167 A JP 2010529167A JP 2010511627 A JP2010511627 A JP 2010511627A JP 2010511627 A JP2010511627 A JP 2010511627A JP 2010529167 A JP2010529167 A JP 2010529167A
- Authority
- JP
- Japan
- Prior art keywords
- phenanthroline
- compound
- carbaldehyde
- alkyl
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 *c1cc(C=N*)nc2c1ccc1c2nccc1 Chemical compound *c1cc(C=N*)nc2c1ccc1c2nccc1 0.000 description 2
- RWXRKPTUONDSEA-UHFFFAOYSA-N Cc1cc(OCCOC)c(ccc2c3nccc2)c3n1 Chemical compound Cc1cc(OCCOC)c(ccc2c3nccc2)c3n1 RWXRKPTUONDSEA-UHFFFAOYSA-N 0.000 description 2
- AEXLFFUDBSFTKU-GIJQJNRQSA-N CC(C)Sc1c(ccc2c3nccc2)c3nc(/C=N/O)c1 Chemical compound CC(C)Sc1c(ccc2c3nccc2)c3nc(/C=N/O)c1 AEXLFFUDBSFTKU-GIJQJNRQSA-N 0.000 description 1
- BWIZIVLLXVTVQS-UHFFFAOYSA-N CC(C)Sc1c(ccc2c3nccc2)c3nc(C=O)c1 Chemical compound CC(C)Sc1c(ccc2c3nccc2)c3nc(C=O)c1 BWIZIVLLXVTVQS-UHFFFAOYSA-N 0.000 description 1
- LDVCBRUWLAPPAI-UHFFFAOYSA-N COCCOc1c(ccc2c3nccc2)c3nc(C=O)c1 Chemical compound COCCOc1c(ccc2c3nccc2)c3nc(C=O)c1 LDVCBRUWLAPPAI-UHFFFAOYSA-N 0.000 description 1
- GMKFEESYFPUWNQ-UHFFFAOYSA-N Cc1cc(Cl)c(ccc2c3nccc2)c3n1 Chemical compound Cc1cc(Cl)c(ccc2c3nccc2)c3n1 GMKFEESYFPUWNQ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/02—Non-specific cardiovascular stimulants, e.g. drugs for syncope, antihypotensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Diabetes (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Psychiatry (AREA)
- Hematology (AREA)
- Pain & Pain Management (AREA)
- Emergency Medicine (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Endocrinology (AREA)
- Obesity (AREA)
- Hospice & Palliative Care (AREA)
- Psychology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Description
本発明は、神経変性または血液の疾患または状態、特にアルツハイマー病(AD)の治療および/または予防のためのいくつかの[1,10]−フェナントロリン誘導体の使用に関する。加えて、新規[1,10]−フェナントロリン誘導体、かかる化合物を製造するための方法およびそれらを含んでなる医薬組成物を提供する。
ADとパーキンソン病(PD)は、最もよく見られる進行性神経変性疾患であり、世界中で何百万人もの人々が罹患している。かなりの割合の患者が両疾患からの共通の臨床的および病理学的症状を抱えているため、これは共通の病理学的機構が存在することを示しているように思われる。
R7は、−CH=N−OR8または−CHOから選択され;
R3およびR4は、C1−C6アルキル、場合によってC1−C6アルキル、C6−C15アリール、ハロゲン(好ましくは1〜6個、より好ましくは1〜3個のハロゲン原子で)、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている、C6−C15アリールおよびヘテロアリールからなる群から独立に選択され、
R5およびR6は、水素およびC1−C6アルキルから独立に選択され、
R8は、水素およびC1−C6アルキルから選択される)
の化合物;あるいはそれらの任意の塩または溶媒和物または立体異性体または互変異性体の使用に向けられる。
R7は、−CH=N−OR8または−CHOから選択され;
R3およびR4は、C1−C6アルキル、場合によってC1−C6アルキル、C6−C15アリール、ハロゲン、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている、C6−C15アリールおよびヘテロアリールからなる群から独立に選択され、
R5およびR6は、水素およびC1−C6アルキルから独立に選択され、
R8は、水素およびC1−C6アルキルから選択される)
の化合物;あるいはそれらの任意の塩または溶媒和物または立体異性体または互変異性体(ただし、R1がClである場合には、R7は−CHOではない)に向けられる。
「C1−C6アルキル」とは、炭素原子と水素原子からなる、不飽和を含まない、1〜6個、好ましくは1〜3個の炭素原子を有する線状または分枝状炭化水素鎖ラジカルを指し、この線状または分枝状炭化水素鎖ラジカルは、残りの分子と一重結合によって結合している。例えば、メチル、エチル、n−プロピル、i−プロピル、n−ブチル、t−ブチル、n−ペンチルなどがある。
一つの実施態様によれば、本発明は、式(I)(式中、
R1は、−S−R3、−O−R4およびハロゲンから選択され;
R7は、−CH=N−OR8または−CHOから選択され;
R3およびR4は、独立に、場合によってC1−C6アルコキシおよび/または−NR5R6で置換されている、C1−C6アルキルであり、
R5およびR6は、水素およびC1−C6アルキルから独立に選択され、
R8は、水素およびC1−C6アルキルから選択される)
の化合物の使用に向けられる。
4−メトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−クロロ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−クロロ−[1,10]フェナントロリン−2−カルバルデヒド;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−アミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
2−[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−N,N−ジメチル−アセトアミド;
4−(2,2,2−トリフルオロ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸メチルエステル;
4−(チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸;
4−(5−メチル−チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(5−メチル−[1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−([1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒド;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
あるいはそれらの塩、溶媒和物または立体異性体または互変異性体から選択される。
本発明の実施態様は、式(I)
(式中、
R1は、−S−R3、−O−R4およびハロゲンから選択され;
R7は、−CH=N−OR8または−CHOから選択され;
R3およびR4は、独立に、場合によってC1−C6アルコキシおよび/または−NR5R6で置換されている、C1−C6アルキルであり、
R5およびR6は、水素およびC1−C6アルキルから独立に選択され、
R8は、水素およびC1−C6アルキルから選択される)
の化合物、あるいはそれらの任意の塩または溶媒和物または立体異性体(ただし、R1がClまたはOCH3である場合には、R7は−CHOまたは−CH=N−OHではない)
に向けられる。
4−メトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−アミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
2−[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−N,N−ジメチル−アセトアミド;
4−(2,2,2−トリフルオロ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸メチルエステル;
4−(チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸;
4−(5−メチル−チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(5−メチル−[1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−([1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒド;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
およびそれらの塩または溶媒和物または立体異性体または互変異性体から選択される。
さらなる態様によれば、本発明は、上記に定義した少なくとも1種の式(I)化合物、それらの塩または溶媒和物または立体異性体または互変異性体と、少なくとも1種の薬学上許容される担体とを含んでなる医薬組成物に向けられる。
本発明の化合物は、当技術分野で公知の反応の組合せによって製造してよい。
a)式(I)の化合物を形成するために酸化剤を用いて式(II)の化合物のメチル基を酸化すること:
および所望により、
b)ヒドロキシルアミンまたはO−(C1−C6)アルキルヒドロキシルアミンの存在下で、式(I)の化合物中のアルデヒド基−CHOを、R8が水素およびC1−C6アルキルから選択されたオキシム基−CH=N−OR8へと変換すること:
a)式(II)の化合物を形成するために、化合物 式(III)を式−OR3または−OR4の対応するアルコキシドまたはチオラートのナトリウム塩と反応させること:
Xは、ハロゲンであり;
R1は、−S−R3、−O−R4およびハロゲンから選択され;
R3およびR4は、C1−C6アルキル、場合によってC1−C6アルキル、C6−C15アリール、ハロゲン、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている、C6−C15アリールおよびヘテロアリールからなる群から独立に選択される;
ただし、式(II)中のR1がハロゲンである場合には、この工程は省略される);
b)式(I)の化合物を形成するために酸化剤を用いて式(II)の化合物のメチル基を酸化すること;
および所望により、
c)ヒドロキシルアミンまたはO−(C1−C6)アルキルヒドロキシルアミンの存在下で、式(I)の化合物中のアルデヒド基−CHOを、R8が水素およびC1−C6アルキルから選択されたオキシム基−CH=N−OR8へと変換すること:
:を含む方法に関する。
本発明による式(I)化合物を、以下に詳述する一般的な製法に従って製造した。
1.2−メチル−[1,10]フェナトロリン−4−オール(2-Methyl-[1,10]phenathrolin-4-ol)の製造
合成手順は、Hazlewood, S. J.; Hughes, G. K.; Lions F., J. Proc. R. Soc. N. S. W. 1938, 71, 462-474から適合させた。
合成手順は、Harrison R. J.; Cuesta J.; Chessari, G.; Read M. A.; Basra, S. K.; Reszka, A. P.; Morrell, J.; Gowan, S. M.; Incles, C. M.; Tanious, F. A.; Wilson, W. D.; Kelland, L. R.; Neidle, S., J. Med. Chem. 2003, 46, 4463-4476から適合させた。
11.95 (s, 1H); 9.12 (dd, 1H, J= 1.6, 4.2 Hz); 8.50 (dd, 1H, J= 1.6, 8.1 Hz); 8.33 (s, 1H); 8.06 (AB system, 2H, SAB= 9.1 Hz); 7.92 (s, 1H); 7.78 (dd, 1H, J= 4.2, 8.1 Hz); 2.72 (s, 3H)
151.2; 150.3; 149.1; 148.5; 145.1; 144.2; 136.2; 128.4; 127.1; 125.3; 123.5; 121.1, 121.0; 112.5; 13.4
11.96 (s, 1H); 9.11 (dd, 1H, J= 1.6, 4.0 Hz); 8.49 (dd, 1H, J= 1.6, 8.0 Hz); 8.33 (s, 1H); 8.10 (d, 1H, J= 9.2 Hz); 8.03 (d, 1H, J= 9.2 Hz); 7.96 (s, 1H); 7.78 (dd, 1H, J= 4.0, 8.0 Hz); 3.23 (t, 2H, J=7.2 Hz); 1.79 (m, 2H); 1.08 (t, 3H, J= 7.2 Hz)
151.09; 150.29; 149.14; 147.45; 145.17; 144.54; 136.20; 128.42; 127.09; 125.59; 123.50; 121.25; 113.31; 32.19; 21.00; 13.28
11.85 (s, 1H); 9.10 (dd, 1H, J= 1.6, 4.0 Hz); 8.48 (dd, 1H, J= 1.6, 8.0 Hz); 8.32 (s, 1H); 8.17 (d, 1H, J= 9.2 Hz); 7.96 (d, 1H, J= 9.2 Hz); 7.76 (dd, 1H, J= 4.0, 8.0 Hz); 7.57 (s, 1H); 4.39 (q, 2H, J= 6.8 Hz); 1.52 (t, 3H, J= 6.8 Hz)
160.85; 153.28; 149.96; 149.61; 146.06; 144.96; 136.15; 128.61; 126.05; 123.27; 120.27; 119.57; 99.11; 64.34; 14.22
11.98 (s, 1H); 9.12 (dd, 1H, J= 1.6, 4.0 Hz); 8.51 (dd, 1H, J= 1.6, 8.0 Hz); 8.35 (s, 1H); 8.12 (d, 1H, J= 9.2 Hz); 8.04 (d, 1H, J= 9.2 Hz); 8.03 (s, 1H); 7.79 (dd, 1H, J= 4.0, 8.0 Hz, 1H); 3.89 (m, 1H); 1.46(d, 6H, J= 6.4 Hz)
151.12; 150.28; 149.13; 146.52; 145.18; 144.81; 136.19; 128.43; 127.11; 125.97; 123.52; 121.44; 114.84; 35.40; 22.27
1.4−(2−メトキシ−エトキシ)−2−メチル−[1,10]フェナントロリンの合成
11.94 (s, 1H); 9.06 (dd, 1H, J= 1.6, 4.0 Hz); 8.46 (dd, 1H, J= 1.2, 8.0 Hz); 8.35 (s, 1H); 8.13 (d, 1H, J= 8.8 Hz); 7.95 (d, 1H, J= 8.8 Hz); 7.75 (dd, 1H, J= 4.4, 8.0 Hz); 7.57 (s, 1H); 4.43 (t, 2H, J= 4.4 Hz); 3.83 (t, 2H, J= 4.4 Hz); 3.36 (s, 3H)
161.3; 153.5; 150.3; 150.0; 146.1; 145.0; 136.6; 128.9; 126.4; 123.7; 120.5; 119.9; 99.7; 70.2; 68.4; 58.6
1.[2−(2−メチル−[1,10]フェナントロリン−4−イルオキシ)−エチル]−カルバミン酸tert−ブチルエステルの合成
12.13 (s, 1H); 9.09 (dd, 1H, J= 1.2 Hz, J= 4.0 Hz); 8.50 (dd, 1H, J= 1.2 Hz, J= 8.0 Hz); 8.40 (m, 2H); 7.97 (d, 1H, J= 8.8 Hz); 7.81 (dd, 1H, J= 4.0 Hz, J= 8.0 Hz); 7.26 (s, 1H); 3.73 (d, 2H, J= 9.2 Hz); 3.52 (d, 2H, J= 9.2 Hz)
152.72, 150.00, 146.82, 136.29, 128.51, 124.69, 124.00, 120.02, 116.91, 104.21, 96.79, 58.68, 45.62
1.ジエチル−[2−(2−メチル−[1,10]フェナントロリン−4−イルオキシ)−エチル]アミンの合成
11.85 (s, 1H); 9.09 (dd, 1H, J= 2.0, 4.4 Hz); 8.46 (dd, 1H, J= 1.0, 8.0 Hz); 8.31 (s, 1H); 8.13 (d, 1H, J= 8.8 Hz); 7.96 (d, 1H, J= 8.8 Hz); 7.92 (s, 1H); 7.75 (dd, 1H, J= 4.4, 8.0 Hz); 4.36 (t, 2H, J= 5.6 Hz); 2.96 (t, 2H, J= 5.6 Hz); 2.60 (q, 4H, 7.2 Hz); 1.01 (t, 6H, d= 7.2 Hz)
161.0; 153.3; 150.0; 149.6; 146.1; 145.0; 136.2; 128.6; 126.1; 123.3; 120.3; 119.5; 99.3; 67.5; 50.8; 47.1; 12.0
実施例8
毒性
SH−SY5Yヒト神経芽腫細胞において、乳酸デヒドロゲナーゼ(LDH)活性放出の定量により、アッセイ化合物についての細胞生存に対する潜在的影響をアッセイする。SH−SY5Yヒト神経芽腫細胞を96ウェル培養プレートに104細胞/ウェルで播種する。その後、この培地を取り出し、細胞を異なる濃度の化合物とともに24時間インキュベートする。化合物は、化合物が毒性を有する最小濃度を見つけるために、新しい培養培地で、1μMから出発する漸増濃度で、最大で1mMまで試験する。24時間後に、培地を除去し、ウェルの底に付着した細胞を、50μlのKrebs−Hepes;Triton X−100 1%を加えることにより室温で5分間溶解する。LDH放出定量には、Roche社製細胞傷害性検出キット(カタログ番号11 644 793 001)を使用する。LDH活性は、492nmと参照波長620nmにおけるその吸光度により測定する。
過酸化水素による細胞死からの保護
このアッセイの目的は、細胞に極めて有害であり、蓄積することによって細胞内標的例えばDNA、タンパク質、および脂質の酸化が起こり、突然変異誘発および細胞死へとつながる、過酸化水素による酸化的ストレスにヒト神経芽腫細胞を暴露して、式(I)の化合物の神経保護効果を判定することである。
この実験の目的は、式(I)の化合物についての、6−OHDAによってもたらされる毒性からの保護効果を判定することである。この毒素は、パーキンソン病において起こるような、ドーパミンニューロンを破壊する細胞死を引き起こす("MPTP and 6-hydroxydopamine-induced neurodegeneration as models for Parkinson's disease: neuroprotective strategies"; Grunblatt E, et al.; J Neurol. 2000 Apr; 247 Suppl 2:1195-102)。
A)6−OHDA 75μMでの16時間の処理の前にNACおよび式(I)の化合物を2時間プレインキュベートする。このアッセイは10%胎児ウシ血清を含む培地で行う。
B)6−OHDA 50μMでの24時間の処理の前にNACおよび式(I)の化合物を1時間プレインキュベートする。このアッセイはウシ胎児血清を含まない培地で行う。
Aβ毒性からの神経保護
化合物の潜在的神経保護を評価するために、96ウェルプレートで培養したSH−SY5Y細胞を化合物で異なる濃度において1時間前処理した後、200μM Aβ25−35(Neosystem)に24時間暴露し、大きな酸化的ストレスおよび細胞死を誘発した。その後、化合物についてのこの毒性からの保護能力を、比色LDHアッセイを用いて細胞内LDHを測定することにより評価する。
Aβ(1−40)分泌の阻害
Aβ分泌を定量するために、ELISAに基づく方法を用いた。このアッセイは、「サンドイッチ錯体」を形成する2つの異なるエピトープにおける選択的モノクローナル抗Aβ−抗体により抗原を検出することにあり、そしてそれはサンプル中のペプチド量に正比例する基質または色素原、TMB、の有色生成物への変換を触媒するペルオキシダーゼとコンジュゲートした二次抗体の結合による比色分析手段により検出される。Aβ産生は、ELISAにより比色分析用の市販のキット:イムノアッセイキットヒトβアミロイド1−40(Biosource)を用いて分析されている。
スクリーニング 薬物動態研究
この研究の目的は、経口および静脈内投与後の経口バイオアベイラビリティと血漿および脳薬物動態パラメーターを評価し、その結果、式(I)の化合物が血液脳関門(BBB)を通過することができるかどうかを判定することである。血漿および脳中の式(I)化合物レベルを測定するために、マウス(C57BL6/J、8週齢の雄)に異なる化合物の1種類の静脈内投与(1mg/kg)と2種類の経口投与(20mg/kgおよび200mg/kg)により投薬した。各化合物を適当な賦形剤に溶かした。経口投与の場合には、化合物を、シリンジに連結する経口胃管栄養法により投与した。静脈内投与の動物では、試験品目を、30G注射針を取り付けたシリンジを用いて1回の注射により投与した。
次の表において、略語は以下に示す意味を有する:
AUC=曲線下面積
T1/2=半減期
Tmax=薬物投与から最大血漿中濃度に達するまでの時間;吸収速度が消失速度に等しい時点
Cmax=薬物の最大血漿中濃度
V. Adm.およびVol. Adm.=投与容量
上記表(7−12)に示した結果に関して、試験した式(I)化合物は総て、脳内で検出されるため、血液脳関門を通過することができる。経口バイオアベイラビリティは、低用量では7〜10%の範囲であり、高濃度では著しく増加する。
一部の式(I)の化合物についてのFe(II)とのキレート化能力の評価
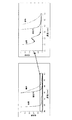
キレート配位子である化合物4、化合物7、化合物8および化合物10の存在下で行ったアッセイにより、各配位子と鉄の混合物の場合に得られるスペクトルがそれぞれの個別スペクトルの合計とは異なるため、これらの配位子はFe(II)を錯化することができるということが示された(図2、図3、図4および図5参照)。
a)一部の式(I)の化合物についてのFe(III)とのキレート化能力の評価
Fe(III)の存在下で行ったアッセイにより、Fe(III)の存在下で配位子の吸光度スペクトルにおける変化が認められないため、式(I)の化合物はいずれもこの金属を錯化することができないということが示された;化合物4、7、8および10について図1に示されるとおりである。スペクトルが重なり合っているため、1本の線しか認められない(図1参照)。
キレート配位子である化合物4、化合物7および化合物8の存在下で行ったアッセイにより、各配位子と銅の混合物の場合に得られるスペクトルはそれぞれの個別スペクトルの合計と一致するため、これらの配位子はいずれもCu(II)を錯化することができないということが示された(図6および図7参照)。
化合物4、7、8および10は総て、Zn(II)とある程度錯化したが、生成定数が相対的に低く、解離度が相対的に高いため、これらの錯体があまり安定していないことが分かる(図8、図9、図10および図11参照)。
金属イオンとクェラトンス(quelatns)との錯体形成では、生成定数が高く、解離度が低いほど、錯体が安定している。そのため、式(I)の化合物は、残りの試験金属イオンと比較してFe(II)に対して高い親和性を有するということが認められ得る。
Claims (34)
- 神経変性または血液の疾患または状態の治療または予防のための医薬の製造における、式(I):
R7は、−CH=N−OR8または−CHOから選択され;
R3およびR4は、C1−C6アルキル、場合によってC1−C6アルキル、C6−C15アリール、ハロゲン、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている、C6−C15アリールおよびヘテロアリールからなる群から独立に選択され、
R5およびR6は、水素およびC1−C6アルキルから独立に選択され、
R8は、水素およびC1−C6アルキルから選択される)
の化合物、あるいはそれらの任意の塩または溶媒和物または立体異性体または互変異性体の使用。 - R1が、−S−R3、−O−R4およびハロゲンから選択され;
R7が、−CH=N−OR8または−CHOから選択され;
R3およびR4が、独立に、場合によってC1−C6アルコキシおよび/または−NR5R6で置換されている、C1−C6アルキルであり、
R5およびR6が、水素およびC1−C6アルキルから独立に選択され、
R8が、水素およびC1−C6アルキルから選択される式(I)の化合物の、請求項1に記載の使用。 - 前記神経変性疾患が、アルツハイマー病、パーキンソン病、筋萎縮性側索硬化症(ALS)、統合失調症、ハンチントン病、脳損傷、例えば卒中および虚血、多発性硬化症、癲癇、フリートライヒ運動失調、海綿状脳症、アミロイドーシス、血管認知症、タウオファティイズ (tauophaties)、進行性核上麻痺、前頭側頭葉変性症、亜急性硬化性全脳炎性パーキンソン症候群、脳炎後パーキンソン症候群、拳闘家脳炎(pugilistic encephalitis)、グアム島パーキンソン症候群−認知症複合、ピック病、大脳皮質基底核変性症、前頭側頭型認知症、エイズ関連認知症、多発性硬化症、気分障害例えば鬱病、統合失調症および双極性障害、脳卒中後の機能回復促進ならびに脳損傷、とりわけ外傷性脳損傷から選択される、請求項1または2に記載の使用。
- 前記神経変性疾患がアルツハイマー病である、請求項3に記載の使用。
- 前記血液疾患が、サラセミア、貧血、再生不良性貧血、ダイヤモンド・ブラックファン貧血、鎌形赤血球症、定期的な赤血球輸血を必要とする血液障害、骨髄異形成症候群、鉄誘発性心機能障害、鉄誘発性心不全および糖尿病から選択される、請求項1または2に記載の使用。
- 前記血液疾患がサラセミア、貧血、再生不良性貧血、骨髄異形成症候群および糖尿病から選択される、請求項5に記載の使用。
- 式(I)の化合物が、次の化合物:
4−メトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−クロロ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−クロロ−[1,10]フェナントロリン−2−カルバルデヒド;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−アミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
2−[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−N,N−ジメチル−アセトアミド;
4−(2,2,2−トリフルオロ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸メチルエステル;
4−(チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸;
4−(5−メチル−チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(5−メチル−[1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−([1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒド;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
あるいはそれらの塩、溶媒和物または立体異性体または互変異性体から選択される、請求項1に記載の使用。 - 請求項3〜6に記載の神経変性または血液の疾患または状態を治療または予防する方法であって、かかる治療を必要とする患者に治療上有効な量の、請求項1〜7に記載の少なくとも1種の式(I)化合物、あるいはそれらの塩、溶媒和物、立体異性体もしくは互変異性体、またはそれらの医薬組成物を投与することを含む、方法。
- 式(I):
R1は、−S−R3、−O−R4およびハロゲンから選択され;
R7は、−CH=N−OR8または−CHOから選択され;
R3およびR4は、C1−C6アルキル、場合によってC1−C6アルキル、C6−C15アリール、ハロゲン、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている、C6−C15アリールおよびヘテロアリールからなる群から独立に選択され、
R5およびR6は、水素およびC1−C6アルキルから独立に選択され、
R8は、水素およびC1−C6アルキルから選択され、
ただし、R1がClである場合には、R7は−CHOではない)
の化合物、あるいはそれらの任意の塩または溶媒和物または立体異性体。 - R1が、−S−R3、−O−R4およびハロゲンから選択され;
R7が、−CH=N−OR8または−CHOから選択され;
R3およびR4は、独立に、場合によってC1−C6アルコキシおよび/または−NR5R6で置換されている、C1−C6アルキルであり、
R5およびR6が、水素およびC1−C6アルキルから独立に選択され、
R8が、水素およびC1−C6アルキルから選択される(ただし、R1がClまたはOCH3である場合には、R7は−CHOまたは−CH=N−OHではない)、
請求項9に記載の式(I)の化合物、あるいはそれらの任意の塩または溶媒和物または立体異性体。 - R7が−CH=N−OR8である、請求項1または2に記載の化合物。
- R8が水素である、請求項11に記載の化合物。
- R1が−S−R3である、請求項9〜12のいずれか一項に記載の化合物。
- R3がメチル、エチル、プロピルおよびイソプロピルから選択される、請求項13に記載の化合物。
- R1が−O−R4である、請求項9に記載の化合物。
- R4がメチルおよびエチルから選択される、請求項15に記載の化合物。
- R4が、−NR5R6またはメトキシで置換されているエチルであり、R5およびR6が、水素およびC1−C6アルキルから独立に選択される、請求項16に記載の化合物。
- 前記アミンが第1級または第3級アミンである、請求項17に記載の化合物。
- 前記第3級アミンがジエチルアミンである、請求項18に記載の化合物。
- 前記オキシム基−CH=NOR8の二重結合がE配座を示す、請求項11に記載の化合物。
- R1がクロロである、請求項9、10および20のいずれか一項に記載の化合物。
- R1が、ヘテロアリール基が場合によってC1−C6アルキル、C6−C15アリール、ハロゲン、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている−S−ヘテロアリールである、請求項13に記載の化合物。
- 前記ヘテロアリール基がC1−C3アルキルで置換されている、請求項22に記載の化合物。
- R3が、−(C=O)NR5R6または−(C=O)OR5で置換されているC1−C3アルキル基である、請求項9に記載の化合物。
- 式(I)の化合物が、
4−メトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−アミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(2−メトキシ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
2−[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−N,N−ジメチル−アセトアミド;
4−(2,2,2−トリフルオロ−エチルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸メチルエステル;
4−(チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
[2−(ヒドロキシイミノ−メチル)−[1,10]フェナントロリン−4−イルスルファニル]−酢酸;
4−(5−メチル−チアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−(5−メチル−[1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−([1,3,4]チアジアゾール−2−イルスルファニル)−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−メチルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−プロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒドオキシム;
4−エトキシ−[1,10]フェナントロリン−2−カルバルデヒド;
4−イソプロピルスルファニル−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−メトキシ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
4−(2−ジエチルアミノ−エトキシ)−[1,10]フェナントロリン−2−カルバルデヒド;
あるいはそれらの塩、溶媒和物、立体異性体または互変異性体から選択される、請求項9に記載の化合物。 - 医薬として用いるための、請求項9〜25のいずれか一項に記載の式(I)の化合物、それらの塩または溶媒和物、立体異性体または互変異性体。
- 請求項9〜25のいずれか一項に記載の少なくとも1種の式(I)化合物、それらの塩または溶媒和物または互変異性体と、少なくとも1種の薬学上許容される担体とを含んでなる、医薬組成物。
- 請求項10〜21のいずれか一項に記載の式(I)の化合物の製造のための方法であって、
a)式(I)の化合物を形成するために酸化剤を用いて式(II)の化合物のメチル基を酸化する工程:
および所望により、
b)ヒドロキシルアミンまたはO−(C1−C6)アルキルヒドロキシルアミンの存在下で、式(I)の化合物中のアルデヒド基−CHOを、R8が水素およびC1−C6アルキルから選択されたオキシム基−CH=N−OR8へと変換する工程:
- 前記酸化剤がSeO2である、請求項28に記載の方法。
- 任意選択の工程b)がエタノールおよび水酸化ナトリウム水溶液の混合物中で行われる、請求項28に記載の方法。
- 請求項10〜21のいずれか一項に記載の式(I)の化合物の製造のための方法であって、
a)式(II)の化合物を形成するために、化合物 式(III)を式−OR3または−OR4の対応するアルコキシドまたはチオラートのナトリウム塩と反応させる工程:
Xは、ハロゲンであり;
R1は、−S−R3、−O−R4およびハロゲンから選択され;
R3およびR4は、C1−C6アルキル、場合によってC1−C6アルキル、C6−C15アリール、ハロゲン、−(C=O)NR5R6、−(C=O)OR5、C1−C6アルコキシおよび/または−NR5R6で置換されている、C6−C15アリールおよびヘテロアリールからなる群から独立に選択される;
ただし、式(II)中のR1がハロゲンである場合には、この工程は省略される);
b)式(I)の化合物を形成するために酸化剤を用いて式(II)の化合物のメチル基を酸化する工程;
および所望により、
c)ヒドロキシルアミンまたはO−(C1−C6)アルキルヒドロキシルアミンの存在下で、式(I)の化合物中のアルデヒド基−CHOを、R8が水素およびC1−C6アルキルから選択されたオキシム基−CH=N−OR8へと変換する工程:
- 工程a)において用いるナトリウムが、ナトリウムエトキシド、ナトリウム2−プロパンチオラートまたはナトリウム1−プロパンチオラートである、請求項31に記載の方法。
- 工程a)が溶媒としてのアルコールまたはテトラヒドロフラン中で行われる、請求項31および32に記載の方法。
- 請求項9〜25のいずれか一項に記載の式(I)の化合物、あるいはそれらの任意の塩または溶媒和物の、生物学的アッセイでの試薬としての、好ましくは、薬物動態アッセイ、血液脳関門通過アッセイ、キレートアッセイ、過酸化水素による細胞死からの保護、6−OHDAによる細胞死からの保護、Aβ毒性からの神経保護およびβ−アミロイド分泌の阻害についてのアッセイでの反応性物質としての、使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07380167A EP2002863A1 (en) | 2007-06-11 | 2007-06-11 | [1,10]-phenanthroline derivatives for the treatment of neurodegenerative or haematological diseases |
| PCT/EP2008/057319 WO2008152068A2 (en) | 2007-06-11 | 2008-06-11 | [1,10]-phenanthroline derivatives for the treatment of neurodegenerative or haematological diseases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010529167A true JP2010529167A (ja) | 2010-08-26 |
| JP2010529167A5 JP2010529167A5 (ja) | 2014-01-30 |
Family
ID=38596362
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010511627A Pending JP2010529167A (ja) | 2007-06-11 | 2008-06-11 | 神経変性疾患または血液疾患の治療のための[1,10]−フェナントロリン誘導体 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US8592446B2 (ja) |
| EP (2) | EP2002863A1 (ja) |
| JP (1) | JP2010529167A (ja) |
| CN (1) | CN101801461A (ja) |
| AR (1) | AR066956A1 (ja) |
| AU (1) | AU2008263897A1 (ja) |
| CA (1) | CA2690455A1 (ja) |
| CL (1) | CL2008001719A1 (ja) |
| MX (1) | MX2009013482A (ja) |
| RU (1) | RU2009148821A (ja) |
| TW (1) | TW200914016A (ja) |
| UY (1) | UY31143A1 (ja) |
| WO (1) | WO2008152068A2 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103380137B (zh) | 2010-12-01 | 2016-02-10 | 中国石油化工股份有限公司 | 一种n邻位酰基取代的含氮杂环化合物及其缩胺合铁(ⅱ)配合物的制备方法 |
| CN102532201B (zh) * | 2010-12-01 | 2014-11-05 | 中国石油化工股份有限公司 | 甲酰基取代的1,10-菲咯啉配合物的制备及由此制备的配合物作为催化剂的应用 |
| CN102558241B (zh) * | 2010-12-01 | 2014-11-26 | 中国石油化工股份有限公司 | 丙酰基取代的1,10-菲咯啉配合物的制备及由此制备的配合物作为催化剂的应用 |
| CN106083713B (zh) * | 2016-07-15 | 2019-07-26 | 浙江工业大学 | 一种喹(喔)啉-2-甲醛类化合物的化学合成方法 |
| WO2021176428A1 (en) * | 2020-03-06 | 2021-09-10 | Jawaharlal Nehru Centre For Advanced Scientific Research | Phenanthroline, carbazole and flavylium based cyanines and compositions and methods of making and using the same |
| MX2024003892A (es) * | 2021-09-28 | 2024-05-23 | Zevra Denmark As | Oximas y su uso en el tratamiento de enfermedades relacionadas con gba. |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL76345B1 (ja) * | 1971-02-13 | 1975-06-30 |
-
2007
- 2007-06-11 EP EP07380167A patent/EP2002863A1/en not_active Withdrawn
-
2008
- 2008-06-11 JP JP2010511627A patent/JP2010529167A/ja active Pending
- 2008-06-11 RU RU2009148821/15A patent/RU2009148821A/ru not_active Application Discontinuation
- 2008-06-11 CN CN200880102953A patent/CN101801461A/zh active Pending
- 2008-06-11 WO PCT/EP2008/057319 patent/WO2008152068A2/en active Application Filing
- 2008-06-11 CA CA2690455A patent/CA2690455A1/en not_active Abandoned
- 2008-06-11 CL CL2008001719A patent/CL2008001719A1/es unknown
- 2008-06-11 EP EP08760868A patent/EP2170464A2/en not_active Withdrawn
- 2008-06-11 AR ARP080102479A patent/AR066956A1/es unknown
- 2008-06-11 MX MX2009013482A patent/MX2009013482A/es not_active Application Discontinuation
- 2008-06-11 US US12/664,130 patent/US8592446B2/en active Active - Reinstated
- 2008-06-11 TW TW097121744A patent/TW200914016A/zh unknown
- 2008-06-11 UY UY31143A patent/UY31143A1/es not_active Application Discontinuation
- 2008-06-11 AU AU2008263897A patent/AU2008263897A1/en not_active Abandoned
-
2013
- 2013-09-15 US US14/027,225 patent/US20140011835A1/en not_active Abandoned
Non-Patent Citations (3)
| Title |
|---|
| JPN6013027849; MLOCHOWSKI, J. et al: 'Synthesis of phenanthroline analogs of cerulomycin' ROCZNIKI CHEMII Vol.45, No.5, 1971, p.803-9 * |
| JPN6013027852; GAETA, A. et al: 'The crucial role of metal ions in neurodegeneration: the basis for a promising therapeutic strategy' BRITISH JOURNAL OF PHARMACOLOGY Vol.146, No.8, 2005, p.1041-1059 * |
| JPN7013002151; ポーランド国特許発明第76345号明細書 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2690455A1 (en) | 2008-12-18 |
| US20100240692A1 (en) | 2010-09-23 |
| MX2009013482A (es) | 2010-01-27 |
| TW200914016A (en) | 2009-04-01 |
| US20140011835A1 (en) | 2014-01-09 |
| UY31143A1 (es) | 2009-01-30 |
| WO2008152068A3 (en) | 2009-05-07 |
| EP2170464A2 (en) | 2010-04-07 |
| WO2008152068A2 (en) | 2008-12-18 |
| RU2009148821A (ru) | 2011-07-20 |
| CL2008001719A1 (es) | 2009-01-02 |
| US8592446B2 (en) | 2013-11-26 |
| AU2008263897A1 (en) | 2008-12-18 |
| EP2002863A1 (en) | 2008-12-17 |
| CN101801461A (zh) | 2010-08-11 |
| AR066956A1 (es) | 2009-09-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9815825B2 (en) | Coumarin derivatives and methods of use in treating cystic fibrosis, chronic obstructive pulmonary disease, and misfolded protein disorders | |
| JP2020509004A (ja) | Oga阻害剤としての、ピペリジン、モルホリンまたはピペラジンで置換されている[1,2,4]−トリアゾロ[1,5−a]−ピリミジニル誘導体 | |
| CA2891962A1 (en) | Small molecule cftr correctors | |
| US20140011835A1 (en) | [1,10]-phenanthroline derivatives for the treatment of neurodegenerative or haematological diseases | |
| US10772884B2 (en) | Sulphate salts of N-(3-(4-(3-(diisobutylamino)propyl)piperazin-1-yl)propyl)-1H-benzo[d]imidazol-2-amine, preparation thereof and use of the same | |
| WO2019106434A1 (en) | Heterobicyclic aromatic derivatives for the treatment of ferroptosis-related disorders | |
| EP2922853A2 (en) | Small Molecule Bicyclic and Tricyclic CFTR Correctors | |
| US9447056B2 (en) | Solid forms of epalrestat | |
| US9221840B2 (en) | Treating protein folding disorders with small molecule CFTR correctors | |
| WO2010011926A2 (en) | A novel betaine cocrystal of epalrestat | |
| JP5220601B2 (ja) | コリスマイシンおよびその誘導体の、酸化ストレス抑制剤としての使用 | |
| RU2680138C2 (ru) | Трициклические ингибиторы гиразы | |
| CN110869011A (zh) | 用于治疗神经退行性疾病的组合物 | |
| US20230331679A1 (en) | Naphthalene monoimide compounds and methods thereof | |
| CA3005212A1 (en) | Benzofuran derivatives for the treatment of cns and other disorders | |
| US20240033234A1 (en) | Therapeutic compounds, formulations, and use thereof | |
| JP2023507180A (ja) | Oga阻害剤化合物 | |
| CN112714761A (zh) | 用作分子伴侣介导的自噬调节剂的化合物 | |
| EP2373650B1 (en) | Triple substituted phenanthroline derivatives for the treatment of neurodegenerative or haematological diseases or conditions, or cancer | |
| US10925848B2 (en) | Amide derivative |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110610 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130607 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130701 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130708 |
|
| A524 | Written submission of copy of amendment under section 19 (pct) |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20131205 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140218 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140722 |