JP2010060375A - 電気化学測定装置用電極およびバイオセンサ用電極 - Google Patents
電気化学測定装置用電極およびバイオセンサ用電極 Download PDFInfo
- Publication number
- JP2010060375A JP2010060375A JP2008224938A JP2008224938A JP2010060375A JP 2010060375 A JP2010060375 A JP 2010060375A JP 2008224938 A JP2008224938 A JP 2008224938A JP 2008224938 A JP2008224938 A JP 2008224938A JP 2010060375 A JP2010060375 A JP 2010060375A
- Authority
- JP
- Japan
- Prior art keywords
- electrode
- biosensor
- electrochemical
- immobilized
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Abstract
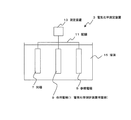
【解決手段】溶液中の特定成分の濃度を測定する電気化学測定装置3に用いられる作用電極9(電気化学測定装置用電極1)は、イリジウムとニッケルを含む合金が用いられており、作用電極9は溶液中に含まれる特定成分を検出可能に構成されている。
【選択図】図1
Description
図1に示す電気化学測定装置3をイリジウム−ニッケル合金の電極を用いて作製し、指示電解質溶液に対するサイクリックボルタンメトリ測定を行い、イリジウムおよびニッケルのみで構成された電極を用いた場合と比較した。
イリジウムとニッケルの原子比率が100:0(イリジウム単体)、25:75、および白金単体の電極をそれぞれ実施例1と同様に製作し、同様に作用電極9として実験に供試した。なお、白金電極の白金はフルウチ社製の白金ワイヤを用いた。
実施例2で用いた電極のうち、イリジウムとニッケルの原子比率が25:75の電極を用意し、0.1M(100mol/m3)の硫酸ナトリウム溶液中で電気化学クリーニングを行った。
繰り返し再現性の値(%)=(電流値の標準偏差/電流値の平均値)×100…(式)
初めに実施例2で記載したイリジウムとニッケル比が25:75の電極を用意し、0.1Mの硫酸ナトリウム溶液中で電気化学クリーニングを行った。
初めにイリジウムとニッケルの原子比率が25:75の電極をアーク放電法で製作し、ガラス基板上に接着剤で固定した。次に、電極基板と結線し、シリコーンシール材で封止した。
3…………電気化学測定装置
3a………バイオセンサ
3b………バイオセンサ
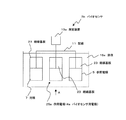
4…………バイオセンサ用電極
5…………参照電極
6…………固定化触媒層
7…………対極
9…………作用電極
11………配線
13………測定装置
15………溶液
23………絶縁基板
24………結合層
Claims (31)
- 溶液中に含まれる特定成分を検出可能な組成となるようにイリジウムとニッケルを含有していることを特徴とする電気化学測定装置用電極。
- イリジウムとニッケルとを、過酸化水素に対して電流出力を生じさせることが可能な組成となるように含有した合金で構成されていることを特徴とする請求項1記載の電気化学測定装置用電極。
- 前記合金は、イリジウムとニッケルの原子比率が50:50〜5:95の範囲であることを特徴とする請求項1または2のいずれかに記載の電気化学測定装置用電極。
- 前記合金は、イリジウムとニッケルの原子比率が40:60〜10:90の範囲であることを特徴とする請求項1または2のいずれかに記載の電気化学測定装置用電極。
- 前記合金は、
イリジウム−ニッケル合金であることを特徴とする請求項2〜4のいずれかに記載の電気化学測定装置用電極。 - 請求項1〜5のいずれかに記載の電気化学測定装置用電極を有することを特徴とする電気化学測定装置。
- 請求項1〜5のいずれかに記載の電気化学測定装置用電極の表面に、固定化触媒層を設けてなることを特徴とするバイオセンサ用電極。
- 前記固定化触媒層は、固定化酵素層であり、
前記固定化酵素層は、
前記特定成分を、過酸化水素に変換可能な少なくとも1つの種類の酵素を有し、
前記固定化酵素層が変換した過酸化水素を前記電気化学測定装置用電極が検出することにより、前記特定成分を検出することを特徴とする請求項7記載のバイオセンサ用電極。 - 前記酵素は、
乳酸酸化酵素、グルコース酸化酵素、尿酸酸化酵素、尿素酸化酵素、アルコール酸化酵素、クレアチニナーゼ、クレアチナーゼ、サルコシンオキシダーゼのうちの少なくとも1つであることを特徴とする請求項8記載のバイオセンサ用電極。 - 前記固定化触媒層は、固定化抗体層であり、
前記固定化抗体層は、
前記特定成分と反応可能な少なくとも1つの種類の抗体を有し、
前記固定化抗体層中の前記抗体と前記特定成分との反応により生じる電流を、前記電気化学測定装置用電極が検出することにより、前記特定成分を検出することを特徴とする請求項7記載のバイオセンサ用電極。 - 前記抗体は、
ダイオキシン抗体、内分泌攪乱物質の抗体、残留農薬の抗体のいずれかであることを特徴とする請求項10記載のバイオセンサ用電極。 - 前記固定化触媒層は、アプタマーを有する層であることを特徴とする、請求項7記載のバイオセンサ用電極。
- 前記アプタマーは、DNAアプタマー、RNAアプタマー、ペプチドアプタマーのいずれかであることを特徴とする請求項12記載のバイオセンサ用電極。
- 前記アプタマーは、コカインアプタマー、トロンビンアプタマー、トリニトロトルエンアプタマーのいずれかであることを特徴とする請求項12記載のバイオセンサ用電極。
- 前記電気化学測定装置用電極を保持する絶縁基板と、
前記電気化学測定装置用電極と前記固定化触媒層の間に設けられ、かつ前記電気化学測定装置用電極を覆うように、前記絶縁基板および電気化学測定装置用電極上に設けられた結合層と、
をさらに有することを特徴とする請求項7記載のバイオセンサ用電極。 - 請求項7〜15のいずれかに記載のバイオセンサ用電極を有することを特徴とするバイオセンサ。
- 溶液中に含まれる特定成分を検出可能な組成となるようにイリジウムとニッケルを含む合金を、アーク放電法、蒸着法、スパッタリング法のいずれかで製造する工程を有することを特徴とする電気化学測定装置用電極の製造方法。
- 前記工程は、イリジウムとニッケルとを、過酸化水素に対して電流出力を生じさせることが可能な組成となるように含有した合金を製造する工程であることを特徴とする請求項17記載の電気化学測定装置用電極の製造方法。
- 前記工程は、イリジウムとニッケルの原子比率が50:50〜5:95の範囲である合金を製造する工程であることを特徴とする請求項17または18のいずれかに記載の電気化学測定装置用電極の製造方法。
- 前記合金は、イリジウムとニッケルの原子比率が40:60〜10:90の範囲である合金を製造する工程であることを特徴とする請求項17または18のいずれかに記載の電気化学測定装置用電極の製造方法。
- 請求項1〜5のいずれかに記載の電気化学測定装置用電極の表面に固定化触媒層を設ける工程を有することを特徴とするバイオセンサ用電極の製造方法。
- 前記工程は、
固定化触媒層として、前記特定成分を、過酸化水素に変換可能な少なくとも1つの酵素を前記電気化学測定装置用電極の表面に固定して固定化酵素層を設ける工程であることを特徴とする請求項21記載のバイオセンサ用電極の製造方法。 - 前記工程は、
乳酸酸化酵素、グルコース酸化酵素、尿酸酸化酵素、尿素酸化酵素、アルコール酸化酵素、クレアチニナーゼ、クレアチナーゼ、サルコシンオキシダーゼのうち、少なくとも1つを前記電気化学測定装置用電極の表面に固定して固定化酵素層を設ける工程であることを特徴とする請求項22記載のバイオセンサ用電極の製造方法。 - 前記工程は、
固定化触媒層として、前記特定成分と反応可能な少なくとも1つの抗体を前記電気化学測定装置用電極の表面に固定して固定化抗体層を設ける工程であることを特徴とする請求項21記載のバイオセンサ用電極の製造方法。 - 前記工程は、
ダイオキシン抗体、内分泌攪乱物質の抗体、残留農薬の抗体のうちのいずれかを前記電気化学測定装置用電極の表面に固定して固定化抗体層を設ける工程であることを特徴とする請求項24記載のバイオセンサ用電極の製造方法。 - 前記工程は、
固定化触媒層として、前記特定成分と反応可能な少なくとも1つのアプタマーを前記電気化学測定装置用電極の表面に固定する工程であることを特徴とする請求項21記載のバイオセンサ用電極の製造方法。 - 前記工程は、コカインアプタマー、トロンビンアプタマー、トリニトロトルエンアプタマーのうちのいずれかを前記電気化学測定装置用電極の表面に固定する工程であることを特徴とする請求項26記載のバイオセンサ用電極の製造方法。
- 請求項6記載の電気化学測定装置を用い、電流検出方式により、溶液中の過酸化水素の濃度を測定することを特徴とする測定方法。
- 請求項16記載のバイオセンサを用い、電流検出方式により、溶液中の特定成分の濃度を測定することを特徴とする測定方法。
- 少なくともサイクリックボルタンメトリ法とパルスボルタンメトリ法のいずれか一方の測定方法を実施することを特徴とする請求項28または29記載の測定方法。
- 前記パルスボルタンメトリ法は、ノーマルパルスボルタンメトリ法、微分パルスボルタンメトリ法、方形波ボルタンメトリ法のいずれかであることを特徴とする請求項30記載の測定方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008224938A JP5135548B2 (ja) | 2008-09-02 | 2008-09-02 | 電気化学測定装置用電極およびバイオセンサ用電極 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008224938A JP5135548B2 (ja) | 2008-09-02 | 2008-09-02 | 電気化学測定装置用電極およびバイオセンサ用電極 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010060375A true JP2010060375A (ja) | 2010-03-18 |
| JP5135548B2 JP5135548B2 (ja) | 2013-02-06 |
Family
ID=42187330
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008224938A Expired - Fee Related JP5135548B2 (ja) | 2008-09-02 | 2008-09-02 | 電気化学測定装置用電極およびバイオセンサ用電極 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5135548B2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012024026A (ja) * | 2010-07-23 | 2012-02-09 | Tdk Corp | Sm菌特異的アプタマー、Sm菌増殖抑制剤及びSm菌の検出方法 |
| JP2014533845A (ja) * | 2011-12-02 | 2014-12-15 | コーニンクレッカ フィリップス エヌ ヴェ | 溶液のpH値を検出するための方法及び装置 |
| CN104374765A (zh) * | 2014-11-17 | 2015-02-25 | 济南大学 | 一种电化学发光适配体传感器、其制备方法及其用途 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5926049A (ja) * | 1982-08-04 | 1984-02-10 | Denki Kagaku Keiki Co Ltd | 過酸化水素測定方法 |
| JPH01153952A (ja) * | 1987-12-11 | 1989-06-16 | Terumo Corp | 酵素センサ |
| JPH0282152A (ja) * | 1988-09-20 | 1990-03-22 | Seiko Epson Corp | 酵素センサー |
| JPH0294364A (ja) * | 1988-09-20 | 1990-04-05 | Reiko Notoya | 酸素電極反応用電極とその製造方法 |
| JPH09127053A (ja) * | 1995-10-30 | 1997-05-16 | Kdk Corp | 過酸化水素の測定方法、その方法を用いた過酸化水素測定センサーおよびその製造方法 |
| JP2001116716A (ja) * | 1999-10-19 | 2001-04-27 | Nec Corp | 過酸化水素電極およびそれを用いた過酸化水素センサ、測定器 |
| JP2006308463A (ja) * | 2005-04-28 | 2006-11-09 | National Institute Of Advanced Industrial & Technology | ナノカーボンセンサー |
| JP2007014646A (ja) * | 2005-07-11 | 2007-01-25 | National Institute Of Advanced Industrial & Technology | 針一体型バイオセンサー |
-
2008
- 2008-09-02 JP JP2008224938A patent/JP5135548B2/ja not_active Expired - Fee Related
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5926049A (ja) * | 1982-08-04 | 1984-02-10 | Denki Kagaku Keiki Co Ltd | 過酸化水素測定方法 |
| JPH01153952A (ja) * | 1987-12-11 | 1989-06-16 | Terumo Corp | 酵素センサ |
| JPH0282152A (ja) * | 1988-09-20 | 1990-03-22 | Seiko Epson Corp | 酵素センサー |
| JPH0294364A (ja) * | 1988-09-20 | 1990-04-05 | Reiko Notoya | 酸素電極反応用電極とその製造方法 |
| JPH09127053A (ja) * | 1995-10-30 | 1997-05-16 | Kdk Corp | 過酸化水素の測定方法、その方法を用いた過酸化水素測定センサーおよびその製造方法 |
| JP2001116716A (ja) * | 1999-10-19 | 2001-04-27 | Nec Corp | 過酸化水素電極およびそれを用いた過酸化水素センサ、測定器 |
| JP2006308463A (ja) * | 2005-04-28 | 2006-11-09 | National Institute Of Advanced Industrial & Technology | ナノカーボンセンサー |
| JP2007014646A (ja) * | 2005-07-11 | 2007-01-25 | National Institute Of Advanced Industrial & Technology | 針一体型バイオセンサー |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012024026A (ja) * | 2010-07-23 | 2012-02-09 | Tdk Corp | Sm菌特異的アプタマー、Sm菌増殖抑制剤及びSm菌の検出方法 |
| JP2014533845A (ja) * | 2011-12-02 | 2014-12-15 | コーニンクレッカ フィリップス エヌ ヴェ | 溶液のpH値を検出するための方法及び装置 |
| CN104374765A (zh) * | 2014-11-17 | 2015-02-25 | 济南大学 | 一种电化学发光适配体传感器、其制备方法及其用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5135548B2 (ja) | 2013-02-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Salimi et al. | Amperometric and voltammetric detection of hydrazine using glassy carbon electrodes modified with carbon nanotubes and catechol derivatives | |
| US4927516A (en) | Enzyme sensor | |
| Kurzweil | Metal oxides and ion-exchanging surfaces as pH sensors in liquids: State-of-the-art and outlook | |
| Yang et al. | Amperometric glucose biosensor based on chitosan with improved selectivity and stability | |
| Privett et al. | Electrochemical sensors | |
| Yang et al. | Covalent immobilization of an enzyme (glucose oxidase) onto a carbon sol–gel silicate composite surface as a biosensing platform | |
| Canbay et al. | MWCNT–cysteamine–Nafion modified gold electrode based on myoglobin for determination of hydrogen peroxide and nitrite | |
| EP2159572A1 (en) | Electrodes selective for solid-contact ions based on carbon nanotubes | |
| Suzuki et al. | An integrated three-electrode system with a micromachined liquid-junction Ag/AgCl reference electrode | |
| Wu et al. | Amperometric cholesterol biosensor based on zinc oxide films on a silver nanowire–graphene oxide modified electrode | |
| JP4863398B2 (ja) | カーボンナノチューブを用いたバイオセンサ | |
| Rahman | Fabrication of mediator-free glutamate sensors based on glutamate oxidase using smart micro-devices | |
| Fan et al. | Direct electrochemistry of horseradish peroxidase on Nafion/[bmim] PF6/agarose composite film modified glassy carbon electrode | |
| JP5135548B2 (ja) | 電気化学測定装置用電極およびバイオセンサ用電極 | |
| Salimi et al. | Electrocatalytic reduction of H2O2 and oxygen on the surface of thionin incorporated onto MWCNTs modified glassy carbon electrode: application to glucose detection | |
| CN115266865A (zh) | 一种提高电化学传感器稳定性的方法 | |
| Rahman | Fabrication of L-lactate biosensor based on redox species mediated lactate oxidase using micro-device | |
| Cai et al. | Miniaturized electroanalytical sensor systems in micromachined structures | |
| JPWO2009102045A1 (ja) | 電気化学測定装置用電極およびバイオセンサ用電極 | |
| Xu et al. | Low‐Potential Detection of Glucose with a Biosensor Based on the Immobilization of Glucose Oxidase on Polymer/Manganese Oxide Layered Nanocomposite | |
| Shankaran et al. | An Amperometric Sensor for Hydrogen Peroxide Based on a (3‐Mercaptopropyl) trimethoxysilane Self‐Assembled Layer Containing Hydrazine | |
| Zhu et al. | An overview of Si-based biosensors | |
| JP5061375B2 (ja) | 電気化学測定装置用電極およびバイオセンサ用電極 | |
| JP5212982B2 (ja) | 電気化学測定装置用電極およびバイオセンサ用電極 | |
| Tong et al. | Amperometric biosensor for hydrogen peroxide based on Hemoglobin/DNA/Poly-2, 6-pyridinediamine modified gold electrode |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110810 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20110810 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120725 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120726 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120921 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121010 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121015 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151122 Year of fee payment: 3 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |