JP2010043029A - スチレン化ビスフェノール化合物の製造方法 - Google Patents
スチレン化ビスフェノール化合物の製造方法 Download PDFInfo
- Publication number
- JP2010043029A JP2010043029A JP2008208703A JP2008208703A JP2010043029A JP 2010043029 A JP2010043029 A JP 2010043029A JP 2008208703 A JP2008208703 A JP 2008208703A JP 2008208703 A JP2008208703 A JP 2008208703A JP 2010043029 A JP2010043029 A JP 2010043029A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- chemical formula
- styrenated
- bisphenol
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 CC(C)(*)c1ccccc1 Chemical compound CC(C)(*)c1ccccc1 0.000 description 1
- QHDHNVFIKWGRJR-UHFFFAOYSA-N OC1=CCCCC1 Chemical compound OC1=CCCCC1 QHDHNVFIKWGRJR-UHFFFAOYSA-N 0.000 description 1
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Description
で表されるビスフェノール化合物と、下記化学式2:
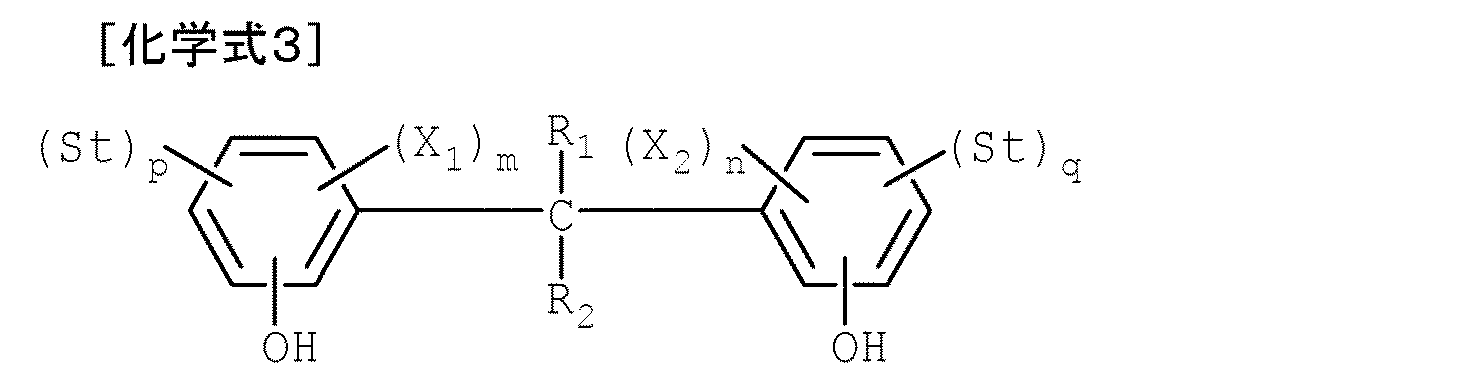
で表されるスチレン系化合物とを、酸触媒の存在下で反応させて、下記化学式3:
で表される置換または非置換のスチリル基であり、pおよびqは、それぞれ独立して、0〜2の整数である(ただし、1≦p+q≦4である)、
で表されるスチレン化ビスフェノール化合物を得るスチレン化ビスフェノール化合物の製造方法であって、前記スチレン系化合物の5〜100質量%を初期仕込みした状態で反応系を加熱し、70℃以上140℃未満の反応温度で反応を進行させることを特徴とする、スチレン化ビスフェノール化合物の製造方法が提供される。
下記化学式5:
で表されるスチレン化フェノール化合物の含有量が10質量%以下であることを特徴とする、スチレン化ビスフェノール化合物もまた、提供される。
で表されるビスフェノール化合物と、下記化学式2:
で表されるスチレン系化合物とを、酸触媒の存在下で反応させて、下記化学式3:
で表される置換または非置換のスチリル基であり、pおよびqは、それぞれ独立して、0〜2の整数である(ただし、1≦p+q≦4である)、
で表されるスチレン化ビスフェノール化合物を得るスチレン化ビスフェノール化合物の製造方法であって、前記スチレン系化合物の5〜100質量%を初期仕込みした状態で反応系を加熱し、70℃以上140℃未満の反応温度で反応を進行させることを特徴とする、スチレン化ビスフェノール化合物の製造方法である。以下、用いられる原料、生成物、および反応について、順に説明する。
(ビスフェノール化合物)
原料の1つは、下記化学式1:
原料のもう1つは、下記化学式2:
本発明の製造方法によれば、上記化学式1で表されるビスフェノール化合物と、上記化学式2で表されるスチレン系化合物とを反応させることで、下記化学式3:
本発明の製造方法では、原料の1つであるスチレン系化合物を初期仕込みした状態で、ビスフェノール化合物を反応系に添加する点に特徴を有する。このように、常温で液体であるスチレン系化合物を初期仕込みすることで、特段の問題なく所望のスチレン化ビスフェノール化合物が高純度で製造されうるのである。
1Lコルベンに、ビスフェノールF200g(1.00モル)、スチレン50g、および酸触媒であるパラトルエンスルホン酸2gを室温で仕込み、均一に混合した。その後、反応系の温度を80℃まで昇温させた。次いで、反応系の温度を80℃に保ったまま、スチレン366gを3時間かけて反応系に滴下した。スチレンの最終添加量は、4.00モルであった。スチレンの滴下終了後、95〜100℃にて2時間熟成させて、テトラスチレン化ビスフェノール604g(収率98%)を主成分とする生成物を得た。
1Lコルベンに、ジスチレン化フェノール312g、および塩基触媒である水酸化ナトリウム50gを仕込み、均一に混合した。その後、反応系の温度を80℃まで昇温させた。次いで、反応系の温度を80℃に保ったまま、ホルマリン(40質量%ホルムアルデヒド水溶液)95gを2時間かけて反応系に滴下した。ホルマリンの滴下終了後、80℃にて3時間熟成させた。次いで、硫酸水溶液を用いた中和水洗により生成物を中和精製して、テトラスチレン化ビスフェノール(604g、収率98%)を含む生成物を得た。
1LコルベンにビスフェノールF200g(1モル)、スチレン416g(4モル)、および酸触媒であるパラトルエンスルホン酸2gを仕込み、80℃まで昇温させて反応を開始させた。そうしたところ、反応が急激に進行し、反応温度が140℃まで上昇した。その後、70〜130℃にて2時間熟成させて、スチレン化ビスフェノールを得た。得られた生成物を分析したところ、上記化学式3におけるp+qの理論値は4であるが、実際には3.5であった。換言すれば、スチレン化反応が十分に進行しなかった。
オートクレーブに、上記の実施例1で得られたテトラスチレン化ビスフェノール308g、水酸化カリウム2gを仕込み、均一に混合した。その後、反応系の温度を140℃まで昇温させた。次いで、反応系の温度を140℃に保ったまま、エチレンオキシド220gを5時間かけて反応系に滴下した。エチレンオキシドの滴下終了後、145℃にて2時間熟成させて、テトラスチレン化ビスフェノールのフェノール性水酸基にエチレンオキサイドが合計で10モル付加したビスポリオキシエチレン多環フェニルエーテル(EO10モル体)523g(収率99%)を得た。
テトラスチレン化ビスフェノールの量を308gとし、エチレンオキシドの量を484gとしたこと以外は、上述した実施例2と同様の手法により、ビスポリオキシエチレン多環フェニルエーテル(EO21モル体)784g(収率99%)を得た。
テトラスチレン化ビスフェノールの量を185gとし、エチレンオキシドの量を528gとしたこと以外は、上述した実施例2と同様の手法により、ビスポリオキシエチレン多環フェニルエーテル(EO40モル体)706g(収率99%)を得た。
テトラスチレン化ビスフェノールの量を154gとし、エチレンオキシドの量を660gとしたこと以外は、上述した実施例2と同様の手法により、ビスポリオキシエチレン多環フェニルエーテル(EO60モル体)806g(収率99%)を得た。
テトラスチレン化ビスフェノールの量を62gとし、エチレンオキシドの量を704gとしたこと以外は、上述した実施例2と同様の手法により、ビスポリオキシエチレン多環フェニルエーテル(EO80モル体)758g(収率99%)を得た。
テトラスチレン化ビスフェノールの量を46gとし、エチレンオキシドの量を660gとしたこと以外は、上述した実施例2と同様の手法により、ビスポリオキシエチレン多環フェニルエーテル(EO100モル体)699g(収率99%)を得た。
1Lコルベンに、上記の実施例2で得たビスポリオキシエチレン多環フェニルエーテル(EO10モル体)528gを仕込んだ。その後、反応系の温度を120℃まで昇温させた。次いで、スルファミン酸50g、および尿素5gを反応系に添加した。添加後、110〜120℃にて3時間反応させた。これにより、ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩572g(収率98%)を得た。
1Lコルベンに、上記の実施例3で得たビスポリオキシエチレン多環フェニルエーテル(EO21モル体)792gを仕込んだ。その後、反応系の温度を120℃まで昇温させた。次いで、スルファミン酸50g、および尿素5gを反応系に添加した。添加後、110〜120℃にて3時間反応させた。これにより、ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩840g(収率98%)を得た。
1Lコルベンに、上記の実施例4で得たビスポリオキシエチレン多環フェニルエーテル(EO40モル体)713gを仕込んだ。その後、反応系の温度を120℃まで昇温させた。次いで、スルファミン酸30g、および尿素3gを反応系に添加した。添加後、110〜120℃にて3時間反応させた。これにより、ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩731g(収率98%)を得た。
1Lコルベンに、上記の実施例5で得たビスポリオキシエチレン多環フェニルエーテル(EO60モル体)814gを仕込んだ。その後、反応系の温度を120℃まで昇温させた。次いで、スルファミン酸25g、および尿素2.5gを反応系に添加した。添加後、110〜120℃にて3時間反応させた。これにより、ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩826g(収率98%)を得た。
1Lコルベンに、上記の実施例6で得たビスポリオキシエチレン多環フェニルエーテル(EO80モル体)778gを仕込んだ。その後、反応系の温度を120℃まで昇温させた。次いで、スルファミン酸12.5g、および尿素1.25gを反応系に添加した。添加後、110〜120℃にて3時間反応させた。これにより、ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩776g(収率98%)を得た。
1Lコルベンに、上記の実施例7で得たビスポリオキシエチレン多環フェニルエーテル(EO100モル体)706gを仕込んだ。その後、反応系の温度を120℃まで昇温させた。次いで、スルファミン酸7.5g、および尿素0.75gを反応系に添加した。添加後、110〜120℃にて3時間反応させた。これにより、ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩800g(収率98%)を得た。
1Lコルベンに、上記の実施例2で得たビスポリオキシエチレン多環フェニルエーテル(EO21モル体)792g、および軟水10gを仕込んだ。次いで、無水リン酸35gを添加した後、反応系の温度を80℃まで昇温させた。70℃にて4時間熟成させた後、軟水20gを添加して、70℃にてさらに2時間熟成させた。最後に、ジエタノールアミン26gを添加して、ビスポリオキシエチレン多環フェニルエーテルリン酸ジエタノールアミン塩866g(収率98%)を得た。
乳化重合用乳化剤として、上記の実施例8〜13で得たビスポリオキシアルキレン多環フェニルエーテル化合物を準備した。一方、比較用の乳化重合用乳化剤として、以下のものを準備した。
比較例4:ポリオキシエチレン(5)ラウリルエーテル硫酸エステルナトリウム塩
比較例5:ポリオキシエチレン(10)ジスチレン化フェニル硫酸エステルアンモニウム塩
比較例6:比較例1で得たテトラスチレン化ビスフェノールを精製せずに用い、上記の実施例3および実施例9と同様の手法により製造したビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩(EO21モル体)
上記で準備したそれぞれの乳化重合用乳化剤2g(固形分換算)をイオン交換水50gに溶解し、これに単量体であるアクリル酸ブチル50g、メタクリル酸メチル35g、スチレン15g、アクリル酸2g、および重合開始剤である過硫酸アンモニウム1gを添加して混合し、単量体エマルジョン155gを調製した。次いで、撹拌機、還流冷却器、滴下装置、温度計、窒素導入管を備えた反応器に、水5gおよび上記で調製した単量体エマルジョン2gを仕込んだ。その後、反応系の温度を昇温させ、80℃にて30分間先行重合を行なった。
乳化重合終了後の重合体エマルジョンを100メッシュスクリーンで濾過し、スクリーン上に残存した凝集物を充分に水洗した後に110℃にて2時間乾燥し、質量を測定した。測定された質量の、仕込み単量体質量に対する百分率によって、評価を行なった。
□:0.1〜0.5%
△:0.5〜1%
×:1%以上
(重合転化率)
重合体エマルジョン1gを秤量し、105±2℃にて2時間乾燥して、エマルジョン固形分を得た。得られた固形分の質量の、理論値に対する百分率によって、評価を行なった。
△:95〜99%
×:95%以下
(粒子径)
重合体エマルジョンの粒子径については、光散乱式粒度分布計(ベックマン・コールター株式会社製、LS−211)を用いて測定を行なった。
△:0.15μm以上0.20μm未満
(起泡性)
10質量%固形分に調整した重合体エマルジョン100mLを、直径45mm、高さ350mmの共栓付き500mLメスシリンダーに秤量し、30秒間強制振盪した直後の全体の容積(mL)を初期起泡性とした。
△:250mL以上300mL未満
×:300mL以上
(貯蔵安定性)
重合体エマルジョンを室温にて6ヶ月間放置した。その後、外観の変化を観察した。
△:エマルジョンの増粘が認められた
×:エマルジョンの分離またはゲル化が認められた
上記の実施例9〜14で得たビスポリオキシエチレン多環フェニルエーテル化合物の分散剤としての性能を、以下の条件により評価した。なお、比較例としては、上述した比較例6(ビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩(EO21モル体))および、ポリオキシエチレン(7)ジスチリルフェニルエーテルリン酸エステルジエタノールアミン塩(比較例7)を用いて評価を行なった。
分散剤濃度:0.5質量%/酸化チタン(石原産業株式会社製、CR−90)
攪拌条件:450rpm/min、1週間
その結果を下記の表2に示す。
実施例3〜7で得たビスポリオキシエチレン多環フェニルエーテル、および実施例9〜13で得たビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩の1質量%水溶液について、ロスマイルス法により、25℃における起泡性試験を行なった。具体的には、直後および5分後の泡の高さを測定し、比較した。ここで、実施例3〜7で得たビスポリオキシエチレン多環フェニルエーテルに対する比較例として、下記の比較例7および8を用い、実施例9〜13で得たビスポリオキシエチレン多環フェニルエーテル硫酸エステルアンモニウム塩に対する比較例として、下記の比較例9および10を用いた。なお、これらの比較例はいずれも、ビス化されていない低泡性の良好な公知の界面活性剤である。
比較例9:ポリオキシエチレン(50)ジスチレン化フェニルエーテルの1質量%水溶液
比較例10:ポリオキシエチレン(10)ジスチレン化フェニル硫酸エステルアンモニウム塩の1質量%水溶液
比較例11:ポリオキシエチレン(50)ジスチレン化フェニル硫酸エステルアンモニウム塩の1質量%水溶液
この起泡性試験の結果を下記の表3および表4に示す。なお、起泡力(mm)の値が小さいほど、低泡性に優れることを意味する。
Claims (3)
- 下記化学式1:
で表されるビスフェノール化合物と、下記化学式2:
で表されるスチレン系化合物とを、酸触媒の存在下で反応させて、下記化学式3:
で表される置換または非置換のスチリル基であり、pおよびqは、それぞれ独立して、0〜2の整数である(ただし、1≦p+q≦4である)、
で表されるスチレン化ビスフェノール化合物を得るスチレン化ビスフェノール化合物の製造方法であって、
前記スチレン系化合物の5〜100質量%を初期仕込みした状態で反応系を加熱し、70℃以上140℃未満の反応温度で反応を進行させることを特徴とする、スチレン化ビスフェノール化合物の製造方法。 - 前記ビスフェノール化合物がビスフェノールFである、請求項1に記載の製造方法。
- 下記化学式3:
で表される置換または非置換のスチリル基であり、pおよびqは、それぞれ独立して、0〜2の整数である(ただし、1≦p+q≦4である)、
で表される未精製のスチレン化ビスフェノール化合物であって、
下記化学式5:
で表されるスチレン化フェノール化合物の含有量が10質量%以下であることを特徴とする、スチレン化ビスフェノール化合物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008208703A JP5261069B2 (ja) | 2008-08-13 | 2008-08-13 | スチレン化ビスフェノール化合物の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008208703A JP5261069B2 (ja) | 2008-08-13 | 2008-08-13 | スチレン化ビスフェノール化合物の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010043029A true JP2010043029A (ja) | 2010-02-25 |
| JP5261069B2 JP5261069B2 (ja) | 2013-08-14 |
Family
ID=42014722
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008208703A Expired - Fee Related JP5261069B2 (ja) | 2008-08-13 | 2008-08-13 | スチレン化ビスフェノール化合物の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5261069B2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018070564A (ja) * | 2016-11-04 | 2018-05-10 | エア・ウォーター株式会社 | ビニルベンジル化フェノール化合物、当該ビニルベンジル化フェノール化合物の製造方法、活性エステル樹脂、当該活性エステル樹脂の製造方法、熱硬化性樹脂組成物、当該熱硬化性樹脂組成物の硬化物、層間絶縁材料、プリプレグ、およびプリプレグの製造方法 |
| JP7488648B2 (ja) | 2019-12-24 | 2024-05-22 | 日本乳化剤株式会社 | ヒドロキシ基含有化合物と酸化アルキレンとの反応生成物の製造方法 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5219643A (en) * | 1975-08-02 | 1977-02-15 | Bayer Ag | Process for preparing nuclear alkylated polynucleous phenol and application thereof |
| JPS615037A (ja) * | 1984-06-18 | 1986-01-10 | Sumitomo Chem Co Ltd | アラルキルモノ置換多価フエノ−ル類の製造方法 |
| JPS63502283A (ja) * | 1986-03-06 | 1988-09-01 | モンテディソン・エッセ・ピ・ア | スチレン化ヒドロキノンの製造方法 |
| JPH04211031A (ja) * | 1990-02-20 | 1992-08-03 | Aristech Chem Corp | 精製パラ−クミルフェノール |
| JPH0662685B2 (ja) * | 1985-07-09 | 1994-08-17 | 日本乳化剤株式会社 | 乳化重合用乳化剤 |
| JPH08109149A (ja) * | 1994-06-30 | 1996-04-30 | Hoechst Ag | アルキル化及びアルアルキル化されたポリヒドロキシ芳香族化合物及びそれらの製造方法 |
| JPH0924254A (ja) * | 1995-07-14 | 1997-01-28 | Hitachi Ltd | 濾過装置 |
-
2008
- 2008-08-13 JP JP2008208703A patent/JP5261069B2/ja not_active Expired - Fee Related
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5219643A (en) * | 1975-08-02 | 1977-02-15 | Bayer Ag | Process for preparing nuclear alkylated polynucleous phenol and application thereof |
| JPS615037A (ja) * | 1984-06-18 | 1986-01-10 | Sumitomo Chem Co Ltd | アラルキルモノ置換多価フエノ−ル類の製造方法 |
| JPH0662685B2 (ja) * | 1985-07-09 | 1994-08-17 | 日本乳化剤株式会社 | 乳化重合用乳化剤 |
| JPS63502283A (ja) * | 1986-03-06 | 1988-09-01 | モンテディソン・エッセ・ピ・ア | スチレン化ヒドロキノンの製造方法 |
| JPH04211031A (ja) * | 1990-02-20 | 1992-08-03 | Aristech Chem Corp | 精製パラ−クミルフェノール |
| JPH08109149A (ja) * | 1994-06-30 | 1996-04-30 | Hoechst Ag | アルキル化及びアルアルキル化されたポリヒドロキシ芳香族化合物及びそれらの製造方法 |
| JPH0924254A (ja) * | 1995-07-14 | 1997-01-28 | Hitachi Ltd | 濾過装置 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018070564A (ja) * | 2016-11-04 | 2018-05-10 | エア・ウォーター株式会社 | ビニルベンジル化フェノール化合物、当該ビニルベンジル化フェノール化合物の製造方法、活性エステル樹脂、当該活性エステル樹脂の製造方法、熱硬化性樹脂組成物、当該熱硬化性樹脂組成物の硬化物、層間絶縁材料、プリプレグ、およびプリプレグの製造方法 |
| JP7488648B2 (ja) | 2019-12-24 | 2024-05-22 | 日本乳化剤株式会社 | ヒドロキシ基含有化合物と酸化アルキレンとの反応生成物の製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5261069B2 (ja) | 2013-08-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6242611B2 (ja) | 界面活性剤組成物 | |
| JP6096115B2 (ja) | ポリカルボン酸減水剤の製造法 | |
| JP5367928B1 (ja) | 乳化重合用乳化剤 | |
| JP4137445B2 (ja) | (メタ)アクリル酸系重合体の製造方法 | |
| JP5281278B2 (ja) | 乳化重合用界面活性剤組成物 | |
| CN111302960B (zh) | 一种具有还原性的可聚合表面活性剂及其制备方法 | |
| JP6329153B2 (ja) | アニオン性界面活性剤組成物およびその使用 | |
| JP6556991B2 (ja) | 乳化重合用乳化剤 | |
| JP3868831B2 (ja) | 反応性界面活性剤 | |
| JP5261069B2 (ja) | スチレン化ビスフェノール化合物の製造方法 | |
| JP5968679B2 (ja) | 乳化重合用反応性乳化剤 | |
| JP3756391B2 (ja) | 乳化重合用界面活性剤組成物 | |
| JP4166369B2 (ja) | 界面活性剤 | |
| ITMI962548A1 (it) | Agenti anti-incrostazione,composizioni che li contengono e loro impiego nei processi di polimerizzazione | |
| US8519071B2 (en) | Low-viscosity aqueous compositions | |
| KR101927789B1 (ko) | 에멀젼 중합을 위한 연장된 계면활성제 | |
| JP4542235B2 (ja) | セメント添加剤の製造方法 | |
| JPH08113602A (ja) | 重合体エマルジョンの製造方法 | |
| JPH10298210A (ja) | 乳化重合用活性剤及びこれを用いた水性重合体の製造方法 | |
| JP6781329B2 (ja) | 架橋性界面活性剤 | |
| JP2014152187A (ja) | ポリカルボン酸系重合体の製造方法 | |
| WO2000012576A1 (fr) | Procede de production de polymere d'acide (meth)acrylique | |
| JP3179007B2 (ja) | 重合体エマルジョンの製造方法 | |
| JPH0199639A (ja) | 水性樹脂分散体用乳化剤 | |
| JP2015054787A (ja) | セメント分散剤の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110811 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111014 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20121212 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121218 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130214 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130416 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130426 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160502 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 5261069 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |