JP2010019765A - 検出方法、検出用試料セルおよび検出用キット - Google Patents
検出方法、検出用試料セルおよび検出用キット Download PDFInfo
- Publication number
- JP2010019765A JP2010019765A JP2008182209A JP2008182209A JP2010019765A JP 2010019765 A JP2010019765 A JP 2010019765A JP 2008182209 A JP2008182209 A JP 2008182209A JP 2008182209 A JP2008182209 A JP 2008182209A JP 2010019765 A JP2010019765 A JP 2010019765A
- Authority
- JP
- Japan
- Prior art keywords
- substance
- fluorescence
- detection
- fluorescent
- fluorescent label
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
Abstract
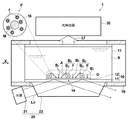
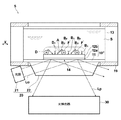
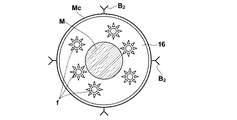
【解決手段】金属層12を含むセンサ部14に試料Sを供給し、励起光Loを照射することにより、センサ部14上に増強した光電場Dを発生せしめ、蛍光標識を励起し、この励起に起因して生じる光の量に基づいて、被検出物質Aの量を検出する検出方法において、蛍光標識として、複数の蛍光色素分子fと1以上の蛍光増強微粒子Mを、複数の蛍光色素分子fから生じる蛍光を透過する透光材料16により包含してなる蛍光物質Fを用いる。そして、この蛍光増強微粒子Mと、上記光電場D、金属層12、または近傍にある他の蛍光増強微粒子Mとの相互作用等により、蛍光標識から生じる蛍光Lfを増強する
【選択図】図1
Description
センサ部に試料を接触させることにより、試料に含有される被検出物質の量に応じた量の蛍光標識結合物質を、センサ部上に結合させ、
センサ部に励起光を照射することにより、センサ部上に増強した光電場を発生せしめ、
増強した光電場により、蛍光標識結合物質の蛍光標識を励起し、この励起に起因して生じる光の量に基づいて、被検出物質の量を検出する検出方法において、
蛍光標識として、複数の蛍光色素分子および1以上の蛍光増強微粒子を、複数の蛍光色素分子から生じる蛍光を透過する透光材料により包含してなる蛍光物質を用いることを特徴とするものである。
液体試料が流下される流路を有する基台と、
流路の上流側に設けられた流路に液体試料を注入するための注入口と、
流路の下流側に設けられた、注入口から注入された液体試料を下流側に流すための空気孔と、
注入口と空気孔との間の流路に設けられたセンサチップ部であって、流路の内壁面の一部として設けられた誘電体プレート、および誘電体プレートの試料接触面の所定領域に設けられたセンサ部を備えるセンサチップ部とを備え、
センサ部が、誘電体プレートに隣接する金属層を含む積層構造からなることを特徴とするものである。
液体試料が流下される流路を有する基台と、流路の上流側に設けられた流路に液体試料を注入するための注入口と、流路の下流側に設けられた、注入口から注入された液体試料を下流側に流すための空気孔と、注入口と空気孔との間の流路に設けられたセンサチップ部であって、流路の内壁面の一部として設けられた誘電体プレート、および誘電体プレートの試料接触面の所定領域に設けられたセンサ部を備えるセンサチップ部と、蛍光標識結合物質をセンサ部上に固定するための、センサ部上に固定された第1の結合物質とを備え、センサ部が、誘電体プレートに隣接する金属層を含む積層構造からなる、センサチップとして使用される検出用試料セル、および
液体試料と同時もしくは液体試料の流下後に流路内に流下される標識用溶液であって、被検出物質と特異的に結合する第2の結合物質、および被検出物質と競合して第1の結合物質と特異的に結合する第3の結合物質のうちのいずれか一方の結合物質と、この一方の結合物質が修飾された蛍光物質とからなる蛍光標識結合物質を含む標識用溶液を備えてなることを特徴とするものである。
<第1の実施形態>
本発明の検出方法は、例えば図1に示すように、誘電体プレート11の一面に金属層12を含むセンサ部14を有してなるセンサチップ10を用い、センサ部14に試料を接触させることにより、該試料に含有される被検出物質Aの量に応じた量の蛍光標識結合物質BFを、該センサ部14上に結合させ、センサ部14に励起光Loを照射し、励起光Loの照射によりセンサ部14上の光電場を増強させ、該増強された光電場D内における、蛍光標識結合物質BFの蛍光標識の励起に起因して生じる光の量に基づいて、被検出物質Aの量を検出する検出方法であって、蛍光標識として、複数の蛍光色素分子fおよび1以上の蛍光増強微粒子Mを、複数の蛍光色素分子fから生じる蛍光を透過する透光材料16により包含してなる蛍光物質Fを用いることを特徴とするものである。
(1)金微粒子となる金コロイドの合成
(2)金コロイド表面分散剤の置換(クエン酸→シロキサン)
5×=10−4molの金コロイド水溶液500ml(ミリ・リットル)に、APS((3-Aminopropyl)trimethoxysilane)水溶液(2.5ml、1mmol)を添加し、15分間強攪拌することにより、金コロイド表面のクエン酸を置換する。
(3)金コロイド表面のSiO2修飾
pH10〜11に調整したsodium silicate 0.54重量%水溶液20mlを工程(2)の金コロイド水溶液に添加し、強攪拌する。24時間経過すると、厚さが約4nmのSiO2被膜が形成される。この溶液を遠心分離により30mlまで濃縮した溶液に、170mlのエタノールを添加する。さらに0.6mlのNH4OH(28%)を滴下し、80μl(マイクロ・リットル)のTES(テトラエトキシシラン)を添加し、24時間ゆっくり攪拌すると、厚さ20nmのSiO2被膜からなる透光材料16が形成される。
平均粒径が約30nmのクエン酸安定化金ナノ粒子を最大約360pmol(=7×10−11重量%)含む水分散液を1ml用意し、これを遠心分離にかけた後、上澄み0.95mlを捨てる。残った暗赤色、粘稠性の沈殿物を1mlのDMF(N,N-dimethylformamide)に再分散させる。なお、過剰のクエン酸イオンは粒子のカプセル化を阻害する。また、小粒径の粒子を用いる場合は、DMFを加える前に水で洗浄した方が良い。
(2)金ナノ粒子のカプセル化
上記(1)の工程で得られた、平均粒径が約30nmのクエン酸安定化金ナノ粒子を約648pmol(=7×10−11重量%)含むDMF分散液1mlに、ポリスチレン-ポリアクリル酸ブロック共重合体(ポリスチレンが約100量体、ポリアクリル酸が約13量体)のDMF溶液(約10−2g/ml) 10μlを加え、シリンジポンプにより8.3μl/minの流量で水200μlを加えて激しく撹拌する。10分撹拌すると溶液の色が徐々に紫色に変化するので、そこで1重量%のドデカンチオールDMF溶液5μlを加え、24時間撹拌する。その後、さらにシリンジポンプにより、2ml/hの流量で水3mlを加える。
次に透析により24時間かけてDMFを除去する。次いで撹拌しながら72μlのEDC溶液(水に対して0.1重量%:24nmol)を一気に添加し、30分撹拌したところで144μlのEDODEA溶液(水に対して0.1重量%:96nmol)を一気に添加し、撹拌する。
その後、透析により24時間かけて試薬を除去し、次いで4000Gで30分間遠心分離を行い、体積で80%に相当する上澄みを捨てる。次に捨てた上澄みと同体積の水を加えて同様に遠心分離を行う。この遠心分離から遠心分離までの操作を3回以上繰り返すことにより、ポリスチレン-ポリアクリル酸ブロック共重合体の架橋物からなる被膜が金ナノ粒子(金微粒子)の周りに透光材料16として形成される。
次に、蛍光色素分子(林原生物化学研究所、NK−2014、励起波長:780nm)0.3mgの酢酸エチル溶液(1mL)を作製する。
上記ポリスチレン溶液と蛍光色素溶液を混合し、エバポレートしながら含浸を行った後、遠心分離(15000rpm、4℃、20分を2回)を行い、上清を除去する。
以上の工程により、蛍光色素分子fおよび1以上の蛍光増強微粒子Mを、蛍光色素分子fから生じる蛍光を透過する機能を有するポリスチレンにより内包してなる蛍光物質Fを得ることができる。このような手順で、ポリスチレン粒子に蛍光色素分子fを含浸させて作製された蛍光物質Fの粒径はポリスチレン粒子の粒径と同一(上記例ではφ150nm)となる。
ここでは、一例として、試料Sに含まれる被検出物質として抗原Aを検出する場合について説明する。
まず、試料保持部13中に検査対象である試料Sを流し、センサチップ10の金属膜12上に試料Sを接触させる。次いで同様に、抗原Aと特異的に結合する第2の結合物質である2次抗体B2と、蛍光標識Fとからなる蛍光標識結合物質BFとを含む溶液を流す。この場合、金属膜12に表面修飾される1次抗体B1と、蛍光標識結合物質BFの2次抗体B2とは、被検出物質である抗原Aに対してそれぞれ別の部位(エピトープ)に結合するものを用いる。なお、蛍光標識Fとして、蛍光色素分子fと1の蛍光増強微粒子Mとを内包する蛍光物質Fを用いている(図1)。試料S中に抗原Aが存在すれば、1次抗体B1に抗原Aが特異的に結合し、さらに抗原Aに蛍光標識結合物質BFの2次抗体B2が結合して、サンドイッチが形成される。その後、結合物と、未反応の蛍光標識結合物質BFを分離するため、バッファ溶液を流し、未反応の蛍光標識結合物質を排除する。
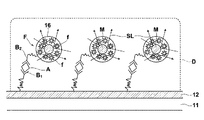
図2Aに示すように、蛍光増強微粒子Mによる散乱光SLを二次的な励起光として用いることにより、蛍光色素分子fをさらに効率的に照明することができる。前述したように光電場Dは、センサ部14の表面から離れるにしたがって、急激に減衰する。したがって、センサ部14の表面から離れた蛍光色素分子fは、励起するに充分な光を吸収することができない。つまり、蛍光増強微粒子Mは、このような蛍光色素分子fを励起する二次的な励起光として、上記の散乱光を生じせしめることにより、蛍光量増大に寄与する。
図2Bに示すように、例えば蛍光増強微粒子Mが金属微粒子である場合には、光電場Dと金属微粒子Mとの相互作用により、局在プラズモンが生じ、その結果、この局在プラズモンによって増強された近接場光NLが金属微粒子Mの周囲に染み出すこととなる。そして、蛍光増強微粒子Mの近傍にある蛍光色素分子fが、この近接場光NLに励起されることとなる。つまり、蛍光増強微粒子Mは、このような近接場光NLを生じせしめることにより、蛍光量増大に寄与する。なお、励起光Loの波長に応じて局在プラズモンを誘起できるように、金属微粒子Mの粒径は適宜選択することができる。
図2Cに示すように、例えば蛍光増強微粒子Mが金属微粒子である場合には、金属微粒子Mの近傍に金属膜12が存在するとき、金属微粒子M−金属膜12間の隙間にホットスポットHS1が生じる。「ホットスポット」とは、微小構造の物質に静電気力が集中(電界集中)する結果形成される局所的な強い電場領域である。したがって、このホットスポットHS1内に存在する蛍光色素分子fからの蛍光Lfを増強することができる。つまり、蛍光増強微粒子Mは、このようなホットスポットHS1を生じせしめることにより、蛍光量増大に寄与する。
図2Dに示すように、例えば蛍光増強微粒子Mが金属微粒子である場合には、複数の金属微粒子Mが近傍に存在するとき、金属微粒子M−金属微粒子Mの隙間にホットスポットHS2が生じる。したがって、このホットスポットHS2内に存在する蛍光色素分子fからの蛍光Lfを増強することができる。つまり、蛍光増強微粒子Mは、このようなホットスポットHS2を生じせしめることにより、蛍光量増大に寄与する。
上述第1の実施形態においては励起光Loとして、界面に所定の角度θで入射する平行光を入射するものとしたが、励起光としては、図3に模式的に示すような、角度θを中心に角度幅Δθを持つファンビーム(集束光)を用いてもよい。ファンビームの場合、プリズム122とプリズム上の金属膜112との界面に対して、角度θ―Δθ/2〜θ+Δθ/2の範囲の入射角度で入射することになり、この角度範囲内に共鳴角があれば、金属膜112に表面プラズモンを励起することができる。金属膜上への試料供給の前後において、金属膜上の媒質の屈折率が変化し、そのために表面プラズモンが生じる共鳴角が変化する。したがって、上述の実施形態のように平行光を励起光として用いる場合、共鳴角が変化するたびに平行光の入射角度を調整する必要がある。しかし、図3に示すような、界面に入射する入射角度に幅を持たせたファンビームを用いることにより、入射角度の調整をすることなく、共鳴角の変化に対応することができる。なお、ファンビームは入射角度による強度変化が少ないフラットな分布を持つものであることがより好ましい。また、以上のことは後述する第2〜第5の実施形態においても同様である。
第2の実施形態である検出方法および装置について図4を参照して説明する。図4は第2の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および検出装置は、局在プラズモン共鳴により光電場を増強させ、増強された光電場において励起された蛍光を検出する検出方法および装置である。なお、以下においては、第1の実施形態と同じ構成要素には同じ参照符号を付してある。
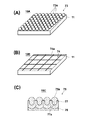
図5Aに示すセンサチップ10Aは、誘電体プレート11と、該誘電体プレート11の所定領域上にアレイ状に固着された複数の金属粒子73aからなる金属微細構造体73で構成されている。金属粒子73aの配列パターンは適宜設計できるが、略規則的であることが好ましい。かかる構成では、金属粒子73aの平均的な径及びピッチが励起光Loの波長よりも小さく設計される。
図5Cに示す例では、マッシュルーム状の金属75aの頭部が粒子状であり、サンプルプレート表面から見れば、金属微粒子が配列されたような構造になっている。かかる構成では、マッシュルーム状の金属75aの頭部が凸部であり、その平均的な径およびピッチが励起光Loの波長よりも小さく設計される。
センサチップを用意し、抗原―抗体反応をさせる工程は、第1の実施形態と同様であるため、説明を省略する。以下の実施形態においても同様とする。
本実施形態では、蛍光色素分子fと1の蛍光増強微粒子Mとを内包する蛍光物質Fを蛍光標識として用いている。そして、センサチップ10’の誘電体プレート11の所定領域に向けて励起光照射光学系20により励起光Loを照射する。光源21から出射された励起光Loはハーフミラー23により反射されてセンサチップ10’の試料接触面上に入射される。この励起光Loの照射により、金属層12’の表面で局在プラズモンが励起される。この局在プラズモンにより金属層12’上に増強された光電場Dが形成される。そして、増強された光電場内にある、蛍光物質F中の蛍光色素分子fが励起されて蛍光Lfが発生する。この蛍光Lfを光検出器30により検出をすることにより、蛍光標識結合物質と結合した被検出物質の有無および/または量を検出することができる。
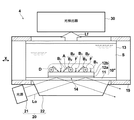
第3の実施形態の検出方法および装置について図6を参照して説明する。図6は第3の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および装置は、表面プラズモン共鳴により光電場を増強させ、増強された光電場において励起された蛍光が金属層に新たにプラズモンを誘起することにより、誘電体プレートに対して金属層形成面と反対の面側へ放射される、新たに誘起されたプラズモンからの放射光を検出するものである。
本実施形態では、蛍光色素分子fと1の蛍光増強微粒子Mとを内包する蛍光物質Fを蛍光標識として用いている。そして、第1の実施形態と同様に、励起光照射光学系20により励起光Loを照射する。励起光照射光学系20により励起光Loが誘電体プレート11と金属膜12との界面に対して全反射角以上の特定の入射角度で入射されることにより、金属膜上12の試料S中にエバネッセント光が滲み出し、このエバネッセント光によって金属膜12中に表面プラズモンが励起される。この表面プラズモンにより金属膜12表面に増強された光電場Dが形成される。そして、増強された光電場Dにある、蛍光物質F中の蛍光色素分子fが励起されて蛍光Lfが発生する。このとき、表面プラズモンによる電場増強の効果により蛍光は増強される。金属膜12上で生じたこの蛍光Lfが、金属膜12に表面プラズモンを新たに誘起し、この表面プラズモンによりセンサチップ10の金属膜形成面と反対側へ特定の角度で放射光Lpが射出される。光検出器30によって、この放射光Lpを検出することにより、蛍光標識結合物質と結合した被検出物質の有無および/または量を検出することができる。
第4の実施形態の検出方法および装置について図7を参照して説明する。図7は第4の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および装置は、金属層上に光導波層を備えたセンサチップを用い、励起光の照射により光導波層に光導波モードを励起し、光導波モードにより光電場を増強させ、増強された光電場において励起された蛍光を検出する検出方法および装置である。
本実施形態では、蛍光色素分子fと1の蛍光増強微粒子Mとを内包する蛍光物質Fを蛍光標識として用いている。そして、第1の実施形態と同様に、励起光照射光学系20により励起光Loを照射する。励起光照射光学系20により励起光Loが誘電体プレート11と金属層12aとの界面に対して全反射角以上の特定の入射角度で入射されることにより、金属層12a上にエバネッセント光が滲み出し、このエバネッセント光が光導波層12bの光導波モードと結合し、光導波モードが励起されることにより、光導波層12b上に増強された光電場Dが形成される。そして、増強された光電場にある、蛍光物質F中の蛍光色素分子fが励起されて蛍光Lfが発生する。このとき、表面プラズモンによる電場増強の効果により蛍光は増強されたものとなる。光検出器30によって、この蛍光Lfを検出することにより、蛍光標識結合物質と結合した被検出物質の有無および/または量を検出することができる。
第5の実施形態の検出方法および装置について図8を参照して説明する。図8は第5の実施形態の検出装置の概略構成示す全体図である。本実施形態の検出方法および装置は、金属層上に光導波層を備えたセンサチップを用い、励起光の照射により光導波層に光導波モードを励起し、光導波モードにより電場を増強させ、増強された電場において励起された蛍光が金属層に新たにプラズモンを誘起することにより、誘電体プレートの金属層形成面と反対の面側から放射される、新たに誘起されたプラズモンからの放射光を検出する検出方法および装置である。
本実施形態では、蛍光色素分子fと1の蛍光増強微粒子Mとを内包する蛍光物質Fを蛍光標識として用いている。そして、第1の実施形態と同様に、励起光照射光学系20により励起光Loを照射する。励起光照射光学系20により励起光Loが誘電体プレート11と金属層12aとの界面に対して全反射角以上の特定の入射角度で入射されることにより、金属層12a上にエバネッセント光が滲み出し、このエバネッセント光が光導波層12bの光導波モードと結合し、光導波モードが励起されることにより、光導波層12b上に増強された光電場Dが形成される。そして、増強された光電場Dにある、蛍光物質F中の蛍光色素分子fが励起されて蛍光Lfが発生する。このとき、表面プラズモンによる電場増強の効果により蛍光Lfは増強されたものとなる。光導波層12b上で生じたこの蛍光Lfが、金属膜12に表面プラズモンを新たに誘起し、この表面プラズモンによりセンサチップ10”の金属膜形成面と反対側へ特定の角度で放射光Lpが射出される。光検出器30によって、この放射光Lpを検出することにより、蛍光標識Fが標識された被検出物質の有無および/または量を検出することができる。
まず、前述手順により蛍光物質を作製し、その表面にポリエチレンイミン(PEI)(エポミン、日本触媒社)を修飾する。
次に、粒子表面のPEIに粒径15nmのPdナノ粒子(平均粒径19nm、徳力本社)を吸着させる。
Pdナノ粒子が吸着したポリスチレン粒子を無電解金メッキ液(HAuCl4、小島化学薬品社)に浸漬させることで、Pdナノ粒子を触媒とする無電界メッキを利用して、ポリスチレン粒子表面に金膜を作製する。
本発明の検出方法のセンサチップとして使用される検出用試料セルについて説明する。
図10Aは、第1の実施形態の検出用試料セル50の構成を示す平面図、図10Bは検出用試料セル50の側断面図である。
検出用試料セル50は、誘電体プレートからなる基台51と、基台51上に液体試料Sを保持し、液体試料Sの流路52を形成するスペーサ53と、試料Sを注入する注入口54aおよび流路52を流下した試料を排出する排出口となる空気孔54bを備えたガラス板からなる上板54とから構成され、流路52の注入口54aと空気孔54bとの間の試料接触面となる基台51の所定領域上にそれぞれ設けられた金属層58a、59aからなるセンサ部58、59が備えられている。また、注入口54aから流路52に至る箇所にはメンブレンフィルター55が備えられ、流路52下流の空気孔54bに接続する部分には廃液だめ56が形成されている。
図11は、サンドイッチ法によるアッセイに適した第2の実施形態の検出用試料セルの側断面を示すものである。本実施形態の検出用試料セル50Aにおいては、標識2次抗体吸着エリア57と、第1のセンサ部58と、第2のセンサ部59とが、基台51上に流路52上流側から順に設けられている。ここで、標識2次抗体吸着エリア57には、被検出物質である抗原と特異的に結合する2次抗体(第2の結合物質)B2と、該2次抗体B2が表面修飾された蛍光物質Fとからなる標識2次抗体BF(蛍光標識結合物質)が物理吸着によって配置されている。そして、第1のセンサ部58には、被検出物質である抗原と特異的に結合する1次抗体(第1の結合物質)B1が固定されている。また、第2のセンサ部59には、被検出物質である抗原Aとは結合せず標識2次抗体BFと特異的に結合する1次抗体B0が固定されている。本例では、流路52内に2つのセンサ部を設けた例を挙げているが、センサ部は1つのみであってもよい。なお、蛍光物質Fは、蛍光色素分子fと1の蛍光増強微粒子Mとを内包するものである。
step2:血液Soはメンブレンフィルター55により濾過され、赤血球、白血球などの大きな分子が残渣となる。
step3:メンブレンフィルター55で血球分離された血液S(血漿)が毛細管現象で流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔54bにポンプを接続し、血漿Sをポンプの吸引、押し出し操作によって流下させてもよい。図12中において血漿Sは斜線領域で示している。
step4:流路52に染み出した血漿Sと流路52内に配置された標識2次抗体BFとが混ぜ合わされ、血漿S中の抗原Aが標識2次抗体BFと結合する。
step5:血漿Sは流路52に沿って空気孔54b側へと徐々に流れ、標識2次抗体BFと結合した抗原Aが、第1のセンサ部58上に固定されている1次抗体B1と結合し、抗原Aが1次抗体B1と標識2次抗体BFで挟み込まれたいわゆるサンドイッチが形成される。
step6:抗原Aと結合しなかった標識2次抗体BFの一部は第2のセンサ部59上に固定されている1次抗体B0と結合する。さらに抗原Aまたは1次抗体B0と結合しなかった標識2次抗体BFがセンサ部上に残っている場合があっても、後続の血漿Sが洗浄の役割を担い、プレート上に浮遊および非特異吸着していた標識2次抗体BFを洗い流す。
図13は、競合法によるアッセイに適した第3の実施形態の検出用試料セルを示すものである。本実施形態の検出用試料セル50Bにおいては、標識2次抗体吸着エリア57’と、第1のセンサ部58’と、第2のセンサ部59’とが、基台51上に流路52上流側から順に設けられている。ここで、標識2次抗体吸着エリア57’には、被検出物質である抗原とは結合せず後述の1次抗体C1と特異的に結合する2次抗体C3(第3の結合物質)と、該2次抗体C3が表面修飾された蛍光物質Fとからなる標識2次抗体CF(蛍光標識結合物質)が物理吸着によって配置されている。そして、第1のセンサ部58’には、被検出物質である抗原および2次抗体C3と特異的に結合する1次抗体C1(第1の結合物質)が固定されている。また、第2のセンサ部59’には、被検出物質である抗原とは結合せず標識2次抗体CFと特異的に結合する1次抗体C0が固定されている。本例では、流路52内に2つのセンサ部を設けた例を挙げているが、センサ部は1つのみであってもよい。なお、蛍光物質Fは、蛍光色素分子fと1の蛍光増強微粒子Mとを内包するものである。
step2:血液Soはメンブレンフィルター55により濾過され、赤血球、白血球などの大きな分子が残渣となる。
step3:メンブレンフィルター55で血球分離された血液S(血漿)が毛細管現象で流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔54bにポンプを接続し、血漿Sをポンプの吸引、押し出し操作によって流下させてもよい。図14において血漿Sは斜線領域で示している。
step4:流路52に染み出した血漿Sと流路52内に配置された標識2次抗体CFとが混ぜ合わされる。
step5:血漿Sは流路52に沿って空気孔54b側へと徐々に流れ、抗原Aと標識2次抗体CFとが競合して、第1のセンサ部58’上に固定されている1次抗体C1と結合する。
step6:第1のセンサ部58’上の1次抗体C1と結合しなかった標識2次抗体CFの一部は、第2のセンサ部59’上に固定されている1次抗体C0と結合する。さらに1次抗体C1またはC0と結合していない標識2次抗体CFがセンサ部上に残っている場合があっても、後続の血漿Sが洗浄の役割を担い、プレート上に浮遊および非特異吸着していた標識2次抗体CFを洗い流す。
図15は、光導波モードによる光電場増強を利用する検出方法および装置に用いる検出用試料セルの断面図である。この検出用試料セルは、図10に示した第1の実施形態の検出用試料セルの構成と略同一であるが、それぞれのセンサ部の金属層58a、59a上にさらに光導波層58b、59bを備えている点で異なる。この検出用試料セルは、光導波層58b、59b上に上記のような抗体を適宜固定することにより、検出装置および方法の第4・第5の実施形態でのセンサチップとして使用することができる。
本発明の検出方法に使用される検出用キットについて説明する。図16は検出用キット60の構成を示す模式図である。
step2:血液Soはメンブレンフィルター55により濾過され、赤血球、白血球などの大きな分子が残渣となる。引き続き、メンブレンフィルター55で血球分離された血液S(血漿)が毛細管現象で流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔にポンプを接続し、血漿Sをポンプの吸引、押し出し操作によって流下させてもよい。図17において血漿Sは斜線領域で示している。
step3:血漿Sは流路52に沿って空気孔54b側へと徐々に流れ、血漿S中の抗原Aが、第1のセンサ部58上に固定されている1次抗体B1と結合する。
step4:標識2次抗体BFを含む標識用溶液63を注入口54aから注入する。
step5:標識2次抗体BFが毛細管現象により流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔にポンプを接続し、標識用溶液63をポンプの吸引、押し出し操作によって流下させてもよい。
step6:標識2次抗体BFが徐々に下流側に流れ、標識2次抗体BFが抗原Aと結合し、抗原Aが1次抗体B1と結合することにより、抗原Aが1次抗体B1と標識2次抗体BFで挟み込まれたいわゆるサンドイッチが形成される。抗原Aと結合しなかった標識2次抗体BFの一部は、第2のセンサ部59上に固定されている1次抗体B0と結合する。さらに、抗原Aまたは1次抗体B0と結合しなかった標識2次抗体BFがセンサ部上に残っている場合があっても、後続の血漿が洗浄の役割を担い、プレート上に浮遊および非特異吸着していた標識2次抗体BFを洗い流す。
前述の手順で作製した蛍光物質溶液(蛍光物質の直径φ150nm、励起波長780nm)に50mM MESバッファおよび、5.0mg/mLの抗hCGモノクローナル抗体(Anti−hCG 5008 SP−5、Medix Biochemica社)溶液を加えて撹拌する。これにより蛍光物質への抗体の修飾がなされる。
次に、400mg/mLのWSC(品番01−62−0011、和光純薬)水溶液を加え室温で攪拌する。
さらに、2mol/L Glycine水溶液を添加し撹拌した後、遠心分離にて、粒子を沈降させる。
最後に、上清を取り除き、PBS(pH7.4)を加え、超音波洗浄機により、表面修飾された蛍光物質を再分散させる。さらに遠心分離を行い、上清を除いた後、1%BSAのPBS(pH7.4)溶液500μL加え、表面修飾された蛍光物質を再分散させて標識用溶液とする。
本発明に係る検出用キットは、付属の検出用試料セルとして、光導波層を有する図13に示す検出用試料セルを用いることにより、競合法によるアッセイを行う検出装置および方法に好適なものとなる。
10、10’、10” センサチップ
11 誘電体プレート
12 金属層(金属膜)
12’ 金属層(金属微細構造体)
13 試料保持部
14 センサ部
16 透光材料
19 センサチップ収容部
20、20’ 励起光照射光学系
21 光源
22 プリズム
30 光検出器
50、50A、50B、61 試料セル
51 誘電体プレート
52 流路
53 スペーサ
54 上板
54a 注入口
54b 空気孔
55 メンブレンフィルター
57 標識2次抗体吸着エリア
58、59 センサ部
60 検出用キット
63 検出用キットの標識用溶液
A 抗原(被検出物質)
B1、C1 1次抗体(第1の結合物質)
B2 2次抗体(第2の結合物質)
BF、CF 標識2次抗体(蛍光標識結合物質)
C3 2次抗体(第3の結合物質)
D 光電場
F 蛍光物質
f 蛍光色素分子
Lo 励起光
Lf 蛍光
Lp 放射光
LS 散乱光
M 蛍光増強微粒子
Mc 金属被膜
Claims (15)
- 誘電体プレートの一面に、該誘電体プレートに隣接する金属層を含む積層構造からなるセンサ部を備えるセンサチップを用い、
前記センサ部に試料を接触させることにより、該試料に含有される被検出物質の量に応じた量の蛍光標識結合物質を、前記センサ部上に結合させ、
前記センサ部に励起光を照射することにより、該センサ部上に増強した光電場を発生せしめ、
該増強した光電場により、前記蛍光標識結合物質の蛍光標識を励起し、該励起に起因して生じる光の量に基づいて、前記被検出物質の量を検出する検出方法において、
前記蛍光標識として、複数の蛍光色素分子および1以上の蛍光増強微粒子を、該複数の蛍光色素分子から生じる蛍光を透過する透光材料により包含してなる蛍光物質を用いることを特徴とする検出方法。 - 前記蛍光増強微粒子が、散乱性微粒子であることを特徴とする請求項1に記載の検出方法。
- 前記蛍光増強微粒子が、金属微粒子であることを特徴とする請求項2に記載の検出方法。
- 前記蛍光増強微粒子が、金属ナノロッドであることを特徴とする請求項3に記載の検出方法。
- 前記蛍光増強微粒子の粒径が、10〜200nmであることを特徴とする請求項1から4いずれかに記載の検出方法。
- 前記励起光の照射により前記金属層にプラズモンを励起し、該プラズモンによって前記増強した光電場を発生せしめ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光を検出することを特徴とする請求項1から5いずれかに記載の検出方法。 - 前記励起光の照射により前記金属層にプラズモンを励起し、該プラズモンによって前記増強した光電場を発生せしめ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光が前記金属層に新たにプラズモンを誘起することにより、前記誘電体プレートに対し前記一面と対向する他面側へ放射される、前記新たに誘起されたプラズモンからの放射光を検出することを特徴とする請求項1から5いずれかに記載の検出方法。 - 前記センサチップとして、前記積層構造が光導波層を備えるものを用い、
前記励起光の照射により前記光導波層に光導波モードを励起し、該光導波モードによって前記増強した光電場を発生せしめ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光を検出することを特徴とする請求項1から5いずれかに記載の検出方法。 - 前記センサチップとして、前記積層構造が光導波層を備えるものを用い、
前記励起光の照射により前記光導波層に光導波モードを励起し、該光導波モードによって前記増強した光電場を発生せしめ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光が前記金属層に新たにプラズモンを誘起することにより、前記誘電体プレートに対し前記一面と対向する他面側へ放射される、前記新たに誘起されたプラズモンからの放射光を検出することを特徴とする請求項1から5いずれかに記載の検出方法。 - 請求項1から9いずれかに記載の検出方法において前記センサチップとして使用される検出用試料セルであって、
液体試料が流下される流路を有する基台と、
前記流路の上流側に設けられた該流路に前記液体試料を注入するための注入口と、
前記流路の下流側に設けられた、前記注入口から注入された前記液体試料を該下流側に流すための空気孔と、
前記注入口と前記空気孔との間の前記流路に設けられたセンサチップ部であって、前記流路の内壁面の一部として設けられた誘電体プレート、および該誘電体プレートの試料接触面の所定領域に設けられたセンサ部を備えるセンサチップ部とを備え、
前記センサ部が、前記誘電体プレートに隣接する金属層を含む積層構造からなることを特徴とする検出用試料セル。 - 前記蛍光標識結合物質を前記センサ部上に固定するための第1の結合物質であって、前記センサ部上に固定されているものを備えることを特徴とする請求項10に記載の検出用試料セル。
- 前記被検出物質と特異的に結合する第2の結合物質、および前記被検出物質と競合して前記第1の結合物質と特異的に結合する第3の結合物質のうちいずれか一方の結合物質と、該一方の結合物質が修飾された前記蛍光物質とからなる蛍光標識結合物質であって、前記センサ部より上流側の前記流路内に配置されている前記蛍光標識結合物質を備えることを特徴とする請求項11に記載の検出用試料セル。
- 前記積層構造が、光導波層を備えることを特徴とする請求項10から12いずれかに記載の検出用試料セル。
- 請求項1から9いずれかに記載の検出方法において使用される検出用キットであって、
液体試料が流下される流路を有する基台と、前記流路の上流側に設けられた該流路に前記液体試料を注入するための注入口と、前記流路の下流側に設けられた、前記注入口から注入された前記液体試料を該下流側に流すための空気孔と、前記注入口と前記空気孔との間の前記流路に設けられたセンサチップ部であって、前記流路の内壁面の一部として設けられた誘電体プレート、および該誘電体プレートの試料接触面の所定領域に設けられたセンサ部を備えるセンサチップ部と、前記蛍光標識結合物質を前記センサ部上に固定するための、該センサ部上に固定された第1の結合物質とを備え、前記センサ部が、前記誘電体プレートに隣接する金属層を含む積層構造からなる、前記センサチップとして使用される検出用試料セル、および
前記液体試料と同時もしくは前記液体試料の流下後に前記流路内に流下される標識用溶液であって、前記被検出物質と特異的に結合する第2の結合物質、および前記被検出物質と競合して前記第1の結合物質と特異的に結合する第3の結合物質のうちのいずれか一方の結合物質と、該一方の結合物質が修飾された前記蛍光物質とからなる蛍光標識結合物質を含む前記標識用溶液を備えてなることを特徴とする検出用キット。 - 前記積層構造が、光導波層を備えることを特徴とする請求項14に記載の検出用キット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008182209A JP5450993B2 (ja) | 2008-07-14 | 2008-07-14 | 検出方法、検出用試料セルおよび検出用キット |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008182209A JP5450993B2 (ja) | 2008-07-14 | 2008-07-14 | 検出方法、検出用試料セルおよび検出用キット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010019765A true JP2010019765A (ja) | 2010-01-28 |
| JP5450993B2 JP5450993B2 (ja) | 2014-03-26 |
Family
ID=41704816
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008182209A Active JP5450993B2 (ja) | 2008-07-14 | 2008-07-14 | 検出方法、検出用試料セルおよび検出用キット |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5450993B2 (ja) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010048756A (ja) * | 2008-08-25 | 2010-03-04 | Fujifilm Corp | 検出方法、検出装置、検出用試料セルおよび検出用キット |
| WO2011096394A1 (ja) * | 2010-02-02 | 2011-08-11 | コニカミノルタホールディングス株式会社 | アナライト検出プローブおよびこれを用いたアナライトの検出方法 |
| WO2012132384A1 (ja) * | 2011-03-31 | 2012-10-04 | 富士フイルム株式会社 | 局在プラズモン増強蛍光粒子、局在プラズモン増強蛍光検出用担体、局在プラズモン増強蛍光検出装置および蛍光検出方法 |
| JP2013002986A (ja) * | 2011-06-17 | 2013-01-07 | Fujifilm Corp | 蛍光検出装置、蛍光検出用の試料セルおよび蛍光検出方法 |
| JPWO2012008258A1 (ja) * | 2010-07-14 | 2013-09-09 | コニカミノルタ株式会社 | 蛍光検出装置およびこれを用いた蛍光検出方法 |
| CN106370832A (zh) * | 2016-11-09 | 2017-02-01 | 苏州呼医疗科技有限公司 | 智能呼气分子诊断系统 |
| CN106442955A (zh) * | 2016-11-09 | 2017-02-22 | 苏州呼医疗科技有限公司 | 智能呼气分子诊断系统的反射式光学检测装置 |
| JPWO2017082043A1 (ja) * | 2015-11-11 | 2018-08-30 | コニカミノルタ株式会社 | 光学式検体検出システム |
| US11604188B2 (en) | 2018-03-16 | 2023-03-14 | Panasonic Intellectual Property Management Co., Ltd. | Detection apparatus, detection substrate, and detection method |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07174693A (ja) * | 1991-06-08 | 1995-07-14 | Hewlett Packard Co <Hp> | 生体分子検出方法および装置 |
| JP2001513198A (ja) * | 1997-02-20 | 2001-08-28 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | プラズモン共鳴粒子、方法、および装置 |
| JP2004069397A (ja) * | 2002-08-02 | 2004-03-04 | Nec Corp | 分析チップおよび分析装置 |
| WO2005002045A1 (en) * | 2003-06-27 | 2005-01-06 | Sige Semiconductor (U.S.), Corp. | Integrated power amplifier circuit |
| JP2005189085A (ja) * | 2003-12-25 | 2005-07-14 | Canon Chemicals Inc | 光学プローブ及びその製造方法 |
| WO2005078415A1 (ja) * | 2004-02-13 | 2005-08-25 | Omron Corporation | 表面プラズモン共鳴センサー |
| WO2005095927A1 (ja) * | 2004-03-31 | 2005-10-13 | Omron Corporation | 局在プラズモン共鳴センサ及び検査装置 |
| JP2006010515A (ja) * | 2004-06-25 | 2006-01-12 | Aisin Seiki Co Ltd | 蛍光強度検出装置 |
| JP2007502716A (ja) * | 2003-08-18 | 2007-02-15 | エモリー ユニバーシティー | 表面増強ラマン分光法(sers)活性複合体ナノ粒子、前記の製造の方法及び前記の使用の方法 |
| JP2008145309A (ja) * | 2006-12-12 | 2008-06-26 | Fujifilm Corp | 表面プラズモン増強蛍光センサ |
| JP4851367B2 (ja) * | 2007-03-05 | 2012-01-11 | 富士フイルム株式会社 | ローカルプラズモン増強蛍光センサ |
-
2008
- 2008-07-14 JP JP2008182209A patent/JP5450993B2/ja active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07174693A (ja) * | 1991-06-08 | 1995-07-14 | Hewlett Packard Co <Hp> | 生体分子検出方法および装置 |
| JP2001513198A (ja) * | 1997-02-20 | 2001-08-28 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | プラズモン共鳴粒子、方法、および装置 |
| JP2004069397A (ja) * | 2002-08-02 | 2004-03-04 | Nec Corp | 分析チップおよび分析装置 |
| WO2005002045A1 (en) * | 2003-06-27 | 2005-01-06 | Sige Semiconductor (U.S.), Corp. | Integrated power amplifier circuit |
| JP2007502716A (ja) * | 2003-08-18 | 2007-02-15 | エモリー ユニバーシティー | 表面増強ラマン分光法(sers)活性複合体ナノ粒子、前記の製造の方法及び前記の使用の方法 |
| JP2005189085A (ja) * | 2003-12-25 | 2005-07-14 | Canon Chemicals Inc | 光学プローブ及びその製造方法 |
| WO2005078415A1 (ja) * | 2004-02-13 | 2005-08-25 | Omron Corporation | 表面プラズモン共鳴センサー |
| WO2005095927A1 (ja) * | 2004-03-31 | 2005-10-13 | Omron Corporation | 局在プラズモン共鳴センサ及び検査装置 |
| JP2006010515A (ja) * | 2004-06-25 | 2006-01-12 | Aisin Seiki Co Ltd | 蛍光強度検出装置 |
| JP2008145309A (ja) * | 2006-12-12 | 2008-06-26 | Fujifilm Corp | 表面プラズモン増強蛍光センサ |
| JP4851367B2 (ja) * | 2007-03-05 | 2012-01-11 | 富士フイルム株式会社 | ローカルプラズモン増強蛍光センサ |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010048756A (ja) * | 2008-08-25 | 2010-03-04 | Fujifilm Corp | 検出方法、検出装置、検出用試料セルおよび検出用キット |
| JPWO2011096394A1 (ja) * | 2010-02-02 | 2013-06-10 | コニカミノルタホールディングス株式会社 | アナライト検出プローブおよびこれを用いたアナライトの検出方法 |
| WO2011096394A1 (ja) * | 2010-02-02 | 2011-08-11 | コニカミノルタホールディングス株式会社 | アナライト検出プローブおよびこれを用いたアナライトの検出方法 |
| JP2015129773A (ja) * | 2010-02-02 | 2015-07-16 | コニカミノルタ株式会社 | アナライト検出プローブ |
| JPWO2012008258A1 (ja) * | 2010-07-14 | 2013-09-09 | コニカミノルタ株式会社 | 蛍光検出装置およびこれを用いた蛍光検出方法 |
| JP2012211799A (ja) * | 2011-03-31 | 2012-11-01 | Fujifilm Corp | 局在プラズモン増強蛍光粒子、局在プラズモン増強蛍光検出用担体、局在プラズモン増強蛍光検出装置および蛍光検出方法 |
| WO2012132384A1 (ja) * | 2011-03-31 | 2012-10-04 | 富士フイルム株式会社 | 局在プラズモン増強蛍光粒子、局在プラズモン増強蛍光検出用担体、局在プラズモン増強蛍光検出装置および蛍光検出方法 |
| JP2013002986A (ja) * | 2011-06-17 | 2013-01-07 | Fujifilm Corp | 蛍光検出装置、蛍光検出用の試料セルおよび蛍光検出方法 |
| JPWO2017082043A1 (ja) * | 2015-11-11 | 2018-08-30 | コニカミノルタ株式会社 | 光学式検体検出システム |
| US10648914B2 (en) | 2015-11-11 | 2020-05-12 | Konica Minolta, Inc. | Optical sample detection system |
| CN106370832A (zh) * | 2016-11-09 | 2017-02-01 | 苏州呼医疗科技有限公司 | 智能呼气分子诊断系统 |
| CN106442955A (zh) * | 2016-11-09 | 2017-02-22 | 苏州呼医疗科技有限公司 | 智能呼气分子诊断系统的反射式光学检测装置 |
| CN106442955B (zh) * | 2016-11-09 | 2023-05-16 | 苏州一呼医疗科技有限公司 | 智能呼气分子诊断系统的反射式光学检测装置 |
| US11604188B2 (en) | 2018-03-16 | 2023-03-14 | Panasonic Intellectual Property Management Co., Ltd. | Detection apparatus, detection substrate, and detection method |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5450993B2 (ja) | 2014-03-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5152917B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP5301894B2 (ja) | 検出方法 | |
| JP5143668B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP5190945B2 (ja) | 検出方法、検出装置、検出用試料セルおよび検出用キット | |
| JP5450993B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP5180703B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP5160985B2 (ja) | 検出方法、検出装置、検出用試料セルおよび検出用キット | |
| EP2110658B1 (en) | Optical signal detection method, sample cell and kit | |
| US8107071B2 (en) | Method for detecting molecular analysis light, and apparatus and sample plate for use with the same | |
| US8106368B2 (en) | Fluorescence detecting method | |
| JP2010043934A (ja) | 検出方法、検出用試料セル、検出用キット及び検出装置 | |
| JP2010038624A (ja) | 検出方法及び検出装置 | |
| JP2010145272A (ja) | プラズモン励起センサを用いたアッセイ法 | |
| JP2009258034A (ja) | 表面プラズモン放射光検出方法および装置、表面プラズモン放射光検出用試料セルおよびキット | |
| JP5315381B2 (ja) | 蛍光検出装置、蛍光検出用の試料セルおよび蛍光検出方法 | |
| JP2009236709A (ja) | 表面プラズモンセンシング方法および表面プラズモンセンシング装置 | |
| WO2012132384A1 (ja) | 局在プラズモン増強蛍光粒子、局在プラズモン増強蛍光検出用担体、局在プラズモン増強蛍光検出装置および蛍光検出方法 | |
| JP2009080011A (ja) | 蛍光検出方法 | |
| JP2009192259A (ja) | センシング装置 | |
| JP5563789B2 (ja) | 検出方法 | |
| JP2009128136A (ja) | 蛍光検出方法 | |
| JP2006003217A (ja) | センサチップ及びそれを用いたセンサ装置 | |
| JP5655125B2 (ja) | 蛍光検出方法 | |
| He et al. | Study of cell adhesion and migration by using a plasmon-enhanced total internal reflection fluorescence microscope | |
| JP2013053902A (ja) | 表面プラズモン励起増強蛍光分光法を利用して蛍光量を測定する定量分析方法ならびにそれに用いられる定量分析用キットおよびアナライト解離抑制剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110126 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120829 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120904 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121105 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130305 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20131203 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20131226 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5450993 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |