JP2009523438A - 細胞の富化 - Google Patents
細胞の富化 Download PDFInfo
- Publication number
- JP2009523438A JP2009523438A JP2008550832A JP2008550832A JP2009523438A JP 2009523438 A JP2009523438 A JP 2009523438A JP 2008550832 A JP2008550832 A JP 2008550832A JP 2008550832 A JP2008550832 A JP 2008550832A JP 2009523438 A JP2009523438 A JP 2009523438A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- mscs
- msc
- cell
- mesenchymal stem
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000002901 mesenchymal stem cell Anatomy 0.000 claims abstract description 339
- 210000004027 cell Anatomy 0.000 claims abstract description 300
- 238000000034 method Methods 0.000 claims abstract description 109
- 102000029816 Collagenase Human genes 0.000 claims abstract description 75
- 108060005980 Collagenase Proteins 0.000 claims abstract description 75
- 229960002424 collagenase Drugs 0.000 claims abstract description 73
- 210000001519 tissue Anatomy 0.000 claims abstract description 71
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 claims abstract description 15
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 claims abstract description 15
- 210000002744 extracellular matrix Anatomy 0.000 claims abstract description 15
- 239000007788 liquid Substances 0.000 claims abstract description 8
- 210000001185 bone marrow Anatomy 0.000 claims description 101
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 claims description 88
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 claims description 88
- 210000000988 bone and bone Anatomy 0.000 claims description 55
- 238000011282 treatment Methods 0.000 claims description 41
- 210000000577 adipose tissue Anatomy 0.000 claims description 37
- 230000008439 repair process Effects 0.000 claims description 29
- 230000029087 digestion Effects 0.000 claims description 24
- 210000000845 cartilage Anatomy 0.000 claims description 22
- 201000008482 osteoarthritis Diseases 0.000 claims description 22
- 210000001258 synovial membrane Anatomy 0.000 claims description 21
- 238000002659 cell therapy Methods 0.000 claims description 19
- 230000002792 vascular Effects 0.000 claims description 15
- 208000001132 Osteoporosis Diseases 0.000 claims description 11
- 239000000872 buffer Substances 0.000 claims description 11
- 108010003272 Hyaluronate lyase Proteins 0.000 claims description 8
- 102000001974 Hyaluronidases Human genes 0.000 claims description 8
- 229960002773 hyaluronidase Drugs 0.000 claims description 8
- 230000008901 benefit Effects 0.000 claims description 7
- 238000007667 floating Methods 0.000 claims description 7
- 238000007388 punch biopsy Methods 0.000 claims description 6
- 239000003814 drug Substances 0.000 claims description 5
- 239000007787 solid Substances 0.000 claims description 5
- 238000002054 transplantation Methods 0.000 claims description 5
- 230000008929 regeneration Effects 0.000 claims description 4
- 238000011069 regeneration method Methods 0.000 claims description 4
- 239000011324 bead Substances 0.000 claims description 3
- 239000003795 chemical substances by application Substances 0.000 claims description 3
- 210000003041 ligament Anatomy 0.000 claims description 3
- 210000002826 placenta Anatomy 0.000 claims description 3
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 3
- 239000000126 substance Substances 0.000 claims description 3
- 210000002435 tendon Anatomy 0.000 claims description 3
- 208000018737 Parkinson disease Diseases 0.000 claims description 2
- 238000001415 gene therapy Methods 0.000 claims description 2
- 230000000302 ischemic effect Effects 0.000 claims description 2
- 230000001404 mediated effect Effects 0.000 claims description 2
- 230000002107 myocardial effect Effects 0.000 claims description 2
- 230000004770 neurodegeneration Effects 0.000 claims description 2
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 2
- 210000002027 skeletal muscle Anatomy 0.000 claims description 2
- 208000020431 spinal cord injury Diseases 0.000 claims description 2
- 210000001562 sternum Anatomy 0.000 claims description 2
- 210000000689 upper leg Anatomy 0.000 claims description 2
- 231100000216 vascular lesion Toxicity 0.000 claims description 2
- 208000019695 Migraine disease Diseases 0.000 claims 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 claims 1
- 206010027599 migraine Diseases 0.000 claims 1
- 238000010420 art technique Methods 0.000 abstract description 4
- 238000011176 pooling Methods 0.000 abstract 1
- 238000001574 biopsy Methods 0.000 description 33
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 21
- 238000001727 in vivo Methods 0.000 description 21
- 239000002953 phosphate buffered saline Substances 0.000 description 21
- 210000000130 stem cell Anatomy 0.000 description 21
- 210000002950 fibroblast Anatomy 0.000 description 20
- 230000003321 amplification Effects 0.000 description 18
- 238000003199 nucleic acid amplification method Methods 0.000 description 18
- 239000011325 microbead Substances 0.000 description 17
- 210000003668 pericyte Anatomy 0.000 description 17
- 210000002945 adventitial reticular cell Anatomy 0.000 description 16
- 239000000243 solution Substances 0.000 description 16
- 210000001789 adipocyte Anatomy 0.000 description 15
- 230000004069 differentiation Effects 0.000 description 15
- 230000000694 effects Effects 0.000 description 14
- 239000002609 medium Substances 0.000 description 14
- 210000005222 synovial tissue Anatomy 0.000 description 14
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 11
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 11
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 11
- 239000008188 pellet Substances 0.000 description 11
- 238000000926 separation method Methods 0.000 description 11
- 102000004190 Enzymes Human genes 0.000 description 10
- 108090000790 Enzymes Proteins 0.000 description 10
- 229940088598 enzyme Drugs 0.000 description 10
- 239000012894 fetal calf serum Substances 0.000 description 10
- 238000000338 in vitro Methods 0.000 description 10
- 210000001612 chondrocyte Anatomy 0.000 description 9
- 201000010099 disease Diseases 0.000 description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 9
- 230000002255 enzymatic effect Effects 0.000 description 9
- 210000005087 mononuclear cell Anatomy 0.000 description 9
- 210000000963 osteoblast Anatomy 0.000 description 9
- 230000002648 chondrogenic effect Effects 0.000 description 8
- 230000007547 defect Effects 0.000 description 8
- 238000000684 flow cytometry Methods 0.000 description 8
- 239000003550 marker Substances 0.000 description 8
- 239000000203 mixture Substances 0.000 description 8
- 230000002188 osteogenic effect Effects 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 230000001225 therapeutic effect Effects 0.000 description 8
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 7
- 210000004271 bone marrow stromal cell Anatomy 0.000 description 7
- 210000003128 head Anatomy 0.000 description 7
- 238000011534 incubation Methods 0.000 description 7
- 208000014674 injury Diseases 0.000 description 7
- 210000004786 perivascular cell Anatomy 0.000 description 7
- 238000000746 purification Methods 0.000 description 7
- 230000001464 adherent effect Effects 0.000 description 6
- 230000000735 allogeneic effect Effects 0.000 description 6
- 230000006862 enzymatic digestion Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 239000003102 growth factor Substances 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 210000002536 stromal cell Anatomy 0.000 description 6
- 238000002560 therapeutic procedure Methods 0.000 description 6
- 238000012876 topography Methods 0.000 description 6
- 229920002683 Glycosaminoglycan Polymers 0.000 description 5
- 201000005569 Gout Diseases 0.000 description 5
- 230000005856 abnormality Effects 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 239000013553 cell monolayer Substances 0.000 description 5
- 230000003021 clonogenic effect Effects 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 230000018109 developmental process Effects 0.000 description 5
- 238000002405 diagnostic procedure Methods 0.000 description 5
- 210000002889 endothelial cell Anatomy 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 210000002468 fat body Anatomy 0.000 description 5
- 238000009472 formulation Methods 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 230000012010 growth Effects 0.000 description 5
- 230000036541 health Effects 0.000 description 5
- 238000002826 magnetic-activated cell sorting Methods 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 238000001356 surgical procedure Methods 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 4
- 206010031243 Osteogenesis imperfecta Diseases 0.000 description 4
- 102100024616 Platelet endothelial cell adhesion molecule Human genes 0.000 description 4
- 210000002449 bone cell Anatomy 0.000 description 4
- 239000011575 calcium Substances 0.000 description 4
- 238000005119 centrifugation Methods 0.000 description 4
- 210000004748 cultured cell Anatomy 0.000 description 4
- 230000002068 genetic effect Effects 0.000 description 4
- 210000002540 macrophage Anatomy 0.000 description 4
- 210000004663 osteoprogenitor cell Anatomy 0.000 description 4
- 210000000229 preadipocyte Anatomy 0.000 description 4
- 230000002062 proliferating effect Effects 0.000 description 4
- 210000004872 soft tissue Anatomy 0.000 description 4
- 230000008736 traumatic injury Effects 0.000 description 4
- 102100022464 5'-nucleotidase Human genes 0.000 description 3
- 102100022749 Aminopeptidase N Human genes 0.000 description 3
- 208000010392 Bone Fractures Diseases 0.000 description 3
- 206010017076 Fracture Diseases 0.000 description 3
- 101000678236 Homo sapiens 5'-nucleotidase Proteins 0.000 description 3
- 101000757160 Homo sapiens Aminopeptidase N Proteins 0.000 description 3
- 102000000704 Interleukin-7 Human genes 0.000 description 3
- 108010002586 Interleukin-7 Proteins 0.000 description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 description 3
- 230000002293 adipogenic effect Effects 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 238000007470 bone biopsy Methods 0.000 description 3
- 208000015322 bone marrow disease Diseases 0.000 description 3
- 230000022159 cartilage development Effects 0.000 description 3
- 230000032823 cell division Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 210000000704 endosteal cell Anatomy 0.000 description 3
- 239000012634 fragment Substances 0.000 description 3
- 210000001624 hip Anatomy 0.000 description 3
- 230000002055 immunohistochemical effect Effects 0.000 description 3
- 238000011065 in-situ storage Methods 0.000 description 3
- 150000002632 lipids Chemical class 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 102100024210 CD166 antigen Human genes 0.000 description 2
- 102000012422 Collagen Type I Human genes 0.000 description 2
- 108010022452 Collagen Type I Proteins 0.000 description 2
- 208000032170 Congenital Abnormalities Diseases 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 241000283086 Equidae Species 0.000 description 2
- DHCLVCXQIBBOPH-UHFFFAOYSA-N Glycerol 2-phosphate Chemical compound OCC(CO)OP(O)(O)=O DHCLVCXQIBBOPH-UHFFFAOYSA-N 0.000 description 2
- 206010020100 Hip fracture Diseases 0.000 description 2
- 101000800116 Homo sapiens Thy-1 membrane glycoprotein Proteins 0.000 description 2
- MIJPAVRNWPDMOR-ZAFYKAAXSA-N L-ascorbic acid 2-phosphate Chemical compound OC[C@H](O)[C@H]1OC(=O)C(OP(O)(O)=O)=C1O MIJPAVRNWPDMOR-ZAFYKAAXSA-N 0.000 description 2
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 2
- 206010062164 Seronegative arthritis Diseases 0.000 description 2
- 102100033523 Thy-1 membrane glycoprotein Human genes 0.000 description 2
- 102100033725 Tumor necrosis factor receptor superfamily member 16 Human genes 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- RGCKGOZRHPZPFP-UHFFFAOYSA-N alizarin Chemical compound C1=CC=C2C(=O)C3=C(O)C(O)=CC=C3C(=O)C2=C1 RGCKGOZRHPZPFP-UHFFFAOYSA-N 0.000 description 2
- 238000011882 arthroplasty Methods 0.000 description 2
- 210000001188 articular cartilage Anatomy 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000000481 breast Anatomy 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000010307 cell transformation Effects 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 238000012258 culturing Methods 0.000 description 2
- 238000004163 cytometry Methods 0.000 description 2
- 210000000805 cytoplasm Anatomy 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 229960003957 dexamethasone Drugs 0.000 description 2
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 2
- 230000001079 digestive effect Effects 0.000 description 2
- 238000001976 enzyme digestion Methods 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 230000035876 healing Effects 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 238000001000 micrograph Methods 0.000 description 2
- 210000003205 muscle Anatomy 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- 230000000626 neurodegenerative effect Effects 0.000 description 2
- 230000000399 orthopedic effect Effects 0.000 description 2
- 230000002138 osteoinductive effect Effects 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 210000004176 reticulum cell Anatomy 0.000 description 2
- 238000010079 rubber tapping Methods 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 230000008733 trauma Effects 0.000 description 2
- 238000011269 treatment regimen Methods 0.000 description 2
- 210000003954 umbilical cord Anatomy 0.000 description 2
- APIXJSLKIYYUKG-UHFFFAOYSA-N 3 Isobutyl 1 methylxanthine Chemical compound O=C1N(C)C(=O)N(CC(C)C)C2=C1N=CN2 APIXJSLKIYYUKG-UHFFFAOYSA-N 0.000 description 1
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- 206010001513 AIDS related complex Diseases 0.000 description 1
- 108010075348 Activated-Leukocyte Cell Adhesion Molecule Proteins 0.000 description 1
- 208000017234 Bone cyst Diseases 0.000 description 1
- 208000020084 Bone disease Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 208000031229 Cardiomyopathies Diseases 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 206010061762 Chondropathy Diseases 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 241000193159 Hathewaya histolytica Species 0.000 description 1
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 206010023203 Joint destruction Diseases 0.000 description 1
- 241001272720 Medialuna californiensis Species 0.000 description 1
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 102000003729 Neprilysin Human genes 0.000 description 1
- 108090000028 Neprilysin Proteins 0.000 description 1
- 108010032605 Nerve Growth Factor Receptors Proteins 0.000 description 1
- 102000007339 Nerve Growth Factor Receptors Human genes 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 206010053159 Organ failure Diseases 0.000 description 1
- 206010031264 Osteonecrosis Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 241000219061 Rheum Species 0.000 description 1
- 108010049264 Teriparatide Proteins 0.000 description 1
- 102000056172 Transforming growth factor beta-3 Human genes 0.000 description 1
- 108090000097 Transforming growth factor beta-3 Proteins 0.000 description 1
- 206010049514 Traumatic fracture Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 210000004504 adult stem cell Anatomy 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 239000005667 attractant Substances 0.000 description 1
- 238000011130 autologous cell therapy Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 239000000560 biocompatible material Substances 0.000 description 1
- 230000033558 biomineral tissue development Effects 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 230000007698 birth defect Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 230000010478 bone regeneration Effects 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- DEGAKNSWVGKMLS-UHFFFAOYSA-N calcein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC(CN(CC(O)=O)CC(O)=O)=C(O)C=C1OC1=C2C=C(CN(CC(O)=O)CC(=O)O)C(O)=C1 DEGAKNSWVGKMLS-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 230000003848 cartilage regeneration Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000032677 cell aging Effects 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 210000001728 clone cell Anatomy 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 210000001608 connective tissue cell Anatomy 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000000875 corresponding effect Effects 0.000 description 1
- 238000010908 decantation Methods 0.000 description 1
- 238000000432 density-gradient centrifugation Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 229940077085 diagnostic agent for diabetes testing Drugs 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000012137 double-staining Methods 0.000 description 1
- 230000002500 effect on skin Effects 0.000 description 1
- 210000001671 embryonic stem cell Anatomy 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000011436 enzymatic extraction method Methods 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 230000009395 genetic defect Effects 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 230000004957 immunoregulator effect Effects 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000012606 in vitro cell culture Methods 0.000 description 1
- 229960000905 indomethacin Drugs 0.000 description 1
- 108040006861 interleukin-7 receptor activity proteins Proteins 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 238000002595 magnetic resonance imaging Methods 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 239000004579 marble Substances 0.000 description 1
- 210000004086 maxillary sinus Anatomy 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 210000001872 metatarsal bone Anatomy 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 238000011206 morphological examination Methods 0.000 description 1
- 210000002894 multi-fate stem cell Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 201000006938 muscular dystrophy Diseases 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 206010028537 myelofibrosis Diseases 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 210000004967 non-hematopoietic stem cell Anatomy 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 229960002378 oftasceine Drugs 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000011164 ossification Effects 0.000 description 1
- 230000004824 osteo-anabolic effect Effects 0.000 description 1
- 230000004072 osteoblast differentiation Effects 0.000 description 1
- 230000000278 osteoconductive effect Effects 0.000 description 1
- 230000001009 osteoporotic effect Effects 0.000 description 1
- 230000009340 pathogen transmission Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 210000004197 pelvis Anatomy 0.000 description 1
- 210000001778 pluripotent stem cell Anatomy 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000012342 propidium iodide staining Methods 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000005057 refrigeration Methods 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 230000009758 senescence Effects 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 231100001055 skeletal defect Toxicity 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 229940054269 sodium pyruvate Drugs 0.000 description 1
- YEENEYXBHNNNGV-XEHWZWQGSA-M sodium;3-acetamido-5-[acetyl(methyl)amino]-2,4,6-triiodobenzoate;(2r,3r,4s,5s,6r)-2-[(2r,3s,4s,5r)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound [Na+].CC(=O)N(C)C1=C(I)C(NC(C)=O)=C(I)C(C([O-])=O)=C1I.O[C@H]1[C@H](O)[C@@H](CO)O[C@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 YEENEYXBHNNNGV-XEHWZWQGSA-M 0.000 description 1
- 208000028528 solitary bone cyst Diseases 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 238000009168 stem cell therapy Methods 0.000 description 1
- 238000009580 stem-cell therapy Methods 0.000 description 1
- 229940079488 strontium ranelate Drugs 0.000 description 1
- XXUZFRDUEGQHOV-UHFFFAOYSA-J strontium ranelate Chemical compound [Sr+2].[Sr+2].[O-]C(=O)CN(CC([O-])=O)C=1SC(C([O-])=O)=C(CC([O-])=O)C=1C#N XXUZFRDUEGQHOV-UHFFFAOYSA-J 0.000 description 1
- 210000002437 synoviocyte Anatomy 0.000 description 1
- OGBMKVWORPGQRR-UMXFMPSGSA-N teriparatide Chemical compound C([C@H](NC(=O)[C@H](CCSC)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@@H](N)CO)C(C)C)[C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)C1=CNC=N1 OGBMKVWORPGQRR-UMXFMPSGSA-N 0.000 description 1
- 229960005460 teriparatide Drugs 0.000 description 1
- 210000000115 thoracic cavity Anatomy 0.000 description 1
- 229950003937 tolonium Drugs 0.000 description 1
- HNONEKILPDHFOL-UHFFFAOYSA-M tolonium chloride Chemical compound [Cl-].C1=C(C)C(N)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 HNONEKILPDHFOL-UHFFFAOYSA-M 0.000 description 1
- 238000011541 total hip replacement Methods 0.000 description 1
- 238000007631 vascular surgery Methods 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 108010047303 von Willebrand Factor Proteins 0.000 description 1
- 102100036537 von Willebrand factor Human genes 0.000 description 1
- 229960001134 von willebrand factor Drugs 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0663—Bone marrow mesenchymal stem cells (BM-MSC)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/04—Drugs for skeletal disorders for non-specific disorders of the connective tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0667—Adipose-derived stem cells [ADSC]; Adipose stromal stem cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0668—Mesenchymal stem cells from other natural sources
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K2035/124—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells the cells being hematopoietic, bone marrow derived or blood cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2509/00—Methods for the dissociation of cells, e.g. specific use of enzymes
Abstract
本発明は、細胞と細胞外マトリックスを含む組織試料を、液体培地中で細胞外マトリックスから間充織幹細胞(MSC)を遊離させるのに十分な量のコラゲナーゼで処理すること、およびその後MSCを含む培地のフラクションを分離することを含む、間充織幹細胞(MSC)を分離し、富化する方法に関する。分離MSCは、フラクションが多くの臨床背景において直ちに使用できるような驚くほど多くの数で分離され得る。これは、種々のソースから大量の試料組織をプールすることを必要とするかまたはMSCを培養下で増幅することを必要とする先行技術の手法からの前進を表す。それ故、本発明は、さらに、本発明の最初の態様の方法に従って分離された細胞の臨床使用に関する。
Description
本発明は、間充織幹細胞(MSC)の富化に関する。
MSCは、多くの学術および臨床適用において使用され得る重要な細胞とみなされる。例えばMSCは、細胞に基づく治療における使用のために提案され、検討されてきた。
MSCは、骨、軟骨および脂肪細胞系統を含む多くの細胞型に分化するように誘導され得る万能性幹細胞であるため、有用である。MSCはインビトロで分化するように誘導して、その後「成熟」細胞として使用し得るか、または未分化形態に維持して、インサイチューで分化させ得る。MSCはまた、インビトロで接着細胞単層として増殖することができる有用な特徴を有する。
残念ながら、MSCは現在まで学術的および臨床的に使用が制限されてきた。このことの1つの理由は、有用な数のMSCを簡単に分離するのが困難であったことである。例えば骨髄はMSCのソースとして公知であり、多くの研究者たちが骨髄吸引液からそのような細胞を分離することを試みてきた。しかし、少数の細胞が分離されただけであり、このことから学会では、そのような組織中には非常の少数のMSCしか存在しないと考えられるに至った。臨床的に有用な数のMSCを分離するためには非現実的な容量の組織が必要とされるため、これは問題である。
有用な数を生成する唯一の方法は、MSCを分離し、その後数を増幅するまたは「増大させる(bulk−up)」ために、インビトロで、時として数週間、それらを培養することであった。
しかしそのような培養工程は多くの難点を有する。
第一に、培養増殖は時間がかかる。これはMSCの臨床的有用性を制限する。一部の場合には、幹細胞が緊急に必要とされる。例えば臨床医が、骨折した被験者に治癒を促進するために幹細胞を投与したいと考える場合、損傷から数時間以内に適切な数の幹細胞が使用可能となることが望ましい。しかし、一般通念では、臨床医が損傷した被験者の骨髄吸引液からMSCを分離し、培養で個体群を増殖させ、しばらく後に幹細胞を損傷した骨に導入すべきであると命じる。しかしながら、MSCは部分的に治癒した組織ではほとんど役に立たないと考えられる。従って、多くの細胞療法は、細胞のソースが容易に入手可能ではないため、非実用的である。
第二に、MSCの培養は、培養細胞において「表現型ドリフト」を導き得る。このドリフトは、培養したMSCが分化し始めた場合に起こり得る。この分化は予測不能であり得、しばしば望ましくない系譜をたどり得る。あるいは、人工培養条件が、細胞をインビボのままにしておいた場合に可能な表現型へと分化するのを妨げることがある。それ故、培養細胞はインビボでの細胞と同じように成長しないことがあると認識される。これはまた、臨床および科学界が培養で増殖されたMSCの価値に疑問を呈することを導く。
第三に、培養下のMSCの操作と増殖は、その後のインビボでの機能喪失に寄与し得るMSCの老化を導き得る。MSCの長期間の培養増殖はまた、遺伝的不安定性と細胞形質転換を導き得る。さらに、FDAなどの規制機関は、MSCのための細胞培養増殖手順に関する場合のように、ヒトでの治療的使用のための細胞の生成において動物製品を使用することの妥当性を疑問視してきた。
最後に、幹細胞集団のエクスビボでの増殖を成功裏に達成することはしばしば困難である。この困難を克服するには、幹細胞増殖を促進するために血清および増殖因子などの外因性因子を使用することがしばしば必要である。そのような因子は、コストがかかり、熟達した技術者の労力を必要とする複雑な培養条件を導き得る。
それ故、インビトロで増殖する必要がないMSCの迅速で便利なソースを確保することが望ましいことは認識される。しかし、現在までそのような細胞の容易に入手可能なソースは存在せず、MSCのそのようなソースを提供することが本発明の1つの目的である。
本発明の最初の態様によれば、
(a)細胞と細胞外マトリックスを含む組織試料を、液体培地中で細胞外マトリックスから間充織幹細胞(MSC)を遊離させるのに十分な量のコラゲナーゼで処理すること、および
(b)MSCを含む培地のフラクションを分離すること、
を含む、間充織幹細胞(MSC)を富化する方法が提供される。
(a)細胞と細胞外マトリックスを含む組織試料を、液体培地中で細胞外マトリックスから間充織幹細胞(MSC)を遊離させるのに十分な量のコラゲナーゼで処理すること、および
(b)MSCを含む培地のフラクションを分離すること、
を含む、間充織幹細胞(MSC)を富化する方法が提供される。
工程(b)は、以下で詳細に論じるような厳密な表現型判定基準を使用してMSCを分離することを含む。
本発明の第二の態様によれば、本発明の最初の態様に従って富化された分離間充織幹細胞(MSC)が提供される。
本発明の第三の態様によれば、薬剤としての使用のための、本発明の最初の態様に従って富化された分離間充織幹細胞(MSC)が提供される。
本発明の第四の態様によれば、コラゲナーゼおよび場合により、細胞を維持し、増殖させるまたは分化させるための培地を含む、間充織幹細胞(MSC)を富化するためのキットが提供される。
「間充織幹細胞」という用語により、我々は、接着細胞単層として増殖することができ、中胚葉系統の細胞(例えば骨、軟骨、筋肉、腱、靭帯または脂肪細胞)に分化するように誘導され得る万能性(pluripotent)または多能性(multipotent)幹細胞を意味する。上述した分化のための適切な合図は、可溶性因子(増殖因子など)を含む環境因子、および幹細胞またはそれらの子孫が位置する基質によって提供され得る。万能性および多能性は、それらの従来の意味を有すると解釈され、すなわち万能性細胞は、いくつかの分化した系譜を生じるように分化することができ、一方多能性細胞は、より限られた分化潜在能を有する、すなわち同じ系譜内で多様な細胞型を生じることができる、始原細胞または前駆細胞を含み得る。
本発明に関連して間充織幹細胞は、骨髄腔(吸引液および海綿骨の芯を含む)、滑膜または脂肪体(以下でさらに論じる)に由来する幹細胞を含み得る。例えば本発明に関連して間充織幹細胞は、これまでに処理脂肪誘引物(processed lipoaspirates)(LPA)から分離され、骨芽細胞、軟骨細胞、筋細胞、脂肪細胞およびニューロン様細胞を含む系統を生じる能力を有すると同定された型の幹細胞を含み得る。
本発明は、本発明者らが、驚くべき数のMSCが骨髄腔、滑膜および関節脂肪体からそれぞれ富化され得ることを確認した、実施例1、2および3で述べる試験に基づく。それらは、富化工程が、本発明の最初の態様に従った比較的簡単な酵素による組織消化を含み得ることを確認した。この工程は、意外にも、表現型:CD45lowD7−FIB+LNGFR+を有するMSCの集団を生成することが認められた。D7−FIBは、線維芽細胞/上皮細胞を認識するモノクローナル抗体であり(Serotec、Novus BiologicalsまたはAbcamなどの供給業者から市販されている)、LNGFRは、低親和性神経成長因子受容体、CD271である(Becton DickinsonまたはMiltenyi Biotecなどの供給業者から市販されている)。
本発明者らは、このCD45lowD7−FIB+LNGFR+細胞集団がクローン化可能な万能性MSCを含むことを明らかにした。このことから本発明者らは、常套的な臨床組織材料が、種々の重要な治療、診断および研究目的のために直接使用される十分な数のMSC(約106の高度精製細胞)のソースとして使用し得ることを認識するに至った。従来の方法によって分離された試料は、有用な数を形成するためには、上記で論じた全ての関連する難点を伴う、増幅するまたは「増大させる」必要がある少数のMSCしか生じないので、これは非常に驚くべきことであると考えられた。組織試料のコラゲナーゼ処理によって生成される驚くべき数のMSCは、臨床医または科学者が、インビトロ細胞培養の人工環境に曝露することを必要とせずに使用し得る有用な数の細胞を入手できることを可能にする。
本発明に従ってMSCが富化される組織試料は、MSCを含むことが当業者に周知である多くのソースに由来し得る。これらは、骨髄、海綿骨(どちらも同じ器官、骨髄腔の不可欠な部分として認められる)およびまた、滑膜および関節脂肪体などの軟組織を含む。本発明は、MSCがそのような組織において認められると予想されるか否かという事実には関係しない。例えば、骨髄がMSCを含み、そのようなMSCが骨髄吸引液から非常に少数だけ分離されることは周知である。これらの細胞は、吸引液から分離して、MSCの数を学術的または臨床的に有用な数まで培養して増幅する必要がある。本発明の発明性の根拠となる工程は、組織(例えば骨髄と海綿骨の両方を含む生検試料)から前例のない数の新鮮MSCを遊離させるためにコラゲナーゼを使用し得るという事実にある。学術的および/または臨床的に有用な数の新鮮MSCが、(i)比較的小さな容積の組織中に含まれること、および(ii)酵素処理によって遊離され得ることは、先行技術からは予測できなかった。実際に、本発明に従ってMSCを富化しようと試みることに対しては技術的な偏見があった。これは、当業者が、細胞の収率があまりに低いので、有用な数のMSCを生成するために処理する必要がある組織の容量は非現実的であると予想していたからである。この一般的な見解は、MSCが間葉系始原細胞階層の頂点に位置するまれな細胞であるという歴史的な認識に基づくが、本発明者らは、現在のMSCの定義と一致する高度の可塑性が、一部のあらかじめ拘束された前駆細胞および間葉系統の血管周囲細胞(周皮細胞)を含む多くの結合組織細胞に固有であると考える。
本発明の方法の工程(b)は、厳密な表現型判定基準を適用することによってMSCの集団を選択することを含むことが最も好ましい。技術水準によれば、(1)インビボでのMSCの表現型に関する十分な知識の欠如、(2)新鮮抽出されたMSCは培養増殖されたMSCに比べてより高い増殖潜在能を有する(従って当業者によって予想されるよりも少ない「新鮮」細胞しか必要としないと考えられる)ので、新鮮MSCは臨床的に有用であり得ることの理解の欠如、および(3)部分的にしか精製されていないが新鮮なMSC製剤(工程(b)に従って分離されたフラクションは血小板、マクロファージおよび他の増殖因子産生細胞を含み得る)は、表現型的に均一な培養操作されたMSCよりも臨床的に有用であり得るという認識の欠如が存在する。
MSCの表現型選択/同定は、標的細胞集団に関する多くのMSCマーカーを同定することに基づき得る。これらのマーカーは、表1において特定されるものを含み得る。
本発明者らは、多くのマーカーが有用であるが、一部のマーカーは本発明に従って調製された新鮮MSCを同定するために特に有用であることを認めた。従ってD7−FB、LNGFR(すなわちCD271)、CD13、CD73およびCD90は特に有用なマーカーである。新鮮MSCを同定するための最も好ましいマーカーは、表現型:CD45lowD7−FIB+LNGFR+を有する細胞を同定する。本発明者らは、LNGFR+が本発明に従ってMSCを同定するための単一の最も重要なマーカーであると考えられる。
上記マーカーは、本発明の工程(b)に従ってMSCを分離するためならびに細胞を同定するために有用であることが認識される。例えば、以下でより詳細に論じるように、MSC表現型についての本発明者らの知識は、螢光励起細胞選別機(FACS)による選別によってMSCを分離するときに利用し得る。
組織試料は、骨髄(BM)またはBMと海綿骨(TB)の両方を含むコア生検であることが好ましい。これらの組織からMSCを富化する方法を、以下でより詳細におよび実施例1において述べる。本発明は、BM吸引液から回収されるMSCの表現型を特性決定し、MSCの低い収率(この表現型に基づく)を明らかにする本発明者らの研究に基づく。本発明者らは、BM吸引液中の全てのMSC活性がCD45lowD7−FIB+LNGFR+細胞の希少な集団に限定されることを確認した。従って、MSCを分離しようとするものは、CD45lowD7−FIB+LNGFR+細胞を選択すべきである。実施例は、本発明者らがどのようにしてこの細胞集団の発生率とクローン原性をさらに検討したかを述べる。これらの検討の間に、本発明者らは、喜ばしい驚きと共に、表現型的に純粋なMSCが間質外膜細網細胞(ARC)と共通する多くの性質を有することを見出した。BMの間質ネットワークは、ARC、内皮細胞および周囲の血管周囲細胞、脂肪細胞、マクロファージおよび骨内膜細胞から成り、後者の細胞は骨表面の内側を覆っている。ARCは、造血−支持間質機能に関与する細胞の相互結合ネットワークを形成し、脂肪細胞および骨芽細胞の前駆細胞としてのそれらの役割が示唆されてきた。本発明者らは、MSCの活性と可塑性が、全てではないにせよ多くのARC、血管周囲細胞、前脂肪細胞および骨内膜細胞に固有であり、これらの細胞全部が同じ間葉細胞系譜に属すると仮定した。ARCとMSCの類似の表現型に関する本発明者らのデータはこの仮説を裏付けた。かなり特殊な間葉系細胞(脂肪細胞または骨芽細胞など)はインビトロでトランス分化および脱分化し得るという事実が文献に記述されている。それ故、本発明者らは、同様の工程がインビボで起こり得ることおよびこれらの間葉系譜細胞の採集(これは酵素による処理によってのみ達成され得る)は高い数の高度可塑的MSCを遊離させることを示唆した。逆に、BM吸引の間、これらの間葉系細胞はインサイチューのままであり、互いにおよび周囲の細胞外マトリックスに密接に結合している(容易に吸引されるゆるく結合した造血細胞と比較して)。本発明者らは、それ故、BM吸引液においてこれまでに認められた低い数のMSCは、インビボでのそれらの実際の数を全く表していないと仮定した。従って、本発明者らは、本発明の最初の態様の方法に従って組織試料をコラゲナーゼで処理することにより、かつてないほどの数のCD45lowD7−FIB+LNGFR+細胞(MSC)を組織から遊離させ得ることを認めた。このことから本発明者らは、学術的および臨床的に有用な量のCD45lowD7−FIB+LNGFR+細胞/MSCが小さな容量の組織から迅速におよび容易に入手できることを認識するに至った。
MSCはまた、他の結合組織または軟組織から本発明に従って分離することができる。これらの組織は、滑膜および関節脂肪体(それぞれ実施例2および3で述べるように)を含む。
本発明者らは、骨髄生検試料で使用した方法が、同じ基本的表現型と類似の機能性を有する驚くべき数のMSC(すなわちCD45lowD7−FIB+LNGFR+)を富化するためにこれらの組織に適用し得ることを明らかにした。本発明者らはまた、異なる組織中に内在するCD45lowD7−FIB+LNGFR+細胞は特異的な局所分化経路に規定されると考えられ、それ故、異なる適用のために有用であり得る(すなわちBM CD45lowD7−FIB+LNGFR+細胞は骨髄修復により適しており、一方滑膜CD45lowD7−FIB+LNGFR+細胞は軟骨修復適用により適する)ことを認識した。本発明者らは、滑膜および脂肪体において、CD45lowD7−FIB+LNGFR+細胞が血管周囲細胞(すなわち組織の血管新生および新生血管形成を支えることに関与する間葉系細胞)のトポグラフィーを有することを示した。本発明者らは、これらのCD45lowD7−FIB+LNGFR+が血管周囲細胞と同じニッチを占め、おそらく同一で、クローン原性であり、BM MSCと類似の機能性を有することを示した。それ故、本発明の方法は、滑膜および脂肪を含む固形組織中のこの特定の血管周囲ニッチからMSCを富化する手段を提供する。本発明の方法は、骨髄MSC活性の大部分の精製を可能にし、また大部分の滑膜および脂肪体のMSC活性の精製も可能にする。
本発明の最初の態様の方法は、胎盤および臍帯を含むがこれらに限定されない、他の組織からの血管周囲ニッチからMSCを分離するために使用できる。これらの組織ソースは、神経変性適用に特に適するMSCに富むと考えられる。それ故、本発明の方法に従って胎盤または臍帯から富化されたMSCは、好ましくは神経変性状態の治療において使用され得る。血管周囲分布中の分離された軟組織MSCは、BM MSCと同じ表現型を有するだけでなく、BM MSCの全ての潜在能も有すると考えられ、それ故、以下で論じる全ての適用において使用できる。
組織試料のソースは、富化されるMSCの最終的用途に依存する。
好ましい組織試料は骨から、特に骨髄(BM)からである。BM試料から富化されたMSCは、骨修復適用のために特に有用である。BM生検材料は多くの身体部位(例えば胸骨、大腿骨、骨盤または腸骨稜)から入手し得る。BMの好ましいソースは、大腿骨頭または腸骨稜である。標本はパンチ生検によって収集し得る(例えば4mmパンチ生検を使用して)。あるいは、大腿骨頭を半分に切断し、酵素消化を受けるさらに一層小さな断片を得るためにBone Mill(De Puyまたは他の製造業者)を用いて均質化する。自己BMは、患者または志願者からの腸骨稜生検より入手でき、より多数のMSCが、研究目的または同種MSC適用のために死体ドナーの何らかの海綿骨から入手できる。
コラゲナーゼ処理の前に、コア生検試料または小さな組織断片は、乾燥を防ぐためにPBSに(リン酸緩衝食塩水)に入れてもよい。しかし、試料をPBSで何度も洗浄すべきではない。これは、骨髄(ARC)を横断するMSCおよび骨に付着したMSC(骨内膜細胞)の両方が酵素抽出のために使用可能であるように、BMを保存するためである。
好ましい実施形態では、本発明に従った富化を実施しようとする組織試料は、骨髄由来の浮遊脂肪フラクション(FFF)を含み得る。本発明者らは、これまでMSCの分離の間に廃棄されていたこのフラクションが、MSCの驚くべき豊富なソースであることを認めた。
単なる例として、組織試料(単一生検として採取した)0.1gをコラゲナーゼ溶液(例えば20%(v/v)胎仔ウシ血清(FCS)中の0.25%コラゲナーゼ溶液である、Stem Cell Technologiesからの市販のコラゲナーゼ溶液(製品番号07902))0.5mlに入れてもよい。
コラゲナーゼが多くの商業的ソース(例えばStemcell technologies Inc,Vancouver,CA)から入手し得ることは認識される。多くの異なるコラゲナーゼを使用し得る。しかし、この酵素はI型コラーゲンを消化するために有効であることが好ましい。
処理する試料からMSCを遊離させるのに十分なコラゲナーゼの量が必要であることは認識される。量は、使用する試料のタイプ(例えば骨生検または脂肪体からの試料)、処理する試料の量、試料が含まれている緩衝液/溶液の容量、および酵素とのインキュベーション時間を含む、多くの因子に依存する。一般的な指針として、本発明者らは、約100〜500単位の酵素、より好ましくは250〜375単位の酵素が、BM生検試料、滑膜または脂肪体試料0.1g(0.5ml容量中、370℃で3〜4時間のインキュベーション時間)からMSCを遊離させるために十分であることを認めた。
さらに100〜500単位の酵素、より好ましくは250〜375単位の酵素が、BM試料0.1gから約10,000〜50,000MSC、より好ましくは約25,000〜150,000MSC(螢光励起細胞選別機(FACS)によって100%純度に精製)を遊離させるのに十分である。同様の、さらにはより低い用量の新鮮MSCが、OIを有する小児においておよび骨偽関節の治療において効果を有することが知られているので、そのような重要な数のMSCが遊離され得ることは意外であり、重要である。「半純粋な」MSCだけが必要とされる場合は(例えばさらなる富化工程、例えばマイクロビーズまたは螢光励起細胞選別機(FACS)による選別を用いたさらなる精製を受けていないコラゲナーゼ処理試料を傾瀉した細胞フラクション)、製剤中により多くの細胞が存在することは認識される。
試料のインキュベーションは、コラゲナーゼ活性のために最適の温度で実施されるべきである。これは通常約37℃である。しかし、一部のコラゲナーゼは触媒作用のためにわずかに異なる最適温度を有しおよび/または一連の温度にわたって(例えば20℃〜47℃)操作し得ることが認識される。
本発明の最初の態様の方法の好ましい実施形態では、4mmパンチ生検BM試料を0.25%コラゲナーゼ0.5ml中に入れる。酵素を37℃で0.5〜8時間、より好ましくは3〜4時間放置して試料を消化させ得る。
インキュベーションの間、生検からの細胞の遊離を観測するために試料の1時間に一度の検査および「タッピング(軽くたたくこと)」を実施し得る。細胞の遊離後、コラゲナーゼ溶液は混濁し、一方BM生検自体はより白くなり(骨を露出する)、または軟組織生検は完全に溶解する。特にBM生検試料に関して、2回目の別途の1時間のコラゲナーゼ処理が、骨ライニング細胞を遊離させ、それ故、最も高い潜在的骨形成能を有するMSCが特に富化された細胞フラクションを得るために好ましいと考えられる。好ましいインキュベーションの終了時に、最大細胞遊離を確実にするために最後のタッピングを実施し得る。
コラゲナーゼ活性は、当技術分野で公知の多くの手順(例えば希釈、ろ過または遠心分離とそれに続く傾瀉)を用いて停止し得る。コラゲナーゼ活性を停止し、工程(b)に従って細胞を分離する好ましい手段は、試料を20倍以上過剰のPBS(v/v)または同様の緩衝液で希釈することを含む。遊離された細胞をPBSと混合し、残存する細胞を生検から溶液中に強制的に放出させるために注射器/針を使用し得る。直後に、PBS/細胞混合物を70ミクロンの細胞ストレーナーで篩過し、その後遠心分離(1800rpmで5分間)のためにもう1つの遠心管に移し得る。次にコラゲナーゼ/PBS溶液を廃棄し、細胞ペレットを、細胞計数およびその後の操作(磁気および螢光励起細胞選別機(FACS)による分離)に適した培地、通常は2%FCSを含むDMEMに再懸濁する。
コラゲナーゼ消化および細胞分離(例えば前の項で述べたような)後、本発明者らは、表現型的に純粋なMSC集団(CD45lowD7−FIB+LNGFR+細胞)の割合が吸引液中より100倍以上高いことを認めた。細胞数は遊離された全細胞の5〜10%またはそれ以上であり得る。そのような製剤は、本発明に従って臨床的に有用である。
本発明の一部の実施形態では、本発明者らは、工程(a)にさらなる酵素消化を含めることによって最適MSC製剤が調製され得ることを確認した。それ故、さらなる酵素消化の選択は、処理される組織試料によっておよびMSCの最終的用途によって決定されることが認識される。例として、本発明者らは、2回目のコラゲナーゼ処理および/またはヒアルロニダーゼ処理が骨に関して最大数のMSCを遊離させるために特に有用であり得ることを認めた。2回目のコラゲナーゼ処理およびヒアルロニダーゼ処理を実施するためのプロトコールは実施例の中で述べる。組織が骨であり、MSCを骨修復のために使用するときは、工程(a)を、2回目のコラゲナーゼ処理および/またはヒアルロニダーゼ処理を含むように適合させることが最も好ましい。
本発明のある実施形態によれば、工程(b)を、MSC製剤の量を改善するために適用し得るさらなる手順工程によって補足してもよく、これらは、(1)死細胞/デブリの除去および(2)MSCのさらなる富化を含み得る。
細胞デブリ/死細胞の除去は多くの公知の手段によって(例えばMiltenyi BiotecからのDead Cell Removal Kitを使用して)達成され得る。この工程は、さらなる富化が磁気ビーズを使用して実施される予定である場合に望ましい(下記参照)。しかし本発明者らは、さらなる富化工程が螢光励起細胞選別機(FACS)による選別である場合にはこの細胞デブリ/死細胞の除去は必要でないことを認めた(同じく下記参照)。
遊離された細胞フラクションからのその後の磁気ベースのMSC富化のために、いくつかのアプローチを使用し得る。例えば本発明者らは、抗線維芽細胞マイクロビーズ(D7−FIB抗体と直接結合した)、MACSelectマイクロビーズ(LNGFR抗体と直接結合した)またはCD271−APCマイクロビーズ(全てMiltenyi Biotec,Bisley,UKより)による陽性選択を実施した。いずれの方法も、MSC比率のその後の10倍以上の増加(コラゲナーゼ消化物中の全細胞の50〜60%まで)を導いた。MSCの表現型についての本発明者らの知識に基づき、本発明者らは、有用であり得る他のマイクロビーズは、CD73結合またはCD105結合(後者はMiltenyi Biotecより市販されている)であると考える。あるいは、MSCと明確に交差反応しない慎重に選択した抗体カクテルを利用する系統陰性枯渇法(lineage−negative depletion methods)が使用できる。それ故、マイクロビーズの使用を伴う本発明の使用は、これまで可能と思われていたよりも少なくとも10倍大きい、治療開発のためのMSCの入手可能性を導き得る。
螢光励起細胞選別機(FACS)による選別は、本発明の方法に従って生産されたMSCフラクションをさらに富化するために使用し得る。95%以上のMSC純度が螢光励起細胞選別機(FACS)による選別によって容易に達成され得る。さらに、PI、7AADまたは他の死細胞排除染色に基づき、死細胞/デブリを除去し得る。螢光励起細胞選別機(FACS)による選別は、MSC精製を1時間以内で達成することを可能にする。
MSC富化はまた、細胞上の細胞表面マーカーを認識する抗体または他の物質を利用することによって達成され得ることが認識される。表2は、MSCを分離するために使用し得る抗体の例およびそれらが認識するマーカーを示す。
MSCを含むフラクションは直ちに使用し得る。あるいはMSCは、後日の使用のために従来の冷凍手法を用いて凍結してもよい。
本発明の最初の態様に従って精製されたMSCは、一般にMSCおよび幹細胞分野における学術研究者にとって極めて有用である。
当業者は、本発明に従った方法、細胞およびキットがまた、様々な予後および診断試験において特に有用であることを認識する。例えば血液検査室は、骨髄線維症、骨髄腫および骨髄異形成症候群を含むが、これらに限定されない疾患における間質異常をスクリーニングするための診断試験の一部としてMSC(本発明に従って)/骨髄間質支持細胞を富化し得る。骨/整形外科/リウマチ科/内分泌科および他の臨床科が、骨粗しょう症、大理石骨病、変形性関節症および骨壊死における骨芽細胞異常をスクリーニングするための診断試験の一部としてMSC/骨芽細胞前駆細胞を富化し得る。糖尿病/肥満についての診断試験は、そのような疾患における脂肪細胞発生の異常をスクリーニングするための診断試験の一部として、本発明に従って富化されたMSC/脂肪細胞前駆細胞/前脂肪細胞を利用し得る。さらに、「加齢」に関する診断および予後試験は、移植前の自家治療のための潜在能をスクリーニングする/予測するための診断試験の一部として本発明に従って富化されたMSCを使用し得る。
本発明の方法は、骨髄微小環境の生物学を明らかにする科学者にとって特に有用である。本発明の方法は、彼らの生物学を健康状態および疾患においてエクスビボで検討することを可能にする多数の間質支持細胞を精製する方法を提供する。骨髄間質細胞/MSCは培養増幅後にかなりの変化を受け、現在のDexter型間質細胞培養をインビボ生物学のための信頼できない代用法にする。本発明は、正常骨髄、骨髄異形成性骨髄および悪性骨髄において骨髄微小環境をよりよく理解することを可能にする。骨髄間質をエクスビボで検討できることは、数多くの原発性骨髄疾患、例えば多発性骨髄腫および転移性骨髄疾患の増殖因子、ケモカインおよびサイトカインの支持を定義するために重要な意味を有し得る。これは、骨髄疾患のための多数の新しい治療法を導き得る。同様に、健康状態および疾患における骨髄微小環境を理解するための潜在的可能性は、骨粗しょう症を含む骨関連疾患の治療のための新しい治療法の開発にとって意味を有し得る。
本発明の方法は、細胞治療手法において使用し得る本発明の第三の態様に従った薬剤を生産するために使用し得る。細胞療法は、自己および同種MSCの両方を利用することができる。
本発明の第三の態様に従った薬剤は、本発明の最初の態様の方法に従って分離された細胞と生理的に許容される緩衝液またはスカフォールドを含むべきである。緩衝液は、MSCを生存可能状態に維持し、同時に治療される被験者への投与のために安全である無菌細胞培養培地(および好ましくは血清等の添加を必要としない規定培地)を含み得る。スカフォールドは、MSCの付着と分化を支持し、同時に治療される被験者への投与のために安全である無菌生体適合性材料を含み得る。
本発明の最初の態様に従って提供されるMSCは、自己細胞療法が必要とされるとき特に有用である。本発明の最初の態様の方法は、臨床医が被験者から組織の試料を入手し、臨床的に有用な数のMSCを遊離させるために組織をコラゲナーゼで処理して、その後治療される被験者に細胞を再導入することを可能にする。本発明の方法は、臨床医が、組織試料を採取した被験者にMSCを迅速に再導入することを可能にする。例えば細胞は、試料の採取から数日以内に、採取と同日に、または臨床および支援スタッフの慎重な連携の下で数時間以内に(例えば3時間以内に)再導入され得る。これは、被験者を処置室または手術室から移動させる必要なしに組織試料を採取し、富化されたMSCを再導入し得ることを意味し得る。これは、MSCを採集すること、数を増大させるためにMSCを培養すること、およびその後被験者に細胞を再導入すること(通常は少なくとも数週間後に)を含む先行技術の手法に比べて重要な改善である。これは本発明の特に重要な特徴で表す。それ故、本発明の第五の態様によれば、
(a)被験者からMSCと細胞外マトリックスを含む組織試料を得ること、
(b)前記組織試料を、液体培地中で細胞外マトリックスからMSCを遊離させるのに十分な量のコラゲナーゼで処理すること、
(c)MSCを含む培地のフラクションを分離すること、および
(d)前記被験者が細胞療法から利益を得ることを可能にする身体部位で前記フラクションを前記被験者に再導入すること、
を含む、そのような治療を必要とする被験者に細胞療法を実施する方法が提供される。
(a)被験者からMSCと細胞外マトリックスを含む組織試料を得ること、
(b)前記組織試料を、液体培地中で細胞外マトリックスからMSCを遊離させるのに十分な量のコラゲナーゼで処理すること、
(c)MSCを含む培地のフラクションを分離すること、および
(d)前記被験者が細胞療法から利益を得ることを可能にする身体部位で前記フラクションを前記被験者に再導入すること、
を含む、そのような治療を必要とする被験者に細胞療法を実施する方法が提供される。
本発明者らは、MSCが、治療上適切な量で同じ被験者に再導入するために十分な、驚くべき数で被験者から分離され得ることを認めた。
MSCは、本発明の最初の態様の方法を用いることにより、本発明の第五の態様に従って富化され得ること(例えば骨髄/海綿骨から)が好ましい。
フラクションは、試料を入手してから24時間以内に、好ましくは12時間以内に、好ましくは3〜4時間以内に再導入されることが好ましい。
本発明の第五の態様の方法に従って使用される細胞は、前記MSCを凍結する必要がないように使用されることが好ましい。
本発明者らは、本発明が、以下を含むが、これらに限定されない多くの自己細胞療法レジメンに適用できることを確認した:
(1)骨修復(外傷性骨折、分節性骨欠損、頭蓋顔面再建、上顎洞底挙上術適応症、脊椎固定適応症、骨腫瘍/嚢胞適応症)
(2)軟骨修復(外傷性損傷、変形性関節症)
(3)骨格筋修復(デュシェーヌ筋ジストロフィーその他)
(4)腱修復(運動選手における外傷性損傷)
(5)靭帯修復(運動選手における外傷性損傷)
(6)半月修復(運動選手における外傷性損傷)
(7)心筋修復(心筋梗塞後および心筋症後)
(8)脊髄損傷、パーキンソン病および他の神経変性疾患
(9)免疫媒介性組織拒絶反応、移植片対宿主病および慢性関節リウマチ(免疫調節細胞療法として)
(10)脂肪物質の再生(例えば中足骨に関連する脂肪体の再建等、または乳房に関連する脂肪組織の再生、例えば手術または事故後の乳房のリモデリングにおいて)
(11)MSCは内皮細胞に分化し得る。従って本発明の方法は、内皮を形成することができる非常に多くの細胞が治療において必要とされ得る血管手術または虚血性血管病変のために有用である
(12)骨粗しょう症。
(1)骨修復(外傷性骨折、分節性骨欠損、頭蓋顔面再建、上顎洞底挙上術適応症、脊椎固定適応症、骨腫瘍/嚢胞適応症)
(2)軟骨修復(外傷性損傷、変形性関節症)
(3)骨格筋修復(デュシェーヌ筋ジストロフィーその他)
(4)腱修復(運動選手における外傷性損傷)
(5)靭帯修復(運動選手における外傷性損傷)
(6)半月修復(運動選手における外傷性損傷)
(7)心筋修復(心筋梗塞後および心筋症後)
(8)脊髄損傷、パーキンソン病および他の神経変性疾患
(9)免疫媒介性組織拒絶反応、移植片対宿主病および慢性関節リウマチ(免疫調節細胞療法として)
(10)脂肪物質の再生(例えば中足骨に関連する脂肪体の再建等、または乳房に関連する脂肪組織の再生、例えば手術または事故後の乳房のリモデリングにおいて)
(11)MSCは内皮細胞に分化し得る。従って本発明の方法は、内皮を形成することができる非常に多くの細胞が治療において必要とされ得る血管手術または虚血性血管病変のために有用である
(12)骨粗しょう症。
本発明に従って調製したMSCが骨修復(上記(1))において利用されることは、本発明の特に好ましい実施形態である。年間100万例以上の整形外科手術が、置換手術、外傷、癌、変形性関節症、骨粗しょう症、先天異常または骨格欠損の結果としての骨修復を含む。大きな骨欠損の再構築は依然として骨移植を必要とするが、これは、ドナー部位の損傷、疼痛および感染や病原体伝播の潜在的危険性を含む、多くの難点を有する。骨粗しょう症では、股関節全置換手術が、転位型股関節骨折のために現在使用可能な唯一の治療である。新たな骨折の危険度を低下させる骨同化促進薬(テリパラチドおよびラネリン酸ストロンチウムなど)における新しい進歩を以ってしても、骨粗しょう症性股関節骨折の世界的な発生率は、母集団が高齢化すると共に今後50年間に少なくとも3倍上昇すると予想される。これらの骨折を修復し、一般的に骨を治癒する新しい方法を見出すことは保健医療の緊急優先課題である。これに関して、MSCによる細胞療法は新しい解決法を提供する。
MSCは、胚幹細胞に関連する倫理的な問題がない成体幹細胞であり、インビボで骨を形成することが知られている。従って、MSCで(場合により骨伝導的スカフォールドおよび骨誘導的増殖因子と共に)工作される骨組織は、外傷および再建手術における骨同種移植片および自己移植片に代わる代替的戦略である。骨折治療に関して、骨癒合の割合および修復された骨の質の劇的な改善がMSCの局所送達によって達成された。MSC細胞療法はまた、骨形成不全症(OI)の非常に有用な治療である。
現在までこれらの公知の治療は、臨床的に有用な数を生成するために培養でのMSCの増幅に基づいてきた。MSCの培養増幅はほとんど無限の細胞供給を生じるが、製造プロセスは長く、コストがかかる。これは、一般の人々(例えばイギリスにおけるNHSなどの政府が資金援助する保健医療)にとってこれらの製品へのアクセスを排除するかまたはアクセスを厳密に制限する。高いコストに加えて、増幅MSC培養は、細胞形質転換の潜在的可能性、突然変異の蓄積、細胞老化および多能性の喪失などの深刻な生物学的問題に結びつく。最後に、重要な規制上の問題が、増幅MSCの純度および骨形成「能」の評価に関してまだ存在する。例えばCD73、CD105および培養したMSCの他の「古典的」マーカーは、現在、多能性細胞(皮膚および他のタイプの線維芽細胞で発現される)に特異的ではないことが証明されている。それ故、新しいコスト効果的でよりよく特徴付けられたMSC製品についてのニッチが存在する。
本発明の最初の態様の方法に従って調製されるMSCはこのニッチを埋めることが認識される。本発明者らは、驚くべきことに、新鮮MSCが組織試料から臨床的に有用な数で分離され得ることを見出した。増幅MSCと異なり、新鮮分離したMSCの明らかな利点は、この細胞製品が入手できる速度である。本発明の最初の態様の方法によれば、小さな海綿骨生検試料は、5時間の分離手順後に約5×105の純粋MSC(CD45lowD7−FIB+LNGFR+細胞)を生じ得る。新鮮分離MSCの2番目の利点は、高い純度を示すそれらの完全な表現型特徴付けられたのである。3番目の利点は、骨形成についてのそれらのより高い潜在能である。
本発明のさらなる好ましい実施形態では、本発明に従って調製したMSCは、軟骨修復において(上記(2))、特に変形性関節症(OA)を治療するために使用される。OAは、関節器官不全を伴う関節破壊によって特徴づけられる疾患である。関節軟骨の喪失は、患者の小群における鍵となる主要事象であると考えられる。低分子による治療的介入処置が軟骨再生における役割は実証されていない。細胞療法を利用する軟骨修復のための現在のゴールドスタンダードは、自己軟骨細胞移植(ACI)手順である。しかし、従来のACIは、最初の軟骨採集の時点から治療までを完了するのに数ヶ月を要し得る。これは非常に費用のかかる手順であり、その結果として使用可能性は限定されている。さらに、軟骨からの細胞は加齢と共に増殖と分化が低下し、高齢被験者でのACI手順の成功が少ないことに寄与するので、この手順はより若い被験者にしか適さない。またこの手順は、最初に軟骨から生検を採取することを含むので、潜在的に有害である。それにもかかわらず、ACI手順はすべての他の細胞療法を判断する基準である。最近、細胞移植を助けるためのマトリックスの使用を含むACI関連の開発が為されたが、これらは手順のより広い制限を回避しなかった。多くの骨誘導マトリックス、増殖因子および細胞製品が既に市販されている骨再生と比較すると、軟骨修復については状況がかなり困難である。
それ故、関節軟骨に分化する可能性を有するMSCは、ACI手順を想起させる手法でのOAの治療開発のための細胞の潜在的ソースとみなし得ることが認識される。しかし、認識されているMSCの希少性は、これらの細胞が、付随する感染の危険性、胎仔ウシ血清への曝露、細胞老化、効力の喪失、費用および/またはコストを伴う長期にわたる培養増幅手順を通過しなければならないことを意味する。本発明の方法は、臨床医が多数の幹細胞を迅速に入手し、速やかにこれらをOA関節軟骨欠損患者に戻すことを可能にする。これは、OAの治療における重大な進歩を表す。多数のMSCを迅速に分離できることは、軟骨欠損がOAの評価のための磁気共鳴画像法の広く行き渡った使用と共にますます認識されつつあることを考慮すると、現在の状況では特に重要である。
本発明のさらに一層好ましい実施形態では、本発明に従って調製したMSCは、骨粗しょう症の治療において利用される。本発明者らは、骨前駆細胞を含むMSC(本発明に従って調製した)の生物学および表現型が培養増幅されたMSCとかなり異なることに注目した。培養増幅されたMSCは、人における骨前駆細胞機能の評価のためのゴールドスタンダードを形成してきた。MSC/骨前駆細胞の大規模精製を実施できることは、骨粗しょう症の治療経路発見のために新しい道を切り開き得る。
本発明のさらなる実施形態によれば、本発明者らは、MSCがまた、本発明に従って外来性ソースから分離でき、その後幹細胞療法によって治療され得る医学的状態(例えば骨折またはOA)に罹患している被験者での細胞療法において利用され得ることを確認した。同種MSCは、股関節、椎骨および胸骨髄を含む様々な部位から死体ドナーより、血縁者/子孫、またはマッチする無関係なドナーから富化し得る。それ故、本発明の6番の態様によれば、
(a)死体またはドナーからMSCと細胞外マトリックスを含む組織試料を得ること、
(b)前記組織試料を、液体培地中で細胞外マトリックスからMSCを遊離させるのに十分な量のコラゲナーゼで処理すること、
(c)MSCを含む培地のフラクションを分離すること、および
(d)被験者が細胞療法から利益を得ることを可能にする身体部位で前記フラクションを前記被験者に導入すること
を含む、そのような治療を必要とする被験者に細胞療法を実施する方法が提供される。
(a)死体またはドナーからMSCと細胞外マトリックスを含む組織試料を得ること、
(b)前記組織試料を、液体培地中で細胞外マトリックスからMSCを遊離させるのに十分な量のコラゲナーゼで処理すること、
(c)MSCを含む培地のフラクションを分離すること、および
(d)被験者が細胞療法から利益を得ることを可能にする身体部位で前記フラクションを前記被験者に導入すること
を含む、そのような治療を必要とする被験者に細胞療法を実施する方法が提供される。
死体またはドナーは被験者と同じ種であることが認識される。被験者はヒトであることが最も好ましい。しかし、本発明者らは、LNGFRマーカーが多くの他の動物(例えばウシ、ウマ、ヤギおよびヒツジ)において保存されていることに注目した。それ故、同じ手順が動物(例えばイヌおよび特にウマなどの愛玩動物)において骨または軟骨修復のための細胞を入手するために使用できることが認識される。
富化されたMSCの同種ソースは、本発明の第五の態様に関して列挙したものと同じ治療レジメン(1〜12)において使用し得る。
本発明の方法に従ってMSCが富化される組織は、細胞のその後の分化に関して達成されるべき所望治療特性に準拠して選択され得る。例えば本発明者らは、滑膜組織から富化されたMSCが著明な軟骨形成特性を有する細胞を生じることを見出し、従って軟骨の生成を治療的に促進することが望ましい状況では、MSCを滑膜から富化することが好ましいと考えられる。
同様に、本発明者らは、膝蓋下脂肪体から富化されたMSCが一貫して高い脂肪生成特性を有する細胞を生じることを認め、従って脂肪組織の生成を治療的に促進することが望ましい状況では、MSCを脂肪体から富化することが好ましいと考えられる。
本発明の第六の態様に従って富化されたMSCはまた、同種MSCが、治療される被験者における遺伝的欠陥を矯正する遺伝子型を有する状況下での遺伝子治療において適用され得る。そのような細胞で治療される状態は以下を含む。
(a)骨形成不全症およびまれな軟骨形成不全症および筋肉の遺伝的疾患を含むが、これらに限定されない、骨および軟骨機能の喪失に関連する先天異常
(b)骨髄腫および骨髄異形成症候群その他を含む、間質機能の喪失に関連する血液学的異常。
(b)骨髄腫および骨髄異形成症候群その他を含む、間質機能の喪失に関連する血液学的異常。
本発明のさらなる実施形態によれば、本発明の第五および第六の態様の治療レジメンは、工程(c)で分離されたフラクションが、被験者に導入される(または再導入される)前に富化されたMSCを遺伝的に修飾して処理されるように適合させ得る。
被験者からのMSC(すなわち自己MSC)は、遺伝的に修飾されて被験者に再導入されることが好ましい。しかし、一部の臨床状況は、死体またはドナーソースからのMSCが必要とされることを決定付け得ることが認識される。実際に、そのようなMSC(死体またはドナーソースからの)は所望遺伝子型を含み得る。細胞は、それ故、1つの遺伝的異常(上記で考慮されるような)を矯正するために被験者に導入され得、治療される被験者においてさらなる遺伝的影響を及ぼすために遺伝的修飾を施され得る。従って、本発明に従って富化された細胞は、遺伝的成分を有する多くの状態の治療において使用でき、これらは、上記(1)〜(9)および特に(10)および(11)で考慮されるものを含む。
本発明の第四の態様に従ったキットは、上記で論じた何らかのコラゲナーゼを含み得る。コラゲナーゼはI型コラーゲンを消化することが好ましい。コラゲナーゼはヒストリチクス菌(Clostridium histolyticum)(例えばStemcell Technolgies Inc,Vancouver,CAによって供給されるような)に由来し得る。
キットは、場合により、コラゲナーゼのための適切な希釈剤および緩衝液(例えばリン酸緩衝食塩水(PBS)、場合により最終濃度20%の胎仔ウシ血清を含む)および試料(これも、好ましくは2%胎仔牛血清を含む、PBSであるか、またはDMEMなどの生理的に許容される緩衝液であり得る)を含み得る。
工程(b)がMSCのさらなる精製を含む予定であるとき、キットは、これを実施するための試薬をさらに含むことが好ましい。従ってキットは、MSCの磁気ビーズ分離に適する試薬および装置を含み得る。従ってキットは、本明細書で論じるようにMACSカラム、マイクロビーズ、MACS緩衝液(0.1%ウシ血清アルブミンを含む)を含み得る。あるいはキットは、遊離されたMSCのさらなる精製のための螢光励起細胞選別機(FACS)試薬(例えば表2に列挙する抗体および緩衝液(例えばPBS))を含み得る。
本発明を、実施例によっておよび以下の図面を参照してさらに説明する。
骨髄試料からの間充織幹細胞の富化
1.1 実験材料および方法
1.1.1 試料の収集
(i)BM吸引液(2〜10ml)を正常ドナーの後腸骨稜から得た。Lymphoprep(Nycomed,Oslo,Norway)による分離後にBM単核細胞(MNC)を収集した。浮遊脂肪フラクション(FFF)に集中する細胞凝集物を手動で攪拌によって分散させ、遠心分離した。単房性脂肪細胞は上部に浮遊したままであったが、間質細胞はペレットに集中した。
1.1 実験材料および方法
1.1.1 試料の収集
(i)BM吸引液(2〜10ml)を正常ドナーの後腸骨稜から得た。Lymphoprep(Nycomed,Oslo,Norway)による分離後にBM単核細胞(MNC)を収集した。浮遊脂肪フラクション(FFF)に集中する細胞凝集物を手動で攪拌によって分散させ、遠心分離した。単房性脂肪細胞は上部に浮遊したままであったが、間質細胞はペレットに集中した。
(ii)BM生検材料を、同意を得た変形性関節症(OA)を有する患者の股関節形成術の間に除去された大腿骨頭から得た。大腿骨頭は外科医によって半分に切断され、PBSの入った無菌容器中で検査室に送達された。4mmパンチ生検を用いて標本を収集した。あるいは、Bone Mill(De Puyまたは他の製造業者)を用いて大腿骨頭を均質化し、酵素消化を受けるさらに一層小さな断片を得た。
1.1.2 コラゲナーゼ消化
パンチ生検試料0.1gを0.25%コラゲナーゼ(Stem Cell Technologies,Vancouver,Canada)0.25mlで3〜4時間消化した。これは、酵素約250〜375単位に相当した。本発明者らは、これが細胞の回収率および生存度のために最適であることを見出した。
パンチ生検試料0.1gを0.25%コラゲナーゼ(Stem Cell Technologies,Vancouver,Canada)0.25mlで3〜4時間消化した。これは、酵素約250〜375単位に相当した。本発明者らは、これが細胞の回収率および生存度のために最適であることを見出した。
1.1.3 MSCフラクションの取扱い
好ましいインキュベーション時間の終了時に、コラゲナーゼ溶液を20倍以上過剰のPBS(v/v)で希釈し、注射器/針を使用して放出された細胞をPBSと混合し、残存する細胞を生検から溶液中に強制的に放出させた。直後に、PBS/細胞混合物を70ミクロンの細胞ストレーナーで篩過し、遠心分離(1800rpmで5分間)のためにもう1つの遠心管に移した。次にコラゲナーゼ/PBS溶液を廃棄し、細胞ペレットを、細胞計数およびその後の操作(磁気および螢光励起細胞選別機(FACS)による分離)に適した培地、通常は2%FCSを含むDMEMに再懸濁した。
好ましいインキュベーション時間の終了時に、コラゲナーゼ溶液を20倍以上過剰のPBS(v/v)で希釈し、注射器/針を使用して放出された細胞をPBSと混合し、残存する細胞を生検から溶液中に強制的に放出させた。直後に、PBS/細胞混合物を70ミクロンの細胞ストレーナーで篩過し、遠心分離(1800rpmで5分間)のためにもう1つの遠心管に移した。次にコラゲナーゼ/PBS溶液を廃棄し、細胞ペレットを、細胞計数およびその後の操作(磁気および螢光励起細胞選別機(FACS)による分離)に適した培地、通常は2%FCSを含むDMEMに再懸濁した。
一部の試料から、CD45lowD7−FIB+LNGFR+細胞を、以前に述べられているように(Jones et al.Arthritis Rheum 2002:46:3349−60)、フローサイトメトリーのために処理し、精製し、増幅し、分化させた。
1.2 結果
1.2.1 骨髄(BM)吸引液中のまれな間充織幹細胞(MSC)がD7−FIB+CD45lowLNGFR+表現型を有することの確認
本発明者らは、BM吸引液において全てのMSC活性がCD45lowD7−FIB+LNGFR+細胞の希少集団に限定されることを確認した。本発明者らはさらに、この集団の発生率とクローン原性を検討した。同じドナーに関して、4色サイトメトリーによって測定した、BM(単核細胞)MNCフラクション中のCD45lowD7−FIB+LNGFR+細胞の平均発生率は0.039±0.037%であり(図1、上)、同じ試料中で生じるCFU−Fの平均発生率0.007±0.006%(n=30)に匹敵する大きさであった。
1.2.1 骨髄(BM)吸引液中のまれな間充織幹細胞(MSC)がD7−FIB+CD45lowLNGFR+表現型を有することの確認
本発明者らは、BM吸引液において全てのMSC活性がCD45lowD7−FIB+LNGFR+細胞の希少集団に限定されることを確認した。本発明者らはさらに、この集団の発生率とクローン原性を検討した。同じドナーに関して、4色サイトメトリーによって測定した、BM(単核細胞)MNCフラクション中のCD45lowD7−FIB+LNGFR+細胞の平均発生率は0.039±0.037%であり(図1、上)、同じ試料中で生じるCFU−Fの平均発生率0.007±0.006%(n=30)に匹敵する大きさであった。
さらに、本発明者らは、これのまれな細胞集団の発生率が、D7−FIBマイクロビーズによる前富化後に約100倍上昇する(7±6%まで、n=38)ことを見出した(図1、中央のパネル)。この前富化工程は、D7−FIBに直接結合したマイクロビーズ(Anti−Fibroblast Microbeads,Miltenyi Biotec)による正の選択(positive selection)である。簡単に述べると、108BM MNCをマイクロビーズ100μlと共に室温で15分間インキュベートし、その後1800rpm×5分間洗浄して非結合マイクロビーズを除去する。次に細胞をMiniMacsカラム(磁石内に置いた)に適用し、非結合フラクションをMACS緩衝液(0.5%BSAを含むPBS)6ml中に収集する。その後、カラムを磁石から取り出し、結合フラクション(MSCを含む)をMACS緩衝液0.5〜1ml中に遊離させる。これがMACS分離の標準プロトコールである。
CD45lowD7−FIB+LNGFR+集団を選択するための螢光励起細胞選別機(FACS)による選別後、CD45lowD7−FIB+LNGFR+細胞集団の純度は95%超に上昇した(図1、下のパネル)。この富化された集団について、標準CFU−Fアッセイ(Castro−Malaspina et al.(1980)Blood 56 p289−301)において6細胞のうち1個(17±4%、n=6)が30以上の細胞の定義されたコロニーを形成した。
マッチするCD45+細胞からはコロニーが成長しなかった。これらのデータは、BM吸引液中の全てのクローン原性MSCがまれなCD45lowD7−FIB+LNGFR+集団内に含まれることを確認した。
1.2.2 インビボでのBM MSCの間質特徴
本発明者らは、BM吸引液から精製したMSCが、BM外膜細網細胞(ARC)を想起させる間質形態(数多くの突起を有する星形)を示すこと、および小さな脂肪滴がそれらの細胞質に見出されることに注目した(図2A)。BM生検に関して、ARC形態を有する細胞は、インビボMSCで発現されたCD10マーカーに関して陽性であった(図2B)。さらに、精製したインビボBM MSCは、ARCの主要特徴である、アルカリホスファターゼ(ALP)に関して均一に陽性であった(図2C)。ALPに対する抗体(ALP骨/肝アイソフォームに対する、B4−78クローン)での染色は、全てのインビボMSCでの均一な発現を明らかにした(図2D)。ALP発現は、MSCの培養増幅後徐々に消失した(図2E)。リンパ球産生の間質支持のために非常に重要であり、ARCによって産生されることが公知のサイトカイン、IL−7の発現も、増幅後に低下した(図2F)。培養した皮膚線維芽細胞はALPについて常に陰性であり、極わずかなIL−7を発現した(図2EおよびF)。
本発明者らは、BM吸引液から精製したMSCが、BM外膜細網細胞(ARC)を想起させる間質形態(数多くの突起を有する星形)を示すこと、および小さな脂肪滴がそれらの細胞質に見出されることに注目した(図2A)。BM生検に関して、ARC形態を有する細胞は、インビボMSCで発現されたCD10マーカーに関して陽性であった(図2B)。さらに、精製したインビボBM MSCは、ARCの主要特徴である、アルカリホスファターゼ(ALP)に関して均一に陽性であった(図2C)。ALPに対する抗体(ALP骨/肝アイソフォームに対する、B4−78クローン)での染色は、全てのインビボMSCでの均一な発現を明らかにした(図2D)。ALP発現は、MSCの培養増幅後徐々に消失した(図2E)。リンパ球産生の間質支持のために非常に重要であり、ARCによって産生されることが公知のサイトカイン、IL−7の発現も、増幅後に低下した(図2F)。培養した皮膚線維芽細胞はALPについて常に陰性であり、極わずかなIL−7を発現した(図2EおよびF)。
本発明者らは、これらのデータを合わせて考慮したとき、インビボでのBM MSCはARCと一致する多くの特徴を有し、これらの特徴がインビトロ培養後に失われることを認識して驚いた。これは2つのことを示唆した。第一に、MSCの培養は表現型の変化を導くので、望ましくないと考えられる。第二に、当業者はインビボでのMSCがARC様の性質を有することを認識していない。ARCは細胞の相互結合ネットワークを形成し、酵素処理によって遊離され得る。従って本発明者らは、酵素消化を用いてMSCを分離することも可能であることを認識した。本発明者らは、MSC活性が、ARCおよびおそらく骨ライニング細胞、血管周囲細胞および前脂肪細胞などの他のこれまで見過ごされてきた細胞に存すると考える。これらは全て吸引することが不可能であり、それが、酵素消化が必要とされる理由である。
1.2.3 BM間質細胞凝集物からのインビボMSCの酵素による遊離
MSCがARC様の性質を有し得ることが認識されたので、本発明者らは、組織の酵素消化がMSCを遊離するかどうかを検討した。本発明者らは、この着想を、変形性関節症(OA)を有する患者の股関節形成術の間に除去された大腿骨頭から得た材料で試験した。
MSCがARC様の性質を有し得ることが認識されたので、本発明者らは、組織の酵素消化がMSCを遊離するかどうかを検討した。本発明者らは、この着想を、変形性関節症(OA)を有する患者の股関節形成術の間に除去された大腿骨頭から得た材料で試験した。
MSCは、BM吸引液からの単一細胞懸濁液中の非常にまれな集団である。108の吸引BM MNCからの高度に純粋なMSC(CD45lowD7−FIB+LNGFR+)の平均細胞収量は、吸引骨髄1ミリリットル当たり約2,000MSCに等しい、11,000細胞(4,000〜63,000の範囲、n=14)であった。この収率は臨床的に有用であるためにはあまりに低く、有用な数の細胞を生成するためにインビトロでの増幅を必要とする。さらに、上記で指摘したように、本発明者らは、増幅工程がMSC表現型の変化を導き得ると考えられる。
インビボでのBM MSCがARC細胞と同じ特徴の多くを共有することが認識されたので、本発明者らは次に、1.1で述べた方法(ARC/マトリックスネットワークを解体することができる方法に基づく)を用いた酵素による抽出の方法が、従来の骨髄吸引液ソースと異なって、固体組織生検から高い数のMSCを遊離させるのに適するかどうかを試験した。
3時間、または3〜4時間の、生検のコラゲナーゼ処理はCD45lowD7−FIB+LNGFR+細胞を遊離させ、それらの細胞は、吸引液から精製されたMSCと形態および表現型的に類似するが、驚くべきことに、生検試料から遊離された集団におけるそれらの細胞の割合は、吸引液中で認められるレベルよりも約100倍高かった(BM吸引液中での0.039±0.037%生細胞、n=30に対し、5±3%生細胞、n=8)。この上昇は、図3の上のパネルに示す螢光励起細胞選別機(FACS)による結果において指示されている。
さらに、本発明者らは意外にも、疾患微小環境が起源であるにもかかわらず、本発明の最初の態様の方法に従って消化生検から精製されたCD45lowD7−FIB+LNGFR+細胞は、軟骨形成のレベルは低下していたが(正常BM対照によって生産された3±2μgに比べて硫酸化グリコサミノグリカン(GAG)/ペレットの1±1μg、n=4)、増殖および分化に関して正常なMSC機能を保持することを認めた。この所見は、OA患者のBMに由来するMSCの公知の特徴と一致した。正常個人からの海綿骨生検を使用したときは、正常レベルのMSC軟骨形成が得られた(データは示していない)。
この試験の結果は図3の下のパネルに示され、本発明の最初の態様の方法に従って富化したMSCの顕微鏡写真と螢光励起細胞選別機(FACS)による分析を例示する。このパネルの左側の図に示す螢光励起細胞選別機(FACS)による結果は、MSCの性質を例証するマーカーの、ゲートCD45lowD7−FIB+LNGFR+細胞(すなわち新鮮MSC)での発現を示す。このパネルの右側の図に示す顕微鏡写真は、コラゲナーゼ消化によって得たCD45lowD7−FIB+LNGFR+細胞が3つの間葉系統に分化できることを示す。
消化生検から選別された高度富化MSC(CD45lowD7−FIB+LNGFR+)の収量は、吸引液から通常得られる収量よりも平均で50倍(一部の場合には100倍超)高かった(108の吸引BM MNCからの11,000細胞、4,000〜63,000の範囲、n=14に比べて、108総細胞当たり約550,000細胞、80,000〜800,000の範囲、n=6)。平均で、0.1g生検は、約25,000CFU−Fに等しい、約150,000CD45lowD7−FIB+LNGER+細胞を生じた(n=7)。遊離された細胞フラクション中のCFU−Fの割合はCD45lowD7−FIB+LNGFR+細胞の発生率と直接相関した(R=0.89、n=7)。それ故、本発明者らは、単一の0.1cm3(0.1g重量)生検から約10,000MSCまたは25,000または150,000MSCを得ることができた。本発明者らは、この収量が本方法によって誘導されるMSCの直接臨床使用を可能にするのに十分なほど高いことを認識して驚いた。これらの収量は、BM吸引液150〜350ミリリットルを使用するのに等しい。
実際に、本発明者らは、本発明の最初の態様の方法に従ったコラゲナーゼ消化によって遊離されるCD45lowD7−FIB+LNGFR+細胞の発生率(2〜9%、n=8)が非常に高いので、それらの検出、分離または治療としての使用を可能にするためにマイクロビーズによる前富化がもはや必要ではないことを見出した。他方で、従来のBM吸引液からの同じMSC用量を同じ目的に使用する場合(すなわち150〜350ミリリットル)、同様のレベルの純度を確保するためにMSCをかなり濃縮しなければならない。本発明は、臨床医が複雑で時間のかかる富化工程または培養での増幅を必要とせずに試料から採取したMSCを迅速に利用することを可能にするので、これは本発明者らの方法がいかに有利であるかを例示する。さらに、本発明者らは、1名の患者からの1つの大腿骨頭が、本発明の方法に従って処理され、BM吸引液を使用した場合には不可能である多数の治療のために十分なMSCを提供できることを立証した。
1.2.3 コラゲナーゼによる二重消化を用いた高度骨形成性MSCの酵素による遊離
骨修復適用のためには、卓越した骨形成能力を有するMSCの使用が望ましい。MSC活性が骨ライニング細胞に存在し得ることが認識されたので、本発明者らは、1.1で述べた3〜4時間のコラゲナーゼ消化工程に加えて、付加的な酵素による抽出の方法が、高い骨形成能力を有するMSCを遊離させるのに適することを示すことができた。図4AおよびBに認められるように、本発明者らは、1.1で述べた方法を用いるコラゲナーゼ消化工程が、大部分の骨ライニング細胞を除去するが、全部ではない(平均で全DNAの約2%が骨に残る、n=3)ことを明らかにすることができた。2回目の1時間のコラゲナーゼ消化工程を1回目の消化物の収集後の生検断片で実施したとき、骨に残された細胞の割合は5倍近く低下し、回収された細胞の総収量が平均5%上昇した(n=3)。2回目の消化物のクローン原性は1回目の消化物と同様であったが(それぞれ、12CFU−F/5,000遊離細胞に比べて13CFU−F/5,000遊離細胞、n=3)、その骨形成能はしばしば2倍高かった(それぞれ、90μg Ca++/5,000遊離細胞に比べて170μg Ca++/5,000遊離細胞)(図4C)。本発明者らはまた、2回目のコラゲナーゼ消化工程が、PBS中で50U/mlの最終濃度に希釈したヒアルロニダーゼ(Sigma)の0.5ml溶液での1時間の処理に置き換え得ることを明らかにすることができた。コラゲナーゼ消化と同様に、ヒアルロニダーゼでの処理は、細胞振とう機にて37℃で実施する。この処理も、遊離される総細胞の追加の5%に寄与する骨ライニング細胞を遊離させた(n=3)。コラゲナーゼまたはヒアルロニダーゼを用いて得られた、2回目の消化物中のCD45lowD7−FIB+LNGFR+細胞のMSCマーカー表現型は、1回目の消化物のものと同様であった(CD73+++CD105+CD90+++CD146++、n=2)。この二重消化手順後、インサイチューで残存する唯一の残留細胞は骨の内部に位置した(骨細胞)(図4D)。
骨修復適用のためには、卓越した骨形成能力を有するMSCの使用が望ましい。MSC活性が骨ライニング細胞に存在し得ることが認識されたので、本発明者らは、1.1で述べた3〜4時間のコラゲナーゼ消化工程に加えて、付加的な酵素による抽出の方法が、高い骨形成能力を有するMSCを遊離させるのに適することを示すことができた。図4AおよびBに認められるように、本発明者らは、1.1で述べた方法を用いるコラゲナーゼ消化工程が、大部分の骨ライニング細胞を除去するが、全部ではない(平均で全DNAの約2%が骨に残る、n=3)ことを明らかにすることができた。2回目の1時間のコラゲナーゼ消化工程を1回目の消化物の収集後の生検断片で実施したとき、骨に残された細胞の割合は5倍近く低下し、回収された細胞の総収量が平均5%上昇した(n=3)。2回目の消化物のクローン原性は1回目の消化物と同様であったが(それぞれ、12CFU−F/5,000遊離細胞に比べて13CFU−F/5,000遊離細胞、n=3)、その骨形成能はしばしば2倍高かった(それぞれ、90μg Ca++/5,000遊離細胞に比べて170μg Ca++/5,000遊離細胞)(図4C)。本発明者らはまた、2回目のコラゲナーゼ消化工程が、PBS中で50U/mlの最終濃度に希釈したヒアルロニダーゼ(Sigma)の0.5ml溶液での1時間の処理に置き換え得ることを明らかにすることができた。コラゲナーゼ消化と同様に、ヒアルロニダーゼでの処理は、細胞振とう機にて37℃で実施する。この処理も、遊離される総細胞の追加の5%に寄与する骨ライニング細胞を遊離させた(n=3)。コラゲナーゼまたはヒアルロニダーゼを用いて得られた、2回目の消化物中のCD45lowD7−FIB+LNGFR+細胞のMSCマーカー表現型は、1回目の消化物のものと同様であった(CD73+++CD105+CD90+++CD146++、n=2)。この二重消化手順後、インサイチューで残存する唯一の残留細胞は骨の内部に位置した(骨細胞)(図4D)。
それ故、骨修復適用のために骨試料を処理する好ましい方法は、2回目のコラゲナーゼ処理または代替的に、上述したようなヒアルロニダーゼ処理を実施することである。
1.2.3 浮遊脂肪凝集物からのインビボMSCの酵素による遊離
正常BMは浮遊脂肪フラクション(FFF)と称される浮揚性の脂肪滴を含み、これは、MSC富化の準備としてBM MNCの調製の間に密度勾配遠心分離によって廃棄される。FFFは、高齢者(骨髄が徐々に脂肪性になるので)または一部の疾患(慢性関節リウマチまたは骨粗しょう症など)を有する人々において増加する。
正常BMは浮遊脂肪フラクション(FFF)と称される浮揚性の脂肪滴を含み、これは、MSC富化の準備としてBM MNCの調製の間に密度勾配遠心分離によって廃棄される。FFFは、高齢者(骨髄が徐々に脂肪性になるので)または一部の疾患(慢性関節リウマチまたは骨粗しょう症など)を有する人々において増加する。
本発明者らは、意外にも、本発明の方法がMSC収率を高めるために吸引液に適用できることを見出した。これはFFFの収集を必要とする。次にそれを、成熟脂肪細胞から間質細胞/ARC/MSCを分離するために本発明に従ってコラゲナーゼ処理する。
本発明者らは、従来の先行技術の手法を用いて正常BMから収集した吸引液中の浮遊脂肪フラクション(FFF)を分析した。同じドナーを使用した試験では、分散FFF中のCD45lowD7−FIB+LNGFR+表現型を有する細胞の割合は0.3±0.1%であり、それ故、対応するMNCフラクション中に存在する割合(0.03±0.006、n=5)よりも約10倍高かった。そこで本発明者らは、驚くべきことに、先行技術の手法によれば通常は廃棄されるFFFがMSCの貴重な供給源を表すことを見出した。
さらに、本発明者らは、FFF細胞をコラゲナーゼで消化したとき、生成されるCD45lowD7−FIB+LNGFR+細胞の割合がさらに上昇し、総生細胞の7±5%に達することを認めた(n=5)(図5、上のパネル)。この収率は、先行技術の手法に従ってMSCのソースとして使用されるMNCフラクションにおける収率より約200倍高かった。FFFから遊離されるCD45lowD7−FIB+LNGFR+細胞は、それらのMNC対応物と比較して同様の広範な表現型を有し、増幅後も多能性であった(上述したものと同じ細胞系譜を検討した螢光励起細胞選別機(FACS)による結果および形態学的試験を提示する図5の下のパネルに示すように)。FFFから富化したCD45lowD7−FIB+LNGFR+細胞はALP陽性であり、それらの細胞質内に脂肪小滴を有した。これは、細胞がインビボで「前脂肪細胞」状態を有することを指示する。それらのインビボでのアルカリホスファターゼの発現は、それらの「前骨芽細胞」状態を示唆する。合わせて考慮すると、これは、個々の単一細胞に固有の多能性を示唆する。
全体として見ると、これらのデータは、BM中に存在するMSCの大部分が単一細胞の形態(先行技術によって示唆されるように吸引液を使用して収集されることが予想され得るタイプの)では見出されないことを示した。その代わりに、驚くべきことに、BM MSCの大部分が間質細胞ネットワークに組み込まれ、浮遊脂肪細胞を含む隣接細胞および膠原性基質と共に凝集物を形成することが認められた。
本発明の最初の態様の方法(間質細胞のネットワークおよびマトリックスからMSCを遊離させるためにコラゲナーゼ消化を利用する)は、先行技術の手法を用いて達成され得るよりもはるかに多くの出発集団からMSCを分離し、富化するために使用し得ることがこの驚くべき所見に照らして認識される。それ故、本発明の最初の態様の方法は、MSCの高い富化が達成され得る新しい独創的な方法を提供する。
滑膜からの間充織幹細胞の富化
2.1 実験材料および方法
2.1.1 試料の収集
8つの滑膜組織ソース、即ち、1名の正常ドナー、RAを有する4名の患者、OAを有する1名の患者、痛風を有する1名の患者および血清反応陰性関節炎を有する1名の患者から得た試料を調べた。
2.1 実験材料および方法
2.1.1 試料の収集
8つの滑膜組織ソース、即ち、1名の正常ドナー、RAを有する4名の患者、OAを有する1名の患者、痛風を有する1名の患者および血清反応陰性関節炎を有する1名の患者から得た試料を調べた。
診断関節鏡検査中に、滑膜生検を採取した。小さな組織生検(平均44mg)を培地(通常はDMEM/2%FCS)2mlと共に、15ml遠心管に入れて、実験室に運んだ。
2.1.2 コラゲナーゼ消化
実験室に到着した後、培地を取り除き、生検を0.25%コラゲナーゼ溶液に入れて、一定な回転下で3または4時間消化した。試料が完全に消化されたとき、コラゲナーゼ溶液は混濁し、細胞生検は崩壊して、完全に消失する。インキュベーション後、PBS 10mlを添加し、注射器/針を使用して残存する可能性のある組織塊を破壊した。直後に、PBS/細胞混合物を70ミクロンの細胞ストレーナーで篩過し、遠心分離(1800rpmで5分間)のためにもう1つの遠心管に移した。次にコラゲナーゼ/PBS溶液を廃棄し、細胞ペレットを、細胞計数およびその後の操作(磁気および螢光励起細胞選別機(FACS)による分離)に適した培地、通常は2%FCSを含むDMEMに再懸濁した。
実験室に到着した後、培地を取り除き、生検を0.25%コラゲナーゼ溶液に入れて、一定な回転下で3または4時間消化した。試料が完全に消化されたとき、コラゲナーゼ溶液は混濁し、細胞生検は崩壊して、完全に消失する。インキュベーション後、PBS 10mlを添加し、注射器/針を使用して残存する可能性のある組織塊を破壊した。直後に、PBS/細胞混合物を70ミクロンの細胞ストレーナーで篩過し、遠心分離(1800rpmで5分間)のためにもう1つの遠心管に移した。次にコラゲナーゼ/PBS溶液を廃棄し、細胞ペレットを、細胞計数およびその後の操作(磁気および螢光励起細胞選別機(FACS)による分離)に適した培地、通常は2%FCSを含むDMEMに再懸濁した。
2.1.3 細胞選別戦略
上述したコラゲナーゼ消化手法を用いて滑膜試料から遊離された細胞を、図9に概略的に示すプロトコールを用いてCD45lowD7−FIB+LNGFR+細胞に関して富化した。簡単に述べると、高ヨウ化プロピジウム(PI)染色に基づいて死細胞を廃棄し、残存する生細胞を、低いCD45発現を有するがLNGFRの高発現を有するものを選択するために連続的に選別した。
上述したコラゲナーゼ消化手法を用いて滑膜試料から遊離された細胞を、図9に概略的に示すプロトコールを用いてCD45lowD7−FIB+LNGFR+細胞に関して富化した。簡単に述べると、高ヨウ化プロピジウム(PI)染色に基づいて死細胞を廃棄し、残存する生細胞を、低いCD45発現を有するがLNGFRの高発現を有するものを選択するために連続的に選別した。
この戦略によって得られた選別細胞の線維芽細胞形態が図9の最後の画像に示されている。これらの選別されたCD45lowD7−FIB+LNGFR+細胞は、その後、それらの高い増殖性と一致して、培養下で増殖する細胞単層を生成することができた。
2.2 結果
2.2.1 免疫化学およびフローサイトメトリー分析
間充織幹細胞は多くの他の組織で報告されているが、それらのインビボでのトポグラフィーおよび表現型はこれまで不明であった。本発明者らは、滑膜および関節脂肪体を含む固体組織中でのCD45lowD7−FIB+LNGFR+細胞のトポグラフィーを検討した。滑膜では、D7−FIB抗体は全ての線維芽細胞を染色したのに対し、LNGFRは血管周囲領域内の線維芽細胞だけを染色した(図6)。
2.2.1 免疫化学およびフローサイトメトリー分析
間充織幹細胞は多くの他の組織で報告されているが、それらのインビボでのトポグラフィーおよび表現型はこれまで不明であった。本発明者らは、滑膜および関節脂肪体を含む固体組織中でのCD45lowD7−FIB+LNGFR+細胞のトポグラフィーを検討した。滑膜では、D7−FIB抗体は全ての線維芽細胞を染色したのに対し、LNGFRは血管周囲領域内の線維芽細胞だけを染色した(図6)。
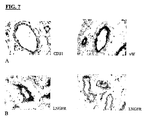
CD45lowD7−FIB+LNGFR+細胞の血管周皮細胞様の分布を示す結果が図7に示されている。CD45lowD7−FIB+LNGFR+細胞は、血管の内腔に1細胞の深さの層を形成した内皮細胞(CD31+およびフォン・ビルブラント因子+であることが知られる)(図7Aに示す免疫標識)とは異なった。
これに対し、固体組織中のMSCが血管周皮細胞であるという認識と一致して、CD45lowD7−FIB+LNGFR+細胞は組織内に広がる陽性細胞のいくつかの層として血管支持体を形成した(図7B)。
2.2.2 滑膜からのMSCの酵素による遊離
上記2.1で概説した方法を用いて滑膜からMSCを遊離させた。
上記2.1で概説した方法を用いて滑膜からMSCを遊離させた。
本発明の最初の態様の方法に従った滑膜の酵素消化は、図8に示すように、大きな割合のCD45lowD7−FIB+LNGFR+細胞を生じた。CD45lowD7−FIB+LNGFR+細胞のこの富化は、細胞が分離された試料の健康状態には無関係であることが見出され(例えばパネル(iii)では痛風からの組織試料)、病気にかかっている患者からであっても、本発明の最初の態様の方法が自己MSCの治療的分離のために適切であることをさらに例証する。
CD45lowD7−FIB+LNGFR+細胞を様々な滑膜試料から富化した(1つは正常ドナーから、4つはRAを有する患者から、1つはOAを有する患者から、1つは痛風を有する患者からおよび1つはセロネガティブ関節炎を有する1名の患者から)。疾患の性質とは無関係に、CD45lowLNGFR+細胞は、全ての滑膜消化物において15±9%の平均比率で、および他のデータセットでは16±10%の比率で存在した。
全ての線維芽細胞がD7−FIBに関して陽性標識することを示す免疫組織化学データと一致して、CD45lowD7−FIB+細胞は滑膜消化物中に高い割合で存在した(76±20%の平均比率、およびもう1つのデータセットでは50±12%)。
滑膜組織のコラゲナーゼ消化物でのLNGFRおよびD7−FIBの発現を明らかにする代表的実験を図8、パネル(ii)および(iii)に示す。特にパネル(iii)は、免疫組織化学データと一致して、CD45lowLNGFR+細胞(滑膜血管周皮細胞)がCD45lowD7−FIB+細胞(滑膜線維芽細胞)のフラクションを構成することを示す。表現型の共通性は、それらの共通する間葉系統の性質および両方の表現型を有する細胞におけるMSCの存在の可能性を示唆する。
2.2.3 選別したCD45lowD7−FIB+LNGFR+細胞がMSCを含むことの機能的証明
細胞単層(第4継代)を、本発明の最初の態様の方法に従って富化した滑膜組織(すなわち滑膜血管周囲細胞)からの選別CD45lowD7−FIB+細胞から生成した。これらの細胞単層を、以下で述べるような骨芽細胞、脂肪細胞および軟骨細胞の分化(n=1)の機能的インビトロアッセイに供した。
細胞単層(第4継代)を、本発明の最初の態様の方法に従って富化した滑膜組織(すなわち滑膜血管周囲細胞)からの選別CD45lowD7−FIB+細胞から生成した。これらの細胞単層を、以下で述べるような骨芽細胞、脂肪細胞および軟骨細胞の分化(n=1)の機能的インビトロアッセイに供した。
i)骨芽細胞の分化を、100nMデキサメタゾン、0.05mM L−アスコルビン酸−2−ホスフェートおよび10mM β−グリセロホスフェート(全てSigmaより)によって誘導した。アルカリホスファターゼ(AP)活性およびマトリックス鉱化作用を、それぞれSigmaキット82および1%アリザリンレッド(Sigma)を使用して検出した。Ca++沈着はSigmaキット85を用いて測定した。
ii)脂肪細胞の分化を、0.5mMイソブチルメチルキサンチン(Sigma)、60μMインドメタシン(ICN,Basingstoke,UK)および0.5mMヒドロコルチゾン(Sigma)を添加したDMEM/10%FCS中で誘導した。脂質小胞の蓄積を、以前に述べられているように0.5%オイルレッドで視覚化した。
iii)軟骨細胞の分化のために、2.5×105細胞を、高グルコースDMEM(Gibco)、100μg/mlピルビン酸ナトリウム、40μg/mlプロリン、50μg/ml L−アスコルビン酸−2−ホスフェート、1mg/ml BSA、I×ITS+、100nMデキサメタゾン(全てSigmaより)および10ng/ml TGF−β3(R&D Systems)からなる無血清培地に入れた。培地を1日おきに交換した。3週間目にペレットを採集し、凍結切片(5μmの薄さ)を調製した。硫酸化GAGを1%トルイジンブルー(Sigma)で視覚化した。アルシアンブルー結合アッセイ(IDS)を用いてsGAGを測定した。
3週間の分化後、本発明に従って滑膜組織から遊離させたCD45lowD7−FIB+LNGFR+細胞に由来する培養物は、脂肪細胞、骨芽細胞および軟骨細胞表現型へと成功裏に分化した。この試験の結果を図9に示し、培養細胞によって実現された表現型を示す顕微鏡写真を提示している。
選別した滑膜CD45lowD7−FIB+LNGFR+細胞に由来する細胞の多能性を、標準プラスチック付着法によって培養物を生成した、BM(n=5)または滑膜(n=5)由来の培養物と比較した。生じた脂肪細胞の割合は同様であり(それぞれ30%対33±15%および22±15%)、生産されたカルシウムの量(骨芽細胞形成を指示する)は同じ範囲内であった(それぞれ100μg/皿対80±37μgおよび121±47μg/皿)。軟骨細胞形成は、特に、非常に強力であり、生産されたプロテオグリカン(GAG)の量は対照培養物を上回った(それぞれ9μg/ペレット対2.6±1.9μgおよび2.2±1.4μg/ペレット)。
データセットを、滑膜に関してn=15で比較できるように拡大した。同様の結果が得られ、この場合、生産されたプロテオグリカン(GAG)の量は対照培養物を上回った(それぞれ9μg/ペレット対2.6±1.9μgおよび1.8±1.7μg/ペレット)。
全体として、CD45lowD7−FIB+LNGFR+フラクションは全消化物の軟骨細胞形成活性の3分の2超を含み、その1/3だけが残留フラクション中に残った。これらのデータは、滑膜CD45lowD7−FIB+LNGFR+細胞(滑膜血管周皮細胞)が、対照培養物に匹敵するMSC活性を含み、軟骨細胞形成活性に関して特異的に富化されたことを示した。
2.2.4 本発明に従って富化した滑膜CD45lowD7−FIB+LNGFR+集団内のMSCの存在の単細胞レベルでの確認
本発明者らは、本発明に従って滑膜組織から遊離させた個々の細胞のクローン形成能を検討した(n=3ドナー、全てRAを有する)。
本発明者らは、本発明に従って滑膜組織から遊離させた個々の細胞のクローン形成能を検討した(n=3ドナー、全てRAを有する)。
CD45lowD7−FIB+細胞(滑膜線維芽細胞)を、図9に概略的に示すプロトコールを用いて螢光励起細胞選別機(FACS)による選別によって精製した。平均して、このプロトコールによって選別された接着細胞の10%が12〜13細胞分裂を受けることができたが、これらの25%(または全接着CD45lowD7−FIB+細胞の2.5%)だけが高度に増殖性であった(20〜22細胞分裂を受けることができる)。
加えて、1つの滑膜組織(RA)のコラゲナーゼ消化によって遊離される細胞を、CD45lowD7−FIB+LNGFR+集団(滑膜血管周皮細胞)を選択するために選別した。この実験では、全接着CD45lowD7−FIB+LNGFR+細胞の4%が高度増殖性であり、クローン原性であった(20〜22細胞分裂を受けることができる)。3つの単一MSC由来クローン全てが三分化能性であった(図10)。
これらの実験は、本発明に従ったコラゲナーゼ消化によって滑膜組織から遊離された滑膜線維芽細胞と滑膜血管周皮細胞の両方の集団内に、高度にクローン原性で多能性のMSCが存在したこと、およびそれらが血管周皮細胞フラクション(CD45lowD7−FIB+LNGFR+細胞)において数的に富化されたことを示した。さらに、これらの結果は、富化された滑膜血管周囲CD45lowD7−FIB+LNGFR+細胞が軟骨前駆細胞の特に良好なソースであることを示す。
1つの小さな44mg生検から入手し得る滑膜血管周皮細胞の細胞収量は、平均して400,000細胞であった(n=8)。この量は、小さな限局性軟骨欠損(標準自家軟骨細胞移植(ACI)手順のために現在使用される細胞密度は106細胞/cm2である)の治療のために十分である。滑膜線維芽細胞または全滑膜組織消化物を使用する場合は、1つの小さな生検を使用してはるかに大きな軟骨欠損が治療できる(10cm2まで)。滑膜組織は再生のための高い能力を有し、滑膜のいくつかの生検またはより大きな部分の収集は、OAおよびRAで見られるような非常に大きな軟骨欠損の治療を可能にする。滑膜血管周囲細胞の高い増殖活性およびクローン形成活性は、従来のACI標準と比較して、はるかに小さな細胞播種密度(例えば初期細胞数)を使用し得ることを示唆する。
MSCは膝蓋下脂肪体中に存在する
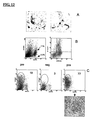
関節脂肪体中のMSC(LNGFR+免疫標識によって指示される)は、図11および12Aに例示するように、滑膜中のそのような細胞のトポグラフィーに類似した血管周囲トポグラフィーを有した。
関節脂肪体中のMSC(LNGFR+免疫標識によって指示される)は、図11および12Aに例示するように、滑膜中のそのような細胞のトポグラフィーに類似した血管周囲トポグラフィーを有した。
膝蓋下脂肪体(予備実験ではn=4であり、n=6に拡大した、全ての患者がOAを有した)を本発明に従ってコラゲナーゼ消化に供した。フローサイトメトリーデータは、脂肪体血管周皮細胞(CD45lowLNGFR+細胞)が脂肪体線維芽細胞(CD45lowD7−FIB+細胞)のフラクションに寄与することを確認した(図12B)。フローサイトメトリーは、CD45lowLNGFR+細胞の平均比率が予備実験(n=4)では20±12%であり、n=6のときにはさらに良好である(37±9)ことを指示した。
そのような消化物中のCD45lowD7−FIB+細胞(線維芽細胞)の割合もフローサイトメトリーによって検討し、その結果は、(滑膜試験からのデータと一致して)これらの細胞が消化物のより大きな割合を構成する(60±12%(n=4)および51±17%(n=6))ことを指示した。本発明者らが分析した滑膜消化物と比較して、脂肪体における線維芽細胞の割合は同様である(それぞれ50%対51%)が、血管周皮細胞(CD45lowLNGFR+細胞)の割合は2倍高かった(それぞれ37%対16%)。これは、細胞収率に関して、脂肪体がMSCの選択のために特に有用な組織ソースであり得ることを示唆した。
脂肪体消化物からCD45lowD7−FIB+LNGFR+細胞(血管周皮細胞)を精製するため、本発明者らは、MACSelect Anti−LNGFRマイクロビーズ(図12C)によるマイクロビーズベースの技術を使用した。MACSelect Anti−LNGFRマイクロビーズはMiltenyi Biotecより入手可能である。選択プロトコールは、D7−FIBマイクロビーズに関して述べたものと全く同じである(上記参照)。
この磁気ソーティング手順後の細胞純度(n=4)は、直接螢光励起細胞選別機(FACS)による選別によって得られるものより低かった(約60〜70%純度対95%)(図20C)。しかし、本発明者らは、これは実際の純度そのものではなく純度を評価する方法の限界によるものであると考える。これらの限界にもかかわらず、コラゲナーゼ消化物からの脂肪体由来のCD45lowLNGFR+血管周皮細胞のクローン原性は、滑膜由来のCD45lowLNGFR+細胞のものと同様であった(総接着CD45lowLNGFR+細胞の4%)。選別した脂肪体血管周皮細胞由来のコロニーを図12Cに示す。
選別した脂肪体由来のCD45lowLNGFR+血管周皮細胞は、培養増幅前であってもある程度の多能性を有した。遊離/選別細胞の数が分化アッセイにおけるインビトロ試験のために十分であったので、これを評価することができた。
これらのアッセイの結果を表3に示すが、表3は、
i)コラゲナーゼ消化物によって生産されたCD45lowLNGFR+細胞、および
ii)コラゲナーゼ消化物によって生産されたCD45lowLNGFR−細胞、
iii)培養下での増幅(標準方法)後の対照脂肪体由来のプラスチック接着細胞
の性質を比較する。
i)コラゲナーゼ消化物によって生産されたCD45lowLNGFR+細胞、および
ii)コラゲナーゼ消化物によって生産されたCD45lowLNGFR−細胞、
iii)培養下での増幅(標準方法)後の対照脂肪体由来のプラスチック接着細胞
の性質を比較する。
上記(iii)からの細胞は、標準増幅プロトコールを用いて入手した。簡単に述べると、脂肪体を標準プロトコールに従って消化した。5×105〜106細胞を小さな25cm2フラスコに接種し、集密に達するまで培養した。集密細胞をトリプシン処理し、さらに2つのフラスコに分けて集密まで培養した。増幅した細胞(第1継代)を、上述したように多能性を試験するために使用した。
表3に見られるように、脂肪体由来のCD45lowLNGFR+細胞はCD45lowLNGFR−細胞よりも軟骨形成性であった。平均して、対照培養脂肪体由来MSCは新鮮CD45lowLNGFR+細胞よりも高い軟骨細胞を生産した(それぞれ9±7対2.4±4.4、n=6およびn=4)。治療的に投与した、本発明に従って富化したMSCから患者において誘導される分化細胞が、本明細書で同定される高いおよび有益な軟骨形成特性を提供することは当業者に認識される。
1つの小さな30mg生検から入手できる脂肪体血管周皮細胞の細胞収量は平均して700,000細胞であった(n=2)。この量は、小さな限局性軟骨欠損(標準自家軟骨細胞移植(ACI)手順のために現在使用される細胞密度は106細胞/cm2である)の治療のために十分である。組織1gから入手し得る脂肪体血管周皮細胞の細胞収量は、平均で23×106細胞であった(n=2)。全脂肪体から入手し得る脂肪体血管周皮細胞の細胞収量は、平均で500×106細胞であった(n=2)。これは、OAおよびRAで見られるような非常に大きな軟骨欠損の治療を可能にする。これは、同種環境での脂肪体の使用を可能にし、数多くの治療のために軟骨形成性フラクションを提供する。
全体でこれらの結果は、関節脂肪体に存在するCD45lowLNGFR+細胞が、
i)血管周囲細胞、
ii)クローン原性、および
iii)多能性
であることを明らかにした。
i)血管周囲細胞、
ii)クローン原性、および
iii)多能性
であることを明らかにした。
これらの性質はすべて、間充織幹細胞を含むというこれらの細胞の同定と一致する。
本発明の富化方法を使用して、これらの細胞を、インビトロ培養増幅への再選別を行わずに直接それらの多能性を試験するのに十分な数(106細胞超)で精製することが可能であった。この方法による富化のための細胞のソースである膝蓋下脂肪体の使用は、この組織の大きなサイズおよび脂肪体中に存在するCD45lowLNGFR+細胞の比較的高い割合の故に、特に好ましい。これの性質は、膝蓋下脂肪体を、本発明の最初の態様の方法を利用して未操作MSCを得るための卓越したソースにする。そのような富化細胞は組織工学適用に特に適している。
要約すると、これらのデータは、
(1)初めて、新鮮選別された細胞集団を、多能性に関して増幅細胞と比較し、MSC活性を有することが示された、
(2)CD45lowLNGFR+細胞は、CD45lowLNGFR−細胞よりも軟骨形成性および骨形成性であった(従ってCD45lowLNGFR+は、本発明の最初の態様の工程(b)における選択のための好ましい表現型であった)、および
(3)新鮮細胞の脂肪生成活性は増幅細胞と同様であり、それ故、身体の一部から簡単に脂肪を収集し、消化して、他の部分に細胞を注入/移植することができる。培養下で細胞を増幅することは、それらの脂肪生成能を改善するために必要ではない。
(1)初めて、新鮮選別された細胞集団を、多能性に関して増幅細胞と比較し、MSC活性を有することが示された、
(2)CD45lowLNGFR+細胞は、CD45lowLNGFR−細胞よりも軟骨形成性および骨形成性であった(従ってCD45lowLNGFR+は、本発明の最初の態様の工程(b)における選択のための好ましい表現型であった)、および
(3)新鮮細胞の脂肪生成活性は増幅細胞と同様であり、それ故、身体の一部から簡単に脂肪を収集し、消化して、他の部分に細胞を注入/移植することができる。培養下で細胞を増幅することは、それらの脂肪生成能を改善するために必要ではない。
Claims (30)
- (a)細胞と細胞外マトリックスとを含む組織試料を、液体培地中で細胞外マトリックスから間充織幹細胞(MSC)を遊離させるのに十分な量のコラゲナーゼで処理する工程、および
(b)間充織幹細胞(MSC)を含む培地のフラクションを分離する工程
を含む、間充織幹細胞(MSC)を分離し、富化する方法。 - 前記組織試料が骨髄から得られる、請求項1に記載の方法。
- 前記試料が、胎盤、胸骨または大腿骨からのパンチ生検である、請求項2に記載の方法。
- 前記組織試料が浮遊脂肪フラクション(FFF)を含む、請求項1から3のいずれか1つに記載の方法。
- 前記組織試料が、骨髄穿刺液、滑膜および脂肪体を含む群より選択された組織から得られる、請求項1に記載の方法。
- 前記試料を、0.25%コラゲナーゼを含む緩衝液中に入れる、請求項1から5のいずれか1つに記載の方法。
- 前記試料をコラゲナーゼで3〜4時間の間処理する、請求項1から6のいずれか1つに記載の方法。
- MSCを含む前記フラクションが、単一細胞を含むフラクションを分離するために、固体を除去し、そして、液体培地を遠心分離することによって得られる、請求項1から7のいずれか1つに記載の方法。
- 工程(a)が2回の別々のコラゲナーゼ消化を含む、請求項1から8のいずれか1つに記載の方法。
- 工程(a)がヒアルロニダーゼ消化をさらに含む、請求項1から9のいずれか1つに記載の方法。
- 前記組織試料が骨であり、前記間充織幹細胞(MSC)が骨修復用である、請求項9または10に記載の方法。
- 工程(b)が、さらなる富化工程をさらに含む、請求項1から11のいずれか1つに記載の方法。
- 前記さらなる富化工程が磁気ビーズを使用する、請求項12に記載の方法。
- 前記さらなる富化工程が、螢光励起細胞選別機(FACS)による選別を含む、請求項12に記載の方法。
- 前記さらなる富化工程が、表1で特定されたマーカーのうちの1つによって特徴づけられる表現型を有する間充織幹細胞(MSC)を分離することに基づく、請求項12から14のいずれか1つに記載の方法。
- 前記表現型が、CD45lowLNGFR+、CD45lowD7−FIB+LNGFR+またはCD45lowD7−FIB+である、請求項15に記載の方法。
- 請求項1〜16のいずれか1つによって特定された方法に従って富化された分離間充織幹細胞(MSC)。
- 薬剤としての使用のための、請求項17に記載の分離間充織幹細胞(MSC)。
- 細胞療法における使用のための、請求項18に記載の薬剤。
- 前記間充織幹細胞(MSC)が、遺伝子治療における使用のために遺伝的に操作されている、請求項18または19に記載の薬剤。
- コラゲナーゼを含む間充織幹細胞(MSC)を富化するためのキット。
- (a)間充織幹細胞(MSC)と細胞外マトリックスとを含む組織試料を被験者から得る工程、
(b)前記組織試料を、液体培地中で細胞外マトリックスから間充織幹細胞(MSC)を遊離させるのに十分な量のコラゲナーゼで処理する工程、
(c)間充織幹細胞(MSC)を含む培地のフラクションを分離する工程、および
(d)細胞療法から利益を得ることを可能にする身体部位で前記フラクションを前記被験者に再導入する工程
を含む、治療を必要とする被験者に細胞療法を実施する方法。 - (a)間充織幹細胞(MSC)と細胞外マトリックスとを含む組織試料を死体またはドナーから得る工程、
(b)前記組織試料を、液体培地中で細胞外マトリックスから間充織幹細胞(MSC)を遊離させるのに十分な量のコラゲナーゼで処理する工程、
(c)間充織幹細胞(MSC)を含む培地のフラクションを分離する工程、および
(d)細胞療法から利益を得ることを可能にする身体部位で前記フラクションを前記被験者に導入する工程
を含む、治療を必要とする被験者に細胞療法を実施する方法。 - 前記間充織幹細胞(MSC)を遺伝的に操作するさらなる工程を含む、請求項22または23に記載の方法。
- 前記細胞療法が、骨修復、軟骨修復、骨格筋修復、腱修復、靭帯修復、半月修復、心筋修復、脊髄損傷、パーキンソン病および他の神経変性疾患、免疫媒介性組織拒絶反応、対宿主性移植片病、慢性関節リウマチ、脂肪物質の再生、血管修復または虚血性血管病変または骨粗しょう症を含む群より選択される状態を臨床的に管理することを目的とする、請求項22〜24のいずれか1つに記載の方法。
- 骨を修復するための、請求項22から24のいずれか1つに記載の方法。
- 軟骨を修復するための、請求項22から24のいずれか1つに記載の方法。
- 変形性関節症を治療するための、請求項22から24のいずれか1つに記載の方法。
- 骨粗しょう症を治療するための、請求項22から24のいずれか1つに記載の方法。
- 請求項25〜29のいずれか1つによって特定された状態の治療のための、請求項19によって定義される薬剤の使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0600972.4A GB0600972D0 (en) | 2006-01-18 | 2006-01-18 | Enrichment of cells |
| PCT/GB2007/000107 WO2007083093A1 (en) | 2006-01-18 | 2007-01-17 | Enrichment of cells |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009523438A true JP2009523438A (ja) | 2009-06-25 |
| JP2009523438A5 JP2009523438A5 (ja) | 2010-03-04 |
Family
ID=36010490
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008550832A Pending JP2009523438A (ja) | 2006-01-18 | 2007-01-17 | 細胞の富化 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20100260721A1 (ja) |
| EP (1) | EP1979471A1 (ja) |
| JP (1) | JP2009523438A (ja) |
| CN (1) | CN101400786A (ja) |
| AU (1) | AU2007206750A1 (ja) |
| GB (1) | GB0600972D0 (ja) |
| WO (1) | WO2007083093A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016074648A (ja) * | 2014-10-06 | 2016-05-12 | 佛教慈濟醫療財團法人 | 関節疾患を治療するための組成物及び方法 |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20140107677A (ko) | 2007-09-19 | 2014-09-04 | 플루리스템 리미티드 | 지방 또는 태반 조직 유래의 부착 세포 및 이의 치료 용도 |
| JP5645197B2 (ja) * | 2009-06-23 | 2014-12-24 | 学校法人日本大学 | 幹細胞の未分化状態を維持する新規方法 |
| CA2777718A1 (en) | 2009-10-16 | 2011-04-21 | University Of Medicine And Dentistry Of New Jersey | Closed system separation of adherent bone marrow stem cells for regenerative medicine applications |
| SG181878A1 (en) * | 2009-12-22 | 2012-07-30 | Agency Science Tech & Res | Treatment of bone fracture |
| JP2014529406A (ja) * | 2011-08-29 | 2014-11-13 | セーフガードセル テクノロジー インク. | 血管周囲薬用細胞の単離および治療的使用 |
| CN103857401B (zh) * | 2011-09-09 | 2018-06-05 | 麦瑟布莱斯特公司 | 增加成骨细胞功能的方法 |
| CN103266081B (zh) * | 2012-01-21 | 2015-05-13 | 中国人民解放军军事医学科学院附属医院 | 从脐带中分离培养间充质干细胞的高效方法 |
| EP3030279B1 (en) | 2013-08-06 | 2020-11-04 | Regenexx, LLC | Bone marrow adipose portion isolation device and methods |
| EP2998392A1 (en) * | 2014-09-16 | 2016-03-23 | The Provost, Fellows, Foundation Scholars, & the other members of Board, of the College of the Holy & Undiv. Trinity of Queen Elizabeth near Dublin | A population of cells for use in single-stage cell-based cartilage regeneration |
| US20160193254A1 (en) * | 2015-01-05 | 2016-07-07 | Gary M. Petrucci | Methods and materials for treating arthritis |
| US10342830B2 (en) | 2015-01-05 | 2019-07-09 | Gary M. Petrucci | Methods and materials for treating lung disorders |
| US10993969B2 (en) | 2016-02-05 | 2021-05-04 | Gary M. Petrucci | Methods and materials for treating nerve injuries and neurological disorders |
| TWI689589B (zh) * | 2016-08-31 | 2020-04-01 | 宣捷細胞生物製藥股份有限公司 | 區別間質幹細胞的方法及測定間質幹細胞的純度的方法 |
| JPWO2018207918A1 (ja) * | 2017-05-12 | 2020-03-26 | 国立大学法人 東京医科歯科大学 | 移植効率を向上させる間葉系幹細胞の純化方法 |
| US10478531B2 (en) | 2017-06-22 | 2019-11-19 | Gary M. Petrucci | Methods and materials for treating blood vessels |
| US10251917B1 (en) | 2017-09-19 | 2019-04-09 | Gary M. Petrucci | Methods and materials for treating tumors |
| US11285177B2 (en) | 2018-01-03 | 2022-03-29 | Globus Medical, Inc. | Allografts containing viable cells and methods thereof |
| US20220098553A1 (en) * | 2019-02-08 | 2022-03-31 | Regrow Biosciences Private Limited | Method for mesenchymal stem cell isolation and osteoblast differentiation |
| US11697799B2 (en) | 2019-04-15 | 2023-07-11 | Ossium Health, Inc. | System and method for extraction and cryopreservation of bone marrow |
| EP4181675A4 (en) | 2020-07-18 | 2024-04-24 | Ossium Health Inc | PERMEATION OF WHOLE VERTEBRAL BODY WITH CRYOPROTECTIVE USING VACUUM-ASSISTED DIFFUSION |
| EP4228406A1 (en) | 2020-10-14 | 2023-08-23 | Ossium Health, Inc. | Systems and methods for extraction and cryopreservation of bone marrow |
| CN117279650A (zh) | 2020-12-18 | 2023-12-22 | 奥瑟姆健康公司 | 细胞治疗方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002504503A (ja) * | 1998-02-24 | 2002-02-12 | エムシーピー・ハーネマン・ユニバーシテイ | 中枢神経系の疾病の処置における使用のための単離されたストロマ細胞 |
| US20030103947A1 (en) * | 2001-02-23 | 2003-06-05 | Urlich Noth | In vitro engineered cartilage constructs produced by coating biodegradable polymer with human mesenchymal stem cells |
| US20040033217A1 (en) * | 2002-05-31 | 2004-02-19 | Padmavathy Vanguri | Intraperitoneal delivery of genetically engineered mesenchymal stem cells |
| WO2005001078A2 (en) * | 2003-06-27 | 2005-01-06 | Ethicon, Incorporated | Regeneration and repair of neural tissue using postpartum-derived cells |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5226914A (en) * | 1990-11-16 | 1993-07-13 | Caplan Arnold I | Method for treating connective tissue disorders |
| US5486359A (en) * | 1990-11-16 | 1996-01-23 | Osiris Therapeutics, Inc. | Human mesenchymal stem cells |
| US5811094A (en) * | 1990-11-16 | 1998-09-22 | Osiris Therapeutics, Inc. | Connective tissue regeneration using human mesenchymal stem cell preparations |
| US6482231B1 (en) * | 1995-11-20 | 2002-11-19 | Giovanni Abatangelo | Biological material for the repair of connective tissue defects comprising mesenchymal stem cells and hyaluronic acid derivative |
| ES2329953T3 (es) * | 1996-04-19 | 2009-12-02 | Osiris Therapeutics, Inc. | Regeneracion e incremento de hueso utilizando celulas madre mesenquimales. |
| US6835377B2 (en) * | 1998-05-13 | 2004-12-28 | Osiris Therapeutics, Inc. | Osteoarthritis cartilage regeneration |
| US6893900B1 (en) * | 1998-06-24 | 2005-05-17 | Amkor Technology, Inc. | Method of making an integrated circuit package |
| US7670628B2 (en) * | 1999-07-07 | 2010-03-02 | Angioblast Systems, Inc. | Mesenchymal precursor cell |
| ATE489101T1 (de) * | 2000-04-25 | 2010-12-15 | Osiris Therapeutics Inc | Wiederherstellung der gelenken mit mesenchymalen stammzellen |
| ATE328067T1 (de) * | 2000-04-28 | 2006-06-15 | Childrens Medical Center | Isolierung von mesenchymalen stammzellen und deren verwendung |
-
2006
- 2006-01-18 GB GBGB0600972.4A patent/GB0600972D0/en not_active Ceased
-
2007
- 2007-01-17 US US12/223,056 patent/US20100260721A1/en not_active Abandoned
- 2007-01-17 EP EP07700381A patent/EP1979471A1/en not_active Withdrawn
- 2007-01-17 AU AU2007206750A patent/AU2007206750A1/en not_active Abandoned
- 2007-01-17 CN CNA2007800087785A patent/CN101400786A/zh active Pending
- 2007-01-17 JP JP2008550832A patent/JP2009523438A/ja active Pending
- 2007-01-17 WO PCT/GB2007/000107 patent/WO2007083093A1/en active Application Filing
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002504503A (ja) * | 1998-02-24 | 2002-02-12 | エムシーピー・ハーネマン・ユニバーシテイ | 中枢神経系の疾病の処置における使用のための単離されたストロマ細胞 |
| US20030103947A1 (en) * | 2001-02-23 | 2003-06-05 | Urlich Noth | In vitro engineered cartilage constructs produced by coating biodegradable polymer with human mesenchymal stem cells |
| US20040033217A1 (en) * | 2002-05-31 | 2004-02-19 | Padmavathy Vanguri | Intraperitoneal delivery of genetically engineered mesenchymal stem cells |
| WO2005001078A2 (en) * | 2003-06-27 | 2005-01-06 | Ethicon, Incorporated | Regeneration and repair of neural tissue using postpartum-derived cells |
| WO2005001076A2 (en) * | 2003-06-27 | 2005-01-06 | Ethicon, Incorporated | Postpartum cells derived from placental tissue, and methods of making and using the same |
| WO2005001079A2 (en) * | 2003-06-27 | 2005-01-06 | Ethicon, Incorporated | Soft tissue repair and regeneration using postpartum-derived cells |
| WO2005003334A2 (en) * | 2003-06-27 | 2005-01-13 | Ethicon, Incorporated | Postpartum cells derived from umbilical cord tissue, and methods of making and using the same |
| WO2005038012A2 (en) * | 2003-06-27 | 2005-04-28 | Ethicon Incorporated | Cartilage and bone repair and regeneration using postpartum-derived cells |
Non-Patent Citations (3)
| Title |
|---|
| JPN6012038749; Mol Biotechnol. 2003 Jan;23(1):37-49. * |
| JPN6012038750; Transplant Proc. 2005 Nov;37(9):4080-3. * |
| JPN6012038751; Arthritis Rheum. 2002 Dec;46(12):3349-60. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016074648A (ja) * | 2014-10-06 | 2016-05-12 | 佛教慈濟醫療財團法人 | 関節疾患を治療するための組成物及び方法 |
| US10624928B2 (en) | 2014-10-06 | 2020-04-21 | Hualien Tzu Chi Hospital, Buddhist Tzu Chi Medical Foundation | Composition for treatment of joint disease and method thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| US20100260721A1 (en) | 2010-10-14 |
| AU2007206750A1 (en) | 2007-07-26 |
| CN101400786A (zh) | 2009-04-01 |
| WO2007083093A1 (en) | 2007-07-26 |
| GB0600972D0 (en) | 2006-03-01 |
| EP1979471A1 (en) | 2008-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2009523438A (ja) | 細胞の富化 | |
| Francis et al. | Adipose-derived mesenchymal stem cells in the use of cartilage tissue engineering: the need for a rapid isolation procedure | |
| US8440440B2 (en) | Ultrasonic cavitation derived stromal or mesenchymal vascular extracts and cells derived therefrom obtained from adipose tissue and use thereof | |
| EP1845154A1 (en) | Multipotent stem cells derived from placenta tissue and cellular therapeutic agents comprising the same | |
| Fernandez-Moure et al. | Enhanced osteogenic potential of mesenchymal stem cells from cortical bone: a comparative analysis | |
| KR100871984B1 (ko) | 태반 조직 유래 다능성 줄기세포 및 이를 함유하는세포치료제 | |
| Bernacki et al. | Isolation of human mesenchymal stem cells from bone and adipose tissue | |
| Danišovič et al. | Comparative analysis of mesenchymal stromal cells from different tissue sources in respect to articular cartilage tissue engineering | |
| US20200270579A1 (en) | Method for preparing dental pulp stem cells from cells derived from dental pulp tissue | |
| RU2433172C2 (ru) | Способ получения гомогенной популяции стволовых клеток и ее применение | |
| US20140017783A1 (en) | Non-Enzymatic Method for Isolating Human Adipose-Derived Stromal Stem Cells | |
| CN109628388B (zh) | 用消化酶组合物从胎盘血管分离间充质干细胞 | |
| US9434923B2 (en) | Preparation of parental cell bank from foetal tissue | |
| WO2017051421A1 (en) | Methods for propagating mesenchymal stem cells (msc) for use in transplantation | |
| WO2014036094A1 (en) | Isolation of stromal vascular fraction from adipose tissue obtained using homogenization with beads | |
| CN114480261B (zh) | 一种脐带来源骨骼干细胞的提取分离方法 | |
| Talakoob et al. | Capability of cartilage extract to in vitro differentiation of rat mesenchymal stem cells (MSCs) to chondrocyte lineage | |
| JP2020516241A (ja) | 筋肉由来の前駆細胞分化した細胞を取得する方法 | |
| Ai et al. | Repair of critical size rat calvarial defects using endometrial-derived stem cells embedded within gelatin/apatite nanocomposite scaffold | |
| Samoylovich et al. | The influence of mesenchymal stromal cells on B-cell line growth and immunoglobulin synthesis | |
| El-Sheshtawy | Isolation and Characterization of Human Dental Pulp Stem Cells and Their In Vitro Dif-ferentiation into Odontoblast and Nerve-Like Cells | |
| Woju | Silica-Collagen Composite (B30) Performed Better as Scaffold Biomaterial than its Modification for Stem Cell Based Bone Healing in vitro | |
| Zhang et al. | Isolation, Culture, Identification and Differentiation of Canine Amniotic Mesenchymal Stem Cells in Vitro | |
| Umran et al. | Comparative Study of Expansion and Proliferation of Adult Mice Mesenchymal Stem Cells Derived from Bone Marrow and Adipose Tissue | |
| Trombi et al. | Mesenchymal Stromal Cell culture in autologous conditions for orthopedic applications |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100118 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100118 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120731 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130108 |