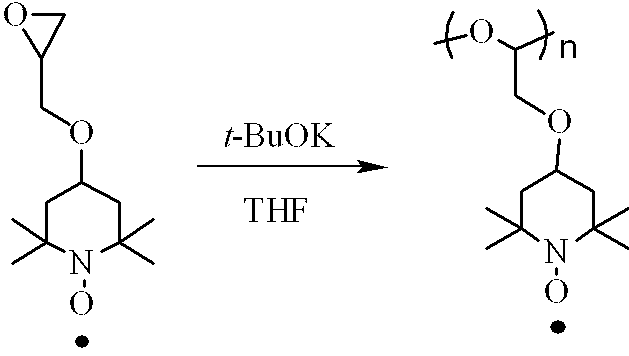JP2009102461A - Conductive water-containing gel - Google Patents
Conductive water-containing gel Download PDFInfo
- Publication number
- JP2009102461A JP2009102461A JP2007273189A JP2007273189A JP2009102461A JP 2009102461 A JP2009102461 A JP 2009102461A JP 2007273189 A JP2007273189 A JP 2007273189A JP 2007273189 A JP2007273189 A JP 2007273189A JP 2009102461 A JP2009102461 A JP 2009102461A
- Authority
- JP
- Japan
- Prior art keywords
- polymer
- water
- conductive
- gel
- oxyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- UKEHVVSQVDPYGR-UHFFFAOYSA-N CC(C)(C1)NCCC1N Chemical compound CC(C)(C1)NCCC1N UKEHVVSQVDPYGR-UHFFFAOYSA-N 0.000 description 1
- BDDPVQYDOLBQIO-UHFFFAOYSA-N CC(C)(C1)NCCC1NC(C=C)=O Chemical compound CC(C)(C1)NCCC1NC(C=C)=O BDDPVQYDOLBQIO-UHFFFAOYSA-N 0.000 description 1
- CSGAUKGQUCHWDP-UHFFFAOYSA-N CC(C)(CC(CC1(C)C)O)N1O Chemical compound CC(C)(CC(CC1(C)C)O)N1O CSGAUKGQUCHWDP-UHFFFAOYSA-N 0.000 description 1
- MRLMKQBXPODULZ-UHFFFAOYSA-N CC(C)(CC(CC1(C)C)OC=C)N1[O-] Chemical compound CC(C)(CC(CC1(C)C)OC=C)N1[O-] MRLMKQBXPODULZ-UHFFFAOYSA-N 0.000 description 1
Abstract
Description
本発明は、吸湿あるいは水中で膨潤する主鎖を有する有機ラジカルポリマーから形成される導電性含水ゲルに関する。 The present invention relates to a conductive hydrogel formed from an organic radical polymer having a main chain that absorbs moisture or swells in water.
従来、導電性含水ゲルとしては、例えば以下に示すものが知られている。 Conventionally, as a conductive water-containing gel, for example, the following are known.
(1)局部的な生体電気信号の測定および電気治療などに使用される生体用電極に好適に利用できる導電性高分子ゲルが開発されている(特許文献1参照)。具体的には、架橋された合成高分子、水、多価アルコールおよび電解質塩を含む導電性高分子ゲルに関し、架橋された合成高分子が8〜25質量%の範囲にあるときに、作成されたゲル中に含まれる高分子主鎖の割合が最適となり、ゲル強度が高くて腰強度の大きな導電性含水ゲルが得られると記載されている。 (1) Conductive polymer gels that can be suitably used for biomedical electrodes used for local bioelectric signal measurement and electrotherapy have been developed (see Patent Document 1). Specifically, regarding a conductive polymer gel containing a crosslinked synthetic polymer, water, a polyhydric alcohol and an electrolyte salt, it is prepared when the crosslinked synthetic polymer is in the range of 8 to 25% by mass. Further, it is described that the ratio of the polymer main chain contained in the gel is optimized, and a conductive hydrogel having high gel strength and high waist strength can be obtained.
(2)容易にゲル化し、良好な導電性を備えてなる導電性高分子ゲルおよびその製造方法、該導電性高分子ゲルを用いたアクチュエータ、イオン導入用パッチラベル、生体電極が開発されている(特許文献2参照)。具体的には、水、ポリ(3,4−エチレンジオキシチオフェン)−ポリ(スチレンスルホン酸)、界面活性剤および/またはアルコールを含み、水の含有量が66質量%以上、98質量%以下のものであり、このゲルは電子伝導とイオン伝導の両者を備えていることから、水の凝固点以下の温度域からなる雰囲気に曝されるような事態に陥っても、導電性が損なわれないと記載されている。 (2) A conductive polymer gel that easily gels and has good conductivity and a method for producing the same, an actuator using the conductive polymer gel, an iontophoretic patch label, and a bioelectrode have been developed. (See Patent Document 2). Specifically, it contains water, poly (3,4-ethylenedioxythiophene) -poly (styrenesulfonic acid), a surfactant and / or an alcohol, and the water content is 66 mass% or more and 98 mass% or less. Since this gel has both electron conduction and ion conduction, its conductivity is not impaired even if it is exposed to an atmosphere with a temperature range below the freezing point of water. It is described.
(3)モノマーを電解重合する製法により、三次元的なネットワークを形成したゲル状のポリチオフェン誘導体からなる固体フィルムが得られることが知られている(非特許文献1参照)。 (3) It is known that a solid film made of a gel-like polythiophene derivative in which a three-dimensional network is formed can be obtained by a production method in which a monomer is electropolymerized (see Non-Patent Document 1).
しかしながら、上記の従来例における導電性高分子ゲルおよびその製法には、次に述べるような課題が残されている。 However, the following problems remain in the conductive polymer gel and the method for producing the same in the above conventional example.
上記(1)の導電性高分子ゲルは、電解質を含み、この電解質が導電性を発揮する機能を担っていることから、水の凝固点以下の温度域に曝された場合、導電性が不安定となるか、あるいは導電性が確保できなくなる虞があった。つまり、従来の導電性高分子ゲルは、水の凝固点以下とした低温の雰囲気では、良好な導電性を維持することは困難であった。 The conductive polymer gel of (1) above contains an electrolyte, and since this electrolyte has a function of exhibiting conductivity, the conductivity is unstable when exposed to a temperature range below the freezing point of water. There is a concern that the conductivity may not be ensured. That is, it has been difficult for conventional conductive polymer gels to maintain good conductivity in a low temperature atmosphere below the freezing point of water.
上記(2)の導電性高分子ゲルは、ポリ(3,4−エチレンジオキシチオフェン)−ポリ(スチレンスルホン酸)の導電性により、水の凝固点以下の温度域からなる雰囲気に曝されるような事態に陥っても、導電性が損なわれないものの、ポリ(3,4−エチレンジオキシチオフェン)−ポリ(スチレンスルホン酸)と水のみの組み合わせではコロイド分散液となるのみで、ゲル化剤として界面活性剤、および、またはアルコールを添加しなければゲル化することができないものである。またポリ(3,4−エチレンジオキシチオフェン)−ポリ(スチレンスルホン酸)は黒色材料であるため光透過性が悪く、透明電極の用途には用いることができない。 The conductive polymer gel (2) is exposed to an atmosphere having a temperature range below the freezing point of water due to the conductivity of poly (3,4-ethylenedioxythiophene) -poly (styrenesulfonic acid). Even if it falls into a serious situation, the electrical conductivity is not impaired, but the combination of poly (3,4-ethylenedioxythiophene) -poly (styrenesulfonic acid) and water only becomes a colloidal dispersion, and the gelling agent As described above, it cannot be gelled unless a surfactant and / or alcohol is added. In addition, poly (3,4-ethylenedioxythiophene) -poly (styrenesulfonic acid) is a black material, and therefore has poor light transmission and cannot be used for a transparent electrode.
上記(3)の導電性高分子ゲルは、電解質を含むことなく導電性を発揮するが、モノマーの重合とゲル化が同一の工程で行われる必要があるため、工程が複雑となり、制御性という観点からは高度な技術を求められる。 The conductive polymer gel (3) exhibits conductivity without containing an electrolyte, but the monomer polymerization and gelation need to be performed in the same process, which makes the process complicated and controllable. From the viewpoint, advanced technology is required.
一方、安定ラジカル分子を高分子化したポリマーが、酸化還元樹脂の一つとして従来から合成されている。このようなポリマーは、2,2,6,6−テトラメチルピペリジン−1−オキシル(以下「TEMPO」と略すことがある)が置換したアクリレートやスチレン誘導体のポリマーに代表され、例えばアルコールのアルデヒドやケトンへの酸化触媒能等を示す。 On the other hand, polymers obtained by polymerizing stable radical molecules have been conventionally synthesized as one of redox resins. Such polymers are represented by polymers of acrylates and styrene derivatives substituted by 2,2,6,6-tetramethylpiperidine-1-oxyl (hereinafter sometimes abbreviated as “TEMPO”). Shows oxidation catalyst ability to ketone, etc.
本発明者は、電極反応が一般に一電子移動であるため安定ラジカル経由の有機電極反応が可逆性高く生起する点に着目し、このような酸化還元能を電子の授受機能としてとらえ、電荷貯蔵材料として応用している。 The inventor of the present invention pays attention to the point that the organic electrode reaction via a stable radical occurs with high reversibility because the electrode reaction is generally one-electron transfer. It is applied as.
例えば、電荷貯蔵材料の例として、有機ラジカルを側鎖に用いたポリマーの蓄電性能に着目し、正極、負極およびプロピレンカーボネート、アセトニトリルなどを用いた有機電解液を構成要素とする非水系二次電池の電極活物質として応用した例を先に出願した(特許文献3〜10参照)。 For example, as an example of a charge storage material, paying attention to the power storage performance of a polymer using organic radicals in the side chain, a non-aqueous secondary battery comprising a positive electrode, a negative electrode, and an organic electrolyte using propylene carbonate, acetonitrile, etc. An example of application as an electrode active material was previously filed (see Patent Documents 3 to 10).
しかしながら、これらの出願は、非水系二次電池向けの蓄電材料としての開発に関するものであり、水中における安定的な導電性については全く検討されていない。 However, these applications relate to development as a power storage material for a non-aqueous secondary battery, and stable conductivity in water has not been studied at all.
本発明はこのような事情に鑑み、水の凝固点以下の温度域からなる雰囲気に曝された場合でも、良好な導電性を維持することが可能であり、かつ、界面活性剤やアルコールのようなゲル化剤を添加する必要が無く、簡便な作業工程により安定して製造できる、光透過性の良好な導電性高分子ゲルを提供することを課題とする。 In view of such circumstances, the present invention is capable of maintaining good conductivity even when exposed to an atmosphere having a temperature range below the freezing point of water, and is not limited to surfactants or alcohols. It is an object of the present invention to provide a conductive polymer gel with good light transmission, which does not require the addition of a gelling agent and can be stably produced by a simple work process.
本発明者らは前記課題を解決するために鋭意研究を重ねた結果、親水性の主鎖を有し、ニトロキシドラジカル基からなる側鎖を少なくとも有するポリマーを含水させた導電性含水ゲルが、良好な導電性を有することを見出し、本発明を完成させた。 As a result of intensive studies to solve the above problems, the present inventors have found that a conductive water-containing gel containing a polymer having a hydrophilic main chain and at least a side chain composed of a nitroxide radical group is good. As a result, the present invention was completed.
かかる本発明の第1の態様は、親水性の主鎖に、ニトロキシドラジカル基からなる側鎖を少なくとも有するポリマーと、水とを含有することを特徴とする導電性含水ゲルにある。 The first aspect of the present invention resides in a conductive hydrogel characterized in that a hydrophilic main chain contains at least a polymer having a side chain composed of a nitroxide radical group and water.
本発明の第2の態様は、前記ポリマーの主鎖が、ポリアクリルアミド、ポリエーテル、ポリビニルエーテル、およびそれらの共重合体からなる群から選択される一種であることを特徴とする請求項1に記載の導電性含水ゲルにある。 The second aspect of the present invention is characterized in that the main chain of the polymer is a kind selected from the group consisting of polyacrylamide, polyether, polyvinyl ether, and copolymers thereof. It exists in the electroconductive water-containing gel of description.
本発明の第3の態様は、前記ニトロキシドラジカル基からなる側鎖が、前記ポリマーの主鎖に環状ニトロキシドが置換することにより形成されたものであることを特徴とする請求項1又は2に記載の導電性含水ゲルにある。 According to a third aspect of the present invention, the side chain composed of the nitroxide radical group is formed by substituting a cyclic nitroxide for the main chain of the polymer. The conductive water-containing gel.
本発明の第4の態様は、前記環状ニトロキシドが、2,2,6,6−テトラメチルピペリジン−1−オキシル(=TEMPO)、2,2,5,5−テトラメチルピロリジン−1−オキシル(以下PROXYLと略すことがある)、又は4,4,5,5−テトラメチルイミダゾリン−1−オキシル−3−オキシド(以下ニトロニルニトロキシドと略すことがある)であることを特徴とする請求項3に記載の導電性含水ゲルにある。 In a fourth aspect of the present invention, the cyclic nitroxide is 2,2,6,6-tetramethylpiperidine-1-oxyl (= TEMPO), 2,2,5,5-tetramethylpyrrolidine-1-oxyl ( (Hereinafter, abbreviated as PROXYL) or 4,4,5,5-tetramethylimidazoline-1-oxyl-3-oxide (hereinafter abbreviated as nitronyl nitroxide). It exists in the electroconductive water-containing gel of description.
本発明の第5の態様は、前記ポリマーの主鎖が架橋構造を含むものであることを特徴とする請求項1〜4の何れか1項に記載の導電性含水ゲルにある。 5th aspect of this invention exists in the electroconductive water-containing gel of any one of Claims 1-4 in which the principal chain of the said polymer contains a crosslinked structure.
本発明の第6の態様は、前記水と共に支持電解質を含有していることを特徴とする請求項1〜5の何れか1項に記載の導電性含水ゲルにある。 The sixth aspect of the present invention resides in the conductive hydrogel according to any one of claims 1 to 5, wherein a supporting electrolyte is contained together with the water.
本発明によれば、水の凝固点以下の温度域からなる雰囲気に曝された場合でも、良好な導電性を維持することが可能であり、かつ、界面活性剤やアルコールのようなゲル化剤を添加する必要が無く、簡便な作業工程により安定して製造できる、導電性高分子ゲルを提供することができる。 According to the present invention, even when exposed to an atmosphere having a temperature range below the freezing point of water, it is possible to maintain good conductivity, and a gelling agent such as a surfactant or alcohol can be used. It is possible to provide a conductive polymer gel that does not need to be added and can be stably produced by a simple work process.
ニトロキシドラジカル基からなる側鎖を有するポリマーの主鎖が架橋構造を含むことで、任意に導電性含水ゲルの機械的強度を高めることも可能となる。 When the main chain of the polymer having a side chain composed of a nitroxide radical group contains a crosslinked structure, it is possible to arbitrarily increase the mechanical strength of the conductive hydrous gel.
導電性含水ゲルは支持電解質を含有した場合には、水の凝固点より高い温度域とした雰囲気に曝された場合において、一段と優れた導電性を備えることが可能となる。 When the conductive hydrogel contains a supporting electrolyte, the conductive hydrogel can be provided with more excellent conductivity when exposed to an atmosphere having a temperature range higher than the freezing point of water.
本発明で用いられるポリマーは、親水性の主鎖を有し、ニトロキシドラジカル基からなる側鎖を少なくとも有する有機ラジカルポリマーである。 The polymer used in the present invention is an organic radical polymer having a hydrophilic main chain and having at least a side chain composed of a nitroxide radical group.
ここで、有機ラジカルポリマーの主鎖は、親水性を有し、高分子鎖内に水分あるいは水溶性電解質を取り込んでゲル化できるものであればいかなるものでもよい。 Here, the main chain of the organic radical polymer may be any as long as it has hydrophilicity and can be gelled by incorporating moisture or a water-soluble electrolyte into the polymer chain.
ここでいう親水性を有するポリマーの主鎖とは、水に対する親和性が高いポリマー鎖を指す。より具体的には、主鎖となるポリマー鎖からなるポリマー単体と多量の水とを接触させることで、ポリマーの10質量%以上の水が含浸できて、かつゲル化するポリマー鎖を指す。 The main chain of the polymer having hydrophilicity here refers to a polymer chain having a high affinity for water. More specifically, it refers to a polymer chain that can be impregnated with 10% by mass or more of water and gelled by bringing a polymer alone consisting of a polymer chain as a main chain into contact with a large amount of water.
具体的には、ポリアクリルアミド、ポリエーテル、ポリビニルエーテル、およびそれらの共重合体からなる群から選択されるものを主鎖とすることができる。 Specifically, the main chain can be selected from the group consisting of polyacrylamide, polyether, polyvinyl ether, and copolymers thereof.
また、有機ラジカルポリマーの主鎖は、架橋構造を含むものであってもよい。架橋構造を含むことにより、任意に導電性含水ゲルの機械的強度を高めることが可能となる。 Further, the main chain of the organic radical polymer may include a crosslinked structure. By including a crosslinked structure, it is possible to arbitrarily increase the mechanical strength of the conductive hydrogel.
本発明において、主鎖が架橋構造を有するとは、高分子化合物が共有結合等により分子間に結合を生じ、三次元ポリマーもしくは網目ポリマーが形成された構造を有することを意味する。本発明の架橋構造を有する重合体は、架橋点の割合に依存して、ある程度の架橋点間距離で、三次元的又は網目状の高分子構造が形成されたものとなる。 In the present invention, the main chain having a crosslinked structure means that the polymer compound has a structure in which a bond is formed between the molecules by a covalent bond or the like to form a three-dimensional polymer or network polymer. The polymer having a crosslinked structure of the present invention has a three-dimensional or network-like polymer structure formed at a certain distance between the crosslinking points depending on the ratio of the crosslinking points.
架橋構造を有する重合体の製造方法は特に限定されないが、例えば、重合反応後に親水性の主鎖を形成するモノマーと、少なくとも一種の多官能性モノマーとを共重合させることにより製造することができる。 The method for producing a polymer having a crosslinked structure is not particularly limited, and can be produced, for example, by copolymerizing a monomer that forms a hydrophilic main chain after the polymerization reaction and at least one polyfunctional monomer. .
多官能性モノマーとしては、重合反応後に親水性の主鎖を形成するモノマーと重合する部位を2つ以上、例えば2〜4程度有するモノマーを使用する。重合反応後に親水性の主鎖を形成するモノマーと共重合することができる官能基としては、例えばエチレン系二重結合が挙げられる。多官能性モノマーとして、具体的には、ジビニルベンゼン、多官能アクリレート、多官能メタクリレート等の多官能ビニル系モノマー等が挙げられる。 As the polyfunctional monomer, a monomer having two or more, for example, about 2 to 4 polymerization sites with a monomer that forms a hydrophilic main chain after the polymerization reaction is used. Examples of the functional group that can be copolymerized with a monomer that forms a hydrophilic main chain after the polymerization reaction include an ethylene double bond. Specific examples of the polyfunctional monomer include polyfunctional vinyl monomers such as divinylbenzene, polyfunctional acrylate, and polyfunctional methacrylate.
本発明使用できる有機ラジカルポリマーの側鎖置換基を構成するためには、水中でも安定な酸化還元を繰り返すラジカル化合物を使用することができ、水中で安定な一電子移動を行うラジカル化合物であればいかなるものでもよく、例としては、環状ニトロキシドラジカルが挙げられる。 In order to constitute the side chain substituent of the organic radical polymer that can be used in the present invention, a radical compound that repeats stable redox in water can be used, and any radical compound that performs stable one-electron transfer in water can be used. Any can be used, and examples include cyclic nitroxide radicals.
環状ニトロキシドラジカルは、環状ニトロキシドを主鎖に置換することに形成され、より詳しくは、2,2,6,6−テトラメチルピペリジン−1−オキシル(=TEMPO)、2,2,5,5−テトラメチルピロリジン−1−オキシル(=PROXYL)、又は4,4,5,5−テトラメチルイミダゾリン−1−オキシル−3−オキシド(=ニトロニルニトロキシド)を置換させることにより形成されたものを挙げることができる。 Cyclic nitroxide radicals are formed by substituting cyclic nitroxides into the main chain, more specifically 2,2,6,6-tetramethylpiperidine-1-oxyl (= TEMPO), 2,2,5,5- List those formed by substituting tetramethylpyrrolidine-1-oxyl (= PROXYL) or 4,4,5,5-tetramethylimidazoline-1-oxyl-3-oxide (= nitronyl nitroxide) Can do.
また、ラジカル化合物は、ラジカル化合物の前駆体となる化合物、すなわち、電極反応等で酸化又は還元されてラジカル状態となる化合物でもよく、この場合、ゲルを作成した後に電極反応等の酸化もしくは還元反応によりラジカル部位を生起させればよい。 Further, the radical compound may be a compound that becomes a precursor of the radical compound, that is, a compound that is oxidized or reduced by an electrode reaction or the like to become a radical state. In this case, an oxidation or reduction reaction such as an electrode reaction after the gel is formed. The radical site may be generated by
本発明に使用できる有機ラジカルポリマーの数平均分子量は、水に膨潤するが溶け出さない限り特に限定されないが、好ましくは500以上500000以下である。 The number average molecular weight of the organic radical polymer that can be used in the present invention is not particularly limited as long as it swells in water but does not dissolve, but is preferably 500 or more and 500,000 or less.
本発明の導電性含水ゲルは、このような有機ラジカルポリマーと水とを含有するものであり、水の少なくとも一部がポリマーの主鎖に取り込まれてゲル化したものである。 The conductive hydrogel of the present invention contains such an organic radical polymer and water, and is gelled by incorporating at least a part of water into the main chain of the polymer.
本発明の導電性含水ゲルとする場合、有機ラジカルポリマーの含水前と含水後の重量変化が、膨潤時にそれほど大きな体積変化を伴わない範囲であることが好ましい。具体的には、0.1質量%以上1000質量%以下であることが好ましく、10質量%以上50質量%以下であることがより好ましい。 When the conductive hydrous gel of the present invention is used, it is preferable that the weight change of the organic radical polymer before and after hydration is in a range that does not involve a large volume change during swelling. Specifically, it is preferably 0.1% by mass or more and 1000% by mass or less, and more preferably 10% by mass or more and 50% by mass or less.
また、本発明の導電性含水ゲルは水と共に支持電解質を含有してもよい。支持電解質を含有することにより、水の凝固点より高い温度域とした雰囲気に曝された場合には、一段と優れた導電性を備えることが可能となる。支持電解質を含有する場合の濃度は、水に溶解する限り特に限定されないが、好ましくは0.01〜10mol/lである。 Moreover, the electroconductive water-containing gel of the present invention may contain a supporting electrolyte together with water. By containing the supporting electrolyte, when exposed to an atmosphere having a temperature range higher than the freezing point of water, it is possible to provide further excellent conductivity. The concentration in the case of containing the supporting electrolyte is not particularly limited as long as it dissolves in water, but is preferably 0.01 to 10 mol / l.
本発明で支持電解質として使用できる電解質塩は、当該分野で公知の電解質塩であってよく、例えば、塩化ナトリウム、塩化カリウム、塩化カルシウム、塩化アンモニウム、塩化鉄、塩化アルミニウム、塩化亜鉛、塩化ニッケル、硫酸ナトリウム、硫酸カリウム、硫酸カルシウム、硫酸アンモニウム、硫酸鉄、硫酸アルミニウム、硫酸亜鉛、硫酸ニッケルなどを挙げることができる。 The electrolyte salt that can be used as the supporting electrolyte in the present invention may be an electrolyte salt known in the art, such as sodium chloride, potassium chloride, calcium chloride, ammonium chloride, iron chloride, aluminum chloride, zinc chloride, nickel chloride, Examples thereof include sodium sulfate, potassium sulfate, calcium sulfate, ammonium sulfate, iron sulfate, aluminum sulfate, zinc sulfate, and nickel sulfate.
以下、本発明の詳細について合成例、実施例により具体的に説明するが、本発明はこれらの実施例に限定されるものではない。 Hereinafter, although the detail of this invention is concretely demonstrated by a synthesis example and an Example, this invention is not limited to these Examples.
<重合体の合成>
[製造例1]
(製造例1−1)N−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミドの合成
<Synthesis of polymer>
[Production Example 1]
(Production Example 1-1) Synthesis of N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide
4−アミノ−2,2,6,6−テトラメチルピペリジン 2.5g(15.9mmol)をベンゼン中、アクリルクロライド 1.29ml(15.9mmol)と反応させる。室温で2時間攪拌後、析出した固体を回収し、再結晶精製を経て白色板上結晶としてN−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミド 1.38g(収率41%)を得た。 2.5 g (15.9 mmol) of 4-amino-2,2,6,6-tetramethylpiperidine are reacted with 1.29 ml (15.9 mmol) of acrylic chloride in benzene. After stirring at room temperature for 2 hours, the precipitated solid was recovered and subjected to recrystallization purification to obtain 1.38 g of N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide as crystals on a white plate. 41%).
得られたN−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミドのNMR測定データ、質量分析、および元素分析結果を以下に示す。 The NMR measurement data, mass spectrometry, and elemental analysis results of the obtained N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide are shown below.
1H−NMR(500MHz,CDCl3)δ(ppm):6.30(d, 1H, J=1.5Hz), 6.09−6.04(q, 1H), 5.63(d, 1H, J=11.6Hz), 5.40(s, 1H), 4.36(m, 1H), 1.92(d, 1H, J=12.5Hz), 1.27(s, 6H), 1.13(s, 6H), 0.95(t, 2H, J=12.2Hz) 1 H-NMR (500 MHz, CDCl 3 ) δ (ppm): 6.30 (d, 1H, J = 1.5 Hz), 6.09-6.04 (q, 1H), 5.63 (d, 1H , J = 11.6 Hz), 5.40 (s, 1H), 4.36 (m, 1H), 1.92 (d, 1H, J = 12.5 Hz), 1.27 (s, 6H), 1.13 (s, 6H), 0.95 (t, 2H, J = 12.2 Hz)
13C−NMR(500MHz,CDCl3)δ(ppm):164.7, 131.3, 126.0, 50.9, 45.2, 42.7, 35.1, 28.6. 13 C-NMR (500 MHz, CDCl 3 ) δ (ppm): 164.7, 131.3, 126.0, 50.9, 45.2, 42.7, 35.1, 28.6.
Mass(m/z): [M+1]: found,211;calcd,211. Mass (m / z): [M + 1]: found, 211; calcd, 211.
元素分析Found:C,62.9; H, 9.5; N, 11.1%. Calcd : C,63.9; H, 9.7; N, 11.7% Elemental Analysis Found: C, 62.9; H, 9.5; N, 11.1%. Calcd: C, 63.9; H, 9.7; N, 11.7%
(製造例1−2)ポリ(N−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミド)の合成 (Production Example 1-2) Synthesis of poly (N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide)
N−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミド 100mg(0.47mmol)をエタノ−ル中、アゾビスイソブチロニトリル(AIBNと略す) 3.8mg(24μmol)を開始剤として、70℃で二時間攪拌し、ポリ(N−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミド)を無色透明固体83mg(収率83%)として得た。 N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide 100 mg (0.47 mmol) in ethanol azobisisobutyronitrile (abbreviated as AIBN) 3.8 mg (24 μmol) Was stirred at 70 ° C. for 2 hours to obtain poly (N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide) as a colorless transparent solid 83 mg (yield 83%). It was.
(製造例1−3)ポリ(N−(2,2,6,6−テトラメチルピペリジン−1−オキシル−4−イル)−アクリルアミド)の合成 (Production Example 1-3) Synthesis of poly (N- (2,2,6,6-tetramethylpiperidin-1-oxyl-4-yl) -acrylamide)
ポリ(N−(2,2,6,6−テトラメチルピペリジン−4−イル)−アクリルアミド) 100mgを、3等量のm−クロロ過安息香酸(mCPBAと略す)246mgとアセトン中で24時間攪拌した。橙色固体を回収し、メタノールを用いて洗浄した。得られたポリマーの分子量は数平均分子量38000(ポリスチレン換算)、分散度(重量平均分子量/数平均分子量)2.2であった。(収量80mg、収率80%)ESR測定およびSQUID磁化測定よりラジカルの定量的な発生を確認した。 100 mg of poly (N- (2,2,6,6-tetramethylpiperidin-4-yl) -acrylamide) was stirred in 246 mg of 3 equivalents of m-chloroperbenzoic acid (abbreviated as mCPBA) in acetone for 24 hours. did. An orange solid was collected and washed with methanol. The obtained polymer had a number average molecular weight of 38000 (polystyrene conversion) and a degree of dispersion (weight average molecular weight / number average molecular weight) of 2.2. (Yield 80 mg, Yield 80%) Quantitative generation of radicals was confirmed by ESR measurement and SQUID magnetization measurement.
[製造例2]
(製造例2−1)4−ビニルオキシ−2,2,6,6−テトラメチルピペリジン−1−オキシルの合成
[Production Example 2]
(Production Example 2-1) Synthesis of 4-vinyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl
4−ヒドロキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル 2.57g(14.9mmol)、炭酸ナトリウム 944mg(8.92mmol)、ビス(1,5−シクロオクタジエン)ジイリジウム(I)ジクロリド(=[Ir(cod)Cl]2)103mg(141μmol)をトルエン中、アルゴン雰囲気下で攪拌し、さらに酢酸ビニル 2.8ml(29.2mmol)を加え、90℃で5時間反応させた。エーテル抽出、クロロホルムを用いカラム精製を経て4−ビニルオキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル 1.44g(収率49%)を得た。 4-hydroxy-2,2,6,6-tetramethylpiperidine-1-oxyl 2.57 g (14.9 mmol), sodium carbonate 944 mg (8.92 mmol), bis (1,5-cyclooctadiene) diiridium ( I) 103 mg (141 μmol) of dichloride (= [Ir (cod) Cl] 2 ) was stirred in toluene under an argon atmosphere, and 2.8 ml (29.2 mmol) of vinyl acetate was further added and reacted at 90 ° C. for 5 hours. It was. After ether extraction and column purification using chloroform, 1.44 g (yield 49%) of 4-vinyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl was obtained.
得られた4−ビニルオキシ−2,2,6,6−テトラメチルピペリジン−1−オキシルのNMR測定データ、質量分析、および元素分析結果を以下に示す。 The NMR measurement data, mass analysis, and elemental analysis results of the resulting 4-vinyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl are shown below.
1H−NMR(500MHz,CDCl3)δ(ppm):6.44(dd, 1H, J=8.7, 7.7Hz), 4.47(d, 1H, J=5.0Hz), 4.19(m, 2H), 1.68(t, 2H, J=12.1Hz), 1.33(s, 6H), 1.30(s, 6H). 1 H-NMR (500 MHz, CDCl 3 ) δ (ppm): 6.44 (dd, 1H, J = 8.7, 7.7 Hz), 4.47 (d, 1H, J = 5.0 Hz), 4 .19 (m, 2H), 1.68 (t, 2H, J = 12.1 Hz), 1.33 (s, 6H), 1.30 (s, 6H).
13C−NMR(500MHz,CDCl3)δ(ppm):150, 88.0, 58.5, 44.0, 20.3. 13 C-NMR (500 MHz, CDCl 3 ) δ (ppm): 150, 88.0, 58.5, 44.0, 20.3.
Mass(m/z): [M]:found,198; calcd,198. Mass (m / z): [M]: found, 198; calcd, 198.
元素分析Found:C,66.2; H,9.9; N, 7.0%. Calcd : C,67.0; H, 9.7; N, 7.1% Elemental Analysis Found: C, 66.2; H, 9.9; N, 7.0%. Calcd: C, 67.0; H, 9.7; N, 7.1%
(製造例2−2)ポリ(4−ビニルオキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル)の合成 (Production Example 2-2) Synthesis of poly (4-vinyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl)
4−ビニルオキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル 97.0g(489mmol)をジクロロメタン溶媒 550ml中、三フッ化ホウ素ジエチルエーテル錯体 1.23ml(9.8mmol)を開始剤として−20℃で20時間反応させた。メタノール中に分散洗浄させた後、50℃で12時間減圧乾燥することでポリ(4−ビニルオキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル)を得た(収量92.6g、収率96%)。 4-vinyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl 97.0 g (489 mmol) in 550 ml of dichloromethane solvent and 1.23 ml (9.8 mmol) of boron trifluoride diethyl ether complex as an initiator The reaction was carried out at −20 ° C. for 20 hours. After being dispersed and washed in methanol, poly (4-vinyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl) was obtained by drying under reduced pressure at 50 ° C. for 12 hours (yield 92.6 g, Yield 96%).
[製造例3]
(製造例3−1)4−グリシジロキシ−2,2,6,6−テトラメチルピペリジン−1−オキシルの合成
[Production Example 3]
(Production Example 3-1) Synthesis of 4-glycidyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl
50質量%水酸化ナトリウム水溶液 4mlにエピクロロヒドリン 2.5ml(30mmol)テトラブチルアンモニウム硫酸水素ナトリウム 84mg(239μmol)を加え、攪拌する。4−ヒドロキシ−2,2,6,6テトラメチルピペリジン−1−オキシル 1.03g(5.98mmol)をさらに加え、室温で12時間反応させる。エーテル抽出、エ−テル/ヘキサン混合溶媒(混合容積比=1/1)を用いカラム精製を経て4−グリシジロキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル 1.14g(収率84%)を得た。 Epichlorohydrin 2.5 ml (30 mmol) 84 mg (239 μmol) sodium tetrabutylammonium hydrogensulfate is added to 4 ml of 50% by mass aqueous sodium hydroxide solution and stirred. Further, 1.03 g (5.98 mmol) of 4-hydroxy-2,2,6,6 tetramethylpiperidine-1-oxyl is added and reacted at room temperature for 12 hours. After ether extraction and column purification using ether / hexane mixed solvent (mixing volume ratio = 1/1), 1.14 g of 4-glycidyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl (yield) 84%).
得られた4−グリシジロキシ−2,2,6,6−テトラメチルピペリジン−1−オキシルのNMR測定データ、質量分析、および元素分析結果を以下に示す。 The NMR measurement data, mass spectrometry, and elemental analysis results of the resulting 4-glycidyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl are shown below.
1H−NMR(500MHz,CDCl3)δ(ppm):3.71(dd, 1H, J=11.3, 3.0Hz), 3.64(m, 1H), 3.40(dd, 1H, J=11.3, 5.8Hz), 3.11(m, 1H), 2.77(t, 1H, J=4.6Hz), 2.58(dd, 1H, J=5.2, 2.7Hz), 1.92(m, 2H), 1.44(q, 2H, J=12.2Hz), 1.14(s, 6H). 1 H-NMR (500 MHz, CDCl 3 ) δ (ppm): 3.71 (dd, 1H, J = 11.3, 3.0 Hz), 3.64 (m, 1H), 3.40 (dd, 1H , J = 11.3, 5.8 Hz), 3.11 (m, 1H), 2.77 (t, 1H, J = 4.6 Hz), 2.58 (dd, 1H, J = 5.2) 2.7 Hz), 1.92 (m, 2H), 1.44 (q, 2H, J = 12.2 Hz), 1.14 (s, 6H).
13C−NMR(500MHz,CDCl3)δ(ppm):71.1, 68.9, 58.9, 50.9, 44.5, 44.3, 32.0 ,20.5. 13 C-NMR (500 MHz, CDCl 3 ) δ (ppm): 71.1, 68.9, 58.9, 50.9, 44.5, 44.3, 32.0, 20.5.
Mass(m/z): [M]: found,228; calcd,228. Mass (m / z): [M]: found, 228; calcd, 228.
元素分析Found:C,62.9; H, 9.5; N, 6.2%. Calcd : C,63.1; H, 9.7; N, 6.1% Elemental Analysis Found: C, 62.9; H, 9.5; N, 6.2%. Calcd: C, 63.1; H, 9.7; N, 6.1%
(製造例3−2)ポリ((2,2,6,6−テトラメチルピペリジン−1−オキシル−4−イル)−グリシジルエーテル)の合成 (Production Example 3-2) Synthesis of poly ((2,2,6,6-tetramethylpiperidin-1-oxyl-4-yl) -glycidyl ether)
4−グリシジロキシ−2,2,6,6−テトラメチルピペリジン−1−オキシル 228mg(1.00mmol)をテトラヒドロフラン(=THF)中、tert−ブトキシカリウム(=t−BuOK) 5.6mg(0.05mmol)を重合開始剤として加え、窒素雰囲気下、60℃で24時間反応後、ジエチルエーテルへの再沈殿精製を経て橙色粉末としてポリ((2,2,6,6−テトラメチルピペリジン−1−オキシル−4−イル)−グリシジルエーテル)を得た。得られたポリマーの分子量は数平均分子量3600(ポリスチレン換算)、分散度(重量平均分子量/数平均分子量)1.4であった(収量150mg、収率66%)。 4-glycidyloxy-2,2,6,6-tetramethylpiperidine-1-oxyl 228 mg (1.00 mmol) in tetrahydrofuran (= THF) tert-butoxy potassium (= t-BuOK) 5.6 mg (0.05 mmol) ) As a polymerization initiator, reacted at 60 ° C. in a nitrogen atmosphere for 24 hours, purified by reprecipitation into diethyl ether, and then converted into poly ((2,2,6,6-tetramethylpiperidine-1-oxyl) as an orange powder. -4-yl) -glycidyl ether) was obtained. The obtained polymer had a number average molecular weight of 3600 (polystyrene conversion) and a dispersity (weight average molecular weight / number average molecular weight) of 1.4 (yield 150 mg, yield 66%).
[製造例4]
(製造例4−1)4−ビニルベンズアルデヒドの合成
[Production Example 4]
(Production Example 4-1) Synthesis of 4-vinylbenzaldehyde
メチルトリフェニルホスフィンブロミド 2.70g(7.58mmol)をTHF中、炭酸カリウム 1.24gと、氷浴中で攪拌し、イリドを形成させる。テレフタルアルデヒド 1.00g(7.46mmol)を加え、室温で12時間攪拌した。クロロホルム抽出、およびヘキサン/クロロホルム混合溶媒(混合容積比=1/2)を用いカラム精製を経て4−ビニルベンズアルデヒド 531mg(収率54%)を得た。 2.70 g (7.58 mmol) of methyltriphenylphosphine bromide are stirred with 1.24 g of potassium carbonate in THF in an ice bath to form an ylide. Terephthalaldehyde (1.00 g, 7.46 mmol) was added, and the mixture was stirred at room temperature for 12 hours. Chloroform extraction and column purification using a hexane / chloroform mixed solvent (mixing volume ratio = 1/2) yielded 531 mg (yield 54%) of 4-vinylbenzaldehyde.
得られた4−ビニルベンズアルデヒドのNMR測定データ、および質量分析結果を以下に示す。 The NMR measurement data and mass spectrometry result of the obtained 4-vinylbenzaldehyde are shown below.
1H−NMR(500MHz,CDCl3)δ(ppm):9.94(s, 1H), 7.78(d, 2H, J=8.5Hz), 7.61(d, 2H, J=8.5Hz), 6.76(dd, 4H, J=10.7, 17.5Hz), 5.86(d, 1H, J=17.4Hz), 5.38(d, 1H, J=11.0Hz). 1 H-NMR (500 MHz, CDCl 3 ) δ (ppm): 9.94 (s, 1H), 7.78 (d, 2H, J = 8.5 Hz), 7.61 (d, 2H, J = 8) .5Hz), 6.76 (dd, 4H, J = 10.7, 17.5 Hz), 5.86 (d, 1H, J = 17.4 Hz), 5.38 (d, 1H, J = 1.11. 0 Hz).
13C−NMR(500MHz,CDCl3)δ(ppm):191.1, 142.9, 135.5, 135.3, 129.6, 126.3, 117.0. 13 C-NMR (500 MHz, CDCl 3 ) δ (ppm): 191.1, 142.9, 135.5, 135.3, 129.6, 126.3, 117.0.
Mass(m/z): [M]: found,132; calcd,132. Mass (m / z): [M]: found, 132; calcd, 132.
(製造例4−2)4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン−1,3−ジオールの合成 (Production Example 4-2) Synthesis of 4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine-1,3-diol
4−ビニルベンズアルデヒド 3.11g(23.5mmol)を水、メタノール混合溶媒中、酢酸ナトリウム 2.12g(25.8mmol)とビスヒドロキシルアンモニウムスルフェート塩 6.36g(25.8mmol)を加え、24時間攪拌した。反応終了後、溶媒を除去し、固体を水洗し、4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン−1,3−ジオール 4.92g(収率80%)を得た。 4-vinylbenzaldehyde 3.11 g (23.5 mmol) was added in water and methanol mixed solvent, sodium acetate 2.12 g (25.8 mmol) and bishydroxylammonium sulfate salt 6.36 g (25.8 mmol) were added, and 24 hours. Stir. After completion of the reaction, the solvent was removed, the solid was washed with water, and 4.92 g of 4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine-1,3-diol (80% yield). )
得られた4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン−1,3−ジオールのNMR測定データ、質量分析、および元素分析結果を以下に示す。 The NMR measurement data, mass spectrometry, and elemental analysis results of the obtained 4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine-1,3-diol are shown below.
1H−NMR(500MHz,CDCl3)δ(ppm):7.48(q, 4H, J=27.7, 4.0Hz), 6.76(dd, 1H, J=10.6, 17.7Hz), 5.84(d, 1H, J=18.0Hz), 5.22(d, 1H, J=10.7Hz), 4.64(s, 1H), 1.15(s, 6H). 1 H-NMR (500 MHz, CDCl 3 ) δ (ppm): 7.48 (q, 4H, J = 27.7, 4.0 Hz), 6.76 (dd, 1H, J = 10.6, 17. 7 Hz), 5.84 (d, 1 H, J = 18.0 Hz), 5.22 (d, 1 H, J = 10.7 Hz), 4.64 (s, 1 H), 1.15 (s, 6 H) .
13C−NMR(500MHz,CDCl3)δ(ppm):165.0, 145.3, 139.8, 131.5, 128.3, 115.8, 93.3, 69.3, 37.5, 32.3, 27.0, 19.7. 13 C-NMR (500 MHz, CDCl 3 ) δ (ppm): 165.0, 145.3, 139.8, 131.5, 128.3, 115.8, 93.3, 69.3, 37.5 , 32.3, 27.0, 19.7.
Mass(m/z): [M+1]: found,263; calcd,263. Mass (m / z): [M + 1]: found, 263; calcd, 263.
元素分析Found:C,49.1; H, 5.7; N, 8.9%. Calcd:C,49.5; H,6.1; N,8.9% Elemental Analysis Found: C, 49.1; H, 5.7; N, 8.9%. Calcd: C, 49.5; H, 6.1; N, 8.9%
(製造例4−3)1,3−ビス−(t−ブチル−ジメチルシロキシ)−4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジンの合成 (Production Example 4-3) Synthesis of 1,3-bis- (t-butyl-dimethylsiloxy) -4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine
4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン−1,3−ジオール 3.00g(11.4mmol)をジメチルホルムアミド(=DMF)中、イミダゾ−ル 3.89g(57.2mmol)とtert−ブチルジメチルシリルクロリド(TBDMS−Clと略す) 8.6g(57.2mmol)を加えて、50℃、アルゴン雰囲気下で12時間攪拌した。クロロホルム抽出、およびヘキサンを用いたカラム精製を経て1,3−ビス−(t−ブチル−ジメチルシロキシ)−4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン 3.81g(収率68%)を得た。 3,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine-1,3-diol (3.00 g, 11.4 mmol) in dimethylformamide (= DMF) 89 g (57.2 mmol) and 8.6-g (57.2 mmol) of tert-butyldimethylsilyl chloride (abbreviated as TBDMS-Cl) were added, and the mixture was stirred at 50 ° C. under an argon atmosphere for 12 hours. After extraction with chloroform and column purification with hexane, 1,3-bis- (t-butyl-dimethylsiloxy) -4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine 3 Obtained .81 g (68% yield).
得られた1,3−ビス−(t−ブチル−ジメチルシロキシ)−4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジンのNMR測定データ、質量分析、および元素分析結果を以下に示す。 NMR measurement data, mass spectrometry, and element of the resulting 1,3-bis- (t-butyl-dimethylsiloxy) -4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine The analysis results are shown below.
1H−NMR(500MHz,CDCl3)δ(ppm):7.37(s, 4H), 6.76(dd, 4H, J=17.7, 11.1Hz), 5.79(d, 1H, J=17.7Hz), 5.29(d, 2H, J=11.0 Hz), 4.63(s, 1H), 1.20(s, 12H), 0.83(s, 18H), −0.04(s, 6H), −0.82(s, 6H). 1 H-NMR (500 MHz, CDCl 3 ) δ (ppm): 7.37 (s, 4H), 6.76 (dd, 4H, J = 17.7, 11.1 Hz), 5.79 (d, 1H , J = 17.7 Hz), 5.29 (d, 2H, J = 11.0 Hz), 4.63 (s, 1H), 1.20 (s, 12H), 0.83 (s, 18H) , -0.04 (s, 6H), -0.82 (s, 6H).
13C−NMR(500MHz,CDCl3)δ(ppm):137.2, 137.0, 130.9, 125.4, 113.2, 93.9, 24.8, 26.3, 17.9, 17.2, −3.8, −5.04. 13 C-NMR (500 MHz, CDCl 3 ) δ (ppm): 137.2, 137.0, 130.9, 125.4, 113.2, 93.9, 24.8, 26.3, 17.9 , 17.2, -3.8, -5.04.
Mass(m/z): [M]: calcd,489;found,490. Mass (m / z): [M]: calcd, 489; found, 490.
元素分析Found:C,66.3; H, 10.0; N, 5.7%. Calcd for C27H52N2O2Si2:C,66.1; H,10.3; N,5.7% Elemental Analysis Found: C, 66.3; H, 10.0; N, 5.7%. Calcd for C 27 H 52 N 2 O 2 Si 2: C, 66.1; H, 10.3; N, 5.7%
(製造例4−4)1,3−ビス−(t−ブチル−ジメチルシロキシ)−4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン−アクリルアミド共重合体の合成 (Production Example 4-4) 1,3-bis- (t-butyl-dimethylsiloxy) -4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine-acrylamide copolymer Composition
1,3−ビス−(t−ブチル−ジメチルシロキシ)−4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン 100mg(204μmol)とアクリルアミド 10mg(136μmol)をTHF溶媒中AIBN 2.7mg(17μmol)を開始剤として用い、70℃で12時間攪拌した。ジエチルエーテルへの再沈殿精製を経て白色粉末として1,3−ビス−(t−ブチル−ジメチルシロキシ)−4,4,5,5−テトラメチル−2−(4−ビニルフェニル)−イミダゾリジン−アクリルアミド共重合体を得た。得られたポリマーの分子量は数平均分子量8600(ポリスチレン換算)、分散度(重量平均分子量/数平均分子量)1.5であった(収量84mg、収率76%)。 1,3-bis- (t-butyl-dimethylsiloxy) -4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine 100 mg (204 μmol) and acrylamide 10 mg (136 μmol) in THF solvent Medium AIBN (2.7 mg, 17 μmol) was used as an initiator, and the mixture was stirred at 70 ° C. for 12 hours. 1,3-bis- (t-butyl-dimethylsiloxy) -4,4,5,5-tetramethyl-2- (4-vinylphenyl) -imidazolidine as white powder after reprecipitation purification into diethyl ether Acrylamide copolymer was obtained. The polymer obtained had a number average molecular weight of 8600 (polystyrene conversion) and a dispersity (weight average molecular weight / number average molecular weight) of 1.5 (yield 84 mg, yield 76%).
(製造例4−5)ニトロニルニトロキシド置換ポリスチレン−ポリアクリルアミド共重合体の合成 (Production Example 4-5) Synthesis of Nitronyl Nitroxide-Substituted Polystyrene-Polyacrylamide Copolymer
前駆体ポリマー 100mg(310μmol)をTHF中でテトラ(n−ブチル)アンモニウムフロリド(=n−Bu4NF) 202mg(775μmol)と室温で24時間攪拌した。続いて過ヨウ素酸ナトリウムの飽和溶液を加え、さらに30分攪拌し、ジクロロメタン抽出、水への再沈殿精製を経てニトロニルニトロキシド置換ポリスチレン−ポリアクリルアミド共重合体を得た。得られたポリマーの分子量は数平均分子量8600(ポリスチレン換算)、分散度(重量平均分子量/数平均分子量)1.6であった(収量36mg、収率81%)。
ESR測定およびSQUID磁化測定よりラジカルの定量的な発生を確認した。
100 mg (310 μmol) of the precursor polymer was stirred with 202 mg (775 μmol) of tetra (n-butyl) ammonium fluoride (= n-Bu 4 NF) in THF at room temperature for 24 hours. Subsequently, a saturated solution of sodium periodate was added, the mixture was further stirred for 30 minutes, extracted with dichloromethane, and purified by reprecipitation into water to obtain a nitronyl nitroxide substituted polystyrene-polyacrylamide copolymer. The polymer obtained had a number average molecular weight of 8600 (polystyrene conversion) and a dispersity (weight average molecular weight / number average molecular weight) of 1.6 (yield 36 mg, 81%).
The quantitative generation of radicals was confirmed by ESR measurement and SQUID magnetization measurement.
<ゲル膜の作成>
(実施例1)
製造例1で合成した重合体100mgにアセトニトリル 1mlを添加して50℃雰囲気下、5時間攪拌して溶解(分散)し、重合体溶液を調製した。この溶液を金電極を基板として1ml塗布することで、合成した重合体の薄膜を厚さ23μmで作成した。さらに、薄膜上に、金電極をのせることで薄膜を挟み込み、純水あるいは0.5Mの食塩水をそれぞれ含浸させることによりゲル膜を作成し、光透過性の良好な導電性含水ゲルを得た。
<Creation of gel film>
(Example 1)
To 100 mg of the polymer synthesized in Production Example 1, 1 ml of acetonitrile was added and dissolved (dispersed) by stirring in a 50 ° C. atmosphere for 5 hours to prepare a polymer solution. By applying 1 ml of this solution using a gold electrode as a substrate, a synthesized polymer thin film was formed with a thickness of 23 μm. Furthermore, a thin film is sandwiched by placing a gold electrode on the thin film, and a gel film is created by impregnating each with pure water or 0.5 M saline to obtain a conductive water-containing gel with good light transmission. It was.
(実施例2)
製造例2で合成した重合体を用いた以外は実施例1と同様に操作することで、合成した重合体の薄膜を厚さ20μmで作成した。さらに、薄膜上に、金電極をのせることで薄膜を挟み込み、純水あるいは0.5Mの食塩水をそれぞれ含浸させることによりゲル膜を作成し、光透過性の良好な導電性含水ゲルを得た。
(Example 2)
A thin film of the synthesized polymer was formed to a thickness of 20 μm by operating in the same manner as in Example 1 except that the polymer synthesized in Production Example 2 was used. Furthermore, a thin film is sandwiched by placing a gold electrode on the thin film, and a gel film is created by impregnating each with pure water or 0.5 M saline to obtain a conductive water-containing gel with good light transmission. It was.
(実施例3)
製造例3で合成した重合体を、および溶液の溶媒にTHFを用いた以外は実施例1と同様に操作することで、合成した重合体の薄膜を厚さ22μmで作成した。さらに、薄膜上に、金電極をのせることで薄膜を挟み込み、純水あるいは0.5Mの食塩水をそれぞれ含浸させることによりゲル膜を作成し、光透過性の良好な導電性含水ゲルを得た。
(Example 3)
A thin film of the synthesized polymer was formed to a thickness of 22 μm by operating in the same manner as in Example 1 except that the polymer synthesized in Production Example 3 and THF was used as the solvent of the solution. Furthermore, a thin film is sandwiched by placing a gold electrode on the thin film, and a gel film is created by impregnating each with pure water or 0.5 M saline to obtain a conductive water-containing gel with good light transmission. It was.
(実施例4)
製造例4で合成した重合体を用いた以外は実施例1と同様に操作することで、合成した重合体の薄膜を厚さ20μmで作成した。さらに、薄膜上に、金電極をのせることで薄膜を挟み込み、純水あるいは0.5Mの食塩水をそれぞれ含浸させることによりゲル膜を作成し、光透過性の良好な導電性含水ゲルを得た。
Example 4
A thin film of the synthesized polymer was formed to a thickness of 20 μm by operating in the same manner as in Example 1 except that the polymer synthesized in Production Example 4 was used. Furthermore, a thin film is sandwiched by placing a gold electrode on the thin film, and a gel film is created by impregnating each with pure water or 0.5 M saline to obtain a conductive water-containing gel with good light transmission. It was.
<電気伝導度の測定>
(試験例1)
実施例1で作成された、純水あるいは0.5Mの食塩水をそれぞれ含浸させたゲル膜それぞれについて、AUTOLAB社製PGATAT30アナライザーを用いて、交流インピーダンス法により電気伝導度を測定した。
<Measurement of electrical conductivity>
(Test Example 1)
For each of the gel membranes impregnated with pure water or 0.5 M saline prepared in Example 1, the electrical conductivity was measured by an alternating current impedance method using a PGATAT30 analyzer manufactured by AUTOLAB.
純水を含浸させたゲル膜の伝導度は2×10-8 Scm-1であり、また0.5Mの食塩水を含浸させたゲル膜の伝導度は5×10-8 Scm-1と良好な導電性を示した。 The conductivity of the gel membrane impregnated with pure water is 2 × 10 −8 Scm −1 , and the conductivity of the gel membrane impregnated with 0.5 M saline is 5 × 10 −8 Scm −1. Conductivity.
(試験例2)
実施例2で作成された、純水あるいは0.5Mの食塩水をそれぞれ含浸させたゲル膜を用いた以外は試験例1と同様の操作を行うことで、実施例2で合成した重合体のゲルの電気伝導度を測定した。
(Test Example 2)
The polymer synthesized in Example 2 was prepared by performing the same operation as in Test Example 1 except that the gel film prepared in Example 2 and impregnated with pure water or 0.5 M saline was used. The electrical conductivity of the gel was measured.
純水を含浸させたサンプルの伝導度は3×10-8 Scm-1であり、また0.5Mの食塩水を含浸させたゲル膜の伝導度は2×10-7 Scm-1と良好な導電性を示した。 The conductivity of the sample impregnated with pure water is 3 × 10 −8 Scm −1 , and the conductivity of the gel membrane impregnated with 0.5 M saline is 2 × 10 −7 Scm −1. It showed conductivity.
(試験例3)
実施例3で作成された、純水あるいは0.5Mの食塩水をそれぞれ含浸させたゲル膜をを用いた以外は試験例1と同様の操作を行うことで、実施例3で合成した重合体の含水ゲルの電気伝導度を測定した。
(Test Example 3)
The polymer synthesized in Example 3 by performing the same operation as in Test Example 1 except that the gel membrane prepared in Example 3 and impregnated with pure water or 0.5 M saline was used. The electrical conductivity of the hydrous gel was measured.
純水を含浸させたサンプルの伝導度は4×10-5 Scm-1であり、また0.5Mの食塩水を含浸させたゲル膜の伝導度は2×10-6 Scm-1と良好な導電性を示した。 The conductivity of the sample impregnated with pure water is 4 × 10 −5 Scm −1 , and the conductivity of the gel membrane impregnated with 0.5 M saline is 2 × 10 −6 Scm −1. It showed conductivity.
(試験例4)
実施例4で作成された、純水あるいは0.5Mの食塩水をそれぞれ含浸させたゲル膜を用いた以外は試験例1と同様の操作を行うことで、実施例4で合成した重合体のゲルの電気伝導度を測定した。
(Test Example 4)
The polymer synthesized in Example 4 was prepared by performing the same operation as in Test Example 1 except that the gel film prepared in Example 4 and impregnated with pure water or 0.5 M saline was used. The electrical conductivity of the gel was measured.
純水を含浸させたサンプルの伝導度は7×10-7 Scm-1であり、また0.5Mの食塩水を含浸させたゲル膜の伝導度は3×10-6 Scm-1と良好な導電性を示した。 The conductivity of the sample impregnated with pure water is 7 × 10 −7 Scm −1 , and the conductivity of the gel membrane impregnated with 0.5 M saline is 3 × 10 −6 Scm −1. It showed conductivity.
Claims (6)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007273189A JP2009102461A (en) | 2007-10-19 | 2007-10-19 | Conductive water-containing gel |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007273189A JP2009102461A (en) | 2007-10-19 | 2007-10-19 | Conductive water-containing gel |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2009102461A true JP2009102461A (en) | 2009-05-14 |
Family
ID=40704487
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007273189A Pending JP2009102461A (en) | 2007-10-19 | 2007-10-19 | Conductive water-containing gel |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2009102461A (en) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011057620A (en) * | 2009-09-10 | 2011-03-24 | Nissan Chem Ind Ltd | Gelling agent of lipid histidine |
| JP2011078706A (en) * | 2009-10-09 | 2011-04-21 | Univ Of Tsukuba | Method for improving quality of surface biocompatibility |
| JP2011126801A (en) * | 2009-12-16 | 2011-06-30 | Sumitomo Seika Chem Co Ltd | N, n-bis-(2,2,6,6-tetramethyl-piperidin-4-yl)-amine-(meth)acrylamide, and crosslinked polymer of n, n-bis-(2,2,6,6-tetramethyl-piperidin-n-oxyl-4-yl)-amine-(meth)acrylamide compound |
| JP2013155267A (en) * | 2012-01-30 | 2013-08-15 | Sumitomo Seika Chem Co Ltd | Method for producing nitroxide polymer |
| JP2014151015A (en) * | 2013-02-08 | 2014-08-25 | Nippon Telegr & Teleph Corp <Ntt> | Body surface-mounted electrode, biological signal measurement method, and biological signal measuring device |
| JP5969981B2 (en) * | 2011-03-31 | 2016-08-17 | 住友精化株式会社 | Radical composition and battery using the same |
| CN114773508A (en) * | 2022-04-29 | 2022-07-22 | 南京邮电大学 | Supramolecular hydrogel and preparation and application thereof |
-
2007
- 2007-10-19 JP JP2007273189A patent/JP2009102461A/en active Pending
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011057620A (en) * | 2009-09-10 | 2011-03-24 | Nissan Chem Ind Ltd | Gelling agent of lipid histidine |
| JP2011078706A (en) * | 2009-10-09 | 2011-04-21 | Univ Of Tsukuba | Method for improving quality of surface biocompatibility |
| JP2011126801A (en) * | 2009-12-16 | 2011-06-30 | Sumitomo Seika Chem Co Ltd | N, n-bis-(2,2,6,6-tetramethyl-piperidin-4-yl)-amine-(meth)acrylamide, and crosslinked polymer of n, n-bis-(2,2,6,6-tetramethyl-piperidin-n-oxyl-4-yl)-amine-(meth)acrylamide compound |
| JP5969981B2 (en) * | 2011-03-31 | 2016-08-17 | 住友精化株式会社 | Radical composition and battery using the same |
| JP2013155267A (en) * | 2012-01-30 | 2013-08-15 | Sumitomo Seika Chem Co Ltd | Method for producing nitroxide polymer |
| JP2014151015A (en) * | 2013-02-08 | 2014-08-25 | Nippon Telegr & Teleph Corp <Ntt> | Body surface-mounted electrode, biological signal measurement method, and biological signal measuring device |
| CN114773508A (en) * | 2022-04-29 | 2022-07-22 | 南京邮电大学 | Supramolecular hydrogel and preparation and application thereof |
| CN114773508B (en) * | 2022-04-29 | 2023-10-24 | 南京邮电大学 | Supermolecule hydrogel and preparation and application thereof |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Wild et al. | All‐organic battery composed of thianthrene‐and TCAQ‐based polymers | |
| JP2009104819A (en) | Electricity storage material and secondary battery using it | |
| JP2009102461A (en) | Conductive water-containing gel | |
| JP5983631B2 (en) | Carbazole polymer | |
| Perumal et al. | Impact of lithium chlorate salts on structural and electrical properties of natural polymer electrolytes for all solid state lithium polymer batteries | |
| Zhu et al. | Soft, flexible and self-healable supramolecular conducting polymer-based hydrogel electrodes for flexible supercapacitors | |
| EP0714149B1 (en) | Solid ion conductive polymer electrolyte and composition and production method therefor | |
| JP4416200B2 (en) | Solid electrolyte and battery using the same | |
| CN101714460B (en) | Preparation method of polypyrrole/polyacrylic compound gel electrolyte | |
| US11643496B2 (en) | Polymer electrolyte having superior ion conductivity and mechanical strength and method of manufacturing same | |
| JP2003151632A (en) | Gel electrolyte and nonaqueous electrolyte battery using the same | |
| Yang et al. | Multiple healing flexible zinc-ion battery based on double cross-linked polyampholyte hydrogel electrolyte | |
| JP4985959B2 (en) | Organic solid electrolyte and secondary battery using the same | |
| JPH06184396A (en) | Conductive polymer composite having high electrical activity density and its preparation | |
| JP2018504466A (en) | POLYMER, PROCESS FOR PRODUCING THE SAME, AND ELECTROLYTE MEMBRANE CONTAINING THE SAME | |
| CN108017784A (en) | Hydridization conductive hydrogel its preparation method and application | |
| JP4389454B2 (en) | Polymer solid electrolyte | |
| JP4214691B2 (en) | Electrode material, method for producing the electrode material, battery electrode using the electrode material, and battery using the electrode | |
| JP3634075B2 (en) | Solid electrolyte battery | |
| KR20230136944A (en) | Hydrogel electrolyte and zinc ion battery using the same | |
| JP5176129B2 (en) | Polyradical compounds and batteries | |
| JP4239632B2 (en) | Lithium ion conductive gel electrolyte | |
| JP2699500B2 (en) | Conductive polymer composite | |
| KR20120078235A (en) | Lewis acid complex-based polymer electrolyte for lithium secondary battery and lithium secondary battery comprising the same | |
| US20220158233A1 (en) | Polymer electrolyte and method of preparing same |