JP2009100687A - microRNA発現プロファイリングに基づく膀胱癌の検出方法 - Google Patents
microRNA発現プロファイリングに基づく膀胱癌の検出方法 Download PDFInfo
- Publication number
- JP2009100687A JP2009100687A JP2007276191A JP2007276191A JP2009100687A JP 2009100687 A JP2009100687 A JP 2009100687A JP 2007276191 A JP2007276191 A JP 2007276191A JP 2007276191 A JP2007276191 A JP 2007276191A JP 2009100687 A JP2009100687 A JP 2009100687A
- Authority
- JP
- Japan
- Prior art keywords
- mir
- mirna
- expression level
- bladder cancer
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Abandoned
Links
Abstract
【課題】miRNAの機能、特に、細胞の癌化との関連を解明し、miRNAの発現量の変動を測定することから成る膀胱癌の検出方法を提供すること。
【解決手段】細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106a、並びに、miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の変動を測定することから成る、膀胱癌の検出方法。
【選択図】なし
Description
Calin GA and Croce CM (2006) MicroRNA signatures in human cancers, Nature Reviews, 6, 857-866. Volinia S et al, (2006) A microRNA expression signature of human solid tumors define cancer gene targets, PNAS, USA, 103, 2257-2261.
[1]細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106a、並びに、miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の変動を測定することから成る、膀胱癌の検出方法。
[2]細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106a、並びに、miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の変動に基づく、膀胱癌の治療又は予防に有効な物質のスクリーニング方法。
[3]本発明スクリーニング方法に用いるスクリーニングキット。
(a) 被検物質の存在下に細胞を培養する工程、
(b)該細胞における各miRNAの発現量を測定する工程、及び
(c)発現量の亢進を抑制するか又は発現量を減少させる物質を選択する工程、を含む方法でスクリーニングすることができる。
(a) 被検物質の存在下に細胞を培養する工程、
(b)該細胞における各miRNAの発現量を測定する工程、及び
(c)発現量の低下を抑制するか又は発現量を増加させる物質を選択する工程、を含む方法でスクリーニングすることができる。
miRNA特異的逆転写反応および定量PCR
膀胱癌患者臨床検体19検体(癌部14検体、非癌部5検体)及び膀胱癌由来細胞株3種(BOY、KK47、T24)よりtotal RNAをtrizol(Gibco BRL, Life Technologies, Gaitherburg, MD, USA)用いて抽出した。cDNAは得られたtotal RNAからmiRNA特異的なプライマー(TaqMan microRNA Assay Protocol, PE, Applied Biosystems, Foster City, CA, UAS)を用いて合成した。逆転写反応は以下のとおり行った。10nM RNA samples, 50nM stem-loop RT primer, 1 x RT buffer, 0.25mM each of dNTPs, 3.33 U/μl MultiScribe reverse transcriptase 及び 0.25 U/μl RNase Inhubitor。また、これら7.5μlの反応液を以下のプロトコールでインキュベートした。16℃・30分、42℃・30分、85℃・5分、反応後4℃で保存した。定量PCRは、ABI 7300 Seqence Detection Systemを用いて以下の反応系で行った。95℃・10分インキュベートした後、95℃・15秒、60度・10分の反応を40回行った。
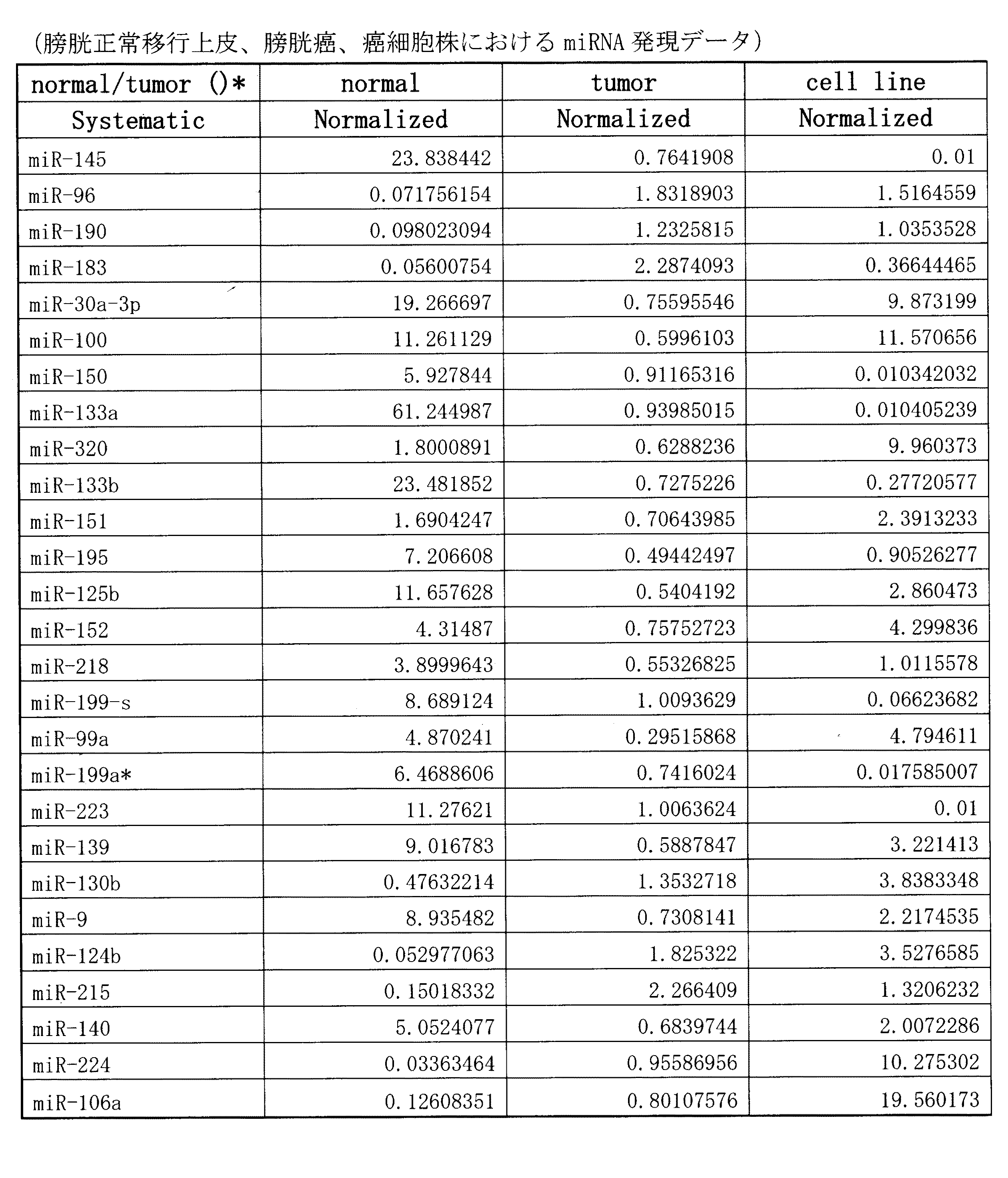
膀胱癌患者臨床検体19例(癌部14検体および非癌部5検体)及び膀胱癌由来細胞株3種について、既に記載したデータベース(miRBase::Sequences, Sanger Institute)から選んだ156種類のmiRNA及びコントロール遺伝子の解析を行った。解析結果について、マイクロアレイで用いられているglobal median normalization法を用いてデータの標準化を行った。この解析データから、癌部および非癌部で優位に(P<0.01)発現差のある遺伝子を選択した。その結果、27種類のmiRNAが癌部で有意に発現変動していることが判明した(8種類のmiRNAは癌部で発現亢進、19種類のmiRNAは癌部で発現低下)。以下の表1及び表2にそのリストを示す。
今回の解析で27種類のmiRNAが膀胱癌に関係するmiRNAとしてリストアップすることができた。この中で、正常移行上皮に比べ、癌部で発現が低下しているmiRNAの中のmiR-30-3p、miR-133b、及びmiR-145は、同じくABI TaqMan法を用いた大腸癌のプロファイルにおいても癌部において発現が低下していることが報告された(Bandres et al, 2006)。miR-145は大腸癌(Cummins et al, 2006)以外にも、肺癌(Yanaihara et al, 2006)や乳癌(Iorio et al, 2005)で発現が低下することが報告されており、癌抑制遺伝子的な働きを担うmiRNAであることが示唆される。
1. Calin GA and Croce CM (2006) MicroRNA signatures in human cancers, Nature Reviews, 6, 857-866.
2. Calin GA et al, (2002) Frequent deletions and down-regulation of micro- RNA genes miR15 and miR16 at 13q14 in chronic lymphocytic leukemia, PNAS, USA, 99, 15524-15529.
3. Hayashida Y et al, (2005) A polycistronic microRNA cluster, miR-17-92, is overexpressed in human lung cancers and enhances cell proliferation. Cancer Res, 65, 9628-9632.
4. Volinia S et al, (2006) A microRNA expression signature of human solid tumors define cancer gene targets, PNAS, USA, 103, 2257-2261.
5. Liu CG et al, (2004)An oligonucleotide microchip for genome-wide microRNA profiling in human and mouse tissues, PNAS, U S A, 101, 9740-9744.
7. Lim LP et al, (2005) Microarray analysis shows that some microRNAs downregulate large numbers of target mRNAs, Nature, 433, 769-773.
8. Allawi HT et al, (2004) Quantitation of microRNAs using a modified Invader assay, Rna., 10, 153-1161.
9. Lu J et al, (2005) MicroRNA expression profiles classify human cancers, Nature, 435, 834-838.
10. Chen C et al, (2005) Real-time quantification of microRNAs by stem-loop RT-PCR, Nucleic Acids Res, 33, e179.
11. Bandres E et al, (2006) Identification by Real-time PCR of 13 mature microRNAs differentially expressed in colorectal cancer and non-tumoral tissues, Molecular Cancer, 5, 29.
12. Cummins JM et al, (2006) The colorectal microRNAome, PNAS, USA, 103, 3687-3692.
13. Hayashita Y et al, (2006) A polycistronic microRNA cluster, miR-17-92, is overexpressed in human lung cancers and enhances cell proliferation, Cancer Res, 65, 9628-9632.
14. Iorio MV et al, (2006) MicroRNA gene expression deregulation in human breast cancer, Cancer Res, 65, 7065-7070.
Claims (18)
- 細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106a、並びに、miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の変動を測定することから成る、膀胱癌の検出方法。
- 細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106aから成る群より選択された少なくとも一つのmiRNAの発現量の亢進を測定することから成る、膀胱癌の検出方法。
- miRNAの発現量が正常組織由来の細胞に比べて2倍以上亢進していることを膀胱癌の判定基準とする、請求項1記載の検出方法。
- miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の低下を測定することから成る、膀胱癌の検出方法。
- miR-145, miR-30a-3p 及びmiR-133b から成る群より選択された少なくとも一つのmiRNAの発現量の低下を測定することから成る、膀胱癌の検出方法。
- miRNAの発現量が正常組織由来の細胞に比べて2分の1以下に低下していることを膀胱癌の判定基準とする、請求項4又は5記載の検出方法。
- 請求項1に記載の各miRNAに特異的にハイブリダイズするプライマーを用いてmiRNAの発現量を測定する、請求項1〜6のいずれか一項に記載の検出方法。
- リアルタイムPCRによりmiRNAの発現量を測定する、請求7記載の検出方法。
- 細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106a、並びに、miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の変動に基づく、膀胱癌の治療又は予防に有効な物質のスクリーニング方法。
- 細胞中のmiR-96, miR-190, miR-183, miR-130b, miR-124b, miR-215, miR-224及びmiR-106aから成る群より選択された少なくとも一つのmiRNAの発現量の亢進に基づく、膀胱癌の治療又は予防に有効な物質のスクリーニング方法。
- 請求10記載のスクリーニング方法であって、
(a) 被検物質の存在下に細胞を培養する工程、
(b)該細胞における各miRNAの発現量を測定する工程、及び
(c)発現量の亢進を抑制するか又は発現量を減少させる物質を選択する工程、を含む方法。 - miR-145, miR-30a-3p, miR-100, miR-150, miR-133a, miR-320, miR-133b, miR-151, miR-195, miR-125b, miR-152, miR-218, miR-199-s, miR-199a, miR-199a*, miR-223, miR-139, miR-9及び miR-140から成る群より選択された少なくとも一つのmiRNAの発現量の低下に基づく、膀胱癌の治療又は予防に有効な物質のスクリーニング方法。
- miR-145, miR-30a-3p 及びmiR-133b から成る群より選択された少なくとも一つのmiRNAの発現量の低下に基づく、膀胱癌の治療又は予防に有効な物質のスクリーニング方法。
- 請求12又は13記載のスクリーニング方法であって、
(a) 被検物質の存在下に細胞を培養する工程、
(b)該細胞における各miRNAの発現量を測定する工程、及び
(c)発現量の低下を抑制するか又は発現量を増加させる物質を選択する工程、を含む方法。 - 請求項1に記載の各miRNAに特異的にハイブリダイズするプライマーを用いてmiRNAの発現量を測定する、請求項9〜14のいずれか一項に記載のスクリーニング方法。
- リアルタイムPCRによりmiRNAの発現量を測定する、請求15記載のスクリーニング方法。
- 請求項9〜16のいずれか一項に記載のスクリーニング方法に用いるスクリーニングキット。
- 請求項1に記載の各miRNAに特異的にハイブリダイズするプライマーの少なくとも一つを有する、請求項17記載のスクリーニングキット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007276191A JP2009100687A (ja) | 2007-10-24 | 2007-10-24 | microRNA発現プロファイリングに基づく膀胱癌の検出方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007276191A JP2009100687A (ja) | 2007-10-24 | 2007-10-24 | microRNA発現プロファイリングに基づく膀胱癌の検出方法 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012287861A Division JP5704575B2 (ja) | 2012-12-28 | 2012-12-28 | microRNA発現プロファイリングに基づく膀胱癌の検出方法 |
| JP2012287862A Division JP5704576B2 (ja) | 2012-12-28 | 2012-12-28 | microRNA発現プロファイリングに基づく膀胱癌の検出方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009100687A true JP2009100687A (ja) | 2009-05-14 |
| JP2009100687A5 JP2009100687A5 (ja) | 2011-02-24 |
Family
ID=40703169
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007276191A Abandoned JP2009100687A (ja) | 2007-10-24 | 2007-10-24 | microRNA発現プロファイリングに基づく膀胱癌の検出方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2009100687A (ja) |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009143379A2 (en) * | 2008-05-21 | 2009-11-26 | Fred Hutchinson Cancer Research Center | Use of extracellular rna to measure disease |
| WO2011001906A1 (ja) | 2009-06-30 | 2011-01-06 | 富士レビオ株式会社 | 培養細胞の評価方法およびバイオマーカーのスクリーニング方法 |
| JP2011036242A (ja) * | 2009-07-16 | 2011-02-24 | Chiba Univ | miRNA発現プロファイリングに基づく尿路上皮癌の検出方法 |
| WO2012121178A1 (ja) * | 2011-03-04 | 2012-09-13 | 独立行政法人国立がん研究センター | 腫瘍血管形成阻害剤 |
| JP2013000067A (ja) * | 2011-06-17 | 2013-01-07 | Toray Ind Inc | 膀胱ガン診断用組成物及び方法 |
| CN102031254B (zh) * | 2009-09-27 | 2014-04-02 | 苏州吉玛基因股份有限公司 | 人miR-150反义核酸及其应用 |
| WO2015020122A1 (ja) * | 2013-08-08 | 2015-02-12 | 国立大学法人 大阪大学 | 尿路上皮癌の診断または治療剤 |
| JPWO2013038737A1 (ja) * | 2011-09-16 | 2015-03-23 | Lsipファンド運営合同会社 | 膀胱癌細胞の検出方法、膀胱癌細胞の検出方法に用いるプライマー及び膀胱癌マーカ |
| US9006201B2 (en) | 2010-07-08 | 2015-04-14 | Takeda Pharmaceutical Company Limited | Prophylactic or therapeutic agent for diabetes |
| CN105999269A (zh) * | 2016-05-05 | 2016-10-12 | 温州医科大学 | miR-411作为膀胱癌的靶标及其应用 |
| WO2019208671A1 (ja) * | 2018-04-25 | 2019-10-31 | 東レ株式会社 | 膀胱がんの検出のためのキット、デバイス及び方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005118806A2 (en) * | 2004-05-28 | 2005-12-15 | Ambion, Inc. | METHODS AND COMPOSITIONS INVOLVING MicroRNA |
| WO2006128245A1 (en) * | 2005-06-03 | 2006-12-07 | Southern Adelaide Health Service-Flinders Medical Centre | Targeting cells with altered microrna expression |
-
2007
- 2007-10-24 JP JP2007276191A patent/JP2009100687A/ja not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005118806A2 (en) * | 2004-05-28 | 2005-12-15 | Ambion, Inc. | METHODS AND COMPOSITIONS INVOLVING MicroRNA |
| JP2008500837A (ja) * | 2004-05-28 | 2008-01-17 | アンビオン インコーポレーティッド | マイクロrnaに関与する方法および組成物 |
| WO2006128245A1 (en) * | 2005-06-03 | 2006-12-07 | Southern Adelaide Health Service-Flinders Medical Centre | Targeting cells with altered microrna expression |
Non-Patent Citations (3)
| Title |
|---|
| JPN6012054374; Annual meeting. Proceedings of the American Association for Cancer Research, 48(Apr. 2007) p.423(#17 * |
| JPN6012054375; Urol. Oncol., 25[5](Sep. 2007) p.387-392 * |
| JPN6012054376; British J. Cancer, 95(2006) p.1415-1418 * |
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009143379A3 (en) * | 2008-05-21 | 2010-02-25 | Fred Hutchinson Cancer Research Center | Use of extracellular rna to measure disease |
| WO2009143379A2 (en) * | 2008-05-21 | 2009-11-26 | Fred Hutchinson Cancer Research Center | Use of extracellular rna to measure disease |
| EP2644706A2 (en) | 2009-06-30 | 2013-10-02 | Fujirebio Inc. | Method for evaluation of cultured cells, and method for screening of biomarker |
| WO2011001906A1 (ja) | 2009-06-30 | 2011-01-06 | 富士レビオ株式会社 | 培養細胞の評価方法およびバイオマーカーのスクリーニング方法 |
| JP2011036242A (ja) * | 2009-07-16 | 2011-02-24 | Chiba Univ | miRNA発現プロファイリングに基づく尿路上皮癌の検出方法 |
| CN102031254B (zh) * | 2009-09-27 | 2014-04-02 | 苏州吉玛基因股份有限公司 | 人miR-150反义核酸及其应用 |
| US9006201B2 (en) | 2010-07-08 | 2015-04-14 | Takeda Pharmaceutical Company Limited | Prophylactic or therapeutic agent for diabetes |
| WO2012121178A1 (ja) * | 2011-03-04 | 2012-09-13 | 独立行政法人国立がん研究センター | 腫瘍血管形成阻害剤 |
| JP2013000067A (ja) * | 2011-06-17 | 2013-01-07 | Toray Ind Inc | 膀胱ガン診断用組成物及び方法 |
| JPWO2013038737A1 (ja) * | 2011-09-16 | 2015-03-23 | Lsipファンド運営合同会社 | 膀胱癌細胞の検出方法、膀胱癌細胞の検出方法に用いるプライマー及び膀胱癌マーカ |
| EP2757154A4 (en) * | 2011-09-16 | 2015-10-14 | Lsip Llc | METHOD FOR DETECTING BLOOD TUMOR CELLS, PRIMER FOR USE IN THIS METHOD FOR DETECTING BLOOD TUMOR CELLS AND BLADDER CANCER MARKERS |
| WO2015020122A1 (ja) * | 2013-08-08 | 2015-02-12 | 国立大学法人 大阪大学 | 尿路上皮癌の診断または治療剤 |
| JPWO2015020122A1 (ja) * | 2013-08-08 | 2017-03-02 | 国立大学法人大阪大学 | 尿路上皮癌の診断または治療剤 |
| CN105999269A (zh) * | 2016-05-05 | 2016-10-12 | 温州医科大学 | miR-411作为膀胱癌的靶标及其应用 |
| WO2019208671A1 (ja) * | 2018-04-25 | 2019-10-31 | 東レ株式会社 | 膀胱がんの検出のためのキット、デバイス及び方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Deb et al. | miRNAs and ovarian cancer: An overview | |
| Wu et al. | Expression profile of mammalian microRNAs in endometrioid adenocarcinoma | |
| Veerla et al. | MiRNA expression in urothelial carcinomas: important roles of miR‐10a, miR‐222, miR‐125b, miR‐7 and miR‐452 for tumor stage and metastasis, and frequent homozygous losses of miR‐31 | |
| JP2009100687A (ja) | microRNA発現プロファイリングに基づく膀胱癌の検出方法 | |
| Heneghan et al. | MicroRNAs as novel biomarkers for breast cancer | |
| Ramdas et al. | miRNA expression profiles in head and neck squamous cell carcinoma and adjacent normal tissue | |
| Porkka et al. | MicroRNA expression profiling in prostate cancer | |
| Muralidhar et al. | Global microRNA profiles in cervical squamous cell carcinoma depend on Drosha expression levels | |
| Tatarano et al. | miR-218 on the genomic loss region of chromosome 4p15. 31 functions as a tumor suppressor in bladder cancer | |
| Li et al. | miR-128 and its target genes in tumorigenesis and metastasis | |
| Mattie et al. | Optimized high-throughput microRNA expression profiling provides novel biomarker assessment of clinical prostate and breast cancer biopsies | |
| Mezzanzanica et al. | Role of microRNAs in ovarian cancer pathogenesis and potential clinical implications | |
| Schaefer et al. | MicroRNAs and cancer: current state and future perspectives in urologic oncology | |
| Vaz et al. | Analysis of microRNA transcriptome by deep sequencing of small RNA libraries of peripheral blood | |
| Maire et al. | Analysis of miRNA-gene expression-genomic profiles reveals complex mechanisms of microRNA deregulation in osteosarcoma | |
| White et al. | MicroRNAs and their potential for translation in prostate cancer | |
| Min et al. | Association of the miR‐146aC> G, 149C> T, 196a2C> T, and 499A> G polymorphisms with colorectal cancer in the Korean population | |
| Nugent et al. | MicroRNAs in colorectal cancer: function, dysregulation and potential as novel biomarkers | |
| Romero-Cordoba et al. | Identification and pathway analysis of microRNAs with no previous involvement in breast cancer | |
| George et al. | MicroRNAs: Potential biomarkers in cancer | |
| Leonardi et al. | microRNAs and thyroid cancer: Biological and clinical significance | |
| US10208353B2 (en) | Biomarkers useful for detection of types, grades and stages of human breast cancer | |
| WO2008125883A1 (en) | Cancer markers for prognosis and screening of anti-cancer agents | |
| Mehterov et al. | A novel panel of clinically relevant miRNAs signature accurately differentiates oral cancer from normal mucosa | |
| EP2283161A2 (en) | Methods for assessing colorectal cancer and compositions for use therein |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101021 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101021 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101201 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121106 |
|
| A762 | Written abandonment of application |
Free format text: JAPANESE INTERMEDIATE CODE: A762 Effective date: 20130121 |