JP2008533005A - 生物学的活性物質の皮内的、経皮的又は経粘膜的送達のための方法 - Google Patents
生物学的活性物質の皮内的、経皮的又は経粘膜的送達のための方法 Download PDFInfo
- Publication number
- JP2008533005A JP2008533005A JP2008500660A JP2008500660A JP2008533005A JP 2008533005 A JP2008533005 A JP 2008533005A JP 2008500660 A JP2008500660 A JP 2008500660A JP 2008500660 A JP2008500660 A JP 2008500660A JP 2008533005 A JP2008533005 A JP 2008533005A
- Authority
- JP
- Japan
- Prior art keywords
- limiting examples
- acid
- biologically active
- water
- isotopologue
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0021—Intradermal administration, e.g. through microneedle arrays, needleless injectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/006—Oral mucosa, e.g. mucoadhesive forms, sublingual droplets; Buccal patches or films; Buccal sprays
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Dermatology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
本発明は、生物学的活性物質をそれを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための方法であって、前記方法は有効量の吸収増強剤を前記生物学的活性物質といっしょに前記哺乳類に共に投与するステップを含み、前記吸収増強剤は約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水である方法に関する。前記生物学的活性物質は、薬剤、生理活性ペプチド、生理活性タンパク質、糖タンパク質、核酸、栄養素、ビタミン及びミネラルからなる群から選択される。
【選択図】なし
【選択図】なし
Description
本発明は、ヒト又は動物の保健衛生に関する。具体的には本発明は、生物活性物質を、それを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための方法に関する。
経皮的又は経粘膜的送達は、注射による方法と経腸的な方法との両方より優れた複数の利点を提供する生物学的活性物質の全身への送達の代替方法である。口腔粘膜又は皮膚を通じて吸収される生物学的活性物質は、胃腸管と、肝臓での初回通過代謝とを経由せずに直接体循環に入る。これは、前記静脈内経路よりもより快適かつ簡便な送達径路を介して迅速な作用の開始をもたらす。しかし生物学的活性物質の経皮的又は経粘膜的送達は、前記物質の吸収を低下させる皮膚及び粘膜の障壁機能により限定的である。特に前記粘膜及び皮膚は、ペプチド、タンパク質及び核酸のような高分子量を有する親水性物質の透過に対する障壁となる。
前記皮膚の深層の中への生物学的活性物質の皮内的送達は、皮膚の障壁機能により制限されることが多い。したがって生物学的活性物質は、皮膚疾患を治療するのに有効なことは証明されているが、前記皮膚の中へ部分的にしか透過しないことによりその効果は制限される。特に皮膚の外層は、ペプチド、タンパク質及び核酸のような高分子量を有する親水性物質の透過に対する障壁となる。
したがって生物学的活性物質を、それを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための有効かつ安全な方法に対する多大なる必要性がある。
活性な薬品の皮内的、経皮的又は経粘膜的送達を増強するための方法は、当業者に知られている。あるアプローチでは吸収促進剤(promoters of absorption)(吸収増強剤(absorption enhancers))は、前記活性な薬品を含む処方に含まれる(非特許文献1及び2)。界面活性剤であるホスファチジルコリン及びグリココール酸ナトリウムは、吸収促進剤の例である。しかしこれらの界面活性剤の添加は、前記障壁組織を損傷させる代わりに透過性の穏やかな向上をわずかにもたらすにすぎない。
Zatz,J.L.,Modification of Skin Permeation by Surface−Active Agents in Skin Permeation Fundamentals and Application,149−162(1993) Barry,B.W.,"Properties That Influence Percutaneous Absorption in Dermatological Formulations,"Percutaneous Absorption,127−233(1983)
Zatz,J.L.,Modification of Skin Permeation by Surface−Active Agents in Skin Permeation Fundamentals and Application,149−162(1993) Barry,B.W.,"Properties That Influence Percutaneous Absorption in Dermatological Formulations,"Percutaneous Absorption,127−233(1983)
したがって特に親水性の生物学的活性物質を、それを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための有効かつ安全な吸収増強剤に対する多大なる必要性がある。
天然水は、(1H及び2Hという)水素及び(16O、17O、18Oという)酸素の安定同位体により形成される(1H2 16O、1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O、2H2 18Oという)9種類の水のアイソトポローグの組成物であり、ここで軽水アイソトポローグ1H2 16Oのレベルは約99.7317%(ウィーン標準平均海水、VSMOW)であり、少なくとも1個の重同位体2H、17O及び18Oを含む8種類全ての重アイソトポローグの総レベルは約0.2683%(例えば1H2 18O 0.199983%、1H2 17O 0.0372%、1H2H16O 0.031069%、1H2H18O 0.0000623%及び1H2H17O 0.0000116%)である(特許文献3及び4)。天然水中の水のアイソトポローグの量は、地球上の地域(Earth regions)と気象条件とによって少しずつ変化し、典型的には前記国際VSMOW標準に対する偏差δとして表現される。主要な軽水アイソトポローグ1H2 16Oが最高に濃縮された天然水は南極で発見され(Standard Light Antarctic Precipitation、SLAP)、前記天然水中では残りの重同位体のδ値は、99.757%の軽水アイソトポローグ1H2 16Oレベルに相当するδ2H=−415.5‰、δ17O=−28.1‰、及び、δ18O=−53.9‰である(非特許文献5)。したがって軽水アイソトポローグ1H2 16Oの量が99.757%を超える水は、自然界には見出されない。
Rothman et al.、J.Quant.Spectrosc.Radiat.Transfer,1998,60,665. Rothman et al.,J.Quant.Spectrosc.Radiat.Transfer,2003,82,p.9 R.van Trigt,Laser Spectrometry for Stable Isotope Analysis of Water Biomedical and Paleoclimatological Applications,2002,Groningen:University Library Groningen,p.50
Rothman et al.、J.Quant.Spectrosc.Radiat.Transfer,1998,60,665. Rothman et al.,J.Quant.Spectrosc.Radiat.Transfer,2003,82,p.9 R.van Trigt,Laser Spectrometry for Stable Isotope Analysis of Water Biomedical and Paleoclimatological Applications,2002,Groningen:University Library Groningen,p.50
水中ではこれらのジューテリウムを含むアイソトポローグの総レベルは0.031%に満たないので、天然水からジューテリウムを含むアイソトポローグ(1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18O)を完全に除去することは、99.76%を超えないレベルまで軽水アイソトポローグ1H2 16Oが濃縮された水を提供するのみである。したがって99.76%を超える軽水アイソトポローグ1H2 16Oを含有する水は、重アイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oを天然水から除去することを可能にする方法により、工業規模で調製される場合がある。
思いがけず我々は、(99.760%から99.999%までという)自然界では知られていないレベルにまで軽水アイソトポローグ1H2 16Oが濃縮された水が、(99.710%から99.757%までという)天然のレベルの軽水アイソトポローグ1H2 16Oを有する水と比較して、生物学的活性物質の皮膚及び粘膜の中への吸収と、皮膚及び粘膜を通り抜ける吸収とを増大させることを発見した。
生物学的活性物質をそれを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための方法であって、前記方法は有効量の吸収増強剤を前記生物学的活性物質といっしょに前記哺乳類に共に投与する(co−administering)ステップを含み、前記吸収増強剤は約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水である方法を提供することが、本発明の目的である。
発明の開示
本発明は、生物学的活性物質をそれを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための方法であって、前記方法は有効量の吸収増強剤を前記生物学的活性物質といっしょに前記哺乳類に共に投与するステップを含み、前記吸収増強剤は約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水である方法を提供する。
本発明は、生物学的活性物質をそれを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための方法であって、前記方法は有効量の吸収増強剤を前記生物学的活性物質といっしょに前記哺乳類に共に投与するステップを含み、前記吸収増強剤は約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水である方法を提供する。
図面の簡単な説明
図1は、約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水の製造装置の側面模式図である。
図1は、約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水の製造装置の側面模式図である。
本明細書で用いられるところの「アイソトポローグ」という用語は、IUPAC Compendium of Chemical Terminology 2nd Edition(1997)に従い、例えば1H2 16O、1H2H16O及び1H2 18Oのような同位体組成(同位体置換の数)のみが異なる分子を指す。
本明細書において「軽水」という用語は、約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水を指す。特定の重アイソトポローグの相対量は本発明の水の調製方法によって変化する場合があるが、重同位体により形成される残りの重アイソトポローグの合計は、0.001%ないし0.240%を超えない。したがって本発明の水における重同位体の残量は、2Hについては0.01ppmから155ppmまで、17Oについては1ppmないし360ppmと、18Oについては1ppmないし2000ppmと変化する場合があるが、これらの残りの重同位体により形成される重アイソトポローグの合計は、0.001%ないし0.240%を超えない。
本明細書で用いられるところの「皮内的」という用語は、本発明の方法において、生物学的活性物質を皮膚の深層へ送達させその結果所望の治療効果を得る目的で、前記物質の治療上の有効量が哺乳類の皮膚に塗布されることを意味する。
本明細書で用いられるところの「経皮的」という用語は、本発明の方法において、生物学的活性物質を体循環へ送達させその結果所望の治療効果を得る目的で、前記物質の治療上の有効量が哺乳類の皮膚に塗布されることを意味する。
本明細書で用いられるところの「経粘膜的」という用語は、本発明の方法において、生物学的活性物質を体循環へ送達させその結果所望の治療効果を得る目的で、前記物質の治療上の有効量が哺乳類の粘膜に塗布されることを意味する。前記粘膜は、鼻腔粘膜、(例えば頬側粘膜又は舌下粘膜のような)口腔粘膜、胃腸粘膜、直腸粘膜又は膣粘膜であるがこれらに限定されない。
本明細書で用いられるところの「吸収増強剤」という用語は、物質の皮膚又は粘膜の中への透過か、皮膚又は粘膜を通り抜ける透過かを増強する薬品を意味する。
本発明の方法では前記生物学的活性物質は、薬剤、生理活性ペプチド、生理活性タンパク質、糖タンパク質、核酸、栄養素、ビタミン及びミネラルからなる群から選択される。
好ましくは前記薬剤は、鎮痛剤と、麻酔剤と、にきび防止剤と、老化防止剤と、抗アレルギー剤と、脱毛症治療薬と、抗貧血剤と、狭心症治療薬と、抗不安薬と、抗不整脈剤と、抗喘息剤と、抗菌剤と、抗癌剤と、抗コリン剤と、抗凝固剤と、抗痙攣剤と、抗うつ剤と、糖尿病治療薬と、下痢止め剤と、抗利尿剤と、解毒剤と、運動障害治療薬と、月経困難症治療薬と、制吐剤と、抗線溶剤と、抗線維化剤と、抗真菌剤と、緑内障治療薬と、抗出血剤と、抗ヒスタミン剤と、高カルシウム血症治療薬と、高血糖治療薬と、高脂血症治療薬と、降圧剤と、甲状腺機能亢進症治療薬と、尿酸降下剤と、低カルシウム血症治療薬と、低血糖治療薬と、低血圧治療薬と、抗炎症剤と、川崎病治療薬と、マラリア治療薬と、メトヘモグロビン血症治療薬と、抗片頭痛剤と、筋無力症治療薬と、抗腫瘍剤と、抗神経痛剤と、好中球減少症治療薬と、抗パニック剤と、多発性神経障害治療薬と、抗原虫剤と、乾癬治療薬と、統合失調症治療薬と、解熱剤と、抗リウマチ剤と、抗脂漏剤と、鎮痙剤と、抗血栓剤と、抗振戦剤と、潰瘍治療薬と、眩暈治療薬(antivertiligo agents)と、抗ウイルス剤と、しわ防止剤と、食欲増進剤と、食欲抑制剤と、喘息予防剤と、骨吸収抑制剤と、気管支拡張剤と、避妊薬と、副腎皮質ステロイド剤と、脱色剤と、利尿剤と、エストロゲンと、毛髪増殖促進剤と、毛髪増殖阻害剤と、造血刺激剤(hemapoietic stimulants)と、肝炎治療薬と、ヒスタミンH2受容体アンタゴニストと、ホルモンと、保湿剤と、免疫抑制剤と、インポテンス治療薬と、インシュリン耐性治療薬と、インターフェロン耐性治療薬と、角質溶解剤と、縮瞳薬と、粘液溶解剤と、散瞳薬と、心筋梗塞の治療薬又は予防薬と、神経筋遮断薬と、栄養補助剤と、ビタミンと、骨粗しょう症の予防薬又は治療薬と、鎮静剤と、骨格筋弛緩薬と、皮膚軟化剤及び皮膚保湿剤と、皮膚美白剤と、交感神経作動薬と、血栓溶解剤と、ワクチンと、血管拡張剤と、創傷治癒促進剤と、反対刺激剤と、ビタミンと、栄養素と、アミノ酸及びその誘導体と、ミネラルと、ハーブ抽出物と、レチノイドと、ビオフラボノイドと、酸化防止剤とからなる群から選択される。
鎮痛剤の限定的でない実施例は、アセトアミノフェンか、重酒石酸ヒドロコドンか、コデインか、カフェインか、アセチルサリチル酸か、ジクロフェナクか、これらの混合物かを含む。
麻酔剤の限定的でない実施例は、リドカイン、テトラカイン及びエピネフリンを含む。
にきび防止剤の限定的でない実施例は、エリスロマイシン、テトラサイクリン、過酸化ベンゾイル、ニコチンアミド、レゾルシノール、ドキシサイクリン及びサリチル酸を含む。
老化防止剤の限定的でない実施例は、ケイ皮酸オクチルメチル及びその誘導体のような日焼け止めと、レチノイドと、ビタミンC、ビタミンB及びこれらの誘導体のようなビタミンと、グリコール酸、クエン酸、乳酸、リンゴ酸、コハク酸、マンデル酸、アスコルビン酸、アルファ−ヒドロキシ酪酸、アルファ−ヒドロキシイソ酪酸、アルファ−ヒドロキシイソカプロン酸、アトロラクチン酸、アルファ−ヒドロキシイソ吉草酸、ピルビン酸エチル、ガラクツロン酸、グルコヘプトン酸(glucopehtonic acid)、グルコヘプトノ1,4−ラクトン(glucopheptono 1,4−lactone)、グルコン酸、グルコノラクトン、グルクロン酸、グルクロノラクトン、グリコール酸、ピルビン酸イソプロピル、ピルビン酸メチル、粘液酸、ピルビン酸、糖酸(saccharic acid)、糖酸1,4−ラクトン(saccaric acid 1,4−lactone)、酒石酸及びタルトロン酸のようなアルファヒドロキシ酸を含む酸化防止剤と、ベータ−ヒドロキシ酪酸、ベータ−フェニル−乳酸、ベータ−フェニルピルビン酸のようなベータヒドロキシ酸と、緑茶、大豆、マリアアザミ、藻類、アロエ、アンゼリカ、ダイダイ、コーヒー、黄蓮、グレープフルーツ、ヘレン(hoellen)、スイカズラ(honeysuckle)、ジュズダマ、ムラサキ(lithospermum)、桑、シャクヤク、クズ(puerarua)、米、ベニバナのような植物抽出物と、これらの混合物とを含む。
抗貧血剤の限定的でない実施例は、シアノコバラミン、エポエチン、フマル酸第一鉄、硫酸第一鉄、クエン酸第一鉄及び鉄デキストランを含む。
狭心症治療薬の限定的でない実施例は、アテノロール、一硝酸イソソルビド、ニトログリセリン、プロプラノロール、チモロール、メトプロロール及びベラパミルを含む。
抗不安薬の限定的でない実施例は、アルプラゾラム、ブロマゼパム、ロラゼパム及びジアゼパムを含む。
抗不整脈剤の限定的でない実施例は、アセブトロール、アテノロール、アトロピン及びメトプロロールを含む。
抗喘息剤の限定的でない実施例は、デキサメタゾン及びロラタジンを含む。
抗菌剤の限定的でない実施例は、アミノサリチル酸、イソニアジド(isoniazide)、エリスロマイシン、ゲンタマイシン、シプロフロキサシン、アモキシシリン、セファキセリン(cephaxelin)及びストレプトマイシンを含む。
抗癌剤の限定的でない実施例はダウノルビシンを含む。
抗コリン剤の限定的でない実施例はアトロピンを含む。
抗凝固剤の限定的でない実施例は、ヘパリン、ワルファリン及びジクマロールを含む。
抗痙攣剤の限定的でない実施例は、クロナゼパム、ジアゼパム及びバルプロ酸を含む。
抗うつ剤の限定的でない実施例は、アミトリプチリン及びフルオキセチンを含む。
糖尿病治療薬の限定的でない実施例は、インシュリンと、メトホルミンと、コハク酸と、グリブリドのようなスルホニル尿素とを含む。
下痢止め剤の限定的でない実施例は、コデイン及び次サリチル酸ビスマスを含む。
抗利尿剤の限定的でない実施例はバソプレッシンを含む。
解毒剤の限定的でない実施例は、カルシウムチャネル遮断薬に対するグルカゴンと、重金属に対するペニシラミンとを含む。
運動障害治療薬の限定的でない実施例はレボドパを含む。
月経困難症治療薬の限定的でない実施例はジクロフェナクを含む。
制吐剤の限定的でない実施例はクロルプロマジンを含む。
抗線溶剤の限定的でない実施例はアミノカプロン酸を含む。
抗線維化剤の限定的でない実施例はアミノ安息香酸カリウムを含む。
抗真菌剤の限定的でない実施例はケトコナゾールを含む。
緑内障治療薬の限定的でない実施例は、カルバコール及びピロカルピンを含む。
抗出血剤の限定的でない実施例は、第IX因子及びアミノカプロン酸を含む。
抗ヒスタミン剤の限定的でない実施例は、塩酸ラニチジン及びロラタジンを含む。
高カルシウム血症治療薬の限定的でない実施例は、カルシトニンと、エチドロネートと、他のビスホスホネートとを含む。
高血糖治療薬の限定的でない実施例はメトホルミンを含む。
高脂血症治療薬の限定的でない実施例は、クロフィブラート及びフルバスタチンを含む。
降圧剤の限定的でない実施例は、アテノロール、カプトプリル、リシノプリル及びベラパミルを含む。
甲状腺機能亢進症治療薬の限定的でない実施例はヨウ化カリウムを含む。
尿酸降下剤の限定的でない実施例はアロプリノールを含む。
低カルシウム血症治療薬の限定的でない実施例は酢酸カルシウムを含む。
低血糖治療薬の限定的でない実施例はグルカゴンを含む。
低血圧治療薬の限定的でない実施例はジヒドロエルゴタミンを含む。
抗炎症剤の限定的でない実施例は、アセチルサリチル酸、サリチル酸コリン、イブプロフェン、ジクロフェナク、インドメタシン及びデキサメタゾンを含む。
川崎病治療薬の限定的でない実施例は免疫グロブリンを含む。
マラリア治療薬の限定的でない実施例はキニジン(quanidine)を含む。
メトヘモグロビン血症治療薬の限定的でない実施例はメチレンブルーを含む。
筋無力症治療薬の限定的でない実施例はネオスチグミン(neostygmine)を含む。
抗腫瘍剤の限定的でない実施例は、アスパラギナーゼ、カルボプラチン、ダウノルビシン、インターフェロン、タモキシフェン及びフルオロウラシルを含む。
抗神経痛剤の限定的でない実施例はカルバマゼピンを含む。
抗パニック剤の限定的でない実施例はクロナゼパムを含む。
多発性神経障害治療薬の限定的でない実施例は免疫グロブリンを含む。
抗原虫剤の限定的でない実施例は、クロロキン及びフラゾリドンを含む。
乾癬治療薬の限定的でない実施例はメトトレキサートを含む。
統合失調症治療薬の限定的でない実施例はカルバマゼピンを含む。
解熱剤の限定的でない実施例はアセトアミノフェンを含む。
抗リウマチ剤の限定的でない実施例はメトトレキサートを含む。
抗脂漏剤の限定的でない実施例は、ピリチオン、サリチル酸を含む。
鎮痙剤の限定的でない実施例はグルカゴンを含む。
抗血栓剤の限定的でない実施例はアセチルサリチル酸を含む。
抗振戦剤の限定的でない実施例はジアゼパムを含む。
潰瘍治療薬の限定的でない実施例はオメプラゾールを含む。
眩暈治療薬の限定的でない実施例はジフェニドール(diphenidol)を含む。
抗ウイルス剤の限定的でない実施例は、アシクロビル及びリバビリンを含む。
食欲増進剤の限定的でない実施例はドロナビノールを含む。
食欲抑制剤の限定的でない実施例はフェンテルミンを含む。
喘息予防剤の限定的でない実施例はテオフィリンを含む。
骨吸収抑制剤の限定的でない実施例はカルシトニンを含む。
気管支拡張剤の限定的でない実施例は、テオフィリン及びアルブテロールを含む。
避妊薬の限定的でない実施例はレボノルゲストレルを含む。
副腎皮質ステロイド剤の限定的でない実施例はデキサメタゾンを含む。
皮膚美白剤の限定的でない実施例は、ヒドロキノンと、カテコール及びその誘導体と、アスコルビン酸及びその誘導体と、これらの混合物とを含む。
反対刺激剤の限定的でない実施例は、カンフルと、メントールと、サリチル酸メチルと、ペパーミント及びチョウジ油と、イクタモール(ichtammol)と、これらの混合物とを含む。
利尿剤の限定的でない実施例は、フロセミド及びヒドロクロロチアジドを含む。
エストロゲンの限定的でない実施例はエストラジオールを含む。
造血刺激剤の限定的でない実施例はエポエチン(epoietin)を含む。
肝炎治療薬の限定的でない実施例はインターフェロンアルファを含む。
ヒスタミンH2受容体アンタゴニストの限定的でない実施例はシメチジンを含む。
ホルモンの限定的でない実施例は、メラトニン、甲状腺ホルモン、チロキシン、トリヨードチロニン、アドレナリン、ノルアドレナリン、(例えばコルチゾールのような)グルココルチコイド、(例えばアルドステロンのような)ミネラルコルチコイド、(例えばエストラジオールのような)エストロゲン、プロゲステロン、(例えばテストステロンのような)アンドロゲン、カルシトリオール及びカルシフェロールを含む。
免疫抑制剤の限定的でない実施例はシクロスポリンを含む。
インポテンス治療薬の限定的でない実施例はパパベリンを含む。
角質溶解剤の限定的でない実施例は過酸化ベンゾイルを含む。
縮瞳薬の限定的でない実施例はカルバコールを含む。
粘液溶解剤の限定的でない実施例はアセチルシステインを含む。
散瞳薬の限定的でない実施例はアトロピンを含む。
心筋梗塞の治療薬又は予防薬の限定的でない実施例はアセチルサリチル酸を含む。
神経筋遮断薬の限定的でない実施例はスクシニルコリンを含む。
栄養補助剤の限定的でない実施例は、乳酸カルシウム、グルコン酸銅、フマル酸第一鉄、塩化マグネシウム、亜セレン酸(selenous acid)、アスコルビン酸、ベータ−カロテン、ビオチン、カルシトリオール、パントテン酸カルシウム、シアノコバラミン、エルゴカルシフェロール、葉酸、ナイアシン、ナイアシンアミド、パントテン酸、ピリドキシン、リボフラビン、アスコルビン酸ナトリウム、リポ酸、イノシトール及びチアミンを含む。
骨粗しょう症の予防薬又は治療薬の限定的でない実施例はエストロゲンを含む。
鎮静剤の限定的でない実施例はジアゼパムを含む。
骨格筋弛緩薬の限定的でない実施例はフェニトインを含む。
血栓溶解剤の限定的でない実施例はウロキナーゼを含む。
血管拡張剤の限定的でない実施例はエナラプリルを含む。
典型的には本発明の薬剤は本発明の方法では、医学文献で詳述されるようにその通常の用量に近い量で、かつ、毎日の投与計画の範囲内で投与される。
好ましくは前記生理活性ペプチド又は生理活性タンパク質は、サイトカインと、ペプチドホルモンと、増殖因子と、心臓循環系に作用する因子と、中枢及び抹消神経系に作用する因子と、体液性電解質に作用する因子と、造血因子と、骨及び骨格に作用する因子と、胃腸系に作用する因子と、免疫系に作用する因子と、生殖器官に作用する因子と、酵素とからなる群から選択される。
サイトカインの限定的でない実施例は、(例えばインターフェロン−アルファ、ベータ及びガンマのような)インターフェロンと、(例えばインターロイキン2から12までのような)インターロイキンとを含む。
タンパク質ホルモン又はペプチドホルモンの限定的でない実施例は、インシュリン、インシュリン様増殖因子−1、成長ホルモン、黄体形成ホルモン放出ホルモン(LH−RH)、副腎皮質刺激ホルモン(ACTH)、アミリン、オキシトシン、アクチビン、アミリン、アンジオテンシン、心房性ナトリウム利尿ペプチド(ANP)、カルシトニン、コレシストキニン(CCK)、繊毛様神経栄養因子(CNTF)、コルチコトロピン放出ホルモン(CRH又はCRF)、エリスロポエチン、卵胞刺激ホルモン(FSH)、ガストリン、ガストリン抑制ペプチド(GIP)、ガストリン放出ペプチド、グレリン、グルカゴン(glucogon)、ゴナドトロピン放出因子(GnRF又はGNRH)、成長ホルモン放出ホルモン(GRF、GRH)、ヒト絨毛性ゴナドトロピン(hCH)、インヒビンA、インヒビンB、レプチン、リポトロピン(LPH)、黄体形成ホルモン(LH)、モチリン、ニューロペプチドY、オキシトシン、膵臓ポリペプチド、副甲状腺ホルモン(PTH)、胎盤性ラクトゲン、プロラクチン(PRL)、プロラクチン遊離阻害因子(PIF)、プロラクチン放出因子(PRF)、PYY3−36、セクレチン、ソマトスタチン(SIF、成長ホルモン放出抑制因子、GIF)、トロンボポエチン、チロトロピン(甲状腺刺激ホルモン、TSH)、チロトロピン放出因子(TRH又はTRF)、血管作用性小腸ペプチド(VIP)、バソプレッシン(抗利尿ホルモン、ADH)及びこれらの組合せを含む。
増殖因子の限定的でない実施例は、神経成長因子(NGF、NGF−2/NT−3)、上皮増殖因子(EGF)、繊維芽細胞増殖因子(FGF)、インシュリン様増殖因子(IGF)、トランスフォーミング増殖因子(TGF)、血小板由来細胞増殖因子(PDGF)、ケラチノサイト増殖因子(TGF)及び肝細胞増殖因子(HGF)を含む。
心臓循環系に作用する因子の限定的でない実施例は、エンドセリン、エンドセリン阻害剤、エンドセリンアンタゴニスト、バソプレッシン、レニン、アンジオテンシンI、アンジオテンシンII、アンジオテンシンIII、アンジオテンシンI阻害剤、アンジオテンシンII受容体アンタゴニスト、心房性ナトリウム利尿ペプチド(ANP)及び抗不整脈ペプチドのような、血圧、動脈硬化等を制御する因子を含む。
中枢及び抹消神経系に作用する因子の限定的でない実施例は、(例えばエンケファリン、エンドルフィン、キョートルフィンのような)オピオイドペプチド、神経栄養因子(NTF)、カルシトニン遺伝子関連ペプチド(CGRP)、甲状腺ホルモン放出ホルモン(TRH)、グリア細胞由来神経栄養因子(GDNF)、脳由来神経栄養因子(BDNF)及び(例えばNT3、NT4のような)ニューロトロフィンを含む。
体液性電解質に作用する因子の限定的でない実施例はカルシトニンを含む。
造血因子の限定的でない実施例は、エリスロポエチンと、顆粒球コロニー刺激因子(G−CSF)と、顆粒球マクロファージ刺激因子(GM−CSF)及びマクロファージコロニー刺激因子(M−CSF)と、トロンボポエチンとを含む。
胃腸系に作用する因子の限定的でない実施例は、セクレチン及びガストリンを含む。
免疫系に作用する因子の限定的でない実施例は、(例えばインターフェロン−アルファ及びガンマのような)インターフェロンと、モノクローナル抗体と、天然に存在するか、化学的に合成されるか、組換え体かの、抗原として作用する場合があるペプチド又はタンパク質とを含む。本発明にしたがう処方中でこれらの因子は、ハプテンに結合された状態で、独立に、又は、アジュバントと一緒に投与される。
骨及び骨格に作用する因子の限定的でない実施例は、副甲状腺ホルモン及びカルシトニンを含む。
生殖器官に作用する因子の限定的でない実施例は、黄体形成ホルモン放出ホルモン(LH−RH)及び黄体形成ホルモンを含む。
酵素の限定的でない実施例は、スーパーオキシドジスムターゼ(SOD)、ウロキナーゼ、アスパラギナーゼ及びカリクレインを含む。
これらのペプチド又はタンパク質は、グリコシル化されたペプチド又はタンパク質と、化学的に修飾されたペプチド又はタンパク質とをさらに含む場合がある。化学的に修飾されたペプチド又はタンパク質の限定的でない実施例は、ポリエチレングリコールのような合成高分子、コンドロイチン、多糖類等のような天然高分子に共有化学結合により連結されたペプチド又はタンパク質と、非ペプチド物質で化学的に修飾されたペプチド又はタンパク質とを含む。上述の非ペプチド物質は、受容体に対するリガンドか、抗体に対する抗原かの場合がある。
さらに前記ペプチド又はタンパク質は、化学的手段か、遺伝子工学技術かにより連結された複数のペプチドの場合がある。
核酸の限定的でない実施例は、プラスミドDNA、RNA及びオリゴヌクレオチドを含む。
典型的には本発明のペプチド、タンパク質又は核酸は本発明の方法では、注射投与形態についての医学文献で詳述されるようにその通常の用量に近い量で、及び、毎日の投与計画の範囲内で投与される。
本発明の方法では前記ペプチド、タンパク質又は核酸は、前記生理活性ペプチド又は生理活性タンパク質の活性に顕著には影響せず、かつ生理学的に許容可能であるpH範囲で投与される。好ましい範囲は約pH2ないしpH10である。より好ましい範囲は約pH3ないしpH9であり、最も望ましい範囲は約pH3.5ないしpH8である。好ましくは本発明の緩衝剤は、グリシン、クエン酸、コハク酸、フマル酸、リンゴ酸又はリン酸緩衝剤を含むがこれらに限定されない。
好ましくは前記栄養素は、炭水化物、タンパク質、脂肪、水、必須脂肪酸、ジカルボン酸及び(例えばアラニン、アルギニン、アスパラギン、アスパラギン酸、システイン、グルタミン、グルタミン酸、グリシン、ヒスチジン、イソロイシン、ロイシン、リジン、メチオニン、フェニルアラニン、プロリン(praline)、セリン、スレオニン、トリプトファン、チロシン、バリン及びこれらの混合物と、これらの誘導体とのような)アミノ酸からなる群から選択される。
好ましくは前記ビタミンは、チアミン、リボフラビン、ナイアシン、パントテン酸塩、ピリドキシン、葉酸、コバラミン、ビオチン、コリン、イノシトール、アスコルビン酸、リポ酸及びカルニチンからなる群から選択される。
好ましくは前記ミネラルは、カルシウム、クロム、コバルト、銅、フッ化物(fluoride)、ゲルマニウム、ヨウ素、鉄、リチウム、マグネシウム、マンガン、モリブデン、リン、カリウム、セレン、ケイ素、ナトリウム、硫黄、バナジウム及び亜鉛からなる群から選択される。
本発明の方法では、任意でない(non−optional)成分が、前記生物学的活性物質と、吸収を促進する量の軽水といっしょに、共に投与される場合がある。前記成分は限定的ではないが、当業者に知られている保存料、香料、着色料及び吸収促進剤を含む。前記吸収促進剤は、医薬品として許容可能ないずれかの促進剤の場合がある。したがって(アセチルサリチル酸塩、サリチル酸コリン、サリチルアミド等のような)サリチル酸ナトリウム及びサリチル酸誘導体と、(例えばグリシン、アラニン、フェニルアラニン、プロリン、ヒドロキシプロリン等のようなモノアミノカルボン酸と、セリン等のようなヒドロキシアミノ酸と、アスパラギン酸、グルタミン酸等のような酸性アミノ酸と、リジン等のような塩基性アミノ酸と、これらのアルカリ金属塩又はアルカリ土類金属塩とのような)アミノ酸及びそれらの塩と、(N−アセチルアラニン、N−アセチルフェニルアラニン、N−アセチルセリン、N−アセチルグリシン、N−アセチルリジン、N−アセチルグルタミン酸、N−アセチルプロリン、N−アセチルヒドロキシプロリン等のような)N−アセチルアミノ酸及び(アルカリ金属塩及びアルカリ土類金属塩のような)それらの塩と、(例えばオレイルリン酸ナトリウム、ラウリルリン酸ナトリウム、ラウリル硫酸ナトリウム、ミリスチル硫酸ナトリウム、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンアルキルエステル等のような)乳化剤として一般的に使用される物質と、カプロン酸、乳酸、リンゴ酸及びクエン酸並びにこれらのアルカリ金属塩と、ピロリドンカルボン酸、アルキルピロリドンカルボン酸エステル、N−アルキルピロリドン及びプロリンアシルエステル等との場合がある。
本発明の方法を実施する際、前記生物学的活性物質と吸収を促進する量の軽水とは、さまざまな単位投与形態で、それを必要とする哺乳類に対して共に投与される場合がある。前記投与形態は、ゲル錠剤、エアロゾル剤、スプレー剤、シロップ剤、滴下剤、坐剤、ローション剤、クリーム剤及び溶液剤を含むがこれらに限定されない。
(例えば舌下スプレー剤、舌下ゲル錠剤又は舌下溶液剤のような)舌下投与形態は前記哺乳類の舌下粘膜に少なくとも10秒間塗布され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば頬側スプレー剤又はゲル錠剤のような)頬側投与形態は前記哺乳類の頬側粘膜に少なくとも10秒間塗布され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えばシロップ剤、ゲル錠剤のような)経口投与形態は経口摂取され、前記生物学的活性物質は前記哺乳類の胃腸粘膜に適用され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば直腸坐剤のような)直腸投与形態は指で肛門の中に挿入され、前記生物学的活性物質は前記哺乳類の直腸粘膜に適用され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば膣坐剤のような)膣内投与形態は指か付属の塗布器かで膣の中に挿入され、前記生物学的活性物質は前記哺乳類の膣粘膜に適用され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば鼻腔用スプレー又は点鼻剤のような)経鼻投与形態は前記哺乳類の鼻腔粘膜に塗布され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば目薬のような)局所的投与形態は、前記哺乳類の目の周囲の粘膜に適用され、この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば皮内ゲル剤のような)局所的投与形態は前記哺乳類の皮膚に塗布され、好ましくは少なくとも約15分間、より好ましくは少なくとも約30分間、さらにより好ましくは少なくとも約1時間、最も好ましくは例えば約12時間までのような少なくとも数時間、前記皮膚の表面で静置される。この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
(例えば経皮ゲル剤のような)局所的投与形態は前記哺乳類の皮膚に塗布され、好ましくは少なくとも約15分間、より好ましくは少なくとも約30分間、さらにより好ましくは少なくとも約1時間、最も好ましくは例えば約12時間までのような少なくとも数時間、前記皮膚の表面で静置される。この方法は1日当たり1回から約5回まで、好ましくは1回から3回まで繰り返し適用される場合がある。
本発明の方法を実施する際、前記生物学的活性物質は、前記物質の軽水溶液を含む浴槽にそれを必要とする哺乳類の身体を少なくとも約15分間置くことにより、前記哺乳類に対して投与される場合がある。
本発明の方法を実施する際、軽水の有効量は0.00001kgから100kgまでであり、前記生物学的活性物質を投与する特定の方法により異なる。ある好ましい実施態様では、前記生物学的活性物質が単位投与形態で投与される場合には、軽水の有効量は0.00001kgから0.01kgまでである。別の好ましい実施態様では、前記生物学的活性物質の軽水溶液が満たされた浴槽中に身体が置かれる哺乳類に対して前記生物学的活性物質が投与される場合には、軽水の有効量は1kgから100kgまでである。好ましくは前記哺乳類はヒトである。
本発明の方法を実施する際、前記生物学的活性物質と吸収を促進する量の軽水とは、
前記物質の皮膚又は粘膜の中への能動拡散か、皮膚又は粘膜を通り抜ける能動拡散かを提供する物理的工程を使用してそれを必要とする哺乳類に対して共に投与される場合がある。前記物理的工程は、ソノフォレシスと、イオントフォレシスと、マイクロポレーションと、加熱と、気体による加圧とを含むがこれらに限定されない。
前記物質の皮膚又は粘膜の中への能動拡散か、皮膚又は粘膜を通り抜ける能動拡散かを提供する物理的工程を使用してそれを必要とする哺乳類に対して共に投与される場合がある。前記物理的工程は、ソノフォレシスと、イオントフォレシスと、マイクロポレーションと、加熱と、気体による加圧とを含むがこれらに限定されない。
以下の実施例は、本発明を実証するために提示される。実施例は例示を目的とするものであって、本発明の範囲を限定することは決して意図されない。
本実施例は、軽水の製造方法を示す。
99.99%の軽アイソトポローグ1H2 16Oを含む軽水は、図1に記載の装置を温度60°C及び圧力0.2バール下で使用する、99.73%の軽アイソトポローグ1H2 16Oを含む天然水の高度に有効な蒸留により調製される。前記蒸留工程は、水蒸気を製造するための煮沸手段1中で99.73%(C1)の軽アイソトポローグ1H2 16Oを含む天然水を蒸発させるステップと、蒸留塔3の底部2へ前記水蒸気を供給するステップと、前記蒸留塔の軸の方向に沿う主な流れの向きに沿って、前記蒸留塔の内側の(例えば構造化又はランダム充填された)接触デバイス4の表面上で下降する液体と上昇する蒸気とが相互に反対向きへ流れるときに、主に前記接触デバイスの表面で前記液体及び前記蒸気の間での気液接触を行うステップと、蒸留塔3の最上部に設置されるコンデンサー5で軽アイソトポローグ1H2 16Oの濃度が99.99%(C2)の水蒸気を凝結させるステップと、製薬用軽水の製造に適する99.99%の軽アイソトポローグ1H2 16O(C2>C1)を含む凝結した原軽水として凝結物の一部を収集するステップとを含む。その後前記原軽水は、濾過、消毒、脱イオン化及び超濾過の方法により引き続き処理される。その結果として得られる、99.99%の軽アイソトポローグ1H2 16Oを含む水は、本発明の方法で使用される場合がある。
本実施例は、経皮的送達の方法を示す。
材料 メトヘモグロビン血症治療薬であるメチレンブルー(MB)が使用された。
処理 水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)で調製された(マウス1匹当たりの量である100μgのメチレンブルーを含む100μLの)メチレンブルー溶液は、C57BLマウスの皮膚の(約1cm2の)脱毛された領域に局所的に投与された。血漿中のメチレンブルーレベルは、前記投与後10分の時点で測定された。データは、対照に対する百分率で示した血漿中のメチレンブルーレベルの平均値±標準偏差(n=5)として表1に表される。
表1は、軽水が水に比較して経皮的送達の吸収促進剤としてはるかに効果的であることを示す。
本実施例は、経粘膜的送達の方法を示す。
材料 ヒト組換えインターフェロン−アルファ(IFN)が使用された。
処理 体重が約20gのオスのC57BLマウスは、クエン酸緩衝液でpH5.4−5.5とした、水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)で調製されたマウス1匹当たり20μLの溶液という形態のマウス1匹当たり170ngのIFNで舌下を処理された。血漿中のIFNレベルは、7分の時点で、ヒトIFNに特異的な免疫酵素アッセイにより測定された。データは、血漿中のIFNの平均値±標準偏差(n=6)としてng/mLの単位で表2に表される。
本実施例は、経皮的送達の方法を示す。
材料 ヒト組換えインターフェロン−アルファ(IFN)が使用された。
処理 体重が約20gのオスのC57BLマウスは、実験の72時間前に脱毛された。コハク酸緩衝液でpH5.1とした、水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)で調製されたマウス1匹当たり100μLの溶液という形態で、マウス1匹当たり100ngのIFNが、皮膚の脱毛された領域約1cm2に塗布された。血漿中のIFNレベルは、10分の時点で、ヒトIFNに特異的な免疫酵素アッセイにより測定された。データは、血漿中のIFNの平均値±標準偏差(n=5)としてng/mLの単位で表3に表される。
本実施例は、経粘膜的送達の方法を示す。
材料 抗原タンパク質としてオボアルブミンが使用された。
処理 体重が約20gのオスのC57BLマウスは、(一次免疫として)1日目から3日目までの間と、(二次免疫として)単独に15日目とに、水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)で調製されたマウス1匹当たり20μLの溶液という形態のマウス1匹当たり100μgのオボアルブミンで舌下を処理された。21日目に測定されたマウス血漿中におけるIgGの総レベルは、免疫下での血液循環中への抗原送達の指標として使用された。データは、5を底とするマウスIgG(mouse IgG plasma IFN)の力価の逆数の対数の平均値±標準偏差(n=5)としてng/mLの単位でとして表4に表される。
本実施例は、経粘膜的送達の方法を示す。
材料 ヒト組換えインシュリンが使用された。
処理 アロキサン糖尿病を有するオスの成体ラットは、対照ラット(n=5)及び実験ラット(n=5)の2群に割り当てられた。ラットの平均空腹時血中グルコースレベルは、10.0±0.2mmol/Lであった。ラットは、水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)に溶解された、マウス一匹当たり0.1mgのインシュリンで、10分間舌下を処理された。血中グルコースレベルは、血液循環中へのインシュリン送達の指標として測定された。データは、血中グルコースレベルの平均値±標準偏差(n=5)として表5に表される。
本実施例は、経皮的送達の方法を示す。
材料 ヒト組換えインシュリンが使用された。
処理 アロキサン糖尿病を有するオスの成体ラットは、実験の48時間前に剪毛された。ラットは、対照ラット(n=5)及び実験ラット(n=5)の2群に割り当てられた。ラットの平均空腹時血中グルコースレベルは、11.0±0.4mmol/Lであった。水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)に溶解されたマウス一匹当たり0.1mgのインシュリンは、脱毛された皮膚に10分間塗布された。血中グルコースレベルは、血液循環中への経皮的なインシュリン送達の指標として測定された。データは、血中グルコースレベルの平均値±標準偏差(n=5)として表6に表される。
本実施例は、皮膚細胞に対する薬品の送達の方法を示す。
材料 メチルレッド色素が使用された。
細胞培養 ヒトケラチン生成細胞A431が使用された。
処理 A431ケラチン生成細胞は、水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)に溶解された0.3mg/mLのメチルレッドといっしょに20分間インキュベーションされた。細胞によるメチルレッドの取り込みが測定された。データは、対照に対する百分率で示したメチルレッドの取り込みの平均値±標準偏差(n=8)として表7に表される。
本実施例は、皮内的送達の方法を示す。
材料 メチレンブルー(MB)が使用された。
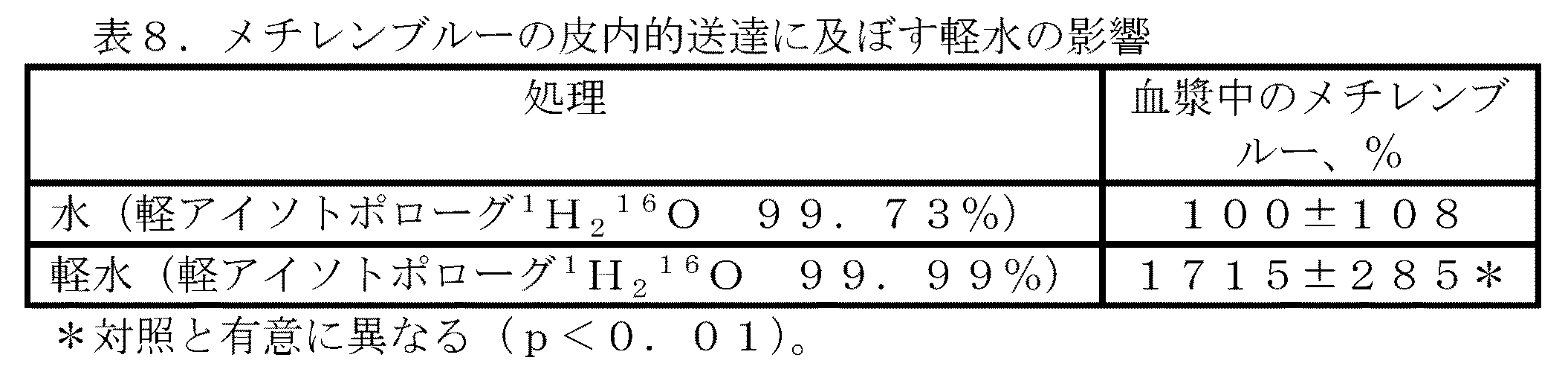
処理 水(軽アイソトポローグ1H2 16O 99.73%、対照)又は軽水(軽アイソトポローグ1H2 16O 99.99%)で調製された(マウス1匹当たりの量である100μgのメチレンブルーを含む100μLの)メチレンブルー溶液は、C57BLマウスの皮膚の(約1cm2の)脱毛された領域に局所的に投与された。皮膚は洗浄され、皮膚中のメチレンブルーレベルは、前記投与後5分の時点で測定された。データは、対照に対する百分率で示した皮膚中のメチレンブルーレベルの平均値±標準偏差(n=5)として表8に表される。
表8は、軽水が水に比較して皮内送達の吸収促進剤としてはるかに効果的であることを示す。
1 煮沸手段
2 底部
3 蒸留塔
4 接触デバイス
5 コンデンサー
2 底部
3 蒸留塔
4 接触デバイス
5 コンデンサー
Claims (2)
- 生物学的活性物質をそれを必要とする哺乳類に対して皮内的に、経皮的に、又は、経粘膜的に送達するための方法であって、前記方法は有効量の吸収増強剤を前記生物学的活性物質といっしょに前記哺乳類に共に投与するステップを含み、前記吸収増強剤は約99.760%から約99.999%までの軽アイソトポローグ1H2 16Oと、100%とする残りのアイソトポローグ1H2 17O、1H2 18O、1H2H16O、1H2H17O、1H2H18O、2H2 16O、2H2 17O及び2H2 18Oとを含む水であることを特徴とする方法。
- 前記生物学的活性物質は、薬剤、生理活性ペプチド、生理活性タンパク質、糖タンパク質、核酸、栄養素、ビタミン及びミネラルからなる群から選択されることを特徴とする請求項1に記載の方法。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/RU2005/000108 WO2006096084A1 (en) | 2005-03-11 | 2005-03-11 | Methods for intradermal, transdermal or transmucosal delivery of biologically active substances |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2008533005A true JP2008533005A (ja) | 2008-08-21 |
Family
ID=35789261
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008500660A Pending JP2008533005A (ja) | 2005-03-11 | 2005-03-11 | 生物学的活性物質の皮内的、経皮的又は経粘膜的送達のための方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20080103092A1 (ja) |
| JP (1) | JP2008533005A (ja) |
| EA (1) | EA012187B1 (ja) |
| WO (1) | WO2006096084A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008533003A (ja) * | 2005-03-11 | 2008-08-21 | ヴァーダ コンサルティング リミテッド | 製薬用軽水、治療用組成物及びその方法 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012112340A2 (en) * | 2011-02-18 | 2012-08-23 | Nestec S.A. | Methods and compositions for treating, reducing, or preventing damage to the nervous system of animals |
| US9855234B2 (en) * | 2014-07-08 | 2018-01-02 | Insys Development Company, Inc. | Diclofenac sublingual spray |
| RU2612667C1 (ru) * | 2015-10-13 | 2017-03-13 | Общество с ограниченной ответственностью "МТК Айсберг" | Устройство для получения воды с пониженным содержанием тяжелых молекул |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003049748A1 (de) * | 2001-12-12 | 2003-06-19 | HYD Kutató-Fejlesztő Kft. | Arzneimittel und lebensmittelprodukte enthaltend deuterium zur behandlung der zuckerkranheit und verfahren zu ihrer herstellung |
| JP2008515766A (ja) * | 2004-04-13 | 2008-05-15 | ビンセント シー. ジャンパパ, | Uv光への曝露によって生じる皮膚の損傷を予防および処置するための局所用組成物 |
| JP2008533003A (ja) * | 2005-03-11 | 2008-08-21 | ヴァーダ コンサルティング リミテッド | 製薬用軽水、治療用組成物及びその方法 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2108570A (en) * | 1933-06-27 | 1938-02-15 | American Security And Trust Co | Kinds of water and methods of producing them |
| US4139619A (en) * | 1976-05-24 | 1979-02-13 | The Upjohn Company | 6-Amino-4-(substituted amino)-1,2-dihydro-1-hydroxy-2-iminopyrimidine, topical compositions and process for hair growth |
| USH269H (en) * | 1985-03-11 | 1987-05-05 | A. E. Staley Manufacturing Company | Disinfectant and/or sanitizing cleaner compositions |
| US4847079A (en) * | 1985-07-29 | 1989-07-11 | Schering Corporation | Biologically stable interferon compositions comprising thimerosal |
| HU208084B (en) * | 1991-10-31 | 1993-08-30 | Hyd Kutato Fejlesztoe Kft | Process for producing compositions suitable for curing tumorous diseases |
| US6645520B2 (en) * | 1999-12-16 | 2003-11-11 | Dermatrends, Inc. | Transdermal administration of nonsteroidal anti-inflammatory drugs using hydroxide-releasing agents as permeation enhancers |
| US6582724B2 (en) * | 1999-12-16 | 2003-06-24 | Dermatrends, Inc. | Dual enhancer composition for topical and transdermal drug delivery |
| WO2004056314A2 (en) * | 2002-12-17 | 2004-07-08 | Nastech Pharmaceutical Company Inc. | Compositions and methods for enhanced mucosal delivery of y2 receptor-binding peptides and methods for treating and preventing obesity |
| US6984327B1 (en) * | 2004-11-23 | 2006-01-10 | Patterson James A | System and method for separating heavy isotopes of hydrogen oxide from water |
-
2005
- 2005-03-11 US US11/817,919 patent/US20080103092A1/en not_active Abandoned
- 2005-03-11 EA EA200701948A patent/EA012187B1/ru not_active IP Right Cessation
- 2005-03-11 WO PCT/RU2005/000108 patent/WO2006096084A1/en active Application Filing
- 2005-03-11 JP JP2008500660A patent/JP2008533005A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003049748A1 (de) * | 2001-12-12 | 2003-06-19 | HYD Kutató-Fejlesztő Kft. | Arzneimittel und lebensmittelprodukte enthaltend deuterium zur behandlung der zuckerkranheit und verfahren zu ihrer herstellung |
| JP2008515766A (ja) * | 2004-04-13 | 2008-05-15 | ビンセント シー. ジャンパパ, | Uv光への曝露によって生じる皮膚の損傷を予防および処置するための局所用組成物 |
| JP2008533003A (ja) * | 2005-03-11 | 2008-08-21 | ヴァーダ コンサルティング リミテッド | 製薬用軽水、治療用組成物及びその方法 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008533003A (ja) * | 2005-03-11 | 2008-08-21 | ヴァーダ コンサルティング リミテッド | 製薬用軽水、治療用組成物及びその方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EA200701948A1 (ru) | 2008-02-28 |
| WO2006096084A1 (en) | 2006-09-14 |
| EA012187B1 (ru) | 2009-08-28 |
| US20080103092A1 (en) | 2008-05-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1855699B1 (en) | Light pharmaceutical water and therapeutic compositions and methods thereof | |
| CN101325944B (zh) | 用于鼻部给药的组合物 | |
| US20190008795A1 (en) | Compositions for topical application of compounds | |
| US9687495B2 (en) | Methods and systems for the delivery of a therapeutic agent | |
| US8911751B2 (en) | Compositions for nasal delivery | |
| JP6295314B2 (ja) | 治療薬を送達するための方法および組成物 | |
| JP2012526840A (ja) | 膜貫通送達のための製剤系 | |
| DE19627392A1 (de) | Medikament zur Verabreichung durch die Nase | |
| JP5611033B2 (ja) | ポリペプチドの経粘膜送達組成物 | |
| WO2007014391B1 (en) | Tight junction modulating peptide components for enhancing mucosal delivery of therapeutic agents | |
| EP0803255A1 (en) | Medicinal composition | |
| JP2008533005A (ja) | 生物学的活性物質の皮内的、経皮的又は経粘膜的送達のための方法 | |
| EP0230264A2 (de) | Nasal applizierbares Arzneimittel, Verfahren zu seiner Herstellung und seine Verwendung | |
| KR20070119667A (ko) | 제약용 경수 및 이를 이용한 치료 조성물 및 방법 | |
| CN108969754B (zh) | 一种鲑降钙素鼻喷雾剂及其制备方法 | |
| EP3693006A1 (en) | Nasal hepatitis b vaccine composition and method for producing same | |
| CN105801684B (zh) | 重组人生长激素及其促进卵泡发育的应用 | |
| JPS63258821A (ja) | 鼻腔内投与用薬剤組成物 | |
| US20240108578A1 (en) | Composition in which absorbability of poorly absorbable drug is improved | |
| CN113750046B (zh) | 一种用于过敏性休克的肾上腺素舌下喷雾剂及其制备方法和应用 | |
| JP2005537328A (ja) | 皮膚および粘膜を介した物質の吸収の増大 | |
| RU2277904C2 (ru) | Интерферонсодержащая аэрозольная композиция "никофен" | |
| JPH0764755B2 (ja) | 経粘膜投与用組成物 | |
| EP0704220A1 (de) | Verwendung von Interferon beta enthaltenden Arzneimitteln |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110214 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20111212 |