JP2008531698A - 上皮及び他の細胞及び組織を治療するための方法及び組成物 - Google Patents
上皮及び他の細胞及び組織を治療するための方法及び組成物 Download PDFInfo
- Publication number
- JP2008531698A JP2008531698A JP2007558102A JP2007558102A JP2008531698A JP 2008531698 A JP2008531698 A JP 2008531698A JP 2007558102 A JP2007558102 A JP 2007558102A JP 2007558102 A JP2007558102 A JP 2007558102A JP 2008531698 A JP2008531698 A JP 2008531698A
- Authority
- JP
- Japan
- Prior art keywords
- blood
- tvemf
- stem cells
- blood stem
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 161
- 238000000034 method Methods 0.000 title claims abstract description 104
- 210000001519 tissue Anatomy 0.000 title claims description 87
- 210000000981 epithelium Anatomy 0.000 title claims description 10
- 239000008280 blood Substances 0.000 claims abstract description 390
- 210000004369 blood Anatomy 0.000 claims abstract description 387
- 210000000130 stem cell Anatomy 0.000 claims abstract description 294
- 210000004027 cell Anatomy 0.000 claims abstract description 198
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 claims abstract 4
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 claims abstract 4
- 241000124008 Mammalia Species 0.000 claims description 59
- 238000011282 treatment Methods 0.000 claims description 53
- 239000000126 substance Substances 0.000 claims description 26
- 210000003027 ear inner Anatomy 0.000 claims description 24
- 230000009931 harmful effect Effects 0.000 claims description 16
- 239000003814 drug Substances 0.000 claims description 14
- 238000002360 preparation method Methods 0.000 claims description 10
- 239000003937 drug carrier Substances 0.000 claims description 9
- 239000012503 blood component Substances 0.000 claims description 5
- 238000002347 injection Methods 0.000 claims description 5
- 239000007924 injection Substances 0.000 claims description 5
- 238000002156 mixing Methods 0.000 claims description 5
- 238000010253 intravenous injection Methods 0.000 claims description 4
- 238000010254 subcutaneous injection Methods 0.000 claims description 2
- 239000007929 subcutaneous injection Substances 0.000 claims description 2
- 210000000214 mouth Anatomy 0.000 abstract description 14
- 230000035755 proliferation Effects 0.000 abstract description 10
- 230000002062 proliferating effect Effects 0.000 abstract description 4
- 208000032625 disorder of ear Diseases 0.000 abstract description 3
- 208000025157 Oral disease Diseases 0.000 abstract 1
- 208000030194 mouth disease Diseases 0.000 abstract 1
- 208000017520 skin disease Diseases 0.000 abstract 1
- 210000000601 blood cell Anatomy 0.000 description 29
- 230000012010 growth Effects 0.000 description 27
- 210000005259 peripheral blood Anatomy 0.000 description 25
- 239000011886 peripheral blood Substances 0.000 description 25
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 24
- 210000002381 plasma Anatomy 0.000 description 24
- 210000004700 fetal blood Anatomy 0.000 description 22
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 238000005138 cryopreservation Methods 0.000 description 21
- 210000003743 erythrocyte Anatomy 0.000 description 20
- 230000006378 damage Effects 0.000 description 19
- 239000000523 sample Substances 0.000 description 19
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 18
- 238000007710 freezing Methods 0.000 description 16
- 230000008014 freezing Effects 0.000 description 16
- 210000002768 hair cell Anatomy 0.000 description 16
- 238000004113 cell culture Methods 0.000 description 15
- 208000016354 hearing loss disease Diseases 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- 201000010099 disease Diseases 0.000 description 14
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 14
- 210000000265 leukocyte Anatomy 0.000 description 14
- 238000001816 cooling Methods 0.000 description 13
- 239000000463 material Substances 0.000 description 13
- 230000008569 process Effects 0.000 description 12
- 239000002577 cryoprotective agent Substances 0.000 description 11
- 239000002609 medium Substances 0.000 description 11
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 10
- 206010011878 Deafness Diseases 0.000 description 10
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 10
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 10
- 102000008100 Human Serum Albumin Human genes 0.000 description 10
- 108091006905 Human Serum Albumin Proteins 0.000 description 10
- 239000006143 cell culture medium Substances 0.000 description 10
- 229910052802 copper Inorganic materials 0.000 description 10
- 239000010949 copper Substances 0.000 description 10
- 239000003102 growth factor Substances 0.000 description 10
- 231100000888 hearing loss Toxicity 0.000 description 10
- 230000010370 hearing loss Effects 0.000 description 10
- 239000007788 liquid Substances 0.000 description 10
- 239000000872 buffer Substances 0.000 description 9
- 210000000959 ear middle Anatomy 0.000 description 9
- 210000001671 embryonic stem cell Anatomy 0.000 description 9
- 210000002919 epithelial cell Anatomy 0.000 description 9
- 239000012530 fluid Substances 0.000 description 9
- 210000002569 neuron Anatomy 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- 238000002054 transplantation Methods 0.000 description 9
- 102000009027 Albumins Human genes 0.000 description 8
- 108010088751 Albumins Proteins 0.000 description 8
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 8
- 239000002738 chelating agent Substances 0.000 description 8
- 239000000306 component Substances 0.000 description 8
- 229940088597 hormone Drugs 0.000 description 8
- 229910052757 nitrogen Inorganic materials 0.000 description 8
- 238000003860 storage Methods 0.000 description 8
- 238000001356 surgical procedure Methods 0.000 description 8
- 210000001185 bone marrow Anatomy 0.000 description 7
- 239000000969 carrier Substances 0.000 description 7
- 210000000613 ear canal Anatomy 0.000 description 7
- 239000005556 hormone Substances 0.000 description 7
- 208000015181 infectious disease Diseases 0.000 description 7
- 235000015097 nutrients Nutrition 0.000 description 7
- 230000001172 regenerating effect Effects 0.000 description 7
- 230000008929 regeneration Effects 0.000 description 7
- 238000011069 regeneration method Methods 0.000 description 7
- 230000001225 therapeutic effect Effects 0.000 description 7
- 239000003440 toxic substance Substances 0.000 description 7
- 102000004127 Cytokines Human genes 0.000 description 6
- 108090000695 Cytokines Proteins 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 239000000654 additive Substances 0.000 description 6
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 6
- 230000010261 cell growth Effects 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 208000014674 injury Diseases 0.000 description 6
- 239000001301 oxygen Substances 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- 210000004976 peripheral blood cell Anatomy 0.000 description 6
- 231100000614 poison Toxicity 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 6
- 238000011476 stem cell transplantation Methods 0.000 description 6
- 238000010257 thawing Methods 0.000 description 6
- 231100000331 toxic Toxicity 0.000 description 6
- 230000002588 toxic effect Effects 0.000 description 6
- 241000282412 Homo Species 0.000 description 5
- QSDSSSQWVNLFIG-UHFFFAOYSA-N Neosporin Natural products CC(O)CC1=C(OC)C(=O)C2=CC(O)=C3OCOC4=C(O)C=C5C6=C4C3=C2C1=C6C(CC(C)O)=C(OC)C5=O QSDSSSQWVNLFIG-UHFFFAOYSA-N 0.000 description 5
- 241000283973 Oryctolagus cuniculus Species 0.000 description 5
- 206010033109 Ototoxicity Diseases 0.000 description 5
- 208000027418 Wounds and injury Diseases 0.000 description 5
- 238000010322 bone marrow transplantation Methods 0.000 description 5
- 210000000133 brain stem Anatomy 0.000 description 5
- 108010046161 drug combination polymyxin B neomycin sulfate bacitracin zinc Proteins 0.000 description 5
- 210000003754 fetus Anatomy 0.000 description 5
- 239000012737 fresh medium Substances 0.000 description 5
- 239000001963 growth medium Substances 0.000 description 5
- 210000000067 inner hair cell Anatomy 0.000 description 5
- 230000033001 locomotion Effects 0.000 description 5
- 210000003739 neck Anatomy 0.000 description 5
- 229940049337 neosporin Drugs 0.000 description 5
- 231100000262 ototoxicity Toxicity 0.000 description 5
- 230000002093 peripheral effect Effects 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 241000894007 species Species 0.000 description 5
- 208000024891 symptom Diseases 0.000 description 5
- 210000003454 tympanic membrane Anatomy 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 241000894006 Bacteria Species 0.000 description 4
- 208000003098 Ganglion Cysts Diseases 0.000 description 4
- 102000001554 Hemoglobins Human genes 0.000 description 4
- 108010054147 Hemoglobins Proteins 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 208000005400 Synovial Cyst Diseases 0.000 description 4
- 230000000735 allogeneic effect Effects 0.000 description 4
- 239000002647 aminoglycoside antibiotic agent Substances 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 238000010171 animal model Methods 0.000 description 4
- 239000003242 anti bacterial agent Substances 0.000 description 4
- 229940088710 antibiotic agent Drugs 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 239000001569 carbon dioxide Substances 0.000 description 4
- 229910002092 carbon dioxide Inorganic materials 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 229960004316 cisplatin Drugs 0.000 description 4
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 4
- 210000000860 cochlear nerve Anatomy 0.000 description 4
- 239000000356 contaminant Substances 0.000 description 4
- 230000002338 cryopreservative effect Effects 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 239000008103 glucose Substances 0.000 description 4
- 210000000987 immune system Anatomy 0.000 description 4
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 4
- 210000002540 macrophage Anatomy 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 231100000199 ototoxic Toxicity 0.000 description 4
- 230000002970 ototoxic effect Effects 0.000 description 4
- 229920003023 plastic Polymers 0.000 description 4
- 230000002265 prevention Effects 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- 210000001323 spiral ganglion Anatomy 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- 230000008733 trauma Effects 0.000 description 4
- 210000003954 umbilical cord Anatomy 0.000 description 4
- 230000001720 vestibular Effects 0.000 description 4
- 206010067484 Adverse reaction Diseases 0.000 description 3
- 229920002307 Dextran Polymers 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- 239000004677 Nylon Substances 0.000 description 3
- 230000006838 adverse reaction Effects 0.000 description 3
- 238000002617 apheresis Methods 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 210000003952 cochlear nucleus Anatomy 0.000 description 3
- 210000000883 ear external Anatomy 0.000 description 3
- 210000005069 ears Anatomy 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 210000003714 granulocyte Anatomy 0.000 description 3
- 239000000383 hazardous chemical Substances 0.000 description 3
- 208000026278 immune system disease Diseases 0.000 description 3
- 230000030214 innervation Effects 0.000 description 3
- 210000003734 kidney Anatomy 0.000 description 3
- 208000032839 leukemia Diseases 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 229920001778 nylon Polymers 0.000 description 3
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 3
- 238000010827 pathological analysis Methods 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000013074 reference sample Substances 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 229960004889 salicylic acid Drugs 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- 230000035924 thermogenesis Effects 0.000 description 3
- 238000011200 topical administration Methods 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 210000000752 vestibulocochlear nerve Anatomy 0.000 description 3
- 239000002699 waste material Substances 0.000 description 3
- LJRDOKAZOAKLDU-UDXJMMFXSA-N (2s,3s,4r,5r,6r)-5-amino-2-(aminomethyl)-6-[(2r,3s,4r,5s)-5-[(1r,2r,3s,5r,6s)-3,5-diamino-2-[(2s,3r,4r,5s,6r)-3-amino-4,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-6-hydroxycyclohexyl]oxy-4-hydroxy-2-(hydroxymethyl)oxolan-3-yl]oxyoxane-3,4-diol;sulfuric ac Chemical compound OS(O)(=O)=O.N[C@@H]1[C@@H](O)[C@H](O)[C@H](CN)O[C@@H]1O[C@H]1[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](N)C[C@@H](N)[C@@H]2O)O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)N)O[C@@H]1CO LJRDOKAZOAKLDU-UDXJMMFXSA-N 0.000 description 2
- KMZHZAAOEWVPSE-UHFFFAOYSA-N 2,3-dihydroxypropyl acetate Chemical compound CC(=O)OCC(O)CO KMZHZAAOEWVPSE-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- 208000035473 Communicable disease Diseases 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 229930182566 Gentamicin Natural products 0.000 description 2
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 2
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 2
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 2
- 208000026350 Inborn Genetic disease Diseases 0.000 description 2
- 241000588748 Klebsiella Species 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 206010033078 Otitis media Diseases 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- LOUPRKONTZGTKE-WZBLMQSHSA-N Quinine Chemical compound C([C@H]([C@H](C1)C=C)C2)C[N@@]1[C@@H]2[C@H](O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-WZBLMQSHSA-N 0.000 description 2
- 229940126575 aminoglycoside Drugs 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 229940127219 anticoagulant drug Drugs 0.000 description 2
- 239000000427 antigen Substances 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- 239000004599 antimicrobial Substances 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- 210000003926 auditory cortex Anatomy 0.000 description 2
- 210000003984 auditory pathway Anatomy 0.000 description 2
- 210000002469 basement membrane Anatomy 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 210000002798 bone marrow cell Anatomy 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 238000002659 cell therapy Methods 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 230000004087 circulation Effects 0.000 description 2
- 210000003477 cochlea Anatomy 0.000 description 2
- 239000004020 conductor Substances 0.000 description 2
- ALEXXDVDDISNDU-JZYPGELDSA-N cortisol 21-acetate Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)COC(=O)C)(O)[C@@]1(C)C[C@@H]2O ALEXXDVDDISNDU-JZYPGELDSA-N 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000004744 fabric Substances 0.000 description 2
- 208000016361 genetic disease Diseases 0.000 description 2
- 229960002518 gentamicin Drugs 0.000 description 2
- 230000035876 healing Effects 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 2
- 208000006454 hepatitis Diseases 0.000 description 2
- 231100000283 hepatitis Toxicity 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 239000002171 loop diuretic Substances 0.000 description 2
- 230000008774 maternal effect Effects 0.000 description 2
- 210000005087 mononuclear cell Anatomy 0.000 description 2
- 210000004126 nerve fiber Anatomy 0.000 description 2
- 230000003204 osmotic effect Effects 0.000 description 2
- 229960001639 penicillamine Drugs 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 210000002826 placenta Anatomy 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000008439 repair process Effects 0.000 description 2
- 230000010076 replication Effects 0.000 description 2
- 210000003491 skin Anatomy 0.000 description 2
- 210000001988 somatic stem cell Anatomy 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 230000009469 supplementation Effects 0.000 description 2
- 230000001502 supplementing effect Effects 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 210000000225 synapse Anatomy 0.000 description 2
- 238000007910 systemic administration Methods 0.000 description 2
- 230000017423 tissue regeneration Effects 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- GUBGYTABKSRVRQ-DCSYEGIMSA-N Beta-Lactose Chemical compound OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-DCSYEGIMSA-N 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 206010050337 Cerumen impaction Diseases 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 235000001258 Cinchona calisaya Nutrition 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000588722 Escherichia Species 0.000 description 1
- 108010074864 Factor XI Proteins 0.000 description 1
- 241000192125 Firmicutes Species 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 208000016621 Hearing disease Diseases 0.000 description 1
- 101100220044 Homo sapiens CD34 gene Proteins 0.000 description 1
- 101000746367 Homo sapiens Granulocyte colony-stimulating factor Proteins 0.000 description 1
- 101000716729 Homo sapiens Kit ligand Proteins 0.000 description 1
- 229920001612 Hydroxyethyl starch Polymers 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 208000027601 Inner ear disease Diseases 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 241000186781 Listeria Species 0.000 description 1
- 206010029155 Nephropathy toxic Diseases 0.000 description 1
- 241000187654 Nocardia Species 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 241000589516 Pseudomonas Species 0.000 description 1
- 241000219492 Quercus Species 0.000 description 1
- 206010040030 Sensory loss Diseases 0.000 description 1
- 241000607768 Shigella Species 0.000 description 1
- 241000191940 Staphylococcus Species 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 208000009205 Tinnitus Diseases 0.000 description 1
- WYHIICXRPHEJKI-UHFFFAOYSA-N Trientine hydrochloride Chemical compound Cl.Cl.NCCNCCNCCN WYHIICXRPHEJKI-UHFFFAOYSA-N 0.000 description 1
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 241000607734 Yersinia <bacteria> Species 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 210000003766 afferent neuron Anatomy 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 238000011316 allogeneic transplantation Methods 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 230000000202 analgesic effect Effects 0.000 description 1
- 210000003484 anatomy Anatomy 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 230000001754 anti-pyretic effect Effects 0.000 description 1
- 230000002785 anti-thrombosis Effects 0.000 description 1
- 229940034982 antineoplastic agent Drugs 0.000 description 1
- 239000002221 antipyretic Substances 0.000 description 1
- 210000001841 basilar artery Anatomy 0.000 description 1
- 230000002146 bilateral effect Effects 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 239000010836 blood and blood product Substances 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 229940125691 blood product Drugs 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000009087 cell motility Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 210000002421 cell wall Anatomy 0.000 description 1
- 230000004098 cellular respiration Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 210000002939 cerumen Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- LOUPRKONTZGTKE-UHFFFAOYSA-N cinchonine Natural products C1C(C(C2)C=C)CCN2C1C(O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-UHFFFAOYSA-N 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000002498 deadly effect Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 229940119744 dextran 40 Drugs 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 235000012489 doughnuts Nutrition 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 208000027043 ear symptom Diseases 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- 230000005672 electromagnetic field Effects 0.000 description 1
- 230000013020 embryo development Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 210000002388 eustachian tube Anatomy 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 210000000256 facial nerve Anatomy 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 230000009969 flowable effect Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 150000002337 glycosamines Chemical class 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000000122 growth hormone Substances 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 210000003897 hepatic stem cell Anatomy 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 102000055151 human KITLG Human genes 0.000 description 1
- 229940050526 hydroxyethylstarch Drugs 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 208000022760 infectious otitis media Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 238000009421 internal insulation Methods 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 210000005061 intracellular organelle Anatomy 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 210000003127 knee Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 210000001595 mastoid Anatomy 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 230000009347 mechanical transmission Effects 0.000 description 1
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 210000003643 myeloid progenitor cell Anatomy 0.000 description 1
- 231100000417 nephrotoxicity Toxicity 0.000 description 1
- 230000007694 nephrotoxicity Effects 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 210000000944 nerve tissue Anatomy 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 210000000461 neuroepithelial cell Anatomy 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- JCXJVPUVTGWSNB-UHFFFAOYSA-N nitrogen dioxide Inorganic materials O=[N]=O JCXJVPUVTGWSNB-UHFFFAOYSA-N 0.000 description 1
- 210000004923 pancreatic tissue Anatomy 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 210000004049 perilymph Anatomy 0.000 description 1
- 210000002856 peripheral neuron Anatomy 0.000 description 1
- 230000003169 placental effect Effects 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 1
- -1 platinum coordination complex Chemical class 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920006316 polyvinylpyrrolidine Polymers 0.000 description 1
- 238000011176 pooling Methods 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 229960000948 quinine Drugs 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- HEBKCHPVOIAQTA-ZXFHETKHSA-N ribitol Chemical compound OC[C@H](O)[C@H](O)[C@H](O)CO HEBKCHPVOIAQTA-ZXFHETKHSA-N 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 210000004761 scalp Anatomy 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000001953 sensory effect Effects 0.000 description 1
- 210000001044 sensory neuron Anatomy 0.000 description 1
- 230000021317 sensory perception Effects 0.000 description 1
- 238000010583 slow cooling Methods 0.000 description 1
- 150000003384 small molecules Chemical group 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 210000003478 temporal lobe Anatomy 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- 210000001103 thalamus Anatomy 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 238000001149 thermolysis Methods 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 231100000886 tinnitus Toxicity 0.000 description 1
- 229960000707 tobramycin Drugs 0.000 description 1
- NLVFBUXFDBBNBW-PBSUHMDJSA-N tobramycin Chemical compound N[C@@H]1C[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N NLVFBUXFDBBNBW-PBSUHMDJSA-N 0.000 description 1
- 231100000167 toxic agent Toxicity 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 239000012780 transparent material Substances 0.000 description 1
- 229960002408 trientine hydrochloride Drugs 0.000 description 1
- 208000013679 tropical endomyocardial fibrosis Diseases 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/28—Bone marrow; Haematopoietic stem cells; Mesenchymal stem cells of any origin, e.g. adipose-derived stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0647—Haematopoietic stem cells; Uncommitted or multipotent progenitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K2035/124—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells the cells being hematopoietic, bone marrow derived or blood cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2529/00—Culture process characterised by the use of electromagnetic stimulation
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- General Health & Medical Sciences (AREA)
- Cell Biology (AREA)
- Immunology (AREA)
- Genetics & Genomics (AREA)
- Hematology (AREA)
- Wood Science & Technology (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Developmental Biology & Embryology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Virology (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
本発明は、哺乳動物血液幹細胞、好ましくは、CD34+/CD38−細胞のTVEMF増殖、TVEMF−増殖細胞から生じる組成物、及びこの組成物を用いて皮膚、口腔、又は耳の疾患又は症状を治療する方法又は皮膚、口腔、又は耳の組織を治療する方法に関する。
Description
本発明は、組織の治療、より具体的には、TVEMF−バイオリアクター中で調製した血液幹細胞を使用する、上皮細胞を含む皮膚組織、口腔組織、及び内耳組織、及び他の組織の治療に関し、ならびにこのような調製のプロセス、その組成物、及び細胞又は組成物を用いて哺乳動物を治療する方法に関する。
哺乳動物、特にヒトの組織の再生は、医学界の長い間の要望であった。これまでは、ヒト組織の治療は、ドナーからの同様の組織の移植によって大部分達成されてきた。ヘリック(Herrick)双子の一方から他方への腎移植から本質的に始まり、後には、南アフリカの医師クリスチャン・バーナード(Christian Barnard)による1967年12月3日のデニス・ダーバル氏(Denise Darval)からルイス・ワシュカンスキー氏(Louis Washkansky)への心臓移植によって有名になり、組織移植は末期の患者において寿命を延長する広範に受け入れられる方法となった。
ヒト組織の移植は、その最初の使用から、主だった問題、第一には身体の自然の免疫系に起因する組織拒絶に遭遇した。これは、しばしば、組織移植の使用による寿命の延長を制限してきた(ワシュカンスキー氏は手術後18日間生きたのみであった)。
身体の免疫系の問題を克服するために、やがて多数の拒絶反応抑制剤(例えば、イムラン、シクロスポリン)が、免疫系を抑制し、従って拒絶の前の組織の使用を延長するために開発された。しかし、拒絶の問題は継続し、組織移植に対する代替についての必要性が生じている。
骨髄移植もまた使用されており、これは、骨髄などの特定の組織を治療するための、白血病などのある病気の治療のためのなお最適な手法であるが、骨髄移植はまた問題を有している。これはドナーからの適合を必要とし(当時で50%未満で見出される)、これは痛みを伴い、高価であり、そしてリスクが高い。結果として、骨髄移植に対する代替が強く望まれている。米国特許第6,129,911号に見出されるような肝幹細胞の移植などの組織幹細胞の移植は同様の制限を有し、それらの広範な使用を疑問視させる。
近年、研究者らは、組織移植の代替としての多能性胚性幹細胞の使用を伴う実験を行ってきた。胚性幹細胞の使用の背後にある理論は、それらが理論的には身体中の実質的に任意の組織を再生するために利用することができるということであった。しかし、組織再生のための胚性幹細胞の使用もまた、問題に遭遇している。これらの問題の中でより深刻なものは、移植された胚性幹細胞は制御可能性が限られており、これらは時折腫瘍に成長し、そして研究のために利用可能であるヒト胚性幹細胞は、患者の免疫系によって拒絶されることである(ネイチャー(Nature)、6月17日、2002年、ピアソン(Pearson)著、「幹細胞は2つを望む(Stem Cell Hopes Double)」、news@nature.com、オンライン発行:2002年6月21日)。更に、胚性幹細胞の広範な使用は、倫理的、道徳的、及び政治的な問題を多く抱えているので、その広範な使用は疑問視されたままである。
上皮細胞を含む組織の治療は特に望ましい。上皮細胞は、哺乳動物の身体の表面(皮膚)全体を覆う上皮組織を含む。口腔の裏層でさえ上皮細胞を含み、種々の他の組織及び細胞タイプと関連している。これらの細胞は、歯を支持し、唾液の分泌を補助し、他の口腔機能に寄与する。また、ある上皮細胞は、内耳上皮有毛細胞のように感覚受容のために特定化されている。皮膚、口腔及び耳は、哺乳動物の生存及び健康の維持及び感覚認識のために不可欠である。
口腔組織及び皮膚組織の治療及び再生は、これまでに、損傷(口腔組織の場合においては、主として外科手術から)の部位において感染を予防することによって治癒を促進する、抗生物質及び他の生成物を用いる治療によって行われてきた。しかし、このような方法は、身体がそれ自体の治療系を用いて組織を修復させる時間を著しく短縮しない。
聴覚障害は、一般的に哺乳動物において共通であり、何百万もの人に影響を与える深刻なハンディキャップである。聴覚障害は、末梢聴覚系のニューロン及び/又は有毛細胞に損傷を与える、感染、機械的損傷、大音量の音、加齢、及び化学誘導性耳毒性を含む広範な種々の原因が存在し得る。末梢聴覚系は、聴覚受容器、コルティ組織中の有毛細胞、及び一次聴覚ニューロン、蝸牛中のらせん神経節ニューロンからなる。末梢聴覚系の損傷は治癒欠損の大部分の原因である。
らせん神経節ニューロン(「SGN」)は、末梢聴覚受容器、コルティ組織中の有毛細胞から、蝸牛神経を通して脳までシグナルを送達する一次求心性聴覚神経である。第八脳神経は、らせん神経節中の一次聴覚ニューロンを脳幹に接続する。また、第八脳神経は、平衡の原因である一次求心性感覚ニューロンであり、かつ内耳の卵形嚢、球形嚢、及び膨大部から、脳まで、脳幹まで、シグナルを送達する前庭神経節ニューロン(「VGN」)を接続する。らせん神経節における一次求心性ニューロンの破壊は、聴覚障害の主要な原因とされてきた。
更に、外耳道から中枢神経系までの聴覚経路に沿ったいずれかの場所での障害は、聴覚の損傷を生じる可能性がある。聴覚器官は、外耳及び中耳、内耳、及び聴覚神経及び中枢聴覚伝導路に分けることができる。種によっていくつかのバリエーションを有するが、その一般的な特徴付けはすべての哺乳動物に共通である。聴覚刺激は、外耳道、鼓膜、及び耳小骨連鎖を通して内耳に機械的に伝達される。中耳及び乳様突起は、通常、空気で満たされている。外耳及び中耳の障害は、通常、この機械的な伝達と干渉することによって、伝音喪失を生じる。伝音喪失の一般的な原因には、外耳道閉鎖症又は耳垢によって引き起こされ得るような、外耳道の閉塞;外傷又は感染によって引き起こされ得るような、鼓膜の肥厚又は穿孔;耳小骨連鎖の成分の固定又は吸収;及び液体で満たされた中耳空間を生じる、エウスタキオ管の閉塞が含まれる。
聴覚情報は、機械的シグナルから、内耳における神経上皮細胞(有毛細胞)及びSGNの作用によって神経的に伝導される電気的パルスに変換される。SGNのすべての中心繊維は、橋脳幹の蝸牛神経核中のシナプスを形成する。蝸牛神経核からの聴覚投射は両側性であり、下丘に位置する主要核、視床の内側膝状体、及び側頭葉の聴覚皮質を伴う。聴覚に関与するニューロンの数は、蝸牛から聴覚脳幹及び聴覚皮質までで劇的に増加する。すべての聴覚情報は、限られた数の有毛細胞によって伝達され、そのうちの比較的少ない数のいわゆる内有毛細胞が決定的に重要である。なぜなら、これらは、主要な聴覚ニューロンのおよそ90パーセントとシナプスを形成するからである。比較として、蝸牛神経核のレベルにおいて、含まれる神経要素の数は、数十万で測定される。従って、聴覚末梢系における比較的少ない有毛細胞に対する損傷は、実質的な聴覚喪失をもたらし得る。それゆえに、感音喪失の多くの原因は、内耳における傷害が原因であり得る。この型の聴覚喪失は進行性であり得る。加えて、聴覚は、動物の年齢に伴う耳の解剖学的構造の変化のために、著しく敏感ではなくなる。
胚形成の間、前庭神経節、らせん神経節、及び耳胞は、同じ神経外胚葉、耳プラコードから導き出される。従って、前庭及び聴覚系は、有毛細胞の末梢ニューロン神経支配及び脳幹核への中心からの突出を含む多くの特徴を共有する。これらの系の両方は、治療薬剤、抗新生物薬剤、食品又は医薬品の中の夾雑物、ならびに環境及び工業的な汚染物質を含む、耳有害物質に対して敏感である。耳毒性薬物には、広範に使用されている化学療法剤シスプラチン及びそのアナログ、グラム陰性細菌によって引き起こされる感染の治療のために一般的に使用されているアミノグリコシド抗生物質、例えば、ゲンタマイシン、キニーネ及びそのアナログ、サリチル酸及びそのアナログ、ならびにループ利尿薬が含まれる。
聴細胞及び神経節ニューロンに対するこれらの薬物の毒性効果は、しばしば、これらの治療的な有用性を限定する要因である。例えば、ゲンタマイシン、ストレプトマイシン、カナマイシン、トブラマイシンなどのような抗微生物アミノグリコシドは、このような抗微生物剤の有効性を低下させる、深刻な毒性、特に、耳毒性及び腎毒性を有することが知られている。アミノグリコシド抗生物質は、例えば、グラム陽性細菌、グラム陰性細菌、及び抗酸菌に対して有効である、広範なスペクトルを有する抗微生物剤として一般的に利用される。感染しやすい微生物には、エシェリキア(Escherichia)種、ヘモフィルス(Hemophilus)種、リステリア(Listeria)種、シュードモナス(Pseudomonas)種、ノカルジア(Nocardia)種、エルシニア(Yersinia)種、クレブシエラ(Klebsiella)種、エンテロバクター(Enterbacter)種、ラルモネラ(Lalmonella)種、スタヒロコッカス(Staphylococcus)種、ストレプトコッカス(Streptococcus)種、ミコバクテリア(Mycobacteria)種、シゲラ(Shigella)種、及びセラチア(Serratia)種が含まれる。それにも関わらず、アミノグリコシドは、グラム陰性細菌によって引き起こされる感染を治療するために主として、例えば、相乗効果のためにペニシリンと組み合わせて、使用される。そのファミリーの一般名によって暗示されるように、すべてのアミノグリコシド抗生物質は、グリコシド結合中にアミノ糖を含む。
中耳炎は、中耳の炎症を説明するために使用される用語であり、これは、特に小児において非常に一般的である。典型的には、抗生物質を、例えば、応答的又は予防的な様式で、中耳の感染のために全身投与する。中耳感染と戦うための抗生物質の全身投与は、中耳における治療レベルを達成するために、一般的に長い時間のずれを生じ、そしてこのようなレベルを達成するために高い初期用量を必要とする。これらの欠点は、治療レベルを得るための能力を複雑にし、そしてある抗生物質の使用を全く排除する可能性がある。全身投与は、最も頻繁には、感染が進行した段階に達し、しかしこの時点で永続的な損傷が中耳及び内耳の構造に対してすでになされている可能性がある場合に有効である。明確に、耳毒性は、用量を制限する抗生物質投与の副作用である。
例えば、60〜120日間毎日2グラムのストレプトマイシンを与えられた患者のほぼ75%がある程度の前庭障害を示したのに対して、1日あたり1グラムでは発生率は25%に減少した(米国特許第5,059,591号)。聴覚障害が観察された:1週間を超えて1日あたり1グラムを受容した患者の4〜15%が測定可能な聴覚損失を発症する。これはゆっくりと悪化し、処置が継続されれば、完全に永続的な難聴に導き得る。また、耳毒性は、精巣癌、卵巣癌、膀胱癌及び頭頸部癌を含む種々のヒトの癌に対して有効であることが判明している、白金配位錯体であるシスプラチンについての用量限定的な深刻な副作用である。シスプラチンは、聴覚系及び前庭系に損傷を与える。アスピリンなどのサリチル酸は、それらの抗炎症効果、鎮痛効果、解熱効果、及び抗血栓効果のために、最も一般的に使用されている治療薬物である。不運なことに、これらは耳毒性副作用を有する。これらはしばしば、耳鳴り(tinnitus)(「耳鳴り(ringing in the ears)」)及び一時的聴力損失に導く。しかし、薬物が高用量で長期間使用されるならば、聴覚障害は、永続的かつ不可逆的になり得る。従って、内耳障害並びに内耳組織、特に、内耳有毛細胞及び選択的に、付随する聴神経を含む聴覚障害の発生及び/又は重症度を予防、減少、又は治療するための手段が必要とされている。特に関心が持たれるものは、シスプラチン及びそのアナログ、アミノグリコシド抗生物質、サリチル酸及びそのアナログ、又はループ利尿薬を含む、耳毒性治療薬物の望ましくない副作用として生じるこれらの状態である。必要とされるものは、聴覚を回復するために内耳有毛細胞を再生する方法である。本発明は、これらの目的及び他の目的を同様に達成するための方法を提供する。
幹細胞の多能性性質は、最初に、骨髄中に見出された成熟幹細胞から発見された。ヴェルフェイユ,CMら(Verfaille, CM. et al.)、「成人骨髄由来の間葉幹細胞の多能性(Pluripotency of mesenchymal stem cells derived from adult marrow)」。ネイチャー(Nature)417、オンライン発行6月20日;doi:10.1038/nature00900、(2002年)であって、ピアソン,H(Pearson, H)が、「幹細胞は2つを望む(Stem Cell Hopes Double)」、news@nature.com、オンライン発行:2003年6月21日、doi:10.1038/news020617-11において引用。
ボイズら(Boyse et al.)の米国特許第6,569,427号には、貧血症、悪性腫瘍、自己免疫疾患などの様々な疾病及び疾患、及び様々な免疫機能障害及び欠損症についての治療又は予防における、凍結保存、及び、凍結保存された胎児又は新生児の血液の実用性が開示されている。また、ボイズは、異種遺伝子配列を用いた遺伝子治療における造血再構成の使用を開示している。しかしながら、ボイズの開示は治療的使用のための細胞増殖にまでは至っていない。臍帯血バンクであるコルセル(CorCell)は、臍帯血幹細胞の増殖、凍結保存及び移植に関する統計を提供する。「臍帯血幹細胞の増殖(Expansion of Umbilical cord 血液幹細胞)」、情報シート 臍帯血、コールセル株式会社(2003年)。ある増殖工程は、バイオリアクター(生物反応器)を中央コラーゲンベースのマトリックスに利用することを開示する。ユーリッヒ研究所(Research Center Julich)、「バイオリアクターからの血液幹細胞(Blood Stem Cells from the Bioreactor)」、プレスリリース2001年5月17日。
本願を通して、「末梢血」という用語は、哺乳動物において全身的に循環しているか、又は循環した血液を意味する。「末梢血細胞」という用語は、末梢血中に見られる細胞を意味する。
成熟幹細胞は、多数の成熟組織において見られるが、これらはより少ない量で見られ、位置を把握することが難しい。
一般的に、哺乳動物から採集される時、末梢血は、好ましくは、抗凝血剤を含む1つ以上の注射器に採集される。臍帯血は、好ましくは、当該分野において周知の手段で、生後すぐに採集される。血液は、注射器中に保存されても、別の容器に移されてもよい。次いで、血液は、その成分(白血球、赤血球、及び血漿)に分離されてもよい。これは、遠心分離(血液が分離するまで血液の容器を回転させる装置)又は沈殿(血液の容器に沈殿物を投入して血液の分離させる方法)によって行われる。第2に、血液が、底部に赤血球(RBC)、中間部に白血球(WBC)、及び上部に血漿というように分離したら、白血球は保存のために取り除かれる。「軟膜」としても知られる中間層には、興味のある血液幹細胞が含まれる。血液の他の成分は不要である。いくつかの血液バンクにおいては、これが処理する範囲である。しかしながら、他のバンクは、続いて、WBCから単核球(この場合、白血球のサブセット)を除去することによって軟膜を処理する。皆がこの方法に賛成ではないが、保存する量を低減することができ、細胞を保存するため必要な低温窒素を低減することができる。
血液を処理する別の方法は、コベスペクトラ(Cobe Spectra)製細胞分離機などの分離機で、採集した血液の全てを1回以上(好ましくは3回)、のラウンドの連続的なフロー白血球搬出法で廻すことである。このような処理によって、1つの核を有する血球は他の血球から分離される。幹細胞は1つの核を有するグループの一部である。
血液サンプルからRBCを取り除くことが好ましい。人は同じHLA型を有するかもしれないが(幹細胞の移植に必要である)、同じ血液型ではないかもしれない。RBCを除去することによって、幹細胞移植に不都合な反応を最小限と留めることができる。したがって、RBCを除去することによって、幹細胞サンプルがより多くの人と適合する機会が多くなる。RBCは解凍された時に破裂することがあり、遊離ヘモグロビンを放出する。このタイプのヘモグロビンは、移植を受ける人の腎臓に深刻な影響を及ぼすことがある。さらに、幹細胞の生存能力は、RBCが破裂した時に低下する。
また、特に血液を低温保存する場合、又は他の哺乳動物に輸血する場合、HIV/AIDS、肝炎、白血病又は免疫障害など感染性又は遺伝的疾患を有していないか確認する検査が行われてもよい。血液にそのような疾患がある時は、廃棄されるか、将来の使用者が検討するようにリスクの記録を伴って血液が保存される。
したがって、臓器移植、骨髄移植、又は胚性幹細胞に基づかず、日々の使用のために免疫応答を誘発しそうにない増殖した幹細胞の組成物をなお提供する、ヒト組織を治療する方法及びプロセスを提供することが必要とされている。より好ましくは、聴覚を回復するために内耳有毛細胞を再生する方法及びプロセス、口腔組織を治療する方法及びそのプロセス、並びに、皮膚組織を治療する方法及そのプロセスが必要とされている。本発明は、これらの目的及び他の目的を同様に達成するための方法及びプロセスを提供する。
本発明は、上皮細胞又は組織、及び/又は皮膚、口腔、及び内耳に関連する他の組織を治療、再生、補充するための方法に関する。特に、本発明は、損なわれたか又は摩耗した皮膚組織、口腔の手術、好ましくは歯肉の手術を受けた口腔組織、及び例えば、薬物からの耳毒性、生来の聴力損失又は大音量の音からの聴覚損害に起因して損傷した内耳組織を治療する方法に関する。皮膚、口腔、及び/又は耳の状態を有する哺乳動物、好ましくは、ヒトを治療するための本発明の方法は、血液由来の増殖した成熟幹細胞の治療有効量を哺乳動物に導入する工程を含み、この幹細胞は、それらが由来した血液中の体積あたりの細胞の数よりも、少なくとも7倍多い体積あたりの細胞数に増殖されており、TVEMF−増殖した血液幹細胞は、それらの三次元形状及び細胞間支持及び細胞間形状を維持している。この方法は、損傷した組織を効果的に治療するための、ヒトの体組織が血球を利用できる十分な時間内におけるこのような導入する工程を含む。
また、本発明は、哺乳動物、好ましくはヒトからの血液幹細胞に部分的に関し、好ましくは、該幹細胞はTVEMF−増殖された幹細胞である。また、本発明は、哺乳動物、好ましくはヒトからのTVEMF−増殖した血液幹細胞に関し、該幹細胞の体積あたりの数は、それらの供給源材料(例えば、TVEMF増殖の前の幹細胞の血液供給源)よりも少なくとも7倍であり、該血液幹細胞は、天然に存在する(すなわち、供給源の)血液の幹細胞と同じ又は本質的に同一である、三次元形状及び細胞間支持及び細胞間形状を有する。また、本発明は、薬学的に受容可能なキャリア、凍結保存剤、及び細胞培養培地を含み、必要であれば他の成分が添加される、皮膚、口腔又は耳の障害を治療するための上記細胞を含む組成物に関する。
また、本発明は、TVEMF−バイオリアクターの培養チャンバー中に血液混合物を配置する工程、及びTVEMF−バイオリアクター中で、血液混合物を、TVEMF胞にさらして血液幹細をTVEMF−増殖させ、TVEMF−増殖した血液幹細胞及び幹細胞組成物を調製する工程によって、皮膚、口腔及び耳の症状を治療するための幹細胞及び幹細胞組成物を調製するためのプロセスに関する。好ましくは、細胞に適用されるTVEMFは、約0.05〜約6.0ガウスである。また、本発明は、1年以上、−120℃〜−196℃に低下させる工程、及び、その後該温度を、該細胞の哺乳動物への導入に適切な温度まで上昇させる工程によって、増殖した幹細胞を凍結保存する方法に関する。
また、本発明としては、このような治療が必要である口腔、耳、及び/又は皮膚の治療のための本発明の組成物の使用、又はその治療のための医薬の調製のための本発明の組成物の使用が含まれる。
[図面の詳細な説明]
最も単純な表現において、回転TVEMF−生物反応器には、細胞培養チャンバー及び時間変動する電磁気力の供給源が含まれる。実施においては、血液混合物を細胞培養チャンバーに配置する。時間変動する電磁気力の供給源によって、チャンバー内で時間変動する電磁気力が発生するまで細胞培養チャンバーを回転させる。その期間が終了すると、TVEMF−増殖された血液混合物をチャンバーから取り出す。より複雑なTVEMF−生物反応器システムにおいては、図2〜5に示すように、時間変動する電磁気力の供給源をTVEMF−生物反応器と一体化することができるが、図6〜8のように、バイオリアクター(生物反応器)と隣接させてもよい。さらに、培養液又はバッファ(好ましくは、後述するように、血液混合物に添加される該培養液と似ているもの)など栄養を細胞にもたらす流動性キャリアは、定期的に新しくする及び除去することができる。好ましいTVEMF−生物反応器をここで説明する。
最も単純な表現において、回転TVEMF−生物反応器には、細胞培養チャンバー及び時間変動する電磁気力の供給源が含まれる。実施においては、血液混合物を細胞培養チャンバーに配置する。時間変動する電磁気力の供給源によって、チャンバー内で時間変動する電磁気力が発生するまで細胞培養チャンバーを回転させる。その期間が終了すると、TVEMF−増殖された血液混合物をチャンバーから取り出す。より複雑なTVEMF−生物反応器システムにおいては、図2〜5に示すように、時間変動する電磁気力の供給源をTVEMF−生物反応器と一体化することができるが、図6〜8のように、バイオリアクター(生物反応器)と隣接させてもよい。さらに、培養液又はバッファ(好ましくは、後述するように、血液混合物に添加される該培養液と似ているもの)など栄養を細胞にもたらす流動性キャリアは、定期的に新しくする及び除去することができる。好ましいTVEMF−生物反応器をここで説明する。
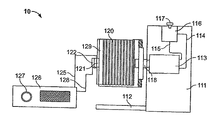
まず、図1を参照する。図1は、細胞培養チャンバー19、好ましくは回転細胞培養チャンバー、酸素供給器21、培養キャリアの方向性のある流れを助ける装置、好ましくは主ポンプ15を用いて、及び、これに限定されないが、栄養素3、バッファ5、新しい培地7、サイトカイン9、増殖因子11、及びホルモン13など培養キャリアの要求の選択的な入力のための供給マニホールド17を有する哺乳動物細胞を培養するための全体的なバイオリアクター培養系における培養キャリアフローループ1の好ましい実施形態を示す。この好ましい実施形態において、主ポンプ15は、新しい流動性キャリアを、流動性キャリアが酸素で処理され、細胞培養チャンバー19を通過する酸素供給器21へ供給する。細胞培養チャンバー19からの使用済みの流動性キャリア中の排出物は除去され、排出物18へ移送され、残りの細胞培養キャリアは、マニホールド17へ戻される。該マニホールド17は、必要であれば、再利用の前に、ポンプ15で酸素供給器21を経て細胞培養チャンバー19に、新しい供給を受ける。
培養キャリアフローループ1においては、図1に示すように、チャンバー19中の生きた細胞培養を通り、培養キャリアフローループ1を周って、培養キャリアは循環する。ループ1においては、細胞培養リアクターチャンバー19内を一定条件に維持する化学センサー(図示せず)に応じて調整が行われる。二酸化炭素の調整によって圧力を与え、酸又は塩基の導入によってpHを補正する。酸素、窒素及び二酸化炭素は、細胞呼吸をサポートするために、ガス交換システム(図示せず)に溶解されている。閉じたループ1には、循環ガスキャパシタンスから酸素が添加され、二酸化炭素を除去する。図1は、本発明で用いることができる培養キャリアフローループの1つの好ましい実施形態であるが、本発明はこれに限定されるものではない。バイオリアクターへの、これらに限定されないが、酸素、栄養素、バッファ、新しい培地、サイトカイン、増殖因子、及びホルモンなど培養キャリアの入力は、排出物及び二酸化炭素を制御及び除去することができるのであれば、手動、自動又は他の調整手段で行ってもよい。
図2及び図3に、一体の時間変動する電磁気力の供給源を有するTVEMF−生物反応器10の好ましい実施形態を示す。図4は、本発明で用いられる好ましい形態における回転可能なTVEMF−生物反応器10の断面図である。図4のTVEMF−生物反応器10は、一体の時間変動する電磁気力の供給源を有する状態で示されている。また、図5も一体の時間変動する電磁気力の供給源を有するTVEMF−生物反応器の好ましい実施形態を示す。図6〜8には、隣接する時間変動する電磁気力の供給源を有する回転バイオリアクターが示されている。
ここで図2を参照する。図2には、本発明のTVEMF−生物反応器10の好ましい実施形態の高側面図が示されている。図2には、ベース112に支持されたモータハウジング111が含まれる。モータ113はモータハウジング111内に取り付けられ、第1ワイヤー114及び第2ワイヤー115によって、制御つまみ117を回転することによってモータ113の速度を増加的に制御することができる制御手段を有するコントロールボックス116へ接続されている。モータハウジング111は、モータシャフト118がハウジング111を通って延在するように、内部にモータ113を有し、該モータシャフト118は、縦のチャンバー119において、シャフト118の中心が地面と平行になるように、長手方向にあり、これに限定されないが、プラスチックなど透明の材料で形成されていることが好ましい。
この好ましい実施形態において、縦のチャンバー119は、チャンバー119が、縦軸が地面と平行の状態で、自身の縦軸の周りを回転するように、シャフト118と連結されている。チャンバー119には、ワイヤーコイル120が捲回されている。ワイヤーコイル120のサイズ及び捲回数は以下のとおりである。好ましくは0.1mA〜1000mAの方形波電流がワイヤーコイル120へ供給される時、チャンバー119で、好ましくは0.05ガウス〜6ガウスの時間変動する電磁気力が発生する。ワイヤーコイル120は、シャフト118の端部において、ワイヤー123及び124によって第1リング121及び第2リング122と連結されている。そして、これらのリング121及び122は、電流がコイル120に絶えず供給されながらチャンバー119が回転できるように、第1電磁気供給ワイヤー125及び第2電磁気供給ワイヤー128によって接続されている。電磁気発生装置126は、ワイヤー125及び128と連結されている。電磁気発生装置126は、電磁気発生装置ノブ127を回すことによって出力を調整することで、方形波をワイヤー125及び128、及びコイル120に供給する。
図3は、本発明において用いることができる図2に示すTVEMF−生物反応器10の側面斜視図である。
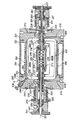
ここで、図4に示す回転TVEMF−生物反応器10を参照する。回転TVEMF−生物反応器10は、好ましくは透明の培養チャンバー230であって、血液混合物を含有するように構成されているものを有し、さらに内側円筒状ガラス部材293及び外側円筒状ガラス部材294を受け入れるように配置された、対向する第1及び第2端面228、229を有する第1及び第2円筒状横端キャップ部材290、291を含む外側ハウジング220を含む。適切な圧力シールが付与される。内側及び外側円筒状部材293、294の間は、細胞の成長に適切な培養温度の確保に用いられる環状ワイヤーヒーター296である。ワイヤーヒーター296は、時間変動する電場を培養チャンバー230に供給するための、時間変動する電磁気力装置として用いることもできる。または、図5に示すように、別のワイヤーコイル144を時間変動する電磁気力の供給に使用することができる。第1端キャップ部材290及び第2端キャップ部材291は、チャンバー230内でより円滑な混合液の流れを促進するために、端面228、229を隣接する内側曲面を有する。第1端キャップ部材290、及び第2端キャップ部材291は、それぞれ、入力軸223及び出力軸225に回転自在に受け入れられる第1中央液移送軸頸292及び第2中央液移送軸頸295を有する。各移送軸頸294、295は、フランジを有し、端キャップ部材290、291の埋め込み式対の孔に設けられ、シャフト223、225との相対的な長手方向の動きに対して第1ロックワッシャ及びリング297及び第2ロックワッシャ及びリング298で取り付けられる。各軸顎294、295は、長手方向に延在し、周辺に配置された流路と連結されている中間環状凹部を有する。軸顎292、295の各環状凹部はそれぞれ、端キャップ部材290及び291の第1放射状流路278及び第2放射状流路279によって、第1入力カップリング203及び第2入力カップリング204と対になっている。放射状流路278又は279中のキャリアは、軸顎294又は295の第1環状凹部及び縦流路を通って流れ、キャリアは軸顎292、295を通じて、シャフト223、225の周囲で各軸顎292、295の端に接近することができる。
端キャップ部材290及び291には、入力軸223及び出力軸225において外側ハウジング220を相対的に支持するボールベアリングを含む第1管状ベアリングハウジング205及び第2管状ベアリングハウジング206が取り付けられている。第1ベアリングハウジング205には、外側ハウジング220に入力軸223及び出力軸225及び縦軸221の周囲における回転方向で回転する動きを与えるための、第1スプロケットギア210が取り付けられている。第1ベアリングハウジング205及び第2ベアリングハウジング206は、ワイヤーヒーター296の電気的取り出し設備、及び他のセンサーも有する。
内部フィルターアッセンブリ235には、長さに沿って穿孔又は開口を有する内側及び外側円筒状部材215、216が含まれ、穿孔を有する第1及び第2内部フィルターアッセンブリ端キャップ部材217、218を有する。内側円筒状部材215は、互いに係合する中央に位置する対の部分を有する2つの部材として形成され、各部分は、端キャップ217又は218に取り付けられている。外側円筒状部材216は、第1及び第2内部フィルターアッセンブリ端キャップ217の間に設けられている。
端キャップ部材217、218は、それぞれ、入力軸223及び出力軸225において回転可能に支持されている。内側部材215はピン及び嵌合溝219によって、出力軸225に回転可能に取り付けられている。10ミクロ織のポリエステル布224が、外側部材216の外面の上に配置され、両端でOリングに取り付けられている。内側部材215は、連結ピンで出力駆動軸225のスロットに取り付けられているため、出力駆動軸225は内側部材215を回転させることができる。内側部材215は、外側部材216を支持する第1及び第2端キャップ217、218で連結されている。出力軸225は、第1固定ハウジング240のベアリングを通って延在し、第1スプロケットギア241に連結している。図示されているように、出力軸225は、シールの間に位置する第1固定ハウジング240の第1ポート又は流路289から内側部材215へ、流動性キャリアの流れが内側部材215から固定ハウジング240を通って延在できるように、延在する管状ボア222を有する。
内部部材235のための第1及び第2端キャップ217、218の間、及び外側ハウジング220中の軸頸292、295の間には、ブレード部材50a及び50bのための第1及び第2ハブ227、226がある。入力軸223の第2ハブ226は、第2ハブ226が入力軸223と回転するように、ピン231で、入力軸223に連結されている。各ハブ227、226は、軸方向に延在する、ハブを通じてキャリアを伝送するための流路を有する。
入力軸223は、入力軸223の回転可能な支持のために、第2固定ハウジング260のベアリングを通って延在する。第2縦流路267は、入力軸223を通って、面板とハウジング260の間の第2環状凹部232に設けられたリテーニングワッシャ及びリングの中間地点へと延在する。第2端キャップ部材291の第3放射状流路272によって、凹部の流動性キャリアは、第2端キャップ部材291から流出することができる。図示されていないが、第3流路272は、パイピング及びY分岐接続部を通じて各流路278及び279に接続している。
図4に、第1軸に沿って延在する第1ボア237がチャンバー230の隅部233と交差し、制限のある開口部234が形成されたサンプルポートを示す。ボア237は、逆のボア及びネジ式リングを一端に有し、ネジ廻して円筒状のバルブ部材236を受け入れる。バルブ部材236には、開口部234を係合し、チャンバー230の内部へ少し突出するための先端が補助的に形成される。バルブ部材236のOリング243は封をする。第2軸に沿った第2ボア244は、Oリング243と開口部234との間で、第1ボア237と交差する。エラストマー又はプラスチックのストッパー245によって、第2ボア244は閉じられ、サンプルを取り除く皮下注射器で入ることができる。サンプルを取り除くには、バルブ部材236を後へ引き、開口部234及びボア244に近づく。そして、注射器を用いてサンプルを抽出し、開口部234は再び封止することができる。外部の汚染物質は、TVEMF−生物反応器10の内部に届かない。
実施において、キャリアは第2ポート又は流路266、シャフト流路、第3放射状流路272を介して第1放射状流路278及び第2放射状流路279へ、投入される。キャリアが軸頸292、294の縦流路を介してチャンバー230に入ると、キャリアはハブ227、226の端面228、229に突きあたり、放射状及び軸方向に、ハブ227、226の流路を通って分散する。ハブ227、226を通るキャリアは、端キャップ部材217、218に突きあたり、放射状に分散する。そのため、流入される流動性キャリアの流れは、放射状に縦軸221から外へ向かい、ドーナツ状に各端部から流れ、ポリエステル布224及びフィルターアッセンブリ235の開口部を通って流れ、流路266及び289を介して流出する。外側ハウジング220、チャンバー230、及び内部フィルターアッセンブリ235の回転速度及び回転方向を制御することによって、いかなる要望のタイプのキャリアの動きも得ることができる。しかしながら、主として重要なのは、絶え間ない新しい流動性キャリアの供給と共に、植物回転器の運転を得ることができるという事実である。
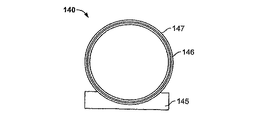
一体の環状ワイヤーヒーター296を用いて時間変動する電磁気力が付与されていない場合には、他の好ましい時間変動する電磁気力の供給源で付与することができる。例えば、図6〜8に、バイオリアクターの細胞培養に電磁力を供給する時間変動する電磁気力装置140であって、一体の時間変動する電磁気力ではなく、隣接する時間変動する電磁気力装置を有するものを示す。具体的に、図6は、時間変動する電磁気力装置140の好ましい実施形態である。図6は、装置140の高側面図斜視図であって支持基盤145、基盤145上に支持されたシリンダーコイル支持体146であって、支持体146の周囲に捲回されたワイヤーコイル147を有するものを含む。図7は、図6に示された時間変動する電磁気力装置140の正面斜視図である。図8は時間変動する電磁気力装置140の正面斜視図であって、実施において、支持基盤145に支持され、ワイヤーコイル147で捲回されたシリンダーコイル支持体146に、バイオリアクター148全体が挿入されたものが示されている。時間変動する電磁気力装置140がバイオリアクター148と隣接しているため、時間変動する電磁気力装置140は再利用することができ、さらに、時間変動する電磁気力装置140がバイオリアクター148に隣接しているため、装置140は、いかなる種類のバイオリアクター、好ましくは回転式においても、電磁力の発生に用いることができる。
実施において、TVEMF−増殖中、本発明のTVEMF−生物反応器10は、細胞培養チャンバーに血液混合物を含有する。TVEMF−増殖中、血液混合物含有チャンバーの回転速度を評価して調整することができ、これにより血液混合物は実質的に縦軸又はその周囲に残る。回転速度の増加は、壁の衝撃の予防に値する。例えば、血液混合物中の血液幹細胞が、回転円の下方側に、非常に内に向って且つ下に向って落下する場合、及び、回転円の上方側に、非常に外に向って且つ非効率的に上に向かって落下する場合には、回転の増加が好ましい。最適には、好ましくは操作者が、血液幹細胞の三次元形状及び細胞間支持及び細胞間形状が維持されるように、最小壁衝突回数及び強度を促進する回転速度を選択するとよい。本発明の好ましい速度は5〜120RPMであり、より好ましくは10〜30RPMである。
血液混合物は、好ましくは透明の培養チャンバーを通して目視で評価し、手動で調整されることが好ましい。また、血液混合物の評価及び調整は、TVEMF−生物反応器10における血液幹細胞の位置を監視するセンサー(例えば、レーザー)で自動に行われてもよい。多すぎる細胞の動きを示すセンサーの読み取りは、それに応じてメカニズムに回転速度を自動的に調整させる。
さらに、実施において、本発明は、電磁発生装置が作動され、方形波出力が血液混合物含有チャンバーに所望の電磁場を生じさせ、好ましくは0.05ガウス〜6ガウスの範囲となるように調整されることを意図する。
好ましくは、方形波の波長が約2〜約25サイクル/秒、より好ましくは約5〜約20サイクル/秒、例えば、約10サイクル/秒であり、コンダクターのRMS値が、約1〜1000mA、好ましくは1〜6mAである。しかしながら、これらのパラメータは、本発明の他の態様に基づいて変化するため、本発明のTVEMFを限定するものではない。TVEMFは、例えば、ENl 31 セルセンサーガオスメータ(Cell Sensor Gauss Meter)など一般的な装置によって測定することができる。
本発明で意図する時間変動する電磁気力に適用される回転バイオリアクターに対しては、本発明の範囲から逸脱しない範囲で、様々な変更を加えることができるため、上述した明細書に含まれる全ての事項は、限定としてではなく、説明として解釈される。
[発明を実施するための最良の形態]
本発明は、ヒトにおける皮膚、口腔、及び耳の組織、特にその中に含まれる上皮組織を治療、補充及び再生する方法に関する。
本発明は、ヒトにおける皮膚、口腔、及び耳の組織、特にその中に含まれる上皮組織を治療、補充及び再生する方法に関する。
本発明は、以下に記載するように、好ましい実施形態によってより十分に説明されるが、それに限定されるものではない。
本発明の好ましい実施形態において、組織、特に皮膚、口腔及び耳の組織、特にその中の上皮組織の治療、交換及び再生において身体を助けることができる成熟幹細胞を調製する方法が説明されている。血球は、患者から取り除かれる。これらの細胞の下位個体群は現在、成熟幹細胞と呼ばれている。血球は、本明細書で説明する生物反応器に配置される。生物反応器の容器は、血球の懸濁液が三次元形状及び細胞間支持及び形状を維持できる速度で回転される。反応器に細胞が置かれている間、栄養が供給され、ホルモン、サイトカイン又は増殖因子に曝され、及び/又は遺伝子の組み換えが行われ、有害物質は好ましくは除去される。通常除去される有害物質は、死にかけの細胞の有毒な顆粒物質、顆粒球の有毒物質、及びマクロファージを含む血球からくるものである。これらの細胞の下位個体群は、大量の細胞を生みながら増殖する。細胞の増殖は、充分な期間、好ましくは7日間で少なくとも7倍に細胞が増殖するように制御される。そして、細胞は静脈内に又は治療する膵臓組織に直接又は隣接して注射され、身体の自然なシステムが組織を治療及び再生するようにする。
以下の定義は、本発明の文脈において定義された用語の説明及び理解を助けるものである。定義はこれらの用語を本明細書を通じた記載以下に限定するものではない。さらに、いくつかの定義がTVEMFに関して含まれるが、これに関する全ての定義は、互いに補完するように考えられるべきであり、互いに反するように解釈すべきでない。
本願において、「成熟幹細胞」は、未分化で、より分化された細胞を生じさせる多能性細胞を意味する。本発明に関して、成熟幹細胞は、好ましくはCD34+/CD38−である。また、成熟幹細胞は、体性幹細胞としても知られており、胎児に直接由来する胚幹細胞ではない。
本願において、「血液」は、哺乳動物における2つの主要な血液幹細胞の供給源である末梢血又は臍帯血を意味する。「末梢血」は全身の血液である。すなわち、哺乳動物において全身的に循環する又は循環した血液である。哺乳動物は胎児を意味しない。本発明の目的において、同じ循環ループの異なる部分に位置する末梢血を区別する必要はない。本願において、「臍帯血」は、胎児又は乳児の臍帯及び/又は胎盤からの血液を意味する。臍帯血は、知られる限りでは幹細胞の最も豊富な供給源の1つである。「臍帯」は、本発明の「臍帯血」を臍帯からの血液に限定するものではない。本願において、胎児又は乳児の胎盤の血液は、臍帯の血液と合流する。本発明の目的において、同じ循環ループにある異なる部分に位置する血液を区別する必要はない。典型的には、50〜100mlの臍帯血を出産直後に採集することができる。好ましくは、この血液の全てを本発明の治療方法に利用可能である。
本願において、「血球」は、血液からの細胞を意味する。「末梢血細胞」は、末梢血からの細胞を意味し、「臍帯血細胞」は、臍帯血からの細胞を意味する。複製可能な血球は、TVEMF−生物反応器でTVEMF−増殖を行い、本発明の組成物に存在することができる。
本願において、「血液幹細胞」は、血液からの成熟幹細胞を意味する。上述したように、血液幹細胞は成熟幹細胞であり、体性幹細胞としても知られ、胎児に直接由来する胚幹細胞ではない。好ましくは、本発明の血液幹細胞は、CD34+/CD38−細胞である。
本願において、「血液幹細胞組成物」又はその引用は、本発明の血液幹細胞であって、(1)体積当たりの数が、少なくとも天然に存在する血液源の7倍であり、天然に存在する血液幹細胞の幹細胞と同一又は極めて類似の三次元形状及び細胞間形状及び細胞間支持を有するもの、及び/又は、(2)TVEMF−増殖を行いながら上記三次元形状及び支持を維持しているものを意味する。本発明の血液幹細胞組成物の幹細胞には、医薬上許容しうる担体など種々の担体、血漿、血液、アルブミン、細胞培養液、増殖因子、銅キレート剤、ホルモン、バッファ、凍結保存剤又は他の物質が含まれる。本発明の血液幹細胞と元々の血液供給源(すなわち、末梢血、臍帯血、末梢血と臍帯血の混合又は他の血液)とを比較するために、天然に存在する血液を参照することが好ましい。しかしながら、そのような比較ができない場合には、天然に存在する血液において、本発明の血液幹細胞の情報源として、そのような血液、好ましくは同じ哺乳動物の種の血液の平均的な又は典型的な特徴を参照してもよい。
本発明の「薬学的な血液幹細胞組成物」は、哺乳動物、好ましくはヒトへの投与に好適な血液幹細胞組成物である。そのような組成物には、治療有効量の増殖した(好ましくはTVEMF−増殖した)血液幹細胞及び医薬上許容しうる担体が含まれる。増殖した血液幹細胞の治療有効量は(本明細書においても述べられている)、好ましくは少なくとも幹細胞1000個、より好ましくは少なくとも幹細胞104個、さらに好ましくは少なくとも幹細胞105個、よりさらに好ましくは少なくとも幹細胞107〜109、又は、幹細胞1012個など更に多くの幹細胞数である。そのような数の増殖した幹細胞の投与は、1回以上の投与であってもよい。本発明の増殖によって増殖した時に、本願に記載したように、患者に投与される幹細胞の数は、供給源の血液の元々ある幹細胞の数に制限される。理論に束縛されることはないが、投与後、身体に使用されなかった幹細胞は単に自然な身体システムによって除去されると考えられている。
本願において、「血液混合物」は、血液又は血球の、TVEMF−生物反応器(例えば、細胞培養チャンバー)に配置される細胞成長のための培地のような細胞増殖を可能とする物質との混合液を意味する。「血液混合物」血球は、単に血液全体を細胞培養液などの物質と混合することによって、血液混合物に存在させてもよい。また、血液混合物は、本明細書に記載されているように、「軟膜」など血液幹細胞を含有する血液からの細胞を調製することによって作製することができる。血液混合物は、CD34+/CD38−血液幹細胞及びダルベッコの培地(DMEM)を含むことが好ましい。少なくとも血液混合物の約半分がDMEMなどの細胞培養液であることが好ましい。
本願において、「TVEFM」は、「時間変動する電磁気力」を意味する。上述したように、本発明のTVEMFは、方形波(フーリエ曲線に従う)。好ましい方形波の振動数は、約10周期/秒であり、導体のRMS値が約1〜1000mA、好ましくは1〜6mAである。しかしながら、これらのパラメータは、本発明の他の形態に基づき変動するため、本発明のTVEMFを限定するものではない。TVEMFは例えば、EN131セルセンサーガウスメータ(Cell Sensor Gauss Meter)など一般的な装置で測定することができる。
本願において、「TVEMF−生物反応器」は、TVEMFが適用された回転バイオリアクターを意味し、上述した図面の詳細な説明により十分に説明されている。バイオリアクターに適用されるTVEMFは、好ましくは0.05〜6.0ガウス、好ましくは0.05〜0.5ガウスの範囲である。例えば、図2、3、4及び5のTVEMF−生物反応器の例(限定するわけではなく)を参照。単純な実施形態において、本発明のTVEMF−生物反応器は、含有する血液混合物を、適切なガウスレベルで回転させ(TVEMFを付与して)、その中の血球(幹細胞を含む)を増殖させる。好ましくは、TVEMF−生物反応器において成長培地(好ましくは添加剤と共に)を交換することができ、血液混合物に酸素を含ませることができる。TVEMF−生物反応器は、細胞を数日以上で成長させる機構を提供する。理論に束縛されることはないが、TVEMF−生物反応器では、TVEMFするために細胞をバイオリアクターに投入し、TVEMFが細胞を通過し、又は細胞に曝され、このようにしてTVEMF−増殖が行われる。TVEMF−増殖中のTVEMF−生物反応器の回転において、三次元形状及び細胞間支持及び細胞間形状を維持するために、壁面衝突の回数及び強度を最小限にする好ましい回転速度は5〜120rpm、より好ましくは、10〜30rpmである。
本願において、「TVEMF−増殖した血球」は、TVEMF−生物反応器に配置され、約0.05〜6.0ガウスのTVEMFが適用された後の体積当たり数が増加した血球を意味する。体積当たりの細胞の数の増加は、TVEMF−生物反応器における細胞複製の結果であり、細胞の合計数は増加する。体積当たりの細胞の数の増加は、明確に、単なる流動体の体積の低減、例えば、血液の体積を70mlから10mlへ低減し、それによりml当たりの細胞の数を増加することによるものではない。
本願において、「TVEMF−増殖した血液幹細胞」は、TVEMF−生物反応器に配置され、約0.05〜6.0ガウスのTVEMFが適用された後の体積当たり数が増加した血液幹細胞を意味する。体積当たりの幹細胞の数の増加は、TVEMF−生物反応器における細胞複製の結果であり、バイオリアクター中の幹細胞の合計数は増加する。体積当たりの幹細胞の数の増加は、明確に、単なる流動体の体積の低減、例えば、血液の体積を70mlから10mlへ低減し、それによりml当たりの幹細胞の数を増加することによるものではない。
本願において、「TVEMF−増殖」は、TVEMF−(回転)バイオリアクターでTVEMFの存在下、複製(分裂及び成長)する、TVEMF−生物反応器における細胞の段階を意味する。血液幹細胞(好ましくはCD34+/CD38−幹細胞)は、好ましくは、生物反応器内で、さらなる分化を行わずに複製し、本発明の増殖した全ての又は実質的に全てのCD34+/CD38−幹細胞が複製するが、分化しない。「実質的に全て」とは、少なくとも70%、好ましくは少なくとも80%、より好ましくは少なくとも90%、更に好ましくは少なくとも95%、より更に好ましくは少なくとも97%、最も好ましくは少なくとも99%のCD34+CD38−細胞が、TVEMF−増殖中に分化してCD34+/CD38−ではなくならないことを意味する。
本願において、「TVEMF−増殖」は、細胞を約0.05〜約6.0ガウスのTVEMFにさらして、TVEMF−生物反応器中の血球、好ましくは血液幹細胞の数を増加するプロセスを意味する。血液幹細胞の数の増加は、少なくとも体積当たりの数が元の血液供給源の少なくとも7倍であることが好ましい。本発明のTVEMF−生物反応器における血液幹細胞の増殖は、TVEMF−増殖前の血液幹細胞と実質的に同一の三次元形状及び細胞間支持及び細胞間形状を維持する又は有する血液幹細胞をもたらす。TVEMF−増殖の他の側面においては、本発明の血液幹細胞の優れた性質をもたらす。理論に束縛されることはないが、TVEMF−増殖は、三次元形状及び細胞間支持及び形状を維持する高濃度の血液幹細胞を提供するだけでない。理論に束縛されることはないが、TVEMFはTVEMF−増殖中のいくつかの幹細胞の性質に影響を与えることができる。例えば、遺伝子の成長促進する上向き調整、又は、遺伝子の成長を妨げる下向き調整である。全体として、TVEMF−増殖は、血液幹細胞の分化ではなく、成長を促進する結果となる。
本願において、「TVEMF−増殖した細胞」は、TVEMF−増殖のプロセスに提供された細胞を意味する。
本願において、「治療」、「補充」及び「再生」という用語が用いられている。これらの用語は、互いに排除するものではなく、むしろ細胞の治療全般に関係するものである。
本願において、皮膚、口腔又は耳の組織の治療、皮膚、口腔又は耳の疾患又は症状の治療への言及は、排除的ではなく、本明細書に記載した幹細胞の投与によって、組織を向上する組織の治療全般の目的に関係する。上皮細胞及び組織の補充及び治療は、これらの組織に関して好ましい。しかしながら、聴覚に関連する神経及び耳における聴覚損失の治療など別の形の治療をおこなってもよい。また、本発明において、例えば、皮膚及び口腔における結合組織及び/又は神経組織の治療が行われてもよい。
本発明は一つとして、症状として及び恐らく致命的である疾患又は症状に関係するが、本発明は、小規模な修復の治療、さらに、哺乳動物(好ましくはヒト)の健康に症状又は問題が見つかる前における、増殖した幹細胞の早期の導入による上記疾患又は症状の防止又は予防を含む。
本発明は一つとして、症状として及び恐らく致命的である疾患又は症状に関係するが、本発明は、小規模な修復の治療、さらに、哺乳動物(好ましくはヒト)の健康に症状又は問題が見つかる前における、増殖した幹細胞の早期の導入による上記疾患又は症状の防止又は予防を含む。
本願において、「有害物質」又は関係用語は、細胞、好ましくは血液幹細胞、又は患者に有害な物質を意味する。特に、「有害物質」は、死細胞、マクロファージ、血液において他とは異なる又は通常ではない物質(例えば、末梢血の鎌状細胞、臍帯血の母体血又は母体の尿、又は他の組織又は排出物)を意味する。他の有害物質は、本明細書中で説明されている。血液からのこれらの有害物質の除去は、従来技術、特に患者に血液製剤の導入に関する技術において知られている。
本願において、「骨髄のアフェレーシス療法」は、骨に針を挿入し、骨髄を抽出することを意味する。そのようなアフェレーシス療法は従来技術において広く知られている。
本願において、「自己移植」は、ドナー(増殖前の血液幹細胞の供給源)及び臓器被提供者が同じ哺乳動物である状況を意味する。本発明には、自己移植の皮膚、口腔、及び耳の組織の治療及び補充が含まれる。
本願において、「同種異系移植」は、ドナー(増殖前の血液幹細胞の供給源)及び臓器被提供者が同じ哺乳動物ではない状況を意味する。本発明には、同種異系移植の皮膚、口腔、及び耳の組織の治療及び補充が含まれる。
本願において、「CD34+」は、血球の表面の表面抗原(CD34)の存在を意味する。CD34プロテインは、発展の全ての状態の造血幹細胞の表面に存在する。
本願において、「CD38−」は、血球の表面の表面抗原(CD38)の欠乏を意味する。CD38は、本発明の幹細胞の表面に存在しない。
本願において、「細胞間形状」は、他の細胞との関係における細胞の間隔、間の距離及び物理的な関係など細胞の形状を意味する。例えば、本発明のTVEMF−増殖した幹細胞は、体内において互いに関係をもって留まる。例えば、そのような間隔が維持されない二次元の増殖容器とは対照的に、増殖した細胞は、細胞間の自然な間隔において結合している。
本願において、「細胞間支持」とは、ある細胞が隣接する細胞に与える支持を意味する。例えば、身体の中で、健康な組織及び細胞は他の細胞と、化学的な、ホルモンの、神経の(当てはまる場合、又は適切な場合)相互作用を維持する。本発明において、これらの相互作用は、通常に機能するパラメータ内で維持される。例えば、これは他の細胞に有害な又は損害を与えるシグナルを送信し始めないこと(天然の血液環境でそのようなことが行われる限り)を意味する。
本願において、「三次元形状」は、三次元の状態(自然状態と同じ又は非常に似ている)における細胞の形状を意味し、例えば、細胞が平らになる及び/又は伸長するペトリ皿の細胞成長に見られる二次元形状とは対照的である。
上記3つの定義のそれぞれにおいて、本発明の幹細胞における細胞間支持及び形状及び三次元形状の維持に関して、「実質的に同一」は、本発明のTVEMF−増殖した細胞に通常の形状及び指示がもたらされることによって、例えば、細胞が機能しない、又は組織を治療することができない、又は他の細胞に有害な又は害を及ぼすような変化をしない。
本発明によって提供される耳の機能及び再生をより充分に説明するために、以下の定義を提供する。
本願において、「外耳」又は関連する用語は、耳介、外耳道、及び鼓膜の外層を含む。音は外耳道に入る。鼓膜において、音エネルギー(空気圧の変化)は、鼓膜の動きの力学的エネルギーに変換される。
本願において、「中耳」又は関連する用語は、インピーダンス整合変成器として働き、外耳道における空気のインピーダンスを、内耳の外リンパのインピーダンスと整合させるものを意味する。
本願において、「内耳」又は関連する用語は、力学的エネルギーを基底膜の進行波パターンに変換できるものを意味する。最後のエネルギー変換がここで起こる。
本願において、「外有毛細胞」又は関連する用語には、約12000個の3つの横列の細胞が含まれる。外有毛細胞は、内有毛細胞よりも数がはるかに多いが、第8脳神経の聴覚部分からの神経繊維の神経支配の約5%のみを受ける。これらの細胞には、刺激に際して収縮し、進行波の動きに対する基底膜の応答を微調整するする筋様糸状体が含まれる。これらの調整された応答のために、健常な外有毛細胞は刺激後に鳴り響く。この「鳴り響き」が耳音響放射のための音響源となる。
本願において、「内有毛細胞」又は関連する用語は、約3500個の1つの横列の細胞である。これらの細胞は、第7脳神経の聴覚部分からの神経繊維の神経支配の約95%を受ける。これらの細胞は、ヒトの聴覚の発生を主に担う。内有毛細胞が喪失又は損傷された場合には、通常、重度から深刻な聴覚損失が生じる。
本願において、「内溝」又は関連する用語は、内有毛細胞に不活性な支持細胞である。
上記用語に言及した他の記述又は本願において用いられている他の用語は上記定義を限定するものではなく、前記定義に寄与してもよい。本発明の様々な態様に関係する情報は本願を通して提供され、含まれる部分のみに限定されないが、本発明全体の理解に寄与する。
本発明は、ヒトにおける内耳、皮膚及び口腔の組織を治療、補充及び再生するためのTVEMF−増殖した血液幹細胞の直ちに利用可能な供給源を提供することに関する。本発明は、以下に記載されるように、好ましい実施形態によってより充分に説明されるが、これに限定されるものではない。
上記用語に言及した他の記述又は本願において用いられている他の用語は上記定義を限定するものではなく、前記定義に寄与してもよい。本発明の様々な態様に関係する情報は本願を通して提供され、含まれる部分のみに限定されないが、本発明全体の理解に寄与する。
操作方法−TVEMF−増殖した血液幹細胞組成物の調製
本発明の好ましい実施形態において、皮膚、口腔又は耳の組織の治療、交換及び再生及び/又は内耳上皮細胞などの細胞の補充において身体を助けることができ、又は、口腔又は耳の症状の研究又は治療に有用であるTVEMF−増殖した血液幹細胞を調製する方法が説明されている。
本発明の好ましい実施形態において、皮膚、口腔又は耳の組織の治療、交換及び再生及び/又は内耳上皮細胞などの細胞の補充において身体を助けることができ、又は、口腔又は耳の症状の研究又は治療に有用であるTVEMF−増殖した血液幹細胞を調製する方法が説明されている。
この好ましい方法において、血液は、例えば、本願に記載のように、及び、従来技術として知られているように、好ましくは従来技術において知られる注射器によって、哺乳動物、好ましくは霊長類哺乳動物、より好ましくはヒトから採集される。血液は採集し、直ちに増殖及び用いてもよく、又は、使用のために増殖又は未増殖の形態で凍結保存してもよい。被験者を脅かさないと思われる量の血液のみをヒトから取り出す。好ましくは、約10〜約500mlの血液が採集されるが、より好ましくは100〜300ml、更に好ましくは150〜200mlである。本発明における血液の採集は、限定されないが、例えば、哺乳動物の血液を直接採集する、1又は複数の供給源から血液を溜める、例えば、「血液バンク」からの凍結保存した末梢血又は臍帯血、又は、さもなければ後の使用のために貯蔵された血液など商業的又は他の供給源から血液を取得するなど間接的に血液を収集するなど他の手段を含むことができる。
一般的に、哺乳動物から直接採集する時、1以上の注射器(好ましくは、抗凝血剤を含む)に採取する。血液は注射器に保存されても、他の容器に移送されてもよい。そして、血液はその成分ごと(白血球、赤血球及び血漿)に分離されてもよい。これは、遠心分離機(血液が分離するまで血液の容器を回転させる装置)又は沈澱(沈殿物を血液の容器に投入して血液を分離させる方法)によって行われる。第2に、血液が底部に赤血球(RBC)、中間部に白血球(WBC)、上部に血漿というように分離したら、白血球は保存のために取り除かれる。「軟膜」としても知られる中間層には、興味のある血液幹細胞が含まれる。血液の他の成分は不要である。いくつかの血液バンクにおいては、これが処理する範囲である。しかしながら、他のバンクは、続いて、WBCから単核球(この場合、白血球のサブセット)を除去することによって軟膜を処理する。皆がこの方法に賛成ではないが、保存する量を低減することができ、細胞を保存するため必要な低温窒素を低減することができる。
血球を分離する別の方法は、コベスペクトラ(Cobe Spectra)製細胞分離機などの分離機で、採集した血液の全てを1回以上(好ましくは3回)、連続的なフロー白血球搬出法で廻すことである。このような処理によって、1つの核を有する血球は他の血球から分離される。幹細胞は1つの核を有するグループの一部である。血球の分離の他の方法は従来技術において知られている。
血液サンプルからRBCを取り除くことが好ましい。人は同じHLA型を有するかもしれないが(幹細胞の移植に必要である)、同じ血液型ではないかもしれない。RBCを除去することによって、幹細胞移植に不都合な反応を最小限と留めることができる。したがって、RBCを除去することによって、幹細胞サンプルがより多くの人と適合する機会が多くなる。RBCは解凍された時に破裂することがあり、遊離ヘモグロビンを放出する。このタイプのヘモグロビンは、移植を受ける人の腎臓に深刻な影響を及ぼすことがある。さらに、幹細胞の生存能力は、RBCが破裂した時に低下する。
また、特に血液を低温保存する場合、又は他の哺乳動物に輸血する場合、HIV/AIDS、肝炎、白血病又は免疫障害など感染性又は遺伝的疾患を有していないか確認する検査が行われてもよい。血液にそのような疾患がある時は、廃棄されるか、将来の使用者が検討するようにリスクの記録を伴って血液が保存される。
また、本発明の別の実施形態においては、血球はドナーから得てもよい。採集の前に、ドナーはG−CSF(好ましい量は0.3ng〜5μg、より好ましくは1ng/kg〜100ng/kg、更に好ましくは5ng/kg〜20ng/kg、より更に好ましくは6ng/kg)を12時間ごとに3日間、続いて4日目に1度投与される。好ましい方法において、同量のGM−CSFも投与する。他の方法としてはGM−CSFのみの使用、又は、他の増殖因子分子、インターロイキンの使用である。それからドナーから血液を採集し、全て血液混合物に用いてもよいし、又は、最初に本願に記載のとおり細胞部分に分離して、幹細胞(CD34+/CD38−)を含む細胞部分は増殖される血液混合物の調製に用いる。細胞は、例えば、ドナーの血液全量を、3回コベスペクトラ(Cobe Spectra)製細胞分離機などの分離機で連続的なフロー白血球搬出法で廻すことによって分離することができる。増殖した幹細胞は、同じドナー(本明細書に記載の皮膚、口腔又は耳の治療を必要とするドナー)に再導入することが好ましい。しかし、本明細書に示す同種異系の導入を用いてもよい。他の採集前の投与は、いわゆる当業者には明らかである。
血液から赤血球が除去され、血液幹細胞を含む残りの細胞を、本明細書で説明するTVEMF−生物反応器(「血液混合物」参照)の適切な培地に配置することが好ましい。本発明のより好ましい実施形態においては、上述した「軟膜」(本明細書で説明する血液幹細胞を含む)のみをTVEMF−生物反応器に細胞材料として配置する。他の実施形態には、他の非幹細胞及び血液の成分を除き、異なる血液調製液を調製することが含まれる。そのような血液調製液は、ただ1つの血液成分として、CD34+/CD38−血液幹細胞を有してもよい。血液細胞の非幹細胞タイプの除去は、これに限定されないが、沈殿及び遠心分離など消極的な分離技術で行うことができる。多くの消極的な分離技術は、従来技術として知られている。しかし、積極的な分離技術を用いてもよく、本発明においては好ましい。血液の様々な成分を除去する方法及びCD34+/CD38−のための積極的な分離は、従来技術として知られており、所望の血液幹細胞を溶解させる又は不可逆的に傷つけない限り使用してもよい。例えば、CD34+/CD38−を分離するアフィニティー法を用いてもよい。好ましくは、上記「軟膜」を血液から調製し、その中のCD34+/CD38−細胞は、TVEMF−増殖のために軟膜から分離される。
採集された血液、又は上述した所望の細胞部分は、TVEMF−増殖が起こるように、TVEMF−生物反応器に配置しなければならない。上述したように、「血液混合物」には、TVEMF−生物反応器に配置される、血液(又は所望の細胞部分、例えば赤血球のない血液、又は好ましくは血液から分離されたCD34+/CD38−血液幹細胞)と、細胞の成長のための培地など細胞を増殖させる物質との混合液が含まれる。細胞培養基、細胞を成長及び増殖させる培地は従来技術として知られている。好ましくは、細胞増殖させる物質は細胞培養基であり、より好ましくはダルベッコの培地である。細胞培地の成分は、当然幹細胞を殺したり、ダメージを与えないものでなくてはならない。他の成分を、TVEMF−増殖前又はその最中に、血液混合物に添加してもよい。例えば、血液はダルベッコの培地と共にバイオリアクターに配置され、さらに5%(また、他の所望の量、例えば約1%〜約10%の範囲で)のヒト血清アルブミンが補充される。バイオリアクターに配置される前に、バイオリアクターの外又は中で、これらに限定されないが、増殖因子、銅キレート剤、サイトカイン、ホルモン及び他の物質TVEMF−増殖を促進する他の物質など血液混合物への他の添加剤を血液に添加してもよい。好ましくは、一人の個体から採集した血液の全量(好ましくは約10ml〜約500mlの量のヒトの血液、より好ましくは100ml〜約300ml、更に好ましくは約150〜約200mlの血液)に、ダルベッコの培地(DMEM)など細胞培養基、及び補助される5%ヒト血清アルブミンが混合され、TVEMF−増殖用の血液混合物が調製される。例えば、50〜100mlの血液サンプルには、好ましくは、約25〜約100mlのDMEM/5%ヒト血清アルブミンが用いられ、血液混合物の全量は、バイオリアクターに配置された時に約75〜約200mlである。一般的な規則として、収集する血液は多いほどよい。一人の個体からの採集が100mlを超える場合には、その血液の全てを使用することが好ましい。例えば、血液を溜めることによって(同じ又は異なる供給源から)、より大きい体積を利用できる場合には、1ダースを超えることが好ましい。血液の採集を溜め、一緒にTVEMF−増殖を行う時に、かん流TVEMF−生物反応器の使用は特に有用である。
本発明の銅キレート剤は、いかなる無害の銅キレート剤であってもよく、好ましくはペニシラミン又は塩酸トリエンチン、より好ましくはペニシラミンとしては、DMSOに溶解したD(−)−2−アミノ−3−メルカプトル−3−ブタン酸メチル(シグマ−アルドリッチ(Sigma-Aldrich))であって、約10ppmの血液混合物に添加したものである。銅キレート剤を哺乳動物に投与してもよいが、その場合、血液は直接哺乳動物から採集されたものとする。そのような投与は、哺乳動物から採血する1日以上前、より好ましくは2日以上前であることが好ましい。銅キレート剤の目的は、血液混合物に添加される場合、又は、血液ドナーの哺乳動物に投与する場合、又は両方の場合、TVEMF−増殖の前に血液中の銅の量を低減することである。理論に束縛されることはないが、利用可能な銅の量を低減することによってTVEMF−増殖が促進する可能性があると考えられている。
「TVEMF−生物反応器に配置する」は、限定されるものではなく、血液混合物はバイオリアクターの全く外で作成され、そして該混合物がバイオリアクター内に配置されてもよい。また、血液混合物はバイオリアクター内で完全に混合されてもよい。例えば、血液(又はその細胞部分)はバイオリアクターに配置され、バイオリアクターの中で、バイオリアクターに同時に添加して、又は血液の後にバイオリアクターに添加するかのいずれ
本発明の好ましい血液混合物には、以下が含まれる。血液サンプルの軟膜から分離されたCD34+/CD38−幹細胞、及び、CD34+/CD38−細胞と共に、全量で約150〜250ml、好ましくは約200mlであるダルベッコの培地。さらに好ましくは、G−CSF(顆粒球コロニー刺激因子)が血液混合物に含まれる。好ましくは、G−CSFは、血液混合物のTVEMF−増殖を刺激するのに充分な量存在する。より好ましくは、TVEMF−増殖前の血液混合物のG−CSFの量は、約25〜約200ng/mlの血液混合物であり、より好ましくは約50〜約150ng/ml、さらにより好ましくは約100ng/mlである。
TVEMF−生物反応器の容器(血液幹細胞を含む血液混合物を含有する)は、三次元形状及び細胞間支持及び細胞間形状を維持するために血液幹細胞が懸濁液となる速度で回転される。好ましくは、回転速度は5〜120rpm、より好ましくは、10〜30rpmである。これらの回転速度は、限定されるものではない。回転速度は、少なくとも生物反応器のタイプおよび細胞培養チャンバーのサイズ及び配置されるサンプルなどにも依存する。細胞がTVEMF−生物反応器中にある間、細胞には、栄養素及び新しい培地(例えば、DMEM及び5%ヒト血清アルブミン。流動キャリアについては上述の記載を参照)を与えること、ホルモン、サイトカイン、及び/又は増殖因子(好ましくはG−CSF)に触れさせること、有毒物質を除去することが好ましい。TVEMF−生物反応器中の血球から除去される有毒物質としては、死にかけの細胞の有毒な顆粒物質、顆粒球の有毒物質、及びマクロファージが含まれる。細胞のTVEMF−増殖は、好ましくは細胞が少なくとも7倍に増殖する(体積当たりの数の増加)ように制御されている。好ましくは、血液幹細胞(もし存在するのであれば、他の細胞も)は、少なくとも4日間、好ましくは約7〜約14日間、より好ましくは約7〜約10日間、さらに好ましくは約7日間、TVEMF−増殖を行う。TVEMF−増殖はTVEMF−生物反応器で160日間まで継続することができる。TVEMF−増殖は160日間よりも更に長く行われるかもしれないが、そのような長い増殖は、本発明の好ましい実施形態ではない。
好ましくは、TVEMF−増殖は、約26℃〜約41℃、より好ましくは約37℃のTVEMF−生物反応器で行われる。
TVEMF−増殖を行う細胞の増殖全体を監視する方法の1つとして、目視観察がある。血液幹細胞は、典型的には暗赤色である。血液混合物の作製に用いられた培地の色は、薄い又は透明であることが好ましい。バイオリアクターが回転し始め、TVEMFが印加されると、細胞は、好ましくはバイオリアクター容器の中央にクラスター化し、培地は着色した細胞のクラスターを取り囲む。酸素を含有させること及び他の栄養素を添加することによっては、バイオリアクターに設けられた視覚化する窓(典型的には透明なプラスチック)を通じて、しばしば細胞集合を視覚化する能力を弱めない。クラスターの形成は、幹細胞が三次元形状及び細胞間支持及び細胞間形状を維持することを助けるのに重要である。クラスターが散乱しているようであったり、細胞がバイオリアクター容器の壁面に接触し始めた場合には、回転速度を上げ(手動で又は自動的に)、中央に細胞集合が再び形成されるようにする。形成直後に行われる、目に見えるようにできる細胞集合の直径の測定は、後の塊の直径と比較し、TVEMF−生物反応器の細胞のおよその増加数を示すことができる。また、TVEMF増殖中の細胞の増加数の測定は、従来技術に知られているように様々な方法で行うことができる。自動センサーをTVEMF−生物反応器に設け、監視及びクラスターのサイズの増大を測定することができる。
TVEMF−増殖のプロセスは、例えば、細胞がバイオリアクター中でクラスターのままであるように細胞クラスターの形成を確認し、細胞クラスターが散乱し始めたらバイオリアクターの回転を増やす検査の専門家によって、注意深く監視される。バイオリアクター中の細胞クラスター及び血液混合物の粘度を監視する自動システムによって、細胞クラスターが監視されてもよい。細胞クラスターの粘度の変化は、TVEMF−増殖プロセスを開始してから早くても2日後に見られ、TVEMF−生物反応器の回転速度は、その時期くらいに増大されてもよい。TVEMF−生物反応器の速度は、TVEMF−増殖を通じて様々であってよい。TVEMF−増殖中の細胞がTVEMF−生物反応器の容器の側面に接触しないように、回転速度は適時に調整されることが好ましい。
また、検査の専門家は、TVEMF−増殖において、例えば1日1回又は2日に1回、手動で(例えば注射器を用いて)新しい培地及び好ましくは上述したような栄養素及び増殖因子など他の所望の添加剤をバイオリアクターに投入し、細胞の排泄物及び毒素を含有する古い培地を取り除いてもよい。また、新しい培地及び他の添加剤は、TVEMF−増殖中、自動的にTVEMF−生物反応器に汲み上げ、排泄物は自動的に除去されてもよい。
血液幹細胞は、TVEMF−生物反応器に配置され、TVEMF−増殖してから約7〜約14日で、元の数より少なくとも7倍に増加してもよい。好ましくは、TVEMF−増殖は約7〜10日続き、より好ましくは約7日続く。したがって、幹細胞の数の測定は、TVEMF−増殖中に行われなくてもよい。上述及び本願を通して記載されているように、TVEMF−増殖した本発明の血液幹細胞は、天然のTVEMF−増殖していない血液幹細胞と実質的に同一の三次元形状及び細胞間支持及び細胞間形状を有する。
TVEMF−増殖の完了において、TVEMF−生物反応器の細胞物質には、本発明の組成物に含まれる本発明の幹細胞が含有されている。更なる使用のために、組成物から様々な物質が除去されたり、添加される。本発明の別の実施形態は、組織、例えば、本願に記載したような組織を治療、補充及び再生するために、身体システム又は組織を助けるように機能する生体外の哺乳動物の血液幹細胞組成物に関する。組成物には、好ましくは、元々の血液の体積当たりの血液幹細胞の少なくとも7倍の体積当たりの量のTVEMF−増殖した血液幹細胞が含まれる。例えば、好ましくは、X個の血液幹細胞がTVEMF−生物反応器にある体積で配置された場合、TVEMF−増殖後、TVEMF−生物反応器の血液幹細胞の数は、少なくとも7X個である(増殖工程において細胞の除去がなければ)。少なくとも7倍であることは、本発明の実施に必要ではないが、この増殖は特に治療目的に好ましい。例えば、TVEMF−増殖した細胞は、必要に応じて、天然に存在する血液の血液幹細胞の数の2倍のみであってもよい。TVEMF−増殖した細胞は、天然に存在する血液中の血液幹細胞の数の体積当たり約4倍〜約25倍であることが好ましい。また、本発明は哺乳動物の血液幹細胞を含む組成物に関し、該血液幹細胞の体積当たりの数が哺乳動物の天然に存在する血液よりも少なくとも7倍であり、血液幹細胞が天然に存在する血液の幹細胞と基本的な同一の三次元形状及び細胞間支持及び細胞間形状を有する。本発明の組成物には、医薬上許容しうる担体、例えば、これに限定されないが、血漿、血液、アルブミン、細胞培養液、増殖因子、銅キレート剤、ホルモン、バッファ又は凍結保存剤が含まれる。「医薬上許容しうる担体」は、哺乳動物、好ましくはヒトに幹細胞を導入することができる薬剤である。そのような担体(キャリア)には、ここで記載した物質、特に輸血に用いられるいかなる物質、例えば血液、血漿、アルブミン、また生理食塩水又はバッファ(好ましくはアルブミンに補充されるバッファ)、好ましくは組成物が導入される哺乳動物からのものが含まれる。哺乳動物に組成物を「導入」することは、動物に組成物を「投与」することを意味する。本発明の幹細胞を哺乳動物に静脈内投与することが好ましい。しかし、従来において知られている他の投与方法を用いてもよい。特に、例えば、口腔もしくは耳、又は口腔もしくは耳の近くに直接注射すること、又は、皮膚への局所的投与、例えば、皮下注射が行われる。さらに、許容できるG−CSF量でそのような導入を行うことが好ましく、量としては、0.3ng〜5μg、より好ましくは1ng/kg〜100ng/kg、更に好ましくは5ng/kg〜20ng/kg、より更に好ましくは6ng/kgである。幹細胞の投与は一般的な技術として記載されている薬剤担体と共に行ってもよい。本発明の増殖する幹細胞の投与量は、治療有効量(後述)であって、好ましくは少なくとも幹細胞1000個、より好ましくは少なくとも幹細胞104個、更に好ましくは少なくとも幹細胞105個、更により好ましくは少なくとも幹細胞107〜109個、更により多くの幹細胞、例えば1012個である。このような数の増殖した幹細胞の投与は、1以上の回数に分けて行うことができる。本願に記載されたように、患者に投与される幹細胞の数は、本発明に従って増殖によって増加するため、供給源の血液で元々利用可能な幹細胞の数に制限される可能性がある。理論に束縛されることはないが、投与後身体に使用されなかった幹細胞は、単に自然な身体システムによって除去されると考えられている。「許容しうる担体」は、通常、TVEMF−増殖後、凍結保存前又は後、又は哺乳動物への導入(投与)前の、本発明の血液幹細胞が生存できる物質、すなわち細胞に有毒ではない物質を意味する。そのようなキャリアは従来技術において知られており、本願でそのような目的のために記載された物質など様々な物質を含んでよい。例えば、血漿、血液、アルブミン、細胞培養液、バッファ及び凍結保存剤は全て、本発明の許容しうる担体である。所望のキャリアは、ある程度所望の利用方法に依存する。
従来の他の増殖方法(いずれもTVEMFを使用しない)は、血液幹細胞の三次元形状及び細胞間支持を維持しながら、天然に存在する血液の血液幹細胞の量の少なくとも7倍となる血液幹細胞の増殖は提供しない。TVEMF−増殖した血液幹細胞は、元の臍帯血と実質的に同一の三次元形状及び細胞間支持及び細胞間形状を有する又は維持する。前記組成物には、TVEMF−増殖した血液幹細胞、好ましくはダルベッコの培地又は直ぐに凍結保存できる溶液の懸濁液の状態のTVEMF−増殖した血液幹細胞が含まれる。前記組成物には、例えば、死にかけの細胞及び有毒物質、顆粒球の中身及びマクロファージなど有毒な顆粒物質が含まれないことが好ましい。前記組成物は、−120℃〜−196℃に組成物の温度を低減し、治療又は他の用途に必要となるまで凍結保存組成物をその温度に維持することによって、TVEMF−増殖した血液幹細胞を含む凍結保存組成物としてもよい。後述するように、凍結保存前に組成物から有毒物質をできる限り除去することが好ましい。
本発明の別の実施形態は、凍結保存を行った又はTVEMF−増殖完了直後のTVEMF−血液幹細胞の薬剤組成物で、皮膚、耳及び口腔の組織を治療する及び関連する症状を治療するために、組織及び/又は細胞を再生する方法に関する。前記細胞は、哺乳動物の身体、好ましくはヒトの身体に導入され、例えば静脈内に又は直接治療される組織へ注射され、身体の自然システムに組織を治療及び再生させる。哺乳動物の身体に導入される前記組成物には有毒物質、及び、投与されたTVEMF−増殖した血液幹細胞に対して不利な反応をする可能性がある他の材料が含まれないことが好ましい。前記細胞は、特に、疾病が発生し、疾病にかかっていない細胞が必要である場合に、個人の血球が必要である治療又は研究において、治療又は研究に直ぐに利用可能である。後年聴覚損失が発症した人にとって、保存された増殖された末梢血又は臍帯血は有用である。
実施例I−TVEMF生物反応器における実際の細胞のTVEMF−増殖
末梢血を採集し、末梢血細胞を表1及び以下に示すとおり増殖した。
末梢血を採集し、末梢血細胞を表1及び以下に示すとおり増殖した。
A)細胞の採集及び維持
ヒトの末梢血(75ml;約0.75×106細胞/ml)を、上述した注射器によって、タイプI糖尿病を有する10人のヒトドナーから採集し、約75mlのイスコブ(Iscove)変形ダルベッコ(Dulbecco)培地(IMDM)(ギブコ社、グランドアイランド、ニューヨーク州(GIBCO, Grand Island, NY))に20%の5%ヒトアルブミン(HA)、100ng/mlの組み換えヒトG−CSF(アムゲン社、サウザンドオークス、カリフォルニア州(Amgen Inc., Thousand Oaks, CA))、及び100ng/mlの組み換えヒト幹細胞因子(SCF)(アムゲン社(Amgen))を追加したもので懸濁し、血液混合物を調製した。血液サンプル10個(各ドナーについて1つ)を参照サンプルとして取っておいた。末梢血液混合物を本明細書の図2及び図3に示すTVEMF−生物反応器に配置した。TVEMF−増殖は37℃、6%のCO2、通常の空気比O2/Nにおいて行った。TVEMF−生物反応器は1分当たり10回転(rpm)の速度で最初回転させ、その後必要に応じて本願に記載のとおり調整し、末梢血細胞の生物反応器における懸濁を維持した。生物反応器に6mAの時間変動する電流を印加した。末梢血液混合物に印加した方形波TVEMFは約0.5ガウスであった(約10回転/秒)。TVEMF−生物反応器の末梢血液混合物の培養基は、1〜2日に一度、変更又は新しくされた。10日目には、細胞をTVEMF−生物反応器から移動し、PBSで洗浄及び分析した。結果を表1に示す。参照データは、増殖しなかったヒト末梢血のサンプルを意味する。増殖サンプルは、TVEMF−増殖後のそれぞれの参照サンプルを意味する。
ヒトの末梢血(75ml;約0.75×106細胞/ml)を、上述した注射器によって、タイプI糖尿病を有する10人のヒトドナーから採集し、約75mlのイスコブ(Iscove)変形ダルベッコ(Dulbecco)培地(IMDM)(ギブコ社、グランドアイランド、ニューヨーク州(GIBCO, Grand Island, NY))に20%の5%ヒトアルブミン(HA)、100ng/mlの組み換えヒトG−CSF(アムゲン社、サウザンドオークス、カリフォルニア州(Amgen Inc., Thousand Oaks, CA))、及び100ng/mlの組み換えヒト幹細胞因子(SCF)(アムゲン社(Amgen))を追加したもので懸濁し、血液混合物を調製した。血液サンプル10個(各ドナーについて1つ)を参照サンプルとして取っておいた。末梢血液混合物を本明細書の図2及び図3に示すTVEMF−生物反応器に配置した。TVEMF−増殖は37℃、6%のCO2、通常の空気比O2/Nにおいて行った。TVEMF−生物反応器は1分当たり10回転(rpm)の速度で最初回転させ、その後必要に応じて本願に記載のとおり調整し、末梢血細胞の生物反応器における懸濁を維持した。生物反応器に6mAの時間変動する電流を印加した。末梢血液混合物に印加した方形波TVEMFは約0.5ガウスであった(約10回転/秒)。TVEMF−生物反応器の末梢血液混合物の培養基は、1〜2日に一度、変更又は新しくされた。10日目には、細胞をTVEMF−生物反応器から移動し、PBSで洗浄及び分析した。結果を表1に示す。参照データは、増殖しなかったヒト末梢血のサンプルを意味する。増殖サンプルは、TVEMF−増殖後のそれぞれの参照サンプルを意味する。
表1に見られるように、末梢血細胞のTVEMF−増殖においては、増殖しない参照サンプルと比較して、10日目過ぎに細胞数が約10倍に増加し、CD34+細胞においても対応するように増加したという結果であった。細胞が成長する培養基は1〜2日に一度変更又は新しくされた。
B)TVEMF−増殖した細胞の分析
血球計算板(ある量の参照サンプルの細胞懸濁液又は増殖サンプルを、マイクロ格子(micro grid)を有する特製顕微鏡用スライドに配置し、サンプル中の細胞数を数えることによって用いられる血球計などの装置)によって、参照サンプル及び増殖サンプルの細胞の総数を得た。TVEMF−増殖から10日後の参照サンプル及び増殖サンプルにおける細胞の合計数の結果を表1に示す。
血球計算板(ある量の参照サンプルの細胞懸濁液又は増殖サンプルを、マイクロ格子(micro grid)を有する特製顕微鏡用スライドに配置し、サンプル中の細胞数を数えることによって用いられる血球計などの装置)によって、参照サンプル及び増殖サンプルの細胞の総数を得た。TVEMF−増殖から10日後の参照サンプル及び増殖サンプルにおける細胞の合計数の結果を表1に示す。
表1における対応CD34+の増加の表示は、以下のように測定された。ヒューマンCD34セレクションキット(Human CD34 Selection Kit)(EasySep positive selection、ステムセルテクノロジーズ社(StemCell Technologies))によって、他の細胞から増殖サンプルのCD34+細胞を分離し、上述した血球計算板を用いて数え、FACScanフロー血球計算器(ベクトン−ディキンソン社(Becton-Dickinson))で確認した。クローン形成法でCFU−GEMM及びCFU−GMを数えた。トリパン青排除試験によって細胞の生存率(生存能力のある細胞が生存し、生存能力のない細胞が死亡している)を決定した。増殖サンプルにおける「有り」は、CD34+細胞の数が細胞の合計数に対応する量だけ増加したことを示す。
操作方法−口腔組織の治療
少なくとも15人の口腔手術(好ましくは歯肉手術)を受けるヒトの患者から末梢血(好ましくは約250ml)を回収し、例えば上述した実施例のようにTVEMF−増殖する。各ドナーの血漿も調製する。TVEMF増殖から10日後、TVEMF−増殖した細胞を生物反応器から移動し、5%ヒト血清アルブミンを含むヘパリン化生理食塩水で洗浄し、例えば、100ミクロンのナイロン網又は他の適当な濾過システムで濾過して細胞の凝集体を除去する。有害物質も除去する。続いて、後述するように、前記細胞を約1.0ml又は約20mlの各ドナーの血漿と混合し、全てのTVEMF−増殖した細胞をドナーの身体に自己移植導入するための薬学的な血液幹細胞組成物を調製する(同種異系の導入を用いてもよい)。好ましい導入する幹細胞の数は、本願に記載されているが、最も好ましくは約1ml又は約20mlの105〜109の幹細胞である。
少なくとも15人の口腔手術(好ましくは歯肉手術)を受けるヒトの患者から末梢血(好ましくは約250ml)を回収し、例えば上述した実施例のようにTVEMF−増殖する。各ドナーの血漿も調製する。TVEMF増殖から10日後、TVEMF−増殖した細胞を生物反応器から移動し、5%ヒト血清アルブミンを含むヘパリン化生理食塩水で洗浄し、例えば、100ミクロンのナイロン網又は他の適当な濾過システムで濾過して細胞の凝集体を除去する。有害物質も除去する。続いて、後述するように、前記細胞を約1.0ml又は約20mlの各ドナーの血漿と混合し、全てのTVEMF−増殖した細胞をドナーの身体に自己移植導入するための薬学的な血液幹細胞組成物を調製する(同種異系の導入を用いてもよい)。好ましい導入する幹細胞の数は、本願に記載されているが、最も好ましくは約1ml又は約20mlの105〜109の幹細胞である。
すでに歯肉手術を受けている5人のドナーにおいて、歯肉手術によって損傷した組織に隣接する口腔組織に、1mlの血漿及びTVEMF−増殖した血球を含む血液幹細胞組成物を直接注射する。他の5人のドナーにおいては、20mlの血漿及びTVEMF−増殖した血液幹細胞を含む血液幹細胞組成物を、ドナーの末梢血の血流に注射する。
これらの実験から予測される結果は、口腔外科医によってモニターされる回復は、細胞治療をしない患者よりも実質的に時間が短いことである。
上述した条件下で動物モデルに行われる実験が、組織学的又は病理学的分析、又は必要に応じて他の分析において、本発明を用いた口腔組織の治療によって、本発明の組成物の投与後に関連する症状、疾患又は治療の目的が向上する旨を示すことが予測される。
操作方法−皮膚組織の治療
少なくとも15羽のウサギから末梢血(好ましくは、約50ml)を回収し、例えば上述した実施例のようにTVEMF−増殖する。各ドナーの血漿も調製する。採集した血液の約40mlのTVEMF増殖から10日後、TVEMF−増殖した細胞を生物反応器から移動し、5%ヒト血清アルブミンを含むヘパリン化生理食塩水で洗浄し、例えば、100ミクロンのナイロン網又は他の適当な濾過システムで濾過して細胞の凝集体を除去する。有害物質も除去する。
少なくとも15羽のウサギから末梢血(好ましくは、約50ml)を回収し、例えば上述した実施例のようにTVEMF−増殖する。各ドナーの血漿も調製する。採集した血液の約40mlのTVEMF増殖から10日後、TVEMF−増殖した細胞を生物反応器から移動し、5%ヒト血清アルブミンを含むヘパリン化生理食塩水で洗浄し、例えば、100ミクロンのナイロン網又は他の適当な濾過システムで濾過して細胞の凝集体を除去する。有害物質も除去する。
次いで、前記TVEMF−増殖した細胞組成物の中の5つを、市販のネオスポリン(ワーナー・ランバート社(Warner-Lambert))と混合して(好ましくはすべての細胞を、約1ml〜約100ml、好ましくは約10ml〜約50ml、この場合、約15mlのネオスポリン)、局所的投与のための薬学的な血液幹細胞組成物を調製する。各ウサギに、互いに近傍であるが接触しない、皮膚を擦過した2つのパッチを与える(すなわち、皮膚の層を除去する擦り傷であって深い創傷ではない)。好ましくは、擦過が存在する(同種異系の導入を用いてもよいが、本実施例は自己移植導入に言及する)。好ましい導入する幹細胞の数は、本願に記載されているが、最も好ましくは105〜109の幹細胞である。局所的投与のための薬学的な組成物は、1つの擦過部に直接的投与する。他方の擦過部にはネオスポリンのみを投与する。
前記幹細胞組成物で覆われている擦過部は、ネオスポリンのみで覆われている部分の半分未満の時間で治癒することが予測される。
ドナーの中の5羽において、上述のように洗浄されたTEMF−増殖した血液幹細胞組成物を、5mlのドナー自身の血漿中に再懸濁し、静脈内注射のための薬学的な血液幹細胞組成物を調製する。該組成物を、各ドナーの末梢血の血流に直接注射する。残りの5羽のドナーにおいては、実験対照の血漿のみをネオスポリンと混合し、血漿をドナーの血流に注射する。また、薬学的な血液幹細胞組成物を注射する場合には、各ウサギの2つの擦過部の中の一方をネオスポリンで覆い、他方を医薬で覆わない。
薬学的な幹細胞組成物が注射されるウサギの擦過部が、血漿の注射のみを受けているドナーウサギの半分未満の時間で治癒することが予測される。
動物モデル又は皮膚の治療が望まれる他の状況における実験が、組織学的又は病理学的分析、又は必要に応じて他の分析において、本発明を用いた皮膚組織の治療によって、本発明の組成物の投与後に関連する症状、疾患又は治療の目的が向上する旨を示すことが予測される。
また、上記操作方法は、約100mlの末梢血の採集からスタートして、同様に皮膚を擦過したヒトに対して実施されることが予測される。薬学的な幹細胞組成物を注射された又は局所的に投与された擦過部は、同様の擦過部を有するが血漿のみ注射されているヒトよりも、半分未満の時間で治癒することが予測される。
(操作方法−耳組織の治療)
聴覚損失を有する少なくとも5人のヒト患者(「ドナー」)から末梢血(好ましくは、約100ml)を採集する(注射器を用いて取り出す)。好ましくは、採血する前に、ドナーを、12時間毎に3日間、4日目は1回、G−CSF 6ng/kgで処理し、4日目に採血する。末梢血細胞を、コベスペクトラ(Cobe Spectra)製細胞分離機などの分離機で、3回のラウンドの連続的なフロー白血球搬出法で廻す。また、各ドナーからの血漿も調製する。該血液細胞は、上記実施例1に記載したように、同量のIMDM(分離した血液の量と同様)と混合して血液混合物を調製し、次いで、また上記実施例1に記載したように、TVEMF−増殖する。10日間のTVEMF増殖後、TVEMF−増殖した細胞をバイオリアクターから取り出し、5%ヒト血清アルブミンを含むヘパリン化生理食塩水で洗浄し、例えば、100ミクロンのナイロン網又は他の適切な濾過システムで濾過して細胞の凝集体を除去する。有害物質も除去する。
聴覚損失を有する少なくとも5人のヒト患者(「ドナー」)から末梢血(好ましくは、約100ml)を採集する(注射器を用いて取り出す)。好ましくは、採血する前に、ドナーを、12時間毎に3日間、4日目は1回、G−CSF 6ng/kgで処理し、4日目に採血する。末梢血細胞を、コベスペクトラ(Cobe Spectra)製細胞分離機などの分離機で、3回のラウンドの連続的なフロー白血球搬出法で廻す。また、各ドナーからの血漿も調製する。該血液細胞は、上記実施例1に記載したように、同量のIMDM(分離した血液の量と同様)と混合して血液混合物を調製し、次いで、また上記実施例1に記載したように、TVEMF−増殖する。10日間のTVEMF増殖後、TVEMF−増殖した細胞をバイオリアクターから取り出し、5%ヒト血清アルブミンを含むヘパリン化生理食塩水で洗浄し、例えば、100ミクロンのナイロン網又は他の適切な濾過システムで濾過して細胞の凝集体を除去する。有害物質も除去する。
細胞をドナー自身の血漿中に再懸濁し、薬学的な血液幹細胞組成物を調製する。次いで、各ドナーに投与する。ドナーの中の3人においては、少量の増殖した細胞を、一方の耳の内耳上皮有毛細胞に直に隣接する耳組織に注射する。他の2人のドナーについては、少量の増殖した細胞を、一方の耳の脳底動脈に注射する。
本発明の薬学的な幹細胞組成物を用いる処置後、機能的な内耳上皮有毛細胞の顕著な増加、好ましくは3〜20倍の増加があること、及び、約1ヶ月以内の間に、聴力が実質的に改善することが予測される。
上記条件下の動物モデルにおける実験が、組織学的又は病理学的分析、又は必要に応じて他の分析において、本発明を用いた耳組織の治療によって、本発明の組成物の投与後に関連する症状、疾患又は治療の目的が向上する旨を示すことが予測される。
操作方法−凍結保存
上述したように、哺乳動物、好ましくはヒトから血液を採集する。少なくとも赤血球を血液から除去することが好ましい。血液幹細胞(必要であれば、他の細胞及び培地と共に)は、TVEMF−生物反応器に配置され、TVEMFされ、増殖する。RBCがTVEMF−増殖前に除去されない場合には、TVEMF−増殖後に除去されることが好ましい。TVEMF−増殖した細胞は、低温で保存される。TVEMF−増殖した血液幹細胞の凍結保存の方法及びそのような細胞を含む組成物に関する更なる詳細は、本明細書に記載されており、特に以下に記載する。
上述したように、哺乳動物、好ましくはヒトから血液を採集する。少なくとも赤血球を血液から除去することが好ましい。血液幹細胞(必要であれば、他の細胞及び培地と共に)は、TVEMF−生物反応器に配置され、TVEMFされ、増殖する。RBCがTVEMF−増殖前に除去されない場合には、TVEMF−増殖後に除去されることが好ましい。TVEMF−増殖した細胞は、低温で保存される。TVEMF−増殖した血液幹細胞の凍結保存の方法及びそのような細胞を含む組成物に関する更なる詳細は、本明細書に記載されており、特に以下に記載する。
TVEMF−増殖後、TVEMF−増殖した血液幹細胞を含むTVEMF−増殖した細胞は、少なくとも1つの凍結保護剤を含有する少なくとも1つの凍結保存容器に移送されることが好ましい。TVEMF−増殖した血液幹細胞は、まず好ましくは溶液(例えば、バッファ溶液又は所望の凍結保存剤の溶液)で洗浄してTVEMF−増殖中に存在した培地及び他の成分を除去し、好ましくは細胞を凍結保存可能な溶液に混合する。このような溶液は、一般的に、凍結保存剤、凍結保存溶液又は凍結保護剤と呼ばれる。前記細胞は適切な低温容器に移され、該容器の温度は通常−120℃〜−196℃、好ましくは約−130〜約−150℃に低減され、その温度が維持される。凍結工程において幹細胞にダメージを与えない、又はダメージを最小限にするように、温度の低減はゆっくりと慎重に行われることが好ましい。必要であれば、細胞の温度(およそ低温容器の温度)は、ヒトの身体への導入に適合する温度(通常およそ室温からおよそ体温)に上昇され、TVEMF−増殖した細胞は、例えば上述したように哺乳動物の身体、好ましくはヒトの身体に導入されてもよい。
凍結した細胞は通常有害である。理論に束縛されることはないが、冷却において、細胞中の水が凍る。この時、細胞膜における浸透圧効果、細胞内脱水、溶質濃度、及び氷晶生成によって損傷が生じことがある。細胞の外側が結氷するため、やがて細胞の破壊に至る浸透脱水及び溶質濃度の上昇を引き起こす水を溶液から除去及び細胞から取り出す(内容の詳細はマズールP.(Mazur, P.)、1977年、クリオバイオロジー(Cryobiology)14、251〜272参照)。
異なる材料は異なる氷点を有する。結晶化及び凍結工程における細胞壁のダメージを最小限に抑えるために、直ちに凍結保存できる血液幹細胞組成物には、可能な限り汚染物質が含まれていないことが好ましい。
これらの有害な影響は、次の方法で低減又は回避することができる。(a)凍結保護剤の使用、(b)凍結速度の制御、及び(c)分解反応を最小限に留める十分に低い温度での保存。
本発明においては、凍結保存剤を含有させることが好ましい。使用可能な凍結保護剤には、これに限定されないが、十分な量ジメチルスルホキシド(DMSO)(ラブロックJ.E.(Lovelock, J. E.)及びビショップM.W.H(Bishop, M. W. H.)、1959、ネイチャー(Nature)183、1394〜1395;アッシュウッド−スミスM.J.(Ashwood-Smith, M. J.)、1961、ネイチャー(Nature)190、1204〜1205)、グリセロール、ポリビニルピロリジン(フィンフレットA.P.(Rinfret, A. P.)、1960、Ann.N.Y.Acad.Sci.85、576)、ポリエチレングリコール(スロビターH.A.(Sloviter, H. A.)及びラドビンR.G.(Ravdin, R. G.)、1962、ネイチャー(Nature)196、548)、アルブミン、デキストラン、スクロース、エチレングリコール、i−エリスリトール、D−リビトール、D−マニトール(ロウェA.W.ら(Rowe, A. W. et al.)、1962、Fed.Proc.21、157)、D−ソルビトール、i−イノシトール、D−ラクトース、塩化コリン(ベンダーM.A.ら(Bender, M. A., et al.)、1960、J.Appl.Physiol.15、520)、アミノ酸−グルコース溶液又はアミノ酸(Phan The Tran and Bender、M.A.、1960、Exp.Cell Res.20、651)、メタノール、アセトアミド、グリセリンモノアセタート(ラブロックJ.E.(Lovelock, J. E.)、1954、バイオケミ.J.(Biochem. J.)56、265)、及び無機塩(Phan The Tran and Bender、M.A.、1960、Proc.Soc.Exp.Biol.Med.104、388;Phan The Tran and Bender、M.A.、1961、放射線生物学、放射線生学に関する第3回オーストラリア会議の手続き(Proceedings of the Third Australian Conference on Radiobiology)、イルベリーP.L.T.(Ilbery, P. L. T.)編、バッターウォルス(Butterworth)、ロンドン、p.59)。好ましい実施形態においては、DMSOが用いられている。液体のDMSOは低濃度では細胞に害はない。小さい分子であるため、DMSOは自由に細胞を通り抜け、凍結性を緩和するために水と結合して細胞内の細胞小器官を保護し、結氷からのダメージを防止する。血漿の添加(例えば、20〜25%の濃度まで)によって、DMSOの保護効果を増大させることができる。4℃を超えるとDMSO濃度が約1%であると有害であるため、DMSOの添加後、細胞は0℃に保たれていなければならない。好ましい凍結保護剤は、全組成物において、TVEMF−増殖した血液幹細胞との組み合わせで、60〜80%アミノ酸−グルコース溶液中の20〜40%ジメチルスルホキシド溶液、15〜25%ヒドロキシエチルでんぷん溶液、4〜6%グリセロール、3〜5%グルコース、6〜10%デキストランT10、15〜25%ポリエチレングリコール、又は75〜85%アミノ酸−グルコース溶液である。上記凍結保護剤の量は、組成物における凍結保護剤の総量(単に組成物に添加した物質の量ではなく)であることが好ましい。
本発明の凍結保存する組成物には、血球及び凍結保護剤以外の他の物質が含まれてもよいが、例えば上述した凍結のメカニズムにおいて述べた理由により、本発明のTVEMF−増殖した血液幹細胞組成物の凍結保存においては、可能な限り他の物質が少ないことが好ましい。
本発明のTVEMF−増殖した血液幹細胞組成物は、約−120℃〜約−196℃、好ましくは約−130℃〜約−196℃、より好ましくは約−130℃〜約−150℃の範囲の温度に冷却することが好ましい。
ゆっくりとした冷却速度に制御することは重要である。異なる凍結保護剤(ラパズG.ら(Rapatz, G., et al.)、1968、低温生物学(Cryobiology)5(1)、18〜25)及び異なる細胞タイプは、最適な冷却速度が異なる(例えば、冷却速度の体皮細胞の生存に対する影響(及びそれらの移植の可能性)について、ロウA.W.(Rowe, A. W.)及びリンフレットA.P.(Rinfret,A. P.)、1962、血液20、636;ロウA.W.(Rowe, A. W.)、1966、低温生物学(Cryobiology)3(1)、12〜18;ルイスJ.P.ら(Lewis, J. P., et al.)、1967、輸血(Transfusion)7(1)、17〜32;及びマズールP.(Mazur, P.)、1970、サイエンス(Science)168、939〜949を参照)。水が氷に変る融解熱は最小限にすべきである。冷却工程は、例えば、プログラムで制御できる凍結装置又はメタノールバス手法を用いて行うことができる。
プログラムで制御できる凍結装置によって、最適な冷却速度を決定することができ、再現可能な標準的な冷却を促進することができる。クリオメッド(Cryomed)又はプラナー(Planar)などのプログラムで制御された速度の冷蔵庫は、凍結管理を、望ましい冷却速度曲線に調整することができる。その他の条件を満たした冷凍庫は、例えば、サンヨー製Modl MDF−1155ATN−152C及びModel MDF−2136ATN−135C、プリンストン(Princeton)製CryoTech TEC 2000が挙げられる。例えば、血球、又は、10%DMSO及び20%血漿のCD34+/CD38−細胞において、最適な速度は1〜3℃/分で0℃〜−200℃である。
好ましい実施形態においては、この冷却速度は本発明の細胞に用いることができる。細胞を有する低温容器は、低温で安定していなければならず、冷却及び解凍の効果的な制御のために速い熱伝導が可能である。複数の少量(1〜2ml)に、封止されたプラスチックの小瓶(例えば、ヌンク(Nunc)、ウィートン クリウレ(Wheaton cryules))又はガラスアンプルを用いることができる。一方、より大きい容量(100〜200ml)は、冷却時のよりよい熱交換のために金属板で挟まれたポリオレフィンバッグの中で(例えば、デルメッド(Delmed))凍結することができる(骨髄細胞のバッグは、骨髄細胞のバッグを、冷却速度約3℃/分である−80℃の冷凍庫に置くことによって思いがけずうまく凍結することができる)。
別の実施形態においては、メタノールバスの冷却手法を用いることができる。メタノールバス手法は、大規模に複数の少量を繰り返し凍結保存する場合に非常に適している。この方法には、凍結速度の手動制御も速度を監視するレコーダーも必要ない。好ましい形態においては、DMSO-治療された細胞は、予め氷で冷却され、冷却したメタノールを含むトレーに、次に、メタノールバスの−130℃の機械冷蔵庫(例えば、ハリス(Harris)又はレボコ(Revco))に移送される。メタノールバス及びサンプルの熱電対測定は、望ましい冷却速度1〜3℃/分を示す。少なくとも2時間後、検査サンプルの温度は−80℃に達し、永久保存のために液体窒素(−196℃)に直接配置してもよい。
完全な凍結後、TVEMF−増殖した幹細胞は、直ぐに長期凍結保存容器(例えば冷凍庫)に移される。好ましい実施形態において、細胞は、液体窒素(−196℃)又はその気体(−165℃)の中に低温で保存することができる。保存温度は、−120℃未満、好ましくは−130℃未満とすべきである。このような保存は、高効率な液体窒素冷蔵庫の利用によってより促進される。該液体窒素冷蔵庫は、大きな魔法瓶容器のようであり、熱もれ及び窒素のもれが極めて最小限に維持されるように、非常に低い真空で、優れた内部断熱材を有する。
細胞の凍結保存のための好ましい装置及び手順は、テルモジェネシス(Thermogenesis Corp.)(ランチョ コルドボ(Rancho Cordovo、カリフォルニア州)で製造されているものであり、彼らの細胞の温度を−130℃未満に低減する手順を利用する。細胞は、凍結及び保存中、テルモジェネシス社の血漿バッグに保持される。
他の冷蔵庫が商業的に入手可能である。例えば、「バイオアーカイブ(BioArchive)」冷凍庫は、凍結するだけでなく、本発明の血液や細胞などの低温サンプルの目録を作成し、例えば、凍結した血液の3,626個のバッグを一度に管理することができる。この冷凍庫は、指示に応じて特定のサンプルを取り出すロボットアームを有し、他のサンプルが温かい温度に阻害される又は曝されないようにする。その他の商業的に入手可能な冷凍庫としては、限定されないが、サンヨー製Modl MDF−1155ATN−152C及びModel MDF−2136ATN−135C、プリンストン(Princeton)製CryoTech TEC 2000が挙げられる。
TVEMF−増殖した血液幹細胞組成物の温度が−120℃未満、好ましくは−130℃未満に降下された後、テルモジェネシス社の冷凍庫などの装置に保持される。温度は約−120℃〜−196℃、好ましくは−130℃〜−150℃に維持される。本発明の凍結保存TVEMF−増殖した血液幹細胞組成物の温度は、長期間約−120℃を超えるべきではない。
本発明の凍結保存したTVEMF−増殖した血液幹細胞又はその組成物は、不定期間、凍結することができ、必要な時に解凍することができる。例えば、組成物は18年まで凍結することができる。さらに長い期間は可能であり、おそらく血液ドナーの一生と同じくらいの期間が可能である。
必要である時には、テルモジェネシス社(Thermogenesis)の血漿解凍器、又は、テルモリン社(Thermoline)の解凍器シリーズなど他の装置などの解凍システムに、細胞の入ったバッグを置いてもよい。凍結保存組成物の温度は、室温に上昇される。凍結保護剤と混合した細胞の解凍の他の好ましい方法において、液体窒素中で凍結保存した本発明のTVEMF−増殖した血液幹細胞組成物を有するバッグを、15分間液体窒素の気相に放置し、5分間外気室温にさらし、最後に37℃のウォーターバスで可能な限り素早く解凍してもよい。解凍されたバッグの中身は、直ちに同量の2.5%(重量/体積)ヒト血清アルブミン及び5%(重量/体積)デキストラン40(ソルプレックス40(Solplex 40)、シフラ(Sifra)、ヴェロナ(Verona)、イタリア)を含むアイソトニック塩溶液を含有する溶液で希釈され、続いて400gで10分間、遠心分離機にかけられる。浮遊物は除去され、沈殿した細胞は、アルブミン/デキストラン溶液で再度沈澱される。高圧力の抗凍結剤の除去については、ルビンスタインP.ら(Rubinstein, P. et al.)、「無関係な骨髄の再構成のための胎盤/臍帯血の処理及び凍結保存」(Processing and cryopreservation of placental/umbilical cord blood for unrelated bone marrow reconstitution)、Proc.Natl.Acad.ScL92、10119〜1012(1995)を参照。細胞の解凍の好ましい方法のバリエーションについては、ラザッリLら(Lazzari, L. et al.)、「臍帯血からの造血系幹細胞の生体外増殖における凍結保存の効果の向上(Evaluation of the effect of cryopreservation on ex vivo expansion of hematopoetic progenitors from cord blood)。骨髄移植28、693〜698(2001)を参照。
細胞の温度が室温に上げられた後は、細胞は研究又は再生治療に利用可能である。解凍されたTVEMF−増殖した血液幹細胞組成物は、直接哺乳動物、好ましくはヒトに導入することができ、又は、解凍された状態で所望の研究に用いることができる。解凍した細胞を含む溶液は、必要であれば、完全に洗浄して、他と交換してもよく、又は、操作してもよい。哺乳動物の身体に導入する前に、好ましくはそのような導入の直前に、種々の添加剤を解凍された組成物に添加することができる(又は、非凍結保存のTVEMF−増殖した血液幹細胞組成物に)。そのような添加剤としては、これらに限られないが、増殖因子、銅キレート剤、サイトカイン、ホルモン、好適なバッファ又は希釈剤が含まれる。好ましくは、G−CSFが添加される。より好ましくは、ヒトにおいて、約20〜約40μg/kg体重の量、より好ましくは約30μg/kg体重の量のG−CSFが添加される。また、導入の前に、TVEMF−増殖した血液幹細胞組成物は、哺乳動物自身の又は適合するドナーの血漿、血液又はアルブミン、又は輸血に付随する他の材料と混合してもよい。解凍された血液幹細胞は、例えば、治療に用いることが望ましい又は治療に用いることができる薬剤に不利な反応がないか確認する試験に用いることができる。
アメリカ合衆国ではFDAが増殖した血液幹細胞の組織の再生への使用を認めていないが、そのような認可は間近であると思われる。増殖された血液幹細胞の十分な量の直接注射は、本願に記載し皮膚、耳、及び口腔の組織の再生に用いることができる。
本発明のTVEMF−増殖した血液幹細胞組成物は、哺乳動物、好ましくはヒトに、組織の治療又は再生の達成、又は、所望の疾病又は状態の治療に十分な量を導入すべきである。好ましくは、少なくとも20mlの、ml当たり107〜109の幹細胞を有するTVEMF−増殖した血液幹細胞組成物が様々な治療に用いられ、特に外傷が発生し早急な組織の治療が必要である場合に、一度に用いることが好ましい。この量は特に75〜80kgの人間において好ましい。哺乳動物に導入される組成物におけるTVEMF−増殖した血液幹細胞の量は、本質的に供給源の血液材料に存在する細胞の数(特に、極めて限られた量しか利用可能でない場合)に関係する。患者に導入されるTVEMF−増殖した血液幹細胞の好ましい範囲は、例えば、ml当たり107〜109の幹細胞を有するTVEMF−増殖した血液幹細胞組成物を約10ml〜約50ml、又は潜在的にそれ以上である。哺乳動物に投与されるいかなる物質が高濃度であることは、有害又は致命的であると理解されているが、TVEMF−増殖した血液幹細胞の全てを導入することが、例えばTVEMF−増殖後に少なくとも7倍、TVEMF−増殖した血液幹細胞の投与のし過ぎとはなりにくい。数人のドナーの血液、又は同じドナーの複数の採集が用いられる場合には、哺乳動物に導入される血液幹細胞の数は増加してもよい。また、患者に導入してもよいTVEMF−細胞の量は、1人の個体から採集した血液の量に限定されない。複数の投与、例えば1日1回、1日2回、1週間に1回、又はその他の回数の投与は、より容易に用いることができる。また、組織が治療される時には、組織の種が、利用可能なTVEMF−増殖した血液幹細胞の使用、又はより少ない投与量の使用を保証する。例えば、肝臓が最も治療しやすく、他の組織よりも必要とする幹細胞が少ないことが多い。
当然ながら、上記実施形態は、広くTVEMF−増殖した血液幹細胞の凍結保存に関し、凍結保存された、又は、増殖されていない、又は、非TVEMF−増殖の血液幹細胞の解凍後に、TVEMF−増殖を行ってもよい。また、凍結保存が望まれるのであれば、TVEMF−増殖は細胞の凍結前及び後に行われてもよい。例えば、血液バンクは、必要な時に備えて、凍結保存された血液幹細胞を含む凍結保存組成物を有する。そのような組成物は従来の方法で解凍され、その後、本明細書に記載のようにTVEMF−増殖されてもよく、本明細書に記載のTVEMF処理のバリエーションを含む。その後、そのようなTVEMF−増殖した血液幹細胞は、上述したように、本発明の組成物と考えられる。例えば外傷が生じた時に、患者の血液幹細胞が既に増殖され、調製にさらに貴重な日を要しないために、凍結保存前のTVEMF−増殖が好ましい。
また、好ましくはないが、注目すべきは、TVEMF−増殖した本発明の血液幹細胞は、凍結保存、及びその後解凍され、その後使用しなければ、再度凍結保存してもよい。凍結する前に細胞をTVEMF−増殖する(すなわち数の増加であってサイズではない)ことが好ましい。たとえ凍結前に増殖されたとしても、凍結し、その後解凍された後、細胞を増殖してもよい。
血液幹細胞の増殖には数日かかることがある。生死に関わる状況又は外傷の場合など血液幹細胞の早急な供給が重要である状況において、特に、細胞の再導入の前に検査を完了する必要がある場合には血液幹細胞の増殖に数日も待てないかもしれない。したがって、毎分の治療の遅れが生死を違える緊急事態に備えて出生からそのような増殖した血液幹細胞を用意することが特に望ましい。
また、当然ながら、本願のTVEMF−増殖した血液幹細胞は、TVEMF−増殖後、凍結保存して又は凍結保存せずに、哺乳動物、好ましくは哺乳動物の供給源(血液の供給源である哺乳動物)に導入してもよい。しかしながら、そのような導入は、元々の哺乳動物(自己移植)に限られる必要はない。TVEMF−増殖した細胞は、異なる哺乳動物(同種移植)に移転してもよい。
また、当然のことながら、血液(臍帯血(好ましくは凍結保存されたもの)又は末梢血(好ましくは新しく採集されたもの)は本発明の成熟幹細胞の好ましい供給源であるが、骨髄からの成熟幹細胞をTVEMF−増殖し、本発明の血液幹細胞と同様に用いてもよい。骨髄は幹細胞の直ちに利用可能な供給源ではないが、アフェレーシス療法、又は他の高価で苦痛を伴う方法で収集しなければならない。
また、本発明には、皮膚、口腔、又は耳の聴覚の症状又は他の病状、病状を研究する方法であって、病状の試験系にTVEMF−増殖した幹細胞を導入する工程を含むものが含まれる。そのような系としては、限定されないが、例えば、疾患を有する哺乳動物、疾患を研究するための適切な動物モデル、又は疾患を研究するための体外試験系が含まれる。TVEMF−増殖した血液幹細胞を、いわゆる当業者が周知であるような種々の病状の治療可能性の研究に用いてもよい。
増殖、保存、及び解凍の全ての工程の間、本発明の血液幹細胞は、三次元形状、細胞間支持、及び細胞間形状を維持する。
本願において好ましい実施形態を説明したが、いわゆる当業者は、種々の変更及び改良が含まれることを理解するであろう。本発明の範囲は、上述した実施形態に限定されるものではない。
Claims (35)
- 天然に存在する血液よりも少なくとも7倍多い、体積あたりの数の増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を含む、上皮組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 天然に存在する血液よりも少なくとも2倍多い、体積あたりの数のTVEMF−増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を含む、上皮組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 前記体積あたりのTVEMF−増殖した血液幹細胞の数が少なくとも7倍多いことを特徴とする、請求項2に記載の方法。
- 天然に存在する血液よりも少なくとも7倍多い、体積あたりの数の増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を含む、皮膚組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 天然に存在する血液よりも少なくとも2倍多い、体積あたりの数のTVEMF−増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を包含する、皮膚組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 前記体積あたりのTVEMF−増殖した血液幹細胞の数が少なくとも7倍多いことを特徴とする、請求項5に記載の方法。
- 前記投与する工程が、局所的、静脈内注射、及び皮下注射の少なくとも1つの投与方法を介する薬学的な血液幹細胞組成物の投与を含むことを特徴とする、請求項6に記載の方法。
- 前記哺乳動物がヒトであることを特徴とする、請求項7に記載の方法。
- 前記投与する工程の前に以下の工程を更に含むことを特徴とする、請求項5に記載の方法:
a.TVEMF−バイオリアクターの培養チャンバー中に血液混合物を配置する工程;
b.TVEMF−増殖した血液幹細胞の体積あたりの数が、TVEMF−バイオリアクター中に配置された血液幹細胞の体積あたりの数の7倍よりも多くなるまで、該TVEMF−バイオリアクター中で、該血液混合物をTVEMFにさらし、該血液幹細胞をTVEMF−増殖させる工程;及び
c.該TVEMF−増殖した細胞を薬学的に受容可能なキャリアと混合して、薬学的な血液幹細胞組成物を形成する工程。 - 前記TVEMF−増殖した細胞から有害物質を除去する工程を更に含むことを特徴とする、請求項9に記載の方法。
- 前記血液混合物が、他の血液成分から分離されたCD34+/CD38−血液幹細胞を含むことを特徴とする、請求項9に記載の方法。
- 天然に存在する血液よりも少なくとも7倍多い、体積あたりの数の増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を含む、口腔組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 天然に存在する血液よりも少なくとも2倍多い、体積あたりの数のTVEMF−増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を含む、口腔組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 体積あたりのTVEMF−増殖した血液幹細胞の数が少なくとも7倍多いことを特徴とする、請求項13に記載の方法。
- 前記投与する工程が、局所的、静脈内注射、及び歯肉組織への注射の少なくとも1つの投与方法を介する薬学的な血液幹細胞組成物の投与を含むことを特徴とする、請求項14に記載の方法。
- 前記哺乳動物がヒトであることを特徴とする、請求項15に記載の方法。
- 前記投与する工程の前に以下の工程を更に含むことを特徴とする、請求項13に記載の方法:
a.TVEMF−バイオリアクターの培養チャンバー中に血液混合物を配置する工程;
b.TVEMF−増殖した血液幹細胞の体積あたりの数が、該TVEMF−バイオリアクター中に配置された血液幹細胞の体積あたりの数の7倍よりも多くなるまで、該TVEMF−バイオリアクター中で、該血液混合物をTVEMFにさらし、該血液幹細胞をTVEMF−増殖させる工程;及び
c.該TVEMF−増殖した細胞を薬学的に受容可能なキャリアと混合して、薬学的な血液幹細胞組成物を形成する工程。 - 前記TVEMF−増殖した細胞から有害物質を除去する工程を更に含むことを特徴とする、請求項17に記載の方法。
- 前記血液混合物が、他の血液成分から分離されたCD34+/CD38−血液幹細胞を含むことを特徴とする、請求項17に記載の方法。
- 天然に存在する血液よりも少なくとも7倍多い、体積あたりの数の増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を含む、内耳組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 天然に存在する血液よりも少なくとも2倍多い、体積あたりの数のTVEMF−増殖した血液幹細胞を含む薬学的な血液幹細胞組成物の治療有効量を哺乳動物に投与する工程を包含する、内耳組織を治療する方法であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする方法。
- 体積あたりのTVEMF−増殖した血液幹細胞の数が少なくとも7倍多いことを特徴とする、請求項2に記載の方法。
- 前記投与する工程が、局所的、静脈内注射、及び歯肉組織への注射の少なくとも1つの投与方法を介する薬学的な血液幹細胞組成物の投与を含むことを特徴とする、請求項22に記載の方法。
- 前記哺乳動物がヒトであることを特徴とする、請求項23に記載の方法。
- 前記投与する工程の前に以下の工程を更に包むことを特徴とする、請求項21に記載の方法:
a.TVEMF−バイオリアクターの培養チャンバー中に血液混合物を配置する工程;
b.TVEMF−増殖した血液幹細胞の体積あたりの数が、前記TVEMF−バイオリアクター中に配置された血液幹細胞の体積あたりの数の7倍よりも多くなるまで、該TVEMF−バイオリアクター中で、該血液混合物をTVEMFにさらし、該血液幹細胞をTVEMF−増殖させる工程;及び
c.該TVEMF−増殖した細胞を薬学的に受容可能なキャリアと混合して、薬学的な血液幹細胞組成物を形成する工程。 - 前記TVEMF−増殖した細胞から有害物質を除去する工程を更に含むことを特徴とする、請求項25に記載の方法。
- 前記血液混合物が、他の血液成分から分離されたCD34+/CD38−血液幹細胞を含むことを特徴とする、請求項25に記載の方法。
- 天然に存在する血液よりも少なくとも7倍多い体積あたりの数のTVEMF−増殖した血液幹細胞を含む、哺乳動物の上皮組織を治療するための薬学的な血液幹細胞組成物であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする組成物。
- 天然に存在する血液よりも少なくとも7倍多い体積あたりの数のTVEMF−増殖した血液幹細胞を含む、哺乳動物の皮膚組織を治療するための薬学的な血液幹細胞組成物であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする組成物。
- 天然に存在する血液よりも少なくとも7倍多い体積あたりの数のTVEMF−増殖した血液幹細胞を含む、哺乳動物の口腔組織を治療するための薬学的な血液幹細胞組成物であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする組成物。
- 天然に存在する血液よりも少なくとも7倍多い体積あたりの数のTVEMF−増殖した血液幹細胞を含む、哺乳動物の内耳組織を治療するための薬学的な血液幹細胞組成物であって、該血液幹細胞は、天然に存在する血液の幹細胞と本質的に同じである三次元形状及び細胞間支持及び細胞間形状を有することを特徴とする組成物。
- 上皮組織の治療のための医薬の調製における請求項28に記載の組成物の使用。
- 皮膚組織の治療のための医薬の調製における請求項29に記載の組成物の使用。
- 口腔組織の治療のための医薬の調製における請求項30に記載の組成物の使用。
- 内耳組織の治療のための医薬の調製における請求項31に記載の組成物の使用。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US65728805P | 2005-02-28 | 2005-02-28 | |
| US65754505P | 2005-02-28 | 2005-02-28 | |
| US65728305P | 2005-02-28 | 2005-02-28 | |
| PCT/US2006/006876 WO2006093881A2 (en) | 2005-02-28 | 2006-02-27 | Method and composition for repairing epithelial and other cells and tissue |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008531698A true JP2008531698A (ja) | 2008-08-14 |
| JP2008531698A5 JP2008531698A5 (ja) | 2009-04-09 |
Family
ID=36941695
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007558102A Pending JP2008531698A (ja) | 2005-02-28 | 2006-02-27 | 上皮及び他の細胞及び組織を治療するための方法及び組成物 |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US20060193837A1 (ja) |
| EP (1) | EP1853282A4 (ja) |
| JP (1) | JP2008531698A (ja) |
| KR (1) | KR20070111532A (ja) |
| BR (1) | BRPI0608294A2 (ja) |
| CA (1) | CA2601306A1 (ja) |
| EA (1) | EA200701598A1 (ja) |
| IL (1) | IL185556A0 (ja) |
| WO (1) | WO2006093881A2 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20070114378A (ko) * | 2005-02-28 | 2007-12-03 | 리제네텍 인코포레이티드 | 말초혈액으로부터 유도된 쉽게 이용가능한 세포 물질을 제공하는 방법 및 그의 조성물 |
| US20090081752A1 (en) * | 2007-09-24 | 2009-03-26 | Dennis Robert G | Bioreactor, kit and method of using same |
| US8993231B2 (en) * | 2008-03-18 | 2015-03-31 | Marshall University Research Corporation | Methods for stem cell production and therapy |
| US10617721B2 (en) | 2013-10-24 | 2020-04-14 | Ospedale San Raffaele S.R.L. | Methods for genetic modification of stem cells |
| US9410143B1 (en) | 2014-06-10 | 2016-08-09 | Endonovo Therapeutics, Inc. | Biological molecules produced by electromagnetically stimulating living mammalian cells |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002044346A2 (de) * | 2000-11-29 | 2002-06-06 | William Rader | Stammzellen, verfahren zu deren expansion in vitro sowie deren verwendung |
| US20040076620A1 (en) * | 2002-09-03 | 2004-04-22 | Donnie Rudd | Method of repairing primate mammalian tissue |
| WO2004045666A1 (ja) * | 2002-11-15 | 2004-06-03 | Kyushu Tlo Company, Limited. | 臓器の再生方法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000508922A (ja) * | 1996-04-26 | 2000-07-18 | ケース ウエスターン リザーブ ユニバーシティ | 間葉幹細胞を用いる皮膚再生 |
| US6962698B1 (en) * | 1998-02-17 | 2005-11-08 | Gamida Cell Ltd. | Methods of controlling proliferation and differentiation of stem and progenitor cells |
| US6485963B1 (en) * | 2000-06-02 | 2002-11-26 | The United States Of America As Represented By The Administrator Of The National Aeronautics And Space Administration | Growth stimulation of biological cells and tissue by electromagnetic fields and uses thereof |
| US7498171B2 (en) * | 2002-04-12 | 2009-03-03 | Anthrogenesis Corporation | Modulation of stem and progenitor cell differentiation, assays, and uses thereof |
| NZ542127A (en) * | 2003-02-13 | 2008-04-30 | Anthrogenesis Corp | Use of umbilical cord blood to treat individuals having a disease, disorder or condition |
| WO2005007799A2 (en) * | 2003-07-17 | 2005-01-27 | Gamida-Cell Ltd. | Methods for ex-vivo expanding stem/progenitor cells |
| US20050084962A1 (en) * | 2003-08-20 | 2005-04-21 | Bruce Simon | Methods of treatment using electromagnetic field stimulated stem cells |
| US20080057042A1 (en) * | 2005-01-27 | 2008-03-06 | Donnie Rudd | Method of providing readily available cellular material derived from cord blood, and a composition thereof |
| US20080050348A1 (en) * | 2006-02-27 | 2008-02-28 | Donnie Rudd | Method and composition for repairing heart tissue |
| US20080075700A1 (en) * | 2006-02-27 | 2008-03-27 | Wolf David A | Method and composition for treating diabetes |
-
2006
- 2006-02-27 JP JP2007558102A patent/JP2008531698A/ja active Pending
- 2006-02-27 US US11/363,592 patent/US20060193837A1/en not_active Abandoned
- 2006-02-27 CA CA002601306A patent/CA2601306A1/en not_active Abandoned
- 2006-02-27 WO PCT/US2006/006876 patent/WO2006093881A2/en active Application Filing
- 2006-02-27 BR BRPI0608294-7A patent/BRPI0608294A2/pt not_active IP Right Cessation
- 2006-02-27 KR KR1020077021369A patent/KR20070111532A/ko not_active Application Discontinuation
- 2006-02-27 EP EP06736235A patent/EP1853282A4/en not_active Withdrawn
- 2006-02-27 EA EA200701598A patent/EA200701598A1/ru unknown
-
2007
- 2007-08-20 US US11/894,150 patent/US20080171020A1/en not_active Abandoned
- 2007-08-28 IL IL185556A patent/IL185556A0/en unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002044346A2 (de) * | 2000-11-29 | 2002-06-06 | William Rader | Stammzellen, verfahren zu deren expansion in vitro sowie deren verwendung |
| US20040076620A1 (en) * | 2002-09-03 | 2004-04-22 | Donnie Rudd | Method of repairing primate mammalian tissue |
| WO2004045666A1 (ja) * | 2002-11-15 | 2004-06-03 | Kyushu Tlo Company, Limited. | 臓器の再生方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EA200701598A1 (ru) | 2008-02-28 |
| IL185556A0 (en) | 2008-01-20 |
| US20080171020A1 (en) | 2008-07-17 |
| BRPI0608294A2 (pt) | 2010-01-12 |
| WO2006093881A2 (en) | 2006-09-08 |
| WO2006093881A3 (en) | 2007-11-29 |
| KR20070111532A (ko) | 2007-11-21 |
| US20060193837A1 (en) | 2006-08-31 |
| EP1853282A2 (en) | 2007-11-14 |
| EP1853282A4 (en) | 2010-04-28 |
| CA2601306A1 (en) | 2006-09-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20070117087A1 (en) | Method of providing readily available cellular material derived from peripheral blood, and a compositoin thereof | |
| JP2008528034A (ja) | 直ぐに利用可能な臍帯血から誘導される細胞物質、及びその組成物の提供方法 | |
| JP5775667B2 (ja) | 臍帯血幹細胞の増殖および成長因子産生のリチウム刺激の方法 | |
| US20060193836A1 (en) | Method and composition for repairing heart tissue | |
| JP2008531698A (ja) | 上皮及び他の細胞及び組織を治療するための方法及び組成物 | |
| JP2008531695A (ja) | 糖尿病の治療の方法及び組成物 | |
| AU2013259255B2 (en) | Trehalose-containing mammalian cell suspension for prevention of pulmonary embolism formation | |
| WO2009025827A1 (en) | Method and composition for repairing epithelial and other cells and tissue | |
| CN101166820A (zh) | 用于修复上皮和其它细胞及组织的方法和组合物 | |
| WO2007058929A2 (en) | Composition for reducing problems associated with sickle cell disease using low temperature storage | |
| CN101160046A (zh) | 提供容易获得的源于外周血的细胞材料的方法及其组合物 | |
| CA2597971A1 (en) | Method and composition for repairing epithelial and other cells and tissue | |
| JP2023550328A (ja) | トロンビン処理幹細胞に由来したエクソソームを含む感染性疾患治療用組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090219 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090219 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110913 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120228 |