JP2008526318A - 器官および組織の細胞再形成促進 - Google Patents
器官および組織の細胞再形成促進 Download PDFInfo
- Publication number
- JP2008526318A JP2008526318A JP2007549596A JP2007549596A JP2008526318A JP 2008526318 A JP2008526318 A JP 2008526318A JP 2007549596 A JP2007549596 A JP 2007549596A JP 2007549596 A JP2007549596 A JP 2007549596A JP 2008526318 A JP2008526318 A JP 2008526318A
- Authority
- JP
- Japan
- Prior art keywords
- tissue
- cells
- donor
- human
- organ
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000000056 organ Anatomy 0.000 title claims abstract description 413
- 238000007634 remodeling Methods 0.000 title description 12
- 210000004027 cell Anatomy 0.000 claims abstract description 548
- 238000000034 method Methods 0.000 claims abstract description 141
- 230000014509 gene expression Effects 0.000 claims abstract description 113
- 210000005260 human cell Anatomy 0.000 claims abstract description 57
- 239000007787 solid Substances 0.000 claims abstract description 52
- 108090000623 proteins and genes Proteins 0.000 claims description 123
- 241001465754 Metazoa Species 0.000 claims description 80
- 241000124008 Mammalia Species 0.000 claims description 68
- 210000003754 fetus Anatomy 0.000 claims description 61
- 210000004185 liver Anatomy 0.000 claims description 60
- 238000002054 transplantation Methods 0.000 claims description 41
- 108700019146 Transgenes Proteins 0.000 claims description 40
- 230000001605 fetal effect Effects 0.000 claims description 34
- 230000001939 inductive effect Effects 0.000 claims description 28
- 230000002147 killing effect Effects 0.000 claims description 26
- 230000012010 growth Effects 0.000 claims description 25
- 210000000130 stem cell Anatomy 0.000 claims description 25
- 210000001161 mammalian embryo Anatomy 0.000 claims description 22
- 238000012546 transfer Methods 0.000 claims description 20
- 210000004962 mammalian cell Anatomy 0.000 claims description 18
- 230000030833 cell death Effects 0.000 claims description 17
- 239000003550 marker Substances 0.000 claims description 17
- 210000002216 heart Anatomy 0.000 claims description 15
- 210000003734 kidney Anatomy 0.000 claims description 15
- 210000004072 lung Anatomy 0.000 claims description 15
- 230000004044 response Effects 0.000 claims description 14
- 210000000496 pancreas Anatomy 0.000 claims description 13
- 241000894007 species Species 0.000 claims description 13
- 230000009036 growth inhibition Effects 0.000 claims description 10
- 230000002401 inhibitory effect Effects 0.000 claims description 8
- 230000008569 process Effects 0.000 claims description 8
- 230000001105 regulatory effect Effects 0.000 claims description 6
- 230000010261 cell growth Effects 0.000 claims 1
- 230000002708 enhancing effect Effects 0.000 claims 1
- 238000004519 manufacturing process Methods 0.000 abstract description 11
- 241000282412 Homo Species 0.000 abstract description 8
- 238000002689 xenotransplantation Methods 0.000 abstract description 5
- 230000001976 improved effect Effects 0.000 abstract description 4
- 230000001413 cellular effect Effects 0.000 abstract description 3
- 210000001557 animal structure Anatomy 0.000 abstract 1
- 210000001519 tissue Anatomy 0.000 description 380
- 239000000427 antigen Substances 0.000 description 50
- 108091007433 antigens Proteins 0.000 description 50
- 102000036639 antigens Human genes 0.000 description 50
- 230000009261 transgenic effect Effects 0.000 description 50
- 210000003494 hepatocyte Anatomy 0.000 description 29
- 108090000790 Enzymes Proteins 0.000 description 26
- 102000004190 Enzymes Human genes 0.000 description 24
- 241000282898 Sus scrofa Species 0.000 description 24
- 229940088598 enzyme Drugs 0.000 description 24
- 235000018102 proteins Nutrition 0.000 description 24
- 102000004169 proteins and genes Human genes 0.000 description 24
- 229940002612 prodrug Drugs 0.000 description 23
- 239000000651 prodrug Substances 0.000 description 23
- 125000003169 alpha-Gal epitope group Chemical group [C@H]1([C@H](O)[C@@H](O)[C@@H](O)[C@H](O1)CO)O[C@@H]1[C@H]([C@@H](O[C@@H]([C@@H]1O)CO)O[C@H]1[C@@H]([C@H](C(O[C@@H]1CO)*)NC(C)=O)O)O 0.000 description 18
- 210000004204 blood vessel Anatomy 0.000 description 18
- 238000012217 deletion Methods 0.000 description 18
- 230000037430 deletion Effects 0.000 description 18
- FDJKUWYYUZCUJX-KVNVFURPSA-N N-glycolylneuraminic acid Chemical compound OC[C@H](O)[C@H](O)[C@@H]1O[C@](O)(C(O)=O)C[C@H](O)[C@H]1NC(=O)CO FDJKUWYYUZCUJX-KVNVFURPSA-N 0.000 description 17
- 239000003795 chemical substances by application Substances 0.000 description 17
- 210000000988 bone and bone Anatomy 0.000 description 16
- 150000001720 carbohydrates Chemical class 0.000 description 16
- 238000012423 maintenance Methods 0.000 description 16
- 235000014633 carbohydrates Nutrition 0.000 description 15
- 230000005017 genetic modification Effects 0.000 description 15
- 241000282887 Suidae Species 0.000 description 14
- 230000000694 effects Effects 0.000 description 14
- 238000012239 gene modification Methods 0.000 description 14
- 235000013617 genetically modified food Nutrition 0.000 description 14
- 230000002829 reductive effect Effects 0.000 description 14
- 241001494479 Pecora Species 0.000 description 13
- 238000000338 in vitro Methods 0.000 description 13
- 210000003491 skin Anatomy 0.000 description 13
- 210000004700 fetal blood Anatomy 0.000 description 12
- 230000004048 modification Effects 0.000 description 12
- 238000012986 modification Methods 0.000 description 12
- 230000001737 promoting effect Effects 0.000 description 12
- 210000004369 blood Anatomy 0.000 description 11
- 239000008280 blood Substances 0.000 description 11
- 210000001185 bone marrow Anatomy 0.000 description 11
- 210000000170 cell membrane Anatomy 0.000 description 11
- 229930004094 glycosylphosphatidylinositol Natural products 0.000 description 11
- BRZYSWJRSDMWLG-CAXSIQPQSA-N geneticin Natural products O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](C(C)O)O2)N)[C@@H](N)C[C@H]1N BRZYSWJRSDMWLG-CAXSIQPQSA-N 0.000 description 10
- 210000000987 immune system Anatomy 0.000 description 10
- 210000003462 vein Anatomy 0.000 description 10
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 9
- 108010013423 CMPacetylneuraminate monooxygenase Proteins 0.000 description 9
- 108020004440 Thymidine kinase Proteins 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 230000035772 mutation Effects 0.000 description 9
- 108010088751 Albumins Proteins 0.000 description 8
- 102000009027 Albumins Human genes 0.000 description 8
- 108010043685 GPI-Linked Proteins Proteins 0.000 description 8
- 102000002702 GPI-Linked Proteins Human genes 0.000 description 8
- 241000699670 Mus sp. Species 0.000 description 8
- 102000006601 Thymidine Kinase Human genes 0.000 description 8
- 230000006378 damage Effects 0.000 description 8
- 230000009368 gene silencing by RNA Effects 0.000 description 8
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 8
- 102100028725 Alpha-1,3-galactosyltransferase 2 Human genes 0.000 description 7
- 241000701022 Cytomegalovirus Species 0.000 description 7
- 241000699666 Mus <mouse, genus> Species 0.000 description 7
- ZSJLQEPLLKMAKR-UHFFFAOYSA-N Streptozotocin Natural products O=NN(C)C(=O)NC1C(O)OC(CO)C(O)C1O ZSJLQEPLLKMAKR-UHFFFAOYSA-N 0.000 description 7
- 108010078334 UDP-galactose beta-D-galactosyl-1,4-glycosylceramide alpha-1,3-galactosyltransferase Proteins 0.000 description 7
- 210000001367 artery Anatomy 0.000 description 7
- SQVRNKJHWKZAKO-UHFFFAOYSA-N beta-N-Acetyl-D-neuraminic acid Natural products CC(=O)NC1C(O)CC(O)(C(O)=O)OC1C(O)C(O)CO SQVRNKJHWKZAKO-UHFFFAOYSA-N 0.000 description 7
- 230000002255 enzymatic effect Effects 0.000 description 7
- 230000002068 genetic effect Effects 0.000 description 7
- 210000004379 membrane Anatomy 0.000 description 7
- 239000012528 membrane Substances 0.000 description 7
- 108020004999 messenger RNA Proteins 0.000 description 7
- 230000035935 pregnancy Effects 0.000 description 7
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 7
- 229960001052 streptozocin Drugs 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 6
- 102100022002 CD59 glycoprotein Human genes 0.000 description 6
- 108060003306 Galactosyltransferase Proteins 0.000 description 6
- 230000008901 benefit Effects 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- 230000018109 developmental process Effects 0.000 description 6
- 210000003038 endothelium Anatomy 0.000 description 6
- 239000003623 enhancer Substances 0.000 description 6
- 239000012634 fragment Substances 0.000 description 6
- 230000006870 function Effects 0.000 description 6
- IRSCQMHQWWYFCW-UHFFFAOYSA-N ganciclovir Chemical compound O=C1NC(N)=NC2=C1N=CN2COC(CO)CO IRSCQMHQWWYFCW-UHFFFAOYSA-N 0.000 description 6
- 229960002963 ganciclovir Drugs 0.000 description 6
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 6
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 230000007246 mechanism Effects 0.000 description 6
- 230000035945 sensitivity Effects 0.000 description 6
- 238000006467 substitution reaction Methods 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- 108010080611 Cytosine Deaminase Proteins 0.000 description 5
- 102000030902 Galactosyltransferase Human genes 0.000 description 5
- 101000856513 Homo sapiens Inactive N-acetyllactosaminide alpha-1,3-galactosyltransferase Proteins 0.000 description 5
- 102100025509 Inactive N-acetyllactosaminide alpha-1,3-galactosyltransferase Human genes 0.000 description 5
- SQVRNKJHWKZAKO-PFQGKNLYSA-N N-acetyl-beta-neuraminic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)O[C@H]1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-PFQGKNLYSA-N 0.000 description 5
- 210000001744 T-lymphocyte Anatomy 0.000 description 5
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 description 5
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 description 5
- QIGJYVCQYDKYDW-SDOYDPJRSA-N alpha-D-galactosyl-(1->3)-D-galactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@H]1[C@@H](O)[C@@H](CO)OC(O)[C@@H]1O QIGJYVCQYDKYDW-SDOYDPJRSA-N 0.000 description 5
- 210000000013 bile duct Anatomy 0.000 description 5
- 230000004087 circulation Effects 0.000 description 5
- 210000003743 erythrocyte Anatomy 0.000 description 5
- 210000002950 fibroblast Anatomy 0.000 description 5
- 150000002632 lipids Chemical class 0.000 description 5
- 210000000822 natural killer cell Anatomy 0.000 description 5
- 230000010412 perfusion Effects 0.000 description 5
- 230000010076 replication Effects 0.000 description 5
- 238000007920 subcutaneous administration Methods 0.000 description 5
- 210000003556 vascular endothelial cell Anatomy 0.000 description 5
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 4
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 4
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 description 4
- 101000897400 Homo sapiens CD59 glycoprotein Proteins 0.000 description 4
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 description 4
- 101000638161 Homo sapiens Tumor necrosis factor ligand superfamily member 6 Proteins 0.000 description 4
- 108090000157 Metallothionein Proteins 0.000 description 4
- 108010076504 Protein Sorting Signals Proteins 0.000 description 4
- 241000283984 Rodentia Species 0.000 description 4
- 108700025910 Suicide Transgenic Genes Proteins 0.000 description 4
- 208000027418 Wounds and injury Diseases 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 230000000692 anti-sense effect Effects 0.000 description 4
- 210000003719 b-lymphocyte Anatomy 0.000 description 4
- 210000004556 brain Anatomy 0.000 description 4
- 239000004074 complement inhibitor Substances 0.000 description 4
- 230000002950 deficient Effects 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 210000001671 embryonic stem cell Anatomy 0.000 description 4
- 108020001507 fusion proteins Proteins 0.000 description 4
- 102000037865 fusion proteins Human genes 0.000 description 4
- 230000030279 gene silencing Effects 0.000 description 4
- 239000005090 green fluorescent protein Substances 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 238000001802 infusion Methods 0.000 description 4
- 208000014674 injury Diseases 0.000 description 4
- 210000004153 islets of langerhan Anatomy 0.000 description 4
- 210000000287 oocyte Anatomy 0.000 description 4
- 230000000750 progressive effect Effects 0.000 description 4
- 210000001147 pulmonary artery Anatomy 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 210000001631 vena cava inferior Anatomy 0.000 description 4
- -1 α-galactosyl Chemical group 0.000 description 4
- 102000014914 Carrier Proteins Human genes 0.000 description 3
- 102000011727 Caspases Human genes 0.000 description 3
- 108010076667 Caspases Proteins 0.000 description 3
- 102000000311 Cytosine Deaminase Human genes 0.000 description 3
- 108010024164 HLA-G Antigens Proteins 0.000 description 3
- GRRNUXAQVGOGFE-UHFFFAOYSA-N Hygromycin-B Natural products OC1C(NC)CC(N)C(O)C1OC1C2OC3(C(C(O)C(O)C(C(N)CO)O3)O)OC2C(O)C(CO)O1 GRRNUXAQVGOGFE-UHFFFAOYSA-N 0.000 description 3
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 3
- 102000004877 Insulin Human genes 0.000 description 3
- 108090001061 Insulin Proteins 0.000 description 3
- 102000010789 Interleukin-2 Receptors Human genes 0.000 description 3
- 108010038453 Interleukin-2 Receptors Proteins 0.000 description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 3
- 102100039373 Membrane cofactor protein Human genes 0.000 description 3
- SUHQNCLNRUAGOO-UHFFFAOYSA-N N-glycoloyl-neuraminic acid Natural products OCC(O)C(O)C(O)C(NC(=O)CO)C(O)CC(=O)C(O)=O SUHQNCLNRUAGOO-UHFFFAOYSA-N 0.000 description 3
- FDJKUWYYUZCUJX-UHFFFAOYSA-N N-glycolyl-beta-neuraminic acid Natural products OCC(O)C(O)C1OC(O)(C(O)=O)CC(O)C1NC(=O)CO FDJKUWYYUZCUJX-UHFFFAOYSA-N 0.000 description 3
- JMENXJYBCQFIRK-KRJDXUSZSA-N N-hexacosanoylisoglobotriaosyl ceramide Chemical compound O[C@@H]1[C@@H](O)[C@H](OC[C@H](NC(=O)CCCCCCCCCCCCCCCCCCCCCCCCC)[C@H](O)\C=C\CCCCCCCCCCCCC)O[C@H](CO)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@@H](CO)O1 JMENXJYBCQFIRK-KRJDXUSZSA-N 0.000 description 3
- 108010006232 Neuraminidase Proteins 0.000 description 3
- 102000005348 Neuraminidase Human genes 0.000 description 3
- 101710132082 Pyrimidine/purine nucleoside phosphorylase Proteins 0.000 description 3
- 102100031372 Thymidine phosphorylase Human genes 0.000 description 3
- 108010084455 Zeocin Proteins 0.000 description 3
- 210000003484 anatomy Anatomy 0.000 description 3
- 210000004102 animal cell Anatomy 0.000 description 3
- 108091008324 binding proteins Proteins 0.000 description 3
- 210000002798 bone marrow cell Anatomy 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 210000004413 cardiac myocyte Anatomy 0.000 description 3
- 238000010367 cloning Methods 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 239000000306 component Substances 0.000 description 3
- 230000001143 conditioned effect Effects 0.000 description 3
- 238000012258 culturing Methods 0.000 description 3
- 229940127089 cytotoxic agent Drugs 0.000 description 3
- 239000002254 cytotoxic agent Substances 0.000 description 3
- 231100000599 cytotoxic agent Toxicity 0.000 description 3
- 210000004207 dermis Anatomy 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- 210000002257 embryonic structure Anatomy 0.000 description 3
- 108010064306 endo-beta-D-galactosidase C Proteins 0.000 description 3
- 210000002615 epidermis Anatomy 0.000 description 3
- 230000002440 hepatic effect Effects 0.000 description 3
- GRRNUXAQVGOGFE-NZSRVPFOSA-N hygromycin B Chemical compound O[C@@H]1[C@@H](NC)C[C@@H](N)[C@H](O)[C@H]1O[C@H]1[C@H]2O[C@@]3([C@@H]([C@@H](O)[C@@H](O)[C@@H](C(N)CO)O3)O)O[C@H]2[C@@H](O)[C@@H](CO)O1 GRRNUXAQVGOGFE-NZSRVPFOSA-N 0.000 description 3
- 229940097277 hygromycin b Drugs 0.000 description 3
- 238000007654 immersion Methods 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 229940125396 insulin Drugs 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 210000004698 lymphocyte Anatomy 0.000 description 3
- 238000013508 migration Methods 0.000 description 3
- 230000005012 migration Effects 0.000 description 3
- 210000003205 muscle Anatomy 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- CWCMIVBLVUHDHK-ZSNHEYEWSA-N phleomycin D1 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC[C@@H](N=1)C=1SC=C(N=1)C(=O)NCCCCNC(N)=N)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C CWCMIVBLVUHDHK-ZSNHEYEWSA-N 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 239000003053 toxin Substances 0.000 description 3
- 238000013518 transcription Methods 0.000 description 3
- 230000035897 transcription Effects 0.000 description 3
- 108091008023 transcriptional regulators Proteins 0.000 description 3
- 102000035160 transmembrane proteins Human genes 0.000 description 3
- 108091005703 transmembrane proteins Proteins 0.000 description 3
- 210000005166 vasculature Anatomy 0.000 description 3
- 230000009278 visceral effect Effects 0.000 description 3
- CXNPLSGKWMLZPZ-GIFSMMMISA-N (2r,3r,6s)-3-[[(3s)-3-amino-5-[carbamimidoyl(methyl)amino]pentanoyl]amino]-6-(4-amino-2-oxopyrimidin-1-yl)-3,6-dihydro-2h-pyran-2-carboxylic acid Chemical compound O1[C@@H](C(O)=O)[C@H](NC(=O)C[C@@H](N)CCN(C)C(N)=N)C=C[C@H]1N1C(=O)N=C(N)C=C1 CXNPLSGKWMLZPZ-GIFSMMMISA-N 0.000 description 2
- KRHRWPPVNXJWRG-LUWBGTNYSA-N (4S,5R,6R)-5-acetamido-4-hydroxy-2-phosphonooxy-6-[(1R,2R)-1,2,3-trihydroxypropyl]oxane-2-carboxylic acid Chemical compound P(=O)(O)(O)OC1(C(O)=O)C[C@H](O)[C@@H](NC(C)=O)[C@@H](O1)[C@H](O)[C@H](O)CO KRHRWPPVNXJWRG-LUWBGTNYSA-N 0.000 description 2
- IAKHMKGGTNLKSZ-INIZCTEOSA-N (S)-colchicine Chemical compound C1([C@@H](NC(C)=O)CC2)=CC(=O)C(OC)=CC=C1C1=C2C=C(OC)C(OC)=C1OC IAKHMKGGTNLKSZ-INIZCTEOSA-N 0.000 description 2
- UHDGCWIWMRVCDJ-UHFFFAOYSA-N 1-beta-D-Xylofuranosyl-NH-Cytosine Natural products O=C1N=C(N)C=CN1C1C(O)C(O)C(CO)O1 UHDGCWIWMRVCDJ-UHFFFAOYSA-N 0.000 description 2
- JKOKCKNZKIETPU-GWTDSMLYSA-N 2-amino-9-[(2r,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]-3h-purin-6-one;3,7-dihydropurine-2,6-dione Chemical compound O=C1NC(=O)NC2=C1NC=N2.C1=NC=2C(=O)NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O JKOKCKNZKIETPU-GWTDSMLYSA-N 0.000 description 2
- RJYQLMILDVERHH-UHFFFAOYSA-N 4-Ipomeanol Chemical compound CC(O)CCC(=O)C=1C=COC=1 RJYQLMILDVERHH-UHFFFAOYSA-N 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 2
- 101800001288 Atrial natriuretic factor Proteins 0.000 description 2
- 101800001890 Atrial natriuretic peptide Proteins 0.000 description 2
- 102400001282 Atrial natriuretic peptide Human genes 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 101100381481 Caenorhabditis elegans baz-2 gene Proteins 0.000 description 2
- 102000013392 Carboxylesterase Human genes 0.000 description 2
- 108010051152 Carboxylesterase Proteins 0.000 description 2
- 102000005367 Carboxypeptidases Human genes 0.000 description 2
- 108010006303 Carboxypeptidases Proteins 0.000 description 2
- 241000700199 Cavia porcellus Species 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- UHDGCWIWMRVCDJ-PSQAKQOGSA-N Cytidine Natural products O=C1N=C(N)C=CN1[C@@H]1[C@@H](O)[C@@H](O)[C@H](CO)O1 UHDGCWIWMRVCDJ-PSQAKQOGSA-N 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 108020004437 Endogenous Retroviruses Proteins 0.000 description 2
- 108010003471 Fetal Proteins Proteins 0.000 description 2
- 102000004641 Fetal Proteins Human genes 0.000 description 2
- 101150042360 GGTA1 gene Proteins 0.000 description 2
- 206010064571 Gene mutation Diseases 0.000 description 2
- 229930186217 Glycolipid Natural products 0.000 description 2
- 102100028967 HLA class I histocompatibility antigen, alpha chain G Human genes 0.000 description 2
- 101001074244 Homo sapiens Glycophorin-A Proteins 0.000 description 2
- 241000700195 Hydrochoerus hydrochaeris Species 0.000 description 2
- 102100037872 Intercellular adhesion molecule 2 Human genes 0.000 description 2
- 101710148794 Intercellular adhesion molecule 2 Proteins 0.000 description 2
- 108010019421 Janus Kinase 3 Proteins 0.000 description 2
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 2
- 102000003792 Metallothionein Human genes 0.000 description 2
- 108700011259 MicroRNAs Proteins 0.000 description 2
- 102000004459 Nitroreductase Human genes 0.000 description 2
- 208000000733 Paroxysmal Hemoglobinuria Diseases 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- 102100036050 Phosphatidylinositol N-acetylglucosaminyltransferase subunit A Human genes 0.000 description 2
- 102000006486 Phosphoinositide Phospholipase C Human genes 0.000 description 2
- 108010044302 Phosphoinositide phospholipase C Proteins 0.000 description 2
- 241000881705 Porcine endogenous retrovirus Species 0.000 description 2
- 241000288906 Primates Species 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 101100372762 Rattus norvegicus Flt1 gene Proteins 0.000 description 2
- 241000700584 Simplexvirus Species 0.000 description 2
- WFWLQNSHRPWKFK-UHFFFAOYSA-N Tegafur Chemical compound O=C1NC(=O)C(F)=CN1C1OCCC1 WFWLQNSHRPWKFK-UHFFFAOYSA-N 0.000 description 2
- 102000004357 Transferases Human genes 0.000 description 2
- 108090000992 Transferases Proteins 0.000 description 2
- 102100031988 Tumor necrosis factor ligand superfamily member 6 Human genes 0.000 description 2
- 101710187743 Tumor necrosis factor receptor superfamily member 1A Proteins 0.000 description 2
- 102100033732 Tumor necrosis factor receptor superfamily member 1A Human genes 0.000 description 2
- 102100025387 Tyrosine-protein kinase JAK3 Human genes 0.000 description 2
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 2
- OIRDTQYFTABQOQ-KQYNXXCUSA-N adenosine Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O OIRDTQYFTABQOQ-KQYNXXCUSA-N 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 2
- 108010030291 alpha-Galactosidase Proteins 0.000 description 2
- 102000005840 alpha-Galactosidase Human genes 0.000 description 2
- 230000003872 anastomosis Effects 0.000 description 2
- 230000000890 antigenic effect Effects 0.000 description 2
- 230000001640 apoptogenic effect Effects 0.000 description 2
- 230000006907 apoptotic process Effects 0.000 description 2
- 230000002146 bilateral effect Effects 0.000 description 2
- CXNPLSGKWMLZPZ-UHFFFAOYSA-N blasticidin-S Natural products O1C(C(O)=O)C(NC(=O)CC(N)CCN(C)C(N)=N)C=CC1N1C(=O)N=C(N)C=C1 CXNPLSGKWMLZPZ-UHFFFAOYSA-N 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 239000003633 blood substitute Substances 0.000 description 2
- 230000036770 blood supply Effects 0.000 description 2
- NSQLIUXCMFBZME-MPVJKSABSA-N carperitide Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)=O)[C@@H](C)CC)C1=CC=CC=C1 NSQLIUXCMFBZME-MPVJKSABSA-N 0.000 description 2
- 239000013043 chemical agent Substances 0.000 description 2
- 230000019113 chromatin silencing Effects 0.000 description 2
- 210000002808 connective tissue Anatomy 0.000 description 2
- UHDGCWIWMRVCDJ-ZAKLUEHWSA-N cytidine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O1 UHDGCWIWMRVCDJ-ZAKLUEHWSA-N 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000007547 defect Effects 0.000 description 2
- 230000007812 deficiency Effects 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 210000001198 duodenum Anatomy 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 210000002889 endothelial cell Anatomy 0.000 description 2
- 210000003989 endothelium vascular Anatomy 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 108010052621 fas Receptor Proteins 0.000 description 2
- 102000018823 fas Receptor Human genes 0.000 description 2
- 230000008175 fetal development Effects 0.000 description 2
- 108010079306 galactoside 2-alpha-L-fucosyltransferase Proteins 0.000 description 2
- 125000002519 galactosyl group Chemical group C1([C@H](O)[C@@H](O)[C@@H](O)[C@H](O1)CO)* 0.000 description 2
- 238000012224 gene deletion Methods 0.000 description 2
- 238000003209 gene knockout Methods 0.000 description 2
- 238000007429 general method Methods 0.000 description 2
- 230000013595 glycosylation Effects 0.000 description 2
- 238000006206 glycosylation reaction Methods 0.000 description 2
- 230000003394 haemopoietic effect Effects 0.000 description 2
- 210000004209 hair Anatomy 0.000 description 2
- 230000011132 hemopoiesis Effects 0.000 description 2
- 210000002767 hepatic artery Anatomy 0.000 description 2
- 230000006801 homologous recombination Effects 0.000 description 2
- 238000002744 homologous recombination Methods 0.000 description 2
- 210000002865 immune cell Anatomy 0.000 description 2
- 230000006058 immune tolerance Effects 0.000 description 2
- 238000002513 implantation Methods 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 230000013011 mating Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 210000004165 myocardium Anatomy 0.000 description 2
- 230000001537 neural effect Effects 0.000 description 2
- 108020001162 nitroreductase Proteins 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 125000003729 nucleotide group Chemical group 0.000 description 2
- 210000004940 nucleus Anatomy 0.000 description 2
- 201000003045 paroxysmal nocturnal hemoglobinuria Diseases 0.000 description 2
- 150000003905 phosphatidylinositols Chemical group 0.000 description 2
- 210000002826 placenta Anatomy 0.000 description 2
- 210000004991 placental stem cell Anatomy 0.000 description 2
- 210000003240 portal vein Anatomy 0.000 description 2
- 230000010411 postconditioning Effects 0.000 description 2
- 230000001124 posttranscriptional effect Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 210000003492 pulmonary vein Anatomy 0.000 description 2
- 239000000784 purine nucleoside phosphorylase inhibitor Substances 0.000 description 2
- 230000001172 regenerating effect Effects 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- WYWHKKSPHMUBEB-UHFFFAOYSA-N tioguanine Chemical compound N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 2
- 238000012033 transcriptional gene silencing Methods 0.000 description 2
- 210000000626 ureter Anatomy 0.000 description 2
- 210000004291 uterus Anatomy 0.000 description 2
- 230000002792 vascular Effects 0.000 description 2
- 108010047303 von Willebrand Factor Proteins 0.000 description 2
- 102100036537 von Willebrand factor Human genes 0.000 description 2
- 229960001134 von willebrand factor Drugs 0.000 description 2
- DIGQNXIGRZPYDK-WKSCXVIASA-N (2R)-6-amino-2-[[2-[[(2S)-2-[[2-[[(2R)-2-[[(2S)-2-[[(2R,3S)-2-[[2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2R)-2-[[(2S,3S)-2-[[(2R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2R)-2-[[2-[[2-[[2-[(2-amino-1-hydroxyethylidene)amino]-3-carboxy-1-hydroxypropylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1-hydroxyethylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxyethylidene]amino]-1-hydroxypropylidene]amino]-1,3-dihydroxypropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxybutylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1-hydroxypropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxyethylidene]amino]-1,5-dihydroxy-5-iminopentylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxybutylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxyethylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1-hydroxyethylidene]amino]hexanoic acid Chemical compound C[C@@H]([C@@H](C(=N[C@@H](CS)C(=N[C@@H](C)C(=N[C@@H](CO)C(=NCC(=N[C@@H](CCC(=N)O)C(=NC(CS)C(=N[C@H]([C@H](C)O)C(=N[C@H](CS)C(=N[C@H](CO)C(=NCC(=N[C@H](CS)C(=NCC(=N[C@H](CCCCN)C(=O)O)O)O)O)O)O)O)O)O)O)O)O)O)O)N=C([C@H](CS)N=C([C@H](CO)N=C([C@H](CO)N=C([C@H](C)N=C(CN=C([C@H](CO)N=C([C@H](CS)N=C(CN=C(C(CS)N=C(C(CC(=O)O)N=C(CN)O)O)O)O)O)O)O)O)O)O)O)O DIGQNXIGRZPYDK-WKSCXVIASA-N 0.000 description 1
- UQQHOWKTDKKTHO-ICQCTTRCSA-N (2r,3s,4s,5r)-2-(hydroxymethyl)-5-(6-methoxypurin-9-yl)oxolane-3,4-diol Chemical compound C1=NC=2C(OC)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@@H]1O UQQHOWKTDKKTHO-ICQCTTRCSA-N 0.000 description 1
- LPJXPACOXRZCCP-VIFPVBQESA-N (2s)-2-benzamidopentanedioic acid Chemical compound OC(=O)CC[C@@H](C(O)=O)NC(=O)C1=CC=CC=C1 LPJXPACOXRZCCP-VIFPVBQESA-N 0.000 description 1
- 125000001340 2-chloroethyl group Chemical group [H]C([H])(Cl)C([H])([H])* 0.000 description 1
- HVCOBJNICQPDBP-UHFFFAOYSA-N 3-[3-[3,5-dihydroxy-6-methyl-4-(3,4,5-trihydroxy-6-methyloxan-2-yl)oxyoxan-2-yl]oxydecanoyloxy]decanoic acid;hydrate Chemical compound O.OC1C(OC(CC(=O)OC(CCCCCCC)CC(O)=O)CCCCCCC)OC(C)C(O)C1OC1C(O)C(O)C(O)C(C)O1 HVCOBJNICQPDBP-UHFFFAOYSA-N 0.000 description 1
- SYMHUEFSSMBHJA-UHFFFAOYSA-N 6-methylpurine Chemical group CC1=NC=NC2=C1NC=N2 SYMHUEFSSMBHJA-UHFFFAOYSA-N 0.000 description 1
- RJOXFJDOUQJOMQ-UHFFFAOYSA-N 6-sulfanylidene-3,7-dihydropurin-2-one Chemical compound S=C1NC(=O)NC2=C1NC=N2 RJOXFJDOUQJOMQ-UHFFFAOYSA-N 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- 108091023037 Aptamer Proteins 0.000 description 1
- 241001465318 Aspergillus terreus Species 0.000 description 1
- 210000002237 B-cell of pancreatic islet Anatomy 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 101100336562 Bos taurus GGTA1 gene Proteins 0.000 description 1
- ODZBBRURCPAEIQ-DJLDLDEBSA-N Brivudine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(C=CBr)=C1 ODZBBRURCPAEIQ-DJLDLDEBSA-N 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- 239000002126 C01EB10 - Adenosine Substances 0.000 description 1
- 108010009575 CD55 Antigens Proteins 0.000 description 1
- 108010055167 CD59 Antigens Proteins 0.000 description 1
- 101710196874 Cadherin-16 Proteins 0.000 description 1
- 206010057248 Cell death Diseases 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 102100025680 Complement decay-accelerating factor Human genes 0.000 description 1
- 229940124073 Complement inhibitor Drugs 0.000 description 1
- 206010010144 Completed suicide Diseases 0.000 description 1
- 102000004420 Creatine Kinase Human genes 0.000 description 1
- 108010042126 Creatine kinase Proteins 0.000 description 1
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 1
- 102000005927 Cysteine Proteases Human genes 0.000 description 1
- 108010005843 Cysteine Proteases Proteins 0.000 description 1
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 1
- 108030004122 Cytidine kinases Proteins 0.000 description 1
- 230000005778 DNA damage Effects 0.000 description 1
- 231100000277 DNA damage Toxicity 0.000 description 1
- 108010033174 Deoxycytidine kinase Proteins 0.000 description 1
- 102100029588 Deoxycytidine kinase Human genes 0.000 description 1
- 102000016607 Diphtheria Toxin Human genes 0.000 description 1
- 108010053187 Diphtheria Toxin Proteins 0.000 description 1
- 102000001039 Dystrophin Human genes 0.000 description 1
- 108010069091 Dystrophin Proteins 0.000 description 1
- UPEZCKBFRMILAV-JNEQICEOSA-N Ecdysone Natural products O=C1[C@H]2[C@@](C)([C@@H]3C([C@@]4(O)[C@@](C)([C@H]([C@H]([C@@H](O)CCC(O)(C)C)C)CC4)CC3)=C1)C[C@H](O)[C@H](O)C2 UPEZCKBFRMILAV-JNEQICEOSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 108010039471 Fas Ligand Protein Proteins 0.000 description 1
- 101150083447 Foxn1 gene Proteins 0.000 description 1
- 230000010337 G2 phase Effects 0.000 description 1
- 102100040837 Galactoside alpha-(1,2)-fucosyltransferase 2 Human genes 0.000 description 1
- 108010001498 Galectin 1 Proteins 0.000 description 1
- 102100021736 Galectin-1 Human genes 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 102100031132 Glucose-6-phosphate isomerase Human genes 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 108010031186 Glycoside Hydrolases Proteins 0.000 description 1
- 102000005744 Glycoside Hydrolases Human genes 0.000 description 1
- 102000009485 HLA-D Antigens Human genes 0.000 description 1
- 108010048896 HLA-D Antigens Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 206010019670 Hepatic function abnormal Diseases 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 102000007625 Hirudins Human genes 0.000 description 1
- 108010007267 Hirudins Proteins 0.000 description 1
- 102000018713 Histocompatibility Antigens Class II Human genes 0.000 description 1
- 101001052060 Homo sapiens Beta-1,4-mannosyl-glycoprotein 4-beta-N-acetylglucosaminyltransferase Proteins 0.000 description 1
- 101000856022 Homo sapiens Complement decay-accelerating factor Proteins 0.000 description 1
- 101000976075 Homo sapiens Insulin Proteins 0.000 description 1
- 101000961414 Homo sapiens Membrane cofactor protein Proteins 0.000 description 1
- 101001135770 Homo sapiens Parathyroid hormone Proteins 0.000 description 1
- 101001135995 Homo sapiens Probable peptidyl-tRNA hydrolase Proteins 0.000 description 1
- 101001086862 Homo sapiens Pulmonary surfactant-associated protein B Proteins 0.000 description 1
- 101000653189 Homo sapiens Tissue factor pathway inhibitor Proteins 0.000 description 1
- 101001047681 Homo sapiens Tyrosine-protein kinase Lck Proteins 0.000 description 1
- 206010061598 Immunodeficiency Diseases 0.000 description 1
- 108020005350 Initiator Codon Proteins 0.000 description 1
- 102000018682 Interleukin Receptor Common gamma Subunit Human genes 0.000 description 1
- 108010066719 Interleukin Receptor Common gamma Subunit Proteins 0.000 description 1
- 102000008193 Interleukin-2 Receptor beta Subunit Human genes 0.000 description 1
- 108010060632 Interleukin-2 Receptor beta Subunit Proteins 0.000 description 1
- 108010025815 Kanamycin Kinase Proteins 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 102100035838 Lactosylceramide 4-alpha-galactosyltransferase Human genes 0.000 description 1
- 241000446313 Lamella Species 0.000 description 1
- 101150028321 Lck gene Proteins 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 239000000232 Lipid Bilayer Substances 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 108090000362 Lymphotoxin-beta Proteins 0.000 description 1
- 102000043129 MHC class I family Human genes 0.000 description 1
- 108091054437 MHC class I family Proteins 0.000 description 1
- 108091054438 MHC class II family Proteins 0.000 description 1
- 208000007466 Male Infertility Diseases 0.000 description 1
- 101710146216 Membrane cofactor protein Proteins 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 241000713869 Moloney murine leukemia virus Species 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 101000902195 Mus musculus Cytidine monophosphate-N-acetylneuraminic acid hydroxylase Proteins 0.000 description 1
- 101100067103 Mus musculus Foxn1 gene Proteins 0.000 description 1
- 101100121730 Mus musculus Ggta1 gene Proteins 0.000 description 1
- 101100179574 Mus musculus Il2rg gene Proteins 0.000 description 1
- 102100026925 Myosin regulatory light chain 2, ventricular/cardiac muscle isoform Human genes 0.000 description 1
- 230000004988 N-glycosylation Effects 0.000 description 1
- 206010028851 Necrosis Diseases 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 230000004989 O-glycosylation Effects 0.000 description 1
- 101710160107 Outer membrane protein A Proteins 0.000 description 1
- 208000012868 Overgrowth Diseases 0.000 description 1
- 102000001746 Pancreatic alpha-Amylases Human genes 0.000 description 1
- 108010029785 Pancreatic alpha-Amylases Proteins 0.000 description 1
- 102000016387 Pancreatic elastase Human genes 0.000 description 1
- 108010067372 Pancreatic elastase Proteins 0.000 description 1
- 108010058828 Parathyroid Hormone Receptors Proteins 0.000 description 1
- 208000006735 Periostitis Diseases 0.000 description 1
- 102000011420 Phospholipase D Human genes 0.000 description 1
- 108090000553 Phospholipase D Proteins 0.000 description 1
- 102000015439 Phospholipases Human genes 0.000 description 1
- 108010064785 Phospholipases Proteins 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 241000125945 Protoparvovirus Species 0.000 description 1
- 108010041520 Pulmonary Surfactant-Associated Proteins Proteins 0.000 description 1
- 102000000528 Pulmonary Surfactant-Associated Proteins Human genes 0.000 description 1
- 102100032617 Pulmonary surfactant-associated protein B Human genes 0.000 description 1
- 229940123827 Purine nucleoside phosphorylase inhibitor Drugs 0.000 description 1
- 102000001183 RAG-1 Human genes 0.000 description 1
- 108060006897 RAG1 Proteins 0.000 description 1
- 108091030071 RNAI Proteins 0.000 description 1
- 101000915090 Rattus norvegicus Alpha-1,3-galactosyltransferase 2 Proteins 0.000 description 1
- 102000018120 Recombinases Human genes 0.000 description 1
- 108010091086 Recombinases Proteins 0.000 description 1
- 102000006382 Ribonucleases Human genes 0.000 description 1
- 108010083644 Ribonucleases Proteins 0.000 description 1
- 101000718529 Saccharolobus solfataricus (strain ATCC 35092 / DSM 1617 / JCM 11322 / P2) Alpha-galactosidase Proteins 0.000 description 1
- 102000003838 Sialyltransferases Human genes 0.000 description 1
- 108090000141 Sialyltransferases Proteins 0.000 description 1
- 102000008063 Small Heat-Shock Proteins Human genes 0.000 description 1
- 108010088928 Small Heat-Shock Proteins Proteins 0.000 description 1
- 108091027967 Small hairpin RNA Proteins 0.000 description 1
- 108020004459 Small interfering RNA Proteins 0.000 description 1
- 208000000223 Solitary Kidney Diseases 0.000 description 1
- 241000203644 Streptoalloteichus hindustanus Species 0.000 description 1
- 201000001322 T cell deficiency Diseases 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- 108060008539 Transglutaminase Proteins 0.000 description 1
- 206010052779 Transplant rejections Diseases 0.000 description 1
- 102000004903 Troponin Human genes 0.000 description 1
- 108090001027 Troponin Proteins 0.000 description 1
- 102000013534 Troponin C Human genes 0.000 description 1
- 108050002568 Tumor necrosis factor ligand superfamily member 6 Proteins 0.000 description 1
- 102100024036 Tyrosine-protein kinase Lck Human genes 0.000 description 1
- 108010070808 UDP-galactose-lactosylceramide alpha 1-4-galactosyltransferase Proteins 0.000 description 1
- 102000007410 Uridine kinase Human genes 0.000 description 1
- 108010053096 Vascular Endothelial Growth Factor Receptor-1 Proteins 0.000 description 1
- 102000016549 Vascular Endothelial Growth Factor Receptor-2 Human genes 0.000 description 1
- 102100033178 Vascular endothelial growth factor receptor 1 Human genes 0.000 description 1
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 1
- 108010051583 Ventricular Myosins Proteins 0.000 description 1
- 108010027570 Xanthine phosphoribosyltransferase Proteins 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 229960005305 adenosine Drugs 0.000 description 1
- 210000004504 adult stem cell Anatomy 0.000 description 1
- 102000013640 alpha-Crystallin B Chain Human genes 0.000 description 1
- 108010051585 alpha-Crystallin B Chain Proteins 0.000 description 1
- NNISLDGFPWIBDF-MPRBLYSKSA-N alpha-D-Gal-(1->3)-beta-D-Gal-(1->4)-D-GlcNAc Chemical compound O[C@@H]1[C@@H](NC(=O)C)C(O)O[C@H](CO)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@@H](CO)O1 NNISLDGFPWIBDF-MPRBLYSKSA-N 0.000 description 1
- UPEZCKBFRMILAV-UHFFFAOYSA-N alpha-Ecdysone Natural products C1C(O)C(O)CC2(C)C(CCC3(C(C(C(O)CCC(C)(C)O)C)CCC33O)C)C3=CC(=O)C21 UPEZCKBFRMILAV-UHFFFAOYSA-N 0.000 description 1
- WYTGDNHDOZPMIW-RCBQFDQVSA-N alstonine Natural products C1=CC2=C3C=CC=CC3=NC2=C2N1C[C@H]1[C@H](C)OC=C(C(=O)OC)[C@H]1C2 WYTGDNHDOZPMIW-RCBQFDQVSA-N 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229940126575 aminoglycoside Drugs 0.000 description 1
- 210000002159 anterior chamber Anatomy 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 210000000612 antigen-presenting cell Anatomy 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- 210000000702 aorta abdominal Anatomy 0.000 description 1
- 239000002473 artificial blood Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- WPIHMWBQRSAMDE-YCZTVTEBSA-N beta-D-galactosyl-(1->4)-beta-D-galactosyl-N-(pentacosanoyl)sphingosine Chemical compound CCCCCCCCCCCCCCCCCCCCCCCCC(=O)N[C@@H](CO[C@@H]1O[C@H](CO)[C@H](O[C@@H]2O[C@H](CO)[C@H](O)[C@H](O)[C@H]2O)[C@H](O)[C@H]1O)[C@H](O)\C=C\CCCCCCCCCCCCC WPIHMWBQRSAMDE-YCZTVTEBSA-N 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 229960001561 bleomycin Drugs 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 230000023555 blood coagulation Effects 0.000 description 1
- 239000003130 blood coagulation factor inhibitor Substances 0.000 description 1
- 239000012503 blood component Substances 0.000 description 1
- 101150046240 bsd gene Proteins 0.000 description 1
- 229960002092 busulfan Drugs 0.000 description 1
- 210000001715 carotid artery Anatomy 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 101150055276 ced-3 gene Proteins 0.000 description 1
- 230000011712 cell development Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 230000006037 cell lysis Effects 0.000 description 1
- 210000003855 cell nucleus Anatomy 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 229960001338 colchicine Drugs 0.000 description 1
- 230000001447 compensatory effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 230000001010 compromised effect Effects 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 210000004087 cornea Anatomy 0.000 description 1
- 229960004397 cyclophosphamide Drugs 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 239000005549 deoxyribonucleoside Substances 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 230000000447 dimerizing effect Effects 0.000 description 1
- ZWAOHEXOSAUJHY-ZIYNGMLESA-N doxifluridine Chemical compound O[C@@H]1[C@H](O)[C@@H](C)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ZWAOHEXOSAUJHY-ZIYNGMLESA-N 0.000 description 1
- 230000002183 duodenal effect Effects 0.000 description 1
- UPEZCKBFRMILAV-JMZLNJERSA-N ecdysone Chemical compound C1[C@@H](O)[C@@H](O)C[C@]2(C)[C@@H](CC[C@@]3([C@@H]([C@@H]([C@H](O)CCC(C)(C)O)C)CC[C@]33O)C)C3=CC(=O)[C@@H]21 UPEZCKBFRMILAV-JMZLNJERSA-N 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 210000002308 embryonic cell Anatomy 0.000 description 1
- 210000003372 endocrine gland Anatomy 0.000 description 1
- 210000001339 epidermal cell Anatomy 0.000 description 1
- 230000004049 epigenetic modification Effects 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 210000003617 erythrocyte membrane Anatomy 0.000 description 1
- 230000012173 estrus Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 210000003020 exocrine pancreas Anatomy 0.000 description 1
- 230000001815 facial effect Effects 0.000 description 1
- 108091022862 fatty acid binding Proteins 0.000 description 1
- 210000001105 femoral artery Anatomy 0.000 description 1
- 210000003191 femoral vein Anatomy 0.000 description 1
- 230000004720 fertilization Effects 0.000 description 1
- 230000004578 fetal growth Effects 0.000 description 1
- XRECTZIEBJDKEO-UHFFFAOYSA-N flucytosine Chemical group NC1=NC(=O)NC=C1F XRECTZIEBJDKEO-UHFFFAOYSA-N 0.000 description 1
- 229960000390 fludarabine Drugs 0.000 description 1
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- NBVXSUQYWXRMNV-UHFFFAOYSA-N fluoromethane Chemical compound FC NBVXSUQYWXRMNV-UHFFFAOYSA-N 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000012226 gene silencing method Methods 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 210000004907 gland Anatomy 0.000 description 1
- 150000002339 glycosphingolipids Chemical class 0.000 description 1
- 210000003780 hair follicle Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000003209 hepatic oval cell Anatomy 0.000 description 1
- 210000002989 hepatic vein Anatomy 0.000 description 1
- 229940006607 hirudin Drugs 0.000 description 1
- WQPDUTSPKFMPDP-OUMQNGNKSA-N hirudin Chemical compound C([C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC(OS(O)(=O)=O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H]1NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@@H]2CSSC[C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(=O)N[C@H](C(NCC(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N2)=O)CSSC1)C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=2C=CC(O)=CC=2)NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)C(C)C)[C@@H](C)O)CSSC1)C(C)C)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 WQPDUTSPKFMPDP-OUMQNGNKSA-N 0.000 description 1
- 101150029559 hph gene Proteins 0.000 description 1
- 102000051442 human CD59 Human genes 0.000 description 1
- 102000058004 human PTH Human genes 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical group O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- PBGKTOXHQIOBKM-FHFVDXKLSA-N insulin (human) Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H]1CSSC[C@H]2C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3NC=NC=3)NC(=O)[C@H](CO)NC(=O)CNC1=O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O)=O)CSSC[C@@H](C(N2)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C1=CN=CN1 PBGKTOXHQIOBKM-FHFVDXKLSA-N 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 210000004347 intestinal mucosa Anatomy 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229960004768 irinotecan Drugs 0.000 description 1
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 description 1
- 210000004731 jugular vein Anatomy 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000005229 liver cell Anatomy 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 210000003519 mature b lymphocyte Anatomy 0.000 description 1
- 230000007102 metabolic function Effects 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 230000011987 methylation Effects 0.000 description 1
- 238000007069 methylation reaction Methods 0.000 description 1
- 239000011325 microbead Substances 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 102000035118 modified proteins Human genes 0.000 description 1
- 108091005573 modified proteins Proteins 0.000 description 1
- 210000005087 mononuclear cell Anatomy 0.000 description 1
- 210000002894 multi-fate stem cell Anatomy 0.000 description 1
- 210000003098 myoblast Anatomy 0.000 description 1
- 230000002107 myocardial effect Effects 0.000 description 1
- 210000000754 myometrium Anatomy 0.000 description 1
- 108010065781 myosin light chain 2 Proteins 0.000 description 1
- 230000017074 necrotic cell death Effects 0.000 description 1
- 230000001338 necrotic effect Effects 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 239000000082 organ preservation Substances 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 210000000277 pancreatic duct Anatomy 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 230000009984 peri-natal effect Effects 0.000 description 1
- 210000003460 periosteum Anatomy 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 210000001322 periplasm Anatomy 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 231100000654 protein toxin Toxicity 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 210000002254 renal artery Anatomy 0.000 description 1
- 210000002796 renal vein Anatomy 0.000 description 1
- 230000008261 resistance mechanism Effects 0.000 description 1
- 210000001525 retina Anatomy 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 210000004761 scalp Anatomy 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- SQVRNKJHWKZAKO-OQPLDHBCSA-N sialic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)OC1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-OQPLDHBCSA-N 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 210000003625 skull Anatomy 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 210000002460 smooth muscle Anatomy 0.000 description 1
- 238000010374 somatic cell nuclear transfer Methods 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 150000003408 sphingolipids Chemical class 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 210000000106 sweat gland Anatomy 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- 229960002180 tetracycline Drugs 0.000 description 1
- 229930101283 tetracycline Natural products 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 230000002992 thymic effect Effects 0.000 description 1
- 229960003087 tioguanine Drugs 0.000 description 1
- 210000003014 totipotent stem cell Anatomy 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 210000003437 trachea Anatomy 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 102000003601 transglutaminase Human genes 0.000 description 1
- 108010058734 transglutaminase 1 Proteins 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 230000007306 turnover Effects 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- 210000005167 vascular cell Anatomy 0.000 description 1
- 108700026220 vif Genes Proteins 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/027—New or modified breeds of vertebrates
- A01K67/0271—Chimeric vertebrates, e.g. comprising exogenous cells
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/30—Animal model comprising expression system for selective cell killing, e.g. toxins, enzyme dependent prodrug therapy using ganciclovir
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/02—Animal zootechnically ameliorated
- A01K2267/025—Animal producing cells or organs for transplantation
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Environmental Sciences (AREA)
- Cell Biology (AREA)
- Animal Behavior & Ethology (AREA)
- Zoology (AREA)
- Animal Husbandry (AREA)
- Biodiversity & Conservation Biology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Materials For Medical Uses (AREA)
Abstract
本発明の一態様は、非ヒト哺乳動物宿主の少なくとも実質的に細胞でヒト固形器官および固形組織を作製するための改善された方法を提供する。本発明の関連した態様は、固形器官または組織の選択された細胞型および/または少なくとも実質的に全ての細胞型に関して、器官および/または組織特異的遺伝子発現および/または表現形を得るための、移植ベースの方法と、器官または組織の選択された細胞種および/または少なくとも実質的に全ての細胞種に関して、置換細胞、例えばヒト細胞によって、固形器官および組織を細胞的に再構成するための方法と、細胞的に再構成された固形器官および組織とを提供する。本発明によるヒト器官または組織の作製は、動物の器官または組織をヒトに移植する異種移植に関連した限界を克服する。
Description
この出願は、米国特許出願第11/306,414号(2005年12月27日出願)、米国特許出願第11/162,715号(2005年9月20日出願)、米国特許仮出願番号60/597,009号(2005年11月3日出願)、および米国特許仮出願第60/640,445号(2004年12月30日出願)の優先権を主張するもので、各々の出願の全体を本明細書に援用する。
本発明は、組織工学および移植生物学の分野に関する。
Beschornerらの国際特許出願番号PCT/US2003/029251号(公開番号WO2004/027029A2)は、キメラ哺乳動物器官の作製に関する方法を開示しており、この方法では、妊娠雌によって扶養される胎児哺乳動物の標的器官への外来置換細胞の取込みは、一連の状況に応じた胎児標的器官の細胞の選択的殺害によって促進されるが、妊娠雌の対応する器官の細胞は同一状況では殺害されない。このように、胎児では肝機能等の生体機能が混乱して細胞置換を促進し得るが、胎児を宿している動物は傷つくことなく、この胎児を維持し、胎児における機能喪失を補填し続ける。
Rhim et al., Proc. Natl. Acad. Sci. USA, Vol. 92, 4942-46 (1995)は、肝潜在成長力および肝機能の欠陥によって特徴づけられるトランスジェニックマウスでの正常異種移植成体肝細胞によるマウス肝臓の肝細胞含有物の選択的な再増殖を開示している。
本発明は、選択された種の置換細胞による器官および組織の細胞再形成のための方法を提供する。一態様では、本発明は、非ヒト哺乳動物宿主でキメラ・ヒト、非ヒト器官および組織を作製する改善された方法ならびに非ヒト哺乳動物宿主で少なくとも実質的に完全にヒト器官および組織を作製する改善された方法を提供する。
本発明の一態様は、置換細胞によるドナー器官を再構成するための方法を提供するもので、該方法は、ドナー器官または組織、例えばヒトまたは非ヒト哺乳動物ドナー由来の固形器官または組織、あるいはその一部を、生きた状態でドナー器官または組織を維持し、ドナー器官または組織の少なくとも一部または少なくとも実質的に全部の細胞が少なくとも実質的かつ選択的に殺害可能である非ヒト哺乳動物宿主に、移植するステップと、ドナー器官または組織細胞の少なくとも一部を選択的に殺害するステップと、ドナー器官または組織の中に置換細胞を導入することで器官または組織の内因性ドナー細胞と置き換えるステップとを含む。一変形例では、広範囲活性プロモーターの制御下で自殺遺伝子を発現させることで、ドナー器官または組織が1セットの1つ以上の条件に反応してドナー細胞または非ヒト宿主哺乳動物の細胞が殺害可能となり、非ヒト哺乳動物の細胞および置換細胞がドナー細胞を殺害する1セットの1つ以上の条件に反応して殺害可能とはならず、ならびに少なくとも一部のドナー細胞を選択的に殺害するステップが前記1セットの1つ以上の条件の適用を含むようにする。
別の変形例では、ドナー細胞を選択的に殺害するステップは、ドナー器官または組織が宿主に移植された後におこなわれる。置換細胞を宿主器官または組織に導入するステップは、ドナー器官または組織を宿主に移植する前および/または後におこなってもよい。一実施形態では、置換細胞がドナー器官または組織に取り込まれるドナー哺乳動物に置換細胞を導入する。
本発明の関連態様は、置換細胞によってドナー器官を再構成するための方法を提供するもので、該方法は、固形器官(例えば腎臓、肺、心臓、肝臓、および膵臓)または固形組織あるいはその一部をヒトまたは非ヒト哺乳動物ドナーから、生きた状態でドナー器官または組織あるいはその一部を維持する非ヒト哺乳動物宿主に移植するステップと、ドナー器官または組織が宿主に移植された後に、ネイティブのドナー器官または組織細胞の少なくとも一部を選択的に殺害するステップと、器官または組織あるいはその一部が宿主に移植される前および/または後に、少なくとも一部の内因性細胞またはドナー器官または組織の細胞型を置換することができる置換細胞(例えばヒト置換細胞)をドナー器官または組織あるいはその一部に導入するステップとを有する。したがって、置換細胞による器官または組織あるいはその一部の細胞再形成が促進される。一変形例では、ドナーは非ヒト哺乳動物であり、置換細胞をドナー器官または組織に導入するステップは、成長過程の胎児または新生児段階にある幹細胞をドナー哺乳動物動物に導入することで、非ヒト宿主哺乳動物に移植される前に、固形器官または固形組織あるいはその固形部分がそれに既に取り込まれた幹細胞由来置換細胞を含む。別の変形例では、ドナー器官または組織は、広範囲活性プロモーターの制御下で自殺遺伝子を発現することで、非ヒト宿主哺乳動物の細胞および置換細胞は、ドナー細胞を殺す1セットの1つ以上の条件に応じて実質的に殺害可能とはならず、ならびに少なくとも一部のドナー細胞を選択的に殺害するステップが1セットの1つ以上の条件の適用を含むようにする。
本発明の別の態様は、置換細胞によるドナー器官を再構成するための方法を提供するもので、該方法は、ヒトまたは非ヒト哺乳動物ドナーからドナー器官または組織あるいはその一部を生きた状態で維持する非ヒト哺乳動物宿主に固形器官または固形組織あるいはその一固形部分を移植することであって、ドナー器官または組織の少なくとも一部または少なくとも実質的に全部の細胞の成長を1セットの1つ以上の条件に応じて選択的に阻害することが可能であり、また内因性宿主細胞および置換細胞の成長が1セットの1つ以上の条件によって実質的に妨げられることのないステップと、1セットの1つ以上の条件を適用することで組織または器官が宿主に移植された後に、ドナー器官または組織の少なくとも一部の成長を選択的に妨げるステップと、器官または組織あるいはその一部を宿主に移植する前および/または後に、ヒト置換細胞等の置換細胞をドナー器官または組織あるいはその一部に導入するステップとを含む。
本発明のさらなる態様は、非ヒト哺乳動物等の非ヒト動物によって維持される事前選択された器官または組織あるいはその一部に所望の形質が限定される、該非ヒト動物を得るための方法を提供するもので、該方法は、非ヒト動物等の非ヒトドナーまたは非ヒト動物ドナー由来の事前選択された固形器官または固形組織あるいはその一固形部分を非ヒト哺乳動物宿主等の非ヒト動物宿主に移植するステップを含み、固形器官または固形組織あるいはその一固形部分が生きた状態で維持され、少なくとも一部の内因性細胞型の移植されたドナー固形器官または固形組織あるいはその一固形部分が所望の形質を持ち、ならびに宿主動物の内因性細胞は実質的にはその形質を少なくとも発現しない。対応の宿主器官または組織は定位置に残してもよく、あるいは少なくとも部分的に摘出してもよい。一変形例では、ドナーまたは宿主は同一種の各々の非ヒト動物(例えば、同一種の非ヒト哺乳動物)である。別の変形例では、形質はネガティブ選択マーカーの誘導発現または構成的発現を含む。特定の実施形態では、形質は、ネガティブ選択マーカーの発生的に調整された発現を含む。別の変形例では、形質は細胞死または成長阻害に対して、1セットの1つ以上の既知または事前選択された条件に応じた細胞死または成長阻害に対する感受性を含む。関連した変形例は、細胞死または成長阻害を引き起こす1セットの条件を提供するステップをさらに含む。異なる変形例では、形質は、宿主のゲノム内に機能的形態では存在しない、または実質的に存在しない事前選択された導入遺伝子の誘導発現または構成的発現あるいは発生的に調整された発現を含む。導入遺伝子の発現を、例えば、広範囲活性プロモーターまたは一つ以上の細胞型特異的プロモーターの管理下に置いてもよい。一実施形態では、事前選択された導入遺伝子は、事前選択された自殺遺伝子または事前選択された成長阻害遺伝子である。
発明の別の態様は、非ヒト宿主動物を提供するもので、該ヒト宿主動物は、生きている非ヒトほ乳動物宿主、少なくとも、ヒトまたは非ヒト・ドナー哺乳動物から移植された、宿主によって生きた状態で維持された固形器官または固形組織の一部、および宿主哺乳動物に由来する器官または組織の少なくとも一部分に存在する置換細胞(例えば、ヒト置換細胞)を含む。一変形例では、ドナーから移植された器官または組織の少なくとも一部分のドナー哺乳動物細胞の少なくともいくつかは、内因性宿主細胞および置換細胞と対比して、選択的に殺害可能または成長を妨げることが可能である。
本発明のさらに別の態様は、器官または組織を置換細胞によって再構成するための方法を提供するもので、該方法は、自殺遺伝子または任意の種類の選択マーカー(形質)の器官または組織特異的発現を与える導入遺伝子についてヘテロ接合またはホモ接合である、あるいはさもなければネガティブ選択マーカーの器官または組織特異発現を有する、少なくとも1つの非ヒト哺乳動物胚または胎児を提供するステップと、少なくとも1つの胚または胎児を、少なくとも実質的に導入遺伝子を発現しない(例えば該導入遺伝子の機能的コピーが欠如している結果として)または少なくともネガティブ選択マーカーを実質的に発現しない、同一種または異種の代理母(該胚または胎児の遺伝的親ではない)移入するステップとを含み、移入された胚または胎児が代理母によって生きた状態で維持されるとともに、代理母内で成長を続ける。変形例では、胚または胎児の成長の胎児期の過程で、ヒト置換細胞等の置換細胞を直接または間接的に胎児の器官または組織に導入するステップを、さらに含む。ある変形例では、胎児が代理母に移植される前または該移植時に、置換細胞を胎児に導入する。別の変形例では、胎児が代理母内に定着された後に、置換細胞を胎児(代理母に移入された胎児、あるいは移入された胚に由来する胎児)に導入する。置換細胞を器官または組織に取り込むステップは、幹細胞(例えば、ヒト幹細胞)を胎児に導入することを含んでもよい。次いで、胎児の器官または組織の内因性細胞を選択的に殺害または成長を妨げることで、置換細胞による置換を促進する。
本発明の関連態様は、非ヒト代理動物を提供するもので、該動物は、非ヒト哺乳動物代理動物と、該代理動物の子孫ではない代理動物によって維持される非ヒト動物胚または胎児とを含み、胚または胎児が、1セットの1つ以上の条件に応じて事前選択された器官または組織の少なくともいくつかの細胞を選択的に殺害または成長を妨げる能力を与える形質について、ヘテロ接合またはホモ接合であり、また代理動物は上記形質を欠いていることから、移入された胎児を有する、または該代用動物に維持された移入された胚に由来する胎児を有する代用物を、1セットの1つ以上の条件にさらすことで、事前選択された胎児器官または胎児組織の細胞の殺害または成長阻害を生じさせる、あるいは対応する宿主哺乳動物細胞の殺害または成長阻害を少なくとも実質的には生じさせない。一変形例では、移入された胚または該移入された胚に由来する胎児が、事前選択された器官または組織に存在する置換細胞、例えばヒト置換細胞を含み、上記置換細胞が1セットの1つ以上の条件によって、少なくとも実質的に殺害可能または成長を妨げられるうる。
本発明は、宿主から該宿主が宿していた異種細胞への1つ以上の異種抗原の移動が低下する、および/または宿主から該宿主が宿していた細胞への1つ以上のトレランス促進生体分子の移動を促進する非ヒト哺乳動物宿主において、任意の形態(例えば、固形または分散、キメラまたは非キメラ器官もしくは組織または体の一部、あるいは幹細胞)で、異種細胞を培養する方法も提供する。
図面の簡単な説明
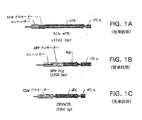
図1A、1B、および1Cは、自殺遺伝子を発現するトランスジェニック動物の作製に使用し得る導入遺伝子コンストラクトを示す模式図である。
図1A、1B、および1Cは、自殺遺伝子を発現するトランスジェニック動物の作製に使用し得る導入遺伝子コンストラクトを示す模式図である。
発明の詳細な説明
本発明は、器官または組織の選択された細胞種および/または少なくとも実質的に全ての細胞種に関して、宿主動物内で、固形器官および組織に対して器官および/または組織特異的遺伝子発現および/または表現型を得るための移植に基づく方法、器官または組織の選択された細胞種および/または少なくとも実質的に全ての細胞種について、置換細胞(例えばヒト細胞)によって固形器官および組織の細胞再構成をおこなう方法、置換細胞による固形器官および組織の細胞再構成のための修飾非ヒト哺乳動物、ならびに細胞再構成固形器官および組織を提供する。
本発明は、器官または組織の選択された細胞種および/または少なくとも実質的に全ての細胞種に関して、宿主動物内で、固形器官および組織に対して器官および/または組織特異的遺伝子発現および/または表現型を得るための移植に基づく方法、器官または組織の選択された細胞種および/または少なくとも実質的に全ての細胞種について、置換細胞(例えばヒト細胞)によって固形器官および組織の細胞再構成をおこなう方法、置換細胞による固形器官および組織の細胞再構成のための修飾非ヒト哺乳動物、ならびに細胞再構成固形器官および組織を提供する。
本発明の一態様によれば、1セットの条件に応じて殺害される、または成長を妨げられる細胞を含むドナー個体からの選択されたドナー器官および/または組織の細胞の少なくとも一部分を、細胞が同一セットの条件によって殺害可能ではない、または成長を妨げられることない非ヒト宿主個体に対して、外科的に移植する。移植されたドナー器官または組織は、宿主によって生きた状態で維持される。このように、選択されたドナー器官または組織の細胞の少なくともいくつかが選択的に殺害される、または成長を妨げられるキメラ動物が、提供される。一実施形態において、ドナー個体および宿主個体は、ともに哺乳動物である。本発明の別の態様によれば、この種のキメラ動物を用いて、以下のようにして、外来置換細胞によって少なくとも部分的に再構築される器官および組織を調製することができる。一実施形態において、ドナー器官または組織は、固形器官、固形組織または固形器官または固形組織の一部あるいは一区域である。組織は、単組織または複合組織であってもよい。
ドナー器官または組織の細胞と置き換わることができる外来の置換細胞は、ドナー器官または組織が非ヒト動物宿主に移植される前および/または後に、直接または間接的にドナー組織に導入することができる。ドナー器官または組織の外来の置換細胞の移植および成長は、その細胞を殺害または阻害する1セットの条件でドナー器官または組織を処置することによって、促進される。ドナー器官または組織が宿主動物に移植される前および/または後に、そのような処置をおこなうことができる。一実施形態では、ドナー個体と宿主個体は各々の哺乳動物であり、外来置換細胞も哺乳動物のものである。関連実施形態では、ドナー個体は非ヒト哺乳動物またはヒトであり、宿主個体は非ヒト哺乳動物、さらに外来置換細胞はヒト細胞である。別の実施形態では、ドナーおよび宿主個体は各々非ヒト哺乳動物動物であり、外来弛緩細胞はヒト細胞である。
本発明の関連態様では、成長が阻害された(または損なわれる可能性のある)ネイティブな細胞を含むドナー個体由来のドナー器官および/または組織を、細胞が成長を阻害されない(または同様に阻害される可能性のない)第2の非ヒト宿主個体に対して、外科的に移植する。また、移植されたドナー器官または組織は、宿主によって生きた状態で維持されている。この種類のキメラ動物を、成長が阻害されたドナー器官または組織細胞に対して生着上の利点(populative advantage)を有する外来の置換細胞によって、少なくとも部分的に再生着させる器官および組織の調製に用いてもよい。
本発明の一態様は、そのような導入遺伝子または遺伝学的修飾もしくは感受性を持つ選択された器官または組織あるいはその一部分を、ドナー(例えば、非ヒト哺乳動物またはヒト)から、同様の導入遺伝子または遺伝学的修飾もしくは感受性を有しない非ヒト宿主(例えば、非ヒト哺乳動物宿主)へ移植することによって、ドナーの導入遺伝子または遺伝学的修飾もしくは感受性の特異的効果が宿主のドナー器官または組織に感知されるだけであるように、細胞死促進もしくは成長抑制導入遺伝子および/または遺伝学的修飾(自然発生的または人為的)もしくは感受性の効果を、非ヒト哺乳動物宿主内での選択されたドナー器官および組織またはその一部分に限定する。
例えば、本発明にもとづく第1の戦略では、非ヒト・トランスジェニック・ドナー生物は、宿主細胞に対して、自殺遺伝子または他の種類のネガティブ選択マーカーを発現するか、あるいはドナー器官または組織細胞が条件的(conditional)かつ少なくとも実質的に選択的に削除(殺害)可能となるように提供され得る。本発明の第2の戦略では、ドナー器官または組織が、例えば、宿主に欠けている感受性である、細胞を殺す化学剤に対する感受性によって特徴づけられる。この戦略は、任意のタイプのドナーおよび宿主で使用することができるが、特に有用なのは、ドナーがヒトである場合であり、その理由は、一般的なこととして、ヒトの機能的に発達したドナー器官または組織が、ネガティブ選択マーカーにより大規模に安定的に遺伝学的修飾を受けることができないからである。例えば、哺乳動物細胞選択剤G418(ジェネテシン)に対する抵抗を与えるneoR(ネオマイシン/カナマイシン耐性)遺伝子を一般に発現するトランスジェニック哺乳動物宿主(例えばブタ)を作製することができる。選択されたヒト・ドナー器官または組織は、哺乳動物宿主に移植され、該宿主によって生きた状態で維持される。未修飾のヒト細胞はG418に対して感受性であることから、細胞死の選択的誘導を、宿主への移植後および/または宿主体内にヒト器官または組織を移植する前に、宿主動物にG418を投与することによって、ヒト・ドナー器官または組織の細胞型全体でおこなうことができる。目的がヒト器官の発達再形成(progressive reconstitution)または置換細胞による組織である場合、植え付けられた置換細胞が選択剤投与を複数回行う過程で殺害されることがないように、ヒトまたは非ヒトを遺伝的に修飾して選択剤に耐性にすることもできる。実際問題として、上記した戦略のどちらを使うかにかかわりなく、選択剤の投与や、移植片が失われてしまうようなドナー器官または組織の完全壊死が起こる程度の選択の誘導は避けるよう注意すべきである。特定の生体、器官/組織型、および選択メカニズムに適した投与計画は、日常的におこなわれる実験プロセスによって、経験的に決定される。
いくつかの利点は、限定されるものではないが以下のものを含む本発明の種々の態様によって提供される。
第一に、対応する宿主器官または組織の細胞はかなりな程度までに有害な影響を及ぼさないことから、ドナー器官細胞またはドナー組織細胞の欠失または阻害にもかかわらず、該細胞は機能し続けるとともに宿主を維持し続ける。このことは、ドナー器官または組織が宿主の対応器官または組織と置換しないまたは完全には置換しない場合に、特に明らかである。このことは、本発明にもとづいて、宿主に対するドナー器官または組織の異所移植(対応宿主器官を摘出することなく、またはその全てを摘出することなく)または宿主の一対の器官(例えば、哺乳動物の肺または腎臓)をドナーの対応器官によって置換する一方で、その対の他方を宿主に残しておく半同所移植によって、達成することが可能である。
したがって、Beschornerらとは対照的に、本発明は、外来置換細胞のレシピエント哺乳動物が妊娠雌によって維持された胎児であることを必要としない。その代わりに、本発明の哺乳動物による実施形態によれば、置換細胞を含む、または置換細胞を含むことになる哺乳動物ドナー器官または組織を担持する宿主哺乳動物は成長過程の胎児期または出生後期である。
第二に、本発明の一態様にもとづいて、所定の器官または組織に関して、ドナー器官または組織を構成する各々の細胞型での発現を得るために器官または組織もしくは細胞型特異的プロモーターの同定または使用を必要とすることなく、ドナー器官または組織を構成するより広範な細胞型に対する(該細胞型の少なくとも実質的に全てについてさえ)より完全な選択的欠失および/または成長阻害を達成し得る。多くの器官および組織は複雑であり、2種類以上またはいくつかの異なる細胞型からなる。この利点は、以下の実施形態で例示される。
一実施形態では、トランスジェニック非ヒト・ドナー哺乳動物が提供され、該動物は、1セットの条件に反応して細胞が死ぬように構成的または誘導性の広範囲活性プロモーター(構成的または誘導的に、目的とする器官または組織の細胞種あるいはさらに生体全体の細胞種の多くまたは少なくとも実質的に全てで活性ある)の制御下で細胞死促進自殺遺伝子を有する。少なくとも実質的には細胞の全てがこの条件セットに反応して欠失可能ではない非ヒト哺乳動物宿主も提供される。選択された器官または組織は、ドナーから宿主に移植され、そこで宿主によって生きた状態で維持される。必要な場合、ドナー細胞は感受性だが、対応宿主細胞および/または宿主細胞は一般に有害的な影響を受けることはない1セットの条件を宿主に与えることで、移植されたドナー器官または組織の複数の細胞型を欠失させるができる。ドナー細胞の欠失前および/またはその過程中に、ドナー器官または組織に対する少なくともいくつかの置換細胞の局在化をもたらすように、置換細胞をドナー器官または組織を含む宿主に導入することができる。このように、置換細胞によるドナー器官または組織を構成する広範囲または少なくとも実質的に全ての細胞型の置換が促進されるが、宿主の内在の器官や組織、例えば脈管内皮および/または内皮は一般に置換は阻害される。
被検体器官または組織について、様々な細胞型特異的プロモーターの組合せを、置換細胞が被検体器官または組織において、様々な細胞型の置換を促進するために用いることもできる。そのようなプロモーターが、様々なタイプの自殺遺伝子またはネガティブ選択マーカーの発現を差別的に誘導可能または駆動する場合、各被検体細胞型のコンディショナルな細胞欠失が同時あるいは時差的、累進的方法でおこなわれる。広範囲活性プロモーターと少なくとも1つの細胞型に特異的なプロモーターの組合せは、時差的かつ特異的な外来の置換細胞との置換(例えば、被検体ドナー器官または組織の少なくとも実質的に全ての細胞の置換)を得るのに用いることもできる。この場合、組織特異的プロモーターを用いる欠失を、広範囲活性プロモーターによる欠失の前に実行することができる。以下の実施例では、本発明にもとづいて、このことがどのようにして達成し得るかを説明する。
実施例−異なる自殺遺伝子
トランスジェニック非ヒト・ドナー哺乳動物(例えば、有蹄類)を提供する:このドナー哺乳動物では、第1の組織細胞型特効薬プロモーターが第1の自殺遺伝子の発現を駆動することで、自殺遺伝子を発現している細胞が第1条件セット下で殺され、第2の広範囲活性(構成的または誘導性)プロモーターが第2の異なる自殺遺伝子の発現を駆動することで、第2の自殺遺伝子を発現している細胞が第1条件セットとは異なる第2条件セットによって殺される。使用する細胞型特異的プロモーターは、置換細胞によって改変される組織または器官に存在する少なくとも1つの細胞型では活性である。例えば、第1のプロモーターは哺乳動物アルブミン・プロモーターであり、肝臓の肝細胞で第1の自殺遺伝子の発現を駆動する。次に、器官または組織(例えば、肝臓)を非ヒト哺乳動物宿主に移植するが、この宿主は、例えば同一または別種の有蹄類であり、その細胞は、例えばドナー哺乳物の同一プロモーター−自殺遺伝子コンストラクトを持たないことによる結果として、第1または第2の条件セットによって、少なくとも実質的に削除可能ではない。次に、第1の置換法では、移植された器官の細胞を殺すために、宿主哺乳動物に第1の条件セットが与えられ、該移植器官では、第1の自殺遺伝子が第1のプロモーターの制御下で発現されるとともに、殺された細胞と置き換わることが可能である置換細胞の第1セットが、移植および置換のために移植体に対して直接または間接的に提供される。置換細胞の第1セットによって第1の自殺遺伝子を発現する細胞の置換をさらに促進するために、必要に応じて第1条件セットを断続的または連続的に継続してもよい。第2の置換法では、第2条件セットを与えてドナーに由来する移植体の残存細胞を殺し、これらの置換細胞と置き換わることが可能である外来置換細胞の第2のセットが移植体に直接または間接的に与えられる。置換細胞の第2セットによる置換およびその移植をさらに促進するために、必要に応じて第2条件セットを断続的または連続的に継続してもよい。
トランスジェニック非ヒト・ドナー哺乳動物(例えば、有蹄類)を提供する:このドナー哺乳動物では、第1の組織細胞型特効薬プロモーターが第1の自殺遺伝子の発現を駆動することで、自殺遺伝子を発現している細胞が第1条件セット下で殺され、第2の広範囲活性(構成的または誘導性)プロモーターが第2の異なる自殺遺伝子の発現を駆動することで、第2の自殺遺伝子を発現している細胞が第1条件セットとは異なる第2条件セットによって殺される。使用する細胞型特異的プロモーターは、置換細胞によって改変される組織または器官に存在する少なくとも1つの細胞型では活性である。例えば、第1のプロモーターは哺乳動物アルブミン・プロモーターであり、肝臓の肝細胞で第1の自殺遺伝子の発現を駆動する。次に、器官または組織(例えば、肝臓)を非ヒト哺乳動物宿主に移植するが、この宿主は、例えば同一または別種の有蹄類であり、その細胞は、例えばドナー哺乳物の同一プロモーター−自殺遺伝子コンストラクトを持たないことによる結果として、第1または第2の条件セットによって、少なくとも実質的に削除可能ではない。次に、第1の置換法では、移植された器官の細胞を殺すために、宿主哺乳動物に第1の条件セットが与えられ、該移植器官では、第1の自殺遺伝子が第1のプロモーターの制御下で発現されるとともに、殺された細胞と置き換わることが可能である置換細胞の第1セットが、移植および置換のために移植体に対して直接または間接的に提供される。置換細胞の第1セットによって第1の自殺遺伝子を発現する細胞の置換をさらに促進するために、必要に応じて第1条件セットを断続的または連続的に継続してもよい。第2の置換法では、第2条件セットを与えてドナーに由来する移植体の残存細胞を殺し、これらの置換細胞と置き換わることが可能である外来置換細胞の第2のセットが移植体に直接または間接的に与えられる。置換細胞の第2セットによる置換およびその移植をさらに促進するために、必要に応じて第2条件セットを断続的または連続的に継続してもよい。
必要に応じて、非ヒト宿主哺乳動物はトランスジェニックであってもよく、その細胞は第1および第2条件セットとは異なる第3条件セットに応じて、ドナー細胞および外来置換細胞に対して選択的に欠失可能である。このことは、例えば第2および第2自殺遺伝子とは異なる宿主の第3の自殺遺伝子を発現することで、達成し得る。このように、少なくともいくつかのドナー哺乳動物細胞の移植および置換によって得られる器官または組織産物は、該器官または器官に存在すると思われる不要な宿主哺乳動物細胞から取り除かれる。
生成器官または移植体は哺乳動物宿主にあるうちに、ならびに/あるいは哺乳動物宿主から除去された後で、任意のドナー哺乳動物細胞の生成器官または組織を取り除くプロセスを実行することができる。
実施例−肝臓
キメラ非ヒト、ヒト肝臓、または少なくとも実質的に、完全に細胞状のヒト肝臓(fully cellularly human liver)を提供することに関連した先の実施例のより具体的な変形例をさらに説明する。
キメラ非ヒト、ヒト肝臓、または少なくとも実質的に、完全に細胞状のヒト肝臓(fully cellularly human liver)を提供することに関連した先の実施例のより具体的な変形例をさらに説明する。
トランスジェニック豚ドナーを提供する:この豚ドナーでは、第1の肝細胞特異的プロモーター(構成的または誘導性)(例えばアルブミン・プロモーター)が第1の自殺遺伝子の発現を誘導して、自殺遺伝子を発現する細胞が第1条件セット下で殺され、第2の広範囲活性プロモーター(構成的または誘導性)が第2の異なる自殺遺伝子の発現を誘導することで、第2の自殺遺伝子を発現する細胞が、第1条件セットとは異なる第2条件セットによって殺される。あるいは、自殺遺伝子の代わりに、複製を阻害する遺伝子、例えばウロキナーゼ型プラスミノーゲン活性化因子(uPA)をアルブミン・プロモーターの制御下に置くことで置換細胞はuPAを発現する肝細胞に対して選択的に再生着する(repopulative)利点を有している。
トランスジェニック・ドナー豚の肝臓の少なくとも一部分を、例えば、ドナー豚の同一プロモーター−自殺遺伝子コンストラクトを持たないことの結果として、第1または第2条件セットによって少なくとも実質的には細胞を取り除くことが可能ではない宿主豚に対して、例えば異所形成的(heterotopically)または両所的(parallelotopically)に、移植する。第1の置換法では、宿主哺乳動物は、次に移植肝臓の肝細胞細胞を殺す第1条件セットを備えており、移植および置換のためのドナー肝臓に対して、殺された細胞(例えばヒト肝細胞またはヒト肝細胞始原細胞)を置き換えることができるヒト置換細胞の第1のセットが直接または間接的に提供される。ヒト置換細胞もまた、第1または第2条件セットによって取り除くことが可能ではない。さらに、ヒト置換細胞は非トランスジェニックでもよく、あるいはトランスジェニックであってもよい。第1条件セットは、断続的または連続的であることを原則として、任意に継続され、ヒト置換細胞の第1セットによるドナー肝臓肝細胞の置換をさらに促進するものであってもよい。
第2の置換法では、ドナー肝臓の豚残存細胞を殺すために、第2条件セットをブタ宿主に提供し、またこれらの残存ドナー細胞と置き換わることが可能なヒト置換細胞の第2セットを移植体へ直接または間接的に提供する。第1の置換後に残存する豚細胞は、大部分が肝臓の非肝細胞であり、ここではアルブミン・プロモーターによる第1の自殺遺伝子(例えば胆管胆管細胞および門脈路血管細胞)の発現は実質的には駆動されない。また、第2条件セットは、断続的または連続的であることを原則として、提供され続けることで、ヒト置換細胞の第2セットによるドナー肝臓肝細胞の置換をさらに促進することができる。
免疫寛容
本発明によれば、宿主動物は、移植されたドナー器官または組織あるいは置換細胞に対して、少なくとも実質的に免疫学的に寛容である。関連した実施形態において、宿主動物およびドナー器官または組織は、総じて、その系にもたらされる置換細胞に対して、少なくとも実質的に免疫学的に寛容である。本発明は、十分に寛容な宿主動物が得られるか、または作製される方法に限定されるものではなく、任意の方法または方法の組合せを用いることができる。
本発明によれば、宿主動物は、移植されたドナー器官または組織あるいは置換細胞に対して、少なくとも実質的に免疫学的に寛容である。関連した実施形態において、宿主動物およびドナー器官または組織は、総じて、その系にもたらされる置換細胞に対して、少なくとも実質的に免疫学的に寛容である。本発明は、十分に寛容な宿主動物が得られるか、または作製される方法に限定されるものではなく、任意の方法または方法の組合せを用いることができる。
ドナー器官または組織に寛容な宿主を得ることができる1つの方法は、同一種またはその同一種の近縁種に由来する宿主およびドナー動物を用いて得ることができる。関連した実施形態では、宿主およびドナー動物は、同一近交系またはクローン的に関連したものであることから、宿主およびドナー動物は少なくとも実質的にコンジェニック(遺伝的背景が同一)である。近交系の樹立とクローニングのための方法とは、非ヒト哺乳動物(例えば齧歯動物および有蹄類)で十分に確立されている。さもなければ少なくとも実質的にコンジェニックである宿主およびドナー動物に対する宿主特異的遺伝学的修飾および/またはドナー特異的遺伝学的修飾(例えば自殺遺伝子または耐性遺伝子の発現)は、通常、ドナー細胞に対する宿主の寛容に影響を及ぼすものではなく、本明細書では少なくとも実質的にコンジェニックと考えられる。ドナー特異的導入遺伝子が他の尺度がない状態でドナー細胞に対する宿主の寛容に対してネガティブな影響を与えるという希な現象では、宿主は、例えば導入遺伝子産物または少なくともその問題のエピトープを初期発生段階(例えば、哺乳動物の胎児発育過程)で導入することによって、導入遺伝子産物に対して寛容となるように条件付けられる。
1つの方法は、胎児哺乳動物環境が外来のヒト細胞および組織に対して寛容であることから、胎児、非ヒト哺乳動物宿主、例えばブタまたはヒツジあるいは齧歯動物(マウス、ラット、モルモット、カピバラ等)の胎児を用いることで、ヒト組織に十分に寛容な宿主を提供する。この実施形態では、非ヒト哺乳動物胎児が、宿主動物であるが、理解すべきことは、そのような宿主は、本発明によれば、出生後、ドナーおよび/または置換細胞を維持し続ける。
別の方法は、出生後段階の非ヒト哺乳動物宿主(例えば、豚)を提供することで、ヒト組織に十分に寛容な宿主を提供するもので、該宿主は、胎児発育の過程で、使用される種類のドナーに由来する細胞と、または該ドナーに特徴的な細胞抗原、ならびに/あるいは同様に、置換細胞または抗原的に類似の細胞、あるいは使用される置換細胞の特徴を示す細胞性抗原とに接触する。一方法では、実際のドナーまたは同一種類のドナー哺乳動物(ドナー細胞に対して寛容を与える)に由来する骨髄ならびに/あるいは置換細胞または目的の置換細胞に少なくとも抗原的に類似しているもの(置換細胞に対して寛容を与える)が誘導される哺乳動物に由来する骨髄を、植え付けられるべき非ヒト哺乳動物胎児に移植することで、外来細胞に対する寛容が哺乳動物宿主に与えられる。出生後、そのような動物ではヒト組織/細胞に対する寛容が改善されている。
さらなる方法は、化学処理および/または放射線を用いて宿主の免疫系を弱らせることで、宿主および/または置換細胞に十分に寛容なある発生の出生後段階にある非ヒト宿主を提供する。任意には、宿主の切除骨髄を、使用されるドナー動物のタイプの骨髄および/または置換細胞が誘導される生物のタイプの骨髄(例えばヒトまたは非ヒト哺乳動物)と置換することができる。例えば、宿主骨髄の少なくとも実質的に大部分を破壊するのに十分なX線またはγ線を用いることができる。そのような方法は、例えば、米国特許第6,018,096号(その全体を本明細書に援用)に開示されている。放射線の有無にかかわらず、シクロホスファミド、ブスルファンまたはその組合せ等の骨髄破壊剤による動物宿主の骨髄の少なくとも実質的に全ての化学的切除を用いることで、ヒト組織に対する相当な寛容を得ることができる。
もう一つの方法は、米国特許第6,296,846号(その全体を本明細書に援用)にもとづいて条件づけられた宿主を提供することで、宿主および/または置換細胞に十分に寛容な非ヒト哺乳動物宿主を提供する。
もう一つの方法は、遺伝的に免疫無防備状態である宿主を提供することによって、提供者および/または置換細胞に十分に寛容な宿主を提供する。そのような宿主は、意図的に導入された(例えば、標的化)またはさもなければ、過去の任意の時間または任意の以前の世代に生じ、宿主の免疫系を混乱させる少なくとも1つの遺伝学的修飾または突然変異を含む。例えば、Rag1遺伝子(組替え活性化遺伝子1)における変異についてホモ接合の非ヒト哺乳動物は、T細胞およびB細胞が欠乏していることによって特徴づけられる。Rag1遺伝子欠損マウス(ノックアウト方法によって得られる)は、既に報告されており、周知の技術である(Mombaerts, P. et al., RAG-1-deficient mice have no mature B and T lymphocytes Cell, (1992) 68 (5), 869-77、該文献の全体を本明細書中に援用する)。Rag1遺伝子が欠乏するように遺伝的に修飾された豚は、米国特許公開第20050155094号(特許出願第10/503,464号)(全体を本明細書中に援用する)に開示されている。当該技術分野で一種のSCID(重症複合型免疫不全症)として知られているPrkdc遺伝子の突然変異についてホモ接合である非ヒト哺乳動物もまた、T細胞およびB細胞の欠乏によって特徴づけられる。Foxn1遺伝子の突然変異についてホモ接合型であるヒト哺乳動物は、ヌード哺乳動物として知られており、T細胞の欠乏およびB細胞発生の部分的欠陥を持つ胸腺発育不全によって特徴づけられる。これら3種類の突然変異の全ては、例えば、抗原提示細胞(APB)およびナチュラルキラー細胞(NK細胞)に関した二次免疫欠乏によっても、特徴づけられる。
インターロイキン2受容体γ鎖および/またはβ2ミクログロブリンにさらに変異を有する非ヒト哺乳動物もまた、使用することが可能である。例えば、SCID/IL2受容体γ鎖nullまたはSCID/β2ミクログロブリンnull非ヒト哺乳動物も宿主および/またはドナーとして使用してもよい。Ishikawa et al., Development of functional human blood and immune systems in NOD/SCID/IL2 receptor {gamma} chain(null) mice Blood (2005) 106(5), 1565-1573,およびYoshida et al., Human cord blood-derived cells generate insulin producing cells in vivo, Stem Cells 2005 23(9): 1409-1416,を参照せよ。各々の文献は全体を本明細書中に援用する。NOD/SCID/IL2受容体γ鎖nullマウスをストック番号004048としてジャクソン・ラボラトリー(Jackson Laboratory)から購入して利用可能である。NOD/Cg−PRkdcscidB2mtm1Unc/Jマウスをストック番号002570としてジャクソン・ラボラトリー(Jackson Laboratory)から購入して利用可能である。これらの株の各々は、ヒト細胞および優れた移植に対する寛容とその中のヒト細胞の多重系列発生(multi-lineage development)によって特徴づけられる。例えば、Ishikawa他(2005)は、1x105個のLin−hCD34+細胞または2x104個のLin−hCD34+hCD38− 細胞を、放射線処理(100cGy)されたGGTA1null/NOD/SCID/IL2rγnull に対して、誕生後48時間以内に顔面静脈経由で移植し、持続的な多重系列統造血を生じた。マウス・インターロイキン2受容体γ鎖のmRNA配列は、GenBank受託番号D13821(配列番号15、8ないし1117にCDS)として報告されている。さらに、ヨシダ(Yoshida)他(2005)に報告されているように、誕生後48時間以内にNOD/SCID/β2ミクログロブリンnullマウスに移植されたヒト臍帯血細胞は、ヒトのインシュリン産生細胞を生じた。
非ヒト哺乳動物ドナーが用いられる実施形態に関し、導入された置換細胞に対してドナー体内の免疫細胞またはドナー器官もしくは組織を有する宿主動物に移される免疫細胞が攻撃する可能性を妨げる、あるいは減少させるために、必要に応じて、ドナーは、例えば本明細書に記載された方法のいずれかによって、置換細胞に寛容であってもよい。例えば、物理的、化学的および/または、遺伝学的な技術の結果として免疫不全であるドナーを用いることができる。あるいは、重症の免疫不全ではないが、置換細胞に対して寛容であるドナーを用いることができる。また、置換細胞が移植可能であるドナー体内に置換細胞が誘導される生体(またはある種の生体)から得た骨髄細胞を導入する方法を、例えば、ドナー免疫系を調整するために使用することができ、それによってドナー器官または組織が宿主に移植された後に含まれる置換細胞に寛容となる。
遺伝学的に修飾され、条件的(conditional)に免疫不全である非ヒト哺乳動物もまた、免疫欠損を条件的に誘導する十分に寛容な宿主動物(またはドナー動物)として使用することができる。例えば、プロ毒素−毒素変換酵素型の自殺遺伝子の発現がリンパ球特異的なプロモーター(例えば、jak3(ヤヌス・キナーゼ3)プロモーターの制御下にある導入遺伝子コンストラクトを含むトランスジェニック哺乳動物を作製することができる。T細胞およびB細胞は、トランスジェニック動物にプロ毒素(プロドラッグ)を与えることで、条件的に誘発される。そのような哺乳動物の作製は、例えば、国際特許出願番号WO2004/027029A2およびその対応の米国国際段階出願第10/527,587号(各々全体を本明細書中に援用する)によって、さらに提供される。
少なくともヒト細胞に対して実質的に寛容な非ヒト哺乳動物宿主を提供し得る一つの方法は、ヒト・ドナー器官または組織を宿主体内の免疫学的寛容部位に移植することによる。既報告の免疫学的寛容部位として、精巣、眼(前眼房、角膜、および網膜)、脳、ならびに胎盤が挙げられる。非ヒト哺乳動物宿主の腎臓嚢下の異種組織移植が、少なくとも場合によっては、拒絶を回避することができるとも報告されている。
移植
移植
本発明にもとづく動物宿主によって支持されるドナー器官または組織(例えば、ヒトまたは非ヒト哺乳動物)は、任意の日数にわたって生きた状態で維持することができる。置換細胞によるドナー器官または組織のde novoおよび/または累進的な再形成はこの時期の任意の部分で、起こり得る。さらに、再構成された器官または組織は、宿主動物で生きた状態で維持され続けることができる。それを、必要に応じて、別の宿主に移入することもできる。実験、さらなる処理、別の非ヒト宿主に対する移植、および/またはヒトに対する移植等の目的に必要とされる場合、非ヒト宿主から、再構成されたドナー器官または組織を除去、すなわち外植することも可能である。
種々の器官および組織を1つの個体から別の個体(豚から豚へ、ヒトからヒトへ、豚からヒツジへ、豚から霊長類へ、または霊長類から豚、例えばヒトから豚へ)に移植するのに必要な外科的技術は、十分に開発されている。本発明によれば、ヒトまたは非ヒト哺乳動物ドナーからの器官または器官は非ヒト哺乳動物宿主の任意の適当な位置に移植することが可能であり、該宿主によって生きた状態で維持される。血管が新生された器官および組織またはそれらの一部分への血液供給は、例えばドナー動脈血管を互いに吻合することで、また必要に応じて宿主静脈血管とドナー静脈血管とを互いに吻合することによって、確立することができる。ドナーまたは宿主からの血管移植片も、必要に応じて使用することができ、それによって宿主体内のドナー器官または組織に対する血液の流入および流出が得られる。より小さなドナー器官(例えば内分泌腺)またはより薄いドナー組織(例えば皮膚)に対して、十分な血液供給を、例えば、宿主哺乳動物の血管化部位または表面と接触して器官または組織を移植することによって、短期間で確立することができる。
本発明にもとづいて置換細胞により少なくとも部分的に再構成されるドナー器官または組織の移植を、正所的、半正所的、両所的、または異所的移植としておこなうことができる。正所性移植体は、本明細書中に定義されるように、ドナー器官または組織が、宿主体内の同一または相同な構造のうちの少なくとも1つと置換される移植体である。半正所性移植体は、本明細書中に定義されるように、ドナー器官または組織が、宿主体内の一対の同一または相同な構造の少なくとも一方と置換される。ドナーおよび宿主が同一の種または型である場合、ドナーと宿主との間の機能解剖学は、同一または少なくとも実質的に同一である。
両所性移植体は、本明細書中に定義されるように、宿主体内の同一または相同な構造の同一供給源の少なくとも一部分から血液を受け取るようにしてドナー器官または組織が移植される移植体である。任意には、ドナー器官または組織の血液ドレナージが内在性宿主構造と同じ血管のうちの少なくとも1つに対するもの、または、少なくとも実質的に対応する血管に対するものであり得る。また、任意に、宿主の中に残る相応する宿主器官または組織は必要に応じて大きさを外科的に縮小することができる。
本明細書中に定義されるように、異所的な移植体はドナー器官または組織がドナー体内の器官または組織の位置の特徴的でない場所または環境で宿主に移植されるものである。
以下の実施例は器官または組織で発明の方法を実行するために種々のヒトまたは非ヒト哺乳動物ドナー器官または組織を非ヒト哺乳動物宿主に移植するための外科的技術を例示するが、各々のために使用可能な技術を限定するものではない。
(1)腎臓
腎臓は、対をなした器官である。したがって、それぞれ、宿主の腹大動脈と下大静脈に、または宿主の対応する構造に、ドナー腎の腎動脈と静脈を吻合することによって、一部の取付けられた提供者側尿管に加えて、片腎を宿主と移植体ドナー腎から切除することは、簡便である。提供者側尿管は、例えば、粘膜下トンネルを経てそれを膀胱に移植することによって、宿主膀胱に接続される。両腎臓は、必要に応じて置き換えることもできる。
腎臓は、対をなした器官である。したがって、それぞれ、宿主の腹大動脈と下大静脈に、または宿主の対応する構造に、ドナー腎の腎動脈と静脈を吻合することによって、一部の取付けられた提供者側尿管に加えて、片腎を宿主と移植体ドナー腎から切除することは、簡便である。提供者側尿管は、例えば、粘膜下トンネルを経てそれを膀胱に移植することによって、宿主膀胱に接続される。両腎臓は、必要に応じて置き換えることもできる。
(2)肺
肺は、対をなした器官である。従って、1つの肺を宿主から切除し、肺動脈と宿主心臓の肺静脈とを吻合することでその位置にドナー肺を移植することは、簡便である。このステップは、例えば、宿主の心臓に連結されたままになっている肺動脈の切片に、ドナー肺に接続している肺動脈残留切片を吻合して、同様にドナーと宿主肺静脈切片とを接続することでおこなうことができる。通常、移植された肺は、宿主で換気されなければならず、それによって、直接または間接的にそれを道管(気管)または宿主の対応する構築物に接続することによってその構造と機能の保持を助ける。しかし、非換気の肺移植も本発明の範囲内である。もしも要望または必要とされるならば、葉または残存宿主肺の部分を取り出すができる。両方の宿主肺必要に応じて完全に置き換えることもできる。
肺は、対をなした器官である。従って、1つの肺を宿主から切除し、肺動脈と宿主心臓の肺静脈とを吻合することでその位置にドナー肺を移植することは、簡便である。このステップは、例えば、宿主の心臓に連結されたままになっている肺動脈の切片に、ドナー肺に接続している肺動脈残留切片を吻合して、同様にドナーと宿主肺静脈切片とを接続することでおこなうことができる。通常、移植された肺は、宿主で換気されなければならず、それによって、直接または間接的にそれを道管(気管)または宿主の対応する構築物に接続することによってその構造と機能の保持を助ける。しかし、非換気の肺移植も本発明の範囲内である。もしも要望または必要とされるならば、葉または残存宿主肺の部分を取り出すができる。両方の宿主肺必要に応じて完全に置き換えることもできる。
(3)心臓
第1の方法では、ドナー心臓は宿主心臓を切除して、宿主の少なくとも実質的に対応する血管にドナー心臓の必要な主な動脈および静脈血管の全てを吻合することによって、宿主に同所的に移植される。当該技術分野で、有蹄類の心臓および特にブタの心臓の機能解剖学が、ヒト心臓のそれと全く類似しているとよく認められている。第2の方法では、ドナー心臓は、宿主頸動脈(例えば、端側)と宿主頸静脈(例えば、端側)に対するドナー心臓の肺動脈にドナー心臓の大動脈を吻合することによって、異所形成的に非ヒト哺乳動物宿主(そのようなヒツジまたはウシ)に移植される。
第1の方法では、ドナー心臓は宿主心臓を切除して、宿主の少なくとも実質的に対応する血管にドナー心臓の必要な主な動脈および静脈血管の全てを吻合することによって、宿主に同所的に移植される。当該技術分野で、有蹄類の心臓および特にブタの心臓の機能解剖学が、ヒト心臓のそれと全く類似しているとよく認められている。第2の方法では、ドナー心臓は、宿主頸動脈(例えば、端側)と宿主頸静脈(例えば、端側)に対するドナー心臓の肺動脈にドナー心臓の大動脈を吻合することによって、異所形成的に非ヒト哺乳動物宿主(そのようなヒツジまたはウシ)に移植される。
(4)肝臓
第1の方法において、ドナー肝臓の同所的移植は、宿主肝臓を切除し、(i)ドナー肝臓に接続されている一部のドナー肝動脈に対する宿主肝動脈の残りの部分、(ii)ドナー肝臓に接続されている一部のドナー門脈に宿主門脈の残りの部分、および(iii)ドナー肝臓に結合されるドナー肝静脈を、下大静脈に接続されている宿主肝静脈または直接宿主下大静脈に接続されている宿主肝静脈のいずれかに吻合することによってなされる。
第1の方法において、ドナー肝臓の同所的移植は、宿主肝臓を切除し、(i)ドナー肝臓に接続されている一部のドナー肝動脈に対する宿主肝動脈の残りの部分、(ii)ドナー肝臓に接続されている一部のドナー門脈に宿主門脈の残りの部分、および(iii)ドナー肝臓に結合されるドナー肝静脈を、下大静脈に接続されている宿主肝静脈または直接宿主下大静脈に接続されている宿主肝静脈のいずれかに吻合することによってなされる。
第2の方法では、ドナー肝臓またはその部分が宿主肝臓またはその残留する部分に関して両所的に移植されることで、肝臓の各々が肝動脈血液の少なくとも一部分と門脈の血液とを受け、また各々が直接、または、間接的に、下大静脈へ流出する。変形例では、宿主門脈流入がドナーと宿主肝臓との間で分割されることで、ドナー肝臓は腸の膵臓排液が与えられ、また宿主肝臓は胃脾静脈血が与えられる (例えばLilly et al., Split portal flow in heterotopic hepatic transplantation J Pediatr Surg. 1975 Jun; 10(3): 339-48.を参照せよ)。当業者は、種々の補助肝移植技術が当該技術分野で知られていており、本発明にもとづく両所的および異所的移植に容易に適応し得る認識するであろう。
(5)膵臓
1つの方法では、結合したドナー十二指腸の少なくとも一部分を有するドナー膵臓が宿主に移植される一方で、結合した宿主膵臓が定位置に残されている。それぞれ、ドナー膵臓動脈および静脈を宿主の骨動脈および静脈に取り付けることができる。ドナー十二指腸が宿主小腸に取り付けらることで、主膵管の外分泌酵素が入るのを可能にする。第2の関連方法では、宿主膵臓が少なくとも部分的に摘出される。
1つの方法では、結合したドナー十二指腸の少なくとも一部分を有するドナー膵臓が宿主に移植される一方で、結合した宿主膵臓が定位置に残されている。それぞれ、ドナー膵臓動脈および静脈を宿主の骨動脈および静脈に取り付けることができる。ドナー十二指腸が宿主小腸に取り付けらることで、主膵管の外分泌酵素が入るのを可能にする。第2の関連方法では、宿主膵臓が少なくとも部分的に摘出される。
(6)皮膚
ヒト皮膚は毛を持つもの(大部分の体(例えば頭皮))または毛を持たないもの(例えば手の掌と足の裏)がある。皮膚は、3層(外側から内部にかけて)からなる。すなわち、表皮、真皮、および皮下層であって、該皮下層は疎性結合組織および脂肪結合組織を有する。毛嚢および関連皮脂(油)腺は、有毛皮膚に存在する。ヒトでは、汗腺は有毛および無毛皮膚で存在する。ドナー皮膚の切片、例えばヒト皮膚(表皮および真皮のみまたは皮下層の表皮、真皮、および少なくとも一部分を含む)を、非ヒト哺乳動物宿主の領域(宿主皮膚は、少なくとも部分的に除去されている)に、外科的に移植することができる。移植皮膚に包帯をすることで、循環の確立を促進し、かつ宿主の調製された領域との良好な接触を確実にすることができる。
ヒト皮膚は毛を持つもの(大部分の体(例えば頭皮))または毛を持たないもの(例えば手の掌と足の裏)がある。皮膚は、3層(外側から内部にかけて)からなる。すなわち、表皮、真皮、および皮下層であって、該皮下層は疎性結合組織および脂肪結合組織を有する。毛嚢および関連皮脂(油)腺は、有毛皮膚に存在する。ヒトでは、汗腺は有毛および無毛皮膚で存在する。ドナー皮膚の切片、例えばヒト皮膚(表皮および真皮のみまたは皮下層の表皮、真皮、および少なくとも一部分を含む)を、非ヒト哺乳動物宿主の領域(宿主皮膚は、少なくとも部分的に除去されている)に、外科的に移植することができる。移植皮膚に包帯をすることで、循環の確立を促進し、かつ宿主の調製された領域との良好な接触を確実にすることができる。
(7)骨
骨の血管は、非常に多い。緻密組織の血管は、骨膜で分岐している血管が稠密となったネットワークから誘導される。この膜から、血管は緻密組織で微細な口に移って、その物質を横断する管を貫く。海綿骨組織は、類似の方法で供給されるが、血管の数は少なく、また血管がより大きいことから、外側の緻密組織を穿孔して骨の海綿質部分の空洞に分布する。長骨において、多数の孔は、関節面の近くの端で見ることができ、それらのうちのいくつかは、言及される血管からなる大きなセットの同脈に対して、経路を作る。しかし、最も多数のおよび最も大きな開口は海綿骨組織の静脈のいくつかのためであり、それは動脈とは別に現れる。大部分の扁平骨および多くの短い海綿骨で、一つ以上の大きな開口が観察され、骨の中心部に向けて栄養動脈および静脈に対応している血管を送る。静脈は、3つの場所で長骨から現れる。すなわち、(1)1または2本の大静脈は動脈を伴う;(2)多数の大きなおよび小さい静脈は、関節性の四肢で現れる;(3)多くの小血管は、緻密骨質の外に出て行く。平坦な頭蓋骨では、静脈は太くて数が多く、板間層の組織内の蛇行管内を走り巡り、骨の細いラメラによって形成されている管の側面が近隣の格子構造からの分岐を通過させるために、あちらこちらに穿孔される。Gray, Henry. Anatomy of the Human Body. Philadelphia: Lea & Febiger, 1918; Bartleby.com, 2000.。
骨の血管は、非常に多い。緻密組織の血管は、骨膜で分岐している血管が稠密となったネットワークから誘導される。この膜から、血管は緻密組織で微細な口に移って、その物質を横断する管を貫く。海綿骨組織は、類似の方法で供給されるが、血管の数は少なく、また血管がより大きいことから、外側の緻密組織を穿孔して骨の海綿質部分の空洞に分布する。長骨において、多数の孔は、関節面の近くの端で見ることができ、それらのうちのいくつかは、言及される血管からなる大きなセットの同脈に対して、経路を作る。しかし、最も多数のおよび最も大きな開口は海綿骨組織の静脈のいくつかのためであり、それは動脈とは別に現れる。大部分の扁平骨および多くの短い海綿骨で、一つ以上の大きな開口が観察され、骨の中心部に向けて栄養動脈および静脈に対応している血管を送る。静脈は、3つの場所で長骨から現れる。すなわち、(1)1または2本の大静脈は動脈を伴う;(2)多数の大きなおよび小さい静脈は、関節性の四肢で現れる;(3)多くの小血管は、緻密骨質の外に出て行く。平坦な頭蓋骨では、静脈は太くて数が多く、板間層の組織内の蛇行管内を走り巡り、骨の細いラメラによって形成されている管の側面が近隣の格子構造からの分岐を通過させるために、あちらこちらに穿孔される。Gray, Henry. Anatomy of the Human Body. Philadelphia: Lea & Febiger, 1918; Bartleby.com, 2000.。
種々の骨およびその一部の宿主に対する同所的および異所的な移植は、宿主の適当な動脈および静脈にドナー骨の主要動脈および血管を吻合することによっておこなうことが可能である。移植片の大きさによって、end-to-sideの様式で、ドナー骨を宿主大腿動脈および静脈に対して拡大下で吻合することが可能である。例えば、Lee et al., Use of swine model in transplantation of vascularized skeletal tissue allografts, Transplantation Proc. (1998) 30, 2743-2745(その全体の内容を本明細書中に援用)を参照せよ。
(8)血管
例えば、血管内の血流が宿主で確立されるように、ドナー血管は宿主に同所的または異所的方法で移植される。
例えば、血管内の血流が宿主で確立されるように、ドナー血管は宿主に同所的または異所的方法で移植される。
(9)ドナー器官または組織の異所的移植のための一般的な部位は、例えば、一般に腎臓被膜、皮下腔と内臓脈管系を含む。腎臓および腎臓被膜が多数の種類の器官または組織またはその一部が異所形成的に移植され、かつ生きた状態で維持される高度に血管形成された環境を提供することは、周知の技術である。宿主哺乳動物への組織の皮下移植も、周知の技術である。内臓脈管系は、ドナー器官または組織と宿主の循環系との間に循環系接続を移植するか、さもなければ得るための一般的な部位と認められる。したがって、例えば、ドナー器官または組織あるいはその一部を異所形成的に非ヒト哺乳動物宿主の腎臓被膜下に移植、宿主に皮下移植、あるいは宿主の内臓脈管系に移植、さもなければ宿主による支えられた生きた状態とするために、接続することができる。
ヒトおよび非ヒト哺乳動物器官または組織をヒトへ移植するための外科移植技術が確立されている。これらの技術は、非ヒト哺乳動物宿主が宿していた、および該非ヒト哺乳動物宿主内で置換細胞によって少なくとも部分的に再構成されたヒトまたは非ヒト哺乳動物ドナー器官または組織が、後にヒトに移植される本発明の実施形態に容易に適用可能である。
本発明の一実施形態において、ドナー脳またはその実質的な一部分は本発明の促進された器官および組織の細胞再形成方法によってヒト細胞で少なくとも実質的に細胞再構成可能である器官または組織から、特別に除外される。関連した実施形態は、特別にヒト神経単位によってドナー脳の最も少なく実質的な器官および組織の細胞再形成またはその実質的な一部分を除外する。
置換細胞およびドナー器官または組織への該置換細胞の導入
本明細書中で言及される置換細胞が、該細胞が導入されるドナー器官または組織で増殖して、少なくとも部分的に器官または組織の成熟天然ドナー細胞の一部と置き変わることができる。例えば、器官または組織の増殖および再構成が可能である分化細胞を用いることができ、また同様に、器官または組織の内因性成熟細胞を置き換えるために器官または組織で成熟または分化することができる任意の未熟または未分化細胞型を用いることもできる。置換細胞は、任意の適当な細胞型であり、限定されるものではないが、分化細胞、始原細胞、組織特異的幹細胞、多分化能幹細胞、および全能の幹細胞が挙げられる。したがって、本明細書中で使用される「置換細胞」は、本来ドナー哺乳動物またはその器官もしくは組織またはその一部分に導入された状態にある細胞のみならず、細胞分裂および/または分化および/または退行分化のプロセスによって導入された細胞に由来する細胞を包含するものであると理解すべきである。置換細胞がドナー器官および/または宿主動物として同一種または異なる種に由来のものであってもよく、また初代細胞または細胞株の細胞であってもよい。例えば、本発明の一実施形態において、ヒト置換細胞は、ヒトまたは非ヒト哺乳動物ドナー器官または組織に導入され、このことは、器官または組織が宿主で器官または組織生きた状態で支えられる非ヒト哺乳動物宿主に移植される前および/または後になされる。外来の置換細胞は遺伝学的に修飾または無修飾のものであってもよく、例えばトランスジェニックまたは非トランスジェニックとすることができる。
本明細書中で言及される置換細胞が、該細胞が導入されるドナー器官または組織で増殖して、少なくとも部分的に器官または組織の成熟天然ドナー細胞の一部と置き変わることができる。例えば、器官または組織の増殖および再構成が可能である分化細胞を用いることができ、また同様に、器官または組織の内因性成熟細胞を置き換えるために器官または組織で成熟または分化することができる任意の未熟または未分化細胞型を用いることもできる。置換細胞は、任意の適当な細胞型であり、限定されるものではないが、分化細胞、始原細胞、組織特異的幹細胞、多分化能幹細胞、および全能の幹細胞が挙げられる。したがって、本明細書中で使用される「置換細胞」は、本来ドナー哺乳動物またはその器官もしくは組織またはその一部分に導入された状態にある細胞のみならず、細胞分裂および/または分化および/または退行分化のプロセスによって導入された細胞に由来する細胞を包含するものであると理解すべきである。置換細胞がドナー器官および/または宿主動物として同一種または異なる種に由来のものであってもよく、また初代細胞または細胞株の細胞であってもよい。例えば、本発明の一実施形態において、ヒト置換細胞は、ヒトまたは非ヒト哺乳動物ドナー器官または組織に導入され、このことは、器官または組織が宿主で器官または組織生きた状態で支えられる非ヒト哺乳動物宿主に移植される前および/または後になされる。外来の置換細胞は遺伝学的に修飾または無修飾のものであってもよく、例えばトランスジェニックまたは非トランスジェニックとすることができる。
多くの器官または組織は、一つ以上の成熟した細胞型から成る。特定のタイプの置換細胞は、特徴的に所定の器官または組織を構成する成熟した細胞型の総数より少ないものを置き換えることが実質的にできるだけである。例えば、ドナー肝臓の置換細胞として使用される成熟肝細胞は通常、他のタイプの細胞(例えば胆管細胞)でなく肝臓を構成する肝細胞を置き換えることができる。本発明の一実施形態において、所定の器官または組織について、組織の一つ以上の細胞型が置き換えられることができるように、一つ以上のタイプの置換細胞(少なくとも、もう一方に関して、少なくとも部分的に重なる可能性のないもの)がドナー器官または組織に導入される。多分化能または全能性置換細胞も使用してもよく、利用可能である場合、所定のドナー器官または組織の一つ以上の細胞型を置き換えるために利用することができる。所定の器官または組織(例えば肝臓)のために、可能性の異なる範囲による種々の異なるタイプの置換細胞は、当該技術分野で知られている。
任意の方法または複数の方法の組合せで、置換細胞をドナー器官または組織に導入することができ、任意の形態または複数の形態の組合せであってもよい。例えば、ヒトであるか非ヒト哺乳動物プロバイダ由来の初代細胞は、対応するドナー器官または組織の置換細胞として使用するために得ることができる。初代細胞は、得られるように、混合型であってもよく、あるいは選択および単離されたもの、あるいは必要に応じて組み合わされたものであってもよい。都合のよいことに、置換細胞プロバイダ器官または組織(「プロバイダ器官または組織」)に存在する細胞型の混合物の使用によって、少なくともドナー器官または組織の細胞の型の各々を実質的に置き換えるのに必要な置換細胞の型の全てとまではいかないが、大部分が提供される。初代細胞置換細胞がとる形に関しては、一実施形態において、プロバイダ器官または組織の一部を、外科的に移植可能であり、ドナー器官または組織と外科的に組み合わせることが可能である。例えば、プロバイダ器官または組織から組織の一つ以上のプラグを対応するドナー器官または組織に移植することができ、あるいはプロバイダ器官または組織の切片を、外科的に、十分に調製されたドナー器官または組織に、それらの内部構造が接触するようにして、界面的に連結させることができる。このように、プロバイダ組織の移植された一部の細胞の組織学配列は実質的に妨げられない。別の例では、プロバイダ皮膚の断片をドナー皮膚の断片に移植することができ、または切断面を有する肝臓切片をドナー肝臓の切断面に外科的に取り付けることができる。別の実施形態において、単細胞および/または凝集体の細胞懸濁液は、プロバイダ器官または組織の一部または全体から作られる。さらに懸濁液は、ドナー器官または組織(どちらでも直接および/または間接的に)に導入される。例えば、このことは、ドナー器官または組織がその中に確立された後に、宿主動物の血流量に懸濁液を注入することによって、あるいはドナー器官または組織が宿主動物に移植される前に、ドナー動物の血流に懸濁液を注入することによってなされる。例えば、プロバイダ膵臓からの膵島または膵臓細胞の一般の懸濁液をドナー膵臓に注入する、および/またはプロバイダ膵臓の一つ以上のプラグをドナー膵臓に挿入する。プロバイダ血管内皮または器官血管内皮細胞の懸濁液を、例えば、輸液または潅流によって、ドナー器官または組織内皮で接触させることができる。別の実施形態において、置換細胞は胎児または出生後ドナー哺乳動物に導入され、そこでそ一つ以上の器官に統合され、ドナー哺乳動物の細胞と置換細胞の含む一つ以上のキメラ器官または組織を形成する。このように、置換細胞は、ドナー哺乳動物から外植される(explant)ドナー器官または組織に、すでに存在する。任意の適当な技術(例えばカテーテルまたは針を使用する技術)を、直接または間接的に、ドナー器官または組織またはドナーまたは宿主の任意の所望の位置へ単細胞および/または細胞集塊の懸濁液を注入または注射することに使用することが可能である。
以下の実施例は、特定のドナー器官または組織のための置換細胞として使用し得る細胞の特定型式を例示する。
組織ベースの幹細胞には、増殖して、対応する組織細胞に分化する能力がある。例えば、膵臓胆管細胞は、ランゲルハンス島に分化することができる。肝性卵形細胞は、肝細胞に分化することができる。成人性幹細胞と特定の組織ベースの幹細胞は、他のタイプの細胞に分化することができる柔軟性によって特徴づけられる。例えば、造血幹細胞は、血管内皮細胞、神経単位、グリア、肝細胞、心筋細胞、尿細管細胞、肺上皮、腸細胞、皮膚上皮、骨、軟骨、筋肉、脂肪、および脳等の細胞に分化することができる。脂肪幹細胞は、多種多様な細胞型に分化することもできる。胚性幹細胞には、増殖して、任意の組織に分化する能力がある。例えば、胚性幹細胞、胚性幹細胞から作り出される細胞株あるいは胚性幹細胞または細胞株から誘導される始原細胞は、本発明によってドナー器官または組織を再構成するのに用いられる。分化型の幹細胞を提供する方法は、例えば米国特許第6,576,464号によって提供される。ヒト胚性生殖細胞を分化させる方法は、例えば、米国特許第6,562,619号によって提供される。
二分化能胚性肝臓幹細胞系は、マウスで示されるように、肝再生に関与することもでき、胆管および肝細胞として分化することもできる(Strick-Marchand et al. Proc. Natl. Acad. Sci. USA June 1, 2004, vol. 10, no. 22, 8360-8365)。米国特許第6,129,911号また、肝臓幹細胞を開示しており、その全体の内容を本明細書に援用する。二分化能胚性肝臓幹細胞系は、マウスで示されるように、肝再生に関与することもでき、胆管および肝細胞として分化することもできる(Strick-Marchand et al. Proc. Natl. Acad. Sci. USA June 1, 2004, vol. 10, no. 22, 8360-8365)。米国特許第6,129,911号また、肝臓幹細胞を開示しており、その全体の内容を本明細書に援用する。
筋芽細胞(平滑筋に分化)、骨格筋、または心筋(心筋細胞)が、筋組織の置換細胞として使用し得る。心筋細胞もまた、心筋の置換細胞として使用し得る。
置換細胞提供動物または細胞系統に対して、例えば、事前選択された選択剤に対する耐性の付与および/または異種抗原の除去のための、遺伝学的な修飾をおこなってもよい。一実施形態では、ヒト置換細胞に対して、選択剤に対する耐性を発現させるための遺伝学的に修飾を施す。そのような細胞を同様な耐性を持つ宿主と上記選択剤の影響を受けやすい(耐性ではない)ドナー器官または組織とともに、使用し得る。
好ましくは、外来の置換細胞は、実質的に無菌的方法でドナー器官または組織に導入される。外来置換細胞は、ドナー器官または組織固有の細胞を選択的かつ条件的に傷害する前中後に導入され、傷害が生じた後の置換細胞の生存を可能にする。一実施形態において、置換細胞は、置換細胞がドナーから外植またはそれ前に宿主に移植された後、ドナーまたは組織に導入される。任意には、ドナー器官または組織への置換細胞の1回以上の導入を、宿主体内に器官または組織を確立した後に、実施する。別の実施形態では、宿主に移植された後に、ドナー器官または組織に置換細胞が導入される。本発明の別の実施形態は、移植用提供組織または器官を宿主に移植する前に、該移植用提供組織または器官を一般の方法(例えば放射線照射)で選択的に傷つけることを提供する。この実施形態の変形例では、置換細胞が傷害によって害されないように、そのような一般的傷害の後に該置換細胞を導入する。さらなる変形例では、ドナー器官または組織を宿主に移植した後に該ドナー器官または組織のさらなる選択的かつ条件的欠失を実行することができる。
実施例−ドナー哺乳動物から外植後、ドナー器官または組織に移植される置換細胞
トランスジェニック・ブタ由来CMV−xTKドナー肝臓を、実質的にコンジェニックな宿主ブタ(xTKを発現せずに宿主体内で生きた状態で維持される)に同所的に移植する。一度、ドナー肝臓が宿主で確立されると、ガンシクロビルを静注により投与することで、ドナー肝臓で細胞死が引き起こされる。次に、肝臓(例えば肝細胞、肝臓始原細胞または造血幹細胞)を再生させることができるヒト置換細胞を、例えば、門脈を経た輸液および/または直接注射によって、ドナー肝臓に導入する。置換細胞がドナー肝臓に植え付けられる。ガンシクロビル投与のさらなるラウンドは、置換細胞によるドナー肝細胞のさらなる置換を促進する。別の場合において、一つ以上のヒト肝臓プラグが、宿主に移植される前に、ドナー肝臓に挿入される。宿主に対するガンシクロビル投与が、置換細胞(プラグから生じる)によってドナー肝細胞のさらなる置換を促進するのに再び用いられる。
トランスジェニック・ブタ由来CMV−xTKドナー肝臓を、実質的にコンジェニックな宿主ブタ(xTKを発現せずに宿主体内で生きた状態で維持される)に同所的に移植する。一度、ドナー肝臓が宿主で確立されると、ガンシクロビルを静注により投与することで、ドナー肝臓で細胞死が引き起こされる。次に、肝臓(例えば肝細胞、肝臓始原細胞または造血幹細胞)を再生させることができるヒト置換細胞を、例えば、門脈を経た輸液および/または直接注射によって、ドナー肝臓に導入する。置換細胞がドナー肝臓に植え付けられる。ガンシクロビル投与のさらなるラウンドは、置換細胞によるドナー肝細胞のさらなる置換を促進する。別の場合において、一つ以上のヒト肝臓プラグが、宿主に移植される前に、ドナー肝臓に挿入される。宿主に対するガンシクロビル投与が、置換細胞(プラグから生じる)によってドナー肝細胞のさらなる置換を促進するのに再び用いられる。
置換細胞の懸濁液が導入される症例において、導入される細胞の最適数は、供給源次第であって、日常的な実験で測定することができる。胎児ブタに関して、例えば、プロドラッグが投与された(114日妊娠に対する範囲25)あと、置換細胞は、例えば、52日妊娠または7日に導入されることができる。妊娠52日目またはプロドラッグが投与されてから7日後(妊娠25ないし114日の範囲)、置換細胞を導入することができる。例えば、5x106個/胎児のヒト肝細胞(1x105〜5x107細胞/胎児)の投与量を用いることができる。5×105個/胎児の肝臓幹細胞(1〜5x107個/胎児)を使用することができる。骨髄および臍帯血も、肝細胞に分化することができる多能性始原細胞の供給源となる。例えば、使用するヒト臍帯血量を2.5×107有核細胞/胎児(1x106〜108)とすることができる。
本発明の一実施形態において、置換細胞(例えばヒト置換細胞)は非ヒト・ドナー哺乳動物、例えばブタ、ヒツジ、または齧歯動物(例えば、マウス、ラット、モルモット、カピバラ等)に導入される。この導入は、置換細胞が目的とする器官および/または組織に取り込まれ、導入置換細胞由来の細胞とドナー哺乳動物それ自身の細胞に湯対するキメラ器官および/または組織を形成する、免疫前胎児期におこなわれる。ドナー哺乳動物細胞を、置換細胞に対して、さらに、例えば、本明細書中に述べられるように、自殺遺伝子を発現することによって、または置換細胞および宿主哺乳動物に存在する耐性機構を発現しないことによって、キメラ器官が移植される宿主の細胞に対して、選択的に取り除くことが可能である(または選択的に成長阻害をもたらすことができる)。胎児期の間、または出生後の任意の段階で、すでに置換細胞を含むキメラのドナー器官または組織は、すでに置換細胞を含むドナー器官または組織は、哺乳動物宿主、例えば非ヒト哺乳動物宿主に移植(本明細書中に述べられる方法のいずれかによって)され、そこで生きた状態で維持される。一旦キメラのドナー器官または組織が宿主で確立されるならば、それを、キメラの器官で選択的にドナー哺乳動物細胞を削除(または阻害)を生ずる条件に1回以上さらすことで、該器官に存在する置換細胞によって、器官または組織上の累進的かつ選択的な再生着が促進される。キメラのドナー器官または組織由来のドナー細胞の(置換細胞対して)選択的な欠失は、例えば、ドナー器官の宿主哺乳動物および/または宿主哺乳動物への移植前あるいは移植直前に、開始される可能性がある。
以下の実施例は、ヒト細胞が集中する肝臓を作製するためにヒツジ・ドナーおよび宿主とヒト置換細胞とを使用する実施形態の変形例を例示する。
実施例−ドナー哺乳動物からの外植前にドナー器官または組織に取り込まれる置換細胞
トランスジェニック・ヒツジ胎児(または代わりにトランスジェニック・ブタ胎児)を提供するもので、該胎児は、構成的広範囲プロモーター(例えばCMV−xTK導入遺伝子)の制御下で自殺遺伝子を発現し、少なくとも1つの異種抗原(異種間物質のヒトトレランス(寛容)に関して)の発現を低下させ、および/または、少なくとも1つの移動可能なトレランス促進生体分子(例えばhDAFおよび/またはMIRL)の発現のためのトランスジェニックである。上記胎児は妊娠雌により維持される。
トランスジェニック・ヒツジ胎児(または代わりにトランスジェニック・ブタ胎児)を提供するもので、該胎児は、構成的広範囲プロモーター(例えばCMV−xTK導入遺伝子)の制御下で自殺遺伝子を発現し、少なくとも1つの異種抗原(異種間物質のヒトトレランス(寛容)に関して)の発現を低下させ、および/または、少なくとも1つの移動可能なトレランス促進生体分子(例えばhDAFおよび/またはMIRL)の発現のためのトランスジェニックである。上記胎児は妊娠雌により維持される。
ヒツジ胎児で肝細胞、他の肝臓細胞、および/または造血性細胞を生ずることができるヒト細胞を、その免疫前期間中における胎児への導入に提供される。そのようなヒト細胞として、限定されるものではないが、ヒト成人骨髄、臍帯血細胞、胎盤幹細胞、胎盤幹細胞、および移動末梢血幹細胞が挙げられる。ヒツジ胎児は妊娠約77日目までが免疫前である。置換細胞の調製および移植は、例えば、米国特許出願公開第20020100065号(その全体を本明細書に援用)にもとづいて実施することが可能である。ヒト骨髄または臍帯血を分画化(例えば、磁気菌体分離および/または蛍光活性化細胞ソーティングによって)して、表現型(例えば、造血幹細胞に関連した選択された表現型(例えば、造血幹細胞(例えばCD34+Lin”表現型)に対して濃縮してもよい。例えば、非分画化ヒト骨髄またはヒト臍帯血もまた、使用してもよい。
妊娠55〜60日目の免疫前胎児ヒツジに対して、表現型によって分画化されていない胎児1匹あたり1×106〜1×108(例えば、2.5×107)個の有核ヒト臍帯血細胞、または胎児1匹あたり1〜5×105個のCD34+Lin−ヒト骨髄細胞、胎児1匹あたり1.1×106個のCD34+Lin−ヒト臍帯血細胞、あるいは胎児1匹あたり1.1×106個のCD34−Lin−ヒト臍帯血細胞を、任意の適当な方法によって、例えば、25ゲージ針を用いて腹腔内注射する。この際の一般的な方法は、Flake et al. Transplantation of fetal hematopoietic stem cells in utero: the creation of hematopoietic chimeras Science, Vol. 233, p. 766 (1986)に記載されており、羊膜バブル内で直接視覚的に胎児に注射しうる。細胞の注射後、子宮筋層を二重層で閉じて妊娠を進行させる。
ヒト臍帯血(CB)細胞またはヒト骨髄細胞は、例えば、同意を得ると即座に、標準的方法によって得ることが可能である。単核細胞は、マウス抗hCD3、hCD4、hCD8、hCD1Ib、hCD19、hCD20、hCD56とヒト・グリコホリンA(hGPA)モノクローナル抗体(BD Immunocytometry、San Jose、CA)を用いることで、Lin+細胞が減少したものとなる。試料を、抗hCD34ミクロビーズ(Miltenyi Biotec社、Auburn、CA)を用いて、hCD34+細胞を豊富化(または代わりに、hCD34+細胞を減少)させることができる。
ヒツジにおける先行研究では、そのような移植体が移植後約1ヶ月によって顕著な多系統ヒト造血活性を全ての血液成分にもたらすとともに、出生時に顕著な数のヒト肝細胞をもたらす((移植後約3ヶ月;全細胞性の5〜40%、置換細胞の表現型および投与量に応じて)。米国特許出願公開番号第20020100065号。さらに、そのような移植から生じているキメラの肝臓は正常な肝細胞の機能特性を保持するヒト肝細胞のみならず、ヒト内皮および胆管胆管細胞も含み、該肝臓は循環中にヒトアルブミンを分泌する。Almeida-Porada, Formation of human 肝細胞 by human hematopoietic stem cells in sheep, Blood, (2004) 104(8) 2582-2590、その全体を本明細書中に援用する。ヒト細胞は、長期間にわたり、生存する。
自殺遺伝子(例えば実施例のキメラの肝臓)の広範囲活性発現を持つ胎児哺乳動物(すなわちドナー哺乳動物)の中で発育したキメラ固形器官または組織を、それが生きた状態で維持される同じ自殺遺伝子の発現を有しない第2の非ヒト哺乳動物(すなわち宿主)に移植する。ドナー哺乳動物がまだ胎児期、またはドナー哺乳動物出生後の任意の段階にある間に、キメラ・ドナー器官または組織を非ヒト哺乳動物宿主に移植してもよい。移植後、宿主に対するプロドラッグの投与によって、実質的にキメラの器官または組織のヒト細胞を害することのなく、また実質的に宿主の細胞を害することなく、非ヒト・ドナー哺乳動物動物由来のキメラ器官または組織の非ヒト細胞が選択的に殺されることで、移植された固形器官または組織の細胞化が、ドナー哺乳動物細胞よりもヒト細胞によってより完全に促進される。このように、より細胞化されたヒト器官または組織、例えば少なくとも実質的に完全細胞化ヒト器官または組織を得ることができる。そのような器官または組織を、例えば、必要に応じて、ヒト患者にさらに移植することが可能である。
本発明の一実施形態では、キメラの器官または組織を形成するために置換細胞で植え付けられた目的の器官または組織(例えば肝臓)を、宿主哺乳動物(自殺導入遺伝子を発現しない)に対して後で移植することができ、ここでキメラの器官または組織の少なくとも一部のドナー哺乳動物細胞が選択的に削除され(または増殖阻害が生ずる)、それによってキメラの器官または組織に存在する置換細胞(例えばヒト置換細胞)が選択的に器官または組織を占有することになる。
複数動物移植手技
本発明の一実施形態では、個々の非ヒト哺乳動物は、別の非ヒト哺乳動物に対する固形器官または組織あるいはその一部分の両方のドナーとして、さらにヒトまたは非ヒト哺乳動物由来の固形器官または組織あるいはその一部分の宿主として機能する。本発明は、さらに、少なくとも2種類の非ヒト哺乳動物が提供される関連した実施形態を提供するもので、該少なくとも2種類の非ヒト哺乳動物のうち、少なくとも2つがドナー動物および宿主動物として機能する。そのような実施形態は、細胞的に再構成された器官または組織の作製効率を上昇させる。例えば、一実施形態は、細胞を殺すのに必要とされる条件セットが第1の自殺遺伝子および第2の自殺遺伝子で異なり、第1の自殺遺伝子を誘導的または構成的に発現する第1の非ヒト哺乳動物と第2の自殺遺伝子と第2の自殺遺伝子を誘導的または構成的に発現する第2の非ヒト哺乳動物とを提供するステップと、第1の非ヒト哺乳動物から器官または組織あるいはその一部を第2の非ヒト哺乳動物へ移植し、第2の動物から器官または組織あるいはその一部を第1の動物へ移植するステップとを含み、同一器官または組織あるいはその一部分を動物間(相互対称型移植)および/または異なる器官または組織あるいはその一部分を動物間(相互非対称移植)で移植する。移植された器官または組織は、各々の宿主によって生きた状態で維持される。このようにして、各々の動物に関して、そこを宿主とする移植された器官または組織の細胞を、各々のドナー宿主に対して各々のドナー動物細胞の細胞を殺す条件セットを提供することによって、宿主細胞を殺すことなく選択的に殺すことができる。同一または異なるプロモーターまたはプロモーター型は、第1および第2の自殺遺伝子の発現を駆動するのに用いることが可能である。プロモーターは、広範囲活性プロモーター(例えば普遍的プロモーター)および/または細胞型特異的プロモーターであってもよい。細胞の複製および/または健康を損なうか、さもなければ条件セットに応じて該細胞を殺すことなく細胞に対して損害を与える誘導性成長阻害遺伝子もまた、1つ以上の自殺遺伝子の代わりに使用することが可能である。
本発明の一実施形態では、個々の非ヒト哺乳動物は、別の非ヒト哺乳動物に対する固形器官または組織あるいはその一部分の両方のドナーとして、さらにヒトまたは非ヒト哺乳動物由来の固形器官または組織あるいはその一部分の宿主として機能する。本発明は、さらに、少なくとも2種類の非ヒト哺乳動物が提供される関連した実施形態を提供するもので、該少なくとも2種類の非ヒト哺乳動物のうち、少なくとも2つがドナー動物および宿主動物として機能する。そのような実施形態は、細胞的に再構成された器官または組織の作製効率を上昇させる。例えば、一実施形態は、細胞を殺すのに必要とされる条件セットが第1の自殺遺伝子および第2の自殺遺伝子で異なり、第1の自殺遺伝子を誘導的または構成的に発現する第1の非ヒト哺乳動物と第2の自殺遺伝子と第2の自殺遺伝子を誘導的または構成的に発現する第2の非ヒト哺乳動物とを提供するステップと、第1の非ヒト哺乳動物から器官または組織あるいはその一部を第2の非ヒト哺乳動物へ移植し、第2の動物から器官または組織あるいはその一部を第1の動物へ移植するステップとを含み、同一器官または組織あるいはその一部分を動物間(相互対称型移植)および/または異なる器官または組織あるいはその一部分を動物間(相互非対称移植)で移植する。移植された器官または組織は、各々の宿主によって生きた状態で維持される。このようにして、各々の動物に関して、そこを宿主とする移植された器官または組織の細胞を、各々のドナー宿主に対して各々のドナー動物細胞の細胞を殺す条件セットを提供することによって、宿主細胞を殺すことなく選択的に殺すことができる。同一または異なるプロモーターまたはプロモーター型は、第1および第2の自殺遺伝子の発現を駆動するのに用いることが可能である。プロモーターは、広範囲活性プロモーター(例えば普遍的プロモーター)および/または細胞型特異的プロモーターであってもよい。細胞の複製および/または健康を損なうか、さもなければ条件セットに応じて該細胞を殺すことなく細胞に対して損害を与える誘導性成長阻害遺伝子もまた、1つ以上の自殺遺伝子の代わりに使用することが可能である。
本発明の器官および組織の細胞再形成を促進させる態様によれば、置換細胞(例えばヒト置換細胞)を、任意の方法によって、例えば、幹細胞または始原細胞を胎児段階または周産期段階でドナー動物に導入することによって、および/あるいはドナーから外植後に直接または間接的に置換細胞をドナー器官に導入することによって、宿主への移植前および/または移植後にドナー器官または組織に(例えば各々のドナーからの外植前に)導入することが可能である。ドナー器官または組織に導入される置換細胞が、2頭の動物にとって同一または異なるものであってもよく、また同一のソースまたは異なるソースに由来するものであってもよい。このように、各々の宿主内のドナー器官または組織の内因性細胞の選択的殺害または成長阻害は、置換細胞による器官または組織の選択的な再形成を促進する。置換細胞による器官または組織の十分な器官および組織細胞再形成の後に、再構成された器官または組織を、宿主から外植することが可能である。再構成された器官または組織で存在し得る任意のコンタミした宿主細胞を、各々の宿主細胞を殺害または傷つける条件を提供することで、殺害または傷つけることが可能である。
3匹以上の非ヒト哺乳動物が用いられ、かつ個々の動物がドナーおよび宿主として機能する例では、個体間の器官または組織移植は、相互的(各々2つの個体がその器官または組織または一部を交換する)および/または非相互的(移植体が与えられた同一個体から移植体は受け取られない)である。
ドナー細胞および宿主細胞の選択的欠失
本発明は、1つ以上の条件からなる条件セットに応じて置換細胞の宿主細胞と対比させてドナー器官または組織の細胞が条件的および選択的に殺害可能(欠失可能)である実施形態を提供する。このように、本発明によれば、少なくとも、ドナー器官または組織のドナー細胞のいくつかを、置換細胞によって少なくとも部分的な再形成を促進するために、削除することができる。
本発明は、1つ以上の条件からなる条件セットに応じて置換細胞の宿主細胞と対比させてドナー器官または組織の細胞が条件的および選択的に殺害可能(欠失可能)である実施形態を提供する。このように、本発明によれば、少なくとも、ドナー器官または組織のドナー細胞のいくつかを、置換細胞によって少なくとも部分的な再形成を促進するために、削除することができる。
本発明は、第1条件セットとは異なる第2条件セットに応じて宿主細胞を取り除くことが可能である実施形態を提供することから、再構成された器官または組織に浸透可能である宿主細胞をそこから取り除くことができる。宿主が宿している再構成ドナー器官または組織に移動して存在可能である宿主細胞の種類として、例えば、繊維芽細胞、リンパ球および/または他免疫細胞、血管内皮細胞、および/またはドナー器官または組織が類型に分けるヒトに対応する宿主を誘導された器官または組織型特異的細胞が挙げられる。
限定されるものではないが、以下の例を含む種々のタイプの自殺遺伝子戦略が用いられる。
プロトキシン−毒素間転換酵素自殺遺伝子
適当な転換酵素自殺遺伝子の例として、限定されるものではないが、チミジンキナーゼ(野生型または突然変異を含むこと)、シトシンデアミナーゼ、カルボキシエステラーゼ、カルボキシペプチダーゼ、デオキシシチジン・キナーゼ、ニトロレダクターゼ、グアノシン・キサンチン・ホスホリボシルトランスフェラーゼ、プリンヌクレオシドホスホリラーゼ阻害剤、およびチミジンホスホリラーゼが挙げられる。プロトキシン(プロドラッグ)が欠如している場合、自殺遺伝子の発現は、正常な細胞の代謝に対してほとんど悪影響を生ずることはない。転換酵素型自殺遺伝子の生成物は、適当なプロドラッグに作用し、このプロドラッグを毒素に変換する。自殺遺伝子産物が存在しない場合、プロドラッグは比較的無害である。チミジンキナーゼの適当なプロドラッグとして、ガンシクロビル、6−メトキシ・プリン・アラビノシドおよび(E)−5−(2−ブロモビニル)−2’−デオキシウリジンが挙げられる。シトシンデアミナーゼの適当なプロドラッグとして、5−フルシトシンが挙げられる。カルボキシエステラーゼの適当なプロドラッグとして、イリノテカンが挙げられる。カルボキシペプチダーゼの適当なプロドラッグとして、4−([2−クロロエチル][2−メシロエチル]アミノ)ベンゾイル−L−グルタミン酸が挙げられる。デオキシシチジン・キナーゼの適当なプロドラッグとして、4−イポメアノールシトシンアラビノサイドとフルダラビンが挙げられる。グアノシン−キサンチン・ホスホリボシル転移酵素の適当なプロドラッグとして、6−チオキサンチンおよび6−チオグアニンが挙げられる。ニトロレダクターゼのための適当なプロドラッグとして、5−アジリジン−2,4−ジニトロ・ベンズアミジンが挙げられる。プリンヌクレオシドホスホリラーゼ阻害剤の適当なプロドラッグは、6−メチルプリン・デオキシリボヌクレオシドである。チミジンホスホリラーゼの適当なプロドラッグとして、デオキシフロロウリジンおよび1−(テトラヒドロフリル)−5−フルオロウラシルが挙げられる。チミジンホスホリラーゼの適当なプロドラッグとして、5‘−デオキシ−5−フルオロウリジンおよび1−(テトラヒドロフリル)−5−フルオロウラシルが挙げられる。
適当な転換酵素自殺遺伝子の例として、限定されるものではないが、チミジンキナーゼ(野生型または突然変異を含むこと)、シトシンデアミナーゼ、カルボキシエステラーゼ、カルボキシペプチダーゼ、デオキシシチジン・キナーゼ、ニトロレダクターゼ、グアノシン・キサンチン・ホスホリボシルトランスフェラーゼ、プリンヌクレオシドホスホリラーゼ阻害剤、およびチミジンホスホリラーゼが挙げられる。プロトキシン(プロドラッグ)が欠如している場合、自殺遺伝子の発現は、正常な細胞の代謝に対してほとんど悪影響を生ずることはない。転換酵素型自殺遺伝子の生成物は、適当なプロドラッグに作用し、このプロドラッグを毒素に変換する。自殺遺伝子産物が存在しない場合、プロドラッグは比較的無害である。チミジンキナーゼの適当なプロドラッグとして、ガンシクロビル、6−メトキシ・プリン・アラビノシドおよび(E)−5−(2−ブロモビニル)−2’−デオキシウリジンが挙げられる。シトシンデアミナーゼの適当なプロドラッグとして、5−フルシトシンが挙げられる。カルボキシエステラーゼの適当なプロドラッグとして、イリノテカンが挙げられる。カルボキシペプチダーゼの適当なプロドラッグとして、4−([2−クロロエチル][2−メシロエチル]アミノ)ベンゾイル−L−グルタミン酸が挙げられる。デオキシシチジン・キナーゼの適当なプロドラッグとして、4−イポメアノールシトシンアラビノサイドとフルダラビンが挙げられる。グアノシン−キサンチン・ホスホリボシル転移酵素の適当なプロドラッグとして、6−チオキサンチンおよび6−チオグアニンが挙げられる。ニトロレダクターゼのための適当なプロドラッグとして、5−アジリジン−2,4−ジニトロ・ベンズアミジンが挙げられる。プリンヌクレオシドホスホリラーゼ阻害剤の適当なプロドラッグは、6−メチルプリン・デオキシリボヌクレオシドである。チミジンホスホリラーゼの適当なプロドラッグとして、デオキシフロロウリジンおよび1−(テトラヒドロフリル)−5−フルオロウラシルが挙げられる。チミジンホスホリラーゼの適当なプロドラッグとして、5‘−デオキシ−5−フルオロウリジンおよび1−(テトラヒドロフリル)−5−フルオロウラシルが挙げられる。
細胞死誘導自殺遺伝子
本発明によって使用可能な自殺遺伝子の他の種類として、遺伝子産物(それ自体)が細胞死を生じるか、または細胞死を誘発するものが挙げられる。そのような自殺遺伝子とそれによる細胞死の発現とは、誘導性プロモーターの制御下で自殺遺伝子を発現させることによって、条件的におこなうことができる。細胞死誘導自殺遺伝子の1つのタイプは、それが発現される細胞を殺すタンパク質毒素(例えばジフテリアトキシン)をコードする。細胞死誘導自殺遺伝子のもう一つのタイプは、細胞死を引き起こすか起動させるために細胞の基質に作用する酵素を、コードする。例えば、適当な細胞死を引き起こしている酵素遺伝子として、細胞傷害性プロテアーゼ(例えばシステインプロテアーゼおよびカスパーゼ(例えばカスパーゼ8hまたはカスパーゼ8i)のICE/CED−3ファミリーのメンバー)をコードしているものが挙げられる(米国特許第6,172,190号に開示。その全体を本明細書中に援用)。
本発明によって使用可能な自殺遺伝子の他の種類として、遺伝子産物(それ自体)が細胞死を生じるか、または細胞死を誘発するものが挙げられる。そのような自殺遺伝子とそれによる細胞死の発現とは、誘導性プロモーターの制御下で自殺遺伝子を発現させることによって、条件的におこなうことができる。細胞死誘導自殺遺伝子の1つのタイプは、それが発現される細胞を殺すタンパク質毒素(例えばジフテリアトキシン)をコードする。細胞死誘導自殺遺伝子のもう一つのタイプは、細胞死を引き起こすか起動させるために細胞の基質に作用する酵素を、コードする。例えば、適当な細胞死を引き起こしている酵素遺伝子として、細胞傷害性プロテアーゼ(例えばシステインプロテアーゼおよびカスパーゼ(例えばカスパーゼ8hまたはカスパーゼ8i)のICE/CED−3ファミリーのメンバー)をコードしているものが挙げられる(米国特許第6,172,190号に開示。その全体を本明細書中に援用)。
シグナル伝達活性化自殺遺伝子機構
細胞を二量化剤(または一般にクラスター形成剤)と接触させることで細胞死を生じさせるシグナル伝達経路を活性化させるように設計されたトランスジェニック動物もまた、本発明に使用することができる。例えば、当該技術分野は、アポトーシス・メディエイタ分子(例えばFas受容体またはTNF-R1)の細胞内領域を含むトランスジェニック融合タンパク質のクラスターを形成することによって、細胞をラパマイシンまたはラパログと接触させることでアポトーシスを起動させるトランスジェニック動物を提供する。適当なシグナル伝達機構は、例えば米国特許第6,649,595号、米国特許第6,187,757号、および米国特許出願公開第20030206891 号(出願第10/341,967号)、各々その全体を本明細書中に援用)。別の実施形態では、アポトーシス・メディエータ分子(例えば、Fas受容体またはTNF−R1および事前選択された細胞外エピトープ)の細胞内ドメインを含むタンパク質を発現するトランスジェニック動物を用いることができる。事前選択された細胞外エピトープを認識する二価または多価抗体を、それらのタンパク質を発現する細胞と接触させることで、それらの細胞内ドメインを隣接化(クラスター形成)させることができる。
細胞を二量化剤(または一般にクラスター形成剤)と接触させることで細胞死を生じさせるシグナル伝達経路を活性化させるように設計されたトランスジェニック動物もまた、本発明に使用することができる。例えば、当該技術分野は、アポトーシス・メディエイタ分子(例えばFas受容体またはTNF-R1)の細胞内領域を含むトランスジェニック融合タンパク質のクラスターを形成することによって、細胞をラパマイシンまたはラパログと接触させることでアポトーシスを起動させるトランスジェニック動物を提供する。適当なシグナル伝達機構は、例えば米国特許第6,649,595号、米国特許第6,187,757号、および米国特許出願公開第20030206891 号(出願第10/341,967号)、各々その全体を本明細書中に援用)。別の実施形態では、アポトーシス・メディエータ分子(例えば、Fas受容体またはTNF−R1および事前選択された細胞外エピトープ)の細胞内ドメインを含むタンパク質を発現するトランスジェニック動物を用いることができる。事前選択された細胞外エピトープを認識する二価または多価抗体を、それらのタンパク質を発現する細胞と接触させることで、それらの細胞内ドメインを隣接化(クラスター形成)させることができる。
成長および複製阻害遺伝子発現
Rhimによって述べられるように、プロテアーゼ、肝細胞(アルブミン・プロモーターの制御下)のウロキナーゼ型プラスミノーゲンアクティベーター(uPA)の発現は、複製的欠陥を生ぜしめ、トランスジェニック肝臓に導入された正常異種間肝細胞に比べてトランスジェニック肝細胞に対する選択的生着床を不利にする。一般に、置換細胞と比較して、目的の非ヒト哺乳動物ドナー細胞の複製/成長を損なう任意の種類の方法またはシステムを本発明にもとづいて使用することが可能である。
Rhimによって述べられるように、プロテアーゼ、肝細胞(アルブミン・プロモーターの制御下)のウロキナーゼ型プラスミノーゲンアクティベーター(uPA)の発現は、複製的欠陥を生ぜしめ、トランスジェニック肝臓に導入された正常異種間肝細胞に比べてトランスジェニック肝細胞に対する選択的生着床を不利にする。一般に、置換細胞と比較して、目的の非ヒト哺乳動物ドナー細胞の複製/成長を損なう任意の種類の方法またはシステムを本発明にもとづいて使用することが可能である。
一般的ネガティブ選択マーカー
一般に、目的とする非ヒト哺乳動物の選択的殺害を許可または可能にする任意の種類のネガティブ選択マーカーまたはシステムを、本発明にもとづいて使用することができる。例えば、ドナー器官または組織(自然に、または遺伝学的修飾の結果)は宿主または置換細胞によって発現されない細胞表面エピトープを一般に発現する場合、エピトープに特異的に結合する抗体または他の結合タンパク質を用いて、細胞傷害剤は抗体を使用しているドナー細胞(宿主および置換細胞と対比して)を好ましくは標的化することができる。一種類以上の細胞傷害剤を、例えば、そのような抗体または結合タンパク質あるいは該抗体または結合タンパク質を提示する免疫リポソームに直接連結させることができ、該細胞傷害剤の含有させることを標的細胞へこの薬剤を往復させることに用いることができる。
一般に、目的とする非ヒト哺乳動物の選択的殺害を許可または可能にする任意の種類のネガティブ選択マーカーまたはシステムを、本発明にもとづいて使用することができる。例えば、ドナー器官または組織(自然に、または遺伝学的修飾の結果)は宿主または置換細胞によって発現されない細胞表面エピトープを一般に発現する場合、エピトープに特異的に結合する抗体または他の結合タンパク質を用いて、細胞傷害剤は抗体を使用しているドナー細胞(宿主および置換細胞と対比して)を好ましくは標的化することができる。一種類以上の細胞傷害剤を、例えば、そのような抗体または結合タンパク質あるいは該抗体または結合タンパク質を提示する免疫リポソームに直接連結させることができ、該細胞傷害剤の含有させることを標的細胞へこの薬剤を往復させることに用いることができる。
宿主および/または置換細胞での耐性遺伝子発現
化学選択剤に対する耐性を有する宿主および置換細胞(例えば、該宿主および・または細胞を遺伝学的に修飾して耐性遺伝子を発現させる結果として)を用い、例えばドナー器官または組織を維持しているトランスジェニック宿主に選択剤を投与することによって、ドナー器官または組織細胞の選択的欠失を得ることができる。
化学選択剤に対する耐性を有する宿主および置換細胞(例えば、該宿主および・または細胞を遺伝学的に修飾して耐性遺伝子を発現させる結果として)を用い、例えばドナー器官または組織を維持しているトランスジェニック宿主に選択剤を投与することによって、ドナー器官または組織細胞の選択的欠失を得ることができる。
宿主および/または置換細胞での耐性遺伝子発現
アミノグリコシド3−ホスホトランスフェラーゼ遺伝子製品(APH、neoR、kanR)の発現を用いることで、G418(Geneticin(登録商標))に対する耐性を与えることができる。使用されるG418濃度を、例えば10〜1,000mg/l、例えば400mg/l、または10〜1000mg/kg(宿主重量に対する薬物重量)とすることができる。
アミノグリコシド3−ホスホトランスフェラーゼ遺伝子製品(APH、neoR、kanR)の発現を用いることで、G418(Geneticin(登録商標))に対する耐性を与えることができる。使用されるG418濃度を、例えば10〜1,000mg/l、例えば400mg/l、または10〜1000mg/kg(宿主重量に対する薬物重量)とすることができる。
bsd遺伝子産物(Aspergillus terreus由来)の発現は、ブラストシジン(Blastocydin)Sに耐性を与える際に用いることができる。使用されるブラストシジンS濃度を、例えば1〜100mg/lの範囲、例えば有効量を10mg/lとし、または例えば1〜100mg/lの範囲、例えば10mg/kgとすることがきる。
shble遺伝子産物(Streptoalloteichus hindustanus由来)の発現を用いて、ゼオシン(Zeochin(登録商標))(ブレオマイシン・ファミリーの一員)に対する耐性を与えることができる。使用するゼオシン濃度を、例えば400〜1000mg/lまたは400〜1000mg/kgとすることができる。
hph遺伝子産物の発現を利用して、ヒグロマイシンBに耐性を与えることができる。ヒグロマイシンBを、例えば50〜1000mg/lまたは50〜1,000mg/kgの濃度範囲で使用することができる。
G418、ブラストシジンS、ゼオシン、およびハイグロマイシンBの各々は、いくつかの異なるタイプの動物細胞に対する選択剤として有効であり、各々は哺乳動物細胞に有効であることが当該技術分野において知られている。示唆された作用濃度は、哺乳動物細胞に対する使用に基づいている。任意の動物または細胞型に対する有効濃度および用量は、日常的実験で決定される。哺乳類に関するこれらの遺伝子のコドン最適化バージョンまたは他の発現は、当該技術分野において公知であり、商業的に入手可能である。
ストレプトゾトシンは、優先して膵臓すい島細胞を殺して、糖尿病を誘発する。少なくとも膵臓β細胞(例えば広範囲活性プロモーターまたはインシュリン・プロモーターの制御下)でタンパク質メタロチオネインを過剰発現させているトランスジェニック非ヒト哺乳動物宿主は、ストレプトゾトシンに耐性である(Chen et al. Overexpression of metallothionein in pancreatic [beta]-cells reduces streptozotocin-induced DNA damage and diabetes, Diabetes 50:2040-2046, 2001)。トランスジェニック・ストレプトゾトシン耐性宿主を、宿主細胞内でストレプトゾトシンをそのDNA標的から隔離するペプチドおよび/またはアプタマー等のストレプトゾトシン結合部分を発現することによって、提供することもできる。膵島細胞を破壊するためのストレプトゾトシンの適当な投薬量範囲として、例えば、1〜100mg/kg(例えば30〜60mg/kg)が挙げられる。
プロモーター
遺伝子発現(例えば、自殺遺伝子発現)を駆動するための広範囲活性プロモーター(細胞型に関する)は、多くの細胞型で活性のあるものであり、該細胞型として、少なくとも実質的に全ての細胞型(普遍的プロモーター)、あるいは本発明の実施形態で用いられるように、対象宿主、ドナー器官もしくは組織、またはドナー置換細胞プロバイダ由来のプロバイダ細胞に関連した細胞型の少なくとも実質的に全てに活性があるものである。広範囲活性プロモーターは構成的または誘導性であり得る。本明細書中で用いられる用語「プロモーター」は、広く解釈されなければならず、例えばプロモーターおよびエンハンサーならびにそれらの組み合わせが含まれる。
遺伝子発現(例えば、自殺遺伝子発現)を駆動するための広範囲活性プロモーター(細胞型に関する)は、多くの細胞型で活性のあるものであり、該細胞型として、少なくとも実質的に全ての細胞型(普遍的プロモーター)、あるいは本発明の実施形態で用いられるように、対象宿主、ドナー器官もしくは組織、またはドナー置換細胞プロバイダ由来のプロバイダ細胞に関連した細胞型の少なくとも実質的に全てに活性があるものである。広範囲活性プロモーターは構成的または誘導性であり得る。本明細書中で用いられる用語「プロモーター」は、広く解釈されなければならず、例えばプロモーターおよびエンハンサーならびにそれらの組み合わせが含まれる。
適当な広範囲活性構成的プロモーターとして、限定されるものではないが、MoMLV LTR、RSV LTR、フレンドMuLv LTR、アデノウィルス・プロモーター、ネオマイシンホスホトランスフェラーゼ・プロモーター/エンハンサー、遅延パルボウィルス・プロモーター、ヘルペスTKプロモーター、SV40プロモーター、メタロチオネインIIa遺伝子エンハンサー/プロモーター、サイトメガロウィルス最初期プロモーター、およびサイトメガロウィルス最後期プロモーターが挙げられる。適当な広範囲活性誘導性プロモーターまたは誘導性発現系として、限定されるものではないが、誘導性メタロチオネイン遺伝子プロモーター、テトラサイクリン・リプレッサーおよび/またはアクチベーターをベースとした誘導発現系(例えば、米国特許第6,252,136号、第6,136,954号、第5,912,411号、および第5,589,362号(その全体を本明細書中に援用)によって提供されるもの)、lacオペロンをベースとした誘導発現系(例えば、米国特許出願公開第20040171824号(出願第10/469,881号)(その全体を本明細書中に援用)によって提供されるもの)、またはエクダイソン誘導発現系(例えば、米国特許出願公開第20020187972号(出願第09/949,278号))が挙げられる。ドナー器官または組織における自殺遺伝子形質発現を駆動する広範囲活性調節因子(例えば万能のプロモーター)を用いることで、ドナー細胞の選択的な欠失が単純化され、置換細胞による再形成が促進される。同様に、広範囲活性プロモーターを使用して、宿主細胞および置換細胞でのポジティブ選択マーカー(例えば、耐性遺伝子)の発現を駆動することも、ドナー器官または組織細胞が耐性ではないドナー器官または組織細胞の選択的欠失を単純化する。広範囲活性プロモーターの使用も、再構成された器官または組織に存在すると思われる汚染宿主細胞の欠失を単純化する。しかし、本発明は、組織または細胞型特異的なプロモーターおよび調節因子の1つまたはそれらの組合せを一般に使用し得ることも定める。本明細書中に言及するように、組織特異的および細胞型特異的な転写性調節因子(例えば、プロモーターおよびエンハンサーならびにそれらの組合せ)もまた、組織に好ましく、細胞型に好ましい転写性調節因子が挙げられる。先に述べられるように、組織特異的プロモーターを、逐次的な細胞の置換を得るために広範囲活性プロモーターとともに使用してもよい。
多数の適当な組織特異的および細胞型特異的な転写調節因子は、当該技術分野で知られている。所定の組織について、または一般的には、さらなる組織特異的および細胞型特異的因子の同定および特徴づけは、当該技術分野における日常的研究課題かつ通常の課題である。したがって、以下の実施例は説明のために提供されるものであって、本発明を本明細書中に詳述されるそれらの要素だけに決して限定するものではない。
肝細胞および/または肝細胞特異的な発現は、アルブミン・プロモーターによって、また胎児特異的な肝臓発現に関しては、アルファ胎仔タンパク質プロモーターによって提供される。
筋肉特異的な発現は、例えば、ミオシンL鎖−2プロモーター、αアクチン・プロモーター、トロポニン1プロモーター、Na+/Ca2+イオン交換体プロモーター、ジストロフィン・プロモーター、クレアチンキナーゼ・プロモーター、α−7インテグリン・プロモーター、トロポニンCプロモーター−エンハンサー、α−B−クリスタリン/スモールヒートショック・タンパク質プロモーターによって提供することができる。心筋特異的な発現を、例えば、α−ミオシン重鎖プロモーターと心房ナトリウム利尿因子(ANF)プロモーターによってもたらすことができる。
血管内皮細胞特異的発現は、例えば、fms様チロシン・キナーゼ−1(Flt−1)、細胞間接着分子−2(ICAM−2)、フォンビルブラント因子(vWF)、および血管内皮生長因子レセプター−2(Flk−1)の遺伝子プロモーターによって、もたらすことができる。Flt−1プロモーターは、肝臓の以外のすべての血管床の発現を導くと報告されている。
肺特異的なプロモーターとして、種々の肺表面活性剤タンパク質(例えばサーファクタント蛋白Bプロモーター)に対するものが挙げられる。
リンパ球および/またはそれらの前駆体の発現は、例えば、通常リンパ球特異的な蛋白チロシン・キナーゼの発現を駆動するjak3(ヤヌス・キナーゼ3)遺伝子プロモーターまたはLCK遺伝子プロモーターによってもたらすことができる。
腎臓特異的な発現は、例えば、Ksp−カドヘリン遺伝子プロモーターまたはヒトPTH/PTHrP受容体遺伝子腎臓特異的プロモーターによってもたらすことができる。
表皮細胞特異的な発現は、例えば、ヒト表皮1型トランスグルタミナーゼ(トランスグルタミナーゼI)遺伝子プロモーター(米国特許第5,643,746号(その全体を本明細書中に援用))によってもたらすことができる。
脂肪特異的発現は、例えば、脂肪酸結合タンパク質遺伝子(α−P2)の脂肪特異的なプロモーター/エンハンサーでもたらすことができる。
膵臓特異的な発現は、例えば、内分泌膵特異的インシュリン・プロモーター(第1のイントロンをプラスあるいはマイナス)、膵臓αアミラーゼ・プロモーター、膵臓特異的十二指腸ホメオボックス1(PDX−1)プロモーター、ならびにエラスターゼI遺伝子の外分泌膵臓特異的プロモーターによってもたらすことができる (Hall et al., J. Biotechnology (1993) 11: 376-379)。
多数の自殺遺伝子発現コンストラクトと当該技術分野で既に述べられているそれらを含む方法を用いて、条件的に欠失可能(殺害可能)な細胞を持つ非ヒト哺乳動物を、本発明にもとづく使用のために提供することができる。例えば、国際特許出願公報WO 2004/027029 A2(国際出願PCT/US2003/029251)によって提供される以下の配列および方法を用いることができる。配列番号1は、ブタのアルブミン・プロモーターの配列を提供する。配列番号2〜5は、事前選択された自殺遺伝子を発現しているトランスジェニック非ヒト哺乳動物を作製するための導入遺伝子コンストラクトを提供する。具体的には、配列番号2は肝臓特異的ブタ・アルブミン・プロモーターの制御下にあるヘルペス・チミジンキナーゼ自殺遺伝子(xTK)の変異体と、転写産物用ポリA付加シグナル配列とを含む導入遺伝子コンストラクトを提供する。配列番号3は、胎生期肝臓特異的アルファ胎仔タンパク質プロモーターの制御下にある自殺遺伝子シトシンデアミナーゼ(fCY)と転写産物用ポリA付加シグナル配列とを含む導入遺伝子コンストラクトを提供する。配列番号4は、広範囲活性、構成的サイトメガロウィルス(CMV)プロモーターの制御下にあるヘルペス・チミジンキナーゼ自殺遺伝子(xTK)の変異体と、転写産物用ポリA付加シグナル配列とを含む導入遺伝子コンストラクトを提供する。配列番号5は、広範囲活性、構成的サイトメガロウィルス(CMV)プロモーターの制御下にある自殺遺伝子シトシンデアミナーゼ(fCY)と、ポリA付加シグナル配列とを含む導入遺伝子コンストラクトを転写産物に提供する。説明のために、図1に配列番号2(AlbxTK)、配列番号3(AFP Fcy)、および配列番号4(CMV xTK)の導入遺伝子コンストラクトの構成要素の配置を示す。
xTKは、塩基位置130および180でシトシンをアデノシンと置換することによって特徴づけられる単純ヘルペスウイルス(HSV)チミジンキナーゼ遺伝子の変異バージョンである。ヌクレオチド置換によってロイシンからメチオニンへのコドン変化が生じ、既報によれば無修飾形態で生じ得る男性不妊症の現象を予防する。これらの突然変異は、酵素活性を実質的には損なわない。配列番号2〜5のコンストラクトは、普遍的プロモーターの制御下にある緑色蛍光タンパク質(GFP)の形態に関するコード配列を含むものであってもよい。GFP発現によって宿主細胞が視覚的に同定されることが可能となり、ヒト細胞を容易に区別する。しかし、GFP発現は、本発明の実施には必要ではない任意の特徴である。
当業者は、トランスジェニック動物および細胞株を作製するいくつかの方法があり、任意の適当な方法を使用することができることを認識する。
実施例−自殺遺伝子を発現するトランスジェニック・ブタの作製
実施例−自殺遺伝子を発現するトランスジェニック・ブタの作製
この実施例は、当該技術分野で知られているように、体細胞核移植法を用いて、自殺遺伝子発現コンストラクトを含むトランスジェニック・ブタの作製を説明する。手短に言うと、35日齢胎児ブタから得た繊維芽細胞を培養した後に、電気穿孔法または任意の適当な技術を用いて自殺導入遺伝子コンストラクト(例えば、突然変異チミジンキナーゼかシトシンデアミナーゼ・コンストラクト)を形質移入する。コルヒチンの添加によって、形質移入繊維芽細胞をG2/M期に引き止める。ブタ卵母細胞を単離して摘出する。数個または多数の摘出卵母細胞の各々について、マイクロマニピュレーターを用いて形質移入繊維芽細胞を囲卵腔に挿入し、電気的融合を用いて摘出卵母細胞に対して効果的にドナー繊維芽細胞核を移入する。電気的融合および活性化は同時に行ってもよいし、電気的融合ステップの後に活性化を行なってもよい。転移の別の方法では、核を取り除かれた卵母細胞に対して、体細胞ドナー核をマイクロインジェクションによって注入し、続いて活性化させることができる。いずれにせよ、活性化の後で、再建された胚を、発情期に代用の雌ブタに移植する。同腹の子は、超音波によってモニターすることができる。期間終了時に、必要に応じて、トランスジェニック・ブタは帝王切開によって出産させる場合もある。
ブタにおける自殺導入遺伝子コンストラクトの存在を、PCRを使用して評価することができる。導入遺伝子の発現は、ウェスタンブロッティングによって評価することができる。トランスジェニック・ブタは、性的に成熟したら繁殖させることができる。必要に応じて、自殺遺伝子コンストラクト用のホモ接合のブタは、交配によって得ることができる。さらなるトランスジェニック・ブタを、交配および/またはクローニングによって得ることができる。
プロドラッグおよび/または転写インデューサーおよび/または多量化/二量化剤の投与のための適当な用量を、日常的な実験として経験的に決定することができる。適当かつ最適な用量を、異なるタイプの宿主および発現コンストラクトに応じて変えることが可能である。例えば、そのような薬剤を非ヒト動物宿主に対して、1〜1,000mg/kg、1〜100mg/kg、または5〜50mg/kgの用量で投与してもよい。チミジンキナーゼを発現しているブタに関しては、ガンシクロビルの有効量を、例えば、1〜1,000mg/kg、1〜100mg/kg、5〜50mg/kg、または約25mg/kgとすることができる。外植されたヒト化ドナー器官または組織に存在する非ヒト宿主細胞の生体外での殺害を目的として、例えば、1〜1000mg/l、1〜100mg/l、5〜50mg/l、または20〜50mg/lの濃度範囲を用いることができる。外植されたヒト化ドナー器官または組織からチミジンキナーゼを発現しているブタ宿主細胞を欠失させるために、使用するガンシクロビル濃度を2〜1000mg/l、例えば約100mg/lとすることができる。プロドラッグを用いた生体外のチミジンキナーゼ・ベースのネガティブ選択を目的として、例えば、プロドラッグ5−BrdU(5−ブロモ−2−デオキシウリジン)(濃度1〜1000mg/l、1〜100mg/l、または25〜30mg/lの範囲)を用いることができる。
再構成されたドナー器官または組織がまだ宿主の中に残存しているあいだに、選択的に宿主細胞を殺害するプロセスが開始または始動される実施形態では、そのような殺害を開始または始動させるのに必要な薬剤を、例えば静脈内注射によって宿主に投与することができる。例えば、自殺遺伝子の転換酵素型の発現が誘導性である実施形態で、そのような誘導は再構成されたドナー器官または組織が外植される前に開始され得る。プロドラッグは、ドナー器官または組織が宿主に残存している間も投与することができ、および/または該宿主からの除去後のドナー器官または組織と接触することができる。
宿主細胞を生体外で殺害するため、ネガティブ選択のために必要な薬剤は、液浸および/または潅流によって外植された器官または組織と接触する液体メディウム中に調製することが可能である。
宿主から再構成された器官または組織への異種抗原の移動の減少
本発明の特定の実施形態は、宿主哺乳動物に存在する外来細胞の細胞表面に自然な機構によって非ヒト哺乳動物宿主の細胞表面抗原が移動することができるという認識に基づく。本発明の一実施形態は、非ヒト哺乳動物宿主での少なくとも1つの異種抗原の発現を減少させることで、非ヒト哺乳動物宿主に生着し、かつ該宿主によって維持されている外来ドナー細胞、器官および/または組織ならびに/あるいは置換細胞に対するその発現を減少または除去する。例えば、ヒトの主要異種抗原(例えばα−ガラクトシル・エピトープ、すなわちGal−α(1,3)Galエピトープ)および/またはヒトのマイナー異種抗原の移動を減少させることができる。
本発明の特定の実施形態は、宿主哺乳動物に存在する外来細胞の細胞表面に自然な機構によって非ヒト哺乳動物宿主の細胞表面抗原が移動することができるという認識に基づく。本発明の一実施形態は、非ヒト哺乳動物宿主での少なくとも1つの異種抗原の発現を減少させることで、非ヒト哺乳動物宿主に生着し、かつ該宿主によって維持されている外来ドナー細胞、器官および/または組織ならびに/あるいは置換細胞に対するその発現を減少または除去する。例えば、ヒトの主要異種抗原(例えばα−ガラクトシル・エピトープ、すなわちGal−α(1,3)Galエピトープ)および/またはヒトのマイナー異種抗原の移動を減少させることができる。
本明細書中に言及するように、グリコシルホスファチジルイノシトールアンカー型(anchored)タンパク質は、ホスファチジルイノシトール群に連結される複合オリゴグリカンであるグリコシルホスファチジルイノシトール・アンカー(GPIアンカー)またはGPI様アンカー(すなわちスフィンゴ脂質イノシトール群に連結される類似の複合オリゴグリカン)を介して、膜の脂質二重層に結合し、それによって膜に対してタンパク質のC末端が付着するタンパク質である。特定の細胞外炭水化物エピトープは、細胞膜脂質にも直接連結される。
グリコシルホスファチジルイノシトール(GPI)アンカー型タンパク質が生体内で生細胞の膜間で交換されることが知られており、例えば赤血球から内皮へ、さらにその逆におこなわれる(Medof et al., Cell-surface engineering with GPI-anchored proteins. Cell Surface Eng’g (1996) Vol. 10, pp. 574-586; Kooyman et al. (1995) In vivo-transfer of GPI-linked complement restriction factors from erythrocytes to endothelium Science, Vol. 269, pp. 89-92)。GPIアンカー型タンパク質が赤血球の膜間で交換されることも知られてもいる(Sloand et al. (2004) Transfer of glycosylphosphatidylinositol-anchored proteins to deficient cells after erythrocyte transfusion in paroxysmal nocturnal hemoglobinuria Blood (12):3782-3788. See also: Babiker et al. (2005) Transfer of functional prostasomal CD59 of metastatic prostatic cancer cell origin protects cells against complement attack Prostate. 62(2):105-114; Dunn et al. (1996) A knock-out model of paroxysmal nocturnal hemoglobinuria: Pig-a(-) hematopoiesis is reconstituted following intercellular transfer of GPI-anchored proteins. Proc Natl Acad Sci U S A. 93(15):7938-7943; and Anderson et al. (1996) Intercellular transfer of a glycosylphosphatidylinositol (GPI)-linked protein: release and uptake of CD4-GPI from recombinant adeno-associated virus-transduced HeLa cells Proc Natl Acad Sci U S A. 93(12):5894-5898)。GPIアンカー/結合生体分子は、細胞間接触を経て、微細小胞を経ておよび/または微小粒子(例えばリポ蛋白粒子)を経て、細胞間を移動すると考えられている。本発明は、細胞間転送の機構によって限定されない。細胞膜にゆるく組み込まれるタンパク質(例えば、細胞膜を貫通せず、細胞膜中に組み込まれた短い尾部を持つもの)は、自然な機構による細胞間移動にさらされる可能性がある。
ドナー細胞(例えば、器官または組織あるいはその一部分の形で)が宿主哺乳動物によって生きた状態で維持され、部分的に少なくとも置換細胞で再構成された後にレシピエント哺乳動物(例えばヒト患者)に移植または移動される本発明の実施形態では、宿主哺乳動物からドナー材料および/または置換細胞へ移動される抗原は、レシピエントによって再構成された器官または組織の免疫拒絶に関与することができる。そのような異種抗原として、例えば、直接細胞膜脂質に連結されるか、さもなければ細胞膜に連結される炭水化物エピトープと同様に、移動されたタンパク質のペプチド・エピトープおよび/または移動されたタンパク質上に存在する炭水化物エピトープ(例えばα−ガラクトシル・エピトープとN−グリコリルノイラミン酸(NeuGc)エピトープ)が挙げられる。
α−ガラクトシル・エピトープ
宿主哺乳動物が、α−ガラクトシル(Gal−α(1,3)Gal)エピトープ修飾されたタンパク質および/または脂質(例えば有蹄類または齧歯動物)を作製するタイプであり、宿主が宿している細胞は、α−ガラクトシル・エピトープ陰性細胞(すなわちα−ガラクトシル・エピトープを産生しない細胞)(例えばヒト細胞)を含む場合、本発明によって、タンパク質および/または脂質上でのα−ガラクトシル・エピトープの発現を減少または除去するように修飾された非ヒト哺乳動物宿主を使用することによって、エピトープ陰性細胞へ移動されるα−ガラクトシル・エピトープの量が減少または除去される。
宿主哺乳動物が、α−ガラクトシル(Gal−α(1,3)Gal)エピトープ修飾されたタンパク質および/または脂質(例えば有蹄類または齧歯動物)を作製するタイプであり、宿主が宿している細胞は、α−ガラクトシル・エピトープ陰性細胞(すなわちα−ガラクトシル・エピトープを産生しない細胞)(例えばヒト細胞)を含む場合、本発明によって、タンパク質および/または脂質上でのα−ガラクトシル・エピトープの発現を減少または除去するように修飾された非ヒト哺乳動物宿主を使用することによって、エピトープ陰性細胞へ移動されるα−ガラクトシル・エピトープの量が減少または除去される。
α−ガラクトシル・エピトープの発現減少を呈する遺伝子操作された動物を作製する多数の方法は、当該技術分野で知られており、例えば(1)相同組換えによるGal−α(1,3)ガラクトシル転移酵素遺伝子(「α-ガラクトシル転移酵素遺伝子」、GGTA1)の遺伝学的ノックアウト、(2)基質に関してα−ガラクトシル転移酵素と拮抗するα−フコシル転移酵素(例えば、ヒトFUT1および/またはFUT2)等の他の転移酵素をコードする導入遺伝子の発現、ならびに(3)N結合糖分岐を阻害することで、α−ガラクトシル・エピトープの形成を減らすヒトN−アセチルグルコサミニル転移酵素IIIをコードする導入遺伝子の発現が挙げられる。炭水化物エピトープ異種抗原に関して本明細書中に使用される用語「発現」は、その異物抗原状態でのエピトープの提示量に関連する。したがって、炭水化物エピトープ異種抗原の発現を低下させることは、例えば、そのような炭水化物異種抗原−生成酵素のために、炭水化物エピトープ異種抗原を切断する酵素処理により、および/またはより異物抗原性でない構造または状態に炭水化物異種抗原を改変することにより、基質と競争する酵素活性を提供して、炭水化物エピトープ異種抗原を作製する一つ以上の酵素の活性を減らすか除去することにより達成可能である。
α−ガラクトシル・エピトープ発現が減少した遺伝学的改変非ヒト哺乳類動物と該動物を作製する方法は、例えば以下の特許または特許出願によって提供される(これらの文献はその全体を本明細書中に援用する)。米国特許第6,413,769号、米国特許第6,331,658号、米国特許6,166,288号、米国特許第5,821,117号、米国特許5,849,991号、米国特許出願公開第20040268424号(特許出願第10/646,970号)、米国特許出願公開第20030203427号(特許出願第10/125,994号)、米国特許出願公開第20030068818号(特許出願第10/105,963号)、米国特許出願公開第20020031494号(特許出願第10/254,077号)、米国特許出願公開第20030014770号(特許出願第10/098,276号)、米国特許出願公開第20040073963号(特許出願第10/362,429号)、米国特許出願公開第20040171155号(特許出願第10/762,888号)、および米国特許出願公開第20030131365号(特許出願第10/172,459)が挙げられる。GGTA1遺伝子に関するマウス・ホモ接合型欠失およびそれを作製する方法は、例えば、米国特許第5,849,991号によって提供される。GGTA1遺伝子に関する豚ホモ接合型欠失およびそれを作製する方法は、例えば、米国特許出願公開第20040268424号によって開示される。配列番号6(16ないし1128位のCDS)は、ブタのα(1,3)ガラクトシル転移酵素遺伝子(GGTA1)のmRNA配列を提供する。ヒツジおよび牛のGGTA1遺伝子mRNA配列をGenBank受託番号NM_001009764(配列番号7、11ないし1120位のCDS)およびNM_177511(配列番号8、469ないし1575位のCDS)として提供する。マウスのGGTA1遺伝子mRNA遺伝子をGenBank受託番号NM_010283(配列番号9、445ないし1560位のCDS)として提供する。
イソグロボシド3(iGb3)合成酵素は別の酵素であり、α(1,3)ガラクトシル転移酵素に加えて、Galα(1,3)Gal部分を合成する。α(1,3)ガラクトシル転移酵素とは対照的に、iGb3合成酵素は、好ましくは、糖タンパク質基質上で糖脂質を修飾する(Keusch et al. (2000) Cloning of Gb3 synthase, the key enzyme in globo-series glycosphingolipid synthesis, predicts a family of alpha1,4-glycosyl transferases conserved in plants, insects, and mammals J. Bio. Chem. 275:25308-25314)。iGb3合成酵素は、ラクトシルセラミド(LacCer(Galβ1,4Glcβ1Cer))に作用して糖脂質イソグロボイド構造iGb3(Galα1,3Galβ1,4Glcβ1−Cer)を形成し、グリコシンゴ脂質のイソグロボ系の合成を開始させる。iGb3合成酵素の発現が減少または除去された遺伝的改変ブタならびにそれを作製するための方法および配列は、例えば、米国特許出願公開第20050155095号(特許出願第10/981,935号)その全体を本明細書中に援用)によって提供される。ラットiGb3合成酵素のmRNA配列は、GenBank受託番号NM_138524(配列番号10、78ないし1097位のCDS)およびマウス遺伝子のそれはGenBank受託番号NM_001009819(配列番号11、1ないし113位のCDS)として報告されている。
本発明によれば、α−ガラクトシル転移酵素(GGTA1)、iGb3合成酵素、またはCMP−NeuAc水酸化酵素等の選択された酵素、またはタンパク質異種抗原の発現を、dsRNAを用いた転写サイレンシング(RNA干渉、RNAi)および/またはdsRNAを用いた転写遺伝子サイレンシングによって、ならびに/あるいはアンチセンス方法によって、非ヒト哺乳動物宿主(または一般的には非ヒト哺乳動物またはその器官もしくは組織)において減少させることが可能であり、あるいは完全に除去することが可能である。そのようなサイレンシングに用いられる二重鎖RNA分子を、宿主の細胞内で、宿主ゲノムまたは該細胞に導入されたベクターから、作製することが可能であり、および/または外から細胞に提供することが可能である。転写後サイレンシングおよび/または転写遺伝子サイレンシングを誘発する二本鎖RNAの形態のいずれも、用いることができ、該形態として、限定されるものではないが、siRNA(例えば、ダイサー等のRNアーゼIIIの消化産物または類似の大きさおよび構成の短dsRNA分子)、短ヘアピンRNA、および設計されたたマイクロRNA(miRNA)が挙げられる。RNAサイレンシングに対する有効な分子および戦略の設計および選択ならびに事前選択された標的のアンチセンス調節は、当該技術分野で確立されている。RNAサイレンシングのための有効な分子および戦略の設計および選択ならびに事前選択された標的のアンチセンス調節は、当該技術分野において十分に確立されている。ブタのα−ガラクトシル転移酵素 (GGTA1)のヌクレオチド配列は、例えば、米国特許第5,849,991号、米国特許第5,821,117号、および米国特許出願公開第20030203427号(各々の全体を本明細書中に援用)によって提供される。
さらに理解されなければならないことは、必ずしも必要とは限らないが、異種抗原および/または異種抗原産生酵素の減少および/または除去を、非ヒト哺乳動物宿主にヒト細胞が導入される前に行うことができる。例えば、ヒト細胞を、胎児非ヒト哺乳動物宿主に導入して、宿主の一つ以上の器官または組織に組み込むことが可能であり、また宿主の誕生後、異種抗原および/または異種抗原産生酵素の減少または除去を任意の方法(例えば、異種抗原または異種抗原-生成酵素の発現を静まらせるRNAサイレンシング分子による処置)によって誘導することが可能である。トランスジェニック宿主もまた提供され、該トランスジェニック宿主は、異種抗原または異種抗原産生酵素のRNAスプライシングが誘導され、および/または異種抗原の産生を分断または妨げる酵素の発現を誘導することができる。
本発明の一実施形態では、宿主および/またはドナーは、α(1,3)ガラクトシル転移酵素合成Ga1−α(1,3)Galエピトープの発現を、例えば修飾および/または処置の結果として、減少させる。別の実施形態では、宿主および/またはドナーは、iGb3合成酵素合成Ga1−α(1,3)Galエピトープの発現を、例えば修飾および/または処置の結果として、減少させる。関連の実施形態では、宿主および/またはドナーは、α(1,3)ガラクトシル転移酵素合成およびiGb3合成酵素合成Gal−α(1,3)Gal1エピトープの両方の発現が減少している。
α−ガラクトシル・エピトープを発現しない細胞に既に転移されたα−ガラクトシル・エピトープと同様に、α−ガラクトシル・エピトープを発現しない細胞に転移され得る宿主細胞上で発現したα−ガラクトシル・エピトープもまた、酵素的に、例えば、α−ガラクトシダーゼまたはエンド−β−ガラクトシダーゼCによって、除去し得る。そのような酵素を、例えば、ヒト・ドナー器官または組織を維持している宿主に対して、静注により注入することができ、および/または適当な宿主内で構成的または誘導的に発現させることができる。α−ガラクトシル・エピトープの酵素的除去は、例えば、米国特許第6,758,865号、米国特許第6,491,912号、米国特許第6,331,319号、米国特許第6,046,379号、およびMaruyama et al., Xenotransplantation 11(5), pp. 444-51 (2004)(各々、その全体を本明細書中に援用)に教示されている。
本発明の実施形態では、ヒト置換細胞を用いてヒトに対する後期移植用の非ヒト哺乳動物ドナー器官または組織を少なくとも部分的に再構成する本発明の実施形態では、本明細書中に述べられているように、特に最終器官または組織産物がキメラ状である(すなわち、ヒト置換細胞のみならず、ドナー動物細胞も含む)場合、ドナー器官または組織もまたα−ガラクトシル・エピトープおよび/または他の異種抗原に対してネガティブであることが好ましい。置換細胞が非ヒトであり、また目的とするレシピエントがヒトであるならば、置換細胞が異種抗原に対してネガティブであることも好ましい。関連した実施形態において、修飾および/または処置の結果として、実施例に関して、置換細胞またはそのプロバイダはα(1、3)ガラクトシル転移酵素合成Gal−α(1,3)Galエピトープおよび/またはiGb3合成酵素合成Gal−α(1,3)Galエピトープの発現を低下させた。
N−グリコリルノイラミン酸(NeuGc)エピトープ
N‐アセチルノイラミン酸(NeuAc)およびN−グリコリルノイラミン酸(NeuGc)は、タンパク質および脂質に対する細胞表面炭水化物修飾として見出されるシアル酸が豊富な形態である。NeuGcは、大部分の動物に存在し、注目すべき例外はヒトおよび鶏である。したがって、NeuGcはヒト免疫系に関する異種抗原である。NeuGcは、シチジン・モノホスホN‐アセチルノイラミン酸水酸化酵素(CMP−NeuAc水酸化酵素)による一つの水酸基の追加によって、N‐アセチルノイラミン酸(NeuAc)から、生体内で合成される。本発明によって、NeuGcエピトープの発現が減少または完全に除去された非ヒト哺乳動物、あるいはその器官または組織を、任意の適当な方法によって、作製することができ、該方法として、例えば、(i)相同組換えによるCMP−NeuAc水酸化酵素遺伝子の遺伝学的なノックアウト、(ii)転写後RNAサイレンシング、転写のdsRNA媒介遺伝子サイレンシング、および/またはCMP−NeuAc水酸化酵素遺伝子に対するアンチセンス技術、(iii)ノイラミニダーゼ等の適当な酵素を用いたNeuGcエピトープの酵素的除去が挙げられる。ノイラミニダーゼは、NeuGcおよびNeuAc細胞表面エピトープを除去する。必要に応じて、基質としてシチジン・モノホスホ−N‐アセチルノイラミン酸(CMP−NeuAc)を使用して、シアリル転移酵素でさらに処置することによって、NeuAcエピトープを再生することができる。CMP−NeuAc水酸化酵素遺伝子発現およびそれに必要とされるヌクレオチド配列を除去するために遺伝学的に修飾された非ヒト哺乳動物の作製、同様にNeuGCエピトープを酵素的に除去する方法は、米国特許出願公開第20030165480号(特許出願第10/135,919号)および第20050223418号(特許出願第10/863,116号)(各々の全体を本明細書中に援用)によって提供される。同様に、国際公報WO 2004/108904も参照せよ。配列番号12(1ないし672位にCDS)は、米国特許出願公開第20030165480号に由来するブタのCMP−NeuAc水酸化酵素遺伝子の部分mRNAコーディング配列である。マウスCMP−NeuAc水酸化酵素遺伝子のメジャーおよびマイナーの選択的スプライスによる形態のmRNA配列は、それぞれGenBank受託番号AB061276(配列番号13、461ないし2191位にあるCDS)およびAB061277(配列番号14、623ないし2353位にあるCDS)によって、提供される。
N‐アセチルノイラミン酸(NeuAc)およびN−グリコリルノイラミン酸(NeuGc)は、タンパク質および脂質に対する細胞表面炭水化物修飾として見出されるシアル酸が豊富な形態である。NeuGcは、大部分の動物に存在し、注目すべき例外はヒトおよび鶏である。したがって、NeuGcはヒト免疫系に関する異種抗原である。NeuGcは、シチジン・モノホスホN‐アセチルノイラミン酸水酸化酵素(CMP−NeuAc水酸化酵素)による一つの水酸基の追加によって、N‐アセチルノイラミン酸(NeuAc)から、生体内で合成される。本発明によって、NeuGcエピトープの発現が減少または完全に除去された非ヒト哺乳動物、あるいはその器官または組織を、任意の適当な方法によって、作製することができ、該方法として、例えば、(i)相同組換えによるCMP−NeuAc水酸化酵素遺伝子の遺伝学的なノックアウト、(ii)転写後RNAサイレンシング、転写のdsRNA媒介遺伝子サイレンシング、および/またはCMP−NeuAc水酸化酵素遺伝子に対するアンチセンス技術、(iii)ノイラミニダーゼ等の適当な酵素を用いたNeuGcエピトープの酵素的除去が挙げられる。ノイラミニダーゼは、NeuGcおよびNeuAc細胞表面エピトープを除去する。必要に応じて、基質としてシチジン・モノホスホ−N‐アセチルノイラミン酸(CMP−NeuAc)を使用して、シアリル転移酵素でさらに処置することによって、NeuAcエピトープを再生することができる。CMP−NeuAc水酸化酵素遺伝子発現およびそれに必要とされるヌクレオチド配列を除去するために遺伝学的に修飾された非ヒト哺乳動物の作製、同様にNeuGCエピトープを酵素的に除去する方法は、米国特許出願公開第20030165480号(特許出願第10/135,919号)および第20050223418号(特許出願第10/863,116号)(各々の全体を本明細書中に援用)によって提供される。同様に、国際公報WO 2004/108904も参照せよ。配列番号12(1ないし672位にCDS)は、米国特許出願公開第20030165480号に由来するブタのCMP−NeuAc水酸化酵素遺伝子の部分mRNAコーディング配列である。マウスCMP−NeuAc水酸化酵素遺伝子のメジャーおよびマイナーの選択的スプライスによる形態のmRNA配列は、それぞれGenBank受託番号AB061276(配列番号13、461ないし2191位にあるCDS)およびAB061277(配列番号14、623ないし2353位にあるCDS)によって、提供される。
α−ガラクトシル・エピトープおよびNeuGcエピトープの還元によって特徴付けられる動物あるいはその器官または組織もまた、本発明にもとづいて使用することが可能である。本発明の一実施形態では、α−ガラクトシル転移酵素およびCMP−NeuAcヒドロキシラーゼに関してホモ接合的にネガティブである二倍遺伝子ノックアウト非ヒト哺乳動物(例えば、有蹄類)を、非ヒト哺乳動物宿主(および/または置換細胞のドナーおよび/またはプロバイダ)として使用する。ヘテロ接合ノックアウトは本発明の範囲内でもある。別の実施形態では、非ヒト哺乳動物宿主(および/またはドナーおよび/または置換細胞のプロバイダ)は、α−ガラクトシル転移酵素およびCMP−NeuAcヒドロキシラーゼ遺伝子ノックアウト(ホモ接合的に)の両方を有し、少なくとも1つのトレランス促進生体分子の発現を目的とする導入遺伝子を含む。単純な遺伝子欠失に代わるものとして、本発明によって使用される遺伝学的なノックアウトを、条件つきで、当該技術分野で知られているように、遺伝子欠失のための誘導性レコンビナーゼ発現方法およびシステム(例えばCRE−LOXシステム)を用いて、得ることが可能性である。
宿主細胞から外来ドナー細胞および/または外来置換細胞への異種抗原の細胞間移入に加えて、宿主異種抗原は、生または死宿主細胞および/またはフラグメント(例えば細胞膜フラグメント)の形で、宿主が宿しているヒト器官または組織に存在することもありえる(少なくとも一部の例で)。したがって、本発明の一実施形態は、非ヒト哺乳動物宿主を遺伝学的に修飾して、宿主からドナー細胞または置換細胞までの細胞間で移動可能ではない少なくとも1つの異種抗原(例えば細胞間で移動可能でない異種抗原宿主膜内外タンパク質)の発現を減少または完全に除去することによって、該非ヒト哺乳動物宿主を用いて、宿主が宿しているヒト細胞再構成器官または組織を、ヒト・レシピエントに対する移植に対して、より忍容性を高くする方法を提供する。異種抗原膜貫通タンパク質の例としては、ヒト・レシピエント免疫系に関して、非ヒト膜貫通型MHCクラスIおよびMHCクラスII分子が挙げられる。
宿主からドナー器官または組織へのトレランス促進生体分子の移入
本発明の別の態様は、再構成されたドナー器官または組織のドナー細胞および/または置換細胞(ヒトおよび/または非ヒト)へ移される際に目的とするレシピエント(例えばヒト)の事前選択された型の免疫系に対する再構成産物器官または組織の耐容性を改善する少なくとも1つの移動可能な「トレランス促進」生体分子を発現または該発現を高めるように修飾された非宿主哺乳類を提供する。
本発明の別の態様は、再構成されたドナー器官または組織のドナー細胞および/または置換細胞(ヒトおよび/または非ヒト)へ移される際に目的とするレシピエント(例えばヒト)の事前選択された型の免疫系に対する再構成産物器官または組織の耐容性を改善する少なくとも1つの移動可能な「トレランス促進」生体分子を発現または該発現を高めるように修飾された非宿主哺乳類を提供する。
選択されたGPIアンカー型タンパク質を発現する方法は、確立されている。例えば、DAF(減衰加速因子、CD55)、MIRL(反応性溶解の細胞膜抑制因子、CD59)、およびMCP(細胞膜補因子タンパク質、CD46)のヒトまたは非ヒト形態等、いくつかの補体抑制因子がGPIにアンカーした形態として生ずる。これらの補体阻害剤は、例えば、免疫寛容または拒絶のための重要な部位である赤血球および内皮上で見出される。これらのGPIにアンカーした補体阻害剤の少なくとも1つのヒトまたは非ヒト形態を発現する、またはその発現を高める(正常な内因性発現に対して)トランスジェニック非ヒト宿主哺乳動物は、置換細胞で再構成されている、あるいは再構成されると思われるドナー器官または組織の動物の宿主として使用される。関連した実施形態は、少なくとも1つのトレランス促進生体分子を発現させるもので、このトレランス促進生体分子は、例えば、タンパク質であり、該タンパク質は、自然に存在しないか、または非ヒト哺乳動物宿主によって、トレランス促進生体分子の発現を増加させるものではなく、例えば、限定されるものではないが、列挙された補体阻害剤の少なくとも1つであり、それによって、宿主哺乳動物に常在する外来細胞(ドナー細胞および/または置換細胞)の少なくともいくつかに対してトレランス促進生体分子の移入または移入の増加をもたらす。
さらに、GPIアンカー型タンパク質またはGPIアンカー型融合タンパクとして、GPIをアンカーされた形態では全く発現されない選択されたタンパク質の細胞外領域またはその一つ以上の選択された部分を発現する方法は、当該技術分野で確立されており、本方法は、宿主(例えばドナー細胞および/または置換細胞)に常在する外来細胞に対して選択トレランス促進導入遺伝子産物が移入可能であるトランスジェニック非ヒト哺乳動物宿主を生じさせるために、本発明によって使用され得る。
GPIアンカー型タンパク質は、他の膜結合タンパク質と同様に、炭水化物部分の追加によって、修飾される。例えば、ヒトCD59は単一のN−グリコシル化部位といくつかの潜在的O−グリコシル化部位とを有する(Rudd et al. The glycosylation of the complement regulatory protein, human erythrocytes CD59. (1997) J. Biol. Chem., 272, 7229-7244)。したがって、本発明の一実施形態は、移入可能なトレランス促進生体分子(例えば、hCD59)を発現するように遺伝学的に修飾され、また、例えば本明細書中に記載されたような遺伝学的修飾の結果として、α−ガラクトシルまたはNeuGcエピトープ等の少なくとも一つの炭水化物異種抗原の発現が減少している、非ヒト宿主哺乳動物を提供する。そのような宿主を、記載した方法で、宿主器官、組織、および/または細胞を生きた状態で維持するために、使用することができる。都合のよいことに、そのような宿主の使用は、望ましくない炭水化物異種抗原によるトレランス促進生体分子の修飾(例えばトレランス促進タンパク質)を予防し、それによって、宿主が宿しているヒト器官、組織、および/または細胞に対するそれらの移入を予防する一方で、移入されたトレランス促進生体分子のトレランス促進作用が改善される。
別の実施形態は、非ヒト哺乳動物宿主で生きた状態にある再構成キメラまたは少なくとも実質的にヒト器官を受け入れるするステップを含む方法を提供するもので、該ヒト哺乳動物宿主は、少なくとも1つの移入可能なトレランス促進生体分子を発現するように、遺伝学的に修飾されており、また該トレランス促進生体分子は、生体内グリコシル化にさらされ、さらにその後、例えば、外植後、器官または組織産物(例えば、トレランス促進生体分子に結合されている可能性もある)を酵素的に処置することで、炭水化物移植抗原(例えば、器官または組織産物に対して宿主から移入されたもの)を除去する。
以下の実施例は本発明にもとづくトランスジェニック哺乳類宿主での発現のための種々のトレランス促進生体分子を例示しており、および/またはそのような宿主を提供する。
米国特許第6,825,395号および米国特許出願公開第20030165480号(各々その全体を本明細書中に援用)は、hDAFを発現するトランスジェニック非ヒト哺乳動物を提供する。
米国特許第6,639,122号(その全体を本明細書中に援用)は、トランスジェニック・ブタの発現HLA−Dを提供する。
血液凝固阻止剤ヒト組織因子経路阻害剤およびヒルジンの一方または両方の膜連結融合タンパク質形態を発現するトランスジェニック哺乳動物を、用いることができる。Chen et al., Complete inhibition of acute humoral rejection using regulated expression of membrane-tethered anticoagulants on xenograft endothelium. Am J Transplant. 2004 Dec; 4(12):1958-63 および米国特許第6,423,316号(各々その全体を本明細書中に援用)を参照せよ。
ヒトHLA−Gを発現することによってヒトNK細胞による細胞溶解から保護されるトランスジェニック哺乳動物を使うことができる。ヒト・ナチュラル・キラー(NK)細胞(ブタ血管内皮細胞を直接溶解することができる)は、異種移植において重要な役割を果たす。HLA−Gは、NK細胞によって影響を受けやすい標的細胞を細胞溶解から保護することに関係した非古典的主組織適合性複合系(MHC)クラスI分子である(Wang et al., A study of HLA-G1 protection of porcine endothelial cells against human NK cell cytotoxicity. Transplant Proc. 2004 Oct; 36(8): 2473-4)。
細胞表面ヒトFasリガンドを発現しているトランスジェニック哺乳動物(Fas受容体保持細胞のアポトーシスを誘発)を用いることができる(Rodriguez-Gago et al., Human anti-swinegammadelta T-cell xenoreactivity is inhibited by human FasL (Fas ligand) expression on swine endothelial cells, Transplantation. 2001 Aug 15; 72(3):503-9)。非ヒト哺乳動物宿主で維持されているヒト・ドナー器官または組織のヒト細胞は、移入宿主抗原のためヒト・レシピエントの免疫系に対して非ヒトと見ることができることから、本発明は、ヒト・ドナー器官または組織に移入されうるヒトFasLを宿主において発現させることにより、ヒトに対するさらなる移植に応じたヒト細胞に対する免疫拒絶を制限する。FasLは、膜貫通タンパク質として天然に存在する。本発明によれば、トランスジェニック非ヒト宿主哺乳動物において、ヒトFasL(例えばLeu 281に対するアミノ酸Leu 107)の細胞外領域は、構成的または誘導的に、単一または多量体形態で、GPIアンカー型タンパク質または融合タンパクとして発現し得る。
先に述べたように、宿主細胞からドナー細胞および/または置換細胞への異種抗原の細胞間移入に加えて、宿主異種抗原は、一部の例でも、生または死宿主細胞および/またはフラグメント(例えば細胞膜フラグメント)の形で、再構成された器官または組織産物に存在し得る。したがって、本発明の一実施形態は、非ヒト哺乳動物宿主を用いて再構成器官または組織が、ヒト・レシピエントに対する移植に応じて、よりトレランスが良好となるようにする方法を提供するもので、該非ヒト哺乳動物宿主を遺伝学的に修飾して、宿主からドナー細胞までの細胞間を移動可能または移動可能ではない少なくとも1つのトレランス促進生体分子を発現または該発現を増加させる。このように、トレランス促進生体分子は、宿主細胞またはフラグメント上に存在する異種抗原に対するレシピエント免疫反応を少なくとも部分的に改善し、ヒト・レシピエントにおける再構成された器官または組織に向けたネガティブ免疫応答の一般的な発生を低下させる。宿主細胞フラグメントおよび/または細胞間マトリックスは、取り除く時間がなかった場合および/または能動的に取り除かれなかった場合、宿主細胞が選択的に殺害された後にも、再構成された器官または組織に存在するものであってもよい。再構成されたヒト器官または組織から宿主抗原と細胞形質成分を取り除く方法は、後述する本発明の更なる実施形態によって提供される。
条件付け後の実施形態
本発明のさらなる態様は、再構成器官または組織を条件づける方法を、提供するもので、該再構成器官または組織はヒト置換細胞を含み、該ヒト置換細胞が非ヒト哺乳動物宿主によって生きた状態に維持され、ヒト等の事前選択されたタイプのレシピエントの免疫系によって、トレランスがより良好になる。一実施形態では、再構成器官または組織を哺乳動物宿主の循環から、例えば宿主からの外植によって、単離し、異種細胞(事前選択されたレシピエントに関して)から少なくとも部分的に除外される。細胞、異種細胞形質成分、異種細胞外物質、および/または異種抗原で除外される。関連した実施形態において、処置された器官または組織は、それから事前選択されたタイプのレシピエントに移植される。
本発明のさらなる態様は、再構成器官または組織を条件づける方法を、提供するもので、該再構成器官または組織はヒト置換細胞を含み、該ヒト置換細胞が非ヒト哺乳動物宿主によって生きた状態に維持され、ヒト等の事前選択されたタイプのレシピエントの免疫系によって、トレランスがより良好になる。一実施形態では、再構成器官または組織を哺乳動物宿主の循環から、例えば宿主からの外植によって、単離し、異種細胞(事前選択されたレシピエントに関して)から少なくとも部分的に除外される。細胞、異種細胞形質成分、異種細胞外物質、および/または異種抗原で除外される。関連した実施形態において、処置された器官または組織は、それから事前選択されたタイプのレシピエントに移植される。
一実施形態では、再構成ドナー器官または組織、例えば宿主から改変器官または組織生成物または宿主の細胞残屑に移入された再構成ドナー器官または組織(例えば、膜結合タンパク質および/または炭水化物エピトープに結合した膜)内に存在する非ヒト哺乳動物宿主由来のメジャーおよび/またはマイナー異種抗原は、少なくとも部分的に、自然の代謝回転および分解の結果哺乳動物宿主の循環から単離された後、器官または組織から受動的に除去にされる。
別の実施形態では、再構成された産物器官または組織からの異種材料の除去は、哺乳動物宿主からの単離の後、能動的に促進される。本発明による一例では、非ヒト哺乳動物宿主の細胞はドナー哺乳動物の細胞および/または置換細胞に対して選択的に殺害可能であって、再構成された器官または組織を該器官または組織に残留した不必要な哺乳動物宿主細胞を選択的に殺害することが要求される条件(例えば該器官または組織を必要な薬剤と接触させることにより)にさらす。この殺害プロセスによって生ずる壊死細胞片は、例えば、少なくとも部分的に、宿主からの単離後に組織を潅流することによって、器官または組織から除去される。必要に応じて、例えば潅水を単離された再構成器官または組織を通して再循環させれば、細片は灌流液から濾過することも可能である。
別の実施形態では、再構成された器官または組織内で存在可能である異種細胞表面抗原は、例えばメディウムの液浸または潅流により、器官を酵素含有メディウムと接触させることにより哺乳動物宿主から単離した後、能動的に摘出または酵素修飾される。例えば、本発明は、再構成器官または組織に存在する可能性のある炭水化物異種抗原を器官または組織をメディウムで潅流することによって取り除くことが可能であり、該メディウムは適当なグリコシダーゼ、例えばαガラクトシル・エピトープと除去するためのαガラクトシダーゼまたはエンドβガラクトシダーゼC(エンドGalC)ならびに/あるいはNeuGcエピトープを除去するためのニューラミニダーゼを含む(α−galに関しては、例えば、米国特許第6,758,865号、米国特許6,491,912号、米国特許6,331,319; 号、米国特許6,046,379号、およびMaruyama et al. Xenotransplantation. 2004 Sep; 11(5): 444-51を参照せよ。また、NueuGcに関しては、米国特許公開公報第20030165480号(特許出願第10/135,919号)を参照せよ。各々その全体を本明細書中に援用する)。これらの特定のエピトープは、例えば、宿主として用いた非ヒト哺乳動物がその発現を完全に除去するように遺伝学的に修飾されていない場合、存在することがある。
同様に本発明は、GPIアンカー型メジャーおよび/またはマイナー異種抗原(GPIアンカー型タンパク質に連結されるタンパク質または異種抗原部分)を、通常、ホスファチジルイノシトール特異性ホスホリパーゼC(PI−PLC)またはホスファチジルイノシトール特異性ホスホリパーゼD(PI−PLD)等の適当な酵素と再構成された器官または組織とを接触(例えば、液浸または潅流によって)させることによって、GPI連結タンパク質を除去することを定める。適当なホスホリパーゼは、例えば、米国特許第6,689,598号、米国特許第6,638,747号、および米国特許第5,418,147号(各々その全体を本明細書中に援用)によって提供される。都合のよいことに、哺乳動物宿主に起因したGPIアンカー型異種抗原が除去され、その一方で、再構成された器官または組織産物細胞(例えばヒト置換細胞から誘導されたもの)に特異的な、除去されたGPIアンカー型生体分子が、自然に再生する。
別の実施形態は、再構成された器官または組織が哺乳動物宿主の循環からまだ単離されないうちに、上記の細胞死誘導処置または酵素処置を開始することまたは少なくとも部分的に実施することを含む。したがって、宿主の循環系とさらに接触させることで、上記処置の作用が実質的になされないうちに、再構成された器官または組織を、哺乳動物宿主から単離することができる。
器官または組織を還流するための方法およびメディウムは、当該技術分野で十分に開発されている。適当な方法およびメディウムは、例えば、米国特許6,699,231号、米国特許6,699,231号、米国特許6,677,150号、米国特許6,680,305号、米国特許6,627,393号、米国特許6,589,223号、米国特許6,506,549号、米国特許6,589,223号、米国特許6,677,150号、米国特許6,589,223号、米国特許6,524,785号、米国特許6,100,082号、米国特許5,965,433号、米国特許5,586,438号、米国特許5,498,427号、米国特許5,599,659号、米国特許6,492,103号、および米国特許5,362,622号(各々その全体を本明細書中に援用)によって得られる。
体外維持実施形態(extracrporeal support embodiments)
本発明に関連した方法は、再構成器官または組織を維持する非ヒト哺乳動物宿主から再構成器官または組織を外植するステップと、その後に、しばらくの間、体外維持装置および/または方法を用いて非ヒト哺乳動物宿主から分離して生きた状態で器官または組織を維持するステップとを含む。体外維持期間中、非ヒト宿主哺乳類由来および/または非ヒト・ドナー哺乳動物(例えば置換細胞による全置換が求められる)から不要に残留している、少なくともいくつかの異種(事前選択されたタイプのレシピエントに関して)細胞、異種細胞物質、異種細胞外物質、および/または異種抗原が、能動的および/または受動的に、例えば上記と同一の方法で器官または組織から除去される。一つの関連した実施形態では、事前選択されたタイプのレシピエントに対して、処置器官または組織を体外維持期間後に移植する。一実施形態において、体外維持期間は、約1、2、3、4、5、6、7、10、または14日である。別の実施形態において、体外維持期間は、少なくとも1、2、3、4、5、6、7、10、または14日である。
本発明に関連した方法は、再構成器官または組織を維持する非ヒト哺乳動物宿主から再構成器官または組織を外植するステップと、その後に、しばらくの間、体外維持装置および/または方法を用いて非ヒト哺乳動物宿主から分離して生きた状態で器官または組織を維持するステップとを含む。体外維持期間中、非ヒト宿主哺乳類由来および/または非ヒト・ドナー哺乳動物(例えば置換細胞による全置換が求められる)から不要に残留している、少なくともいくつかの異種(事前選択されたタイプのレシピエントに関して)細胞、異種細胞物質、異種細胞外物質、および/または異種抗原が、能動的および/または受動的に、例えば上記と同一の方法で器官または組織から除去される。一つの関連した実施形態では、事前選択されたタイプのレシピエントに対して、処置器官または組織を体外維持期間後に移植する。一実施形態において、体外維持期間は、約1、2、3、4、5、6、7、10、または14日である。別の実施形態において、体外維持期間は、少なくとも1、2、3、4、5、6、7、10、または14日である。
生きているドナー器官を維持するための任意のタイプの体外装置および/または方法を用いることができる。そのような装置のいくつかは、酸素および栄養素を供給するメディウムで被検体器官を潅流させる点で、人工心肺と類似している。このメディウムは、例えば、少なくとも部分的には、血液および/または人工血液(例えばヘモグロビン・ベースの血液代用品または過フッ化炭化水素ベースの血液代用品)にもとづくものであってもよい。そのような装置の一例は、トランスメディック簡易型器官保存システム(Transmedics Portable Organ Preservation System)(POPS)である。適当な細胞外維持装置および/または方法は、限定されるものではないが、米国出願公開第20040171138号、米国特許第6,100,082号、米国特許第6,046,046号、米国特許第6,677,150号、米国特許第6,673,594号、米国特許第6,642,045号、米国特許第6,582,953号、米国特許第6,794,182号、米国特許第5,326,706号、米国特許第5,494,822号、米国特許第4,837,390号、米国特許第4,186,565号、米国特許第4,745,759号、および米国特許第5,807,737号(各々その全体を本明細書中に援用)に記載されている。
1つの体外維持実施形態は、非ヒト哺乳動物宿主から再構成された器官または組織を外植するステップと、その後、しばらく間、体外維持により生きた状態でそれを維持するステップと、体外維持期間の少なくとも一部分の期間中、先に述べたように、非ヒト宿主細胞(および/またはドナー細胞)を選択的に殺害および/または器官または組織を酵素処理して異種抗原を摘出するステップとを含む。関連した方法は、体外維持期間終了後、再構成器官または組織をレシピエント(例えば、ヒト・レシピエント)に移植するステップを含む。
別の体外維持実施形態は、上記したように、哺乳動物宿主循環から器官または組織がまだ分離されないうちに、再構成器官または組織からの宿主細胞の選択的欠失を開始または少なくとも部分的に実行、および/または器官または組織を酵素的に処置することで異種抗原を取り除くステップと、宿主循環系とさらに接触させることで処置の効果が実質的になされないうちに、器官または組織を外植するステップと、その後に、体外維持により生きた状態に器官を維持するステップとを含む。上記した処置の1つ以上は、体外維持装置による器官または組織の維持中に、実行または継続してもよい。関連した方法は、さらに、体外維持期間の後、再構成された器官または組織をレシピエント(例えばヒト・レシピエント)に移植するステップを含む。
胚または胎児移入実施形態
本発明のさらなる実施形態は、既に記載したように、宿主へのドナー器官または組織の移植よりもむしろ胚または胎児の移入を用いる。自殺遺伝子または任意の種類のネガティブ選択マーカー(形質)の組織特異的発現を提供、さもなければネガティブ選択マーカーを組織特異的に発現させる導入遺伝子に関してヘテロ接合またはホモ接合である非ヒト哺乳動物胚または胎児を作製する。胚は、所望のネガティブ選択形質を持つ親動物(例えばトランスジェニック親動物(例えば、一つ以上の所望の自殺導入遺伝子に関して))に由来する親配偶子による体外受精によって容易に得られる。胎児は妊娠した動物から得ることができる。
本発明のさらなる実施形態は、既に記載したように、宿主へのドナー器官または組織の移植よりもむしろ胚または胎児の移入を用いる。自殺遺伝子または任意の種類のネガティブ選択マーカー(形質)の組織特異的発現を提供、さもなければネガティブ選択マーカーを組織特異的に発現させる導入遺伝子に関してヘテロ接合またはホモ接合である非ヒト哺乳動物胚または胎児を作製する。胚は、所望のネガティブ選択形質を持つ親動物(例えばトランスジェニック親動物(例えば、一つ以上の所望の自殺導入遺伝子に関して))に由来する親配偶子による体外受精によって容易に得られる。胎児は妊娠した動物から得ることができる。
1つの方法では、親動物の各々は一般に導入遺伝子または組織特異的ネガティブ選択形質に関してホモ接合であり、得られる胚または胎児はどれも形質に関してホモ接合である。もし片方の親がその形質に関してホモ接合であり、また他方がその形質を持たないことに関してホモ接合である場合、その子孫の全てがホモ接合である。片親が形質に関して少なくともヘテロ接合体(および形質が優位)である限り、その形質に関してヘテロ接合である胚および胎児を作製および選択することができる。
次に胚または胎児を、代理母動物は同一組織特異的自殺遺伝子形質発現についてトランスジェニックではなく、また一般的な事柄として同一の組織特異的ネガティブ選択マーカーを発現していない、同一または異なる種の代理母動物に移入する。移入された胚または胎児は、代理母によって維持される。例えば、胚は当該技術分野で知られている方法によって、偽妊娠雌に、例えば移入することができる。胎児は、例えば、すでに妊娠した代理母動物の子宮に、外科的に移植することができる。
胎児(母親体内に移転または移入された胚から母親体内で成長)のネガティブ選択形質を母親が欠いていることから、ネガティブ選択形質を発現する胎児組織の細胞を、この母親の対応組織に対して、条件的かつ選択的に削除することができる。代理母もまた、ネガティブ選択形質を発現する胎児の器官または組織の細胞を選択的に殺すことによって、胎児が損なっているであろう代謝的機能に関する代償的なサポートを提供する。
したがって、ネガティブ選択形質を発現する器官または組織の置換細胞を、胎児に導入することができ、ネガティブ選択形質を発現している細胞を削除する1セットの条件を胎児に提供することで、それらの移植および拡大を促進することができる。一条件セットがプロドラッグ等の少なくとも一種類の化学剤を含む場合、それが胎盤を通過することが可能な限り、母親への投与によって間接的に胎児へ導入する事が可能である。置換細胞を、ネガティブ選択処置前、後、および/またはその途中で、カテーテルからの輸液によって胎児に導入することが可能であり、または標的器官または組織に注射してもよい。ひとたび置換細胞を移植すると、さらなるネガティブ選択処置を用いることで置換細胞による器官または組織の選択的な再形成が促進される。
この実施形態の長所は、Beschornerの発明とは対照的に、ここでは、ネガティブ選択形質に関するホモ接合の胎児が使われるということにある。
実施形態の一変形例では、置換細胞はヒト細胞または該ヒト細胞を含むものである。別の実施形態では、置換細胞は非ヒト細胞を含む。別の変形例では、母親および胚または胎児は同一の種、例えば同一の有蹄類、例えば両方ともブタ由来とする。
実施形態の別の変形例では、少なくとも部分的に再構成された器官または組織を、胎児個体が誕生した後に、該胎児個体内で成長させる。さらに別の変形例では、胎児由来、別の哺乳類(例えばヒト)の胎児である誕生後の個体由来の再構成組織または器官を移植するさらなるステップを含む。別の変形例では、母および胎児の一方または両方が非ヒト哺乳動物であり、該非ヒト哺乳動物は、本明細書中に記載したような異種抗原の発現が低下される遺伝学的修飾等による改変がなされる。例えば、置換細胞が非ヒトでもある場合、置換細胞は遺伝学的修飾等の改変をおこなうことで、異種抗原の発現を低下させることも可能である。この実施形態の再構成器官または組織はまた、任意の条件付け後処置(例えば、酵素処置、および/または上記の体外維持法)を施すことができる。
一般的な異種抗原関連および条件付け後処置の実施形態
本発明者はまた、本明細書中に記載したような移動可能異種抗原の発現が減少した宿主を使用することで、任意の種類のヒト細胞および/またはヒト細胞含有組成物(例えば、ヒトまたはキメラ・ヒト、非ヒト器官または組織、例えば体の一部、固体もしくは分散した組織型等)を維持および/または拡大するための別な利点が、特にそのような細胞またはヒト細胞含有組成物がヒトに移植される場合、提供されることを見出した。限定されるものではないが、これには非ヒト哺乳動物宿主によって維持される生存または死亡しているヒト・ドナー由来のヒト器官または組織もしくはその一部分が含まれる。一変形例では、ヒト器官または組織は、非ヒト宿主に移植する際に、既に機能的に発達しており、例えば、発達の出生後段階にあるドナーに由来するものであってもよい。異なる変形例では、ヒト器官または組織は、非ヒト宿主に移植する際に、発達の原基段階にまだある。そのような原基は、宿主に対する移植に応じて、機能している器官または組織の中でその成長および分化を続けることが可能である。発達のための宿主哺乳動物に対する原基の移植法は、米国特許出願公開第20040191228号、第20040136972号、第20040082064号、第20030198628号、第20030096016号、および第20030086909号に開示されている(各々その全体を本明細書中に援用)。異種性を低減させた動物宿主で維持されるキメラ・ヒト、非ヒト哺乳動物器官または組織を任意の方法、例えばBeschornerの促進細胞置換法により、または促進置換することなく非ヒト哺乳動物(例えば胎児または出生後の個体)へのヒト細胞の導入により(例えば米国特許出願公開第20020100065号(特許出願第09/895,895号)および第20030096410号(特許出願第09/178,036号の方法)により、作製することが可能である。
本発明者はまた、本明細書中に記載したような移動可能異種抗原の発現が減少した宿主を使用することで、任意の種類のヒト細胞および/またはヒト細胞含有組成物(例えば、ヒトまたはキメラ・ヒト、非ヒト器官または組織、例えば体の一部、固体もしくは分散した組織型等)を維持および/または拡大するための別な利点が、特にそのような細胞またはヒト細胞含有組成物がヒトに移植される場合、提供されることを見出した。限定されるものではないが、これには非ヒト哺乳動物宿主によって維持される生存または死亡しているヒト・ドナー由来のヒト器官または組織もしくはその一部分が含まれる。一変形例では、ヒト器官または組織は、非ヒト宿主に移植する際に、既に機能的に発達しており、例えば、発達の出生後段階にあるドナーに由来するものであってもよい。異なる変形例では、ヒト器官または組織は、非ヒト宿主に移植する際に、発達の原基段階にまだある。そのような原基は、宿主に対する移植に応じて、機能している器官または組織の中でその成長および分化を続けることが可能である。発達のための宿主哺乳動物に対する原基の移植法は、米国特許出願公開第20040191228号、第20040136972号、第20040082064号、第20030198628号、第20030096016号、および第20030086909号に開示されている(各々その全体を本明細書中に援用)。異種性を低減させた動物宿主で維持されるキメラ・ヒト、非ヒト哺乳動物器官または組織を任意の方法、例えばBeschornerの促進細胞置換法により、または促進置換することなく非ヒト哺乳動物(例えば胎児または出生後の個体)へのヒト細胞の導入により(例えば米国特許出願公開第20020100065号(特許出願第09/895,895号)および第20030096410号(特許出願第09/178,036号の方法)により、作製することが可能である。
したがって、非ヒト動物(例えば、非ヒト哺乳動物)でヒト細胞を培養する一般的方法を提供する。この方法は、任意の形態のヒト細胞(例えば、ヒト器官またはヒト固体もしくは分散組織、あるいは上記したようなヒト細胞含有組成物)を、ヒト細胞に対して少なくとも実質的に免疫学的に寛容(トレランス)であり、遺伝学的修飾、さもなければ修飾または処置されることで、α−ガラクトシル・エピトープおよび/またはNeuGcエピトープ等の少なくとも1つの異種抗原の発現(ヒト免疫系に関して定義)を低下させ、それによってヒト細胞へ移される異種抗原の量を低下させる、非ヒト宿主動物(例えば、非ヒト哺乳動物)に、導入するステップと、一定期間(例えば、少なくとも2日、または少なくとも1週間もしくは少なくとも1ヶ月)にわたって宿主動物内で細胞を維持するステップとを、含む。関連した方法は、さらに、動物宿主からヒト細胞を除去する方法を含む。
宿主がα−ガラクトシル・エピトープの発現を低下させるために修飾される場合には、例えば、それをα(1,3)ガラクトシル転移酵素合成および/またはiGb3合成酵素合成α−ガラクトシル・エピトープの発現が低下するように修飾することが可能である。
もう一つの変形例では、次にヒト細胞と宿主細胞との混合物を宿主から除去し、宿主細胞を選択的に殺害することで、少なくとも実質的に純粋なヒト細胞組成物を得る。本明細書中に述べられるように、宿主動物(または置換細胞)の選択的欠失が可能になるように遺伝学的に修飾した宿主動物または置換細胞を、この場合に用いることができる。
異なる変形例では、次にヒト細胞含有組成物を動物宿主から除去し、少なくとも1つの酵素的処置による後条件付けをおこない、上記したように、宿主異種抗原を除去する。
さらに別の変形例では、非ヒト動物を宿主としたヒト細胞含有組成物を宿主から除去し、例えば少なくとも1、2、3、4、7、または30日間にわたって、体外維持される。
実施形態のさらなる変形例またはその任意の上記変形例では、ヒト細胞含有組成物、例えば、機能的に成長したヒト器官または組織を、必要に応じて、ヒト患者に対して移植することができる。このようにして、例えば、ヒト器官または組織を、必要があるまで、非ヒト動物宿主体内に生きた状態で預けておくことができる。関連した変形例において、ヒト小児、青年期、または成人に関して、機能的に発達した固形ヒト器官または組織または少なくともその実質的な部分(例えばヒト肝臓、膵臓、腎臓、心臓または肺)を維持するために、宿主はサイズ設定される。例えば、有蹄類の宿主(例えばブタ、ヒツジ、およびウシ)を、適当なサイズに設定することができる。
遺伝学的に修飾された動物は、突然変異(例えば欠失、置換、逆位、転移および/または挿入)等の遺伝学的修飾および/または現在もしくは任意の先の世代で導入された導入遺伝子(トランスジェニック動物)を含む動物である。異種抗原の発現を減少または完全除去するドナーまたは宿主動物の修飾は、任意の種類(例えば遺伝学的修飾または後成的修飾)のものであってよく、また宿主が修飾を含む限り、それは任意の現在または先の世代で導入されるものであってもよい。転写産物(例えば必要な開始コドンまたはリボソーム結合配列の除去)の発現を抑える、あるいは機能性タンパク質の発現を抑える遺伝子または対立遺伝子を不活性化する遺伝学的修飾は、任意の種類のものであってよく、例えば、遺伝子の転写を減らすか、排除する遺伝子のプロモーターの突然変異を含むものであってよい。遺伝子配列の遺伝子突然変異は、任意の種類(例えばその欠失、挿入、置換、逆位および/または組合せ)によるものであってもよい。異種抗原の発現を低下させ得る宿主のもう一種類の遺伝学的修飾は、導入遺伝子の宿主(任意の現在または先の世代)への統合を含むもので、該導入遺伝子は、異種抗原の発現を低下させる作用がある遺伝子産物(例えばRNAまたはタンパク質)を作製する。一実施例では、選択された遺伝子(例えばタンパク質異種抗原のための、または異種抗原−生成酵素のための遺伝子)のmRNA転写産物をサイレンシングするRNA−サイレンシング分子の発現(例えば、構成的であるか誘導性)を駆動させるゲノムに統合された導入遺伝子が使われる。別の例では、異種抗原を切断または改変する遺伝子の発現(例えば、構成的または誘導性)を駆動するゲノムに統合された導入遺伝子を使用する。さらに別の実施例においては、異種抗原−生成酵素と基質を争う酵素を産生する遺伝子の発現(例えば、構成的または誘導性)を駆動するゲノムに統合した導入遺伝子を使うことができる。後天的修飾により、遺伝子の活性を減少させることも、完全に除去することもできる。例えば、遺伝子のプロモーターおよび/または遺伝子の他の部分の二重鎖RNA媒介遺伝子サイレンシングは、遺伝子の翻訳をサイレンシングすることができる。理論によって制限されるものではないが、RNA媒介遺伝子サイレンシングはDNAレベルで遺伝子のメチル化および/または他の修飾によって媒介されると考えられている。
本明細書中に言及される用語の「ヒト細胞」として、ヒト細胞およびヒト細胞から誘導された細胞(ヒト細胞由来細胞)が挙げられる。限定されるものではないが、例えば、初代培養細胞および継代培養細胞、非不死化、不死化、または条件的(conditional)不死化ヒト細胞、少なくとも実質的にヒト細胞、遺伝学的に修飾されたヒト細胞、後成的に修飾されたヒト細胞、および無修飾ヒト細胞が挙げられる。ヒト細胞によって細胞再構成された器官または組織が指定のヒト・レシピエントに移植される本発明の実施形態の一変形例では、使用する置換細胞は該指定されたレシピエントから誘導されたものである。ヒト細胞で細胞再構成される器官または組織は、ヒト・レシピエントに移植される本発明の実施形態のもう一つの変形例において、所定のHLA型を有するヒト置換細胞を用いて器官または組織の細胞再構成をおこなうことで、再構成された器官または組織がレシピエントに適合し得るようにする。下位変形例においては、目的とするヒト・レシピエントのHLA型を決定した後、目的とするレシピエントのHLA型を最も少なく実質的に適合させる置換細胞を使用して、本発明にもとづく器官または組織の細胞再構成をおこなう。ヒト細胞で細胞再構成される器官または組織がヒト・レシピエントに移植される本発明の実施形態のさらに別の変形例では、HLA決定基が1つ以上欠けた修飾ヒト置換細胞を使用する。下位の変形例において、ヒト置換細胞は、移植に対するHLA決定基の障壁に関して、少なくとも実質的に普遍的に受け入れられる。
当業者は、本発明にもとづく宿主、ドナーおよび/または置換細胞として使われる非ヒト哺乳動物または細胞株またはそのプロバイダに対して、任意の内在性レトロウイルスを除去するために遺伝学的修飾を施すことができることを、理解するであろう。ここで、内在性レトロウイルスは、動物または細胞株のゲノムで特徴的に存在すると思われる。例えば、ブタ内在性レトロウイルス(PERV)を欠いたブタを、本発明による哺乳動物宿主、ドナーおよび/または置換細胞のプロバイダとして使用してもよい。
発行された米国特許を、本明細書中では、「米国特許」と記し、その後に特許番号を付した。公開された米国特許出願を、本明細書中では、「米国特許出願公開」と記し、その後に公開番号を付した。この開示で引用した特許、特許出願、遺伝子配列、論文、および他の刊行物の各々は、あたかも本明細書中に述べられるかのように、その全体を本明細書中に援用する。
この開示のどこかで引用または引用されていないかもしれない以下の米国特許は、その全体を本明細書中に援用する。米国特許第6,923,959号、米国特許第6,916,654号、米国特許第6,911,220号、米国特許第6,825,395号、米国特許第6,794,182号、米国特許第6,758,865号、米国特許第6,734,295号、米国特許第6,718,986号、米国特許第6,700,037号、米国特許第6,699,231号、米国特許第6,689,598号、米国特許第6,680,305号、米国特許第6,677,150号、米国特許第6,673,987号、米国特許第6,673,594号、米国特許第6,660,905号、米国特許第6,558,663号、米国特許第6,498,285号、米国特許第6,649,595号、米国特許第6,642,045号、米国特許第6,639,122号、米国特許第6,638,747号、米国特許第6,627,393号、米国特許第6,589,223号、米国特許第6,582,953号、米国特許第6,576,464号、米国特許第6,562,619号、米国特許第6,524,785号、米国特許第6,521,448号、米国特許第6,514,752号、米国特許第6,506,549号、米国特許第6,500,929号、米国特許第6,495,735号、米国特許第6,492,103号、米国特許第6,491,912号、米国特許第6,469,229号、米国特許第6,447,767号、米国特許第6,423,316号、米国特許第6,368,572号、米国特許第6,413,769号、米国特許第6,368,572号、米国特許第6,353,150号、米国特許第6,342,344号、米国特許第6,331,658号、米国特許第6,331,319号、米国特許第6,325,999号、米国特許第6,296,846号、米国特許第6,280,718号、米国特許第6,258,998号、米国特許第6,255,474号、米国特許第6,252,136号、米国特許第6,245,566号、米国特許第6,215,039号、米国特許第6,194,635号、米国特許第6,187,757号、米国特許第6,172,190号、米国特許第6,166,288号、米国特許第6,136,954号、米国特許第6,132,708号、米国特許第6,129,911号、米国特許第6,100,443号、米国特許第6,100,082号、米国特許第6,093,872号、米国特許第6,090,622号、米国特許第6,060,049号、米国特許第6,046,379号、米国特許第6,046,046号、米国特許第6,030,833号、米国特許第6,018,096号、米国特許第5,976,524号、米国特許第5,965,433号、米国特許第5,925,802号、米国特許第5,912,411号、米国特許第5,871,997号、米国特許第5,866,757号、米国特許第5,849,991号、米国特許第5,821,117号、米国特許第5,807,737号、米国特許第5,752,929号、米国特許第5,709,843号、米国特許第5,672,346号、米国特許第5,652,373号、米国特許第5,643,746号、米国特許第5,639,939号、米国特許第5,633,426号、米国特許第5,625,127号、米国特許第5,599,659号、米国特許第5,589,362号、米国特許第5,586,438号、米国特許第5,556,954; 号、米国特許第5,523,226号、米国特許第5,498,427号、米国特許第5,494,822号、米国特許第5,476,997号、米国特許第5,418,147号、米国特許第5,416,260号、米国特許第5,362,622号、米国特許第5,326,706号、米国特許第4,837,390号、米国特許第4,745,759号、および米国特許第4,186,565号。
この開示のどこかで引用または引用されていないかもしれない以下の米国特許出願公開は、全体を本明細書中に援用する。米国特許出願公開第20050268347号(特許出願第10/857,613号)、米国特許出願公開第20050266561号(米国特許出願第10/996,217号)、米国特許出願公開第20050265995号(米国特許出願第11/116,939号)、米国特許出願公開第20050223418 (米国特許出願第10/863,116号)、米国特許出願公開第20050201990号(米国特許出願第11/076,668号)、米国特許出願公開第20050177883号(米国特許出願第10/470,785号)、米国特許出願公開第20050176139号(米国特許出願第11/032,153号)、米国特許出願公開第20050170452号(米国特許出願第10/500,240号)、米国特許出願公開第米国特許出願公開番号第. 20050164210号(米国特許出願第10/ 763,479号)、米国特許出願公開第20050155095号(米国特許出願第10/981,935号)、米国特許出願公開第20050155094号(米国特許出願第10/503,464号)、米国特許出願公開第20050148072号(米国特許出願第10/944,919号)、米国特許出願公開第20050142121号(米国特許出願第10/949,411号)、米国特許出願公開第20050125853号(米国特許出願第10/505,760号)、米国特許出願公開第20050120400号(米国特許出願第10/499,407号)、米国特許出願公開第20050112122号(米国特許出願第10/933,933号)、米国特許出願公開第20050108783号(米国特許出願第10/947,920号)、米国特許出願公開第20050108780号(米国特許出願第10/894,194号)、米国特許出願公開第20050076399号(米国特許出願第10/500,748号)、米国特許出願公開第20050028230号(米国特許出願第10/843,038号)、米国特許出願公開第20040268424号(米国特許出願第10/646,970号)、米国特許出願公開第20040258669号(米国特許出願第10/701,789号)、米国特許出願公開第20040209357号(米国特許出願第10/769,686号)、米国特許出願公開第20040191228号(米国特許出願第10/487,944号)、米国特許出願公開第20040180041 (Ser. No 10/809,556号)、米国特許出願公開第20040171824号(米国特許出願第10/469,881号)、米国特許出願公開第20040171155号(米国特許出願第10/762,888号)、米国特許出願公開第20040171138号(米国特許出願第10/640,867号)、米国特許出願公開第20040136972号(米国特許出願第10/759,033号)、米国特許出願公開第20040110286号(米国特許出願第10/ 313,195号)、米国特許出願公開第20040073963号(米国特許出願第10/362,429号)、米国特許出願公開第20030224350号(米国特許出願第10/113,664号)、米国特許出願公開第20030211098号(米国特許出願第10/181,896号)、米国特許出願公開第20030206891号(米国特許出願第10/341,967号)、米国特許出願公開第20030203427号(米国特許出願第10/125,994号)、米国特許出願公開第20030165480号(米国特許出願第10/135,919号)、米国特許出願公開第20030147859号(米国特許出願第09/881,721号)、米国特許出願公開第20030131365号(米国特許出願第10/172,459号)、米国特許出願公開第20030115616号(米国特許出願第10/243,087号)、米国特許出願公開第20030096410号(米国特許出願第09/ 178036号)、米国特許出願公開第20030092174号(米国特許出願第10/147,286号)、米国特許出願公開第20030086909号(米国特許出願第09/222,460号)、米国特許出願公開第20030068818号(米国特許出願第10/105,963号)、米国特許出願公開第20030068818号(米国特許出願第10/105,963号)、米国特許出願公開第20030049235号(米国特許出願第09/477,737号)、米国特許出願公開第20030014770号(米国特許出願第10/098,276号)、米国特許出願公開第20030068308号(米国特許出願第10/132,443号)、米国特許出願公開第20030003574号(米国特許出願第10/099,539号)、米国特許出願公開第20030003083号(米国特許出願第10/169,028号)、米国特許出願公開第20030198628号(米国特許出願第10/ 395,552号)、米国特許出願公開第20020197240号(米国特許出願第10/146,092号)、米国特許出願公開第20020187972号(米国特許出願第09/949,278号)、米国特許出願公開第20020164571号(米国特許出願第09/798,790号)、米国特許出願公開第20020100065号(米国特許出願第09/895,895号)、米国特許出願公開第20020090370号(米国特許出願第09/753,007号)、米国特許出願公開第20020031494号(米国特許出願第10/254,077号)、米国特許出願公開第20010053362号(米国特許出願第09/802,350号)、および米国特許出願公開第20010049139号(米国特許出願第08/ 816,750号)。
さらに、以下の国際特許出願公開および該国際特許出願公開に関連する米国特許出願を各々その全体を本明細書中に援用する。PCT/US2004/018106および米国特許仮出願第60/476,396号(優先権主張の基礎をなす)の国際特許出願公開第WO 2004/108904 A2号、PCT/US2003/029251、米国特許仮出願第60/411,790号(優先権主張の基礎をなす)、米国国内段階第10/527,587号の国際特許出願公開第WO2004/027029A2号、ならびにPCT/US2003/025199および米国特許仮出願第60/403,405号(優先権主張の基礎をなす)の国際特許出願公開第WO2004/016742A2号)。
理解すべきことは、この開示に述べられる実施形態および実施例は、本発明の種々の態様の例示を意図しており、その範囲を限定するものではない。本発明の精神および範囲内にある多くの実施形態および変形例はこの開示を検討することで当業者にとって明らかであろうことである。
Claims (25)
- 置換細胞によってドナー器官または組織を再構成する方法であって、
ヒトまたは非ヒト哺乳動物ドナーから固形器官または固形組織あるいはその一固形部分を、該ドナー器官または組織あるいはその一部を生きた状態で維持する非ヒト哺乳動物宿主に、移植するステップであり、前記ドナー器官または組織の少なくとも一部の細胞が、前記宿主細胞および前記置換細胞と比較して、少なくとも実質的に選択的に殺害可能である、ステップと、
前記ドナー器官または組織あるいはその一部を前記宿主に移植した後に、前記ドナー器官または組織あるいはその一部の内因性ドナー細胞の少なくとも一部を選択的に殺害するステップと、
前記ドナー器官または組織あるいはその一部に置換細胞を導入して、前記移植された器官または組織あるいはその一部の内因性ドナー細胞と置き換えるステップと、を含み、
前記内因性ドナー細胞の少なくとも一部を選択的に殺害するステップは、前記置換細胞による前記ドナー細胞の置換を促進する、前記方法。 - 前記ドナー器官または組織が、広範囲活性プロモーターの制御下にあるネガティブ選択マーカー遺伝子を有することで、1セットの1つ以上の条件に反応して選択的に殺害可能である前記ドナー器官または組織の細胞型が少なくともかなりの割合を占めるようにし、
前記非ヒト宿主哺乳動物の細胞と置換細胞とが、前記ドナー細胞を殺害する前記1セットの1つ以上の条件に反応して実質的に殺害可能ではなく、ならびに、
少なくとも一部のドナー細胞を選択的に殺害するステップが1セットの1つ以上の条件の適用を含む、請求項1に記載の方法。 - 前記ネガティブ選択マーカー遺伝子が自殺遺伝子である、請求項2に記載の方法。
- 前記ドナー器官または組織へ置換細胞を導入するステップが、
前記ドナー器官または組織あるいはその一部を前記宿主に移植する前に、前記置換細胞を導入することを含む、請求項1に記載の方法。 - 前記置換細胞を前記ドナー器官または組織あるいはその一部に導入するステップが、
前記ドナー器官または組織あるいはその一部を前記ドナー哺乳動物から取り除く前に、前記置換細胞を前記ドナー器官または組織に導入することを含む、請求項4に記載の方法。 - 前記ドナーが非ヒト哺乳類動物である、請求項4に記載の方法。
- 前記置換細胞を前記ドナー器官または組織に導入するステップが、
前記固形器官または固形組織あるいはその一固形部分が、非ヒト宿主哺乳動物に対する移植ためのドナーから除去される前に、それに既に取り込まれた置換細胞を含むように、成長における胎児または新生児段階の過程で幹細胞を前記ドナー哺乳動物に導入するものである、請求項6に記載の方法。 - 前記置換細胞を前記ドナー器官または組織に導入するステップが、
前記ドナー器官または組織あるいはその一部を前記宿主に移植した後に、前記置換細胞を移植することを含む、請求項1に記載の方法。 - 前記ドナー動物が非ヒト哺乳動物である、請求項8に記載の方法。
- 前記置換細胞がヒト細胞を含む、請求項1に記載の方法。
- 前記置換細胞が本質的にヒト細胞からなる、請求項10に記載の方法。
- 前記器官または組織が腎臓、肺、心臓、肝臓、および膵臓からなる群から選択される、請求項1に記載の方法。
- 前記置換細胞がヒト細胞を含む、請求項12に記載の方法。
- ドナー器官または組織を置換細胞によって再構成する方法であって、
ヒトまたは非ヒト哺乳動物ドナーから固形器官または固形組織あるいはその一固形部分を、該ドナー器官または組織あるいはその一部を生きた状態で維持する非ヒト哺乳動物宿主に移植するステップであり、前記ドナー器官または組織の少なくとも一部の細胞の成長が、1セットの1つ以上の条件に反応して選択的に阻害可能であり、および宿主細胞の内因性細胞の成長が、1セットの1つ以上の条件によって実質的に阻害可能でない、ステップと、
前記ドナー器官または組織の細胞の少なくとも一部分の成長を、前記1セットの1つ以上の条件を提供することによって前記宿主に前記器官または組織が移植された後に、選択的に阻害するステップと、
ヒト置換細胞を前記ドナー器官または組織に導入するステップとを含み、
前記置換細胞の成長が、前記1セットの1つ以上の条件によって実質的に阻害可能ではない、前記方法。 - 前記ヒト置換細胞を前記ドナー器官または組織に導入するステップが、前記器官または組織あるいはその一部を前記宿主に移植する前に、前記置換細胞を導入することを含む、請求項14の方法。
- 非ヒト動物によって維持される事前選択された器官または組織あるいはその一部に形質が限定される前記非ヒト動物を提供する方法であって、
ヒト・ドナーまたは非ヒト動物ドナーから事前選択された固形器官または固形組織あるいはその一固形部分を、該固形器官または固形組織あるいはその一固形部分が生きた状態で維持される非ヒト動物宿主に移植するステップを含み、
移植されたドナー固形器官または固形組織あるいはその一固形部分の内因性細胞型の少なくとも一部は、所望の形質を持ち、
前記宿主動物の内因性細胞は、少なくとも実質的に前記形質を持たない、前記方法。 - 前記形質が、ネガティブ選択マーカーの誘導性または構成的または発生的に調節された発現を含む、請求項16に記載の方法。
- 前記形質が、1セットの一つ以上の既知の条件に反応した細胞死または成長阻害に対する感受性を含む、請求項16に記載の方法。
- 前記形質が、事前選択された導入遺伝子の誘導性または構成性または発生的に調節された発現を含む、請求項16に記載の方法。
- 前記導入遺伝子の発現が、広範囲活性プロモーターの制御下にある、請求項19に記載の方法。
- 前記事前選択された導入遺伝子が、事前選択された自殺遺伝子または事前選択された成長阻害遺伝子である、請求項19に記載の方法。
- 前記ドナーおよび宿主が、同一種の非ヒト動物である、請求項16に記載の方法。
- 前記ドナーおよび宿主が、同一種の非ヒト哺乳動物である、請求項22に記載の方法。
- 置換細胞によって器官または組織を再構成する方法であって、
ネガティブ選択マーカーまたは成長阻害形質の器官または組織特異的発現に関してヘテロ接合またはホモ接合である少なくとも1つの非ヒト哺乳動物胚または胎児を提供するステップと、
少なくとも実質的には前記ネガティブ選択マーカーを発現しない同一または異なる種の代理母動物に対して前記少なくとも1つの胚または胎児を移入することで、前記移入された胚または胎児を、代理母により生きた状態で維持し、前記代理母の体内で成長を続けさせる、ステップと、
置換細胞を、前記代理母動物に対する移入の前または後に前記胎児に移入、あるいは前記移入された胚から成長する胎児に移入するステップと、
前記移入された胎児または前記移入された胚から成長する前記胎児の器官または組織の細胞の少なくとも一部を、実質的に代理母の対応する細胞を害することなく、選択的に殺害または成長阻害を与えることで、前記置換細胞で前記胎児の器官または組織集団を高めるステップと、を含み、
前記選択的殺害または成長阻害が、前記ネガティブ選択マーカーまたは成長阻害形質に、少なくとも部分的にもとづいている、前記方法。 - 前記置換細胞がヒト細胞を含む、請求項24に記載の方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US64044504P | 2004-12-30 | 2004-12-30 | |
| US11/162,715 US20060148080A1 (en) | 2004-12-30 | 2005-09-20 | Methods for supporting and producing human cells and tissues in non-human mammal hosts |
| US59700905P | 2005-11-03 | 2005-11-03 | |
| US11/306,414 US20060147429A1 (en) | 2004-12-30 | 2005-12-27 | Facilitated cellular reconstitution of organs and tissues |
| PCT/US2005/047291 WO2006074012A2 (en) | 2004-12-30 | 2005-12-29 | Facilitated cellular reconstitution of organs and tissues |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008526318A true JP2008526318A (ja) | 2008-07-24 |
| JP2008526318A5 JP2008526318A5 (ja) | 2009-02-12 |
Family
ID=36648050
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007549596A Pending JP2008526318A (ja) | 2004-12-30 | 2005-12-29 | 器官および組織の細胞再形成促進 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20060147429A1 (ja) |
| EP (1) | EP1855534A4 (ja) |
| JP (1) | JP2008526318A (ja) |
| AU (1) | AU2005322907A1 (ja) |
| CA (1) | CA2592574A1 (ja) |
| WO (1) | WO2006074012A2 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9388427B2 (en) * | 2002-12-02 | 2016-07-12 | Biovec, Llc | In vivo and ex vivo gene transfer into renal tissue using gutless adenovirus vectors |
| US7687265B2 (en) * | 2003-11-25 | 2010-03-30 | The General Hospital Corporation | Foxn1 and pigmentation |
| US20070033666A1 (en) * | 2005-06-24 | 2007-02-08 | Harris Reuben S | Using cytosine deaminases to diminish retroelement transfer from pigs to humans |
| US20100115640A1 (en) * | 2007-03-09 | 2010-05-06 | The Curators Of The University Of Missouri | Methods for Conditional and Inducible Transgene Espression to Direct the Development of Embryonic, Embryonic Stem, Precursor and Induced Pluripotent Stem Cells |
| JP5771147B2 (ja) * | 2008-09-26 | 2015-08-26 | トカジェン インコーポレーテッド | 遺伝子治療ベクターおよびシトシンデアミナーゼ |
| US20110076303A1 (en) * | 2009-06-25 | 2011-03-31 | Tokuro Iwabuchi | Methods for Screening for Anti-Graying Agents on the Basis of AFF-4 |
| JP6396909B2 (ja) * | 2012-09-29 | 2018-09-26 | ノーティス,インク. | インビトロで組織及び器官の機能単位を再現するためのマイクロ流体システム |
| WO2014066700A1 (en) | 2012-10-25 | 2014-05-01 | Tocagen Inc. | Retroviral vector with mini-promoter cassette |
| WO2014151423A1 (en) * | 2013-03-15 | 2014-09-25 | Newlink Genetics Corporation | Carbohydrate-modified glycoproteins and uses thereof |
| US11559605B2 (en) * | 2016-06-29 | 2023-01-24 | Takashi Yokoo | Kidney production method |
| KR102525607B1 (ko) * | 2016-06-29 | 2023-04-25 | 다카시 요코오 | 신장의 제조 방법 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003507131A (ja) * | 1999-08-26 | 2003-02-25 | アブソーバー アクチボラゲット | 非ヒト移植片の免疫原性の低下 |
| JP2003512846A (ja) * | 1999-11-02 | 2003-04-08 | ユニバーシティ オブ コネチカット | ヒト以外の動物におけるヒト肝細胞の増殖 |
| JP2003521461A (ja) * | 1998-12-09 | 2003-07-15 | ラ ホヤ ファーマシューティカル カンパニー | ガラクトースα1,3ガラクトシルエピトープを含有する結合体およびそれを使用する方法 |
| WO2004027029A2 (en) * | 2002-09-19 | 2004-04-01 | Ximerex, Inc. | Growth of foreign cells in fetal animals facilitated by conditional and selective destruction of native host cells |
| JP2004533242A (ja) * | 2001-04-30 | 2004-11-04 | アールビーシー バイオテクノロジー, インコーポレイテッド | 異種移植のための改変された器官および細胞 |
Family Cites Families (93)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4186565A (en) * | 1978-05-19 | 1980-02-05 | Henry Ford Hospital | Perfusion system for organ preservation |
| US4837390A (en) * | 1983-05-11 | 1989-06-06 | Keyes Offshore, Inc. | Hyperbaric organ preservation apparatus and method for preserving living organs |
| US4745759A (en) * | 1986-12-23 | 1988-05-24 | Bauer Dan O | Kidney preservation machine |
| US5639939A (en) * | 1987-12-23 | 1997-06-17 | The Board Of Trustees For The Leland Stanford Junior University | Chimeric immunocompromised mammal comprosing vascularized fetal organ tissue |
| US6677311B1 (en) * | 1988-07-20 | 2004-01-13 | The Salk Institute For Biological Studies | Inducible HSV-TK in transformed cell populations |
| US6093872A (en) * | 1989-05-05 | 2000-07-25 | Systemix, Inc. | Extended human hematopoiesis in a heterologous host |
| US5326706A (en) * | 1989-07-17 | 1994-07-05 | Research Foundation Of State University Of New York | Homeostatic organ preservation system |
| US5574205A (en) * | 1989-07-25 | 1996-11-12 | Cell Genesys | Homologous recombination for universal donor cells and chimeric mammalian hosts |
| DE69034263D1 (de) * | 1989-07-25 | 2009-04-02 | Cell Genesys Inc | Homologe Rekombination für universelle Donorzellen und chimerische Säugetierzellen |
| US5434341A (en) * | 1989-08-17 | 1995-07-18 | Systemix, Inc. | Xenogeneic lymph node in mammary fat pad |
| US5652373A (en) * | 1990-01-15 | 1997-07-29 | Yeda Research And Development Co. Ltd. | Engraftment and development of xenogeneic cells in normal mammals having reconstituted hematopoetic deficient immune systems |
| US5633426A (en) * | 1990-05-25 | 1997-05-27 | Systemix, Inc. | In vivo use of human bone marrow for investigation and production |
| EP0477739A3 (en) * | 1990-09-27 | 1992-12-09 | F. Hoffmann-La Roche Ag | Glycosyl-phosphatidylinositol-specific phospholipase d |
| US5584804A (en) * | 1990-10-10 | 1996-12-17 | Life Resuscitation Technologies, Inc. | Brain resuscitation and organ preservation device and method for performing the same |
| US5498427A (en) * | 1990-11-20 | 1996-03-12 | Pasteur Merieux Serums Et Vaccines | Solutions for the perfusion, preservation and reperfusion of organs |
| US6503277B2 (en) * | 1991-08-12 | 2003-01-07 | Peter M. Bonutti | Method of transplanting human body tissue |
| US6353150B1 (en) * | 1991-11-22 | 2002-03-05 | Hsc Research And Development Limited Partnership | Chimeric mammals with human hematopoietic cells |
| US5858354A (en) * | 1991-12-06 | 1999-01-12 | The Trustees Of The University Of Pennsylvania | Repopulation of testicular Seminiferous tubules with foreign cells, corresponding resultant germ cells, and corresponding resultant animals and progeny |
| WO1993015209A1 (en) * | 1992-01-23 | 1993-08-05 | Research Corporation Technologies, Inc. | Human epidermal gene promoter |
| US6911220B1 (en) * | 1992-02-19 | 2005-06-28 | The General Hospital Corporation | Allogeneic and xenogeneic transplantation |
| US5866757A (en) * | 1992-06-02 | 1999-02-02 | Yeda Research And Development Co. Ltd. | Engraftment and development of xenogeneic cells in normal mammals having reconstituted hematopoetic deficient immune systems |
| US5338662A (en) * | 1992-09-21 | 1994-08-16 | Bio-Preserve Medical Corporation | Organ perfusion device |
| IL108422A (en) * | 1993-02-05 | 1998-10-30 | Yeda Res & Dev | A method for assessing pathology caused by bacterial toxins in humans using a non-human animal as a model |
| US5599659A (en) * | 1993-03-11 | 1997-02-04 | Breonics, Inc. | Preservation solution for ex vivo, warm preservation of tissues, explants,organs and vascular endothelial cells comprising retinal-derived fibroblast growth factor, cyclodextrin and chondroitin sulfate |
| US20040071637A1 (en) * | 1993-04-27 | 2004-04-15 | Elia James P. | Method for repairing a damaged portion of a human organ |
| US6018096A (en) * | 1993-05-03 | 2000-01-25 | Surrogen, Inc. | Animal model for engraftment, proliferation and differentiation of human hematopoietic stem cells |
| US5523226A (en) * | 1993-05-14 | 1996-06-04 | Biotechnology Research And Development Corp. | Transgenic swine compositions and methods |
| ATE221382T1 (de) * | 1993-05-24 | 2002-08-15 | Ximerex Inc | Die erzeugung von toleranz gegen fremdtransplantate durch tolerogenese mit hilfe von ersatzlebewesen |
| US6680305B1 (en) * | 1993-06-04 | 2004-01-20 | Biotime, Inc. | Physiologically acceptable aqueous solutions and methods for their use |
| US5945272A (en) * | 1993-06-04 | 1999-08-31 | Biotime, Incorporated | Plasma expanders and blood substitutes |
| US5859310A (en) * | 1993-06-14 | 1999-01-12 | Basf Aktiengesellschaft | Mice transgenic for a tetracycline-controlled transcriptional activator |
| US5912411A (en) * | 1993-06-14 | 1999-06-15 | University Of Heidelberg | Mice transgenic for a tetracycline-inducible transcriptional activator |
| EP0755402B1 (en) * | 1994-04-13 | 2008-05-14 | Biotransplant, Inc | Alpha(1,3) galactosyltransferase negative swine |
| US5871997A (en) * | 1994-07-21 | 1999-02-16 | Alexion Pharmaceuticals, Inc. | Methods and compositions for protecting retroviral vector particles and producer cells from inactivation by complement via reduction of the expression or recognition of galactose alpha (1,3) galactosyl epitopes |
| US5925802A (en) * | 1995-06-07 | 1999-07-20 | Estes; Don Mark | Functional reconstitution of SCID-bo mice with bovine fetal hematopoietic tissues |
| US6046379A (en) * | 1995-06-07 | 2000-04-04 | Stone; Kevin R. | Meniscal xenografts |
| US6187757B1 (en) * | 1995-06-07 | 2001-02-13 | Ariad Pharmaceuticals, Inc. | Regulation of biological events using novel compounds |
| US6030833A (en) * | 1995-08-04 | 2000-02-29 | The General Hospital | Transgenic swine and swine cells having human HLA genes |
| AU4353696A (en) * | 1996-01-09 | 1997-08-01 | Regents Of The University Of California, The | Ungulate embryonic stem-like cells, making and using the cells to produce transgenic ungulate |
| US6006752A (en) * | 1996-05-09 | 1999-12-28 | The General Hospital Corporation | Mixed chimerism and tolerance |
| ATE314466T1 (de) * | 1996-05-17 | 2006-01-15 | Nippon Meat Packers | Promotoren von komplementinhibitoren des schweines. |
| AUPO182396A0 (en) * | 1996-08-23 | 1996-09-12 | Austin Research Institute, The | Improved nucleic acids for reducing carbohydrate epitopes |
| US6547826B2 (en) * | 1996-09-03 | 2003-04-15 | Maulana Azad Medical College | Method of organogenesis and tissue regeneration/repair using surgical techniques |
| US5837837A (en) * | 1997-02-27 | 1998-11-17 | Millennium Pharmaceuticals, Inc. | Nucleic acids molecules encoding Caspase-8h and Caspase-8i |
| US6331406B1 (en) * | 1997-03-31 | 2001-12-18 | The John Hopkins University School Of Medicine | Human enbryonic germ cell and methods of use |
| US6090622A (en) * | 1997-03-31 | 2000-07-18 | The Johns Hopkins School Of Medicine | Human embryonic pluripotent germ cells |
| US20010007153A1 (en) * | 1997-06-16 | 2001-07-05 | Jennifer June Brown | Solid chimeric organs, animal models having same, process for preparing same, non-tumorigenic immortalized human cell lines, susceptible cells and cytopathic mammalian viruses |
| US6521448B1 (en) * | 1997-08-19 | 2003-02-18 | Diacrin, Inc. | Porcine MHC class I genes and uses thereof |
| US6100082A (en) * | 1997-09-23 | 2000-08-08 | Hassanein; Waleed H. | Perfusion apparatus and method including chemical compositions for maintaining an organ |
| US6699231B1 (en) * | 1997-12-31 | 2004-03-02 | Heartport, Inc. | Methods and apparatus for perfusion of isolated tissue structure |
| US7074762B2 (en) * | 1998-01-05 | 2006-07-11 | Washington University | Composition and method for improving function of embryonic kidney transplants |
| US6342344B1 (en) * | 1998-07-31 | 2002-01-29 | Stemcell Technologies Inc. | Antibody composition for isolating human cells from human-murine chimeric hematopoietic cell suspensions |
| US6673594B1 (en) * | 1998-09-29 | 2004-01-06 | Organ Recovery Systems | Apparatus and method for maintaining and/or restoring viability of organs |
| FR2785501B1 (fr) * | 1998-11-10 | 2001-01-05 | Centre Nat Rech Scient | Solution de perfusion et/ou de conservation et/ou de reperfusion lors de la transplantation d'organes |
| US6700037B2 (en) * | 1998-11-24 | 2004-03-02 | Infigen, Inc. | Method of cloning porcine animals |
| US6258998B1 (en) * | 1998-11-24 | 2001-07-10 | Infigen, Inc. | Method of cloning porcine animals |
| US20040038193A1 (en) * | 1999-04-14 | 2004-02-26 | Breonics, Inc. | System for exsanguinous metabolic support of an organ or tissue |
| US6582953B2 (en) * | 1999-04-14 | 2003-06-24 | Breonics, Inc. | Organ chamber for exsanguinous metabolic support system |
| US20040038192A1 (en) * | 1999-04-14 | 2004-02-26 | Breonics, Inc. | System for exsanguinous metabolic support of an organ or tissue |
| US6365338B1 (en) * | 1999-04-27 | 2002-04-02 | David A. Bull | Organ preservative solution containing trehalose, anti-oxidant, cations and an energy source |
| JP2001086989A (ja) * | 1999-09-17 | 2001-04-03 | Univ Osaka | 哺乳類型Creリコンビナーゼ遺伝子 |
| US6995299B2 (en) * | 1999-11-02 | 2006-02-07 | University Of Connecticut | Propagation of human hepatocytes in non-human animals |
| AUPQ488499A0 (en) * | 1999-12-24 | 2000-02-03 | Commonwealth Scientific And Industrial Research Organisation | Repressible sterility of animals |
| US6544506B2 (en) * | 2000-01-05 | 2003-04-08 | Yeda Research & Development Co. Ltd. | Veto cells effective in preventing graft rejection and devoid of graft versus host potential |
| US7544509B2 (en) * | 2000-01-24 | 2009-06-09 | Mcgill University | Method for preparing stem cell preparations |
| US6509514B1 (en) * | 2000-03-17 | 2003-01-21 | Kmt Hepatech, Inc. | Chimeric animal model susceptible to human hepatitis C virus infection |
| GB2360522A (en) * | 2000-03-24 | 2001-09-26 | Geron Corp | A strategy for maintaining pregnancy |
| WO2001083731A1 (en) * | 2000-05-04 | 2001-11-08 | Biotime, Inc. | Methods and compositions for producing donor cells |
| US7485769B2 (en) * | 2000-08-25 | 2009-02-03 | Nippon Meat Packers, Inc. | Transgenic mammals |
| US6391606B1 (en) * | 2000-09-14 | 2002-05-21 | Pe Corporation | Isolated human phospholipase proteins, nucleic acid molecules encoding human phospholipase proteins, and uses thereof |
| EP1323821A4 (en) * | 2000-09-14 | 2005-01-12 | Atsushi Yuki | METHOD FOR THE PRODUCTION OF NORMAL PARENCHYM CELLS, TISSUE OR ORGANS WITH A BIO INCUBATOR |
| US6576464B2 (en) * | 2000-11-27 | 2003-06-10 | Geron Corporation | Methods for providing differentiated stem cells |
| US6696074B2 (en) * | 2000-12-04 | 2004-02-24 | Tei Biosciences, Inc. | Processing fetal or neo-natal tissue to produce a scaffold for tissue engineering |
| AU2002251935B2 (en) * | 2001-02-14 | 2007-11-29 | Celularity Inc. | Post-partum mammalian placenta, its use and placental stem cells therefrom |
| US7126039B2 (en) * | 2001-03-21 | 2006-10-24 | Geron Corporation | Animal tissue with carbohydrate antigens compatible for human transplantation |
| WO2002092791A1 (en) * | 2001-05-14 | 2002-11-21 | Stell | Tissues or organs for use in xenotransplantation |
| US20020182261A1 (en) * | 2001-05-31 | 2002-12-05 | Jianwu Dai | EB matrix production from fetal tissues and its use for tissue repair |
| US6972195B2 (en) * | 2002-09-27 | 2005-12-06 | Rongxiang Xu | Composition and method for culturing potentially regenerative cells and functional tissue-organs in vitro |
| US6677150B2 (en) * | 2001-09-14 | 2004-01-13 | Organ Transport Systems, Inc. | Organ preservation apparatus and methods |
| US20030068308A1 (en) * | 2001-10-09 | 2003-04-10 | Jacek Rozga | Intrasplenic encapsulated cell therapy |
| US20030096410A1 (en) * | 2001-11-19 | 2003-05-22 | Fanyi Zeng | Methodology for constructing human / goat chimeras for the production of human cells |
| AU2002364596A1 (en) * | 2001-12-21 | 2003-07-15 | Immerge Biotherapeutics, Inc. | Knockout swine and methods for making the same |
| CN1582332A (zh) * | 2001-12-29 | 2005-02-16 | Seoul大学校产学协力财团 | 转染gfp的克隆猪、敲除gt的克隆猪及其生产方法 |
| US20050108780A1 (en) * | 2002-01-24 | 2005-05-19 | Erasmus University | Intracellular antibodies for a retrovirus protein |
| AU2003213813A1 (en) * | 2002-03-22 | 2003-10-13 | St. Jude Children's Research Hospital | Improved method for generating genetically modified animals |
| US20060110375A1 (en) * | 2002-08-09 | 2006-05-25 | Herbert Zech | Method for producing cell lines and organs by means of differentiable cells |
| KR20050086606A (ko) * | 2002-11-15 | 2005-08-30 | 가부시키가이샤 상가쿠렌케이키코큐슈 | 장기의 재생 방법 |
| US20040110286A1 (en) * | 2002-12-06 | 2004-06-10 | The John P. Robarts Research Institute | Method for making hematopoietic cells |
| AU2004256021A1 (en) * | 2003-05-09 | 2005-01-20 | University Of Massachusetts | Non-human animals expressing heterologous complement receptor type 1 (CR1) molecules on erythrocytes and uses therefor |
| WO2005021734A2 (en) * | 2003-09-02 | 2005-03-10 | University Of Massachussets | Generation of hematopoietic chimerism and induction of central tolerance |
| US20050108783A1 (en) * | 2003-09-23 | 2005-05-19 | Chihiro Koike | Porcine invariant chain protein, full length cDNA, genomic organization, and regulatory region |
| US20050142121A1 (en) * | 2003-12-24 | 2005-06-30 | Gold Joseph D. | System for improving acceptance of tissue grafts made from embryonic stem cells |
| US20060008451A1 (en) * | 2004-07-06 | 2006-01-12 | Michigan State University | In vivo methods for effecting tissue specific differentiation of embryonic stem cells |
-
2005
- 2005-12-27 US US11/306,414 patent/US20060147429A1/en not_active Abandoned
- 2005-12-29 EP EP05855792A patent/EP1855534A4/en not_active Withdrawn
- 2005-12-29 JP JP2007549596A patent/JP2008526318A/ja active Pending
- 2005-12-29 WO PCT/US2005/047291 patent/WO2006074012A2/en active Application Filing
- 2005-12-29 AU AU2005322907A patent/AU2005322907A1/en not_active Abandoned
- 2005-12-29 CA CA002592574A patent/CA2592574A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003521461A (ja) * | 1998-12-09 | 2003-07-15 | ラ ホヤ ファーマシューティカル カンパニー | ガラクトースα1,3ガラクトシルエピトープを含有する結合体およびそれを使用する方法 |
| JP2003507131A (ja) * | 1999-08-26 | 2003-02-25 | アブソーバー アクチボラゲット | 非ヒト移植片の免疫原性の低下 |
| JP2003512846A (ja) * | 1999-11-02 | 2003-04-08 | ユニバーシティ オブ コネチカット | ヒト以外の動物におけるヒト肝細胞の増殖 |
| JP2004533242A (ja) * | 2001-04-30 | 2004-11-04 | アールビーシー バイオテクノロジー, インコーポレイテッド | 異種移植のための改変された器官および細胞 |
| WO2004027029A2 (en) * | 2002-09-19 | 2004-04-01 | Ximerex, Inc. | Growth of foreign cells in fetal animals facilitated by conditional and selective destruction of native host cells |
Non-Patent Citations (3)
| Title |
|---|
| JPN6012022993; Graca Almeida-Porada et al.: 'Formation of human hepatocytes by human hematopoietic stem cells in sheep' Blood Vol. 104, 20040701, 2582-2590 * |
| JPN6012022996; W. Beschorner et al.: 'Transgenic pigs expressing the suicide gene thymidine kinase in the liver' Xenotransplantation Vol. 5, 20030901, 530 * |
| JPN6012022997; W. Beschoner et al.: 'Selective and Conditional Depletion of Pig Cells with Transgenic Pigs and Specific Liposomes' Xenotransplantation Vol. 10, No. 5, 20030901, 497 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1855534A2 (en) | 2007-11-21 |
| EP1855534A4 (en) | 2008-12-17 |
| AU2005322907A2 (en) | 2006-07-13 |
| CA2592574A1 (en) | 2006-07-13 |
| US20060147429A1 (en) | 2006-07-06 |
| AU2005322907A1 (en) | 2006-07-13 |
| WO2006074012A2 (en) | 2006-07-13 |
| WO2006074012A3 (en) | 2007-02-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008526318A (ja) | 器官および組織の細胞再形成促進 | |
| AU2010200016B2 (en) | Growth of foreign cells in fetal animals facilitated by conditional and selective destruction of native host cells | |
| US20150017130A1 (en) | Methods and compositions for inhibition of immune responses | |
| AU2002308533B2 (en) | Modified organs and cells for xenotransplantation | |
| JP2001517924A (ja) | 抗体媒介性拒絶反応を低減させた異種移植のためのトランスジェニック動物 | |
| Aigner et al. | Transgenic pigs for xenotransplantation: selection of promoter sequences for reliable transgene expression | |
| AU2002308533A1 (en) | Modified organs and cells for xenotransplantation | |
| US20070240235A1 (en) | Methods for supporting and producing human cells and tissues in non-human mammal hosts | |
| Murakami et al. | Transgenic pigs expressing human decay‐accelerating factor regulated by porcine MCP gene promoter | |
| US20170251646A1 (en) | Transgenic pigs lacking one or more cellular transport genes | |
| CN108024522A (zh) | Etv2及其用途 | |
| WO2002015681A1 (fr) | Mammiferes transgeniques | |
| EP1004238B1 (en) | Transgenic pigs | |
| JP4245332B2 (ja) | ヒト多発性骨髄腫の動物モデル | |
| AU671158B2 (en) | Delivery of proteins by intermembrane transfer for preaccommodation of xenogeneic organ transplants and other purposes | |
| WO2006113220A9 (en) | Transgenic mammals expressing human preproinsulin | |
| JP2001309783A (ja) | 遺伝子導入用mcp改変遺伝子 | |
| WO1996028966A1 (fr) | Transformant de mammifere autre que primate et dont un serotype de primate superieur s'exprime par transduction d'un gene etranger, procede de fabrication de ce transformant |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081219 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081219 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120508 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20121009 |