JP2007529199A - ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 - Google Patents
ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 Download PDFInfo
- Publication number
- JP2007529199A JP2007529199A JP2006536883A JP2006536883A JP2007529199A JP 2007529199 A JP2007529199 A JP 2007529199A JP 2006536883 A JP2006536883 A JP 2006536883A JP 2006536883 A JP2006536883 A JP 2006536883A JP 2007529199 A JP2007529199 A JP 2007529199A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- virus
- oas1
- polypeptide
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/70—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving virus or bacteriophage
- C12Q1/701—Specific hybridization probes
- C12Q1/706—Specific hybridization probes for hepatitis
- C12Q1/707—Specific hybridization probes for hepatitis non-A, non-B Hepatitis, excluding hepatitis D
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/45—Transferases (2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1137—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/12—Transferases (2.) transferring phosphorus containing groups, e.g. kinases (2.7)
- C12N9/1241—Nucleotidyltransferases (2.7.7)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6888—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for detection or identification of organisms
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/70—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving virus or bacteriophage
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/172—Haplotypes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Virology (AREA)
- Microbiology (AREA)
- Medicinal Chemistry (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Pathology (AREA)
- Gastroenterology & Hepatology (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Plant Pathology (AREA)
- Pulmonology (AREA)
- Obesity (AREA)
- Tropical Medicine & Parasitology (AREA)
Abstract
Description
本発明は、ヒトのオリゴアデニレートシンセターゼ遺伝子中の変異を検出するための方法(ここで、変異は、C型肝炎ウイルスによる感染を含む、フラビウイルス感染に対する抵抗性を与え、そして変異は、前立腺癌および糖尿病を含む、他の疾患の状態に関する)、ならびにそのコードされるタンパク質およびそれに対する抗体の使用に関する。
多くの疾患は、これまでに、ヒト集団において感染に対する自然抵抗性が存在するということについて同定されてきた。非特許文献1は、注射薬物使用者のような高危険率群において、90%程度高いC型肝炎ウイルス(HCV)感染率を報告する。しかし、残りの10%が、感染に対して明らかに抵抗性であることの機構は、この文献中には確認されなかった。HCV感染に関与するタンパク質としては、2’,5’オリゴアデニレートシンセターゼが挙げられる。OASは、アデノシンの2’,5’オリゴマー(2−5A)の合成を触媒するその能力によって特徴付けられるインターフェロン誘導性タンパク質である。非特許文献2は、インターフェロンで処理されたヒト細胞が、40kDのタンパク質(OAS1)、46kDのタンパク質(OAS1)、69kDのタンパク質、および100kDのタンパク質に対応する数種のOASを含むことを見出した。非特許文献3は、p69に対して高度に特異的なポリクロナール抗体である、69−kD OASを産生した。抗p69抗体を含む、インターフェロンで処理されたヒト細胞の発現ライブラリーをスクリーニングすることによって、非特許文献4は、部分的なOAS2 cDNAを単離した。この研究者らは、この部分的なcDNAを用いて、さらなるライブラリーをスクリーニングし、そして2つのOAS2アイソフォームをコードするcDNAを回収した。このより小さいアイソフォームは、3’非翻訳領域の長さが異なる2つのmRNAによってコードされる。
AlterおよびMoyer、「J.Acquir.Immune Defic.Syndr.Hum Retrovirol.」、1998年、18 補遺 1、S6−10 Hovanessianら、「EMBO」、1987年、6、1273−1280 Marieら、「Biochem.Biophys.Res.Commun.」、1989年、160、580−587 MarieおよびHovanessian、「J.Biol.Chem.」、1992年、267、9933−9939 Hovanianら、「Genomics」、1998年、52、267−277 Eskildsenら、「Nuc.Acids Res.」、2003年、31、3166−3173 Kakutaら、「J.Interferon & Cytokine Res.」、2002年、22、981−993
本発明は、オリゴアデニレートシンセターゼ1遺伝子中の点変異として特徴付けられる、C型肝炎耐性に関連する変異の検出に関する。
(導入および定義)
本発明は、オリゴアデニレートシンセターゼ遺伝子における新規な変異、ウイルス感染についての疑いの診断または、ウイルス感染に対する抵抗性の診断のためのこれらの変異の使用、本発明の変異を有する遺伝子によってコードされるタンパク質、ならびにこのタンパク質、抗体および関連する核酸を使用するウイルス感染の防御または阻害に関する。これらの変異は、フラビウイルス(特に、C型肝炎ウイルス)による感染に対するキャリアの抵抗性に相関する。
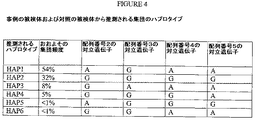
A:アデニン;C:シトシン;G:グアニン;T:チミン(DNAにおいて);およびU:ウラシル(RNAにおいて)。
本発明は、フラビウイルス(特に、C型肝炎ウイルス)による感染に対する抵抗性に関するオリゴアデニレートシンセターゼ対立遺伝子についてヒトをスクリーニングするための新規な方法を提供する。本発明は、このような抵抗性が、ヒトOAS1遺伝子をコードするGenbank登録番号NT_009775.13(配列番号19)の、ヌクレオチド位置2135728、2135749、2135978、2144072、2144088、2144116、2144321、2131025、2133961、2139587、2144294、2144985、2156523、2156595、または2156638におけるオリゴアデニレートシンセターゼ遺伝子のDNA配列中の点変異(塩基置換)に関するという発見に基づく。
オリゴアデニレートシンセターゼ遺伝子は、そのヌクレオチド配列が、オリゴアデニレートシンセターゼ、変異オリゴアデニレートシンセターゼ、またはオリゴアデニレートシンセターゼ偽遺伝子についてコードする核酸である。これは、ゲノムDNAの形態、mRNAの形態またはcDNAの形態であり得、そして1本鎖形態または2本鎖形態であり得る。mRNAと比較しての、生物学的試料におけるその相対的安定性に起因して、(好ましくは、ゲノムDNAが)用いられる。参照オリゴアデニレートシンセターゼ遺伝子の完全なゲノム配列の、連続したヌクレオチド2,130,000〜2,157,999からなるポリヌクレオチドの配列は、配列番号19として配列表中に提供され、そしてそれは、Genbank登録番号NT_009775.13に対応する。
プライマー、プローブおよびプライマー伸長によって合成される核酸フラグメントまたは核酸セグメントに関連して本明細書中で使用される場合、用語「ポリヌクレオチド」は、2つ以上の(好ましくは、3つより多い)デオキシリボヌクレオチドまたはリボヌクレオチドで構成される分子として定義される。その正確な大きさは、多くの要因に依存し、そして、最終的な使用条件に依存する。
オリゴアデニレートシンセターゼ遺伝子は、ポリヌクレオチドコード鎖(例えば、mRNAおよび/またはゲノムDNAのセンス鎖)で構成される。アッセイされるべき遺伝子物質が、2本鎖のゲノムDNAの形態である場合、それは通常、代表的に融解によって最初に一本鎖に変性される。この核酸は、この試料をPCRプライマー対(上記対の各メンバーは、前もって選択されたヌクレオチド配列を有する)とを処理する(接触させる)ことによってPCR反応に供される。このPCRプライマー対は、オリゴアデニレートシンセターゼ対立遺伝子内に保存されるヌクレオチド配列(好ましくは少なくとも約10ヌクレオチド長、より好ましくは少なくとも約20ヌクレオチド長)とハイブリダイズすることによってプライマー伸長反応を開始し得る。PCRプライマー対のこの第1のプライマーは、それが、核酸の非コード鎖またはアンチセンス鎖(すなわち、コード鎖に相補的な鎖)に対してハイブリダイズすることに起因して、ときとして本明細書中で「アンチセンスプライマー」と称される。PCRプライマー対のこの第2のプライマーは、それが、核酸のコード鎖またはセンス鎖に対してハイブリダイズすることに起因して、ときとして本明細書中で「センスプライマー」と称される。
核酸配列分析は、(a)プローブ鎖とその相補的な標的とのハイブリダイゼーションまたは変性に基づく生理化学的技術と、(b)エンドヌクレアーゼ、リガーゼおよびポリメラーゼによる酵素反応との組み合わせによって取り組まれる。核酸は、DNAレベルまたはRNAレベルにてアッセイされ得る。前者は、個々のヒトの遺伝子的可能性を分析し、そして後者は、特定の細胞の発現情報を分析する。
DNA(サザン)ブロット技術において、これまでに議論されたように、DNAは、PCR増幅によって調製される。このPCR産物(DNAフラグメント)は、アガロースゲル中で、大きさに従って分離され、そしてニトロセルロース膜またはナイロン膜上に移される(ブロットされる)。従来の電気泳動は、100塩基対〜30,000塩基対の範囲のフラグメントを分離するが、パルスフィールドゲル電気泳動は、2000万塩基対の長さまでのフラグメントを分離する。含まれる特定のPCR産物の膜上での配置は、特定の標識された核酸プローブを用いるハイブリダイゼーションによって決定される。
核酸の精製または核酸の固定を必要としない数種の迅速な技術が、開発されてきた。例えば、プローブ/標的ハイブリッドは、2本鎖核酸を優先的に結合するヒドロキシアパタイトのような固体マトリックス上で選択的に単離され得る。あるいは、プローブ核酸は、固体支持体に固定され、そして溶液から標的配列を捕捉するために使用され得る。標的配列の検出は、競合型アッセイにおいて標的配列によって上記支持体から動かされるか、またはサンドウィッチ型形式においてこの標的配列の架橋作用を介してその支持体に結合されるかのいずれかである第2の標識されたプローブの補助によって達成され得る。
3つの技術は、未知の1ヌクレオチド置換または他の配列の相違に関する数百塩基対の長さのプローブ/標的2重鎖の分析を可能にする。リボヌクレアーゼ(RNase)A技術において、この酵素は、標識されたRNAプローブが、標的RNA配列または標的DNA配列に対してミスマッチである位置にて、このプローブを切断する。このフラグメントは、変異のおおよその位置の決定を可能にする大きさにしたがって分離され得る。米国特許第4,946,773号を参照のこと。
OAS1遺伝子中の変異が、不完全なOAS1機能を生じ、そしてこの不完全な機能が、病原体の感染に対する患者の上昇した感受性に関連する場合、OAS1タンパク質の低レベル、その機能に影響を与えるタンパク質中の変異、または他の機構を介するか否かにかかわらず、それは、野生型OAS1タンパク質を有する患者を処置するのに有利である。
本発明はまた、OAS1ポリヌクレオチドの正常な機能と干渉するように設計されたアンチセンスオリゴヌクレオチドに関する。アンチセンス技術に広く適用できる当該分野において公知であるアンチセンス分子の、任意の修飾または改変は、本発明の範囲内に含まれる。このような修飾としては、米国特許第5,536,821号、同第5,541,306号、同第5,550,111号、同第5,563,253号、同第5,571,799号、同第5,587,361号、同第5,625,050号および同第5,958,773号に開示されるようなリン含有結合の調製が挙げられる。
OAS1インヒビターは、リボザイムであり得る。リボザイムは、RNA基質(例えば、mRNA)を特異的に切断し、細胞の遺伝子発現の特異的な阻害、または干渉を生じる。本明細書中で使用される場合、用語リボザイムとしては、特異的認識のためのアンチセンス配列、およびRNAを切断する酵素活性を含むRNA分子が挙げられる。この触媒的な鎖は、化学量論の濃度より大きい濃度にて、標的RNA中の特定の部位を切断する。
本発明はまた、部分的な2本鎖性質もしくは完全な2本鎖性質を有するRNAの、細胞または細胞外環境中への導入を提供する。阻害は、OAS1発現に対して特異的であり、ここで標的OAS1遺伝子の部分由来のヌクレオチド配列が阻害性のRNAを生成するために選択される。このプロセスは、(1)遺伝子発現の阻害を生じるのに有効であり、そして(2)標的化されたOAS1遺伝子に対して特異的である。この手順は、標的OAS1遺伝子に機能の部分的な喪失または完全な喪失を与える。少なくとも99%の、標的化された細胞における遺伝子発現の減少または喪失が、他の標的遺伝子を用いる同等の技術を使用して示された。より低い用量の注射用物質およびdsRNAの投与後のより長い時間は、より少ない部分の細胞における阻害を生じ得る。細胞中の遺伝子発現の定量化は、標的mRNAの蓄積のレベルまたは標的タンパク質の翻訳のレベルにおける、同様の量の阻害を示し得る。RNAiを調製する方法およびRNAiを使用する方法は概して、本明細書中に参考として援用される米国特許第6,506,559号に開示される。
本明細書中に開示されるアンチセンス分子およびリボザイムに加えて、本発明のOAS1インヒビターとしてはまた、OAS1遺伝子の発現を減少させるのに有効であるか、または1つ以上のOAS1の生物学的活性(酵素活性、1本鎖RNAとの相互作用、立体配置、およびC型肝炎ウイルスのNS5Aまたはそのフラグメントのような他のタンパク質との結合が挙げられるが、これらに限定されない)を減少させるのに有効な、タンパク質またはポリペプチドが挙げられる。当業者が、慣習的な実験を通じてこのようなOAS1インヒビターを迅速に同定し得る種々の方法は、当該分野で容易に利用できる。本発明は、以下の例示的な方法論に限定されない。
本発明はまた、ハイスループットスクリーニング(HTS)方法論の慣習的な適用を通じて容易に同定され得る、小分子OAS1インヒビターを提供する。Persidis,A.,Nature Biotechnology 16:488−89,1998年による総説。HTS法とは一般的に、リード化合物(例えば、小分子)の治療的可能性についての迅速なアッセイを可能にするこれらの技術を指す。HTS方法論は、試験物質陽性シグナルの検出およびデータの解析のロボット操作を利用する。このような方法論としては、例えば、可溶性分子ならびに上に詳細に記載される2−ハイブリッドシステムのような細胞に基づくシステムを使用するロボット利用のスクリーニング技術が挙げられる。
リード分子またはリード化合物(アンチセンス分子またはリボザイムであっても、タンパク質および/またはペプチドであっても、抗体および/または抗体フラグメントあるいは小分子であっても)は、本明細書に記載される方法の1つによってか、またはそうでなければ当該分野において利用可能な技術を介して、種々のインビトロ、エキソビボ、およびインビボの動物モデルアッセイシステム中で、これらのOAS1遺伝子発現を阻害する能力またはこれらの生物学的活性について、さらに特徴付けられ得る。以下に提供される実施例おいてさらに詳細に議論されるように、本発明のOAS1インヒビターは、OAS1の発現レベルを減少するのに有効である。したがって、本発明は、当業者に候補のインヒビターの効果を評価させる方法を、さらに開示する。
本発明のアンチセンスオリゴヌクレオチドおよびリボザイムは、リボヌクレオチドのヌクレオチドまたはデオキシリボヌクレオチドのヌクレオチドについて当該分野において公知である任意の方法によって合成され得る。例えば、このオリゴヌクレオチドは、Applied Biosystems 380B DNA合成機におけるような固相合成を使用して調製され得る。このオリゴヌクレオチドの最終的な純度は、当該分野において公知である通りに決定される。
上記の方法および当該分野において公知である他の方法を利用して、本発明は、増幅条件下で、オリゴアデニレートシンセターゼ(OAS1、配列番号19)のオリゴヌクレオチド(nt)位置2135728、2135749、2135978、2144072、2144088、2144116、2144321、2131025、2133961、2139587、2144294、2144985、2156523、2156595、または2156638のいずれかを含むヒトゲノムDNAの領域を増幅するためのPCRプライマー対によって、ヒトから単離されたゲノムDNAの試料を処理する工程を包含するスクリーニング方法を企図する。増幅条件としては、DNA合成のために有効な量のPCR緩衝液の存在、および温度循環の温度が挙げられる。したがって、このPCR産物は、関連するヌクレオチド位置における点変異の存在についてアッセイされる。1つの実施形態において、このPCR産物は、5’方向から3’方向に書き込まれた約358塩基対(bp)を含み、そして位置2135728(変異1)、2135749(変異2)、2135978(変異3)、2144072(変異4)、2144088(変異5)、2144116(変異6)、または2144321(変異7)および各側における位置に隣接する約175塩基を含む連続したヌクレオチド配列を含む。別の実施形態において、表1および表2における上記のような単位複製配列は、例示的なPCR産物および対応するプライマーである。
(ゲノムDNAの調製および予備的スクリーニング)
この実施例は、患者の2つの特定の集団から得たDNAのスクリーニングに関するが、HCVに対する度重なる曝露が実証され、ここでこの曝露は、感染を生じない他の患者群に対して等しく適用できる。この実施例はまた、上で議論されるような他のフラビウイルスに対して曝された患者のスクリーニングに関し、ここでこの曝露は、感染を生じなかった。
(HCV感染に対する抵抗性に関連するOAS1遺伝子中の変異)
実施例1に記載される方法を使用して、血友病患者および静脈内用薬物使用者に関係のない集団を研究し、そして配列番号1〜配列番号7および配列番号57〜配列番号64に開示されるようなOAS1における変異の存在または非存在を決定した。
(cDNAの調製および配列決定)
細胞の全RNAは、C型肝炎抵抗性の表現型を有する患者から得た、培養したリンパ芽球または培養した線維芽細胞から精製される。この精製手順は、Chomczynskiら,Anal.Biochem.,162:156−159(1987)に記載される通りに行われる。要約すると、この細胞は、実施例1に記載されるように調製される。その後、この細胞は、4.0Mのグアニジンチオシアネート、0.1MのTris−HCl(pH7.5)、および0.1Mのβ−メルカプトエタノールを含む10ミリリットル(ml)の変性溶液中でホモジェナイズされ、細胞溶解物を形成する。その後、ラウリルサルコシン酸ナトリウムは、0.5%の最終濃度になるまでこの細胞溶解物に混合され、その後この混合物を室温にて10分間、5000×gで遠心分離した。この得られた全RNAを含む上清は、5.7Mの塩化セシウムおよび0.01MのEDTA(pH7.5)のクッション上に重層され(layered)、そして遠心分離によってペレットにされる。この生じたRNAペレットは、10mMのTris−HCl(pH7.6)および0.1%のドデシル硫酸ナトリウム(SDS)を含む1mMのEDTA(TE)の溶液中に溶解される。フェノールクロロホルム抽出およびエタノール沈殿の後、この精製された細胞の全RNAの濃度は、260nmにおける吸光度を測定することによって見積もられる。
(点変異を含むPCRで増幅されたゲノムDNAの調製および対立遺伝子に特異的なオリゴヌクレオチドのハイブリダイゼーションによる検出)
ヌクレオチド位置2135728、2135749、2135978、2144072、2144088、2144116、2144321、2131025、2133961、2139587、2144294、2144985、2156523、2156595、または2156638の1つにおける、オリゴアデニレートシンセターゼ(OAS1)遺伝子中の点変異は、その変異を含むPCRで増幅されたゲノムDNAが、その領域に対してハイブリダイゼーションしたオリゴヌクレオチドプローブを用いたハイブリダイゼーションによって検出されるアプローチによって決定され得る。オリゴヌクレオチド特異的プローブを用いるハイブリダイゼーションについて、この点変異を有する領域を増幅するために、PCR増幅は、例えば、180ngの表1に示されるプライマーの各々を用いて、本質的に実施例3に記載される通りに行われる。
(標的RNAのアンチセンス阻害)
(A.トランスフェクションのためのオリゴヌクレオチドの調製)
リピトイド(lipitoid)またはコレステロイド(cholesteroid)のいずれかを含むキャリア分子は、トランスフェクションのために、水中に0.5mMになるまで希釈され、その後、均一な溶液を生成するために超音波処理され、そして0.45μmのPVDF膜を通して濾過されることによって調製される。その後、このリピトイドまたはコレステロイドは、最終濃度が、オリゴヌクレオチド1μgあたり約1.5〜2nmolリピトイドであるように、適切な量のOptiMEMTM(Gibco/BRL)中に希釈される。
HCV感染に対して感受性であり、かつHCV複製を支持するヒトPH5CH8肝細胞が使用される(Dansakoら,Virus Res.97:17−30,2003年;Ikedaら,Virus Res.56:157−167,1998年;NoguchiおよびHirohashi,In Vitro Cell Dev.Biol Anim.32:135−137,1996年)。混合直後に、この細胞は、上記オリゴヌクレオチド/リピトイド混合物を、オリゴヌクレオチドの最終濃度が300nMになるまで添加することによってトランスフェクトされる。その後、この細胞は、5%のCO2、37℃で一晩、上記トランスフェクション混合物と一緒にインキュベートされ、そしてこのトランスフェクション混合物は、この細胞を3〜4日間維持する。
全RNAは、RNeasyTM kit(Qiagen Corporation,Chatsworth,CA)を使用して、この製造業者によって提供されるプロトコルにしたがって、上記トランスフェクトされた細胞から抽出される。抽出の後、このRNAは、PCRの鋳型として使用するために逆転写される、一般的に、0.2〜1μgの全抽出RNAは、滅菌したマイクロフュージチューブ中におかれ、そして水が、全量3μLになるまで添加される。7μLの緩衝液/酵素混合物は、各チューブに添加される。この緩衝液/酵素混合物は、以下に記載される順序で混合される:
4μLの25mM MgCl2
2μLの10X反応緩衝液
8μLの2.5mM dNTPs
1μLのMuLV逆転写酵素(50u)(Applied Biosystems)
1μLのRNaseインヒビター(20u)
1μLのオリゴdT(50pmol)。
逆転写の後、標的遺伝子は、Roche Light CyclerTMリアルタイムPCR機を使用して増幅される。PCR増幅混合物の20μLのアリコートは、以下の構成成分を、以下に記載される順序で混合することによって調製される:2μLの10X PCR緩衝液II(10mMのTris(pH8.3)および50mMのKClを含む、Perkin−Elmer,Norwalk,CT)、3mMのMgCl2、140μMの各dNTP、0.175pmolの各OAS1オリゴ、1:50,000希釈のSYBR(登録商標)Green、0.25mg/mLのBSA、1単位のTaqポリメラーゼならびに20μLまでのH2O。SYBR(登録商標)Green(Molecular Probes,Eugene,OR)は、2本鎖DNAに結合したときに蛍光を発する色素であり、このことは、各反応において生成されたPCR産物の量が直接的に測定されることを可能にする。完了した逆転写反応の2μLは、PCR増幅混合物の各20μLのアリコートに添加され、そして増幅は、標準的なプロトコルによって行われる。
(OAS1 RNAIを用いる細胞の処理)
アンチセンス処理のために実施例5の方法を使用して、細胞は、上記OAS1配列(配列番号19)に基づくオリゴヌクレオチドを用いて処理される。3’末端におけるデオキシ−TTを有する2つの相補的なリボヌクレオチドモノマーが合成され、そしてアニールされる。上記PH3CH8肝細胞株は、1:3のL2リピトイドを含む50〜200nMのRNAiによって処理される。細胞は、1日目、2日目、3日目および4日目に収集され、そしてDansakoら,Virus Res.97:17−30,2003年に記載されるようなウェスタン分析によってOAS1タンパク質に関して分析される。
(C型肝炎ウイルスのNS5Aタンパク質とのOAS1相互作用)
本発明のOAS1タンパク質またはOAS1ポリペプチドの、C型肝炎ウイルスのNS5Aと相互作用する能力は、Taguchi,T.ら,J.Gen.Virol.85:959−969,2004年に記載される方法を使用してアッセイされる。OAS1タンパク質およびOAS1ポリペプチドをコードするポリヌクレオチドは、上記のように調製され、そしてプラスミドは、Taguchi,T.らに記載されるような慣習的な方法を使用して構築される。1つのプラスミドは、OAS1タンパク質またはOAS1ポリペプチドをコードするポリヌクレオチドを含み、そして第2のプラスミドは、NS5Aをコードするポリヌクレオチドを含む。このプラスミドはまた、それぞれのタンパク質に対して適切なタグ(例えば、FLAGタグ、HA、またはGST)をコードする。適切な細胞(例えば、HeLa細胞)は、タグおよびNS5Aタンパク質をコードするプラスミドならびに異なるタグおよびOAS1タンパク質またはOAS1ポリペプチドをコードするプラスミドによって一過性にトランスフェクトされる。インキュベーションおよび(Taguchi,T.ら)に記載されるような上清の調製後、種々の分析技術が、OAS1タンパク質またはOAS1ポリペプとNS5Aとの結合を、検出および定量するために使用され得る。このような技術は、当該分野において公知であり、これらとしては、共沈分析、免疫蛍光分析、および免疫ブロット分析が挙げられる。NS5Aに対する結合を示さないOAS1タンパク質およびOAS1ポリヌクレオチドは、C型肝炎感染のインヒビターとしてのさらなる分析にふさわしい。
(OAS1の化学的かつ立体的に保存された領域)
当業者が認識するように、酵素活性または治療的可能性を改良するためにOAS1の構造を修飾する場合、特定の残基または残基の領域は、化学的かつ構造的に保存される必要がある。例として、数種の保存的ドメインが、以下に記載される。当業者が認識するように、このタンパク質の構造および機能を妨害する、いくつかのアミノ酸に対する化学的に保存された変化が許容され得る。例えば、Asp75およびAsp77の両方は、OAS1機能について本質的である、触媒的な2価の金属イオンを配位する。これらの塩基に対する修飾(例えば、アスパラギンまたはグルタミン酸)が許容され得、これらの残基の本質的に極性の性質および酸の性質は、保存される必要がある。
アミノ酸40〜アミノ酸47:FLKERCFR(配列番号75)
アミノ酸55〜アミノ酸82:VSKVVKGGSSGKGTTLRGRSDADLVVFL(配列番号76)
アミノ酸94〜アミノ酸112:RRGEFIQEIRRQLEACQRE(配列番号77)
アミノ酸128〜アミノ酸138:NPRALSFVLSS(配列番号78)
アミノ酸145〜アミノ酸158:VEFDVLPAFDALGQ(配列番号79)
アミノ酸182〜アミノ酸198:KEGEFSTCFTELQRDFL(配列番号80)
アミノ酸201〜アミノ酸217:RPTKLKSLIRLVKHWYQ(配列番号81)
アミノ酸225〜アミノ酸241:KLPPQYALELLTVYAWE(配列番号82)
アミノ酸296〜アミノ酸307:PVILDPADPTGN(配列番号83)
アミノ酸337〜アミノ酸343:GSPVSSW(配列番号84)。
(酵素活性部位を改良するアミノ酸の変化)
OASアミノ酸配列における変化は、上記タンパク質の酵素活性の改良を想定し得る。1つの好ましい実施形態において、この酵素の活性部位内のアミノ酸は、ATPまたは金属イオン結合、酵素の有効性、および酵素の進化性を改良するために改変され得る。このような変化の例は、配列番号26、配列番号27、配列番号33、配列番号34、配列番号35、または配列番号48のアミノ酸位置61におけるグリシンに対するチロシンの置換である。化学的に不活性なグリシンから極性のチロシンへの置換は、ATPのN3原子とこのアミノ酸位置との間の水素結合を容易にするはずであり、それによって、この相互作用の解離定数およびエネルギー特性を改良する。チロシンは、例えば、より進化したポリ−Aポリメラーゼにおいてこの位置に見出される。当業者が認識するように、他の改変が想定され得る。
(2本鎖RNAの結合を改良するアミノ酸の変化)
酵素活性を改良する、OASに対するアミノ酸改変の第2の例は、このタンパク質と2本鎖ウイルスRNAとの間の相互作用を安定化する改変であり得る。以下の表は、このタンパク質に対してRNAが結合する溝におけるそれらのアミノ酸、および基本的に、正に荷電したアミノ酸側鎖と負に荷電したリボ核酸との間の相互作用を安定化するように設計された数種の変化案を記載する。当業者が認識するように、RNAが結合する溝に対する同様の型の改変が、想定され得る。
(遺伝子変異の分析)
当業者は、多くの他の分析方法が、遺伝子の分析における特定の変異の進化の重要性を評価するために存在することを認識する。1つの例は、一般的にD’と称される連鎖不平衡係数の周知の算出である(Lewontin,Genetics 49:49−67,1964年)。他の特に関連する方法は、遺伝子座における、高頻度、中頻度、または低頻度の変異の相対的な量を比較することによって、その遺伝子座内の選択圧および/または最近の進化的事象(例えば、選択的蔓延(selective sweep))を推定することを試みる。これらの試験で最もよく知られたものは、Tajima D統計量(Tajima,Genetics 123:585−595,1989年)である。FuおよびLi,Genetics 133:693−709(1993)はまた、Tajima統計量および他の統計量に対する変形を開発し、これはまた、各変異に対する祖先の対立遺伝子に関する知識を使用する。これらの方法および他の方法は、上記観察された効果に対する相対的寄与率を評価するために、本発明の変異に適用される。
Claims (81)
- オリゴアデニレートシンセターゼ遺伝子(OAS1)の変異を同定するためのヒトの遺伝学的スクリーニング方法であって、該方法が、参照配列の配列番号19のヌクレオチド位置2135728、2135749、2135978、2144072、2144088、2144116、2144321、2131025、2133961、2139587、2144294、2144985、2156523、および2156638における参照ヌクレオチドとの非参照ヌクレオチドの置換、ならびに参照配列の配列番号19の位置2156595における参照ヌクレオチドの欠失からなる群より選択されるOAS1の点変異の存在を核酸試料において検出し、それよって該変異を同定する工程を包含する、方法。
- 配列番号20〜配列番号30、配列番号32〜配列番号35および配列番号46〜配列番号52からなる群より選択されるアミノ酸配列からなる、単離されたポリペプチド。
- 配列番号75〜配列番号84からなる群より選択される少なくとも1つのアミノ酸配列からなり、そして配列番号20〜配列番号30、配列番号32〜配列番号35および配列番号46〜配列番号52からなる群より選択されるポリペプチドに対して少なくとも80%の配列類似性を有する、単離されたポリペプチド。
- 単離されたポリペプチドであって、配列番号75〜配列番号84からなる群より選択される少なくとも1つのアミノ酸配列からなり、そして以下:
(a)配列番号22および配列番号25のいずれか1つの配列のアミノ酸219〜アミノ酸238;
(b)配列番号23のアミノ酸231〜アミノ酸250;
(c)配列番号26〜配列番号29、配列番号33〜配列番号34、および配列番号50のいずれか1つの配列のアミノ酸347〜アミノ酸366;
(d)配列番号32のアミノ酸295〜アミノ酸314;
(e)配列番号46のアミノ酸189〜アミノ酸208;
(f)配列番号47のアミノ酸61〜アミノ酸80;
からなる群より選択されるポリペプチドに対して少なくとも80%の配列類似性を有する単離されたポリペプチド。 - タンパク質変換ドメインを含むポリペプチドに対して共有結合される、請求項2〜請求項4のいずれか1項に記載のポリペプチド。
- 前記タンパク質変換ドメインが、配列番号85〜配列番号94からなる群より選択されるポリペプチドで構成される、請求項5に記載のポリペプチド。
- 前記タンパク質変換ドメインが、配列番号85〜配列番号94からなる群より選択されるポリペプチドに対して少なくとも80%の配列類似性を有するポリペプチドで構成される、請求項5に記載のポリペプチド。
- 前記タンパク質変換ドメインが、アルギニン、リジン、もしくはヒスチジンの付加または置換によって、配列番号85〜配列番号94からなる群より選択されるポリペプチドとは異なる、請求項5に記載のポリペプチド。
- ポリエチレングリコールに対して共有結合される、請求項2〜請求項8のいずれか1項に記載のポリペプチド。
- リポソーム中に被包される、請求項2〜請求項8のいずれか1項に記載のポリペプチド。
- エンドソーム崩壊因子に対して共有結合される、請求項2〜請求項8のいずれか1項に記載のポリペプチド。
- エンドソーム崩壊因子に対して非共有結合性に結合される、請求項2〜請求項8のいずれか1項に記載のポリペプチド。
- 前記エンドソーム崩壊因子が、pH感受性である、請求項11または請求項12に記載のポリペプチド。
- 糖部分に対して共有結合される、請求項2〜請求項13のいずれか1項に記載のポリペプチド。
- 前記糖部分が、ガラクトースまたはマンノースで構成される、請求項14に記載のポリペプチド。
- (a)細胞によって、請求項2〜請求項8のいずれか1項に記載のポリペプチドを発現させる工程;および
(b)該ポリペプチドを回収する工程;
を包含する方法によって生成される、単離されたポリペプチド。 - 組換え宿主細胞によって生成される、請求項2〜請求項8のいずれか1項に記載のポリペプチド。
- 異種なポリペプチド配列を含む、請求項2〜請求項8のいずれか1項に記載のポリペプチド。
- 請求項2〜請求項18のいずれか1項に記載のポリペプチドおよび薬学的に受容可能なキャリアを含有する、組成物。
- 請求項2〜請求項8のいずれか1項に記載のポリペプチド配列をコードするヌクレオチド配列を含む、単離されたポリヌクレオチド。
- 配列番号31、配列番号36〜配列番号45および配列番号55〜配列番号56からなる群より選択されるヌクレオチド配列を含む、単離されたポリヌクレオチド。
- 請求項20および請求項21のいずれか1項に記載の単離されたポリヌクレオチドを含む、組換えベクター。
- 発現制御配列に対して作動可能に連結された、請求項20および請求項21のいずれか1項に記載の単離されたポリヌクレオチドを含む、発現ベクター。
- 請求項23に記載の発現ベクターによって、形質転換されたかまたはトランスフェクトされた、宿主細胞。
- 前記ベクターが、ウイルスベクターである、請求項23に記載の発現ベクター。
- 前記ベクターが、アデノウイルスベクター、アデノ関連ウイルスベクター、バキュロウイルス、セムリキ森林ウイルスベクター、シンドビスウイルスベクター、ポックスウイルスベクター、ワクシニアウイルスベクター、トリポックスウイルスベクター、アビポックスウイルスベクター、鶏痘ウイルスベクター、カナリア痘ウイルスベクター、アルファウイルスベクター、鶏痘ウイルスベクターまたはレンチウイルスベクターからなる群より選択されるウイルスベクターである、請求項23に記載の発現ベクター。
- 薬学的に受容可能なキャリアからなる群より選択される第1の成分、ならびに請求項23、請求項25および請求項26のいずれか1項に記載の発現ベクターからなる群より選択される第2の成分を含有する、組成物。
- 哺乳動物においてウイルス感染を処置する方法であって、該方法が、このような処置の必要がある哺乳動物に対して、オリゴアデニレートシンセターゼ1を含有する組成物を投与する工程を包含する、方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項2〜請求項8のいずれか1項に記載のポリペプチドである、請求項28に記載の方法。
- 前記オリゴアデニレートシンセターゼ1が、前記請求項20および請求項21のいずれか1項に記載のポリヌクレオチドによって発現される、請求項28に記載の方法。
- 請求項19および請求項27のいずれか1項に記載の組成物を投与する工程を包含する、請求項28に記載の方法。
- 前記ウイルス感染が、2本鎖RNAウイルスによる感染である、請求項28に記載の方法。
- 前記ウイルス感染が、フラビウイルスによる感染である、請求項28に記載の方法。
- 前記フラビウイルスが、C型肝炎ウイルスである、請求項33に記載の方法。
- 前記ウイルス感染が、パラミクソウイルスによる感染である、請求項28に記載の方法。
- 前記ウイルス感染が、HIV、RSウイルス、インフルエンザウイルス、コロナウイルス、パラインフルエンザウイルス、A型肝炎ウイルス、麻疹ウイルス、流行性耳下腺炎ウイルス、西ナイルウイルス、デング熱ウイルス、黄熱病ウイルス、ポリオウイルス、ヘルペスウイルス、およびヒトパピローマウイルスからなる群より選択されるウイルスによる感染である、請求項28に記載の方法。
- 前記ウイルス感染が、重症急性呼吸器症候群である、請求項28に記載の方法。
- 前記哺乳動物が、前記オリゴアデニレートシンセターゼ1を、天然に産生しない、請求項28に記載の方法。
- 哺乳動物において癌を処置する方法であって、該方法が、このような処置の必要がある哺乳動物に対してオリゴアデニレートシンセターゼ1を含有する組成物を投与する工程を包含する、方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項2〜請求項8のいずれか1項に記載のポリペプチドである、請求項39に記載の方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項20および請求項21に記載のポリヌクレオチドの1つによって発現される、請求項39に記載の方法。
- 請求項19および請求項27のいずれか1項に記載の組成物を投与する工程を包含する、請求項39に記載の方法。
- 前記癌が、前立腺癌である、請求項39に記載の方法。
- 請求項2〜請求項8のいずれか1項に記載のポリペプチド上のエピトープに対して指向される、モノクローナル抗体。
- 前記抗体が、請求項2〜請求項8のいずれか1項に記載の別の異なるポリペプチドと交差反応性ではない、請求項44に記載の抗体。
- 薬学的に受容可能なキャリアおよび請求項44および請求項45のいずれか1項から選択される抗体を含有する、組成物。
- 請求項20および請求項21のいずれか1項に記載のポリヌクレオチドを含む標的に特異的に結合する、単離された干渉するポリヌクレオチド。
- 標的結合部位が、少なくとも25個の連続したヌクレオチドである、請求項47に記載の干渉するポリヌクレオチド。
- 請求項47に記載の干渉するポリヌクレオチドおよび薬学的キャリアを含有する、組成物。
- 配列番号19に特異的に結合する、単離されたアンチセンスポリヌクレオチド。
- 請求項50に記載のアンチセンスポリヌクレオチド、および薬学的キャリアを含有する、組成物。
- 請求項20および請求項21のいずれか1項に記載のポリヌクレオチドを含む標的に対して指向される、単離されたリボザイム。
- 請求項52に記載のリボザイムおよび薬学的キャリアを含有する、組成物。
- 哺乳動物においてウイルス感染を処置する方法であって、該処置の必要がある哺乳動物中のオリゴアデニレートシンセターゼ1を阻害する工程を包含する、方法。
- 前記オリゴアデニレートシンセターゼ1を阻害する工程が、請求項46、請求項49、請求項51、請求項53、および請求項80のいずれか1項に記載の組成物を投与する工程を包含する、請求項54に記載の方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項2〜請求項8のいずれか1項に記載のポリペプチドである、請求項54に記載の方法。
- 前記オリゴアデニレートシンセターゼ1は、請求項20および請求項21のいずれか1項に記載のポリヌクレオチドによって発現される、請求項54に記載の方法。
- 前記ウイルス感染が、HIV、RSウイルス、インフルエンザウイルス、コロナウイルス、パラインフルエンザウイルス、A型肝炎ウイルス、麻疹ウイルス、流行性耳下腺炎ウイルス、西ナイルウイルス、デング熱ウイルス、黄熱病ウイルス、ポリオウイルス、ヘルペスウイルス、およびヒトパピローマウイルスからなる群より選択されるウイルスによる感染である、請求項54に記載の方法。
- 前記ウイルス感染が、重症急性呼吸器症候群である、請求項54に記載の方法。
- 哺乳動物においてインスリン依存性糖尿病を処置する方法であって、該方法が、該処置の必要がある哺乳動物においてオリゴアデニレートシンセターゼ1を阻害する工程を包含する、方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項2〜請求項8のいずれか1項に記載のポリペプチドである、請求項60に記載の方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項20および請求項21のいずれか1項に記載のポリヌクレオチドによって発現される、請求項60に記載の方法。
- 前記オリゴアデニレートシンセターゼ1を阻害する工程が、請求項46、請求項49、請求項51、請求項53、および請求項80のいずれか1項に記載の組成物を投与する工程を包含する、請求項60に記載の方法。
- 前記スクリーニング方法が、ヒトにおけるウイルス感染に対する感受性を同定する、請求項1に記載の方法。
- 前記スクリーニング方法が、ヒトにおける糖尿病についての疾病素質を同定する、請求項1に記載の方法。
- 前記スクリーニング方法が、ヒトにおける精神分裂病についての疾病素質を同定する、請求項1に記載の方法。
- 前記スクリーニング方法が、ヒトにおける癌に対する感受性を同定する、請求項1に記載の方法。
- 前記癌が、前立腺癌である、請求項67に記載の方法。
- 前記スクリーニング方法が、ウイルス感染についての治療的処置に対する患者の応答性を同定する、請求項1に記載の方法。
- 前記治療的処置が、インターフェロンに基づく処置である、請求項69に記載の方法。
- 前記患者の応答が、持続性のウイルスのクリアランスによって測定される、請求項69に記載の方法。
- ヒトにおいて精神分裂病を処置するための方法であって、該方法が、該処置の必要があるヒト中のオリゴアデニレートシンセターゼ1を阻害する工程を包含する、方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項2〜請求項8のいずれか1項に記載のポリペプチドである、請求項72に記載の方法。
- 前記オリゴアデニレートシンセターゼ1が、請求項20および請求項21のいずれか1項のポリヌクレオチドによって発現される、請求項72に記載の方法。
- 前記オリゴアデニレートシンセターゼ1を阻害する工程が、請求項46、請求項49、請求項51、請求項53、および請求項80のいずれか1項に記載の組成物を投与する工程を包含する、請求項72に記載の方法。
- インヒビターが、小分子の薬物を含む、請求項72に記載の方法。
- インヒビターが、小分子の薬物を含む、請求項54に記載の方法。
- インヒビターが、小分子の薬物を含む、請求項60に記載の方法。
- 請求項2〜請求項8のいずれか1項に記載のポリペプチド上のエピトープに対して指向されるモノクローナル抗体から発生される抗体フラグメント。
- 薬学的に受容可能なキャリアおよび請求項79に記載の抗体フラグメントを含有する、組成物。
- 前記スクリーニング方法が、前記ヒトにおけるC型肝炎ウイルス感染に対する感受性を同定する、請求項1に記載の方法。
Applications Claiming Priority (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US51388803P | 2003-10-23 | 2003-10-23 | |
| US54237304P | 2004-02-06 | 2004-02-06 | |
| US55475804P | 2004-03-19 | 2004-03-19 | |
| US56052404P | 2004-04-08 | 2004-04-08 | |
| US57832304P | 2004-06-09 | 2004-06-09 | |
| US58350304P | 2004-06-28 | 2004-06-28 | |
| US60524304P | 2004-08-26 | 2004-08-26 | |
| PCT/US2004/035284 WO2005040428A2 (en) | 2003-10-23 | 2004-10-22 | Detection of mutations in a gene associated with resistance to viral infection, oas1 |
Related Child Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011021746A Division JP2011142913A (ja) | 2003-10-23 | 2011-02-03 | ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 |
| JP2012111782A Division JP2012183069A (ja) | 2003-10-23 | 2012-05-15 | ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 |
| JP2013097618A Division JP2013208117A (ja) | 2003-10-23 | 2013-05-07 | ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007529199A true JP2007529199A (ja) | 2007-10-25 |
| JP2007529199A5 JP2007529199A5 (ja) | 2012-07-05 |
Family
ID=36591413
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006536883A Pending JP2007529199A (ja) | 2003-10-23 | 2004-10-22 | ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 |
Country Status (10)
| Country | Link |
|---|---|
| US (8) | US8192973B2 (ja) |
| EP (4) | EP1689888A2 (ja) |
| JP (1) | JP2007529199A (ja) |
| KR (1) | KR20060116825A (ja) |
| CN (3) | CN103495153A (ja) |
| AU (1) | AU2004283294B2 (ja) |
| BR (1) | BRPI0415771A (ja) |
| CA (1) | CA2543789A1 (ja) |
| HK (1) | HK1161740A1 (ja) |
| WO (1) | WO2005040428A2 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1689888A2 (en) | 2003-10-23 | 2006-08-16 | Illumigen Biosciences Inc. | Detection of mutations in a gene associated with resistance to viral infection, oas1 |
| UA95446C2 (ru) | 2005-05-04 | 2011-08-10 | Іллюміджен Байосайєнсіз, Інк. | Мутаци в генах oas1 |
| WO2007061690A2 (en) | 2005-11-23 | 2007-05-31 | Illumigen Biosciences, Inc. | Novel pharmaceutical compositions for the treatment of virus infection and cancer |
| CN103540575A (zh) * | 2006-08-01 | 2014-01-29 | 奇尼塔二有限责任公司 | 医药制造方法 |
| EP2207902A1 (en) * | 2007-11-09 | 2010-07-21 | INSERM (Institut National de la Santé et de la Recherche Medicale) | A method for predicting the therapeutic responsiveness of patients to a medical treatment with an interferon |
| EP2123748A1 (en) | 2008-05-20 | 2009-11-25 | Institut Pasteur | 2'-5'-oligoadenylate synthetase 3 for preventing and treating positive-sense single-stranded rna virus infection |
| US20110104138A1 (en) | 2009-11-03 | 2011-05-05 | Institut Pasteur | Use of the innate immunity gene oasl for preventing or treating infection with negative strand rna viruses |
| CN102517338B (zh) * | 2011-12-09 | 2014-07-23 | 宁夏共享集团有限责任公司 | 一种微生物发酵糠醛渣生产生化腐植酸的方法 |
| EP3811081A1 (en) * | 2018-06-21 | 2021-04-28 | Universiteit Utrecht Holding B.V. | Method for monitoring kinase activity in a sample |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10506001A (ja) * | 1991-09-30 | 1998-06-16 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 核酸複合体を高等真核生物の細胞に導入するための組成物 |
| WO2002090552A2 (en) * | 2001-05-08 | 2002-11-14 | Switch Biotech Ag | Use of 2'-5'-oligoadenylate synthetase and/or rnasel or nucleic acids encoding them for diagnosis, prophylaxis or treatment of wound healing |
Family Cites Families (88)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4356270A (en) | 1977-11-08 | 1982-10-26 | Genentech, Inc. | Recombinant DNA cloning vehicle |
| SE428332B (sv) | 1979-03-08 | 1983-06-20 | Wallac Oy | Forfarande for fluorescensspektroskopisk bestemning av biologiskt aktivt emne, sasom hapten, antikropp eller antigen |
| US4293652A (en) | 1979-05-25 | 1981-10-06 | Cetus Corporation | Method for synthesizing DNA sequentially |
| US4530901A (en) | 1980-01-08 | 1985-07-23 | Biogen N.V. | Recombinant DNA molecules and their use in producing human interferon-like polypeptides |
| US4863873A (en) * | 1980-01-14 | 1989-09-05 | Esa, Inc. | Method for biological testing and/or developing pharmaceuticals for treatment of disorders |
| US4458066A (en) | 1980-02-29 | 1984-07-03 | University Patents, Inc. | Process for preparing polynucleotides |
| US4416988A (en) | 1980-12-23 | 1983-11-22 | Harvey Rubin | Detection and isolation of enkephalin mRNA using a synthetic oligodeoxynucleotide |
| DE3207053A1 (de) | 1982-02-26 | 1983-09-15 | Esselte Pendaflex Corp., 11530 Garden City, N.Y. | Etikettiergeraet |
| SE8301395L (sv) | 1983-03-15 | 1984-09-16 | Wallac Oy | Kelatiserande foreningar med funktionella grupper vilka tillater kovalent koppling till bio-organiska molekyler |
| US4582789A (en) | 1984-03-21 | 1986-04-15 | Cetus Corporation | Process for labeling nucleic acids using psoralen derivatives |
| US4617261A (en) | 1984-03-21 | 1986-10-14 | Cetus Corporation | Process for labeling nucleic acids and hybridization probes |
| US4569790A (en) | 1984-03-28 | 1986-02-11 | Cetus Corporation | Process for recovering microbially produced interleukin-2 and purified recombinant interleukin-2 compositions |
| US4707404A (en) | 1984-04-03 | 1987-11-17 | Mitsubishi Paper Mills, Ltd. | Thermal transfer recording material |
| JPS60222842A (ja) | 1984-04-19 | 1985-11-07 | Fuji Photo Film Co Ltd | ハロゲン化銀写真乳剤およびその製造方法 |
| US5550111A (en) | 1984-07-11 | 1996-08-27 | Temple University-Of The Commonwealth System Of Higher Education | Dual action 2',5'-oligoadenylate antiviral derivatives and uses thereof |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US4965188A (en) | 1986-08-22 | 1990-10-23 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences using a thermostable enzyme |
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| JP2509574B2 (ja) | 1985-08-15 | 1996-06-19 | アモコ・コーポレーション | 標識付けした核酸 |
| EP0244471A4 (en) | 1985-10-24 | 1988-01-28 | Siska Diagnostics Inc | NUCLEIC ACID SAMPLES MARKED WITH LANTHANIDE CHELATE. |
| US4946773A (en) | 1985-12-23 | 1990-08-07 | President And Fellows Of Harvard College | Detection of base pair mismatches using RNAase A |
| US4800159A (en) | 1986-02-07 | 1989-01-24 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences |
| US4889818A (en) | 1986-08-22 | 1989-12-26 | Cetus Corporation | Purified thermostable enzyme |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| DE3788914T2 (de) | 1986-09-08 | 1994-08-25 | Ajinomoto Kk | Verbindungen zur Spaltung von RNS an eine spezifische Position, Oligomere, verwendet bei der Herstellung dieser Verbindungen und Ausgangsprodukte für die Synthese dieser Oligomere. |
| US5116742A (en) | 1986-12-03 | 1992-05-26 | University Patents, Inc. | RNA ribozyme restriction endoribonucleases and methods |
| US4987071A (en) | 1986-12-03 | 1991-01-22 | University Patents, Inc. | RNA ribozyme polymerases, dephosphorylases, restriction endoribonucleases and methods |
| US4863876A (en) | 1987-01-15 | 1989-09-05 | Hevey Richard C | Method of detecting and quantifying ligands in liquids via biotin-avidin-medicated fluorescence polarization |
| US5585481A (en) | 1987-09-21 | 1996-12-17 | Gen-Probe Incorporated | Linking reagents for nucleotide probes |
| ATE151467T1 (de) | 1987-11-30 | 1997-04-15 | Univ Iowa Res Found | Durch modifikationen an der 3'-terminalen phosphodiesterbindung stabilisierte dna moleküle, ihre verwendung als nukleinsäuresonden sowie als therapeutische mittel zur hemmung der expression spezifischer zielgene |
| US5403711A (en) | 1987-11-30 | 1995-04-04 | University Of Iowa Research Foundation | Nucleic acid hybridization and amplification method for detection of specific sequences in which a complementary labeled nucleic acid probe is cleaved |
| US5254678A (en) | 1987-12-15 | 1993-10-19 | Gene Shears Pty. Limited | Ribozymes |
| US5614395A (en) | 1988-03-08 | 1997-03-25 | Ciba-Geigy Corporation | Chemically regulatable and anti-pathogenic DNA sequences and uses thereof |
| US5789214A (en) | 1988-03-08 | 1998-08-04 | Novartis Finance Corporation | Method of inducing gene transcription in a plant |
| CA1340323C (en) | 1988-09-20 | 1999-01-19 | Arnold E. Hampel | Rna catalyst for cleaving specific rna sequences |
| US5457183A (en) | 1989-03-06 | 1995-10-10 | Board Of Regents, The University Of Texas System | Hydroxylated texaphyrins |
| US5168053A (en) | 1989-03-24 | 1992-12-01 | Yale University | Cleavage of targeted RNA by RNAase P |
| US5272262A (en) | 1989-06-21 | 1993-12-21 | City Of Hope | Method for the production of catalytic RNA in bacteria |
| US5144019A (en) | 1989-06-21 | 1992-09-01 | City Of Hope | Ribozyme cleavage of HIV-I RNA |
| US5587361A (en) | 1991-10-15 | 1996-12-24 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| DE4039415A1 (de) | 1990-02-03 | 1991-08-08 | Boehringer Mannheim Gmbh | Verfahren zur herstellung rekombinanter proteine ohne n-terminalen methioninrest |
| NZ236819A (en) | 1990-02-03 | 1993-07-27 | Max Planck Gesellschaft | Enzymatic cleavage of fusion proteins; fusion proteins; recombinant dna and pharmaceutical compositions |
| US5149797A (en) | 1990-02-15 | 1992-09-22 | The Worcester Foundation For Experimental Biology | Method of site-specific alteration of rna and production of encoded polypeptides |
| US5321131A (en) | 1990-03-08 | 1994-06-14 | Hybridon, Inc. | Site-specific functionalization of oligodeoxynucleotides for non-radioactive labelling |
| US5180818A (en) | 1990-03-21 | 1993-01-19 | The University Of Colorado Foundation, Inc. | Site specific cleavage of single-stranded dna |
| US5245022A (en) | 1990-08-03 | 1993-09-14 | Sterling Drug, Inc. | Exonuclease resistant terminally substituted oligonucleotides |
| US5639949A (en) | 1990-08-20 | 1997-06-17 | Ciba-Geigy Corporation | Genes for the synthesis of antipathogenic substances |
| DK0558676T3 (da) | 1990-11-23 | 2000-09-25 | Aventis Cropscience Nv | Fremgangsmåde til transformering af enkimbladede planter |
| US5571799A (en) | 1991-08-12 | 1996-11-05 | Basco, Ltd. | (2'-5') oligoadenylate analogues useful as inhibitors of host-v5.-graft response |
| US5700922A (en) | 1991-12-24 | 1997-12-23 | Isis Pharmaceuticals, Inc. | PNA-DNA-PNA chimeric macromolecules |
| US5565552A (en) | 1992-01-21 | 1996-10-15 | Pharmacyclics, Inc. | Method of expanded porphyrin-oligonucleotide conjugate synthesis |
| US5266459A (en) * | 1992-02-24 | 1993-11-30 | The Scripps Research Institute | Gaucher's disease: detection of a new mutation in intron 2 of the glucocerebrosidase gene |
| US5593874A (en) | 1992-03-19 | 1997-01-14 | Monsanto Company | Enhanced expression in plants |
| US5652355A (en) | 1992-07-23 | 1997-07-29 | Worcester Foundation For Experimental Biology | Hybrid oligonucleotide phosphorothioates |
| US5574142A (en) | 1992-12-15 | 1996-11-12 | Microprobe Corporation | Peptide linkers for improved oligonucleotide delivery |
| US5866781A (en) | 1993-03-08 | 1999-02-02 | The Cleveland Clinic Foundation | Antiviral transgenic plants, vectors, cells and methods |
| PT733059E (pt) | 1993-12-09 | 2001-03-30 | Univ Jefferson | Compostos e metodos para mutacoes dirigidas ao local em celulas eucarioticas |
| US5597709A (en) * | 1994-01-27 | 1997-01-28 | Human Genome Sciences, Inc. | Human growth hormone splice variants hGHV-2(88) and hGHV-3(53) |
| EP0753992A4 (en) | 1994-02-18 | 1998-02-04 | Cleveland Clinic Foundation | ANTIVIRAL TRANSGENIC PLANTS, VECTORS, CELLS AND METHODS |
| US5625050A (en) | 1994-03-31 | 1997-04-29 | Amgen Inc. | Modified oligonucleotides and intermediates useful in nucleic acid therapeutics |
| US5597696A (en) | 1994-07-18 | 1997-01-28 | Becton Dickinson And Company | Covalent cyanine dye oligonucleotide conjugates |
| US5514758A (en) | 1994-09-30 | 1996-05-07 | The Goodyear Tire & Rubber Company | Process for making latex for high performance masking tape |
| US5480640A (en) | 1995-05-02 | 1996-01-02 | Schering Corporation | Alpha interferon for treating prostate cancer |
| US5840565A (en) * | 1995-08-22 | 1998-11-24 | The Regents Of The University Of California | Methods for enhancing the production of viral vaccines in PKR-deficient cell culture |
| US5693512A (en) | 1996-03-01 | 1997-12-02 | The Ohio State Research Foundation | Method for transforming plant tissue by sonication |
| NZ333802A (en) | 1996-08-02 | 2001-09-28 | Genesense Technologies Inc | Antitumor antisense sequences directed against R1 and R2 components of ribonucleotide reductase |
| AU9131698A (en) | 1997-09-08 | 1999-03-29 | Princeton University | Human genes regulated by human cytomegalovirus and interferon |
| EP1036165A4 (en) | 1997-12-04 | 2003-05-14 | Isis Pharmaceuticals Inc | HUMAN RNASE, COMPOSITIONS AND USES THEREOF |
| US6506559B1 (en) | 1997-12-23 | 2003-01-14 | Carnegie Institute Of Washington | Genetic inhibition by double-stranded RNA |
| EP0998579A1 (en) | 1998-03-30 | 2000-05-10 | ESA, Inc. | Methodology for predicting and/or diagnosing disease |
| US5958773A (en) | 1998-12-17 | 1999-09-28 | Isis Pharmaceuticals Inc. | Antisense modulation of AKT-1 expression |
| US20010034023A1 (en) * | 1999-04-26 | 2001-10-25 | Stanton Vincent P. | Gene sequence variations with utility in determining the treatment of disease, in genes relating to drug processing |
| US20030165921A1 (en) * | 2000-02-03 | 2003-09-04 | Tang Y. Tom | Novel nucleic acids and polypeptides |
| CA2402293A1 (en) * | 2000-03-07 | 2001-09-13 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| JP2004502406A (ja) * | 2000-03-09 | 2004-01-29 | カイロン コーポレイション | ヒト遺伝子およびヒト遺伝子発現産物 |
| AU2001251613A1 (en) * | 2000-04-14 | 2001-10-30 | Millennum Pharmaceuticals, Inc. | Novel genes, compositions and methods for the identification, assessment, prevention, and therapy of human cancers |
| FR2823224B1 (fr) * | 2001-04-04 | 2003-10-31 | Pasteur Institut | Utilisation de genes oas impliques dans la sensibilite/resistance a l'infection par les flaviviridae pour le criblage de molecules antivirales |
| DE10122206A1 (de) | 2001-05-08 | 2002-11-28 | Switch Biotech Ag | Verwendung von Polypeptiden oder diese kodierende NukleInsäuren einer 2'-5'- Oligoadenylate Synthetase und/oder RNAseL zur Diagnose, Prävention oder Behandlung von Hauterkrankungen oder Wundheilung sowie ihre Verwendung zur Identifizierung von pharmakologisch aktiven Substanzen |
| US6818420B2 (en) * | 2002-02-27 | 2004-11-16 | Biosource International, Inc. | Methods of using FET labeled oligonucleotides that include a 3′-5′ exonuclease resistant quencher domain and compositions for practicing the same |
| GB0208928D0 (en) * | 2002-04-19 | 2002-05-29 | Imp College Innovations Ltd | Methods |
| CA2484251C (en) * | 2002-04-30 | 2015-06-23 | University Of South Florida | Materials and methods for inhibition of respiratory syncytial virus infection |
| EP1576142A2 (en) * | 2002-05-17 | 2005-09-21 | Baylor College of Medicine | Identification of oligoadenylate synthetase-like genes |
| WO2004000998A2 (en) * | 2002-06-19 | 2003-12-31 | Georgia State University Research Foundation, Inc. | Compositions and methods for viral resistance genes |
| BR0311527A (pt) | 2002-06-20 | 2005-02-22 | Unilever Nv | Processo para preparação de composição detergente sólida não-granular com bolhas de gás aprisionadas |
| NZ591879A (en) | 2003-10-23 | 2012-11-30 | Kineta Two Llc | Detection of mutations in a gene associated with resistance to viral infection, OAS1 |
| EP1689888A2 (en) | 2003-10-23 | 2006-08-16 | Illumigen Biosciences Inc. | Detection of mutations in a gene associated with resistance to viral infection, oas1 |
| UA95446C2 (ru) | 2005-05-04 | 2011-08-10 | Іллюміджен Байосайєнсіз, Інк. | Мутаци в генах oas1 |
| DE102006036763A1 (de) | 2006-08-05 | 2008-02-07 | Khs Ag | Vorrichtung und Verfahren zur Sterilisation von Behältern |
-
2004
- 2004-10-22 EP EP04810020A patent/EP1689888A2/en not_active Ceased
- 2004-10-22 EP EP10183642A patent/EP2267154A1/en not_active Withdrawn
- 2004-10-22 CN CN201310187575.4A patent/CN103495153A/zh active Pending
- 2004-10-22 CN CN2004800386069A patent/CN1910293B/zh not_active Expired - Fee Related
- 2004-10-22 CA CA002543789A patent/CA2543789A1/en not_active Abandoned
- 2004-10-22 KR KR1020067010053A patent/KR20060116825A/ko not_active Application Discontinuation
- 2004-10-22 AU AU2004283294A patent/AU2004283294B2/en not_active Ceased
- 2004-10-22 BR BRPI0415771-0A patent/BRPI0415771A/pt not_active IP Right Cessation
- 2004-10-22 WO PCT/US2004/035284 patent/WO2005040428A2/en active Application Filing
- 2004-10-22 EP EP10183284A patent/EP2305798A3/en not_active Ceased
- 2004-10-22 EP EP09154553A patent/EP2083089A1/en not_active Withdrawn
- 2004-10-22 JP JP2006536883A patent/JP2007529199A/ja active Pending
- 2004-10-22 CN CN2011100363548A patent/CN102174538B/zh not_active Expired - Fee Related
-
2006
- 2006-11-02 US US11/592,711 patent/US8192973B2/en not_active Expired - Fee Related
- 2006-11-02 US US11/592,758 patent/US20070154467A1/en not_active Abandoned
-
2008
- 2008-04-02 US US12/061,548 patent/US8088907B2/en not_active Expired - Fee Related
-
2011
- 2011-04-07 US US13/082,119 patent/US20110237501A1/en not_active Abandoned
- 2011-11-22 US US13/302,081 patent/US8551772B2/en not_active Expired - Fee Related
-
2012
- 2012-03-02 HK HK12102152.6A patent/HK1161740A1/xx not_active IP Right Cessation
- 2012-05-10 US US13/468,937 patent/US20120321608A1/en not_active Abandoned
-
2013
- 2013-05-28 US US13/903,926 patent/US9090947B2/en not_active Expired - Fee Related
- 2013-09-05 US US14/019,432 patent/US20140037717A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10506001A (ja) * | 1991-09-30 | 1998-06-16 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 核酸複合体を高等真核生物の細胞に導入するための組成物 |
| WO2002090552A2 (en) * | 2001-05-08 | 2002-11-14 | Switch Biotech Ag | Use of 2'-5'-oligoadenylate synthetase and/or rnasel or nucleic acids encoding them for diagnosis, prophylaxis or treatment of wound healing |
Non-Patent Citations (5)
| Title |
|---|
| JPN6010044120; FASEB JOURNAL (ABSTRACTS PART I) , 2002, A152 * |
| JPN6010044123; Genes and Immunity Vol.4, 200309, p.411-419 * |
| JPN6010044125; Immunogenetics Vol.30, 1989, p.427-431 * |
| JPN6011059446; CMLS, Cell. Mol. Life Sci. Vol.57, 2000, p.1593-1612 * |
| JPN6011059447; THE JOURNAL OF BIOLOGICAL CHEMISTRY Vol.278, No.1, 200301, p.585-590 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US8551772B2 (en) | 2013-10-08 |
| EP2305798A3 (en) | 2011-04-20 |
| AU2004283294A1 (en) | 2005-05-06 |
| AU2004283294B2 (en) | 2011-03-17 |
| US8088907B2 (en) | 2012-01-03 |
| CA2543789A1 (en) | 2005-05-06 |
| CN102174538B (zh) | 2013-06-19 |
| WO2005040428A3 (en) | 2005-09-15 |
| US8192973B2 (en) | 2012-06-05 |
| BRPI0415771A (pt) | 2006-12-26 |
| US20110237501A1 (en) | 2011-09-29 |
| US20090123472A1 (en) | 2009-05-14 |
| KR20060116825A (ko) | 2006-11-15 |
| CN1910293B (zh) | 2011-04-13 |
| US20070154467A1 (en) | 2007-07-05 |
| HK1161740A1 (en) | 2012-08-03 |
| EP2083089A1 (en) | 2009-07-29 |
| US20120253027A1 (en) | 2012-10-04 |
| EP2267154A1 (en) | 2010-12-29 |
| US9090947B2 (en) | 2015-07-28 |
| EP1689888A2 (en) | 2006-08-16 |
| CN103495153A (zh) | 2014-01-08 |
| US20140037717A1 (en) | 2014-02-06 |
| US20140010800A1 (en) | 2014-01-09 |
| EP2305798A2 (en) | 2011-04-06 |
| US20120321608A1 (en) | 2012-12-20 |
| US20110071073A1 (en) | 2011-03-24 |
| WO2005040428A2 (en) | 2005-05-06 |
| CN102174538A (zh) | 2011-09-07 |
| CN1910293A (zh) | 2007-02-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9090947B2 (en) | Detection of mutations in a gene associated with resistance to viral infection, OAS1 | |
| US20070111231A1 (en) | Detection of mutations in a gene associated with resistance to viral infection, OAS2 and OAS3 | |
| JP2013208117A (ja) | ウイルス感染に対する抵抗性に関連する遺伝子である、oas1における変異の検出 | |
| US20090155234A1 (en) | Detection of mutations in a gene associated with resistance to viral infection, mx1 | |
| US20060257850A1 (en) | Methods of treatment and diagnosis of patients with hepatitis c infection | |
| AU2013228050B2 (en) | Detection of mutations in a gene associated with resistance to viral infection, oas1 | |
| US20090186028A1 (en) | Detection of mutations in a gene associated with resistance to viral infection | |
| TWI415944B (zh) | 偵測與病毒感染抗性有關基因(oasi)中之突變之方法 | |
| MXPA06004493A (en) | Detection of mutations in a gene associated with resistance to viral infection, oas1 | |
| EP1649067A1 (en) | Methods to identify polynucleotide and polypeptide sequences which may be associated with physiological and medical conditions |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071022 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20071022 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20081022 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20081017 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100803 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20101028 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20101105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110203 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111115 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120202 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120209 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20120515 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130108 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20130312 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130507 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20130529 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20130529 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20130625 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20130809 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150217 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150317 |