JP2005297435A - 多層膜、複合材料、インプラント及び複合材料の製造方法 - Google Patents
多層膜、複合材料、インプラント及び複合材料の製造方法 Download PDFInfo
- Publication number
- JP2005297435A JP2005297435A JP2004119023A JP2004119023A JP2005297435A JP 2005297435 A JP2005297435 A JP 2005297435A JP 2004119023 A JP2004119023 A JP 2004119023A JP 2004119023 A JP2004119023 A JP 2004119023A JP 2005297435 A JP2005297435 A JP 2005297435A
- Authority
- JP
- Japan
- Prior art keywords
- oxide
- group
- ammonium
- multilayer film
- composite material
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Landscapes
- Application Of Or Painting With Fluid Materials (AREA)
- Laminated Bodies (AREA)
- Materials For Medical Uses (AREA)
Abstract
【解決手段】 複数の金属酸化物から構成された金属酸化物下地層と、該下地層を被覆する少なくとも1種類の金属酸化物から構成された被覆層とからなることを特徴とする多層膜及び基材上に該多層膜を有する複合材料。本発明の複合材料は、一般式:AxMeFyで示されるフルオロ金属錯化合物の少なくとも2種類と、フッ素捕捉剤とを含む下地層形成水溶液中に基材を浸漬することによって基材表面に下地層を形成し、6フッ化チタンアンモニウムとフッ素捕捉剤を含む被覆層形成水溶液又は6フッ化チタンアンモニウムとフッ素捕捉剤とともに、その他のフルオロ金属錯化合物の少なくとも1種類を含む被覆層形成水溶液中に浸漬することによって被覆層を形成することによって製造することができる。
【選択図】 図1
Description
しかし、近年の一連の研究では、いわゆる生体親和性は相互不可侵の要件だけでは十分ではなく、本来の代替材料(人工骨、人工関節)の表面に、生体と人工材料の橋渡しとなるヒドロキシアパタイトの核形成を誘起し、爾後アパタイト表面に生体が取り入れ易い環境を形成することが重要なことが判明した。
例えば、チタン金属では、生体組織との間に10〜50nmの厚さの表面反応場としての均質層が形成され、表面が酸化されてこれら非晶質酸化チタンの一部が生体に取り込まれ再構成されながら、次第に生体親和性を高めていくことが確認されている(非特許文献1)。
詳述すれば、チタン金属表面に形成される酸化物非晶質物質が、生体に一部取り込まれ再構成される過程で表面に多数のTi−OHを形成する。これらの官能基の存在が周囲の体液中のアパタイト成分を濃集させ、増加したアパタイト成分はアパタイトの核形成を誘起し、これらの核は周囲からカルシウムイオンとリン酸イオンを取り込んでアパタイトの成長を促進させる。これらのプロセスを経由することによってチタン金属表面に緻密で均一な骨類似構造を有するアパタイトの層が形成される。
近年、ペースメーカー、人工関節、人工骨、人工歯根、経皮端子、人工血管、血流センサー、各種カテーテルなど、生体組み込み型の機器,器具が実用化されるに伴い、むしろこれらの生体親和性がよりいっそう問題となっている。現在一般に考えられている生体材料が生体内で活性を有するということは、その表面にアパタイト層を形成し、‘骨’となって生体に親和することであるが、チタン金属以外の材料としては、現在CaO−SiO2系ガラスが検討されている。この材料は、生体内でその表面に多数のSi−OH基を形成し、これが周囲のアパタイト成分の濃度を増大させアパタイトの核形成を誘起することで生体活性を発現する。
これら人工材料が生体内でその表面にアパタイトを形成する条件は、表面にアパタイトの核形成を誘起する官能基(−OH)を有することであるとされている。Si−OHの他にもTi−OH、Zr−OH、Ta−OHもアパタイトの核形成を誘起し得ることが確認されている(非特許文献2)。
従って、ポリエチレンやPMMAのようなプラスチック素材に生体親和性を付与するためには、ヒドロキシアパタイトが表面に成長し易いように表面処理を施す必要がある。
実際、既にポリエチレンテレフタレート(PET)表面を処理し生体親和性を高めた実例が存在する。まず、PETの極細繊維の織物を、酸素ガス中でグロー放電処理し、その表面に多数のCOOHなどの極性基を形成しておく。これを予め擬似体液に浸漬したCaOとSiO2を主成分とするガラス粒子の上に置くと、ガラスから溶出した珪酸イオンが効率よくPET表面に付着し,アパタイトの核形成を誘起する。このようにしてアパタイト核をプランニングしたPETを別の擬似体液中に浸漬すると、それらの核が擬似体液からカルシウムイオンとリン酸イオンを取り込んで成長し個々のPET繊維の表面に緻密で均一なアパタイト層を形成する(非特許文献3)。
また、シランカップリング法に基づきTiO2 膜を、PET、エチレンビニルアルコール共重合体(EVOH)、ポリアミド6、ポリアミド66等に成膜形成し、これらプラスチックに生体活性を付与した例がある(非特許文献4)。
しかし、これらの例はいずれもプロセスが複雑で膜形成に時間がかかり、かつ生体材料にとって重要な要件である膜の機械的強度が十分とはいえない点が問題であった。
村上・鵜飼、表面科学Vol.20,No.9,pp640−649,1999 小久保・金、表面科学Vol.20,No.9,pp612−628,1999 小久保・金、表面科学Vol.20,No.9,pp621−628,1999 Balas, Kawasaki et al. ISCM, Proceeding of the 16th International symposium、pp667−670、2003
上記の下地層を構成する金属酸化物は、周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択された少なくとも2種の金属の酸化物であることが好ましい。
本発明の多層膜において、下地層の構成主要成分である金属酸化物は、酸化ケイ素、酸化チタン及び酸化ジルコニウムから選ばれた2種又は3種であるのが好ましい。
また、被覆層の構成主要成分は、酸化チタンであり、酸化チタンの一部の代わりに酸化ケイ素、酸化ジルコニウム、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含んでいてもよい。
本発明は、さらに基材上に前記多層膜を有することを特徴とする複合材料に関する。
なお、本明細書において、構成主要成分とは、構成成分のうち60%〜100%を占める成分を言うものとする。
本発明の複合材料の製造方法は、下記の一般式(I):
AxMeFy ・・・(I)
[式中、AはNH4 、Na、K又はHを表わし、Meは周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択した金属の酸化物を表わし、x及びyは化合物の電気的中性を満たす数である]で示されるフルオロ金属錯化合物の少なくとも2種類と、フッ素捕捉剤とを含む下地層形成水溶液中に基材を浸漬することによって基材表面に下地層を形成し、6フッ化チタンアンモニウムとフッ素捕捉剤とを含む被覆層形成水溶液又は6フッ化チタンアンモニウムとフッ素捕捉剤とともに、6フッ化ケイ素アンモニウム、6フッ化ジルコニウムアンモニウム、7フッ化ニオブアンモニウム、6フッ化スズアンモニウム、7フッ化タンタルアンモニウム、6フッ化ガリウムアンモニウム、6フッ化ハフニウムアンモニウム、6フッ化ゲルマニウムアンモニウム及び6フッ化アルミニウムアンモニウムからなる群から選ばれる少なくとも1種類のフルオロ金属錯化合物を含む被覆層形成水溶液中に浸漬することによって被覆層を形成するのが好ましい。
したがって、本発明によれば、プラスチック等の生体活性を有しない基材を用いても高い生体親和性を有し、生体活性に極めて優れた複合材料を提供することができる。また、本発明の方法によれば、低温(室温)環境下で、かつ複雑な形状を有する基材に対しても高い生体活性を有する多層膜を高付着力で形成することができ、生体活性に優れた複合材料を簡単な操作で効率よく製造することができる。
さらに、本発明の複合材料を、インプラントとして生体内に埋入するか又はリン酸カルシウム系化合物形成溶液に浸漬すると、リン酸カルシウム系化合物をその表面に形成することができる。
上記の下地層を構成する金属酸化物は、周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択される少なくとも2種の金属の酸化物であることが好ましい。
下地層は、主として、酸化ケイ素、酸化チタン及び酸化ジルコニウムから選ばれた2種又は3種から構成するのが好ましく、特に、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内で含むのが好ましく、SiO2 0.1〜0.3:TiO2 0.03〜0.2:ZrO2 0.5〜0.9のモル比範囲内で含むのがより好ましい。
また、下地層の構成としては、主要成分が、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内で存在し、かつ酸化ジルコニウムの代わりに、或いは酸化ジルコニウムとともに、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含む構成も好適である。
本発明の多層膜において、下地層は、0.05〜0.5μmの層厚であるのが好ましく、0.02〜0.1μmの層厚であるのがより好ましい。
被覆層の層厚は、0.1〜1.0μmであるのが好ましく、0.2〜0.5μmであるのがより好ましい。
ここで基材としては、広範な材料から選択することができ、例えば、合成高分子化合物、天然高分子化合物、生体高分子化合物、プラスチック等を含む高分子化合物、金属、半導体、ガラス、セラミックス、カーボン材料、ダイヤモンド、カルサイト等の塩、無機高分子化合物、貝殻、水晶等の天然物などを挙げることができる。特に高分子樹脂材料からなるものが好適である。具体的には、ポリエチレン、アクリル樹脂(PMMA)やこれらにアクリル系、シリコン系ハードコート、メラミン系ハードコートなどのハードコートを施したものでもよい。
これらの基材の形状は、特に制限されるものはなく、板状、繊維状、編物状、多孔質、粒状、その他複雑形状などいかなるものでもよい。
また、これらの基材は、基本的に平坦なものでもよいが、金属酸化物膜やその上にアパタイト膜が形成されやすくするため或いはこれらと基材との間の密着強度を向上させるため、凹凸状に表面が荒れた状態のものでもよい。
基材は、紫外線照射、プラズマ照射、酸化雰囲気曝露又は酸若しくは塩基中への浸漬により粗面化した後、下地層を形成するのが好ましい。例えば、プラスチック基材に直に酸化物膜を成膜する場合、表面が撥水状態になっていることが多く、表面処理(プラズマ照射、薬品処理)を施すことによってプラスチック表面を活性化し、親水状態にした後に、下地層形成水溶液中に浸漬して成膜を実施するのが好ましい。
AxMeFy ・・・(I)
[式中、AはNH4 、Na、K又はHを表わし、Meは周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択した金属の酸化物を表わし、x及びyは化合物の電気的中性を満たす数である]で示されるフルオロ金属錯化合物の少なくとも2種類と、フッ素捕捉剤とを含む下地層形成水溶液中に基材を浸漬することによって実施するのが好ましい。
上記一般式(I)で示されるフルオロ金属錯化合物の具体例としては、6フッ化チタンアンモニウム:(NH4)2TiF6、6フッ化珪素アンモニウム:(NH4)2SiF6、6フッ化ジルコニウムアンモニウム:(NH4)2ZrF6、7フッ化タンタルアンモニウム:(NH4)2TaF7 、7フッ化ニオブアンモニウム:(NH4)2NbF7、6フッ化スズアンモニウム:(NH4)2SnF6、6フッ化ガリウムアンモニウム:(NH4)2GaF6 、6フッ化ハフニウムアンモニウム:(NH4)2HfF6、6フッ化ゲルマニウムアンモニウム:(NH4)2GeF6、6フッ化アルミニウムアンモニウム:(NH4)3AlF6などがある。
上記のようなフルオロ金属錯化合物とフッ素捕捉剤を含む水溶液中に、或いは前者水溶液にフッ素捕捉剤を直接添加混合し、この水溶液に基材を浸漬することによって化学反応が開始され成膜が進行する。
下地層の場合、基本的に6フッ化チタンアンモニウム、6フッ化珪素アンモニウム及び6フッ化ジルコニウムアンモニウムを適当な比率(図3参照)で混合したものにフッ素捕捉剤を添加することによって、複合酸化物下地層の組成範囲をモル比で、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0の範囲内で形成する。ここで、酸化ジルコニウムの代わりに、その一部が酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナであってもよい。
以上のような成膜プロセスからなる本発明によれば、基材上にフォトリソグラフィなどの方法でレジスト膜を形成し、金属酸化物膜が形成される部位を制限することもできる。
被覆層の形成は、6フッ化チタンアンモニウムとフッ素捕捉剤を含む被覆層形成水溶液又は6フッ化チタンアンモニウムとフッ素捕捉剤とともに、6フッ化ケイ素アンモニウム、6フッ化ジルコニウムアンモニウム、7フッ化ニオブアンモニウム、6フッ化スズアンモニウム、7フッ化タンタルアンモニウム、6フッ化ガリウムアンモニウム、6フッ化ハフニウムアンモニウム、6フッ化ゲルマニウムアンモニウム及び6フッ化アルミニウムアンモニウムからなる群から選ばれる少なくとも1種類のフルオロ金属錯化合物を含む被覆層形成水溶液中に下地層を有する基材を浸漬することによって実施するのが好ましい。
一般に先に述べた析出粒子から構成される凹凸の表面構造は、特に凹部ではOH‐イオンが特に濃集し易い環境にあるため、これら水酸イオン濃度の増加によってアパタイト結晶の核形成が起こり易く、爾後のヒドロキシアパタイト形成を容易にする。
これによってアパタイト形成を大きく促進させることが可能となった。これは金属酸化物膜表面に析出成長させるにあたって、その原料となるカルシウムを複合材料の被覆層中に混入させておくと、アパタイト形成においてより親和性の高い環境を提供する働きがあるためである。
これらの事実は実験によってカルシウムの混入がある場合とない場合とで比較し、前者の場合では明らかにアパタイトの形成が顕著であることを確かめることができた。
本発明において当該材料の生体活性(生体親和性)の発現を確認する手段として用いられるリン酸カルシウム系化合物形成溶液或いは擬似体液は、カルシウムイオン(Ca2+)を0.02〜25mM、リン酸水素イオン(HPO4 2-)を0.01〜10mM含有し、pHが6〜8であることが好ましい。より好ましくはカルシウムイオンを0.2〜20mM、リン酸水素イオンを0.1〜8mM含み、pHは6.8〜7.6である。更に好ましくは、カルシウムイオンを1.2〜5mM、リン酸水素イオンを0.5〜2mM含み、pHは7.2〜7.5である。
生体適合性に優れたリン酸カルシウム系化合物を形成させるためには、カルシウムイオンとリン酸水素イオンに加えて、例えば、塩化ナトリウム、炭酸水素ナトリウム、塩化カリウム、塩化マグネシウム・六水和物、硫酸ナトリウムなどをさらに含むことが好ましい。この場合、ナトリウムイオン(Na+)を1.4〜1420mM、カリウムイオン(K+)を0.05〜50mM、マグネシウムイオン(Mg2+)を0.01〜15mM、塩素イオン(Cl-)を1.4〜1500mM、炭酸水素イオン(HCO3 -)を0.04〜45mM、硫酸イオン(SO4 2-)を5.0×10-3mM〜5mM含有していてもよい。好ましくは、ナトリウムイオンを14〜1140mM、カリウムイオンを0.5〜40mM、マグネシウムイオンを0.1〜12mM、塩素イオンを14.5〜1200mM、炭酸水素イオンを0.4〜36mM、硫酸イオンを0.05〜4mM含む。より好ましくはナトリウムイオンを70〜290mM、カリウムイオンを2.5〜10mM、マグネシウムイオンを0.7〜3.0mM、塩素イオンを70〜300mM、炭酸水素イオンを2.0〜9.0mM、硫酸イオンを0.2〜1.0mM含有していてもよい。
また第二に体液中でヒドロキシアパタイトが比較的容易に形成される複合材料の表面形状を提示したことである。更に第三に、一般には特定の製法で作成された水酸基を有する酸化物では生体親和性が確認されているが、これらの酸化物を複数種複合させたものでは、相乗的効果によって生体活性を高める傾向にある点を見出したことである。
そこで表面形状制御及び金属酸化物の複合化という観点から、以下により具体的に詳しく述べる。
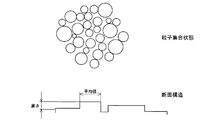
本発明では金属酸化物の析出反応を進行させるために、まずフルオロ金属錯化合物塩(例えばフッ化金属アンモニウム塩)を溶解した水溶液に、金属からフッ素を取り去るためにフッ素捕捉剤として酸化ホウ素等を添加する。これによってホウ素とフッ素が反応して安定なフルオロホウ素錯化合物を形成し、そのため溶液中のフッ化物イオンの濃度が減少し、これを補うためフルオロ金属錯化合物が加水分解して、基材表面に金属酸化物粒子として析出を開始する。この際水溶液中での析出反応は、ほぼ均質核形成プロセスに類似し、数ナノ〜数百ナノメートルサイズの粒子となって析出する。これらの球状粒子はアモルファス状態からなることもあり、多結晶集合体や前者との混合状態或いは単結晶からなることもある。ここで単結晶粒子は、基材表面に対して表面自由エネルギーの高い結晶方位で接合し、結晶配向性を示す場合もある。
このようなナノサイズの析出粒子は、基材表面に付着析出し特異な表面構造を形成する。形成粒子のサイズが均一である場合は,基材表面にナノ粒子が整然とかつ緻密に配列しながら膜形成が進行する。一層が形成されると更にその上に第二層が形成され始め、ところどころに島状析出物が形成される。しかし、一般的には形成粒子のサイズが不均一であるため、積層が進行するにつれて粒子配列の不整が生じ形成膜表面に凹凸が生じたり膜の各所に空隙がつながって生じるホローが形成されたりする。
これらの表面構造を機能発現にとって適正なものとするためには、水溶液中の溶解した試薬の濃度や、析出温度及び析出時間等を適当な範囲に制御しておくことが望ましい。
温度領域を大まかに30℃未満、30〜40℃及び40℃を超える範囲にその析出物の粒子集合状態から分割すると、30℃未満での析出では数ナノメートルレベルの析出粒子の集合によって基材表面を整然と覆い、一層が形成されるとさらにその上に島状粒子集合体を形成しながら析出が進行していく。したがって膜は緻密で表面の凹凸も少ない。30〜40℃の温度領域になると数ナノメートル〜数十ナノメートルと粒子分布に幅が生じ、サイズ的に混在した粒子より構成されるようになる。これによって表面構造に凹凸が生じるようになる。本発明の目的とするリン酸カルシウム系化合物の核形成が誘起され易い構造とは、即ち、適度のOH基の密度分布からなり、リン酸カルシウム系化合物成分の過飽和状態が増大しやすく、かつ核形成のサイトを提供するような表面構造に相当する。さらに40℃を超えると、数十ナノメートル〜数百ナノメートルサイズの粒子が出現し、形成された膜に亀裂が入り易くなる。粒子径が大きくなることによって可視光波長領域の光を散乱するため膜が白濁して見える。表面構造は、顕微鏡レベルでラフになり,多孔質体に近い状態になる。
なお40℃を超えて形成された金属酸化物膜であっても本発明の目的を著しく損なうものではなく、そのまま使用に供することができる。
また上記のような温度は、酸化物組成、金属種、フッ素捕捉剤の濃度、原料水溶液濃度等に応じて適宜変化するが、いずれにせよ、100℃以下の温度であれば、本発明の目的とする金属酸化物を形成することができる。
本発明における膜形成のための水溶液中での反応は下記のように表現される。
例えば、フルオロ金属アンモニウム錯体を純水中に溶解させると、下記の反応式(1)により溶解する。
(NH4)XMeFy + H2O =xNH4 + + MeFy x- + H2O (1)
MeFy x- + (y-x)/2H2O = MeO(y-x)/2↓+ yF― + (y-x)H+ (2)
B2O3 + 8F― + 6H+ =2BF4― + 3H2O (3)
例えば酸化チタン、酸化ジルコニウム及び二酸化ケイ素はそれぞれ特殊な製法によればそれぞれ生体活性を示すが、これらを複合化することによりこれらの相乗効果により、生体活性の高さが大幅に増強されることを本発明者は見出し、そして更に検討した結果、これら酸化物複合体の析出条件を特定し、試薬調合組成比と生成された膜組成、膜特性との関連性について検討し、生体適合性が強く現れる組成領域を特定できた。
一般に、(NH4)2SiF6―(NH4)2TiF6―(NH4)2ZrF6―B2O3―H2O系では、上述の式において、Me=Si,Ti,Zr
のそれぞれにおいて反応式が相互作用しながら進行し、それぞれの酸化物或いは複合酸化物は酸化物複合体として共析する。
即ち同時に表現すると、
(NH4)2(Si,Ti,Zr)F6 + H2O = 2NH4 + + (Si,Ti,Zr)F6 2- + H2O
(Si,Ti,Zr)F6 2- + 2H2O = (Si,Ti,Zr)O2 ↓ + 6F- + 4H+
B2O3 + 8F― + 6H+ =2BF4― + 3H2O
具体的な膜組成は,上記したように、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内にあり、これらの酸化ジルコニウムの一部は、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム及びアルミナ等で置換されてもよい。
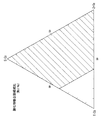
原料として6フッ化珪素アンモニウム,6フッ化チタンアンモニウム、6フッ化ジルコニウムアンモニウム(それぞれASF,ATF,AZFと略記)を用いたとき特に生体活性強度が強く発現し、機械的化学的耐性が良好な複合成分比を図3に、そして図4に対応析出酸化物複合膜の組成比の領域を示している。
なおSi,Ti,Zr系酸化物複合体が形成されれば、図3の最適領域は適宜変更することができる。
なお、下記の実施例で測定する基材と多層膜との接着強度は、基材の表と裏にステンレス治具を接着剤を用いて接着し、上下に引っ張り力を印加したときの破断応力で示す。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム及び6フッ化ジルコニウムアンモニウムをそれぞれ30g、8g、2g加え、更に酸化ホウ素30gを加えた水溶液を攪拌しながら純水を加えて1リットルに調製し完全に溶解させた。この水溶液の温度を40℃に保ちながら、モデルサンプルをプラズマ照射後ただちにこの水溶液に浸漬した。
20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。
その後、別の容器に6フッ化チタンアンモニウム2g及び硝酸カルシウム0.5g入れ、純水中に溶解させ、更に1リットルになるまで純水を加え40℃としたものを用意しておき、酸化ホウ素15gを添加混合溶解させ、これに先に洗浄乾燥させたサンプルを6時間浸漬放置した。放置後、サンプルを取り出して純水にて洗浄乾燥させ、サンプル上に2層膜を形成した。同様にPMMA基板(60×60×1mm)をモデルと同じ条件下で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は8.0MPであった。
その後、サンプルの生体親和性を確認するために、浸漬するための擬似体液を調製した。
まず蒸留水700mlにNaClを7.996g、NaHCO3を0.350g、KClを0.224g、K2HPO4・3H2Oを0.228g、MgCl2/6H2Oを0.306g、1M塩酸を35ml、CaCl2を0.278g、Na2SO4を0.072g、トリスヒドロキシメチルアミノメタンを6.058g溶解させ、36.5℃でpHが7.4となるように、1M塩酸で調製し、その後蒸留水を加えて溶液全体を1リットルとした。
この表面にプラズマ照射装置(ヤマト科学製PB1000S)によって200W、4分プラズマ照射を行い、表面処理を行なった。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム及び6フッ化ジルコニウムアンモニウムをそれぞれ30g、8g、2g加え,更に酸化ホウ素30g加えた水溶液を攪拌しながら純水を加えて1リットルに調製し、完全に溶解させた。この水溶液を40℃に保ちながら、モデルサンプルをこの水溶液に浸漬した。20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。
その後、別の容器に6フッ化チタンアンモニウム3.5g及び硝酸カルシウム0.5gを純水中に加え完全に溶解後、酸化ホウ素30gを添加しながら純水を加えて1リットルに調製し、完全に溶解した水溶液中に、上記サンプルを再度浸漬した。6時間後これを取り出して洗浄後乾燥させ、モデルサンプル上に2層膜を形成した。同様にポリエチレン基板(10×10×1mm)をモデルと同一条件で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は、12MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日間ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム及び6フッ化ジルコニウムアンモニウムをそれぞれ30g、8g、2g加え,更に酸化ホウ素30gを加えた水溶液を攪拌しながら純水を加えて1リットルに調製し、完全に溶解させた。この水溶液を40℃に保ちながら、モデルサンプルをこの水溶液に浸漬した。20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。
その後、別の容器に6フッ化チタンアンモニウム3.5g及び硝酸カルシウム0.5gを純水中に加え完全に溶解後、酸化ホウ素30gを添加しながら純水を加えて1リットルに調製し、完全に溶解した水溶液中に、上記サンプルを再度浸漬した。6時間後これを取り出して洗浄後、70℃で2時間乾燥させ、モデルサンプル上に2層膜を形成した。同様にPMMA基板(アクリル系ハードコート付基板)(10×10×1mm)をモデルと同じ条件下で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は、5.5MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日間ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
この表面にプラズマ照射装置(ヤマト科学製PB1000S)によって200Wで4分プラズマ照射を行い、表面処理を行なった。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウムをそれぞれ19.1g、5.6g加え、更に酸化ホウ素30g加えた水溶液を攪拌しながら純水を加えて1リットルに調製し、完全に溶解させた。この水溶液を40℃に保ちながら、モデルサンプルをこの水溶液に浸漬した。20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し乾燥させた。その後、別の容器に6フッ化チタンアンモニウム3.5g及び硝酸カルシウム0.5gを純水中に加え完全に溶解後、酸化ホウ素30gを添加しながら純水を加えて1リットルに調製し、完全に溶解した水溶液中に、上記サンプルを再度浸漬した。6時間後これを取り出して洗浄後乾燥させ、モデルサンプル上に2層膜を形成した。
一方ポリエチレン基板(10×10×1mm)を上記と全く同様に処理して、形成された膜の基板に対する接着強度を測定したところ8MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
同様にポリエチレン基板(10×10×1mm)を同じ条件下で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は、7.5MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
同様にポリエチレン基板(10×10×1mm)を同じ条件で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は、6MPであった。
実施例1と同じ擬似体液中に,2層膜を形成したモデルサンプルを浸漬し、10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類のX線回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
同様にポリエチレン基板(10×10×1mm)を同じ条件で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は、5.5MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類のX線回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
同様に、ポリエチレン基板(10×10×1mm)を同じ条件で処理し、同じく2層膜を形成した。これによって形成した2層膜の基板に対する接着強度は、6.8MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイトに帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
同様にポリエチレン基板(10×10×1mm)を同一条件で処理し、同じく2層膜を形成した。こうして形成した2層膜の基板に対する接着強度は、10MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム、6フッ化ジルコニウムアンモニウム、7フッ化ニオブアンモニウム、6フッ化スズアンモニウムをそれぞれ、30g、8g、1g、0.7g、0.4g加え、更に酸化ホウ素30gを加えた水溶液を攪拌しながら純水を加えて1リットルに調製し完全に溶解させた。この水溶液を40℃に保ちながら、モデルサンプルをプラズマ照射後直ちにこの水溶液に浸漬した。
20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。その後、別の容器に6フッ化チタンアンモニウム3.5g及び硝酸カルシウム0.5gを純水中に加え完全に溶解後、酸化ホウ素30gを添加しながら純水を加えて1リットルに調製し、完全に溶解した水溶液中に上記サンプルを再度浸漬した。6時間後これを取り出して洗浄後乾燥させ、モデルサンプル上に2層膜を形成した。
一方ポリエチレン基板(10×10×1mm)を上記と全く同様に処理して、形成された膜の基板に対する接着強度を測定したところ10MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し10日ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
この表面にプラズマ照射装置(ヤマト科学製PB1000S)によって200Wで4分間プラズマ照射を行い、表面処理を行なった。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム及び6フッ化ジルコニウムアンモニウムをそれぞれ30g、8g、2g加え、更に酸化ホウ素30gを加えた水溶液を攪拌しながら純水を加えて1リットルに調製し、完全に溶解させた。この水溶液を40℃に保ちながら、モデルサンプルをこの水溶液に浸漬した。20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。
その後別の容器に6フッ化チタンアンモニウム、6フッ化ジルコニウムアンモニウム、7フッ化タンタルアンモニウムをそれぞれ3.5g、0.5g、0.8g及び硝酸カルシウム0.5gを純水中に加え完全に溶解後、酸化ホウ素30gを添加しながら純水を加えて1リットルに調製し、完全に溶解した水溶液中に、上記サンプルを再度浸漬した。6時間後これを取り出して洗浄後乾燥させ、モデルサンプル上に2層膜を形成した。同様にポリエチレン基板(10×10×1mm)をモデルと同一条件で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する接着強度は、7.5MPであった。
実施例1と同じ擬似体液中に、2層膜を形成したモデルサンプルを浸漬し、10日間ほど保持した。その後モデルを擬似体液中から取り出して表面に形成された薄膜のX線回折測定を実施した。浸漬後3〜4日でヒドロキシアパタイト類に帰属される回折ピークが観察され、1週間後にそのピーク強度が増大したことからモデル表面におけるヒドロキシアパタイト類の生成が確認された。
基材としてポリエチレン製平板(10.0mm×10.0mm×1.0mm)を用意した。この表面にプラズマ照射装置(ヤマト科学製PB1000S)によって200Wで4分間プラズマ照射を行い、表面処理を行なった。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム及び6フッ化ジルコニウムアンモニウムをそれぞれ30g、8g、2g加え、更に酸化ホウ素30g加えた水溶液を攪拌しながら純水を加えて1リットルに調製し、完全に溶解させた。この水溶液を40℃に保ちながら、基材をこの水溶液に浸漬した。20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。
その後、別の容器に6フッ化チタンアンモニウム3.5g及び硝酸カルシウム0.5gを純水中に加え完全に溶解後、酸化ホウ素30gを添加しながら純水を加えて1リットルに調製し、完全に溶解した水溶液中に、上記基材を再度浸漬した。6時間後これを取り出して洗浄後乾燥させ、基材上に被覆層を形成した。
基材の表と裏に実施例1と同様にステンレス治具を接着剤を用いて接着し、上下に引っ張り力を印加したときの破断応力を測定した。このときの破断応力は、5サンプルの平均で13.09MPであった。破断面を観察すると、下地層と基材の間で破断した部分と、下地層と被覆層の間で破断した部分が混在していた。
実施例1と同様の方法で、破断応力を測定した。破断応力は、10サンプルの平均で6.70MP、最大で10.41MPであった。破断面を観察すると、アパタイト内で破断していた。
ポリエチレン製骨状モデル(120×30×30mm)を用意し、下地層形成用の処理液の調製組成を、6フッ化珪素アンモニウム、6フッ化チタンアンモニウム、6フッ化ジルコニウムアンモニウムそれぞれ、4.8g、9.0g、6.5gとした以外は、実施例9と全く同一の条件で処理し、2層膜を形成した。しかし形成した下地層は、従来のように透明ではなく白濁半透明状態であった。
同様にポリエチレン基板(10×10×1mm)を同一条件で処理し、同じく2層膜を形成した。これによって測定した形成膜の基板に対する付着強度は、4.0MP弱で、必要とされる5.0MPを下回った。この結果、この2層膜は、生体材料としての要件を欠くものであった。
(下地層の接着強度)
基材としてポリメチルメタクリレート製平板(アクリル系ハードコート付)(10.0mm×10.0mm×1.0mm)を用意した。この基材の表面をプラズマ照射装置(ヤマト科学製PB1000S)によって、200Wで4分間プラズマ照射を行い、表面処理を行った。
その後純水中に6フッ化珪素アンモニウム、6フッ化チタンアンモニウム及び6フッ化ジルコニウムアンモニウムをそれぞれ30g、8g、2g加え、更に酸化ホウ素30gを加えた水溶液を攪拌しながら純水を加えて1リットルに調製し完全に溶解させた。この水溶液の温度を40℃に保ちながら、基材をプラズマ照射後ただちにこの水溶液に浸漬した。
20時間浸漬後サンプルを処理液から取り出し純水によって洗浄し、乾燥させた。
下地層を形成した基材の表と裏にステンレス治具(接着面の大きさ:10.0mm×10.0mm)を接着剤を用いて接着し、上下に引っ張り力を印加したときの破断応力を測定した。破断応力は、4サンプルの平均で10.64MP、最大で11.41MPであった。
1.人工骨、人工歯根、医療用ならびに歯科用インプラント材、人工血管、人工臓器、骨接合材
2.医療器具、経皮端子等の生体用端子
3.ハイブリッド生体材料
4.バイオセンサー、チップデバイス(プロティンチップ、DHAチップ)、
化学反応マイクロチップ、化学実験プラント、ドラッグデリバリー、マイクロマシーン、ナノマシーン
5.細胞(特にSE細胞)培養の型、スキャホールド(アパタイトだけで作るよりも丈夫)
6.微細マシーン
7.マイクロアレイとマイクロTAS
Claims (24)
- 複数の金属酸化物から構成された金属酸化物下地層と、該下地層を被覆する少なくとも1種類の金属酸化物から構成された被覆層とからなることを特徴とする多層膜。
- 下地層を構成する金属酸化物が、周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択された少なくとも2種の金属の酸化物である請求項1記載の多層膜。
- 下地層を構成する主要成分が酸化ケイ素、酸化チタン及び酸化ジルコニウムから選ばれた2種又は3種である請求項2記載の多層膜。
- 下地層の構成主要成分が、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内で存在する請求項3記載の多層膜。
- 下地層の構成主要成分が、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内で存在し、かつ酸化ジルコニウムの代わりに、或いは酸化ジルコニウムとともに、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含む請求項3記載の多層膜。
- 被覆層の構成主要成分が酸化チタンであり、酸化チタンの一部の代わりに酸化ケイ素、酸化ジルコニウム、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含んでいてもよい請求項1記載の多層膜。
- 下地層が周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択された少なくとも2種の金属の酸化物から構成され、被覆層の構成主要成分が酸化チタン化であり、酸化チタンの一部の代わりに酸化ケイ素、酸化ジルコニウム、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含んでいてもよい請求項1記載の多層膜。
- 下地層を構成する主要成分が酸化ケイ素、酸化チタン及び酸化ジルコニウムから選ばれた2種又は3種であり、被覆層の構成主要成分が酸化チタンであり、酸化チタンの一部の代わりに酸化ケイ素、酸化ジルコニウム、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含んでいてもよい請求項1記載の多層膜。
- 下地層の構成主要成分が、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内で存在し、被覆層の構成主要成分が酸化チタンであり、酸化チタンの一部の代わりに酸化ケイ素、酸化ジルコニウム、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含んでいてもよい請求項1記載の多層膜。
- 下地層の構成主要成分が、SiO2 0〜1.0:TiO2 0〜0.6:ZrO2 0〜1.0のモル比範囲内で存在し、かつ酸化ジルコニウムの代わりに、或いは酸化ジルコニウムとともに、酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含み、被覆層の構成主要成分が酸化チタンであり、酸化チタンの一部の代わりに酸化ニオブ、酸化スズ、酸化タンタル、酸化ガリウム、酸化ハフニウム、酸化ゲルマニウム及びアルミナから選ばれる少なくとも1種類を含んでいてもよい請求項1記載の多層膜。
- 被覆層の表面で金属酸化物が水又は水溶液中で水酸基を形成する請求項1記載の多層膜。
- 被覆層の表面が、平均径1〜300nmの大きさの金属酸化物粒子の集合体から構成される多孔組織からなる請求項1記載の多層膜。
- 基材上に請求項1〜12のいずれか1項記載の多層膜を有することを特徴とする複合材料。
- 基材が高分子化合物からなる請求項13記載の複合材料。
- 多層膜上にリン酸カルシウム系化合物層を有する請求項13記載の複合材料。
- 請求項13〜15のいずれか1項記載の複合材料からなるインプラント。
- 基材表面に構成主要成分として複数の金属酸化物から構成された金属酸化物下地層と、該下地層を被覆する構成主要成分が少なくとも1種類の金属酸化物から構成された被覆層とからなる多層膜を形成することを特徴とする複合材料の製造方法。
- 下記の一般式
AxMeFy
[式中、AはNH4、Na、K又はHを表わし、Meは周期表の4族金属、5族金属、13族金属及び14族金属からなる群から選択した金属の酸化物を表わし、x及びyは化合物の電気的中性を満たす数である]で示されるフルオロ金属錯化合物の少なくとも2種類と、フッ素捕捉剤とを含む下地層形成水溶液中に基材を浸漬することによって基材表面に下地層を形成し、6フッ化チタンアンモニウムとフッ素捕捉剤とを含む被覆層形成水溶液又は6フッ化チタンアンモニウムとフッ素捕捉剤とともに、6フッ化ケイ素アンモニウム、6フッ化ジルコニウムアンモニウム、7フッ化ニオブアンモニウム、6フッ化スズアンモニウム、7フッ化タンタルアンモニウム、6フッ化ガリウムアンモニウム、6フッ化ハフニウムアンモニウム、6フッ化ゲルマニウムアンモニウム及び6フッ化アルミニウムアンモニウムからなる群から選ばれる少なくとも1種類のフルオロ金属錯化合物を含む被覆層形成水溶液中に浸漬することによって被覆層を形成する請求項17記載の複合材料の製造方法。 - フッ素捕捉剤がホウ素化合物である請求項18記載の複合材料の製造方法。
- 基材を紫外線照射、プラズマ照射又は酸若しくは塩基中への浸漬により表面処理した後、下地層形成水溶液中に浸漬する請求項17記載の複合材料の製造方法。
- 被覆層形成水溶液に水溶性カルシウム塩を10-5〜1モル/リットルの量で添加する請求項17記載の複合材料の製造方法。
- 使用するフルオロ金属錯化合物を、対応する金属酸化物にフッ化水素酸水溶液を作用させ、さらにアンモニア水によって中和することによって調製する請求項18記載の複合材料の製造方法。
- 下地層の形成後及び被覆層の形成後に、40〜150℃で1〜20時間加熱処理する請求項18記載の複合材料の製造方法。
- 下地層及び/又は被覆層の形成を、ゾル・ゲル法、溶射法、電極法、真空蒸着法或いはスパッタリング法を用いて行う請求項17記載の複合材料の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004119023A JP2005297435A (ja) | 2004-04-14 | 2004-04-14 | 多層膜、複合材料、インプラント及び複合材料の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004119023A JP2005297435A (ja) | 2004-04-14 | 2004-04-14 | 多層膜、複合材料、インプラント及び複合材料の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005297435A true JP2005297435A (ja) | 2005-10-27 |
Family
ID=35329562
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004119023A Withdrawn JP2005297435A (ja) | 2004-04-14 | 2004-04-14 | 多層膜、複合材料、インプラント及び複合材料の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005297435A (ja) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007303944A (ja) * | 2006-05-10 | 2007-11-22 | Osaka Univ | 硬組織の評価方法 |
| WO2008029612A1 (en) * | 2006-09-08 | 2008-03-13 | Japan Medical Materials Corporation | Bioimplant |
| JP2008061897A (ja) * | 2006-09-08 | 2008-03-21 | Saga Univ | 生体インプラント |
| JP2008073098A (ja) * | 2006-09-19 | 2008-04-03 | Saga Univ | 生体インプラント |
| JPWO2013129292A1 (ja) * | 2012-02-29 | 2015-07-30 | 石原産業株式会社 | 骨セメント組成物 |
| CN106400087A (zh) * | 2016-09-08 | 2017-02-15 | 西安交通大学 | 一种水汽处理含锡微弧氧化涂层制备具有生物电活性钛种植体的方法 |
| US10610614B2 (en) | 2006-09-08 | 2020-04-07 | Kyocera Corporation | Bioimplant with evanescent coating film |
| US11278642B2 (en) | 2006-09-08 | 2022-03-22 | Takao Hotokebuchi | Bioimplant with evanescent coating film |
| US12226550B2 (en) | 2012-02-03 | 2025-02-18 | Saga University | Method of manufacturing a bioimplant |
| WO2026023475A1 (ja) * | 2024-07-22 | 2026-01-29 | 日本化学工業株式会社 | 基材粒子、その製造方法、導電性粒子及び導電性材料 |
-
2004
- 2004-04-14 JP JP2004119023A patent/JP2005297435A/ja not_active Withdrawn
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007303944A (ja) * | 2006-05-10 | 2007-11-22 | Osaka Univ | 硬組織の評価方法 |
| WO2008029612A1 (en) * | 2006-09-08 | 2008-03-13 | Japan Medical Materials Corporation | Bioimplant |
| JP2008061897A (ja) * | 2006-09-08 | 2008-03-21 | Saga Univ | 生体インプラント |
| US10004604B2 (en) | 2006-09-08 | 2018-06-26 | Kyocera Corporation | Bioimplant for artifical joint with evanescent coating film |
| US10610614B2 (en) | 2006-09-08 | 2020-04-07 | Kyocera Corporation | Bioimplant with evanescent coating film |
| US11278642B2 (en) | 2006-09-08 | 2022-03-22 | Takao Hotokebuchi | Bioimplant with evanescent coating film |
| US11998659B2 (en) | 2006-09-08 | 2024-06-04 | Kyocera Corporation | Bioimplant with evanescent coating film |
| JP2008073098A (ja) * | 2006-09-19 | 2008-04-03 | Saga Univ | 生体インプラント |
| US12226550B2 (en) | 2012-02-03 | 2025-02-18 | Saga University | Method of manufacturing a bioimplant |
| JPWO2013129292A1 (ja) * | 2012-02-29 | 2015-07-30 | 石原産業株式会社 | 骨セメント組成物 |
| CN106400087A (zh) * | 2016-09-08 | 2017-02-15 | 西安交通大学 | 一种水汽处理含锡微弧氧化涂层制备具有生物电活性钛种植体的方法 |
| WO2026023475A1 (ja) * | 2024-07-22 | 2026-01-29 | 日本化学工業株式会社 | 基材粒子、その製造方法、導電性粒子及び導電性材料 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Heimann | Plasma-sprayed hydroxylapatite coatings as biocompatible intermediaries between inorganic implant surfaces and living tissue | |
| Karamian et al. | Surface characteristics and bioactivity of a novel natural HA/zircon nanocomposite coated on dental implants | |
| Kizuki et al. | Preparation of bioactive Ti metal surface enriched with calcium ions by chemical treatment | |
| EP2595669B1 (en) | Implant having a multilayered coating and a process for preparing thereof | |
| Li et al. | Na-doped hydroxyapatite coating on carbon/carbon composites: Preparation, in vitro bioactivity and biocompatibility | |
| US20060216494A1 (en) | Organic-inorganic nanocomposite coatings for implant materials and methods of preparation thereof | |
| SE0900560A1 (sv) | Jonsubstituerade hydroxiapatitytbeläggningar | |
| Qadir et al. | Surface characterization and biocompatibility of hydroxyapatite coating on anodized TiO2 nanotubes via PVD magnetron sputtering | |
| Oshida | Hydroxyapatite: synthesis and applications | |
| JP3461818B2 (ja) | 硬組織修復材及びその製造方法 | |
| JP2005297435A (ja) | 多層膜、複合材料、インプラント及び複合材料の製造方法 | |
| Xia et al. | Biomimetic hydroxyapatite deposition on titanium oxide surfaces for biomedical application | |
| KR20230012649A (ko) | 레이저를 이용한 아파타이트 분말 합성 방법 | |
| Li et al. | Chemical surface modification of metallic biomaterials | |
| Nguyen et al. | The effect of two-step surface modification for Ti-Ta-Mo-Zr alloys on bone regeneration: An evaluation using calvarial defect on rat model | |
| JP2004123484A (ja) | 金属酸化物膜およびその用途 | |
| JP2002248163A (ja) | 水溶液合成により表面に直接酸化チタン層を形成した生体活性酸化チタン被覆材料 | |
| Xiao et al. | Low-temperature fabrication of titania layer on 3D-printed 316L stainless steel for enhancing biocompatibility | |
| Yamaguchi et al. | Chemical and heat treatments for inducing bone-bonding ability of Ti-6Al-4V pedicle screw | |
| Vranceanu et al. | Pulsed electrochemical deposition of Ag doped hydroxyapatite bioactive coatings on Ti6Al4V for medical purposes | |
| Tas | Electroless deposition of brushite (CaHPO4· 2H2O) crystals on Ti–6Al–4V at room temperature | |
| Ranga et al. | In-vitro study of sol gel synthesized bioactive glass ceramics for anti-microbial properties | |
| Reiner et al. | Biomimetic calcium phosphate growth over differently shaped Ti substrates: modeling the effect of surface curvature | |
| Doroshenko et al. | Electrodeposition of Calcium Phosphate Coatings in Polyvinyl Alcohol | |
| Yabutsuka et al. | Changes in surface condition during fabrication process of bioactive apatite nuclei incorporated peek |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070413 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20091023 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091104 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100104 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100107 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20100119 |