JP2005296033A - 体液浄化用吸着材 - Google Patents
体液浄化用吸着材 Download PDFInfo
- Publication number
- JP2005296033A JP2005296033A JP2004111963A JP2004111963A JP2005296033A JP 2005296033 A JP2005296033 A JP 2005296033A JP 2004111963 A JP2004111963 A JP 2004111963A JP 2004111963 A JP2004111963 A JP 2004111963A JP 2005296033 A JP2005296033 A JP 2005296033A
- Authority
- JP
- Japan
- Prior art keywords
- hmgb1
- body fluid
- adsorbent
- insoluble carrier
- water
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000001124 body fluid Anatomy 0.000 title claims abstract description 43
- 239000010839 body fluid Substances 0.000 title claims abstract description 38
- 239000003463 adsorbent Substances 0.000 title claims abstract description 36
- 239000000463 material Substances 0.000 title abstract description 12
- 102000055207 HMGB1 Human genes 0.000 claims abstract description 59
- 108700010013 HMGB1 Proteins 0.000 claims abstract description 56
- 101100339431 Arabidopsis thaliana HMGB2 gene Proteins 0.000 claims abstract description 53
- 101150021904 HMGB1 gene Proteins 0.000 claims abstract description 53
- 210000000265 leukocyte Anatomy 0.000 claims abstract description 19
- 125000000524 functional group Chemical group 0.000 claims abstract description 17
- 125000000129 anionic group Chemical group 0.000 claims abstract description 11
- 238000000746 purification Methods 0.000 claims description 17
- 238000001179 sorption measurement Methods 0.000 claims description 10
- 239000011324 bead Substances 0.000 claims description 9
- 206010040047 Sepsis Diseases 0.000 claims description 6
- 201000010099 disease Diseases 0.000 claims description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 6
- 239000002245 particle Substances 0.000 claims description 6
- QAOWNCQODCNURD-UHFFFAOYSA-L sulfate group Chemical group S(=O)(=O)([O-])[O-] QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 claims description 5
- 238000000034 method Methods 0.000 claims description 4
- 125000000542 sulfonic acid group Chemical group 0.000 claims description 3
- 210000001772 blood platelet Anatomy 0.000 abstract description 15
- 210000000601 blood cell Anatomy 0.000 abstract description 7
- 238000006243 chemical reaction Methods 0.000 abstract description 3
- 210000004369 blood Anatomy 0.000 description 17
- 239000008280 blood Substances 0.000 description 17
- 230000004087 circulation Effects 0.000 description 11
- 239000001913 cellulose Substances 0.000 description 7
- 229920002678 cellulose Polymers 0.000 description 7
- 239000002158 endotoxin Substances 0.000 description 7
- 241000699670 Mus sp. Species 0.000 description 5
- 229920006008 lipopolysaccharide Polymers 0.000 description 5
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 4
- -1 anionic amino acids Chemical class 0.000 description 4
- 210000002381 plasma Anatomy 0.000 description 4
- 101710168537 High mobility group protein B1 Proteins 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 2
- ALWXETURCOIGIZ-UHFFFAOYSA-N 1-nitropropylbenzene Chemical compound CCC([N+]([O-])=O)C1=CC=CC=C1 ALWXETURCOIGIZ-UHFFFAOYSA-N 0.000 description 2
- 208000023275 Autoimmune disease Diseases 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- 206010040070 Septic Shock Diseases 0.000 description 2
- 239000012670 alkaline solution Substances 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 229940127219 anticoagulant drug Drugs 0.000 description 2
- 238000004820 blood count Methods 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000004744 fabric Substances 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 239000012510 hollow fiber Substances 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000001509 sodium citrate Substances 0.000 description 2
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 2
- 239000001593 sorbitan monooleate Substances 0.000 description 2
- 229940035049 sorbitan monooleate Drugs 0.000 description 2
- 235000011069 sorbitan monooleate Nutrition 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 206010003445 Ascites Diseases 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 102000052510 DNA-Binding Proteins Human genes 0.000 description 1
- 101710096438 DNA-binding protein Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 229920000875 Dissolving pulp Polymers 0.000 description 1
- 108010033040 Histones Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical group OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000700157 Rattus norvegicus Species 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000027455 binding Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000000921 elemental analysis Methods 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 210000003722 extracellular fluid Anatomy 0.000 description 1
- 239000002657 fibrous material Substances 0.000 description 1
- XUCNUKMRBVNAPB-UHFFFAOYSA-N fluoroethene Chemical group FC=C XUCNUKMRBVNAPB-UHFFFAOYSA-N 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 230000009545 invasion Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 239000012466 permeate Substances 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000036303 septic shock Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 210000001179 synovial fluid Anatomy 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000002759 woven fabric Substances 0.000 description 1
Landscapes
- External Artificial Organs (AREA)
- Solid-Sorbent Or Filter-Aiding Compositions (AREA)
Abstract
【課題】 体液中のHMGB1を高い効率で吸着除去し、かつ白血球、血小板などの生体反応に必要な血液細胞は除去しない性質を持つ吸着材。
【解決手段】 アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする体液浄化用吸着材。
【選択図】なし
【解決手段】 アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする体液浄化用吸着材。
【選択図】なし
Description
本発明は、体液中のHMGB1タンパクを吸着する吸着材およびそれを用いた体液浄化カラムに関するものである。本発明は、ヒト体液中のHMGB1を除去することにより、敗血症などの病態を改善させる用途に好適に用いられる。
HMGB1タンパク(ハイモビリティーグループボックスタンパク1,HMG−1とも呼ばれる)は、真核細胞内に存在する非ヒストン性のDNA結合タンパクであり、本来細胞内でDNAに結合して転写の促進や細胞の増殖などの機能に関与する細胞内タンパクの一つである。
最近、このHMGB1が細胞外に分泌され、敗血症ショックの強力なメディエーターとして作用するという報告がなされた(たとえば、非特許文献1参照)。すなわち、マウスにリポポリサッカライド(LPS)を投与すると8−24時間後に血清中のHMGB1濃度が顕著に上昇しマウスは死に至る。精製したHMGB1自体をLPSと同時にマウスに投与した場合も相乗的に作用して致死活性を示すことから、HMGB1がエンドトキシンショックの重要なメディエーターとなることが示された。ヒトにおいても、敗血症患者血中でHMGB1濃度が顕著に上昇し、特に死亡例において高いことが示された。このため、患者血液中に存在するHMGB1の除去あるいは活性中和により、敗血症などのHMGB1の細胞外産生を伴う炎症性疾患を治療しうる可能性が示唆されている。また、HMGB1は癌の転移やリウマチ等の自己免疫疾患にも関与しているとの報告もある。 血液中のHMGB1を除去する方法として、HMGB1と結合する性質を持つ官能基を固定化した吸着材が報告されている。(WO01/074420。) HMGB1は、分子内にアニオン性のアミノ酸が30個程度連続して存在するカルボキシ末端領域があり、この部分でカチオン性の材料とイオン性相互作用で結合することが予想され、実際アミノ基を有する材料に効率よく吸着することが示されている。しかし、一方カチオン性の官能基は、白血球などの血液細胞との相互作用が強いことが知られており、このため全血を流した場合には、HMGB1だけでなく、生体の防御反応に必要な白血球、血小板などの血液細胞も吸着材により吸着除去されてしまうという問題点があった。
ワン(Wang H)他18名、「マウスにおけるエンドトキシン侵襲の後期メディエーターとしてのHMG−1(HMG−1 as a late mediator of endotoxin lethality in mice)」、(米国)、サイエンス(Science)、1999年、285巻、p248−251
ワン(Wang H)他18名、「マウスにおけるエンドトキシン侵襲の後期メディエーターとしてのHMG−1(HMG−1 as a late mediator of endotoxin lethality in mice)」、(米国)、サイエンス(Science)、1999年、285巻、p248−251
上述のように、体液中のHMGB1は敗血症などの疾患の病態と密接に関連することが示されており、体液中のHMGB1を高い効率で吸着除去し、かつ白血球、血小板などの生体反応に必要な血液細胞は除去しない性質を持つ吸着材の開発が強く望まれている。
かかる課題を解決するため検討を行った結果、本発明者らは、硫酸基、硫酸エステル基などのアニオン性基を固定化した吸着材が、HMGB1を高い効率で吸着するが、血球細胞を吸着しないことを見いだし、本発明に到達した。すなわち、本発明は以下のような構成を有する。
(1)アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする体液浄化用吸着材
(2)アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球および血小板のいずれも実質的に吸着しないことを特徴とする体液浄化用吸着材
(3)HMGB1を含有する体液を接触させた際に、HMGB1の吸着率が50%以上であり、かつ白血球および血小板の吸着率がいずれも20%以下であることを特徴とする、(1)−(2)いずれかに記載の体液浄化用吸着材
(4)前記不溶性担体に固定されているアニオン性基が硫酸基または硫酸エステル基であることを特徴とする、(1)−(3)のいずれかに記載の体液浄化用吸着材
(5)前記水不溶性担体がビーズ状の形状を持つことを特徴とする(1)−(4)のいずれかに記載の体液浄化用吸着材
(6)前記ビーズ状の水不溶性担体の平均粒径が50〜1000μmの範囲にあることを特徴とする(5)記載の体液浄化用吸着材
(7)(1)−(6)のいずれかに記載の体液浄化用吸着体を充填してなる体液浄化用カラム
(8)血液中にHMGB1が検出される疾患に用いられる(7)記載の体液浄化用カラム
(9)前記疾患が敗血症であることを特徴とする(7)記載の体液浄化用カラム
(10)(1)−(6)のいずれかに記載の吸着材と体液とを接触させて、体液中のHMGB1を該吸着材に吸着させることを含む体液中のHMGB1の除去方法
(1)アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする体液浄化用吸着材
(2)アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球および血小板のいずれも実質的に吸着しないことを特徴とする体液浄化用吸着材
(3)HMGB1を含有する体液を接触させた際に、HMGB1の吸着率が50%以上であり、かつ白血球および血小板の吸着率がいずれも20%以下であることを特徴とする、(1)−(2)いずれかに記載の体液浄化用吸着材
(4)前記不溶性担体に固定されているアニオン性基が硫酸基または硫酸エステル基であることを特徴とする、(1)−(3)のいずれかに記載の体液浄化用吸着材
(5)前記水不溶性担体がビーズ状の形状を持つことを特徴とする(1)−(4)のいずれかに記載の体液浄化用吸着材
(6)前記ビーズ状の水不溶性担体の平均粒径が50〜1000μmの範囲にあることを特徴とする(5)記載の体液浄化用吸着材
(7)(1)−(6)のいずれかに記載の体液浄化用吸着体を充填してなる体液浄化用カラム
(8)血液中にHMGB1が検出される疾患に用いられる(7)記載の体液浄化用カラム
(9)前記疾患が敗血症であることを特徴とする(7)記載の体液浄化用カラム
(10)(1)−(6)のいずれかに記載の吸着材と体液とを接触させて、体液中のHMGB1を該吸着材に吸着させることを含む体液中のHMGB1の除去方法
本発明により、体液中の有用な血球成分を除去せずに、生体に好ましくない細胞外のHMGB1を除去することが可能になる。
本発明の吸着材は、アニオン性の官能基が固定化された水不溶性担体からなり、血液、血漿、リンパ液、組織間液、腹水、滑膜液などの体液中に含まれるHMGB1を高い効率で吸着しかつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする。HMGB1を高い効率で吸着するとは、例えば直径0.7cm、流路長2.4cmの円筒状のカラムに2mlの吸着材を充填しHMGB1を含む全血を1〜2ml/分の流量で通過させた際に、カラムに流入したHMGB1のうちの50%以上が吸着されることをいい、好ましくは70%以上、さらに好ましくは90%以上が吸着されることをいう。また白血球または血小板を実質的に吸着しないとは、同条件でカラムに流入した白血球または血小板を20%以下しか吸着されないことをいい、好ましくは15%以下より好ましくは10%以下しか吸着されないことをいう。水不溶性担体に固定化されたアニオン性基としては、カルボキシル基、スルホン酸基、硫酸エステル基、リン酸基などの官能基が用いられる。特に、HMGB1の吸着性能が高いスルホン酸基または硫酸エステル基を固定化した担体が吸着材として望ましい。これらの官能基は、単独でも組み合わせても採用することができる。上述した官能基の密度は特に限定されないが、官能基が固定化された水不溶性担体の乾燥重量1gあたりの官能基の数(複数の官能基がある場合にはそれらの合計)が1μmol〜1mmol程度が好ましく、さらに好ましくは10μmol〜1mmol程度である。水不溶性担体に固定化されている官能基の数は、例えば元素分析を行うことにより決定できる。本発明に用いられる水不溶性担体の材料は、本発明に用いられる不溶性担体の材料は、ポリアミド、ポリイミド、ポリ(芳香族ビニル化合物)、ポリエステル、ポリメチルメタクリレート、ポリスルホン、ポリエチレン、ポリビニルアルコール、ポリテトラフルオロエチレンなどの合成高分子や、セルロース、コラーゲン、キチン、キトサン、デキストランおよびそれらの誘導体を含む天然高分子、などが好適に用いられる。さらに、金属、セラミックス、ガラスなどの無機材料を適当な高分子で被覆したり、表面を直接修飾したものも好適に用いられる。
本発明の材料の形状は、繊維状、中空糸状、ビーズ状、平膜状、粉状などを用いることができるが、特に血球と血漿を分離せずにカラムに循環する全血体外循環にも適した、繊維状、中空糸状あるいはビーズ状のものが好ましく用いられる。HMGB1の吸着率を上げるには、接触面積の大きい多孔性の材料が好ましい。また、ビーズとしては、カラムに充填した際の圧損が少なくかつ表面積の大きいものが良いので、粒径が50〜1000μmのものが好ましく、100〜700μmのものがさらに好ましい。粒径は、例えばコールターカウンターを用いることにより測定できる。ここでいうビーズとは、形状が球状であり、真球度が0.7以上であるものをいい、好ましくは0.8以上、より好ましくは0.9以上であるものをいう。真球度とは最短径(短径)と最長径(長径)との比(短径/長径)で定義され、この値が1.0に近づくほど真球度が高いことを意味する。例えば、上記のようなアニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする体液浄化用吸着材として、具体的には、粒径が50〜1000μmの範囲にあり、硫酸エステルを導入した球状セルロースのビーズが挙げられる。
このようなビーズは、セルロース粉末をチオシアン酸カルシウム溶液に溶解し、得られた液をソルビタンモノオレートを含むO−ジクロロベンゼンに滴下・撹拌することで球状セルロースを作製した後、得られた球状セルロースとN,N'−ジメチルホルムアルデヒド3酸化硫酸塩複合体を混合したのち、アルカリ溶液で中和し蒸留水で洗浄することで製造することができる。
本発明の材料のカラムへの充填方法は、繊維状材料であれば、織物、編物、不織布など布状の形態にして積層充填して、あるいは孔のあいた中空の中心パイプの周りに巻き付けて液を内側から外側に透過させる方法などが用いられる。
本発明の材料はカラムに充填することでHMGB1除去用体液浄化用カラムとして用いることが出来る。本発明の吸着材充填したカラムを用いてHMGB1を含む患者の体液を体外循環の方法で透過させることにより、敗血症などの疾患の治療を行うことが出来る。本吸着材を充填したカラムは細菌成分を吸着する血液浄化カラムと合わせて用いることにより、特に高い治療効果を得ることが期待できる。さらには、本吸着材はガン、自己免疫疾患などの治療にも好適に用いられ得る。
以下、本発明を実施例により更に具体的に説明するが本発明の範囲はこれらの実施例に限定されるものではない。
(実施例1)
インビトロでのヒト血液通過実験
セルロース粉末をチオシアン酸カルシウム溶液に加え、100℃に加熱して溶解した。得られた液を130℃に加熱したソルビタンモノオレートを含むO−ジクロロベンゼンに滴下し、撹拌することで造粒した。その後常温まで冷却し、メタノールを数回に分けて滴下することで洗浄したのち、大量の水で洗浄することで球状セルロースを得た。得られた球状セルロースとN,N'−ジメチルホルムアルデヒド3酸化硫酸塩複合体を20分×70℃および5時間×50℃にて混合したのち、アルカリ溶液で中和し蒸留水で洗浄することで硫酸化エステル基を導入した球状セルロースを得た。
得られた硫酸エステル基を硫黄原子含量として2.9%の密度で含有する平均粒子径224μmのセルローズビーズ2mlを直径0.7cm、流路長2.4cmの円筒状のカラムに充填し、20mlの生理食塩水で洗浄した。このカラムに、500μg/mlの精製HMGB1溶液を2500分の1容量および抗凝固剤として3.8%クエン酸ナトリウムを1/10容量添加した正常ヒト全血を1ml/分の流量で通過させ、通過後の血液を1mlずつチューブに回収した。 回収した血液は、直ちに血球計数器(日本光電製)を用いて白血球数および血小板数の測定を行った。
HMGB1濃度の定量は、血液サンプルを遠心分離して得た血漿画分をサンプルとして、ELISA法により行った。
(実施例1)
インビトロでのヒト血液通過実験
セルロース粉末をチオシアン酸カルシウム溶液に加え、100℃に加熱して溶解した。得られた液を130℃に加熱したソルビタンモノオレートを含むO−ジクロロベンゼンに滴下し、撹拌することで造粒した。その後常温まで冷却し、メタノールを数回に分けて滴下することで洗浄したのち、大量の水で洗浄することで球状セルロースを得た。得られた球状セルロースとN,N'−ジメチルホルムアルデヒド3酸化硫酸塩複合体を20分×70℃および5時間×50℃にて混合したのち、アルカリ溶液で中和し蒸留水で洗浄することで硫酸化エステル基を導入した球状セルロースを得た。
得られた硫酸エステル基を硫黄原子含量として2.9%の密度で含有する平均粒子径224μmのセルローズビーズ2mlを直径0.7cm、流路長2.4cmの円筒状のカラムに充填し、20mlの生理食塩水で洗浄した。このカラムに、500μg/mlの精製HMGB1溶液を2500分の1容量および抗凝固剤として3.8%クエン酸ナトリウムを1/10容量添加した正常ヒト全血を1ml/分の流量で通過させ、通過後の血液を1mlずつチューブに回収した。 回収した血液は、直ちに血球計数器(日本光電製)を用いて白血球数および血小板数の測定を行った。
HMGB1濃度の定量は、血液サンプルを遠心分離して得た血漿画分をサンプルとして、ELISA法により行った。
循環開始直後、4mlの血液通過後のいずれにおいても、HMGB1の吸着率は99%以上の高い数値であり、かつ白血球または血小板の吸着率は6%以下と低いレベルであった。
(実施例2)
ラット体外循環実験
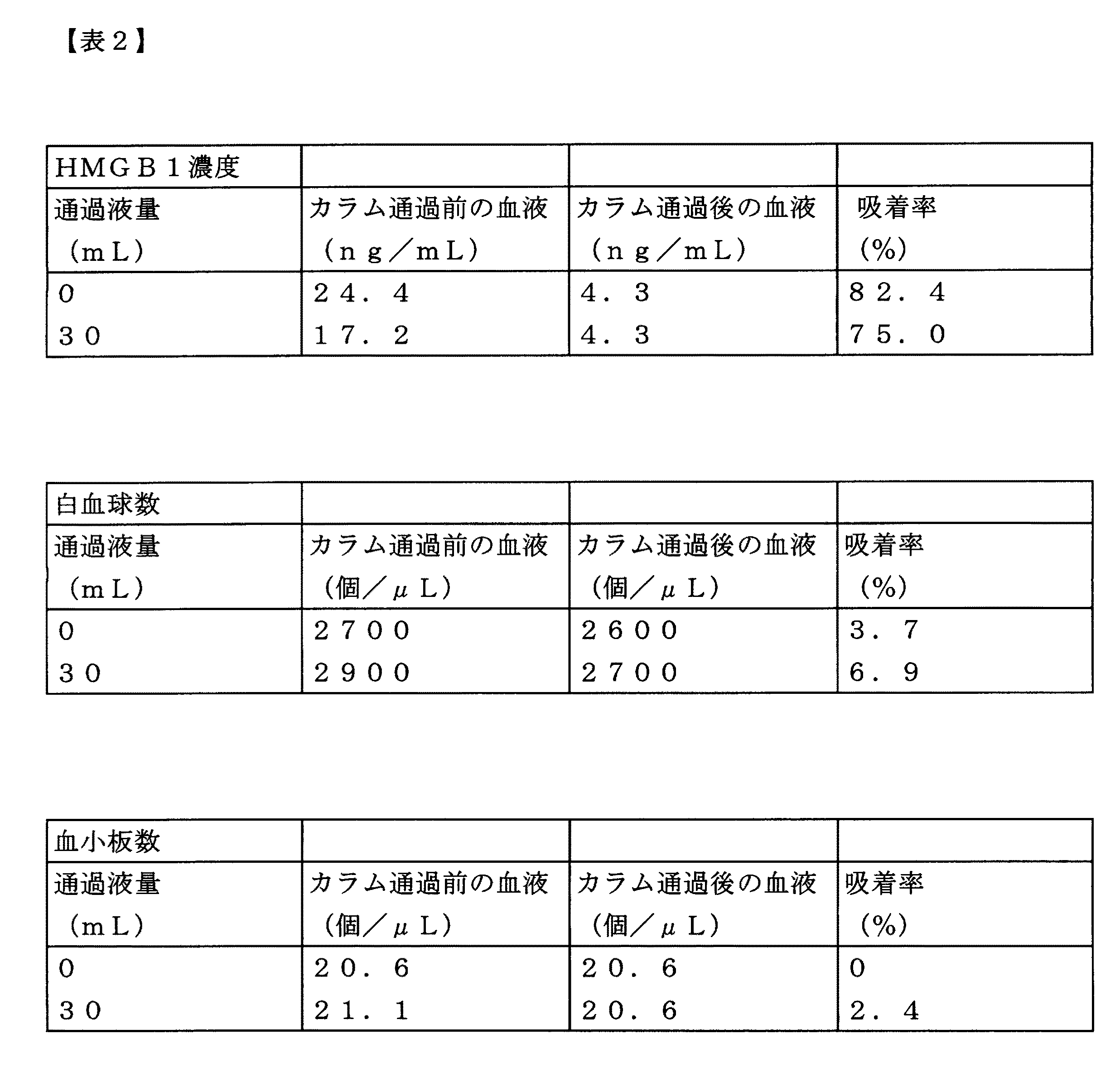
生理食塩水で10mg/mLに希釈したLPSを、オス、8週齢のWistar系ラット(体重300g)に150μL(投与量5mg/kg)静脈内投与した。LPS投与後6時間経過した時点で、上記実施例1のカラムを用いて体外循環を行った。体外循環は循環流量2mL/分で行い、循環時間を30分とした。血液サンプルは循環中のカラムの入側と出側にて0分(循環開始時)、30分(循環終了時)のタイミングで1mLずつチューブに回収した。回収した血液には抗凝固剤として3.8%クエン酸ナトリウムを1/10容量添加し、直ちに血球計数器(日本光電製)を用いて白血球数および血小板数の測定を行った。HMGB1濃度の定量は、血液サンプルを遠心分離して得た血漿画分をサンプルとして、ELISA法により行った。
(実施例2)
ラット体外循環実験
生理食塩水で10mg/mLに希釈したLPSを、オス、8週齢のWistar系ラット(体重300g)に150μL(投与量5mg/kg)静脈内投与した。LPS投与後6時間経過した時点で、上記実施例1のカラムを用いて体外循環を行った。体外循環は循環流量2mL/分で行い、循環時間を30分とした。血液サンプルは循環中のカラムの入側と出側にて0分(循環開始時)、30分(循環終了時)のタイミングで1mLずつチューブに回収した。回収した血液には抗凝固剤として3.8%クエン酸ナトリウムを1/10容量添加し、直ちに血球計数器(日本光電製)を用いて白血球数および血小板数の測定を行った。HMGB1濃度の定量は、血液サンプルを遠心分離して得た血漿画分をサンプルとして、ELISA法により行った。
循環開始直後、30分後(循環終了時)のいずれにおいても、HMGB1の吸着率は50%以上を保っており、かつ白血球または血小板の吸着率は20%以下に抑えられていた。
Claims (10)
- アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球または血小板の少なくともいずれかを実質的に吸着しないことを特徴とする体液浄化用吸着材。
- アニオン性の官能基が水不溶性担体に固定化されてなるHMGB1の吸着体で、体液中のHMGB1を高い効率で吸着し、かつ白血球および血小板のいずれも実質的に吸着しないことを特徴とする体液浄化用吸着材。
- HMGB1を含有する体液を接触させた際に、HMGB1の吸着率が50%以上であり、かつ白血球および血小板の吸着率がいずれも20%以下であることを特徴とする、請求項1−2いずれかに記載の体液浄化用吸着材。
- 前記不溶性担体に固定されているアニオン性基がスルホン酸基または硫酸エステル基であることを特徴とする、請求項1−3いずれかに記載の体液浄化用吸着材。
- 前記水不溶性担体がビーズ状の形状を持つことを特徴とする請求項1−4いずれかに記載の体液浄化用吸着材。
- 前記水不溶性担体がビーズ状の形状を持ち、その平均粒径が50〜1000μmの範囲にあることを特徴とする請求項5記載の体液浄化用吸着材。
- 請求項1−6のいずれかに記載の体液浄化用吸着材を充填してなる体液浄化用カラム。
- 体液中にHMGB1が検出される疾患に用いられる請求項7記載の体液浄化用カラム。
- 前記疾患が敗血症であることを特徴とする請求項8記載の体液浄化用カラム。
- 請求項1−6のいずれかに記載の吸着材と体液とを接触させて、体液中のHMGB1を該吸着材に吸着させることを含む体液中のHMGB1の除去方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004111963A JP2005296033A (ja) | 2004-04-06 | 2004-04-06 | 体液浄化用吸着材 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004111963A JP2005296033A (ja) | 2004-04-06 | 2004-04-06 | 体液浄化用吸着材 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005296033A true JP2005296033A (ja) | 2005-10-27 |
Family
ID=35328317
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004111963A Pending JP2005296033A (ja) | 2004-04-06 | 2004-04-06 | 体液浄化用吸着材 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005296033A (ja) |
-
2004
- 2004-04-06 JP JP2004111963A patent/JP2005296033A/ja active Pending
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2804920B2 (ja) | 全血及び/又は血漿から腫瘍壊死因子α及び細菌性リポ多糖類を同時体外除去する装置 | |
| EP3173145B1 (en) | Adsorbent for removing histone and purification device for liquid derived from living organism | |
| JP2006505385A (ja) | ポリマーアフィニティーマトリックス、その製造方法、及びその使用 | |
| WO2006106972A1 (ja) | 吸着材および体外循環用カラム | |
| JP4945876B2 (ja) | ハイモビリティーグループタンパクの吸着材および体液浄化カラム | |
| CN113509919B (zh) | 一种可用于清除脓毒症患者血液中内毒素和炎症因子的吸附剂及其制备方法 | |
| JP4578405B2 (ja) | 全血処理が可能な低密度リポ蛋白およびフィブリノーゲンの吸着材、及び吸着器 | |
| WO2019167441A1 (ja) | 毒素分離器具 | |
| JP3901216B2 (ja) | 腫瘍壊死因子−αの吸着剤、吸着除去方法および前記吸着剤を用いた吸着器 | |
| JP3926573B2 (ja) | フィブリノーゲンおよび/またはフィブリンの濃度を減少させるための吸着剤の製造法、吸着剤、および吸着装置の製造のための吸着剤の使用 | |
| JPWO1996025228A1 (ja) | 腫瘍壊死因子−αの吸着剤、吸着除去方法および前記吸着剤を用いた吸着器 | |
| JPH01171638A (ja) | 血清アミロイドa蛋白用吸着体 | |
| JPH0667472B2 (ja) | 血清アミロイドp蛋白用吸着体 | |
| Chen et al. | Functionalized carbon nanotube-embedded poly (vinyl alcohol) microspheres for efficient removal of tumor necrosis factor-α | |
| JP4983070B2 (ja) | 吸着材および体外循環用カラム | |
| JPH01119264A (ja) | 吸着体およびそれを用いた除去装置 | |
| JP2005296033A (ja) | 体液浄化用吸着材 | |
| JPH0977790A (ja) | 糖脂質抗体吸着材 | |
| CN116618024B (zh) | 一种清除过量铁调素的吸附剂及其制备方法 | |
| RU2448897C1 (ru) | Способ комплексной очистки физиологических жидкостей | |
| JPH01181875A (ja) | 免疫複合体の吸着体およびそれを用いた免疫複合体の除去装置 | |
| JP2014135976A (ja) | 塩基性線維芽細胞増殖因子の吸着材とその利用 | |
| JP5924637B2 (ja) | Pcsk9の吸着器 | |
| JP3084436B2 (ja) | 抗dna抗体の除去装置 | |
| JPH0771632B2 (ja) | 吸着体およびそれを用いた除去装置 |