JP2005283380A - バイオアベイラブルステロイドホルモンの測定方法 - Google Patents
バイオアベイラブルステロイドホルモンの測定方法 Download PDFInfo
- Publication number
- JP2005283380A JP2005283380A JP2004098637A JP2004098637A JP2005283380A JP 2005283380 A JP2005283380 A JP 2005283380A JP 2004098637 A JP2004098637 A JP 2004098637A JP 2004098637 A JP2004098637 A JP 2004098637A JP 2005283380 A JP2005283380 A JP 2005283380A
- Authority
- JP
- Japan
- Prior art keywords
- bioavailable
- testosterone
- shbg
- lectin
- steroid hormone
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
Abstract
【解決手段】 生体由来血清試料にレクチンを添加し、放置する工程を含むことを特徴とする、バイオアベイラブルステロイドホルモンの測定方法。
【選択図】 なし
Description
測定方法の概略:生体由来血清試料にレクチンのリン酸緩衝液(PBS)溶液を添加して混和し、室温にて放置する。その後、PBSでさらに希釈した後、凝集及び/又は沈殿物を除去し、溶液中に含まれる測定対象物を定量する。
実施例1:コンカナバリンAを用いたバイオアベイラブルテストステロンの測定
(1)測定条件、補正値等についての検討
(i)コンカナバリンAによる血清処理条件の検討
SHBGを凝集及び/又は沈殿させるためのコンカナバリンAの濃度及び反応時間について検討した。
まず、4本のプラスチックチューブそれぞれにボランティア健常男性の血清試料100μLを加え、それに125I−SHBG(セティカンパニーより購入、ヒト血清由来)をそれぞれ添加した。さらに、2.5%、5%、10%及び20%の濃度に調製したコンカナバリンA(アマシャムバイオサイエンシズより購入)のPBS(0.05mol/Lリン酸緩衝液、0.9%NaCl含有、pH7.4。以下、「PBS−1」という。)溶液50μLをそれぞれのチューブに加えて混和した。これらを室温にて1時間放置した後、PBS−1溶液500μLを加えて希釈し、遠心分離(4℃、3000rpm、10分)して、沈殿物に含まれる125I−SHBGの量をγ−カウンター(ARC−1000M、アロカ社)にて測定した。そして、添加した125I−SHBGの放射活性に対する測定値の割合を求めた。その結果を図1−A)に示す。
上記実験の結果、反応時間が1時間及び加えるコンカナバリンAのPBS−1溶液の濃度が5%のときに、SHBGの除去率が最大で約80%となることがわかった。
125I−SHBGを添加した後にコンカナバリンAにより処理した(血清試料100μLにコンカナバリンAの5%PBS−1溶液50μLを加えて混和し、室温にて1時間放置したもの。以下、単に「処理」という。)血清及び125I−SHBGを添加しコンカナバリンAで処理しない血清を、それぞれSephadex G100(アマシャムバイオサイエンスより購入、PBS−1に懸濁して調製)のカラムクロマトグラフィー(0.5×60cmのガラスカラム)に添加した。そして、移動相をPBS−1、流速を1mL/分とし、溶出物を2mLごとに分画してそれぞれの画分に含まれる125I−SHBG及びテストステロンを、γ−カウンター及び液体クロマトグラフィー/タンデム型質量分析装置(LC−MS/MS、QuattroII、マイクロマス社)により測定した。その結果を図2に示す。
バイオアベイラブルテストステロンの測定における補正値を得るため、血清中のアルブミンの回収率を求めた。
まず、14C−ヒトアルブミン(パーキンエルマーより購入)のPBS−1溶液(14C−ヒトアルブミンを適量のPBS−1に溶解したもの)1mLと、コンカナバリンAの10%水溶液1mLを混合し、14C−ヒトアルブミンを含有するコンカナバリンAの5%PBS溶液を調製した(以下、この溶液を「ConA5%液」という)。そして、ConA5%液50μLの放射活性を測定したところ、3770.7dpmであった。
ボランティア健常男性の血清試料100μLに、14C−ヒトアルブミン及び125I−SHBGを加え、これを、コンカナバリンAを結合させたSephadexカラム(アマシャムバイオサイエンスより購入、PBS−1溶液にて調製したもの)に添加した。そして、移動相をPBS−1、流速を1mL/分として、溶出画分に含まれる放射活性をシンチレーションカウンター及びγ−カウンターにて測定したところ、14C−ヒトアルブミンは殆んど溶出されたが、125I−SHBGは約20%しか溶出されなかった。溶出した20%の125I−SHBGは、前記(ii)の実験にて確認されたレクチン結合性糖鎖構造を有しないSHBGであると推察される。
コンカナバリンAを用いて、血清中のバイオアベイラブルテストステロンをLC−MS/MSにより測定した(以後、下記の方法を「ConA法」と呼ぶ)。
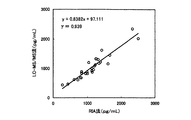
ボランティア健常男性の血清試料100μLにコンカナバリンAの5%PBS−1溶液50μLを加え、室温にて1時間放置した。その後、さらにPBS−1を500μL加え、遠心分離(4℃、3000rpm、10分)した。上清をエーテル5mLで抽出し、抽出物に2−フルオロ−N−メチルピリジニウム p−スルフォネート(2−FMS、東京化成より購入)の2%ジクロロメタン溶液200μL及びトリエチルアミンの10%ジクロロメタン溶液30μLを加え、室温にて1.5時間放置した。次いで、溶媒を窒素ガスで留去した後、25%メタノール水溶液1mLに溶解し、これを、予めメタノール6mL及び精製水6mLで調製したBond Elut C18カラムに添加した。このカラムを、精製水1mL、0.3%アンモニア水3mL、メタノール2mL及び0.01%ギ酸:メタノール=1:1混合液3mLで順次洗浄した後、10%ギ酸:アセトニトリル=1:4混合液2.5mLにて溶出した。溶出液を減圧下にて留去後、0.05%ギ酸:メタノール=3:2混合液100μLに溶解して、そのうちの10μLをLC−MS/MSに注入した。そして、観察された測定イオン(m/z)=253の強度より、2H3−テストステロン(シグマより購入)を内部標準としたテストステロンの強度と量の関係を示す検量線に基づき、試料中のテストステロンの量を求めた。その結果を、後で述べるRIAによるバイオアベイラブルテストステロンの測定における結果と合わせて、表2に示す。また、LS−MS/MSによる測定値とRIAによる測定値との相関を、図3に示す。図3より、LC−MS/MSによる測定値とRIAによる測定値とは良好な相関を示すことがわかる。
上記(2)で得られた上清を用い、そこに含まれるテストステロンの量をRIA測定キット(三菱ヤトロンより購入)を用いて測定した。その結果を、上記(2)における結果と合わせて、下記表2に示す。
本実験においては、上記(2)及び(3)で使用したのと同じボランティア健常男性の血清試料を用いた。
血清試料300μLに飽和硫酸アンモニウム水溶液300μLを加えて混和し、4℃にて10分間放置した。その後、遠心分離(4℃、1100×g、30分)し、その上清に含まれるテストステロンを上記(2)と同様にして測定した。その結果を、後述するISSAM法との比較における項の表3において示す。
上記(2)〜(4)で使用したのと同じ血清試料を用いて、ISSAM法によりバイオアベイラブルテストステロンの値を測定した。すなわち、血清中の総テストステロンをLC−MS/MSにて、また、総SHBGをRIAにて定量し、それぞれの値をISSAM法の計算式(http://www.issam.ch/freetesto.htmを参照)に代入した。そして、アルブミンの量を4.3g/100mLとして、バイオアベイラブルテストステロンの値を算出した。その結果を、下記表3において、ConA法及び硫安沈殿法における結果と合わせて示す。
Claims (11)
- 生体由来血清試料にレクチンを添加し、放置する工程を含むことを特徴とする、バイオアベイラブルステロイドホルモンの測定方法。
- レクチンを用いて、生体由来血清試料中のSHBG結合型ステロイドホルモンを、レクチン結合性糖鎖構造を有するタンパク質と一緒になって凝集及び/又は沈殿させる工程を含むことを特徴とする、バイオアベイラブルステロイドホルモンの測定方法。
- レクチンがコンカナバリンAである、請求項1又は2のいずれか1項に記載の方法。
- バイオアベイラブルステロイドホルモンが、バイオアベイラブルテストステロンである、請求項1〜3のいずれか1項に記載の方法。
- レクチンを含むことを特徴とする、バイオアベイラブルステロイドホルモン測定用試薬。
- レクチンが、コンカナバリンAである、請求項5に記載の試薬。
- 請求項1〜4のいずれか1項に記載の方法に用いるための、請求項5又は6に記載の試薬。
- 請求項5〜7のいずれか1項に記載の試薬を含む、バイオアベイラブルステロイドホルモンの測定キット。
- 請求項5〜7のいずれか1項に記載の試薬を含む、血中バイオアベイラブルステロイドホルモン値に顕著な影響を及ぼす疾患の鑑別キット。
- 請求項1〜4のいずれか1項に記載の方法を用いることを特徴とする、血中バイオアベイラブルステロイドホルモン値に顕著な影響を及ぼす疾患の鑑別方法。
- 血中バイオアベイラブルステロイドホルモン値に顕著な影響を及ぼす疾患が、パダム(Partia1 Androgen Deficiencyin Aging Ma1e)である、請求項10に記載の鑑別方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004098637A JP2005283380A (ja) | 2004-03-30 | 2004-03-30 | バイオアベイラブルステロイドホルモンの測定方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004098637A JP2005283380A (ja) | 2004-03-30 | 2004-03-30 | バイオアベイラブルステロイドホルモンの測定方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005283380A true JP2005283380A (ja) | 2005-10-13 |
| JP2005283380A5 JP2005283380A5 (ja) | 2007-03-22 |
Family
ID=35181929
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004098637A Pending JP2005283380A (ja) | 2004-03-30 | 2004-03-30 | バイオアベイラブルステロイドホルモンの測定方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005283380A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011506965A (ja) * | 2007-12-13 | 2011-03-03 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストロンを検出するための方法 |
| JP2014238419A (ja) * | 2007-11-27 | 2014-12-18 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストラジオールを検出するための方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6283666A (ja) * | 1985-10-04 | 1987-04-17 | ダイアグノステイツク プロダクツ コ−ポレ−シヨン | 生物学的液体中の遊離リガンドの測定方法および測定用キツト |
| JPH02502632A (ja) * | 1986-12-22 | 1990-08-23 | トリオン、フォルスクニング‐オホ、ウトベクリングス、アクチェボラーグ | 新規ポリペプチド及びその用途 |
| WO1999034213A1 (fr) * | 1997-12-25 | 1999-07-08 | Mochida Pharmaceutical Co., Ltd. | Analyseur pour echantillons liquides |
| JP2001343387A (ja) * | 2000-03-31 | 2001-12-14 | Shino Test Corp | 複合体を形成する物質の測定方法及び測定試薬 |
| WO2002061437A2 (en) * | 2001-01-30 | 2002-08-08 | Ken Adams | Method and system for diagnosing andropause in males |
| JP2003302404A (ja) * | 2002-04-09 | 2003-10-24 | Toyobo Co Ltd | レセプターの固定化方法、並びにその方法により製造されたレセプター組成物 |
-
2004
- 2004-03-30 JP JP2004098637A patent/JP2005283380A/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6283666A (ja) * | 1985-10-04 | 1987-04-17 | ダイアグノステイツク プロダクツ コ−ポレ−シヨン | 生物学的液体中の遊離リガンドの測定方法および測定用キツト |
| JPH02502632A (ja) * | 1986-12-22 | 1990-08-23 | トリオン、フォルスクニング‐オホ、ウトベクリングス、アクチェボラーグ | 新規ポリペプチド及びその用途 |
| WO1999034213A1 (fr) * | 1997-12-25 | 1999-07-08 | Mochida Pharmaceutical Co., Ltd. | Analyseur pour echantillons liquides |
| JP2001343387A (ja) * | 2000-03-31 | 2001-12-14 | Shino Test Corp | 複合体を形成する物質の測定方法及び測定試薬 |
| WO2002061437A2 (en) * | 2001-01-30 | 2002-08-08 | Ken Adams | Method and system for diagnosing andropause in males |
| JP2003302404A (ja) * | 2002-04-09 | 2003-10-24 | Toyobo Co Ltd | レセプターの固定化方法、並びにその方法により製造されたレセプター組成物 |
Non-Patent Citations (2)
| Title |
|---|
| JPN6009041052, 石井延久, 永尾光一, 加藤聡彦, "診断のための検査", モダンフィジシャン, 20040315, Vol.24/No.3, 279−281, JP, 新興医学出版社 * |
| JPN6009041053, J. M. G. BONFRER, P. F. BRUNING, W. J. NOOIJEN, "A SIMPLE METHOD FOR THE MEASUREMENT OF THE STEROID FRACTION BOUND TO SEX HORMONE BINDING GLOBULIN IN", Journal of steroid Biochemistry, 19890209, Vol.33/No.2, 227−231, GB, Pergamon Press * |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014238419A (ja) * | 2007-11-27 | 2014-12-18 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストラジオールを検出するための方法 |
| JP2017198703A (ja) * | 2007-11-27 | 2017-11-02 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストラジオールを検出するための方法 |
| JP2020112562A (ja) * | 2007-11-27 | 2020-07-27 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストラジオールを検出するための方法 |
| JP7199392B2 (ja) | 2007-11-27 | 2023-01-05 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストラジオールを検出するための方法 |
| JP2011506965A (ja) * | 2007-12-13 | 2011-03-03 | クエスト ダイアグノスティックス インヴェストメンツ インコーポレイテッド | 質量分析によってエストロンを検出するための方法 |
| US8916385B2 (en) | 2007-12-13 | 2014-12-23 | Quest Diagnostics Investments, Inc. | Methods for detecting estrone by mass spectrometry |
| US9678087B2 (en) | 2007-12-13 | 2017-06-13 | Quest Diagnostics Investments Incorporated | Methods for detecting estrone by mass spectrometry |
| US10422804B2 (en) | 2007-12-13 | 2019-09-24 | Quest Diagnostics Investments Incorporated | Methods for detecting estrone by mass spectrometry |
| US11280798B2 (en) | 2007-12-13 | 2022-03-22 | Quest Diagnostics Investments Incorporated | Methods for detecting estrone by mass spectrometry |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ke et al. | A sensitive, simple and robust LC–MS/MS method for the simultaneous quantification of seven androgen-and estrogen-related steroids in postmenopausal serum | |
| Shea et al. | Free testosterone: clinical utility and important analytical aspects of measurement | |
| Murphy | Some studies of the protein-binding of steroids and their application to the routine micro and ultramicro measurement of various steroids in body fluids by competitive protein-binding radioassay | |
| Holst et al. | Steroid hormones: relevance and measurement in the clinical laboratory | |
| Dechaud et al. | Radioimmunoassay of testosterone not bound to sex-steroid-binding protein in plasma. | |
| USRE44401E1 (en) | Thyroid hormone analysis by mass spectrometry | |
| US8227259B2 (en) | Free thyroxine and free triiodothyronine analysis by mass spectrometry | |
| Søeborg et al. | Serum concentrations of DHEA, DHEAS, 17α-hydroxyprogesterone, Δ4-androstenedione and testosterone in children determined by TurboFlow-LC–MS/MS | |
| Higashi | Salivary hormone measurement using LC/MS/MS: specific and patient-friendly tool for assessment of endocrine function | |
| Jänne et al. | Assay of estosterone progesterone and 17α-hydroxyprogesterone in human plasma by radioimmunoassay after separation on hydroxyalkoxypropyl sephade | |
| Demers | Androgen deficiency in women; role of accurate testosterone measurements | |
| Dury et al. | Validated LC–MS/MS simultaneous assay of five sex steroid/neurosteroid-related sulfates in human serum | |
| Higashi et al. | Salivary chenodeoxycholic acid and its glycine-conjugate: their determination method using LC–MS/MS and variation of their concentrations with increased saliva flow rate | |
| Sizonenko et al. | Hormonal changes during puberty: IV. Longitudinal study of adrenal androgen secretions | |
| WO2015161078A1 (en) | Methods for comprehensive profiling of steroid metabolome | |
| Starcevic et al. | Liquid chromatography–tandem mass spectrometry assay for human serum testosterone and trideuterated testosterone | |
| Bruce et al. | Discrepancy between radioimmunoassay and high performance liquid chromatography tandem-mass spectrometry for the analysis of androstenedione | |
| Higashi et al. | Determination of salivary dehydroepiandrosterone using liquid chromatography–tandem mass spectrometry combined with charged derivatization | |
| US20200003795A1 (en) | Determination of analytes in liquid samples by mass spectrometry | |
| Lapčı́k et al. | Immunoassay of 7-hydroxysteroids: 2. Radioimmunoassay of 7α-hydroxy-dehydroepiandrosterone | |
| Higashi | Trace determination of steroids causing age-related diseases using LC/MS combined with detection-oriented derivatization | |
| Liu et al. | Development and validation of a sensitive LC-MS/MS method for simultaneous quantification of thirteen steroid hormones in human serum and its application to the study of type 2 diabetes mellitus | |
| WO2012087438A1 (en) | Methods for simultaneous quantification of thyroid hormones and metabolites thereof by mass spectrometry | |
| JP3774888B2 (ja) | ステロイド類化合物のlc−msによる高感度検出法 | |
| Agrawal et al. | LC-MS/MS based quantification of steroidal biomarkers in polycystic ovary syndrome induced rats |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070206 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070206 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20090217 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090818 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091014 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100511 |