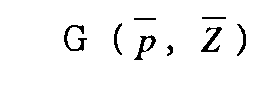JP2004132964A - 試験片較正コードを記憶している一定のメモリーを有する診断キットおよび関連の方法 - Google Patents
試験片較正コードを記憶している一定のメモリーを有する診断キットおよび関連の方法 Download PDFInfo
- Publication number
- JP2004132964A JP2004132964A JP2003296598A JP2003296598A JP2004132964A JP 2004132964 A JP2004132964 A JP 2004132964A JP 2003296598 A JP2003296598 A JP 2003296598A JP 2003296598 A JP2003296598 A JP 2003296598A JP 2004132964 A JP2004132964 A JP 2004132964A
- Authority
- JP
- Japan
- Prior art keywords
- calibration
- test strip
- area
- codes
- certain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000012360 testing method Methods 0.000 title claims abstract description 253
- 238000009007 Diagnostic Kit Methods 0.000 title claims abstract description 90
- 230000015654 memory Effects 0.000 title claims abstract description 38
- 238000000034 method Methods 0.000 title claims description 47
- 238000013139 quantization Methods 0.000 claims abstract description 46
- 239000012530 fluid Substances 0.000 claims abstract description 23
- 239000003153 chemical reaction reagent Substances 0.000 claims description 31
- 238000003149 assay kit Methods 0.000 claims description 8
- 238000004458 analytical method Methods 0.000 claims description 5
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 44
- 239000008103 glucose Substances 0.000 description 44
- 239000008280 blood Substances 0.000 description 43
- 210000004369 blood Anatomy 0.000 description 43
- 239000000523 sample Substances 0.000 description 22
- 230000006870 function Effects 0.000 description 21
- 238000005259 measurement Methods 0.000 description 19
- 238000009826 distribution Methods 0.000 description 17
- DLURHXYXQYMPLT-UHFFFAOYSA-N 2-nitro-p-toluidine Chemical compound CC1=CC=C(N)C([N+]([O-])=O)=C1 DLURHXYXQYMPLT-UHFFFAOYSA-N 0.000 description 15
- 238000000840 electrochemical analysis Methods 0.000 description 13
- 238000004422 calculation algorithm Methods 0.000 description 12
- 102100027378 Prothrombin Human genes 0.000 description 10
- 108010094028 Prothrombin Proteins 0.000 description 10
- 229940039716 prothrombin Drugs 0.000 description 10
- 230000008859 change Effects 0.000 description 8
- 238000010586 diagram Methods 0.000 description 7
- 230000003287 optical effect Effects 0.000 description 7
- 239000011159 matrix material Substances 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 238000003860 storage Methods 0.000 description 6
- 238000011156 evaluation Methods 0.000 description 3
- 238000005457 optimization Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000003556 assay Methods 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 238000001712 DNA sequencing Methods 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 230000015271 coagulation Effects 0.000 description 1
- 238000005345 coagulation Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/4875—Details of handling test elements, e.g. dispensing or storage, not specific to a particular test method
- G01N33/48771—Coding of information, e.g. calibration data, lot number
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/10—Composition for standardization, calibration, simulation, stabilization, preparation or preservation; processes of use in preparation for chemical testing
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/10—Composition for standardization, calibration, simulation, stabilization, preparation or preservation; processes of use in preparation for chemical testing
- Y10T436/104998—Glucose, ketone, nitrate standard or control
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Pathology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Biophysics (AREA)
- Biotechnology (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
【課題】一定の流体サンプルの特性を測定するための一定の診断キットを提供する。
【解決手段】一定の流体サンプルの特性を測定するための一定の診断キットが一定の試験片および当該試験片の一定の特性を測定するための装置を備えている。上記装置はまた、上記試験片の測定された特性に基づいて、当該試験片に供給される一定のサンプルの一定の特性も計算する。この装置における一定のメモリー内に保管されるものとして、複数の試験片較正コードがあり、これらのコードは一定の多次元的な較正パラメーターの区域における複数の幾何学的領域を示す。これらの試験片較正コードおよび幾何学的領域は、上記試験片に対する当該試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように、上記多次元的な較正パラメーターの区域にわたり分布される。
【選択図】図1
【解決手段】一定の流体サンプルの特性を測定するための一定の診断キットが一定の試験片および当該試験片の一定の特性を測定するための装置を備えている。上記装置はまた、上記試験片の測定された特性に基づいて、当該試験片に供給される一定のサンプルの一定の特性も計算する。この装置における一定のメモリー内に保管されるものとして、複数の試験片較正コードがあり、これらのコードは一定の多次元的な較正パラメーターの区域における複数の幾何学的領域を示す。これらの試験片較正コードおよび幾何学的領域は、上記試験片に対する当該試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように、上記多次元的な較正パラメーターの区域にわたり分布される。
【選択図】図1
Description
本発明は一般に一定の流体サンプルの特性の測定のための診断キットに関連しており、特に、試験片較正コードを含む診断キットおよび関連の方法に関連している。
一定の流体サンプルの特性の測定のための一般的な診断キットは一定の手持型計器等のような一定の装置、および一定のサンプルが供給される一定の試験片(例えば、一定の廃棄可能な血液グルコース試験片)を含む。この装置および試験片は流体サンプルにおける一定物の濃度(例えば、血液グルコース濃度)またはその他の特性(例えば、プロトロンビン時間(PT)および/または国際標準化比率(INR))を測定するために連携して用いられている。この装置は一般的に一定の試験片の1種類以上の特性(例えば、一定の光学的反射率、光学的透過率または一定の電気化学的特性)を測定した後にその測定した1種類以上の特性に基づいてその特徴を計算するための一定のアルゴリズムを採用する。このような従来的な診断キットは、例えば、2000年7月4日に発行されている特許文献1、2001年7月17日に発行されている特許文献2、2002年3月14日に出願されている特許文献3において記載されおり、これらはそれぞれ本明細書において参考文献として含まれており、さらに、特許文献4および特許文献5において記載されている。
上記のような診断キットにおける各種試験片のロット間における変化を考慮するために、これらの製造中に各試験片のロットが較正されることが一般的である。このような較正は一般的に各試験片のロットに対して、各種の較正パラメーターの決定およびこれらの較正パラメーターに付随している一定の試験片の較正コードの割り当てを含む。例えば、一定のロットのプロトロンビン試験片に対して一定の試験片較正コードを割り当てるために、凝固およびPTの較正パラメーターを各種の直交回帰ルーチンを用いて実験的に決定できる。このような直交回帰ルーチンにおいて、各種の実験的な試験結果と基準の試験結果との間のバイアス(偏り)が種々の較正パラメーターを調節することにより一定の二乗和関数を用いて最小化される。このような直交回帰ルーチンの結果は一組の経験的な較正パラメーターになる。これらの較正係数が較正コードとして割り当てられると、無限数の較正コードが存在することになる。そこで、有限の管理可能な数の較正コードを作成するために、上記の経験的な較正パラメーターをその後に変換して一定の予め定められている較正パラメーター・テーブル内に含まれている最も近い較正パラメーターに一致させるようにする。その後、この最も近い較正パラメーターに付随する一定の較正コードがそのプロトロンビン試験片のロットに割り当てられる。
各種のプロトロンビン試験片に関連する上記のような較正技法を含む一定の試験片のロットに対して試験片較正コードを割り当てる従来的な技法は(i)極端な各種の実験結果に対して過度に影響を受けやすい一定の二乗和関数を採用していること、(ii)必ずしも適正であるとは限らない実験的に決定されている各種の較正パラメーターに最も近い予め定められている較正パラメーター・テーブルによる較正パラメーターが最適であると仮定していることにおける欠陥を有している。これらの欠陥により、従来的な技法により各種の較正パラメーターに付随している(それゆえ、各種の試験片ロットに付随している)各種の試験片較正コードを採用している一定の診断キットを用いて得られる結果の精度は最適でない可能性がある。
加えて、特定の状況下において、一定の試験片ロットに対する一定の試験片較正コードの以前の割り当てを確かめるためにその試験片ロットを再較正することが望ましいと考えられる。しかしながら、個々の試験片の較正コードが過度に密接して離れている各種の較正パラメーター(すなわち、わずかな解像度の増加分だけで分離している各種の較正パラメーター)に付随している場合に、以前に割り当てられていた試験片の較正コードとは異なる一定の試験片の較正コードが再較正時に一定の試験片ロットに割り当てることが有り得る。このことは、上記の再較正が適正に行なわれている場合でも、有限数の較正エラーがその再較正に伴うので、起こり得ることである。このような再較正時における一定の異なる試験片較正コードの割り当てにおいて起こり得る不一致が一定の試験片ロットに対する一定の試験片較正コードの割り当てにおける確認を複雑化している。
一定の流体サンプルの特性を測定するために一定の診断キットを用いる場合に、その試験片に割り当てられる試験片較正コードはその装置が上記特性を計算する場合に使用するための各種の較正パラメーターを得ることを可能にする。一定の試験片に対して割り当てられる試験片較正コードをその装置に伝達するために採用できる幾つかの技法が存在している。これらの技法は一定の数字の試験片較正コードを選択するために上記装置における一定のボタンを使用すること、一定の試験片較正コードを伴う一定の集積回路の装置内への挿入、受動的な電子部品(例えば、各種の抵抗器)を採用している一定の試験片較正コードを伴う一定の試験片の装置内への挿入、隣接遠隔測定法、および一定のバーコードまたは読取専用記憶装置(ROM)集積回路(例えば、特許文献6、特許文献7および特許文献8を参照されたい)の使用を含む。一般に、最も簡単で最も安価な技法は一定の使用者が一定の装置における一定の較正コード・ボタンを押すことによりその装置に一定の試験片較正コードを伝達することである。しかしながら、この技法を実用的にするためには、上記装置が最小数の試験片較正コード(例えば、100個以下の試験片較正コード、さらに好ましくは50個以下の試験片較正コード)を採用することが望ましい。これ以外の方法では、上記試験片較正コードを一定の装置に伝達することはその使用者にとって手間のかかることになり、その使用者のエラーの可能性が過度に高まる。一方、一定の診断キットの全体の精度を維持するためには十分な数の試験片較正コードが必要である。
米国特許第6,084,660号明細書
米国特許第6,261,519号明細書
米国特許出願第10/100,531号明細書
PCT国際公開第WO 02/48707A2号
PCT国際公開第WO 01/57510A2号
米国特許第5,489,414号明細書
米国特許第5,366,609号明細書
欧州特許第0880407B1号明細書
それゆえ、この技術分野において依然として要望されていることは最小数の試験片較正コードの使用を可能にして、各種の較正パラメーターに対して最適に付随し、さらに、各種の試験片ロットに対して最適に付随する各種の試験片較正コードを採用している診断キットである。それゆえ、同様に要望されていることは各種の試験片較正コードを各種の較正パラメーターに対して最適に付随させるための一定の方法である。
本発明は各種の較正パラメーターに対して最適に付随する各種の試験片較正コードを含み、それゆえ、一定の最小数の試験片較正コードの使用を可能にする一定の診断キットを提供している。これらの試験片較正コードは各種の較正パラメーターに対して最適に付随するので、これらの試験片較正コードは試験片の較正中における一定の試験片のロットに対しても最適に割り当てられる。
本発明に到達する際に、各試験片較正コードが一定の多次元的な較正パラメーターの区域(例えば、一定の二次元の較正パラメーターの区域)の幾何学的な領域を示すことが認識されている。さらに、上記の多次元的な較正パラメーターの区域が一定の特異的な較正コードにそれぞれ付随している幾つかの非重合性の幾何学的領域により構成されていることが認識されている。また、各幾何学的領域に付随している較正コードの分布およびその較正コードの割り当てが必然的に最適に減少されている一定の「量子化エラー(quantization error)」を導くことも認識されている。このような量子化エラーはまた測定されている各種の較正係数に対して一致しない一定の試験片に対して一定の試験片較正コードを割り当てることにより一定の診断キットの性能に導入されるエラー(誤差)としても考えることもできる。さらに、上記量子化エラーが各種の較正係数の測定に付随する試験誤差に対して相当な量を当然に加えないことが認識されている。
また、上記量子化エラーが各種の較正係数の測定における試験誤差の程度まで最適に減少されるような各種の試験片較正パラメーターの分布および多次元的な較正パラメーターの区域にわたる各種の幾何学的領域が最も効率的な構成を提供することも認識されている。このような効率的な構成は一定の最小数の試験片較正コードの使用および各種較正パラメーターに対する各種試験片較正コードの最適な付随を可能にする。加えて、試験誤差による各種較正パラメーターの測定における不確定性を理解することによる重なりの最小化により、再較正における特定の試験片ロットに対する一定の異なる試験片較正コードの割り当ての可能性が最小化される。このことは、各較正コードに付随する幾何学的領域が各種較正コードの測定における不確定性により重なり合う領域と同等の領域を示すことができるために、起こり得る。
さらに、各種試験片較正コードと一定の試験片較正コードにより示される幾何学的領域の境界との間における解像度の増加が上記多次元的な較正パラメーターの区域内における試験片較正コードの数を定めることが認識されている。この解像度の増加は、例えば、一定の診断キットの全体的な精度の要求条件による上限値に制限できる。この解像度の増加が過度に大きいと、各種較正パラメーターに対する試験片較正コードの割り当てに起因する上記の量子化エラーが不所望に大きくなる。しかしながら、上記解像度の増加が過度に小さければ(例えば、較正誤差がその解像度の増加よりも大きければ)、不要に大きな数の較正コードの結果および再較正における不一致が起こり得る。
上述した理由により、本発明による診断キットは各種の試験片較正コードおよび一定の多次元的な較正パラメーターの区域にわたり最適に分布されている各種の幾何学的領域を含む。このような最適化は試験片較正コードの数を最小化すると共に量子化エラーを最適に減少するために各種試験片較正コードに対応する解像度の一定の増加および各試験片較正コードにより示される幾何学的領域の形状(例えば、境界)を適当に定めることを含む。適当な幾何学的領域の例は各種の六角形、平行四辺形、長方形、およびその他の類似の多角形の構造等である。
本発明の例示的な実施形態による一定の流体サンプルの特性を測定するための一定の診断キットは一定の試験片および当該試験片における1種類以上の特性(例えば、一定の光学的または電子化学的な特性)を測定するための装置(一定の手持型計器等)を含む。この装置はまた上記試験片における1種類以上の特性に基づいて当該試験片に供給される一定の流体サンプルの特性(例えば、上記のPTおよびINR)も計算する。
上記装置は内部に保管されている複数の試験片較正コードを伴う一定のメモリーまたは記憶装置を含む。このメモリー内に保管されている複数の試験片較正コードのそれぞれは一定の多次元的な較正パラメーターの区域における一定の幾何学的領域を示す。加えて、上記複数の試験片較正コードおよび幾何学的領域は上記試験片に対する複数の試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように上記多次元的な較正パラメーターの区域にわたり分布している。
上記量子化エラーの最適な減少は、例えば、所定の量子化エラーの各制限値を維持しながら一定の最小数の試験片較正コードを上記メモリー内に保管するように各種試験片較正コードの分布および各試験片較正コードにより示される幾何学的領域の形状を最適化する処理を含む。この最適化処理において採用される所定の量子化エラーの各制限値は、例えば、全体の診断キットの精度の要求条件および各種較正係数の測定における試験誤差の一定の評価に基づくことができる。例えば、これらの量子化エラーの制限値は全体の診断キットの精度の要求条件の一部分(例えば、1/5または1/12等)に基づくことができる。
上記の各種試験片較正コードおよび幾何学的領域は上記量子化エラーを最適に減少することに基づいて各種精度の要求条件に直接的に関連している一定の様式で分布しているので、各較正パラメーターはそれぞれの試験片較正コードに必ずしも付随しない。このことは、上記診断キットにより、特定の較正パラメーターの組み合わせが一定の自己補正効果を有することができるので、診断キットの性能の精度が最も近い試験片較正パラメーターを割り当てることなく最適化できるために有益的である。
さらに、一定の試験片および一定のメモリーを伴う一定の装置を含む一定の診断キットにおいて使用するための各種の較正パラメーターに各種の試験片較正コードを最適に付随させるための一定の方法も本発明により提供されている。この方法は上記試験片に対する複数の試験片較正コードの内の1個を割り当てることにおける一定の量子化エラーを最適に減少するように一定の較正パラメーターの区域にわたり複数の試験片較正コードおよびこれらにより示される各種の幾何学的領域を最適に分布する処理を含む。このように分布された上記複数の試験片較正コードはその後に上記診断キットにおける一定のメモリー内に保管される。
従って、本発明によれば、最小数の試験片較正コードの使用を可能にして、各種の較正パラメーターに対して最適に付随し、さらに、各種の試験片ロットに対して最適に付随する各種の試験片較正コードを採用している診断キットが提供でき、さらに、各種の試験片較正コードを各種の較正パラメーターに対して最適に付随させるための一定の方法が提供できる。
本明細書の全体を通して一貫するために、さらに、本発明の明瞭な理解のために、本明細書において用いられている一定の用語に対して以下の定義が備えられている。
用語の「量子化エラー(quantization error)」は測定されている各較正係数に一致しない一定の試験片に対する一定の試験片較正コードの割り当てに付随する誤差を意味する。このような量子化エラーは一定の多次元的な較正パラメーターの区域にわたる各種の試験片較正コードおよびこれら試験片較正コードにより示される幾何学的領域に対して非対称的に関連している。それゆえ、この量子化エラーは一定の多次元的な較正パラメーターの区域における一定の全体の幾何学的領域を示す一定の試験片較正コードを有することに付随する一定の誤差として考えることもできる。この説明内容によれば、上記量子化エラーは一定の較正誤差として表現することも可能である。
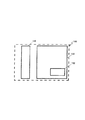
図1は一定の流体サンプルの特性を測定するための一定の診断キット100(各点線の内部に含まれている)を示している簡単化したブロック図である。この診断キット100は一定の試験片110および当該試験片110の特性を測定してその測定から上記流体サンプルの特性を計算するための一定の装置120を備えている。
当該技術分野における熟練者であれば、本発明による各種の診断キットが種々のサンプル、流体またはその他の組織および排出物などのような生物学的サンプルを含む物質に対する使用に適合可能であることが認識できる。加えて、本発明の各種の実施形態が一定範囲のアッセイ用のキット、または当該技術分野における熟練者において知られている生物学的またはその他のキットに適合可能であることも考慮されている。適当なアッセイ用のキットはDNAシーケンス化、タンパク質分析、薬物の発見および薬剤の開発等において採用されるキットを含む。このような適当なアッセイ用のキットは各種の試薬(例えば、液体状の試薬および凍結乾燥処理した試薬)および一定のサンプルの所定の分析を行なうために上記試薬に関連して用いられる一定の分析装置を含む。本発明を知ることにより、上記のようなアッセイ用のキットにより得られる結果の精度が各種の試薬較正用のコードの使用により改善できることが認識されると考える。さらに、上記分析装置内に含まれる一定のメモリーは複数の試薬較正コードをその内部に保管することができ、これら試薬較正コードのそれぞれは一定の較正パラメーターの区域における一定の幾何学的領域を示す。さらに、これらの試薬較正コードおよび幾何学的領域は一定の試薬に対する当該試薬較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように上記の較正パラメーターの区域にわたり分布することができる。
本発明による診断キットは上記試験片110に供給される各種流体サンプル中の特定の分析物の濃度および/または当該試験片110に供給される一定の流体サンプル中の化学的特性(例えば、pH値またはアルカリ度)を含むがこれらに限らない当該技術分野における熟練者において知られている一定の流体サンプルにおける任意の特性を測定するために採用できる。グルコース、コレステロール、たんぱく質、ケトン類、フェニルアラニンおよび血液、尿または唾液等のような一定の生理学的流体中の各種酵素が上記分析物の例であり、一定の血液サンプルにおける一定のプロトロンビン時間(PT)が上記化学的特性の一例である。
上記装置120は、例えば、試験片110の光学特性および/または電気化学的特性を測定して、その測定した特性に基づいて、上記試験片に供給された一定の流体サンプルの特性を計算することができる。このような計算は、たとえば、上記試験片の測定した一定の特性(または測定した複数の特性)および種々の較正パラメーターの両方を採用する一定のアルゴリズムを用いて達成できる。この点に関して、上記試験片110に予め割り当てられて装置120に伝達されている一定の試験片較正コードが上記アルゴリズムにおいて使用するための適当な較正パラメーターを確認するために役立つ。なお、当該技術分野における熟練者であれば、このアルゴリズムが装置120内に備えられているソフトウエアおよびハードウエアにより慣用的に実行可能であることが認識できる。
上記装置120は内部に複数の試験片較正コードを保管している一定のメモリーまたは記憶装置130も備えている。このメモリー130内に保管されている試験片較正コードのそれぞれは多次元的な較正パラメーターの区域における一定の幾何学的領域を示す。さらに、それぞれの較正コードは一定の流体サンプルの特性を計算するために一定のアルゴリズムにおいて用いることのできる一組の較正パラメーターに付随している。このメモリー130は各種の集積回路(例えば、ダイナミック・ランダム・アクセス・メモリー[DRAM]、スタテイック・ランダム・アクセス・メモリー[SRAM]、プログラム可能読取専用メモリーまたはハード配線式論理回路等)に基づく各種メモリーおよびデイスクに基づく各種メモリーを含むがこれらに限らない当該技術分野における熟練者において知られている任意の種類のメモリーとすることができる。
本発明による診断キットにおいて、上記複数の試験片較正コードおよびこれらの試験片較正コードにより示される幾何学的領域がその試験片への一定の試験片較正コードの割り当てにおける一定の量子化エラーが最適に減少されるように多次元的な較正パラメーターの区域にわたり分布される。このような最適な減少は、例えば、一定の流体サンプルの特性を計算するための装置により用いられる一定のアルゴリズムに基づく統計学的な分析、試験片の精度、すなわち、各種較正係数の測定における変化を示す一定の目的関数、および各種較正係数の測定における変化に付随する誤差と上記量子化エラーとの均衡化により達成できる。上記のような統計学的分析は上記各種の試験片較正コードにより示される幾何学的領域の最適な形状および寸法を確認することができる。さらに、このようにして確認される幾何学的領域は、例えば、単一の試験片較正コードに関連付けられて、上記の多次元的な較正パラメーターの区域にわたり分布される。その後、所定の幾何学的領域内にある実験的に測定された各種較正パラメーターを有するあらゆるロットの試験片がその幾何学的領域に関連する単一の試験片較正コードを割り当てられる。
実施例1:血液グルコース測定用の診断キット
本発明による血液グルコース測定用の例示的な診断キット200は、図2において示されているように、一定の廃棄可能な血液グルコース試験片210および当該廃棄可能な血液グルコース試験片における一定の特性を測定するための一定の計器220(すなわち、装置)を備えている。この計器220は以下の単純化された形態の一定のアルゴリズムを用いて上記の廃棄可能な血液グルコース試験片210に供給される一定の血液サンプルの血液グルコース濃度を計算することに適合している。
G=IP (C0 −Z) (1)
この式において、
G=血液グルコース濃度、
IおよびC0 は計器220により測定される廃棄可能な血液グルコース試験片200の特性(この試験片210には一定の流体サンプルが供給されている)、および
pおよびZは試験片較正パラメーターである。
本発明による血液グルコース測定用の例示的な診断キット200は、図2において示されているように、一定の廃棄可能な血液グルコース試験片210および当該廃棄可能な血液グルコース試験片における一定の特性を測定するための一定の計器220(すなわち、装置)を備えている。この計器220は以下の単純化された形態の一定のアルゴリズムを用いて上記の廃棄可能な血液グルコース試験片210に供給される一定の血液サンプルの血液グルコース濃度を計算することに適合している。
G=IP (C0 −Z) (1)
この式において、
G=血液グルコース濃度、
IおよびC0 は計器220により測定される廃棄可能な血液グルコース試験片200の特性(この試験片210には一定の流体サンプルが供給されている)、および
pおよびZは試験片較正パラメーターである。
上記計器220は複数の試験片較正コードを保管している一定のメモリー230を備えている。これら複数の試験片較正コードのそれぞれは二次元のp−Z型の較正パラメーターの区域における一定の六角形の幾何学的領域を示す。上記メモリー230内において、その複数の試験片較正コードおよび六角形の幾何学的領域はその試験片へのこれら複数の試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に最小化されるように一定の二次元のp−Z型の較正パラメーターの区域にわたり分布される。
上記の二次元のp−Z型の較正パラメーターの区域にわたる各種試験片較正コードおよび六角形の幾何学的領域の最適化された分布、およびこの分布により導かれる有益性は当該最適化された分布および各幾何学的領域の六角形の形状を得るために用いる以下の数学的な分析技法の詳細な説明に基づいて当該技術分野における熟練者において明らかになる。先ず、上記の数式(1)は以下のように書き直される。
G(p,Z)=IP (C0 −Z) (2)
次に、上記量子化エラーの最適な減少を容易にするために(すなわち、一定のロットの各試験片に対する一定の試験片較正コードの割り当てによるエラーを制限するために)、以下の2個の「定誤差(constant error)」の式(すなわち、目的関数)が形成されている。
G(p,Z)=IP (C0 −Z) (2)
次に、上記量子化エラーの最適な減少を容易にするために(すなわち、一定のロットの各試験片に対する一定の試験片較正コードの割り当てによるエラーを制限するために)、以下の2個の「定誤差(constant error)」の式(すなわち、目的関数)が形成されている。
上記定誤差の式は試験片較正コードの割り当てによる絶対誤差および相対誤差をそれぞれ示している。上記診断キット200において、上記第1の「εa 」の式は20mg/dL乃至100mg/dLの血液グルコース濃度に対して適応し、第2の「εr 」の式は100mg/dL乃至600mg/dLの血液グルコース濃度に対して適応する。また、上記「εa 」の式は一定の絶対誤差(この例示的な実施形態において2mg/dL)に対応しており、「εr 」の式は一定の相対誤差(この例示的な実施形態において2%対応する)に。また、用語の
は一定の較正コード・テーブルから採択される値の
および
の一定の固定値に対応するグルコースの式である。この場合に、pと
との間、およびZと
との間の差が大きいほど、一定の報告された血液グルコース濃度値
と実際の血液グルコース濃度値G(p,Z)との間の差(または誤差)が大きくなる。
は一定の較正コード・テーブルから採択される値の
および
の一定の固定値に対応するグルコースの式である。この場合に、pと
との間、およびZと
との間の差が大きいほど、一定の報告された血液グルコース濃度値
と実際の血液グルコース濃度値G(p,Z)との間の差(または誤差)が大きくなる。
上記の各定誤差の式は2種類の所定の診断キットの精度の要求条件に基づいている。すなわち、この診断キットは20mg/dL乃至100mg/dLの血液グルコース濃度に対応する±10mg/dLの一定の誤差および100mg/dL以上乃至600mg/dLの血液グルコース濃度に対応する±10%の一定の誤差を有している。しかしながら、これらの要求条件はその診断キットに対する全体の許容可能な誤差を示しているので、その一部分のみが上記較正誤差の予定値に割り当てられている。すなわち、
εa =2mg/dL (4)
および
εr =2% (5)である。
εa =2mg/dL (4)
および
εr =2% (5)である。
実際面において、一定の試験片ロットの較正中に決定される上記pおよびZの各値はその試験片のロットに一定の試験片較正コード
を割り当てるために使用できる。この割り当ては上記試験片較正コードに対する測定したpおよびZの近さに基づいている。すなわち、この近さの測定値は上記試験片較正コードによる血液グルコース濃度と測定したp,Zによる血液グルコース濃度との間の差である。さらに、この近さは上記の各定誤差の式により示される。
を割り当てるために使用できる。この割り当ては上記試験片較正コードに対する測定したpおよびZの近さに基づいている。すなわち、この近さの測定値は上記試験片較正コードによる血液グルコース濃度と測定したp,Zによる血液グルコース濃度との間の差である。さらに、この近さは上記の各定誤差の式により示される。
上記2種類の定誤差の式を満足する上記pおよびZの各値の組は上記のεa およびεr により定められる最大許容誤差の境界を定める。このことはpおよびZの各値による一定の囲まれた幾何学的領域を生じる。このような幾何学的領域内のpおよびZの各値において、
および
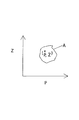
に対する割り当てはεa [絶対誤差]よりも小さくεr [相対誤差]よりも小さい一定の誤差を生じる。図3は上記各定誤差の式が一定の境界を定める方法を示している。図3において、閉じた曲線「A」は上記定誤差の式を満足する各点の組である。それゆえ、この閉じた曲線内の各点は上記において定められた相対誤差および絶対誤差よりも小さい誤差をそれぞれ有している。
および
に対する割り当てはεa [絶対誤差]よりも小さくεr [相対誤差]よりも小さい一定の誤差を生じる。図3は上記各定誤差の式が一定の境界を定める方法を示している。図3において、閉じた曲線「A」は上記定誤差の式を満足する各点の組である。それゆえ、この閉じた曲線内の各点は上記において定められた相対誤差および絶対誤差よりも小さい誤差をそれぞれ有している。
上記診断キット200において、その目的は上記
および
の近辺の幾何学的領域の形状および上記p,Z,IおよびC0 がその形状を定める方法を決定することである。このことにより、一連の
の値が上記p−Z型の較正パラメーターの区域に重なる各試験片較正コードとして生じることができるように一定の決定が上記幾何学的領域を一体に適合する方法に関して作成される。
および
の近辺の幾何学的領域の形状および上記p,Z,IおよびC0 がその形状を定める方法を決定することである。このことにより、一連の
の値が上記p−Z型の較正パラメーターの区域に重なる各試験片較正コードとして生じることができるように一定の決定が上記幾何学的領域を一体に適合する方法に関して作成される。
上記定誤差の式をさらに扱いやすくするために、上記G(p,Z)が一定のテーラー展開において拡張されて、線形の次数よりも高い各項を排除することにより概算される。
この場合に、それぞれの部分的な微分係数は以下のようになる。
さらに、これらの式を上記定誤差の各式に組み込むことにより、以下の式が得られる。
および
上記の定誤差の式(すなわち、数式(7)および(8))が上記
の近くにおける一定の幾何学的領域内のp,Zの各軸についてプロットされている。この結果が図4において示されており、この場合に、図示の容易さのために、上記
は(0,0)として選択されている。さらに、上記較正コードの幾何学的領域を定めるために、上記の各式をサンプルの諸条件における全ての許容される範囲について考慮する必要がある。すなわち、このサンプルの諸条件の範囲内における特定の各値は性能を制限し、それゆえ、その幾何学的領域を定める。この実施例の場合において、これらの制限値はI=10、および20mg/dL、600mg/dL、および100mg/dLの各グルコース量において生じ、これらの量はそれぞれ最低のグルコース量、最高のグルコース量、および上記2個の定誤差の式の間のグルコースの遷移量に相当する。上記の絶対値の各記号(これらは2個の式をそれぞれ形成している)および3種類のグルコース量の制限値により、その結果は一連の6個の線410を生じ、これらの線は一定の六角形の幾何学的領域420の境界を定めている。これらの線およびこれらの線により境界を定められている六角形の幾何学的領域420が図4において示されている。
の近くにおける一定の幾何学的領域内のp,Zの各軸についてプロットされている。この結果が図4において示されており、この場合に、図示の容易さのために、上記
は(0,0)として選択されている。さらに、上記較正コードの幾何学的領域を定めるために、上記の各式をサンプルの諸条件における全ての許容される範囲について考慮する必要がある。すなわち、このサンプルの諸条件の範囲内における特定の各値は性能を制限し、それゆえ、その幾何学的領域を定める。この実施例の場合において、これらの制限値はI=10、および20mg/dL、600mg/dL、および100mg/dLの各グルコース量において生じ、これらの量はそれぞれ最低のグルコース量、最高のグルコース量、および上記2個の定誤差の式の間のグルコースの遷移量に相当する。上記の絶対値の各記号(これらは2個の式をそれぞれ形成している)および3種類のグルコース量の制限値により、その結果は一連の6個の線410を生じ、これらの線は一定の六角形の幾何学的領域420の境界を定めている。これらの線およびこれらの線により境界を定められている六角形の幾何学的領域420が図4において示されている。
上記の説明に基づいて、当該技術分野における熟練者であれば、上記実施例1の本発明が上記グルコースのアルゴリズムの式(1)、および上記誤差の各式(7)および(8)に基づいて一定の試験片較正コードにより示される各幾何学的領域に対応する最適な形状を提供しており、これらの式が一定の診断キットの性能(例えば、精度)の要求条件に関連して設定されることが認識できる。
実施例2:一定の電気化学的試験片および計器装置を備えている血液グルコース測定のための診断キット
血液グルコース測定用の一定の診断キット700(各点線内)は、図5において示されているように、一定の電気化学的試験片710および当該電気化学的試験片710における一定の電気化学的特性を測定するための一定の装置720(例えば、一定の手持型計器)を備えている。この装置720は上記式(1)のアルゴリズムを用いて上記電気化学的試験片710に供給される一定の血液サンプルの血液グルコース濃度を計算することに適合している。
血液グルコース測定用の一定の診断キット700(各点線内)は、図5において示されているように、一定の電気化学的試験片710および当該電気化学的試験片710における一定の電気化学的特性を測定するための一定の装置720(例えば、一定の手持型計器)を備えている。この装置720は上記式(1)のアルゴリズムを用いて上記電気化学的試験片710に供給される一定の血液サンプルの血液グルコース濃度を計算することに適合している。
上記装置720は33個の試験片較正コードを保管している一定のメモリー730を備えている。これら複数の試験片較正コードのそれぞれは一定の二次元のp−Z型の較正パラメーターの区域における一定の六角形の幾何学的領域または一定の部分的な六角形の幾何学的領域を示す。以下においてさらに詳細に説明されているように、この実施形態における二次元のp−Z型の較正パラメーターの区域は0.0乃至0.8の「Z」型較正パラメーターおよび0.50乃至0.80の「p」型較正パラメーターに及ぶ。
上記の33個の試験片較正コード(メモリー730内に保管されている)および六角形の(または部分的に六角形の)幾何学的領域は上記電気化学的試験片710に対する上記試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように上記二次元のp−Z型の較正パラメーターの区域にわたり分布される。
以下の技法は上記p−Z型の較正パラメーターの区域にわたる上記試験片較正コードおよび幾何学的領域の分布を決定するために用いられる。先ず、上記診断キット700により一定の正確な血液グルコースの測定値を得るために上記試験片較正コードの各較正係数(すなわち、pおよびZ)に対する割り当てを最適化する必要があることが認識される。換言すれば、この量子化エラーを最適に減少する必要がある。そこで、この量子化エラーを最適に減少するために、一定の平均絶対偏り(MAB)目的関数が利用できる。このMAB目的関数は以下のように定められている。
この場合に、
Bias=G−YSI (YSI≦100mg/dL)
%Bias=[(G−YSI)÷YSI]×100 (YSI>100mg/dL)
さらに、Gが上記の式(1)において定められている場合に、
mはYSIグルコース値≦100mg/dLにより試験した各試験片の数であり、
nはYSIグルコース値>100mg/dLにより試験した各試験片の数であり、
YSI=一定の標準的なイエロー・スプリングズ(Yellow Springs)基準装置により測定した血漿グルコース値である。
Bias=G−YSI (YSI≦100mg/dL)
%Bias=[(G−YSI)÷YSI]×100 (YSI>100mg/dL)
さらに、Gが上記の式(1)において定められている場合に、
mはYSIグルコース値≦100mg/dLにより試験した各試験片の数であり、
nはYSIグルコース値>100mg/dLにより試験した各試験片の数であり、
YSI=一定の標準的なイエロー・スプリングズ(Yellow Springs)基準装置により測定した血漿グルコース値である。
上記MAB目的関数を定める場合に、その絶対的なバイアス値およびパーセント(%)バイアス値の両方の平均値が一定の混合状態の構成様式で一体に組み合わされている。このようなバイアス値の組み合わせは上記診断キット700におけるグルコース応答の不等分散性の性質を考慮して行なわれている。
その後、意図的に導入されたプロセスの変化を含む20個の電気化学的試験片のロットを調製した。この意図的に導入されたプロセスの変化は各種の電気化学的試験片の製造時期の全体を通して経験すると考えられるプロセスにより誘発する変化に似せて設計されている。各電気化学的試験片のロットについて、その最適なp型およびZ型の各較正パラメーターを上記MAB目的関数を最小化することにより経験的に決定した。この観察されたp型およびZ型の各値の範囲に基づいて、上記の二次元のp−Z型の較正パラメーターの区域が0.5乃至0.8の「p」型の値および0乃至0.8の「Z」型の値に広がると考えられることが決定された。
本発明を知ることにより、当該技術分野における通常の熟練者であれば、上記目的関数の評価において採用される電気化学的試験片のロットの数が予想されるプロセスの変化の大きさおよび上記較正パラメーターの区域を定める場合に必要とされる信頼性の程度に応じて変更可能であることが認識できる。実際において、上記試験片のロットの数は一般的に上記較正パラメーターの区域を初期的に定める場合に約20個乃至60個の試験片のロットの範囲内になる。
次に、血液の供与者、装置および血液グルコースの濃度による上記p型およびZ型の各較正パラメーターの較正誤差が各電気化学的試験片のロットに対して決定される。例えば、血液供与者による較正誤差は一定時間における一定の血液供与者に対応するデータを系統的に除去して残りのデータの組からp型およびZ型の各値を再最適化することにより決定されている。さらに、全体的な変化の可能性を決定するために電気化学的試験片のロットの1個当たりにおける各変化の供給源(すなわち、血液供与者、装置および血液グルコース濃度)に対応するp型およびZ型の各値についてその較正誤差の最小値、最大値および範囲が決定される。その後、このp型およびZ型の各値についてその誤差範囲における95番目の百分順位の数が全体のロットにわたる一定の固定された試験計画に対して決定される。次に、この各較正係数の測定における誤差についての95番目の百分順位の数が上記較正パラメーターの区域を調べるための解像度の増加分として用いられる。これらの相関データに基づいて、上記p型の95番目の百分順位の数=0.03および上記Z型の95番目の百分順位の数=0.10であることが決定された。さらに、これら95番目の百分順位の値は上記p−Z型の較正パラメーターの区域にわたり各試験片較正コードを分布するための解像度の一定の増加分として選択されている。
その後、一定の摂動行列技法を用いて上記MAB目的関数を評価した。図6はこの摂動行列において用いられているp型およびZ型の較正パラメーターの各値の組み合わせを示している一定のデカルト座標のプロット図である。換言すれば、このMAB目的関数は以下の8個の組み合わせに対応して計算し直されている。
・(0.03,0):p=最適化されたp+0.03、およびZ=最適化されたZ
・(−0.03,0):p=最適化されたp−0.03、およびZ=最適化されたZ
・(0,0.1):p=最適化されたp、およびZ=最適化されたZ+0.1
・(0,−0.1):p=最適化されたp、およびZ=最適化されたZ−0.1
・(0.03,0.1):p=最適化されたp+0.03、およびZ=最適化されたZ+0.1
・(−0.03,0.1):p=最適化されたp−0.03、およびZ=最適化されたZ+0.1
・(0.03,−0.1):p=最適化されたp+0.03、およびZ=最適化されたZ−0.1
・(−0.03,−0.1):p=最適化されたp−0.03、およびZ=最適化されたZ−0.1
・(0.03,0):p=最適化されたp+0.03、およびZ=最適化されたZ
・(−0.03,0):p=最適化されたp−0.03、およびZ=最適化されたZ
・(0,0.1):p=最適化されたp、およびZ=最適化されたZ+0.1
・(0,−0.1):p=最適化されたp、およびZ=最適化されたZ−0.1
・(0.03,0.1):p=最適化されたp+0.03、およびZ=最適化されたZ+0.1
・(−0.03,0.1):p=最適化されたp−0.03、およびZ=最適化されたZ+0.1
・(0.03,−0.1):p=最適化されたp+0.03、およびZ=最適化されたZ−0.1
・(−0.03,−0.1):p=最適化されたp−0.03、およびZ=最適化されたZ−0.1
次に、図6における各座標に対応する上記MAB関数の値を計算して上記20個の電気化学的試験片のロットのそれぞれに対応する一定の摂動行列上にプロットした。この実施例において、その許容可能な量子化エラーは0.50のMAB値に設定された。これらの摂動行列の観察により、上記0.5のMABの量子化エラーの制限値を満たすことに関して、その大部分が一定の六角形のパタンを示すことが分かった(図7を参照されたく、この図は20個の電気化学的試験片のロットの内の1個に対応する各MAB値の一定のテーブルを示している)。さらに、各MABの値の下のイタリック体の数字が最初の段階における元のMAB値に対する新しいMAB値の差を示していることに注目されたい。さらに、それぞれの長方形の箱の中に囲まれている値は0.5以下だけ最適化されているp型およびZ型の各値に対して異なっているMAB値である。この六角形の(ハチの巣型の)パタンは、それゆえ、上記メモリー730に保管される一定の試験片較正コードにより示される各幾何学的領域に対応する基本的な形状として選択される。
上記の結果として得られるp−Z型の較正パラメーターの区域800が図8において示されている。さらに、0.03および0.10の解像度の各増加分および六角形の形状の幾何学的領域を用いて、上記33個の試験片較正コード(図8において塗りつぶされた各円により示されている)および六角形の幾何学的領域810が図8において示されているように上記p−Z型の較正パラメーターの区域800にわたり分布されている。さらに、部分的な六角形の幾何学的な領域820がこのp−Z型の較正パラメーターの区域800の各エッジ部分に用いられているが、この場合に、完全な六角形の幾何学的領域がこのエッジ部分を越えて延在していると考えることができる。このような分布は一定の試験片較正コードを上記p−Z型の較正パラメーターの区域の中心部分の近くに割り当てた後に(すなわち、この試験片較正コードおよび六角形の幾何学的領域はp=0.62およびZ=0.40に割り当てられる)、各試験片較正コードおよび六角形の幾何学的領域を定められた解像度の各増加分において上記較正パラメーターの区域にわたり分布することにより開始される。各試験片較正コードに割り当てられる較正パラメーターは各試験片較正コードを示している塗りつぶされた各円の上方の括弧の中にそれぞれ示される。
上記p−Z型の較正パラメーターの区域内に形成される六角形および部分的な六角形の幾何学的領域の数は上記診断キット700に対して要求される試験片較正コードの全数(すなわち、33個)を示す。さらに、各試験片較正コードは各多角形の幾何学的領域(すなわち、各六角形の幾何学的領域または部分的な六角形の幾何学的領域)の中心点として定められる。さらに、20個の電気化学的試験片のロットのそれぞれに対応する最適化されたpおよびZの位置が図8における記号Xにより示されている。
実施例3:プロトロンビン時間(PT)およびINRの測定のための一定の光度測定式の装置および計器を伴う診断キット
PTおよびINRの測定用の一定の診断キット900は図9において示されているように一定の試験片910および当該試験片910の光学特性を測定するための一定の装置920(例えば、一定の手持型計器)を備えている。この装置920は以下のアルゴリズムを用いて上記試験片910に供給される一定の血液サンプルの国際標準化比率(INR)を計算することに適合している。
この場合に、
PTは装置920により測定される一定のプロトロンビン時間であり、
MNPTおよびISIはそれぞれ較正パラメーターである。
PTおよびINRの測定用の一定の診断キット900は図9において示されているように一定の試験片910および当該試験片910の光学特性を測定するための一定の装置920(例えば、一定の手持型計器)を備えている。この装置920は以下のアルゴリズムを用いて上記試験片910に供給される一定の血液サンプルの国際標準化比率(INR)を計算することに適合している。
PTは装置920により測定される一定のプロトロンビン時間であり、
MNPTおよびISIはそれぞれ較正パラメーターである。
上記装置920は14個の試験片較正コードを保管している一定のメモリー930を有しており、これらのコードはそれぞれ一定のMNPT−ISIの較正パラメーターの区域における一定の多角形の幾何学的領域を示す。以下においてさらに詳細に示されているように、この実施例3のMNPT−ISIの較正パラメーターの区域は7.04乃至9.07の各MNPT較正パラメーターおよび0.99乃至1.32の各ISI較正パラメーターに及ぶ。
上記メモリー930において、14個の試験片較正コードおよび多角形の幾何学的領域が上記試験片910に対する各種試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように上記二次元のMNPT−ISI型の較正パラメーターの区域にわたり分布される。
上記診断キット900において、試験片910はその実験的に決定したISIおよびMNPTの各較正パラメーターに基づく一定の試験片較正コードが割り当てられる。各試験片910は固定されたISIおよびMNPTの各較正パラメーターによる一定の試験片較正コードを必要とする。このような固定されたISIおよびMNPTの各較正パラメーターは、上記装置920がINRの計算において一定の試験片較正コードに対応するISIおよびMNPTの各較正パラメーターを採用できるように、一定の使用者が当該装置920に対してその試験片較正コードを伝達することを可能にする。
実験的なデータに基づいて、上記診断キット900に対応するMNPT−ISI型の較正パラメーターの区域は0.99乃至1.32の範囲の各ISI値および7.04乃至9.07の範囲の各MNPT値を有する一定の長方形の区域として初期的に考えられている。しかしながら、この長方形の較正パラメーターの区域はその後に(図10において示されていて、以下においてさらに説明されているような)その長方形の区域内における一定の対角状のMNPT−ISI型の較正パラメーターの区域に限定される。この限定は全体のMNPT−ISIの較正パラメーターの区域内におけるINRの各測定結果が25%以上異ならないという一定の診断キット精度の要求条件に基づいている。
上記ISIおよびMNPTの各較正パラメーターに付随する較正誤差を推定するために、それぞれの95%信頼区間が計算されている。このような実施例において、これらISIおよびMNPTの各較正パラメーターは一定の正常な分布状態に従う。それゆえ、これらの信頼性区間はパラメーター統計学の適用により直接的に計算されている。さらに、これらISIおよびMNPTに対応する95%信頼区間の半分の幅はそれぞれ0.045および0.38の平均の幅を有している。この結果は0.09の一定のISIの幅および0.76の一定のMNPTの幅が類似の診断キットの性能を生じることを示している。しかしながら、この診断キットの性能はISIおよびMNPTの増加に伴って許容可能な状態に維持されることが知られており、この理由は、これらの較正パラメーターがINR測定に対して逆の影響を及ぼすからである。
上記の分析に基づいて、上記14個の試験片較正コードが上記MNPT−ISI型の較正パラメーターの区域内における多角形の各幾何学的区域に割り当てられ、これらの区域はその全体の形状において実質的に対角状であり、各多角形の幾何学的領域は一定の「段付き状の(stepped)」外形を有している。図10は結果として得られる較正パラメーターの区域950を示しており、この区域にわたり、14個の試験片較正コード(1乃至14)および14個の多角形の幾何学的領域955が分布している。これら段付き状の多角形の幾何学的領域955は隣接している平行四辺形の組み合わせとして考えることができる。
その後、以下の技法を用いて上記メモリー930内におけるMNPT−ISI型の較正パラメーターの区域にわたる上記14個の試験片較正コードおよび多角形の幾何学的領域の分布が決定される。量子化エラーを最適に減少するために、絶対差および相対差の両方の関数が用いられる。これらの関数はそれぞれ以下の形態を採る。
I.
絶対差=|患者 INR−基準値 INR│
II.
絶対的相対差={|患者 INR 基準値 INR│/(基準値−INR)}*100
この場合に、
患者 INRは診断キットにより得られるINR応答であり、
基準値−INRは一定の基準測定システムにより得られるINR応答である。
I.
絶対差=|患者 INR−基準値 INR│
II.
絶対的相対差={|患者 INR 基準値 INR│/(基準値−INR)}*100
この場合に、
患者 INRは診断キットにより得られるINR応答であり、
基準値−INRは一定の基準測定システムにより得られるINR応答である。
以下の2種類の診断キットの精度の要求条件もまた上記MNPT−ISI型の較正パラメーターの区域にわたる各試験片較正コードおよび多角形の幾何学的領域の分布において考慮されている。
(a)平均の絶対的相対偏差(MARD)、すなわち、一定のアッセイ範囲にわたる全体の診断キットの精度に対する患者の母集団にわたる絶対的相対差の平均は適正な試験片較正コードが用いられる場合に15%よりも小さいことが必要であること、および
(b)一定の統計学的に関連性のあるサンプルの大きさの場合に、対を成す各値の95%が±1.0のINR値の範囲内であることが必要であり、この要求条件は上記絶対差の95番目の百分順位の値が1.0のINR値よりも小さい場合に確実になる。
(a)平均の絶対的相対偏差(MARD)、すなわち、一定のアッセイ範囲にわたる全体の診断キットの精度に対する患者の母集団にわたる絶対的相対差の平均は適正な試験片較正コードが用いられる場合に15%よりも小さいことが必要であること、および
(b)一定の統計学的に関連性のあるサンプルの大きさの場合に、対を成す各値の95%が±1.0のINR値の範囲内であることが必要であり、この要求条件は上記絶対差の95番目の百分順位の値が1.0のINR値よりも小さい場合に確実になる。
上記実施例において2種類の性能の測定基準が存在しており、上記ISI−MNPT型の較正パラメーターの区域の広がりおよび一定の試験片較正コードにより示される各幾何学的領域の大きさおよび形状の決定において、MARDが一次的な測定基準として採用されており、対を成す差の値の95番目の百分順位の値が二次的な測定基準として与えられている。さらに、このISI−MNPT型の較正パラメーターの区域の広がりおよび各幾何学的領域の大きさが上記一次的な測定基準により決定されて、上記二次的な測定基準により確認されている。最適なISIおよびMNPTによる上記のMARD値および対を成す各差の95番目の百分順位の値は一定の実験的なデータの組においてそれぞれ4乃至7.5および0.2乃至0.45の範囲内である。
図10は上記14個の試験片較正コードおよび14個の段付き状の多角形の幾何学的領域955がメモリー930内のISI−MNPT型の較正パラメーターの区域950にわたり分布されている様式を示している。当該技術分野における熟練者であれば、このメモリー930が従来的な各種の方法により上記のような分布状態を保管できることが認識できると考える。例えばこのメモリー930は各種の試験片較正コード(例えば、1乃至14)を各種のMNPT較正パラメーター(例えば、A1 乃至A14)およびISI較正パラメーター(例えば、B1 乃至B14)に付随させる、以下の表1のような、一定のテーブルを含むことができる。
図11は各種の試験片較正コードを一定の試験片および一定のメモリーを伴う装置を含む一定の診断キットにおいて使用するための各種の較正パラメーターに最適に付随させるための本発明による一定の例示的な方法970における一連の工程を示しているフロー図である。
上記方法970は、工程980において記載されているように、一定の較正パラメーターの区域にわたり複数の試験片較正コードおよび当該複数の較正コードにより示される幾何学的領域を分布する処理を含む。さらに、この分布は一定の診断キットにおける試験片に対する複数の試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように行なわれる。これら複数の試験片較正コードおよび幾何学的領域の分布は当該複数の試験片較正コードのそれぞれを上記較正パラメーターの区域における各較正パラメーターに付随させることに役立つ。
上記較正パラメーターの区域は当該技術分野における熟練者において知られている任意の適当な較正パラメーターの区域とすることができる。例えば、この較正パラメーターの区域は上記実施例2および3の診断キットにおけるp−Z型の較正パラメーターおよびMNPT−ISI型の較正パラメーターの各区域等のような一定の多次元的な較正パラメーターの区域とすることができる。
上記量子化エラーは当該技術分野における熟練者において知られている任意の数学的で統計的な技法(例えば、定誤差式技法等)または実験的な技法(各種MAB目的関数による一定の摂動行列技法等)により最適に減少できる。上記実施例1,2および3に関連して説明されているように、一定の目的関数(例えば、MAB、MARDまたは定誤差式等)により上記量子化エラーを最適に減少することが特に有利になると考えられる。
上記方法970はまた、工程990において記載されているように、上記診断キットにおける一定のメモリー内に上述したように分布される複数の試験片較正コードを保管する工程も含む。この保管は当該技術分野における通常の熟練者において知られている一定のテーブルまたはその他のソフトウエア備品の形態を採ることができ、任意の適当な保管技法により達成できる。
本発明による方法および診断キットは最小数の試験片較正コードを備えているので、複数の試験片較正コードおよび一定の試験片ロットについて収集した実験データを用いて当該試験片ロットの実用的な評価を可能にしている。その後、誤差を最小にする一定の試験片較正コードが(例えば、MAB等のような一定の目的関数に基づいて)その試験片のロットに割り当てることが可能になる。
さらに、上記の例示的な方法が当該技術分野における熟練者により一定の試薬および一定のメモリーを伴う分析装置を含む各種のアッセイ用キット内において使用するために各種の試薬較正コードを各種の較正パラメーターに最適に付随させることに適合可能であることも考慮されている。このような状況において、この結果として得られる方法は一定の試薬に対する複数の試薬較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように一定の較正パラメーターの区域にわたり複数の試薬較正コードおよび当該試薬較正コードにより示される幾何学的領域を分布する処理を含む。このことを行なう場合に、上記複数の試薬較正コードは上記較正パラメーターの区域における各種の較正パラメーターに付随すると考えられる。上記方法はまた上記分析装置の一定のメモリー内に上述したように分布される複数の試薬較正コードを保管する処理も含む。
本明細書において記載されている本発明の各実施形態に対する種々の変更例が本発明の実施において使用可能であることが当然に理解されると考える。添付の特許請求の範囲における各請求項は本発明の範囲を定めており、これらの請求項の範囲内の各種の構造および方法およびこれらの等価物もまた当然に本発明の範囲に含まれると考えられる。
本発明は各種の較正パラメーターに対して最適に付随する各種の試験片較正コードを含み、それゆえ、一定の最小数の試験片較正コードの使用を可能にする一定の診断キットに適用可能であり、これらの試験片較正コードは各種の較正パラメーターに対して最適に付随するので、これらの試験片較正コードは試験片の較正中における一定の試験片のロットに対しても最適に割り当てられる。
本発明の具体的な実施態様は以下のとおりである。
(1)前記試験片較正コードのそれぞれが一定の多次元的な較正パラメーターの区域における一定の幾何学的領域を示す請求項1に記載の診断キット。
(2)前記試験片および装置が一定の血液サンプルにおける一定の血液グルコース濃度を測定することに適合しており、前記装置が血液グルコース濃度を計算するために以下の数式の単純化された形態の一定のアルゴリズムを採用しており、前記試験片較正コードが一定の二次元のp−Z型の較正パラメーターの区域における各種六角形の幾何学的領域を示す請求項1に記載の診断キット。
G=IP (C0 −Z)
この式において、G=血液グルコース濃度、IおよびC0 は前記試験片の測定された各特性、およびpおよびZは各較正パラメーターである。
(3)前記試験片較正コードが各種の定誤差式による最適化に基づいて前記二次元のp−Z型の較正パラメーターの区域にわたり分布される実施態様(2)に記載の診断キット。
(4)前記試験片較正コードが前記二次元のp−Z型の較正パラメーターの区域における六角形の幾何学的領域および部分的な六角形の幾何学的領域の内の1個を示す実施態様(2)に記載の診断キット。
(5)前記試験片較正コードが一定の較正パラメーターの較正誤差における95番目の百分順位の値に基づく一定の増加分の解像度を用いて分布される実施態様(4)に記載の診断キット。
(1)前記試験片較正コードのそれぞれが一定の多次元的な較正パラメーターの区域における一定の幾何学的領域を示す請求項1に記載の診断キット。
(2)前記試験片および装置が一定の血液サンプルにおける一定の血液グルコース濃度を測定することに適合しており、前記装置が血液グルコース濃度を計算するために以下の数式の単純化された形態の一定のアルゴリズムを採用しており、前記試験片較正コードが一定の二次元のp−Z型の較正パラメーターの区域における各種六角形の幾何学的領域を示す請求項1に記載の診断キット。
G=IP (C0 −Z)
この式において、G=血液グルコース濃度、IおよびC0 は前記試験片の測定された各特性、およびpおよびZは各較正パラメーターである。
(3)前記試験片較正コードが各種の定誤差式による最適化に基づいて前記二次元のp−Z型の較正パラメーターの区域にわたり分布される実施態様(2)に記載の診断キット。
(4)前記試験片較正コードが前記二次元のp−Z型の較正パラメーターの区域における六角形の幾何学的領域および部分的な六角形の幾何学的領域の内の1個を示す実施態様(2)に記載の診断キット。
(5)前記試験片較正コードが一定の較正パラメーターの較正誤差における95番目の百分順位の値に基づく一定の増加分の解像度を用いて分布される実施態様(4)に記載の診断キット。
(6)前記試験片および装置が一定の血液サンプルにおけるINR値を測定することに適合しており、前記装置が当該INR値を計算するために以下の数式の単純化された形態の一定のアルゴリズムを採用しており、前記試験片較正コードが一定の二次元のMNPT−ISI型の較正パラメーターの区域における各種多角形の幾何学的領域を示す請求項1に記載の診断キット。
この場合に、PTは前記装置により測定される一定のプロトロンビン時間であり、MNPTおよびISIは各較正パラメーターである。
(7)前記試験片較正コードが前記二次元のISI−MNPT型の較正パラメーターの区域における段付き状の多角形の幾何学的領域を示す実施態様(6)に記載の診断キット。
(8)前記段付き状の多角形の幾何学的領域が複数の隣接している平行四辺形を含む実施態様(6)に記載の診断キット。
(9)前記メモリーが一定の最小数の試験片較正コードを伴って所定の量子化エラーの各制限値を維持することにより前記量子化エラーを最適に減少する複数の試験片較正コードを保管する請求項1に記載の診断キット。
(10)前記所定の量子化エラーの各制限値が前記診断キットの一定の精度の要求条件に基づいている実施態様(9)に記載の診断キット。
(7)前記試験片較正コードが前記二次元のISI−MNPT型の較正パラメーターの区域における段付き状の多角形の幾何学的領域を示す実施態様(6)に記載の診断キット。
(8)前記段付き状の多角形の幾何学的領域が複数の隣接している平行四辺形を含む実施態様(6)に記載の診断キット。
(9)前記メモリーが一定の最小数の試験片較正コードを伴って所定の量子化エラーの各制限値を維持することにより前記量子化エラーを最適に減少する複数の試験片較正コードを保管する請求項1に記載の診断キット。
(10)前記所定の量子化エラーの各制限値が前記診断キットの一定の精度の要求条件に基づいている実施態様(9)に記載の診断キット。
(11)前記試験片較正コードのそれぞれが一定の二次元の較正パラメーターの区域における一定の六角形の幾何学的領域または一定の部分的な六角形の幾何学的領域の内の1個を示す請求項1に記載の診断キット。
(12)前記メモリーが、前記試験片較正コードのそれぞれが一定の二次元の較正パラメーターの区域における一定の多角形の幾何学的領域を示すように、分布されている複数の試験片較正コードを保管する請求項1に記載の診断キット。
(13)前記多角形の幾何学的領域が複数の隣接している平行四辺形を含む一定の段付き状の多角形の幾何学的領域である実施態様(12)に記載の診断キット。
(14)前記試験片が一定の廃棄可能な血液グルコース試験片であり、前記装置が当該廃棄可能な血液グルコース試験片の一定の光学特性を測定するための一定の手持型計器である請求項1に記載の診断キット。
(15)前記試験片が一定の廃棄可能な血液グルコース試験片であり、前記装置が当該廃棄可能な血液グルコース試験片の一定の電気化学的特性を測定するための一定の手持型計器である請求項1に記載の診断キット。
(12)前記メモリーが、前記試験片較正コードのそれぞれが一定の二次元の較正パラメーターの区域における一定の多角形の幾何学的領域を示すように、分布されている複数の試験片較正コードを保管する請求項1に記載の診断キット。
(13)前記多角形の幾何学的領域が複数の隣接している平行四辺形を含む一定の段付き状の多角形の幾何学的領域である実施態様(12)に記載の診断キット。
(14)前記試験片が一定の廃棄可能な血液グルコース試験片であり、前記装置が当該廃棄可能な血液グルコース試験片の一定の光学特性を測定するための一定の手持型計器である請求項1に記載の診断キット。
(15)前記試験片が一定の廃棄可能な血液グルコース試験片であり、前記装置が当該廃棄可能な血液グルコース試験片の一定の電気化学的特性を測定するための一定の手持型計器である請求項1に記載の診断キット。
(16)前記試験片が一定のプロトロンビン試験片であり、前記装置が当該プロトロンビン試験片の光学特性を測定するための一定の装置である請求項1に記載の診断キット。
(17)所定の試験片較正コードが、さらに、全体の試験片の較正誤差を定める一定の目的関数に依存している一定の幾何学的パタンを用いて、前記較正パラメーターの区域にわたり分布される請求項1に記載の診断キット。
(18)前記装置が一定の手持型計器である請求項1に記載の診断キット。
(19)前記流体サンプルが一定の生理学的な流体サンプルである請求項1に記載の診断キット。
(20)前記試験片が一定の付随している較正コードを有している請求項1に記載の診断キット。
(17)所定の試験片較正コードが、さらに、全体の試験片の較正誤差を定める一定の目的関数に依存している一定の幾何学的パタンを用いて、前記較正パラメーターの区域にわたり分布される請求項1に記載の診断キット。
(18)前記装置が一定の手持型計器である請求項1に記載の診断キット。
(19)前記流体サンプルが一定の生理学的な流体サンプルである請求項1に記載の診断キット。
(20)前記試験片が一定の付随している較正コードを有している請求項1に記載の診断キット。
(21)前記分布工程が前記試験片較正コードを一定の多次元的な較正パラメーターの区域にわたり分布する請求項2に記載の方法。
(22)前記分布工程が一定の二次元の較正パラメーターの区域における一定の六角形の幾何学的領域または一定の部分的な六角形の幾何学的領域の内の1個を示す複数の試験片較正コードを分布する請求項2に記載の方法。
(23)前記分布工程が一定の二次元の較正パラメーターの区域における多角形の幾何学的領域を示す複数の試験片較正コードを分布する請求項2に記載の方法。
(24)前記分布工程が一定の二次元の較正パラメーターの区域における段付き状の多角形の幾何学的領域に付随する複数の試験片較正コードを分布する実施態様(23)に記載の方法。
(25)前記分布工程が前記診断キットの性能に関連する一定の目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
(22)前記分布工程が一定の二次元の較正パラメーターの区域における一定の六角形の幾何学的領域または一定の部分的な六角形の幾何学的領域の内の1個を示す複数の試験片較正コードを分布する請求項2に記載の方法。
(23)前記分布工程が一定の二次元の較正パラメーターの区域における多角形の幾何学的領域を示す複数の試験片較正コードを分布する請求項2に記載の方法。
(24)前記分布工程が一定の二次元の較正パラメーターの区域における段付き状の多角形の幾何学的領域に付随する複数の試験片較正コードを分布する実施態様(23)に記載の方法。
(25)前記分布工程が前記診断キットの性能に関連する一定の目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
(26)前記分布工程が一定の平均絶対偏り(MAB)目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
(27)前記分布工程が前記診断キットの性能に関連する各種の定誤差目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
(28)前記分布工程が一定の平均絶対的相対偏差(MARD)目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
(27)前記分布工程が前記診断キットの性能に関連する各種の定誤差目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
(28)前記分布工程が一定の平均絶対的相対偏差(MARD)目的関数に基づいて前記量子化エラーを最適に減少することにより複数の試験片較正コードを分布する請求項2に記載の方法。
本発明の特徴および利点の比較的に良好な理解が本発明の原理を利用している例示的な各実施形態を述べている以下の詳細な説明、および以下の添付図面を参照することにより得られる。
本発明の一定の例示的な実施形態による診断キットの簡単化したブロック図である。
本発明の別の例示的な実施形態による診断キットの簡単化したブロック図である。
一定のp−Z型の較正パラメーターの区域におけるp値およびZ値の一定の幾何学的領域を囲っている最大許容誤差の一定の境界を示している略図である。
一定の試験片較正コードによる表示に対応する一定の境界を有する幾何学的領域を定めるために各種の定誤差方程式がプロット可能な様式を示している一定のグラフである。
本発明のさらに別の例示的な実施形態による一定の診断キットの簡単化したブロック図である。
本発明に関連して使用する一定の摂動行列技法に対応するデカルト座標を示しているグラフである。
本発明の一定の実施例における一定の試験片に付随する一定のMAB目的関数に対応する一定の摂動行列を示しているグラフである。
本発明の例示的な実施形態における一定のp−Z型の較正パラメーターの区域にわたる各種試験片較正コードおよびこれらにより示される幾何学的領域の一定の分布を示している図である。
本発明のさらに別の例示的な実施形態による一定の診断キットの単純化したブロック図である。
本発明の例示的な実施形態における一定のMNPT−ISI型の較正パラメーターの区域にわたる各種試験片較正コードおよびこれらにより示される段階型多角形の幾何学的領域の分布を示している図である。
本発明の一例の例示的な実施形態による一定の方法における一連の工程を示しているフロー図である。
100 診断キット
110 試験片
120 装置
130 メモリー(記憶装置)
110 試験片
120 装置
130 メモリー(記憶装置)
Claims (4)
- 一定の流体サンプルの特性を測定するための診断キットにおいて、
一定の試験片、および
前記試験片の少なくとも1種類の特性を測定して、その特性から、当該試験片に供給される一定の流体サンプルの特性を計算するための一定の装置を備えており、当該装置が
複数の試験片較正コードを内部に保管している一定のメモリーを有しており、
前記試験片較正コードのそれぞれが一定の較正パラメーターの区域における一定の幾何学的領域を示し、この場合に、これらの試験片較正コードおよび幾何学的領域が、前記試験片に対する前記試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように、前記較正パラメーターの区域にわたり分布される診断キット。 - 一定の試験片および一定のメモリーを伴う一定の装置を備えている一定の診断キットにおいて使用するための複数の較正パラメーターに対して複数の試験片較正コードを最適に付随させるための方法において、
複数の試験片較正コードおよびこれら試験片較正コードにより示される幾何学的領域を、前記試験片に対する前記試験片較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように、一定の較正パラメーターの区域にわたり分布することにより、前記複数の試験片較正コードを前記較正パラメーターの区域における各較正パラメーターに付随させる工程、
前記のように分布された試験片較正コードを前記診断キットの一定のメモリー内に保管する工程を含む方法。 - 一定のサンプルを分析するためのアッセイ用キットにおいて、
一定の試薬、および
前記サンプルの所定の分析を行なうために前記試薬と共に用いられる一定の分析装置を備えており、当該分析装置が
複数の試薬較正コードを内部に保管している一定のメモリーを有しており、
前記試薬較正コードのそれぞれが一定の較正パラメーターの区域における一定の幾何学的領域を示し、この場合に、これらの試薬較正コードおよび幾何学的領域が、前記試薬に対する前記試薬較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように、前記較正パラメーターの区域にわたり分布されるアッセイ用キット。 - 一定の試薬および一定のメモリーを伴う一定の分析装置を備えている一定のアッセイ用キットにおいて使用するための複数の較正パラメーターに対して複数の試薬較正コードを最適に付随させるための方法において、
複数の試薬較正コードおよびこれら試薬較正コードにより示される幾何学的領域を、前記試薬に対する前記試薬較正コードの内の1個の割り当てにおける一定の量子化エラーが最適に減少されるように、一定の較正パラメーターの区域にわたり分布することにより、前記複数の試薬較正コードを前記較正パラメーターの区域における各較正パラメーターに付随させる工程、
前記のように分布された試薬較正コードを前記分析装置の一定のメモリー内に保管する工程を含む方法。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/224,888 US6780645B2 (en) | 2002-08-21 | 2002-08-21 | Diagnostic kit with a memory storing test strip calibration codes and related methods |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2004132964A true JP2004132964A (ja) | 2004-04-30 |
Family
ID=31187982
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003296598A Pending JP2004132964A (ja) | 2002-08-21 | 2003-08-20 | 試験片較正コードを記憶している一定のメモリーを有する診断キットおよび関連の方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US6780645B2 (ja) |
| EP (1) | EP1391728B1 (ja) |
| JP (1) | JP2004132964A (ja) |
| KR (1) | KR20040018161A (ja) |
| CN (1) | CN100587488C (ja) |
| CA (1) | CA2437681C (ja) |
| ES (1) | ES2519791T3 (ja) |
| IL (1) | IL157381A (ja) |
| SG (1) | SG109525A1 (ja) |
| TW (1) | TWI317810B (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007108171A (ja) * | 2005-09-30 | 2007-04-26 | Lifescan Inc | 迅速な電気化学的分析のための方法および装置 |
| JP2016122012A (ja) * | 2007-04-12 | 2016-07-07 | トリビディア ヘルス,インコーポレーテッド | 診断テストシステムにおけるエラーの検出及び排除 |
Families Citing this family (153)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6036924A (en) | 1997-12-04 | 2000-03-14 | Hewlett-Packard Company | Cassette of lancet cartridges for sampling blood |
| US6391005B1 (en) | 1998-03-30 | 2002-05-21 | Agilent Technologies, Inc. | Apparatus and method for penetration with shaft having a sensor for sensing penetration depth |
| US6290646B1 (en) | 1999-04-16 | 2001-09-18 | Cardiocom | Apparatus and method for monitoring and communicating wellness parameters of ambulatory patients |
| US8419650B2 (en) | 1999-04-16 | 2013-04-16 | Cariocom, LLC | Downloadable datasets for a patient monitoring system |
| US20060091006A1 (en) * | 1999-11-04 | 2006-05-04 | Yi Wang | Analyte sensor with insertion monitor, and methods |
| US6616819B1 (en) | 1999-11-04 | 2003-09-09 | Therasense, Inc. | Small volume in vitro analyte sensor and methods |
| US8641644B2 (en) | 2000-11-21 | 2014-02-04 | Sanofi-Aventis Deutschland Gmbh | Blood testing apparatus having a rotatable cartridge with multiple lancing elements and testing means |
| US7025774B2 (en) | 2001-06-12 | 2006-04-11 | Pelikan Technologies, Inc. | Tissue penetration device |
| AU2002315180A1 (en) | 2001-06-12 | 2002-12-23 | Pelikan Technologies, Inc. | Electric lancet actuator |
| EP1404235A4 (en) | 2001-06-12 | 2008-08-20 | Pelikan Technologies Inc | METHOD AND DEVICE FOR A LANZETTING DEVICE INTEGRATED ON A BLOOD CARTRIDGE CARTRIDGE |
| AU2002344825A1 (en) | 2001-06-12 | 2002-12-23 | Pelikan Technologies, Inc. | Method and apparatus for improving success rate of blood yield from a fingerstick |
| US7981056B2 (en) | 2002-04-19 | 2011-07-19 | Pelikan Technologies, Inc. | Methods and apparatus for lancet actuation |
| US9795747B2 (en) | 2010-06-02 | 2017-10-24 | Sanofi-Aventis Deutschland Gmbh | Methods and apparatus for lancet actuation |
| JP4209767B2 (ja) | 2001-06-12 | 2009-01-14 | ペリカン テクノロジーズ インコーポレイテッド | 皮膚の性状の一時的変化に対する適応手段を備えた自動最適化形切開器具 |
| US8337419B2 (en) | 2002-04-19 | 2012-12-25 | Sanofi-Aventis Deutschland Gmbh | Tissue penetration device |
| US9427532B2 (en) | 2001-06-12 | 2016-08-30 | Sanofi-Aventis Deutschland Gmbh | Tissue penetration device |
| CA2448681C (en) | 2001-06-12 | 2014-09-09 | Pelikan Technologies, Inc. | Integrated blood sampling analysis system with multi-use sampling module |
| US9226699B2 (en) | 2002-04-19 | 2016-01-05 | Sanofi-Aventis Deutschland Gmbh | Body fluid sampling module with a continuous compression tissue interface surface |
| ES2335576T3 (es) | 2001-06-12 | 2010-03-30 | Pelikan Technologies Inc. | Aparato y procedimiento de toma de muestras de sangre. |
| US7344507B2 (en) | 2002-04-19 | 2008-03-18 | Pelikan Technologies, Inc. | Method and apparatus for lancet actuation |
| US7344894B2 (en) | 2001-10-16 | 2008-03-18 | Agilent Technologies, Inc. | Thermal regulation of fluidic samples within a diagnostic cartridge |
| US7374544B2 (en) | 2002-04-19 | 2008-05-20 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7232451B2 (en) | 2002-04-19 | 2007-06-19 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7485128B2 (en) | 2002-04-19 | 2009-02-03 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US8360992B2 (en) | 2002-04-19 | 2013-01-29 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for penetrating tissue |
| US8579831B2 (en) | 2002-04-19 | 2013-11-12 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for penetrating tissue |
| US7244265B2 (en) | 2002-04-19 | 2007-07-17 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7717863B2 (en) | 2002-04-19 | 2010-05-18 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7976476B2 (en) | 2002-04-19 | 2011-07-12 | Pelikan Technologies, Inc. | Device and method for variable speed lancet |
| US7297122B2 (en) | 2002-04-19 | 2007-11-20 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7582099B2 (en) | 2002-04-19 | 2009-09-01 | Pelikan Technologies, Inc | Method and apparatus for penetrating tissue |
| US7141058B2 (en) | 2002-04-19 | 2006-11-28 | Pelikan Technologies, Inc. | Method and apparatus for a body fluid sampling device using illumination |
| US7291117B2 (en) | 2002-04-19 | 2007-11-06 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7229458B2 (en) | 2002-04-19 | 2007-06-12 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7708701B2 (en) | 2002-04-19 | 2010-05-04 | Pelikan Technologies, Inc. | Method and apparatus for a multi-use body fluid sampling device |
| US7648468B2 (en) | 2002-04-19 | 2010-01-19 | Pelikon Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7563232B2 (en) | 2002-04-19 | 2009-07-21 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US9314194B2 (en) | 2002-04-19 | 2016-04-19 | Sanofi-Aventis Deutschland Gmbh | Tissue penetration device |
| US7524293B2 (en) | 2002-04-19 | 2009-04-28 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7901362B2 (en) | 2002-04-19 | 2011-03-08 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7491178B2 (en) | 2002-04-19 | 2009-02-17 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7410468B2 (en) | 2002-04-19 | 2008-08-12 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US8267870B2 (en) | 2002-04-19 | 2012-09-18 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for body fluid sampling with hybrid actuation |
| US7674232B2 (en) | 2002-04-19 | 2010-03-09 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US8372016B2 (en) | 2002-04-19 | 2013-02-12 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for body fluid sampling and analyte sensing |
| WO2003088824A2 (en) | 2002-04-19 | 2003-10-30 | Pelikan Technologies, Inc. | Device and method for variable speed lancet |
| US9795334B2 (en) | 2002-04-19 | 2017-10-24 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for penetrating tissue |
| US8784335B2 (en) | 2002-04-19 | 2014-07-22 | Sanofi-Aventis Deutschland Gmbh | Body fluid sampling device with a capacitive sensor |
| US8221334B2 (en) | 2002-04-19 | 2012-07-17 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for penetrating tissue |
| US7547287B2 (en) | 2002-04-19 | 2009-06-16 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7909778B2 (en) | 2002-04-19 | 2011-03-22 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US7892183B2 (en) | 2002-04-19 | 2011-02-22 | Pelikan Technologies, Inc. | Method and apparatus for body fluid sampling and analyte sensing |
| US9248267B2 (en) | 2002-04-19 | 2016-02-02 | Sanofi-Aventis Deustchland Gmbh | Tissue penetration device |
| US7371247B2 (en) | 2002-04-19 | 2008-05-13 | Pelikan Technologies, Inc | Method and apparatus for penetrating tissue |
| US7331931B2 (en) | 2002-04-19 | 2008-02-19 | Pelikan Technologies, Inc. | Method and apparatus for penetrating tissue |
| US8702624B2 (en) | 2006-09-29 | 2014-04-22 | Sanofi-Aventis Deutschland Gmbh | Analyte measurement device with a single shot actuator |
| US8574895B2 (en) | 2002-12-30 | 2013-11-05 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus using optical techniques to measure analyte levels |
| US8262614B2 (en) | 2003-05-30 | 2012-09-11 | Pelikan Technologies, Inc. | Method and apparatus for fluid injection |
| WO2004107964A2 (en) | 2003-06-06 | 2004-12-16 | Pelikan Technologies, Inc. | Blood harvesting device with electronic control |
| WO2006001797A1 (en) | 2004-06-14 | 2006-01-05 | Pelikan Technologies, Inc. | Low pain penetrating |
| WO2004112602A1 (en) | 2003-06-13 | 2004-12-29 | Pelikan Technologies, Inc. | Method and apparatus for a point of care device |
| US7186566B2 (en) * | 2003-07-28 | 2007-03-06 | Suyue Qian | Combining transmittance detection and chromatographic strip techniques for quantification of analyte in biological fluids |
| US7920906B2 (en) | 2005-03-10 | 2011-04-05 | Dexcom, Inc. | System and methods for processing analyte sensor data for sensor calibration |
| US8282576B2 (en) | 2003-09-29 | 2012-10-09 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for an improved sample capture device |
| EP1680014A4 (en) | 2003-10-14 | 2009-01-21 | Pelikan Technologies Inc | METHOD AND APPARATUS PROVIDING A VARIABLE USER INTERFACE |
| US9247900B2 (en) | 2004-07-13 | 2016-02-02 | Dexcom, Inc. | Analyte sensor |
| US7822454B1 (en) | 2005-01-03 | 2010-10-26 | Pelikan Technologies, Inc. | Fluid sampling device with improved analyte detecting member configuration |
| WO2005065414A2 (en) | 2003-12-31 | 2005-07-21 | Pelikan Technologies, Inc. | Method and apparatus for improving fluidic flow and sample capture |
| US8828203B2 (en) | 2004-05-20 | 2014-09-09 | Sanofi-Aventis Deutschland Gmbh | Printable hydrogels for biosensors |
| US9775553B2 (en) | 2004-06-03 | 2017-10-03 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for a fluid sampling device |
| WO2005120365A1 (en) | 2004-06-03 | 2005-12-22 | Pelikan Technologies, Inc. | Method and apparatus for a fluid sampling device |
| US8515516B2 (en) | 2004-07-13 | 2013-08-20 | Dexcom, Inc. | Transcutaneous analyte sensor |
| US8652831B2 (en) | 2004-12-30 | 2014-02-18 | Sanofi-Aventis Deutschland Gmbh | Method and apparatus for analyte measurement test time |
| JP4903783B2 (ja) | 2005-05-17 | 2012-03-28 | エフ.ホフマン−ラ ロシュ アーゲー | 測定プロセスにおいて消耗試薬を使用する測定装置に較正情報および試薬情報を提供するホスト装置および方法 |
| US8016154B2 (en) * | 2005-05-25 | 2011-09-13 | Lifescan, Inc. | Sensor dispenser device and method of use |
| US8323464B2 (en) * | 2005-05-25 | 2012-12-04 | Universal Biosensors Pty Ltd | Method and apparatus for electrochemical analysis |
| US8192599B2 (en) * | 2005-05-25 | 2012-06-05 | Universal Biosensors Pty Ltd | Method and apparatus for electrochemical analysis |
| KR100675487B1 (ko) * | 2005-06-02 | 2007-01-30 | 주식회사 파이컴 | 프로브 카드 |
| US8101415B2 (en) * | 2005-07-05 | 2012-01-24 | Bayer Healthcare Llc | Calibration system for use with lateral flow assay test strips |
| CA2620586A1 (en) | 2005-08-31 | 2007-03-08 | Boris P. Kovatchev | Improving the accuracy of continuous glucose sensors |
| US8789756B2 (en) * | 2006-02-25 | 2014-07-29 | Roche Diagnostics Operations, Inc. | Test element coding apparatuses, systems and methods |
| EP1826705A1 (de) * | 2006-02-25 | 2007-08-29 | F.Hoffmann-La Roche Ag | Analytisches Verbrauchsmittel und Anordnung zum Auslesen von Informationen |
| US8388905B2 (en) * | 2006-03-13 | 2013-03-05 | Nipro Diagnostics, Inc. | Method and apparatus for coding diagnostic meters |
| US8388906B2 (en) * | 2006-03-13 | 2013-03-05 | Nipro Diagnostics, Inc. | Apparatus for dispensing test strips |
| US11559810B2 (en) | 2006-03-13 | 2023-01-24 | Trividia Health, Inc. | Method and apparatus for coding diagnostic meters |
| US8940246B2 (en) | 2006-03-13 | 2015-01-27 | Nipro Diagnostics, Inc. | Method and apparatus for coding diagnostic meters |
| US7653425B2 (en) | 2006-08-09 | 2010-01-26 | Abbott Diabetes Care Inc. | Method and system for providing calibration of an analyte sensor in an analyte monitoring system |
| US8224415B2 (en) | 2009-01-29 | 2012-07-17 | Abbott Diabetes Care Inc. | Method and device for providing offset model based calibration for analyte sensor |
| US9675290B2 (en) | 2012-10-30 | 2017-06-13 | Abbott Diabetes Care Inc. | Sensitivity calibration of in vivo sensors used to measure analyte concentration |
| US8219173B2 (en) | 2008-09-30 | 2012-07-10 | Abbott Diabetes Care Inc. | Optimizing analyte sensor calibration |
| US8163162B2 (en) | 2006-03-31 | 2012-04-24 | Lifescan, Inc. | Methods and apparatus for analyzing a sample in the presence of interferents |
| ES2655564T3 (es) | 2006-09-07 | 2018-02-20 | Otago Innovation Limited | Biomarcador para la detección precoz de trastornos cardiacos agudos |
| US20080124693A1 (en) * | 2006-10-26 | 2008-05-29 | Mcevoy Mary | System for determining an analyte in a bodily fluid sample that includes a graphics-based step-by-step tutorial module |
| US20080274552A1 (en) * | 2007-05-04 | 2008-11-06 | Brian Guthrie | Dynamic Information Transfer |
| US8239166B2 (en) | 2007-05-14 | 2012-08-07 | Abbott Diabetes Care Inc. | Method and apparatus for providing data processing and control in a medical communication system |
| US20080294024A1 (en) * | 2007-05-24 | 2008-11-27 | Cosentino Daniel L | Glucose meter system and monitor |
| ES2818194T3 (es) | 2007-10-02 | 2021-04-09 | Labrador Diagnostics Llc | Dispositivos modulares para puntos de atención y usos de los mismos |
| US8001825B2 (en) * | 2007-11-30 | 2011-08-23 | Lifescan, Inc. | Auto-calibrating metering system and method of use |
| US8603768B2 (en) * | 2008-01-17 | 2013-12-10 | Lifescan, Inc. | System and method for measuring an analyte in a sample |
| WO2009090392A1 (en) * | 2008-01-18 | 2009-07-23 | Lifescan Scotland Limited | Method and system of manufacturing test strip lots having a predetermined calibration characteristic |
| USD612279S1 (en) | 2008-01-18 | 2010-03-23 | Lifescan Scotland Limited | User interface in an analyte meter |
| EP2098863A1 (en) | 2008-03-04 | 2009-09-09 | Visgeneer, Inc. | A bio-monitoring system and methods of use thereof |
| US20090223287A1 (en) * | 2008-03-04 | 2009-09-10 | Visgeneer, Inc. | Bio-Monitoring System and Methods of Use Thereof |
| DK2265641T3 (en) | 2008-03-12 | 2018-04-23 | Otago Innovation Ltd | Biomarkers |
| CA2715921A1 (en) | 2008-03-12 | 2009-09-17 | Otago Innovation Limited | Biomarkers |
| IL197532A0 (en) | 2008-03-21 | 2009-12-24 | Lifescan Scotland Ltd | Analyte testing method and system |
| USD612275S1 (en) | 2008-03-21 | 2010-03-23 | Lifescan Scotland, Ltd. | Analyte test meter |
| USD611853S1 (en) | 2008-03-21 | 2010-03-16 | Lifescan Scotland Limited | Analyte test meter |
| USD615431S1 (en) | 2008-03-21 | 2010-05-11 | Lifescan Scotland Limited | Analyte test meter |
| WO2009126900A1 (en) | 2008-04-11 | 2009-10-15 | Pelikan Technologies, Inc. | Method and apparatus for analyte detecting device |
| USD611151S1 (en) | 2008-06-10 | 2010-03-02 | Lifescan Scotland, Ltd. | Test meter |
| USD611489S1 (en) | 2008-07-25 | 2010-03-09 | Lifescan, Inc. | User interface display for a glucose meter |
| USD611372S1 (en) | 2008-09-19 | 2010-03-09 | Lifescan Scotland Limited | Analyte test meter |
| US20110174618A1 (en) * | 2008-09-30 | 2011-07-21 | Menai Medical Technologies Limited | Sample measurement system |
| US8046175B2 (en) * | 2008-10-13 | 2011-10-25 | Actherm Inc | Analytical strip reading apparatus and the analyical strip used therein |
| US9375169B2 (en) | 2009-01-30 | 2016-06-28 | Sanofi-Aventis Deutschland Gmbh | Cam drive for managing disposable penetrating member actions with a single motor and motor and control system |
| EP2473098A4 (en) | 2009-08-31 | 2014-04-09 | Abbott Diabetes Care Inc | ANALYTICAL SIGNAL PROCESSING APPARATUS AND METHOD |
| KR101044556B1 (ko) * | 2009-09-03 | 2011-06-28 | 주식회사 인포피아 | 카메라를 이용한 검체 정량 측정 기기, 방법 및 시스템 |
| US8101065B2 (en) | 2009-12-30 | 2012-01-24 | Lifescan, Inc. | Systems, devices, and methods for improving accuracy of biosensors using fill time |
| US8877034B2 (en) * | 2009-12-30 | 2014-11-04 | Lifescan, Inc. | Systems, devices, and methods for measuring whole blood hematocrit based on initial fill velocity |
| GB201005357D0 (en) | 2010-03-30 | 2010-05-12 | Menai Medical Technologies Ltd | Sampling plate |
| GB201005359D0 (en) | 2010-03-30 | 2010-05-12 | Menai Medical Technologies Ltd | Sampling plate |
| US8965476B2 (en) | 2010-04-16 | 2015-02-24 | Sanofi-Aventis Deutschland Gmbh | Tissue penetration device |
| US9539374B2 (en) | 2010-05-12 | 2017-01-10 | Haemonetics Corporation | Donated blood collection kit |
| CN103140498B (zh) | 2010-07-19 | 2017-05-17 | 奥塔哥创新有限公司 | 信号生物标志物 |
| WO2012012341A1 (en) | 2010-07-19 | 2012-01-26 | Cilag Gmbh International | System and method for measuring an analyte in a sample |
| US8932445B2 (en) | 2010-09-30 | 2015-01-13 | Cilag Gmbh International | Systems and methods for improved stability of electrochemical sensors |
| US8617370B2 (en) | 2010-09-30 | 2013-12-31 | Cilag Gmbh International | Systems and methods of discriminating between a control sample and a test fluid using capacitance |
| EP4024029A3 (en) | 2011-01-21 | 2022-09-14 | Labrador Diagnostics LLC | Systems and methods for sample use maximization |
| US9927445B2 (en) * | 2011-05-18 | 2018-03-27 | Balwant Rai | Biomarkers for prediction, diagnosis, and monitoring of parkinson's disease |
| US9529002B2 (en) * | 2011-05-18 | 2016-12-27 | Balwant Rai | Biomarkers for prediction, diagnosis, and monitoring of Alzheimer's disease |
| US20140170735A1 (en) | 2011-09-25 | 2014-06-19 | Elizabeth A. Holmes | Systems and methods for multi-analysis |
| US8475739B2 (en) | 2011-09-25 | 2013-07-02 | Theranos, Inc. | Systems and methods for fluid handling |
| US9268915B2 (en) | 2011-09-25 | 2016-02-23 | Theranos, Inc. | Systems and methods for diagnosis or treatment |
| US8840838B2 (en) | 2011-09-25 | 2014-09-23 | Theranos, Inc. | Centrifuge configurations |
| US9619627B2 (en) | 2011-09-25 | 2017-04-11 | Theranos, Inc. | Systems and methods for collecting and transmitting assay results |
| US9664702B2 (en) | 2011-09-25 | 2017-05-30 | Theranos, Inc. | Fluid handling apparatus and configurations |
| US9632102B2 (en) | 2011-09-25 | 2017-04-25 | Theranos, Inc. | Systems and methods for multi-purpose analysis |
| US9810704B2 (en) | 2013-02-18 | 2017-11-07 | Theranos, Inc. | Systems and methods for multi-analysis |
| US10012664B2 (en) | 2011-09-25 | 2018-07-03 | Theranos Ip Company, Llc | Systems and methods for fluid and component handling |
| US9250229B2 (en) | 2011-09-25 | 2016-02-02 | Theranos, Inc. | Systems and methods for multi-analysis |
| ES2661516T3 (es) | 2012-03-20 | 2018-04-02 | Otago Innovation Limited | Biomarcadores |
| WO2014052136A1 (en) | 2012-09-26 | 2014-04-03 | Abbott Diabetes Care Inc. | Method and apparatus for improving lag correction during in vivo measurement of analyte concentration with analyte concentration variability and range data |
| US9244036B2 (en) * | 2012-11-16 | 2016-01-26 | Cilag Gmbh International | System and method for determination of a concentration of at least one interfering substance and correction of glucose concentration based on the concentration of the interfering substance |
| US10466247B2 (en) | 2012-11-20 | 2019-11-05 | Becton, Dickinson And Company | System and method for diagnosing sensor performance using analyte-independent ratiometric signals |
| US9395234B2 (en) | 2012-12-05 | 2016-07-19 | Cardiocom, Llc | Stabilizing base for scale |
| US9459231B2 (en) | 2013-08-29 | 2016-10-04 | Lifescan Scotland Limited | Method and system to determine erroneous measurement signals during a test measurement sequence |
| US9500616B2 (en) | 2013-12-23 | 2016-11-22 | Cilag Gmbh International | Multi-orientation test strip |
| US10379125B2 (en) | 2013-12-27 | 2019-08-13 | Becton, Dickinson And Company | System and method for dynamically calibrating and measuring analyte concentration in diabetes management monitors |
| CN105675603B (zh) * | 2015-05-16 | 2018-07-06 | 乔爱军 | 一种临床症状筛查试剂盒 |
| CN105137097A (zh) * | 2015-07-27 | 2015-12-09 | 王天星 | 智能凝血酶原时间监控系统及其监控方法 |
| EP3618712A1 (en) | 2017-05-03 | 2020-03-11 | Abbott Diabetes Care Inc. | Systems, devices, and methods with duration-based adjustment of sensor data |
| AU2018316818B2 (en) | 2017-08-18 | 2022-03-03 | Abbott Diabetes Care Inc. | Systems, devices, and methods related to the individualized calibration and/or manufacturing of medical devices |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5126952A (en) | 1991-01-22 | 1992-06-30 | Eastman Kodak Company | Bar coding calibration |
| DE59408870D1 (de) | 1993-04-23 | 1999-12-09 | Roche Diagnostics Gmbh | System zur Bevorratung und Zurverfügungstellung von Testelementen |
| US5366609A (en) | 1993-06-08 | 1994-11-22 | Boehringer Mannheim Corporation | Biosensing meter with pluggable memory key |
| US5989917A (en) | 1996-02-13 | 1999-11-23 | Selfcare, Inc. | Glucose monitor and test strip containers for use in same |
| US5856195A (en) | 1996-10-30 | 1999-01-05 | Bayer Corporation | Method and apparatus for calibrating a sensor element |
| US6168957B1 (en) * | 1997-06-25 | 2001-01-02 | Lifescan, Inc. | Diagnostic test strip having on-strip calibration |
| FI107080B (fi) * | 1997-10-27 | 2001-05-31 | Nokia Mobile Phones Ltd | Mittauslaite |
| US6084660A (en) | 1998-07-20 | 2000-07-04 | Lifescan, Inc. | Initiation of an analytical measurement in blood |
| US6261519B1 (en) | 1998-07-20 | 2001-07-17 | Lifescan, Inc. | Medical diagnostic device with enough-sample indicator |
| CA2351398A1 (en) * | 1998-11-30 | 2000-06-08 | Abbott Laboratories | Analyte test instrument having improved calibration and communication processes |
| US6475372B1 (en) | 2000-02-02 | 2002-11-05 | Lifescan, Inc. | Electrochemical methods and devices for use in the determination of hematocrit corrected analyte concentrations |
| US6514460B1 (en) * | 1999-07-28 | 2003-02-04 | Abbott Laboratories | Luminous glucose monitoring device |
| WO2002000112A2 (en) * | 2000-06-26 | 2002-01-03 | Boston Medical Technologies, Inc. | Glucose metering system |
| US6620310B1 (en) | 2000-12-13 | 2003-09-16 | Lifescan, Inc. | Electrochemical coagulation assay and device |
| US20030207441A1 (en) * | 2002-05-01 | 2003-11-06 | Eyster Curt R. | Devices and methods for analyte concentration determination |
| CN1218909C (zh) * | 2002-08-17 | 2005-09-14 | 吴嫦华 | 抗盐碱水稻壮秧肥 |
-
2002
- 2002-08-21 US US10/224,888 patent/US6780645B2/en not_active Expired - Lifetime
-
2003
- 2003-08-13 IL IL157381A patent/IL157381A/en active IP Right Grant
- 2003-08-20 ES ES03255154.1T patent/ES2519791T3/es not_active Expired - Lifetime
- 2003-08-20 KR KR1020030057528A patent/KR20040018161A/ko not_active Ceased
- 2003-08-20 JP JP2003296598A patent/JP2004132964A/ja active Pending
- 2003-08-20 EP EP03255154.1A patent/EP1391728B1/en not_active Expired - Lifetime
- 2003-08-20 TW TW092122801A patent/TWI317810B/zh not_active IP Right Cessation
- 2003-08-20 CA CA2437681A patent/CA2437681C/en not_active Expired - Fee Related
- 2003-08-21 CN CN03147083A patent/CN100587488C/zh not_active Expired - Fee Related
- 2003-08-21 SG SG200304849A patent/SG109525A1/en unknown
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007108171A (ja) * | 2005-09-30 | 2007-04-26 | Lifescan Inc | 迅速な電気化学的分析のための方法および装置 |
| JP2016122012A (ja) * | 2007-04-12 | 2016-07-07 | トリビディア ヘルス,インコーポレーテッド | 診断テストシステムにおけるエラーの検出及び排除 |
Also Published As
| Publication number | Publication date |
|---|---|
| IL157381A0 (en) | 2004-02-19 |
| EP1391728B1 (en) | 2014-07-30 |
| ES2519791T3 (es) | 2014-11-07 |
| US6780645B2 (en) | 2004-08-24 |
| KR20040018161A (ko) | 2004-03-02 |
| IL157381A (en) | 2009-09-01 |
| CN100587488C (zh) | 2010-02-03 |
| SG109525A1 (en) | 2005-03-30 |
| TW200407541A (en) | 2004-05-16 |
| CA2437681C (en) | 2011-07-19 |
| HK1061573A1 (en) | 2004-09-24 |
| CA2437681A1 (en) | 2004-02-21 |
| CN1495427A (zh) | 2004-05-12 |
| EP1391728A1 (en) | 2004-02-25 |
| US20040038411A1 (en) | 2004-02-26 |
| TWI317810B (en) | 2009-12-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2004132964A (ja) | 試験片較正コードを記憶している一定のメモリーを有する診断キットおよび関連の方法 | |
| Edition et al. | Quantifying uncertainty in analytical measurement | |
| US7129038B2 (en) | Method for selectively combining multiple membranes for assembly into test strips | |
| Ellison et al. | Quantifying uncertainty in analytical measurement | |
| Dutta et al. | Is it possible to estimate the parameters of the sigmoid Emax model with truncated data typical of clinical studies? | |
| Dunn et al. | Modelling method comparison data | |
| Varela et al. | Comprehensive evaluation of the internal and external quality control to redefine analytical quality goals | |
| JP2006503296A (ja) | ショートサンプルとロングサンプルとを検出するためのシステムおよび方法 | |
| AU2019250160B2 (en) | System and method for producing statistically valid assay means and ranges for quality control materials | |
| Linko et al. | Evaluation of uncertainty of measurement in routine clinical chemistry-applications to determination of the substance concentration of calcium and glucose in serum | |
| Tran et al. | Practical application of biological variation and Sigma metrics quality models to evaluate 20 chemistry analytes on the Beckman Coulter AU680 | |
| EP0422646B1 (en) | Improvement in calibration | |
| Simpson | Accuracy and precision of breath-alcohol measurements for a random subject in the postabsorptive state. | |
| Jing et al. | Reference materials for molecular diagnostics: Current achievements and future strategies | |
| JPH0627116A (ja) | スライド要素による被検体の定量方法 | |
| HK1061573B (en) | Method for assigning calibration codes to diagnostic test strips on the basis of calibration parameters | |
| Petersen et al. | A model for setting analytical quality specifications and design of control for measurements on the ordinal scale | |
| Han et al. | Sigma Metrics used to Evaluate the Performance of Internal Quality Control in a Clinical Biochemistry Laboratory. | |
| Milinković et al. | Bias in medical biochemistry-what laboratory professionals need to know? | |
| Simeon-Rudolf et al. | Interlaboratory study into the proficiency of serum cholinesterase activity measurement | |
| Bulska et al. | On the importance of metrology in chemistry | |
| Becker Jr | Analytical validation of in vitro diagnostic tests | |
| JPH09264893A (ja) | 乾式分析素子の測定値校正方法 | |
| Buzoianu et al. | Traceable measurements in clinical laboratories | |
| Petersen et al. | 4. Guidelines for Assessing Analytical Quality Requirements |