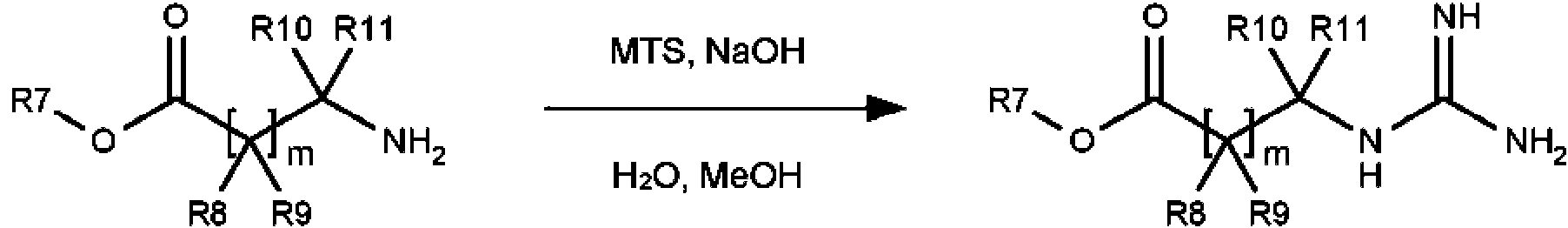ES2885451T3 - Inhibidores del transporte de creatina y usos de los mismos - Google Patents
Inhibidores del transporte de creatina y usos de los mismos Download PDFInfo
- Publication number
- ES2885451T3 ES2885451T3 ES15786453T ES15786453T ES2885451T3 ES 2885451 T3 ES2885451 T3 ES 2885451T3 ES 15786453 T ES15786453 T ES 15786453T ES 15786453 T ES15786453 T ES 15786453T ES 2885451 T3 ES2885451 T3 ES 2885451T3
- Authority
- ES
- Spain
- Prior art keywords
- cancer
- group
- alkyl
- compound
- optionally substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CCCC(*I*)(*(C)*(O)O)N(*)NI Chemical compound CCCC(*I*)(*(C)*(O)O)N(*)NI 0.000 description 12
- VLECESDFWJSSBT-UHFFFAOYSA-N COc1ccc(CN(CCN)N)cc1 Chemical compound COc1ccc(CN(CCN)N)cc1 VLECESDFWJSSBT-UHFFFAOYSA-N 0.000 description 1
- PIIYVEHKZLSCFD-WHFBIAKZSA-N C[C@@H](C1)[C@H](C)N1C(N)=N Chemical compound C[C@@H](C1)[C@H](C)N1C(N)=N PIIYVEHKZLSCFD-WHFBIAKZSA-N 0.000 description 1
- PSEFTPJIAYIZRD-IUYQGCFVSA-N C[C@@H]([C@@H](C1)C(O)=O)N1C(N)=N Chemical compound C[C@@H]([C@@H](C1)C(O)=O)N1C(N)=N PSEFTPJIAYIZRD-IUYQGCFVSA-N 0.000 description 1
- QLPMVIPQPSQTDY-UHFFFAOYSA-N NC(N(C1C2)C1C2(C(O)=O)O)=N Chemical compound NC(N(C1C2)C1C2(C(O)=O)O)=N QLPMVIPQPSQTDY-UHFFFAOYSA-N 0.000 description 1
- MIQRWLVALMQSLT-UHFFFAOYSA-N OC(CN(CCN1)C1=S)=O Chemical compound OC(CN(CCN1)C1=S)=O MIQRWLVALMQSLT-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C279/00—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups
- C07C279/04—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to acyclic carbon atoms of a carbon skeleton
- C07C279/14—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to acyclic carbon atoms of a carbon skeleton being further substituted by carboxyl groups
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/155—Amidines (), e.g. guanidine (H2N—C(=NH)—NH2), isourea (N=C(OH)—NH2), isothiourea (—N=C(SH)—NH2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/397—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having four-membered rings, e.g. azetidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4168—1,3-Diazoles having a nitrogen attached in position 2, e.g. clonidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4402—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 2, e.g. pheniramine, bisacodyl
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/704—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin attached to a condensed carbocyclic ring system, e.g. sennosides, thiocolchicosides, escin, daunorubicin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7105—Natural ribonucleic acids, i.e. containing only riboses attached to adenine, guanine, cytosine or uracil and having 3'-5' phosphodiester links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C257/00—Compounds containing carboxyl groups, the doubly-bound oxygen atom of a carboxyl group being replaced by a doubly-bound nitrogen atom, this nitrogen atom not being further bound to an oxygen atom, e.g. imino-ethers, amidines
- C07C257/10—Compounds containing carboxyl groups, the doubly-bound oxygen atom of a carboxyl group being replaced by a doubly-bound nitrogen atom, this nitrogen atom not being further bound to an oxygen atom, e.g. imino-ethers, amidines with replacement of the other oxygen atom of the carboxyl group by nitrogen atoms, e.g. amidines
- C07C257/14—Compounds containing carboxyl groups, the doubly-bound oxygen atom of a carboxyl group being replaced by a doubly-bound nitrogen atom, this nitrogen atom not being further bound to an oxygen atom, e.g. imino-ethers, amidines with replacement of the other oxygen atom of the carboxyl group by nitrogen atoms, e.g. amidines having carbon atoms of amidino groups bound to acyclic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C259/00—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups
- C07C259/12—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups with replacement of the other oxygen atom of the carboxyl group by nitrogen atoms, e.g. N-hydroxyamidines
- C07C259/14—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups with replacement of the other oxygen atom of the carboxyl group by nitrogen atoms, e.g. N-hydroxyamidines having carbon atoms of hydroxamidine groups bound to hydrogen atoms or to acyclic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C275/00—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups
- C07C275/70—Compounds containing any of the groups, e.g. isoureas
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C279/00—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups
- C07C279/16—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to carbon atoms of rings other than six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C279/00—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups
- C07C279/20—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups containing any of the groups, X being a hetero atom, Y being any atom, e.g. acylguanidines
- C07C279/24—Y being a hetero atom
- C07C279/26—X and Y being nitrogen atoms, i.e. biguanides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C279/00—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups
- C07C279/30—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to nitro or nitroso groups
- C07C279/32—N-nitroguanidines
- C07C279/36—Substituted N-nitroguanidines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C281/00—Derivatives of carbonic acid containing functional groups covered by groups C07C269/00 - C07C279/00 in which at least one nitrogen atom of these functional groups is further bound to another nitrogen atom not being part of a nitro or nitroso group
- C07C281/16—Compounds containing any of the groups, e.g. aminoguanidine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C281/00—Derivatives of carbonic acid containing functional groups covered by groups C07C269/00 - C07C279/00 in which at least one nitrogen atom of these functional groups is further bound to another nitrogen atom not being part of a nitro or nitroso group
- C07C281/16—Compounds containing any of the groups, e.g. aminoguanidine
- C07C281/18—Compounds containing any of the groups, e.g. aminoguanidine the other nitrogen atom being further doubly-bound to a carbon atom, e.g. guanylhydrazones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/01—Sulfonic acids
- C07C309/02—Sulfonic acids having sulfo groups bound to acyclic carbon atoms
- C07C309/03—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton
- C07C309/13—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing nitrogen atoms, not being part of nitro or nitroso groups, bound to the carbon skeleton
- C07C309/14—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing nitrogen atoms, not being part of nitro or nitroso groups, bound to the carbon skeleton containing amino groups bound to the carbon skeleton
- C07C309/15—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing nitrogen atoms, not being part of nitro or nitroso groups, bound to the carbon skeleton containing amino groups bound to the carbon skeleton the nitrogen atom of at least one of the amino groups being part of any of the groups, X being a hetero atom, Y being any atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C313/00—Sulfinic acids; Sulfenic acids; Halides, esters or anhydrides thereof; Amides of sulfinic or sulfenic acids, i.e. compounds having singly-bound oxygen atoms of sulfinic or sulfenic groups replaced by nitrogen atoms, not being part of nitro or nitroso groups
- C07C313/08—Sulfenic acids; Derivatives thereof
- C07C313/18—Sulfenamides
- C07C313/26—Compounds containing any of the groups, X being a hetero atom, Y being any atom
- C07C313/30—Y being a hetero atom
- C07C313/34—Y being a hetero atom either X or Y, but not both, being nitrogen atoms, e.g. N-sulfenylureas
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D205/00—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom
- C07D205/02—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom not condensed with other rings
- C07D205/04—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D205/00—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom
- C07D205/02—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom not condensed with other rings
- C07D205/06—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D205/08—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with one oxygen atom directly attached in position 2, e.g. beta-lactams
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/04—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D207/10—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D207/16—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/18—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having one double bond between ring members or between a ring member and a non-ring member
- C07D207/22—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/76—Nitrogen atoms to which a second hetero atom is attached
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/12—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/04—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D233/20—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with substituted hydrocarbon radicals, directly attached to ring carbon atoms
- C07D233/26—Radicals substituted by carbon atoms having three bonds to hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/04—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D233/28—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/44—Nitrogen atoms not forming part of a nitro radical
- C07D233/46—Nitrogen atoms not forming part of a nitro radical with only hydrogen atoms attached to said nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/04—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D233/28—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/44—Nitrogen atoms not forming part of a nitro radical
- C07D233/52—Nitrogen atoms not forming part of a nitro radical with hetero atoms directly attached to said nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/64—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms, e.g. histidine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/66—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/88—Nitrogen atoms, e.g. allantoin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/06—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/06—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D239/08—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms directly attached in position 2
- C07D239/12—Nitrogen atoms not forming part of a nitro radical
- C07D239/14—Nitrogen atoms not forming part of a nitro radical with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, attached to said nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
- C07D249/10—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D249/14—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D253/00—Heterocyclic compounds containing six-membered rings having three nitrogen atoms as the only ring hetero atoms, not provided for by group C07D251/00
- C07D253/02—Heterocyclic compounds containing six-membered rings having three nitrogen atoms as the only ring hetero atoms, not provided for by group C07D251/00 not condensed with other rings
- C07D253/06—1,2,4-Triazines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/08—Six-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/22—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with hetero atoms directly attached to ring nitrogen atoms
- C07D295/28—Nitrogen atoms
- C07D295/32—Nitrogen atoms acylated with carboxylic or carbonic acids, or their nitrogen or sulfur analogues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/095—Compounds containing the structure P(=O)-O-acyl, P(=O)-O-heteroatom, P(=O)-O-CN
- C07F9/097—Compounds containing the structure P(=O)-O-N
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/22—Amides of acids of phosphorus
- C07F9/24—Esteramides
- C07F9/2454—Esteramides the amide moiety containing a substituent or a structure which is considered as characteristic
- C07F9/2458—Esteramides the amide moiety containing a substituent or a structure which is considered as characteristic of aliphatic amines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)]
- C07F9/3804—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)] not used, see subgroups
- C07F9/3808—Acyclic saturated acids which can have further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)]
- C07F9/40—Esters thereof
- C07F9/4003—Esters thereof the acid moiety containing a substituent or a structure which is considered as characteristic
- C07F9/4006—Esters of acyclic acids which can have further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/48—Phosphonous acids [RP(OH)2] including [RHP(=O)(OH)]; Thiophosphonous acids including [RP(SH)2], [RHP(=S)(SH)]; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/553—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having one nitrogen atom as the only ring hetero atom
- C07F9/568—Four-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/553—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having one nitrogen atom as the only ring hetero atom
- C07F9/572—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/645—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having two nitrogen atoms as the only ring hetero atoms
- C07F9/6503—Five-membered rings
- C07F9/6506—Five-membered rings having the nitrogen atoms in positions 1 and 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/05—Isotopically modified compounds, e.g. labelled
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/02—Systems containing only non-condensed rings with a three-membered ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/04—Systems containing only non-condensed rings with a four-membered ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
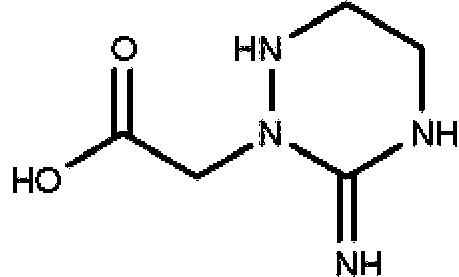
Un compuesto que tiene la estructura: **(Ver fórmula)** en donde b y c son cada uno, independientemente, 0 o 1; **(Ver fórmula)** Q1 es R9 es hidrógeno, halo, hidroxilo, NH2, alquilo C1-C3 opcionalmente sustituido; R10 es hidrógeno o alquilo C1-C4 opcionalmente sustituido: R11 es hidrógeno; o una sal farmacéuticamente aceptable del mismo.
Description
DESCRIPCIÓN
Inhibidores del transporte de creatina y usos de los mismos
Antecedentes de la invención
La creatina se sintetiza en el hígado y el riñón y se transporta por todo el cuerpo a tejidos con altas demandas de energía a través de un sistema de transporte activo. La creatina es usada por el cuerpo durante los momentos de mayor demanda de energía para volver a sintetizar rápidamente el ATP del ADP a través de la conversión anaeróbica de creatina fosforilada (fosfocreatina) en creatina en una reacción reversible de la enzima creatina quinasa. En momentos de bajas demandas de energía, puede utilizarse un exceso de ATP para convertir la creatina en fosfocreatina. La expresión aumentada de la creatina quinasa promueve la metástasis mejorando la supervivencia de las células cancerosas diseminadas en el hígado donde encuentran hipoxia hepática. La expresión aumentada de creatina quinasa da como resultado la producción de un exceso de fosfocreatina que puede usarse como un depósito energético para generar el ATP necesario para soportar la hipoxia hepática. La inhibición del sistema de fosfocreatina a través de la inhibición de la captación de creatina y/o la creatina quinasa en células cancerosas es por tanto un objetivo terapéutico para el tratamiento del cáncer y la metástasis. Fitch et al, Metabolism, Vol. 29, (7), 1980, 686 describe inhibidores de la acumulación de creatina y fosfocreatina en el músculo esquelético y el corazón.
Sumario de la invención
En un aspecto, la invención presenta un compuesto que tiene la estructura:
en donde b y c son cada uno, independientemente, 0 o 1; Q1 es
R9 es hidrógeno, halo, hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido; R10 es hidrógeno o alquilo C1-C4 opcionalmente sustituido; R11 es hidrógeno; o una sal farmacéuticamente aceptable del mismo.
En un aspecto, la invención presenta un compuesto que tiene la estructura:
o una sal farmacéuticamente aceptable del mismo.
En un aspecto, la invención presenta una composición farmacéutica que comprende un compuesto de la invención y un excipiente farmacéuticamente aceptable.
En un aspecto, la invención presenta un compuesto de la invención, o una composición farmacéutica de la invención, para su uso en un método para tratar el cáncer.
En un aspecto, la invención presenta un compuesto de la invención, o una composición farmacéutica de la invención, para su uso en un método para ralentizar la propagación de un cáncer migratorio; preferiblemente en donde dicho método comprende la supresión de la colonización metastásica de dicho cáncer migratorio en el hígado.
En un aspecto, la invención presenta un compuesto de la invención, o una composición farmacéutica de la invención, para su uso en un método para tratar el cáncer metastásico en un sujeto con necesidad de ello que comprende: (a) proporcionar a un sujeto al que se le ha identificado que tiene, o está en riesgo de tener, cáncer metastásico en base al nivel de expresión de miR-483-5p y/o miR-551a está por debajo de un valor de referencia predeterminado o el nivel de expresión de CKB y/o SLC6a8 está por encima de un valor de referencia predeterminado; y (b) administrar a dicho sujeto una cantidad eficaz de un compuesto de la invención o una
composición farmacéutica de la invención.
Esta invención presenta compuestos que inhiben el transporte de creatina y/o creatina quinasa, composiciones farmacéuticas que incluyen los compuestos de la invención y métodos para utilizar esas composiciones para inhibir el transporte de creatina y/o creatina quinasa (por ejemplo, para el tratamiento del cáncer).
Por consiguiente, en un primer aspecto la divulgación presenta un compuesto que tiene la estructura de Fórmula I:
en donde X1 está ausente, NH o CH2 ;
R1 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o arilo C6-C10 opcionalmente sustituido, alquilo C1-C6 ; R2, R3, y R4 son independientemente hidrógeno o alquilo C1 -C6 opcionalmente sustituido; y
R5 y R6 son hidrógeno o NH2 ;
en donde si R5 y R6 son ambos hidrógeno o R5 es NH2 y R6 es hidrógeno, entonces R2 es alquilo C1 -C6 opcionalmente sustituido,
o una sal farmacéuticamente aceptable del mismo.
En algunas realizaciones de la divulgación, R1 es hidrógeno. En otras realizaciones de la divulgación, R3 y R4 son hidrógeno. En ciertas realizaciones de la divulgación, R2 es hidrógeno o alquilo C1-C6 opcionalmente sustituido (por ejemplo, metilo, etilo, isopropilo, propilo, isobutilo, o haloalquilo C1-C6 opcionalmente sustituido como, trifluorometilo.
En algunas realizaciones de la divulgación, R5 y R6 son ambos hidrógeno y R2 es alquilo C1-C6 opcionalmente sustituido (por ejemplo, metilo, etilo, isopropilo, o isobutilo).
En otras realizaciones de la divulgación, R5 y R6 son ambos NH2. En ciertas realizaciones de la divulgación, R2 es hidrógeno. En algunas realizaciones de la divulgación, R2 es alquilo C1-C6 opcionalmente sustituido (por ejemplo, metilo o isopropilo).
En otras realizaciones de la divulgación, R5 es NH2 , R6 es hidrógeno y R2 es alquilo C1-C6 opcionalmente sustituido (por ejemplo, metilo o isopropilo).
En ciertas realizaciones de la divulgación, R5 es hidrógeno y R6 es NH2. En algunas realizaciones de la divulgación, R2 es hidrógeno. En otras realizaciones de la divulgación, R2 es alquilo C1-C6 opcionalmente sustituido (por ejemplo, metilo o isopropilo).
En ciertas realizaciones de la divulgación, X1 está ausente. En algunas realizaciones de la divulgación, X1 es CH2. En otras realizaciones de la divulgación, X1 es NH2.
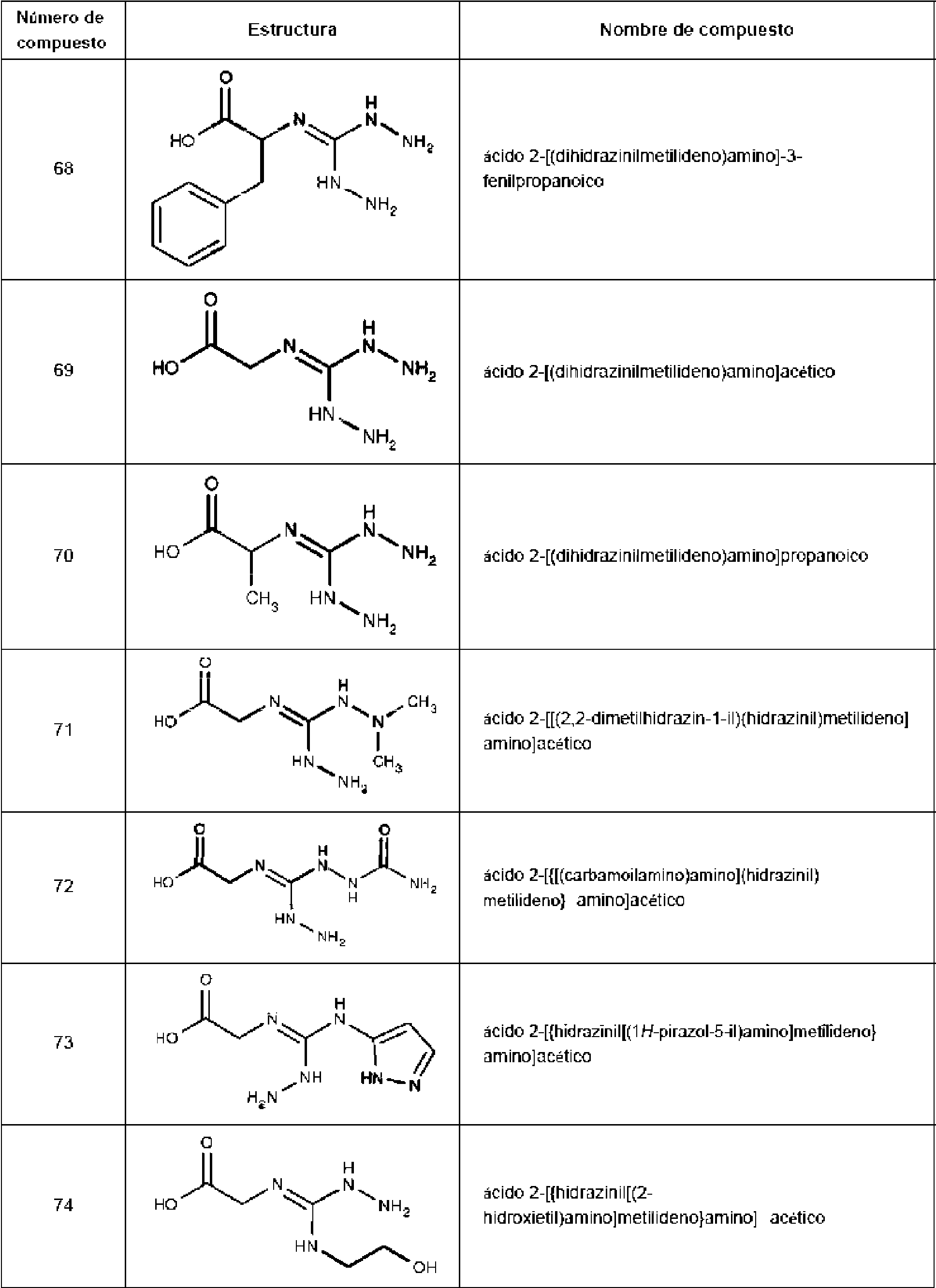
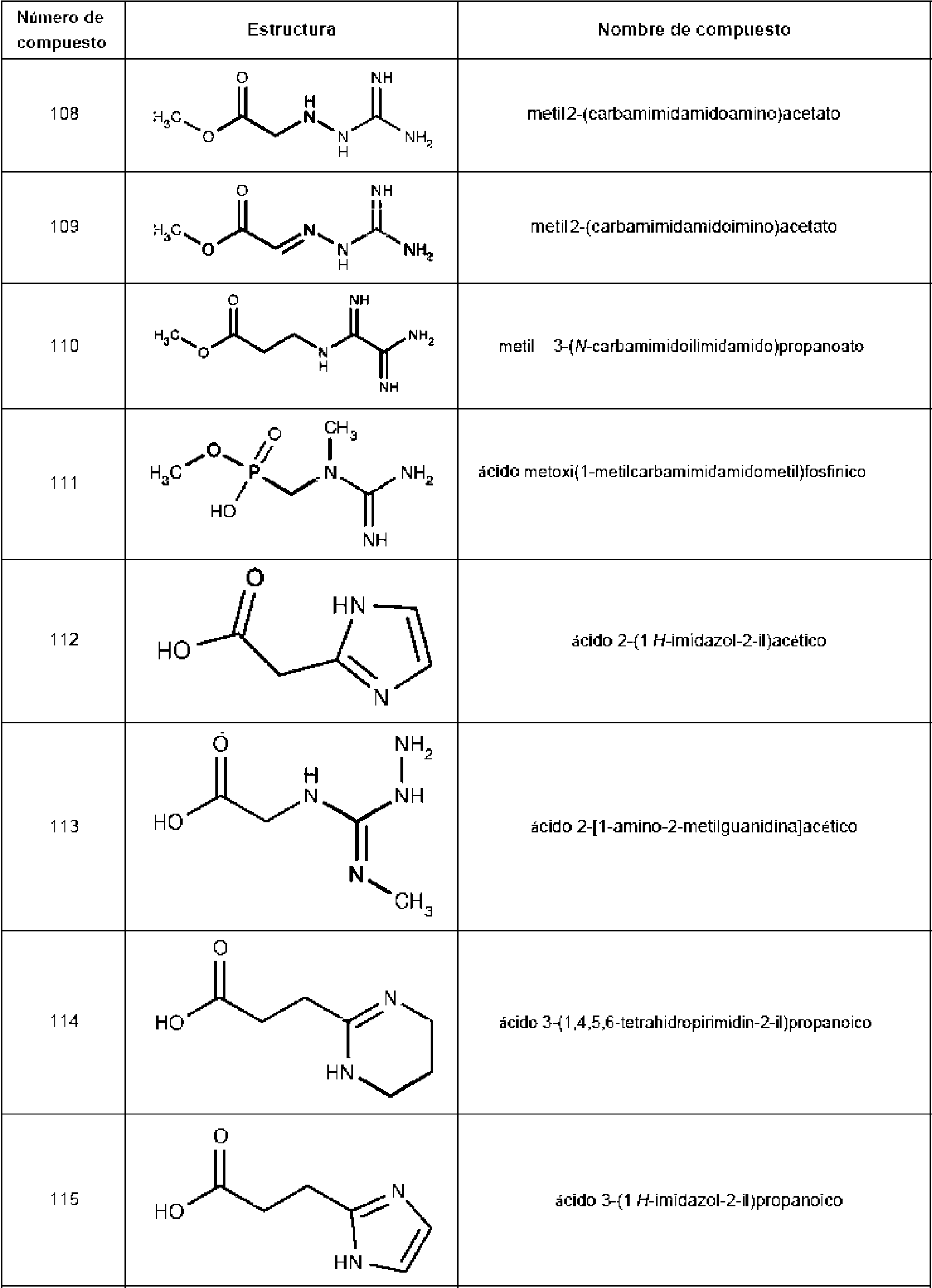
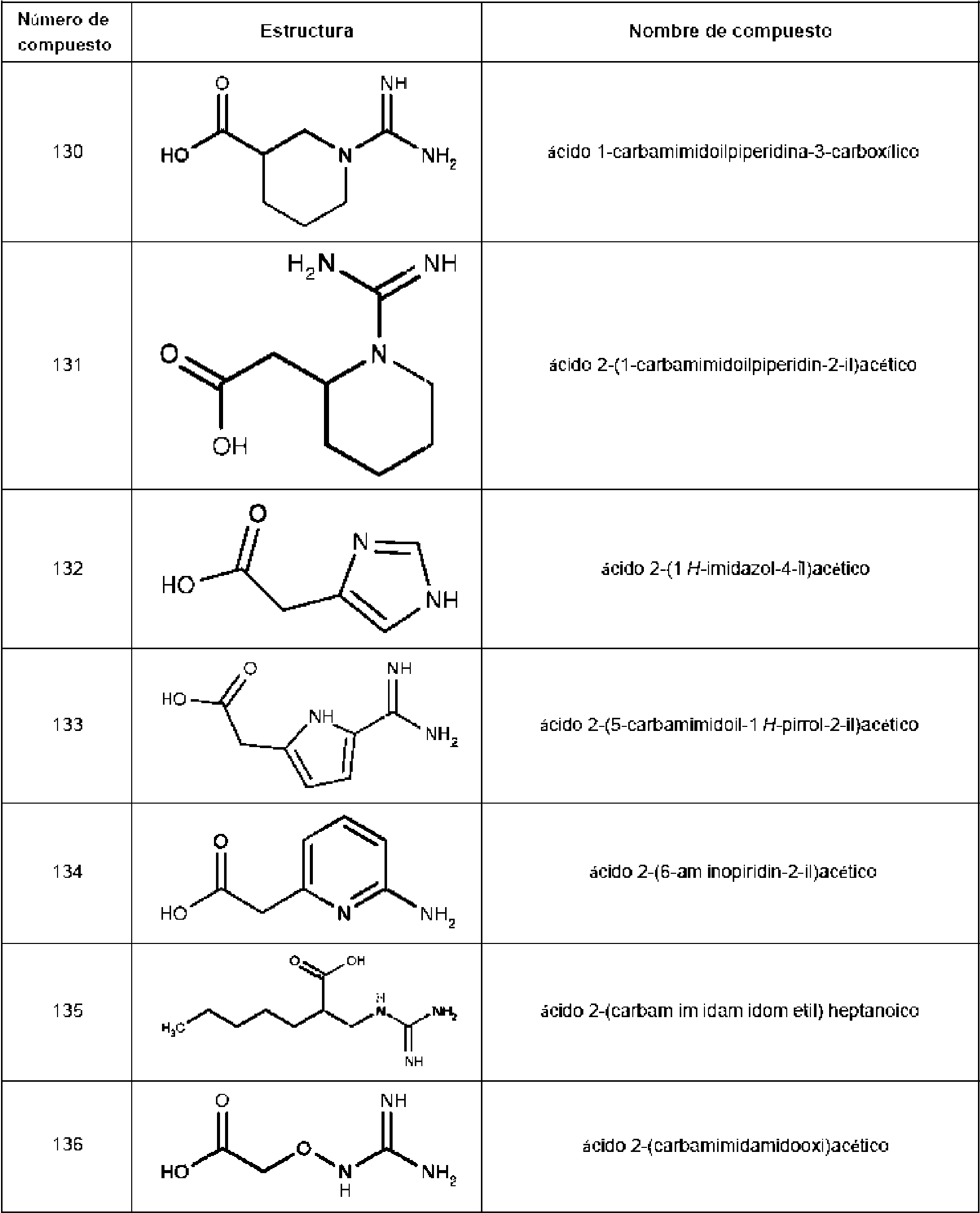
En ciertas realizaciones de la divulgación, el compuesto es un compuesto de la Tabla 1 (por ejemplo, el compuesto 225, 229, 230, 234 o 235).
Tabla 1: Inhibidores del sistema de fosfocreatina divulgados
(continuación)
(continuación)
En algunas realizaciones de la divulgación, el compuesto es un compuesto de la Tabla 2 (por ejemplo, el compuesto 237, 238, 241, 242, 244, 245, 247 o 248).
Tabla 2: Inhibidores del sistema de fosfocreatina divulgados
(continuación)
continuación
En otras realizaciones de la divulgación, el compuesto es un compuesto de la Tabla 3 (por ejemplo, compuesto 250 o 251).
Tabla 3. Inhibidores del sistema de fosfocreatina divul ados
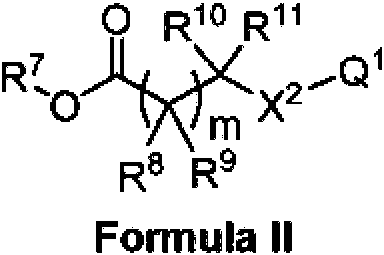
En otro aspecto, la divulgación presenta un compuesto que tiene la estructura de Fórmula II:
en donde Q1 es amidino opcionalmente sustituido o 2-piridilo opcionalmente sustituido;
X2 es S o NR12; m es 0 o 1;
R7 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o arilo C6-C10 alquilo C1-C6 opcionalmente sustituido; R8 y R9 son independientemente hidrógeno, deuterio, halo, hidroxilo, NH2 , alquilo C1-C6 opcionalmente sustituido, o R8 o R9 pueden combinarse con R10 o R11 para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido o con R12 para formar un heterociclo C3-C6 opcionalmente sustituido;
R10 y R11 son independientemente hidrógeno, deuterio, alquilo C1-C6 opcionalmente sustituido, o R10 o R11 pueden combinarse con R8 o R9 para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido;
R12 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o R12 puede combinarse con R8 o R9 para formar un heterociclo C3-C6 opcionalmente sustituido, y
en donde si R9 es halo, entonces R8 es halo o alquilo C1-C6 opcionalmente sustituido,
o una sal farmacéuticamente aceptable del mismo.
En algunas realizaciones de la divulgación, si Q1 es 2-piridilo opcionalmente sustituido, entonces R12 es hidrógeno.
En algunas realizaciones de la divulgación, R7 es hidrógeno. En otras realizaciones de la divulgación, m es 1. En ciertas realizaciones de la divulgación, R9 es hidrógeno, deuterio, o halo (por ejemplo, fluoro). En algunas realizaciones de la divulgación, R11 es hidrógeno o deuterio.
En otras realizaciones de la divulgación, R8 y R10 se combinan para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido (por ejemplo, ciclopropilo o ciclobutilo). En ciertas realizaciones, R10 y R11 son deuterio. En otras realizaciones de la divulgación, R8 y R9 son deuterio. En algunas realizaciones de la divulgación, tanto R8 como R9 son halo (por ejemplo, fluoro).
En otras realizaciones de la divulgación, R10 es alquilo C1-C6 opcionalmente sustituido (por ejemplo, haloalquilo C1-C6 opcionalmente sustituido, como trifluorometilo).
En ciertas realizaciones de la divulgación, R8 es NH2. En algunas realizaciones de la divulgación, R10 es alquilo C1-C6 opcionalmente sustituido (por ejemplo, metilo).
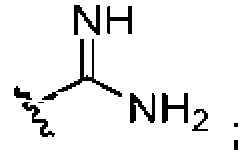
En otras realizaciones de la divulgación, Q1 es amidino opcionalmente sustituido (por ejemplo,
NH
Y ^ n h 2
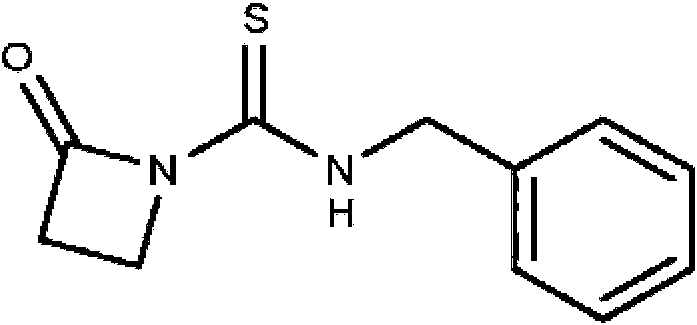
). En ciertas realizaciones de la divulgación, X2 es NR12. En algunas realizaciones de la divulgación, R8 y R12 se combinan para formar un heterociclo C3-C6 opcionalmente sustituido (por ejemplo, azetidina). En otras realizaciones de la divulgación, R12 es hidrógeno. En ciertas realizaciones, X2 es S.
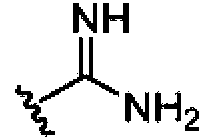
En algunas realizaciones de la divulgación, Q1 es 2-piridilo opcionalmente sustituido (por ejemplo,
). En otras realizaciones de la divulgación, X2 es NR12 y R12 es hidrógeno.
En algunas realizaciones de la divulgación, el compuesto tiene la estructura de Fórmula II:
en donde que Q1 es amidino opcionalmente sustituido o 2-piridilo opcionalmente sustituido;
X 2 es S o NR12; m es 1 o 2;
R7 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o arilo C6-C10 alquilo C1-C6 opcionalmente sustituido; R8 y R9 son independientemente hidrógeno, deuterio, halo, hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido, o R8 y R9 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6
opcionalmente sustituido; o R8 o R9 se combinan con R10 o R11 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R8 o R9 se combinan con R12 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido;
R10 y R11 son independientemente hidrógeno, deuterio, alquilo C1-C4 opcionalmente sustituido, alquenilo C2-C6 opcionalmente sustituido, alquinilo C2-C6 opcionalmente sustituido o R10 y R11 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido; o R10 o R11 se combinan con R8 o R9 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R10 o R11 se combinan con R12 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido;
R12 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o R12 se combina con R8, R9, R10 o R11 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido,
en donde si Q1 es 2-piridilo opcionalmente sustituido y R8 es alquilo C1-C3 opcionalmente sustituido, halo o hidroxilo, entonces por lo menos uno de R10 y R11 son independientemente deuterio, alquenilo C2-C6 opcionalmente sustituido, alquinilo C2-C6 opcionalmente sustituido o R10 y R11 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido; o R10 o R11 se combinan con R9 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R10 o R11 se combinan con R12 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido;
en donde si Q1 es 2-piridilo opcionalmente sustituido y R10 es alquilo C1-C4 opcionalmente sustituido, entonces por lo menos uno de R8 y R9 son independientemente deuterio, hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido, o R8 y R9 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido; o R8 o R9 se combinan con R11 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R8 o R9 se combinan con R12 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido;
en donde si m es 1 y R8 es hidrógeno, fluoro, hidroxilo o metilo, entonces por lo menos uno de R9, R10 y R11 no es hidrógeno;
en donde si m es 1 y R10 es metilo, entonces por lo menos uno de R8, R9 y R11 no es hidrógeno;
en donde si m es 1 y R8 es NH2 y R10 es hidrógeno, metilo o -CH2CH2OH entonces por lo menos uno de R9 o R11 no es hidrógeno;
o una sal farmacéuticamente aceptable del mismo.
En algunas realizaciones de la divulgación, si Q1 es 2-piridilo opcionalmente sustituido, entonces R12 es hidrógeno,
En otro aspecto, la divulgación presenta un compuesto que tiene la estructura de Fórmula V:
en donde Q1 es amidino opcionalmente sustituido o 2-piridilo opcionalmente sustituido;
m es 1 o 2;
R7 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o arilo C6-C10 alquilo C1-C6 opcionalmente sustituido; R8 y R9 son independientemente hidrógeno, deuterio, halo, hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido, o R8 y R9 se combinan con los átomos a los que están unidos para forma un anillo cicloalquilo C3-C6 opcionalmente sustituido; o R8 o R9 se combinan con R10 o R11 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R8 o R9 se combinan con R12 con los átomos a los que están unidos para forma un heterociclo C3-C5 opcionalmente sustituido;
R10 y R11 son independientemente hidrógeno, deuterio, alquilo C1-C4 opcionalmente sustituido, alquenilo C2-C6 opcionalmente sustituido, alquinilo C2-C6 opcionalmente sustituido o R10 y R11 se combinan con los átomos a los que están unidos para forma un anillo cicloalquilo C3-C6 opcionalmente sustituido; o R10 o R11 se combinan con R8 o R9 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R10 o R11 se combinan con R12 con los átomos a los que están unidos para forma un heterociclo C3-C4 opcionalmente sustituido;
R12 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o R12 se combina con R8 o R9 con los átomos a los que están unidos para forma un heterociclo C3-C5 opcionalmente sustituido, o R12 se combina con R10 o R11 con los átomos a los que están unidos para forma un heterociclo C3-C4 opcionalmente sustituido
en donde si m es 1 y R8 es hidrógeno, halo, hidroxilo o metilo, entonces por lo menos uno de R9, R10 y R11 no es hidrógeno;
en donde si m es 1 y R10 es metilo, entonces por lo menos uno de R8, R9 y R11 no es hidrógeno;
en donde si m es 1 y R8 es NH2 y R10 es hidrógeno, metilo o -CH2CH2OH entonces por lo menos uno de R9 o R11
no es hidrógeno;
en donde si m es 1, R8 es halo y R10 es alquilo C1-C4 opcionalmente sustituido, entonces por lo menos uno de R9 y R10 no es hidrógeno;
o una sal farmacéuticamente aceptable del mismo.
R7 es hidrógeno. Q1 es
NH
Y ^ n h 2
En algunas realizaciones, de la divulgación, Q1 es 2-piridilo opcionalmente sustituido (por ejemplo, 2-piridilo).
En algunas realizaciones de la divulgación, R8 se combina con R10 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido. En algunas realizaciones de la divulgación, el compuesto tiene la estructura de Fórmula VI:
en donde a es 0 o 1.
En otras realizaciones de la divulgación, el compuesto tiene la estructura de Fórmula VII:
Formula Vil
En algunas realizaciones de la divulgación, R9 es hidrógeno, hidroxilo o NH2. En otras realizaciones de la divulgación, R11 es hidrógeno.
En algunas realizaciones de la divulgación, m es 1 y R10 es deuterio, alquilo C1-C4 opcionalmente sustituido, alquenilo C2-C6 opcionalmente sustituido, alquinilo C2-C6 opcionalmente sustituido, o R10 y R11 se combinan con los átomos al que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido.
En otras realizaciones de la divulgación, R10 es deuterio. En algunas realizaciones de la divulgación, R11 es deuterio. En otras realizaciones de la divulgación, R8 y R9 son ambos deuterio. En algunas realizaciones de la divulgación, R10 es alquilo C1-C4 opcionalmente sustituido, alquenilo C2-C6 opcionalmente sustituido, alquinilo C2-C6 opcionalmente sustituido. En otras realizaciones de la divulgación, R10 es metilo, etilo, n-propilo, iso-propilo, -CD3 , -CF3 , -CH2F, -CHF2 , -CH=CH2 , o -C=CH. En algunas realizaciones de la divulgación, R11 es hidrógeno o metilo. En otras realizaciones de la divulgación, R8 es hidrógeno. En algunas realizaciones de la divulgación, R9 es hidrógeno, NH2 o metilo. En otras realizaciones de la divulgación, R10 y R11 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido (por ejemplo, un anillo cicloalquilo C3-C4 opcionalmente sustituido como ciclopropilo o ciclobutilo). En algunas realizaciones de la divulgación, R8 y R9 son ambos hidrógeno.
En otras realizaciones de la divulgación, R8 es halo, alquilo C1-C3 opcionalmente sustituido, o R8 y R9 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido. En algunas realizaciones de la divulgación, R8 es halo (por ejemplo, fluoro). En otras realizaciones de la divulgación, R9 es halo (por ejemplo, fluoro). En algunas realizaciones de la divulgación, R8 es alquilo C1-C3 opcionalmente sustituido (por ejemplo, metilo). En otras realizaciones, R9 es alquilo C1-C3 opcionalmente sustituido (por ejemplo,
metilo). En algunas realizaciones de la divulgación, R8 y R9 se combinan con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido (por ejemplo, un anillo cicloalquilo C3-C4 opcionalmente sustituido como ciclopropilo o ciclobutilo). En algunas realizaciones de la divulgación, R10 y R11 son ambos hidrógeno.
En ciertas realizaciones de la divulgación de los compuestos de Fórmula V, R12 es hidrógeno.
R12 se combina con R8 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido (por ejemplo, un heterociclo C4-C5 opcionalmente sustituido).
El compuesto tiene la estructura de Fórmula VIII:
en donde b y c son cada uno, independientemente, 0 o 1.
R10 es hidrógeno o alquilo C1-C4 opcionalmente sustituido (por ejemplo, metilo). R11 es hidrógeno. R9 es hidrógeno, halo (por ejemplo, fluoro), hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido (por ejemplo, metilo).
En otras realizaciones de la divulgación, R12 se combina con R10 con los átomos a los que están unidos para formar un heterociclo C3-C4 opcionalmente sustituido.
En algunas realizaciones de la divulgación, el compuesto tiene la estructura de Fórmula IX:
En algunas realizaciones de la divulgación, R11 es hidrógeno. En otras realizaciones de la divulgación, R8 y R9 son ambos hidrógeno.
En los compuestos de Fórmula V, Q1 es
En algunas realizaciones de la divulgación, el compuesto de Fórmula II o Fórmula V es cualquiera de los compuestos 253-262 o 327-385 en la Tabla 4. En algunas realizaciones, un compuesto de la invención es cualquiera de los compuestos 258, 335, 336, 337, 338, 339, 340, 341, 342, 376, 377, 378, o 385.
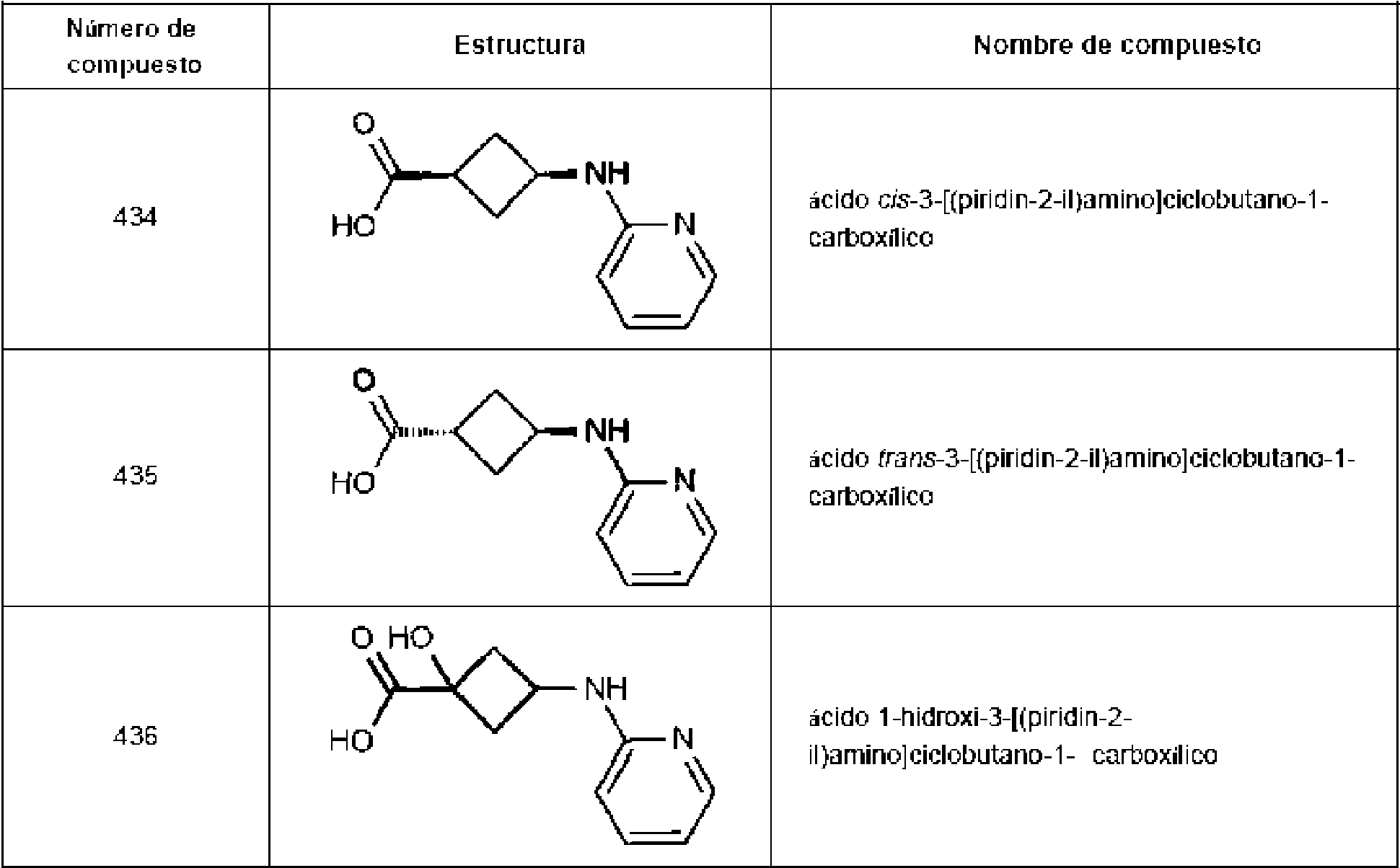
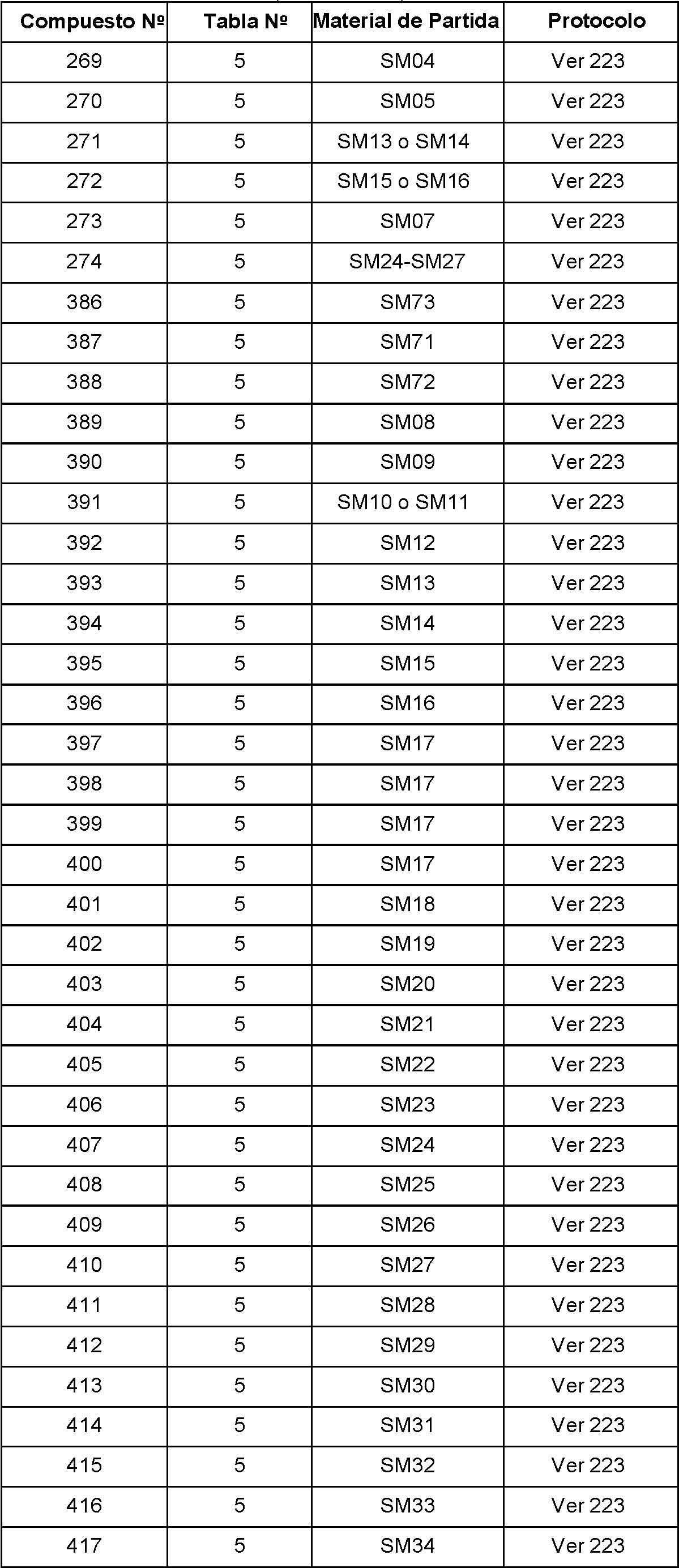
En algunas realizaciones de la divulgación, el compuesto de Fórmula II o Fórmula V es cualquiera de los compuestos 263-274 o 386-436 en la Tabla 5.
En otro aspecto, la invención presenta un compuesto seleccionado de cualquiera de los compuestos 258, 335, 336, 337, 338, 339, 340, 341, 342, 376, 377, 378, o 385 en la Tabla 4. En otro aspecto la divulgación presenta un compuesto seleccionado de cualquiera de los compuestos 253-262 y 327-385 en la Tabla 4. En algunas realizaciones de la divulgación, el compuesto es cualquiera de los compuestos 258, 327-338, 340, 343-348, 351 352, 366-367, 369-370, 372-375 y 379-385 en la Tabla 4.
Ċ
continuación
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
En otro aspecto, la divulgación presenta un compuesto seleccionado de cualquiera de los compuestos 263 y 386-436 en la Tabla 5.
Tabla 5. Inhibidores del sistema de fosfocreatina divulgados
(continuación)
(continuación)
continuación
(continuación)
(continuación)
(continuación)
Ċ
(continuación)
continuación
En otro aspecto, la divulgación presenta un compuesto seleccionado de cualquiera de los compuestos 275 en la Tabla 6.
Tabla 6. Inhibidores del sistema de fosfocreatina divulgados
continuación
continuación
En otro aspecto, la divulgación presenta un compuesto de la Tabla 7 que es sustancialmente enantioméricamente puro.
Tabla 7. Inhibidores del sistema de fosfocreatina divulgados
continuación
continuación
En otro aspecto, la divulgación presenta un compuesto que tiene la estructura:
A-B Fórmula III
en donde A es un inhibidor del transporte de creatina y/o creatina quinasa que comprende un grupo amidino;
B tiene la estructura:
Formula IV
en donde n es 0 o 1;
Q2 es hidroxilo, amino opcionalmente sustituido o -SO2OH; y
R13 y R14 son independientemente hidrógeno, -CO2H, o se combinan para formar C=O;
en donde B está conjugado con A en uno de los nitrógenos amidino,
o una sal farmacéuticamente aceptable del mismo.
En algunas realizaciones de la divulgación, R14 es hidrógeno. En otras realizaciones de la divulgación, R13 es -CO2H. En ciertas realizaciones de la divulgación, R13 es hidrógeno. En algunas realizaciones de la divulgación, R13 y R14 se combinan para formar C=O. En otras realizaciones de la divulgación, n es 0. En ciertas realizaciones de la divulgación, n es 1. En algunas realizaciones de la divulgación, Q 2 es amino opcionalmente sustituido (por ejemplo, -NH2 o
). En otras realizaciones de la divulgación, Q2 es hidroxilo. En ciertas realizaciones de la divulgación, Q 2 es -SO2OH.
En algunas realizaciones de la divulgación, B tiene la estructura:
En otras realizaciones de la divulgación, A tiene la estructura de cualquiera de los compuestos anteriores.
En otro aspecto, la divulgación presenta un compuesto seleccionado de cualquiera de los compuestos 1 8 o 323-326 en la Tabla 8.
Tabla 8. Inhibidores del sistema de fosfocreatina divul ados
Ċ
(continuación)
Continuación
(continuación)
(continuación)
continuación
(continuación)
continuación
(continuación)
Ċ
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
continuación
(continuación)
(continuación)
(continuación)
(continuación)
continuación
continuación
Ċ
(continuación)
Ċ
(continuación)
continuación
(continuación)
(continuación)
(continuación)
En otro aspecto, la divulgación presenta un compuesto seleccionado de cualquiera de los compuestos 287 8 en la Tabla 9.
Tabla 9. Inhibidores del sistema de fosfocreatina divulgados
En otro aspecto, la divulgación presenta un compuesto seleccionado de cualquiera de los compuestos 299 2 en la Tabla 10.
Tabla 10. Inhibidores del sistema de fosfocreatina divul ados
continuación
(continuación)
En otro aspecto, la invención presenta una composición que comprende un compuesto de la invención y un excipiente farmacéuticamente aceptable. En algunas realizaciones, la composición es una composición farmacéutica. En algunas realizaciones, el inhibidor del transporte de creatina o el inhibidor de la creatina quinasa en la composición es sustancialmente enantioméricamente puro.
En otro aspecto, la invención presenta un compuesto de la invención para su uso en un método para tratar el cáncer (por ejemplo, cáncer gastrointestinal como cáncer de esófago, cáncer de estómago, cáncer de páncreas, cáncer de hígado, cáncer de vesícula biliar, cáncer colorrectal, cáncer anal, cáncer de tejido linfoide asociado a mucosas, tumores del estroma gastrointestinal, cánceres del árbol biliar y tumor carcinoide gastrointestinal), que comprende administrar a un sujeto con necesidad de ello, un compuesto de la invención en una cantidad suficiente para tratar dicho cáncer. En algunas realizaciones de la divulgación, el compuesto es cualquiera de los compuestos
anteriores de Fórmula I, Fórmula II o Fórmula III. En otras realizaciones, el compuesto es cualquier compuesto de cualquiera de las Tablas 1-11 (por ejemplo, un compuesto de cualquiera de las Tablas 1-7, 9 o 10).
Tabla 11. Inhibidores del sistema de fosfocreatina divulgados
En otro aspecto, la invención presenta un compuesto de la invención para su uso en un método para ralentizar la propagación de un cáncer migratorio, que incluye administrar a un sujeto con necesidad de ello, un inhibidor del transporte de creatina y/o creatina quinasa en una cantidad suficiente para ralentizar la propagación de dicho cáncer migratorio. En algunas realizaciones, el método comprende la supresión de la colonización metastásica de dicho cáncer migratorio en el hígado de dicho sujeto. En algunas realizaciones, el cáncer migratorio es cáncer metastásico (por ejemplo, que incluye células que presentan migración, invasión de células migratorias, reclutamiento endotelial y/o angiogénesis). En otras realizaciones, el cáncer migratorio se propaga mediante la
siembra de la superficie de los espacios peritoneal, pleural, pericárdico o subaracnoideo. En ciertas realizaciones, el cáncer migratorio se propaga a través del sistema linfático. En algunas realizaciones, el cáncer migratorio se propaga por vía hematógena. En otras realizaciones, el cáncer migratorio es un cáncer de migración celular (por ejemplo, un cáncer de migración celular no metastásico como cáncer de ovario, mesotelioma o cáncer de pulmón primario).
En otro aspecto, la invención presenta un método para inhibir la proliferación o el crecimiento de células madre cancerosas o células iniciadoras de cáncer, que incluye poner en contacto la célula con un inhibidor del transporte de creatina y/o creatina quinasa en una cantidad suficiente para inhibir la proliferación o el crecimiento de dicha célula.
En otro aspecto, la invención presenta un compuesto de la invención para su uso en un método para reducir la tasa de siembra tumoral de un cáncer que incluye administrar a un sujeto con necesidad de ello un inhibidor del transporte de creatina y/o creatina quinasa en una cantidad suficiente para reducir la siembra tumoral.
En otro aspecto, la invención presenta un compuesto de la invención para su uso en un método para reducir o tratar la formación de nódulos metastásicos de cáncer que incluye administrar a un sujeto con necesidad de ello un inhibidor del transporte de creatina y/o creatina quinasa en una cantidad suficiente para tratar dicha formación de nódulos metastásicos del cáncer.
En otro aspecto, la invención presenta un compuesto de la invención para su uso en un método para tratar cáncer metastásico en un sujeto con necesidad de ello. El método incluye: (a) proporcionar a un sujeto al que se ha identificado que tiene, o que está en riesgo de tener, cáncer metastásico en base a que el nivel de expresión de miR-483-5p y/o miR-551a está por debajo de un valor de referencia predeterminado o el nivel de expresión de CKB y/o SLC6a8 está por encima de un valor de referencia predeterminado; y (b) administrar a dicho sujeto una cantidad eficaz de cualquiera de los compuestos anteriores de la invención.
En otro aspecto, la invención presenta un compuesto de la invención para su uso en un método para tratar cáncer metastásico en un sujeto con necesidad de ello, que comprende poner en contacto el canal de transporte de creatina SLC6a8 con cualquiera de los compuestos anteriores de la invención en una cantidad eficaz para suprimir la colonización metastásica de dicho cáncer.
En algunas realizaciones de cualquiera de los métodos anteriores, el cáncer es cáncer de mama, cáncer de colon, cáncer de células renales, cáncer de pulmón de células no pequeñas, carcinoma hepatocelular, cáncer gástrico, cáncer de ovario, cáncer de páncreas, cáncer de esófago, cáncer de próstata, sarcoma, o melanoma. En otras realizaciones de cualquiera de los métodos anteriores, el cáncer es cáncer gastrointestinal como cáncer de esófago, cáncer de estómago, cáncer de páncreas, cáncer de hígado, cáncer de vesícula biliar, cáncer colorrectal, cáncer anal, cáncer de tejido linfoide asociado a mucosas, tumores del estroma gastrointestinal, cánceres del árbol biliar y tumor carcinoide gastrointestinal.
En ciertas realizaciones de cualquiera de los métodos anteriores, el método incluye la administración de cualquiera de las composiciones anteriores de la invención. En algunas realizaciones de cualquiera de los métodos anteriores, el método incluye la administración de una composición que incluye un inhibidor del transporte de creatina o un inhibidor de creatina quinasa que es sustancialmente enantioméricamente puro.
En otras realizaciones de cualquiera de los métodos anteriores, el cáncer es un cáncer resistente a fármacos (por ejemplo, el cáncer es resistente a vemurafenib, dacarbazina, un inhibidor de CTLA4, un inhibidor de BRAF, un inhibidor de MEK, un inhibidor de PD1 o un inhibidor de PDL1).
En otras realizaciones de cualquiera de los métodos anteriores, el método incluye además la administración de un antiproliferativo (por ejemplo, capecitabina, gemcitabina, fluorouracilo, FOLFOX (5-FU, leucovorina y Eloxatina), FOLFIRI (5-FU, leucovorina y Camptosar), EOX (epirrubicina, oxaliplatino y Xeloda), Taxotere, Erbitux, Zaltrap, Vectibix, Ramucirumab, Tivozanib, Stivarga, CRS-207, un anticuerpo p D-1 o PDL-1 (por ejemplo, Nivolumab, pembrolizumab, MEDI4736 o MPDL3280A) y terapias que se dirigen a CDK4/6, EGFR, Pa Rp ), en donde cualquiera de los compuestos anteriores y el antiproliferativo se administran en una cantidad que, en conjunto, es suficiente para ralentizar la progresión del cáncer migratorio. En ciertas realizaciones, cualquiera de los compuestos anteriores y el antiproliferativo se administran en el plazo de 28 días entre sí en cantidades que en conjunto son eficaces para tratar al sujeto.
En ciertas realizaciones de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos anteriores de la invención. En ciertas realizaciones de la divulgación de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos anteriores de Fórmula I, Fórmula II, Fórmula III o Fórmula V. En otras realizaciones de la divulgación, el compuesto es cualquier compuesto de cualquiera de las Tablas 1-11 o una sal farmacéuticamente aceptable del mismo (por ejemplo, un compuesto de cualquiera de las Tablas 1-7, 9 o 10). En algunas realizaciones
de la divulgación, el compuesto es cualquier compuesto de la Tabla 4 o una sal farmacéuticamente aceptable del mismo.
En algunas realizaciones de la divulgación, de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos 7-9, 11, 15, 16, 28, 29, 30, 32, 33, 34, 43, 47, 48, 51, 52, 54, 67, 69, 70, 79, 80, 85, 124, 132, 149, 150, 187, 188, 190, 192-195, 199, 210-213, 215, 217, 324, 447 o 448 o una sal farmacéuticamente aceptable de los mismos. En otras realizaciones de la divulgación, de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos 16, 28, 29, 33, 34, 43, 47, 85, 124, 149, 150, 210- 213, 215, 217, 324, 447 o 448 o una sal farmacéuticamente aceptable de los mismos. En ciertas realizaciones de cualquiera de la divulgación de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos 26, 28, 34, 92, 96, 124, 125, 149, 150, 161, 163, 207, 324, 447 o 448 o una sal farmacéuticamente aceptable de los mismos. En ciertas realizaciones de la divulgación de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos 28, 34, 124, 149 o 150 o una sal farmacéuticamente aceptable de los mismos. En algunas realizaciones de la divulgación de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es el compuesto 34, un estereoisómero del mismo y/o una sal farmacéuticamente aceptable del mismo. En algunas realizaciones de la divulgación de cualquiera de los métodos anteriores, el inhibidor del transporte de creatina y/o creatina quinasa es cualquiera de los compuestos 219-224, o una sal farmacéuticamente aceptable del mismo.
Térm inos quím icos
Como se usa en la presente, se pretende que el término "compuesto" incluya todos los estereoisómeros, isómeros geométricos, tautómeros e isótopos de las estructuras representadas.
Los compuestos descritos en la presente pueden ser asimétricos (por ejemplo, tener uno o más estereocentros). Todos los estereoisómeros, como enantiómeros y diastereómeros, están incluidos a menos que se indique lo contrario. Los compuestos de la presente divulgación que contienen átomos de carbono asimétricamente sustituidos pueden aislarse en formas ópticamente activas o racémicas. En la técnica se conocen métodos sobre cómo preparar formas ópticamente activas a partir de materiales de partida ópticamente activos, como por resolución de mezclas racémicas o por síntesis estereoselectiva. En los compuestos descritos en la presente también pueden estar presentes muchos isómeros geométricos de olefinas y enlaces dobles C=N, y todos estos isómeros estables se contemplan en la presente divulgación. Se describen los isómeros geométricos cis y trans de los compuestos de la presente divulgación y pueden aislarse como una mezcla de isómero o como formas isoméricas separadas.
Los compuestos de la presente divulgación también incluyen formas tautoméricas. Las formas tautoméricas son el resultado del intercambio de un enlace simple con un enlace doble adyacente y la migración concomitante de un protón. Las formas tautoméricas incluyen tautómeros prototrópicos que son estados de protonación isoméricos que tienen la misma fórmula empírica y carga total. Los ejemplos de tautómeros prototrópicos incluyen parejas cetona-enol, parejas amida-ácido imídico, parejas lactama-lactima, parejas amida-ácido imídico, parejas enaminaimina y formas anulares donde un protón puede ocupar dos o más posiciones de un sistema heterocíclico, como, 1H- y 3H-imidazol, 1H-, 2H- y 4H-1,2,4-triazol, 1H- y 2H-isoindol y 1H- y 2H-pirazol. Las formas tautoméricas pueden estar en equilibrio o bloqueadas estéricamente en una forma mediante una sustitución apropiada.
Los compuestos de la presente divulgación también incluyen todos los isótopos de los átomos que se encuentran en los compuestos intermedios o finales. "Isótopos" se refiere a átomos que tienen el mismo número atómico pero diferentes números de masa resultantes de un número diferente de neutrones en los núcleos. Por ejemplo, los isótopos de hidrógeno incluyen tritio y deuterio.
Los compuestos y sales de la presente divulgación pueden prepararse en combinación con moléculas de agua o solvente para formar solvatos e hidratos mediante métodos rutinarios.
En varios lugares de la presente memoria descriptiva, los sustituyentes de los compuestos de la presente divulgación se divulgan en grupos o en intervalos. Se pretende específicamente que la presente divulgación incluya todas y cada una de las subcombinaciones individuales de los miembros de tales grupos e intervalos. Por ejemplo, se pretende específicamente que el término "alquilo C W divulgue individualmente metilo, etilo, alquilo C3 , alquilo C4 , alquilo C5 y alquilo C6. En la presente, se pretende que una frase de la forma "X opcionalmente sustituido" (por ejemplo, alquilo opcionalmente sustituido) sea equivalente a "X, donde X está opcionalmente sustituido" (por ejemplo, "alquilo, donde el alquilo está opcionalmente sustituido"). No se pretende que signifique que la característica "X" (por ejemplo, alquilo) per se sea opcional.
El término "acilo", como se usa en la presente, representa un hidrógeno o un grupo alquilo (por ejemplo, un grupo haloalquilo), como se define en la presente, que está unido al grupo molecular original a través de un grupo carbonilo, como se define en la presente, y se ejemplifica por formilo (es decir, un grupo carboxialdehído), acetilo,
trifluoroacetilo, propionilo y butanoílo. Los grupos acilo no sustituidos ejemplares incluyen de 1 a 7, de 1 a 11 o de 1 a 21 carbonos. En algunas realizaciones, el grupo alquilo está sustituido además con 1, 2, 3 o 4 sustituyentes como se describe en la presente.
Los ejemplos no limitativos de grupos acilo opcionalmente sustituidos incluyen alcoxicarbonilo, alcoxicarbonilacilo, arilalcoxicarbonilo, ariloílo, carbamoílo, carboxialdehído, (heterociclil) imino y (heterociclil)oilo:
El grupo "alcoxicarbonilo", que como se usa en la presente, representa un alcoxi, como se define en la presente, unido al grupo molecular original a través de un átomo de carbonilo (por ejemplo, -C(O)-OR, donde R es H o un grupo alquilo C1 -6, C1-10 o C1-20 opcionalmente sustituido). Los alcoxicarbonilos no sustituidos ejemplares incluyen de 1 a 21 carbonos (por ejemplo, de 1 a 11 o de 1 a 7 carbonos). En algunas realizaciones, el grupo alcoxi está sustituido además con 1, 2, 3 o 4 sustituyentes como se describe en la presente.
El grupo "alcoxicarbonilacilo", como se usa en la presente, representa un grupo acilo, como se define en la presente, que está sustituido con un grupo alcoxicarbonilo, como se define en la presente (por ejemplo, -C(O)-alquil-C(O)-OR, donde R es un grupo alquilo C1-6, C1-10 o C1-20 opcionalmente sustituido). Los alcoxicarbonilacilos no sustituidos ejemplares incluyen de 3 a 41 carbonos (por ejemplo, de 3 a 10, de 3 a 13, de 3 a 17, de 3 a 21 o de 3 a 31 carbonos, como alcoxicarbonil C1-6-acilo C1-6, alcoxicarbonil C1-10-acilo C1-10 , o alcoxicarbonil C1-20-acilo C1-20). En algunas realizaciones, cada grupo alcoxi y alquilo está sustituido además independientemente con 1, 2, 3 o 4 sustituyentes, como se describe en la presente (por ejemplo, un grupo hidroxi) para cada grupo.
El grupo "arilalcoxicarbonilo", como se usa en la presente, representa un grupo arilalcoxi, como se define en la presente, unido al grupo molecular original a través de un carbonilo (por ejemplo, -C(O)-O-alquil-arilo). Los grupos arilalcoxi no sustituidos ejemplares incluyen de 8 a 31 carbonos (por ejemplo, de 8 a 17 o de 8 a 21 carbonos, como aril C6-10-alcoxicarbonilo C1-6, aril C6-10-alcoxicarbonilo C1-10 o aril C6-10-alcoxicarbonilo C1-20). En algunas realizaciones, el grupo arilalcoxicarbonilo puede estar sustituido con 1, 2, 3 o 4 sustituyentes como se define en la presente.
El grupo "ariloílo", como se usa en la presente, representa un grupo arilo, como se define en la presente, que está unido al grupo molecular original a través de un grupo carbonilo. Los grupos ariloílo no sustituidos ejemplares tienen de 7 a 11 carbonos. En algunas realizaciones, el grupo arilo puede estar sustituido con 1, 2, 3 o 4 sustituyentes como se define en la presente.
El grupo "carbamoílo", como se usa en la presente, representa -C(O)-N(RN1) 2 , donde el significado de cada RN1 se encuentra en la definición de "amino" proporcionada en la presente.
El grupo "carboxialdehído", como se usa en la presente, representa un grupo acilo que tiene la estructura -CHO.
El grupo "(heterociclil) imino", como se usa en la presente, representa un grupo heterociclilo, como se define en la presente, unido al grupo molecular original a través de un grupo imino. En algunas realizaciones, el grupo heterociclilo puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente.
El grupo "(heterociclil)oilo", como se usa en la presente, representa un grupo heterociclilo, como se define en la presente, unido al grupo molecular original a través de un grupo carbonilo. En algunas realizaciones, el grupo heterociclilo puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente.
El término "alquilo", como se usa en la presente, incluye grupos saturados tanto de cadena lineal como de cadena ramificada de 1 a 20 carbonos (por ejemplo, de 1 a 10 o de 1 a 6), a menos que se especifique lo contrario. Los grupos alquilo están ejemplificados por metilo, etilo, n- e iso-propilo, n-, sec-, iso- y terc-butilo y neopentilo, y pueden estar opcionalmente sustituidos con uno, dos, tres o, en el caso de grupos alquilo de dos carbonos o más, cuatro sustituyentes seleccionados independientemente del grupo que consiste de: (1) alcoxi C1-6; (2) alquilsulfinilo C1-6; (3) amino, como se define en la presente (por ejemplo, amino no sustituido (es decir, -NH2) o un amino sustituido (es decir, -N(RN1)2 , donde RN1 es como se define para amino); (4) aril C6-10-alcoxi C1-6; (5) azido; (6) halo; (7) (heterociclil C2-9)oxi; (8) hidroxi, opcionalmente sustituido con un grupo protector O-; (9) nitro; (10) oxo (por ejemplo, carboxialdehído o acilo); (11) espirociclilo C1-7; (12) tioalcoxi; (13) tiol; (14) -CO2RA opcionalmente sustituido con un grupo protector O- y donde RA' se selecciona del grupo que consiste de (a) alquilo C1-20 (por ejemplo, alquilo C1-6), (b) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c) arilo C6-10, (d) hidrógeno, (e) alq C1-6-arilo-C6-10, (f) amino-alquilo C1-20, (g) polietilenglicol de-(CH2)s2(OCH2CH2)s1(CH2)s3OR', donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6, o de 1 a 10), y R' es H o alquilo C1-20, y (h) amino-polietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6, o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; (15) -C(O)NRB'RC', donde cada uno de RB' y RC' se selecciona, independientemente, del grupo que consiste de (a)
hidrógeno, (b) alquilo Ci-6, (c) arilo C6-10 y (d) alqu Ci-6-arilo C{6-io; (16) -SO2RD', donde RD' se selecciona del grupo que consiste de (a) alquilo C1-6 , (b) arilo C6-10 , (c) alqu C1-6-arilo C6-10 , y (d) hidroxi; (17) - SO2NRE'RF', donde cada uno de RE’ y RF' se selecciona, independientemente, del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6 , (c) arilo C6-10 y (d) alqu C1-6-arilo C{6-1o; (18) -C(O) RG', donde RG' se selecciona del grupo que consiste de (a) alquilo C1-20 (por ejemplo, alquilo C1-6), (b) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c) arilo C6-10 , (d) hidrógeno, (e) alqu C1-6-arilo C6-10 , (f) amino- alquilo C1-20, (g) polietilenglicol de -(CH2)s2(OCH2CH2)s1(CH2)s3OR', donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y R' es h o alquilo C1-20, y (h) aminopolietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6, o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; (19) -NRH'C(O)RI', donde RH’ se selecciona del grupo que consiste de (a1) hidrógeno y (b1) alquilo C1-6 , y R1’ se selecciona del grupo que consiste de (a2) alquilo C1-20 (por ejemplo, alquilo C1-6), (b2) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c2) arilo C6-10 , (d2) hidrógeno, (e2) alqu C1-6-arilo C6-10 , (f2) amino-alquilo C1-20, (g2) polietilenglicol de -(CH2)s2(OCH2CH2)s1(CH2)s3OR', en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y R' es H o alquilo C1-20 y (h2) amino-polietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; (20) -NRJ'C(O)ORK', donde RJ' se selecciona del grupo que consiste de (a1) hidrógeno y (b1) alquilo C1-6, y RK' se selecciona del grupo que consiste de (a2) alquilo C1-20 (por ejemplo, alquilo C1-6), (b2) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c2) arilo C6-10, (d2) hidrógeno, (e2) alqu C1-6-arilo C6-10 , (f2) amino-alquilo C1-20, (g2) polietilenglicol de -(CH2)s2(OCH2CH2)s1(CH2)s3OR', donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y R' es H o alquilo C1-20, y (h2) amino-polietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; y (21) amidina. En algunas realizaciones, cada uno de estos grupos puede sustituirse adicionalmente como se describe en la presente. Por ejemplo, el grupo alquileno de un alcarilo C1 puede sustituirse adicionalmente con un grupo oxo para proporcionar el sustituyente ariloílo respectivo.
El término "alquileno" y el prefijo "alqu-", como se usan en la presente, representan un grupo hidrocarburo divalente saturado derivado de un hidrocarburo saturado de cadena lineal o ramificada mediante la eliminación de dos átomos de hidrógeno, y se ejemplifica por metileno, etileno e isopropileno.. El término "alquileno Cx-y" y el prefijo " alqu Cx-y" representan grupos alquileno que tienen entre x e y carbonos. Los valores ejemplares para x son 1, 2, 3, 4, 5 y 6, y los valores ejemplares para y son 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, o 20 (por ejemplo, alquileno C1-6 , C1-10 , C2-20, C2-6 , C2-10 o C2-20). En algunas realizaciones, el alquileno puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente para un grupo alquilo.
Los ejemplos no limitativos de grupos alquilo y alquileno opcionalmente sustituidos incluyen acilaminoalquilo, aciloxialquilo, alcoxialquilo, alcoxicarbonilalquilo, alquilsulfinilo, alquilsulfinilalquilo, aminoalquilo, carbamoilalquilo, carboxialquilo, carboxiaminoalquilo, haloalquilo, hidroxialquilo, perfluoroalquilo y sulfoalquilo.
El grupo "acilaminoalquilo", que como se usa en la presente, representa un grupo acilo, como se define aquí, unido a un grupo amino que a su vez está unido al grupo molecular original a través de un grupo alquileno, como se define en la presente (es decir, -alquil-N(RN1)-C(O)-R, donde R es H o un grupo alquilo C1-6 , C1-10 o C1-20 opcionalmente sustituido (por ejemplo, haloalquilo) y RN1 es como se define en la presente). Los grupos acilaminoalquilo no sustituidos ejemplares incluyen de 1 a 41 carbonos (por ejemplo, de 1 a 7, de 1 a 13, de 1 a 21, de 2 a 7, de 2 a 13, de 2 a 21 o de 2 a 41 carbonos). En algunas realizaciones, el grupo alquileno está además sustituido con 1, 2, 3 o 4 sustituyentes como se describe en la presente, y/o el grupo amino es -NH2 o -NHRN1, donde RN1 es, independientemente, OH, NO2 , NH2 , NRN22 , SO2RN2, SORN2, alquilo, arilo, acilo (por ejemplo, acetilo, trifluoroacetilo u otros descritos en la presente), o alcoxicarbonilalquilo, y cada RN2 puede ser H, alquilo o arilo.
El grupo "aciloxialquilo", como se usa en la presente, representa un grupo acilo, como se define en la presente, unido a un átomo de oxígeno que a su vez está unido al grupo molecular original a través de un grupo alquileno (es decir, -alquil-O-C(O)-R, donde R es H o un grupo alquilo C1-6 , C1-10 o C1-20 opcionalmente sustituido). Los grupos aciloxialquilo no sustituidos ejemplares incluyen de 1 a 21 carbonos (por ejemplo, de 1 a 7 o de 1 a 11 carbonos). En algunas realizaciones, el grupo alquileno está además independientemente sustituido con 1, 2, 3 o 4 sustituyentes como se describe en la presente.
El grupo "alcoxialquilo", como se usa en la presente, representa un grupo alquilo que está sustituido con un grupo alcoxi. Los grupos alcoxialquilo no sustituidos ejemplares incluyen entre 2 y 40 carbonos (por ejemplo, de 2 a 12 o de 2 a 20 carbonos, como alcoxi C1-6-alquilo C1-6 , alcoxi C1-10-alquilo C1-10 , o alcoxi C1-20-alquilo C1-20. En
algunas realizaciones, el alquilo y el alcoxi pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente para el grupo respectivo.
El grupo "alcoxicarbonilalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, está sustituido con un grupo alcoxicarbonilo, como se define en la presente (por ejemplo, -alquil-C(O)-OR, donde R es un grupo alquilo C1-20, C1-10 o C1-6 opcionalmente sustituido). Los alcoxicarbonilalquilo no sustituido ejemplares incluyen de 3 a 41 carbonos (por ejemplo, de 3 a 10, de 3 a 13, de 3 a 17, de 3 a 21 o de 3 a 31 carbonos, como alcoxicarbonil C1-6-alquilo C1- 6, alcoxicarbonil C1-10-alquilo C1-10 , o alcoxicarbonil C1-20-alquilo C1-20). En algunas realizaciones, cada grupo alquilo y alcoxi está sustituido además independientemente con 1, 2, 3 o 4 sustituyentes como se describe en la presente (por ejemplo, un grupo hidroxi).
El grupo "alquilsulfinilalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con un grupo alquilsulfinilo. Los grupos alquilsulfinilalquilo no sustituidos ejemplares tienen de 2 a 12, de 2 a 20 o de 2 a 40 carbonos. En algunas realizaciones, cada grupo alquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente.
El grupo "aminoalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con un grupo amino, como se define en la presente. El alquilo y el amino pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para el grupo respectivo (por ejemplo, CO2RA', donde RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno, y (d) alque C1-6-arilo C6-10, por ejemplo, carboxi, y/o un grupo protector de N).
El grupo "carbamoilalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con un grupo carbamoílo, como se define en la presente. El grupo alquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente.
El grupo "carboxialquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con un grupo carboxi, como se define en la presente. El grupo alquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente, y el grupo carboxi puede estar opcionalmente sustituido con uno o más grupos protectores de O.
El grupo "carboxiaminoalquilo", que como se usa en la presente, representa un grupo aminoalquilo, como se define en la presente, sustituido con un carboxi, como se define en la presente. El carboxi, alquilo y amino pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para el grupo respectivo (por ejemplo, CO2RA', donde RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno, y (d) alqu C1-6-arilo C 6-10, por ejemplo, carboxi, y/o un grupo protector de N, y/o un grupo protector de O).
El grupo "haloalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con un grupo halógeno (es decir, F, Cl, Br o I). Un haloalquilo puede estar sustituido con uno, dos, tres o, en el caso de grupos alquilo de dos carbonos o más, cuatro halógenos. Los grupos haloalquilo incluyen perfluoroalquilos (por ejemplo, -CF3), -CHF2 , -CH2F, -CCI3 , -CH2CH2Br, -CH2CH(CH2CH2Br)CHa y -CHICH3. En algunas realizaciones, el grupo haloalquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para los grupos alquilo.
El grupo "hidroxialquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con de uno a tres grupos hidroxi, con la condición de que no más de un grupo hidroxi pueda estar unido a un solo átomo de carbono del grupo alquilo, y se ejemplifica por hidroximetilo y dihidroxipropilo. En algunas realizaciones, el grupo hidroxialquilo puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes (por ejemplo, grupos protectores de O) como se define en la presente para un alquilo.
El grupo "perfluoroalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, donde cada radical hidrógeno unido al grupo alquilo ha sido reemplazado por un radical fluoruro. Los grupos perfluoroalquilo están ejemplificados por trifluorometilo, pentafluoroetilo.
El grupo "sulfoalquilo", que como se usa en la presente, representa un grupo alquilo, como se define en la presente, sustituido con un grupo sulfo de -SO3H. En algunas realizaciones, el grupo alquilo puede estar sustituido además con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente, y el grupo sulfo puede estar sustituido adicionalmente con uno o más grupos protectores de O (por ejemplo, como se describe en la presente).
El término "alquenilo", como se usa en la presente, representa grupos monovalentes de cadena lineal o ramificada de, a menos que se especifique lo contrario, de 2 a 20 carbonos (por ejemplo, de 2 a 6 o de 2 a 10 carbonos) que contienen uno o más enlaces dobles carbono-carbono y está ejemplificado por etenilo, 1-propenilo, 2-propenilo, 2-metil-1-propenilo, 1-butenilo y 2-butenilo. Los alquenilos incluyen isómeros tanto cis como trans. Los grupos alquenilo pueden estar opcionalmente sustituidos con 1, 2, 3 o 4 grupos sustituyentes que se seleccionan,
independientemente, de amino, arilo, cicloalquilo o heterociclilo (por ejemplo, heteroarilo), como se define en la presente, o cualquiera de los grupos sustituyentes de alquilo ejemplares descritos en la presente.
Los ejemplos no limitativos de grupos alquenilo opcionalmente sustituidos incluyen alcoxicarbonilalquenilo, aminoalquenilo e hidroxialquenilo:
El grupo "alcoxicarbonilalquenilo", que como se usa en la presente, representa un grupo alquenilo, como se define en la presente, que está sustituido con un grupo alcoxicarbonilo, como se define en la presente (por ejemplo, -alquenil-C(O)-OR, donde R es un grupo alquilo C1-20, C1-10 o C1-6 opcionalmente sustituido). Los alcoxicarbonilalquenilos no sustituidos ejemplares incluyen de 4 a 41 carbonos (por ejemplo, de 4 a 10, de 4 a 13, de 4 a 17, de 4 a 21 o de 4 a 31 carbonos, como alcoxicarbonil C1-6-alquenilo C2- 6, alcoxicarbonil C1-10-alquenilo C2-10 o alcoxicarbonil C1-20-alquenilo C2-20). En algunas realizaciones, cada grupo alquilo, alquenilo y alcoxi está sustituido además independientemente con 1, 2, 3 o 4 sustituyentes como se describe en la presente (por ejemplo, un grupo hidroxi).
El grupo "aminoalquenilo", que como se usa en la presente, representa un grupo alquenilo, como se define en la presente, sustituido con un grupo amino, como se define en la presente. El alquenilo y el amino pueden estar sustituidos cada uno además con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para el grupo respectivo (por ejemplo, CO2RA', donde RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno, y (d) alqu C1-6-arilo C6-10, por ejemplo, carboxi, y/o un grupo protector de N).
El grupo "hidroxialquenilo", que como se usa en la presente, representa un grupo alquenilo, como se define en la presente, sustituido con de uno a tres grupos hidroxi, con la condición de que no más de un grupo hidroxi pueda estar unido a un solo átomo de carbono del grupo alquilo, y está ejemplificado por dihidroxipropenilo e hidroxiisopentenilo. En algunas realizaciones, el grupo hidroxialquenilo puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes (por ejemplo, grupos protectores de O) como se define en la presente para un alquilo.
El término "alquinilo", como se usa en la presente, representa grupos monovalentes de cadena lineal o ramificada de 2 a 20 átomos de carbono (por ejemplo, de 2 a 4, de 2 a 6 o de 2 a 10 carbonos) que contienen un enlace triple carbono-carbono y está ejemplificado por etinilo y 1-propinilo. Los grupos alquinilo pueden estar opcionalmente sustituidos con 1, 2, 3 o 4 grupos sustituyentes que se seleccionan, independientemente, de arilo, cicloalquilo o heterociclilo (por ejemplo, heteroarilo), como se define en la presente, o cualquiera de los grupos sustituyentes de alquilo ejemplares descritos en la presente.
Ejemplos no limitativos de grupos alquinilo opcionalmente sustituidos incluyen alcoxicarbonilalquinilo, aminoalquinilo e hidroxialquinilo:
El grupo "alcoxicarbonilalquinilo", que como se usa en la presente, representa un grupo alquinilo, como se define en la presente, que está sustituido con un grupo alcoxicarbonilo, como se define en la presente (por ejemplo, -alquinil-C(O)-OR, donde R es un grupo alquilo C1-20, C1-10 o C1-6 opcionalmente sustituido). Los alcoxicarbonilalquinilos no sustituidos ejemplares incluyen de 4 a 41 carbonos (por ejemplo, de 4 a 10, de 4 a 13, de 4 a 17, de 4 a 21 o de 4 a 31 carbonos, como alcoxicarbonil C1-6-alquinilo C2- 6, alcoxicarbonil C1-10-alquinilo C2-10 o alcoxicarbonil C1-20-alquinilo C2-20). En algunas realizaciones, cada grupo alquilo, alquinilo y alcoxi se sustituye además independientemente con 1, 2, 3 o 4 sustituyentes como se describe en la presente (por ejemplo, un grupo hidroxi).
El grupo "aminoalquinilo", que como se usa en la presente, representa un grupo alquinilo, como se define en la presente, sustituido con un grupo amino, como se define en la presente. El alquinilo y el amino pueden estar sustituidos adicionalmente cada uno con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para el grupo respectivo (por ejemplo, CO2RA', donde RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno, y (d) alqu C1-6-arilo C6-10, por ejemplo, carboxi, y/o un grupo protector de N).
El grupo "hidroxialquinilo", que como se usa en la presente, representa un grupo alquinilo, como se define en la presente, sustituido con de uno a tres grupos hidroxi, con la condición de que no más de un grupo hidroxi pueda estar unido a un único átomo de carbono del grupo alquilo. En algunas realizaciones, el grupo hidroxialquinilo puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes (por ejemplo, grupos protectores de O) como se define en la presente para un alquilo.
El término "amidino", como se usa en la presente, representa un grupo con la estructura
en donde cada RN1 es, independientemente, H, OH, NO2 , N(RN2)2 , SO2ORN2, SO2RN2, SORN2, un grupo protector de N, alquilo, alquenilo, alquinilo, alcoxi, arilo, alcarilo, cicloalquilo, alqucicloalquilo, carboxialquilo (por ejemplo, opcionalmente sustituido con un grupo protector de O, como grupos arilalcoxicarbonilo opcionalmente sustituidos o cualquiera de los descritos en la presente), sulfoalquilo, acilo (por ejemplo, acetilo, trifluoroacetilo u otros descritos en la presente), alcoxicarbonilalquilo (por ejemplo, opcionalmente sustituido con un grupo protector de O, como grupos arilalcoxicarbonilo opcionalmente sustituidos o cualquiera de los descritos en la presente), heterociclilo (por ejemplo, heteroarilo) o alquheterociclilo (por ejemplo, alquheteroarilo), en donde cada uno de estos grupos RN1 enumerados puede estar opcionalmente sustituido, como se define en la presente para cada grupo o dos RN1 se combinan para formar un heterociclilo o un grupo protector de N, y en donde cada RN2 es, independientemente, H, alquilo o arilo. Los ejemplos no limitativos de grupos amidino opcionalmente sustituidos incluyen guanidino, 2-aminoimidazoilo, 2-iminoimidazolidino, 2-imino-1,3-diazinan-1-ilo, 3-amino-1,2,4-triazol-4-ilo, imidazol-2ilo, 1,4,5,6-tetrahidropirimidin-2-ilo, 1,2,4-triazol-3-ilo, 5-amino-3,4-dihidro-pirrol-5-ilo, imidazol-1-ilo, carbamimidoilsulfanilo, carbamoilamino, carbamotioilamino, 2-amino-1,3-benzotiazol-2-ilo, 2-amino-1,3-tiazol-2-ilo, 2-amino-1,3-benzodiazol-2-ilo y 2-aminopiridilo.
El término "amino", como se usa en la presente, representa -N(RN1)2 , donde cada RN1 es, independientemente, H, OH, NO2 , N(RN2)2 , SO2ORN2, SO2RN2, SORN2, un grupo protector de N, alquilo, alquenilo, alquinilo, alcoxi, arilo, alcarilo, cicloalquilo, alqucicloalquilo, carboxialquilo (por ejemplo, opcionalmente sustituido con un grupo protector de O, como grupos arilalcoxicarbonilo opcionalmente sustituidos o cualquiera de los descritos en la presente), sulfoalquilo, acilo (por ejemplo, acetilo, trifluoroacetilo u otros descritos en la presente), alcoxicarbonilalquilo (por ejemplo, opcionalmente sustituido con un grupo protector de O, como grupos arilalcoxicarbonilo opcionalmente sustituidos o cualquiera de los descritos en la presente), heterociclilo (por ejemplo, heteroarilo) o alquheterociclilo (por ejemplo, alqueteroarilo), en donde cada uno de estos grupos RN1 enumerados puede estar opcionalmente sustituido, como se define en la presente para cada grupo; o dos RN1 se combinan para formar un heterociclilo o un grupo protector de N, y en donde cada RN2 es, independientemente, H, alquilo o arilo. Los grupos amino de la invención pueden ser un amino no sustituido (es decir, -NH2) o un amino sustituido (es decir, -N(RN1)2). En una realización preferida, amino es -NH2 o -NHRN1, donde RN1 es, independientemente, OH, NO2 , NH2 , NRN22 , SO2ORN2, SO2RN2, SORN2, alquilo, carboxialquilo, sulfoalquilo, acilo (por ejemplo, acetilo, trifluoroacetilo u otros descritos en la presente), alcoxicarbonilalquilo (por ejemplo, t-butoxicarbonilalquilo) o arilo, y cada RN2 puede ser H, alquilo C1-20 (por ejemplo, alquilo C1-6) o arilo C6-10.
Los ejemplos no limitativos de grupos amino opcionalmente sustituidos incluyen acilamino y carbamilo: El grupo "acilamino", que como se usa en la presente, representa un grupo acilo, como se define en la presente, unido al grupo molecular original a través de un grupo amino, como se define en la presente (es decir, -N(RN1)-C(O)-R, donde R es H o un grupo alquilo C1-6, C1-10 o C1-20 opcionalmente sustituido (por ejemplo, haloalquilo) y RN1 es como se define en la presente). Los grupos acilamino no sustituidos ejemplares incluyen de 1 a 41 carbonos (por ejemplo, de 1 a 7, de 1 a 13, de 1 a 21, de 2 a 7, de 2 a 13, de 2 a 21 o de 2 a 41 carbonos). En algunas realizaciones, el grupo alquilo está sustituido además con 1, 2, 3 o 4 sustituyentes como se describe en la presente, y/o el grupo amino es -NH2 o -NHRN1, donde RN1 es, independientemente, OH, NO2 , NH2 , NRN22 , SO2ORN2, SO2RN2, SORN2, alquilo, arilo, acilo (por ejemplo, acetilo, trifluoroacetilo u otros descritos en la presente), o alcoxicarbonilalquilo, y cada RN2 puede ser H, alquilo o arilo.
El grupo "carbamilo", que como se usa en la presente, se refiere a un grupo carbamato que tiene la estructura -NRN1C(=O)OR o -OC(=O)N(RN1)2 , donde el significado de cada RN1 se encuentra en la definición de "amino" proporcionada en la presente, y R es alquilo, cicloalquilo, alqucicloalquilo, arilo, alcarilo, heterociclilo (por ejemplo, heteroarilo) o alquheterociclilo (por ejemplo, alquheteroarilo), como se define en la presente.
El término "aminoácido", como se describe en la presente, se refiere a una molécula que tiene una cadena lateral, un grupo amino y un grupo de ácido (por ejemplo, un grupo carboxi de -CO2H o un grupo sulfo de -SO3H), en donde el aminoácido está unido al grupo molecular original por la cadena lateral, el grupo amino o el grupo de ácido (por ejemplo, la cadena lateral). En algunas realizaciones, el aminoácido está unido al grupo molecular original mediante un grupo carbonilo, donde la cadena lateral o el grupo amino está unido al grupo carbonilo. Las cadenas laterales ejemplares incluyen un alquilo, arilo, heterociclilo, alcarilo, alquheterociclilo, aminoalquilo, carbamoilalquilo y carboxialquilo opcionalmente sustituidos. Los aminoácidos ejemplares incluyen alanina, arginina, asparagina, ácido aspártico, cisteína, ácido glutámico, glutamina, glicina, histidina, hidroxinorvalina, isoleucina, leucina, lisina, metionina, norvalina, ornitina, fenilalanina, prolina, pirrolisina, selenocisteína, serina, taurina, treonina, triptófano, tirosina y valina. Los grupos de aminoácidos pueden estar opcionalmente sustituidos con uno, dos, tres o, en el caso de grupos de aminoácidos de dos carbonos o más, cuatro sustituyentes seleccionados independientemente del grupo que consiste de: (1) alcoxi C1-6; (2) alquilsulfinilo C1-6; (3) amino, como se define en la presente (por ejemplo, amino no sustituido (es decir, -NH2) o un amino sustituido (es decir, -N(RN1)2 , donde RN1 es como se define para amino); (4) aril C6-10-alcoxi C1-6; (5) azido; (6) halo; (7) (heterociclil C2-9)oxi; (8) hidroxi; (9) nitro; (10) oxo (por ejemplo, carboxialdehído o acilo); (11) espirociclilo C1-7; (12) tioalcoxi; (13) tiol; (14) -CO2RA', donde RA' se selecciona del grupo que consiste de (a) alquilo C1 -20 (por ejemplo, alquilo C1-6), (b) alquenilo C2-20 (por ejemplo, alquenilo C2-6),
(c) arilo C6-10, (d) hidrógeno, (e) alqu Ci-6-arilo C6-10, (f) amino-alquilo C1-20, (g) polietilenglicol de -(CH2)s2(OCH2CH2)si(CH2)s3OR', donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3 es, independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6, o de 1 a 10), y R' es H o alquilo C1-20, y (h) aminopolietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3 es, independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y cada RN1 es, independientemente, hidrógeno u alquilo C1-6 opcionalmente sustituido; (15) -C(O) NRB'RC', donde cada uno de RB' y RC' se selecciona, independientemente, del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6, (c) arilo C6-10 y (d) alqu C1-6-arilo C6-10; (16) -SO2RD ', donde RD' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) alqu C1-6-arilo C610 y (d) hidroxi; (17) -SO2NRE'RF', donde cada uno de RE' y RF' se selecciona, independientemente, del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6, (c) arilo C6-10 y (d) alqu C1-6-arilo C6-10; (18) -C(O)RG', donde RG' se selecciona del grupo que consiste de (a) alquilo C1-20 (por ejemplo, alquilo C1-6), (b) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c) arilo C6-10, (d) hidrógeno, (e) alqu C1-6-arilo C6-10, (f) amino-alquilo C1-20, (g) polietilenglicol de -(CH2)s2(OCH2CH2)s1(CH2)s3OR', en donde s1 es un número entero de 1 a 10 (por ejemplo, De 1 a 6 o de 1 a 4), cada uno de s2 y s3 es, independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y R' es H o alquilo C1-20, y (h) aminopolietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3, independientemente, es un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; (19) -NRH'C(O)RI', donde RH' se selecciona del grupo que consiste de (a1) hidrógeno y (b1) alquilo C1-6, y R1’ se selecciona del grupo que consiste de (a2) alquilo C1-20 (por ejemplo, alquilo C1-6), (b2) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c2) arilo C6-10, (d2) hidrógeno, (e2) alqu C1-6-arilo C6-10, (f2) amino-alquilo C1-20, (g2) polietilenglicol de -(CH2)s2(OCH2CH2)s1(CH2)s3OR', en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3 es , independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y R' es H o alquilo C1-20, y (h2) amino-polietileno glicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3 es, independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6, o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; (20) -NRJ'C(O)ORK', donde RJ' se selecciona del grupo que consiste de (a1) hidrógeno y (b1) alquilo C1-6, y RK' se selecciona del grupo que consiste de (a2) alquilo C1-20 (por ejemplo, alquilo C1-6), (b2) alquenilo C2-20 (por ejemplo, alquenilo C2-6), (c2) arilo C6-10, (d2) hidrógeno, (e2) alqu C1-6-arilo C6-10, (f2) amino-alquilo C1-20, (g2) polietilenglicol de -(CH2)s2(OCH2CH2)s1(CH2)s3OR', en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3 es, independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6 o de 1 a 10), y R' es H o alquilo C1-20, y (h2) amino-polietilenglicol de -NRN1(CH2)s2(CH2CH2O)s1(CH2)s3NRN1, en donde s1 es un número entero de 1 a 10 (por ejemplo, de 1 a 6 o de 1 a 4), cada uno de s2 y s3 es, independientemente, un número entero de 0 a 10 (por ejemplo, de 0 a 4, de 0 a 6, de 1 a 4, de 1 a 6, o de 1 a 10), y cada RN1 es, independientemente, hidrógeno o alquilo C1-6 opcionalmente sustituido; y (21) amidina. En algunas realizaciones, cada uno de estos grupos puede sustituirse adicionalmente como se describe en la presente.
El término "arilo", como se usa en la presente, representa un sistema de anillo carbocíclico mono-, bicíclico o multicíclico que tiene uno o dos anillos aromáticos y está ejemplificado por fenilo, naftilo, 1,2-dihidronaftilo, 1,2,3,4-tetrahidronaftilo, antracenilo, fenantrenilo, fluorenilo, indanilo e indenilo, y puede estar opcionalmente sustituido con 1, 2, 3, 4 o 5 sustituyentes seleccionados independientemente del grupo que consiste de: (1) acilo C1-7 (por ejemplo, carboxialdehído); (2) alquilo C1-20 (por ejemplo, alquilo C1-6, alcoxi C1-6-alquilo C1-6, alquilsulfinilo C1-6-alquilo C1-6, amino-alquilo C1-6, azido-qlquilo C1-6, (carboxialdehído)-alquilo C1-6, halo-alquilo C1-6 (por ejemplo, perfluoroalquilo), hidroxi-alquilo C1-6, nitro-alquilo C1-6 o tioalcoxi C1-6-alquilo C1-6); (3) alcoxi C1-20 (por ejemplo, alcoxi C1-6, como perfluoroalcoxi); (4) alquilsulfinilo C1-6; (5) arilo C6-10; (6) amino; (7) alqu C1-6-arilo C6-10; (8) azido; (9) cicloalquilo C3-8; (10) alqu C1-6-cicloalquilo C3-8; (11) halo; (12) heterociclilo C1-12 (por ejemplo, heteroarilo C1-12); (13) (heterociclil C1-12)oxi; (14) hidroxi; (15) nitro; (16) tioalcoxi C1-20 (por ejemplo, tioalcoxi C1-6); (17) -(CH2)qCO2RA', donde q es un número entero de cero a cuatro, y RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno y (d) alqu C1-6-arilo C6-10; (18) -(CH2)qCONRBRC', donde q es un número entero de cero a cuatro y donde RB' y RC' se seleccionan independientemente del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6, (c) arilo C6-10, y (d) alqu C1-6-arilo C6-10; (19) -(CH2)qSO2RD', donde q es un número entero de cero a cuatro y donde RD' se selecciona del grupo que consiste de (a) alquilo, (b) arilo C6-10, y (c) alqu-arilo C6-10; (20) -(CH2)qSO2NRERF', donde q es un número entero de cero a cuatro y donde cada uno de RE' y RF' se selecciona independientemente del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6, (c) arilo C6-10, y (d) alqu C1-6-arilo C6-10; (21) tiol; (22) ariloxi C6-10; (23) cicloalcoxi C3-8; (24) aril C6-10-alcoxi C1-6; (25) alqu C1-6-heterociclilo C1-12 (por ejemplo, alqu C1-6-heteroarilo C1-12); (26) alquenilo C2-20; y (27) alquinilo C2-20. En algunas realizaciones, cada uno de estos grupos puede estar sustituido además como se describe en la presente. Por ejemplo, el grupo alquileno de un alcarilo C1 o un alquheterociclilo C1 puede sustituirse adicionalmente con un grupo oxo para producir el respectivo grupo sustituyente ariloílo y (heterociclil)oílo.
El grupo "arilalquilo", que como se usa en la presente, representa un grupo arilo, como se define en la presente, unido al grupo molecular original a través de un grupo alquileno, como se define en la presente. Los grupos arilalquilo no sustituidos ejemplares tienen de 7 a 30 carbonos (por ejemplo, de 7 a 16 o de 7 a 20 carbonos,
como alqu Ci-6-arilo C6-10, alquilo C i-10-arilo C6-10, o alquilo C i-20-arilo C6-10). En algunas realizaciones, el alquileno y el arilo pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente para los grupos respectivos. Otros grupos precedidos por el prefijo "alqu-" se definen de la misma manera, donde "alqu" se refiere a un alquileno C1-6, a menos que se indique lo contrario, y la estructura química unida es como se define en la presente.
El término "azido" representa un grupo -N3 , que también puede representarse como -N=N=N.
El término "bicíclico", como se usa en la presente, se refiere a una estructura que tiene dos anillos, que pueden ser aromáticos o no aromáticos. Las estructuras bicíclicas incluyen grupos espirociclilo, como se define en la presente, y dos anillos que comparten uno o más puentes, donde tales puentes pueden incluir un átomo o una cadena que incluye dos, tres o más átomos. Los grupos bicíclicos ejemplares incluyen un grupo carbociclilo bicíclico, donde el primer y el segundo anillos son grupos carbociclilo, como se define en la presente; grupos arilo bicíclicos, donde el primer y el segundo anillos son grupos arilo, como se define en la presente; grupos heterociclilo bicíclicos, donde el primer anillo es un grupo heterociclilo y el segundo anillo es un grupo carbociclilo (por ejemplo, arilo) o heterociclilo (por ejemplo, heteroarilo); y grupos heteroarilo bicíclicos, donde el primer anillo es un grupo heteroarilo y el segundo anillo es un carbociclilo (por ejemplo, arilo) o heterociclilo (por ejemplo, heteroarilo). En algunas realizaciones, el grupo bicíclico puede estar sustituido con 1, 2, 3 o 4 sustituyentes como se define en la presente para los grupos cicloalquilo, heterociclilo y arilo.
El término "boranilo", como se usa en la presente, representa -B(RB1)3, donde cada RB1 se selecciona, independientemente, del grupo que consiste de H y alquilo opcionalmente sustituido. En algunas realizaciones, el grupo boranilo puede estar sustituido con 1, 2, 3 o 4 sustituyentes como se define en la presente para alquilo.
Los términos "carbocíclico" y "carbociclilo", como se usan en la presente, se refieren a una estructura monocíclica, bicíclica o tricíclica C3-12 opcionalmente sustituida en la que los anillos, que pueden ser aromáticos o no aromáticos, están formados por átomos de carbono. Las estructuras carbocíclicas incluyen grupos cicloalquilo, cicloalquenilo y arilo.
El término "carbonilo", como se usa en la presente, representa un grupo C(O), que también puede representarse como C=O.
El término "carboxi", como se usa en la presente, significa -CO2H.
El término "ciano", como se usa en la presente, representa un grupo -CN.
El término "cicloalquilo", como se usa en la presente, representa un grupo hidrocarburo cíclico no aromático saturado o insaturado monovalente de tres a ocho carbonos, a menos que se especifique lo contrario, y está ejemplificado por ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo y bicicloheptilo. Cuando el grupo cicloalquilo incluye un enlace doble carbono-carbono, puede hacerse referencia al grupo cicloalquilo como grupo "cicloalquenilo". Los grupos cicloalquenilo ejemplares incluyen ciclopentenilo y ciclohexenilo. Los grupos cicloalquilo de esta invención pueden estar opcionalmente sustituidos con: (1) acilo C1-7 (por ejemplo, carboxialdehído); (2) alquilo C1-20 (por ejemplo, alquilo C1-6, alcoxi C1-6-alquilo C1-6, alquilsulfinilo C1-6-alquilo C1-6, amino-alquilo C1-6, azidoalquilo C1-6, (carboxaldehído)-alquilo C1-6, halo-alquilo C1-6 (por ejemplo, perfluoroalquilo), hidroxi-alquilo C1-6, nitroalquilo C1-6 o tioalcoxi C1-6-alquilo C1-6); (3) alcoxi C1-20 (por ejemplo, alcoxi C1-6, como perfluoroalcoxi); (4) alquilsulfinilo C1-6; (5) arilo C6-10; (6) amino; (7) alqu C1-6-arilo C6-10; (8) azido; (9) cicloalquilo C3-8; (10) alqu C1-6-cicloalquilo C3-8; (11) halo; (12) heterociclilo C1-12 (por ejemplo, heteroarilo C1-12); (13) (heterociclil C1-12)oxi; (14) hidroxi; (15) nitro; (16) tioalcoxi C1-20 (por ejemplo, tioalcoxi C1-6); (17) -(CH2)qCO2RA', donde q es un número entero de cero a cuatro, y RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno y (d) alqu C1-6-arilo C6-10; (18) -(CH2)qCONRB'RC', donde q es un número entero de cero a cuatro y donde RB' y RC' se seleccionan independientemente del grupo que consiste de (a) hidrógeno, (b) alquilo C6-10, (c) arilo C6-10, y (d) alqu C1-6-arilo C6-10; (19) -(CH2)qSO2RD', donde q es un número entero de cero a cuatro y donde RD' se selecciona del grupo que consiste de (a) alquilo C6-10, (b) arilo C6 -10 y (c) alqu C1-6-arilo C6-10; (20) -(CH2)qSO2NRE'RF', donde q es un número entero de cero a cuatro y donde cada uno de RE' y RF' se selecciona, independientemente, del grupo que consiste de (a) hidrógeno, (b) alquilo C6-10, (c) arilo C6-10 y (d) alqu C1-6-arilo C6-10; (21) tiol; (22) ariloxi C6-10; (23) cicloalcoxi C3-8; (24) aril C6-10-alcoxi C1-6; (25) alqu C1-6-heterociclilo C1-12 (por ejemplo, alqu C1-6-heteroarilo C1-12); (26) oxo; (27) alquenilo C2-20; y (28) alquinilo C2-20. En algunas realizaciones, cada uno de estos grupos puede sustituirse adicionalmente como se describe en la presente. Por ejemplo, el grupo alquileno de un alcarilo C1 o un alquheterociclilo C1 puede sustituirse adicionalmente con un grupo oxo para proporcionar el grupo sustituyente ariloílo y (heterociclil)oílo respectivo.
El grupo "cicloalquilalquilo", que como se usa en la presente, representa un grupo cicloalquilo, como se define en la presente, unido al grupo molecular original a través de un grupo alquileno, como se define en la presente (por ejemplo, un grupo alquileno de 1 a 4, de 1 a 6, de 1 a 10, o de 1 a 20 carbonos). En algunas realizaciones, el alquileno y el cicloalquilo pueden estar sustituidos cada uno además con 1, 2, 3 o 4 grupos
sustituyentes como se define en la presente para el grupo respectivo.
El término "diastereoisóiriero", como se usa en la presente, significa estereoisómeros que no son imágenes especulares entre sí y no pueden superponerse entre sí.
El término "enantiómero", como se usa en la presente, significa cada forma ópticamente activa individual de un compuesto de la invención, que tiene una pureza óptica o exceso enantiomérico (según se determina mediante métodos estándar en la técnica) de por lo menos el 80% (es decir, por lo menos el 90% de un enantiómero y como máximo el 10% del otro enantiómero), preferiblemente por lo menos el 90% y más preferiblemente por lo menos el 98%.
El término "halo", como se usa en la presente, representa un halógeno seleccionado de bromo, cloro, yodo o flúor.
El término "heteroalquilo", como se usa en la presente, se refiere a un grupo alquilo, como se define en la presente, en el que uno o dos de los átomos de carbono constituyentes se han reemplazado cada uno por nitrógeno, oxígeno o azufre. En algunas realizaciones, el grupo heteroalquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para los grupos alquilo. Los términos "heteroalquenilo" y “heteroalquinilo", como se usan en la presente, se refieren a grupos alquenilo y alquinilo, como se definen en la presente, respectivamente, en los que uno o dos de los átomos de carbono constituyentes se han reemplazado cada uno por nitrógeno, oxígeno o azufre. En algunas realizaciones, los grupos heteroalquenilo y heteroalquinilo pueden estar además sustituidos con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para los grupos alquilo.
Los ejemplos no limitativos de grupos heteroalquilo, heteroalquenilo y heteroalquinilo opcionalmente sustituidos incluyen aciloxi, alqueniloxi, alcoxi, alcoxialcoxi, alcoxicarbonilalcoxi, alquiniloxi, aminoalcoxi, arilalcoxi, carboxialcoxi, cicloalcoxi, halociloxi, tioalcoxi, (heterociclil)oxi, perfluoroalcoxi, tioalcoxi ytioheterociclilalquilo.
El grupo "aciloxi", que como se usa en la presente, representa un grupo acilo, como se define en la presente, unido al grupo molecular original a través de un átomo de oxígeno (es decir, -O-C(O)-R, donde R es H o un grupo alquilo C1-6, C1-10 o C1-20 opcionalmente sustituido). Los grupos aciloxi no sustituidos ejemplares incluyen de 1 a 21 carbonos (por ejemplo, de 1 a 7 o de 1 a 11 carbonos). En algunas realizaciones, el grupo alquilo está sustituido además con 1, 2, 3 o 4 sustituyentes como se describe en la presente.
El grupo "alqueniloxi", que como se usa en la presente, representa un sustituyente químico de fórmula -OR, donde R es un grupo alquenilo C2-20 (por ejemplo, alquenilo C2-6 o C2-10), a menos que se especifique lo contrario. Los grupos alqueniloxi ejemplares incluyen eteniloxi y propeniloxi. En algunas realizaciones, el grupo alquenilo puede sustituirse adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente (por ejemplo, un grupo hidroxi).
El grupo "alcoxi", que como se usa en la presente, representa un sustituyente químico de fórmula -OR, donde R es un grupo alquilo C1-20 (por ejemplo, alquilo C1-6 o C1-10), a menos que se especifique lo contrario. Los grupos alcoxi ejemplares incluyen metoxi, etoxi, propoxi (por ejemplo, n-propoxi e isopropoxi) y t-butoxi. En algunas realizaciones, el grupo alquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente (por ejemplo, hidroxi o alcoxi).
El grupo "alcoxialcoxi", que como se usa en la presente, representa un grupo alcoxi que está sustituido con un grupo alcoxi. Los grupos alcoxialcoxi no sustituidos ejemplares incluyen entre 2 y 40 carbonos (por ejemplo, de 2 a 12 o de 2 a 20 carbonos, como alcoxi C1-6-alcoxi C1-6, alcoxi C1-10-alcoxi C1-10, o alcoxi C1-20-alcoxi C1-20). En algunas realizaciones, cada grupo alcoxi puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente.
El grupo "alcoxicarbonilalcoxi", que como se usa en la presente, representa un grupo alcoxi, como se define en la presente, que está sustituido con un grupo alcoxicarbonilo, como se define en la presente (por ejemplo, -O-alquil-C(O)-OR, donde R es un grupo alquilo C1-6, C1-10 o C1-20 opcionalmente sustituido). Los alcoxicarbonilalcoxi no sustituidos ejemplares incluyen de 3 a 41 átomos de carbono (por ejemplo, de 3 a 10, de 3 a 13, de 3 a 17, de 3 a 21, o de 3 a 31 carbonos, como alcoxicarbonil C1-6-alcoxi C1-6, alcoxicarbonil C1-10-alcoxi C1-10 , o alcoxicarbonil C1-20-alcoxi C1-20). En algunas realizaciones, cada grupo alcoxi está además independientemente sustituido con 1, 2, 3 o 4 sustituyentes, como se describe en la presente (por ejemplo, un grupo hidroxi).
El grupo "alquiniloxi", que como se usa en la presente, representa un sustituyente químico de fórmula -OR, donde R es un grupo alquinilo C2-20 (por ejemplo, alquinilo C2-6 o C2-10), a menos que se especifique lo contrario. Los ejemplos de grupos alquiniloxi incluyen etiniloxi y propiniloxi. En algunas realizaciones, el grupo alquinilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente (por ejemplo, un grupo hidroxi).
El grupo "aminoalcoxi", que como se usa en la presente, representa un grupo alcoxi, como se define en la presente, sustituido con un grupo amino, como se define en la presente. El alquilo y el amino pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para el grupo respectivo (por ejemplo, CO2RA', donde RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno, y (d) alqu C1-6-arilo C6-10, por ejemplo, carboxi).
El grupo "arilalcoxi", que como se usa en la presente, representa un grupo alcarilo, como se define en la presente, unido al grupo molecular original a través de un átomo de oxígeno. Los grupos arilalcoxi no sustituidos ejemplares incluyen de 7 a 30 carbonos (por ejemplo, de 7 a 16 o de 7 a 20 carbonos, como aril C6-10-alcoxi C1-6, aril C6-10-alcoxi C1-10 , o aril C6-10-alcoxi C1-20). En algunas realizaciones, el grupo arilalcoxi puede estar sustituido con 1, 2, 3 o 4 sustituyentes como se define en la presente.
El grupo "ariloxi", que como se usa en la presente, representa un sustituyente químico de fórmula -OR', donde R' es un grupo arilo de 6 a 18 carbonos, a menos que se especifique lo contrario. En algunas realizaciones, el grupo arilo puede estar sustituido con 1, 2, 3 o 4 sustituyentes como se define en la presente.
El grupo "carboxialcoxi", que como se usa en la presente, representa un grupo alcoxi, como se define en la presente, sustituido con un grupo carboxi, como se define en la presente. El grupo alcoxi puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para el grupo alquilo, y el grupo carboxi puede estar opcionalmente sustituido con uno o más grupos protectores de O.
El grupo "cicloalcoxi", que como se usa en la presente, representa un sustituyente químico de fórmula -OR, donde R es un grupo cicloalquilo C3-8, como se define en la presente, a menos que se especifique lo contrario. El grupo cicloalquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente. Los grupos cicloalcoxi no sustituidos ejemplares tienen de 3 a 8 carbonos. En alguna realización, el grupo cicloalquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente.
El grupo "haloalcoxi", que como se usa en la presente, representa un grupo alcoxi, como se define en la presente, sustituido con un grupo halógeno (es decir, F, Cl, Br o I). Un haloalcoxi puede estar sustituido con uno, dos, tres o, en el caso de grupos alquilo de dos carbonos o más, cuatro halógenos. Los grupos haloalcoxi incluyen perfluoroalcoxis (por ejemplo, -OCF3), -OCHF2 , -OCH2F, -OCCla, -OCH2CH2Br, -OCH2CH(CH2CH2Br)CHa y -OCHICH3. En algunas realizaciones, el grupo haloalcoxi puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente para los grupos alquilo.
El grupo "(heterociclil)oxi", que como se usa en la presente, representa un grupo heterociclilo, como se define en la presente, unido al grupo molecular original a través de un átomo de oxígeno. En algunas realizaciones, el grupo heterociclilo puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente.
El grupo "perfluoroalcoxi", que como se usa en la presente, representa un grupo alcoxi, como se define en la presente, donde cada radical de hidrógeno unido al grupo alcoxi ha sido reemplazado por un radical de fluoruro. Los grupos perfluoroalcoxi se ejemplifican por trifluorometoxi y pentafluoroetoxi.
El grupo "alquilsulfinilo", que como se usa en la presente, representa un grupo alquilo unido al grupo molecular original a través de un grupo -S(O)-. Los grupos alquilsulfinilo no sustituidos ejemplares tienen de 1 a 6, de 1 a 10 o de 1 a 20 carbonos. En algunas realizaciones, el grupo alquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente.
El grupo "tioarilalquilo", que como se usa en la presente, representa un sustituyente químico de fórmula -SR, donde R es un grupo arilalquilo. En algunas realizaciones, el grupo arilalquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente.
El grupo "tioalcoxi", como se usa en la presente, representa un sustituyente químico de fórmula -SR, donde R es un grupo alquilo, como se define en la presente. En algunas realizaciones, el grupo alquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente.
El grupo "tioheterociclilalquilo", que como se usa en la presente, representa un sustituyente químico de fórmula -SR, donde R es un grupo heterociclilalquilo. En algunas realizaciones, el grupo heterociclilalquilo puede estar sustituido adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se describe en la presente.
El término "heteroarilo", como se usa en la presente, representa ese subconjunto de heterociclilos, como se define en la presente, que son aromáticos: es decir, contienen electrones 4n+2 pi dentro del sistema de anillo mono o multicíclico. Los grupos heteroarilo no sustituidos ejemplares tienen de 1 a 12 (por ejemplo, de 1 a 11, de 1 a 10, de 1 a 9, de 2 a 12, de 2 a 11, de 2 a 10 o de 2 a 9) carbonos. En alguna realización, el heteroarilo está sustituido
con 1, 2, 3 o 4 grupos sustituyentes como se define para un grupo heterociclilo.
El término "heteroarilaiquilo" se refiere a un grupo heteroarilo, como se define en la presente, unido al grupo molecular original a través de un grupo alquileno, como se define en la presente. Los grupos heteroarilalquilo no sustituidos ejemplares tienen de 2 a 32 carbonos (por ejemplo, de 2 a 22, de 2 a 18, de 2 a 17, de 2 a 16, de 3 a 15, de 2 a 14, de 2 a 13 o de 2 a 12 carbonos, como alqu C1-6-heteroarilo C1-12 , alqu C1-10-heteroarilo C1-12 o alqu C1-20-heteroarilo C1-12 ). En algunas realizaciones, el alquileno y el heteroarilo pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente para el grupo respectivo. Los grupos heteroarilalquilo son un subconjunto de grupos heterociclilalquilo.
El término "heterociclilo", como se usa en la presente, representa un anillo de 5, 6 o 7 miembros, a menos que se especifique lo contrario, que contiene uno, dos, tres o cuatro heteroátomos seleccionados independientemente del grupo que consiste de nitrógeno, oxígeno y azufre. El anillo de 5 miembros tiene de cero a dos enlaces dobles, y los anillos de 6 y 7 miembros tienen de cero a tres enlaces dobles. Los grupos heterociclilo no sustituidos ejemplares tienen de 1 a 12 (por ejemplo, de 1 a 11, de 1 a 10, de 1 a 9, de 2 a 12, de 2 a 11, de 2 a 10 o de 2 a 9) carbonos. El término "heterociclilo" también representa un compuesto heterocíclico que tiene una estructura multicíclica puenteada en la que uno o más carbonos y/o heteroátomos forman puentes entre dos miembros no adyacentes de un anillo monocíclico, por ejemplo, un grupo quinuclidinilo. El término "heterociclilo" incluye grupos bicíclicos, tricíclicos, y tetracíclicos en los que cualquiera de los anillos heterocíclicos anteriores está fusionado con uno, dos o tres anillos carbocíclicos, por ejemplo, un anillo arilo, un anillo ciclohexano, un anillo ciclohexeno, un anillo ciclopentano, un anillo ciclopenteno u otro anillo heterocíclico monocíclico, como indolilo, quinolilo, isoquinolilo, tetrahidroquinolilo, benzofurilo y benzotienilo. Los ejemplos de heterociclilos fusionados incluyen tropanos y 1,2,3,5,8,8a-hexahidroindolizina. Los heterocíclicos incluyen pirrolilo, pirrolinilo, pirrolidinilo, pirazolilo, pirazolinilo, pirazolidinilo, imidazolilo, imidazolinilo, imidazolidinilo, piridilo, piperidinilo, homopiperidinilo, pirazinilo, piperazinilo, pirimidinilo, piridazinilo, oxazolilo, oxazolidinilo, isoxazolilo, isoxazolidiniyl, morfolinilo, tiomorfolinilo, tiazolilo, tiazolidinilo, isotiazolilo, isotiazolidinilo, indolilo, indazolilo, quinolilo, isoquinolilo, quinoxalinilo, dihidroquinoxalinilo, quinazolinilo, cinolinilo, ftalazinilo, bencimidazolilo, benzotiazolilo, benzoxazolilo, benzotiadiazolilo, furilo, tienilo, tiazolidinilo, isotiazolilo, triazolilo, tetrazolilo, oxadiazolilo (por ejemplo, 1,2,3-oxadiazolilo), purinilo, tiadiazolilo, (por ejemplo, 1,2,3-tiadiazolilo), tetrahidrofuranilo, dihidrofuranilo, tetrahidrotienilo, dihidrotienilo, dihidroindolilo, dihidroquinolilo, tetrahidroquinolilo, tetrahidroisoquinolilo, dihidroisoquinolilo, piranilo, dihidropiranilo, ditiazolilo, benzofuranilo, isobenzofuranilo, y benzotienilo, incluyendo las formas dihidro y tetrahidro de los mismos, en donde uno o más enlaces dobles se reducen y se reemplazan con hidrógenos. Otros heterociclilos ejemplares más incluyen: 2,3,4,5-tetrahidro-2-oxo-oxazolilo; 2,3-dihidro-2-oxo-1H-imidazolilo; 2,3,4,5-tetrahidro-5-oxo-1H-pirazolilo (por ejemplo, 2,3,4,5-tetrahidro-2-fenil-5-oxo-1H-pirazolilo); 2,3,4,5-tetrahidro-2,4-dioxo-1H-imidazolilo (por ejemplo, 2,3,4,5-tetrahidro-2,4-dioxo-5-metil-5-fenil-1H-imidazolilo); 2,3-dihidro-2-tioxo-1.3.4- oxadiazolilo (por ejemplo, 2,3-dihidro-2-tioxo-5-fenil-1,3,4-oxadiazolilo); 4,5-dihidro-5-oxo-1H-triazolilo (por ejemplo, 4,5-dihidro-3-metil-4-amino 5-oxo-1H-triazolilo); 1,2,3,4-tetrahidro-2,4-dioxopiridinilo (por ejemplo, 1,2,3,4-tetrahidro-2,4-dioxo-3,3-dietilpiridinilo); 2,6-dioxo-piperidinilo (por ejemplo, 2,6-dioxo-3-etil-3-fenilpiperidinilo); 1,6-dihidro-6-oxopiridiminilo; 1,6-dihidro-4-oxopirimidinilo (por ejemplo, 2-(metiltio)-1,6-dihidro-4-oxo-5-metilpirimidin-1-ilo); 1,2,3,4-tetrahidro-2,4-dioxopirimidinilo (por ejemplo, 1,2,3,4-tetrahidro-2,4-dioxo-3-etilpirimidinilo); 1,6-dihidro-6-oxo-piridazinilo (por ejemplo, 1,6-dihidro-6-oxo-3-etilpiridazinilo); 1,6-dihidro-6-oxo-1,2,4-triazinilo (por ejemplo, 1,6-dihidro-5-isopropil-6-oxo-1,2,4-triazinilo); 2,3-dihidro-2-oxo-1H-indolilo (por ejemplo, 3,3-dimetil-2,3-dihidro-2-oxo-1H-indolilo y 2,3-dihidro-2-oxo-3,3'-espiropropano-1H-indol-1-ilo); 1,3-dihidro-1-oxo-2H-iso-indolilo; 1,3-dihidro-1,3-dioxo-2H-iso-indolilo; 1H-benzopirazolilo (por ejemplo, 1-(etoxicarbonil)-1H-benzopirazolilo); 2,3-dihidro-2-oxo-1H-bencimidazolilo (por ejemplo, 3-etil-2,3-dihidro-2-oxo-1H-bencimidazolilo); 2,3-dihidro-2-oxo-benzoxazolilo (por ejemplo, 5-cloro-2,3-dihidro-2-oxo-benzoxazolilo); 2,3-dihidro-2-oxo-benzoxazolilo; 2-oxo-2H-benzopiranilo; 1,4-benzodioxanilo; 1,3-benzodioxanilo; 2,3-dihidro-3-oxo,4H-1,3-benzotiazinilo; 3,4-dihidro-4-oxo-3H-quinazolinilo (por ejemplo, 2-metil-3,4-dihidro-4-oxo-3H-quinazolinilo); 1,2,3,4-tetrahidro-2,4-dioxo-3H-quinazolilo (por ejemplo, 1-etil-1.2.3.4- tetrahidro-2,4-dioxo-3H-quinazolilo); 1,2,3,6-tetrahidro-2,6-dioxo-7H-purinilo (por ejemplo, 1,2,3,6-tetrahidro-1,3-dimetil-2,6-dioxo-7H-purinilo); 1,2,3,6-tetrahidro-2,6-dioxo-1H-purinilo (por ejemplo, 1,2,3,6-tetrahidro-3,7-dimetil-2,6-dioxo-1H-purinilo); 2-oxobenz[c,d]indolilo; 1,1-dioxo-2H-naft[1,8-c,d]isotiazolilo; y 1,8-naftilendicarboxamido. Los heterocíclicos adicionales incluyen 3,3a,4,5,6,6a-hexahidro-pirrolo[3,4-b]pirrol-(2H)-ilo y 2,5-diazabiciclo[2.2.1]heptan-2-ilo, homopiperazinilo (o diazepanilo), tetrahidropiranilo, ditiazolilo, benzofuranilo, benzotienilo, oxepanilo, tiepanilo, azocanilo, oxecanilo y tiocanilo. Los grupos heterocíclicos también incluyen grupos de fórmula
dónde
E' se selecciona del grupo que consiste de -N- y -CH-; F' se selecciona del grupo que consiste de -N=CH-, -NH-CH2-, -NH-C(O)-, -NH-, -CH=N-, -CH2-NH-, -C(O)-NH-, -CH=CH-, -CH2-, -CH2CH2-, -CH2O-, -OCH2-, -O- y -S-; y G' se selecciona del grupo que consiste de -CH- y -N-. Cualquiera de los grupos heterociclilo mencionados en la presente
puede estar opcionalmente sustituido con uno, dos, tres, cuatro o cinco sustituyentes seleccionados independientemente del grupo que consiste de: (1) acilo C1-7 (por ejemplo, carboxialdehído); (2) alquilo C1-20 (por ejemplo, alquilo C1-6, alcoxi C1-6-alquilo C1-6, alquilsulfinilo C1-6-alquilo C1-6, amino-alquilo C1-6, azido-alquilo C1-6, (carboxaldehído)-alquilo C1-6, halo-alquilo C1-6 (por ejemplo, perfluoroalquilo), hidroxi-alquilo C1-6, nitro-alquilo C1-6 o tioalcoxi C1-6-alquilo C1-6); (3) alcoxi C1-20 (por ejemplo, alcoxi C1-6, como perfluoroalcoxi); (4) alquilsulfinilo C1-6; (5) arilo C6-10; (6) amino; (7) alquilo C1-6-arilo C6-10; (8) azido; (9) cicloalquilo C3-8; (10) alquilo C1-6-cicloalquilo C3-8; (11) halo; (12) heterociclilo C1-12 (por ejemplo, heteroarilo C2-12); (13) (heterociclil C1-12)oxi; (14) hidroxi; (15) nitro; (16) tioalcoxi C1-20 (por ejemplo, tioalcoxi C1-6); (17) -(CH2)qCO2RA', donde q es un número entero de cero a cuatro, y RA' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10, (c) hidrógeno y (d) alqu C1-6-arilo C6-10; (18) -(CH2)qCONRBRC', donde q es un número entero de cero a cuatro y donde RB' y RC' se seleccionan independientemente del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6, (c) arilo C6-10 y (d) alqu C1-6-arilo C6-10; (19) -(CH2)qSO2RD', donde q es un número entero de cero a cuatro y donde RD' se selecciona del grupo que consiste de (a) alquilo C1-6, (b) arilo C6-10 y (c) alqu C1-6-arilo C6-10; (20) -(CH2)qSO2NRE'RF', donde q es un número entero de cero a cuatro y donde cada uno de RE' y RF' se selecciona, independientemente, del grupo que consiste de (a) hidrógeno, (b) alquilo C1-6, (c) arilo C6-10, y (d) alqu C1-6-arilo C6-10; (21) tiol; (22) ariloxi C6-10; (23) cicloalcoxi C3-8; (24) arilalcoxi; (25) alqu C1-6-heterociclilo C1-12 (por ejemplo, alqu C1-6-heteroarilo C1-12); (26) oxo; (27) (heterociclil C1-12)imino; (28) alquenilo C2-20; y (29) alquinilo C2-20. En algunas realizaciones, cada uno de estos grupos puede estar sustituido adicionalmente como se describe en la presente. Por ejemplo, el grupo alquileno de un alcarilo C1 o un alquheterociclilo C1 puede sustituirse adicionalmente con un grupo oxo para producir el grupo sustituyente ariloílo y (heterociclil)oílo respectivo.
El grupo "heterociclilalquilo", que como se usa en la presente, representa un grupo heterociclilo, como se define en la presente, unido al grupo molecular original a través de un grupo alquileno, como se define en la presente. Los grupos heterociclilalquilo no sustituidos ejemplares tienen de 2 a 32 carbonos (por ejemplo, de 2 a 22, de 2 a 18, de 2 a 17, de 2 a 16, de 3 a 15, de 2 a 14, de 2 a 13 o de 2 a 12 átomos de carbono, como alqu C1-6-heterociclilo C1-12 , alqu C1-10-heterociclilo C1-12 o alqu C1-2o-heterociclilo C1-12). En algunas realizaciones, el alquileno y el heterociclilo pueden estar sustituidos cada uno adicionalmente con 1, 2, 3 o 4 grupos sustituyentes como se define en la presente para el grupo respectivo.
El término "hidrocarburo", como se usa en la presente, representa un grupo que consiste únicamente de átomos de carbono e hidrógeno.
El término "hidroxi", como se usa en la presente, representa un grupo -OH. En algunas realizaciones, el grupo hidroxi puede estar sustituido con 1, 2, 3 o 4 grupos sustituyentes (por ejemplo, grupos protectores de O) como se define en la presente para un alquilo.
El término "isómero", como se usa en la presente, significa cualquier tautómero, estereoisómero, enantiómero o diastereómero de cualquier compuesto de la invención. Se reconoce que los compuestos de la invención pueden tener uno o más centros quirales y/o enlaces dobles y, por lo tanto, existen como estereoisómeros, como isómeros de doble enlace (es decir, isómeros geométricos E/Z) o diastereómeros (por ejemplo, Enantiómeros (es decir, (+) o (-)) o isómeros cis/trans). De acuerdo con la invención, las estructuras químicas representadas en la presente, y por lo tanto los compuestos de la invención, abarcan todos los estereoisómeros correspondientes, es decir, tanto la forma estereoméricamente pura (por ejemplo, geométricamente pura, enantioméricamente pura o diastereoisomérica pura) como mezclas enantioméricas y estereoisoméricas, por ejemplo, racematos. Las mezclas enantioméricas y estereoisoméricas de los compuestos de la invención pueden resolverse típicamente en sus componentes enantiómeros o estereoisómeros mediante métodos bien conocidos, como cromatografía de gases en fase quiral, cromatografía líquida de alto rendimiento en fase quiral, cristalización del compuesto como un complejo de sal quiral, o cristalización del compuesto en un solvente quiral. Los enantiómeros y estereoisómeros también pueden obtenerse a partir de productos intermedios, reactivos y catalizadores estereomérica o enantioméricamente puros mediante métodos sintéticos asimétricos bien conocidos.
El término "amino N-protegido", como se usa en la presente, se refiere a un grupo amino, como se define en la presente, al que se une uno o dos grupos protectores de N, como se define en la presente.
El término "grupo protector de N", como se usa en la presente, representa aquellos grupos destinados a proteger un grupo amino contra reacciones indeseables durante los procedimientos sintéticos. Los grupos protectores de N usados comúnmente se describen en Greene, “Protective Groups in OrganiCSynthesis”, 3a Edition (John Wiley & Sons, Nueva York, 1999). Los grupos N-protectores incluyen grupos acilo, ariloílo o carbamilo como formilo, acetilo, propionilo, pivaloílo, t-butilacetilo, 2-cloroacetilo, 2-bromoacetilo, trifluoroacetilo, tricloroacetilo, ftalilo, o-nitrofenoxiacetilo, a-clorobutilo 4-clorobenzoílo, 4-bromobenzoílo, 4-nitrobenzoílo y auxiliares quirales como aminoácidos D, L o D, L protegidos o no protegidos como alanina, leucina y fenilalanina; grupos que contienen sulfonilo como bencenosulfonilo y p-toluenosulfonilo; grupos formadores de carbamato como benciloxicarbonilo, pclorobenciloxicarbonilo, p-metoxibenciloxicarbonilo, p-nitrobenciloxicarbonilo, 2-nitrobenciloxicarbonilo, pbromobenciloxicarbonilo, 3,4-dimetoxibenciloxicarbonilo, 3,5-dimetoxibenciloxicarbonilo, 2,4-dimetoxibenciloxicarbonilo, 4-metoxibenciloxicarbonilo, 2-nitro-4,5-dimetoxibenciloxicarbonilo, 3,4,5trimetoxibenciloxicarbonilo, 1-(p-bifenilil)-1-metiletoxicarbonilo, a,a-dimetil-3,5-dimetoxibencilcarbonilo, benzhidriloxi carbonilo, t-butiloxicarbonilo, diisopropilmetoxicarbonilo, isopropiloxicarbonilo, etoxicarbonilo, metoxicarbonilo, aliloxicarbonilo, 2,2,2,-tricloroetoxicarbonilo, fenoxicarbonilo, 4-nitrofenoxi carbonilo, fluorenil-9-metoxicarbonilo, ciclopentiloxicarbonilo, adamantiloxicarbonilo, ciclohexiloxicarbonilo, y feniltiocarbonilo, grupos alcarilo como bencilo, trifenilmetilo y benciloximetilo, y grupos sililo como trimetilsililo. Los grupos protectores de N preferidos son formilo, acetilo, benzoílo, pivaloílo, t-butilacetilo, alanilo, fenilsulfonilo, bencilo, t-butiloxicarbonilo (Boc) y benciloxicarbonilo (Cbz).
El término “nitro”, como se usa en la presente, representa un grupo -NO2.
El término "grupo protector de O", como se usa en la presente, representa aquellos grupos destinados a proteger un grupo que contiene oxígeno (por ejemplo, fenol, hidroxilo o carbonilo) contra reacciones indeseables durante los procedimientos sintéticos. Los grupos protectores de O comúnmente usados se divulgan en Greene, “Protective Groups in OrganiCSynthesis”, 3a Edition (John Wiley & Sons, Nueva York, 1999). Los grupos protectores de O ejemplares incluyen grupos acilo, ariloilo o carbamilo como formilo, acetilo, propionilo, pivaloilo, t-butilacetilo, 2-cloroacetilo, 2-bromoacetilo, trifluoroacetilo, tricloroacetilo, ftalilo, o-nitrofenoxiacetilo, a-clorobutirilo, benzoílo, 4-clorobenzoílo, 4-bromobenzoílo, t-butildimetilsililo, tri-iso-propilsililoximetilo, 4,4'-dimetoxitritilo, isobutirilo, fenoxiacetilo, 4-isopropilpeenoxiacetilo, dimetilformamidino y 4-nitrobenzoilo; grupos alquilcarbonilo, como acilo, acetilo, propionilo y pivaloilo; grupos arilcarbonilo opcionalmente sustituidos, como benzoílo; grupos sililo, como trimetilsililo (TMS), terc-butildimetilsililo (TBDMS), tri-iso-propilsililoximetilo (TOM) y triisopropilsililo (TIPS); grupos formadores de éter con el hidroxilo, como metilo, metoximetilo, tetrahidropiranilo, bencilo, p-metoxibencilo y tritilo; alcoxicarbonilos, como metoxicarbonilo, etoxicarbonilo, isopropoxicarbonilo, n-isopropoxicarbonilo, nbutiloxicarbonilo, isobutiloxicarbonilo, sec-butiloxicarbonilo, t-butiloxicarbonilo, 2-etilhexiloxicarbonilo, ciclohexilcarbonilo y metiloxicarbonilo; grupos alcoxialcoxicarbonilo, como metoximetoxicarbonilo, etoximetoxicarbonilo, 2-metoxietoxicarbonilo, 2-etoxietoxicarbonilo, 2-butoxietoxicarbonilo, 2-metoxietoxicarbonilo, aliloxicarbonilo, propargiloxicarbonilo, 2-butenoetoxicarbonilo y 3-metil-2-butenoxicarbonilo; haloalcoxicarbonilos, como 2-cloroetoxicarbonilo, 2-cloroetoxicarbonilo y 2,2,2-tricloroetoxicarbonilo; grupos arilalcoxicarbonilo opcionalmente sustituidos, como benciloxicarbonilo, p-metilbenciloxicarbonilo, p-metoxibenciloxicarbonilo, pnitrobenciloxicarbonilo, 2,4-dinitrobenciloxicarbonilo, 3,5-dimetilbenciloxicarbonilo, p-clorobenciloxicarbonilo, pbromobenciloxi-carbonilo y fluorenilmetiloxicarbonilo; y grupos ariloxicarbonilo opcionalmente sustituidos, como fenoxicarbonilo, p-nitrofenoxicarbonilo, o-nitrofenoxicarbonilo, 2,4-dinitrofenoxicarbonilo, p-metil-fenoxicarbonilo, mmetilfenoxicarbonilo, o-bromofenoxicarbonilo, 3,5-dimetilfenoxicarbonilo, p-clorofenoxicarbonilo, y 2-cloro-4-nitrofenoxi-carbonilo); éteres de alquilo, arilo y alcarilo sustituidos (por ejemplo, tritilo; metiltiometilo; metoximetilo; benciloximetilo; siloximetilo; 2,2,2,-tricloroetoximetilo; tetrahidropiranilo; tetrahidrofuranilo; etoxietilo; 1-[2-(trimetilsili)etoxi]etilo; 2-trimetilsililetilo, t-butil éter; p-clorofenilo, p-metoxifenilo, p-nitrofenilo, bencilo, p-metoxibencilo y nitrobencilo); éteres de sililo (por ejemplo, trimetilsililo; trietilsililo; triisopropilsililo; dimetilisopropilsililo; tbutildimetilsililo; t-butildifenilsililo; tribencilsililo; trifenilsililo; y difenimetilsililo); carbonatos (por ejemplo, metilo, metoximetilo, 9-fluorenilmetilo; etilo; 2,2,2-tricloroetilo; 2-(trimetilsilil)etilo; vinilo, alilo, nitrofenilo; bencilo; metoxibencilo; 3,4-dimetoxibencilo; y nitrobencilo); grupos protectores de carbonilo (por ejemplo, grupos acetal y cetal, como dimetilacetal y 1,3-dioxolano; grupos acilal; y grupos ditiano, como 1,3-ditianos y 1,3-ditiolano); grupos protectores de ácido carboxílico (por ejemplo, grupos éster, como éster metílico, éster bencílico, éster t-butílico y ortoésteres; y grupos oxazolina.
Los grupos protectores de O y N ejemplares incluyen: Acetilo (Ac); Acilalos; Benzoílo (Bz); Bencilo (Bn, Bnl); ésteres de Bencilo; Carbamato; Carbobenciloxi (Cbz); Dimetoxitritilo, [bis-(4-metoxifenil)fenilmetil] (DMT); Ditianes; éteres de etoxietilo (EE); Metoximetiléter (MOM); Metoxitritil [(4-metoxifenil)difenilmetil], (MMT); Éteres de metilo; Metilo (Me); ésteres de metilo; éter de metiltiometilo; Ortoésteres; Oxazolina; Pivaloilo (Piv); Ftalimido; pmetoxibencil carbonilo (Moz o MeOZ); p-metoxibencilo (PMB); Alcoholes propargílicos; Grupos sililo (por ejemplo, trimetilsililo (TMS), terc-butildimetilsililo (TBDMS), tri-iso-propilsililoximetilo (TOM) y triisopropilsililo (TIPS)); Ésteres de sililo; ésteres de terc-butilo; terc-butiloxicarbonilo (BoC o tBoc); Tetrahidropiranilo (THP); Tosilo (Ts o Tos); Trimetilsililetoximetilo (SEM); Tritilo (trifenilmetilo, Tr); éter p-metoxietoximetílico (MEM); (4-nitrofenil)sulfonilo o (4-nitrofenil)(dióxido)-lambda(6)-sulfanil) (Nosyl); 2-cianoetilo; 2-nitrofenilsulfenilo (Nps); 3,4-dimetoxibencilo (DMPM); y 9-fluorenilmetiloxicarbonilo (FMOC)
El término "oxo", como se usa en la presente, representa =O.
El prefijo "perfluoro", como se usa en la presente, representa cualquier grupo, como se define en la presente, donde cada radical de hidrógeno unido al grupo alquilo ha sido reemplazado por un radical de fluoruro. Por ejemplo, los grupos perfluoroalquilo están ejemplificados por trifluorometilo y pentafluoroetilo.
El término "hidroxilo protegido", como se usa en la presente, se refiere a un átomo de oxígeno unido a un grupo protector de O.
El término "espirociclilo", como se usa en la presente, representa un dirradical de alquileno C2-7, cuyos extremos están unidos al mismo átomo de carbono del grupo original para formar un grupo espirocíclico, y también
un dirradical heteroalquileno Ci-6, cuyos extremos están unidos al mismo átomo. El radical heteroalquileno que forma el grupo espirociclilo puede contener uno, dos, tres o cuatro heteroátomos seleccionados independientemente del grupo que consiste de nitrógeno, oxígeno y azufre. En algunas realizaciones, el grupo espirociclilo incluye de uno a siete carbonos, excluyendo el átomo de carbono al que está unido el dirradical. Los grupos espirociclilo de la invención pueden estar opcionalmente sustituidos con 1, 2, 3 o 4 sustituyentes proporcionados en la presente como sustituyentes opcionales para los grupos cicloalquilo y/o heterociclilo.
El término "estereoisómero", como se usa en la presente, se refiere a todas las posibles formas isoméricas así como conformacionales diferentes que puede poseer un compuesto (por ejemplo, un compuesto de cualquier fórmula descrita en la presente), en particular todas las formas estereoquímica y conformacionalmente isoméricas posibles, todos los diastereómeros, enantiómeros y/o confórmeros de estructura molecular básica. Algunos compuestos de la presente invención pueden existir en diferentes formas tautoméricas, todas las últimas incluidas dentro del alcance de la presente invención.
El término "sulfonilo", como se usa en la presente, representa un grupo -S(O)2-. El término "tiol", como se usa en la presente, representa un grupo -SH.
Definiciones
El término "cáncer" se refiere a cualquier cáncer provocado por la proliferación de células neoplásicas malignas, como tumores, neoplasias, carcinomas, sarcomas, leuquimias y linfomas.
La "migración celular", como se usa en esta solicitud, implica la invasión por las células cancerosas del tejido circundante y el cruce de la pared del vaso para salir de la vasculatura en los órganos distales de la célula cancerosa.
Por "cánceres de migración celular" se entienden los cánceres que migran por invasión de las células cancerosas al tejido circundante y el cruce de la pared del vaso para salir de la vasculatura en los órganos distales de la célula cancerosa.
Como se usa en la presente, "cáncer resistente a fármacos" se refiere a cualquier cáncer que sea resistente a un antiproliferativo en la Tabla 11.
Como se usa en la presente, "nódulo metastásico" se refiere a una añadeción de células tumorales en el cuerpo en un sitio diferente al sitio del tumor original.
Como se usa en la presente, "tumor metastásico" se refiere a un tumor o cáncer en el que las células cancerosas que forman el tumor tienen un alto potencial o han comenzado a hacer metástasis o diseminarse de una localización a otra localización o localizaciones dentro de un sujeto, a través de la sistema linfático o vía diseminación hematógena, por ejemplo, creando tumores secundarios dentro del sujeto. Tal comportamiento metastásico puede ser indicativo de tumores malignos. En algunos casos, el comportamiento metastásico puede estar asociado con un aumento en la migración celular y/o comportamiento de invasión de las células tumorales.
Los ejemplos de cánceres que pueden definirse como metastásicos incluyen, pero no se limitan a, cáncer de pulmón de células no pequeñas, cáncer de mama, cáncer de ovario, cáncer colorrectal, cáncer de vías biliares, cáncer de vejiga, cáncer de cerebro, incluyendo glioblastomas y medulolablastomas, cáncer de cuello uterino, coriocarcinoma, cáncer de endometrio, cáncer de esófago, cáncer gástrico, neoplasias hematológicas, mieloma múltiple, leucemia, neoplasias intraepiteliales, cáncer de hígado, linfomas, neuroblastomas, cáncer oral, cáncer de páncreas, cáncer de próstata, sarcoma, cáncer de piel incluyendo melanoma, cáncer basocelular, cáncer de células escamosas, cáncer testicular, tumores estromales, tumores de células germinales, cáncer de tiroides y cáncer renal.
Como se usa en la presente, "cáncer migratorio" se refiere a un cáncer en el que las células cancerosas que forman el tumor migran y posteriormente crecen como implantes malignos en un sitio distinto que el sitio del tumor original. Las células cancerosas migran sembrando la superficie de los espacios peritoneal, pleural, pericárdico o subaracnoideo para diseminarse hacia las cavidades corporales; mediante invasión del sistema linfático a través de la invasión de células linfáticas y el transporte a los ganglios linfáticos regionales y distantes y luego a otras partes del cuerpo; mediante diseminación hematógena por invasión de células sanguíneas; o mediante invasión del tejido circundante. Los cánceres migratorios incluyen tumores metastásicos y cánceres de migración celular, como cáncer de ovario, mesotelioma y cáncer de pulmón primario, cada uno de los cuales se caracteriza por migración celular.
"Cáncer de migración celular no metastásico", como se usa en la presente, se refiere a cánceres que no migran mediante el sistema linfático o mediante diseminación hematógena.
La "proliferación", como se usa en esta solicitud, implica la reproducción o multiplicación de formas
similares (células) debido a los elementos constitutivos (celulares).
Como se usa en la presente, "ralentizar la propagación de la metástasis" se refiere a reducir o detener la formación de nuevos loci; o reducir, detener o revertir la carga tumoral.
Como se usa en la presente, "ralentizar la propagación del cáncer migratorio" se refiere a reducir o detener la formación de nuevos loci; o reducir, detener o revertir la carga tumoral.
Como se usa en la presente, "sustancialmente enantioméricamente puro", se refiere a una composición (por ejemplo, una composición farmacéutica) en la que más del 85% (por ejemplo, más del 90%, más del 95%, hasta e incluyendo el 100%, es decir, dentro de los límites de detección) de las moléculas del inhibidor del transporte de creatina o del inhibidor de la creatina quinasa en la composición tienen el mismo sentido de quiralidad.
Como se usa en la presente, y como es bien entendido en la técnica, "tratar" una afección o "tratamiento" de la afección (por ejemplo, las afecciones descritas en la presente, como el cáncer) es un enfoque para obtener resultados beneficiosos o deseados, como resultados clínicos. Los resultados beneficiosos o deseados pueden incluir, pero no se limitan a, alivio o mejora de uno o más síntomas o afecciones; disminución de la extensión de la enfermedad, trastorno o afección; estado estabilizado (es decir, sin empeoramiento) de la enfermedad, trastorno o afección; prevenir la propagación de enfermedades, trastornos o afecciones; retrasar o ralentizar el progreso de la enfermedad, trastorno o afección; mejora o paliación de la enfermedad, trastorno o afección; y remisión (ya sea parcial o total), ya sea detectable o indetectable. "Paliar" una enfermedad, trastorno, o afección significa que la extensión y/o las manifestaciones clínicas no deseables de la enfermedad, trastorno o afección se disminuyen y/o el curso temporal de la progresión se ralentiza o alarga, en comparación con la extensión o el curso temporal en ausencia de tratamiento.
Como se usa en la presente, "siembra tumoral" se refiere al derrame de grupos de células tumorales y su posterior crecimiento como implantes malignos en un sitio distinto del sitio del tumor original.
A menos que se defina lo contrario, todos los términos técnicos y científicos usados en la presente tienen el mismo significado que el entendido comúnmente un experto en la técnica a la que pertenece esta invención. Los métodos y materiales se describen en la presente para su uso en la presente divulgación; también pueden usarse otros métodos y materiales adecuados conocidos en la técnica. Los materiales, métodos y ejemplos son solo ilustrativos y no se pretende que sean limitativos de ninguna manera.
En la descripción siguiente se exponen los detalles de una o más realizaciones de la invención. Otras características, objetos y ventajas de la invención resultarán evidentes a partir de la descripción y de las reivindicaciones.
Breve descripción de los dibujos
Las Figuras 1A-E son un conjunto de diagramas y fotografías que muestran que miR-483-5p, miR-551a y CKB son clínicamente relevantes y pueden inhibirse terapéuticamente. a, los niveles de miR-483-5p y miR-551a en 37 muestras de tumores primarios y 30 muestras de metástasis hepáticas se cuantificaron mediante PCR cuantitativa en tiempo real. b, se midieron los niveles de expresión de CKB en 37 muestras de tumores primarios y 30 muestras de metástasis hepáticas mediante PCR cuantitativa en tiempo real. c, Metástasis hepática en ratones inyectados con células LvM3b y tratados con una única dosis de AAV que expresa doblemente miR-483-5p y miR-551a un día después de la inyección de células. d, Mediciones bioluminiscentes de metástasis hepática en ratones inyectados con 5 x 105 células LvM3b y tratados con ciclocreatina diariamente durante dos semanas. Los ratones se sacrificaron y se extirparon los hígados para imagenología ex vivo al final del tratamiento. e, Mediciones bioluminiscentes de metástasis hepática en ratones inyectados con 5 x 105 células LvM3b y tratados con el inhibidor del transportador de creatina ácido beta-guanidinopropiónico ((p-GPA) diariamente durante dos semanas. Barras de error, s.e.m.; todos los valores de P se basan en pruebas t de Student unilaterales. *P<0,05; **P<0,001; ***P<0,0001.
La Figura 2 es un diagrama y una fotografía que muestran que el tratamiento con p-GPA suprimió la metástasis del cáncer colorrectal. Mediciones bioluminiscentes de metástasis hepática en los ratones inyectados con 5 x 105 células LvM3b y tratados con p-GPA al día durante tres semanas. Los ratones se sacrificaron a las tres semanas y se extrajo el hígado para imagenología bioluminiscente e histología macroscópica. Las barras de error representan el s.e.m.; todos los valores de P se basan en pruebas t de Student unilaterales. *P<0,05.
Las Figuras 3A-C son un conjunto de diagramas y fotografías que muestran que el transportador de creatina, SLC6a8, es necesario para la metástasis del cáncer colorrectal y de páncreas. a) Metástasis hepática por células LvM3b altamente agresivas que expresan horquillas cortas dirigidas al canal transportador de creatina, SLC6a8. La metástasis hepática se monitorizó mediante imagenología bioluminiscente y los ratones se sacrificaron tres semanas después de la inoculación de las células cancerosas. Se extrajeron los hígados para histología macroscópica. b) Metástasis hepática en ratones inyectados con 5 x 105 SW480 células transducidas con un ARNhc dirigido a SLC6A8. La progresión metastásica se monitorizó mediante imagenología bioluminiscente. Los
ratones se sacrificaron 28 días después de la inyección y se extirparon los hígados para imagenología bioluminiscente e histología macroscópica. c) Metástasis hepática en ratones inyectados con 5 x 105 células de cáncer de páncreas PANC1 transducidas con un ARNhc dirigido a SLC6a8. La progresión metastásica se monitorizó mediante imagenología bioluminiscente y los ratones se sacrificaron como se ha descrito anteriormente. Las barras de error representan la s.e.m.; todos los valores de P se basan en pruebas t de Student unilaterales. *P<0,05; **P<0,001; ***P<0,0001.
La Figura 4 es un diagrama que muestra que SLC6a8 se regula por incremento en las metástasis hepáticas en comparación con los tumores primarios. La expresión de SLC6a8 en 36 tumores primarios y 30 metástasis hepáticas se cuantificó mediante PCR cuantitativa en tiempo real. Las barras de error representan la s.e.m.; todos los valores de P se basan en pruebas t de Student unilaterales. *P<0,05.
La Figura 5 es un diagrama y una fotografía que muestran que el tratamiento con p-GPA suprime la supervivencia de las células de cáncer de páncreas PANC1 diseminadas en el hígado in vivo. Imagenología bioluminiscente de ratones inmunodeficientes inyectados con 5 x 105 células Panc1 con y sin pretratamiento con p-GPA 10 mM durante 48 h. Se realizó imagenología de los ratones el día 1 después de la inyección y la señal se normalizó al día cero. Los valores de p se basan en pruebas t de Student unilaterales. * P<0,05.
La Figura 6 es un diagrama que muestra que p-GPA aumenta la citotoxicidad de la gemcitabina en las células de cáncer de páncreas PANC1. Viabilidad celular de las células de cáncer de páncreas PANC1 después del tratamiento con dosis crecientes de gemcitabina sola o dosis crecientes de gemcitabina en combinación con p-GPA 10 mM. La viabilidad celular se ensayó usando el reactivo WST-1. Las barras de error representan el error estándar de la media.
La Figura 7 es un diagrama que muestra que p-GPA aumenta la citotoxicidad del 5'-fluorouracilo en células de cáncer colorrectal LS-LvM3b. Viabilidad celular de las células Ls-LvM3b después del tratamiento con dosis crecientes de 5'-fluorouracilo solo o dosis crecientes de 5'-fluorouracilo en combinación con p-GPA 10 mM. La viabilidad celular se ensayó usando el reactivo WST-1. Las barras de error representan el error estándar de la media.
Descripción detallada de la invención
La invención se define en las reivindicaciones adjuntas. La presente invención presenta métodos para prevenir o reducir la proliferación, diferenciación o supervivencia aberrantes de células. Por ejemplo, los compuestos de la invención pueden ser útiles para reducir el riesgo de, o prevenir, que los tumores aumenten de tamaño o alcancen un estado metastásico. Los presentes compuestos pueden administrarse para detener la progresión o el avance del cáncer. Además, la presente invención incluye el uso de los presentes compuestos para reducir el riesgo de, o prevenir, una recurrencia del cáncer.
Compuestos
La invención presenta compuestos útiles en el tratamiento del cáncer. Los compuestos ejemplares descritos en la presente incluyen compuestos que tienen una estructura de acuerdo con las Fórmulas I-III como se describe en la presente:
en donde X1 está ausente, es NH o CH2 ;
R1 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o arilo C6-C10 alquilo C1-C6 opcionalmente sustituido;
R2, R3, y R4 son independientemente hidrógeno o alquilo C1 -C6 opcionalmente sustituido; y
R5 y R6 son hidrógeno o NH2 ;
o una sal farmacéuticamente aceptable del mismo;
en donde Q1 es amidino opcionalmente sustituido o 2-piridilo opcionalmente sustituido;
X2 es S o NR12;
m es 0 o 1;
R7 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, oarilo C6-C10 alquilo C1-C6 opcionalmente sustituido; R8 y R9 son independientemente hidrógeno, deuterio, halo, hidroxilo, NH2 , alquilo C1-C6 opcionalmente sustituido, o R8 o R9 pueden combinarse con R10 o R11 para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido o con R12 para formar un heterociclo C3-C6 opcionalmente sustituido;
R10 y R11 son independientemente hidrógeno, deuterio, alquilo C1-C6 opcionalmente sustituido, o R10 o R11 pueden combinarse con R8 o R9 para formar un anillo cicloalquilo C3-C6 opcionalmente sustituido;
R12 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o R12 puede combinarse con R8 o R9 para formar un heterociclo C3-C6 opcionalmente sustituido, y
en donde si R9 es halo, entonces R8 es halo o alquilo C1-C6 opcionalmente sustituido,
a sal farmacéuticamente aceptable del mismo;
en donde Q1 es amidino opcionalmente sustituido o 2-piridilo opcionalmente sustituido;
m es 1 o 2;
R7 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o arilo C6-C10 alquilo C1-C6 opcionalmente sustituido; R8 y R9 son independientemente hidrógeno, deuterio, halo, hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido, o R8 y R9 se combinan con los átomos a los que están unidos para formar un anillo de cicloalquilo C3-C6 opcionalmente sustituido; o R8 o R9 se combinan con R10 o R11 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R8 o R9 se combinan con R12 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido;
R10 y R11 son independientemente hidrógeno, deuterio, alquilo C1-C4 opcionalmente sustituido, alquenilo C2-C6 opcionalmente sustituido, alquinilo C2-C6 opcionalmente sustituido o R10 y R11 se combinan con los átomos a los que están unidos para formar un anillo de cicloalquilo C3-C6 opcionalmente sustituido; o R10 o R11 se combinan con R8 o R9 con los átomos a los que están unidos para formar un anillo cicloalquilo C3-C4 opcionalmente sustituido; o R10 o R11 se combinan con R12 con los átomos a los que están unidos para formar un heterociclo C3-C4 opcionalmente sustituido;
R12 es hidrógeno, alquilo C1-C6 opcionalmente sustituido, o R12 se combina con R8 o R9 con los átomos a los que están unidos para formar un heterociclo C3-C5 opcionalmente sustituido, o R12 se combina con R10 o R11 con los átomos a los que están unidos para formar un heterociclo C3-C4 opcionalmente sustituido
donde si m es 1 y R 8 es hidrógeno, halo, hidroxilo o metilo, entonces por lo menos uno de R9, R10 y R11 no es hidrógeno;
en donde si m es 1 y R10 es metilo, entonces por lo menos uno de R8, R9 y R11 no es hidrógeno;
en donde si m es 1 y R8 es NH2 y R10 es hidrógeno, metilo o -CH2CH2OH entonces por lo menos uno de R9 o R11 no es hidrógeno;
en donde si m es 1, R8 es halo y R10 es alquilo C1-C4 opcionalmente sustituido, entonces por lo menos uno de R9 y R10 no es hidrógeno;
a sal farmacéuticamente aceptable del mismo; y
A-B Fórmula III
en donde A es un inhibidor del transporte de creatina y/o creatina quinasa que comprende un grupo amidino; B tiene la estructura:
en donde n es 0 o 1;
Q2 es hidroxilo, amino opcionalmente sustituido o -SO2OH; y
R13 y R14 son independientemente hidrógeno, -CO2H, o se combinan para formar C=O;
donde B está conjugado con A en uno de los nitrógenos de amidino,
o una sal farmacéuticamente aceptable del mismo.
En la presente se describen otras realizaciones (por ejemplo, los compuestos 1-326 de las Tablas 1-11) así como métodos ejemplares para la síntesis de estos compuestos.
Utilidad y administración
Los compuestos de la invención son útiles en los métodos de la invención y, aunque no se quiere estar limitado por la teoría, se cree que ejercen sus efectos deseables a través de su capacidad para inhibir el transporte de creatina y/o creatina quinasa. Los compuestos de la invención también pueden usare para el tratamiento de ciertas afecciones como el cáncer.
Los compuestos descritos en la presente (por ejemplo, un compuesto de acuerdo con las Fórmulas I-IX o cualquiera de los compuestos 1-448 de las Tablas 1-11) son útiles en los métodos de la divulgación y, aunque no se quiere estar limitado por la teoría, se cree que ejercen su efectos deseables a través de su capacidad para inhibir el transporte de creatina y/o creatina quinasa. Los compuestos divulgados en la presente (por ejemplo, un compuesto de acuerdo con las Fórmulas I-IX o cualquiera de los compuestos 1-448 de las Tablas 1-11) también pueden usarse para el tratamiento de ciertas afecciones como el cáncer.
La creatina ayuda a suministrar energía a todas las células del cuerpo aumentando la formación de ATP. Es captada por tejidos con alta demanda energética a través de un sistema de transporte activo. La conversión de ADP en ATP por transferencia de fosfato de la fosfocreatina es catalizada por la creatina quinasa. Algunas de las funciones asociadas con el sistema de fosfocreatina incluyen la regeneración eficiente de energía en forma de ATP en células con demanda energética fluctuante y alta, transporte de energía a diferentes partes de la célula, actividad de transporte de fosforilo, regulación del transporte de iones y participación en las vías de transducción de señales.
Se ha demostrado que la creatina quinasa tiene niveles elevados en ciertos tipos de tumores. Estos tipos de tumores pueden utilizar la expresión aumentada de creatina quinasa para prevenir la apoptosis en condiciones hipóxicas o hipoglucémicas. También se ha demostrado que los cánceres malignos con mal pronóstico sobreexpresan las creatina quinasas, lo que puede estar relacionado con un alto recambio de energía y el fallo de eliminación de células cancerosas por apoptosis. La inhibición del transporte activo de la creatina hacia las células cancerosas puede revertir estas tendencias y dar como resultado la inhibición del cáncer y/o metástasis.
Métodos de tratamiento
Como se divulga en la presente, la inhibición del transporte de creatina y/o la creatina quinasa suprime la metástasis. El sistema de fosfocreatina promueve la metástasis mejorando la supervivencia de las células cancerosas diseminadas en el hígado actuando como un depósito energético para la generación de ATP para soportar la hipoxia hepática. La inhibición del transporte de creatina hacia las células cancerosas limita la cantidad de fosfocreatina disponible para usar en la producción de ATP. La inhibición de la creatina quinasa inhibe la producción de ATP mediante la conversión de fosfocreatina en creatina.
Los tumores vascularizados típicos que pueden tratarse con el método incluyen tumores sólidos, particularmente carcinomas, que requieren un componente vascular para el suministro de oxígeno y nutrientes. Los tumores sólidos ejemplares incluyen, pero no se limitan a, carcinomas de pulmón, mama, hueso, ovario, estómago, páncreas, laringe, esófago, testículos, hígado, parótida, tracto biliar, colon, recto, cuello uterino, útero, endometrio, riñón, vejiga, próstata, tiroides, carcinomas de células escamosas, adenocarcinomas, carcinomas de células pequeñas, melanomas, gliomas, glioblastomas, neuroblastomas, sarcoma de Kaposi y sarcomas.
El tratamiento del cáncer puede resultar en una reducción del tamaño o volumen de un tumor. Por ejemplo, después del tratamiento, el tamaño del tumor se reduce en un 5% o más (por ejemplo, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% o más) con respecto a su tamaño antes del tratamiento. El tamaño de un tumor puede medirse mediante cualquier medio de medición reproducible. El número de tumores puede medirse contando tumores
visibles a simple vista o a un aumento específico (por ejemplo, 2x, 3x, 4x, 5x, 10x o 50x).
El tratamiento del cáncer puede resultar en una disminución en el número de nódulos metastásicos en otros tejidos u órganos distantes del sitio del tumor primario. Por ejemplo, después del tratamiento, el número de nódulos metastásicos se reduce en un 5% o más (por ejemplo, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% o más) con respecto al número antes del tratamiento. El número nódulos metastásicos puede medirse mediante cualquier medio de medición reproducible. El número de nódulos metastásicos puede medirse contando los nódulos metastásicos visibles a simple vista o con un aumento específico (por ejemplo, 2x, 10x o 50x).
El tratamiento del cáncer puede dar como resultado un aumento del tiempo medio de supervivencia de una población de sujetos tratados de acuerdo con la presente invención en comparación con una población de sujetos no tratados. Por ejemplo, el tiempo medio de supervivencia se aumenta en más de 30 días (más de 60 días, 90 días o 120 días). Un aumento en el tiempo medio de supervivencia de una población puede medirse mediante cualquier medio reproducible. Un aumento en el tiempo medio de supervivencia de una población puede medirse, por ejemplo, calculando para una población la duración media de supervivencia tras el inicio del tratamiento con el compuesto de la invención. También puede medirse un aumento en el tiempo medio de supervivencia de una población, por ejemplo, calculando para una población la duración media de supervivencia después de la finalización de una primera serie de tratamiento con el compuesto de la invención.
El tratamiento del cáncer también puede dar como resultado una disminución de la tasa de mortalidad de una población de sujetos tratados en comparación con una población no tratada. Por ejemplo, la tasa de mortalidad se reduce en más del 2% (por ejemplo, más del 5%, 10% o 25%). Una disminución en la tasa de mortalidad de una población de sujetos tratados puede medirse mediante cualquier medio reproducible, por ejemplo, calculando para una población el número medio de muertes relacionadas con la enfermedad por unidad de tiempo después del inicio del tratamiento con el compuesto de la invención. También puede medirse una disminución en la tasa de mortalidad de una población, por ejemplo, calculando para una población el número medio de muertes relacionadas con la enfermedad por unidad de tiempo después de completar una primera serie de tratamiento con el compuesto de la invención.
Composiciones
Dentro del alcance de esta invención se encuentra una composición que contiene un portador adecuado y uno o más de los agentes terapéuticos descritos anteriormente. La composición puede ser una composición farmacéutica que contiene un portador farmacéuticamente aceptable, una composición dietética que contiene un portador adecuado dietéticamente aceptable o una composición cosmética que contiene un portador cosméticamente aceptable. El término "composición farmacéutica" se refiere a la combinación de un agente activo con un portador, inerte o activo, lo que hace que la composición sea especialmente adecuada para uso diagnóstico o terapéutico in vivo o ex vivo. Un "portador farmacéuticamente aceptable", después de ser administrado a o sobre un sujeto, no produce efectos fisiológicos indeseables. El portador en la composición farmacéutica debe ser "aceptable" también en el sentido de que sea compatible con el ingrediente activo y pueda ser capaz de estabilizarlo. Pueden utilizarse uno o más agentes solubilizantes como portadores farmacéuticos para la administración de un compuesto activo. Los ejemplos de un portador farmacéuticamente aceptable incluyen, pero no se limitan a, vehículos biocompatibles, adyuvantes, aditivos y diluyentes para lograr una composición utilizable como una forma de dosificación. Los ejemplos de otros portadores incluyen óxido de silicio coloidal, estearato de magnesio, celulosa, lauril sulfato de sodio y D&C Amarillo N° 10.
Como se usa en la presente, el término "sal farmacéuticamente aceptable" se refiere a aquellas sales que, dentro del alcance del buen juicio médico, son adecuadas para su uso en contacto con los tejidos de humanos y animales inferiores sin toxicidad, irritación o respuesta alérgica indebidas, y son proporcionales a una relación beneficio/riesgo razonable. Las sales farmacéuticamente aceptables de aminas, ácidos carboxílicos y otros tipos de compuestos son bien conocidas en la técnica. Por ejemplo, S.M. Berge, et al. describen sales farmacéuticamente aceptables en detalle en J. Pharm aceutica l Sciences, 66: 1-19 (1977). Las sales pueden prepararse in situ durante el aislamiento y la purificación finales de los compuestos de la invención, o por separado haciendo reaccionar una función de base libre o ácido libre con un reactivo adecuado, como se describe de manera general a continuación. Por ejemplo, puede hacerse reaccionar una función de base libre con un ácido adecuado. Además, cuando los compuestos de la invención portan una fracción ácida, sus sales farmacéuticamente aceptables adecuadas pueden incluir sales metálicas como sales de metales alcalinos, por ejemplo, sales de sodio o potasio; y sales de metales alcalinotérreos, por ejemplo, sales de calcio o magnesio. Ejemplos de sales de adición de ácido no tóxicas y farmacéuticamente aceptables son las sales de un grupo amino formado con ácidos inorgánicos como ácido clorhídrico, ácido bromhídrico, ácido fosfórico, ácido sulfúrico y ácido perclórico o con ácidos orgánicos como ácido acético, ácido oxálico, ácido maleico, ácido tartárico, ácido cítrico, ácido succínico o ácido malónico o usando otros métodos usados en la técnica como intercambio iónico. Otras sales farmacéuticamente aceptables, incluyen sales de adipato, alginato, ascorbato, aspartato, bencenosulfonato, benzoato, bisulfato, borato, butirato, canforato, canforsulfonato, citrato, ciclopentanopropionato, digluconato, dodecilsulfato, etanosulfonato, formiato, fumarato, gluceheptonato, glicerofosfato, gluconato, hemisulfato, heptanoato, hexanoato, hidroyoduro, 2-hidroxietanosulfonato,
lactobionato, lactato, laurato, lauril sulfato, malato, maleato, malonato, metanosulfonato, 2-naftalenosulfonato, nicotinato, nitrato, oleato, oxalato, palmitato, pamoato, pectinato, 3-fenilpropionato, fosfato, picrato, pivalato, propionato, estearato, succinato, sulfato, tartrato, tiocianato, p-toluenosulfonato, undecanoato y valerato. Las sales de metales alcalinos o alcalinotérreos representativas incluyen sodio, litio, potasio, calcio y magnesio. Otras sales farmacéuticamente aceptables incluyen, cuando sea apropiado, cationes de amonio, amonio cuaternario y amina no tóxicos formados usando contraiones como haluro, hidróxido, carboxilato, sulfato, fosfato, nitrato, alquilsulfonato inferior y arilsulfonato.
Como se ha descrito anteriormente, las composiciones farmacéuticas de la presente invención incluyen adicionalmente un portador farmacéuticamente aceptable, que, como se usa en la presente, incluye todos y cada uno de los solventes, diluyentes u otros vehículos líquidos, agentes auxiliares de dispersión o suspensión, agentes tensioactivos, agentes isotónicos, espesantes o agentes emulsionantes, conservantes, aglutinantes sólidos y lubricantes, según convenga a la forma de dosificación particular deseada. Remington's Pharmaceutical Sciences, decimosexta edición, E.W. Martin (Mack Publishing Co., Easton, Pa., 1980) divulga varios portadores usados en la formulación de composiciones farmacéuticas y técnicas conocidas para la preparación de los mismos. Excepto en la medida en que cualquier medio portador convencional sea incompatible con los compuestos de la invención, como produciendo cualquier efecto biológico indeseable o interactuando de otra forma de una manera perjudicial con cualquier otro componente de la composición farmacéutica, se contempla que su uso esté dentro del alcance de esta invención. Algunos ejemplos de materiales que pueden servir como portadores farmacéuticamente aceptables incluyen, pero no se limitan a, azúcares como lactosa, glucosa y sacarosa; almidones como almidón de maíz y almidón de patata; celulosa y sus derivados como carboximetilcelulosa de sodio, etilcelulosa y acetato de celulosa; tragacanto en polvo; malta; gelatina; talco; excipientes como manteca de cacao y ceras para supositorios; aceites como aceite de cacahuete, aceite de semilla de algodón; aceite de cártamo, aceite de sésamo; aceite de oliva; aceite de maíz y aceite de soja; glicoles; como propilenglicol; ésteres como oleato de etilo y laurato de etilo; agar; fosfolípidos naturales y sintéticos, como fosfátidos de soja y yema de huevo, lecitina, lecitina de soja hidrogenada, lecitina de dimiristoíl, lecitina de dipalmitoíl, lecitina de diestearoíl, lecitina de dioleoíl, lecitina hidroxilada, lisofosfatolidilcolina, cardiolipina, esfingomielina, fosfatildicolina, fosfatidil etanolamina, diastearoíl fosfatidiletanolamina (DSPE) y sus ésteres pegilados, como DSPE-PEG750 y DSPE-PEG2000, ácido fosfatídico, fosfatidil glicerol y fosfatidil serina. Los grados comerciales de lecitina que se prefieren incluyen los que están disponibles con el nombre comercial Phosal® o Phospholipon® e incluyen Phosal 53 MCT, Phosal 50 PG, Phosal 75 SA, Phospholipon 90H, Phospholipon 90G y Phospholipon 90 NG; se prefieren particularmente fosfatidilcolina de soja (SoyPC) y DSPE-PEG2000; agentes tamponadores como hidróxido de magnesio e hidróxido de aluminio; ácido algínico; agua libre de pirógenos; solución salina isotónica; solución de Ringer; alcohol etílico y soluciones tampón de fosfato, así como otros lubricantes compatibles no tóxicos como el lauril sulfato de sodio y estearato de magnesio, así como agentes colorantes, agentes de liberación, agentes de recubrimiento, agentes edulcorantes, agentes aromatizantes y perfumantes, conservantes y antioxidantes también pueden estar presente en la composición, de acuerdo con el criterio del formulador.
La composición descrita anteriormente, en cualquiera de las formas descritas anteriormente, puede usarse para tratar el melanoma o cualquier otra enfermedad o afección descrita en la presente. Una cantidad eficaz se refiere a la cantidad de un compuesto/agente activo que se requiere para conferir un efecto terapéutico a un sujeto tratado. Las dosis efectivas variarán, como reconocen los expertos en la técnica, dependiendo de los tipos de enfermedades tratadas, la vía de administración, el uso de excipientes y la posibilidad de uso conjunto con otro tratamiento terapéutico. Una composición farmacéutica de esta invención puede administrarse por vía parenteral, oral, nasal, rectal, tópica o bucal. El término "parenteral" como se usa en la presente se refiere a inyección subcutánea, intracutánea, intravenosa, intramuscular, intraarticular, intraarterial, intrasinovial, intraesternal, intratecal, intralesional, ontracreneal, así como cualquier técnica de infusión adecuada.
Una composición inyectable estéril puede ser una solución o suspensión en un diluyente o solvente parenteralmente aceptable no tóxico. Tales soluciones incluyen, pero no se limitan a, 1,3-butanodiol, manitol, agua, solución de Ringer y solución isotónica de cloruro de sodio. Además, los aceites fijos se emplean convencionalmente como solvente o medio de suspensión (por ejemplo, mono- o diglicéridos sintéticos). Los ácidos grasos, como pero no limitados a, el ácido oleico y sus derivados de glicéridos, son útiles en la preparación de inyectables, al igual que los aceites naturales farmacéuticamente aceptables, como pero no limitados a, aceite de oliva o aceite de ricino, versiones polioxietiladas de los mismos. Estas soluciones o suspensiones oleosas también pueden contener un diluyente o dispersante alcohólico de cadena larga como, pero no limitado a, carboximetilcelulosa o agentes dispersantes similares. También pueden usarse otros surfactantes usados comúnmente, como pero no limitados a, Tweens o Spans u otros agentes emulsionantes similares o potenciadores de la biodisponibilidad, que se usan comúnmente en la fabricación de formas de dosificación sólidas, líquidas u otras farmacéuticamente aceptables para propósitos de formulación.
Una composición para administración oral puede ser cualquier forma de dosificación aceptable por vía oral, incluyendo cápsulas, comprimidos, emulsiones y suspensiones, dispersiones y soluciones acuosas. En el caso de comprimidos, los portadores usados comúnmente incluyen, pero no se limitan a, lactosa y almidón de maíz. También se añaden típicamente agentes lubricantes, como, pero no limitados a, estearato de magnesio. Para la
administración oral en forma de cápsula, los diluyentes útiles incluyen, pero no se limitan a, lactosa y almidón de maíz seco. Cuando se administran suspensiones o emulsiones acuosas por vía oral, el ingrediente activo puede suspenderse o disolverse en una fase oleosa combinada con agentes emulsionantes o de suspensión. Si se desea, pueden añadirse ciertos agentes edulcorantes, aromatizantes o colorantes.
Las composiciones farmacéuticas para administración tópica de acuerdo con la invención descrita pueden formularse como soluciones, pomadas, cremas, suspensiones, lociones, polvos, pastas, geles, pulverizaciones, aerosoles o aceites. Alternativamente, las formulaciones tópicas pueden estar en forma de parches o apósitos impregnados con el ingrediente o ingredientes activos, que opcionalmente pueden incluir uno o más excipientes o diluyentes. En algunas realizaciones preferidas, las formulaciones tópicas incluyen un material que mejoraría la absorción o penetración del o de los agentes activos a través de la piel u otras áreas afectadas.
Una composición tópica contiene una cantidad segura y eficaz de un portador dermatológicamente aceptable adecuado para su aplicación a la piel. Una composición o componente "cosméticamente aceptable" o "dermatológicamente aceptable" se refiere a una composición o componente que es adecuado para su uso en contacto con la piel humana sin toxicidad, incompatibilidad, inestabilidad o respuesta alérgica indebidas. El portador permite administrar un agente activo y un componente opcional a la piel a una concentración o concentraciones apropiadas. Por tanto, el portador puede actuar como diluyente, dispersante, solvente o similar para asegurar que los materiales activos se apliquen y distribuyan uniformemente sobre el objetivo seleccionado a una concentración apropiada. El portador puede ser sólido, semisólido o líquido. El portador puede estar en forma de loción, crema o gel, en particular uno que tenga un espesor o límite de elasticidad suficiente para evitar que los materiales activos sedimenten. El portador puede ser inerte o poseer beneficios dermatológicos. También debería ser física y químicamente compatible con los componentes activos descritos en la presente, y no debería perjudicar indebidamente a la estabilidad, eficacia u otros beneficios de uso asociados con la composición.
Terapias de combinación
En algunas realizaciones, la composición farmacéutica puede incluir además un compuesto adicional que tiene actividad antiproliferativa. El compuesto adicional que tiene actividad antiproliferativa puede seleccionarse de un grupo de agentes antiproliferativos que incluyen los que se muestran en la Tabla 12.
También se apreciará que los compuestos y las composiciones farmacéuticas de la presente invención pueden formularse y emplearse en terapias de combinación, es decir, los compuestos y las composiciones farmacéuticas pueden formularse con o administrarse simultáneamente con, antes o después de, uno o más de otros procedimientos terapéuticos o médicos deseados. La combinación particular de terapias (agentes terapéuticos o procedimientos) para emplear en un régimen de combinación tendrá en cuenta la compatibilidad de los agentes terapéuticos y/o procedimientos deseados y el efecto terapéutico deseado a lograr. También se apreciará que las terapias empleadas pueden lograr un efecto deseado para el mismo trastorno, o pueden lograr efectos diferentes (por ejemplo, control de cualquier efecto adverso).
Por “agente antiproliferativo” se entiende cualquier agente antiproliferativo, incluyendo los agentes antiproliferativos enumerados en la Tabla 12, cualquiera de los cuales puede usarse en combinación con un inhibidor del transporte de creatina y/o de la creatina quinasa para tratar las afecciones médicas enumeradas en la presente. Los agentes antiproliferativos también incluyen derivados de organo-platino, derivados de naftoquinona y benzoquinona, ácido crisofánico y derivados de antroquinona de los mismos.
continuación
continuación
continuación
continuación
__________________________________________(continuación)____________________________ Tabla 12
CDA-II (promotor de apoptosis, Everlife) MX6 (promotor de apoptosis, MAXIA)
SDX-101 (promotor de apoptosis, Salmedix)____ apomina (promotor de apoptosis, ILEX Oncology)
EJEMPLOS
(Solo los compuestos que están indicados en la parte anterior de la descripción y que entran dentro del alcance de las reivindicaciones forman parte de la invención)
M ateria les y m étodos
Cultivo de células
Las líneas celulares indicadas se adquirieron de ATCC y se cultivaron en medio DMEM suplementado con FBS al 10%, piruvato de sodio, L-glutamina y antibióticos de penicilina-estreptomicina. Para el pretratamiento con el fármaco, las células se trataron con las cantidades indicadas de fármaco durante 24-48 horas.
Estudios con anim ales
Todo el trabajo con animales se llevó a cabo de acuerdo con un protocolo aprobado por el Comité Institucional de Uso y Cuidado de Animales (IACUC) de la Universidad Rockefeller. Se usaron ratones NOD-SCID macho de 5-6 semanas de la misma edad para ensayos de colonización intrahepática y metástasis hepática.
Ensayo de pro liferación en condiciones hipóxicas
Se sembraron 100K células por triplicado en placas de 6 pocillos y se contaron las células 5 días después de la siembra. Las células se cultivaron en una cámara de cultivo celular que contenía 1% de oxígeno.
C recim iento de l tum or prim ario
Se suspendieron 1x106 células en 100 pl de una mezcla de PBS:Matrigel 1:1 y se inyectaron en los costados subcutáneos de los ratones. El crecimiento del tumor se midió usando calibres digitales comenzando 7 días después de la inyección, cuando los tumores palpables pueden medirse con precisión. El volumen de los tumores se calculó usando la fórmula Volumen = (anchura)2 x (longitud)/2. Cuando se trataron con fármacos, a los ratones se les inyectaron las cantidades indicadas de fármaco en 300 pl de PBS al día hasta que se sacrificó a los ratones.
Ensayo de m etástasis
Se inyectaron 5x106 células cancerosas altamente metastásicas en la circulación portal de ratones inmunodeficientes. Un día después de la inoculación de las células cancerosas, a los ratones se les inyectaron las cantidades indicadas de fármaco en 300 pl de PBS. El tratamiento continuó diariamente y se monitorizó la progresión metastásica mediante imagenología bioluminiscente hasta que se sacrificaron los ratones, momento en el que se extirparon los hígados para imagenología bioluminiscente e histología macroscópica. Cuando se indica, las células cancerosas se pretrataron con las cantidades indicadas de compuesto durante 48 horas antes de la inyección en ratones inmunodeficientes.
Ensayo de inh ib ic ión de l transportador de creatina in vivo
Los compuestos solubles se formularon en solución salina (NaCl al 0,9%). Algunos compuestos se disolvieron primero en ácido clorhídrico 1 N (1,0 equivalente) para preparar la sal de HCl seguido de la adición de PBS para ajustar al volumen final. Los compuestos menos solubles se disolvieron primero en ácido clorhídrico 1 o 2 N (1,0 equivalente) para preparar la sal de HCl seguido de la adición de DMSO y agua para ajustar al volumen final dando como resultado una relación de DMSO a acuosa 1:1.
Los estudios se realizaron en ratones macho C57B16 de 6-7 semanas de edad, que recibieron una dieta regular (Purina 5001, Research Diet) y un ritmo de sueño regular (horario de 12 horas noche/día). Los experimentos se realizaron ~6 h después de la exposición a la luz del día. Los ratones se pesaron y se dividieron aleatoriamente en grupos de 3 ratones por grupo y se inyectaron i.p. con 100-200 pl de solución de dosificación para administrar 250 mg/kg (50 mg/ml o 381 mM) de equivalente de p-GPA (es decir, 1,91 mmol/kg) junto con un control de vehículo. Se disolvió monohidrato de creatina-(metil-d3) (es decir, creatina-d3, Cambridge Isotope Laboratories, catálogo DLM-1302) en 100 pl de NaCl al 0,9% (0,2 mg/ml) y se inyectó i.p. 7 minutos después de la inyección del fármaco. Los volúmenes se ajustaron en base al peso de los ratones para alcanzar una dosis final de 1 mg/kg. Después de una hora, se sacrificaron los ratones, se perfundieron los corazones con PBS, se retiraron, se congelaron al instante en
nitrógeno líquido y se almacenaron a -80° C hasta su procesamiento adicional.
Los corazones de ratón se descongelaron y se pesaron en tubos cónicos Eppendorf de 1,5 ml. Los pesos típicos del corazón varían entre 800-1200 mg. Se añadieron entre seis y doce perlas de zirconia/sílice de 1 mm (BioSpeCProducts, Inc., Bartlesville, OK) a los tubos con un volumen suficiente de 2-propanol al 70% en agua para proporcionar una dilución de 4 veces. Luego las muestras se colocaron en un MiniBeadBeater (BioSpec Products, Inc.) durante 2 minutos para alterar el tejido y homogeneizar la muestra.
Se transfirieron alícuotas (20 j l) de los corazones homogeneizados a una placa de microtitulación de 96 pocillos. Las muestras se extrajeron mediante la adición de acetonitrilo (1,0 ml) que contenía 0,25 pg/ml de creatinad5 (CDN Isotopes, Pointe-Claire, Quebec) como estándar interno. Las muestras se mezclaron en un agitador rotatorio durante 10 minutos y luego se colocaron en una centrífuga para centrifugar durante 10 minutos a 3000 rpm a 4° C. El sobrenadante (900 j l) se transfirió a una placa de 96 pocillos profunda para su análisis.
Los estándares de calibración, las muestras en blanco y las muestras de control de calidad se preparan a partir de corazones de ratón de control homogeneizados como se ha indicado anteriormente. Luego se enriquecieron las alícuotas de homogeneizado con cantidades conocidas de creatina-d3 (CDN Isotopes, Pointe-Claire, Quebec) o solvente, y se procesan junto con las muestras como se ha indicado anteriormente.
El análisis se realizó mediante LC-MS/MS usando un sistema Acquity UPLC(Waters Corp., Milford, MA)/Triple Quad 5500 (AB Sciex, Framingham, MA). Se inyectan cinco microlitros de muestra en una columna HILIC, 2,1 x 50 mm, 3 pm (Fortis Technologies, Cheshire, Inglaterra) a un caudal de 0,4 ml/min. Se usó un gradiente binario de acetonitrilo y acetato de amonio 10 mM para eluir los analitos de la columna. El espectrómetro de masas se hizo funcionar en electropulverización de iones positiva en el modo de monitorización de reacción múltiple para las siguientes transiciones de masa:
Creatina-d5: m/z 137,1/95,0
Creatina-d3: m/z 135,1/93,0
Los datos se recopilaron y procesaron usando un Analyst 1.6.2 (AB Sciex, Framingham, MA). Una calibración lineal de la relación de área de pico de creatina-d3/creatina-d5 varió de 0,05 a 10 pg/ml. Los datos se expresaron como pg de creatina-d3 por gramo de corazón. Los valores medios y las desviaciones estándar se calcularon a partir de tres muestras de corazón y se informó del porcentaje de inhibición del transporte de creatina-d3 con respecto al control del vehículo.
T abl 1 . P r n inhi i i n l r n r r inin - n i r iaco
Selección In vivo
Se suspendieron 1 x 106 células LS174T que expresan un informador de luciferasa en un volumen de 20 pl de mezcla de PBS/Matrigel 1:1y se inyectan por vía intrahepática en los hígados de ratones NOD-SCID. Se permitió que se desarrollaran nódulos metastásicos durante un período de 3-4 semanas y se monitorizaron mediante imagenología bioluminiscente. Los nódulos formados se escindieron y disociaron mediante digestión con colagenasa e hialuronidasa en una suspensión de células individuales. Se permitió que las células se expandieran in vitro antes de reinyectarlas en ratones. Después de tres repeticiones de la selección in vivo, se establecieron líneas celulares de derivados de LvM3a y LvM3b altamente metastásicas.
Selección de b ib lioteca Lenti-m iR
Las células se transdujeron con una biblioteca de lentivirus Lenti-miR de 611 ARNmi (System Biosciences) a una baja multiplicidad de infección (MOI) de tal manera que cada célula sobreexpresara un único ARNmi. Luego, la población transducida se inyectó intrahepáticamente en ratones NOD-SCID para la selección in vivo de ARNmi que, cuando se sobreexpresaban, o promovían o suprimían la colonización hepática metastásica. La amplicación por PCR de ADN genómico y la recuperación de insertos de ARNmi lentivíricos se realizaron en células antes de la
inyección y de nódulos hepáticos de acuerdo con el protocolo del fabricante. El perfil de la matriz de ARNmi permitió la cuantificación del inserto de ARNmi antes y después de la selección in vivo.
Sistem a de cultivo en segm entos organotípico
Las células a inyectar se marcaron con rastreador de células rojo o verde (Invitrogen) y se inocularon en hígados de ratones NOD-SCID mediante inyección intraesplénica. Luego, se extrajeron los hígados y se cortaron en segmentos de 150 um usando un cortador de tejido Mcllwain (Ted Pella) y se colocaron en placas sobre insertos de cultivo de tejidos organotípicos (Millipore) y se cultivaron en medio E de William suplementado con el paquete de suplementos de mantenimiento de hepatocitos (Invitrogen). Después de los períodos de tiempo indicados, los segmentos de hígado se fijaron en paraformaldehído y se sometieron a imagenología usando microscopía multifotónica.
Ensayo de activación de caspasa in vivo
Para medir la actividad de la caspasa in vivo, se usó el sustrato VivoGlo Caspase 3/7 (Z-DEVD-sal de sodio de aminoluciferina, Promega). La luciferina está inactiva hasta que el péptido DEVD es escindido por la caspasa-3 activada en células apoptóticas. Se inyectó DEVD-luciferina en ratones que portaban células de cáncer colorrectal que expresaban luciferasa. Tras la activación por células apoptóticas, pueden realizarse imagenología bioluminiscente para medir la actividad de caspasa in vivo. Cinco horas después de la medición de la actividad caspasa in vivo, se inyecta a los ratones luciferina regular con propósitos de normalización.
Terapia viral adenoasociada
Se clonaron miR-483-5p y miR-551a como un policistrón que consistía de precursor de ARNmi con secuencias genómicas flanqueantes en tándem en el sitio BgIII y NotI de scAAV.GFP (Plásmido 21893, Addgene). A continuación se enumeran las secuencias genómicas que codifican miR-483-5p y miR-551a (SEQ ID NO: 5 y 6), las secuencias precursoras correspondientes (subrayadas, SEQ ID NO: 3 y 4) y las secuencias de microARN maduras correspondientes (subrayadas y en negrita, SEQ ID NO: 1 y 2). Los virus adenoasociados se empaquetaron, purificaron y titularon usando el sistema de expresión AAV-DJ Helper Free de Cell Biolabs.
miR-483-5p:
G G A G A A C C T T C A G C T T C A T G T G A C C C A G A G A C T C C T G T A T G C C T G G C T C T G G G A G T A C A G A A G G G C
C T A G A G C T G A C C C C T G C C C T C C G A A G C C C C T G G G G C A C T A G A T G G A T G T G T G C C A G A G G G T A G T A
G A G G C C T G G G G G T A G A G C C C A G C A C C C C C T T C G C G T A G A G A C C T G G G G G A C C A G C C A G C C C A G C
A A C C C C C T C G C G G C C G A C G C C T G A G G C T G T T C C T G G C T G C T C C G G T G G C T G C C A G A G G G G A C T G C
C G G G T G A C C C T G G A A A T C C A G A G T G G G T G G G G C C A G T C T G A C C G T T T C T A G G C G A C C C A C T C T T G
G T T T C C A G G G T T G C C C T G G A A A C C A C A G A T G G G G A G G G G T T G A T G G C A C C C A G C C T C C C C C A A G C
C T G G G A A G G G A C C C C G G A T C C C C A G A G C C T T T C C C T G C C T A T G G A G C G T T T C T C T T G G A G A A C A G G
G G G G C C T C T C A G C C C C T C A A T G C A A G T T G C T G A G
miR-483-5p:
C C T G C C C C A T T T G G G G G T A G G A A G T G G C A C T G C A G G G C C T G G T G C C A G C C A G T C C T T G C C C A G G G
A G A A G C T T C C C T G C A C C A G G C T T T C C T G A G A G G A G G G G A G G G C C A A G C C C C C A C T T G G G G G A C C C
C C G T G A T G G G G C T C C T G C T C C C T C C T C C G G C T G A T G G C A C C T G C C C T T T G G C A C C C C A A G G T G G A
G C C C C C A G C G A C C T T C C C C T T C C A G C T G A G C A T T G C T G T G G G G G A G A G G G G G A A G A C G G G A G G A
A A G A A G G G A G T G G T T C C A T C A C G C C T C C T C A C T C C T C T C C T C C C G T C T T C T C C T C T C C T G C C C T T G T
C T C C C T G T C T C A G C A G C T C C A G G G G T G G T G T G G G C C C C T C C A G C C T C C T A G G T G G T G C C A G G C C A
G A G T C C A A G C T C A G G G A C A G C A G T C C C T C C T G T G G G G G C C C C T G A A C T G G G C T C A C A T C C C A C A C A
T T T T C C A A A C C A C T C C C A T T G T G A G C C T T T G G T C C T G G T G G T G T C C C T C T G G T T G T G G G A C C A A G A G
C T T G T G C C C A T T T T T C A T C T G A G G A A G G A G G C A G C
A continuación se enumeran las secuencias de ARN correspondientes para las SEQ ID NO: 1-4 (SEQ ID NO: 7 10)
GACCCACUCUUGGUUUCCA (SEQ ID NO: 7) GGGGACUGCCGGGUGACCCUGGAAAUCCAGAGUGGGUGGGGCCAGUCUGACCGUUUCUAGGCG ACCCACUCUUGGUUUCCAGGGUUGCCCUGGAAA (SEQ ID NO: 8) GAAGACGGGAGGAAAGAAGGGAG (SEQ ID NO: 9) GAGGGGGAAGACGGGAGGAAAGAAGGGAGUGGUUCCAUCACGCCUCCUCACUCCUCUCCUCCCG UCUUCUCCUCUC (SEQ ID NO: 10)
Atenuación de CKB, SLC6a8
Se pidieron vectores pLKO que expresan horquillas de ARNhc que se dirigen a CKB y SLC6a8 a Sigma-Aldrich. Para todos los experimentos se usaron dos horquillas independientes que dieron la mejor atenuación de los niveles de transcripción. Estas secuencias de ADN y ARN en horquilla se enumeran a continuación en la Tabla 14:
Tabla 14. Secuencias de ADN y ARN en horquilla seleccionadas
Se usaron los siguientes cebadores para qRT-PCR cuantitativa de SLC6a8: Cebador directo: 5'-GGC AGC TAC AAC CGC TTC AAC A-3' y cebador inverso: 5'-CAG GAT GGA GAA GAC CAC GAA G-3 ' (SEQ ID NO:. 21 y 22, respectivamente).
Tratam iento con ciclocreatina y ácido beta-guanid iopropión ico
Se trató a los ratones con 10 mg de ciclocreatina o vehículo salino, administrados mediante inyección intraperitoneal. El régimen de tratamiento comenzó un día después de la inoculación de las células tumorales y
continuó hasta que se sacrificó a los ratones. Se administró ácido beta-guanidipropiónico a una dosis de 200 |jl de solución 0,5 M mediante inyección intraperitoneal. El régimen de tratamiento fue como el del tratamiento con ciclocreatina.
Ejem plo 1. Síntesis de inh ib idores del transporte de creatina y/o inh ib idores de creatina quinasa de la invención
Los compuestos de la invención pueden sintetizarse usando métodos conocidos en la técnica, por ejemplo usando los métodos descritos en las Patentes de Estados Unidos 5.321.030, 5.324.731, 5.955.617, 5.994.577 o 5.998.457 o los métodos descritos en M etabolism 1980, 29(7), 686, J. Med. Chem. 2001, 44, 1231, J. Biol. Chem.
1972, 247, 4382, J. Chem. Inf. Model. 2008, 48(3), 556 o J. Med. Chem. 2001, 44, 1217. Alternativamente, los compuestos de la invención pueden sintetizarse usando los métodos descritos a continuación.
A breviaturas
ACN Acetonitrilo
P-GPA ácido 3-guanidinopropiónico, es decir, ácido p-guanidinopropiónico
BINAP 2,2'-bis (difenilfosfino) -1,1'-binaftilo racémico
BLQ por debajo del nivel de cuantificación
Boc terc-butiloxicarbonilo
Br2 bromo
BrCN Bromuro de cianógeno
°C grados centígrados
ca. alrededor de o aproximadamente
CAN nitrato de amonio cérico
Cbz Carbobenciloxi
CH2Cl2 diclorometano
Cul Yoduro de cobre (I)
Cs2CÜ3 carbonato de cesio
D2O óxido de deuterio
DCC diciclohexilcarbodiimida
DCI diciclohexilcarbodiimida
DCM diclorometano o cloruro de metileno
DIPEA diisopropiletilamina
DMAP 4-dimetilaminopiridina o N,N-dimetilaminopiridina
DME 1,2-dimetoxietano
DMF N,N-dimetilformamida
DMSO dimetilsulfóxido
eq. equivalentes
ES(pos)MS espectrometría de masas en modo positivo por electropulverización
EtOAC acetato de etilo
EtOH etanol
Et2O éter dietílico
Fmoc cloruro de fluorenilmetiloxicarbonilo
g gramo(s)
HPLC cromatografía líquida de alto rendimiento
h hora
H2 gas hidrógeno
K2CO3 carbonato de potasio
K3 PO4 fosfato de potasio tribásico
KOH hidróxido de potasio
LC/MS espectrometría de masas de cromatografía líquida
LC/MS/MS espectrometría de masas en tándem de cromatografía líquida
LiOH hidróxido de litio
M molar
Mel yoduro de metilo
MeOH metanol
mg miligramo(s)
MgSO4 sulfato de magnesio
min. minuto(s)
ml mililitro(s)
mm milímetro(s)
mmol milimol(es)
MTS sulfato de 2-metil-2-tiopseudourea
m/z relación masa/carga
N normal
Na2S2O3 tiosulfato de sodio
Na2SO4 sulfato de sodio
NaH hidruro de sodio
NaHCO3 bicarbonato de sodio
Yoduro de sodio nal
NalO4 peryodato de sodio
NaOCH3 metóxido de sodio
NaOH hidróxido de sodio
NaNO2 nitrito de sodio
NBS N-bromosuccinimida
NMR resonancia magnética nuclear
PhthNK ftalimida de potasio
Pd/C paladio sobre carbono
Pd(OAc)2 acetato de paladio (II)
PdCl2 cloruro de paladio (II)
psi libras por pulgada cuadrada
PyBOP hexafluorofosfato de benzotriazol-1-il-oxi-tris-(dimetilamino)-fosfonio
RuCl3 hidrato de tricloruro de rutenio
SO2Cl2 cloruro de sulfurilo
SOCl2 cloruro de tionilo
TCl 1,1'-tiocarbonildiimidazol
TEA trietilamina
TFA ácido trifluoroacético
THF tetrahidrofurano
TLC cromatografía en capa fina
TPP trifenilfosfina
TSA ácido p-toluenosulfónico
Método general para elaborar análogos de ciclocreatina de la divulgación.
Los análogos de ciclocreatina pueden elaborarse a partir de ácidos o ésteres aminocarboxílicos y reacción con aziridinas en solventes inertes (por ejemplo, éter dietílico, THF, DME, etanol, DMF, THF, etc.). Estos productos intermedios de diamina se hacen reaccionar luego con bromuro de cianógeno en un solvente inerte (por ejemplo, éter dietílico, THF, DMF, etc.) para formar los productos deseados de iminoimidazolidina.
Método general para elaborar análogos de 1-carboximetil-2-iminohexahidropirimidina de la divulgación
Los análogos de iminohexahidropirimidina pueden elaborarse a partir de ácidos o ésteres ahalocarboxílicos y reacción con 1,3-diaminopropanos. Estos productos intermedios de diamina pueden hacerse reaccionar con bromuro de cianógeno en un solvente inerte (por ejemplo, éter dietílico, THF, DMF, etc.) para formar los productos deseados de iminohexahidropirimidina.
Método general para elaborar análogos de dihidrazinilimidazolidina y dihidrazinilhexahidropirimidina de la divulgación
Los análogos de dihidrazinilo pueden elaborarse a partir de ácidos o ésteres a-halocarboxílicos y reacción con derivados de hidrazinil alquil amino protegidos. Los derivados de hidrazinil alquil amino protegidos pueden elaborarse mediante reacción de trifluoroacetohidrazida con aziridinas o 1-azido-3-halopropano seguido de la reducción de azida posterior en condiciones estándar (por ejemplo, trifenilfosfina-acetona-agua). Estos productos intermedios de diamina pueden hacerse reaccionar con 1,1'-tiocarbonildiimidazol (TCl) en un solvente polar (por ejemplo, DMF, dioxano, etc.) para formar imidazolidinetionas o tetrahidro-2-pirimidinotionas. La activación con haluro de alquilo (por ejemplo, yoduro de metilo) y la posterior reacción con hidrazina escinde el grupo protector de trifluoroacetamida y proporcionaría los productos deseados.
Método general para elaborar análogos de 2-hidrazinilimidazolidina y 2-hidrazinilhexahidropirimidina de la divulgación
Los productos intermedios de éster o ácido diaminocarboxílico generados anteriormente pueden hacerse reaccionar con 1,1-tiocarbonildiimidazol (TCl) en un solvente polar (por ejemplo, DMF, dioxano, etc.) para formar imidazolidinetionas o tetrahidro-2-pirimidinetionas. La activación con haluro de alquilo (por ejemplo, yoduro de metilo) y la reacción posterior con hidrazina proporcionarían los productos deseados.
Método general para elaborar análogos de aminoiminoimidazolidina y aminoiminohexahidropirimidina de la divulgación
Los análogos de aminoiminoimidazolidina y aminoiminohexahidropirimidina pueden elaborarse a partir de ácidos o ésteres a-halocarboxílicos y reacción con azirindas o azetidinas, respectivamente. Estas a-carboxiaziridinas o azetidinas se abren con bromuro de cianógeno para formar productos intermedios de bromuro de alquilo de cianamida (ver J. Org. Chem. 1949, 14, 605 y J. Am. Chem. Soc. 2013, 135(41), 15306). La reacción con hidrazina proporcionaría los productos cíclicos deseados.
Método general para elaborar análogos de imino-1,2,4-triazinanos de la divuglación
Los análogos de imino-1,2,4-triazinanos pueden elaborarse a partir de ácidos o ésteres a-halocarboxílicos y reacción con derivados de hidrazinil alquil azido protegidos. Los derivados de hidrazinil alquil azida protegidos con PMB pueden elaborarse como se describe en Org. Biomol. Chem. 2012, 10(30), 5811. La azida se reduce en condiciones estándar (por ejemplo, trifenilfosfina-acetona-agua) y la diamina resultante se trata con bromuro de
cianógeno para formar el núcleo cíclico. La desprotección del grupo protector de hidrazina PMB en condiciones estándar (por ejemplo, CAN, ácido fuerte, etc.) proporcionaría el producto deseado.
Síntesis del compuesto 225
Se disuelve alanina (2,0 mmol) en eter dietilico (10 ml) y se anade aziridina (2,0 mmol). La mezcla se calienta a reflujo durante 2 h y se enfría a temperatura ambiente. Se añade bromuro de cianógeno (2,3 mmol) y la reacción se agita a temperatura ambiente durante la noche. El precipitado se filtra y se lava con éter dietílico para proporcionar ácido 2-(2-iminoimidazolidin-1-il)propanoico (225).
Los compuestos 226-228 pueden sintetizarse usando métodos similares a los usados para elaborar el compuesto 225 reemplazando la alanina con ácido a-aminobutanoico, valina o isoleucina.
Síntesis del compuesto 237
Se disuelve ácido 2-cloropropiónico (2,0 mmol) en éter dietílico y se añade 1,3-diaminopropano (2,0 mmol). La reacción se agita durante la noche a temperatura ambiente y el precipitado se filtra y se lava con éter dietílico para proporcionar la sal de HCl del ácido 2-[(3-aminopropil)amino]propanoico. La sal se disuelve en agua y se añade carbonato de sodio (2,5 mmol) seguido de bromuro de cianógeno (2,3 mmol). La reacción se agita a temperatura ambiente durante la noche. La reacción se neutraliza con ácido trifluoroacético y la mezcla se concentra a presión reducida. El residuo se purifica mediante cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) y el producto se recoge y liofiliza para producir la sal de trifluoroacetato del ácido 2-(2-imino-1,3-diazinan-1-il)propanoico. (237).
Los compuestos 238-240 pueden sintetizarse usando métodos similares a los usados para elaborar el compuesto 237 reemplazando el ácido 2-cloropropanoico por ácido 2-clorobutanoico, ácido 2-cloro-3-metilbutanoico o ácido 2-cloro-3-metilpentanoico.
Síntesis del compuesto 229
Paso 1: 2-ácido {[2-(trifluoroacetohidrazido)etil]amino} acético (INT-1)
Se disuelven trifluoroacetohidrazida (2,0 mmol) y aziridina (2,0 mmol) en éter dietílico (5 ml) y se agita a temperatura ambiente durante la noche. Se añade ácido 2-cloroacético (2,0 mmol) y la mezcla se agita 3 h a temperatura ambiente. El precipitado se filtra y se lava con éter dietílico para proporcionar INT-1.
Paso 2: ácido 2-[2-sulfaniliden-3-(trifluoroacetamido)imidazolidin-1-il]acético (INT-2)
Se disuelve diamina INT-1 (1,5 mmol) en DMF (5 ml) y se hace reaccionar con 1,1'-tiocarbonildiimidazol (1,5 mmol) a temperatura ambiente durante 3 h. La reacción se vierte en HCl acuoso 0,1 N, la capa acuosa se extrae con acetato de etilo, la capa orgánica se seca sobre sulfato de sodio, se concentra a presión reducida y se purifica mediante cromatografía en columna de gel de sílice (metanol-diclorometano 10-90) para producir INT-2.
Paso 3: ácido 2-[3-amino-2-hidrazinilidenimidazolidin-1-il]acético (229)
Se disuelve INT-2 (1,0 mmol) en etanol (5 ml) y se añade yoduro de metilo (1,0 mmol). La mezcla se agita durante 1 h a temperatura ambiente. Una vez completada, se añade hidrazina (5 mmol) y la mezcla se calienta a reflujo durante 8 h. La mezcla se concentra para eliminar el exceso de hidrazina, el residuo se purifica mediante cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) y el producto se recoge y liofiliza para producir la sal de trifluoroacetato de ácido 2-[3-amino-2-hidrazinilidenimidazolidin-1-il]acético (229).
Los compuestos 230-228 y 241-243 pueden sintetizarse usando métodos similares a los usados para elaborar el compuesto 229 reemplazando el ácido cloroacético con ácido 2-cloroacético, ácido 2-cloropropanoico o ácido 2-cloro-3-metilbutanoico. Para sintetizar los compuestos 241-243, la aziridina puede reemplazarse con 1,3-dibromopropano.
Síntesis del compuesto 232
Se disuelve ácido 2-cloropropiónico (2,0 mmol) en éter dietílico y se añade aziridina (2,0 mmol). La reacción se agita durante la noche a temperatura ambiente y el precipitado se filtra y se lava con éter dietílico para producir la sal de HCl del ácido 2-(aziridin-1-il)propanoico. La sal se disuelve en agua, se añade carbonato de sodio (2,5 mmol) seguido de bromuro de cianógeno (2,3 mmol) y la reacción se agita a temperatura ambiente durante la noche. La reacción se neutraliza con ácido trifluoroacético y la mezcla se concentra a presión reducida. El residuo se purifica mediante cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) y el producto se recoge y liofiliza para producir la sal de trifluoroacetato de ácido 2-(3-amino-2-iminoimidazolidin-1-il)propanoico (232).
Los compuestos 233 y 244-246 pueden sintetizarse usando métodos similares para preparar el compuesto 232 reemplazando el ácido 2-cloropropanoico con ácido 2-cloroacético o ácido 2-cloro-3-metilbutanoico. Para sintetizar los compuestos 244-246, la aziridina puede reemplazarse con azetidina.
Síntesis del compuesto 234
Paso 1: ácido 2-(2-sulfanilidenimidazolidin-1-il)acético (INT-3)
Se disuelve glicina (2 mmol) en éter dietílico (10 ml) y se añade aziridina (2 mmol). La mezcla se calienta a reflujo durante 2 h y se enfría a temperatura ambiente. La mezcla se concentra a presión reducida, se disuelve en DMF (5 ml) y se hace reaccionar con 1,1'-tiocarbonildiimidazol (1,5 mmol) a temperatura ambiente durante 3 h. La reacción se vierte en HCl acuoso 0,1 N, la capa acuosa se extrae con acetato de etilo, la capa orgánica se seca sobre sulfato de sodio, se concentra a presión reducida y se purifica mediante cromatografía en columna de gel de sílice (metanol-diclorometano 10-90) para producir INT-3.
Paso 2: ácido 2-[2-hidrazinilidenimidazolidin-1-il]acético (234)
Se disuelve INT-3 (1,0 mmol) en etanol (5 ml) y se añade yoduro de metilo (1,0 mmol). La mezcla se agita durante 1 h a temperatura ambiente. Una vez completada, se añade hidrazina (5 mmol) y la mezcla se calienta a reflujo durante 8 h. La mezcla se concentra hasta un exceso de hidrazina ambiente, el residuo se purifica mediante cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) y el producto se recoge y liofiliza para proporcionar la sal de trifluoroacetato de ácido 2-[2-hidrazinilidenimidazolidin-1-il]acético (234).
Los compuestos 235-336 pueden sintetizarse usando métodos similares para preparar el compuesto 234 reemplazando glicina con alanina o valina. Los compuestos 247-349 pueden sintetizarse usando métodos similares para elaborar el producto intermedio de diamina para el compuesto 237 y luego siguiendo el protocolo para elaborar 234.
Síntesis del compuesto 250
Paso 1: 1-(2-azidoetil)-1-[(4-metoxifenil)metil]hidrazina (INT-4)
La síntesis de hidrazinil etil azida protegida con PMB se prepara como se describe en Org. Biomol. Chem.
2012, 10(30), 5811.
Paso 2: ácido 2-[2-(2-aminoetil)-2-[(4-metoxifenil)metil]hidrazin-1-il]acético (INT-5)
Se disuelve ácido 2-cloropropiónico (2,0 mmol) en éter dietílico (5 ml) y se añade INT-4 (2,0 mmol). La reacción se agita durante la noche a temperatura ambiente y el precipitado se filtra y se lava con éter dietílico para producir la sal de HCl. La sal se disuelve en agua-acetona (1:10, 5 ml) y se añade trifenilfosfina (TPP). La mezcla se calienta a 50° C durante 14 horas.
Paso 3: ácido 2-(3-imino-1,2,4-triazinan-2-il)acético (250)
Se disuelve INT-5 (1,0 mmol) en agua, se añade carbonato de sodio (2,5 mmol) seguido de bromuro de cianógeno (1,3 mmol) y la reacción se agita a temperatura ambiente durante la noche. La reacción se inactiva con ácido trifluoroacético y la mezcla se concentra a presión reducida. El residuo se purifica mediante cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) y el producto se recoge y liofiliza para proporcionar la sal de trifluoroacetato de ácido 2-(3-imino-1,2,4-triazinan-2-il)acético (250).
Los compuestos 251-252 pueden sintetizarse usando métodos similares para elaborar el compuesto 250 reemplazando el ácido 2-cloroacético con ácido 2-cloropropanoico o ácido 2-cloro-3-metilbutanoico.
Método general para elaborar compuestos que contienen guanidina de la divulgación
Las guanidinas se elaboran a partir de aminas usando agentes de guanilación estándar (por ejemplo, sulfato de 2-metil-2-tiopseudourea [MTS], cianamida, N,N-di-Boc-1H-pirazol-1-carboxamida, etc.). Un método preferido que usa MTS se describe en J. Med. Chem. 2001,44, 1217, J. Chem. Soc. C 1971, 238 y Tetrahedron Lett.
1996, 37, 2483. Brevemente, las aminas se disuelven o suspenden en un solvente alcohólico acuoso básico y se hacen reaccionar con sulfato de 2-metil-2-tiopseudourea (MTS) durante 24-72 h o más y los productos precipitados se aíslan por filtración. Si es necesario, la hidrólisis del éster se realiza mediante tratamiento con ion de hidróxido (por ejemplo, LiOH, NaOH, KOH, etc.) en un solvente alcohólico acuoso o THF, para producir el producto deseado.
W es uno o dos grupos protectores (Boc o Cbz)
En algunos casos, las guanidinas se elaboran a partir de aminas en condiciones anhidras usando agentes guanilantes activados por pirazol (por ejemplo, clorhidrato de 1H-pirazol-1-carboxamidina, nitrato de 3,5-dimetil-1-pirazolilformaminidio, N-Boc-1H-pirazol-1-carboxamidina, N,N'-di-Boc-1H-pirazol-1-carboxamidina, N-(benciloxicarbonil)-1H-pirazol-1-carboxamidina y N,N'-bis(benciloxicarbonil)-1H-pirazol-1-carboxamidina). Los métodos para usar agentes guanilantes activados por pirazol se revisan en Eur. J. Org. Chem. 2002, 3909. Brevemente, las aminas se usan en exceso o con una base (por ejemplo, trietilamina, diisopropiletilamina, etc.) y se disuelven en solvente (por ejemplo, DMF, acetonitrilo, THF, metanol, diclorometano, etc.). La reacción se agita durante 4-72 h y a temperatura ambiente, pero en algunos casos se requiere calentamiento. Cuando se usan agentes guanilantes activados por pirazol protegidos (es decir, W = BoCo Cbz), los productos pueden purificarse mediante cromatografía en columna de gel de sílice en fase normal. Si es necesario, la hidrólisis del éster se realiza mediante tratamiento con ion de hidróxido (por ejemplo, LiOH, NaOH, KOH, etc.) en un solvente alcohólico acuoso o THF, para proporcionar el ácido carboxílico. Finalmente, se usan condiciones de desprotección estándar para eliminar los grupos protectores de guanidina (es decir, eliminación de TFA de Boc o hidrogenación de Cbz) para proporcionar el producto deseado.
W es uno o dos grupos de protección (Boc o Cbz)
En otros casos, se usan aminoalcoholes con el método anterior. Después de la guanilación, el alcohol se oxida al ácido carboxílico usando metaperyodato de sodio y cloruro de rutenio (III) (catalítico) en acetonitrilo, acetato de etilo y agua (Org. Lett. 2008, 10, 5155). Finalmente, se usan condiciones de desprotección estándar para eliminar los grupos protectores de guanidina (es decir, eliminación de TFA de Boc o hidrogenación de Cbz) para proporcionar el producto deseado.
Método general para elaborar compuestos que contienen 2-aminopiridina de la divulgación
Las aminopiridinas pueden elaborarse usando métodos de acoplamiento cruzado como se describe en J. Am. Chem. Soc. 2008, 130(20), 6586 y J. Org. Chem. 1996, 61(21), 7240. Brevemente, se disuelven o suspenden aminas, 2-halopiridinas y una base suficiente (por ejemplo, carbonato de cesio, terc-butóxido de potasio, etc.) en un solvente polar (por ejemplo, DMF, dioxano), luego pueden añadirse paladio catalítico (por ejemplo PdCb o Pd(OAc)2) y ligando de fosfina (por ejemplo, BINAP), y la reacción se calienta a más de 80° C durante 4-6 h. Si es necesario, la hidrólisis del éster por tratamiento con ion de hidróxido (por ejemplo, LiOH, NaOH, KOH, etc.) en un solvente alcohólico acuoso o THF, proporciona el producto deseado.
Alternativamente, se usan métodos de acoplamiento cruzado de amidas de Buchwald para generar compuestos deseados como se describe en ver J. Am. Chem. Soc. 2002, 124, 11684 y J. Am. Chem. Soc. 2001, 123, 7727. Brevemente, las aminas se protegen como amidas o carbamatos (por ejemplo, trifluoroacetamida, Boc, Cbz, etc.) y se hacen reaccionar con 2-bromopiridina en un solvente polar (por ejemplo, dioxano, DMF) con una base (por ejemplo, fosfato de potasio tribásico, carbonato de cesio, terc-butóxido de potasio, etc.), ligando de trans-1,2-diaminociclohexano racémico y yoduro de cobre (I) catalítico. La solución se desgasifica durante 5 minutos burbujeando gas nitrógeno directamente en la solución y la mezcla se calienta a más de 95° C durante 6-12 horas. Los grupos protectores de amina se eliminan usando condiciones estándar y, si es necesario, la hidrólisis del éster por tratamiento con ion de hidróxido (por ejemplo, LiOH, NaOH, KOH, etc.) en un solvente alcohólico acuoso o THF, proporciona el producto deseado.
Método general para elaborar pseudotiourea que contiene compuestos de la divulgación
r x z = n h A c e to n a , re flu jo
N a N 02, 5 N H B r x = C l o r B r
Las pseudotioureas pueden elaborarse mediante la reacción de una tiourea con haluros de alquilo como se describe en J. Med. Chem. 2001, 44, 1217. Brevemente, los ácidos o ésteres 3-cloropropiónicos pueden hacerse reaccionar con tiourea en un solvente polar (por ejemplo, acetona) seguido de reflujo de la mezcla durante 48 h. Los ácidos o ésteres 3-cloropropiónicos pueden elaborarse mediante la reacción de ácidos 3-hidroxipropiónicos con cloruro de tionilo como se describe en la Publicación de Patente Internacional N° WO9933785.
Alternativamente, las pseudotioureas pueden elaborarse a partir de compuestos de amino mediante bromuros de alquilo usando métodos como los descritos en Tetrahedron: A sym m etry 1998, 9(10), 1641 y la Publicación de Patente Internacional N° WO2002009705. Brevemente, los ácidos o ésteres 3-aminocarboxílicos pueden convertirse en ácidos o ésteres 3-bromocarboxílicos mediante activación con nitrito de sodio en presencia de ácido bromhídrico. El compuesto de bromo resultante puede hacerse reaccionar con una tiourea en un solvente adecuado (por ejemplo, tolueno o acetona) a más de 60° C durante 4-24 h. Si es necesario, la hidrólisis del éster por tratamiento con ion de hidróxido (por ejemplo, LiOH, NaOH, KOH, etc.) en un solvente alcohólico acuoso proporcionaría el producto deseado.
Método general para elaborar compuestos que contienen 2-aminopseudotiourea de la divulgación
Las 2-aminopseudotioureas pueden elaborarse a partir de aziridinas mediante métodos similares a los descritos en Chem. Comm. 2000, 7, 619 y Org. Biomol. Chem. 2005, 3(18), 3357. Brevemente, las N-Cbz-2-carboxiaziridinas pueden hacerse reaccionar con tiourea y borotrifluoruro-eterato en un solvente inerte (por ejemplo, cloroformo, diclorometano, etc.). La hidrogenación posterior en presencia de paladio sobre carbono y, si es necesario, la hidrólisis del éster por tratamiento con ion de hidróxido (por ejemplo, LiOH, NaOH, KOH, etc.) en un solvente alcohólico acuoso, proporcionaría el producto deseado. Las 2-carboxiaziridinas pueden elaborarse mediante métodos como se describe en Synlett 2001, 5, 679 y Tetrahedron Lett. 2006, 47(13), 2065 y pueden convertirse en aziridinas protegidas con Cbz mediante métodos estándar.
Muchos materiales de partida para los compuestos de la invención están disponibles comercialmente o se conocen métodos de síntesis en la bibliografía. La Tabla 15 enumera los materiales de partida para la síntesis de los compuestos de la invención y proporciona referencias bibliográficas para reactivos poco comunes.
Tabla 15. Materiales de partida para la síntesis de los compuestos seleccionados
(continuación)
continuación
continuación
continuación
continuación
(continuación)
(continuación)
Síntesis del compuesto 219
Se suspendieron ácido (R)-aminobutírico SM01 (750 mg, 7,27 mmol) y sulfato de 2-metil-2-tiopseudourea (MTS, 1,21 g, 4,36 mmol) en metanol (4 ml). Después de la adición de hidróxido de sodio 3 N en agua (2,62 ml, 1,09 eq.), la solución transparente se agitó durante 3 días a temperatura ambiente. Posteriormente, el precipitado blanco se filtró y se lavó con agua/metanol (15 ml, 1/2). El polvo blanco se secó al aire durante 1 hora y luego se puso a alto vacío durante 2 días para producir el ácido (3R)-3-carbamimidamidobutanoico (219) como un sólido blanco (879 mg, 83%); 1H-NMR (300 MHz, D2O): 83.81 (m, 1H), 2.31 (m, 2H), 1.15 (d, 3H); ES(pos)MS m/z 146.1 (M+H+).
Síntesis del compuesto 220
El ácido (S)-aminobutírico SM02 (750 mg, 7,27 mmol) se convirtió en el ácido (3S)-3-carbamimidamidobutanoico (220) correspondiente de acuerdo con el procedimiento para el compuesto 219. El producto deseado se obtuvo como un polvo blanco después de secado a alto vacío durante 3 días (756 mg, 72%); 1H-NMR (300 MHz, D2O): 83.84 (m, 1H), 2.35 (m, 2H), 1.18 (d, 3H). ES(pos) MS m/z 145.9 (M+H+).
Síntesis del compuesto 221
Se agita una suspensión de ácido (2S,3R) -2,3-diaminobutanoico SM71 (25 mmol) y sulfato de 2-metil-2-tiopseudourea (MTS, 25 mmol) en metanol (25 ml) durante 5 días a temperatura ambiente bajo una atmósfera de nitrógeno. Después, la reacción se enfría a 0° C, se filtra a través de una frita de vidrio de porosidad media y el sólido recogido se lava con agua y se seca para proporcionar el compuesto 221 como una mezcla de regioisómeros. El material se purifica mediante cromatografía HPLC preparativa y el producto se recoge y se liofiliza para producir el compuesto 221.
Síntesis del compuesto 223
Se disuelven 2-cloro-piridina (25 mmol), acetato de paladio (II) (2,5 mmol), 2,2'-bis(difenilfosfino)-1,1’-binaftilo racémico (2,5 mmol) y carbonato de cesio (65 mmol). en tolueno (75 ml) en un recipiente sellado previamente desgasificado. La mezcla se enjuaga con nitrógeno gaseoso. Se añade metil-(R)-3-aminobutirato SM01 (20 mmol) a la solución bajo nitrógeno y la mezcla sellada se calienta durante la noche a 100° C. La reacción se enfría a temperatura ambiente, se diluye con éter dietílico y se lava con tampón pH 7 y agua. La capa orgánica se concentra y se purifica mediante cromatografía en columna de gel de sílice (10:90 metanol-diclorometano) para producir ácido (3R)-3-[(piridin-2-il)amino]butanoico (223).
Síntesis del compuesto 257
Paso 1: (1H-1,2,3-benzotriazol-1-ilmetil)dibencilamina (INT-6)
El hidroximetilbenztriazol (10,4 g, 69,7 mmol) y la dibencilamina (13,4 ml, 69,7 mmol) se convirtieron en INT-6 (rendimiento del 95%) de acuerdo con el protocolo de la US2009/054414.
Paso 2: 3-(dibencilamino)-2,2-difluoropropanoato de etilo (INT-7)
Se acoplaron bromodifluoro acetato de etilo (4,8 g, 23,65 mmol) e INT-6 (7,78 g, 23,7 mmol) de acuerdo con el protocolo de la US2009/054414 para proporcionar INT-7 (53% de rendimiento).
Paso 3: sal de TFA de 3-amino-2,2-difluoropropanoato de etilo (INT-8)
Se disolvió el INT-7 (1,52 g, 4,59 mmol) en etanol (25 ml). Se añadió ácido trifluoroacético (0,372 ml, 4,85 ml) y una cantidad catalítica de hidróxido de paladio sobre carbono y la reacción se sometió a hidrógeno a presión atmosférica durante 16 h. Posteriormente, el catalizador se eliminó mediante filtración a través de celite y se lavó con etanol. El filtrado resultante se evaporó a presión reducida y el residuo se trató con tolueno (50 ml) y se concentró, esto se repitió dos veces para eliminar el solvente residual y el exceso de agua. El residuo se secó a alto vacío durante la noche para proporcionar el INT-8 como un aceite amarillento (usado como bruto en el siguiente paso).
Paso 4: 3-{[(14-{[(terc-butoxi)carbonil]amino}({[(terc-butoxi)carbonil]imino})metil]amino}-2,2-difluoropropanoato de etilo (INT-9)
La sal bruta de TFA de INT-8 se disolvió en THF seco (10 ml) y luego se trató con trietilamina (1,36 ml, 9,73 mmol) y N,N'-di-Boc-1H-pirazol-1-carboxamidina (1,57 g, 5,05 mmol). Después de agitar durante la noche a temperatura ambiente, la mezcla de la reacción se vertió en acetato de etilo (200 ml) y luego se lavó con agua (2 x 100 ml) ajustando el pH de la capa acuosa a pH 1-2 usando HCl 1N. Luego, los lavados acuosos combinados se volvieron a extraer con acetato de etilo (100 ml). La segunda fase orgánica se lavó a su vez con agua acidificada (100 ml) usando HCl 1 N para ajustar el pH a 1-2. Las fases orgánicas combinadas se secaron sobre sulfato de magnesio, se filtraron, se evaporaron y se purificaron mediante cromatografía en columna de gel de sílice para producir INT-9 como un aceite viscoso que solidificó tras reposar (1,25 g, 70% para dos pasos); 1H-NMR (300 MHz, DMSO-d6): 811.42 (s, 1H). 8.60 (t, 1H), 4.26 (q, 2H), 4.05 (td, 2H), 1.49 (s, 9H), 1.39 (s, 9H), 1.26 (t, 3H).
Paso 5: Compuesto 257
Se disuelve INT-9 (0,5 g) en THF (5 ml) y se añade LiOH 1 N (2,5 ml). Una vez que se ha completado la hidrólisis del éster, la mezcla se concentra al vacío y el residuo se disuelve en ácido trifluoroacético-diclorometano 1:4 (5 ml). La mezcla se agita a temperatura ambiente durante la noche para eliminar los grupos protectores de Boc. La mezcla se concentra al vacío, el residuo se purifica mediante cromatografía HPLC preparativa y el producto se recoge y se liofiliza para producir el compuesto 257. Alternativamente, el éster en INT-8 se hidroliza usando hidróxido de litio para elaborar SM05 y el aminoácido resultante se guanilada usando clorhidrato de 1H-pirazol-1-carboxamidina y diisopropiletilamina en DMF como se muestra a continuación para el compuesto 261.
Síntesis del compuesto 258
Se suspendió ácido 3-azetidinacarboxílico SM06 (2,0 g, 19,8 mmol) en agua (2 ml) y luego se trató con una solución de hidróxido de sodio 10 N en agua (1,96 ml, 19,6 mmol). La solución espesa de color amarillento se trató luego con cianamida sólida (1,01 g, 24 mmol) y la mezcla se volvió sólida al instante. Se añadió más agua (5 ml) para asegurar una agitación adecuada y luego se agitó la suspensión a temperatura ambiente durante 3 días. Posteriormente, se filtró el sólido blanco, se lavó con agua fría (10 ml, 0° C) y luego se secó al aire durante 2 horas. El secado a alto vacío durante 2 días proporcionó el compuesto 258 como un sólido blanco (1,48 g, 52%); 1H-NMR (300 MHz, D2O): 84.19 (t, 2H), 4.07 (dd, 2H), 3.34 (m, 1H); ES(pos) MS m/z 143.9 (M+H+).
Síntesis del compuesto 261
Se disolvieron ácido 3-amino-4,4,4-trifluorobutírico SM07 (500 mg, 3,18 mmol) y diisopropiletilamina (1,16 ml, 6,68 mmol) en DMF seca (3 ml). Después de la adición de clorhidrato de 1H-pirazol-1-carboxamidina (593 mg, 3,50 mmol), la mezcla de reacción se agitó durante 20 días a temperatura ambiente. El precipitado se separó por filtración, se lavó con metanol/agua (2/1, 15 ml) y se secó al aire. El secado a alto vacío durante la noche proporciona el compuesto 261 deseado en forma de un polvo blanco (135 mg, 21%); 1H-NMR (300 MHz, D2O): 8 4.09 (m, 1H), 2.47 (dd, 1H), 2.22 (dd, 1H); ES(pos) MS m/z 200.07 (M+H+).
Síntesis del compuesto 275
Se agita tiourea (100 mmol) y clorhidrato de p-cloro-D-alanina SM66 (100 mmol) en acetona (22 ml) a reflujo durante 48 h. Se añade acetona (aproximadamente 150 ml) y la mezcla se agita vigorosamente para promover la solidificación. El sólido se descompone, se agita hasta que está fino, se filtra bajo nitrógeno y se lava con acetona. El sólido bruto se disuelve en 2-propanol caliente (120 ml) y se diluye con éter dietílico hasta que se enturbia (80 ml) y se cristaliza para producir ácido (2R)-2-amino-3-(carbamimidoilsulfanil)propanoico (275).
Síntesis del compuesto 278
A un matraz se le añade ácido cis-2-aminociclobutano-1-carboxílico (18,8 mmol) y 24,5 ml de ácido bromhídrico 5 N. La reacción se enfría en un baño de hielo a 0-5°C, seguido de la adición gota a gota de nitrito de sodio (30,1 mmol) en 7,5 ml de agua durante cinco horas. La temperatura se mantiene por debajo de 5° C durante la adición. Una vez completada la adición, la reacción se agita durante 12 horas a temperatura ambiente. La reacción se diluye con éter dietílico (15 ml), la capa acuosa se elimina y la fase orgánica se lava con ácido clorhídrico 1 N (15 ml). Las capas acuosas combinadas se lavan con acetato de etilo (10 ml) y los extractos orgánicos combinados se secan sobre sulfato de magnesio, se filtran y se concentran a presión reducida.
A una suspensión de tiourea (15 mmol) en tolueno (50 ml) en un baño de aceite a 60° C se le añade ácido trans-2-bromociclobutano-1-carboxílico (2,5 mmol). La reacción se agita a 60° C durante 5 h. Luego, se elimina el tolueno a presión reducida y el residuo resultante se diluye con agua (25 ml) y ácido clorhídrico 1 N (30 ml), para lograr un pH de 1-1,5. La mezcla se agita a temperatura ambiente durante 1-2 horas y luego se extrae con acetato de etilo (3 x 50 ml). Las capas orgánicas combinadas se secan sobre sulfato de magnesio, se filtran y se concentran a presión reducida. El sólido resultante se disuelve en agua (3,0 ml) y se filtra a través de un filtro de nailon de 0,2 pm. El filtrado se purifica mediante HPLC preparativa (por ejemplo, columna de compresión Waters PrepPak cartucho Delta-Pak C18, 15 pm 25 x 100 mm, 95:5 agua-acetonitrilo a 12,0 ml/min). El producto se recoge y liofiliza para proporcionar el producto ácido cis-2-(carbamimidoilsulfanilo)ciclopropano-1-carboxílico (278).
Síntesis del compuesto 286
Paso 1: 1-bencil 2-metil 3-(trifluorometil)aziridina-1,2-dicarboxilato (INT-10)
La INT-10 puede elaborarse mediante métodos como los descritos en Synlett 2001, 5, 679 y Tetrahedron Lett. 2006, 47 (13), 2065 y se convirtió en una aziridina protegida con Cbz mediante métodos estándar (ver Org. Biomol. Chem. 2005, 3 (18), 3357).
Paso 2: 2-{[(benciloxi)carbonil]amino}-3-(carbamimidoilsulfanil)-4,4,4-trifluorobutanoato de metilo (INT-11)
Se disuelve INT-10 (1,0 mmol) en diclorometano (10 ml) y la mezcla se enfría a 0° C. Se añade gota a gota borotrifluoruro-eterato (1,0 mmol, diclorometano 1 M) y la reacción se calienta a temperatura ambiente. La reacción se vierte en HCl acuoso 0,1 N, la capa acuosa se extrae con acetato de etilo, la capa orgánica se seca sobre sulfato de sodio, se concentra a presión reducida y se purifica mediante cromatografía en columna de gel de sílice (metanoldiclorometano 10-90) para producir INT-11.
Paso 3: ácido 2-amino-3-(carbamimidoilsulfanil)-4,4,4-trifluorobutanoico (286)
Se disuelve INT-11 (0,5 mmol) en metanol, se añade paladio al 10% sobre carbono (Pd/C 10% en moles) y el matraz se purga al vacío con gas hidrógeno 5 veces. La mezcla se agita vigorosamente a temperatura ambiente bajo una atmósfera de hidrógeno durante 16 h. Se usa gas nitrógeno para purgar el matraz y la mezcla se filtra a través de Celite para eliminar el Pd/C. La mezcla se concentra a presión reducida y el residuo se trata con hidróxido de sodio 1 N en metanol. Una vez que se ha completado la hidrólisis del éster, la mezcla se concentra de nuevo a presión reducida y el residuo resultante se disuelve en agua (3,0 ml) y se filtra a través de un filtro de nailon de 0,2 |jm. El filtrado se purifica mediante HPLC preparativa (por ejemplo, columna de compresión Waters PrepPak cartucho Delta-Pak C18, 15 jm 25 x 100 mm, 95:5 agua-acetonitrilo a 12,0 ml/min). El producto se recoge y liofiliza para proporcionar el producto ácido 3-(carbamimidoilsulfanil)-4,4,4-trifluorobutanoico (286).
Síntesis del compuesto 358
El ácido aminopentanoico SM37 (500 mg, 4,27 mmol) se convirtió en el derivado de guanidino correspondiente de acuerdo con el procedimiento para el compuesto (219). El compuesto 358 deseado se obtuvo como un polvo blanco después de un secado a alto vacío (291 mg, 43%); 1H-NMR (300 MHz, D2O): 83.63 (m, 1H), 2.39 (dd, 1H), 2.29 (dd, 1H), 1.52 (m, 2H), 0.85 (t, 3H); ES(pos) MS m/z 160.11 (M+H+).
Síntesis del compuesto 376
Se convirtió clorhidrato de ácido pirrolidin-3-carboxílico (500 mg, 3,30 mmol) en el derivado deseado (376) de acuerdo con un procedimiento modificado descrito para el compuesto 258 en el que se aumentó la cantidad de base para neutralizar la sal de HCl del material de partida. El material final se aisló como un polvo blanco (198 mg, 38%); 1H-NMR (300 MHz, D2O): 8 3.4 (m, 4H), 2.99 (m, 1H), 2.17 (m, 1H), 2.03 (m, 1H); ES(pos) MS m/z 158.09 (M+H+).
Síntesis del compuesto 366
Paso 1: N-[(1Z)-{[(terc-butoxi)carbonil]imino}[(3-hidroxi-2,2-dimetilpropil)amino]metil]carbamato de terc-butilo (INT-12)
Se disolvió 3-amino-2,2-dimetilpropanol SM45 (464 mg, 4,5 mmol) en THF seco (7 ml) y luego se trató con N,N'-di-Boc-1H-pirazol-1-carboxamidina (1,24 g, 4,0 mmol). Después de agitar durante 72 horas a temperatura ambiente, la mezcla de la reacción se vertió en acetato de etilo (200 ml) y luego se lavó con agua (2 x 100 ml) ajustando el pH de la capa acuosa a pH 1-2 usando HCl 1N. Luego, los lavados acuosos combinados se volvieron a extraer con acetato de etilo (100 ml). La segunda fase orgánica se lavó a su vez con agua acidificada (100 ml) usando HCl 1 N para ajustar el pH a 1-2. Las fases orgánicas combinadas se secaron sobre sulfato de magnesio, se filtraron, se evaporaron y se purificaron mediante cromatografía en columna de gel de sílice para producir INT-12 como un aceite viscoso que solidificó al reposar (1,32 g, 96%); 1H-NMR (300 MHz, DMSO-d6): 8 11.48 (s, 1H). 8.55 (t, 1H), 4.93 (t, 1H), 3.18 (d, 2H), 3.13 (d, 2H), 1.48 (s, 9H), 1.39 (s, 9H), 0.82 (s, 6H).
Paso 2: ácido 3-{[(1Z)-{[(terc-butoxi)carbonil]amino}({[(terc-butoxi)carbonil]imino})metil]amino}-2,2-dimetilpropanoico (INT-13)
Se disolvió INT-12 (1,30 g, 3,76 mmol) en acetonitrilo (25 ml), tetracloruro de carbono (25 ml) y agua (40 ml). Se añadieron peryodato de sodio (4,83 g, 22,6 mmol) y tricloruro de rutenio (50 mg, catalítico) y la mezcla se agitó durante 3 h a temperatura ambiente o hasta que la TLC mostró que se había consumido el material de partida. La mezcla bifásica resultante se vertió en acetato de etilo (200 ml) y luego se lavó con agua (2 x 100 ml) ajustando el pH de la capa acuosa a pH 1-2 usando HCl 1N. Luego, los lavados acuosos combinados se volvieron a extraer con acetato de etilo (100 ml). La segunda fase orgánica se lavó a su vez con agua acidificada (100 ml) usando HCl 1 N para ajustar el pH a 1-2. Las fases orgánicas combinadas se secaron sobre sulfato de magnesio, se filtraron, se evaporaron y se purificaron mediante cromatografía en columna de gel de sílice para producir INT-13 como una espuma sólida (1,05 g, 78%); 1H-NMR (300 MHz, DMSO-d6): 8 11.47 (s, 1H). 8.53 (t, 1H), 3.42 (d, 2H), 1.47 (s, 9H), 1.39 (s, 9H), 1.13 (s, 6H).
Paso 3: Compuesto 366
INT-14 se disuelve en ácido trifluoroacético-diclorometano 1: 4 (5 ml). La mezcla se agita a temperatura ambiente durante la noche para eliminar los grupos protectores de Boc. La mezcla se concentra al vacío y el residuo se purifica mediante cromatografía HPLC preparativa para producir el compuesto 366.
Además de los compuestos descritos anteriormente, se usan protocolos similares para elaborar numerosos análogos que se muestran en la Tabla 16 a partir de los materiales de partida enumerados en la Tabla 15.
Tabla nados
continuación
continuación
continuación
Esquema genérico para fabricar sulfanil N-amidino profármacos
Los profármacos de sulfanil N-amidino pueden sintetizarse en varios pasos a partir de homodisulfuros a través de N-alquiltiol-ftaMmida. Los disulfuros están disponibles comercialmente o se preparan fácilmente a partir de sulfhidrilos usando condiciones estándar (por ejemplo, yodo-agua U.S. 6.025.488, sodium iodide-peroxide Synthesis, 2007, 3286-3289, etc.). En el paso 1, los disulfuros se hacen reaccionar con bromo o cloruro de sulfurilo para generar bromuros de sulfenilo o cloruros de sulfenilo in situ a de -15° C a 0° C en solvente inerte (por ejemplo, diclorometano, 1,2-dicloroetano, cloroformo, etc.; ver J. Org. Chem. 1971, 36, 3828; and J. Org. Chem. 1986, 51 (26), 5333). La mezcla resultante se agita luego durante de 5 a 30 minutos y posteriormente se transfiere gota a gota a una suspensión de ftalimida de potasio en un solvente adecuado como 1,2-dicloroetano a de -15° C a 0° C (ver J. Med. Chem. 2009, 52 (14), 4142 y Bioorg. Med. Chem. Lett. 2007, 17, 6629). En el paso 2, se hacen reaccionar N-alquiltiol-ftalimidas con compuestos de amidino o guanidina para producir los productos deseados (ver J. Med. Chem. 2009, 52 (14), 4142 y la Publicación de Patente Internacional N° WO2010100337).
Síntesis del compuesto 287
Paso 1: ácido (2S)-2-amino-3-[(1,3-dioxo-2,3-dihidro-1H-isoindol-2-il)sulfanil]propanoico (INT-15)
Se disuelven L-cistina (5 mmol), ftalimida (5 mmol), piridina (10 mmol) en acetonitrilo (10 ml). Se añade bromo (5 mmol) gota a gota a la solución a 0° C y la mezcla se calienta a temperatura ambiente y se agita durante la noche. La reacción se concentra a presión reducida y luego el residuo se purifica por cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%). El producto se recoge y se liofiliza para proporcionar la sal de trifluoroacetato de INT-15.
Paso 2: ácido (2S)-2-amino-3-{[{amino[(2-carboxietil)amino]metiliden}amino]sulfanil}propanoico (287)
Se disuelven ácido p-guanidinopropiónico (1,00 mmol), INT-15 (1,15 mmol) y carbonato de potasio (1,15 mmol) en acetonitrilo anhidro (10 ml) y se agita durante la noche. La reacción se concentra a presión reducida y luego el residuo se purifica por cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%). El producto se recoge y se liofiliza para producir la sal de trifluoroacetato de 287.
Además de la síntesis del compuesto 287 descrita anteriormente, pueden elaborarse profármacos adicionales combinando diferentes compuestos de guanidina (por ejemplo, ácido p-guanidinopropiónico, ácido pguanidinobutanoico, ácido 2-(2-iminoimidazolidin-1-il)acético, L-homocistina, etc.) con diferentes tioles activados (por ejemplo, derivados de L-cistina, N,N-diacetil-L-cistina, ácido 2-(carboximetildisulfanil)acético, etc.) como se enumera en la Tabla 17.
T l 17. M ri l ri r l ín i l m l i n
Síntesis del compuesto 323
Paso 1: N-bencil-2-oxoazetidina-1-carbotioamida
Se disuelve azetidinona (5 mmol) en tetrahidrofurano y se enfría la mezcla en un baño de hielo. Se añade hidruro de sodio (dispersión de aceite mineral al 60%, 6 mmol) seguido de tioisocianato de bencilo (5 mmol) y la mezcla se agita a temperatura ambiente durante 2 h. La reacción se vierte en agua, la capa acuosa se extrae con acetato de etilo, la capa orgánica se seca sobre sulfato de sodio, se concentra a presión reducida y se purifica mediante cromatografía en columna de gel de sílice (50-50 acetato de etilo-hexanos) para producir N-bencil-2-oxoazetidina-1-carbotioamida.
Paso 2: N,N'-dibencil-2-oxoazetidina-1-carboximidamida
A una solución en agitación de N-bencil-2-oxoazetidin-1-carbotioamida (2,5 mmol) en metanol (5 ml) se le añade yoduro de metilo (7,0 mmol). La solución se agita durante 2 h y se elimina el solvente a presión reducida. El residuo se reparte entre acetato de etilo (15 ml) y una solución de bicarbonato acuosa saturada (15 ml), la mezcla se agita y la capa orgánica se seca sobre sulfato de sodio, se concentra a presión reducida y se purifica por cromatografía en columna de gel de sílice (50-50 acetato de etilo-hexanos) para proporcionar la pseudotiourea intermedia.
A una solución en agitación de esta pseudotiourea (1 mmol) en metanol (3 ml) se le añade bencilamina (1 mmol). La solución resultante se calienta a reflujo durante 12 h en un tubo sellado, se enfría a temperatura ambiente, la mezcla se concentra a presión reducida y se purifica mediante cromatografía en columna de gel de sílice (50-50 acetato de etilo-hexanos) para producir N,N'- dibencil-2-oxoazetidina-1-carboximidamida.
Paso 3: 2-oxoazetidina-1-carboximidamida
Se disuelve N,N'-dibencil-2-oxoazetidin-1-carboximidamida (0,5 mmol) en metanol, se añade paladio al 10% sobre carbono (Pd/C 10% en moles) y el matraz se purga al vacío con hidrógeno gaseoso 5 veces. La mezcla se agita vigorosamente a temperatura ambiente bajo una atmósfera de hidrógeno durante 16 h. Se usa gas nitrógeno para purgar el matraz y la mezcla se filtra a través de Celite para eliminar el Pd/C. Se añade ácido clorhídrico 1N en metanol para precipitar la sal de HCl del compuesto 323.
Síntesis del compuesto 324
Se disuelve 2-doro-piridina (25 mmol), acetato de paladio (II) (2,5 mmol), 2,2'-bis(difenilfosfino)-1,1'-binaftilo racémico (2,5 mmol) y carbonato de cesio (65 mmol) en tolueno (75 ml) en un recipiente sellado previamente desgasificado. La mezcla se enjuaga con nitrógeno gaseoso. Se añade azetidinona (20 mmol) a la solución bajo nitrógeno y la mezcla sellada se calienta durante la noche a 100° C. La reacción se enfría a temperatura ambiente, se diluye con éter dietílico y se lava con una solución saturada de bicarbonato y agua. La capa orgánica se concentra y se purifica mediante cromatografía en columna de gel de sílice (metanol-diclorometano 2:98) para proporcionar 1-(piridin-2-il)azetidin-2-ona.
Síntesis del compuesto 325
Paso 1: ácido 3-{[{[(terc-butoxi)carbonil]amino}({[(terc-butoxi)carbonil]imino})metil]amino}propanoico (INT-16)
Se suspenden p-alanina (1,0 mmol) y N,N-di-(Boc)-1H-pirazol-1-carboxamida (1,0 mmol) en piridina (2,0 ml) y se agitan a 25° C durante 2 días. La reacción homogénea se trata con NaOH 1N y se extrae en acetato de etilo. La capa acuosa se acidifica (pH 3) con HCl 1N y luego se extrae en acetato de etilo. Las capas orgánicas combinadas se lavan con salmuera, se secan sobre sulfato de sodio, se filtran y se concentran a presión reducida para proporcionar ácido 3-{[{[(terc-butoxi)carbonil]amino}({[(terc-butoxi)carbonil]imino})metil]amino}propanoico (INT-16).
Paso 2: (2R,3R,4R,5R)-4-[(3-{[{[(terc-butoxi)carbonil]amino}({[(terc-butoxi)carbonil]imino})metil]amino}propanoil)oxi]-5-(5-fluoro-2-oxo-4-{[(pentiloxi)carbonil]amino}-1,2-Dihidropirimidin-1-il)-2-metiloxolan-3-il-3-{[{(tercbutoxi)carbonil]amino}({[(terc-butoxi)carbonil]imino})metil]amino}propanoato (INT-17)
Se añaden INT-17 (0,7 mmol) y hexafluorofosfato de benzotriazol-1-il-oxi-tris-(dimetilamino)-fosfonio
(PyBOP) (0,6 mmol) a una solución de capecitabina (0,30 mmol) en diclorometano (2,0 ml). La mezcla resultante se agita a 25° C durante la noche. El diclorometano se elimina a presión reducida y el residuo se recoge en acetato de etilo. La capa orgánica se lava con agua, salmuera, se seca sobre sulfato de magnesio, se filtra y se concentra a presión reducida. El residuo se purifica mediante cromatografía en columna de gel de sílice (metanol-diclorometano 2:98) para producir el compuesto acoplado protegido con Boc (INT-17).
Paso 3: (2R,3R,4R,5R)-4-[(3-carbamimidamidopropanoil)oxi]-5-(5-fluoro-2-oxo-4-{[(pentiloxi)carbonil]amino}-1,2-dihidropirimidin-1-il)-2-metiloxolan-3-il3-carbamimidamidopropanoato (325)
La desprotección de Boc se logra mediante condiciones estándar usando ácido trifluoroacético puro, mezclas de ácido trifluoroacético (TFA) con cloruro de metileno o ácido de clorhidrato (HCl) en dioxano. El material del paso anterior INT-17 (0,20 mmol) se trata con HCl 4N/dioxano (2,0 mmol). La mezcla se agita a 25° C durante la noche, se concentra a presión reducida y luego se somete a cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) para proporcionar el producto deseado 325.
Síntesis del compuesto 326
Paso 1: 1-(benciloxi)-3-[(3-{[bis({[(terc-butoxi)carbonil]amino})metiliden]amino}propanoil)oxi]propan-2-il-3-{[bis({[(tercbutoxi)carbonil]amino})metilideno]amino}propanoato (INT-18)
Se añaden INT-17 (2,2 mmol) y hexafluorofosfato de benzotriazol-1-il-oxi-tris-(dimetilamino)-fosfonio (PyBOP) (2,1 mmol) a una solución de 3-(benciloxi)propano-1,2-diol (1,0 mmol) en diclorometano (10 ml). La mezcla resultante se agita a 25° C durante la noche. El diclorometano se elimina a presión reducida y el residuo se recoge en acetato de etilo. La capa orgánica se lava con agua, salmuera, se seca sobre sulfato de magnesio, se filtra y se concentra a presión reducida. El residuo se purifica mediante cromatografía en columna de gel de sílice (acetato de etilo-hexano 50:50) para proporcionar el compuesto deseado INT-18.
Paso 2: 1-[(3-{[bis({[(terc-butoxi)carbonil]amino})metiliden]amino}propanoil)oxi]-3-[(clorocarbonil)oxi]propan-2-il-3-{[bis({[(terc-butoxi)carbonil]amino})metilideno]amino}propanoato (INT-19)
Se disuelve INT-18 (0,5 mmol) en metanol, se añade paladio al 10% sobre carbono (Pd al 10%/C, 0,05 mmol) y el matraz se purga al vacío con gas hidrógeno 5 veces. La mezcla se agita vigorosamente a temperatura ambiente bajo una atmósfera de hidrógeno durante 16 h. Se usa gas nitrógeno para purgar el matraz y la mezcla se filtra a través de Celite para eliminar el Pd/C y el solvente se concentra a presión reducida. El residuo se usa tal cual en la siguiente reacción.
Se enfría una mezcla de trifosgeno (0,25 mmol), carbonato de sodio (0,5 mmol) y dimetilformamida (0,018 mmol) como catalizador, en tolueno (2 ml) a 0° C y se agita a esta temperatura durante 30 min. Se añade lentamente una solución del residuo de la reacción anterior en tolueno (2 ml) durante un período de 30 min. La mezcla de la reacción se agita a 0° C durante 8 h. El carbonato de sodio sólido se elimina por filtración y el solvente se concentra a presión reducida. El residuo resultante INT-19 se usa tal cual en la siguiente reacción.
Paso 3: 1-[({1-[(4R,6R,6aS)-2,2,6-trimetil-tetrahidro-2H-furo[3,4-d][1,3]dioxol-4-il]-5-fluoro-2-oxo-1,2,3,4-tetrahidropirimidin-4-il}carbamoil)oxi]-3-[(3-{[bis({[terc-butoxi)carbonil]amino})metilideno]amino}propanoil)oxi]propan-2-il-3-{[bis({[terc-butoxi)carbonil]amino})metiliden]amino}propanoato (lNT-20)
La 5-fluoro-2',3'-o-isopropilidencitidina (5-FIPC) se elabora de acuerdo con los protocolos descritos en las Publicaciones de Patente Internacional N° WO2008144980 y WO2008131062. Se disuelven 5-FIPC (0,25 mmol) y piridina (0,5 mmol) en diclorometano (5 ml) y se añade INT-12 como una solución en diclorometano (5 ml). La mezcla se agita a temperatura ambiente durante 3 h. La reacción se vierte en acetato de etilo (50 ml) y se lava con agua, salmuera, se seca sobre sulfato de magnesio, se filtra y se concentra a presión reducida. El residuo se purifica mediante cromatografía en columna de gel de sílice (acetato de etilo-hexano 50:50) para proporcionar el compuesto deseado INT-20.
Paso 4: 1-[(3-carbamimidamidopropanoil)oxi]-3-[({1-[(2R,3R,4S,5R)-3,4-dihidroxi-5-metiloxolan-2-il]-5-fluoro-2-oxo-1,2-dihidropirimidin-4-il}carbamoil)oxi]propan-2-il3-carbamimidamidopropanoato (326)
Se trata INT-20 (020 mmol) con HCl 4N/dioxano (2,0 mmol). La mezcla se agita a temperatura ambiente durante la noche y luego se añade agua y la mezcla se agita 8 h adicionales. La reacción se concentra a presión reducida y luego el residuo se purifica por cromatografía de fase inversa (acetonitrilo/agua con ácido trifluoroacético al 0,05%) y el producto se recoge y liofiliza para proporcionar la sal de trifluoroacetato del compuesto 326.
Ejem plo 2. Determ inación de la activ idad de l com puesto
La invención proporciona compuestos que son útiles en métodos para tratar el cáncer y/o para inhibir la supervivencia de las células cancerosas, la supervivencia hipóxica, la supervivencia metastásica o la colonización metastásica.
Para determinar la actividad de un compuesto, puede ponerse en contacto el compuesto con un sistema que contiene células de prueba que expresan un gen informador codificado por un ácido nucleico enlazado operativamente con un promotor de un gen marcador seleccionado entre los promotores o supresores de metástasis mencionados anteriormente. El sistema puede ser un modelo de línea celular in vitro o un modelo animal in vivo. Las células pueden expresar de manera natural el gen o pueden modificarse para expresar un ácido nucleico recombinante. El ácido nucleico recombinante puede contener un ácido nucleico que codifica un polipéptido informador a un promotor heterólogo. Luego se mide el nivel de expresión del ARNmi, polipéptido o polipéptido informador.
Para el polipéptido, el nivel de expresión puede determinarse al nivel del ARNm o al nivel de la proteína. Los métodos para medir los niveles de ARNm en una célula, una muestra de tejido o un fluido corporal son bien conocidos en la técnica. Para medir los niveles de ARNm, pueden lisarse las células y pueden determinarse los niveles de ARNm en los lisados o en el ARN purificado o semipurificado a partir de los lisados mediante, por ejemplo, ensayos de hibridación (usando sondas de ADN o a Rn específicas de genes marcadas de manera detectable) y RT-PCR cuantitativa o semicuantitativa (usando cebadores específicos de genes apropiados). Alternativamente, pueden llevarse a cabo ensayos de hibridación in situ cuantitativos o semicuantitativos usando secciones de tejido o suspensiones de células no lisadas, y sondas de ADN o ARN marcadas detectablemente (por ejemplo, fluorescente o enzimática). Los métodos de cuantificación de ARNm adicionales incluyen el ensayo de protección de ARN (RPA) y SAGE. Los métodos para medir los niveles de proteína en una muestra de célula o tejido también son conocidos en la técnica.
Para determinar la eficacia de un compuesto para tratar el cáncer y/o inhibir la supervivencia de las células cancerosas, la supervivencia hipóxica, la supervivencia metastásica o la colonización metastásica, puede compararse el nivel obtenido de la manera descrita anteriormente con un nivel de control (por ejemplo, uno obtenido en ausencia del compuesto candidato). El compuesto se identifica como eficaz si (i) el nivel de un supresor de metástasis es más alto que un valor de control o de referencia o (ii) el nivel de un promotor de metástasis es más bajo que el valor de control o de referencia. Puede verificarse además la eficacia de un compuesto identificado de este modo usando el modelo de cultivo celular in vitro o un modelo animal in vivo como se describe en los ejemplos siguientes.
La actividad de los compuestos también puede determinarse mediante métodos conocidos en la técnica para determinar la inhibición del transporte de creatina o CKB. Por ejemplo, los métodos para determinar la inhibición de CKB se describen en McLaughlin et al. J. Biol. Chem. 1972, 247: 4382-4388. Los métodos para determinar la inhibición del transporte de creatina se describen en Fitch et al. Metabolism, 1980, 29: 686-690, Dodd et al. J. Biol. Chem. 2005, 280: 32649-32654 y Dodd et al. J. Biol. Chem. 2007, 282: 15528-15533.
Ejem plo 3. Selección in vivo
Como primer paso para identificar reguladores moleculares de la colonización hepática por cáncer de colon, se realizó una selección in vivo en la línea de cáncer de colon humano LS-174T para mejorar la colonización hepática mediante la inyección intrahepática iterativa de células cancerosas en ratones inmunodeficientes seguido de resección quirúrgica de las colonias hepáticas y disociación de células. Más específicamente, se examinó la colonización hepática por 5 x 105 células LS-originales, LvM3a y LvM3b después de la inyección intrahepática directa por bioluminiscencia. Se obtuvieron imágenes de los ratones el día 21 después de la inyección y se extrajeron los hígados para imagenología ex vivo y examen morfológico general. Se obtuvieron y compararon las proporciones de flujo de fotones para los grupos. Se descubrió que los colonizadores de hígado de tercera generación LS-LvM3a y LS-LvM3b mostraron una capacidad dramáticamente mejorada (>50 veces) para la colonización hepática tras la inyección intrahepática con respecto a su línea original. Es importante destacar que estos derivados también mostraron una capacidad metastásica hepática significativamente mejorada (>150 veces) tras la inyección en la circulación portal en ensayos de colonización metastásica, lo que revela que la capacidad de colonización hepática es un paso clave en la progresión metastásica del cáncer de colon. Para estos ensayos de bioluminiscencia, todos los valores de P para las proporciones de flujo de protones respectivas de los grupos se basaron en pruebas t de Student unilaterales y se descubrió que eran menores de 0,05, 0,001, o 0,0001.
Para identificar sistemáticamente los microARN reguladores de la progresión metastásica, se transdujo una biblioteca de partículas lentivirales, cada una de las cuales codifica uno de los 611 microARN humanos, en la población de colonizadores LS-LvM3b, la línea original LS-174T así como la población de cáncer de colon SW620. Estas poblaciones de cáncer, que contienen células cancerosas que expresan cada uno de los 661 ARNmi, se inyectaron por vía intrahepática en ratones para permitir la selección de células capaces de colonizar el
hígado. La amplificación por PCR genómica de las secuencias de ARNmi, la transcripción inversa y la realización de perfiles de ARNmi de los insertos de ARNmi permitieron la cuantificación de la representación del inserto de ARNmi. Se identificó que varios ARNmi mostraron abandono en el contexto de la colonización hepática en ambas líneas celulares de cáncer de colon, lo que es consistente con la sobreexpresión de estos ARNmi que suprimen la colonización hepática por células de cáncer de cólon.
Ejem plo 4. Determ inación de l efecto de los niveles endógenos de ARN m i
En este ejemplo, se llevaron a cabo ensayos para examinar si los niveles endógenos de cualquiera de estos ARNmi muestran silenciamiento en derivados altamente metastásicos con respecto a células isogénicas escasamente metastásicas. De hecho, se descubrió que miR-483-5p y miR-551a estaban silenciados en colonizadores hepáticos LS-LVM3a y LS-LVM3b altamente metastásicos con respecto a su línea original y el derivado SW620 metastásico con respecto a su línea original isogénica. En consonancia con el papel supresor de estos ARNmi en la colonización hepática, la sobreexpresión de miR-483-5p o miR-551a suprimió de manera robusta la colonización metastásica por las células LS-LvM3b, mientras que la inhibición de miR-483-5p o miR-551a endógenos en las líneas originales escasamente metastásicas LS-174T y SW480 mejoraron significativamente la colonización metastásica hepática.
Ejem plo 5. Investigación de l m ecanism o de acción de los ARN m i
En este ejemplo, se llevaron a cabo ensayos para investigar el mecanismo o mecanismos por los que estos ARNmi ejercen sus efectos antimetastásicos. Los efectos de estos ARNmi sobre la progresión metastásica no fueron secundarios a la modulación de la capacidad proliferativa ya que la inhibición de miR-551a no afectó la proliferación in vitro, mientras que la inhibición de miR-483-5p aumentó la proliferación. Además, la sobreexpresión de estos ARNmi no alteró la capacidad invasiva ni las tasas apoptóticas de las células cancerosas. Para determinar el mecanismo o los mecanismos por los cuales estos ARNmi impactan en la metástasis, se realizaron ensayos para identificar el punto temporal durante el proceso metastásico cuando las células que sobreexpresan estos ARNmi muestran un defecto en la progresión. Sorprendentemente, se notó que tan pronto como 24 horas después de la inyección de las células en la circulación portal para ensayos de colonización metastásica hepática, las células que sobreexpresan estos ARNmi fueron superadas en su representación con respecto a células que expresan una horquilla de control.
Ejem plo 6. S istem a de cultivo de segm entos organotíp icos
Para dilucidar el mecanismo o los mecanismos mediante los cuales estos ARNmi suprimen la colonización metastásica hepática, se desarrolló un sistema de cultivo de segmentos organotípicos hepáticos in vitro. Este sistema permitió estudiar los eventos tempranos durante la metástasis hepática después de la diseminación unicelular de células de cáncer de colon en el microambiente hepático. En consonancia con estudios anteriores sobre una selección significativa de la supervivencia celular durante la colonización metastásica, hubo una gran disminución en el número de células dentro del microambiente hepático en función del tiempo. Las células colonizadoras de LvM3b altamente metastásicas fueron significativamente mejores para persistir en el microambiente hepático que su línea original escasamente metastásica, lo que es consistente con un papel positivo para la persistencia intrahepática en la progresión metastásica.
Luego, se llevaron a cabo ensayos para investigar si los efectos de esta red reguladora de ARNmi sobre la persistencia de las células cancerosas son provocados por una supervivencia de las células cancerosas disminuida durante la progresión metastásica. Para cuantificar la muerte celular in vivo, se utilizó un informador de luciferina basado en bioluminiscencia de la actividad de caspace-3/7.
Más específicamente, las células SW480 cuyos miR-483-5p o miR-551a endógenos fueron inhibidos y posteriormente se introdujeron en el hígado de ratones inmunodeficientes mediante inyección intraesplénica. Luego, se monitorizó la actividad de caspasa in vivo relativa en estas células usando una luciferina DEVD activada con caspasa-3. Se descubrió que la inhibición de ARNmi redujo significativamente la actividad de caspasa in vivo en células de cáncer de colon durante la fase temprana de colonización hepática, revelando que la supervivencia al cáncer es el fenotipo suprimido por estos ARNmi.
Estos descubrimientos in vivo fueron corroborados por un sistema de cultivo de segmentos organotípicos. Brevemente, la supervivencia de las células SW480 en cultivos organotípicos (n = 8) cuyos miR-483-5p o miR-551a endógenos fueron inhibidos por pretratamiento con 5 x 105 células LNA se marcaron con cell-tracker green (LS-Original) o cell-tracker red (LvM3b) y se introdujeron en el hígado mediante inyección intraesplénica. Inmediatamente después de la inyección, se extirpó el hígado y se hicieron cultivos de segmentos de 150 um usando un cortador de tejidos. Se monitorizó la supervivencia de las células en cultivos organotípicos durante hasta 4 días con un microscopio multifotón. Se realizaron experimentos de intercambio de colorante para excluir los efectos del sesgo del colorante. Se mostraron imágenes representativas en el día 0 y el día 3. Se descubrió que la sobreexpresión de ambos microARN en las células LS-LvM3b suprimió la persistencia del cáncer
de colon, mientras que la inhibición de los niveles endógenos de ambos microARN aumentó la persistencia de las células SW480 escasamente metastásicas. Los descubrimientos anteriores revelan que miR-483-5p y miR-551a suprimen la colonización metastásica hepática y la supervivencia de células metastásicas en el fenotipo a de hígado mostrado por células de cáncer de colon altamente metastásicas.
Ejem plo 7. Investigación de efectores en sentido descendente
En este ejemplo, se llevaron a cabo ensayos para identificar los efectores en sentido descendente de estos ARNmi. A través de realización de perfiles transcriptómicos, se identificaron las transcripciones que estaban reguladas por disminución por la sobreexpresión de cada microARN y que contenían 3'-UTR o elementos de secuencias codificantes (CDS) complementarios a los ARNmi. Curiosamente, la creatina quinasa de tipo cerebral (CKB) se identificó como un objetivo putativo de ambos ARNmi, lo que sugiere que estos ARNmi, que muestran fenotipos comunes in vivo y organotípicos, podrían mediar sus efectos a través de un gen objetivo común. De hecho, la validación cuantitativa por PCR reveló la supresión de los niveles de transcripción de CKB tras la sobreexpresión de los microARN. Se descubrió que los niveles de expresión de CKB en células LvM3b altamente metastásicas se suprimieron mediante la sobreexpresión de miR-483-5p y miR-551a. Adicionalmente, se descubrió que miR-483 y miR-551a endógenos suprimen los niveles de proteína CKB endógena. Por ejemplo, se descubrió que la expresión de CKB se regulaba por incremento en células SW480 escasamente metastásicas cuyos miR-483-5p y miR-551aa endógenos se inhibían con LNA. Los ensayos informadores basados en mutagénesis y luciferasa revelaron que miR-483-5p y miR-551a se dirigen directamente a la 3'UTR o CDS de CKB. Con ese fin, se llevaron a cabo ensayos de informadores de luciferasa de la secuencia codificante y 3'-UTR de CKB, respectivamente. Los ensayos también se realizaron con las regiones complementarias mutadas y se realizaron por lo menos 3 veces.
Ejem plo 8. Investigación de l pape l de la CKB en la m etástasis hepática
En este ejemplo, se llevaron a cabo ensayos para examinar si la CKB es suficiente y necesaria para la colonización metastásica del hígado por cáncer de colon.
Brevemente, se examinó la metástasis del hígado en ratones inyectados intraesplénicamente con 5 x 105 células SW480 escasamente metastásicas y células que sobreexpresan CKB. Los ratones se sacrificaron 28 días después de la inyección y se extirparon los hígados para imagenología bioluminiscente. De manera similar, también se examinó la metástasis hepática en los ratones inyectados intraesplénicamente con 5 x 105 LvM3b altamente agresivas que expresan una horquilla de control o una horquilla dirigida a CKB. Estos ratones se sacrificaron 21 días después de la inyección como se ha descrito anteriormente.
Se descubrió que la sobreexpresión de CKB en las células SW480 escasamente metastásicas era suficiente para promover la metástasis hepática en más de 3 pliegues, mientras que la atenuación de CKB en las células LS-LvM3b y las células SW480 metastásicas, a través de la atenuación de la horquilla independiente en cada línea, suprimía de manera robusta la metástasis hepática en más de 5 pliegues. En consonancia con los efectos de los ARNmi, la sobreexpresión de CKB fue suficiente para mejorar significativamente la capacidad de las células de cáncer de colon para persistir en el microambiente del hígado y mejorar su representación en el hígado, mientras que la atenuación de CKB redujo significativamente la persistencia intrahepática. Con ese fin, se llevó a cabo un estudio para examinar la supervivencia de las células SW480 de control y SW480 que sobreexpresaban CKB en segmentos de hígado organotípicos (n = 8) y cultivos de segmentos organotípicos de células LvM3b que expresan una horquilla de control o una horquilla dirigida a CKB (n = 8). Las imágenes tomadas el día 0 y el día 2 mostraron que la sobreexpresión de CKB era suficiente para mejorar significativamente la capacidad de las células cancerosas. En estos ensayos, se descubrió que los valores de P eran inferiores a 0,001 o 0,0001 en base a las pruebas t de Student unilaterales.
Para investigar si CKB actúa directamente en sentido descendente de miR-483-5p y miR-551a, la secuencia codificante de CKB se sobreexpresó en células que sobreexpresan miR-483-5p o miR-551a. Brevemente, se realizaron ensayos para examinar la progresión metastásica en ratones a los que se les habían inyectado 5 x 105 células LvM3b que sobreexpresan miR-483-5p y miR-551a, con y sin sobreexpresión de CKB. Las metástasis hepáticas se monitorizaron mediante imagenología bioluminiscente y los ratones se sacrificaron 35 días después de la inyección. Se descubrió que la sobreexpresión de CKB era suficiente para rescatar los fenotipos metastásicos hepáticos suprimidos de células que sobreexpresaban miR-483-5p y miR-551a. Por el contrario, la atenuación de CKB en células que muestran inhibición endógena de miR-483-5p o miR-551a evitó el efecto de metástasis mejorada observado con la inhibición de miR-483-5p o miR-551a. Con ese fin, se realizaron ensayos para examinar la metástasis hepática en ratones inyectados con 5 x 105 células SW480 cuyos miR-483-5p y miR-551a endógenos fueron inhibidos por LNA, con y sin atenuación de CKB. Los ratones se sacrificaron después de 28 días y se extirpó el hígado para imagenología bioluminiscente ex vivo. Los resultados de los experimentos mutacionales, de ganancia y pérdida de función anteriores y los análisis de epistasis revelan que CKB es un objetivo directo de miR-483-5p y miR-551a y que actúa como un efector en sentido descendente de estos ARNmi en la regulación de la progresión metastásica del cáncer de colon. En estos ensayos, se descubrió que los valores de P eran inferiores a 0,05 o 0,001 en base a pruebas t de Student unilaterales.
Para confirmar aún más las funciones de CKB, se examinaron las actividades de caspasa in vivo relativas en células de control SW480 y que sobreexpresaban CKB en hígados de ratones. Las actividades se midieron por bioluminiscencia usando una DEVD-luciferina activada con caspasa-3 y se normalizaron a la señal de bioluminiscencia de la luciferina regular (n = 3). También se examinó una actividad de caspasa-3 in vivo relativa similar en células SW480 que expresaban una horquilla de control o una horquilla dirigida a c Kb y se introdujeron en el hígado de ratones mediante inyección intraesplénica. Las actividades de la caspasa se midieron el día 1, el día 4 y el día 7 después de la inyección. En consonancia con los descubrimientos anteriores, la sobreexpresión de CKB se redujo significativamente, mientras que la atenuación de CKB mejoró significativamente la actividad de caspasa-3/7 in vivo en células de cáncer de colon durante la fase inicial de colonización hepática. En estos ensayos, se descubrió que los valores de P eran inferiores a 0,05 o 0,001 en base a pruebas t de Student unilaterales. Estos descubrimientos revelan que CKB es un promotor de la supervivencia del cáncer de colon durante la colonización metastásica hepática.
Ejem plo 9. Experim entos de atenuación de CKB
Se sabe que la CKB regula el depósito de fosfatos de alta energía movilizados rápidamente en tejidos como el cerebro y los riñones catalizando la transferencia de un grupo fosfato de alta energía de la fosfocreatina a ADP, produciendo ATP y creatina. Se planteó la hipótesis de que la generación de ATP por CKB a partir de la fosfocreatina podría proporcionar a las células de cáncer de colon una ventaja energética durante la colonización hepática. Para determinar si la ATP, el producto final de la catálisis de CKB, podría rescatar la supresión de la metástasis observada tras la atenuación de CKB, se cargaron células de atenuación de CKB con ATP antes de la inyección de células en ensayos experimentales de metástasis. Brevemente, se examinó la metástasis hepática en ratones inyectados con 5 x 105 LvM3b con o sin atenuación de CKB y pretratado con ATP 100 uM o vehículo. La carga metastásica se monitorizó mediante imagenología bioluminiscente y los ratones se sacrificaron 21 días después de la inyección. Se descubrió que la carga de ATP de las células era suficiente para mejorar significativamente el fenotipo de metástasis suprimido en células empobrecidas de CKB en más de 10 veces. El rescate por ATP fue específico ya que la carga de ATP no mejoró la actividad metastásica de las células que expresan un control de horquilla corta.
Se realizaron estudios similares para determinar si la creatina y la fosfocreatina podrían rescatar el fenotipo visto en la atenuación de CKB. Más específicamente, se realizaron ensayos para examinar la metástasis hepática en los ratones inyectados con 5 x 105 células LvM3b pretratados con 10 uM de creatina, en el fondo de atenuación de CKB. Luego, los ratones se sacrificaron como se ha descrito anteriormente y se extrajo el hígado para imagenología bioluminiscente ex vivo el día 21 después de la inyección. Además, se examinó la metástasis del cáncer colorrectal en ratones inyectados con 5 x 105 células LvM3b con atenuación de CKB y pretratados con 10 uM de creatinafosfato. La metástasis hepática se monitorizó mediante imagenología bioluminiscente y los ratones se sacrificaron como se ha descrito anteriormente. Se descubrió que tanto la creatina como la creatina-fosfato rescataron la supresión de metástasis.
Para investigar si la metástasis del cáncer de colon podría inhibirse bloqueando el transporte de creatina hacia las células de cáncer de colon, el canal del transportador de creatina SLC6a8 se inhibió en las células LvM3b expresando la horquilla corta dirigida a SLC6a8. Luego, se examinó la metástasis hepática por células LvM3b de la misma manera descrita anteriormente. Se descubrió que la desactivación del canal del transportador de creatina SLC6a8 inhibía la metástasis del cáncer de colon. Estos descubrimientos revelan que las células de cáncer de colon dependen de la ATP generada por CKB para su supervivencia durante la colonización hepática.
Ejem plo 10. A nális is de los n ive les de expresión de A R N m i y CKB en cánceres de colon prim arios y m etástasis hepáticas
Para determinar si esta red reguladora cooperativa de ARNmi que controla la progresión metastásica del cáncer de colon tiene relevancia patológica humana, se analizaron los niveles de expresión de miR-483-5p y miR-551a en un conjunto de 67 cánceres de colon primarios, así como metástasis hepáticas obtenidas de pacientes en MSKCC. Más específicamente, se cuantificaron los niveles de miR-483-5p y miR-551a en 37 muestras de tumores primarios y 30 muestras de metástasis hepáticas mediante PCR cuantitativa en tiempo real. En consonancia con un papel supresor de metástasis para estos ARNmi durante la progresión metastásica, miR-483 y miR-551a mostraron ambos niveles de expresión significativamente reducidos en metástasis hepáticas humanas con respecto a los cánceres de colon primarios (Figura 1a; p<0,05 para miR-483-5p y p<0,05 para miR-551a; N = 67).
También se examinaron los niveles de expresión de CKB en las 37 muestras de tumores primarios y 30 muestras de metástasis hepáticas mediante PCR cuantitativa en tiempo real. Es importante destacar que se descubrió que la expresión de CKB estaba significativamente elevada en las metástasis hepáticas con respecto a los cánceres de colon primarios (p<0,05) y su expresión estaba significativamente anti-correlacionada con los ARNmi, lo que es consistente con su orientación directa por estos ARNmi en el cáncer de colon humano (Figura 1b). Estos descubrimientos son consistentes con análisis histológicos clínicos previos que revelaron niveles elevados de
proteína CKB en cáncer en etapa avanzada.
Ejem plo 11. Investigación de la red reguladora de A R N m i com o objetivo terapéutico
En este ejemplo, se llevaron a cabo ensayos para investigar el potencial terapéutico de dirigirse a esta red reguladora de ARNmi. Con este fin, se inyectó a los ratones una gran cantidad (500k) de células LvM3a altamente metastásicas y 24 horas después se inyectó a los ratones una única dosis intravenosa de virus asociado adenoviral (AAV) que expresaban miR-483-5p y miR-551a de una sola transcripción. Se descubrió que una única dosis terapéutica de virus asociado adenoviral (VAA) que administra ambos ARNmi redujo drástica y significativamente la colonización metastásica en más de 5 veces (Figura 1c).
Finalmente, se llevaron a cabo ensayos para determinar el impacto de la inhibición de CKB por moléculas pequeñas y la restricción de la disponibilidad de creatina sobre la metástasis del cáncer de colon. La ciclocreatina, que se asemeja a la fosfocreatina, es un análogo del estado de transición de las creatina quinasas. Para examinar el efecto de la ciclocreatina, se llevaron a cabo mediciones bioluminiscentes de metástasis hepática en ratones inyectados con 5 x 105 células LvM3b y se trataron con ciclocreatina diariamente durante dos semanas. Luego los ratones se sacrificaron y se extirparon los hígados para imagenología ex vivo al final del tratamiento. Se descubrió que, a pesar de ser un pobre inhibidor de CKB (5000 uM ki), el tratamiento de ratones con ciclocreatina redujo significativamente la colonización metastásica y demostró ser superior a la quimioterapia FOLFOX estándar de atención actual (Figura 1d).
Se llevaron a cabo ensayos similares usando un inhibidor del transportador de creatina ácido betaguanidinopropiónico (p-GPA). Se usaron mediciones bioluminiscentes para examinar la metástasis de hígado en ratones inyectados con 5 x 105 células LvM3b y tratados con p-GPA diariamente durante dos semanas. Se descubrió que el tratamiento de ratones con este inhibidor competitivo del canal del transportador de creatina también redujo significativamente la colonización metastásica (Figura 1e).
Usando un enfoque sistemático, se identificaron dos ARNmi que actúan como supresores de la colonización metastásica hepática por células de cáncer de colon. Se descubrió que estos ARNmi se dirigen convergentemente a CKB, un gen clave que otorga a las células que sufren hipoxia hepática la capacidad de generar ATP a partir de las reservas de fosfocreatina. La focalización con éxito de esta vía usando 4 agentes terapéuticos independientes que fueron más efectivos que el estándar de atención clínica actual, y que no mostraron toxicidad aparente, sugieren una promesa para la focalización terapéutica de esta vía en el cáncer de colon humano. El enfoque combinado de selección/cribado de genes in vivo descrito anteriormente, que se designa como MUlti-Gene Screening of Human genes through intra-Organ Tandem Selection (MUGSHOTS) ha identificado eficientemente reguladores robustos y validados patológicamente de colonización y metástasis hepáticas por cáncer de colon y tiene el potencial de descubrir reguladores codificantes y no codificantes de colonización metastásica de cualquier órgano por cualquier tipo de cáncer.
Ejem plo 12. Investigación de l transporte de creatina como objetivo terapéutico
En este ejemplo, se llevaron a cabo ensayos para confirmar el potencial terapéutico de dirigirse al canal del transportador de creatina SLC6a8 mediante la administración de la molécula pequeña p-GPA, que es un inhibidor de SLC6a8. Como se ha mencionado anteriormente, la administración de p-GPA a ratones inyectados con células de cáncer de colon LvM3b dio como resultado la inhibición de la metástasis del cáncer de colon en el hígado después de dos semanas de tratamiento (Figura 1e). Para confirmar este efecto terapéutico, los ratones inyectados con células de cáncer de colon LvM3b se trataron con p-GPA o vehículo de control (PBS) mediante una inyección intraperitoneal diaria durante tres semanas (Figura 2). Los ratones se sacrificaron a las tres semanas y se extrajo el hígado para imagenología bioluminiscente e histología macroscópica.
Se descubrió que el tratamiento diario con p-GPA llevó a una reducción significativa en la metástasis del cáncer de colon en el hígado, según lo evaluado por imagenología bioluminiscente in vivo de ratones in vivo, la imagenología bioluminiscente del hígado extraído y por examen anatómico macroscópico de hígados extraídos de los ratones tratados (Figura 2). Más específicamente, las proporciones de flujo de fotones medio medidas por la imagenología bioluminiscente para el grupo de control (sin tratamiento de p-GPA) y los grupos tratados fueron de aproximadamente 800 y 100, respectivamente. Se descubrió que los valores P eran inferiores a 0,05 en base a pruebas t de Student unilaterales.
Ejem plo 13. A tenuación de SLC6a8
En este ejemplo, se llevaron a cabo ensayos para evaluar el beneficio terapéutico de dirigirse al canal del transportador de creatina SLC6a8 con la atenuación del ARNhc dirigido a SLC6a8.
Brevemente, se inyectaron ratones con células de cáncer de colon LvM3b que expresaban cualquiera de dos ARN de horquilla corta independientes (shSLC6a8 #4 o shSLC6a8 #5) dirigidos al canal del transportador de
creatina SLC6a8 o con ARN de control (vector pLKO vacío, pedido a Sigma Aldrich) (Figura 3a). De nuevo, la metástasis hepática se monitorizó mediante imagenología bioluminiscente y los ratones se sacrificaron tres semanas después de la inoculación de las células cancerosas. Se extrajeron hígados para histología macroscópica. Se descubrió que la atenuación de SLC6a8 con dos ARNhc independientes dio como resultado la inhibición de la metástasis del cáncer de colon (Figura 3a).
Para confirmar adicionalmente el beneficio terapéutico de la atenuación de SLC6a8, se inyectó en ratones otra línea de células de cáncer de colon independiente (línea de células de cáncer de colon SW480) que expresaba un ARN de horquilla corao dirigido a SLC6a8 (shSLC6a8 #2) (Figura 3b). Se descubrió que la atenuación de SLC6a8 inhibió significativamente la metástasis de las células de cáncer de colon SW480 (Figura 3b).
Por último, se investigó el beneficio terapéutico de dirigirse a SLC6a8 en células de cáncer de páncreas. Para lograr esto, se inyectaron en ratones células de cáncer de páncreas PANC1 que expresaban un ARNhc dirigido a SLC6a8 (shSLC6a8 #5) o un ARN de control (vector pLKO vacío). La progresión metastásica se monitorizó mediante imagenología bioluminiscente y los ratones se sacrificaron de la misma manera descrita anteriormente. Se descubrió que, a los 28 días, hubo una reducción significativa en la metástasis del cáncer de páncreas en las células tratadas con ARNhc dirigido a SLC6a8, revelando que SLC6a8 es un objetivo terapéutico para el cáncer de páncreas.
Ejem plo 14. Correlación de l transporte de creatina y la progresión m etastásica
En este ejemplo, se investigó si la expresión del transportador de creatina SLC6a8 en tumores de cáncer de colon humano se correlacionaba con la progresión metastásica.
Para lograr esto, se usó PCR cuantitativa en tiempo real para cuantificar la expresión de SLC6a8 en 36 tumores de cáncer de colon primarios y 30 tumores de cáncer de colon metastásico (Figura 4). De hecho, la expresión de SLC6a8 fue significativamente mayor en los tumores metastásicos (aproximadamente 1,3) en comparación con los tumores primarios (aproximadamente 0,5), lo que confirma aún más el papel central de SLC6a8 en la metástasis (Figura 4). Se descubrió que los valores de P eran inferiores a 0,05 en base a las pruebas t de Student unilaterales.
Ejem plo 15. E fecto de p -G P A sobre el cáncer de páncreas
Como se ha mencionado anteriormente, se demostró que la inhibición del transportador de creatina SLC6a8 con la atenuación mediada por ARNhc dio como resultado la supresión de la metástasis tanto del cáncer de colon como del cáncer de páncreas. También se demostró que la inhibición de SLC6a8 con el inhibidor de molécula pequeña p-GPA dio como resultado un beneficio terapéutico para la metástasis del cáncer de colon in vivo. Para evaluar si el tratamiento con p-GPA da como resultado un beneficio terapéutico en el cáncer de páncreas, se evaluó in vivo en ratones la capacidad del tratamiento con p-GPA para inhibir la supervivencia de las células de cáncer de páncreas humano.
Brevemente, se incubaron células PANC1 de cáncer de páncreas durante 48 horas con y sin la presencia de 10 mM de p-GPA, luego se inyectaron en ratones inmunodeficientes (5 x 105 células Pancl cada ratón; 4 ratones cada en cada una de la cohorte tratada y no tratada). Se realizó imagenología de los ratones con imagenología bioluminiscente el día 1 después de la inyección y la señal se normalizó al día cero. El beneficio terapéutico se observó tan pronto como un día después de las inyecciones, con una reducción significativa en la carga tumoral de las células de cáncer de páncreas in vivo según lo evaluado por imagenología bioluminiscente (Figura 4) que demuestra el beneficio terapéutico del tratamiento con p-GPA para el cáncer de páncreas. Más específicamente, las proporciones de flujo de fotones medias medidas por la imagenología bioluminiscente para el grupo de control (sin tratamiento de p-GPA) y los grupos tratados fueron de aproximadamente 2,7 y 1,6, respectivamente. Se descubrió que los valores P eran inferiores a 0,05 en base a pruebas t de Student unilaterales.
Ejem plo 16. Com binación de p -G PA y fluorouracilo o gem citabina
Los ejemplos anteriores demostraron que el tratamiento con p-GPA solo dio como resultado un beneficio terapéutico para el cáncer de colon y el cáncer de páncreas. En este ejemplo, se investigó si el tratamiento con p-GPA podría mejorar la actividad terapéutica de los agentes quimioterapéuticos 5'-fluorouracilo y gemcitabina. Para lograr esto, se realizaron ensayos de viabilidad celular para comparar la actividad citotóxica del 5'-fluorouracilo o la gemcitabina solos en comparación con la terapia combinada con p-GPA.
Brevemente, se sembraron 10000 células PANC1 por triplicado en placas de 96 pocillos y se trataron con varias concentraciones de gemcitabina (1 nm, 10 nm, 100 nm, 1000 nm, 10000 nm, 100000 nm y 1000000 nm) con o sin 10 mM de p-GPA durante 48 horas. Luego, se ensayó la viabilidad celular usando el reactivo WST-1 (Roche Applied Science), con una absorbancia a 440 nm como indicador del número de células viables. Como se muestra en la Figura 6, se descubrió que la adición de una concentración terapéutica de p-GPA potenciaba la actividad
citotóxica de la gemcitabina en células de cáncer de páncreas PANC1 según lo evaluado mediante un ensayo de viabilidad celular usando el reactivo WST-1.
De igual manera, la adición de una concentración terapéutica de p-GPA potenció la actividad citotóxica del 5'-fluorouracilo sobre las células de cáncer de colon Ls-LvM3b. Con ese fin, se sembraron 10.000 células Ls-LvM3b por triplicado en placas de 96 pocillos y se trataron con varias concentraciones de 5'-fluorouracilo con o sin 10 mM de p-GPA durante 48 horas. La viabilidad celular se ensayó de la misma manera descrita anteriormente con absorbancia a 440 nm como indicador del número de células viables. Como se muestra en la Figura 7, estos resultados demuestran que el p-GPA potencia la actividad terapéutica de los agentes quimioterapéuticos utilizados comúnmente para el tratamiento del cáncer colorrectal y de páncreas.
Los ejemplos anteriores y la descripción de las realizaciones preferidas deben tomarse como ilustrativos, en lugar de limitativos, de la presente invención como se define en las reivindicaciones. Como se apreciará fácilmente, pueden utilizarse numerosas variaciones y combinaciones de las características expuestas anteriormente sin apartarse de la presente invención como se expone en las reivindicaciones. Tales variaciones no se consideran una desviación del alcance de la invención, y se pretende que todas estas variaciones estén incluidas dentro del alcance de las reivindicaciones siguientes.
Claims (13)
1. Un compuesto que tiene la estructura:
en donde b y c son cada uno, independientemente, 0 o 1;
Q1 es
N H
Y ^ nh2.i
R9 es hidrógeno, halo, hidroxilo, NH2 , alquilo C1-C3 opcionalmente sustituido;
R10 es hidrógeno o alquilo C1-C4 opcionalmente sustituido:
R11 es hidrógeno;
o una sal farmacéuticamente aceptable del mismo.
2. El compuesto de la reivindicación 1, en donde R10 es hidrógeno o metilo.
3. El compuesto de cualquiera de las reivindicaciones 1 a 2, en donde R9 es hidrógeno, fluoro, hidroxilo, NH2 o metilo.
7. Una composición farmacéutica que comprende un compuesto de cualquiera de las reivindicaciones 1 a 6 y un excipiente farmacéuticamente aceptable.
8. Un compuesto de cualquiera de las reivindicaciones 1 a 6, o una composición farmacéutica de la reivindicación 7, para su uso en un método para tratar el cáncer.
9. Un compuesto de cualquiera de las reivindicaciones 1 a 6, o una composición farmacéutica de la reivindicación 7, para su uso en un método para ralentizar la propagación de un cáncer migratorio; preferiblemente,
en donde dicho método comprende la supresión de la colonización metastásica de dicho cáncer migratorio en el hígado.
10. El compuesto o composición para el uso de acuerdo con las reivindicaciones 8 a 9, en donde dicho cáncer es cáncer de mama, cáncer de colon, cáncer de células renales, cáncer de pulmón de células no pequeñas, carcinoma hepatocelular, cáncer gástrico, cáncer de ovario, cáncer de páncreas, cáncer de esófago, cáncer de próstata, sarcoma o melanoma.1
11. El compuesto o composición para el uso de acuerdo con las reivindicaciones 8 a 9, en donde dicho cáncer es cáncer gastrointestinal; más preferiblemente,
en donde dicho cáncer gastrointestinal es cáncer de esófago, cáncer de estómago, cáncer de páncreas, cáncer de hígado, cáncer de vesícula biliar, cáncer colorrectal, cáncer anal, cáncer de tejido linfoide asociado a mucosas,
tumores del estroma gastrointestinal, cáncer del árbol biliar o tumor carcinoide gastrointestinal.
12. El compuesto para el uso de acuerdo con las reivindicaciones 8 a 11, en donde dicho cáncer es un cáncer resistente a fármacos.
13. Un compuesto de cualquiera de las reivindicaciones 1 a 6, o una composición farmacéutica de la reivindicación 7, para su uso en un método para tratar un cáncer metastásico en un sujeto con necesidad de ello que comprende: a) proporcionar a un sujeto al que se le ha identificado que tiene, o está en riesgo de tener, cáncer metastásico en base a que el nivel de expresión de miR-483-5p y/o miR-551a está por debajo de un valor de referencia predeterminado o el nivel de expresión de CKB y/o SLC6a8 está por encima de un valor de referencia predeterminado; y
(b) administrar a dicho sujeto una cantidad eficaz de un compuesto de cualquiera de las reivindicaciones 1-6 o una composición farmacéutica de la reivindicación 7.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201461986723P | 2014-04-30 | 2014-04-30 | |
| PCT/US2015/028633 WO2015168465A1 (en) | 2014-04-30 | 2015-04-30 | Inhibitors of creatine transport and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2885451T3 true ES2885451T3 (es) | 2021-12-13 |
Family
ID=54359346
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15786453T Active ES2885451T3 (es) | 2014-04-30 | 2015-04-30 | Inhibidores del transporte de creatina y usos de los mismos |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US10308597B2 (es) |
| EP (2) | EP3137447B1 (es) |
| CA (1) | CA2947425C (es) |
| ES (1) | ES2885451T3 (es) |
| WO (1) | WO2015168465A1 (es) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3736022A3 (en) * | 2012-10-31 | 2021-01-20 | The Rockefeller University | Treatment and diagnosis of colon cancer |
| TWI808055B (zh) | 2016-05-11 | 2023-07-11 | 美商滬亞生物國際有限公司 | Hdac 抑制劑與 pd-1 抑制劑之組合治療 |
| TWI794171B (zh) | 2016-05-11 | 2023-03-01 | 美商滬亞生物國際有限公司 | Hdac抑制劑與pd-l1抑制劑之組合治療 |
| US20210300898A1 (en) * | 2018-09-21 | 2021-09-30 | Jnana Therapeutics, Inc. | Small molecules targeting mutant mammalian proteins |
| US20220339184A1 (en) * | 2019-09-27 | 2022-10-27 | The Rockefeller University | Compositions and methods to treat metastatic gastrointestinal cancer |
| WO2025238550A1 (en) * | 2024-05-14 | 2025-11-20 | Dana-Farber Cancer Institute, Inc. | Creatine kinase inhibitors |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5324731A (en) | 1989-02-14 | 1994-06-28 | Amira, Inc. | Method of inhibiting transformation of cells in which purine metabolic enzyme activity is elevated |
| EP0758681A3 (en) | 1989-02-14 | 1997-06-04 | Massachusetts Inst Technology | Inhibition of the transformation of the cells with increased purine metabolic enzyme activity |
| US5321030A (en) | 1989-02-14 | 1994-06-14 | Amira, Inc. | Creatine analogs having antiviral activity |
| AU6165894A (en) | 1993-01-28 | 1994-08-15 | Trustees Of The University Of Pennsylvania, The | Use of creatine or analogs for the manufacture of a medicament for inhibiting tumor growth |
| US6025488A (en) | 1994-11-14 | 2000-02-15 | Bionumerik Pharmaceuticals, Inc. | Formulations and methods of reducing toxicity of antineoplastic agents |
| US5994577A (en) | 1994-11-23 | 1999-11-30 | Larsen; Scott D. | Aminoguanidine carboxylates for the treatment of non-insulin-dependent diabetes mellitus |
| EP0854712B1 (en) | 1995-10-11 | 2003-05-07 | Avicena Group, Inc. | Use of creatine analogues for the treatment of disorders of glucose metabolism |
| US5998457A (en) | 1995-10-26 | 1999-12-07 | Avicena Group, Inc. | Creatine analogues for treatment of obesity |
| EP0912523A1 (en) | 1996-05-21 | 1999-05-06 | PHARMACIA & UPJOHN COMPANY | Aminoguanidine carboxylate lactams for the treatment of non-insulin-dependent diabetes mellitus |
| WO1999033785A1 (fr) | 1997-12-27 | 1999-07-08 | Kaneka Corporation | PROCEDES POUR PRODUIRE DES ACIDES β-HALOGENO-α-AMINOCARBOXYLIQUES AINSI QUE DES DERIVES DE PHENYLCYSTEINE ET LEURS INTERMEDIAIRES |
| US6426357B1 (en) | 1999-07-27 | 2002-07-30 | Affymax, Inc. | Antagonists of follicle stimulating hormone activity |
| US6518299B1 (en) * | 2000-10-20 | 2003-02-11 | Biocryst Pharmaceuticals, Inc. | Substituted pyrrolidine compounds useful as neuraminidase inhibitors |
| MX2009011255A (es) | 2007-04-20 | 2009-11-23 | Reddys Lab Ltd Dr | Proceso para preparar capecitabina. |
| WO2008144980A1 (fr) | 2007-05-25 | 2008-12-04 | Topharman Shanghai Co., Ltd. | Procédé de préparation et intermédiaires de la capécitabine |
| WO2009015244A1 (en) | 2007-07-23 | 2009-01-29 | Synosia Therapeutics | Rufinamide for the treatment of post-traumatic stress disorder |
| FI20095208A0 (fi) | 2009-03-03 | 2009-03-03 | Kuopion Yliopisto | Metformiinin uudet aihiolääkkeet |
| JP2013507391A (ja) * | 2009-10-09 | 2013-03-04 | アカオジェン インコーポレイテッド | 抗ウイルスアミノグリコシド類似体 |
| US8173181B2 (en) * | 2009-11-09 | 2012-05-08 | Bio-Engineered Supplements & Nutrition, Inc. | Method and composition for improved anabolism |
| EP3736022A3 (en) | 2012-10-31 | 2021-01-20 | The Rockefeller University | Treatment and diagnosis of colon cancer |
| CN104341450B (zh) * | 2013-08-09 | 2018-03-27 | 北京健峤医药科技有限公司 | 一种磷酸肌酸衍生物的合成与药学应用 |
| WO2016176636A1 (en) * | 2015-04-30 | 2016-11-03 | Rgenix, Inc. | Inhibitors of creatine transport and uses thereof |
| US20170056352A1 (en) | 2015-08-25 | 2017-03-02 | Rgenix, Inc. | PHARMACEUTICALLY ACCEPTABLE SALTS OF beta-GUANIDINOPROPIONIC ACID WITH IMPROVED PROPERTIES AND USES THEREOF |
-
2015
- 2015-04-30 US US15/307,178 patent/US10308597B2/en active Active
- 2015-04-30 ES ES15786453T patent/ES2885451T3/es active Active
- 2015-04-30 EP EP15786453.9A patent/EP3137447B1/en active Active
- 2015-04-30 EP EP21182284.6A patent/EP3950673A1/en not_active Withdrawn
- 2015-04-30 WO PCT/US2015/028633 patent/WO2015168465A1/en not_active Ceased
- 2015-04-30 CA CA2947425A patent/CA2947425C/en active Active
-
2019
- 2019-04-19 US US16/389,008 patent/US10717704B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20170050924A1 (en) | 2017-02-23 |
| CA2947425C (en) | 2023-06-13 |
| EP3950673A1 (en) | 2022-02-09 |
| US10717704B2 (en) | 2020-07-21 |
| CA2947425A1 (en) | 2015-11-05 |
| EP3137447A4 (en) | 2018-01-03 |
| EP3137447B1 (en) | 2021-06-30 |
| WO2015168465A1 (en) | 2015-11-05 |
| EP3137447A1 (en) | 2017-03-08 |
| US10308597B2 (en) | 2019-06-04 |
| US20190315680A1 (en) | 2019-10-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2885451T3 (es) | Inhibidores del transporte de creatina y usos de los mismos | |
| ES2989617T3 (es) | Moduladores de receptores de quimioquinas y usos de los mismos | |
| ES2620316T3 (es) | Cicloalquenopirazoles sustituidos como inhibidores de BUB1 para el tratamiento del cáncer | |
| JP5886411B2 (ja) | 新規のピリミジン誘導体 | |
| CA2978085C (en) | .beta.-d-2'-deoxy-2'-.alpha.-fluoro-2'-.beta.-c-substituted-2-modified-n6-substituted purine nucleotides for hcv treatment | |
| AU2018203695A1 (en) | Substituted nucleosides, nucleotides and analogs thereof | |
| AU2014233520A1 (en) | Modulators of the eIF2alpha pathway | |
| CN107531683B (zh) | Usp7抑制剂化合物及使用方法 | |
| AU2015204572A1 (en) | LXR agonists and uses thereof | |
| JP2019507779A (ja) | 尿素系化合物、その製造方法及びその医薬用途 | |
| JP7025022B2 (ja) | 骨髄系由来抑制細胞関連障害の治療のための方法 | |
| EP2685980B1 (en) | Methods and use of bifunctional enzyme-building clamp-shaped molecules | |
| JP2017534657A (ja) | 新型シチジン誘導体およびその適用 | |
| KR102214225B1 (ko) | 5원 헤테로시클릭 아미드계 wnt 경로 억제제 | |
| CA3035882A1 (en) | Runx inhibitor | |
| EP2897952A1 (en) | 4-(indolyl or benzimidazolyl)amino-2-(2-(indol-3-yl)ethyl)aminopyrimidines useful for the treatment of cancer | |
| CN103724251B (zh) | 一种靶向stat3的小分子化合物及其制备方法和应用 | |
| WO2016176636A1 (en) | Inhibitors of creatine transport and uses thereof | |
| CN111278465A (zh) | mIDH1抑制剂和DNA低甲基化剂(HMA)的组合 | |
| CN107056754B (zh) | 内嵌脲类结构的wnt通路抑制剂 | |
| EP4188447A1 (en) | Compounds and uses thereof | |
| WO2014012000A2 (en) | No-releasing guanidine-coxib anti-cancer agents | |
| HK1235391B (en) | Inhibitors of creatine transport and uses thereof | |
| KR101713678B1 (ko) | 신규 화합물 4-Ethyl-7-(2-fluoro-benzylsulfanyl)-2-methyl-1-thia-3b, 5, 6-triaza-cyclopenta[a]indene 및 이를 포함하는 항암제용 약제학적 조성물 | |
| EP2897951A1 (en) | 4-indazolylamino-2-(2-(indol-3-yl)ethyl)aminopyrimidines useful for the treatment of cancer |