ES2749082T3 - Nuevos enfoques terapéuticos para tratar la enfermedad de Parkinson - Google Patents
Nuevos enfoques terapéuticos para tratar la enfermedad de Parkinson Download PDFInfo
- Publication number
- ES2749082T3 ES2749082T3 ES15762523T ES15762523T ES2749082T3 ES 2749082 T3 ES2749082 T3 ES 2749082T3 ES 15762523 T ES15762523 T ES 15762523T ES 15762523 T ES15762523 T ES 15762523T ES 2749082 T3 ES2749082 T3 ES 2749082T3
- Authority
- ES
- Spain
- Prior art keywords
- cinacalcet
- composition
- tadalafil
- baclofen
- acamprosate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/138—Aryloxyalkylamines, e.g. propranolol, tamoxifen, phenoxybenzamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Psychology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Emergency Medicine (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Una composición para su uso en el tratamiento del parkinsonismo en un sujeto necesitado del mismo que comprende tadalafil y cinacalcet, o sales de los mismos, o formulación o formulaciones de liberación sostenida de los mismos.
Description
DESCRIPCIÓN
Nuevos enfoques terapéuticos para tratar la enfermedad de Parkinson
Campo de la invención
La presente invención se refiere a composiciones para el tratamiento de la enfermedad de Parkinson y trastornos relacionados. Más específicamente, la presente invención se refiere a nuevas terapias combinatorias de la enfermedad de Parkinson y trastornos relacionados.
Antecedentes de la invención
El parkisonismo o los síndromes de Parkinson son un grupo de trastornos neurodegenerativos, progresivos y multicéntricos cuyas características principales son el temblor en reposo, la rigidez, la bradiquinesia y la inestabilidad postural. La enfermedad de Parkinson (EP) es la forma más común de Parkinson y el segundo trastorno neurodegenerativo más común después de la enfermedad de Alzheimer. En los países industriales, la prevalencia de la EP se ha estimado en aproximadamente el 0,3% de la población general, siendo los ancianos los que corren más riesgo (4% de la población mayor de 80 años se estima que se ve afectada). La edad media de inicio es de alrededor de 60 años, aunque puede ocurrir un inicio temprano (tan joven como 20 años de edad) [1].
La EP a menudo se clasifica como un trastorno del movimiento. El temblor en reposo es el más común y generalmente está entre los primeros síntomas que se desarrollan. La bradiquinesia también suele aparecer en las primeras etapas con dificultades para realizar tareas como escribir o vestirse. Se han descrito trastornos del movimiento hipercinéticos como efectos secundarios de algunos tratamientos de la enfermedad de Parkinson. A este respecto, la patente US 5.952.389 describe el uso del acamprosato para aliviar los trastornos del movimiento hipercinético inducidos por la levodopa. Sin embargo, limitar los efectos secundarios de los medicamentos es distinto y está fuera del alcance del tratamiento de la enfermedad o de los síntomas relacionados con esta. Aparece la rigidez y progresa hasta cierta rigidez y resistencia al movimiento en todo el cuerpo, reduciendo la capacidad de movimiento. En las últimas etapas, la enfermedad progresa hacia cierta inestabilidad postural, lo que conduce a un deterioro del equilibrio y caídas frecuentes. Pueden surgir otros síntomas motores, como alteraciones en el caminar o en la deglución. Si no se trata, los síntomas motores pueden llevar al paciente a terminar postrado en la cama después de un promedio de diez años [2,3].
En las etapas posteriores de la enfermedad, la EP da lugar a muchos síntomas no motores que varían mucho separadamente. La discapacidad se agrava en gran medida por el desarrollo de trastornos autonómicos y neuropsiquiátricos. Se desarrollarán trastornos del habla, cognición, estado de ánimo, comportamiento y/o pensamiento, lo que eventualmente conduce a la demencia. Otros síntomas comunes incluyen problemas sensoriales, del sueño y emocionales. Esos trastornos disminuyen la esperanza de vida del individuo afectado y las relaciones de mortalidad son alrededor del doble de las de las personas sin EP [2-4].
La EP es una enfermedad idiopática y su fisiopatología también sigue siendo mal entendida [4]. Sin embargo, al menos el 5% de los casos de la EP pueden atribuirse a variaciones genéticas. Las mutaciones dentro de genes como SNCA (alfa-sinucleína), PRKN (parkin), LRRK2 (quinasa de repetición rica en leucina 2), PINK1 (quinasa putativa inducida por PTEN1), DJ-1, ATP13A2 y once loci genéticos (PARK1-PARK11) se han asociado con la EP familiar [5]. Se sospecha que DJ-1 es una proteína citoprotectora sensible al potencial redox y ubicua que responde al ambiente redox, lo que confirma su papel fundamental como factor de estrés oxidativo en la EP [6], lo que se evidencia aún más en el papel protector del factor inducible de la hipoxia (HIF) en la protección de las células dopaminérgicas de la Sustantia Nigra respecto al estrés oxidativo, la disfunción mitocondrial y la alteración de la homeostasis del hierro [7]. Aparte de los factores genéticos, se ha propuesto que muchos factores de riesgo ambiental participan en la aparición de la EP, pero ninguno con pruebas indiscutibles. El factor de riesgo replicado más frecuente es la exposición a metales, pesticidas o herbicidas como el Agent Orange. Por otro lado, el consumo de tabaco y cafeína parece proteger a las personas frente a la EP [1].
La fisiopatología de la EP se caracteriza por cuatro características [4]:
(i) Una sinucleinopatía caracterizada por la acumulación anormal de proteínas alfa-sinucleínas en inclusiones llamadas cuerpos de Lewy en el cerebro. La distribución de los cuerpos de Lewy por todo el cerebro varía de un individuo a otro, pero a menudo se asocia directamente con la expresión y el grado de los síntomas clínicos.
(ii) El glutamato es el neurotransmisor excitatorio más abundante en el sistema nervioso de los mamíferos. En condiciones patológicas, su acumulación anormal en la hendidura sináptica conduce a la sobreactivación de los receptores de glutamato, lo que da lugar a procesos patológicos y, finalmente, a la muerte de las células neuronales. Este proceso, llamado excitotoxicidad, se observa comúnmente en los tejidos neuronales durante los trastornos neurológicos agudos y crónicos. Cada vez es más evidente que la excitotoxicidad está implicada en la patogénesis de la enfermedad de Parkinson.
(iii) Una deficiencia de actividad dopaminérgica debido a la muerte de células generadoras de dopamina en la sustancia nigra, una región del cerebro medio. Esto resulta en una pérdida del movimiento y el control del tono muscular, lo que conduce a los síntomas motores de la EP.
(iv) La degeneración de NANC (ni adrenérgica ni colinérgica) y de las neuronas serotonérgicas y colinérgicas también se produce en las etapas posteriores de la enfermedad, lo que conduce a los síntomas no motores de la EP.
Dado que no se dispone de pruebas biológicas, el diagnóstico de la EP se basa principalmente en la observación de los síntomas clínicos y la exclusión de otros trastornos con características clínicas similares [3]. Se requiere confirmación postmortem para un diagnóstico definitivo. El examen neurológico por neuroimagen puede ser útil para detectar cambios en las neuronas dopaminérgicas y descartar otras enfermedades. La respuesta terapéutica positiva a la levodopa es otro criterio de diagnóstico. Una vez hecho el diagnóstico, la progresión y la gravedad de la enfermedad se clasifica utilizando una escala de etapas como la Escala unificada de clasificación de la enfermedad de Parkinson.
El tratamiento más utilizado, especialmente en las etapas tempranas, es el precursor de la dopamina, levodopa (L-DOPA) [8]. Este fármaco lleva el neurotransmisor faltante a las neuronas dopaminérgicas, disminuyendo así los síntomas motores. Sin embargo, la mayor parte del fármaco se metaboliza antes de alcanzar la barrera hematoencefálica (BBB), causando una variedad de efectos secundarios, especialmente efectos gastrointestinales (como anorexia, náuseas o vómitos), discinesia y síntomas psiquiátricos [9]. Para prevenir el fenómeno de la discinesia, la L-DOPA se administra generalmente en combinación con carbidopa o benserazida (inhibidores de la dopa decarboxilasa periférica) y a menudo también con inhibidores de la catecol-O-metil transferasa como la entacapona. Estos fármacos tienen como objetivo bloquear el metabolismo de la L-DOPA antes de llegar al cerebro, y mejorar así la actividad de este medicamento [8]. Aunque son menos eficaces para mejorar los síntomas motores, se utilizan comúnmente agonistas de la dopamina tales como pergolida, cabergolina, apomorfina o inhibidores de la lisurida y la monoaminooxidasa-B (implicados en la descomposición catabólica de la dopamina) como la selegilina o la rasagilina en las primeras etapas de la enfermedad. Aunque son menos eficaces, pueden ser útiles para retrasar el uso de la levodopa y, por lo tanto, el inicio de la discinesia [9].
Otros medicamentos como los anticolinérgicos y los agonistas de los receptores de acetilcolina nicotínicos pueden ser útiles, pero su eficacia para la EP sigue sin ser confirmada [9]. Las investigaciones actuales también se centran en los tratamientos neuroprotectores, pero ninguno de ellos ha proporcionado ninguna evidencia de que exista una mejor degeneración. Estos afectan a la apoptosis (omigapil, CEP-1347), a los receptores de glutamato, receptores de adenosina A2A, canales de calcio (isradipino), factores de crecimiento (GDNF), alfa-sinucleína y a la inflamación [10].
Las investigaciones farmacéuticas actuales están mostrando un creciente interés en la terapia génica y el trasplante neural [10].
Los documentos WO 2009/133128, WO 2009/133141, WO 2009/133142, WO 2011/054759, WO 2009/068668, WO 2009/153291 describen tratamientos potenciales para varias enfermedades neurodegenerativas, entre las que se encuentra EP.
La EP sigue siendo hasta ahora una enfermedad incurable y todavía no se ha descubierto ningún tratamiento eficaz que modifique dicha enfermedad. Por lo tanto, los tratamientos actuales tienen como objetivo aliviar los síntomas y también la lenta progresión de la enfermedad.
Sumario de la invención
La presente invención se refiere a nuevas composiciones terapéuticas para el tratamiento del Parkinson. La invención se deriva, entre otras cosas, de la identificación de combinaciones de fármacos que proporcionan un mejor efecto terapéutico y beneficio clínico a los sujetos con la condición del Parkinson, en particular, a los sujetos con la enfermedad de Parkinson.
Más particularmente, se describe en este documento una composición para su uso en el tratamiento del Parkinson, particularmente la enfermedad de Parkinson, que comprende al menos dos medicamentos seleccionados de acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil, o una sal, profármaco, o formulación de liberación sostenida de los mismos.
También se describe en este documento un método para el tratamiento del Parkinson, particularmente la enfermedad de Parkinson, en un sujeto necesitado de éste, que comprende administrar al sujeto al menos dos medicamentos seleccionados de acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil, o una sal, profármaco o formulación de liberación sostenida de los mismos.
La invención proporciona composiciones novedosas tal como se definen en las reivindicaciones. Las combinaciones de fármacos para su uso en la invención comprenden cinacalcet y tadalafil. En una realización particular, las composiciones comprenden además la levodopa. En otra realización particular, las composiciones comprenden
además selegilina o rasagilina. En una realización más particular, cuando las composiciones de la invención comprenden un precursor de la dopamina, se puede utilizar además en dicha composición al menos un compuesto seleccionado de carbidopa, benserazida, tolcapona, entacapona, selegilina o rasagilina.
La invención también se refiere a cualquier composición farmacéutica per se que comprenda cinacalcet y tadalafil. Las composiciones de la invención pueden comprender además uno o varios vehículos o excipientes farmacéuticamente aceptables, y pueden administrarse repetidamente al sujeto. Las composiciones preferidas se administran por vía oral. Además, los medicamentos pueden formularse o administrarse juntos, por separado o secuencialmente. La invención es adecuada para el tratamiento del Parkinson en cualquier sujeto mamífero, particularmente en un sujeto humano, en cualquier etapa de la enfermedad. La invención puede utilizarse, por ejemplo, para retrasar el desarrollo de la enfermedad, para reducir, retrasar o prevenir el temblor, la hipocinesia (por ejemplo, bradiquinesia, acinesia, rigidez), inestabilidad postural y/o dolor, y/o para aumentar la supervivencia.
Breve descripción de las figuras
Figura 1: Efecto de una terapia combinada de cinacalcet y mexiletina frente a la toxicidad del glutamato en las células corticales neuronales. La intoxicación por glutamato se previene significativamente mediante la combinación de cinacalcet (64 pM) y mexiletina (25,6 pM), mientras que, a esas concentraciones, el cinacalcet y la mexiletina por sí solas no tienen ningún efecto significativo en la intoxicación. *: p<0,001, significativamente diferente de la intoxicación por glutamato; (Prueba post-hoc de ANOVA Dunett).
Figura 2: Efecto de la terapia combinada de sulfisoxazol y torasemida frente a la toxicidad del glutamato en las células corticales neuronales. La intoxicación por glutamato se previene significativamente por la combinación de sulfisoxazol (6,8 nM) y torasemida (400 nM), mientras que, a esas concentraciones, el sulfisoxazol y la torasemida por sí solos no tienen ningún efecto significativo en la intoxicación. *: p<0,001, significativamente diferente de la intoxicación por glutamato; (Prueba post-hoc de ANOVA Dunett).
Figura 3: Efecto de la terapia combinada de baclofeno y acamprosato frente a la toxicidad del glutamato en las células corticales neuronales. La intoxicación por glutamato se previene significativamente por la combinación de baclofeno (400 nM) y acamprosato (1,6 nM), mientras que, a esas concentraciones, el baclofeno y el acamprosato por sí solos no tienen ningún efecto significativo en la intoxicación. *: p<0,001, significativamente diferente de la intoxicación por glutamato; (Prueba post-hoc de ANOVA+ Dunett).
Figura 4: Efecto protector de la combinación de baclofeno y acamprosato frente a la aparición de lesiones isquémicas. Mientras que no se obtiene una protección significativa cuando se utilizan baclofeno (80 nM) o acamprosato (0,32 nM) por sí solos, se observa una protección significativa (*: p<0,0001) para la combinación de los dos fármacos, a las mismas concentraciones.
Figura 5: Efecto protector de la combinación de torasemida y sulfisoxazol frente a la aparición de lesiones isquémicas. La combinación de sulfisoxazol (1,36 nM) y torasemida (80 nM) induce una protección significativa (*: p<0,0001), un 110% superior a la protección obtenida con la torasemida sola, mientras que no se obtiene ninguna protección cuando se utiliza el sulfisoxazol solo.
Figura 6: Efecto protector de la combinación de cinacalcet y mexiletina frente a la aparición de lesiones isquémicas. No se observó ninguna protección significativa cuando se utilizaban cinacalcet (64 pM) o mexiletina (25,6 pM) por sí solas, mientras que se observó alguna protección significativa (*: p<0,0001) para la combinación de los dos fármacos, a las mismas concentraciones.
Figura 7: Efecto de la terapia combinada de baclofeno y acamprosato frente a la aparición de lesiones por 6-OHDA en células neuronales dopaminérgicas. La protección aumenta correlativamente con la concentración de las mezclas. Se observa un efecto protector significativo con un aumento en la supervivencia de las neuronas TH en un 34% con la dosis 1 (16 nM y 64 pM, respectivamente), en un 46% con la dosis 2 (80 nM y 144 pM) y en un 51% con la dosis 3 (400 nM y 1600 pM) (***: p<0,0001; * : p<0,001: significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett)).
Figura 8: Efecto de la terapia combinada de baclofeno y torasemida frente a la aparición de lesiones por 6-OHDA en células neuronales dopaminérgicas. Se observa un efecto protector significativo con un aumento en la supervivencia de las neuronas TH en un 50% con la dosis baja 1 (80 nM y 16 nM, respectivamente), en un 62% con la dosis media 2 (240 nM y 48 nM) y en un 58% con la dosis alta 3 (720 nM y 144 nM) (*** : p<0,0001: significativamente diferente de las células intoxicadas con 6-OHDA (prueba de ANOVA Dunett)).
Figura 9: Efecto de la terapia combinada de cinacalcet y mexiletina frente a la aparición de lesiones por 6-OHDA en células neuronales dopaminérgicas. Todas las concentraciones probadas ofrecieron una protección significativa contra 6-OHDA. De hecho, se observó un efecto protector significativo con un aumento de la supervivencia de las neuronas TH en un 36 % con la dosis 1 (64 pM y 5 pM, respectivamente), en un 38% con la dosis 2 (64 pM y 26 pM) y en un 46% con la dosis 3 (1600 pM y 64 pM) (***: p<0,0001; *: p<0,001: significativamente diferente de las células intoxicadas con 6-OHDA (prueba de ANOVA Dunett)).
Figura 10: Prueba del tiempo de iniciación, efecto de la terapia combinada de baclofeno y acamprosato contra las lesiones estereotáxicas por 6-OHDA en la sustancia nigra pars compacta izquierda. Pata izquierda: sin cambios significativos. Pata derecha: la inyección de 6-OHDA prolongó significativamente el tiempo de iniciación como resultado de la muerte de las neuronas en la sustancia nigra izquierda. El tratamiento con baclofeno-acamprosato protege fuertemente de la acinesia inducida por 6-OHDA y esto ocurre a la dosis más débil 1 (dosis de baclofenoacamprosato 1: 0,6 mg/kg bid y 0,04 mg/kg bid respectivamente; dosis 2: 1,5 mg/kg bid y 0,1 mg/kg bid; dosis 3: 3,75 mg/kg bid y 0,25 mg bid: p<0,0001; **: p<0,001: significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett)) ; ns: no hubo diferencia significativa entre los datos.
Figura 11: Prueba del tiempo de reacción, efecto de la terapia combinada de baclofeno y acamprosato frente a la lesión estereotáxica por 6-OHDA en la sustancia nigra pars compacta izquierda. Pata izquierda: sin cambios significativos. Pata derecha: inyección de 6-OHDA prolongó significativamente el tiempo de reacción como resultado de la muerte de las neuronas en la sustancia nigra izquierda. El tratamiento con baclofeno-acamprosato protege significativamente de la acinesia inducida por 6-OHDA y esto ocurre a la dosis más débil 1. Dosis 2 y 3 alivian casi completamente la acinesia inducida por 6-OHDA (dosis de baclofeno-acamprosato 1: 0,6 mg/kg bid y 0,04 mg/kg bid; dosis 2: 1,5 mg/kg bid y 0,1 mg/kg bid; dosis 3: 3,75 mg/kg bid y 0,25 mg/kg bid; ***: p<0,0001: *: p<0,05: significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett)) ; ns: no hay diferencias significativas entre los datos.
Figura 12: La combinación de baclofeno (BCL) y acamprosato (ACP) actúa sinérgicamente en la protección de las células neuronales dopaminérgicas de las lesiones por 6-OHDA. A: El baclofeno, a una dosis tan baja como 32 nM, cuando se combina con acamprosato, a una dosis tan baja como 10 pM, protege fuertemente a las neuronas dopaminérgicas de las lesiones por 6-OHDA (+38% supervivencia), mientras que los fármacos individuales a la misma dosis tienen un bajo efecto. B: Baclofeno, 32 nM, combinado con acamprosato a una dosis aún más baja, 4 pM, también protege fuertemente a las neuronas corticales de las lesiones por 6-OHDA (+35%), mientras que los fármacos individuales a la misma dosis tienen un bajo efecto. ***: p<0,001; *: p<0,05, significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett). S: sinergia.
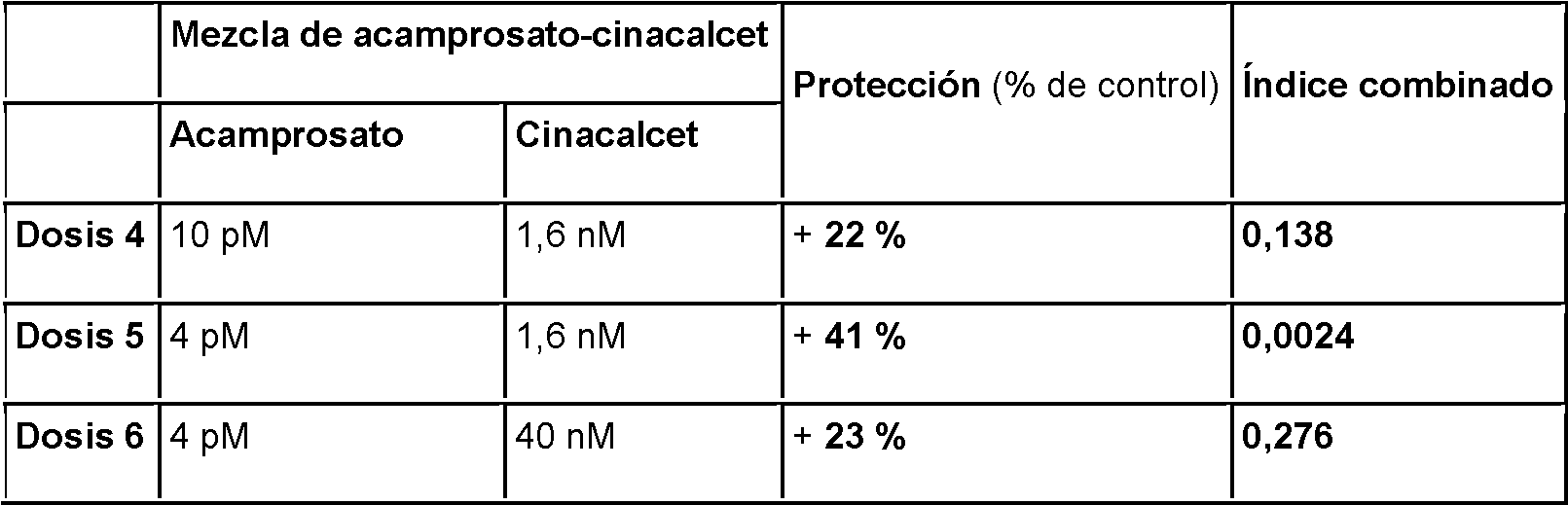
Figura 13: Efecto de la terapia combinada de acamprosato y cinacalcet frente a las lesiones generadas por 6-OHDA en células neuronales dopaminérgicas. Las concentraciones probadas ofrecen una protección significativa frente a 6-OHDA. De hecho, se observa un efecto protector significativo con un aumento en la supervivencia de las neuronas TH del 17 % al 73%. A cada una de estas concentraciones, la combinación ejerce un efecto protector sinérgico. : p<0,001; significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett); 0: <0,05: significativamente diferente de intoxicado por 6-OHDA (prueba de t de Student).
Figura 14: Efecto de la terapia combinada de cinacalcet y tadalafil frente a las lesiones generadas por 6-OHDA en células neuronales dopaminérgicas. La terapia combinada ofrece una protección significativa a diferentes concentraciones de fármacos. Para las diferentes dosis presentadas, los medicamentos actúan sinérgicamente para conferir protección. (***: p<0,001; **: p<0,01, significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett)).
Figura 15: Prueba del cilindro, efecto de la terapia combinada de baclofeno y acamprosato frente a las lesiones estereotáxicas generadas por 6-OHDA en la sustancia nigra pars compacta izquierda. La inyección de 6-OHDA disminuyó drásticamente el número de contactos dobles como resultado de la muerte de neuronas en la sustancia nigra izquierda (control, barra negra). El tratamiento con baclofeno-acamprosato (3,75 mg/kg bid y 0,25 mg/kg bid, respectivamente) protege fuertemente a las ratas de la acinesia inducida por 6-OHDA, el número de contactos se mejora significativamente en comparación con el control: ***p<0,001; **: p<0,01: significativamente diferente de las células intoxicadas por 6-OHDA (prueba de ANOVA Dunett)).
Figura 16: La terapia combinada de baclofeno y acamprosato (BCL - ACP; 3,75 mg/kg bid y 0,25 mg/kg bid, respectivamente) protege a las neuronas dopaminérgicas de su muerte in vivo. A: BCL - ACP protege a los cuerpos celulares de las neuronas dopaminérgicas de la sustancia nigra pars compacta (SN) del daño por lesiones estereotáxicas por 6-OHDA en la SN izquierda. El número de neuronas dopaminérgicas es significativamente mayor en la parte izquierda (intoxicada) del SN de ratas tratadas con BCL-ACP en comparación con el número de neuronas en la parte izquierda (intoxicada) del SN de animales no tratados. Tal efecto neuroprotector no se observa en ratas tratadas con L-DOPA. B: BCL - ACP protege a las proyecciones axonales estriales de las neuronas dopaminérgicas después de una lesión estereotáxica por 6-OHDA en la sustancia nigra pars compacta (SN) izquierda. El tratamiento con BCL - ACP aumentó significativamente la densidad, en el estriado izquierdo, de los terminales neuronales dopaminérgicos de la parte izquierda (6-OHDA intoxicado) de la sustancia nigra en comparación con el estriado izquierdo de ratas intoxicadas no tratadas (control, barra negra). Tal efecto neuroprotector no se observa para ratas tratadas con L-DOPA. OD: densidad óptica relacionada con el nivel del marcador H3-mazindol de terminales dopaminérgicos en el estriado; el marcaje se expresa como el % de la OD obtenida para la parte derecha del estriado. ***: p<0,001; **: p<0,01: significativamente diferente del control; ns: no significativamente diferente del control (prueba de ANOVA Dunett).
Descripción detallada de la invención
Un objeto de la presente invención es proporcionar nuevos enfoques terapéuticos para el tratamiento del Parkinson, más específicamente la enfermedad de Parkinson. Más particularmente, la invención describe un uso novedoso de fármacos y combinaciones de medicamentos, que permiten un alivio eficaz de tales enfermedades y que pueden utilizarse en cualquier sujeto mamífero.
El parkinsonismo define a un grupo de trastornos neurodegenerativos progresivos caracterizados por temblores en reposo y/o bradicinesia asociada con la rigidez, inestabilidad postural, pérdida de reflejos posturales, postura flexionada y/o fenómenos de congelación (cuando se siente a los pies "pegados" eventualmente al suelo). Ejemplos de condiciones parkinsonianas son la enfermedad de Parkinson, parálisis supranuclear progresiva, atrofia del sistema múltiple, degeneración gangliónica cortical-basal, enfermedad corporal difusa de Lewy, demencia de Parkinson, distonía-parkinsonismo ligado al cromosoma X y Parkinsonismo secundario (resultado de etiologías ambientales, por ejemplo, toxinas, fármacos, traumas post-encefalíticos, tumores cerebrales, traumatismo craneal, hidrocefalia de presión normal).
La enfermedad de Parkinson es la forma más común del Parkinson. La enfermedad de Parkinson ("EP") es un trastorno neurodegenerativo que conduce a manifestaciones motoras y no motoras y que se caracteriza por una extensa degeneración de las neuronas dopaminérgicas en el sistema nigroestriatal. Las manifestaciones motoras de la EP son atribuibles a la degeneración de las neuronas dopaminérgicas dentro de la sustancia nigra. Incluyen temblores, hipocinesia (p. ej., bradicinesia, acinesia, rigidez), inestabilidad postural, marcha anormal y alteraciones de la deglución. Los síntomas no motores incluyen alteraciones autonómicas y neuropsiquiátricas como la anosmia o anomalías del sueño. En el contexto de la invención, el término EP incluye cualquiera de las manifestaciones anteriores de la enfermedad.
Tal como se utiliza en el presente documento, el término "tratamiento" incluye la terapia, prevención, profilaxis, retraso o reducción de los síntomas provocados por las causas del Parkinson o como origen de ésta, preferiblemente de la enfermedad de Parkinson. El término tratamiento también designa a un retraso o una demora en el inicio de los temblores, una reducción del dolor, una disminución o reducción de la bradicinesia, acinesia, rigidez, inestabilidad postural, marcha anormal, anosmia y/o anomalías del sueño, y/o un aumento de la supervivencia. El término tratamiento incluye, en particular, el control de la progresión de la enfermedad y los síntomas motores y no motores asociados. El término tratamiento incluye particularmente i) una protección contra la toxicidad causada por la alfa-sinucleína, o una reducción o retraso de dicha toxicidad, y/o ii) una protección de las neuronas dopaminérgicas contra la toxicidad resultante de la acumulación anormal de glutamato, estrés oxidativo, disfunción mitocondrial o neuroinflamación, o una reducción o retraso de dicha toxicidad en los sujetos tratados. La expresión "combinación o tratamiento/terapia combinatoria" designa a un tratamiento en el que al menos dos o más medicamentos se administran conjuntamente a un sujeto para originar un efecto biológico. En una terapia combinada de acuerdo con esta invención, los al menos dos medicamentos pueden administrarse juntos o por separado, al mismo tiempo o secuencialmente. Además, los al menos dos medicamentos pueden administrarse a través de diferentes vías y protocolos. Como consecuencia, aunque pueden formularse juntos, los medicamentos de una combinación también pueden formularse por separado.
Varios procesos biológicos como el estrés oxidativo, la disfunción mitocondrial y la neuroinflamación acompañan a la acumulación de alfa-sinucleína agregada, lo que conduce a la degeneración de las neuronas dopaminérgicas. Por otro lado, la acumulación anormal de glutamato en las hendiduras sinápticas conduce a la sobreactivación de los receptores de glutamato, lo que da lugar a procesos patológicos y, finalmente, a la muerte de las células neuronales. Este proceso conocido como excitotoxicidad se reconoce en la actualidad como un importante factor etiológico implicado en el desarrollo de la enfermedad de Parkinson.
Los inventores pudieron establecer una red subyacente a la agregación de alfa-sinucleína, que es una importante red funcional afectada por la enfermedad de Parkinson. Los inventores han identificado módulos funcionales compuestos por varias proteínas diana, dentro de la red de agregación de alfa-sinucleína. Estas proteínas son funcionalmente relevantes para la génesis y el control de la enfermedad de Parkinson y el Parkinsonismo, y representan objetivos valiosos para las terapias y, particularmente, en las terapias combinadas.
Por lo tanto, se describe en este documento el uso de medicamentos particulares que, solos o preferentemente en combinación o combinaciones, modulan las vías anteriores para tratar el Parkinson, particularmente la enfermedad de Parkinson.
También se describen en este documento composiciones y métodos que utilizan una combinación de fármacos que inhibe la actividad de al menos dos proteínas distintas implicadas en la red de agregación de la alfa-sinucleína. Los enfoques terapéuticos de la invención son eficaces para la protección de las células neuronales, particularmente para la protección de las neuronas dopaminérgicas en el cerebro medio y, más particularmente, en la sustancia nigra.
Más particularmente, se describe en este documento una composición para su uso en el tratamiento del Parkinson, particularmente la enfermedad de Parkinson (EP), que comprende al menos dos medicamentos seleccionados de
acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil, o sales o profármacos o formulaciones de liberación sostenida de los mismos.
De hecho, los inventores han encontrado sorprendentemente que estos compuestos muestran una actividad protectora contra la toxicidad del glutamato, que es una causa conocida de muerte neuronal en la enfermedad de Parkinson y el Parkinsonismo. Los compuestos y terapias combinadas de la invención también muestran una actividad protectora contra el estrés isquémico que comparten características fisiológicas comunes con la enfermedad de Parkinson (en particular, la disfunción mitocondrial y el estrés oxidativo). Más particularmente, los compuestos de la presente invención son particularmente eficientes in vivo e in vitro contra el estrés oxidativo, que es un componente de la toxicidad alfa-sinucleína para las neuronas dopaminérgicas.
También se describe en este documento un método para el tratamiento del Parkinson, particularmente la enfermedad de Parkinson (EP), que comprende administrar a un sujeto necesitado al menos dos compuestos seleccionados de acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil, o sales o profármacos o formulaciones de liberación sostenida de los mismos.
El término "profármaco", tal como se utiliza en el presente documento, se refiere a cualquier derivado funcional (o precursores) de un compuesto de la presente invención, que, cuando se administra a un sistema biológico (por ejemplo, un organismo humano), genera dicho compuesto, como consecuencia de, por ejemplo, reacciones químicas espontáneas, reacciones químicas catalizadas por enzimas y/o reacciones químicas metabólicas. Los profármacos típicamente tienen la estructura X-fármaco, donde X es un resto del vehículo inerte y el fármaco es el compuesto activo. Los profármacos son generalmente inactivos o menos activos que el medicamento resultante y se pueden utilizar, por ejemplo, para mejorar las propiedades fisicoquímicas del fármaco, para dirigir al fármaco a un tejido específico, para mejorar las propiedades farmacocinéticas y farmacodinámicas de los medicamentos y/o para reducir los efectos secundarios indeseables. Algunos de los grupos funcionales comunes que son susceptibles al diseño de profármacos incluyen, entre otros, grupos carboxílicos, hidroxilo, amina, fosfato/fosfonato y carbonilo. Los profármacos típicamente producidos a través de la modificación de estos grupos incluyen, entre otros, ésteres, carbonatos, carbamatos, amidas y fosfatos. La orientación técnica específica para la selección de profármacos adecuados es un conocimiento común general [11-15]. Además, la preparación de profármacos puede realizarse por métodos convencionales conocidos por los expertos en la técnica. Métodos que se pueden utilizar para sintetizar otros profármacos se describen en numerosas revisiones sobre el tema [11,16-22]. Por ejemplo, arbaclofen placarbil aparece en la base de datos ChemID plus Advance (sitio web: chem.sis.nlm.nih.gov/chemidplus/) y arbaclofen placarbil es un conocido profármaco de baclofeno [23,24]. En Hanafi et al., 2011 [25], particularmente los ésteres de baclofeno y los carbamatos del éster de baclofeno, que son de particular interés para la focalización en el SNC, se dan ejemplos específicos de profármacos de baclofeno. Por lo tanto, tales profármacos son particularmente adecuados para las composiciones de esta invención. Como se mencionó anteriormente, arbaclofen placarbil es también un profármaco bastante conocido y, por lo tanto, se puede utilizar en lugar del baclofeno en las composiciones de la invención. Otros profármacos del baclofeno se pueden encontrar en las siguientes solicitudes de patente: WO 2010/102071, US2009197958, WO 2009/096985, WO 2009/061934, WO 2008/086492, US2009216037, WO 2005/066122, US2011021571, WO 2003/077902 y WO 2010/120370.
Profármacos útiles para el acamprosato, tales como el éster del ácido pantórico, ésteres sulfonílicos de neopentilo, profármacos de ésteres sulfonílicos de neopentilo o ésteres sulfonílicos de carboxilato de neopentilo enmascarados de acamprosato se mencionan destacadamente en los documentos WO 2009/033069, WO 2009/033061, WO 2009/033054, WO 2009/052191, WO 2009/033079, US20090099253, US20090069419, US20090082464, US20090082440 y US20090076147.
Los profármacos descritos anteriormente se pueden utilizar en lugar de los compuestos descritos en el presente documento de la invención.
El término "sal" se refiere a una sal de adición, farmacéuticamente aceptable y relativamente no tóxica, inorgánica u orgánica de un compuesto de la presente invención. La formación de una sal farmacéutica consiste en emparejar una molécula de fármaco ácida, básica o zwitteriónica con un contraión para crear una versión salina del fármaco. Una amplia variedad de especies químicas se puede utilizar en las reacciones de neutralización. Las sales farmacéuticamente aceptables de la invención incluyen, así, las obtenidas mediante la reacción del compuesto principal, que funciona como base, con un ácido inorgánico u orgánico para formar una sal, por ejemplo, sales de ácido acético, ácido nítrico, ácido tártrico, ácido clorhídrico, ácido sulfúrico, ácido fosfórico, ácido metanosulfónico, ácido alcanfor sulfónico, ácido oxálico, ácido maleico, ácido succínico o ácido cítrico. Las sales farmacéuticamente aceptables de la invención también incluyen aquellas en las que el compuesto principal funciona como un ácido y en las que se las hace reaccionar con una base adecuada para formar, por ejemplo, sales de sodio, potasio, calcio, magnesio, amonio o colina. Aunque la mayoría de las sales de un principio activo dado son bioequivalentes, algunas pueden tener, entre otras, mayores propiedades de solubilidad o biodisponibilidad. La selección de la sal es en la actualidad una operación estándar común en el proceso de desarrollo de fármacos, como muestra H. Stahl y C.G Wermuth en su manual [29].
En una realización preferida, la designación del compuesto está destinada a diseñar el compuesto per se, así como cualquier sal, hidrato o racemato farmacéuticamente aceptable del mismo.
En la Tabla 1 que figura a continuación se proporcionan ejemplos no limitativos del número CAS de compuestos para su uso en la invención, así como de sal(es), derivados, metabolitos y/o profármacos de estos compuestos.
Tabla 1
En una realización particular, se utiliza una formulación de liberación sostenida del compuesto.
Los inventores han descubierto que el acamprosato, el baclofeno, el cinacalcet, la mexiletina, el sulfisoxazol, la torasemida y el tadalafil son particularmente eficientes para corregir las vías moleculares de agregación de la alfasinucleína.
Como se describe en los ejemplos, las moléculas de la invención tienen un fuerte e inesperado efecto en los procesos biológicos involucrados en el Parkinsonismo, particularmente en la enfermedad de Parkinson, y representan nuevos enfoques terapéuticos de dicha patología. En particular, las composiciones de la invención proporcionan un efecto protector inesperado frente a la toxicidad del glutamato. Además, los medicamentos y las combinaciones de medicamentos de la invención aumentan la supervivencia de las neuronas dopaminérgicas bajo el estrés oxidativo inducido por 6-OHDA, así como el estrés isquémico, y provocan un efecto protector sobre las manifestaciones motoras y no motoras de la EP. Estas mejoras sintomáticas deben estar relacionadas con la protección neuronal real de las neuronas dopaminérgicas que se origina, in vivo, del tratamiento con las composiciones de la invención. Por lo tanto, los enfoques terapéuticos de la invención son eficaces para la protección de las células neuronales, particularmente para la protección de las neuronas dopaminérgicas en el cerebro medio y, más particularmente, en la sustancia nigra como se muestra in vivo.
En este documento se describen composiciones para el tratamiento del Parkinson, particularmente la EP utilizando un compuesto seleccionado de acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil. Las combinaciones de fármacos que modulan la actividad de al menos dos proteínas distintas que intervienen en la red de agregación de alfa-sinucleína constituyen una realización particularmente ventajosa de la invención. De hecho, los inventores han observado que los fármacos anteriores, cuando se administraban en combinación, actuaban sinérgicamente para proteger eficientemente las neuronas dopaminérgicas. En particular, las composiciones de la invención tienen un efecto inesperado sobre la toxicidad del glutamato, la muerte celular inducida por isquemia y el estrés oxidativo. Un efecto tan fuerte e inesperado en los procesos biológicos involucrados en el Parkinsonismo, en particular la EP, hacen que estos nuevos enfoques terapéuticos combinatorios en patología sean de particular interés.
En este documento se describen composiciones y métodos para el tratamiento del Parkinsonismo, particularmente la EP, utilizando al menos dos medicamentos seleccionados de acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil.
Las composiciones de la invención conducen a una mejora de la EP a través de su acción sobre los síntomas motores y no motores de la enfermedad. Los enfoques terapéuticos de la invención proporcionan una protección neuronal eficiente, particularmente de las neuronas dopaminérgicas, contra el estrés oxidativo, la disfunción mitocondrial, los daños por excitotoxicidad, la neuroinflamación o la apoptosis. Más particularmente, pueden proporcionar una protección de las neuronas de la sustancia nigra contra la toxicidad de la alfa-sinucleína agregada para reducir la tasa o el grado de la pérdida de células dopaminérgicas y así afectar al curso de la progresión de la enfermedad.
A este respecto, se describe en el presente documento una composición para su uso en el tratamiento del Parkinson, en particular EP, que comprende cinacalcet y tadalafil y comprende además un compuesto seleccionado
de acamprosato, baclofeno, mexiletina, sulfisoxazol y torasemida o sales o profármacos o formulaciones de liberación sostenida de los mismos.
En el presente documento se describe una composición para su uso en el tratamiento del Parkinson, en particular EP, que comprende cinacalcet y tadalafil, o una sal, profármaco o formulaciones de liberación sostenida de los mismos.
También se describe en este documento una composición para su uso en el tratamiento del Parkinson, particularmente la EP, que comprende compuestos seleccionados de acamprosato, cinacalcet, y torasemida, o una sal, profármaco, o formulaciones de liberación sostenida de los mismos, y al menos un compuesto seleccionado de baclofeno, mexiletina, sulfisoxazol y tadalafil o una sal o formulaciones de liberación sostenida de los mismos.
También se describe en este documento una composición que comprende al menos una de las siguientes combinaciones de fármacos, para la administración simultánea, secuencial o separada:
baclofeno y acamprosato,
baclofeno y cinacalcet,
cinacalcet y acamprosato,
mexiletina y cinacalcet,
torasemida y baclofeno,
torasemida y sulfisoxazol, o
cinacalcet y tadalafil,
o sus sales o profármacos o formulaciones de liberación sostenida de los mismos para su uso en el tratamiento del Parkinsonismo, particularmente la EP.
También se describen en este documento métodos de tratamiento del Parkinsonismo, particularmente la EP en un sujeto que utiliza cualquiera de los medicamentos o composiciones anteriores.
También se describe en este documento una composición o método que utiliza baclofeno y acamprosato, o una sal, profármaco, o formulaciones de liberación sostenida de los mismos.
También se describe en este documento una composición o método que utiliza baclofeno y torasemida, o una sal, profármaco, o formulaciones de liberación sostenida de los mismos.
También se describe en este documento la composición o método utilizando acamprosato y cinacalcet, o sales o formulaciones de liberación sostenida, en el que la dosis diaria de acamprosato es igual o inferior a 10 mg.
También se describen en el presente documento formulaciones de baclofeno, o una sal, profármaco o formulaciones de liberación sostenida de los mismos, para su uso en combinación con acamprosato, o una sal, profármaco, derivado de cualquier pureza química, o formulaciones de liberación sostenida de los mismos para el tratamiento de Parkinsonismo, particularmente la EP, por administración combinada, separada o secuencial a un sujeto.
En el presente documento se describe el uso de cualquiera de las composiciones anteriores para su uso en la protección de un sujeto que lo necesita de la muerte o degeneración de las neuronas dopaminérgicas (DA). Particularmente, dicho sujeto está sufriendo de Parkinsonismo y, más particularmente, EP.
Las composiciones farmacéuticas de la invención comprenden 2, 3, 4 ó 5 medicamentos distintos, más preferiblemente 2, 3 ó 4 medicamentos distintos para el tratamiento combinatorio del Parkinsonismo, en particular la EP en un sujeto que lo necesite. Los fármacos de la invención se utilizan en combinaciones para la administración combinada, separada o secuencial, con el fin de proporcionar el efecto más eficaz.
También se describe en este documento una combinación de, al menos, una combinación de fármacos seleccionada del grupo que consiste en:
• baclofeno y acamprosato,
• baclofeno y cinacalcet,
• mexiletina y cinacalcet,
• cinacalcet y acamprosato,
• torasemida y baclofeno,
• torasemida y sulfisoxazol, o
• cinacalcet ytadalafil,
con un medicamento, diferente a los anteriores, seleccionado de los fármacos acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil y que mejora el efecto terapéutico de la combinación binaria y conduce a composiciones aún más eficientes para su uso en el tratamiento del Parkinson, particularmente la EP. También se describe en el presente documento una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende baclofeno y acamprosato en combinación con un medicamento seleccionado de cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil o sales, profármacos, o formulaciones de liberación sostenida de las mismas, para la administración combinada, separada o secuencial.
También se describe en el presente documento una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende baclofeno y cinacalcet en una combinación con un medicamento seleccionado de acamprosato, mexiletina, sulfisoxazol, torasemida y tadalafil o sales, profármacos, o formulaciones de liberación sostenida de los mismos, para la administración combinada, separada o secuencial.
También se describe en el presente documento una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende mexiletina y cinacalcet en una combinación con un medicamento seleccionado de acamprosato, baclofeno, sulfisoxazol, torasemida y tadalafil o sales, profármacos, o formulaciones de liberación sostenida de los mismos, para la administración combinada, separada o secuencial.
También se describe en el presente documento una composición para su uso en el tratamiento del Parkinson, particularmente la EP, que comprende torasemida y baclofeno en una combinación con un medicamento seleccionado de acamprosato, sulfisoxazol, cinacalcet, mexiletina y tadalafil o sales, profármacos, o formulaciones de liberación sostenida de los mismos, para la administración combinada, separada o secuencial.
La invención se refiere a una composición para su uso en el tratamiento del Parkinsonismo, en particular la EP, que comprende cinacalcet y tadalafil en una combinación con un medicamento seleccionado de acamprosato, baclofeno, mexiletina, sulfisoxazol y torasemida o sales de los mismos, o profármacos de los mismos seleccionados de arbaclofeno, placarbil y sulfisoxazol acetilo, o formulaciones de liberación sostenida de los mismos, para la administración combinada, separada o secuencial.
También se describe en el presente documento una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende torasemida y sulfisoxazol en combinación con un medicamento seleccionado de acamprosato, baclofeno, mexiletina, cinacalcet y tadalafil o sales, profármacos, o formulaciones de liberación sostenida de los mismos, para la administración combinada, separada o secuencial.
También se describen en este documento composiciones para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende al menos una de las siguientes combinaciones de fármacos:
baclofeno y cinacalcet y mexiletina,
cinacalcet y acamprosato y mexiletina,
baclofeno y acamprosato y cinacalcet,
baclofeno y acamprosato y torasemida,
baclofeno y acamprosato y mexiletina,
baclofeno y acamprosato y tadalafil,
torasemida y baclofeno y cinacalcet,
cinacalcet y tadalafil y mexiletina,
cinacalcet y tadalafil y acamprosato, o
cinacalcet y tadalafil y baclofeno,
o sales, profármacos o formulaciones de liberación sostenida de los mismos, para la administración combinada, separada o secuencial. También se describe en este documento el uso de una composición como se define anteriormente para la fabricación de un medicamento para el tratamiento del Parkinsonismo, particularmente la EP. También se describe el uso de una composición como se define anteriormente para la fabricación de un medicamento para proteger a un sujeto que lo necesita de la muerte o degeneración de las neuronas DA.
Como se indicó anteriormente, en una terapia combinada de esta invención, los compuestos o fármacos pueden formularse juntos o por separado, y administrarse juntos, por separado o secuencialmente.
En el presente documento se describe un método de tratamiento del Parkinsonismo, en particular la EP, comprendiendo el método administrar simultáneamente, por separado o secuencialmente a un sujeto que lo necesita una cantidad efectiva de una composición como se ha descrito anteriormente.
También se describe en este documento un método de tratamiento del Parkinsonismo, particularmente la EP, comprendiendo el método administrar simultáneamente, por separado o secuencialmente a un sujeto que lo necesita una cantidad efectiva de una combinación de fármacos como se ha descrito anteriormente.
También se describe en el presente documento un método de tratamiento del Parkinsonismo, particularmente la EP, en un sujeto necesitado del mismo, que comprende administrar simultáneamente, por separado o secuencialmente al sujeto una cantidad efectiva de al menos un compuesto seleccionado del grupo formado por acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil.
También se describe en este documento un método de tratamiento del Parkinsonismo, particularmente la EP en un sujeto necesitado del mismo, que comprende administrar simultáneamente, por separado o secuencialmente al sujeto una cantidad efectiva de una combinación de al menos una de las siguientes combinaciones de fármacos, o sales, profármacos o formulaciones de liberación sostenida de los mismos:
baclofeno y acamprosato,
baclofeno y cinacalcet,
cinacalcet y acamprosato,
mexiletina y cinacalcet,
torasemida y baclofeno,
torasemida y sulfisoxazol, o
cinacalcet y tadalafil.
También se describe en este documento un método de tratamiento del Parkinsonismo, particularmente la EP, en un sujeto necesitado del mismo, que comprende administrar simultáneamente, por separado o secuencialmente al sujeto una cantidad efectiva de una combinación de al menos una de las siguientes combinaciones de fármacos, o sales, profármacos o formulaciones de liberación sostenida de los mismos:
baclofeno y cinacalcet y mexiletina,
cinacalcet y acamprosato y mexiletina,
baclofeno y acamprosato y cinacalcet,
baclofeno y acamprosato y torasemida,
baclofeno y acamprosato y mexiletina,
baclofeno y acamprosato y tadalafil,
torasemida y baclofeno y cinacalcet,
cinacalcet y tadalafil y mexiletina,
cinacalcet y tadalafil y acamprosato, o
cinacalcet y tadalafil y baclofeno.
También se describe en este documento un método de protección de un sujeto que lo necesita de la muerte o degeneración de las neuronas DA, comprendiendo dicho método administrar cualquiera de las composiciones anteriores.
Las composiciones de la invención comprenden típicamente uno o varios vehículos o excipientes farmacéuticamente aceptables. Además, para su uso en la presente invención, los medicamentos o compuestos se mezclan generalmente con excipientes o vehículos farmacéuticamente aceptables.
A este respecto, también se describe en el presente documento un método para preparar una composición farmacéutica, comprendiendo el método mezclar los compuestos anteriores o combinaciones de compuestos en un excipiente o vehículo adecuado.
Aunque sean muy eficaces in vitro e in vivo, dependiendo del sujeto o la condición específica, los métodos, composiciones o terapias combinadas anteriores pueden utilizarse medicamentos o tratamientos adicionales con los fármacos o tratamientos adicionales.
Otras terapias utilizadas en combinación con los medicamentos o las combinaciones de medicamentos según la presente invención pueden comprender uno o más medicamentos que alivian los síntomas de la EP, uno o más medicamentos que podrían utilizarse para el tratamiento paliativo de la EP o uno o más medicamentos actualmente evaluados en el marco de los ensayos clínicos para el tratamiento de la enfermedad de Parkinson.
Por lo tanto, las composiciones de la invención se pueden combinar con fármacos dopaminérgicos como los precursores de dopamina (preferiblemente levodopa, melevodopa), agonistas del receptor de dopamina (preferiblemente talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol o apomorfina) o inhibidores de enzimas metabolizadoras de dopamina (preferiblemente selegilina, rasagilina).
Las composiciones de la invención también pueden combinarse con otros tratamientos conocidos para la EP, tratamientos adjuntos para la EP, o el tratamiento de los síntomas no motores de la EP o, preferiblemente monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina o memantina.
Tal uso de las composiciones o las combinaciones de la invención con las terapias antes mencionadas permitiría reducir las dosis terapéuticas de los medicamentos en cuestión y, por lo tanto, reduciría, retrasaría o evitaría los efectos secundarios conocidos asociados con estos fármacos, por ejemplo, la disquinesia a dosis máximas que se observa en pacientes tratados con levodopa.
También se describe en el presente documento una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende una composición como se define anteriormente, en combinación con al menos un compuesto seleccionado del grupo compuesto por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazicol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o profármacos o derivados de cualquier pureza o formulaciones de liberación sostenida de los mismos.
Por lo tanto, se describe en este documento una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende al menos un compuesto seleccionado del grupo que consiste en acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida, o tadalafil o sales, profármacos, derivados de cualquier pureza química, o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosida, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
En este documento se describe una composición para su uso en el tratamiento del Parkinsonismo, particularmente la EP que comprende al menos una de las siguientes combinaciones de fármacos:
baclofeno y levodopa,
torasemida y levodopa,
sulfisoxazol y levodopa,
mexiletina y levodopa,
cinacalcet y levodopa,
tadalafil y levodopa,
baclofeno y selegilina o rasagilina,
torasemida y selegilina o rasagilina,
sulfisoxazol y selegilina o rasagilina,
• mexiletina y selegilina o rasagilina,
• cinacalcet y selegilina o rasagilina, o
• tadalafil y selegilina o rasagilina,
o sales o profármacos o formulaciones de liberación sostenida de los mismos para la administración combinada, separada o secuencial.
También se describe en este documento una composición per se que comprende al menos una de las siguientes combinaciones de fármacos:
• baclofeno y levodopa,
• torasemida y levodopa,
sulfisoxazol y levodopa,
• mexiletina y levodopa,
• cinacalcet y levodopa,
• tadalafil y levodopa,
• baclofeno y selegilina o rasagilina,
torasemida y selegilina o rasagilina,
• sulfisoxazol y selegilina o rasagilina,
• mexiletina y selegilina o rasagilina,
• cinacalcet y selegilina o rasagilina, o
• tadalafil y selegilina o rasagilina
o sales o profármacos o formulaciones de liberación sostenida de los mismos para la administración combinada, separada o secuencial.
En el presente documento se describe un método de tratamiento del Parkinsonismo, particularmente la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de una combinación de al menos dos compuestos seleccionados del grupo formado por acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida o tadalafil, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o profármacos o formulaciones de liberación sostenida de las mismas.
En el presente documento se describe un método de tratamiento del Parkinsonismo, particularmente la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de baclofeno y acamprosato o sales, profármacos, o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
También se describe en el presente documento un método de tratamiento del Parkinsonismo, en particular la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de mexiletina y cinacalcet o sales, profármacos, o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
En el presente documento se describe un método de tratamiento del Parkinsonismo, en particular la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de torasemida y baclofeno o sales, profármacos o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
En el presente documento se describe un método de tratamiento del Parkinsonismo, en particular la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de sulfisoxazol y torasemida o sales, profármacos, o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
En el presente documento se describe un método de tratamiento del Parkinsonismo, en particular la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de cinacalcet y acamprosato o sales, o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
En el presente documento se describe un método de tratamiento del Parkinsonismo, en particular la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de baclofeno y cinacalcet o sales, profármacos o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
También se describe en el presente documento un método de tratamiento del Parkinsonismo, en particular la EP en un sujeto necesitado del mismo, que comprende administrar simultánea, separada o secuencialmente al sujeto una cantidad efectiva de cinacalcet y tadalafil o sales, o formulaciones de liberación sostenida de los mismos, en combinación con al menos un compuesto seleccionado del grupo formado por levodopa, melevodopa, talipexol, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol, apomorfina, selegilina, rasagilina, monosialotetrahexosilgangliosido, citicolina, droxidopa mazaticol, prometazina, quetiapina, prociclidina, orfenadrina, domperidona, benzatropina, trihexifenidilo, biperiden, clozapina, desipramina, citalopram, nortriptilina, paroxetina, atomoxetina, venlafaxina, amantadina, donepezil, rivastigmina y memantina, o sales o formulaciones de liberación sostenida de los mismos.
También se describen en este documento las composiciones para su uso en el tratamiento del Parkinsonismo, particularmente la EP, comprenden al menos una de las siguientes combinaciones de fármacos, o sales, profármacos, o formulaciones de liberación sostenida de los mismos, siendo los fármacos en cada una de dichas combinaciones para la administración combinada, separada o secuencial de:
baclofeno y acamprosato y levodopa,
mexiletina y cinacalcet y levodopa,
torasemida y baclofeno y levodopa,
baclofeno y cinacalcet y levodopa,
cinacalcet y acamprosato y levodopa,
sulfisoxazol y torasemida y levodopa,
cinacalcet y tadalafil y levodopa,
baclofeno y acamprosato y selegilina o rasagilina,
mexiletina y cinacalcet y selegilina o rasagilina,
torasemida y baclofeno y selegilina o rasagilina,
baclofeno y cinacalcet y selegilina o rasagilina,
cinacalcet y acamprosato y selegilina o rasagilina,
sulfisoxazol y torasemida y selegilina o rasagilina, o
cinacalcet y tadalafil y selegilina o rasagilina.
También se describe en el presente documento una composición per se que comprende al menos una de las siguientes combinaciones de fármacos, o sales, profármacos, o formulaciones de liberación sostenida de los mismos, siendo los fármacos en cada una de dichas combinaciones para la administración simultánea, separada o secuencial de:
baclofeno y acamprosato y levodopa,
mexiletina y cinacalcet y levodopa,
torasemida y baclofeno y levodopa,
baclofeno y cinacalcet y levodopa,
cinacalcet y acamprosato y levodopa,
sulfisoxazol, torasemida y levodopa,
cinacalcet y tadalafil y levodopa,
baclofeno y acamprosato y selegilina o rasagilina,
mexiletina y cinacalcet y selegilina o rasagilina,
torasemida y baclofeno y selegilina o rasagilina,
baclofeno y cinacalcet y selegilina o rasagilina,
cinacalcet y acamprosato y selegilina o rasagilina,
sulfisoxazol y torasemida y selegilina o rasagilina, o
cinacalcet y tadalafil y selegilina o rasagilina.
También se describen en este documento composiciones para su uso en el tratamiento del Parkinsonismo, particularmente la EP, que comprende al menos una de las siguientes combinaciones de fármacos, o sales, profármacos, o formulaciones de liberación sostenida de los mismos, siendo los fármacos en cada una de dichas combinaciones para la administración combinada, separada o secuencial de:
baclofeno, cinacalcet, mexiletina y levodopa,
cinacalcet, acamprosato, mexiletina y levodopa,
baclofeno, acamprosato, cinacalcet y levodopa,
baclofeno, acamprosato, torasemida y levodopa,
baclofeno, acamprosato, mexiletina y levodopa,
baclofeno, acamprosato, tadalafil y levodopa,
torasemida, baclofeno, cinacalcet y levodopa,
cinacalcet, tadalafil, mexiletina y levodopa,
cinacalcet, tadalafil, acamprosato y levodopa,
cinacalcet, tadalafil, baclofeno y levodopa
baclofeno, cinacalcet, mexiletina y selegilina o rasagilina,
cinacalcet, acamprosato, mexiletina y selegilina o rasagilina,
baclofeno, acamprosato, cinacalcet y selegilina o rasagilina,
baclofeno, acamprosato, torasemida y selegilina o rasagilina,
baclofeno, acamprosato, mexiletina, y selegilina o rasagilina,
baclofeno, acamprosato, tadalafil, y selegilina o rasagilina,
torasemida, baclofeno, cinacalcet y selegilina o rasagilina,
cinacalcet, tadalafil, mexiletina y selegilina o rasagilina,
cinacalcet, tadalafil, acamprosato y selegilina o rasagilina, o
cinacalcet, tadalafil, baclofeno y selegilina o rasagilina.
Cuando las composiciones o terapias combinadas de la invención comprenden un precursor de la dopamina, se pueden combinar aún más con al menos un compuesto seleccionado de inhibidores de la dopa decarboxilasa periférica, inhibidores de la catecol-O-metil transferasa o inhibidores de la monoamina oxidasa. Más particularmente, cuando las composiciones o terapias combinadas de la invención comprenden un precursor de la dopamina, se pueden combinar aún más con al menos un compuesto seleccionado de carbidopa, benserazida, tolcapona, entacapona, selegilina o rasagilina.
En otra realización, se pueden utilizar composiciones o terapias combinadas de la invención junto con la terapia quirúrgica para la EP, tal como la estimulación cerebral profunda. Más particularmente, las terapias quirúrgicas son la estimulación cerebral profunda del núcleo subtalámico o del globus pallidus interna.
A este respecto, se describe en el presente documento una composición que comprende al menos un compuesto seleccionado del grupo formado por acamprosato, baclofeno, cinacalcet, mexiletina, sulfisoxazol, torasemida y tadalafil o sales, profármacos, o formulaciones de liberación sostenida de los mismos, para su uso en combinación con la estimulación cerebral profunda del núcleo subtalámico o del globus pallidus interna, en el tratamiento del Parkinsonismo, particularmente la EP.
Los síntomas motores de la EP pueden desarrollarse en última instancia cuando la denervación dopaminérgica del estriado y la pérdida de neuronas dopaminérgicas de la sustancia nigra aparecen muy extendidas. Por lo tanto, el tratamiento de la EP antes de la aparición de los síntomas motores y en la prevención es esencial para modificar la progresión y el curso de la enfermedad.
En este sentido, en una realización preferida, cualquiera de las composiciones o terapias combinadas anteriores de la invención puede utilizarse para la prevención, profilaxis o retraso de los síntomas provocados por las causas de la EP.
La combinación de la detección temprana de síntomas no motores, en particular la anosmia, con técnicas de visualización de imágenes (tecnología computerizada de emisión de un solo fotón, tomografía por emisión de positrones) para evaluar los cambios del transportador de la dopamina en el estriado puede ser un enfoque adecuado para identificar a los pacientes con EP en riesgo antes de la aparición de los síntomas motores, permitiendo así el inicio temprano de la terapia neuroprotectora.
Algunos casos de EP se pueden atribuir a mutaciones dentro de genes tales como SNCA (alfa-sinucleína), PRKN (parkin), LRRK2 (quinasa de repetición rica en leucina 2), PINK1 (quinasa putativa inducida por PTEN 1), DJ-1 y ATP13A2 y once loci genéticos (PARK1-PARK11). En este sentido, se describe en el presente documento el uso de los métodos, composiciones o terapias combinadas anteriores para el tratamiento de la EP en un sujeto que tiene una mutación en al menos uno de los siguientes genes: SNCA, PRKN, LRRK2, PINK1, DJ-1, ATP13A2 y de PARK1 a PARK11.
Es probable que la exposición a altas concentraciones o la exposición crónica a metales como el manganeso, el cobre o el plomo, o a productos químicos como los pesticidas (por ejemplo, paraquat, rotenona y maneb) causen Parkinsonismo, en particular la EP. A este respecto, se describe en el presente documento el uso de los métodos, composiciones o terapias combinadas anteriores en el tratamiento del Parkinsonismo, en particular la EP, en un sujeto expuesto, sospechoso de haber estado expuesto o en riesgo de estar expuesto a sustancias químicas o metales conocidos por ser factores de riesgo para desarrollar la EP o los trastornos relacionados con ésta.
En una realización preferida, las composiciones anteriores o las terapias combinadas de la invención se pueden utilizar en un sujeto que está en riesgo de desarrollar EP o síntomas asociados con EP.
En este documento se describen métodos, composiciones o terapias combinadas que se pueden utilizar para proteger a un sujeto que está en riesgo de desarrollar EP o síntomas asociados con la EP, de la muerte o degeneración de las neuronas DA.
La terapia de acuerdo con la invención se puede proporcionar en casa, el consultorio del médico, una clínica, el departamento ambulatorio de un hospital o en el propio hospital para que el médico pueda observar de cerca los efectos de la terapia y hacer los ajustes que se necesiten.
La duración del tratamiento depende de la etapa de la enfermedad que se esté tratando, la edad y el estado del paciente, y cómo el paciente responde al tratamiento. La dosis, la frecuencia y el modo de administración de cada componente de la combinación se pueden controlar de forma independiente. Por ejemplo, un medicamento se puede administrar por vía oral mientras que el segundo medicamento se puede administrar por vía intramuscular. La terapia combinada se puede administrar en ciclos de administración y no administración que incluyen períodos de descanso para que el cuerpo del paciente tenga la oportunidad de recuperarse de cualquier efecto secundario aún imprevisto. Los medicamentos también pueden formularse juntos de tal forma que una sola administración proporcione todos los medicamentos.
La administración de cada medicamento de la combinación puede ser por cualquier medio adecuado que resulte en una concentración del fármaco que, combinado con el otro componente, sea capaz de mejorar la condición del paciente o tratar eficientemente la enfermedad o el trastorno.
Si bien es posible que los medicamentos de la combinación sean administrados como un producto químico puro, es preferible presentarlos como una composición farmacéutica, también conocida en este contexto como formulación farmacéutica. Las posibles composiciones incluyen aquellas adecuadas para la administración oral, rectal, tópica (incluyendo transdérmica, bucal y sublingual), o parenteral (incluyendo subcutánea, intramuscular, intravenosa e intradérmica).
Más comúnmente, estas formulaciones farmacéuticas se prescriben al paciente en "paquetes para pacientes" que contienen un número de unidades dosificadoras u otros medios para la administración de dosis unitarias medidas para su uso durante un período de tratamiento distinto en un solo envase, por lo general un blíster. Los paquetes para pacientes tienen una ventaja respecto a las recetas tradicionales, en las que los farmacéuticos separan una dosis para el paciente en un producto farmacéutico a partir de una reserva a granel, de modo que el paciente siempre tiene acceso al prospecto contenido en el envase para el paciente, lo que normalmente falta en las recetas tradicionales. Se ha demostrado que la inclusión de un prospecto mejora el cumplimiento por parte del paciente de las instrucciones del médico. Por lo tanto, la invención incluye además una formulación farmacéutica, como se describe anteriormente, en combinación con el material de envasado adecuado para dichas formulaciones. En dicho envase para el paciente, el uso previsto de una formulación para el tratamiento combinado puede deducirse por medio de instrucciones, equipos, suministros, adaptaciones y/u otros medios para ayudar a utilizar la formulación de la manera más adecuada para el tratamiento. Estas medidas hacen que un envase para pacientes sea específicamente adecuado y adaptado para su uso con la combinación de la presente invención.
El medicamento puede estar contenido en cualquier cantidad apropiada y en cualquier sustancia vehículo adecuada. El medicamento puede estar presente en una cantidad de hasta 99% en peso del peso total de la composición. La composición se puede proporcionar en una forma de dosificación que sea adecuada para la vía oral, parenteral (por ejemplo, por vía intravenosa, intramuscular), rectal, cutánea, nasal, vaginal, inhalante, por la piel (parche) o por una vía de administración ocular. Por lo tanto, la composición puede estar en forma, por ejemplo, de comprimidos, cápsulas, píldoras, polvos, granulados, suspensiones, emulsiones, soluciones, geles, incluyendo hidrogeles, pastas, ungüentos, cremas, emplastos, paños humedecidos, dispositivos de administración osmótica, supositorios, enemas, soluciones inyectables, implantes, pulverizaciones o aerosoles.
Las composiciones farmacéuticas pueden formularse de acuerdo con la práctica farmacéutica convencional (véase, por ejemplo, Remington: The Science and Practice of Pharmacy (20a ed.), [30] y Encyclopedia of Pharmaceutical Technology [31]).
Las composiciones farmacéuticas de acuerdo con la invención pueden formularse para liberar el fármaco activo sustancialmente inmediatamente después de la administración o en cualquier período o tiempo predeterminado después de la administración.
Las formulaciones de liberación controlada incluyen (i) formulaciones que crean una concentración sustancialmente constante del fármaco dentro del cuerpo durante un largo período de tiempo; (ii) formulaciones que, después de una demora predeterminada, crean una concentración sustancialmente constante del fármaco dentro del cuerpo durante un período prolongado de tiempo; (iii) formulaciones que mantengan la acción farmacológica durante un período de tiempo predeterminado manteniendo un nivel de fármaco relativamente constante y efectivo en el cuerpo con una minimización concomitante de los efectos secundarios indeseables asociados con las fluctuaciones en el nivel plasmático del principio farmacéutico activo; (iv) formulaciones que localizan la acción farmacológica mediante, por ejemplo, la colocación espacial de una composición de liberación controlada adyacente o en el tejido u órgano
enfermo; y (v) formulaciones que dirigen la acción farmacológica mediante el uso de vehículos o derivados químicos para suministrar el medicamento a un tipo de célula diana particular.
La administración de fármacos en la forma de una formulación de liberación controlada es especialmente preferida en los casos en los que el fármaco tiene (i) un índice terapéutico pequeño (es decir, la diferencia entre la concentración plasmática que conduce a efectos secundarios nocivos o reacciones tóxicas y la concentración plasmática que conduce a un efecto terapéutico es pequeña; en general, el índice terapéutico, TI (por sus siglas en inglés), se define como la relación entre la media de la dosis letal (LD50) y la media de la dosis efectiva (ED50)); (ii) una estrecha ventana de absorción en el tracto gastrointestinal; o (iii) una vida media biológica muy corta para que se requiera una dosificación frecuente durante un día para mantener el nivel plasmático a un nivel terapéutico. Se puede perseguir cualquiera de una serie de estrategias con el fin de obtener una liberación controlada en la que la tasa de liberación supere la tasa de metabolismo del fármaco en cuestión. La liberación controlada puede obtenerse mediante la selección adecuada de diversos parámetros e ingredientes de formulación, incluidos, por ejemplo, varios tipos de composiciones y recubrimientos de liberación controlada. Por lo tanto, el fármaco está formulado con excipientes apropiados en una composición farmacéutica que, tras la administración, libera el fármaco de manera controlada (composiciones de comprimidos o cápsulas de una o varias unidades, soluciones aceitosas, suspensiones, emulsiones, microcápsulas, microesferas, nanopartículas, parches y liposomas).
Formas de dosificación sólida sin uso oral
Las formulaciones para uso oral incluyen comprimidos que contienen la composición de la invención en una mezcla con excipientes farmacéuticamente aceptables no tóxicos. Estos excipientes pueden ser, por ejemplo, diluyentes o rellenos inertes (por ejemplo, sacarosa, celulosa microcristalina, almidones como el almidón de patata, carbonato de calcio, cloruro de sodio, fosfato cálcico, sulfato de calcio o fosfato sódico); agentes granuladores y desintegradores (p. ej., derivados de la celulosa, incluyendo celulosa microcristalina, almidones como el almidón de patata, croscarmelosa sódica, alginatos o ácido algínico); agentes de unión (p. ej., goma acacia, ácido algínico, alginato de sodio, gelatina, almidón, almidón pregelatinizado, celulosa microcristalina, carboximetilcelulosa sódica, metilcelulosa, hidroxipropil metilcelulosa, etilcelulosa, polivinilpirrolidona, o polietilenglicol); y agentes lubricantes, deslizantes y antiadhesivos (por ejemplo, ácido esteárico, sílices o talco). Otros excipientes farmacéuticamente aceptables pueden ser los colorantes, agentes aromatizantes, plastificantes, humectantes, tampones, etc.
Los comprimidos pueden estar sin recubrimiento o pueden ser recubiertos por técnicas conocidas, opcionalmente para retrasar la desintegración y absorción en el tracto gastrointestinal y así proporcionar una acción mantenida durante un período más largo. El recubrimiento puede adaptarse para liberar el principio activo en un patrón predeterminado (por ejemplo, con el fin de lograr una formulación de liberación controlada) o puede adaptarse para no liberar el principio activo hasta después del paso por el estómago (recubrimiento entérico). El recubrimiento puede ser un recubrimiento de azúcar, un recubrimiento de película (p. ej., basado en hidroxipropil metilcelulosa, metilcelulosa, metil hidroxietilcelulosa, hidroxipropilcelulosa, carboximetilcelulosa, copolímeros de acrilato, polietilenglicoles y/o polivinilpirrolidona), o un recubrimiento entérico (p. ej., basado en copolímero de ácido metacrílico, acetato ftalato de celulosa, ftalato de hidroxipropil metilcelulosa, succinato de acetato de hidroxipropil metilcelulosa, ftalato de polivinilacetato, laca y/o etilcelulosa). Se puede emplear un material de retardo como, por ejemplo, el monoestearato de glicerilo o el diestearato de glicerilo.
Las composiciones de comprimidos sólidos pueden incluir un recubrimiento adaptado para proteger la composición de cambios químicos no deseados (por ejemplo, de la degradación química antes de la liberación del principio activo). El recubrimiento se puede aplicar en la forma de una dosificación sólida de una manera similar a la descrita en la Enciclopedia de la Tecnología Farmacéutica.
Los medicamentos pueden mezclarse en el comprimido o dividirse. Por ejemplo, un primer medicamento puede estar contenido en el interior del comprimido, y un segundo medicamento puede estar en el exterior, de modo que una porción sustancial del segundo comprimido se libere antes de la liberación del primer fármaco.
Las formulaciones para uso oral también pueden presentarse como comprimidos masticables, o como cápsulas de gelatina dura en las que el ingrediente activo se mezcla con un diluyente sólido inerte (por ejemplo, almidón de patata, celulosa microcristalina, carbonato de calcio, fosfato de calcio o caolín), o como cápsulas de gelatina blanda en las que el ingrediente activo se mezcla con agua o un medio de aceite, por ejemplo, parafina líquida o aceite de oliva. Se pueden preparar polvos y granulados utilizando los ingredientes mencionados anteriormente como comprimidos y cápsulas de una manera convencional.
Las composiciones de liberación controlada para uso oral pueden, por ejemplo, construirse para liberar el principio activo controlando la disolución y/o la difusión de la sustancia farmacéutica activa.
La disolución o liberación controlada por difusión se puede lograr mediante un recubrimiento adecuado de una comprimido, cápsula, peletes, o formulación granulada de medicamentos, o mediante la incorporación del fármaco en una matriz adecuada. Un recubrimiento de liberación controlada puede incluir una o más de las sustancias de recubrimiento mencionadas anteriormente y/o, por ejemplo, lacas, cera de abejas, glicocera, cera de ricino, cera de carnauba, alcohol estearílico, monoestearato de glicerilo, diestearato de glicerilo, palmitoestearato de glicerol,
etilcelulosa, resinas acrílicas, ácido dl-poliláctico, acetato butirato de celulosa, poli(cloruro de vinilo), poli(acetato de vinilo), vinil-pirrolidona, polietileno, polimetacrilato, metilmetacrilato, 2-hidroximetacrilato, hidrogeles de metacrilato, 1,3-butilenglicol, metacrilato de etilenglicol y/o polietilenglicol. En una formulación de matriz de liberación controlada, el material de matriz también puede incluir, por ejemplo, metilcelulosa hidratada, cera de carnauba y alcohol estearílico, carbopol 934, silicona, triestearato de glicerilo, acrilato de metilo-metacrilato de metilo, poli(cloruro de vinilo), polietileno y/o fluorocarbono halogenado.
Una composición de liberación controlada que contenga uno o más de los medicamentos de las combinaciones reivindicadas también puede estar en la forma de un comprimido o cápsula flotante (es decir, un comprimido o cápsula que, tras la administración oral, flota sobre el contenido gástrico durante cierto período de tiempo). Se puede preparar una formulación de comprimidos flotantes del medicamento o medicamentos mediante la granulación de una mezcla del fármaco o fármacos con excipientes y 20-75% p/p de hidrocoloides, como la hidroxietilcelulosa, hidroxipropilcelulosa o hidroxipropil-metilcelulosa. Los gránulos obtenidos se pueden comprimir en forma de comprimidos. En contacto con los jugos gástricos, el comprimido forma una barrera de gel sustancialmente impermeable al agua alrededor de su superficie. Esta barrera de gel influye en el mantenimiento de una densidad inferior a uno, permitiendo así que el comprimido permanezca flotante en los jugos gástricos.
Líquidos para la administración oral
Son formas de dosificación convenientes para la administración oral polvos, polvos dispersables o gránulos adecuados para la preparación de una suspensión acuosa por adición de agua. La formulación como suspensión proporciona el ingrediente activo en una mezcla con un agente dispersante o humectante, un agente de suspensión y uno o más conservantes. Los agentes de suspensión adecuados son, por ejemplo, carboximetilcelulosa sódica, metilcelulosa, alginato de sodio, etc.
Composiciones parenterales
La composición farmacéutica también se puede administrar por inyección, perfusión o implantación (intravenosa, intramuscular, subcutánea o similar) en formas de dosificación, formulaciones, o a través de dispositivos de administración o implantes adecuados que contengan vehículos y adyuvantes convencionales, no tóxicos y farmacéuticamente aceptables. La formulación y preparación de tales composiciones son bastante conocidas por los expertos en la técnica de la formulación farmacéutica.
Las composiciones para uso parenteral pueden proporcionarse en formas de una dosificación unitaria (por ejemplo, en ampollas monodosis), o en viales que contengan varias dosis y en los que se pueda añadir un conservante adecuado (véase más adelante). La composición puede estar en la forma de una solución, una suspensión, una emulsión, un dispositivo de perfusión, o un dispositivo de administración para la implantación o puede presentarse como un polvo seco para ser reconstituido con agua u otro vehículo adecuado antes de su uso. Aparte de los fármacos activos, la composición puede incluir vehículos y/o excipientes apropiados por vía parenteral. Los fármacos activos pueden incorporarse a microesferas, microcápsulas, nanopartículas, liposomas o similares para la liberación controlada. La composición puede incluir agentes de suspensión, solubilización, estabilización, de ajuste del pH y/o de dispersión.
Las composiciones farmacéuticas según la invención pueden estar en la forma adecuada para una inyección estéril. Para preparar dicha composición, los medicamentos activos adecuados se disuelven o se suspenden en un vehículo líquido paternamente aceptable. Entre los vehículos y disolventes aceptables que pueden emplearse se encuentran el agua, el agua ajustada a un pH adecuado mediante la adición de una cantidad adecuada de ácido clorhídrico, hidróxido de sodio o un tampón adecuado, 1,3-butanodiol, solución de Ringer y solución isotónica de cloruro de sodio. La formulación acuosa también puede contener uno o más conservantes (por ejemplo, p-hidroxibenzoato de metilo, etilo o n-propilo). En los casos en los que uno de los medicamentos sea sólo escasa o ligeramente soluble en agua, se puede añadir un agente potenciador de la disolución o solubilizante, o el disolvente puede incluir 10-60% p/p de propilenglicol o similares.
Las composiciones parenterales de liberación controlada pueden estar en la forma de suspensiones acuosas, microesferas, microcápsulas, microesferas magnéticas, soluciones de aceite, suspensiones de aceite o emulsiones. Alternativamente, los fármacos activos pueden incorporarse en vehículos biocompatibles, liposomas, nanopartículas, implantes o dispositivos de perfusión. Los materiales para uso en la preparación de microesferas y/o microcápsulas son, por ejemplo, polímeros biodegradables/bioerosionables como la poligalactina, poli-(cianoacrilato de isobutilo), poli(2-hidroxietil-L-glutamina). Los vehículos biocompatibles que se pueden utilizar al formular una formulación parenteral de liberación controlada son carbohidratos (por ejemplo, dextranos), proteínas (por ejemplo, albúmina), lipoproteínas o anticuerpos. Los materiales para su uso en implantes pueden ser no biodegradables (por ejemplo, polidimetil siloxano) o biodegradables (por ejemplo, poli(caprolactona), poli(ácido glicólico) o poli(orto-ésteres)). Rutas alternativas
Aunque sean menos preferidas y menos adecuadas, se pueden contemplar otras vías de administración y, por lo tanto, otras formulaciones. En este sentido, para la aplicación rectal, las formas de dosificación adecuadas para una composición incluyen supositorios (tipo de emulsión o suspensión), y cápsulas de gelatina rectal (soluciones o
suspensiones). En una formulación típica en supositorios, los fármacos activos se combinan con una base en supositorio farmacéuticamente aceptable apropiada, como manteca de cacao, ácidos grasos esterificados, gelatina glicerina, y varias bases solubles en agua o dispersables como el polietilenglicol. Se pueden incorporar varios aditivos, potenciadores o tensioactivos.
Las composiciones farmacéuticas también pueden administrarse tópicamente en la piel para la absorción percutánea en formas de dosificación o formulaciones que contengan vehículos y excipientes farmacéuticos convencionales no tóxicos, incluyendo microesferas y liposomas. Las formulaciones incluyen cremas, pomadas, lociones, ungüentos, geles, hidrogeles, soluciones, suspensiones, tiras, aerosoles, pastas, emplastos y otros tipos de sistemas de administración farmacéutica transdérmica. Los vehículos o excipientes farmacéuticamente aceptables pueden incluir agentes emulsionantes, antioxidantes, agentes tampón, conservantes, humectantes, potenciadores de la penetración, agentes quelantes, agentes formadores de gel, bases de pomada, perfumes y agentes protectores de la piel.
Los conservantes, humectantes y potenciadores de la penetración pueden ser parabenos, tales como el phidroxibenzoato de metilo o propilo, y el cloruro de benzalconio, glicerina, propilenglicol, urea, etc.
Las composiciones farmacéuticas descritas anteriormente para la administración tópica en la piel también se pueden utilizar en relación con la administración tópica sobre una parte del cuerpo que se va a tratar o en sus proximidades. Las composiciones pueden adaptarse para su aplicación directa o para su aplicación mediante dispositivos especiales de administración de medicamentos, como apósitos o, alternativamente, emplastes, almohadillas, esponjas, tiras u otras formas de materiales flexibles adecuados.
Dosis y duración del tratamiento
Se puede apreciar que los medicamentos de la combinación pueden administrarse de forma concomitante, ya sea en la misma formulación farmacéutica o diferente o secuencialmente. Si la administración fuera secuencial, el retraso en la administración del segundo ingrediente activo (o adicional) no debería ser tal que se perdiera el beneficio del efecto eficaz de la combinación de los ingredientes activos. Un requisito mínimo para una combinación de acuerdo con esta descripción es que la combinación debe estar destinada a un uso combinado con el beneficio del efecto eficaz de la combinación de los ingredientes activos. El uso previsto de una combinación puede deducirse por los equipos, suministros, adaptaciones y/u otros medios para ayudar a utilizar la combinación de acuerdo con la invención.
Las cantidades terapéuticamente efectivas de los fármacos en una combinación de esta invención incluyen, por ejemplo, las cantidades eficaces para reducir los síntomas de la enfermedad de Parkinson, detener o retrasar la progresión de dicha enfermedad una vez que se ha vuelto clínicamente manifiesta, o la prevención o reducción del riesgo de desarrollar dicha enfermedad.
Aunque los principios activos de la presente invención pueden administrarse en dosis divididas, por ejemplo dos o tres veces al día, se prefiere una sola dosis diaria de cada medicamento en la combinación, siendo lo más preferido una sola dosis diaria de todos los fármacos en una sola composición farmacéutica (forma de dosificación unitaria). La administración puede suministrarse entre una y varias veces al día durante varios días y hasta varios años, e incluso puede ser durante toda la vida del paciente. En la mayoría de los casos se indica una administración crónica o, al menos, periódicamente repetida a largo plazo.
La expresión "forma de dosificación unitaria" se refiere a unidades físicamente discretas (como cápsulas, comprimidos o cilindros de jeringa cargados) adecuadas como dosis unitarias para sujetos humanos, conteniendo cada unidad una cantidad predeterminada de material activo o materiales calculados para producir el efecto terapéutico deseado, en asociación con el vehículo farmacéutico requerido.
La cantidad de cada medicamento en una composición de dosificación unitaria preferida depende de varios factores, incluyendo el método de administración, el peso corporal y la edad del paciente, la etapa de la enfermedad, el riesgo de posibles efectos secundarios teniendo en cuenta el estado de salud general de la persona a tratar. Además, la información farmacogenómica (el efecto del genotipo en el perfil farmacocinético, farmacodinámico o de eficacia del agente terapéutico) sobre un paciente en particular puede afectar a la dosis utilizada.
Excepto cuando se responde a casos especialmente en deterioro, en los que se pueden requerir dosis más altas, la dosis preferida de cada medicamento en la combinación generalmente se encuentra dentro del intervalo de dosis no por encima de la dosis generalmente prescrita para un tratamiento de mantenimiento a largo plazo o que ha demostrado ser seguro para los estudios clínicos en fase 3.
Una ventaja notable de la invención es que cada compuesto puede ser utilizado a dosis bajas en una terapia de combinación, mientras que produce, en combinación, un beneficio clínico sustancial para el paciente. La terapia de combinación puede ser eficaz en dosis en las que los compuestos tienen individualmente poco efecto o ninguno. En consecuencia, una ventaja particular de la invención radica en la capacidad de utilizar dosis subóptimas de cada compuesto, es decir, dosis inferiores a las dosis terapéuticas normalmente prescritas, preferiblemente 1/2 de dosis
terapéuticas, más preferiblemente 1/3, 1/4, 1/5, o incluso más preferiblemente 1/10 de las dosis terapéuticas. En ejemplos particulares, se utilizan dosis tan bajas como 1/20, 1/30, 1/50, 1/100, o incluso inferiores, de las dosis terapéuticas.
Como se mencionó anteriormente, esto es probablemente debido a una actividad simultánea de las composiciones de la invención en varios objetivos involucrados en la red de agregación de alfa-sinucleína. En una realización particular, dicha conjunción de efectos moleculares puede conducir aún más a combinaciones sinérgicas. La sinergia puede ser evaluada por métodos conocidos por los expertos en la materia. Por ejemplo, la sinergia se puede caracterizar mediante el uso de un ANOVA bidireccional para determinar si la interacción entre cada fármaco es significativa o no (es decir, sinergia, [32]), o calculando un índice combinatorio a partir de las curvas de dosisrespuesta de cada uno de los compuestos y de sus combinaciones [33,34].
En tales dosis subterapéuticas, los compuestos no exhibirían ningún efecto secundario permaneciendo la combinación o combinaciones según la invención totalmente eficaces en el tratamiento del parkinsonismo, más preferiblemente la EP.
Una dosis preferida corresponde a cantidades de 1% hasta 50% de las generalmente prescritas para el tratamiento de mantenimiento a largo plazo.
La dosis más preferida puede corresponder a cantidades del 1% al 10% de las normalmente prescritas para el tratamiento de mantenimiento a largo plazo.
A continuación se proporcionan ejemplos específicos de dosis de fármacos (cantidad equivalente frente a molécula activa) para su uso, tal como se describe en la invención:
• acamprosato: 1000 mg o menos por día, preferiblemente menos de 500 mg por día, preferiblemente menos de 400 mg por día, más preferiblemente menos de 200 mg por día, más preferiblemente menos de 50 mg por día, o incluso menos de 10 mg por día; incluso más preferiblemente de aproximadamente 0,1 a 1000 mg por día, además preferiblemente entre 0,5 mg y 100 mg, típicamente 0,8 mg por día, 2 mg por día, 20 mg por día, 40 mg por día, o 80 mg por día, siendo tales dosis particularmente adecuadas para la administración oral.
• baclofeno: 150 mg o menos por día, preferiblemente menos de 100 mg por día, más preferiblemente menos de 50 mg por día, más preferiblemente menos de 30 mg por día, incluso más preferiblemente entre 0,01 mg y 30 mg al día, típicamente 12 mg por día, 24 mg por día, 30 mg por día, siendo tales dosis particularmente adecuadas para la administración oral.
• cinacalcet: 150 mg o menos por día, preferiblemente menos de 100 mg por día, preferiblemente menos de 50 mg por día, más preferiblemente menos de 36 mg por día, e incluso más preferiblemente entre 0,01 y 25 mg al día, siendo tales dosis particularmente adecuadas para la administración oral.
• mexiletina: 120 mg o menos por día, preferiblemente menos de 60 mg por día, más preferiblemente menos de 30 mg por día, más preferiblemente menos de 15 mg por día, incluso más preferiblemente entre 6 y 15 mg por día, siendo tales dosis particularmente adecuadas para la administración oral.
• torasemida: 4 mg o menos por día, preferiblemente menos de 2 mg por día, más preferiblemente menos de 1 mg por día, más preferiblemente menos de 0,5 mg por día, e incluso más preferiblemente entre 0,05 y 0,5 mg al día, siendo tales dosis particularmente adecuadas para la administración oral.
• sulfisoxazol: 800 mg o menos por día, preferiblemente menos de 400 mg, más preferiblemente menos de 200 mg al día, más preferiblemente menos de 100 mg por día, incluso más preferiblemente menos de 20 mg por día, siendo tales dosis particularmente adecuadas para la administración oral.
• tadalafil: 20 mg o menos por día, preferiblemente menos de 10 mg por día, más preferiblemente menos de 4 mg por día, más preferiblemente menos de 2,5 mg por día, e incluso más preferiblemente entre 0,025 y 2,5 mg al día, siendo tales dosis particularmente adecuadas para la administración oral.
• levodopa: 1,5 g o menos por día, preferiblemente menos de 750 mg por día, más preferiblemente menos de 375 mg por día, incluso más preferiblemente menos de 100 mg por día, siendo tales dosis particularmente adecuadas para la administración oral.
• rasagilina: 0,5 mg o menos al día, preferiblemente menos de 0,25 mg al día, más preferiblemente menos de 0,1 mg al día, más preferiblemente menos de 0,05 mg al día, incluso más preferiblemente entre 0,005 y 0,05 mg al día, siendo tales dosis particularmente adecuadas para la administración oral.
• selegilina: 5 mg o menos por día, preferiblemente menos de 2,5 mg por día, más preferiblemente menos de 1 mg por día, más preferiblemente menos de 0,5 mg por día, incluso más preferiblemente entre 0,05 y 0,1 mg por día, siendo tales dosis particularmente adecuadas para la administración oral.
También se describen terapias combinatorias que comprenden la administración de entre 0,4 mg y 50 mg de acamprosato y 6 mg a 15 mg de baclofeno, dos veces al día.
También se describen terapias combinatorias que comprenden la administración de 0,4 mg de acamprosato y 6 mg de baclofeno, dos veces al día.
También se describen terapias combinatorias que comprenden la administración de 1 mg de acamprosato y 15 mg de baclofeno, dos veces al día.
También se describen terapias combinatorias que comprenden la administración de 10 mg de acamprosato y 6 mg de baclofeno, dos veces al día.
También se describen terapias combinatorias que comprenden la administración de 20 mg de acamprosato y 12 mg de baclofeno, dos veces al día.
También se describen terapias combinatorias que comprenden la administración de 40 mg de acamprosato y 12 mg de baclofeno, dos veces al día.
También se describen terapias combinatorias que comprenden la administración de 40 mg de acamprosato y 30 mg de baclofeno, dos veces al día.
También se describen los tratamientos que comprenden la administración de levodopa o melevodopa, ya sea a su dosis y régimen habituales (es decir, como terapia complementaria) o incluso a una dosis más baja, desde el 1% hasta el 50% de las normalmente prescritas para el tratamiento de la enfermedad de Parkinson.
También se describen terapias que comprenden la administración de rasagilina o selegilina ya sea a su dosis y régimen habituales (es decir, como terapia complementaria) o incluso a una dosis más baja, desde el 1% hasta el 50% de las normalmente prescritas para el tratamiento de la EP.
Se entenderá que la cantidad del medicamento o la combinación de medicamentos realmente administrada será determinada por un médico, a la luz de las circunstancias pertinentes, incluyendo la condición o condiciones a tratar, la composición exacta a administrar, la edad, el peso y la respuesta del paciente individual, la gravedad de los síntomas del paciente y la vía de administración elegida. Por lo tanto, los intervalos de dosificación anteriores están destinados a proporcionar orientación general y apoyo para las enseñanzas mencionadas en este documento, pero no están destinadas a limitar el alcance de la invención.
Los siguientes ejemplos se proporcionan con fines ilustrativos y no a modo de limitación.
Ejemplos
Todos los procedimientos animales se han llevado a cabo de conformidad con las directrices del Instituto Nacional de Salud (NIH) para el cuidado y uso de animales de laboratorio, y han sido aprobados por la Junta Nacional de Experimentación con Animales.
A- Prevención de la toxicidad de glutamato en células neuronales
La toxicidad del glutamato está implicada en la patogénesis de la enfermedad de Parkinson. En este conjunto de experimentos, los compuestos candidatos han sido probados por su capacidad para prevenir o reducir los efectos tóxicos de la toxicidad del glutamato en las células neuronales. Los fármacos se prueban primero individualmente, seguido de ensayos de su acción combinatoria.
Preparación de células neuronales
La eficacia de las combinaciones farmacéuticas de la invención se evalúa en las neuronas corticales primarias. Fueron cultivadas neuronas corticales de ratas como se describen en Singer et al. [35]. Se sacrificaron ratas hembra embarazadas de 15 días de gestación por dislocación cervical (Ratas Wistar) y les fueron retirados los fetos del útero. La corteza se extrajo y se colocó en un medio helado de Leibovitz (L15) que contenía un 2% de penicilina 10.000 U/ml y estreptomicina 10 mg/ml y un 1% de albúmina sérica bovina (BSA). Las cortezas fueron disgregadas con tripsina durante 20 min a 37°C (0,05%). La reacción se detuvo mediante la adición de medio Eagle modificado de Dulbecco (DMEM) con DNasa1 grado II y 10% de suero fetal de ternero (FCS). Las células se disociaron mecánicamente mediante 3 pases en serie a través de una pipeta de 10 ml y se centrifugaron a 515 x g durante 10 minutos a 4°C. El sobrenadante fue desechado y el pelete de células fue re-suspendido en un medio de cultivo definido que consistía en Neurobasal complementado con B27 (2%), L-glutamina (0,2 mM), 2% de solución de PS y 10 ng/ml de BDNF. Las células viables se contaron en un citómetro Neubauer utilizando la prueba de exclusión de azul de tripano. Las células fueron sembradas a una densidad de 30.000 células/pocillo en placas de 96 pocillo (los pocillo fueron recubiertos previamente con poli-L-lisina (10 pg/ml)) y se cultivaron a 37°C en una atmósfera de aire humidificado (95%)/CO2 (5%).
Ensayos de toxicidad del glutamato
El efecto neuroprotector de los compuestos se evalúa mediante la cuantificación de la red de neuritas (inmunotinción de neurofilamentos (NF) que describe específicamente las neuronas glutaminérgicas).
Después de 12 días de cultivo de las neuronas, los fármacos de las combinaciones candidatas se disuelven en medio de cultivo (+0,1% de DMSO). Las combinaciones candidatas se preincuban con neuronas durante 1 hora antes del daño por glutamato. Una hora después de la incubación, el glutamato se añade durante 20 min a una concentración final de 40 pM en presencia de combinaciones candidatas con el fin de evitar más diluciones de fármacos. Al final de la incubación, el medio se cambia con medio con la combinación candidata pero sin glutamato. El cultivo se fija 24 horas después del daño por glutamato. Se utiliza como control positivo el MK801 (dizocilpinhidrogeno maleato, 77086-22-7 -20 pm).
Después de la permeabilización con saponina (Sigma), las células se bloquean durante 2 horas con PBS que contiene 10 % de suero de cabra, luego las células se incuban con anticuerpo primario monoclonal de ratón contra el anticuerpo Neurofilamento (NF, Sigma). Este anticuerpo se revela con IgG anti-ratón Alexa Fluor 488 de cabra. Los núcleos de las células se marcan mediante un marcador fluorescente (solución Hoechst, SIGMA) y la red de neuritas se cuantifica. Se utilizan seis pocillos por condición para evaluar la supervivencia neuronal en 3 cultivos diferentes.
Resultados
Todas las combinaciones de fármacos probados dan un efecto protector frente a la toxicidad del glutamato para las células neuronales corticales. Los resultados se muestran en la Tabla 2 a continuación.
Como se ejemplifica en las figuras 1 a 3, las combinaciones de la invención protegen significativamente a las neuronas de la toxicidad del glutamato en las condiciones experimentales descritas anteriormente. Cabe destacar que se aprecia una protección eficaz cuando se utilizan concentraciones de fármacos en las que los medicamentos utilizados por sí solos no tienen ningún efecto protector significativo o éste es menor.
De hecho, como se ejemplifica en la figura 1, la combinación mexiletina - cinacalcet protege eficientemente las células neuronales de la toxicidad del glutamato, mientras que la combinación de un solo medicamento no ofrece protección. La combinación de baclofeno - acamprosato (figura 3) da un efecto protector contra la toxicidad del glutamato para las células neuronales corticales. La combinación de baclofeno y acamprosato induce una mejora de más del 200% en comparación con el acamprosato solo y de más del 47% en comparación con el baclofeno utilizado solo.
Tabla 2
B- Efecto protector contra la muerte celular neuronal inducida por isquemia/hipoxia.
Preparación de células corticales neuronales de rata
Las células se preparan como anteriormente.
Ensayos de privación de oxígeno y glucosa (modelo in vitro de isquemia)
El efecto neuroprotector de los compuestos se evalúa mediante la cuantificación de la red de neuritas utilizando el anticuerpo MAP2. El riluzol, un fármaco neuroprotector, (Riluteck®, 5 j M) se utiliza como control positivo.
Después de 10 días de cultivo de neuronas, los fármacos candidatos se resuelven en medio de cultivo (+0,1 % DMSO) y luego son pre-incubados con neuronas durante 1 hora antes de la privación de oxígeno y glucosa. Una hora después de la incubación del fármaco candidato, se retira el medio y se añade un medio recién preparado sin glucosa. Este medio está compuesto por DMEM sin glucosa (Invitrogen) complementado con 2% de B27, L-glutamina 0,2 mM, 1% de solución PS, 1o ng/ml de BDNF. Las células se transfieren a una incubadora anaeróbica con un 95% de N2 y un 5% de CO2 a 37°C.
Después de 2 horas, se añaden 25 mM de D-Glucosa en el medio de cultivo y las células se transfieren a una incubadora clásica con 95% de aire/5% de CO2 a 37°C. Después de 24 horas de reperfusión de glucosa en oxígeno, las células se fijan mediante una solución fría de alcohol/ácido acético durante 5 minutos.
Después de la permeabilización con saponina (Sigma), las células se bloquean durante 2 horas con PBS que contiene 10% de suero de cabra, luego las células se incuban con anticuerpo monoclonal primario de ratón contra MAP2 (MAP2, Sigma). Estos anticuerpos se describen con IgG anti-ratón Alexa Fluor 488 de cabra (Molecular Probes).
Los núcleos de las células se marcan con un marcador fluorescente (solución Hoechst, SIGMA). Se utilizan seis pocillos por condición para evaluar la supervivencia neuronal en 3 cultivos diferentes.
Para cada condición se toman y analizan imágenes 2x10 por pocillo utilizando un InCell Analyzer TM 1000 (GE Healthcare) con un aumento de 20x.
Resultados
Como se muestra en la Tabla 3 a continuación, todas las combinaciones de fármacos reivindicadas dan un efecto protector contra la muerte celular inducida por isquemia/hipoxia para las células neuronales corticales.
Tabla 3
Las figuras 4-6 muestran además que los tratamientos combinados de la invención protegen significativamente a las neuronas de la privación de oxígeno y glucosa. Como se muestra en las figuras 4-6, se observa una protección eficaz utilizando concentraciones de fármacos en la que los medicamentos, por sí solos, no tienen ningún efecto protector significativo. Por ejemplo, se observa una combinación significativa de efecto protector significativo de baclofeno (80 nM)/acamprosato (0,32 nM) o cinacalcet (64 pM)/mexiletina (25,6 pM) o torasemida (80 nM)/sulfisoxazol (1,36 nM), en isquemia, no se obtiene protección significativa cuando el baclofeno, el acamprosato, el cinacalcet, la mexiletina, la torasemida y el sulfisoxazol se utilizan solos a las mismas concentraciones.
Estos resultados demuestran, por lo tanto, un efecto potente y sinérgico de las terapias combinadas respecto al estrés oxidativo y la disfunción mitocondrial o la apoptosis que subyacen en condiciones isquémicas, así como en la EP.
C- Efecto neuro-protector de medicamentos contra los daños por 6-OHDA en neuronas dopaminérgicas
La 6-hidroxidopamina (6-OHDA) es un fármaco neurotóxico que inicia selectivamente la degeneración neuronal de las neuronas dopaminérgicas mediante la generación de especies reactivas de oxígeno y la disfunción respiratoria mitocondrial que se cree que reflejan los eventos que ocurren en un cerebro parkinsoniano. Se utiliza comúnmente la toxicidad de 6-OHDA in vitro e in vivo para estudiar el Parkinsonismo.
Cultivo de neuronas dopaminérgicas mesencefálicas
Fueron cultivadas neuronas dopaminérgicas de ratas como se describe en Schinelli et al.[36]. Se sacrificaron ratas hembra embarazadas de 15 días de gestación por dislocación cervical (Ratas Wistar; Janvier) y se les extrajeron los fetos del útero. Los cerebros medios embrionarios fueron extirpados y colocados en un medio helado de Leibovitz (L15; PanBiotech) con 2% de Penicilina-Estreptomicina (PS; PanBiotech) y el 1% de albúmina sérica bovina (BSA; PanBiotech). Se utilizaron sólo las porciones ventrales de la flexión mesencefálica para las preparaciones celulares, ya que esta es la región del cerebro en desarrollo rico en neuronas dopaminérgicas. Los cerebros medios se disociaron por tripsinización durante 20 min a 37°C (Tripsina EDTA 1X; PanBiotech). La reacción se detiene por la adición de medio Eagle modificado de Dulbecco (DMEM; PanBiotech) con DNAasa I grado II (0,1 mg/ml; PanBiotech) y el 10% del suero fetal de ternera (FCS; Invitrogen). Las células se disociaron mecánicamente mediante 3 pasajes a través de una pipeta de 10 ml y se centrifugaron a 180 x g durante 10 minutos a 4°C en una capa de BSA (3,5%) en medio L15. El sobrenadante fue desechado y las células del pelete fueron resuspendidas en un medio de cultivo definido que consistía en Neurobasal (Invitrogen) complementado con B27 (2%; Invitrogen), L-glutamina (2 mM; PanBiotech) y el 2% de solución PS y 10 ng/ml de factor neurotrófico derivado del cerebro (BDNF, PanBiotech) y 1 ng/ml de factor neurotrófico derivado de la glía (GDNF, PanBiotech). Las células viables se contaron en un citómetro Neubauer utilizando la prueba de exclusión de azul de tripano. Las células se sembraron a una densidad de 40.000 células/pocillo en placas de 96 pocillos (pre-recubiertos con poli-L-lisina (Greiner)) y se cultivaron a 37°C en una atmósfera de aire humidificado (95%)/CO2 (5%). La mitad del medio se cambió cada 2 días con un medio recién preparado. Entre el cinco y seis por ciento de la población de células neuronales fueron neuronas dopaminérgicas.
Exposición a 6-OHDA y a los compuestos de prueba
En el día 6 del cultivo, se retiró el medio y se añadió un medio recién preparado, sin o con 6-OHDA a las siguientes concentraciones: 20 pM durante 48 horas diluido en medio de control. Los compuestos de prueba se preincubaron durante 1h antes de la aplicación de 6-OHDA durante 48 horas.
Evaluación del punto final: medida del número total de neuronas positivas de tirosina hidroxilasa (TH) Después de 48 horas de intoxicación con 6-OHDA, las células fueron fijadas por una solución de 4% de para formaldehido (Sigma) en PBS, pH a 7,3 durante 20 min a temperatura ambiente. Las células se lavaron de nuevo dos veces en PBS, y luego se bloquearon sitios permeabilizados y no específicos con una solución de PBS que contenía 0,1% de saponina (Sigma) y 1% FCS durante 15 minutos a temperatura ambiente. Luego, las células fueron incubadas con anticuerpo monoclonal anti-tirosina hidroxilasa producido en ratón (TH, Sigma) a una dilución de 1/1000 en PBS con 1% de FCS, 0,1% de saponina durante 2 horas a temperatura ambiente. Estos anticuerpos fueron revelados con IgG anti-ratón Alexa Fluor 488 de cabra (Molecular Probes) en una dilución 1/800 en PBS que contenía 1% de FCS, 0,1% de saponina durante 1 hora a temperatura ambiente.
Para cada condición, se tomaron 2 x 10 imágenes (que representaban el 80% del área total del pocillo) por pocillo utilizando InCell AnalyzerTM 1000 (GE Healthcare) con un aumento de 10x. Todas las imágenes fueron tomadas en las mismas condiciones. El análisis del número de neuronas positivas TH se realizó utilizando el software Developer (GE Healthcare).
Los datos se expresan en porcentaje de las condiciones de control (sin intoxicación, sin 6-OHDA a 100%) para expresar los daños por 6-OHDA. Todos los valores se expresan como media /- SEM (es decir, media) de los 3 cultivos (n a 6 pocillos por condición por cultivo). Los análisis estadísticos consisten en un ANOVA seguido de las pruebas de Dunnett y PLSD Fisher cuando se permitía el uso de la versión 5.0 del software Statview.
Resultados
Se observa un efecto neuroprotector para las combinaciones de la invención en la prueba de supervivencia de las neuronas TH después de 48 horas de daño por 6-OHDA en las neuronas dopaminérgicas.
Una incubación de 48h de 6-OHDA (20 pM) con neuronas mesencefálicas produjo una intoxicación significativa de las neuronas dopaminérgicas (alrededor del -33% de las neuronas TH) en todos los experimentos (control, figuras 7 9, 12-14).
Se utilizó BDNF como control positivo. Una hora de pretratamiento con BDNF a 1,85 nM protegió significativamente a las neuronas dopaminérgicas de este daño por 6-OHDA.
Como se muestra en la tabla 4 a continuación, todas las combinaciones de fármacos reivindicados dan un efecto protector contra los daños por 6-OHDA en las células neuronales dopaminérgicas.
Tabla 4
Como se muestra en las figuras 7-9 y 12-14, el baclofeno-acamprosato, baclofeno-torasemida, mexiletina-cinacalcet, acamprosato-cinacalcet, cinacalcet-tadalafil protegen con éxito las neuronas dopaminérgicas frente a la toxicidad por 6-OHDA.
En particular, la combinación de baclofeno-acamprosato se muestra eficaz en la protección, in vitro, de las neuronas dopaminérgicas para una amplia gama de concentraciones de baclofeno (de 16 nM a 400 nM) y acamprosato (de 4 pM a 1600 pM).
Además, los inventores han podido dibujar las curvas de dosis-respuesta para cada baclofeno, acamprosato, cinacalcet y tadalafil (no mostrados), lo que permite además determinar el índice combinatorio (IC) de la combinación de estos fármacos según Loewe [33,34]. Un índice combinatorio por debajo de 1 caracteriza la existencia de sinergia entre los medicamentos para una combinación dada.
Como se ilustra en la figura 12, también se encuentra que la mezcla de baclofeno-acamprosato que muestra una actividad sinérgica en los modelos anteriores de toxicidad e isquemia de glutamato in vitro, también se encuentra como que tiene una actividad sinérgica en el modelo de toxicidad por 6-OHDA. Por ejemplo, el baclofeno a 32 nM, cuando se combina con acamprosato a 4 pM o 10 pM, muestra una actividad protectora sinérgica (S, figura 12) en células neuronales dopaminérgicas intoxicadas con 6-OHDA, con un CI de 0,4 ó 0,5, respectivamente.
También se encontró que las combinaciones probadas de acamprosato-cinacalcet a diferentes concentraciones de fármacos tenían un efecto protector sinérgico contra la toxicidad inducida por 6-OHDA. Su efecto neuroprotector es particularmente importante, especialmente cuando se tienen en cuenta las concentraciones tan bajas de los fármacos, como se ilustra en la figura 13 y la tabla 5. Los índices combinatorios relacionados con las diferentes composiciones probadas están, con mucho, por debajo del límite de 1, lo que denota un fuerte efecto protector sinérgico de la mezcla acamprosato-cinacalcet en las neuronas dopaminérgicas (tabla 5).
Tabla 5
Las combinaciones probadas de cinacalcet-tadalafil también se encontraron que eran eficientes en la protección de las neuronas dopaminérgicas respecto a la toxicidad por 6-OHDA. Este efecto protector contra la toxicidad inducida por 6-OHDA se ha encontrado que era sinérgico para varias dosis de fármacos individuales. Su efecto neuroprotector se ilustra en la figura 14. Los índices combinatorios relacionados con las diferentes composiciones probadas están por debajo del límite de 1, lo que denota un fuerte efecto protector sinérgico de la mezcla cinacalcet-tadalafil en neuronas dopaminérgicas (tabla 6).
Tabla 6
D- Efectos sobre la pérdida neuronal dopaminérgica in vivo y en los síntomas motores
1) Mejora de la aquinesia in vivo
Procedimiento quirúrgico y de cría de animales
Se utilizaron ratas Wistar (5 semanas) después de un período de aclimatación de al menos 5 días. Se realizó una cirugía bajo ketamina (50 mg/kg) y xilazina (10 mg/kg). Los animales recibieron una inyección unilateral de 12 |jg de 6-OHDA (Sigma Aldrich) disuelto en 6 j l de NaCl estéril al 0,9% con 0,1% de ácido ascórbico (para proteger 6-OHDA de la oxidación), a un caudal de 1 jl/min, en la sustancia nigra pars compacta izquierda. Las coordenadas estereotáxicas del lugar de inyección fueron: anteroposterior 2,2 mm, lateral 2,0 mm, dorsoventral 3 mm con la barra incisiva a 5,0 mm por encima del plano interaural, según el atlas estereotáxico de ratas de De Groot (1959) [37].
Tratamiento con el medicamento o los medicamentos
La primera administración de tratamiento o vehículo se realizó el día anterior a la inyección estereotáxica de 6-OHDA (para los grupos de daños) o vehículo y a lo largo de los 15 días anteriores a las pruebas de comportamiento.
Las ratas del grupo de tratamiento de referencia se administraron con una combinación de L-DOPA (8 mg/kg) y benserazida (un inhibidor periférico de la descarboxilasa DPA, 12,5 mg/kg). Durante el estudio y para cada animal, el volumen de administraciones per os se determinó sobre la base del peso corporal medio de los animales del grupo correspondiente. Los pesos corporales se determinaron dos veces por semana y el volumen de administración se ajustó en consecuencia.
Los vehículos y compuestos se administraron dos veces al día (es decir, bid: bis in die) a través de la vía oral, por la mañana y por la tarde; ocho horas (+/- 30 min) separadas las dos administraciones alrededor de las 9:30 AM y alrededor de las 17:30 PM.
El día de las pruebas de comportamiento, los medicamentos se administraron alrededor de 1 hora para el grupo tratado con L-DOPA y alrededor de 2 horas (+/- 15 min) para las combinaciones de fármacos antes de la prueba conductual, para cada animal.
Pruebas de comportamiento
Cada prueba se realizó antes de la cirugía (2 o 3 días antes) para determinar el valor del nivel basal. La evaluación de las funciones conductuales se realizó 15 días después de la inyección quirúrgica de 6-OHDA utilizando las dos pruebas diferentes.
Prueba de tiempo de iniciación (ITT):El animal fue sujetado por un técnico ilustrado frente a una superficie plana. Sólo una de las dos extremidades delanteras quedó libre para moverse. El tiempo necesario para iniciar el movimiento hacia la superficie del plano se registró utilizando 180 s como punto final [38].
Prueba de caminar (ST):La rata fue sujetada por el experimentador y sólo una de las dos extremidades delanteras se dejaron libres para moverse por encima de una superficie plana. La otra mano fijó la extremidad delantera para no fuera monitoreada con una pata tocando la mesa. El animal se desplazaba lentamente hacia atrás o hacia adelante (5 s durante 0,9 m) por el experimentador. Se contó el número de pasos de ajuste para la pata derecha [38].
Prueba del cilindro (CT): La rata se colocó en un cilindro de plexiglás e, inmediatamente después, se grabó en vídeo durante 15 minutos para examinar la simetría/asimetría del uso de sus patas delanteras durante el comportamiento exploratorio en este nuevo entorno. Se determinó el número de contactos realizados en la pared del cilindro durante este período con la pata ipsilateral, la pata contralateral, y con ambas patas (contactos dobles) y se expresó como un porcentaje del número total de contactos [39,40].
Resultados
Se llevaron a cabo ensayos in vivo con combinaciones de fármacos de la invención. Las combinaciones de fármacos probadas de la invención indujeron una mejora significativa, ya sea en la prueba de tiempo de iniciación o en la prueba de caminar (tabla 7).
Tabla 7
Como se ilustra en las figuras 10 y 11, las combinaciones de fármacos de la invención protegen considerablemente a las ratas frente a las lesiones estereofólicas por 6-OHDA. Cabe destacar que el tratamiento con una combinación de baclofeno-acamprosato da como resultado un alivio casi completo de la acinesia en la prueba de caminar y en la prueba de iniciación, de manera dependiente de la dosis.
Este efecto en las combinaciones de la invención con respecto a la acinesia también se evaluó en una prueba diferente (prueba del cilindro) también utilizada para evaluar la acinesia. Los resultados se ilustran en la figura 15 y muestran que la combinación de baclofeno-acamprosato (3,75 mg/kg bid y 0,25 mg/kg bid, respectivamente) alivia la reducción de los contactos dobles en el cilindro inducida por la intoxicación por 6-OHDA, lo que muestra una mejora del comportamiento motor espontáneo en rata.
Se han probado varias dosis y proporciones de los medicamentos para la combinación de baclofeno-acamprosato. Los resultados recogidos en la tabla 8 a continuación confirman que una amplia gama de dosis o proporciones de baclofeno y acamprosato son eficientes para contrarrestar la aquinesia inducida por la inyección estereotáxica de 6-OHDA.
Tabla 8
2) La mejora de la acinesia in vivo está relacionada con una menor pérdida neuronal en los animales tratados Preparación de tejidos para el análisis macrohistológico
Todos los animales se sacrificaron por inyección letal de pentobarbital. Los cerebros fueron rápidamente retirados, luego se congelaron en hielo seco y se almacenaron a -80°C.
Preparación de cortes de estriado: Las secciones de tejido coronal (10 m de espesor) a nivel de estriado se cortaron a -20°C con un criostato (HM560). Tres secciones estriadas seriales por animal fueron montadas en portas de vidrio SuperFrost Plus (Fisher Scientific) y almacenadas a -80°C hasta su análisis histológico.
Preparación de cortes de sustancia nigra pars compacta (SN): los cortes se distribuyeron en tres conjuntos de secciones que cubrían todo el SN (coordenadas: -4,8, -5,3 y -5,8mm AP de bregma). Los cortes del SN, después de los enjuagues, se sumergieron en 0,3% de H2O2, se preincubaron durante 30 min en PBS con 5% de BSA, y luego se incubaron durante la noche en la misma solución con un anticuerpo monoclonal antitirosina hidroxilasa (TH, Sigma) a una dilución de 1/1000. Posteriormente, la sección se incubó durante dos horas con un anticuerpo secundario antiratón marcado con tinte.
Marcaje de las neuronas terminales dopaminérgicas en estriado con tinción de [3H]-mazindol
La pérdida de terminales DA en el estriado se evaluó como un índice del grado de denervación dopaminérgica mediante el análisis de la unión de [3H]-mazindol a los sitios de captación de dopamina [40]. De hecho, el mazindol es un bloqueador del transportador de reabsorción de dopamina que se utiliza comúnmente para marcar las neuronas dopaminérgicas en biología experimental.
Brevemente, la sección del estriado se secó al aire (con un secador de aire de laboratorio) y se enjuagó durante 5 minutos en tampón Tris 50 mM con NaCl 120 mM y 5 mM de KCl. Luego, fueron incubados durante 40 min con 15 nM de [3H]-mazindol (NEN, DuPont; actividad específica, 17 Ci/mM) en tampón Tris 50 mM con 300 mM de NaCl y 5 mM de KCl añadidos con 0,3 mM de desipramina para bloquear los sitios de absorción de noradrenalina. Las secciones se enjuagaron dos veces durante 3 minutos en el tampón de incubación de Tris y durante 10 s en agua destilada y se secaron al aire. Fue expuesto película fotográfica sensible a [3H] (Kodak BioMax MS Film, Sigma) a los cortes en casetes de rayos X y a temperatura ambiente durante 3 semanas. Los niveles del marcaje con [3H]-mazindol se cuantificaron mediante un análisis de imágenes digitalizado a partir de los autoradiogramas de película utilizando como sistema de análisis BIOCOM (Densirag, BIOCOM). Los niveles grises se convirtieron en densidades ópticas (OD) utilizando estándares externos (comprimido de paso de densidad calibrada, Kodak). El valor medio de la OD se determinó a partir de tres secciones por animal después de restar la señal de fondo medida en cada sección escaneada de un área del cuerpo calloso que se sabe que carece de terminales DA.
Cuantificación de las neuronas positivas TH en el SN
Las neuronas positivas TH se contaron en un conjunto de las tres secciones centradas en la pista de la aguja de inyección 6-OHDA en el SN, cubriendo casi todo el SN. La especificidad del daño de las neuronas DA, las células globales en el SN se cuentan en secciones marcadas de azul de toluidina de la misma región. El recuento de células se realiza mediante un microscopio conectado a un sistema de análisis de imágenes con computadora y una cámara CDD.
Resultados
La inyección de 6-OHDA en el SN izquierdo da como resultado una disminución de la densidad de los cuerpos celulares DA en el SN y la densidad de los terminales DA en el lado izquierdo del estriado (figura 16). La L-DOPA, que se reconoce como el único tratamiento sintomático de la EP, no inhibió esta pérdida inducida por 6-OHDA de las neuronas. La administración de la dosis 3 de la combinación de baclofeno-acamprosato (3,75 mg/kg bid y 0,25 mg/kg bid, respectivamente) indujo una elevación estadísticamente significativa de las neuronas DA en el SN y también en el estriado en comparación con los animales no tratados (figura 16). Por lo tanto, la combinación de baclofeno-acamprosato ofrece una protección real de las neuronas DA contra la degeneración inducida por 6-OHDA a diferencia de L-DOPA, el tratamiento actualmente más eficiente aunque sólo de forma sintomática. No sólo los cuerpos celulares de las neuronas DA del SN, sino que también los terminales nerviosos en el estriado están protegidos; por lo tanto, esta protección parece actuar también contra una degeneración neuronal anterógrada. Referencias
1 De Lau LML & Breteler MMB (2006) Epidemiology of Parkinson's disease. Lancet Neurol. 5, 525-35.
2 Samii A, Nutt JG & Ransom BR (2004) Parkinson's disease. Lancet 363, 1783-93.
3 Savitt JM, Dawson VL & Dawson TM (2006) Diagnosis and treatment of Parkinson disease: molecules to medicine. J. Clin. Invest. 116, 1744-54.
4 Schapira AH & Jenner P (2011) Etiology and pathogenesis of Parkinson's disease. Mov. Disord. 26, 1049-55. 5 Gao H-M & Hong J-S (2011) Gene-environment interactions: key to unraveling the mystery of Parkinson's disease. Prog. Neurobiol. 94, 1-19.
6 Kahle PJ, Waak J & Gasser T (2009) DJ-1 and prevention of oxidative stress in Parkinson's disease and other agerelated disorders. Free Radic. Biol. Med. 47, 1354-61.
7 Lee DW, Rajagopalan S, Siddiq A, Gwiazda R, Yang L, Beal MF, Ratan RR & Andersen JK (2009) Inhibition of prolyl hydroxylase protects against 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine-induced neurotoxicity: model for the potential involvement of the hypoxia-inducible factor pathway in Parkinson disease. J. Biol. Chem. 284, 29065-76. 8 Abbott A (2010) Levodopa: the story so far. Nature 466, S6-7.
9 Rascol O, Lozano A, Stern M & Poewe W (2011) Milestones in Parkinson's disease therapeutics. Mov. Disord. 26, 1072-82.
10 Obeso JA, Rodriguez-Oroz MC, Goetz CG, Marin C, Kordower JH, Rodriguez M, Hirsch EC, Farrer M, Schapira AH V & Halliday G (2010) Missing pieces in the Parkinson's disease puzzle. Nat. Med. 16, 653-61.
11 Ettmayer P, Amidon GL, Clement B & Testa B (2004) Lessons learned from marketed and investigational prodrugs. J. Med. Chem. 47, 2393-404.
12 Beaumont K, Webster R, Gardner I & Dack K (2003) Design of ester prodrugs to enhance oral absorption of poorly permeable compounds: challenges to the discovery scientist. Curr. Drug Metab. 4, 461-85.
13 Heimbach T, Oh DM, Li LY, Rodriguez-Hornedo N, García G & Fleisher D (2003) Enzyme-mediated precipitation of parent drugs from their phosphate prodrugs. Int. J. Pharm. 261, 81-92.
14 Yang CY, Dantzig AH & Pidgeon C (1999) Intestinal peptide transport systems and oral drug availability. Pharm. Res. 16, 1331-43.
15 Steffansen B, Nielsen CU, Brodin B, Eriksson AH, Andersen R & Frokjaer S (2004) Intestinal solute carriers: an overview of trends and strategies for improving oral drug absorption. Eur. J. Pharm. Sci. 21, 3-16.
16 Stella VJ (2007) Prodrugs: challenges and rewards. (A. Press and Springer, eds.) Springer Singapore Pte. Limited, New-York.
17 Wermuth CG (2003) Designing prodrugs and bioprecusrors. In The Practice of Medicinal Chemistry (Hardbound, ed), 2nd ed., pp. 561-585. Academic Press.
18 Pezron I, Mitra AK, Duvvuri S & Tirucherai GS (2002) Prodrug strategies in nasal drug delivery. Expert Opin. Ther. Pat. 12, 331-340.
19 Stella VJ (2004) Prodrugs as therapeutics. Expert Opin. Ther. Pat. 14, 277-280.
20 Stella VJ & Nti-Addae KW (2007) Prodrug strategies to overcome poor water solubility. Adv. Drug Deliv. Rev. 59, 677-94.
21 Higuchi T & Stella VJ (1975) Pro-drugs as Novel Drug Delivery System, ACS Sympos American Chemical Society, Washington, DC.
22 Roche EB (1977) Design of biopharmaceutical properties through prodrugs and analogs: a symposium, American P The Academy, Washington, DC.
23 Lal R, Sukbuntherng J, Tai EHL, Upadhyay S, Yao F, Warren MS, Luo W, Bu L, Nguyen S, Zamora J, Peng G, Dias T, Bao Y, Ludwikow M, Phan T, Scheuerman RA, Yan H, Gao M, Wu QQ, Annamalai T, Raillard SP, Koller K, Gallop MA & Cundy KC (2009) Arbaclofen placarbil, a novel R-baclofen prodrug: improved absorption, distribution, metabolism, and elimination properties compared with R-baclofen. J. Pharmacol. Exp. Ther. 330, 911-21.
24 Xu F, Peng G, Phan T, Dilip U, Chen JL, Chernov-Rogan T, Zhang X, Grindstaff K, Annamalai T, Koller K, Gallop MA & Wustrow DJ (2011) Discovery of a novel potent GABA(B) receptor agonist. Bioorg. Med. Chem. Lett. 21, 6582 5.
25 Hanafi R, Mosad S, Abouzid K, Niess R & Spahn-Langguth H (2011) Baclofen ester and carbamate prodrug candidates: a simultaneous chromatographic assay, resolution optimized with DryLab. J. Pharm. Biomed. Anal. 56, 569-76.
26 Leach AR & Gillet VJ An Introduction to Chemoinformatics (Springer-Verlag New York Inc, ed.).
27 Rahman SA, Bashton M, Holliday GL, Schrader R & Thornton JM (2009) Small Molecule Subgraph Detector (SMSD) toolkit. J. Cheminform. 1, 12.
28 Neugebauer G, Besenfelder E & von Mollendorff E (1988) Pharmacokinetics and metabolism of torasemide in man. Arzneimittelforschung. 38, 164-6.
29 Stahl H & Wermuth CG (2011) Pharmaceutical salts: Properties, selection, and use, 2nd ed. (Wiley-VCH, ed.). 30 Gennaro AR (2000) Remington: The Science and Practice of Pharmacy, 20th ed. (A. D. Gennaro, W. Lippincott, and Wilkins, eds.) Lippincott Williams & Wilkins.
31 Swarbrick J & Boylan JC (eds.) Encyclopedia of Pharmaceutical Technology Dekker, Marcel, New-York.
32 Slinker BK (1998) The Statistics of Synergism. J. Mol. Cell. Cardiol. 30, 723-731.
33 LOEWE S (1953) The problem of synergism and antagonism of combined drugs. Arzneimittelforschung. 3, 285 90.
34 Grabovsky Y & Tallarida RJ (2004) Isobolographic analysis for combinations of a full and partial agonist: curved isoboles. J. Pharmacol. Exp. Ther. 310, 981-6.
35 Singer CA, Figueroa-Masot XA, Batchelor RH & Dorsa DM (1999) The mitogen-activated protein kinase pathway mediates estrogen neuroprotection after glutamate toxicity in primary cortical neurons. J. Neurosci. 19, 2455-63.
36 Schinelli S, Zuddas A, Kopin IJ, Barker JL & di Porzio U (1988) 1-Methyl-4-phenyl-1,2,3,6-tetrahydropyridine metabolism and 1-methyl-4-phenylpyridinium uptake in dissociated cell cultures from the embryonic mesencephalon. J. Neurochem. 50, 1900-7.
37 De GROOT (1959) The rat hypothalamus in stereotaxic coordinates. J. Comp. Neurol. 113, 389-400.
38 Olsson M, Nikkhah G, Bentlage C & Bjorklund A (1995) Forelimb akinesia in the rat Parkinson model: differential effects of dopamine agonists and nigral transplants as assessed by a new stepping test. J. Neurosci. 15, 3863-75.
39 Lundblad M, Andersson M, Winkler C, Kirik D, Wierup N & Cenci MA (2002) Pharmacological validation of behavioural measures of akinesia and dyskinesia in a rat model of Parkinson's disease. Eur. J. Neurosci. 15, 120-32.
40 Jouve L, Salin P, Melon C & Kerkerian-Le Goff L (2010) Deep brain stimulation of the center medianparafascicular complex of the thalamus has efficient anti-parkinsonian action associated with widespread cellular responses in the basal ganglia network in a rat model of Parkinson's disease. J. Neurosci. 30, 9919-28.
Claims (24)
1. Una composición para su uso en el tratamiento del parkinsonismo en un sujeto necesitado del mismo que comprende tadalafil y cinacalcet, o sales de los mismos, o formulación o formulaciones de liberación sostenida de los mismos.
2. La composición para su uso según la reivindicación 1, que comprende además un compuesto seleccionado de acamprosato, baclofeno, mexiletina, sulfisoxazol y torasemida, o sales de los mismos, o un profármaco o varios profármacos de los mismos seleccionados de arbaclofeno, placarbil y sulfisoxazol acetilo, o formulación o formulaciones de liberación sostenida de los mismos.
3. La composición para su uso de la reivindicación 2, que comprende al menos una de las siguientes combinaciones de compuestos:
- tadalafil, cinacalcet y mexiletina,
-tadalafil, cinacalcet y acamprosato, o
-tadalafil, cinacalcet y baclofeno (o su profármaco arbaclofeno placarbil),
o sales de los mismos, o una formulación o varias formulaciones de liberación sostenida de las mismas.
4. La composición para su uso de acuerdo con cualquiera de las reivindicaciones anteriores que comprende además al menos un compuesto seleccionado de un precursor de la dopamina, un agonista del receptor de dopamina, o un inhibidor de una enzima metabolizante de la dopamina.
5. La composición para su uso según la reivindicación 4, donde el precursor de la dopamina es un compuesto seleccionado de levodopa o melevodopa, o sales o formulaciones de liberación sostenida de la misma; el agonista del receptor de dopamina es un compuesto seleccionado del grupo compuesto de talifoexel, piribedil, rotigotina, bromocriptina, pergolida, cabergolina, lisurida, pramipexol, ropinirol o apomorfina, o sales o formulaciones de liberación sostenida de los mismos; y el inhibidor de una enzima metabolizante de la dopamina es un compuesto seleccionado del grupo que consiste en carbidopa, benserazida, entacapona, tolcapona, selegilina y rasagilina, o sales o formulaciones de liberación sostenida de los mismos.
6. La composición para su uso según la reivindicación 5, que comprende al menos una de las siguientes combinaciones de compuestos:
- tadalafil, cinacalcet y levodopa,
-tadalafil, cinacalcet, mexiletina y levodopa,
-tadalafil, cinacalcet, acamprosato y levodopa, o
-tadalafil, cinacalcet, baclofeno y levodopa,
o sales de la misma o una formulación o varias formulaciones de liberación sostenida de la misma.
7. La composición para su uso según la reivindicación 6 que comprende además al menos un compuesto seleccionado de carbidopa, benserazida, entacapona, tolcapona, selegilina y rasagilina, o una formulación de sal o liberación sostenida de los mismos.
8. La composición para su uso según la reivindicación 7, en la que dicho al menos un compuesto es carbidopa, o una sal o formulación de liberación sostenida de la misma.
9. La composición para su uso según la reivindicación 5, que comprende la administración a dicho sujeto de al menos una de las siguientes combinaciones de compuestos:
- tadalafil, cinacalcet y selegilina o rasagilina,
-tadalafil, cinacalcet, mexiletina y selegilina o rasagilina,
-tadalafil, cinacalcet, acamprosato y selegilina o rasagilina, o
-tadalafil, cinacalcet, baclofeno y selegilina o rasagilina,
o sales o formulaciones de liberación sostenida de las mismas.
10. La composición para el uso de cualquiera de las reivindicaciones anteriores, que comprende además un vehículo o excipiente farmacéuticamente aceptable.
11. La composición para el uso de cualquiera de las reivindicaciones anteriores, en la que los compuestos están formulados para ser administrados juntos o por separado.
12. La composición para el uso de cualquiera de las reivindicaciones anteriores, en la que los compuestos se formulan para ser administrados repetidamente al sujeto.
13. La composición para el uso de cualquiera de las reivindicaciones anteriores, en la que los compuestos están formulados para ser administrados por vía oral.
14. La composición para el uso de cualquiera de las reivindicaciones anteriores, en la que el sujeto sufre de una condición seleccionada de la enfermedad de Parkinson, parálisis supranuclear progresiva, atrofia del sistema múltiple, degeneración gangliónica cortical-basal, demencia con cuerpos de Lewy difusiva, demencia de Parkinson, distonía-parkinsonismo ligado al cromosoma X y parkinsonismo secundario.
15. La composición para el uso de cualquiera de las reivindicaciones anteriores, en la que el sujeto está sufriendo de una condición seleccionada de la enfermedad de Parkinson, demencia con cuerpos de Lewy y atrofia del sistema múltiple.
16. La composición de cualquiera de las reivindicaciones 1-13, para su uso en la protección de las neuronas dopaminérgicas del sistema nigroestriatal del sujeto de la degeneración o la muerte.
17. La composición de cualquiera de las reivindicaciones 1-13, para su uso en el tratamiento de la bradicinesia o aquinesia en dicho sujeto.
18. La composición de cualquiera de las reivindicaciones 1-13, para su uso en el tratamiento preventivo de un sujeto en riesgo de parkinsonismo.
19. Una composición que incluya tadalafil y cinacalcet o cualesquiera sales farmacéuticamente aceptables de los mismos, o una formulación de liberación sostenida de los mismos.
20. La composición de la reivindicación 19 que comprende además un compuesto seleccionado de acamprosato, baclofeno, mexiletina, sulfisoxazol y torasemida, cualesquiera sales farmacéuticamente aceptable de los mismos, o una formulación de liberación sostenida de los mismos.
21. La composición de la reivindicación 20, que comprende al menos una de las combinaciones seleccionadas de: - tadalafil, cinacalcet y mexiletina,
-tadalafil, cinacalcet y acamprosato, o
-tadalafil, cinacalcet y baclofeno,
o sales de los mismos o formulaciones de liberación sostenida de las mismas.
22. La composición según cualquiera de las reivindicaciones 19 ó 21 que comprende además la levodopa o cualquier sal farmacéuticamente aceptable de la misma o formulación de liberación sostenida de la misma.
23. La composición según cualquiera de las reivindicaciones 19 ó 21 que comprende además selegilina o rasagilina, o cualesquiera sales farmacéuticamente aceptables de la misma o formulación de liberación sostenida de las mismas.
24. La composición de la reivindicación 22 que comprende además al menos un compuesto seleccionado de carbidopa, benserazida, entacapona, tolcapona, selegilina y rasagilina, o cualquier sal farmacéuticamente aceptable de la misma o formulación de liberación sostenida de la misma.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14/473,142 US9248111B2 (en) | 2011-03-01 | 2014-08-29 | Therapeutic approaches for treating parkinson's disease |
| PCT/EP2015/069783 WO2016030522A1 (en) | 2014-08-29 | 2015-08-28 | New therapeutic approaches for treating parkinson's disease |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2749082T3 true ES2749082T3 (es) | 2020-03-19 |
Family
ID=54072810
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15762523T Active ES2749082T3 (es) | 2014-08-29 | 2015-08-28 | Nuevos enfoques terapéuticos para tratar la enfermedad de Parkinson |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US9248111B2 (es) |
| EP (2) | EP3563841A1 (es) |
| CN (1) | CN107106521B (es) |
| ES (1) | ES2749082T3 (es) |
| WO (1) | WO2016030522A1 (es) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9248111B2 (en) | 2011-03-01 | 2016-02-02 | Pharnext | Therapeutic approaches for treating parkinson's disease |
| US9241933B2 (en) | 2011-03-01 | 2016-01-26 | Pharnext | Compositions for treating amyotrophic lateral sclerosis |
| BR112013022112B1 (pt) | 2011-03-01 | 2021-09-28 | Pharnext | Composição que compreende baclofeno e acamprosato |
| US9867837B2 (en) | 2011-03-01 | 2018-01-16 | Pharnext | Compositions for treating neurological disorders |
| US9931326B2 (en) | 2011-03-29 | 2018-04-03 | Pharnext | Composition comprising torasemide and baclofen for treating neurological disorders |
| AU2015217796B2 (en) | 2014-02-11 | 2020-04-30 | Pharnext | Combination of baclofen, acamprosate and medium chain triglycerides for the treatment of neurological disorders |
| EP3156050A1 (en) * | 2015-10-16 | 2017-04-19 | Universitat Autònoma De Barcelona | New combination therapies for treating neurological damage |
| CA3012900A1 (en) | 2016-02-05 | 2017-08-10 | Pharnext | Novel combinatorial therapies of neurological disorders |
| RU2618620C1 (ru) * | 2016-03-22 | 2017-05-04 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Курский государственный университет" | Способ фармакологической коррекции экспериментальной ишемии скелетной мышцы тадалафилом и пентоксифиллином в условиях комбинированной терапии |
| US10736876B2 (en) | 2017-04-24 | 2020-08-11 | Pharnext | Idalopirdine-based combinatorial therapies of Alzheimer's disease |
| WO2025075499A1 (en) * | 2023-10-02 | 2025-04-10 | Universiteit Van Amsterdam | Reducing dopamine feed-back inhibition in dopaminergic cells by tadalafil. |
Family Cites Families (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2044853C (en) | 1990-07-19 | 2004-11-09 | Susan A. Greenfield | Method for treating parkinson's disease employing an atp-sensitive potassium channel blocker |
| DE4113820A1 (de) | 1991-04-27 | 1992-10-29 | Boehringer Mannheim Gmbh | Verwendung von torasemid zur behandlung von hirnoedemen |
| US5721263A (en) | 1993-06-07 | 1998-02-24 | Takeda Chemical Industries, Ltd. | Pharmaceutical composition for angiotensin II-mediated diseases |
| US6573251B2 (en) | 1994-03-30 | 2003-06-03 | Denis Barritault | Drug and pharmaceutical composition for the treatment of lesions of the nervous system and fractions enriched in heparan sulfate |
| US6391922B1 (en) | 1998-01-13 | 2002-05-21 | Synchroneuron, Llc | Treatment of posttraumatic stress disorder, obsessive-compulsive disorder and related neuropsychiatric disorders |
| US5952389A (en) | 1998-01-13 | 1999-09-14 | Synchroneuron | Methods of treating tardive dyskinesia and other movement disorders |
| WO2001058476A2 (en) | 2000-02-11 | 2001-08-16 | The European Molecular Biology Laboratory | Methods and compositions for treatment of alzheimer's disease by enhancing plasmin or plasmin-like activity |
| UA73981C2 (en) * | 2000-03-10 | 2005-10-17 | Merck Patent Gmbh | (r)-(-)-2-[5-(4-fluorophenyl)-3-pyridylmethylaminomethyl]-chromane for treatment of extrapyramidal movement disorders (variants), pharmaceutical composition and kit |
| OA12983A (en) | 2001-07-19 | 2006-10-13 | Pharmacia Corp | Combination of an aldosterone receptor antagonist and an HMG COA reductase inhibitor. |
| FR2829028B1 (fr) * | 2001-08-29 | 2004-12-17 | Aventis Pharma Sa | Association d'un antagoniste du recepteur cb1 et d'un produit qui active la neurotransmission dopaminergique dans le cerveau, les compositions pharmaceutiques les contenant et leur utilisation pour le traitement de la maladie de |
| WO2003077902A1 (en) | 2002-02-19 | 2003-09-25 | Xenoport, Inc. | Methods for synthesis of prodrugs from 1-acyl-alkyl derivatives and compositions thereof |
| PL373032A1 (en) | 2002-03-18 | 2005-08-08 | Pharmacia Corporation | Combination of an aldosterone receptor antagonist and nicotinic acid or a nicotinic acid derivative |
| US8980952B2 (en) | 2002-03-20 | 2015-03-17 | University Of Maryland, Baltimore | Methods for treating brain swelling with a compound that blocks a non-selective cation channel |
| US20040102525A1 (en) | 2002-05-22 | 2004-05-27 | Kozachuk Walter E. | Compositions and methods of treating neurological disease and providing neuroprotection |
| HUE029417T2 (en) | 2002-10-10 | 2017-02-28 | Ono Pharmaceutical Co | Microspheres containing ONO-1301 |
| PT1660440E (pt) | 2003-08-20 | 2012-05-15 | Xenoport Inc | Pró-fármacos de aciloxialquilcarbamato, métodos de síntese e utilização |
| WO2005066122A2 (en) | 2003-12-30 | 2005-07-21 | Xenoport, Inc. | Synthesis of acyloxyalkyl carbamate prodrugs and intermediates thereof |
| EP1837034A4 (en) | 2004-11-30 | 2009-08-05 | Anges Mg Inc | MEDICATION FOR ALZHEIMER'S DISEASE |
| US20080188510A1 (en) | 2005-05-23 | 2008-08-07 | Eisai R & D Management Co., Ltd. | Novel methods using zonisamide |
| EP2314289A1 (en) | 2005-10-31 | 2011-04-27 | Braincells, Inc. | Gaba receptor mediated modulation of neurogenesis |
| CN101365451A (zh) | 2005-11-21 | 2009-02-11 | 阿拉巴马大学董事会 | 使用小分子化合物用于神经保护的方法 |
| AU2007269090A1 (en) | 2006-07-06 | 2008-01-10 | Roskamp Research Llc | Compounds and combinations thereof for inhibiting beta-amyloid production and methods of use thereof |
| WO2008046014A1 (en) | 2006-10-12 | 2008-04-17 | Remedy Pharmaceuticals, Inc. | Treatment of alzheimer's disease using compounds that reduce the activity of non-selective ca++- activated atp-sensitive cation channels regulated by sur1 receptors |
| CA2674610C (en) | 2007-01-11 | 2013-06-18 | Xenoport, Inc. | Sustained release oral dosage forms of a prodrug of r-baclofen and methods of treatment |
| CN101754758B (zh) | 2007-05-22 | 2012-10-24 | 大塚制药株式会社 | 一种用于治疗阿尔茨海默氏症的包含喹诺酮衍生物和多奈哌齐的药物 |
| WO2009000406A1 (en) | 2007-06-22 | 2008-12-31 | Bayer Healthcare Ag | Use of antibodies against the cd52 antigen for the treatment of neurological disorders, particularly transmissible spongiform encephalopathy and alzheimer's disease |
| US7994218B2 (en) | 2007-09-07 | 2011-08-09 | Xenoport, Inc. | Simple pantoic acid ester neopentyl sulfonyl ester cyclization release prodrugs of acamprosate, compositions thereof, and methods of use |
| WO2009033079A1 (en) | 2007-09-07 | 2009-03-12 | Xenoport, Inc. | Externally masked neopentyl sulfonyl ester cyclization release prodrugs of acamprosate, compositions thereof, and methods of use |
| US20090099253A1 (en) | 2007-10-15 | 2009-04-16 | Xenoport, Inc. | Internally Masked Neopentyl Sulfonyl Ester Cyclization Release Prodrugs of Acamprosate, Compositions Thereof, and Methods of Use |
| US20090118365A1 (en) | 2007-11-06 | 2009-05-07 | Xenoport, Inc | Use of Prodrugs of GABA B Agonists for Treating Neuropathic and Musculoskeletal Pain |
| EP2065038A1 (en) | 2007-11-30 | 2009-06-03 | Pharnext | New therapeutic approaches for treating Charcot-Marie-Tooth disease |
| US20100137442A2 (en) | 2008-02-01 | 2010-06-03 | Xenoport, Inc. | Sustained Release Particulate Oral Dosage Forms of (R)-Baclofen and Methods of Treatment |
| WO2009096985A1 (en) | 2008-02-01 | 2009-08-06 | Xenoport, Inc. | Sustained release particulate oral dosage forms of (r)-baclofen prodrugs and methods of treatment |
| CN104127434B (zh) | 2008-04-29 | 2017-10-13 | 法奈科斯公司 | 使用唑尼沙胺和阿坎酸治疗阿尔茨海默病和相关病症的组合组合物 |
| MX2010011881A (es) | 2008-04-29 | 2011-07-01 | Pharnext | Nuevos enfoques terapeuticos para tratar la enfermedad de alzheimer y trastornos relacionados mediante una modulacion de la angiogenesis. |
| CA2722314C (en) | 2008-04-29 | 2018-01-02 | Pharnext | New therapeutic approaches for treating alzheimer disease and related disorders through a modulation of cell stress response |
| EP2135607A1 (en) | 2008-06-18 | 2009-12-23 | Pharnext | Combination of pilocarpin and methimazol for treating Charcot-MarieTooth disease and related disorders |
| RU2489433C9 (ru) | 2008-11-27 | 2014-06-10 | Нэшнл Юниверсити Корпорейшн Кагава Юниверсити | Производное циклобутилпурина, агент, активирующий ангиогенез, агент, активирующий образование просвета, агент, активирующий рост нейронов, и лекарственное средство |
| KR20110116004A (ko) | 2008-12-04 | 2011-10-24 | 인텍 파마 리미티드 | 잘레플론 위장체류 약물 전달 시스템 |
| CN102341380A (zh) | 2009-01-22 | 2012-02-01 | 神经病治疗药物股份有限公司 | 布美他尼、呋塞米、吡咯他尼、佐塞米和托拉塞米类似物、组合物和使用方法 |
| AU2010221270B2 (en) | 2009-03-03 | 2014-02-27 | Xenoport, Inc. | Sustained release oral dosage forms of an R-baclofen prodrug |
| JP2012524065A (ja) | 2009-04-17 | 2012-10-11 | ゼノポート,インコーポレーテッド | GABAB受容体リガンドとしてのγ−アミノ酪酸誘導体 |
| US9393241B2 (en) | 2009-06-02 | 2016-07-19 | Pharnext | Compositions for treating CMT and related disorders |
| EP2263665A1 (en) | 2009-06-02 | 2010-12-22 | Pharnext | New compositions for treating CMT and related disorders |
| WO2011011692A2 (en) | 2009-07-24 | 2011-01-27 | Stc.Unm | Methods of treating and preventing/reducing the likelihood of mesial temporal lobe epilepsy (tle) |
| US9387206B2 (en) | 2009-11-03 | 2016-07-12 | Pharnext | Therapeutic approaches for treating Alzheimer's disease |
| EP2322163A1 (en) | 2009-11-03 | 2011-05-18 | Pharnext | New therapeutics approaches for treating alzheimer disease |
| US10010515B2 (en) | 2011-03-01 | 2018-07-03 | Pharnext | Therapeutic approaches for treating Parkinson's disease |
| UA115968C2 (uk) | 2011-03-01 | 2018-01-25 | Фарнекст | Нові композиції для лікування неврологічних захворювань |
| EP2705842A1 (en) | 2012-09-05 | 2014-03-12 | Pharnext | Therapeutic approaches for treating parkinson's disease |
| US9867837B2 (en) | 2011-03-01 | 2018-01-16 | Pharnext | Compositions for treating neurological disorders |
| US9241933B2 (en) | 2011-03-01 | 2016-01-26 | Pharnext | Compositions for treating amyotrophic lateral sclerosis |
| BR112013022112B1 (pt) | 2011-03-01 | 2021-09-28 | Pharnext | Composição que compreende baclofeno e acamprosato |
| US9248111B2 (en) | 2011-03-01 | 2016-02-02 | Pharnext | Therapeutic approaches for treating parkinson's disease |
| US9931326B2 (en) | 2011-03-29 | 2018-04-03 | Pharnext | Composition comprising torasemide and baclofen for treating neurological disorders |
-
2014
- 2014-08-29 US US14/473,142 patent/US9248111B2/en not_active Expired - Fee Related
-
2015
- 2015-08-28 ES ES15762523T patent/ES2749082T3/es active Active
- 2015-08-28 US US15/506,308 patent/US10342768B2/en not_active Expired - Fee Related
- 2015-08-28 EP EP19178970.0A patent/EP3563841A1/en not_active Withdrawn
- 2015-08-28 EP EP15762523.7A patent/EP3185859B1/en not_active Not-in-force
- 2015-08-28 WO PCT/EP2015/069783 patent/WO2016030522A1/en active Application Filing
- 2015-08-28 CN CN201580058985.6A patent/CN107106521B/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CN107106521B (zh) | 2020-06-05 |
| EP3563841A1 (en) | 2019-11-06 |
| US10342768B2 (en) | 2019-07-09 |
| US20170273919A1 (en) | 2017-09-28 |
| US9248111B2 (en) | 2016-02-02 |
| WO2016030522A1 (en) | 2016-03-03 |
| US20140371229A1 (en) | 2014-12-18 |
| CN107106521A (zh) | 2017-08-29 |
| EP3185859B1 (en) | 2019-07-17 |
| EP3185859A1 (en) | 2017-07-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2749082T3 (es) | Nuevos enfoques terapéuticos para tratar la enfermedad de Parkinson | |
| AU2018201436B2 (en) | New therapeutic approaches for treating Parkinson's disease | |
| US10010515B2 (en) | Therapeutic approaches for treating Parkinson's disease | |
| HK1203417B (en) | New therapeutic approaches for treating parkinson's disease |