ES2728434B2 - Inhibidores de la cristalización de la xantina - Google Patents
Inhibidores de la cristalización de la xantina Download PDFInfo
- Publication number
- ES2728434B2 ES2728434B2 ES201830385A ES201830385A ES2728434B2 ES 2728434 B2 ES2728434 B2 ES 2728434B2 ES 201830385 A ES201830385 A ES 201830385A ES 201830385 A ES201830385 A ES 201830385A ES 2728434 B2 ES2728434 B2 ES 2728434B2
- Authority
- ES
- Spain
- Prior art keywords
- compound
- xanthine
- use according
- alkyl group
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- LRFVTYWOQMYALW-UHFFFAOYSA-N 9H-xanthine Chemical compound O=C1NC(=O)NC2=C1NC=N2 LRFVTYWOQMYALW-UHFFFAOYSA-N 0.000 title claims description 102
- 229940075420 xanthine Drugs 0.000 title claims description 51
- 238000002425 crystallisation Methods 0.000 title description 23
- 230000008025 crystallization Effects 0.000 title description 23
- 239000003112 inhibitor Substances 0.000 title description 19
- PFWLFWPASULGAN-UHFFFAOYSA-N 7-Methylxanthine Natural products N1C(=O)NC(=O)C2=C1N=CN2C PFWLFWPASULGAN-UHFFFAOYSA-N 0.000 claims description 82
- GMSNIKWWOQHZGF-UHFFFAOYSA-N 3-methyl-9H-xanthine Chemical compound O=C1NC(=O)N(C)C2=C1N=CN2 GMSNIKWWOQHZGF-UHFFFAOYSA-N 0.000 claims description 76
- YAPQBXQYLJRXSA-UHFFFAOYSA-N theobromine Chemical compound CN1C(=O)NC(=O)C2=C1N=CN2C YAPQBXQYLJRXSA-UHFFFAOYSA-N 0.000 claims description 56
- 150000001875 compounds Chemical class 0.000 claims description 41
- 229960004559 theobromine Drugs 0.000 claims description 27
- 206010007027 Calculus urinary Diseases 0.000 claims description 21
- 208000008281 urolithiasis Diseases 0.000 claims description 21
- MVOYJPOZRLFTCP-UHFFFAOYSA-N 1-methyl-7H-xanthine Chemical compound O=C1N(C)C(=O)NC2=C1NC=N2 MVOYJPOZRLFTCP-UHFFFAOYSA-N 0.000 claims description 20
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims description 19
- 239000000203 mixture Substances 0.000 claims description 17
- 230000002265 prevention Effects 0.000 claims description 15
- 244000299461 Theobroma cacao Species 0.000 claims description 13
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 10
- 235000009470 Theobroma cacao Nutrition 0.000 claims description 9
- 239000008194 pharmaceutical composition Substances 0.000 claims description 7
- 235000019219 chocolate Nutrition 0.000 claims description 4
- 150000003839 salts Chemical class 0.000 claims description 4
- 239000012453 solvate Substances 0.000 claims description 3
- 235000015872 dietary supplement Nutrition 0.000 claims description 2
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical compound CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 28
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical compound O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 28
- QUNWUDVFRNGTCO-UHFFFAOYSA-N 1,7-dimethylxanthine Chemical compound N1C(=O)N(C)C(=O)C2=C1N=CN2C QUNWUDVFRNGTCO-UHFFFAOYSA-N 0.000 description 24
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 24
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 20
- 210000002700 urine Anatomy 0.000 description 18
- 201000010099 disease Diseases 0.000 description 16
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 14
- LPHGQDQBBGAPDZ-UHFFFAOYSA-N Isocaffeine Natural products CN1C(=O)N(C)C(=O)C2=C1N(C)C=N2 LPHGQDQBBGAPDZ-UHFFFAOYSA-N 0.000 description 14
- VJEONQKOZGKCAK-UHFFFAOYSA-N caffeine Natural products CN1C(=O)N(C)C(=O)C2=C1C=CN2C VJEONQKOZGKCAK-UHFFFAOYSA-N 0.000 description 14
- 229960001948 caffeine Drugs 0.000 description 14
- 239000013078 crystal Substances 0.000 description 13
- 229960000278 theophylline Drugs 0.000 description 12
- 230000002401 inhibitory effect Effects 0.000 description 10
- 230000005764 inhibitory process Effects 0.000 description 8
- 239000000546 pharmaceutical excipient Substances 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- KWNBDPJHEKVDAW-UHFFFAOYSA-N 4-(4-chlorophenyl)-2-(4-methylphenyl)-4-oxobutanoic acid Chemical compound C1=CC(C)=CC=C1C(C(O)=O)CC(=O)C1=CC=C(Cl)C=C1 KWNBDPJHEKVDAW-UHFFFAOYSA-N 0.000 description 7
- 238000000034 method Methods 0.000 description 7
- OTSBKHHWSQYEHK-UHFFFAOYSA-N 1,3-dimethyluric acid Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC(=O)N2 OTSBKHHWSQYEHK-UHFFFAOYSA-N 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- RTAPDZBZLSXHQQ-UHFFFAOYSA-N 8-methyl-3,7-dihydropurine-2,6-dione Chemical group N1C(=O)NC(=O)C2=C1N=C(C)N2 RTAPDZBZLSXHQQ-UHFFFAOYSA-N 0.000 description 5
- 206010029148 Nephrolithiasis Diseases 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- LEHOTFFKMJEONL-UHFFFAOYSA-N Uric Acid Chemical compound N1C(=O)NC(=O)C2=C1NC(=O)N2 LEHOTFFKMJEONL-UHFFFAOYSA-N 0.000 description 4
- 102100033220 Xanthine oxidase Human genes 0.000 description 4
- 108010093894 Xanthine oxidase Proteins 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- JSDBKAHWADVXFU-UHFFFAOYSA-N 5-amino-1Hpyrazole-4-carboxylic acid Natural products CN1C=CC(=O)N(C)C1=O JSDBKAHWADVXFU-UHFFFAOYSA-N 0.000 description 3
- 244000188472 Ilex paraguariensis Species 0.000 description 3
- 235000003368 Ilex paraguariensis Nutrition 0.000 description 3
- 208000000913 Kidney Calculi Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 235000013305 food Nutrition 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 238000010899 nucleation Methods 0.000 description 3
- 230000006911 nucleation Effects 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 244000228088 Cola acuminata Species 0.000 description 2
- 235000010205 Cola acuminata Nutrition 0.000 description 2
- 101000987144 Homo sapiens Molybdenum cofactor sulfurase Proteins 0.000 description 2
- 206010021131 Hypouricaemia Diseases 0.000 description 2
- 102100027983 Molybdenum cofactor sulfurase Human genes 0.000 description 2
- 240000003444 Paullinia cupana Species 0.000 description 2
- 235000000556 Paullinia cupana Nutrition 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- 208000001647 Renal Insufficiency Diseases 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 244000269722 Thea sinensis Species 0.000 description 2
- 235000006468 Thea sinensis Nutrition 0.000 description 2
- TVWHNULVHGKJHS-UHFFFAOYSA-N Uric acid Natural products N1C(=O)NC(=O)C2NC(=O)NC21 TVWHNULVHGKJHS-UHFFFAOYSA-N 0.000 description 2
- 102000005773 Xanthine dehydrogenase Human genes 0.000 description 2
- 108010091383 Xanthine dehydrogenase Proteins 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000007812 deficiency Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 230000029142 excretion Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- -1 for example Chemical group 0.000 description 2
- 208000020404 hereditary xanthinuria Diseases 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 201000006370 kidney failure Diseases 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 238000001000 micrograph Methods 0.000 description 2
- 230000021962 pH elevation Effects 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 229940116269 uric acid Drugs 0.000 description 2
- 229910001868 water Inorganic materials 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000009304 Acute Kidney Injury Diseases 0.000 description 1
- 108091023020 Aldehyde Oxidase Proteins 0.000 description 1
- 102100036826 Aldehyde oxidase Human genes 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 239000004254 Ammonium phosphate Substances 0.000 description 1
- 208000036487 Arthropathies Diseases 0.000 description 1
- 240000008886 Ceratonia siliqua Species 0.000 description 1
- 235000013912 Ceratonia siliqua Nutrition 0.000 description 1
- 240000007154 Coffea arabica Species 0.000 description 1
- 235000007460 Coffea arabica Nutrition 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000012659 Joint disease Diseases 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 208000015924 Lithiasis Diseases 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- 208000021642 Muscular disease Diseases 0.000 description 1
- 201000009623 Myopathy Diseases 0.000 description 1
- 244000046052 Phaseolus vulgaris Species 0.000 description 1
- 235000010627 Phaseolus vulgaris Nutrition 0.000 description 1
- 206010038419 Renal colic Diseases 0.000 description 1
- 208000033626 Renal failure acute Diseases 0.000 description 1
- 206010038478 Renal lithiasis Diseases 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 241001556367 Theobroma angustifolium Species 0.000 description 1
- 235000002423 Theobroma angustifolium Nutrition 0.000 description 1
- 240000006474 Theobroma bicolor Species 0.000 description 1
- 235000002425 Theobroma bicolor Nutrition 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 229940022663 acetate Drugs 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 201000011040 acute kidney failure Diseases 0.000 description 1
- 208000012998 acute renal failure Diseases 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 229910000148 ammonium phosphate Inorganic materials 0.000 description 1
- 235000019289 ammonium phosphates Nutrition 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000021028 berry Nutrition 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- QXDMQSPYEZFLGF-UHFFFAOYSA-L calcium oxalate Chemical compound [Ca+2].[O-]C(=O)C([O-])=O QXDMQSPYEZFLGF-UHFFFAOYSA-L 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 235000019221 dark chocolate Nutrition 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- MNNHAPBLZZVQHP-UHFFFAOYSA-N diammonium hydrogen phosphate Chemical compound [NH4+].[NH4+].OP([O-])([O-])=O MNNHAPBLZZVQHP-UHFFFAOYSA-N 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 208000000718 duodenal ulcer Diseases 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- HVQAJTFOCKOKIN-UHFFFAOYSA-N flavonol Natural products O1C2=CC=CC=C2C(=O)C(O)=C1C1=CC=CC=C1 HVQAJTFOCKOKIN-UHFFFAOYSA-N 0.000 description 1
- 150000002216 flavonol derivatives Chemical class 0.000 description 1
- 235000011957 flavonols Nutrition 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 235000011184 guayusa Nutrition 0.000 description 1
- XLYOFNOQVPJJNP-ZSJDYOACSA-N heavy water Substances [2H]O[2H] XLYOFNOQVPJJNP-ZSJDYOACSA-N 0.000 description 1
- 208000006750 hematuria Diseases 0.000 description 1
- 125000001183 hydrocarbyl group Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 208000017169 kidney disease Diseases 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 235000001055 magnesium Nutrition 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 238000003760 magnetic stirring Methods 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 210000000885 nephron Anatomy 0.000 description 1
- 229940049964 oleate Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229950008882 polysorbate Drugs 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 208000037920 primary disease Diseases 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 208000037921 secondary disease Diseases 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 230000010248 tubular secretion Effects 0.000 description 1
- 210000000626 ureter Anatomy 0.000 description 1
- 210000001635 urinary tract Anatomy 0.000 description 1
- 208000019206 urinary tract infection Diseases 0.000 description 1
- 235000019220 whole milk chocolate Nutrition 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D473/00—Heterocyclic compounds containing purine ring systems
- C07D473/02—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6
- C07D473/04—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms
- C07D473/06—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms with radicals containing only hydrogen and carbon atoms, attached in position 1 or 3
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
- A61K31/52—Purines, e.g. adenine
- A61K31/522—Purines, e.g. adenine having oxo groups directly attached to the heterocyclic ring, e.g. hypoxanthine, guanine, acyclovir
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D473/00—Heterocyclic compounds containing purine ring systems
- C07D473/02—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6
- C07D473/04—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms
- C07D473/06—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms with radicals containing only hydrogen and carbon atoms, attached in position 1 or 3
- C07D473/10—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms with radicals containing only hydrogen and carbon atoms, attached in position 1 or 3 with methyl radicals in positions 3 and 7, e.g. theobromine
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
DESCRIPCIÓN
Inhibidores de la cristalización de la xantina
La presente invención hace referencia a inhibidores de la cristalización de xantina para su uso en el tratamiento y/o la prevención de la urolitiasis de xantina.
ANTECEDENTES DEL ARTE
La urolitiasis de xantina es un tipo poco frecuente de piedras en el riñón y es una consecuencia de un trastorno hereditario poco común (xantinuria). La xantinuria es una consecuencia de una deficiencia de la actividad de xantina oxidasa en los tejidos, dando como resultado hipouricemia e hipouricosuria (Carpenter TO, et al. Hereditary xanthinuria presenting in infancy nephrolithiasis. J Pediatr 1986; 109: 309-9; Mateos FA, et al., Hereditary xanthinuria: Evidence for enhanced hypoxanthine salvage. J Clin Invest 1987; 79: 847-52). La aparición de síntomas puede ocurrir a cualquier edad. Aproximadamente 50% de los pacientes presentan síntomas de infección del tracto urinario, hematuria, cólico renal, insuficiencia renal aguda y urolitiasis. En algunos pacientes excepcionales, la enfermedad renal puede evolucionar a una insuficiencia renal, o puede incluso producir artropatía, miopatía o úlcera duodenal.
De hecho, la xantinuria hereditaria es una consecuencia de la mutación de los genes xantina deshidrogenasa (XDH, 2p23.1) o cofactor molibdeno sulforasa (MOCOS, 18q12.2), que causa un fallo en la degradación de hipoxantina y xantina a ácido úrico y que conduce a la acumulación de xantina y, en un menor grado, hipoxantina. La xantinuria hereditaria clásica incluye xantinuria de tipo I y II. El tipo I corresponde a un déficit de xantina deshidrogenasa/oxidasa, por mutación de XDH, mientras que el tipo II es el resultado de la combinación de xantina deshidrogenasa y aldehído oxidasa por mutaciones de MOCOS. Ambas deficiencias enzimáticas conducen a un fenotipo clínicamente idéntico.
El diagnóstico de este trastorno se base en mediciones del ácido úrico en plasma y en orina. Si se detectan valores anormalmente bajos, se lleva a cabo la medición de
los niveles de xantina y de hipoxantina en la orina y en plasma. En aproximadamente la mitad de estos pacientes se detecta la presencia de urolitiasis de xantina. En unos pocos casos la enfermedad puede terminar en una insuficiencia renal.
El único tratamiento recomendado para estos pacientes consiste en una dieta baja en purinas y una ingesta elevada de fluidos. Debido a que la solubilidad de la xantina no depende de los valores del pH de la orina, la alcalinización de la orina no produce efecto alguno, al contrario de lo que ocurre en el caso de la litiasis úrica (Nicoletta JA, et al., Medical evaluation and treatment of urolithiasis. Pediatr Clin North Am 2006; 53: 479-91; Hisatome I, et al., Renal hypouricemia due to enhanced tubular secretion of urate associated with urolithiasis: successful treatment of urolithiasis by alkalinization of urineK+, Na+-citrate. Nephron 1993; 65: 578- 82).
Por lo tanto, existe la necesidad de identificar nuevos agentes que pueden ser utilizados clínicamente para prevenir el desarrollo de cristales de xantina en la orina, evitando el desarrollo de los correspondientes cálculos, un problema muy importante en pacientes con xantinuria.
DESCRIPCIÓN DE LA INVENCIÓN
El objeto de la presente invención es proporcionar nuevos productos para el tratamiento y/o prevención de urolitiasis de xantina basados en el descubrimiento de nuevos inhibidores de la cristalización de la xantina.
Por lo tanto, un aspecto principal de la presente invención hace referencia a un compuesto de la fórmula general (I):
una sal o solvato farmacéuticamente aceptable del mismo, en donde
R1 es H o un grupo alquilo (C1-C3),
R2 es H o un grupo alquilo (C1-C3),
R3 es H o un grupo alquilo (C1-C3),
con la condición de que al menos uno de R1, R2 o R3 es un grupo alquilo (C1-C3), para su uso en el tratamiento y/o prevención de la urolitiasis de xantina.
El término "grupo alquilo (C1-C3)” en la presente invención hace referencia a una cadena de hidrocarburo linear o ramificado saturado que tiene de 1 a 3 átomos de carbono, por ejemplo, metilo, etilo, n-propilo, /-propilo, más particularmente es un metilo.
El término "urolitiasis” hace referencia al trastorno causado por la presencia de cálculos o piedras en el interior de los riñones o el tracto urinario (uréteres, vegija). "Urolitiasis”, "nefrolitiasis” y "litiasis renal” son sinónimos. En caso de urolitiasis de xantina, los cálculos renales están compuestos de xantina que se ha concentrado y precipitado formando fragmentos de tamaño variado.
Entre las sales farmacéuticamente aceptables se incluyen, por ejemplo, acetato, gluconato, oleato o salicilato.
Tal como se muestra en los Ejemplos a continuación, los compuestos abarcados por la fórmula (I) son efectivos como inhibidores de la cristalización de la xantina, resultando útiles de este modo en la prevención y tratamiento de la urolitiasis de xantina. Los inhibidores de la cristalización de la xantina de la invención previenen el desarrollo de cálculos o reducen el tamaño de los cálculos que ya se han formado, permitiendo su excreción por la orina. Los inhibidores de la cristalización de la xantina son también de utilidad en la prevención de repeticiones de los episodios de urolitiasis. Además, los compuestos de la invención son de utilidad en la mejora de los síntomas asociados a la enfermedad xantinuria.
Los resultados experimentales muestran que los compuestos 1-metilxantina (1-MX), 7-metilxantina (7-MX) y 3-metilxantina (3-MX) pueden inhibir la nucleación de la xantina, ya que el retraso del tiempo de inducción en el desarrollo del cristal depende de las concentraciones de 1-MX, 7-MX y 3-MX. Curiosamente, los
inventores han observado que los compuestos muy similares en su estructura a la fórmula (I) como la hipoxantina (HX), teofilina (TP), paraxantina (PX), teobromina (TB), cafeína (CF), ácido 1-metilúrico (1-MU) y ácido 1,3-dimetilúrico (1,3-DMUA) no manifestaron ningún efecto inhibidor. Resulta interesante observar la selectividad del proceso de inhibición de la cristalización. Por tanto, únicamente las metil xantinas en la posición 1, 7 y 3 pueden ser incorporadas en la red cristalina de la xantina. La incorporación de estas moléculas a la red cristalina de xantina modificaría la estructura de algunas capas que, como consecuencia, aumentan su energía, modificando su tasa de crecimiento. En este caso, debido a que el pH de la orina no afecta a la solubilidad de la xantina, se han realizado estudios de inhibición a un único valor de pH (pH=6). Curiosamente, no la CF, ni la PX o TP mostraron efectos inhibidores, lo que demuestra la importancia de las posiciones de los grupos metilo en los efectos inhibidores mostrados por la molécula.
Un aspecto adicional de la presente invención hace referencia a una composición que comprende el compuesto de la fórmula (I) tal como se ha descrito anteriormente para el tratamiento y/o la prevención de la urolitiasis de la xantina.
Tal como se ha discutido, un primer aspecto de la invención hace referencia a los compuestos de la fórmula (I).
En una realización en particular, R1 es un grupo alquilo (C1-C3), R2 es un grupo alquilo (C1-C3) y R3 es H.
En una realización en particular, R1 es un grupo alquilo (C1-C3), R2 es H y R3 es H.
En una realización en particular, R1 es H y R2 es un grupo alquilo (C1-C3) y R3 es H.
En una realización en particular, R1 es H, R2 es H y R3 es un grupo alquilo (C1-C3).
En una realización en particular, R1 es un metilo.
En otra realización en particular, R2 es un metilo.
En otra realización en particular, R3 es un metilo.
En una realización en particular, el compuesto de la fórmula (I) se selecciona del grupo que consiste en teobromina, 1-metilxantina (1-MX), 3-metilxantina (3-MX) y 7-metilxantina (7-MX).
En una realización más en particular, el compuesto de la fórmula (I) es teobromina:
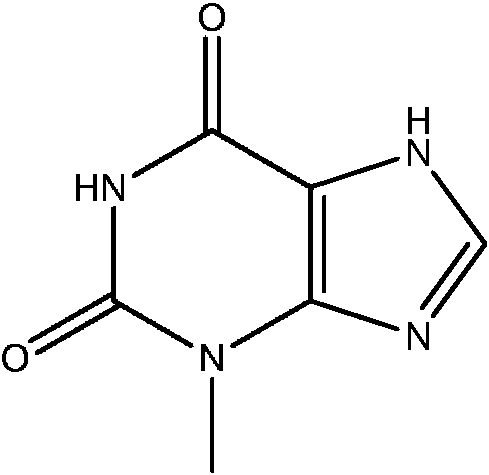
En otra realización más en particular, el compuesto de la fórmula (I) es 3-metilxantina:
En otra realización más en particular, el compuesto de la fórmula (I) es 7-metilxantina:
En otra realización más en particular, el compuesto de la fórmula (I) es 1-metilxantina:
En una realización en particular, el compuesto de la fórmula (I) es administrado por vía oral.
En una realización en particular, la dosis administrada, particularmente por vía oral, del compuesto de fórmula (I) varía entre 100 mg/día y 400 mg/día, más en particular 200 mg/día.
El compuesto con la fórmula (I) puede ser administrado en forma sólida (incluyendo gránulos, polvos o supositorios) o en forma líquida (tal como soluciones, suspensiones o emulsiones). Puede ser administrado de esta forma o incluso después de ser sometido a operaciones tales como esterilización o la adición de conservantes, estabilizantes o emulsionantes.
Los compuestos de la fórmula (I) pueden ser en forma pura o estar comprendidos en productos naturales. La Teobromina por ejemplo se encuentra presente en cantidades elevadas en el cacao y el chocolate (Craig WJ, et al., Caffeine and theobromine levels in cocoa and carob products 2006; J Food Sci, 49: 302-303). El polvo de cacao puede variar en cuanto a la cantidad e teobromina, desde un 2% de teobromina, hasta niveles más elevados de alrededor de un 10%. Hay habitualmente concentraciones más elevadas en el chocolate negro que en el chocolate con leche. Una pieza de chocolate negro o amargo, que contiene un mínimo de un 34% hasta un máximo de un 98% de cacao, puede contener una media de 378 mg teobromina. La Teobromina puede además encontrarse en pequeñas cantidades en la nuez de cola (1,0-2,5%), la baya de guaraná, yerba mate (Ilex paraguariensis), y la planta de té. Los granos de cacao contienen de
forma natural aproximadamente un 1% de teobromina. Las especies vegetales con las mayores cantidades de teobromina son: Theobroma cacao, Theobroma bicolor, Ilex paraguariensis, Ilex guayusa, Camellia sinensis, Cola acuminata, Theobroma angustifolium, Guaraná, Coffea Arabica.
En una realización en particular, el compuesto de la fórmula (I) es teobromina y se encuentra comprendida en el cacao o el chocolate.
En una realización más en particular, se utiliza un extracto de cacao en polvo con un 40% de flavonoles (teobromina).
Es importante considerar que la 7-MX y la 3-MX son dos importantes metabolitos de la teobromina. Por tanto, después del consumo de teobromina, un 20% es excretada como TB, un 21,5% es excretada como 3-MX y un 36 % es excretada como 7-MX. La 1-MX no es un metabolito de teobromina, es únicamente un producto que se obtiene como resultado del metabolismo de la cafeína en un 19% (Maurice J. Arnaud, Pharmacokinetics and metabolism of natural methylxanthines in animal and man, en: Bertid B. Fredholm (Ed), Methylxanthines, Springer, 2011, Nueva York, págs. 33-91).
Puede considerarse que, por ejemplo, la ingesta diaria de únicamente 200 mg de TB, conduciría a la excreción de 43 mg de 3-MX y 72 mg de 7-MX. Estas cantidades, de acuerdo con los resultados presentados aquí, podrían causar una inhibición significativa del desarrollo de cristales de xantina en la orina y por lo tanto podrían proteger pacientes con xantinuria del desarrollo de cálculos renales generados por esta sustancia.
Los compuestos de la fórmula (I) pueden además ser obtenidos mediante síntesis química.
La invención además hace referencia a una composición que comprende los compuestos definidos anteriormente, para su uso en el tratamiento y/o la prevención de urolitiasis de xantina.
La composición podría ser una composición farmacéutica o un complemento
alimenticio.
En una realización en particular, la composición es una composición farmacéutica, en donde el compuesto de la fórmula (I) se combina con excipientes farmacéuticamente aceptables.
Dependiendo de la composición farmacéutica de interés, la persona experta conoce numerosos posibles excipientes farmacéuticamente aceptables adecuados. Por ejemplo, si la composición es una suspensión un excipiente farmacéuticamente aceptable adecuado podría por ejemplo ser polisorbato (por ejemplo, polisorbato 20 = Tween 20), que podría ser un excipiente adecuado presente en un porcentaje adecuado en, por ejemplo, un medio acuoso. Si la composición farmacéutica es un comprimido, los excipientes farmacéuticamente aceptables adecuados podrían ser, por ejemplo, diluyentes, aglutinantes (por ejemplo, metil celulosa), lubricantes, etc. Un agente antioxidante tal como, por ejemplo, ácido ascórbico es también un ejemplo de un excipiente farmacéuticamente aceptable. Además, en algunos casos el agua puede también considerarse un excipiente farmacéuticamente aceptable.
En la composición farmacéutica, el compuesto con fórmula (I) puede combinarse con uno o más compuestos que facilitan su absorción a través de una vía de administración seleccionada. Puede, por lo tanto, ser administrado con lactosa, sacarosa, talco, estearato de magnesio, celulosa, sales de calcio, gelatina, ácidos grasos, además de otras sustancias similares.
En particular, la composición farmacéutica se administra por vía oral.
Los adyuvantes y vehículos farmacéuticamente aceptables que pueden ser utilizados en las composiciones son adyuvantes y vehículos conocidos para los expertos en el campo y se utilizan comúnmente en la preparación de composiciones terapéuticas.
El término composición de “complemento alimenticio” se utiliza en la presente patente para definir un producto alimenticio ingerible (que se puede consumir o beber).
Para un uso terapéutico, resulta preferible si el compuesto con la fórmula (I) se encuentra en una forma farmacéuticamente aceptable o es sustancialmente puro, es decir, que tenga un nivel de pureza farmacéuticamente aceptable excluyendo los aditivos farmacéuticos habituales, tales como los diluyentes y trasportadores, y se encuentre libre de cualquier material que se considere tóxico en niveles de dosificación habituales. Los niveles de pureza para la sustancia activa se encuentran particularmente por encima del 50%, más particularmente por encima del 70%, y aún más particularmente por encima del 90%. En una realización en particular, los niveles del compuesto con la fórmula (I), o sus sales o solvatos, se encuentran por encima del 95%.
Tal como se ha dicho anteriormente, la invención hace referencia a los compuestos de la fórmula (I) o composiciones para el tratamiento y/o la prevención de la urolitiasis de xantina. De forma alternativa, la invención hace referencia a un método para tratar y/o evitar la urolitiasis de xantina que comprende administrar un compuesto o una composición de la invención a un sujeto en necesidad del mismo. De forma alternativa, la invención hace referencia al uso de un compuesto o composición de la invención para la preparación de un medicamento para la prevención y/o tratamiento de la urolitiasis de xantina.
Se entiende ampliamente que el término “Tratamiento” que hace referencia a reducir el potencial para una determinada enfermedad, reducir la presencia de una determinada enfermedad, y/o una reducción en la gravedad de una determinada enfermedad en particular, hasta un grado en el que el sujeto no sufre más molestias y/o función alterada debido a la misma. “Tratamiento” hace referencia a un beneficio terapéutico o resultado clínico deseado, que no es necesariamente una cura para una enfermedad o trastorno en particular, sino que abarca un resultado que habitualmente suele incluir el alivio de la enfermedad, la eliminación de la enfermedad, la reducción o alivio de un síntoma asociado a la enfermedad, la prevención de una enfermedad secundaria que es el resultado de la presencia de una enfermedad primaria, disminución del grado de la enfermedad, estado estabilizado (es decir, sin empeoramiento) de la enfermedad, retraso o ralentización de la progresión de la enfermedad, mejora o atenuación del estado de la enfermedad, y remisión (ya sea parcial o total), ya sea detectable o indetectable de la enfermedad.
La “prevención” pretende evitar la aparición de dicha enfermedad. La prevención puede ser completa (por ejemplo, la total ausencia de una enfermedad). La prevención puede ser también parcial, de tal manera que por ejemplo la presencia de una enfermedad en un sujeto sea menor de lo que habría ocurrido sin la administración de los compuestos de la presente invención. La prevención también hace referencia a la susceptibilidad reducida a una condición clínica.
A menos que se defina de otro modo, todos los términos técnicos y científicos utilizados en la presente patente tienen el mismo significado que el que es entendido comúnmente por un experto habitual en el arte al que esta invención pertenece. Métodos y materiales similares o equivalentes a los descritos en la presente patente pueden ser utilizados en la práctica de la presente invención. A lo largo de la descripción y las reivindicaciones la palabra “comprende” y sus variaciones no pretenden excluir otras características técnicas, aditivos, componentes, o etapas. Objetos, ventajas y características adicionales de la invención resultarán evidentes para los expertos en el arte al examinar la descripción o pueden aprenderse mediante la práctica de la invención. Además, la presente invención cubre todas las posibles combinaciones de las realizaciones en particular descritas en la presente patente. Los siguientes ejemplos, dibujos se proporcionan a modo de ilustración y no pretenden ser limitativos de la presente invención.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
FIG. 1: Curvas de Cristalización para 500 mg/L xantina en orina sintética, en ausencia de inhibidores, y en presencia de 20 mg/l de 1-MX, 20 mg/l de 3-MX y 20 mg/l de 7-MX (T=37 oC; pH=6,0). Se representa la absorbancia (a 550 nm) por el tiempo (en minutos).
FIG. 2: Imágenes de microscopio electrónico de barrido de cristales de xantina obtenidos en orina sintética que contiene 400 mg/L de xantina, e incubada 24 h a 37o C, en presencia de diferentes inhibidores tal como sigue a continuación: (A) sin inhibidores; (B) con 20 mg/L de 3-MX; (C) con 40 mg/L de 3-MX; (D) con 20 mg/L
de 7-MX; (E) con 40 mg/L de 7-MX; (F) con 20 mg/L de 3-MX y 20 mg/L de 7-MX y (G) y (H) con 20 mg/L de 3-MX y 40 mg/L de 7-MX.
EJEMPLOS
Ejemplo 1: Estudio de inhibición de la cristalización de la xantina por 3-metilxantina (3-MX) y 7-metilxantina (7-MX)
Materiales y métodos
Reactivos y soluciones
Se adquirió Xantina (X), 1-metilxantina (1-MX), 3-metilxantina (3-MX) y 7-metilxantina (7-MX) de Sigma-Aldrich (St Louis, MO, EE.UU.). Se obtuvieron componentes de orina sintética de Panreac (Montcada i Reixac, Barcelona, España). Se disolvieron productos químicos de pureza de grado reactivo analítico en agua desionizada ultra-pura de un sistema Milli-Q y se filtró a través de filtros de poros de 0,45 ^m antes de su uso. Se preparó una solución madre de xantina diariamente disolviendo 0,5 g de xantina en 0,1 L de una solución de NaOH 1 M. Para evitar la precipitación de otros compuestos tales como oxalato de calcio, fosfato cálcico, o fosfato de amonio y de magnesio, las cristalizaciones se realizaron en orina sintética simplificada, preparada disolviendo 5,60 g de Na2HPO412H2O; 2,41 g NaH2PO4-2H2O y 13,05 g NaCl en 1L de H2O.
Ensayo turbidimétrico
Se evaluó la formación de cristales de xantina en orina sintética y los efectos de 1-metilxantina (1-MX), 3-metilxantina (3-MX) y 7-metilxantina (7-MX) utilizando un sistema turbodimétrico cinético, que consiste en un fotómetro (Metrohm 662) equipado con una célula detectora de guía de luz de fibra óptica con un reflector acoplado de trayectoria óptica de 2x10 mm y luz monocromática (550 nm). Se evaluó la cristalización a temperatura constante (37oC) con agitación magnética.
Se añadió orina sintética (180 mL) a un matraz de cristalización, seguido de una solución de 20 mL de xantina. La concentración final de xantina fue de 500 mg/L. Si
se sometía a ensayo un inhibidor, éste se disolvía en la correspondiente cantidad en esta solución. Cuando la solución resultante alcanzó una temperatura de 37o C, se añadió 3,6 mL de HCl 6 M para conseguir un pH de 6,0, que es el pH normal de la orina, y el temporizador se puso en marcha. El pH de la solución final se midió al comienzo de cada experimento. La absorbancia de la solución (550 nm) fue registrada durante la totalidad del ensayo cinético.
Las concentraciones máximas sometidas a ensayo fueron: 20 mg/L para 1-MX, 20 mg/L para 3-MX; 40 mg/L para 7-MX. Las cantidades mínimas sometidas a ensayo de las tres metilxantinas (1-MX, 3-MX y 7-MX) a partir de las que ya se han observado efectos inhibidores de la cristalización corresponden a 5mg/L.
Análisis del desarrollo de cristales
Se añadió 100 mL de alícuota de orina sintética que contenía 400 mg/L de xantina a pH=6,0 a 7 placas de cristalización: una sin inhibidores, dos con 20 y 40 mg/L de 3-MX; dos con 20 y 40 mg/L de 7-MX; una con una mezcla de 20 mg/L de 3-MX y 20 mg/L de 7-MX; y la última con una mezcla de 20 mg/L de 3-MX y 40 mg/L de 7-MX. Las placas se cubrieron con película plástica parafilm y se incubó sin agitación a 37o C durante 24 h. Los cristales formados se recogieron cuidadosamente, se secaron, y se examinaron bajo un microscopio electrónico de barrido.
Resultados
Lo compuestos 7-MX y 3-MX además de diferentes mezclas de 1-MX, 3-MX y 7-MX (5, 10 y 20 mg de cada sustancia, mostraron notables efectos inhibidores sobre la cristalización de la xantina, tal como se puede observar en la FIG. 1.
Las imágenes de microscopio electrónico de barrido de los cristales formados en presencia de 7-MX, 3-MX y las mezclas de 3-MX y 7-MX se muestran en la FIG. 2. (A) sin inhibidores, (B) 20 mg/L de 3-MX, (C) 40 mg/L de 3-MX, (D) 20 mg/L de 7-MX, (E) 40 mg/L de 7-MX, (F) 20 mg/L de 3-MX 20 mg/L de 7-MX, (G), 20 mg/L de 3-MX 40 mg/L de 7-MX (H). Tal como puede observarse en presencia de los inhibidores, debido a que el tiempo de inducción de la cristalización fue más prolongado, la nucleación de la fase cristalina resultó menos abundante y los
cristales se formaron más lentamente. Como consecuencia, conduciendo a más material cristalino y también a cristales de mayor tamaño, con caras bien desarrolladas, que claramente demuestra los efectos de estos inhibidores de la cristalización. Los inhibidores son específicamente adsorbidos únicamente en ciertas caras, ya que el proceso de adsorción depende de la estructura molecular del inhibidor y la estructura de la cara (lo que determina el establecimiento de interacciones estables). Como consecuencia de la adsorción en caras específicas, la velocidad de crecimiento de las mismas se modifica y esto conduce a modificaciones en la morfología de los cristales, tal como se muestra en la FIG 2. Por otro lado, cuanto mayor es el efecto inhibidor, menos cantidad de núcleos se forman y como consecuencia, en tiempos muy prolongados (experimento de la FIG.
2), los cristales formados son mucho mayores ya que el material supersaturado se distribuirá entre unos pocos núcleos (FIG. 2, G, H).
Ejemplo 2: (Ejemplo comparativo) Estudio de la inhibición de la cristalización de la xantina por hipoxantina (HX), teofilina (TP), paraxantina (PX), teobromina (TB), cafeína (CF), ácido 1-metilúrico (1-MU) y ácido 1,3-dimetilúrico (1,3-DMUA):
Los compuestos sometidos a ensayo en este ejemplo presentan estructuras similares a la del compuesto (I) de la presente invención, pero se encuentran fuera del alcance de la presente invención.
La Hipoxantina (HX), teofilina (TP), paraxantina (PX), teobromina (TB), cafeína (CF), ácido 1-metilúrico (1-MU) y ácido 1,3-dimetilúrico (1,3-DMUA) fueron adquiridos de Sigma-Aldrich (St Louis, MO, EE.UU.).
El mismo procedimiento descrito en el ejemplo 1 para estudiar la inhibición de la cristalización de la xantina se llevó a cabo en este ejemplo para los compuestos citados (X, HX, TP, PX, TB, CF, 1-MU y 1,3-DMUA).
La concentración máxima sometida a ensayo para todos los compuestos fue de: 40 mg/L para TB, TP, PX y CF; 45 mg/L para 1-MU; 80 mg/L para 1,3-DMU y 200 mg/L para HX.
Resultados
TB, TP, PX, CF, MU, 1,3-DMU y HX no causaron efectos a la concentración más elevada estudiada. Es interesante observar la especificidad de los inhibidores de la cristalización en el caso de cristales moleculares, al igual que en este caso, que es una consecuencia, como ya se ha mencionado, de la interacción entre el inhibidor y la correspondiente cara cristalina, que es determinada de forma selectiva por la estructura de ambas entidades, similar a la interacción entre enzima-sustrato.
Conclusiones
A partir de los presentes resultados, se muestra que 1-MX, 7-MX y 3-MX manifiestan efectos inhibidores importantes de la cristalización de la xantina. Las sustancias pueden inhibir la nucleación de la xantina, ya que el retraso en el tiempo de inducción depende de las concentraciones de 1-MX, 7-MX y 3-MX. Es interesante observar cómo HX, TP, PX, TB, CF, 1-MU y 1,3-DMU no manifestaron ningún efecto inhibidor. Es interesante observar la selectividad del proceso de inhibición de la cristalización. Por tanto, únicamente las metil xantinas en la posición 1, 7 y 3 son capaces de ser incorporadas en la red cristalina de la xantina. La incorporación de estas moléculas a la red cristalina de la xantina modificaría la estructura de algunas capas que, como consecuencia, aumentan su energía, alternado su tasa de crecimiento. En este caso, debido a que el pH de la orina no afecta a la solubilidad de la xantina, los estudios de inhibición han sido realizados a un único valor de pH (pH=6). Curiosamente, ni la CF, ni la PX ni la TP mostraron efectos inhibidores, lo que demuestra la importancia de las posiciones de los grupos metilo en los efectos inhibidores mostrados por la molécula.
Claims (15)
1.- Un compuesto de la fórmula (I),
sal o solvato farmacéuticamente aceptable del mismo, en donde
R1 es H o un grupo alquilo (C1-C3),
R2 es H o un grupo alquilo (C1-C3),
R3 es H o un grupo alquilo (C1-C3),
con la condición de que al menos uno de R1, R2 o R3 es un grupo alquilo (C1-C3), para su uso en el tratamiento y/o prevención de la urolitiasis de xantina.
2. - Compuesto para su uso según la reivindicación 1, en donde R1 es un grupo alquilo (C1-C3), R2 es grupo alquilo (C1-C3) y R3 es H.
3. - Compuesto para su uso según la reivindicación 1, en donde R1 es un grupo alquilo (C1-C3), R2 es H y R3 es H.
4. - Compuesto para su uso según la reivindicación 1, en donde R1 es H y R2 es un grupo alquilo (C1-C3) y R3 es H.
5. - Compuesto para su uso según la reivindicación 1, en donde R1 es H, R2 es H y R3 es un grupo alquilo (C1-C3).
6. - Compuesto para su uso según cualquiera de las reivindicaciones 1-3, en donde
R1 es metilo.
7. - Compuesto para su uso según cualquiera de las reivindicaciones 1, 2 o 4, en donde R2 es metilo.
8. - Compuesto para su uso según cualquiera de las reivindicaciones 1 o 5, en donde R3 es metilo.
9. - Compuesto para su uso según la reivindicación 1, en donde el compuesto de la fórmula (I) se selecciona del grupo que consiste en teobromina, 1-metilxantina, 3-metilxantina y 7-metilxantina.
10. - Compuesto para su uso según la reivindicación 9, en donde el compuesto es teobromina y está comprendida en cacao o chocolate.
11. - Compuesto para su uso según cualquiera de las reivindicaciones 1-10, en donde el compuesto de la fórmula (I) se administra por vía oral.
12. - Compuesto para su uso según cualquiera de las reivindicaciones 1-11, en donde el compuesto de la fórmula (I) se administra a una dosis entre 100 mg/día y 400 mg/día.
13. - Compuesto para su uso según la reivindicación 12, en donde el compuesto de la fórmula (I) se administra a una dosis de 200 mg/día.
14. - Composición que comprende el compuesto definido en cualquiera de las reivindicaciones 1-13, para su uso en el tratamiento y/o prevención de la urolitiasis de xantina.
15. - Compuesto para su uso según la reivindicación 14, en donde la composición es una composición farmacéutica o un complemento alimenticio.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ES201830385A ES2728434B2 (es) | 2018-04-20 | 2018-04-20 | Inhibidores de la cristalización de la xantina |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ES201830385A ES2728434B2 (es) | 2018-04-20 | 2018-04-20 | Inhibidores de la cristalización de la xantina |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| ES2728434A1 ES2728434A1 (es) | 2019-10-24 |
| ES2728434B2 true ES2728434B2 (es) | 2020-02-24 |
Family
ID=68242193
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES201830385A Active ES2728434B2 (es) | 2018-04-20 | 2018-04-20 | Inhibidores de la cristalización de la xantina |
Country Status (1)
| Country | Link |
|---|---|
| ES (1) | ES2728434B2 (es) |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2552706B1 (es) * | 2014-05-29 | 2016-09-13 | Universitat De Les Illes Balears | La teobromina y sus derivados para el tratamiento o prevenciónde la litiasis renal |
-
2018
- 2018-04-20 ES ES201830385A patent/ES2728434B2/es active Active
Also Published As
| Publication number | Publication date |
|---|---|
| ES2728434A1 (es) | 2019-10-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2622504T3 (es) | Nuevos enfoques terapéuticos para el tratamiento de la enfermedad de Alzheimer y trastornos relacionados a través de una modulación de la angiogénesis | |
| ES2950118T3 (es) | Complejo de gadolinio y un ligando quelatante derivado de pcta diastereoisoméricamente enriquecido y método de preparación y de purificación | |
| BRPI0818118B1 (pt) | Composição farmacêutica na forma de uma suspensão aquosa estabilizada de carisbamato e seu processo de formação | |
| Colliou et al. | Oxalate nephropathy following vitamin C intake within intensive care unit | |
| WO2020206623A1 (en) | Crystal forms | |
| US12343338B2 (en) | Ramipril solution for oral dosage | |
| KR20130014534A (ko) | 고양이에서 신장 장애를 장기간 치료하기 위한 멜록시캄의 용도 | |
| ES2728434B2 (es) | Inhibidores de la cristalización de la xantina | |
| ES2984402T3 (es) | Captadores de gamma-cetoaldehído para el tratamiento de la aterosclerosis | |
| US20200282024A1 (en) | Formulations for compound delivery | |
| ES2552706B1 (es) | La teobromina y sus derivados para el tratamiento o prevenciónde la litiasis renal | |
| BR112020000173A2 (pt) | uso de edaravona no tratamento oral de distúrbios neurodegenerativos mediados por estresse oxidativo | |
| PT3119201T (pt) | Soluções de sildenafilo e métodos de as preparar e utilizar | |
| JP2000517331A (ja) | ロルンオキシカム及びedtaのジナトリウム塩を含有する薬剤 | |
| RU2714257C2 (ru) | КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ В СТАБИЛЬНОМ СОСТОЯНИИ ОДНОЦЕПОЧЕЧНУЮ МОЛЕКУЛУ НУКЛЕИНОВОЙ КИСЛОТЫ, КОТОРАЯ ПОДАВЛЯЕТ ЭКСПРЕССИЮ ГЕНА TGF-β1 | |
| ES2952834T3 (es) | Lipoil-Glu-Ala para el tratamiento de daño neurodegenerativo producido por traumatismo craneoencefálico | |
| ES2365429B1 (es) | Solucion para dialisis peritoneal | |
| BRPI0718199A2 (pt) | Composição, e, métodos para estabilizar o ritmo da respiração de um mamífero, e para aumentar a ventilação por minuto no nível dos centros de controle respiratório do tronco cerebral no nucleus tractus solitarius de um indivíduo. | |
| ES2995007T3 (en) | Polymers, compositions and methods for treating hyperuricemia | |
| ES2297536T3 (es) | Composiciones farmaceuticas para el tratamiento de disfunciones renales. | |
| JP5408261B2 (ja) | うつ病、不安、統合失調症、睡眠障害、及びてんかん治療のためのコハク酸のコリン塩 | |
| ES2199541T3 (es) | Aplicacion del 2-amino-6-trifluorometoxi-benzotiazol para la prevencion o el tratamiento de disfunciones del cerebelo. | |
| EP4346791A1 (en) | Lidocaine or articaine for treating covid-19, autoimmune disease or cytokine storm response | |
| CN106580938A (zh) | 一种氨丁三醇有机酸盐及其制备方法和应用 | |
| US20150290176A1 (en) | Use of mtor inhibitors to treat vascular cognitive impairment |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| BA2A | Patent application published |
Ref document number: 2728434 Country of ref document: ES Kind code of ref document: A1 Effective date: 20191024 |
|
| FG2A | Definitive protection |
Ref document number: 2728434 Country of ref document: ES Kind code of ref document: B2 Effective date: 20200224 |