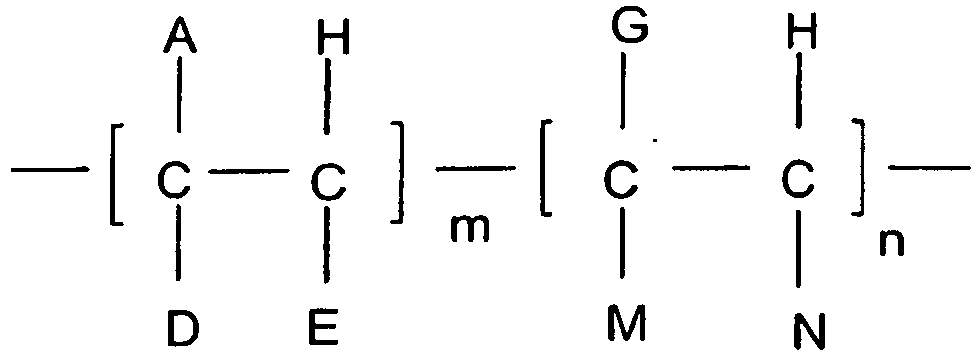EP1555309B1 - Demulgatoren für Mischungen aus MItteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs und Wasser - Google Patents
Demulgatoren für Mischungen aus MItteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs und Wasser Download PDFInfo
- Publication number
- EP1555309B1 EP1555309B1 EP04030573.2A EP04030573A EP1555309B1 EP 1555309 B1 EP1555309 B1 EP 1555309B1 EP 04030573 A EP04030573 A EP 04030573A EP 1555309 B1 EP1555309 B1 EP 1555309B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- oil
- ether
- fuel oil
- acid
- diglycidyl ether
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/146—Macromolecular compounds according to different macromolecular groups, mixtures thereof
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/143—Organic compounds mixtures of organic macromolecular compounds with organic non-macromolecular compounds
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/192—Macromolecular compounds
- C10L1/198—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds homo- or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon to carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid
- C10L1/1985—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds homo- or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon to carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid polyethers, e.g. di- polygylcols and derivatives; ethers - esters
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/234—Macromolecular compounds
- C10L1/238—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds
- C10L1/2383—Polyamines or polyimines, or derivatives thereof (poly)amines and imines; derivatives thereof (substituted by a macromolecular group containing 30C)
- C10L1/2387—Polyoxyalkyleneamines (poly)oxyalkylene amines and derivatives thereof (substituted by a macromolecular group containing 30C)
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/192—Macromolecular compounds
- C10L1/195—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds
- C10L1/196—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds derived from monomers containing a carbon-to-carbon unsaturated bond and a carboxyl group or salts, anhydrides or esters thereof homo- or copolymers of compounds having one or more unsaturated aliphatic radicals each having one carbon bond to carbon double bond, and at least one being terminated by a carboxyl radical or of salts, anhydrides or esters thereof
- C10L1/1966—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds derived from monomers containing a carbon-to-carbon unsaturated bond and a carboxyl group or salts, anhydrides or esters thereof homo- or copolymers of compounds having one or more unsaturated aliphatic radicals each having one carbon bond to carbon double bond, and at least one being terminated by a carboxyl radical or of salts, anhydrides or esters thereof poly-carboxylic
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/192—Macromolecular compounds
- C10L1/195—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds
- C10L1/197—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds derived from monomers containing a carbon-to-carbon unsaturated bond and an acyloxy group of a saturated carboxylic or carbonic acid
- C10L1/1973—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds derived from monomers containing a carbon-to-carbon unsaturated bond and an acyloxy group of a saturated carboxylic or carbonic acid mono-carboxylic
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/192—Macromolecular compounds
- C10L1/198—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds homo- or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon to carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid
- C10L1/1981—Condensation polymers of aldehydes or ketones
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/222—Organic compounds containing nitrogen containing at least one carbon-to-nitrogen single bond
- C10L1/2222—(cyclo)aliphatic amines; polyamines (no macromolecular substituent 30C); quaternair ammonium compounds; carbamates
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/222—Organic compounds containing nitrogen containing at least one carbon-to-nitrogen single bond
- C10L1/224—Amides; Imides carboxylic acid amides, imides
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/234—Macromolecular compounds
- C10L1/236—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds derivatives thereof
- C10L1/2364—Macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds derivatives thereof homo- or copolymers derived from unsaturated compounds containing amide and/or imide groups
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/28—Organic compounds containing silicon
- C10L1/285—Organic compounds containing silicon macromolecular compounds
Definitions
- the present invention relates to the use of an additive as a demulsifier for mixtures of middle distillates with vegetable or animal fuel oils and water.
- Oils obtained from animal or vegetable material are mainly metabolites comprising triglycerides of monocarboxylic acids, eg acids having 10 to 25 carbon atoms, and the formula in which R is an aliphatic radical of 10 to 25 carbon atoms, which may be saturated or unsaturated.
- oils include glycerides of a variety of acids, the number and variety of which varies with the source of the oil, and may additionally contain phosphoglycerides.
- Such oils can be obtained by methods known in the art.
- EP-B-0 665 873 discloses a fuel oil composition
- a fuel oil composition comprising a biofuel, a petroleum-based fuel oil and an additive which comprises (a) an oil-soluble ethylene copolymer or (b) a comb polymer or (c) a polar nitrogen compound or (d) a compound in which at least one substantially linear alkyl group having from 10 to 30 carbon atoms is bonded to a non-polymeric organic radical to provide at least one linear chain of atoms which includes the carbon atoms of the alkyl groups and one or more non-terminal oxygen atoms, or (e) one or more of the components ( a), (b), (c) and (d).
- WO-A-00/31216 discloses a fuel composition comprising a diesel fuel, ethanol and a stabilizer additive.
- the object of this invention was thus to find a suitable demulsifier for mixtures of middle distillates, biofuel oils and water.
- Another object of the invention is the use of the block copolymer defined under C) as a demulsifier in mixtures of middle distillate fuel oils with biofuel oils and water.
- Another object of the invention is a process for the demulsification of water from mixtures of middle distillate fuel oils with biofuel oils by adding to the mixtures the above-defined block copolymer.
- middle distillate fuel oils are used. This refers in particular to those mineral oils which are obtained by distillation of crude oil and boiling in the range of 120 to 450 ° C, for example kerosene, jet fuel, diesel and fuel oil.
- middle distillates are used which contain less than 350 ppm sulfur, more preferably less than 200 ppm sulfur, in particular less than 50 ppm sulfur and in special cases less than 10 ppm sulfur.
- middle distillates which have been subjected to a hydrogenating refining, and therefore contain only small amounts of polyaromatic and polar compounds.
- middle distillates which have 95% distillation points below 370.degree. C., in particular 350.degree. C. and in special cases below 330.degree.
- the middle distillates preferably have aromatics contents of less than 28% by weight, in particular less than 20% by weight.
- biofuel oils are used as component B.
- the biofuel oil which is often referred to as “biodiesel” or “biofuel” to fatty acid alkyl esters of fatty acids having 14 to 24 carbon atoms and alcohols having 1 to 4 carbon atoms.
- fatty acids having 14 to 24 carbon atoms and alcohols having 1 to 4 carbon atoms.
- a major part of the fatty acids contains one, two or three double bonds.
- Rapsölkladremethylester and especially mixtures containing rapeseed, sunflower and / or soybean oil fatty acid methyl ester.
- oils derived from animal or vegetable material which can be used in the composition of the present invention are rapeseed oil, coriander oil, soybean oil, cottonseed oil, sunflower oil, castor oil, olive oil, peanut oil, corn oil, almond oil, palm kernel oil, coconut oil, soybean oil, Mustard seed oil, beef tallow, bone oil and fish oils.
- oils derived from wheat, jute, sesame, shea nut, arachis oil, and linseed oil and may be derived therefrom by methods known in the art.
- oils can be used, which were obtained from used waste oils, such as cooking oil.
- Rapeseed oil which is a mixture of glycerol partially esterified fatty acids, is preferred because it is available in large quantities and is readily available by squeezing rapeseed. Furthermore, the also widespread oils of sunflower and soybeans and their mixtures with rapeseed oil are preferred.
- lower alkyl esters of fatty acids the following are suitable, for example as commercial mixtures: The ethyl, propyl, butyl and especially methyl esters of fatty acids having 12 to 22 carbon atoms, for example of lauric acid, myristic acid, palmitic acid, palmitoleic acid, stearic acid, oleic acid, Elaidic acid, petroselinic acid, ricinoleic acid, elaeostearic acid, linoleic acid, linolenic acid, eicosanoic acid, gadoleic acid, docosanoic acid or erucic acid, which preferably have an iodine value of 50 to 150, in particular 90 to 125.
- Mixtures with particularly advantageous properties are those which are mainly, i. at least 50 wt .-%, contain methyl esters of fatty acids having 16 to 22 carbon atoms and 1, 2 or 3 double bonds.
- the preferred lower alkyl esters of fatty acids are the methyl esters of oleic, linoleic, linolenic and erucic acids.
- Component C) is a crosslinked block copolymer prepared by crosslinking from a block copolymer of at least 2 different C 2 to C 4 alkylene oxides.
- the block copolymer may consist of 2, 3, 4 or more blocks.
- the block copolymers used are prepared by sequential polymerization of alkylene oxides (ethylene oxide, propylene oxide, butylene oxide), preferably under alkaline catalysis, as known in the art.
- alkylene oxides ethylene oxide, propylene oxide, butylene oxide
- the base polymer used to prepare the block copolymer C) generally has a molecular weight of 500 to 100,000 g / mol, preferably 1,000 to 60,000, especially 4,000 to 50,000 g / mol. These molecular weights are the molecular weights before crosslinking.
- crosslinking of the block copolymers used is as known in the art by alkaline or acid catalyzed ring opening of di-, tri- or tetraglycidyl ethers, by esterification with polybasic carboxylic acids or Carboxylic anhydrides or by reaction with polyfunctional isocyanates.
- Suitable crosslinkers are those compounds which can bind to the block polymer with at least 2 binding sites.
- the following crosslinking agents may be mentioned: Bisphenol A diglycidyl ether, butane-1,4-diol diglycidyl ether, hexane-1,6-diol diglycidyl ether, ethylene glycol diglycidyl ether, cyclohexanedimethanol diglycidyl ether, resorcinol diglycidyl ether, glycerol diglycidyl ether, glycerol triglycidyl ether, Glycerinpropoxylattriglycidylether, polyglycerol polyglycidyl ether, p-Aminophenoltriglycidylether, polypropylene glycol diglycidyl ether, pentaerythritol tetraglycidyl ether, sorbitol polyglycidyl ether, trimethyl
- the crosslinked block copolymers C) generally have a molecular weight of 1000-200,000 g / mol, preferably 2000-100,000, in particular 4000-50,000 g / mol, measured by gel permeation chromatography (GPC) against polystyrene standards in THF.
- GPC gel permeation chromatography
- WZ water number
- DIN EN 12836, to which reference is hereby made To a solvent mixture consisting of a specific volume of 97: 3 dioxane and toluene, in which the block copolymer sample is a clear solution, add water at a temperature of (25 ⁇ 1) ° C until a permanent haze occurs. The number of water is given in milliliters of water needed to maintain the permanent turbidity.
- the water number in the crosslinked block copolymer C) is preferably between 6 ml and 25 ml, in particular between 6 ml and 17 ml.
- the crosslinked block copolymers C) are added to the mixtures containing A) and B) in amounts of 0.001 to 5% by weight, preferably 0.005 to 1% by weight and especially 0.01 to 0.05% by weight. They may be dissolved as such or dissolved or dispersed in solvents, such as aliphatic and / or aromatic hydrocarbons or hydrocarbon mixtures such as toluene, xylene, ethylbenzene, decane, pentadecane, gasoline fractions, kerosene, naphtha, diesel, fuel oil, isoparaffins or commercial solvent mixtures such as Solvent Naphtha, ® Shellsol AB, ® Solvesso 150, ® Solvesso 200, ® Exxsol, ® Isopar and ® Shellsol D types are used. Preferably, they are dissolved in fuel oil of animal or vegetable origin based on fatty acid alkyl esters.
- the additives according to the invention preferably contain 1 to
- the crosslinked block copolymers C) may be added to the oil to be treated according to methods known in the art. If more than one copolymer component is to be used, such components may be incorporated into the oil together or separately in any combination.
- the crosslinked block copolymers C) can also be used together with one or more oil-soluble co-additives, which on their own improve the properties of crude oils, lubricating oils or fuel oils.
- oil-soluble co-additives are polar compounds which cause paraffin dispersion (paraffin dispersants), alkylphenol-aldehyde resins, polymeric cold flow improvers and oil-soluble amphiphiles.
- mixtures of the crosslinked block copolymers C) have proven outstandingly well with copolymers which contain from 10 to 40% by weight of vinyl acetate and from 60 to 90% by weight of ethylene.
- the additives according to the invention are mixed with ethylene / vinyl acetate / vinyl 2-ethylhexanoate terpolymers, ethylene / vinyl acetate / vinyl neononanoate terpolymers and / or ethylene / vinyl acetate / vinyl neodecanoate terpolymers to simultaneously improve flowability and lubricity of mineral oils or mineral oil distillates.
- the terpolymers of vinyl 2-ethylhexanoate, Vinyl neononanoate or vinyl neodecanoate contains, in addition to ethylene, 8 to 40% by weight of vinyl acetate and 1 to 40% by weight of the respective long-chain vinyl ester.
- Further preferred copolymers contain, in addition to ethylene, 10 to 40% by weight of vinyl acetate and optionally 1 to 40% by weight of vinyl esters with C 3 to C 12 -alkyl groups in the ester radical and optionally from 0.5 to 20% by weight of olefins with 3 to 10 C atoms such as isobutylene, diisobutylene, propylene, methylpentene or norbornene.
- paraffin dispersants are preferably low molecular weight or polymeric, oil-soluble compounds having ionic or polar groups, for example amine salts, imides and / or amides.
- Particularly preferred paraffin dispersants contain reaction products of primary and / or secondary fatty amines having 8 to 36 carbon atoms, in particular dicocosamine, ditallow fatty amine and distearylamine.
- Paraffin dispersants which have been obtained by reaction of aliphatic or aromatic amines, preferably long-chain aliphatic amines, with aliphatic or aromatic mono-, di-, tri- or tetracarboxylic acids or their anhydrides have proven particularly suitable (cf. US 4 211 534 ).
- paraffin dispersants are copolymers of maleic, fumaric and / or itaconic acid or of maleic anhydride and further ⁇ , ⁇ -unsaturated compounds which can optionally be reacted with primary and / or secondary monoalkylamines and / or aliphatic alcohols (cf. EP-A-0 154 177 ), the reaction products of Alkenylspirobislactonen with amines (see.
- esters are suitable as co-additives which bring about a paraffin dispersion.
- These esters are derived from polyols having 3 or more OH groups, in particular glycerol, trimethylolpropane, pentaerythritol and the oligomers having 2 to 10 monomer units, such as polyglycerol, obtainable therefrom by condensation.
- the polyols are generally reacted with 1 to 100 mol of alkylene oxide, preferably 3 to 70, in particular 5 to 50 mol of alkylene oxide per mole of polyol.
- Preferred alkylene oxides are ethylene oxide, propylene oxide and butylene oxide.
- the alkoxylation is carried out by known methods.
- the fatty acids suitable for the esterification of the alkoxylated polyols preferably have 8 to 50, in particular 12 to 30, especially 16 to 26 C-atoms.
- Suitable fatty acids are, for example, lauric, tridecane, myristic, pentadecane, palmitic, margarine, stearic, isostearic, arachic and behenic, oleic and erucic acid, palmitoleic, myristolein, ricinoleic acid, as well as natural fats and Oils derived fatty acid mixtures.
- Preferred fatty acid mixtures contain more than 50% fatty acids with at least 20 C atoms.
- fatty acids used for esterification contain double bonds, in particular less than 10%; specifically, they are largely saturated. Under largely saturated here is an iodine value of the fatty acid used of up to 5 g of I per 100 g of fatty acid are understood.
- Esterification may also be carried out starting from reactive derivatives of the fatty acids such as esters with lower alcohols (e.g., methyl or ethyl esters) or anhydrides.
- polybasic carboxylic acids dimer fatty acids, alkenylsuccinic acids and aromatic polycarboxylic acids and derivatives thereof such as anhydrides and C 1 - to C 5 -esters.
- Alkenylsuccinic acids and their derivatives with alkyl radicals having 8 to 200, in particular 10 to 50, carbon atoms are preferred. Examples are dodecenyl, octadecenyl and poly (isobutenyl) succinic anhydride.
- the polybasic carboxylic acids are preferably used to lower levels of up to 30 mol%, preferably 1 to 20 mol%, in particular 2 to 10 mol%.
- Ester and fatty acid are used for the esterification based on the content of hydroxyl groups on the one hand and carboxyl groups on the other hand in the ratio of 1.5: 1 to 1: 1.5, preferably 1.1: 1 to 1: 1.1, in particular equimolar.
- the paraffin-dispersing effect is particularly pronounced when working with an acid excess of up to 20 mol%, especially up to 10 mol%, in particular up to 5 mol%.
- the esterification is carried out by conventional methods.
- the separation the reaction water can be carried out by distillation by direct condensation or preferably by azeotropic distillation in the presence of organic solvents, in particular aromatic solvents such as toluene, xylene or higher boiling mixtures such as ® Shellsol A, Shellsol B, Shellsol AB or Solvent Naphtha.
- the esterification is preferably carried out completely, ie for the esterification 1.0 to 1.5 moles of fatty acid are used per mole of hydroxyl groups.
- the acid number of the esters is generally below 15 mg KOH / g, preferably below 10 mg KOH / g, especially below 5 mg KOH / g.
- paraffin dispersants are prepared by reacting compounds containing an acyl group with an amine.
- This amine is a compound of the formula NR 6 R 7 R 8 , in which R 6 , R 7 and R 8 may be identical or different, and at least one of these groups is C 8 -C 36 -alkyl, C 6 - C 36 -cycloalkyl, C 8 -C 36 -alkenyl, in particular C 12 -C 24 -alkyl, C 12 -C 24 -alkenyl or cyclohexyl, and the other groups are either hydrogen, C 1 -C 36 -alkyl, C 2 -C 36 alkenyl, cyclohexyl, or a group of the formulas - (AO) x -E or - (CH 2 ) n -NYZ, where A is an ethylene or propylene group, x is a number from 1 to 50, E Is H, C 1 -C 30 -alkyl
- the paraffin dispersants can be added to the crosslinked block copolymer C) or added separately to the middle distillate to be added.
- alkylphenol-aldehyde resins are also suitable as paraffin dispersants.
- Alkylphenol-aldehyde resins are known in principle and, for example in the Rompp Chemie Lexikon, 9th edition, Thieme Verlag 1988-92, Volume 4, p 3351ff , described.
- the alkyl or alkenyl radicals of the alkylphenol have 6-24, preferably 8-22, in particular 9-18, carbon atoms. They may be linear or preferably branched, wherein the branch may contain secondary as well as tertiary structural elements.
- alkylphenol-aldehyde resin may also contain up to 20 mole% of phenol units and / or alkylphenols with short alkyl chains, such as e.g. B. butylphenol.
- alkylphenol-aldehyde resin the same or different alkylphenols may be used.
- the aldehyde in the alkylphenol-aldehyde resin has 1 to 10, preferably 1 to 4, carbon atoms and may carry further functional groups. It is preferably an aliphatic aldehyde, more preferably it is formaldehyde.
- the molecular weight of the alkylphenol-aldehyde resins is preferably 350 to 10,000, in particular 400 to 5000, g / mol. This preferably corresponds to a condensation degree n of from 3 to 40, in particular from 4 to 20.
- the prerequisite here is that the resins are oil-soluble.
- the preparation of the alkylphenol-aldehyde resins is carried out in a known manner by basic catalysis, resulting in resol-type condensation products, or by acid catalysis to form novolac-type condensation products.
- the condensates obtained according to both types are suitable for the compositions according to the invention.
- the condensation is in the presence of acidic catalysts.
- an alkylphenol having 6-24, preferably 8-22, in particular 9-18, carbon atoms per alkyl group, or mixtures thereof and at least one aldehyde are reacted with each other, wherein about 0.5 mol per mol of alkylphenol compound. 2 mol, preferably 0.7 to 1.3 mol and in particular equimolar amounts of aldehyde are used.
- Suitable alkylphenols are in particular n- and iso-hexylphenol, n- and iso-octylphenol, n- and iso-nonylphenol, n- and iso-decylphenol, n- and iso-dodecylphenol, tetradecylphenol, hexadecylphenol, octadecylphenol, eicosylphenol, tripropenylphenol, tetrapropenylphenol and poly (isobutenyl) phenol -C 24th
- the alkylphenols are preferably para-substituted.
- the alkylphenols may carry one or more alkyl radicals. Preferably, they are substituted at most 5 mol%, especially at most 20 mol% and especially at most 40 mol% with more than one alkyl group. Preferably, at most 40 mol%, in particular at most 20 mol% of the alkylphenols used in the ortho position carry an alkyl radical. Specifically, the alkylphenols ortho to the hydroxyl group are not substituted with tertiary alkyl groups.
- the aldehyde can be a mono- or dialdehyde and carry other functional groups such as -COOH.
- Particularly suitable aldehydes are formaldehyde, acetaldehyde, butyraldehyde, glutaric dialdehyde and glyoxylic acid, with formaldehyde being preferred.
- the formaldehyde can be used in the form of paraformaldehyde or in the form of a preferably 20-40% strength by weight aqueous formalin solution.
- Corresponding amounts of trioxane can also be used.
- alkylphenol and aldehyde is usually carried out in the presence of alkaline catalysts, for example alkali metal hydroxides or alkylamines, or of acidic catalysts, for example inorganic or organic acids, hydrochloric acid, sulfuric acid, phosphoric acid, sulfonic acid, sulfamidic acids or haloacetic acids, and in the presence of an aqueous azeotrope-forming organic solvent, for example toluene, xylene, higher aromatics or mixtures thereof.
- alkaline catalysts for example alkali metal hydroxides or alkylamines
- acidic catalysts for example inorganic or organic acids, hydrochloric acid, sulfuric acid, phosphoric acid, sulfonic acid, sulfamidic acids or haloacetic acids
- an aqueous azeotrope-forming organic solvent for example toluene, xylene, higher aromatics or mixtures thereof.
- the reaction mixture is heated to a
- Solvents that do not release protons under condensation conditions may remain in the products after the condensation reaction.
- the resins can be used directly or after neutralization of the catalyst, optionally after further dilution of the solution with aliphatic and / or aromatic hydrocarbons or hydrocarbon mixtures, eg gasoline fractions, kerosene, decane, pentadecane, toluene, xylene, ethylbenzene or solvents such as ® Solvent Naphtha, ® Shellsol AB, ® Solvesso 150, ® Solvesso 200, ® Exxsol, ® ISOPAR and ® Shellsol D types.
- the crosslinked block copolymers C) are used together with comb polymers.
- This term refers to polymers in which hydrocarbon radicals having at least 8, in particular at least 10, carbon atoms are bonded to a polymer backbone.
- they are homopolymers whose alkyl side chains contain at least 8 and in particular at least 10 carbon atoms.
- at least 20%, preferably at least 30% of the monomers have side chains (cf. Comb-like Polymers-Structure and Properties; NA Plate and VP Shibaev, J. Polym. Sci. Macromolecular Revs. 1974, 8, 117 ff ).
- Suitable comb polymers are, for example, fumarate / vinyl acetate copolymers (cf. EP 0 153 176 A1 ), Copolymers of a C 6 -C 24 - ⁇ -olefin and a NC 6 -C 22 -alkylmaleimide (cf. EP-A-0 320 766 Further, esterified olefin / maleic anhydride copolymers, polymers and copolymers of ⁇ -olefins and esterified copolymers of styrene and maleic anhydride.
- the mixing ratio (in parts by weight) of the crosslinked block copolymers C) with polymeric cold flow improvers, paraffin dispersants, comb polymers or resins is in each case 1: 1000 to 1: 1, preferably 1:10 to 1:50.
- the crosslinked block copolymers C) can be used alone or together with other additives, for.
- additives for.
- pour point depressants or dewaxing aids with corrosion inhibitors, antioxidants, lubricity additives, sludge inhibitors, dehazers, and cloud point depressant additives.
- the CFPP value is determined according to EN 116, the boiling characteristics according to ASTM D-86 and the determination of the cloud point according to ISO 3015.
- Table 1 Analysis of the biodiesel used Oil no. CP CFPP E 1 Rapeseed acid methyl ester (RME) -2.3 -14 ° C E 2 90% rapeseed-oleic acid methyl ester (RME) + 10% soya-oleic acid methyl ester (sojaME) -2.0 -8 ° C C 16 C 16 ' C 18 C 18 ' C 18 " C 18 "' C 20 C 20 ' C 22 ⁇ saturated RME 4.4 0.4 1.6 57.8 21.6 8.8 1.5 0.7 0.2 7.7 SojaME 10.4 0.1 4.1 24.8 51.3 6.9 0.5 0.4 0.4 15.4 F1 F2 F3 F4 Sulfur content, ppm 7.9 4.9 32.0 900 Density, g / cm 3 .8436 0.8306 .8348 .8487 Initial
- the testing of the emulsification of additives is carried out according to ASTM D 1094-85.
Landscapes
- Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Emergency Medicine (AREA)
- Liquid Carbonaceous Fuels (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
- Die vorliegende Erfindung betrifft die Verwendung eines Additivs als Demulgator für Mischungen aus Mitteldestillaten mit pflanzlichen oder tierischen Brennstoffölen und Wasser.
- Im Zuge abnehmender Welterdölreserven und der Diskussion um die Umwelt beeinträchtigenden Konsequenzen des Verbrauchs fossiler und mineralischer Brennstoffe steigt das Interesse an alternativen, auf nachwachsenden Rohstoffen basierenden Energiequellen. Dazu gehören insbesondere native Öle und Fette pflanzlichen oder tierischen Ursprungs. Dies sind in der Regel Triglyceride von Fettsäuren mit 10 bis 24 C-Atomen, die einen den herkömmlichen Brennstoffen vergleichbaren Heizwert haben, aber gleichzeitig als biologisch abbaubar und umweltverträglich eingestuft werden.
- Aus tierischem oder pflanzlichem Material erhaltene Öle sind hauptsächlich Stoffwechselprodukte, die Triglyceride von Monocarbonsäuren umfassen, z.B. Säuren mit 10 bis 25 Kohlenstoffatomen, und der Formel
- Im allgemeinen enthalten solche Öle Glyceride von einer Reihe von Säuren, deren Anzahl und Sorte mit der Quelle des Öls variiert, und sie können zusätzlich Phosphoglyceride enthalten. Solche Öle können nach im Stand der Technik bekannten Verfahren erhalten werden.
- Auf Grund der teilweise unbefriedigenden physikalischen Eigenschaften der Triglyceride ist die Technik dazu übergegangen, die natürlich vorkommenden Triglyceride in Fettsäureester niederer Alkohole wie Methanol oder Ethanol zu überführen. Zum Stand der Technik gehören auch Mischungen aus Mitteldestillaten mit Ölen pflanzlicher oder tierischer Herkunft (im folgenden auch "Biobrennstofföle" genannt).
-
EP-B-0 665 873 offenbart eine Brennstoffölzusammensetzung, die einen Biobrennstoff, ein Brennstofföl auf Erdölbasis und ein Additiv umfasst, welches (a) ein öllösliches Ethylencopolymer oder (b) ein Kammpolymer oder (c) eine polare Stickstoffverbindung oder (d) eine Verbindung, in der mindestens eine im wesentlichen lineare Alkylgruppe mit 10 bis 30 Kohlenstoffatomen mit einem nicht polymeren organischen Rest verbunden ist, um mindestens eine lineare Kette von Atomen zu liefern, die die Kohlenstoffatome der Alkylgruppen und ein oder mehrere nicht endständige Sauerstoffatome einschließt, oder (e) eine oder mehrere der Komponenten (a), (b), (c) und (d) umfasst. -
WO-A-00/31216 - Ein Hindernis für die Verwendung von Mischungen aus Mitteldestillaten und Biobrennstoffölen ist deren starke Neigung, mit Wasser stabile Emulsionen einzugehen. Solche Emulsionen bewirken in der Verteilungskette der Brennstofföle sowie bei deren Verwendung in Kraftfahrzeugen Korrosionsprobleme.
- Aufgabe dieser Erfindung war es somit, einen geeigneten Demulgator für Mischungen aus Mitteldestillaten, Biobrennstoffölen und Wasser zu finden.
- Überraschenderweise wurde nun gefunden, dass bestimmte vernetzte Alkylenoxidblockpolymere ausgezeichnete Demulgatoren für solche Mischungen sind.
- Gegenstand der Erfindung ist ein Brennstofföl, enthaltend einen größeren Anteil einer Mischung aus
- A) einem Mitteldestillat-Brennstofföl, und
- B) einem Biobrennstofföl, im Mischungsverhältnis A:B = 99:1 bis 1:99 sowie
- C) 0,001 bis 5 Gew. % eines öllöslichen, vernetzten Blockcopolymers aus C2- bis C4-Alkylenoxiden.
- Ein weiterer Gegenstand der Erfindung ist die Verwendung des unter C) definierten Blockcopolymers als Demulgator in Mischungen aus Mitteldestillat-Brennstoffölen mit Biobrennstoffölen und Wasser.
- Ein weiterer Gegenstand der Erfindung ist ein Verfahren zur Demulgierung von Wasser aus Mischungen von Mitteldestillat-Brennstoffölen mit Biobrennstoffölen, indem man den Mischungen das oben definierte Blockcopolymer zusetzt.
- Als Bestandteil A) werden Mitteldestillat-Brennstofföle verwendet. Damit bezeichnet man insbesondere solche Mineralöle, die durch Destillation von Rohöl gewonnen werden und im Bereich von 120 bis 450°C sieden, beispielsweise Kerosin, Jet-Fuel, Diesel und Heizöl. Vorzugsweise werden solche Mitteldestillate verwendet, die weniger als 350 ppm Schwefel, besonders bevorzugt weniger als 200 ppm Schwefel insbesondere weniger als 50 ppm Schwefel und in speziellen Fällen weniger als 10 ppm Schwefel enthalten. Es handelt sich dabei im allgemeinen um solche Mitteldestillate, die einer hydrierenden Raffination unterworfen wurden, und die daher nur geringe Anteile an polyaromatischen und polaren Verbindungen enthalten. Vorzugsweise handelt es sich um solche Mitteldestillate, die 95 %-Destillationspunkte unter 370°C, insbesondere 350°C und in Spezialfällen unter 330°C aufweisen. Vorzugsweise haben die Mitteldestillate Aromatengehalte von unter 28 Gew.-%, insbesondere unter 20 Gew.-%.
- Als Bestandteil B) werden Biobrennstofföle verwendet. In einer bevorzugten Ausführungsform handelt es sich bei dem Biobrennstofföl, das häufig auch als "Biodiesel" oder "Biokraftstoff" bezeichnet wird, um Fettsäurealkylester aus Fettsäuren mit 14 bis 24 C-Atomen und Alkoholen mit 1 bis 4 C-Atomen. Gewöhnlich enthält ein größerer Teil der Fettsäuren ein, zwei oder drei Doppelbindungen. Besonders bevorzugt handelt es sich z.B. um Rapsölsäuremethylester und speziell um Mischungen, die Raps-, Sonnenblumen- und/oder Sojaölfettsäuremethylester enthalten.
- Beispiele für Öle, die sich von tierischem oder pflanzlichem Material ableiten, und die in der erfindungsgemäßen Zusammensetzung verwendet werden können, sind Rapsöl, Korianderöl, Sojaöl, Baumwollsamenöl, Sonnenblumenöl, Ricinusöl, Olivenöl, Erdnussöl, Maisöl, Mandelöl, Palmkernöl, Kokosnussöl, Sojaöl, Senfsamenöl, Rindertalg, Knochenöl und Fischöle. Weitere Beispiele schließen Öle ein, die sich von Weizen, Jute, Sesam, Scheabaumnuß, Arachisöl und Leinöl ableiten und können aus diesen nach im Stand der Technik bekannten Verfahren abgeleitet werden. Außerdem können Öle verwendet werden, welche aus gebrauchten Altölen, wie Frittieröl gewonnen wurden. Rapsöl, das eine Mischung von mit Glycerin partiell veresterten Fettsäuren ist, ist bevorzugt, da es in großen Mengen erhältlich ist und in einfacher Weise durch Auspressen von Rapssamen erhältlich ist. Des weiteren sind die ebenfalls weit verbreiteten Öle von Sonnenblumen und Soja sowie deren Mischungen mit Rapsöl bevorzugt.
- Als niedrigere Alkylester von Fettsäuren kommen die folgenden in Betracht, beispielsweise als handelsübliche Mischungen: Die Ethyl-, Propyl-, Butyl- und insbesondere Methylester von Fettsäuren mit 12 bis 22 Kohlenstoffatomen, beispielsweise von Laurinsäure, Myristinsäure, Palmitinsäure, Palmitolsäure, Stearinsäure, Ölsäure, Elaidinsäure, Petroselinsäure, Ricinolsäure, Elaeostearinsäure, Linolsäure, Linolensäure, Eicosansäure, Gadoleinsäure, Docosansäure oder Erucasäure, die bevorzugt eine lodzahl von 50 bis 150, insbesondere 90 bis 125 haben. Mischungen mit besonders vorteilhaften Eigenschaften sind solche, die hauptsächlich, d.h. zu mindestens 50 Gew.-%, Methylester von Fettsäuren mit 16 bis 22 Kohlenstoffatomen und 1, 2 oder 3 Doppelbindungen enthalten. Die bevorzugten niedrigeren Alkylester von Fettsäuren sind die Methylester von Ölsäure, Linolsäure, Linolensäure und Erucasäure.
- Handelsübliche Mischungen der genannten Art werden beispielsweise durch Spaltung und Veresterung von tierischen und pflanzlichen Fetten und Ölen durch ihre Umesterung mit niedrigeren aliphatischen Alkoholen erhalten. Zur Herstellung von niedrigeren Alkylestern von Fettsäuren ist es vorteilhaft, von Fetten und Ölen mit hoher lodzahl auszugehen, wie beispielsweise Sonnenblumenöl, Rapsöl, Korianderöl, Castoröl (Ricinusöl), Sojaöl, Baumwollsamenöl, Erdnussöl oder Rindertalg. Niedrigere Alkylester von Fettsäuren auf Basis einer neuen Rapsölsorte, deren Fettsäurekomponente zu mehr als 80 Gew.-% von ungesättigten Fettsäuren mit 18 Kohlenstoffatomen abgeleitet ist, sind bevorzugt.
- Das Mischungsverhältnis der Bestandteile A und B liegt zwischen A:B = 99:1 bis 1:99, speziell 95:5 bis 5:95, beispielhaft 85:15 bis 15:85 oder 80:20 bis 20:80.
- Bestandteil C) ist ein vernetztes Blockcopolymer, das durch Vernetzung aus einem Blockcopolymer von mindestens 2 verschiedenen C2- bis C4-Alkylenoxiden hergestellt ist. Das Blockcopolymer kann aus 2, 3, 4 oder mehr Blöcken bestehen.
- Die verwendeten Blockcopolymere werden wie im Stand der Technik bekannt durch sequentielle Polymerisierung von Alkylenoxiden (Ethylenoxid, Propylenoxid, Butylenoxid) bevorzugt unter alkalischer Katalyse hergestellt. Folgende Formel veranschaulicht beispielhaft die Struktur eines bevorzugt verwendeten Blockcopolymers auf Basis Propylenoxid/Ethylenoxid mit einem mittleren Molgewicht von M* = 10000 g/mol:
- Das zur Herstellung des Blockcopolymers C) verwendete Basispolymer hat im allgemeinen ein Molekulargewicht von 500 bis 100.000 g/mol, vorzugsweise 1000 bis 60.000, insbesondere 4000 bis 50.000 g/mol. Diese Molekulargewichte sind die Molekulargewichte vor der Vernetzung.
- Die Vernetzung der verwendeten Blockcopolymere wird wie im Stand der Technik bekannt durch alkalisch oder sauer katalysierte Ringöffnung von Di-, Tri- oder Tetraglycidylethern, durch Veresterung mit mehrwertigen Carbonsäuren bzw. Carbonsäureanhydriden oder durch Umsetzung mit mehrwertigen Isocyanaten durchgeführt.
- Als Vernetzer kommen solche Verbindungen in Betracht, die sich mit mindestens 2 Bindungsstellen an das Blockpolymer binden können. Beispielhaft seien folgende Vernetzer aufgeführt: Bisphenol-A-diglycidylether, Butan-1,4-dioldiglycidylether, Hexan-1,6-dioldiglycidylether, Ethylenglykoldiglycidylether, Cyclohexandimethanoldiglycidylether, Resorcindiglycidylether, Glycerindiglycidylether, Glycerintriglycidylether, Glycerinpropoxylattriglycidylether, Polyglycerinpolyglycidylether, p-Aminophenoltriglycidylether, Polypropylenglykoldiglycidylether, Pentaerythrittetraglycidylether, Sorbitolpolyglycidylether, Trimethylolpropantriglycidylether, Castoröltriglycidylether, Diaminobiphenyltetraglycidylether, Sojaölepoxid, Adipinsäure, Maleinsäure, Phthalsäure, Maleinsäureanhydrid, Bernsteinsäureanhydrid, Dodecylbernsteinsäureanhydrid, Phthalsäureanhydrid, Trimellitsäureanhydrid, Pyromellitsäureanhydrid, Dimethoxydimethylsilan, Diethoxydimethylsilan, Toluoldiisoyanat und Diphenylmethandiisocyanat.
- Die vernetzten Blockcopolymere C) haben im allgemeinen ein Molekulargewicht von 1000 - 200.000 g/mol, vorzugsweise 2000 bis 100.000, insbesondere 4000 - 50.000 g/mol, gemessen mittels Gelpermeationschromatographie (GPC) gegen Polystyrolstandards in THF.
- Eine wichtige Bestimmungsgröße für die Blockcopolymere C ist ihre Wasserzahl (WZ). Sie wird nach DIN EN 12836 bestimmt, auf die hiermit bezug genommen wird. Zu einem Lösemittel-Gemisch, das aus einem bestimmten Volumen Dioxan und Toluol im Verhältnis 97:3 besteht, und in dem die Blockcopolymerprobe als klare Lösung vorliegt, wird Wasser bei einer Temperatur von (25 ± 1)°C zugegeben, bis eine bleibende Trübung auftritt. Die Wasserzahl wird angegeben in Millilitern Wasser, die benötigt werden, um die bleibende Trübung zu erhalten.
- Vorzugsweise liegt die Wasserzahl im vernetzten Blockcopolymer C) zwischen 6 ml und 25 ml, insbesondere zwischen 6 ml und 17 ml.
- Die vernetzten Blockcopolymere C) werden den A) und B) enthaltenden Mischungen in Mengen von 0,001 bis 5 Gew.-%, bevorzugt 0,005 bis 1 Gew.-% und speziell 0,01 bis 0,05 Gew.-% zugesetzt. Dabei können sie als solche oder auch gelöst bzw. dispergiert in Lösemitteln, wie z.B. aliphatischen und/oder aromatischen Kohlenwasserstoffen oder Kohlenwasserstoffgemischen wie z.B. Toluol, Xylol, Ethylbenzol, Decan, Pentadecan, Benzinfraktionen, Kerosin, Naphtha, Diesel, Heizöl, Isoparaffine oder kommerziellen Lösemittelgemischen wie Solvent Naphtha, ®Shellsol AB, ®Solvesso 150, ®Solvesso 200, ®Exxsol-, ®Isopar- und ®Shellsol D-Typen eingesetzt werden. Bevorzugt sind sie in Brennstofföl tierischen oder pflanzlichen Ursprungs auf Basis von Fettsäurealkylestern gelöst. Bevorzugt enthalten die erfindungsgemäßen Additive 1 - 80 %, speziell 10 - 70 %, insbesondere 25 - 60 % Lösemittel.
- Die vernetzten Blockcopolymere C) können dem zu additivierenden Öl gemäß im Stand der Technik bekannten Verfahren zugeführt werden. Wenn mehr als eine Copolymerkomponente verwendet werden soll, können solche Komponenten zusammen oder separat in beliebiger Kombination in das Öl eingebracht werden.
- Zur Herstellung von Additivpaketen für spezielle Problemlösungen können die vernetzten Blockcopolymere C) auch zusammen mit einem oder mehreren öllöslichen Co-Additiven eingesetzt werden, die bereits für sich allein die Eigenschaften von Rohölen, Schmierölen oder Brennölen verbessern. Beispiele solcher Co-Additive sind polare Verbindungen, die eine Paraffindispergierung bewirken (Paraffindispergatoren), Alkylphenol-Aldehydharze, polymere Kaltfließverbesserer sowie öllösliche Amphiphile.
- So haben sich Mischungen der vernetzten Blockcopolymere C) mit solchen Copolymeren hervorragend bewährt, die 10 bis 40 Gew.-% Vinylacetat und 60 bis 90 Gew.-% Ethylen enthalten. Nach einer weiteren Ausgestaltung der Erfindung setzt man die erfindungsgemäßen Additive in Mischung mit Ethylen/Vinylacetat/Vinyl-2-ethylhexanoat-Terpolymeren, Ethylen/Vinylacetat/Neononansäurevinylester-Terpolymeren und/oder Ethylen-Vinylacetat/Neodecansäurevinylester-Terpolymeren zur gleichzeitigen Verbesserung der Fließfähigkeit und Schmierwirkung von Mineralölen oder Mineralöldestillaten ein. Die Terpolymere der 2-Ethylhexansäurevinylester, Neononansäurevinylester bzw. der Neodecansäurevinylester enthalten außer Ethylen 8 bis 40 Gew.-% Vinylacetat und 1 bis 40 Gew.-% des jeweiligen langkettigen Vinylesters. Weitere bevorzugte Copolymere enthalten neben Ethylen 10 bis 40 Gew.-% Vinylacetat und gegebenenfalls 1 bis 40 Gew.-% Vinylester mit C3- bis C12-Alkylgruppen im Esterrest und gegebenenfalls 0,5 bis 20 Gew.-% Olefine mit 3 bis 10 C-Atomen wie z.B. Isobutylen, Diisobutylen, Propylen, Methylpenten oder Norbornen.
- Bei den Paraffindispergatoren handelt es sich vorzugsweise um niedermolekulare oder polymere, öllösliche Verbindungen mit ionischen oder polaren Gruppen wie z.B. Aminsalze, Imide und/oder Amide. Besonders bevorzugte Paraffindispergatoren enthalten Umsetzungsprodukte primärer und/oder sekundärer Fettamine mit 8 bis 36 C-Atomen, insbesondere Dicocosfettamin, Ditalgfettamin und Distearylamin. Besonders bewährt haben sich Paraffindispergatoren, die durch Reaktion aliphatischer oder aromatischer Amine, vorzugsweise langkettiger aliphatischer Amine, mit aliphatischen oder aromatischen Mono-, Di-, Tri- oder Tetracarbonsäuren oder deren Anhydriden erhalten werden (vgl.
US 4 211 534 ). Andere Paraffindispergatoren sind Copolymere der Malein-, Fumar- und/oder Itaconsäure oder des Maleinsäureanhydrids und weiterer α,β-ungesättigter Verbindungen, die gegebenenfalls mit primären und/oder sekundären Monoalkylaminen und/oder aliphatischen Alkoholen umgesetzt werden können (vgl.EP-A-0 154 177 ), die Umsetzungsprodukte von Alkenylspirobislactonen mit Aminen (vgl.EP-A-0 413 279 B1) und nachEP-A-0 606 055 A2 Umsetzungsprodukte von Terpolymeren auf Basis α,β-ungesättigter Dicarbonsäureanhydride, α,β-ungesättigter Verbindungen und Polyoxylalkylenether niederer ungesättigter Alkohole. - Als Co-Additive, die eine Paraffindispergierung bewirken sind beispielsweise Ester geeignet. Diese Ester leiten sich von Polyolen mit 3 oder mehr OH-Gruppen ab, insbesondere von Glycerin, Trimethylolpropan, Pentaerythrit sowie die daraus durch Kondensation zugänglichen Oligomere mit 2 bis 10 Monomereinheiten wie z.B. Polyglycerin. Die Polyole sind im allgemeinen mit 1 bis 100 mol Alkylenoxid, bevorzugt 3 bis 70, insbesondere 5 bis 50 mol Alkylenoxid pro mol Polyol umgesetzt. Bevorzugte Alkylenoxide sind Ethylenoxid, Propylenoxid und Butylenoxid. Die Alkoxylierung erfolgt nach bekannten Verfahren.
- Die für die Veresterung der alkoxylierten Polyole geeigneten Fettsäuren haben vorzugsweise 8 bis 50, insbesondere 12 bis 30, speziell 16 bis 26 C-Atome. Geeignete Fettsäuren sind beispielsweise Laurin-, Tridecan-, Myristin-, Pentadecan-, Palmitin-, Margarin-, Stearin-, Isostearin-, Arachin- und Behensäure, Öl- und Erucasäure, Palmitolein-, Myristolein, Ricinolsäure, sowie aus natürlichen Fetten und Ölen gewonnene Fettsäuremischungen. Bevorzugte Fettsäuremischungen enthalten mehr als 50 % Fettsäuren mit mindestens 20 C-Atomen. Bevorzugt enthalten weniger als 50 % der zur Veresterung verwendeten Fettsäuren Doppelbindungen, insbesondere weniger als 10 %; speziell sind sie weitestgehend gesättigt. Unter weitestgehend gesättigt soll hier eine lodzahl der verwendeten Fettsäure von bis zu 5 g I pro 100 g Fettsäure verstanden werden. Die Veresterung kann auch ausgehend von reaktiven Derivaten der Fettsäuren wie Estern mit niederen Alkoholen (z.B. Methyl- oder Ethylester) oder Anhydriden erfolgen.
- Zur Veresterung der alkoxylierten Polyole können auch Gemische obiger Fettsäuren mit fettlöslichen, mehrwertigen Carbonsäuren eingesetzt werden. Beispiele für geeignete mehrwertige Carbonsäuren sind Dimerfettsäuren, Alkenylbernsteinsäuren und aromatische Polycarbonsäuren sowie deren Derivate wie Anhydride und C1- bis C5-Ester. Bevorzugt sind Alkenylbernsteinsäuren und deren Derivate mit Alkylresten mit 8 bis 200, insbesondere 10 bis 50 C-Atomen. Beispiele sind Dodecenyl-, Octadecenyl- und Poly(isobutenyl)bernsteinsäureanhydrid. Bevorzugt werden die mehrwertigen Carbonsäuren dabei zu untergeordneten Anteilen von bis zu 30 Mol-%, bevorzugt 1 bis 20 Mol-%, insbesondere 2 bis 10 Mol-% eingesetzt.
- Ester und Fettsäure werden für die Veresterung bezogen auf den Gehalt an Hydroxylgruppen einerseits und Carboxylgruppen andererseits im Verhältnis 1,5:1 bis 1:1,5 eingesetzt, bevorzugt 1,1:1 bis 1:1,1, insbesondere equimolar. Die paraffindispergierende Wirkung ist besonders ausgeprägt, wenn mit einem Säureüberschuss von bis zu 20 Mol-%, speziell bis zu 10 Mol-%, insbesondere bis zu 5 Mol-% gearbeitet wird.
- Die Veresterung wird nach üblichen Verfahren durchgeführt. Besonders bewährt hat sich die Umsetzung von Polyolalkoxylat mit Fettsäure, gegebenenfalls in Gegenwart von Katalysatoren wie z.B. para-Toluolsulfonsäure, C2- bis C50-Alkylbenzolsulfonsäuren, Methansulfonsäure oder sauren Ionenaustauschern. Die Abtrennung des Reaktionswassers kann destillativ durch Direktkondensation oder bevorzugt mittels azeotroper Destillation in Anwesenheit organischer Lösemittel, insbesondere aromatischer Lösemittel wie Toluol, Xylol oder auch höher siedender Gemische wie ®Shellsol A, Shellsol B, Shellsol AB oder Solvent Naphtha erfolgen. Die Veresterung erfolgt bevorzugt vollständig, d.h. für die Veresterung werden 1,0 bis 1,5 mol Fettsäure pro mol Hydroxylgruppen eingesetzt. Die Säurezahl der Ester liegt im allgemeinen unter 15 mg KOH/g, bevorzugt unter 10 mg KOH/g speziell unter 5 mg KOH/g.
- Besonders bevorzugte Paraffindispergatoren werden durch Reaktion von Verbindungen, die eine Acylgruppe enthalten, mit einem Amin hergestellt. Bei diesem Amin handelt es sich um eine Verbindung der Formel NR6R7R8, worin R6, R7 und R8 gleich oder verschieden sein können, und wenigstens eine dieser Gruppen für C8-C36-Alkyl, C6-C36-Cycloalkyl, C8-C36-Alkenyl, insbesondere C12-C24-Alkyl, C12-C24-Alkenyl oder Cyclohexyl steht, und die übrigen Gruppen entweder Wasserstoff, C1-C36-Alkyl, C2-C36-Alkenyl, Cyclohexyl, oder eine Gruppe der Formeln -(A-O)x-E oder -(CH2)n-NYZ bedeuten, worin A für eine Ethylen- oder Propylengruppe steht, x eine Zahl von 1 bis 50, E = H, C1-C30-Alkyl, C5-C12-Cycloalkyl oder C6-C30-Aryl, und n 2, 3 oder 4 bedeuten, und Y und Z unabhängig voneinander H, C1-C30-Alkyl oder -(A-O)x bedeuten. Unter Acylgruppe wird hier eine funktionelle Gruppe folgender Formel verstanden:
>C=O
- Die Paraffindispergatoren können den vernetzten Blockcopolymeren C) beigemischt oder separat dem zu additivierenden Mitteldestillat zugesetzt werden.
- Als Paraffindispergatoren sind auch Alkylphenol-Aldehydharze geeignet. Alkylphenol-Aldehyd-Harze sind prinzipiell bekannt und beispielsweise im Römpp Chemie Lexikon, 9. Auflage, Thieme Verlag 1988-92, Band 4, S. 3351ff. beschrieben. Die Alkyl- oder Alkenylreste des Alkylphenols besitzen 6 - 24, bevorzugt 8 - 22, insbesondere 9 - 18 Kohlenstoffatome. Sie können linear oder bevorzugt verzweigt sein, wobei die Verzweigung sekundäre wie auch tertiäre Strukturelemente enthalten kann. Bevorzugt handelt es sich um n- und iso-Hexyl, n- und iso-Octyl, n- und iso-Nonyl, n- und iso-Decyl, n- und iso-Dodecyl, Tetradecyl, Hexadecyl, Octadecyl, Eicosyl sowie Tripropenyl, Tetrapropenyl, Pentapropenyl und Polyisobutenyl bis C24. Das Alkylphenol-Aldehyd-Harz kann auch bis zu 20 Mol-% Phenoleinheiten und/oder Alkylphenole mit kurzen Alkylketten wie z. B. Butylphenol enthalten. Für das Alkylphenol-Aldehydharz können gleiche oder verschiedene Alkylphenole verwendet werden.
- Der Aldehyd im Alkylphenol-Aldehyd-Harz besitzt 1 bis 10, bevorzugt 1 bis 4 Kohlenstoffatome und kann weitere funktionelle Gruppen tragen. Bevorzugt ist er ein aliphatischer Aldehyd, besonders bevorzugt ist er Formaldehyd.
- Das Molekulargewicht der Alkylphenol-Aldehyd-Harze beträgt vorzugsweise 350 - 10.000, insbesondere 400 - 5000 g/mol. Bevorzugt entspricht dies einem Kondensationsgrad n von 3 bis 40, insbesondere von 4 bis 20. Voraussetzung ist hierbei, dass die Harze öllöslich sind.
- In einer bevorzugten Ausführungsform der Erfindung handelt es sich bei diesen Alkylphenol-Formaldehydharzen um solche, die Oligo- oder Polymere mit einer repetitiven Struktureinheit der Formel
- Die Herstellung der Alkylphenol-Aldehyd-Harze erfolgt in bekannter Weise durch basische Katalyse, wobei Kondensationsprodukte vom Resoltyp entstehen, oder durch saure Katalyse, wobei Kondensationsprodukte vom Novolaktyp entstehen. Die nach beiden Arten gewonnenen Kondensate sind für die erfindungsgemäßen Zusammensetzungen geeignet. Bevorzugt ist die Kondensation in Gegenwart von sauren Katalysatoren.
- Zur Herstellung der Alkylphenol-Aldehyd-Harze werden ein Alkylphenol mit 6 - 24, bevorzugt 8 - 22, insbesondere 9 - 18 C-Atomen je Alkylgruppe, oder Gemische hiervon und mindestens ein Aldehyd miteinander umgesetzt, wobei pro mol Alkylphenolverbindung etwa 0,5 - 2 mol, vorzugsweise 0,7 - 1,3 mol und insbesondere äquimolare Mengen Aldehyd eingesetzt werden.
- Geeignete Alkylphenole sind insbesondere n- und iso-Hexylphenol, n- und isoOctylphenol, n- und iso-Nonylphenol, n- und iso-Decylphenol, n- und iso-Dodecylphenol, Tetradecylphenol, Hexadecylphenol, Octadecylphenol, Eicosylphenol, Tripropenylphenol, Tetrapropenylphenol und Poly(isobutenyl)phenol bis C24.
- Die Alkylphenole sind vorzugsweise para-substituiert. Die Alkylphenole können einen oder mehrere Alkylreste tragen. Vorzugsweise sind sie zu höchstens 5 Mol-%, insbesondere zu höchstens 20 Mol-% und speziell höchstens 40 Mol-% mit mehr als einer Alkylgruppe substituiert. Bevorzugt tragen höchstens 40 Mol-%, insbesondere höchstens 20 Mol-% der eingesetzten Alkylphenole in ortho-Position einen Alkylrest. Speziell sind die Alkylphenole in ortho-Position zur Hydroxylgruppe nicht mit tertiären Alkylgruppen substituiert.
- Der Aldehyd kann ein Mono- oder Dialdehyd sein und weitere funktionelle Gruppen wie -COOH tragen. Besonders geeignete Aldehyde sind Formaldehyd, Acetaldehyd, Butyraldehyd, Glutardialdehyd und Glyoxalsäure, bevorzugt ist Formaldehyd. Der Formaldehyd kann in Form von Paraformaldehyd oder in Form einer vorzugsweise 20 - 40 gew.-%igen wässrigen Formalinlösung eingesetzt werden. Es können auch entsprechende Mengen an Trioxan verwendet werden.
- Die Umsetzung von Alkylphenol und Aldehyd erfolgt üblicherweise in Gegenwart von alkalischen Katalysatoren, beispielsweise Alkalihydroxiden oder Alkylaminen, oder von sauren Katalysatoren, beispielsweise anorganischen oder organischen Säuren, wie Salzsäure, Schwefelsäure, Phosphorsäure, Sulfonsäure, Sulfamidosäuren oder Halogenessigsäuren, und in Gegenwart eines mit Wasser ein Azeotrop bildenden organischen Lösungsmittels, beispielsweise Toluol, Xylol, höheren Aromaten oder Gemischen hiervon. Das Reaktionsgemisch wird auf eine Temperatur von 90 bis 200°C, bevorzugt 100 - 160°C erhitzt, wobei das entstehende Reaktionswasser während der Umsetzung durch azeotrope Destillation entfernt wird. Lösungsmittel, die unter den Bedingungen der Kondensation keine Protonen abspalten, können nach der Kondensationsreaktion in den Produkten bleiben. Die Harze können direkt oder nach Neutralisation des Katalysators eingesetzt werden, gegebenenfalls nach weiterer Verdünnung der Lösung mit aliphatischen und/oder aromatischen Kohlenwasserstoffen oder Kohlenwasserstoffgemischen, z.B. Benzinfraktionen, Kerosin, Decan, Pentadecan, Toluol, Xylol, Ethylbenzol oder Lösungsmitteln wie ®Solvent Naphtha, ®Shellsol AB, ®Solvesso 150, ®Solvesso 200, ®Exxsol, ®ISOPAR- und ®Shellsol D-Typen.
- Schließlich werden in einer weiteren Ausführungsform der Erfindung die vernetzten Blockcopolymere C) zusammen mit Kammpolymeren verwendet. Hierunter versteht man Polymere, bei denen Kohlenwasserstoffreste mit mindestens 8, insbesondere mindestens 10 Kohlenstoffatomen an einem Polymerrückgrat gebunden sind. Vorzugsweise handelt es sich um Homopolymere, deren Alkylseitenketten mindestens 8 und insbesondere mindestens 10 Kohlenstoffatome enthalten. Bei Copolymeren weisen mindestens 20 %, bevorzugt mindestens 30 % der Monomeren Seitenketten auf (vgl. Comb-like Polymers-Structure and Properties; N.A. Plate and V.P. Shibaev, J. Polym. Sci. Macromolecular Revs. 1974, 8, 117 ff). Beispiele für geeignete Kammpolymere sind z.B. Fumarat/Vinylacetat-Copolymere (vgl.
EP 0 153 176 A1 ), Copolymere aus einem C6-C24-α-Olefin und einem N-C6-C22-Alkylmaleinsäureimid (vgl.EP-A-0 320 766 ), ferner veresterte Olefin/ Maleinsäureanhydrid-Copolymere, Polymere und Copolymere von α-Olefinen und veresterte Copolymere von Styrol und Maleinsäureanhydrid. -
- A
- R', COOR', OCOR', R"-COOR' oder OR';
- D
- H, CH3, A oder R;
- E
- H oder A;
- G
- H, R", R"-COOR', einen Arylrest oder einen heterocyclischen Rest;
- M
- H, COOR", OCOR", OR" oder COOH;
- N
- H, R", COOR", OCOR, COOH oder einen Arylrest;
- R'
- eine Kohlenwasserstoffkette mit 8-150 Kohlenstoffatomen;
- R"
- eine Kohlenwasserstoffkette mit 1 bis 10 Kohlenstoffatomen;
- m
- eine Zahl zwischen 0,4 und 1,0; und
- n
- eine Zahl zwischen 0 und 0,6.
- Das Mischungsverhältnis (in Gewichtsteilen) der vernetzten Blockcopolymere C) mit polymeren Kaltfließverbesserern, Paraffindispergatoren, Kammpolymeren bzw. Harzen beträgt jeweils 1 : 1000 bis 1 : 1 , vorzugsweise 1:10 bis 1:50 .
- Die vernetzten Blockcopolymere C) können allein oder auch zusammen mit anderen Additiven verwendet werden, z. B. mit anderen Stockpunkterniedrigern oder Entwachsungshilfsmitteln, mit Korrosionsinhibitoren, Antioxidantien, Lubricity-Additiven Schlamminhibitoren, Dehazern und Zusätzen zur Erniedrigung des Cloud-Points.
- Die Bestimmung des CFPP-Werts erfolgt gemäß EN 116, die der Siedekenndaten gemäß ASTM D-86 und die Bestimmung des Cloud Points gemäß ISO 3015.
Tabelle 1: Analyse des verwendeten Biodiesel Öl Nr. CP CFPP E 1 Rapsölsäuremethylester (RME) -2,3 -14°C E 2 90% Rapsölsäuremethylester (RME) + 10 % Sojaölsäuremethylester (SojaME) -2,0 -8°C Tabelle 2: C-Kettenverteilung der zur Herstellung der Testöle eingesetzten Fettsäuremethylester (Hauptbestandteile; Fl.-% gemäß GC) C16 C16' C18 C18' C18" C18"' C20 C20' C22 Σ gesättigt RME 4,4 0,4 1,6 57,8 21,6 8,8 1,5 0,7 0,2 7,7 SojaME 10,4 0,1 4,1 24,8 51,3 6,9 0,5 0,4 0,4 15,4 Tabelle 3: Charakterisierung der verwendeten Mitteldestillate F1 F2 F3 F4 Schwefelgehalt, ppm 7,9 4,9 32,0 900 Dichte, g/cm3 0,8436 0,8306 0,8348 0,8487 Siedebeginn, °C 209,9 143,9 209,1 203,7 Siedeende, °C 334,6 363,2 347,8 365,6 Siedebereich (90-20), °C 63,5 87,6 83,8 94,9 Aromatengehalt, Gew.-% 25,7 16,5 20,5 29,9 Tabelle 4: Charakterisierung der Copolymere C Polymer Mw [g/mol] Wasserzahl [ml] P1 3000 12,0 P2 3400 9,1 P3 3600 7,6 P4 3100 15,1 P5 3300 11,8 P6 3000 14,2 Tabelle 5: Charakterisierung der Fließverbesserer Beispiel Comonomer(e) V140 CH3/100 CH2 P7 13,6 Mol-% Vinylacetat 130 mPas 3,7 P8 13,7 Mol-% Vinylacetat und 1,4 Mol-% Neodecansäurevinylester 105 mPas 5,3 P9 9,4 Mol-% Vinylacetat 220 mPas 6,2 - Die Prüfung der Emulgierneigung von Additiven erfolgt gemäß ASTM D 1094-85. 80 ml eines Dieselkraftstoffes (hier Mischung aus Mineraldiesel und Biodiesel) werden in einem 100 ml Standzylinder mit 250 ppm des zu testenden Additivs versetzt und 15 Minuten bei 60°C temperiert und dann geschüttelt. Nach Abkühlen auf Raumtemperatur werden 20 ml Pufferlösung (pH = 7) hinzugegeben und 2 Minuten geschüttelt. Nach 5 Minuten wird die Probe optisch nach folgenden Kriterien beurteilt:
Bewertung der Trennschicht Bewertung der Phasentrennung 1 Klar und sauber 1 Komplette Abwesenheit aller Emulsionen und/oder 1b kleine, klare Blasen, die schätzungsweise nicht mehr als 50 % der Trennschicht bedecken. Keine Schlieren, keine Filmbildung oder sonstige Benetzung an der Trennschicht. Abscheidungen in beiden Phasen oder oben auf der Öl-Phase. 2 Wie (1), aber zusätzlich kleine Luftbläschen oder kleine Wassertröpfchen in der Öl-Phase. 2 Schlieren, Filmbildung oder sonstige Benetzung an der Trennschicht 3 Emulsionen und/oder Niederschläge in beiden Phasen oder oben auf der Öl-Phase, 3 Schmaler Saum oder leichte Schaumbildung, oder beides und/oder Tropfen in der WasserPhase oder an der Wandung anhaftend (ausgenommen die 4 Dichter Saum oder starke Schaumbildung, oder beides Wandung über der Öl-Phase). In Klammern gesetzt: Menge der Wasserphase Tabelle 6: Wirksamkeit von Copolymeren als Demulgator in einer Mischung aus 95 Gew.-% F2 und 5 Gew.-% Biodiesel E1 Bsp. Nr. Copolymer optische Beurteilung Dosierung Copolymer ppm Trennschicht Phasentrennung Öl-Phase WasserPhase 1(V) -- 3-4 12 ml 3 trübe klar -- 2(V) P7 4 14 ml 3 trübe klar 250 3(V) P8 3 15 ml 3 trübe klar 250 4(V) P9 4 17 ml 3 trübe klar 250 5 P1 1* 20 ml 3 trübe klar 250 6 P2 1* 20 ml 3 trübe klar 250 7 P3 1b* 20 ml 3 trübe klar 250 8 P4 1* 20 ml 3 trübe klar 250 9 P5 1* 20 ml 3 trübe klar 250 10 P6 1b* 20 ml 3 trübe klar 250 11 P1 1* 20 ml 3 trübe klar 100 12 P1 1* 20 ml 3 trübe klar 50 13 P1 1* 20 ml 3 trübe klar 25 14 P1 1* 20 ml 3 trübe klar 10 15 P2 1* 20 ml 3 trübe klar 100 16 P2 1* 20 ml 3 trübe klar 50 17 P2 1* 20 ml 3 trübe klar 25 18 P2 1* 20 ml 3 trübe klar 10 19 P4 1* 20 ml 3 trübe klar 100 20 P4 1b* 20 ml 3 trübe klar 50 21 P4 1b* 20 ml 3 trübe klar 10 22 P6 1b* 20 ml 3 trübe klar 50 23 P6 2 20 ml 3 trübe klar 10 * deutliche Phasentrennung bereits nach kurzer Zeit (1 bis 2 Min.) Tabelle 7: Wirksamkeit von Copolymeren als Demulgator in einer Mischung aus 95 Gew.-% F2 und 5 Gew.-% Biodiesel E2 Bsp. Nr. Copolymer optische Beurteilung Dosierung Copolymer ppm Trennschicht Phasentrennung Öl-Phase Wasser-Phase 24(V) -- 3-4 14 ml 3 trübe klar -- 25(V) P7 4 13 ml 3 trübe klar 250 26(V) P8 3 17 ml 3 trübe klar 250 27(V) P9 4 16 ml 3 trübe klar 250 28 P1 1* 20 ml 3 trübe klar 250 29 P2 1* 20 ml 3 trübe klar 250 30 P3 1b* 20 ml 3 trübe klar 250 31 P4 1* 20 ml 3 trübe klar 250 32 P5 1* 20 ml 3 trübe klar 250 33 P6 1b* 20 ml 3 trübe klar 250 34 P1 1* 20 ml 3 trübe klar 100 35 P1 1* 20 ml 3 trübe klar 50 36 P1 1* 20 ml 3 trübe klar 25 37 P1 1* 20 ml 3 trübe klar 10 38 P2 1* 20 ml 3 trübe klar 100 39 P2 1* 20 ml 3 trübe klar 50 40 P2 1* 20 ml 3 trübe klar 25 41 P2 1* 20 ml 3 trübe klar 10 42 P4 1* 20 ml 3 trübe klar 100 43 P4 1b* 20 ml 3 trübe klar 50 44 P4 1b* 20 ml 3 trübe klar 10 45 P6 1b* 20 ml 3 trübe klar 50 46 P6 2 20 ml 3 trübe klar 10 * deutliche Phasentrennung bereits nach kurzer Zeit (1 bis 2 Min.) Tabelle 8: Einfluss unterschiedlicher Mischungsverhältnisse zwischen Mitteldestillat und Biokraftstoff auf das Emulgierverhalten Beispiel Mitteldestillat Biokraftstoff Copolymer optische Beurteilung Dosierung Copolymer ppm Trennschicht Phasentrennung Menge Wasserphase Öl-Phase WasserPhase 47 (V) 90 % F1 10 % E1 - 3-4 3 11 ml trüb klar - 48 (V) 95 % F1 5 % E1 - 1b 3 20 ml trüb klar - 49 90 % F1 10 % E1 P1 1-2 größere, klare Luftblasen 3 20 ml trüb klar 10 50 (V) 90 % F2 10 % E1 - 3-4 3 9 ml trüb klar - 51 (V) 95 % F2 5 % E1 - 3-4 3 12 ml trüb klar - 52 90 % F2 10 % E1 P2 1-2 3 20 ml trüb klar 10 53 (V) 90 % F3 10 % E1 - 4 3 13 ml trüb klar - 54 (V) 95 % F3 5 % E1 - 4 3 9 ml trüb klar - 55 90 % F3 10 % E1 P4 1 3 20 ml trüb klar 10 56 (V) 90 % F1 10 % E2 - 4 3 8 ml trüb klar - 57 (V) 95 % F1 5 % E2 - 3-4 3 13 ml trüb klar - 58 90 % F1 10 % E2 P1 1 3 20 ml trüb klar 10 59 (V) 90 % F2 10 % E2 - 4 3 10 ml trüb klar - 60 (V) 95 % F2 5 % E2 - 3-4 3 14 ml trüb klar - 61 90 % F2 10 % E2 P2 1b 3 20 ml trüb klar 10 62 (V) 90 % F3 10 % E2 - 3-4 3 11 trüb klar - 63 (V) 95 % F3 5 % E2 - 3 3 15 trüb klar - 64 90 % F3 10 % E2 P4 1 3 20 ml trüb klar 10 - Einfluss des Blockcopolymers auf die Wirkung von Kaltfließeigenschaften
- Es wurden ein Mitteldestillat mit einem CFPP von -7°C und dessen Mischung mit 5 % des beschriebenen Biokraftstoffs (CFPP der Mischung ebenfalls -7°C) mit Kaltfließverbesserer und Blockcopolymeren untersucht
Tabelle 9: Beeinflussung der Kaltfließeigenschaften durch Blockcopolymere Copolymere Beispiel Brennstofföl 300 ppm P7 300 ppm P8 300 ppm P7 + 10 ppm P1 300 ppm P8+ 10 ppm P1 65(V) Mitteldestillat -22 -20 -23 -20 66 Mitteldestillat + Biokraftstoff -23 -21 -24 -19 - Einfluss der Blockcopolymere auf das Emulgierverhalten der Diesel/Biodiesel-Mischung in Anwesenheit von Fließverbesserern
- Das Emulgierverhalten des Öls F4 mit Zusatz von 5 Gew.-% Biokraftstoff E1 bzw. E2 wurde durch die Zugabe von 10 ppm P1 deutlich geändert und zeigte kaum Emulgierneigung trotz Anwesenheit von 300 ppm eines Fließverbesserers.
Tabelle 10: Einfluss von Kaltfließverbesserern auf die Emulgierneigung mit und ohne Copolymer C) (hier P1) Bsp. Öl Kälteadditiv optische Beurteilung Dosierung P1 [ppm] Trennschicht Phasentrennung Öl-Phase WasserPhase 67(V) F4 P7 1b 20 ml 3 trüb klar - 68(V) F4+E1 P7 3 14 ml 3 trüb klar - 69 F4+E1 P7 1* 20 ml 3 trüb klar 10 70 F4+E1 P7 1 20 ml 3 trüb klar 250 71 F4+E2 P7 1b 20 ml 3 trüb klar 10 72 F4+E2 P7 1 20 ml 3 trüb klar 250 73(V) F4 P8 1b 20 ml 3 trüb klar - 74(V) F4+E1 P8 3 13 ml 3 trüb klar - 75 F4+E1 P8 1 20 ml 3 trüb klar 10 76 F4+E1 P8 1 20 ml 3 trüb klar 250 77 F4+E2 P8 1b 20 ml 3 trüb klar 10 78 F4+E2 P8 1 20 ml 3 trüb klar 250
Claims (10)
- Brennstofföl, enthaltend einen größeren Anteil einer Mischung ausA) einem Mitteldestillat-Brennstofföl, undB) einem Biobrennstofföl,
im Mischungsverhältnis A:B = 99:1 bis 1:99 sowieC) 0,001 bis 5 Gew.-% eines öllöslichen, vernetzten Blockcopolymers aus C2- bis C4-Alkylenoxiden. - Brennstofföl nach Anspruch 1, worin das Molekulargewicht des vernetzten Bestandteils C) zwischen 1000 und 200.000 g/mol liegt, gemessen mittels Gelpermeationschromatographie gegen Polystyrolstandards in THF.
- Brennstofföl nach Anspruch 1 und/oder 2, worin das Blockcopolymer C) eine Wasserzahl von 6 bis 17 ml aufweist, bestimmt nach DIN EN 12836.
- Brennstofföl nach einem oder mehreren der Ansprüche 1 bis 3, worin der Vernetzer ausgewählt ist aus Bisphenol-A-diglycidylether, Butan-1,4-dioldiglycidylether, Hexan-1,6-dioldiglycidylether, Ethylenglykoldiglycidylether, Cyclohexandimethanoldiglycidylether, Resorcindiglycidylether, Glycerindiglycidylether, Glycerintriglycidylether, Glycerinpropoxylattriglycidylether, Polyglycerinpolyglycidylether, p-Aminophenoltriglycidylether, Polypropylenglykoldiglycidylether, Pentaerythrittetraglycidylether, Sorbitolpolyglycidylether, Trimethylolpropantriglycidylether, Castoröltriglycidylether, Diaminobiphenyltetraglycidylether, Sojaölepoxid, Adipinsäure, Maleinsäure, Phthalsäure, Maleinsäureanhydrid, Bernsteinsäureanhydrid, Dodecylbernsteinsäureanhydrid, Phthalsäureanhydrid, Trimellitsäureanhydrid, Pyromellitsäureanhydrid, Dimethoxydimethylsilan, Diethoxydimethylsilan, Toluoldiisoyanat und Diphenylmethandiisocyanat.
- Brennstofföle nach einem oder mehreren der Ansprüche 1 bis 4, welche zusätzlich zu den Bestandteilen A), B) und C) noch mindestens ein Alkylphenol-Formaldehydharz der Formel
- Brennstofföle nach einem oder mehreren der Ansprüche 1 bis 5, welche zusätzlich zu den Bestandteilen A), B) und C) noch mindestens ein Copolymer enthalten, welches neben Ethylen 10 bis 40 Gew.-% Vinylacetat und gegebenenfalls 1 bis 40 Gew.-% Vinylester mit C3- bis C12-Alkylgruppen im Esterrest und gegebenenfalls 0,5 bis 20 Gew.-% Olefine mit 3 bis 10 C-Atomen enthält.
- Brennstofföle nach einem oder mehreren der Ansprüche 1 bis 6, welche zusätzlich zu den Bestandteilen A), B) und C) noch mindestens ein Aminsalz, Imid oder Amid eines primären und/oder sekundären Fettamins mit 8 bis 36 Kohlenstoffatomen umfassen.
- Brennstofföle nach einem oder mehreren der Ansprüche 1 bis 7, welche zusätzlich zu den Bestandteilen A), B) und C) noch mindestens ein Copolymer enthalten, welches von Amiden, Imiden und/oder Estern der Maleinsäure, Fumarsäure und/oder Itaconsäure abgeleitet ist.
- Brennstofföle nach einem oder mehreren der Ansprüche 1 bis 8, welche zusätzlich zu den Bestandteilen A), B) und C) noch ein Kammpolymer der Formel
- Verwendung eines Blockcopolymers C) wie in Anspruch 1 definiert zur Demulgierung von Mischungen aus Mitteldestillat-Brennstoffölen, Biobrennstoffölen und Wasser.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102004002080 | 2004-01-15 | ||
| DE102004002080A DE102004002080B4 (de) | 2004-01-15 | 2004-01-15 | Demulgatoren für Mischungen aus Mitteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs und Wasser |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP1555309A1 EP1555309A1 (de) | 2005-07-20 |
| EP1555309B1 true EP1555309B1 (de) | 2015-10-21 |
Family
ID=34609561
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP04030573.2A Expired - Lifetime EP1555309B1 (de) | 2004-01-15 | 2004-12-23 | Demulgatoren für Mischungen aus MItteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs und Wasser |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US7815698B2 (de) |
| EP (1) | EP1555309B1 (de) |
| JP (1) | JP2005200651A (de) |
| CA (1) | CA2493178C (de) |
| DE (1) | DE102004002080B4 (de) |
| NO (1) | NO20050180L (de) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20110139106A1 (en) * | 2007-08-09 | 2011-06-16 | 21St Century R & D, Llc | Modification of fats and oils for fuel and lubricating applications |
| US20090038692A1 (en) * | 2007-08-09 | 2009-02-12 | 21St Century R & D, Llc | Modification of vegetable oils for fuel applications |
| US20090293344A1 (en) * | 2008-05-30 | 2009-12-03 | Baker Hughes Incorporated | Process for Removing Water and Water Soluble Contaminants From Biofuels |
| US9127226B2 (en) * | 2008-06-06 | 2015-09-08 | Baker Hughes Incorporated | Process for clarifying biofuels |
| US8962059B1 (en) | 2011-05-27 | 2015-02-24 | Superior Oil Company, Inc. | Bio-based oil composition and method for producing the same |
| GB201113392D0 (en) * | 2011-08-03 | 2011-09-21 | Innospec Ltd | Fuel compositions |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3511882A (en) * | 1964-03-06 | 1970-05-12 | Nalco Chemical Co | Products of reaction of polyoxyalkylene alcohols and di-glycidyl ethers of bis-phenol compounds |
| US3344083A (en) | 1966-03-04 | 1967-09-26 | Petrolite Corp | Process of breaking emulsions |
| DE2227546C3 (de) | 1972-06-07 | 1979-04-05 | Basf Ag, 6700 Ludwigshafen | Verwendung von oxalkylierten PoIyalkylenpolyaminen zur SchneUentwässening von Rohölen |
| US3879308A (en) * | 1973-05-14 | 1975-04-22 | Lubrizol Corp | Lubricants and fuels containing ester-containing compositions |
| US4211534A (en) | 1978-05-25 | 1980-07-08 | Exxon Research & Engineering Co. | Combination of ethylene polymer, polymer having alkyl side chains, and nitrogen containing compound to improve cold flow properties of distillate fuel oils |
| US4183821A (en) * | 1978-05-26 | 1980-01-15 | Basf Wyandotte Corporation | Heteric/block polyoxyalkylene compounds as crude oil demulsifiers |
| US4398921A (en) * | 1981-11-02 | 1983-08-16 | Ethyl Corporation | Gasohol compositions |
| US4460380A (en) * | 1982-12-27 | 1984-07-17 | Exxon Research & Engineering Co. | Water shedding agents in distillate fuel oils |
| DE3300866A1 (de) | 1983-01-13 | 1984-07-19 | Basf Ag, 6700 Ludwigshafen | Oxalkylierte polyamidoamine, deren herstellung und deren verwendung als erdoelemulsionsspalter |
| DE3405843A1 (de) | 1984-02-17 | 1985-08-29 | Bayer Ag, 5090 Leverkusen | Copolymere auf basis von maleinsaeureanhydrid und (alpha), (beta)-ungesaettigten verbindungen, ein verfahren zu ihrer herstellung und ihre verwendung als paraffininhibitoren |
| EP0153177B1 (de) | 1984-02-21 | 1991-11-06 | Exxon Research And Engineering Company | Mitteldestillat-Zusammensetzungen mit Fliesseigenschaften bei Kälte |
| US4561861A (en) * | 1984-11-01 | 1985-12-31 | Texaco Inc. | Motor fuel composition |
| JPH0777986B2 (ja) * | 1985-01-31 | 1995-08-23 | 京セラ株式会社 | 炭化珪素質焼結体の製法 |
| US4551152A (en) * | 1985-04-01 | 1985-11-05 | Texaco Inc. | Alcohol fuel anti-wear additive |
| DE3640613A1 (de) | 1986-11-27 | 1988-06-09 | Ruhrchemie Ag | Verfahren zur herstellung von ethylen-mischpolymerisaten und deren verwendung als zusatz zu mineraloel und mineraloelfraktionen |
| DE3742630A1 (de) | 1987-12-16 | 1989-06-29 | Hoechst Ag | Polymermischungen fuer die verbesserung der fliessfaehigkeit von mineraloeldestillaten in der kaelte |
| US5196486A (en) * | 1989-03-17 | 1993-03-23 | Nalco Chemical Company | Alkoxylated vinyl polymer demulsifiers |
| US4985046A (en) * | 1989-06-09 | 1991-01-15 | E. I. Du Pont De Nemours And Company | Process for preparing poly (paraphenylene terephthalamide) fibers dyeable with cationic dyes |
| DE3926992A1 (de) | 1989-08-16 | 1991-02-21 | Hoechst Ag | Verwendung von umsetzungsprodukten von alkenylspirobislactonen und aminen als paraffindispergatoren |
| DE4136661A1 (de) | 1991-11-07 | 1993-05-13 | Basf Ag | Erdoelemulsionsspalter |
| US5464549A (en) * | 1991-12-12 | 1995-11-07 | Ethyl Corporation | Oil soluble dispersants suitable for use in fuels and lubricants |
| DE4142579A1 (de) | 1991-12-21 | 1993-06-24 | Basf Ag | Erdoelemulsionsspalter auf der basis eines alkoxylats und verfahren zur herstellung dieses alkoxylats |
| GB9204709D0 (en) | 1992-03-03 | 1992-04-15 | Exxon Chemical Patents Inc | Additives for oils |
| GB9222458D0 (en) | 1992-10-26 | 1992-12-09 | Exxon Chemical Patents Inc | Oil additives and compositions |
| IL107927A0 (en) * | 1992-12-17 | 1994-04-12 | Exxon Chemical Patents Inc | Oil soluble ethylene/1-butene copolymers and lubricating oils containing the same |
| DK0606055T3 (da) | 1993-01-06 | 1998-04-14 | Clariant Gmbh | Terpolymerer på basis af alfa,beta-umættede dicarboxylsyreanhydrider, alfa-beta-umættede forbindelser og polyoxyalkylenethere af lavere umættede alkoholer |
| GB9303924D0 (en) | 1993-02-26 | 1993-04-14 | Exxon Chemical Patents Inc | Oil additives and compositions |
| US5749923A (en) * | 1993-11-23 | 1998-05-12 | Degussa Aktiengellschaft | Method for bleaching denim textile material |
| DE4418800A1 (de) | 1994-05-30 | 1995-12-07 | Basf Ag | Verfahren zur Abtrennung vom Wasser aus Rohöl und hierbei verwendete Erdölemulsionsspalter |
| DE59708189D1 (de) | 1997-01-07 | 2002-10-17 | Clariant Gmbh | Verbesserung der Fliessfähigkeit von Mineralölen und Mineralöldestillaten unter Verwendung von Alkylphenol-Aldehydharzen |
| BR9915587A (pt) | 1998-11-23 | 2001-08-07 | Pure Energy Corp | Composição combustìvel |
| GB9827366D0 (en) * | 1998-12-11 | 1999-02-03 | Exxon Chemical Patents Inc | Macromolecular materials |
| DE50011064D1 (de) * | 2000-01-11 | 2005-10-06 | Clariant Gmbh | Mehrfunktionelles Additiv für Brennstofföle |
-
2004
- 2004-01-15 DE DE102004002080A patent/DE102004002080B4/de not_active Expired - Fee Related
- 2004-12-23 EP EP04030573.2A patent/EP1555309B1/de not_active Expired - Lifetime
-
2005
- 2005-01-12 NO NO20050180A patent/NO20050180L/no unknown
- 2005-01-13 JP JP2005006739A patent/JP2005200651A/ja not_active Withdrawn
- 2005-01-14 US US11/036,693 patent/US7815698B2/en not_active Expired - Fee Related
- 2005-01-14 CA CA2493178A patent/CA2493178C/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| DE102004002080A1 (de) | 2005-09-01 |
| EP1555309A1 (de) | 2005-07-20 |
| NO20050180D0 (no) | 2005-01-12 |
| US7815698B2 (en) | 2010-10-19 |
| JP2005200651A (ja) | 2005-07-28 |
| CA2493178C (en) | 2013-07-09 |
| CA2493178A1 (en) | 2005-07-15 |
| NO20050180L (no) | 2005-07-18 |
| US20050155282A1 (en) | 2005-07-21 |
| DE102004002080B4 (de) | 2007-03-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1541664B1 (de) | Brennstofföle aus Mitteldestillaten und Ölen pflanzlichen oder tierischen Ursprungs mit verbesserten Kälteeigenschaften | |
| DE69903545T2 (de) | Ölzusammensetzungen | |
| EP1458837B1 (de) | Schwefelarme mineraloldestillate mit verbesserten kälteeigenschaften, umfassend einen ester eines alkoxylierten polyols und ein copolymer aus ethylen und ungesättigten estern | |
| EP1541662B1 (de) | Brennstofföle aus Mitteldestillaten und Ölen pflanzlichen oder tierischen Ursprungs mit verbesserten Kälteeigenschaften | |
| EP1801187B2 (de) | Detergenzadditive enthaltende Mineralöle mit verbesserter Kältefliessfähigkeit | |
| DE10319028B4 (de) | Demulgatoren für Mischungen aus Mitteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs | |
| EP1380634B1 (de) | Oxidationsstabilisierte Schmieradditive für hochentschwefelte Brennstofföle | |
| DE10155747B4 (de) | Additive für schwefelarme Mineralöldestillate, umfassend einen Ester eines alkoxylierten Polyols und ein Alkylphenol-Aldehydharz | |
| DE102007028306A1 (de) | Detergenzadditive enthaltende Mineralöle mit verbesserter Kältefließfähigkeit | |
| DE102004024532B4 (de) | Demulgatoren für Mischungen aus Mitteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs und Wasser | |
| EP1555309B1 (de) | Demulgatoren für Mischungen aus MItteldestillaten mit Brennstoffölen pflanzlichen oder tierischen Ursprungs und Wasser | |
| EP1621600B1 (de) | Mineralöle mit verbesserter Leitfähigkeit und Kältefliessfähigkeit | |
| EP4127106B1 (de) | Zusammensetzungen und verfahren zur dispergierung von paraffinen in schwefelarmen brennstoffölen | |
| EP1380633B1 (de) | Verwendung von öligen Flüssigkeiten zur Verbesserung der Oxidationsstabilität der Brennstofföle | |
| DE102005045134B4 (de) | Alkylphenol-Aldehydharze, diese enthaltende Zusammensetzungen zu Verbesserung der Kältefließfähigkeit und Schmierfähigkeit von Brennstoffölen sowie deren Verwendung | |
| DE102005020264B4 (de) | Additive für schwefelarme Mineralöldestillate, umfassend Aromaten, welche eine Hydroxygruppe, eine Methoxygruppe und eine Säurefunktion tragen | |
| DE10252973A1 (de) | Oxidationsstabilisierte Schmieradditive für hochentschwefelte Brennstofföle | |
| DE102005061465B4 (de) | Detergenzadditive enthaltende Mineralöle mit verbesserter Kältefließfähigkeit | |
| DE10252972A1 (de) | Oxidationsstabilisierte ölige Flüssigkeiten auf Basis pflanzlicher oder tierischer Öle |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HU IE IS IT LI LT LU MC NL PL PT RO SE SI SK TR |
|
| AX | Request for extension of the european patent |
Extension state: AL BA HR LV MK YU |
|
| RAP1 | Party data changed (applicant data changed or rights of an application transferred) |
Owner name: CLARIANT PRODUKTE (DEUTSCHLAND) GMBH |
|
| 17P | Request for examination filed |
Effective date: 20060120 |
|
| AKX | Designation fees paid |
Designated state(s): AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HU IE IS IT LI LT LU MC NL PL PT RO SE SI SK TR |
|
| 17Q | First examination report despatched |
Effective date: 20061204 |
|
| GRAP | Despatch of communication of intention to grant a patent |
Free format text: ORIGINAL CODE: EPIDOSNIGR1 |
|
| INTG | Intention to grant announced |
Effective date: 20150608 |
|
| RBV | Designated contracting states (corrected) |
Designated state(s): DE FR GB IT |
|
| GRAS | Grant fee paid |
Free format text: ORIGINAL CODE: EPIDOSNIGR3 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): DE FR GB IT |
|
| REG | Reference to a national code |
Ref country code: GB Ref legal event code: FG4D Free format text: NOT ENGLISH |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: PLFP Year of fee payment: 12 |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R096 Ref document number: 502004015058 Country of ref document: DE |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 20151021 Year of fee payment: 12 Ref country code: IT Payment date: 20151021 Year of fee payment: 12 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 20151030 Year of fee payment: 12 |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R097 Ref document number: 502004015058 Country of ref document: DE |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 20160530 Year of fee payment: 12 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed |
Effective date: 20160722 |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R119 Ref document number: 502004015058 Country of ref document: DE |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 20161223 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST Effective date: 20170831 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170102 Ref country code: IT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20161223 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20161223 Ref country code: DE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170701 |