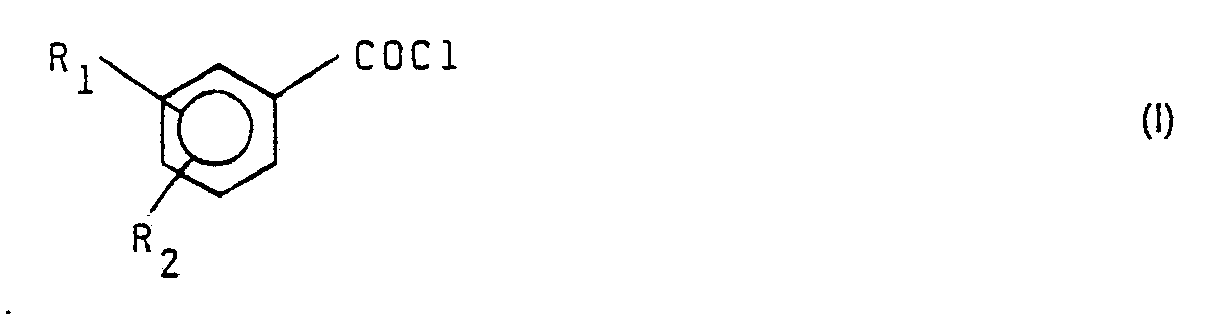EP0012200B2 - Verfahren zur Herstellung von farbstabilisierten, aromatischen Carbonsäurechloriden - Google Patents
Verfahren zur Herstellung von farbstabilisierten, aromatischen Carbonsäurechloriden Download PDFInfo
- Publication number
- EP0012200B2 EP0012200B2 EP79104197A EP79104197A EP0012200B2 EP 0012200 B2 EP0012200 B2 EP 0012200B2 EP 79104197 A EP79104197 A EP 79104197A EP 79104197 A EP79104197 A EP 79104197A EP 0012200 B2 EP0012200 B2 EP 0012200B2
- Authority
- EP
- European Patent Office
- Prior art keywords
- halogen
- alkoxy
- radicals
- alkyl
- aromatic carboxylic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
- -1 aromatic carboxylic acid chlorides Chemical class 0.000 title claims description 95
- 238000004519 manufacturing process Methods 0.000 title 1
- 229910052736 halogen Inorganic materials 0.000 claims description 25
- 150000002367 halogens Chemical class 0.000 claims description 25
- 125000000217 alkyl group Chemical group 0.000 claims description 23
- 239000003381 stabilizer Substances 0.000 claims description 15
- 125000003545 alkoxy group Chemical group 0.000 claims description 14
- 125000004432 carbon atom Chemical group C* 0.000 claims description 14
- 125000003118 aryl group Chemical group 0.000 claims description 12
- 238000000034 method Methods 0.000 claims description 11
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 9
- 150000003254 radicals Chemical class 0.000 claims description 9
- 229910052739 hydrogen Inorganic materials 0.000 claims description 8
- 239000001257 hydrogen Substances 0.000 claims description 8
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 8
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 claims description 6
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims description 5
- RQNWIZPPADIBDY-UHFFFAOYSA-N arsenic atom Chemical compound [As] RQNWIZPPADIBDY-UHFFFAOYSA-N 0.000 claims description 5
- 125000004104 aryloxy group Chemical group 0.000 claims description 5
- 150000001875 compounds Chemical class 0.000 claims description 5
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims description 4
- XEMRAKSQROQPBR-UHFFFAOYSA-N (trichloromethyl)benzene Chemical compound ClC(Cl)(Cl)C1=CC=CC=C1 XEMRAKSQROQPBR-UHFFFAOYSA-N 0.000 claims description 3
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 claims description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 claims description 3
- 125000004423 acyloxy group Chemical group 0.000 claims description 3
- 125000003342 alkenyl group Chemical group 0.000 claims description 3
- 229910052785 arsenic Inorganic materials 0.000 claims description 3
- 125000004429 atom Chemical group 0.000 claims description 3
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 3
- 238000006243 chemical reaction Methods 0.000 claims description 3
- 239000012442 inert solvent Substances 0.000 claims description 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 claims description 3
- 239000011976 maleic acid Substances 0.000 claims description 3
- 150000002825 nitriles Chemical class 0.000 claims description 3
- 229910052698 phosphorus Inorganic materials 0.000 claims description 3
- 239000011574 phosphorus Substances 0.000 claims description 3
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 claims description 3
- FAIAAWCVCHQXDN-UHFFFAOYSA-N phosphorus trichloride Chemical compound ClP(Cl)Cl FAIAAWCVCHQXDN-UHFFFAOYSA-N 0.000 claims description 2
- XYIBRDXRRQCHLP-UHFFFAOYSA-N ethyl acetoacetate Chemical compound CCOC(=O)CC(C)=O XYIBRDXRRQCHLP-UHFFFAOYSA-N 0.000 claims 1
- 230000003019 stabilising effect Effects 0.000 claims 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 14
- 241001550224 Apha Species 0.000 description 11
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 8
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 8
- 229910052801 chlorine Inorganic materials 0.000 description 8
- 239000000460 chlorine Substances 0.000 description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 8
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 8
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 8
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 8
- 239000000463 material Substances 0.000 description 6
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 6
- 125000005425 toluyl group Chemical group 0.000 description 6
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 5
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 5
- 229910052794 bromium Inorganic materials 0.000 description 5
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 5
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 5
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 5
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 4
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 4
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 4
- 229910052731 fluorine Inorganic materials 0.000 description 4
- 239000011737 fluorine Substances 0.000 description 4
- 125000005394 methallyl group Chemical group 0.000 description 4
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 4
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 4
- 229920002554 vinyl polymer Polymers 0.000 description 4
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 3
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 150000005840 aryl radicals Chemical class 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- JBKVHLHDHHXQEQ-UHFFFAOYSA-N epsilon-caprolactam Chemical compound O=C1CCCCCN1 JBKVHLHDHHXQEQ-UHFFFAOYSA-N 0.000 description 3
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 3
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 3
- 230000006641 stabilisation Effects 0.000 description 3
- 238000011105 stabilization Methods 0.000 description 3
- GPZXFICWCMCQPF-UHFFFAOYSA-N 2-methylbenzoyl chloride Chemical compound CC1=CC=CC=C1C(Cl)=O GPZXFICWCMCQPF-UHFFFAOYSA-N 0.000 description 2
- 125000005916 2-methylpentyl group Chemical group 0.000 description 2
- 125000005917 3-methylpentyl group Chemical group 0.000 description 2
- WDJHALXBUFZDSR-UHFFFAOYSA-N Acetoacetic acid Natural products CC(=O)CC(O)=O WDJHALXBUFZDSR-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 2
- XXROGKLTLUQVRX-UHFFFAOYSA-N allyl alcohol Chemical compound OCC=C XXROGKLTLUQVRX-UHFFFAOYSA-N 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 2
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cyclohexene Chemical compound C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 description 2
- 238000002845 discoloration Methods 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- RGSFGYAAUTVSQA-UHFFFAOYSA-N pentamethylene Natural products C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 2
- 125000004817 pentamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 2
- FDPIMTJIUBPUKL-UHFFFAOYSA-N pentan-3-one Chemical compound CCC(=O)CC FDPIMTJIUBPUKL-UHFFFAOYSA-N 0.000 description 2
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- LTMRRSWNXVJMBA-UHFFFAOYSA-L 2,2-diethylpropanedioate Chemical compound CCC(CC)(C([O-])=O)C([O-])=O LTMRRSWNXVJMBA-UHFFFAOYSA-L 0.000 description 1
- CEOCVKWBUWKBKA-UHFFFAOYSA-N 2,4-dichlorobenzoyl chloride Chemical compound ClC(=O)C1=CC=C(Cl)C=C1Cl CEOCVKWBUWKBKA-UHFFFAOYSA-N 0.000 description 1
- ONIKNECPXCLUHT-UHFFFAOYSA-N 2-chlorobenzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1Cl ONIKNECPXCLUHT-UHFFFAOYSA-N 0.000 description 1
- BDDNYDPRCCDQQJ-UHFFFAOYSA-N 3'-(3-hydroxyphenyl)-4-methylspiro[1h-1,4-benzodiazepine-3,2'-oxirane]-2,5-dione Chemical compound CN1C(=O)C2=CC=CC=C2NC(=O)C11OC1C1=CC=CC(O)=C1 BDDNYDPRCCDQQJ-UHFFFAOYSA-N 0.000 description 1
- WHIHIKVIWVIIER-UHFFFAOYSA-N 3-chlorobenzoyl chloride Chemical compound ClC(=O)C1=CC=CC(Cl)=C1 WHIHIKVIWVIIER-UHFFFAOYSA-N 0.000 description 1
- RKIDDEGICSMIJA-UHFFFAOYSA-N 4-chlorobenzoyl chloride Chemical compound ClC(=O)C1=CC=C(Cl)C=C1 RKIDDEGICSMIJA-UHFFFAOYSA-N 0.000 description 1
- 125000006283 4-chlorobenzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1Cl)C([H])([H])* 0.000 description 1
- NQUVCRCCRXRJCK-UHFFFAOYSA-N 4-methylbenzoyl chloride Chemical compound CC1=CC=C(C(Cl)=O)C=C1 NQUVCRCCRXRJCK-UHFFFAOYSA-N 0.000 description 1
- OSDWBNJEKMUWAV-UHFFFAOYSA-N Allyl chloride Chemical compound ClCC=C OSDWBNJEKMUWAV-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- GVOUFPWUYJWQSK-UHFFFAOYSA-N Cyclofenil Chemical group C1=CC(OC(=O)C)=CC=C1C(C=1C=CC(OC(C)=O)=CC=1)=C1CCCCC1 GVOUFPWUYJWQSK-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- IEPRKVQEAMIZSS-UHFFFAOYSA-N Di-Et ester-Fumaric acid Natural products CCOC(=O)C=CC(=O)OCC IEPRKVQEAMIZSS-UHFFFAOYSA-N 0.000 description 1
- IEPRKVQEAMIZSS-WAYWQWQTSA-N Diethyl maleate Chemical compound CCOC(=O)\C=C/C(=O)OCC IEPRKVQEAMIZSS-WAYWQWQTSA-N 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 1
- 238000005863 Friedel-Crafts acylation reaction Methods 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- IKHGUXGNUITLKF-XPULMUKRSA-N acetaldehyde Chemical compound [14CH]([14CH3])=O IKHGUXGNUITLKF-XPULMUKRSA-N 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- MXMOTZIXVICDSD-UHFFFAOYSA-N anisoyl chloride Chemical compound COC1=CC=C(C(Cl)=O)C=C1 MXMOTZIXVICDSD-UHFFFAOYSA-N 0.000 description 1
- OEYOHULQRFXULB-UHFFFAOYSA-N arsenic trichloride Chemical compound Cl[As](Cl)Cl OEYOHULQRFXULB-UHFFFAOYSA-N 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- LDHQCZJRKDOVOX-NSCUHMNNSA-N crotonic acid Chemical compound C\C=C\C(O)=O LDHQCZJRKDOVOX-NSCUHMNNSA-N 0.000 description 1
- 229960002944 cyclofenil Drugs 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- FQPSGWSUVKBHSU-UHFFFAOYSA-N methacrylamide Chemical compound CC(=C)C(N)=O FQPSGWSUVKBHSU-UHFFFAOYSA-N 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- LDHQCZJRKDOVOX-UHFFFAOYSA-N trans-crotonic acid Natural products CC=CC(O)=O LDHQCZJRKDOVOX-UHFFFAOYSA-N 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/58—Preparation of carboxylic acid halides
- C07C51/64—Separation; Purification; Stabilisation; Use of additives
Definitions
- the invention relates to a process for the preparation of color-stabilized, aromatic carboxylic acid chlorides.
- Aromatic carboxylic acid chlorides which were obtained by reacting the corresponding aromatic carboxylic acids with benzotrichloride, often have the unpleasant property of becoming discolored during storage. The discoloration of the aromatic carboxylic acid chlorides can still occur after their distillation.
- a particular advantage of the color stabilization of aromatic carboxylic acid chlorides according to the invention is that, on the one hand, the stabilization is permanent and, on the other hand, the color-stabilized, aromatic carboxylic acid chlorides are surprisingly simple, i. H. without affecting the reactivity of the aromatic carboxylic acid chlorides, for further reactions, e.g. B. Friedel-Crafts acylations can be used.
- Suitable alkyl or alkoxy radicals of the formula I are, for example, those having up to 10 carbon atoms, preferably up to 4 carbon atoms, for.
- Halogen fluorine, chlorine, bromine, preferably chlorine, may be mentioned.
- B. color-stabilized aromatic carboxylic acid chlorides benzoyl chloride, o-toluic acid chloride, p-toluic acid chloride, 2-chloro-benzoyl chloride, 3-chloro-benzoyl chloride, 4-chlorobenzoyl chloride, 2,4-dichlorobenzoyl chloride and anisic acid chloride.
- Color stabilizers are those of the general formula (II) wherein R 3 and R 4 may be the same or different and for hydrogen, optionally substituted by halogen, lower alkyl or lower alkoxy substituted alkoxy, aryioxy, aralkoxy, alkyl, aralkyl, aryl, alkenyl, mono- or dialkylamino radicals stand, furthermore R 3 and R 4 can form a ring with the carbonyl group and where R 3 and R 4 have up to 12 C atoms, used for the process according to the invention.
- Halogen fluorine, chlorine, bromine, preferably chlorine, may be mentioned.
- the radicals R 3 and R 4 in the above formula are preferably hydrocarbon radicals having up to 8 carbon atoms, for.
- Aryloxy radicals such as phenoxy, chlorophenoxy, cresyl, preferably phenoxy;
- Aralkoxy radicals such as benzyloxy, p-chlorobenzyloxy, p-tolyloxy, preferably benzyloxy;
- Alkyl radicals such as methyl, ethyl, n-propyl, iso-propyl, 'n-butyl, iso-butyl, tert-butyl, n-pentyl, iso-pentyl, 2-methylpentyl, 3-methylpentyl, n-hexyl, n Octyl,
- R 5 to R 8 may be the same or different and for hydrogen, nitrile, halogen, carboxyl, carbalkoxy, carbaryloxy, alkoxy, aryloxy, acyloxy, alkyl, aryl optionally substituted by halogen, lower alkyl or lower alkoxy - Aralkyl, alkenyl radicals, furthermore R 5 and R 6 and / or R 7 and R 8 or R 5 and R 7 and / or R 6 and R 8 with the atoms with which they are linked can form a ring and wherein R 5 to R 8 have up to 12 carbon atoms, used for the process according to the invention.
- Halogen fluorine, chlorine, bromine, preferably chlorine, may be mentioned.
- radicals R 5 to R 6 in the above formula are preferably hydrocarbon radicals having up to 8 carbon atoms, for.
- carbalkoxy such as carbomethoxy, carbopentoxy, carboethoxy, carbopropoxy, carbobutoxy, carbo-tert.
- carbohexoxy preferably carbomethoxy, carboethoxy, carbaryloxy radicals such as carbophenoxy, carbochlorophenoxy, carbocresyi, preferably carbophenoxy, alkoxy radicals such as methoxy, ethoxy, propoxy, butoxy, tert-butoxy, pentoxy, hexoxy, preferably methoxy, ethoxy;
- Aryloxy radicals such as phenoxy, chlorophenoxy, cresyl, preferably phenoxy;
- Acyloxy radicals such as acetyloxy, propionyloxy, butyryloxy, benzoyloxy, chlorobenzoyloxy, preferably acetoxy, benzoyloxy, alkyl radicals, such as methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, tert-butyl, n-hexyl, n-octyl,
- alkyl radicals such as methyl, ethyl, n-propyl, iso-propyl, n-butyl, iso-butyl, tert-butyl, n-pentyl, n-hexyl, n-octyl, n-nonyl, n-decyl, n-dodecyl, preferably methyl, ethyl, n-propyl, iso-propyl; Alkoxy radicals, such as methoxy, ethoxy, propoxy, butoxy, pentoxy, hexoxy, preferably methoxy, ethoxy; Aralkoxy radicals, such as benzyloxy, p-chlorobenzyloxy, p-methylbenzyl
- Halogens include: fluorine, chlorine, bromine, preferably chlorine and bromine.
- the following are preferably used as color stabilizers for the aromatic carboxylic acid chlorides: acetone, methyl ethyl ketone, diethyl ketone, benzaldehyde, acetophenone, acetoacetic acid ester, acrylic acid ethyl ester, methacrylic acid methyl ester, crotonic acid, vinyl acetate, maleic acid, maleic acid diethyl ester, fumaric acid dicycloethyl methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, methacrylate, cyclophenyl, methacrylate, cyclophenol Allyl chloride, cinnamic acid, allyl alcohol, acetaldehyde, triethyl phosphite, trip
- E-Caprolactam is very particularly preferably used in the process according to the invention.
- the compounds of the general formula (11), (III) and (IV) mentioned can be used individually or in a mixture with one another for color stabilization of the aromatic carboxylic acid chlorides of the general formula (I), the mixing ratio not playing a role in the effectiveness of the stabilizers.
- the addition of the compounds of the general formula (11), (III) and (IV) used as color stabilizers to the aromatic carboxylic acid chlorides is preferably 0.01 to 0.5% by weight and in particular 0.02 to 0.1% by weight. -%.
- the concentration of the solution of the color stabilizers in the solvent is expediently chosen so that it lies at the upper limit of the solubility of the color stabilizers in order to keep the resulting concentration of the solvent in the aromatic carboxylic acid chlorides as low as possible, e.g. B. a weight ratio of 50 to 50 is preferred for the system toluene-phosphorus trichloride.
- Acetone (0.05 g) is dissolved in benzoyl chloride (100 g). The sample is stored in the dark. The mixture remains colorless for months. In contrast, a treated sample of the same material had a color number of 150 APHA.
- APHA means Hazen color number according to DIN 53409.
- E-Caprolactam (0.039) is dissolved in benzoyl chloride (100 g). The sample is stored in the dark.
- Dicyclopentadiene (0.01 g) is dissolved in benzoyl chloride (100 g). After several months of storage in the dark, the sample is still colorless. A comparative sample of the same material had a color number of 150 APHA.
- Acetophenone (0.02 g) is dissolved in o-toluic acid chloride (100 g). The rehearsal is also after Storage in the dark for several months is still colorless. A comparison sample of the same material had a color number of 100 APHA.
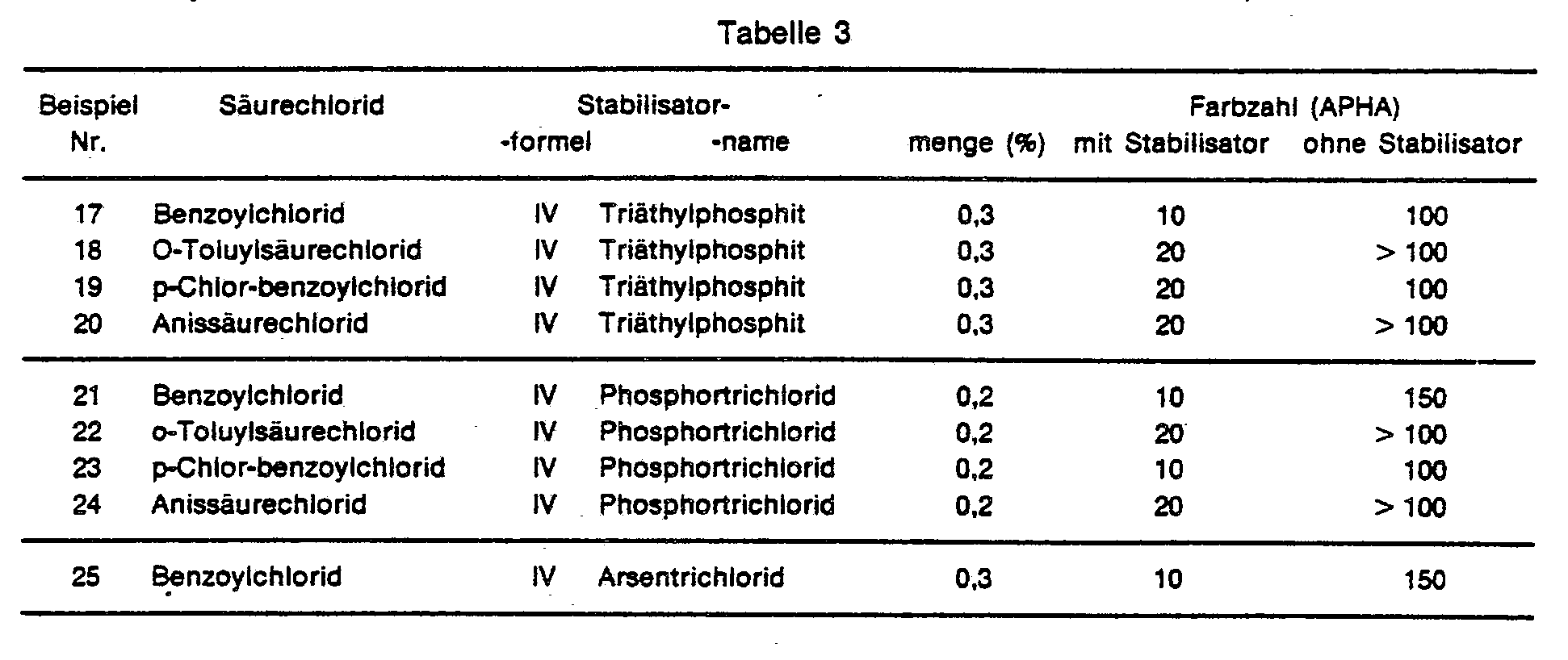
- Triethyl phosphite (0.05 g) is dissolved in benzoyl chloride (100 g). After several months of storage in the dark, the sample is still colorless. A comparative sample of the same material had a color number of 150 APHA.
- E-Caprolactam (0.05 g) is dissolved in benzoyl chloride (100 g) with a color number of 200 APHA. After 4 hours the sample is colorless (APHA ⁇ 15).
- Diethyl malonate (0.02 g) is dissolved in benzoyl chloride (100 g). After several months of storage in the dark, the product is still colorless. A comparative sample of the same material had a color number of 150 APHA.
- Cyclohexene (0.05 g) is dissolved in benzoyl chloride (100 g) with a color number of 100 APHA. After 2 hours the sample is colorless (10 APHA).
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
- Die Erfindung betrifft ein Verfahren zur Herstellung von farbstabilisierten, aromatischen Carbonsäurechloriden.
- Aromatische Carbonsäurechloride, die durch Umsetzung der entsprechenden aromatischen Carbonsäuren mit Benzotrichlorid erhalten wurden, haben häufig die unangenehme Eigenschaft, sich bei der Lagerung zu verfärben. Die Verfärbung der aromatischen Carbonsäurechloride kann auch nach deren Destillation noch auftreten.
- Wird für die weitere Umsetzung der aromatischen Carbonsäurechloride Wert auf deren Farblosigkeit gelegt, so ist eine vorhergehende Destillation erforderlich.
- Es wurde nun gefunden, daß man die Verfärbung von aromatischen Carbonsäurechloriden der Formel (I)
die durch Umsetzung der entsprechenden aromatischen Carbonsäuren mit Benzotrichlorid erhalten wurden, durch Zusatz eines Stabilisators der Formel (11) - R9 bis R11 gleich oder verschieden sein können und für Halogen, gegebenenfalls durch Halogen, niederes Alkyl oder niederes Alkoxy substituierte Alkyl-, Aryl-, Alkoxy- oder Aralkoxyreste stehen, und
- X Phosphor oder Arsen bedeutet, in einer Menge von 0,001-2 Gew.-%, bezogen auf die aromatischen Carbonsäurechioride, vermeiden kann.
- Ein besonderer Vorteil der erfindungsgemäßen Farbstabilisierung von aromatischen Carbonsäurechloriden ist es, daß zum einen die Stabilisierung dauerhaft ist und zum anderen die farbstabilisierten, aromatischen Carbonsäurechloride überraschenderweise ohne weiteres, d. h. ohne Beeinträchtigung der Reaktivität der aromatischen Carbonsäurechloride, für weitere Umsetzungen, z. B. Friedel-Crafts-Acylierungen, verwendet werden können.
- Als Alkyl- oder Alkoxyreste der Formel I kommen beispielsweise solche mit bis zu 10 C-Atomen, bevorzugt bis zu 4 C-Atomen, in Betracht, z. B. Alkylreste, wie Methyl, Äthyl, n-Propyl, iso-Propyl, n-Butyl, iso-Butyl, tert.-Butyl, n-Pentyl, iso-Pentyl, 2-Methylpentyl, 3-Methylpentyl-, n-Hexyl, n-Heptyl, n-Octyl, iso-Octyl, n-Nonyl, n-Decyl, Cyclohexyl, bevorzugt Methyl, Äthyl, n-Propyl, iso-Propyl, n-Butyl, iso-Butyl, tert.-Butyl ; Alkoxyreste, wie Methoxy, Äthoxy, Propoxy, Butoxy, Pentoxy, Hexoxy, bevorzugt Methoxy und Äthoxy.
- Als Halogene seien Fluor, Chlor, Brom, bevorzugt Chlor, genannt.
- Bevorzugt werden z. B. folgende aromatische Carbonsäurechloride farbstabilisiert : Benzoylchlorid, o-Toluylsäurechlorid, p-Toluylsäurechlorid, 2-Chlor-benzoylchlorid, 3-Chlor-benzoylchlorid, 4-Chlorbenzoylchlorid, 2,4-Dichlorbenzoylchlorid sowie Anissäurechlorid.
- Als Farbstabilisatoren werden solche der allgemeinen Formel (II)
- Als Halogene seien Fluor, Chlor, Brom, bevorzugt Chlor, genannt.
- Als Reste R3 und R4 in der obengenannten Formel kommen bevorzugt Kohlenwasserstoffreste mit bis zu 8 C-Atomen in Betracht, z. B. Alkoxyreste, wie Methoxy, Äthoxy, Propoxy, Butoxy, tert.-Butoxy, Pentoxy, Hexoxy, bevorzugt Methoxy, Äthoxy ; Aryloxyreste, wie Phenoxy, Chlorphenoxy, Cresyl, bevorzugt Phenoxy ; Aralkoxyreste, wie Benzyloxy, p-Chlorbenzyloxy, p-Tolyloxy, bevorzugt Benzyloxy ; Alkylreste, wie Methyl, Äthyl, n-Propyl, iso-Propyl, 'n-Butyl, iso-Butyl, tert.-Butyl, n-Pentyl, iso-Pentyl, 2-Methylpentyl, 3-Methylpentyl, n-Hexyl, n-Octyl, iso-Octyl, n-Nonyl, n-Decyl, n-Dodecyl, bevorzugt Methyl, Äthyl, n-Propyl, iso-Propyl ; Aralkylreste, wie Benzyl, p-Chlor-benzyl, p-Methylbenzyl, bevorzugt Benzyl : Arylreste, wie Phenyl, Toluyl, p-Chlorphenyl, p-Methoxyphenyl, bevorzugt Phenyl, Toluyl ; Alkenylreste, wie Vinyl, Propenyl, Allyl, Butenyl-(1), Butenyl-(2), Methallyl, bevorzugt Vinyl, Propenyl, Methallyl ; Mono-und Dialkylaminoreste, wie Methylamino, Äthylamino, Propylamino, Dimethylamino, Diäthylamino, Dipropylamino, bevorzugt Dimethylamino, Diäthylamino ; sowie Alkylenreste, bei denen gegebenenfalls eine oder mehrere Methylengruppen durch Heteroatome ersetzt sein können, wie Äthylen, Trimethylen, Tetramethylen, Pentamethylen, Hexamethylen, 2-Oxatrimethylen, 1-Thiatrimethylen, 1-Iminopentamethylen, bevorzugt Pentamethylen und 1-Iminopentamethylen.
- Weiterhin werden als Farbstabilisatoren solche der allgemeinen Formel (III)
- Als Halogene seien Fluor, Chlor, Brom, bevorzugt Chlor, genannt.
- Als Reste R5 bis R6 in der obengenannten Formel kommen bevorzugt Kohlenwasserstoffreste mit bis zu 8 C-Atomen in Betracht, z. B. Carbalkoxyreste wie Carbomethoxy-, Carbopentoxy-, Carboäthoxy-, Carbopropoxy-, Carbobutoxy-, Carbo-tert. butoxy-, Carbohexoxy-, bevorzugt Carbomethoxy-, Carboäthoxy-, Carbaryloxy-Reste wie Carbophenoxy, Carbochlorphenoxy-, Carbocresyi-, bevorzugt Carbophenoxy-, Alkoxy-Reste wie Methoxy, Äthoxy, Propoxy, Butoxy, tert.-Butoxy, Pentoxy, Hexoxy, bevorzugt Methoxy, Äthoxy ; Aryloxyreste, wie Phenoxy, Chlorphenoxy, Cresyl, bevorzugt Phenoxy ; Acyloxyreste, wie Acetyloxy, Propionyloxy, Butyryloxy, Benzoyloxy, Chlorbenzoyloxy, bevorzugt Acetoxy, Benzoyloxy, Alkylreste, wie Methyl, Athyl, n-Propyl, iso-Propyl, n-Butyl, iso-Butyl, tert.-Butyl, n-Hexyl, n-Octyl, n-Nonyl, Dodecyl, bevorzugt Methyl, Äthyl, n-Propyl, iso-Propyl ; Aralkylreste, wie Benzyl, p-Chlorbenryl, p-Methylbenzyl, bevorzugt Benzyl ; Arylreste, wie Phenyl, Toluyl, p-Chlorphenyl, p-Methoxyphenyl, bevorzugt Phenyl, Toluyl ; Alkenylreste, wie Vinyl, Propenyl, Allyl, Butenyl-(1), Butenyl-(2), Methallyl, bevorzugt Vinyl, Allyl, Methallyl ; sowie Alkylenreste; bei denen gegebenenfalls einer oder mehrere Methylengruppen durch Heteroatome ersetzt sein können, wie Äthylen, Trimethylen, Tetramethylen, Pentamethylen, Hexamethylen, 2-Oxatrimethyien, 1-Thiatrimethylen, bevorzugt Tetramethylen und Pentamethylen.
-
- Rg bis R11 gleich oder verschieden sein können und für Halogen, gegebenenfalls durch Halogen, niederes Alkyl oder niederes Alkoxy substituierte Alkyl-, Aryl-, Alkoxy- oder Aralkoxyreste stehen, und
- X Phosphor oder Arsen bedeutet, für das erfindungsgemäße Verfahren verwendet werden.
- Als gegebenenfalls substituierte Alkyl-, Aryl-, Alkoxy- oder Aralkoxyreste kommen beispielsweise solche mit bis zu 12 C-Atomen, bevorzugt bis zu 8 C-Atomen, in Betracht, z. B. Alkylreste, wie Methyl, Äthyl, n-Propyl, iso-Propyl, n-Butyl, iso-Butyl, tert.-Butyl, n-Pentyl, n-Hexyl, n-Octyl, n-Nonyl, n-Decyl, n-Dodecyl, bevorzugt Methyl, Äthyl, n-Propyl, iso-Propyl ; Alkoxyreste, wie Methoxy, Äthoxy, Propoxy, Butoxy, Pentoxy, Hexoxy, bevorzugt Methoxy, Äthoxy ; Aralkoxyreste, wie Benzyloxy, p-Chlorbenzyloxy, p-Methylbenzyloxy, bevorzugt Benzyloxy sowie Arylreste wie Phenyl, Toluyl, p-Chlorphenyl, p-Methoxyphenyl, bevorzugt Phenyl und Toluyl.
- Als Halogene seien genannt : Fluor, Chlor, Brom, bevorzugt Chlor und Brom.
- Bevorzugt werden als Farbstabilisatoren für die aromatischen Carbonsäurechloride verwendet : Aceton, Methyläthylketon, Diäthylketon, Benzaldehyd, Acetophenon, Acetessigester, Acrylsäureäthylester, Methacrylsäuremethylester, Crotonsäure, Vinylacetat, Maleinsäure, Maleinsäurediäthylester, Fumarsäurediäthylester, Dicyclopentadien, s-Caprolactam, Styrol, Methylvinylketon, Acrolein, Cyclohexen, Allylchlorid, Zimtsäure, Allylalkohol, Acetaldehyd, Triäthylphosphit, Triphenylphosphin, Phosphortrichlorid, Arsentrichlorid, Methacrylsäureamid, Cyclohexanon, wobei Aceton, Cyclohexanon, Dicyclopentadien, Acetessigester, Maleinsäure, s-Caprolactam, Triäthylphosphit, Phosphortrichlorid besonders bevorzugt sind.
- Ganz besonders bevorzugt wird e-Caprolactam in das erfindungsgemäße Verfahren eingesetzt.
- Die genannten Verbindungen der allgemeinen Formel (11), (III), und (IV) können zur Farbstabilisierung der aromatischen Carbonsäurechloride der allgemeinen Formel (I) einzeln oder im Gemisch untereinander verwendet werden, wobei das Mischungsverhältnis keine Rolle für die Wirksamkeit der Stabilisatoren spielt.
- Der Zusatz der als Farbstabilisatoren verwendeten Verbindungen der allgemeinen Formel (11), (III), und (IV) zu den aromatischen Carbonsäurechloriden beträgt vorzugsweise 0,01 bis 0,5 Gew.-% und insbesondere 0,02 bis 0,1 Gew.-%.
- Es ist auch möglich, die als Farbstabilisatoren verwendeten Verbindungen der allgemeinen Formel (II), (III) und (IV) in einem inerten Lösungmittel gelöst zuzusetzen, wenn dies zweckmäßig erscheint, z. B. zwecks leichter Dosierung oder leichterer Durchmischung, jedoch ist dies im allgemeinen nicht erforderlich. Geeignete inerte Lösungsmittel sind z. B. Benzol, Toluol, Xylol, Cyclohexan und Tetrachlorkohlenstoff.
- Die Konzentration der Lösung der Farbstabilisatoren im Lösungsmittel wird zweckmäßig so konzentriert gewählt, daß sie an der oberen.Grenze der Löslichkeit der Farbstabilisatoren liegt, um die sich ergebende Konzentration des Lösungsmittels in den aromatischen Carbonsäurechloriden so gering wie möglich zu halten, z. B. wird für das System Toluol-Phosphortrichlorid ein Gew.-Verhältnis von 50 zu 50 bevorzugt.
- In Benzoylchlorid (100 g) wird Aceton (0,05 g) gelöst. Die Probe wird im Dunkeln gelagert. Die Mischung ist noch nach Monaten farblos. Dagegen hatte eine umbehandelte Probe des gleichen Materials eine Farbzahl von 150 APHA. APHA bedeutet Hazen-Farbzahl gemäß DIN-53409.
- In Benzoylchlorid (100 g) wird e-Caprolactam (0,039) gelöst. Die Probe wird im Dunkeln gelagert.
- Nach mehrmonatiger Lagerung ist die Probe noch farblos. Eine unbehandelte Probe des gleichen Materials hatte eine Farbzahl von 150 APHA.
- In Benzoylchlorid (100 g) wird Dicyclopentadien (0,01 g) gelöst. Nach mehrmonatiger Lagerung im Dunkeln ist die Probe noch farblos. Eine Vergleichsprobe des gleichen Materials hatte eine Farbzahl von 150 APHA.
- In o-Toluylsäurechlorid (100 g) wird Acetophenon (0,02 g) gelöst. Die Probe ist auch nach mehrmonatiger Lagerung im Dunkeln noch farblos. Ein Vergleichsmuster der gleichen Materials hatte eine Farbzahl von 100 APHA.
- In Benzoylchlorid (100 g) wird Triäthylphosphit (0,05 g) gelöst. Die Probe ist nach mehrmonatiger Lagerung im Dunkeln noch farblos. Eine Vergleichsprobe des gleichen Materials hatte eine Farbzahl von 150 APHA.
- In Benzoylchlorid (100 g) mit einer Farbzahl von 200 APHA wird e-Caprolactam (0,05 g) gelöst. Nach 4 Stunden ist die Probe farblos (APHA < 15).
- In Benzoylchlorid (100 g) wird Malonsäurediäthylester (0,02 g) gelöst. Nach mehrmonatiger Lagerung im Dunkeln ist das Produkt noch farblos. Eine Vergleichsprobe des gleichen Materials hatte eine Farbzahl von 150 APHA.
- In Benzoylchlorid (100 g) mit einer Farbzahl von 100 APHA wird Cyclohexen (0,05 g) gelöst. Nach 2 Stunden ist die Probe farblos (10 APHA).
-
Claims (5)
die durch Umsetzung der entsprechenden aromatischen Carbonsäuren mit Benzotrichlorid erhalten wurden, gegen Verfärbung, dadurch gekennzeichnet, daß man 0,001 bis 2 Gew.-% eines Stabilisators der Formel
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19782848356 DE2848356A1 (de) | 1978-11-08 | 1978-11-08 | Farbstabilisierte, aromatische carbonsaeurechloride und ein verfahren zu deren herstellung |
| DE2848356 | 1978-11-08 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0012200A1 EP0012200A1 (de) | 1980-06-25 |
| EP0012200B1 EP0012200B1 (de) | 1981-08-19 |
| EP0012200B2 true EP0012200B2 (de) | 1985-06-05 |
Family
ID=6054105
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP79104197A Expired EP0012200B2 (de) | 1978-11-08 | 1979-10-29 | Verfahren zur Herstellung von farbstabilisierten, aromatischen Carbonsäurechloriden |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US4294777A (de) |
| EP (1) | EP0012200B2 (de) |
| JP (1) | JPS5941977B2 (de) |
| DE (2) | DE2848356A1 (de) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4508857A (en) * | 1983-08-15 | 1985-04-02 | Occidental Chemical Corporation | Color-stabilized aroyl chloride compositions |
| US4508661A (en) * | 1983-08-15 | 1985-04-02 | Occidental Chemical Corporation | Method for the decolorization of aroyl chloride compositions |
| US5114970A (en) * | 1991-07-25 | 1992-05-19 | The Dow Chemical Company | Use of 3-iodo-2-chloro-2-propenenitrile as an antimicrobial |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3349123A (en) * | 1963-09-24 | 1967-10-24 | Hooker Chemical Corp | Stabilization of nitrophenyl acyl halides |
| US3445504A (en) * | 1965-01-26 | 1969-05-20 | Standard Oil Co | Stabilized terephthalate compositions |
| US3520809A (en) * | 1967-07-03 | 1970-07-21 | Universal Oil Prod Co | Stabilization of organic substances |
| US3557205A (en) * | 1967-08-23 | 1971-01-19 | Pennwalt Corp | Stabilization of polyacid halides |
| DE2206300C3 (de) * | 1972-02-10 | 1974-10-24 | Bayer Ag, 5090 Leverkusen | Verfahren zum Stabilisieren von Benzylchlorid und stabilisiertes Benzylchlorid als solches |
| US3923912A (en) * | 1973-02-23 | 1975-12-02 | Diamond Shamrock Corp | Methylene chloride stabilized with ketones |
-
1978
- 1978-11-08 DE DE19782848356 patent/DE2848356A1/de not_active Withdrawn
-
1979
- 1979-10-17 US US06/085,553 patent/US4294777A/en not_active Expired - Lifetime
- 1979-10-29 DE DE7979104197T patent/DE2960662D1/de not_active Expired
- 1979-10-29 EP EP79104197A patent/EP0012200B2/de not_active Expired
- 1979-11-06 JP JP54142871A patent/JPS5941977B2/ja not_active Expired
Also Published As
| Publication number | Publication date |
|---|---|
| US4294777A (en) | 1981-10-13 |
| EP0012200A1 (de) | 1980-06-25 |
| JPS5941977B2 (ja) | 1984-10-11 |
| DE2960662D1 (en) | 1981-11-12 |
| EP0012200B1 (de) | 1981-08-19 |
| JPS5566537A (en) | 1980-05-20 |
| DE2848356A1 (de) | 1980-05-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0708081A2 (de) | Verfahren zur Herstellung von N,N'- disubstituierten p-Chinondiiminen, deren Verwendung und Methacryloxy- oder Acryloxy-Gruppen enthaltende Organosilane, Verfahren zu deren Stabilisierung und deren Herstellung | |
| EP0012200B2 (de) | Verfahren zur Herstellung von farbstabilisierten, aromatischen Carbonsäurechloriden | |
| EP0713854B1 (de) | Verfahren zur Reinigung von Roh-(Meth)acrylsäure | |
| EP1231201A1 (de) | Verfahren zur Herstellung von Anhydriden ungesättiger Carbonsäuren | |
| EP0026311B2 (de) | Verfahren zur Herstellung von sehr reinem epsilon-Caprolacton | |
| EP0032576B1 (de) | Verfahren zur Herstellung von p-substituierten Phenylpropanolen und deren Estern sowie von p-substituierten 3-Phenyl-2-methyl-propanalen | |
| CH622759A5 (de) | ||
| CH634287A5 (de) | Verfahren zur herstellung von 2-methyl-2-hepten-6-on. | |
| DE19840746A1 (de) | Verfahren zur Herstellung gamma,delta-ungesättigter Ketone durch Carroll-Reaktion | |
| DE69201756T2 (de) | Verfahren zur gleichzeitigen Herstellung von Arylformiat und von aromatischer Carbonsäure. | |
| DE2364181C3 (de) | Verfahren zur Herstellung von aromatischen Dihydroxyverbindungen oder deren Monoäthern | |
| DE1768578B2 (de) | Verfahren zur herstellung von 2,4- disubstituierten phenylketonen | |
| DE69516083T2 (de) | Verfahren zur Herstellung von acylsubstituierten Resorcinolen | |
| WO2022238144A1 (de) | Ungesättigte ester, enthaltend ein additiv zur reduktion und stabilisierung des gelbwertes | |
| DE69215037T2 (de) | Verfahren zur gleichzeitigen Herstellung eines Lactons und einer aromatischen Carbonsäure | |
| DE69705354T2 (de) | Verminderung von Carbonylverunreinigungen in alpha,beta-ungesättigten Säuren und Estern | |
| DE2355415C3 (de) | Verfahren zur Herstellung von Terephthalsäure | |
| DE2609126C2 (de) | Verfahren zur Herstellung von [2-(Halogenformyl)-vinyl] organyl-phosphinsäurehalogeniden | |
| EP0050783B1 (de) | Verfahren zur Herstellung von aromatischen Carbonsäurechloriden | |
| DE2949073A1 (de) | Verfahren zur reinigung von aldehyde und/oder acetale enthaltenden carbonsaeureestern | |
| DE3220729A1 (de) | Verfahren zur herstellung von terephthalsaeure- und isophthalsaeuredichlorid | |
| DE842193C (de) | Verfahren zur Herstellung von halogenhaltigen Dicarbonsaeuren oder deren funktionellen Abkoemmlingen | |
| DE1001258C2 (de) | Verfahren zur Herstellung von konjugierten Polyenen der Vitamin-A-Reihe | |
| AT254853B (de) | Verfahren zur Halogenierung der kernständigen Methylgruppe(n) von Methylphenylacetaten | |
| DE1280246B (de) | Verfahren zur Herstellung von 3, 3, 5-Trimethyl-cyclohexanonperoxyden |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed | ||
| AK | Designated contracting states |
Designated state(s): BE CH DE FR GB IT NL |
|
| ITF | It: translation for a ep patent filed | ||
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Designated state(s): BE CH DE FR GB IT NL |
|
| REF | Corresponds to: |
Ref document number: 2960662 Country of ref document: DE Date of ref document: 19811112 |
|
| PLBI | Opposition filed |
Free format text: ORIGINAL CODE: 0009260 |
|
| PLBI | Opposition filed |
Free format text: ORIGINAL CODE: 0009260 |
|
| PLAB | Opposition data, opponent's data or that of the opponent's representative modified |
Free format text: ORIGINAL CODE: 0009299OPPO |
|
| 26 | Opposition filed |
Opponent name: HOECHST AKTIENGESELLSCHAFT, FRANKFURT Effective date: 19820505 |
|
| 26 | Opposition filed |
Opponent name: SOCIETE NATIONALE DES POUDRES ET EXPLOSIFS (SNPE) Effective date: 19820512 |
|
| R26 | Opposition filed (corrected) |
Opponent name: HOECHST AKTIENGESELLSCHAFT, FRANKFURT * 820512 SOC Effective date: 19820505 |
|
| ITF | It: translation for a ep patent filed | ||
| PUAH | Patent maintained in amended form |
Free format text: ORIGINAL CODE: 0009272 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: PATENT MAINTAINED AS AMENDED |
|
| 27A | Patent maintained in amended form | ||
| AK | Designated contracting states |
Kind code of ref document: B2 Designated state(s): BE CH DE FR GB IT NL |
|
| NLR2 | Nl: decision of opposition | ||
| ET2 | Fr: translation filed ** revision of the translation of the modified patent after opposition | ||
| NLR3 | Nl: receipt of modified translations in the netherlands language after an opposition procedure | ||
| ITTA | It: last paid annual fee | ||
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19940916 Year of fee payment: 16 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CH Effective date: 19951031 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19960912 Year of fee payment: 18 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19961016 Year of fee payment: 18 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 19961021 Year of fee payment: 18 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: BE Payment date: 19961023 Year of fee payment: 18 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19961031 Year of fee payment: 18 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19971029 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: THE PATENT HAS BEEN ANNULLED BY A DECISION OF A NATIONAL AUTHORITY Effective date: 19971031 Ref country code: BE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19971031 |
|
| BERE | Be: lapsed |
Owner name: BAYER A.G. Effective date: 19971031 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19980501 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 19971029 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee |
Effective date: 19980501 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19980701 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |