-
Diese Anmeldung beansprucht die Priorität der gleichzeitig anhängigen US-Anmeldungen Nr. 61/524,167, eingereicht am 16. August 2011, 61/604,232, eingereicht am 28. Februar 2012, und 61/607,737, eingereicht am 7. März 2012, die hier durch Bezugnahme ausdrücklich jeweils in vollem Umfang mitaufgenommen sind.
-
Es sind als Markierungen brauchbare Verbindungen mit Eigenschaften offenbart, die mit denen bekannter fluoreszierender Verbindungen vergleichbar sind. Die Verbindungen können mit Proteinen und Nukleinsäuren zur biologischen Bildgebung und Analyse konjugiert sein. Es sind die Synthese der Verbindungen, die Bildung und Verwendung der konjugierten Verbindungen und jeweils spezifische, nicht einschränkende Beispiele für jede davon offenbart.
-
Verbindungen, die mit Biomolekülen (z. B. Antigenen, Antikörpern, DNA-Segmenten mit der entsprechenden komplimentären Spezies zum Bestimmen der Enzymkinetik, Rezeptor-Ligand-Wechselwirkungen, Nukleinsäure-Hybridisierungskinetik in vitro sowie in vivo, usw.) reagieren, sogenannte Label oder Farbstoffe, sind brauchbar z. B. für die pharmakologische Charakterisierung von Rezeptoren und Wirkstoffen, Bindungsdaten, usw. Verbindungen, wie Xanthyliumsalze (
US-Patent Nr. 5,846,737 ) und/oder Cyanine (
US-Patent Nr. 5,627,027 ) werden für solche Anwendungen verwendet, aggregieren jedoch und bilden Dimere, insbesondere in wässriger Lösung, auf Grund der Planarität ihres π-Systems. Verbindungen mit ausreichender Hydrophilie unterliegen nicht-spezifischen Wechselwirkungen mit verschiedenen Oberflächen, was zu Problemen beim Versuch, das entsprechende Konjugat zu reinigen, und zu einem unbefriedigenden Signal-Rausch-Abstand führt.
-
Es gibt Bemühungen, unerwünschte Eigenschaften zu verringern, indem Substituenten eingebracht werden, welche die Hydrophilie der Verbindungen erhöhen. Beispielsweise wurden Substituenten mit Sulfonsäurefunktion in das Cyaninchromophor eingebracht.
US-Patent Nr. 6,083,485 (Licha) und die
US-Patente Nr. 6,977,305 und
6,974,873 (Molecular Probes) offenbaren Cyaninverbindungen mit einer der üblichen Methylgruppen in 3-Position des terminalen Indol-Heterozyklus, substituiert mit einer ω-Carboxyalkylfunktion, wobei die dort zuvor (z. B. in Cy3 oder Cy5) vorhandenen N-Alkyl oder N-ω-Carboxyalkylfunktionen durch N-ω-Alkylsulfonsäurefunktionen ersetzt sind. Die
WO 05/044923 offenbart Cyaninverbindungen mit dem üblichen Methylsubstituenten in 3-Position des terminalen Indol-Heterozyklus, substituiert mit einer N-ω-Alkylsulfonsäurefunktion. In diesen Veröffentlichungen zeigten Cyaninverbindungen mit mehr als zwei Sulfonsäurefunktionssubstituenten eine höhere Löslichkeit und dementsprechend eine niedrigere Tendenz zur Dimerbildung im Vergleich zu Cyaninverbindungen (Cy3, Cy5), die im
US-Patent Nr. 5,627,027 beschrieben sind.
-
Die offenbarten Benzocyaninverbindungen sind brauchbar als Markierungen in optischen, z. B. fluoreszenzoptischen, Bestimmungs- und Detektionsverfahren. Die Verbindungen weisen eine hohe Hydrophilie, einen hohen molaren Extinktionskoeffizienten, hohe Fotostabilität und hohe Lagerstabilität auf. Diese Verbindungen wurden durch monochromatisches (z. B. Laser, Laserdioden) oder polychromatisches (z. B. Weißlichtquellen) Licht im ultravioletten (UV), sichtbaren und Nahinfrarot (NIR)-Spektralbereich angeregt, um eine Emission von Fluoreszenzlicht zu erzeugen.
-
Typische Anwendungsverfahren beruhen auf der Reaktion der Verbindungen mit Biomolekülen, z. B. Proteinen (z. B. Antigenen, Antikörpern usw.), DNA- und/oder RNA-Segmenten usw., mit der entsprechenden komplimentären Spezies. Somit werden die Verbindungen neben anderen Ausführungsformen zur Bestimmung von Enzymkinetik, Rezeptor-Ligand-Wechselwirkungen und Nukleinsäurehybridisierungskinetik in vitro und/oder in vivo verwendet. Die Verbindungen werden für die pharmakologische Charakterisierung von Rezeptoren und/oder Wirkstoffen verwendet. Anwendungen sind insbesondere Verwendungen in der Medizin, der Pharmazie, den biologischen Wissenschaften, der Werkstoffkunde, des Umweltschutzes, der Detektion organischer und anorganischer Mikroproben, die in der Natur vorkommen, usw.
-
Die folgende Nomenklatur wird zur Beschreibung der Ausführungsformen der Verbindungen mit einem einzelnen PEG oder mehreren PEG verwendet.
-
Die folgende Nomenklatur wird für Verbindungen verwendet, die ein Ethylenglykol oder ein (Poly)ethylenglykol aufweisen, das sich stets am Indol-N auf der linken Seite des Cyanins befindet: (die erste Verbindung wird ausführlich erläutert, und alle anderen Verbindungen folgen demselben Nomenklaturformat):
579-Verbindung 1 ((Ethylenglykol) (ist z. B. eine 579-Verbindung; 1 ist die Länge des Ethylenglykols))
579-Verbindung 2 (Diethylenglykol)
579-Verbindung 3 (Polyethylenglykol (3))
579-Verbindung 4 (Polyethylenglykol (4))
579-Verbindung 5 (Polyethylenglykol (5))
579-Verbindung 6 (Polyethylenglykol (6))
679-Verbindung 1 (Ethylenglykol)
679-Verbindung 2 (Diethylenglykol)
679-Verbindung 3 (Polyethylenglykol (3))
679-Verbindung 4 (Polyethylenglykol (4))
679-Verbindung 5 (Polyethylenglykol (5))
679-Verbindung 6 (Polyethylenglykol (6))
779-Verbindung 1 (Ethylenglykol)
779-Verbindung 2 (Diethylenglykol)
779-Verbindung 3 (Polyethylenglykol (3))
779-Verbindung 4 (Polyethylenglykol (4))
779-Verbindung 5 (Polyethylenglykol (5))
779-Verbindung 6 (Polyethylenglykol (6))
-
Die folgende Nomenklatur wird für Verbindungen mit mehr als einem Ethylenglykol oder mehr als einem (Poly)ethylenglykol verwendet, d. h. eines befindet sich stets an dem Indol-N auf der linken Seite des Cyanin, und mindestens 1 weiteres (insgesamt 2) an (einer) anderen Stellen) als dem Indol-N auf der linken Seite des Cyanin (die erste Verbindung wird ausführlich erläutert, und alle anderen Verbindungen folgen demselben Nomenklaturformat):
579-Verbindung 1/X (z. B. steht Verbindung 1 für die Länge des PEG am linken Abschnitt des Cyanin und X für die Gesamtzahl an PEG der gesamten Verbindung).
579-Verbindung 2/X
579-Verbindung 3/X
579-Verbindung 4/X
579-Verbindung 5/X
579-Verbindung 6/X
679-Verbindung 1/X
679-Verbindung 2/X
679-Verbindung 3/X
679-Verbindung 4/X
679-Verbindung 5/X
679-Verbindung 6/X
779-Verbindung 1/X
779-Verbindung 2/X
779-Verbindung 3/X
779-Verbindung 4/X
779-Verbindung 5/X
779-Verbindung 6/X
-
Somit umfassen 579-, 679- und 779-Verbindungen jeweils eine Polymethinkette mit 3, 5 bzw. 7 C-Atomen, wobei sich die erste Zahl 1–6 auf die Länge einer PEG-Gruppe an einer Indol-N-Position bezieht; z. B. steht 1 für Ethylenglykol (PEG1), 2 für Diethylenglykol (PEG2), 3 für Polyethylenglykol (3) (PEG3), 4 für Polyethylenglykol (4) (PEG4), 5 für Polyethylenglykol (5) (PEG5) und 6 für Polyethylenglykol (6) (PEG6), und X bezieht sich auf die Anzahl PEG-Gruppen der Verbindung. Beispielsweise steht gemäß einer Ausführungsform die 679-Verbindung 4/4 für ein PEG4 an einem Indol-N bei insgesamt vier PEG-Gruppen der Verbindung.
-
Gemäß einer Ausführungsform weisen die Benzocyaninverbindungen in einer N-Position eines Heterozyklus eine Ethylenglykolgruppe oder ein Ethylenglykolpolymer (d. h. Poly(ethylen)glykol, gemeinsam als PEG abgekürzt) auf, und der andere Heterozyklus weist in einer N-Position eine Funktion zum Konjugieren der Verbindung mit einem Biomolekül auf. Gemäß einer weiteren Ausführungsform weist die Benzocyaninverbindung in einer beliebigen Position der Verbindung mindestens eine Sulfo (SO3 –)- und/oder Sulfoalkylgruppe auf. Gemäß einer anderen Ausführungsform weist die Benzocyaninverbindung in einer beliebigen Position der Verbindung eine Sulfonamid- und/oder Carboxamidgruppe auf, die eine Ethylenglykolgruppe oder ein Ethylenglykolpolymer (d. h. Poly(ethylen)glykol, gemeinsam als PEG abgekürzt) umfasst, welche(s) entweder direkt oder indirekt an die Verbindung gebunden ist. Eine indirekte Bindung deutet auf die Verwendung eines Linkers hin, eine direkte Bindung auf das Fehlen eines solchen Linkers. Ein Linker kann eine beliebige Einheit sein.
-
Gemäß einer Ausführungsform weisen die Benzocyaninverbindungen in einer N-Position eines Heterozyklus eine Ethylenglykolgruppe oder ein Ethylenglykolpolymer (d. h. Poly(ethylen)glykol, gemeinsam als PEG abgekürzt) auf, und der andere Heterozyklus weist in einer N-Position eine Ethylenglykolgruppe oder ein Ethylenglykolpolymer (d. h. Poly(ethylen)glykol, gemeinsam als PEG abgekürzt) und eine Funktion zum Konjugieren der Verbindung mit einem Biomolekül auf. Gemäß einer weiteren Ausführungsform weisen die Benzocyaninverbindungen eine Ethylenglykolgruppe oder ein Ethylenglykolpolymer (d. h. Poly(ethylen)glykol, gemeinsam als PEG abgekürzt) in einer anderen Position der Benzocyaninverbindung auf. Gemäß einer anderen Ausführungsform weist die Benzocyaninverbindung in einer beliebigen Position der Verbindung mindestens eine Sulfo- und/oder Sulfoalkylgruppe auf. Gemäß einer weiteren Ausführungsform weist die Benzocyaninverbindung in einer beliebigen Position der Verbindung eine Sulfonamid- und/oder Carboxamidgruppe auf, die eine Ethylenglykolgruppe oder ein Ethylenglykolpolymer (d. h. Poly(ethylen)glykol, gemeinsam als PEG abgekürzt) aufweist, welche(s) direkt oder indirekt an die Verbindung gebunden ist.
-
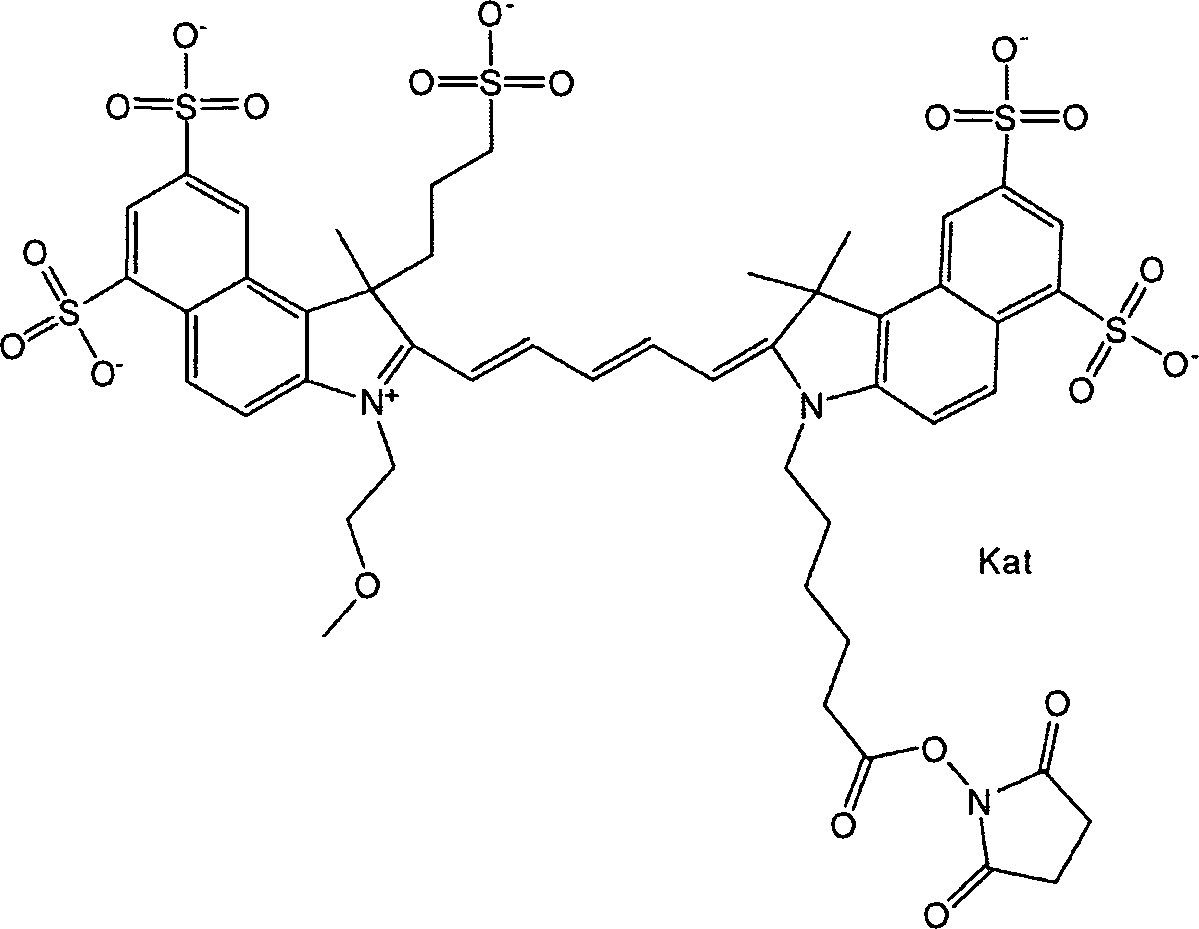
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel Ia
oder die allgemeine Formel IIb
auf, worin R
1 und R
2 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus einer aliphatischen Gruppe, einer heteroaliphatischen Gruppe, Sulfoalkylgruppe, heteroaliphatisch mit terminalem SO
3, einer PEG-Gruppe P-Z, worin P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s für eine ganze Zahl von 3–6 (jeweils einschließlich) steht, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Caboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; X ausgewählt ist aus der Gruppe, bestehend aus -OH, -SH, -NH
2, -NH-NH
2, -F, -Cl, -Br, I, -NHS (Hydroxysuccinimidyl/Sulfosuccinimidyl), -OTFP (2,3,5,6-Tetrafluorphenoxy), -O-STP (4-Sulfo-2,3,5,6-tetrafluorphenoxy), -O-Benzotriazol, -Benzotriazol, -NR-L-OH, -NR-L-O-Phosphoramidit, -NR-L-SH, -NR-L-NH
2, -NR-L-NH-NH
2, -NR-LCO
2H, -NR-L-CO-NHS, -NR-L-CO-STP, -NR-L-CO-TFP, -NR-L-CO-Benzotriazol, -NR-L-CHO, -NR-L-Maleimid, -NR-L-NH-CO-CH
2-, Imidazol, Azid, -NR-L-O-NH
2 und -NR-L-O-CO-NHS, worin R für -H oder eine aliphatische oder heteroaliphatische Gruppe steht, und L ausgewählt ist aus der Gruppe, bestehend aus einer divalenten linearen (-(CH
2)
t-, t = 0 bis 15), verzweigten oder zyklischen Alkylgruppe, gegebenenfalls substituiert mit mindestens einem Sauerstoffatom und/oder Schwefelatom; Kat eine Anzahl von Na
+-, K
+-, Ca
2 +-, Ammoniak- oder (einem) anderen Kation(en) ist, die zum Ausgleichen der durch das Cyanin bedingten negativen Ladung benötigt wird; m eine ganze Zahl von einschließlich 0 bis 5 ist, o eine ganze Zahl von einschließlich 0 bis 12 ist und n eine ganze Zahl von einschließlich 1 bis 3 ist. Gemäß einer Ausführungsform enthält zumindest R
1 und/oder R
2 eine PEG-Gruppe.
-
Gemäß einer Ausführungsform ist die PEG-Gruppe P ausgewählt aus der Gruppe, bestehend aus -C-C-O-C (Ethylenglykol mit terminalem Methyl), -C-C-O-C-C-O-C (Diethylenglykol mit terminalem Methyl), -C-C-O-C-C-O-C-C-O-C (Polyethylenglykol (3) mit terminalem Methyl), -C-C-O-C-C-O-C-C-O-C-C-O-C (Polyethylenglykol (4) mit terminalem Methyl), -C-C-O-C-C-O-C-C-O-C-C-O-C-C-O-C (Polyethylenglykol (5) mit terminalem Methyl) und C-C-O-C-C-O-C-C-O-C-C-O-C-C-C-O-C-C-O-C (Polyethylenglykol (6) mit terminalem Methyl). Gemäß einer Ausführungsform kann die PEG-Gruppe P entweder ungeschützt sein, z. B. kein terminales Methyl aufweisen, oder mit einem anderen Atom oder einer anderen Gruppe als einem Methyl geschützt sein. Gemäß einer Ausführungsform endet die PEG-Gruppe P mit einer Z-Gruppe, wobei Z ausgewählt ist unter H, CH3, einer CH3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel Ia oder die allgemeine Formel Ib auf, die zusammenfassend als allgemeine Formel I bezeichnet werden, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NRL-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer weiteren Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht; m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, 0 = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NRL-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NRL-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl und R2 für Sulfoalkyl steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, 0 = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Methyl steht und R2 für eine PEG-Gruppe steht, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, 0 = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 und R2 jeweils für eine PEG-Gruppe stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, 0 = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel I auf, worin R1 für Sulfoalkyl und R2 für eine Sulfonamidgruppe -L-SO2NH-P steht, worin P eine PEG-Gruppe ist, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
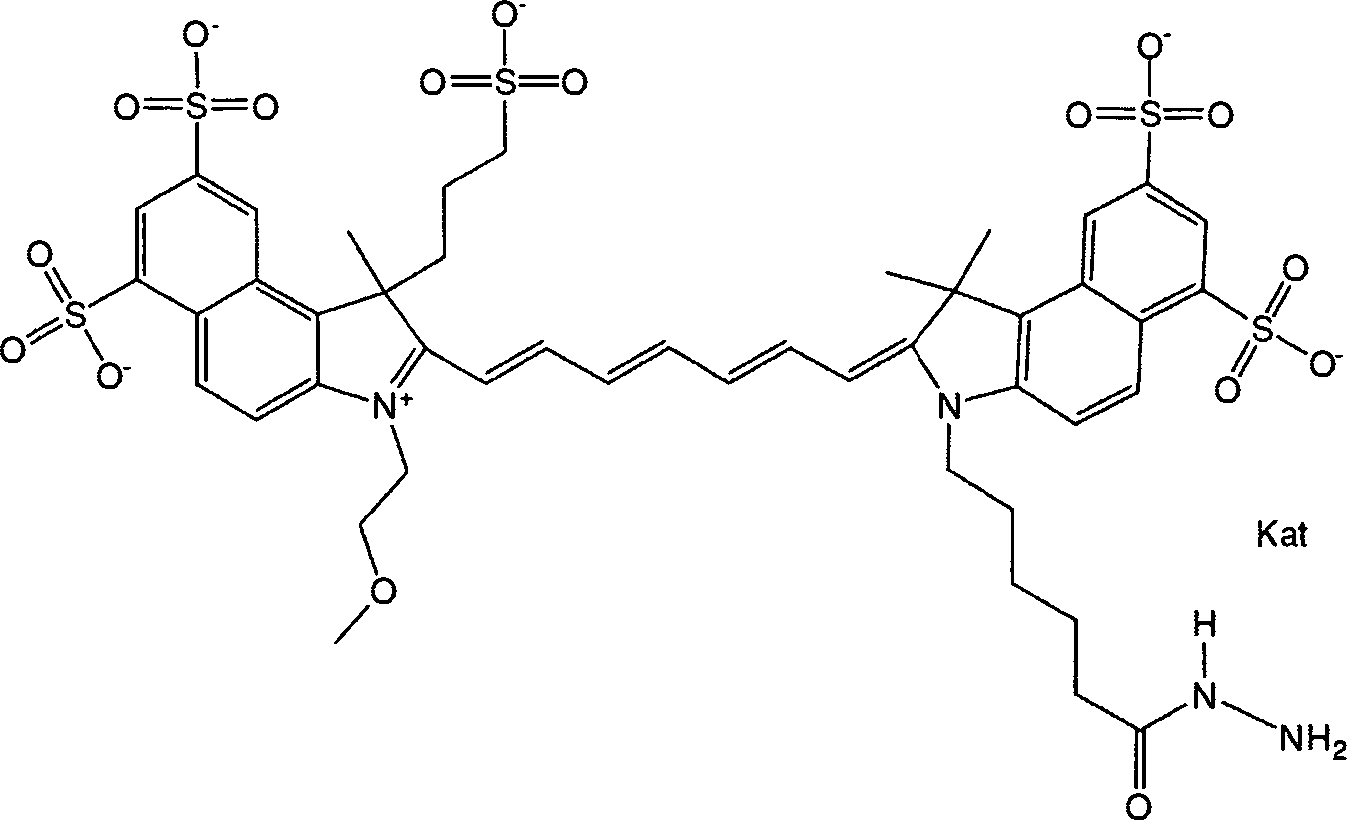
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel IIa
oder die allgemeine Formel IIb
auf, worin R
1, R
2, R
5 und R
6 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus einer aliphatischen Gruppe, einer heteroaliphatischen Gruppe, einer Sulfoalkylgruppe, einer heteroaliphatischen Gruppe mit terminalem SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; R
7, R
8, R
11, R
12, R
13 und R
14 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus H, SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe; X ausgewählt ist aus der Gruppe, bestehend aus -OH, -SH, -NH
2, -NH-NH
2, -F, -Cl, -Br, I, -NHS (Hydroxysuccinimidyl/Sulfosuccinimidyl), -O-TFP (2,3,5,6-Tetrafluorphenoxy), -O-STP (4-Sulfo-2,3,5,6-Tetrafluorphenoxy), -O-Benzotriazol, -Benzotriazol, -NR-L-OH, -NR-L-O-Phosphoramidit, -NR-L-SH, -NR-L-NH
2, -NR-L-NH-NH
2, -NR-LCO
2H, -NR-L-CO-NHS, -NR-L-CO-STP, -NR-L-CO-TFP, -NR-L-CO-Benzotriazol, -NR-L-CHO, -NR-L-Maleimid, -NR-L-NH-CO-CH
2-I, Imidazol, Azid, -NR-L-O-NH
2, und -NR-L-O-CO-NHS, worin R für -H oder eine aliphatische oder heteroaliphatische Gruppe steht und L ausgewählt ist aus der Gruppe, bestehend aus einer divalenten, linearen (-(CH
2)
t-, t = 0 bis 15), verzweigten oder zyklischen Alkylgruppe, gegebenenfalls substituiert mit mindestens einem Sauerstoffatom und/oder Schwefelatom; Kat eine Anzahl von Na
+-, K
+-, Ca
2+-, Ammoniak- oder (einem) anderen Kation(en) ist, die benötigt wird, um die durch das Cyanin bedingte, negative Ladung auszugleichen; m eine ganze Zahl von 0 bis 5 (jeweils einschließlich) ist, o eine ganze Zahl von 0 bis 12 (jeweils einschließlich) ist und n eine ganze Zahl von 1 bis 3 (jeweils einschließlich) ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formeln IIa oder IIb, d. h. die gemeinsame allgemeine Formel II, auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 is methyl und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R1, R5 und R6 jeweils für Methyl stehen und R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen; R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X4 für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, 0 = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, 0 = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3; o ist 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, 0 = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, o = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel II auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, o = 3 und n = 3 ist.
-
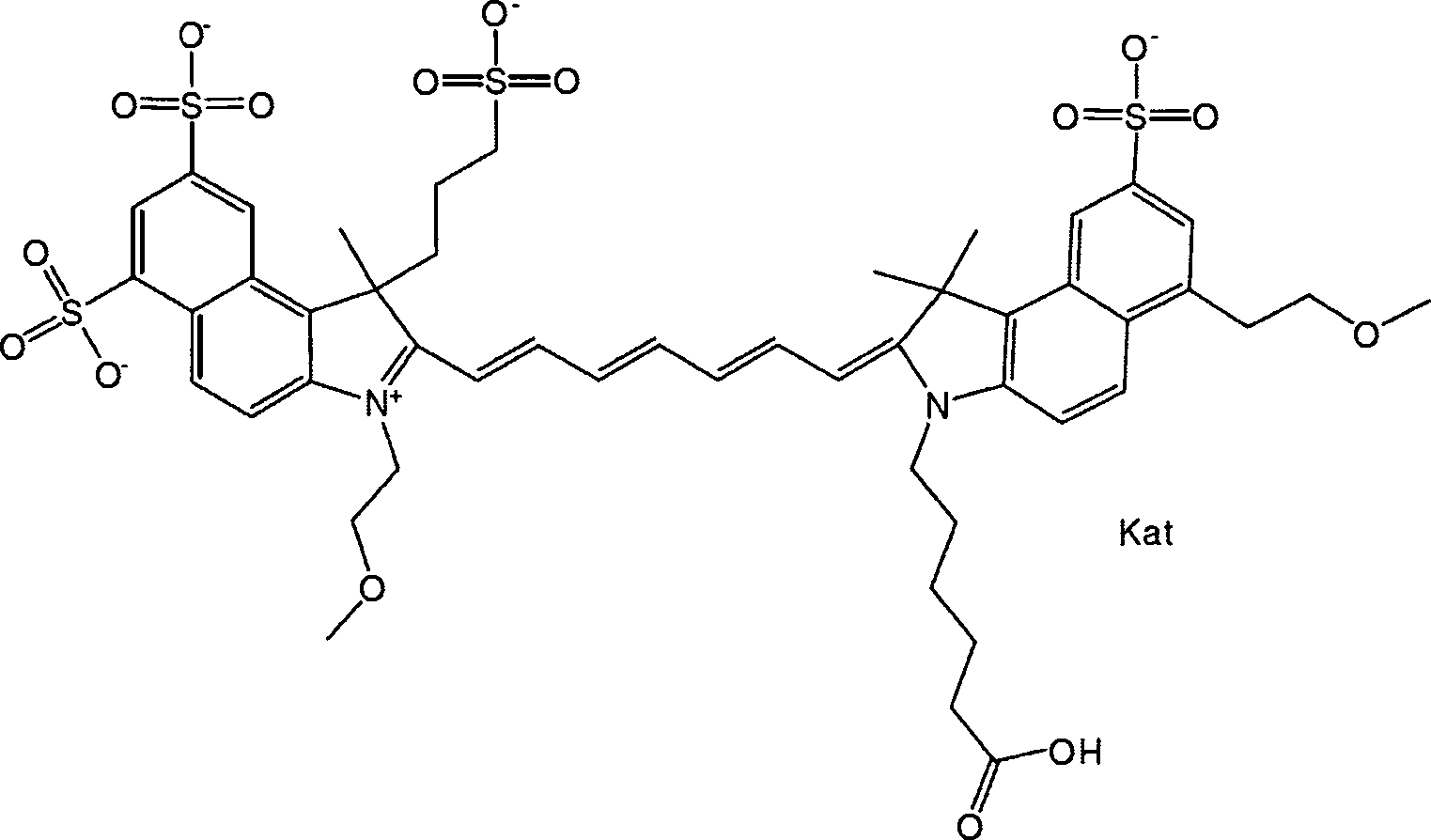
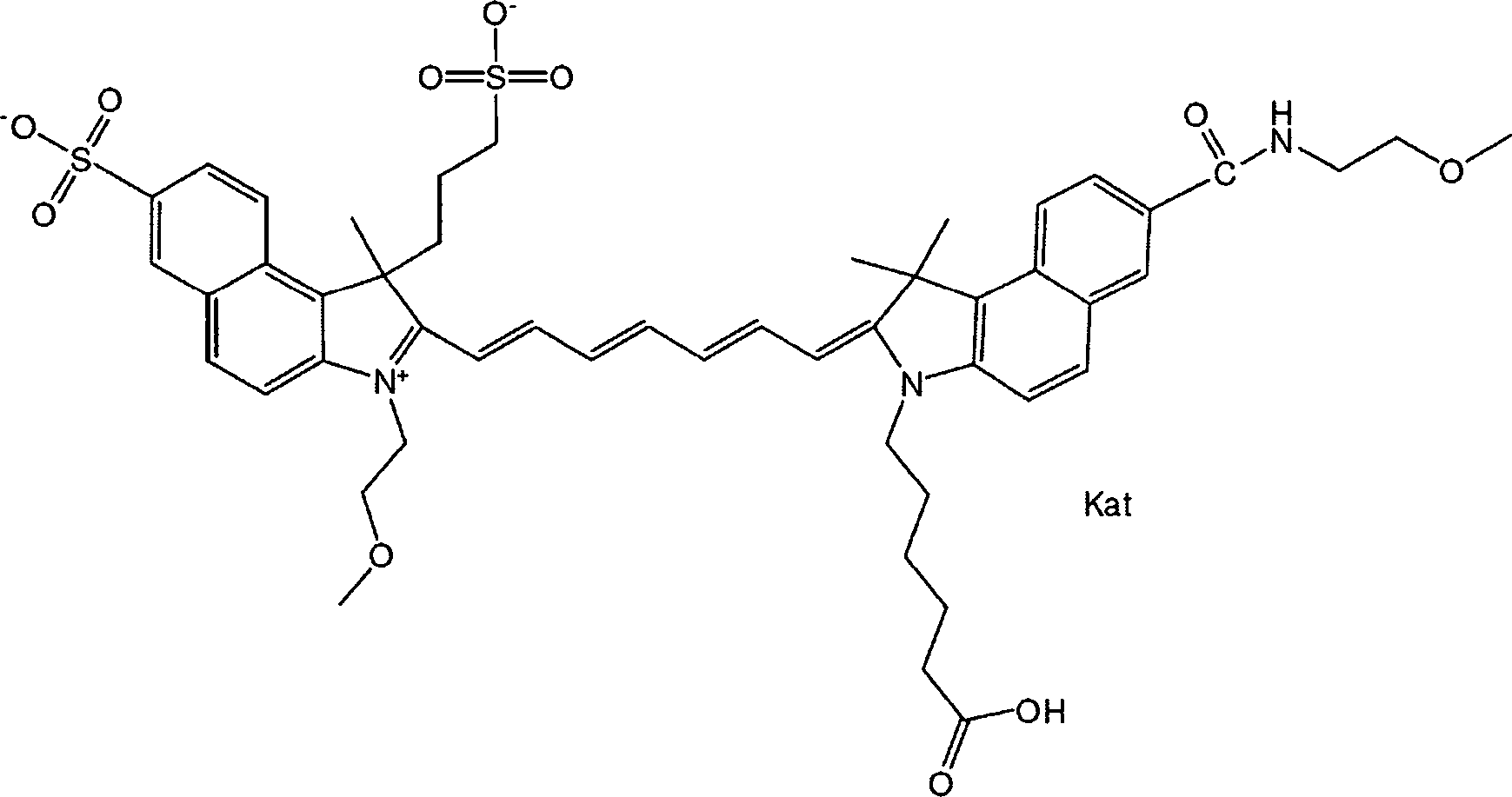
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel IIIa
oder die allgemeine Formel IIIb
auf, worin R
1, R
2, R
5 und R
6 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus einer aliphatischen Gruppe, einer heteroaliphatischen Gruppe, einer Sulfoalkylgruppe, einer heteroaliphatischen Gruppe mit terminalem SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
3 ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe; R
7, R
8, R
11, R
12, R
13 und R
14 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus H, SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
3 ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -SO
2NH-P-Z und einer Carboxamidgruppe -CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; X ausgewählt ist aus der Gruppe, bestehend aus -OH, -SH, -NH
2, -NH-NH
2, -F, -Cl, -Br, I, -NHS (Hydroxysuccinimidyl/Sulfosuccinimidyl), -O-TFP (2,3,5,6-Tetrafluorphenoxy), -O-STP (4-Sulfo-2,3,5,6-Tetrafluorphenoxy), -O-Benzotriazol, -Benzotriazol, -NR-L-OH, -NR-L-O-Phosphoramidit, -NR-L-SH, -NR-L-NH
2, -NR-L-NH-NH
2, -NR-LCO
2H, -NR-L-CO-NHS, -NR-L-CO-STP, -NR-L-CO-TFP, -NR-L-CO-Benzotriazol, -NR-L-CHO, -NR-L-Maleimid, -NR-L-NH-CO-CH
2-I, Imidazol, Azid, -NR-L-O-NH
2, und -NR-L-O-CO-NHS, worin R für -H oder eine aliphatische oder heteroaliphatische Gruppe steht und L ausgewählt ist aus der Gruppe, bestehend aus einer divalenten, linearen (-(CH
2)
t-, t = 0 bis 15), verzweigten oder zyklischen Alkylgruppe, gegebenenfalls substituiert mit mindestens einem Sauerstoffatom und/oder Schwefelatom; Kat eine Anzahl von Na
+-, K
+-, Ca
2+-, Ammoniak- oder (einem) anderen Kation(en) ist, die benötigt wird, um die durch das Cyanin bedingte, negative Ladung auszugleichen; m eine ganze Zahl von 0 bis 5 (jeweils einschließlich) ist, p eine ganze Zahl von 1 bis 6 (jeweils einschließlich) ist und n eine ganze Zahl von 1 bis 3 (jeweils einschließlich) ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeinen Formeln IIIa oder IIIb, gemeinsam als allgemeine Formel III bezeichnet, auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 für eine PEG-Gruppe steht, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R1, R5 und R6 jeweils für Methyl stehen, R2 eine PEG-Gruppe ist, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für Sulfo stehen, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7, R8, R11 und R12 jeweils für H stehen, R13 und R14 jeweils für Sulfo stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -OTFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Sulfonamidgruppe -SO2NH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 3 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 1 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 1 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 2 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 2 ist.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 0, p = 1 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 1, p = 2 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 2, p = 3 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 3, p = 4 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, -NHS, -O-TFP oder -NR-L-Maleimid steht, m = 4, p = 5 und n = 3 ist. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel III auf, worin R5 und R6 jeweils für Methyl stehen, R1 und R2 jeweils für eine PEG-Gruppe stehen, R7 und R8 jeweils für Sulfo stehen, R11 und R12 jeweils für eine Carboxamidgruppe -CONH-P stehen, worin P eine PEG-Gruppe ist, R13 und R14 jeweils für H stehen, X für -OH, NHS, -O-TFP oder -NR-L-Maleimid steht, m = 5, p = 6 und n = 3 ist.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 1
-
Die 579-Verbindung 1 (6-((E)-2-((E)-3-(3-(2-Methoxyethyl)-1-methyl-o,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)allyliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol3(2H)-yl)hexanoat) enthält ein Ethylenglykol am Indol-N des linken Heterozyklus, d. h. ein methyliertes Ethylenglykol. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen.
-
Bei manchen Ausführungsformen, z. B. für Funktionsassays, werden die erfindungsgemäßen Verbindungen aktiviert. Bei der Aktivierung der Verbindung wird eine chemische Einheit hinzugefügt, so dass die Verbindung in einer Form vorliegt, die mit einer biologischen Einheit konjugiert werden kann. Beispiele für chemische Einheiten zur Aktivierung sind nachfolgend unter Bezugnahme auf die Aktivierung der 579-Verbindung 1 beschrieben, wobei für den Fachmann jedoch ersichtlich ist, dass die Aktivierung nicht auf diese Beispiele beschränkt ist. Ein nicht einschränkendes Beispiel für eine aktivierte Verbindung ist der nachfolgend gezeigte NHS-Ester der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 1 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 2 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 3 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 4 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 5 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 6 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1 ist eine nachfolgend gezeigte Tetrafluorphenyl(TFP)-Esterform der 579 Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1 ist eine nachfolgend gezeigte Sulfotetrafluorphenyl(STP)-Esterform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1 ist eine nachfolgend gezeigte Hydrazidform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1 ist eine nachfolgend gezeigte Maleimidform der 579-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 2
-
Die 579-Verbindung 2 (6-((E)-2-((E)-3-(3-(2-(2-Methoxyethoxy)ethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)allyliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3-(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 2 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 3
-
Die 579-Verbindung 3 (6-((E)-2-((E)-3-(3-(2-(2-(2-Methoxyethoxy)ethoxy)ethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)allyliden)-1,1-dimethyl-6,8-disulfonato-1Hbenzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 3 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 4
-
Die 579-Verbindung 4 (6-((E)-1,1-Dimethyl-2-((E)-3-(1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-3-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-3-ium-2-yl)allyliden)-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579 Verbindung 4 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 5
-
Die 579-Verbindung 5 (6-((E)-2-((E)-3-(3-(2,5,8,11,14-Pentaoxahexadecan-16-yl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)allyliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579 Verbindung 5 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 6
-
Die 579-Verbindung 6 (6-((E)-1,1-Dimethyl-2-((E)-3-(1-methyl-3-(2,5,8,11,14,17-hexaoxanonadecan-19-yl)-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)allyliden)-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579 Verbindung 6 wie oben beschrieben aktiviert.
-
Bei manchen Ausführungsformen werden der Grad und/oder der Ort der Sulfonierung variiert, um z. B. den Hydrophilie- oder Hydrophobizitätsgrad der Verbindung zu variieren. Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Monosulfonatform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Disulfonatform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Trisulfonatform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Tetrasulfonatform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Pentasulfonatform der 579-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 1/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel der 579-Verbindung 1/2 (PEG4) (2-((1E,3E)-3-(3-(5-Carboxypentyl)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-2(3H)-yliden)prop-1-enyl)-3-(2-methoxyethyl)-1-methyl-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-6,8-disulfonat) enthält ein Ethylenglykol am Indol-N des linken Heterozyklus, d. h. ein methyliertes Ethylenglykol, und eine metyhlierte PEG4-Gruppe. Die Methylgruppe am Ethylenglykol/PEG verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen.
-
Bei manchen Ausführungsformen, z. B. für Funktionsassays, werden die erfindungsgemäßen Verbindungen aktiviert. Bei der Aktivierung der Verbindung wird eine chemische Einheit hinzugefügt, so dass die Verbindung in einer Form vorliegt, die mit einer biologischen Einheit konjugiert werden kann. Beispiele für chemische Einheiten zur Aktivierung sind nachfolgend unter Bezugnahme auf die Aktivierung der 579-Verbindung 1/2 (PEG
4) beschrieben, wobei für den Fachmann jedoch ersichtlich ist, dass die Aktivierung nicht auf diese Beispiele beschränkt ist. Ein nicht einschränkendes Beispiel für eine aktivierte Verbindung ist der nachfolgend gezeigte NHS-Ester der 579 Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 1 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 2 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 3 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 4 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 5 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 579-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 6 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Tetrafluorphenyl (TFP)-Esterform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Sulfotetrafluorphenyl (STP)-Esterform der 579-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1/2 ist eine nachfolgend gezeigte Hydrazidform der 579-Verbindung 1 (PEG
4):
-
Ein nicht einschränkendes Beispiel für eine aktivierte 579-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Maleimidform der 579-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 2/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel der 579-Verbindung 2/2 (PEG4) (2-((1E,3E)-3-(3-(5-Carboxypentyl)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-2(3H)-yliden)prop-1-enyl)-3-(2-(2-methoxyethoxy)ethyl)-1-methyl-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am (Poly)ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 2/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 3/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel der 579-Verbindung 3/2 (PEG4) (2-((1E,3E)-3-(3-(5-Carboxypentyl)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-2(3H)-yliden)prop-1-enyl)-3-(2-(2-(2-methoxyethoxy)ethoxy)ethyl)-1-methyl-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 3/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 4/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel der 579-Verbindung 4/2 (PEG4) (2-((1E,3E)-3-(3-(5-carboxypentyl)-1,1dimethyl-6,8-disulfonato-1H-benzo[e]indol-2(3H)-yliden)prop-1-enyl)-1-methyl-1,3-di(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 4/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 5/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel der 579-Verbindung 5/2 (PEG4) (2-((1E,3E)-3-(3-(5-Carboxypentyl)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-2(3H)-yliden)prop-1-enyl)-3-(2,5,8,11,14-pentaoxahexadecan-16-yl)-1-methyl-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 5/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 579-Verbindung 6/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel der 579-Verbindung 6/2 (PEG4) (2-((1E,3E)-3-(3-(5-Carboxypentyl)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-2(3H)-yliden)prop-1-enyl)-1-methyl-3-(2,5,8,11,14,17-hexaoxanonadecan-19-yl)-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 579-Verbindung 6/2 (PEG4) wie oben beschrieben aktiviert.
-
Bei manchen Ausführungsformen werden der Grad und/oder der Ort der Sulfonierung variiert, um z. B. den Hydrophilie- oder Hydrophobizitätsgrad der Verbindung zu variieren. Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Monosulfonatform der 579-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Disulfonatform der 579-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Trisulfonatform der 579-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Tetrasulfonatform der 579-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Pentasulfonatform der 579-Verbindung 1/2 (PEG
4):
-
Bei manchen Ausführungsformen enthält die Verbindung eine oder mehrere Substitutionen des Polymethin-Linkers. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel IVa
die allgemeine Formel IVb
die allgemeine Formel IVc
oder die allgemeine Formel IVd
auf, worin R
1, R
2, R
5 und R
6 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus einer aliphatischen Gruppe, einer heteroaliphatischen Gruppe, einer Sulfoalkylgruppe, einer heteroaliphatischen Gruppe mit terminalem SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; R
7, R
6, R
11, R
12, R
13 und R
14 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind unter H, SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z, oder einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe; X ausgewählt ist aus der Gruppe, bestehend aus -OH, -SH, -NH
2, -NH-NH
2, -F, -Cl, -Br, I, -NHS (Hydroxysuccinimidyl/Sulfosuccinimidyl), -O-TFP (2,3,5,6-Tetrafluorphenoxy), -O-STP (4-Sulfo-2,3,5,6-Tetrafluorphenoxy), -O-Benzotriazol, -Benzotriazol, -NR-LOH, -NR-L-O-Phosphoramidit, -NR-L-SH, -NR-L-NH
2, -NR-L-NH-NH
2, -NR-L-CO
2H, -NR-L-CO-NHS, -NR-L-CO-STP, -NR-L-CO-TFP, -NR-L-CO-Benzotriazol, -NR-L-CHO, -NR-L-Maleimid, -NR-L-NH-COCH
2-I, Imidazol, Azid, -NR-L-O-NH
2, und -NR-L-O-CO-NHS, worin R für -H oder eine aliphatische oder heteroaliphatische Gruppe steht und L ausgewählt ist aus der Gruppe, bestehend aus einer divalenten, linearen(-(CH
2)
t-, t = 0 bis 15), verzweigten oder zyklischen Alkylgruppe, gegebenenfalls substituiert mit mindestens einem Sauerstoffatom und/oder Schwefelatom; Kat eine Anzahl von Na
+-, K
+-, Ca
2+-, Ammoniak- oder (einem) anderen Kation(en) ist, die benötigt wird, um die durch das Cyanin bedingte, negative Ladung auszugleichen; m eine ganze Zahl von 0 bis 5 (jeweils einschließlich) ist, o eine ganze Zahl von 0 bis 12 (jeweils einschließlich) ist, p = eine ganze Zahl von 1 bis 6 (jeweils einschließlich) ist, R3 und R4 jeweils gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, eine aliphatische Gruppe, eine heteroaliphatische Gruppe oder eine PEG-Gruppe P-Z stehen, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe; oder R3 und R4 zusammen eine zyklische Struktur bilden, worin R3 und R4 durch ein divalentes Strukturelement verbunden sind, ausgewählt aus der Gruppe, bestehend aus -(CH
2)
q-, -(CH
2)
qO(CH
2)
q-, -(CH
2)
qS(CH
2)
q'-, -(CH
2)
qCH=CH- und -OCH=CH-, worin q und q' jeweils gleich oder verschieden sind und für eine ganze Zahl von 2 bis 6 (jeweils einschließlich) stehen, und Y ausgewählt ist aus der Gruppe, bestehend aus Wasserstoff, Alkyl, Sulfoalkyl, Fluor, Chlor, Brom, einer substituierten oder unsubstituierten Aryl-, Phenoxy-, Phenylmercaptofunktion, und einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel IV auf, worin R3 und R4 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, eine aliphatische Gruppe oder eine heteroaliphatische Gruppe stehen, oder R3 und R4 zusammen eine zyklische Struktur bilden, wobei R3 und R4 direkt miteinander oder mittels eines divalenten strukturellen Elementes verbunden sind, ausgewählt aus der Gruppe, bestehend aus -(CH2)q-und CH=CH, worin q eine ganze Zahl von 1 bis 2 (jeweils einschließlich) ist, um einen 3-, 4-, oder 5-gliedrigen Ring zu ergeben.
-
Bei verschiedenen Ausführungsformen können eine Ethylenglykolgruppe, eine Diethylenglykolgruppe und/oder eine Polyethylenglykolgruppe, die gemeinsam als PEG-Gruppe bezeichnet werden, sofern sie nicht speziell definiert sind, an (einer) Position(en) zusätzlich zu solchen Gruppen anwesend sein, die an dem (den) N-Atom(en) der Indol-Struktur vorhanden sind.
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R1 eine Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R2 eine Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG,) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel einer zusätzlich PEG-substituierten Verbindung ist eine 579-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 1
-
Die 679-Verbindung 1 (6-((E)-2-((2E,4E)-5-(3-(2-Methoxyethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)penta-2,4-dien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein Ethylenglykol am Indol-N des linken Heterozyklus, d. h. ein methyliertes Ethylenglykol. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen.
-
Bei manchen Ausführungsformen, z. B. für Funktionsassays, werden die erfindungsgemäßen Verbindungen aktiviert. Bei der Aktivierung der Verbindung wird eine chemische Einheit hinzugefügt, so dass die Verbindung in einer Form vorliegt, die mit einer biologischen Einheit konjugiert werden kann. Beispiele für chemische Einheiten zur Aktivierung sind nachfolgend unter Bezugnahme auf die Aktivierung der 679-Verbindung 1 beschrieben, wobei für den Fachmann jedoch ersichtlich ist, dass die Aktivierung nicht auf diese Beispiele beschränkt ist. Ein nicht einschränkendes Beispiel für eine aktivierte Verbindung ist der nachfolgend gezeigte NHS-Ester der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 1 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 2 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 3 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 4 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 5 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 6 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1 ist eine nachfolgend gezeigte Tetrafluorphenyl (TFP)-Esterform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1 ist eine nachfolgend gezeigte Sulfotetrafluorphenyl (STP)-Esterform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1 ist eine nachfolgend gezeigte Hydrazidform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1 ist eine nachfolgend gezeigte Maleimidform der 679-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 2
-
Die 679-Verbindung 2 (6-((E)-2-((2E,4E)-5-(3-(2-(2-Methoxyethoxy)ethyl)-1-methyl-6,8-disulfonato-1(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)penta-2,4-dien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein Diethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 2 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 3
-
Die 679-Verbindung 3 (6-((E)-2-((2E,4E)-5-(3-(2-(2-(2-Methoxyethoxy)ethoxy)ethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)penta-2,4-dien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 3 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 4
-
Die 679-Verbindung 4 (6-((E)-1,1-dimethyl-2-((2E,4E)-5-(1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-3-(25,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-3-ium-2-yl)penta-2,4-dien-1yliden)-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 4 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 5
-
Die 679-Verbindung 5 (6-((E)-2-((2E,4E)-5-(3-(2,5,8,11,14-Pentaoxahexadecan-16-yl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)penta-2,4-dien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 5 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 6
-
Die 679-Verbindung 6 (6-((E)-1,1-Dimethyl-2-((2E,4E)-5-(1-methyl-3-(2,5,8,11,14,17-hexaoxanonadecan-19-yl)-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)penta-2,4dien-1-yliden)-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 649-Verbindung 6 wie oben beschrieben aktiviert.
-
Bei manchen Ausführungsformen werden der Grad und/oder der Ort der Sulfonierung variiert, um z. B. den Hydrophilie- oder Hydrophobizitätsgrad der Verbindung zu variieren. Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Monosulfonatform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Disulfonatform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Trisulfonatform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Tetrasulfonatform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Pentasulfonatform der 679-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 1/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel für die 679-Verbindung 1/2 (PEG4) (2-((1E,3E,5E)-5-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)penta-1,3-dienyl)-3-(2-methoxyethyl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein Ethylenglykol am Indol-N des linken Heterozyklus, d. h. ein methyliertes Ethylenglykol, und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen.
-
Bei manchen Ausführungsformen, z. B. für Funktionsassays, werden die erfindungsgemäßen Verbindungen aktiviert. Bei der Aktivierung der Verbindung wird eine chemische Einheit hinzugefügt, so dass die Verbindung in einer Form vorliegt, die mit einer biologischen Einheit konjugiert werden kann. Beispiele für chemische Einheiten zur Aktivierung sind nachfolgend unter Bezugnahme auf die Aktivierung der 679-Verbindung 1/2 (PEG
4) beschrieben, wobei für den Fachmann jedoch ersichtlich ist, dass die Aktivierung nicht auf diese Beispiele beschränkt ist. Ein nicht einschränkendes Beispiel für eine aktivierte Verbindung ist der nachfolgend gezeigte NHS-Ester der 679-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 1 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 2 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 3 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 4 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 5 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 679-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 6 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Tetrafluorphenyl (TFP)-Esterform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Sulfotetrafluorphenyl (STP)-Esterform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Hydrazidform der 679-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 679-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Maleimidform der 679-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 2/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel für die 679-Verbindung 2/2 (PEG4) (2-((1E,3E,5E)-5-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)penta-1,3-dienyl)-3-(2-(2-methoxyethoxy)ethyl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein Diethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 2/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 3/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel für die 679-Verbindung 3/2 (PEG4) (2-((1E,3E,5E)-5-(3-(5-Carboxypentyl)-1-methyl-6, 8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)penta-1,3-dienyl)-3-(2-(2-(2-methoxyethoxy)ethoxy)ethyl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 3/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 4/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel für die 679-Verbindung 4/2 (PEG4) (2-((1E,3E,5E)-5-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)penta-1,3-dienyl)-1-methyl-1-(3-sulfonatopropyl)-3-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 4/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 5/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel für die 679-Verbindung 5/2 (PEG4) (2-((1E,3E,5E)-5-(3-(5-Carboxypentyl)-1-methyl-6, 8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)penta-1,3-dienyl)-3-(2,5,8,11,14-pentaoxahexadecan-16-yl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 679-Verbindung 5/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 679-Verbindung 6/2 (PEG
4)
-
Ein nicht einschränkendes Beispiel für die 679-Verbindung 6/2 (PEG4) (2-((1E,3E,5E)-5-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)penta-1,3-dienyl)-1-methyl-3-(2,5,8,11,14,17-hexaoxanonadecan-19-yl)-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 649-Verbindung 6/2 (PEG4) wie oben beschrieben aktiviert.
-
Bei manchen Ausführungsformen werden der Grad und/oder der Ort der Sulfonierung variiert, um z. B. den Hydrophilie- oder Hydrophobizitätsgrad der Verbindung zu variieren. Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Monosulfonatform der 679-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Disulfonatform der 679-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Trisulfonatform der 679-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Tetrasulfonatform der 679-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Pentasulfonatform der 679-Verbindung 1/2 (PEG
4):
-
Bei manchen Ausführungsformen enthält die Verbindung eine oder mehrere Substitutionen des Polymethin-Linkers. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel Va
die allgemeine Formel Vb
die allgemeine Formel Vc
oder die allgemeine Formel Vd
auf, worin R
1, R
2, R
5 und R
6 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus einer aliphatischen Gruppe, einer heteroaliphatischen Gruppe, einer Sulfoalkylgruppe, einer heteroaliphatischen Gruppe mit terminalem SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; R
7, R
8, R
11, R
12, R
13 und R
14 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind unter H, SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -SO
2NH-P-Z, oder einer Carboxamidgruppe -CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; X ausgewählt ist aus der Gruppe, bestehend aus -OH, -SH, -NH
2, -NH-NH
2, -F, -Cl, -Br, I, -NHS (Hydroxysuccinimidyl/Sulfosuccinimidyl), -O-TFP (2,3,5,6-Tetrafluorphenoxy), -O-STP (4-Sulfo-2,3,5,6-tetrafluorphenoxy), -O-Benzotriazol, -Benzotriazol, -NRL-OH, -NR-L-O-Phosphoramidit, -NR-L-SH, -NR-L-NH
2, -NR-L-NH-NH
2, -NR-L-CO
2H, -NR-L-CO-NHS, -NR-L-CO-STP, -NR-L-CO-TFP, -NR-L-CO-Benzotriazol, -NR-L-CHO, -NR-L-Maleimid, -NR-L-NH-COCH
2-I, Imidazol, Azid, -NR-L-O-NH
2, und -NR-L-O-CO-NHS, worin R für -H oder eine aliphatische oder heteroaliphatische Gruppe steht und L ausgewählt ist aus der Gruppe, bestehend aus einer divalenten, linearen (-(CH
2)
t-, t = 0 bis 15), verzweigten oder zyklischen Alkylgruppe, gegebenenfalls substituiert mit mindestens einem Sauerstoffatom und/oder Schwefelatom; Kat eine Anzahl von Na
+-, K
+-, Ca
2 +-, Ammoniak- oder (einem) anderen Kation(en) ist, die benötigt wird, um die durch das Cyanin bedingte, negative Ladung auszugleichen; m eine ganze Zahl von 0 bis 5 (jeweils einschließlich) ist, 0 eine ganze Zahl von 0 bis 12 (jeweils einschließlich) ist, p eine ganze Zahl von 1 bis 6 (jeweils einschließlich) ist, R3 und R4 jeweils gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, eine aliphatische Gruppe, eine heteroaliphatische Gruppe oder eine PEG-Gruppe P-Z stehen, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe oder einer Heteroalkylgruppe; oder R3 und R4 zusammen eine zyklische Struktur bilden, worin R3 und R4 durch ein divalentes Strukturelement verbunden sind, ausgewählt aus der Gruppe, bestehend aus -(CH
2)
q-, -(CH
2)
qO(CH
2)
q'-, -(CH
2)
qS(CH
2)
q'-, -(CH
2)
qCH=CH-, und -OCH=CH-, worin q und q' jeweils gleich oder verschieden sind und jeweils für eine ganze Zahl von 2 bis 6 (jeweils einschließlich) stehen, und Y ausgewählt ist aus der Gruppe, bestehend aus Wasserstoff, Alkyl, Sulfoalkyl, Fluor, Chlor, Brom, einer substituierten oder unsubstituierten Aryl-, Phenoxy-, Phenylmercaptofunktion und einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
q ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel V auf, worin R3 und R4 jeweils gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, eine aliphatische Gruppe oder einer heteroaliphatische Gruppe stehen oder R3 und R4 zusammen eine zyklische Struktur bilden, wobei R3 und R4 direkt oder mittels eines divalenten strukturellen Elementes miteinander verbunden sind, das ausgewählt ist aus der Gruppe, bestehend aus -(CH2)q- und CH=CH, worin q eine ganze Zahl von 1 bis 2 (jeweils einschließlich) ist, um einen 3-, 4- oder 5-gliedrigen Ring zu ergeben.
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 1, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 2, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 3, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 4, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 5, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 6, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 1, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 2, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 3, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 4, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 5, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 6, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 1/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 2/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 3/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 4/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 5/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 6/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 1/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 2/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 3/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 4/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 5/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 679-Verbindung 6/2 (PEG
4), wie nachfolgend gezeigt:
-
Bei verschiedenen Ausführungsformen kann eine Ethylenglykolgruppe, eine Diethylenglykolgruppe und/oder eine Polyethylenglykolgruppe, die gemeinsam als PEG-Gruppe bezeichnet werden, sofern sie nicht speziell definiert sind, an (einer) Position(en) zusätzlich zu solchen Gruppen, die an (einem) N-Atom(en) der Indol-Struktur vorhanden sind, vorliegen. Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R1 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R2 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 4/4 (V0815173) gemäß der allgemeinen Formel III, worin R1 und R2 jeweils für eine Polyethylenglykol (4)-Gruppe stehen, die mit einer Methylgruppe endet, p = 4 und X = NHS ist, und R7, R8, R11 und R12 jeweils für SO
3 stehen, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 679-Verbindung 4/4 (V1004152) gemäß der allgemeinen Formel III, worin R1 und R2 jeweils für eine Polyethylenglykol (4)-Gruppe stehen, die mit einer Methylgruppe endet, p = 4 und X = OH ist, und R13 und R14 jeweils für SO
3 stehen, wie nachfolgend gezeigt:
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 1
-
Die 779-Verbindung 1 (6-((E)-2-((2E,4E,6E)-7-(3-(2-Methoxyethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)hepta-2,4,6-trien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein Ethylenglykol am Indol-N des linken Heterozyklus, d. h. ein methyliertes Ethylenglykol. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen.
-
Bei manchen Ausführungsformen, z. B. für Funktionsassays, werden die erfindungsgemäßen Verbindungen aktiviert. Bei der Aktivierung der Verbindung wird eine chemische Einheit hinzugefügt, so dass die Verbindung in einer Form vorliegt, die mit einer biologischen Einheit konjugiert werden kann. Beispiele für chemische Einheiten zur Aktivierung sind nachfolgend unter Bezugnahme auf die Aktivierung der 779-Verbindung 1 beschrieben, wobei für den Fachmann jedoch ersichtlich ist, dass die Aktivierung nicht auf diese Beispiele beschränkt ist. Ein nicht einschränkendes Beispiel für eine aktivierte Verbindung ist der nachfolgend gezeigte NHS-Ester der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 1 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 2 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 3 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 4 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 5 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1 gemäß der allgemeinen Formel III, worin m = 1 und p = 6 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1 ist eine nachfolgend gezeigte Tetrafluorphenyl (TFP)-Esterform der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1 ist eine nachfolgend gezeigte Sulfotetrafluorphenyl (STP)-Esterform der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1 ist eine nachfolgend gezeigte Hydrazidform der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1 ist eine nachfolgend gezeigte Maleimidform der 779-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 2
-
Die 779-Verbindung 2 (6-((E)-2-((2E,4E,6E)-7-(3-(2-(2-Methoxyethoxy)ethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)hepta-2,4,6-trien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein Diethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 2 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 3
-
Die 779-Verbindung 3 (6-((E)-2-((2E,4E,6E)-7-(3-(2-(2-(2-Methoxyethoxy)ethoxy)ethyl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)hepta-2,4,6-trien-1-yliden)-1,1-dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 3 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 4
-
Die 779-Verbindung 4 (6-((E)-1,1-Dimethyl-2-((2E,4E,6E)-7-(1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-3-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-3-ium-2-yl)hepta-2,4,6-trien-1-yliden)-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 4 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 5
-
Die 779-Verbindung 5 (6-((E)-2-((2E,4E,6E)-7-(3-(2,5,8,11,14-Pentaoxahexadecan-16-yl)-1-methyl-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)hepta-2,4,6-trien-1-yliden)-1,1dimethyl-6,8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 5 wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 6
-
Die 779-Verbindung 6 (6-((E)-1,1-Dimethyl-2-((2E,4E,6E)-7-(1-methyl-3-(2,5,8,11,14,17-hexaoxanonadecan-19-yl)-6,8-disulfonato-1-(3-sulfonatopropyl)-1H-benzo[e]indol-3-ium-2-yl)hepta-2,4,6-trien-1-yliden)-6, 8-disulfonato-1H-benzo[e]indol-3(2H)-yl)hexanoat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 6 wie oben beschrieben aktiviert.
-
Bei manchen Ausführungsformen werden der Grad und/oder der Ort der Sulfonierung variiert, um z. B. den Hydrophilie- oder Hydrophobizitätsgrad der Verbindung zu variieren. Ein nicht einschränkendes Beispiel ist eine Monosulfonatform der 779-Verbindung 1, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine Disulfonatform der 779-Verbindung 1, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Trisulfonatform der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Tetrasulfonatform der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Pentasulfonatform der 779-Verbindung 1:
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 1/2 (PEG
4)
-
Die 779-Verbindung 1/2 (PEG4) (2-((1E,3E,5E,7E)-7-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)hepta-1,3,5-trienyl)-3-(2-methoxyethyl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein Ethylenglykol am Indol-N des linken Heterozyklus, d. h. ein methyliertes Ethylenglykol und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am Ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen.
-
Bei manchen Ausführungsformen, z. B. für Funktionsassays, werden die erfindungsgemäßen Verbindungen aktiviert. Bei der Aktivierung der Verbindung wird eine chemische Einheit hinzugefügt, so dass die Verbindung in einer Form vorliegt, die mit einer biologischen Einheit konjugiert werden kann. Beispiele für chemische Einheiten zur Aktivierung sind nachfolgend unter Bezugnahme auf die Aktivierung der 779-Verbindung 1/2 beschrieben, wobei für den Fachmann jedoch ersichtlich ist, dass die Aktivierung nicht auf diese Beispiele beschränkt ist. Ein nicht einschränkendes Beispiel für eine aktivierte Verbindung ist der nachfolgend gezeigte NHS-Ester der 779-Verbindung 1/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 1 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 2 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 3 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 4 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 5 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für einen NHS-Ester der 779-Verbindung 1/3 (PEG
4) gemäß der allgemeinen Formel III, worin m = 1 und p = 6 ist, ist nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1/2 (PEG
4) ist eine nachfolgend gezeigte Tetrafluorphenyl (TFP)-Esterform der 779-Verbindung 1:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1/2 (PEG
4) ist eine Sulfotetrafluorphenyl (STP)-Esterform der 779-Verbindung 1/2, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1/2 (PEG
4) ist eine Hydrazidform der 779-Verbindung 1/2, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine aktivierte 779-Verbindung 1/2 (PEG
4) ist eine Maleimidform der 779-Verbindung 1/2, wie nachfolgend gezeigt:
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 2/2 (PEG
4)
-
Die 779-Verbindung 2/2 (PEG4) (2-((1E,3E,5E,7E)-7-(3-(5-carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)hepta-1,3,5-trienyl)-3-(2-(2-methoxyethoxy)ethyl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein Diethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am (Poly)ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 2/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 3/2 (PEG
4)
-
Die 779-Verbindung 3/2 (PEG4) (2-((1E,3E,5E,7E)-7-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)hepta-1,3,5-trienyl)-3-(2-(2-(2-methoxyethoxy)ethoxy)ethyl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am (Poly)ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 3/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 4/2 (PEG
4)
-
Die Verbindung 4/2 (PEG4) (2-((1E,3E,5E,7E)-7-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)hepta-1,3,5-trienyl)-1-methyl-1-(3-sulfonatopropyl)-3-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am (Poly)ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 4/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 5/2 (PEG
4)
-
Die 779-Verbindung 5/2 (PEG4) (2-((1E,3E,5E,7E)-7-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)hepta-1,3,5-trienyl)-3-(2,5,8,11,14-pentaoxahexadecan-16-yl)-1-methyl-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus und eine PEG4-Gruppe am Indol-C. Die Methylgruppe am (Poly)ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 5/2 (PEG4) wie oben beschrieben aktiviert.
-
Gemäß einer Ausführungsform ist die Verbindung die 779-Verbindung 6/2 (PEG
4)
-
Die 779-Verbindung 6/2 (PEG4) (2-((1E,3E,5E,7E)-7-(3-(5-Carboxypentyl)-1-methyl-6,8-disulfonato-1-(2,5,8,11-tetraoxatridecan-13-yl)-1H-benzo[e]indol-2(3H)-yliden)hepta-1,3,5-trienyl)-1-methyl-3-(2,5,8,11,14,17-hexaoxanonadecan-19-yl)-1-(3-sulfonatopropyl)-1H-benzo[e]indolium-6,8-disulfonat) enthält ein (Poly)ethylenglykol am Indol-N des linken Heterozyklus. Die Methylgruppe am (Poly)ethylenglykol verhindert die Oxidierung des terminalen -OH. Bekanntlich erfolgt an einem ungeschützten PEG-Terminus im Laufe der Zeit eine Oxidation. Die Addition eines Methylethers bietet diesen Schutz und verhindert eine Reaktion mit elektrophilen reaktiven Gruppen. Für Funktionsassays wird die 779-Verbindung 6/2 (PEG4) wie oben beschrieben aktiviert.
-
Bei manchen Ausführungsformen werden der Grad und/oder der Ort der Sulfonierung variiert, um z. B. den Hydrophilie- oder Hydrophobizitätsgrad der Verbindung zu variieren. Ein nicht einschränkendes Beispiel ist eine Monosulfonatform der 779-Verbindung 1/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine Disulfonatform der 779-Verbindung 1/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Trisulfonatform der 779-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Tetrasulfonatform der 779-Verbindung 1/2 (PEG
4):
-
Ein nicht einschränkendes Beispiel ist eine nachfolgend gezeigte Pentasulfonatform der 779-Verbindung 1/2 (PEG
4):
-
Bei manchen Ausführungsformen enthält die Verbindung eine oder mehrere Substitutionen des Polymethin-Linkers. Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel VIa
die allgemeine Formel VIb
die allgemeine Formel VIc
oder die allgemeine Formel VId
auf, worin R
1, R
2, R
5 und R
6 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind aus der Gruppe, bestehend aus einer aliphatischen Gruppe, einer heteroaliphatischen Gruppe, einer Sulfoalkylgruppe, einer heteroaliphatischen Gruppe mit terminalem SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z und einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; R
7, R
8, R
11, R
12, R
13 und R
14 jeweils gleich oder verschieden und unabhängig voneinander ausgewählt sind unter H, SO
3, einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, einer Sulfonamidgruppe -L-SO
2NH-P-Z, oder einer Carboxamidgruppe -L-CONH-P-Z, wobei Z ausgewählt ist unter H, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; X ausgewählt ist aus der Gruppe, bestehend aus -OH, -SH, -NH
2, -NH-NH
2, -F, -Cl, -Br, I, -NHS (Hydroxysuccinimidyl/Sulfosuccinimidyl), -O-TFP (2,3,5,6-Tetrafluorphenoxy), -O-STP (4-Sulfo-2,3,5,6-Tetrafluorphenoxy), -O-Benzotriazol, -Benzotriazol, -NR-L-OH, -NR-L-O-Phosphoramidit, -NR-L-SH, -NR-L-NH
2, -NR-L-NH-NH
2, -NR-LCO
2H, -NR-L-CO-NHS, -NR-L-CO-STP, -NR-L-CO-TFP, -NR-L-CO-Benzotriazol, -NR-L-CHO, -NR-L-Maleimid, -NR-L-NH-CO-CH
2-1, Imidazol, Azid, -NR-L-O-NH
2, und -NR-L-O-CO-NHS, worin R für -H oder eine aliphatische oder heteroaliphatische Gruppe steht und L ausgewählt ist aus der Gruppe, bestehend aus einer divalenten, linearen (-(CH
2)
t-, t = 0 bis 15), verzweigten oder zyklischen Alkylgruppe, gegebenenfalls substituiert mit mindestens einem Sauerstoffatom und/oder Schwefelatom; Kat eine Anzahl von Na
+-, K
+, Ca
2+-, Ammoniak- oder (einem) anderen Kation(en) ist, die benötigt wird, um die durch das Cyanin bedingte, negative Ladung auszugleichen; m eine ganze Zahl von 0 bis 5 (jeweils einschließlich) ist, o eine ganze Zahl von 0 bis 12 (jeweils einschließlich) ist, p eine ganze Zahl von 1 bis 6 (jeweils einschließlich) ist, R3 und R4 jeweils gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, eine aliphatische Gruppe, eine heteroaliphatische Gruppe oder einer PEG-Gruppe P-Z stehen, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS; oder R3 und R4 zusammen eine zyklische Struktur bilden, worin R3 und R4 durch ein divalentes Strukturelement verbunden sind, ausgewählt aus der Gruppe, bestehend aus -(CH
2)
q-, -(CH
2)
qO(CH
2)
q'-, -(CH
2)
qS(CH
2)
q'-, -(CH
2)
qCH=CH- und -OCH=CH-, worin q und q' jeweils gleich oder verschieden und eine ganze Zahl von 2 bis 6 (jeweils einschließlich) sind, und Y ausgewählt ist aus der Gruppe, bestehend aus Wasserstoff, Alkyl, Sulfoalkyl, Fluor, Chlor, Brom, einer substituierten oder unsubstituierten Aryl-, Phenoxy-, Phenylmercaptofunktion, und einer PEG-Gruppe P-Z, wobei P ausgewählt ist unter einer Ethylenglykolgruppe, einer Diethylenglykolgruppe und einer Polyethylenglykolgruppe, wobei die Polyethylenglykolgruppe (CH
2CH
2O)
s ist, worin s eine ganze Zahl von 3–6 (jeweils einschließlich) ist, wobei Z ausgewählt ist unter H, CH
3, einer CH
3-Gruppe, einer Alkylgruppe, einer Heteroalkylgruppe oder -CO-NHS.
-
Gemäß einer Ausführungsform weist die Verbindung die allgemeine Formel VI auf, worin R3 und R4 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, eine aliphatische Gruppe oder einer heteroaliphatische Gruppe stehen, oder R3 und R4 zusammen eine zyklische Struktur bilden, worin R3 und R4 direkt oder mittels eines divalenten strukturellen Elementes miteinander verbunden sind, das ausgewählt ist aus der Gruppe, bestehend aus -(CH2)q- und CH=CH, worin q eine ganze Zahl von 1 bis 2 (jeweils einschließlich) ist, um einen 3-, 4-, oder 5-gliedrigen Ring zu ergeben.
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 1, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 2, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 3, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 4, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 5, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 6, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 1/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 2/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 3/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 4/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 5/2 (PEG
4), wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel ist eine substituierte Polymethinform der 779-Verbindung 6/2 (PEG
4), wie nachfolgend gezeigt:
-
Bei manchen Ausführungsformen kann eine Ethylenglykolgruppe, eine Diethylenglykolgruppe und/oder eine Polyethylenglykolgruppe, die gemeinsam als PEG-Gruppe bezeichnet werden, sofern sie nicht speziell definiert sind, an (einer) Position(en) zusätzlich zu solchen Gruppen, die an (dem) den N-Atom(en) der Indol-Struktur vorhanden sind, vorliegen.
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R1 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R2 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R8 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R7 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R12 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R11 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R13 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Ethylenglykolgruppe ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Sulfonamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Ein nicht einschränkendes Beispiel für eine zusätzlich PEG-substituierte Verbindung ist eine 779-Verbindung 1/2 gemäß der allgemeinen Formel II, worin R14 eine Carboxamidgruppe mit einer Ethylenglykolgruppe (PEG
1) ist, die mit einer Methylgruppe endet, wie nachfolgend gezeigt:
-
Die offenbarten Verbindungen sind als Chromophore und/oder Fluorophore brauchbar. Beispielsweise werden sie zur optischen Markierung und daher zur qualitativen und/oder quantitativen Detektion von Proteinen, Nukleinsäuren, Oligomeren, DNA, RNA, biologischen Zellen, Lipiden, Mono-, Oligo- und Polysacchariden, Liganden, Rezeptoren, Polymeren, Wirkstoffen, Polymerkügelchen usw. eingesetzt.
-
Die vorliegenden Verbindungen, welche die offenbarte(n) Funktionalität(en) aufweisen, können mit dem Fachmann bekannten Verfahren synthetisiert werden, wie sie z. B. nachfolgend beschrieben sind, wobei alle Druckschriften ausdrücklich in vollem Umfang durch Bezugnahme hier mitaufgenommen sind.
-
Die Indocyaninhauptstruktur ohne zusätzliche Funktionalitäten wurde, zusammen mit ihrer Synthese, von König im
US-Patent Nr. 1,524,791 und in BP 434875 beschrieben und enthielt 3-, 5- und 7-gliedrige Polymethinketten.
-
-
Die Synthese zahlreicher Modifikationen der Indocyaninhauptstruktur wurde bereits beschrieben. Solche Modifikationen ergaben verschiedene Funktionalitäten, z. B. ist die Synthese von N-Isothiocyanatoalkyl- und aromatischen Carboxyalkyl-funktionalisierten Indocyaninen in den
US-Patenten Nr. 5,627,027 ,
6,048,982 ,
4,981,977 , der
US-Veröffentlichung Nr. 2006/0199949 , und in
Southwick, Anal. Chem. 67 (1995) 1742–48) beschrieben.
-
-
-
Die Synthese von Indocyaninen mit einer oder zwei N-Carboxyalkylfunktionalitäten ist in den
US-Patenten Nr. 5,268,486 ,
5,486,616 ,
5,569,587 ,
5,569,766 und in
JP 03217837 beschrieben.
-
-
Die Synthese von Indocyaninen, die C-Carboxyalkylgruppen enthalten, ist in
JP 05-313304 , den
US-Veröffentlichungen Nr. 2006/0099638 ,
2006/0004188 ,
2002/0077487 ,
2002/0064794 , und den
US-Patenten Nr. 6,977,305 und
6,974,873 beschrieben.
-
-
Die Synthese von Indocyaninen mit N- und C-Sulfoalkylgruppen ist in
JP 05-313304 ,
WO 2005/044923 , und in der
US-Veröffentlichung Nr. 2007/0203343 beschrieben.
-
-
-
-
-
-
Die Synthese von Indocyaninen, die einen PEG-enthaltenden N-Carboxyalkyl-Spacer aufweisen, ist im
US-Patent Nr. 6,939,532 beschrieben.
-
-
Die Funktionalisierung des N-Carboxyalkyls mit einer Amino-funktionalisierten PEG-Alkylkette und N- und C-substituierten PEG-Alkylketten ist in der
US-Veröffentlichung Nr. 2009/0305410 beschrieben.
-
-
-
-
Die Synthese verschiedener Polymethinbrückensubstitutionen und weitere Funktionalisierungen von Indocyaninen beschreiben
Strekowski in: Heterocyclic Polymethine Dyes: Synthesis, Properties and Applications, (2008) Springer-Verlag, Berlin Heidelberg;
Gragg in: Synthesis of Near-Infrared Heptamethine Cyanine Dyes (2010).
Chemistry Theses. Paper 28, Patonay et al. (2004) in: Noncovalent Labeling of Biomolecules with Red and Near-Infrared Dyes. Molcules 9 (2004) 40–49, und das
US-Patent Nr. 7,172,907 . Die Beispiele 1–5 beschreiben die Synthesereaktionen für die Verbindungen.
-
Gemäß einer Ausführungsform wird die Verbindung durch eine dem Fachmann bekannte Kondensationsreaktion der beiden unterschiedlich substituierten Indol-Heterozyklen synthetisiert, die durch eine(n) (Poly)methin-Linker oder -Brücke, z. B. C1, C3 oder C5, voneinander getrennt sind. Auch andere Syntheseverfahren sind möglich. Als nur ein Beispiel wird zunächst einer der Indol-Heterozyklen mit dem C1-, C3- oder C5-Linker zur Reaktion gebracht. Das 1:1-Kondensationsprodukt wird isoliert und dann mit dem zweiten Indol-Heterozyklus kondensiert, um die Cyaninverbindung zu ergeben. Die Reihenfolge der Reaktion der Indol-Heterozyklen ist unerheblich. Somit lassen sich eine Vielzahl unterschiedlich funktionalisierter, stark hydrophiler, diastereomerer Verbindungen, die sich in der Gesamtladung und der Spezifität/Reaktivität der zur ihrer Immobilisierung verwendeten aktiven Gruppen unterscheiden, einfach herstellen.
-
Konjugate der Verbindungen werden durch kovalente Bindung der Verbindungen an ein Biomolekül unter Verwendung des funktionalen Substituenten an der N-Position des Indolrings hergestellt. Dieser funktionale Substituent wird durch übliche Proteinchemie-Reaktionsverfahren, die dem Fachmann bekannt sind, aktiviert. Die aktivierte Verbindung kann, ohne eine Einschränkung vorzunehmen, in einen N-Hydroxysuccinimid (NHS)-Ester, ein saures Fluorid, einen Tetrafluorphenyl (TFP)- oder Sulfotetrafluorphenyl (STP)-Ester, eine Iodacetylgruppe, ein Maleimid, ein Hydrazid, ein Sulfonylchlorid oder ein Phenylazid umgewandelt werden. Verfahren zur Herstellung solcher Verbindungen sind dem Fachmann bekannt. Gemäß einer Ausführungsform wird der aktivierte Substituent dann mit einer Aminogruppe am Biomolekül unter zur Ausbildung der Bindung geeigneten Bedingungen zur Reaktion gebracht. Gemäß einer Ausführungsform wird eine nicht-aktivierte Carboxylgruppe an der N-Position des Indols der Verbindung unter Verwendung eines Carbodimids an ein Amin gebunden.
-
Gemäß einer Ausführungsform wurde ein N-Hydroxysuccinimidylester (X = -NHS) einer Verbindung wie folgt gebildet: 20 μmol Farbstoff mit X = OH (Carboxyalkylgruppe), 8 mg (40 μmol) Dicyclohexylcarbodiimid und 5 mg (40 μmol) N-Hydroxysuccinimid wurden in 2 ml DMF und 100 μl Wasser gelöst. Dann wurden sechs μl (40 μmol) Triethylamin zugegeben. Das Reaktionsgemisch wurde bei Raumtemperatur (etwa 20°C bis etwa 22°C) 24 Stunden gerührt und dann filtriert. Das Lösungsmittel wurde abgezogen, und der Rückstand wurde mit Diethylether gewaschen. Die Reaktion lief quantitativ weiter.
-
Gemäß einer Ausführungsform wurde ein Maleimid (X = -NH-CH2CH2-Maleimid) einer Verbindung wie folgt gebildet: 20 μmol Farbstoff mit X = -NHS (N-Hydroxysuccinimidester) wurden in 2 ml DMF und 100 μl Wasser gelöst und mit 7,6 mg (30 μmol) 2-Maleimidoethylamintrifluoracetat und 5 μl (30 μmol) N-Ethyldiisopropylamin gemischt. Das Reaktionsgemisch wurde drei Stunden bei Raumtemperatur (etwa 20°C bis etwa 22°C) gerührt. Das Lösungsmittel wurde unter reduziertem Druck verdampft. Der Rückstand wurde mit Diethylether und Aceton gewaschen und im Vakuum getrocknet. Die Reaktion lief quantitativ weiter.
-
Gemäß einer Ausführungsform wurde ein Iodacetamid (X = -NH-CH2CH2-NH-CO-CH2-I) einer Verbindung wie folgt hergestellt: 20 μmol Farbstoff mit X = -NHS (N-Hydroxysuccinimidester) wurden in 2 ml DMF und 100 μl Wasser gelöst, gefolgt von der Zugabe von 40 mg (300 μmol) Ethylendiamindihydrochlorid und 26 μl (150 μmol) N-Ethyldiisopropylamin. Das Reaktionsgemisch wurde drei Stunden bei Raumtemperatur (etwa 20°C bis etwa 22°C) gerührt. Dann wurde das Lösungsmittel unter reduziertem Druck verdampft, der Rückstand in Methanol gelöst und das Ethylendiamindihydrochlorid durch Filtration entfernt. Das Methanol wurde unter reduziertem Druck abgedampft. Der Rückstand wurde in 2 ml trockenem DMF gelöst, gefolgt von der Zugabe von 7 mg (25 μmol) N-Succinimidyliodacetat und 4 μl (25 μmol) N-Ethyldiisopropylamin. Das Reaktionsgemisch wurde drei Stunden bei Raumtemperatur gerührt. Dann wurde das Lösungsmittel unter reduziertem Druck verdampft und der Rückstand mittels Umkehrphasen-HPLC gereinigt.
-
Gemäß einer Ausführungsform kann eine Hydroxylgruppe, wie eine terminale Hydroxylgruppe, später zu einem reaktiven Derivat aktiviert werden, das z. B. an Proteine und andere Moleküle binden kann. Beispiele für Aktivierungsgruppen umfassen Tosylchlorid (TsCl), Tresylchlorid (TrCl), Disuccinimidylcarbonat (DSC), Divinylsulfon, Bis-epoxyverbindungen, Carbonyldiimidazol (CDI), 2-Fluor-1-methylpyridin (FMP) und Trichlor-s-triazin (TsT). Gemäß einer Ausführungsform wird die Hydroxylgruppe zu einem Succinimidylcarbonat aktiviert, das mit Aminen reagieren kann. Beispielsweise kann Disuccinimidylcarbonat (DSC) verwendet werden, um in einem einzigen Schritt aminreaktive Gruppen aus Hydroxylen zu erzeugen, wie bei Wilchek, M. und Miron, T. (1985) (Activation of Sepharose with N,N'-disuccinimidyl carbonate. Applied Biochemistry und Biotechnology 11, 191–193) beschrieben. DSC reagiert mit einer Hydroxylgruppe, z. B. am Ende einer PEG-Kette der beschriebenen Verbindungen, um direkt einen reaktiven Ester mit Verlust eines Moleküls von NHS zu bilden. Diese reaktive Gruppe, bei der es sich um ein NHS-Carbonat handelt, kann zum Binden einer beschriebenen Verbindung mit aminhaltigen Molekülen, wie Proteinen, verwendet werden. Beispielsweise erzeugt die Reaktion eines NHS-Carbonats mit einem Amin eine Carbamatbindung (eine Urethanbindung), die so stabil wie die Amidbindungen ist, die durch die Reaktion eines NHS-Esters mit einem Amin gebildet werden. Gemäß einer Ausführungsform kann eine terminale Hydroxylgruppe einer PEG-enthaltenden Verbindung mit DSC aktiviert werden, um eine reaktive NHS-Carbonatgruppe zum Binden an aminhaltige Moleküle zu ergeben. Gemäß einer Ausführungsform ist die Gruppe X, wie sie in den offenbarten, allgemeinen Formeln beschrieben ist, ein Spacerarm, der in einer Hydroxylgruppe, wie einer PEG-Gruppe, endet, die ebenfalls mit DSC aktiviert werden kann, um das NHS-Carbonat zu erzeugen, d. h. wenn X = -NR-L-O-CO-NHS.
-
Die Kopplung zwischen der Verbindung und dem Biomolekül kann wie folgt durchgeführt werden. Die Verbindung wird mit dem Biomolekül in einer organischen oder wässrigen Lösung bei einem pH-Wert zwischen pH 5 und pH 12 (jeweils einschließlich) zur Reaktion gebracht. Die Verbindung muss nicht in einem organischen Lösungsmittel, wie Dimethylformamid (DMF) oder Dimethylsulfoxid (DMSO) gelöst werden, bevor das Biomolekül zugegeben wird. Gemäß einer Ausführungsform kann die Kopplungsreaktion in 100% wässriger Lösung durchgeführt werden. Gemäß einer Ausführungsform erfolgt die Kopplungsreaktion bei Raumtemperatur (etwa 20°C bis etwa 22°C).
-
Um eine Farbstoffzusammensetzung zu bilden, wird mindestens ein biokompatibler Exzipient zu der Verbindung gegeben, wie dies dem Durchschnittsfachmann bekannt ist. Exzipienten sind insbesondere Puffer, löslichkeitsverbessernde Mittel, Stabilisatoren usw.
-
Gemäß einer Ausführungsform umfasst ein Kit zur Durchführung eines Assayverfahrens eine offenbarte Verbindung und Anweisungen zur Durchführung des Verfahrens unter Verwendung der Verbindung.
-
Die offenbarten aktivierten Verbindungen (d. h. die mit einer reaktiven Gruppe modifizierte Verbindung) sind zur Markierung von Makromolekülen (z. B. Antikörpern, Streptavidin usw.) mittels dem Fachmann bekannter Verfahren geeignet, wie sie z. B. bei Hermanson, Bioconjugate Techniques, 2nd Ed., London, Elsevier Inc. 2008, beschrieben sind. Die Reaktion wird ein bis zwei Stunden bei Raumtemperatur (etwa 20°C bis etwa 22°C) durchgeführt, und dann durch Dialyse mit mehrmaligen Wechseln phosphatgepufferter Kochsalzlösung (pH 7,2) entsalzt oder mittels Gelfiltration gereinigt, um nicht umgesetzten, fluoreszierenden Farbstoff zu entfernen. Das resultierende Konjugat aus Verbindung und Biomolekül ist für solche Anwendungen brauchbar, wie Detektion spezifischer Proteine in Immunassays, von Zuckern in Glycoproteinen mit Lektinen, Protein-Protein-Wechselwirkungen, Oligonukleotiden in Nukleinsäure, Hybridisierung und für Elektrophoretische Mobilitätsshift-Assays (EMSA).
-
Die resultierenden Konjugate aus Verbindung und Biomolekül zeigen Fluoreszenzeigenschaften. Sie können in optischen Bestimmungsverfahren, einschließlich fluoreszenzoptischer, qualitativer und quantitativer Bestimmungsverfahren, eingesetzt werden. Beispiele für solche Verfahren sind insbesondere Mikroskopie, Immunassays, Hybridisierungsverfahren, chromatographische und elektrophoretische Verfahren, Fluoreszenz-Resonanz-Energietransfer (FREI)-Systeme, Screening mit hohem Durchsatz, Analyse von Rezeptor-Liganden-Wechselwirkungen an einem Mikroarray usw.
-
Verbindungen gemäß einer beliebigen der Ausführungsformen können als Farbstoffe zur optischen Markierung organischer oder anorganischer Biomoleküle, die auch als Erkennungseinheiten bezeichnet werden, verwendet werden. Erkennungseinheiten sind Moleküle mit Spezifität und/oder Affinität für eine spezifische Gruppe von Molekülen. Beispiele für Erkennungseinheiten umfassen insbesondere Antikörper mit Affinität für Antigene, Enzyme, die an eine oder mehrere spezifische Bindungen innerhalb einer Sequenz von Aminosäuren in einem Peptid binden und/oder damit reagieren oder mit einem Substrat reagieren, Cofaktoren, wie Metalle, die spezifische Wechselwirkungen verstärken oder inhibieren, Lektine, die spezifische Zucker oder Zuckersequenzen binden (z. B. Oligosaccharide, Polysaccharide, Dextrane usw.), Biotin-Bindungsproteine, wie Avidin und Streptavidin, die Biotin und biotinylierte Moleküle binden, Antikörperbindungsproteine, wie Protein A, Protein G, Protein A/G und Protein L, Sequenzen von Aminosäuren oder Metallen mit gegenseitiger Affinität (z. B. binden Histidinsequenzen Nickel oder Kupfer, phosphathaltige Proteine, die Gallium, Aluminium usw. binden), spezifische Sequenzen von Nukleinsäuren, wie DNA- und/oder RNA-Oligonukleotide mit Affinität für Proteine, spezifische Sequenzen von Aminosäuren mit Affinität für DNA und/oder RNA, Haptene, Carotinoide, Hormone (z. B. Neurohormone), Neurotransmitter, Wachstumsfaktoren, Toxine, biologische Zellen, Lipide, Rezeptorbindende Wirkstoffe oder organische oder anorganische Polymerträgermaterialien, Fluoreszenzproteine, wie Phycobilliproteine (z. B. Phycoethrin, Allophycocyanin) usw. Die Ionenwechselwirkungen zwischen diesen Erkennungseinheiten und den offenbarten Verbindungen führen zur Markierung der Erkennungseinheiten. Die Erkennungseinheit und die Verbindung können kovalent aneinander gebunden sein. Das Ergebnis ist ein Konjugat zur qualitativen oder quantitativen Bestimmung verschiedener Biomaterialien oder anderer organischer oder anorganischer Materialien mittels optischer Methoden.
-
Die erfindungsgemäßen Verbindungen und/oder Konjugate sind brauchbar für optische, einschließlich fluoreszenzoptischer, qualitativer und/oder quantitativer Bestimmungsmethoden zur Diagnose der Eigenschaften von Zellen (molekulare Bildgebung), für Biosensoren (Point-of-Care-Messungen), zur Untersuchung des Genoms und für Miniaturisierungstechnologien. Mikroskopie, Cytometrie, Zellsortierung, Fluoreszenzkorrelationsspektroskopie (FCS), Ultra-Screening mit hohem Durchsatz (uHTS), Mehrfarbenfluoreszenz-in situ-Hybridisierung (mc-FISH), FREI-Systeme und Mikroarrays (DNA- und Protein-Chips) sind beispielhafte Anwendungsfelder. Dem Fachmann ist bekannt, dass ein Mikroarray, eine gitterartige Anordnung, in der mehr als zwei unterschiedliche Moleküle in einem bekannten, vordefinierten Bereich oder zumindest einer Oberfläche immobilisiert sind, brauchbar ist, um Rezeptor-Liganden-Wechselwirkungen zu beurteilen. Wie dem Fachmann bekannt ist, handelt es sich bei einem Rezeptor um ein natürlich vorkommendes oder synthetisches Molekül, das eine Affinität für einen bestimmten Liganden zeigt. Rezeptoren können in reiner Form oder an eine andere Spezies gebunden verwendet werden. Rezeptoren können kovalent oder nicht-kovalent an einen Bindungspartner, entweder direkt oder indirekt (z. B. durch einen Bindungsvermittler), gebunden sein. Beispiele für Rezeptoren umfassen insbesondere Agonisten und Antagonisten für Zellmembranrezeptoren, Toxine und andere Gifte, virale Epitope, hormonähnliche Opiate und Steroide, Hormonrezeptoren, Peptide, Enzyme, Enzymsubstrate, als Cofaktoren wirkende Wirkstoffe, Lektine, Zucker, Oligonukleotide, Nukleinsäuren, Oligosaccharide, Zellen, Zellfragmente, Gewebefragmente, Proteine, Antikörper usw. Wie dem Fachmann bekannt ist, handelt es sich bei einem Liganden um ein Molekül, das von einem bestimmten Rezeptor erkannt wird. Beispiele für Liganden umfassen insbesondere Agonisten und Antagonisten für Zellmembranrezeptoren, Toxine und andere Gifte, virale Epitope, hormonähnliche Opiate und Steroide, Hormonrezeptoren, Peptide, Enzyme, Enzymsubstrate, als Cofaktoren wirkende Wirkstoffe, Lektine, Zucker, Oligonukleotide, Nukleinsäuren, Oligosaccharide, Proteine, Antikörper usw.
-
KURZE BESCHREIBUNG DER ZEICHNUNGEN
-
Die Patent- oder Anmeldungsakte enthält mindestens eine in Farbe ausgeführte Zeichnung. Kopien dieser Patent- oder Patentanmeldungsschrift mit Farbzeichnung(en) werden vom Amt auf Anfrage und gegen Entrichtung der erforderlichen Gebühr bereitgestellt.
-
1 zeigt Absorptions-/Emissionsprofile einiger erfindungsgemäßer Verbindungen und handelsüblicher Farbstoffe.
-
2 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, wobei in einer Ausführungsform ein Konjugat produziert wird.
-
3 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, wobei in einer Ausführungsform ein anderes Konjugat produziert wird.
-
4 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, wobei in einer Ausführungsform ein anderes Konjugat produziert wird.
-
5 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, wobei in einer Ausführungsform ein Konjugat produziert wird.
-
6 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, wobei in einer Ausführungsform ein Konjugat produziert wird.
-
7 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, wobei in einer Ausführungsform ein Konjugat produziert wird.
-
8 zeigt Funktionsassay-Ergebnisse mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
9 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
10 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
11 zeigt tabellarisch Funktionsassay-Ergebnisse mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
12 ist eine graphische Darstellung von Funktionsassay-Ergebnissen mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
13 zeigt tabellarisch Funktionsassay-Ergebnisse mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
14 ist ein Histogramm, das Funktionsassay-Ergebnisse mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform zeigt.
-
15A–D zeigen Immunfluoreszenzdaten mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, die in einer Ausführungsform ein Konjugat bilden.
-
16A–D zeigen Immunfluoreszenzdaten mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen, die in einer Ausführungsform ein Konjugat bilden.
-
17A–D zeigen Immunfluoreszenzdaten mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
18A–D zeigen Immunfluoreszenzdaten mit einigen handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
19A–C zeigen Immunfluoreszenzdaten mit handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
20A–C zeigen Immunfluoreszenzdaten mit handelsüblichen Farbstoffen und erfindungsgemäßen Verbindungen gemäß einer Ausführungsform.
-
Die folgenden, nicht einschränkenden Beispiele beschreiben die Verbindungen, Verfahren, Zusammensetzungen, Verwendungen und Ausführungsformen noch näher. Sie zeigen, dass die erfindungsgemäßen Verbindungen erwünschte Eigenschaften gegenüber handelsüblichen Fluoreszenzfarbstoffen aufwiesen. Der Signal-Rausch-Abstand (S/N) ist das Verhältnis zwischen dem gewünschten Signal und dem Mittelwert des Blank-Signals, und ergibt die Standardabweichung des Signals und des Blank-Signals. Das Signal-Hintergrund-Verhältnis (S/B) ist das Verhältnis zwischen dem gewünschten durchschnittlichen Signal und dem durchschnittlichen Blank-Signal.
-
BEISPIEL 1
-
Synthese von 1,2-Dimethyl-1-(3-sulfopropyl)-1H-benzo[e]-Indol-6,8-disulfonsäuretrikaliumsalz
-
-
Fünf g (15,7 mmol) 6-Hydrazinn-naphthalin-1,3-disulfonsäure und 4,93 g (25 mmol) 4-Methyl-5-oxohexansulfonsäure wurden in 50 ml Essigsäure gelöst. Die Lösung wurde vier Stunden bei 140°C erwärmt. Das Lösungsmittel wurde im Vakuum verdampft. Der ölige Rückstand wurde in 20 ml Methanol gelöst; dann wurden 50 ml einer gesättigten Lösung von KOH in 2-Propanol zugegeben, was ein gelbes Präzipitat ergab. Der Feststoff wurde abfiltriert und im Vakuum getrocknet. Ausbeute: 4,1 g, MS (ESI-): 158,2 [M]3–
-
BEISPIEL 2
-
Synthese von 3-(2-Methoxyethyl)-1,2-dimethyl-6,8-disulfo-1-(3-sulfopropyl)-1H-benzo[e]indolium
-
-
Ein Gemisch von 7,56 g (12,8 mmol) 1,2-Dimethyl-1-(3-sulfopropyl)-1H-benzo[e]Indol-6,8-disulfonsäuretrikaliumsalz und 5,89 g (25,6 mmol) 2-Methoxyethyl-p-toluolsulfonat wurde 24 Stunden unter Argon erwärmt. Der Rückstand wurde mittels Säulenchromatographie (Umkehrphase, Silica, Methanol/Wasser, TFA) gereinigt. Ausbeute: 3,2 g, MS (ESI-): 266,5 [M – 2H]2–
-
BEISPIEL 3
-
Synthese von 3-(5-Carboxypentyl)-1,1,2-timethyl-6,8-disulfo-1H-benzo[e]indolium
-
-
Ein Gemisch von 5,7 g (12,8 mmol) 1,1,2-Trimethyl-1H-benzo[e]Indol-6,8-disulfonsäuredikaliumsalz und 5 g (25,6 mmol) 6-Bromhexansäure wurde 24 Stunden unter Argon erwärmt. Der Rückstand wurde mittels Säulenchromatographie (Umkehrphase, Silica, Methanol/Wasser, TFA) gereinigt. Ausbeute: 1,4 g, MS (ESI-): 482,1 [M – H]–
-
BEISPIEL 4
-
Synthese von 3-(5-Carboxypentyl)-1,1-dimethyl-2-((1E,3E)-4-phenylamino-buta-1,3-dienyl)-6,8-disulfo-1H-benzo[e]indolium
-
-
0,97 g (2 mmol) 3-(5-Carboxypentyl)-1,1,2-trimethyl-6,8-disulfo-1H-benzo[e]indolium und 0,57 g (2,2 mmol) Malonaldehydbisphenyliminhydrochlorid wurden in 10 ml Essigsäure und 10 ml Essigsäureanhydrid gelöst und vier Stunden bei 120°C gerührt. Das Lösungsmittel wurde unter Vakuum abgezogen. Der Rückstand wurde vorsichtig mit Ethylacetat gewaschen. Ein dunkelbrauner Feststoff wurde erhalten, der ohne weitere Reinigung verarbeitet wurde. MS (ESI-): 611,2 [M – H]–.
-
BEISPIEL 5
-
Synthese der 679 Verbindung 1/1 (2-((1E,3E)-5-[3-(5-Carboxypentyl)-1,1-dimethyl-6,8-disulfo-1,3-dihydro-benzo[e]Indol-(2E)-ylidene]-penta-1,3-dienyl)-3-(2-methoxy-ethyl)-1-methyl-6,8-disulfo-1(3-sulfopropyl)-1H-benzo[e]indolium)
-
-
612 mg (1 mmol) 3-(5-Carboxypentyl)-1,1-dimethyl-2-((1E,3E)-4-phenylamino-buta-1,3-dienyl)-6,8-disulfo-1H-benzo[e]indolium und 533 mg (1 mmol) 3-(2-Methoxyethyl)-1,2-dimethyl-6,8-disulfo-1-(3-sulfopropyl)-1H-benzo[e]indolium wurden in 20 ml Essigsäure/Essigsäureanhydrid (1/1) gelöst, gefolgt von der Zugabe von 200 mg Natriumacetat. Die Lösung wurde 15 Min. unter Rückfluss gerührt. Nach Abkühlen auf Raumtemperatur wurden 20 ml Diethylether zugegeben. Das resultierende Präzipitat (Gemisch der Diastereomere 679-Verbindung 1/1 (Isomer 1) und 679-Verbindung 1/1 (Isomer 2)) wurde mittels Unterdruck extrahiert, mit Ether gewaschen und getrocknet.
-
Der Rückstand wurde mittels Säulenchromatographie (RP-18, Acetonitril/Wasser und konzentrierte HCl) gereinigt, um die Diastereomere voneinander zu trennen. Das zuerst aus der Säule eluierte Diastereomer wurde als Diastereomer 1 (679-Verbindung 1/1 (Isomer 1)) bezeichnet. Das als zweites aus der Säule eluierte Diastereomer wurde als Diastereomer 2 (679-Verbindung 1/1 (Isomer 2)) bezeichnet. Die Diastereomere wurden getrennt, gefolgt von Neutralisation und Verdampfen. Die Reinigung der einzelnen Diastereomer-Verbindung wurde mit einer RP-18-Säule, Acetonitril/Wasser abgeschlossen. Die entsprechenden Fraktionen wurden vereinigt, und das Lösungsmittel wurde mittels Destillation entfernt. Die zwei Produkte (Diastereomere 679-Verbindung 1/1 (Isomer 1) und 679-Verbindung 1/1 (Isomer 2)) wurden in einem hohen Vakuum getrocknet.
679-Verbindung 1/1 (Isomer 1)
Ausbeute: 10%
UV-vis (PBS): λmax = 679 nm
λem = 698 nm
MS (ESI-) [M/z]: 262,5 [M]4–; 357,7 [M + Na]3–
679-Verbindung 1/1 (Isomer 2)
Ausbeute: 23%
UV-vis (PBS): λmax = 679 nm
λem = 698 nm
MS (ESI-) [M/z]: 262,5 [M]4–; 357,7 [M + Na]3–
-
BEISPIEL 6
-
Die folgenden Eigenschaften von 679-Verbindung 1-NHS wurden mit handelsüblichen Farbstoffen verglichen.
| | DyLight 680-NHS | DyLight 680B-NHS | 679-Verbindung 1-NHS | Verbindung der Firma B-NHS | Cy5.5-Monoester |
| MW (g/mol) | 950 | 1196,16 | 1240,21 | ~1150 | 1128,42 |
| Ex(nm) | 682 | 679 | 679 | 679 | 675 |
| Em (nm) | 715 | 698 | 698 | 702 | 694 |
| ε (M–1 cm–1) (theoretisch) | 140.000 | 180.000 | 180.000 | 184.000 | 250.000 |
-
Emissions-/Anregungsprofile für erfindungsgemäße und handelsübliche Verbindungen wurden durch Rekonstitution der Verbindungen in DMF bei 10 mg/ml und anschließendes Verdünnen in PBS-Puffer bei pH 7,2 auf 10 μg/ml bestimmt. Die Extinktionsspektren wurden mit einem Cary UV-Spektrophotometer erfasst und die Emissionsspektren mit Tecan Safire erfasst, wie dies in
1 gezeigt ist, worin die durchgezogenen Linien für die Extinktionsspektren und die gestrichelten Linien für die Emissionsspektren von DyLight 680-NHS (lila), DyLight 680B-NHS (blau), 679-Verbindung 1-NHS (rot), und Verbindung der Firma B-NHS (schwarz) stehen. Die Extinktions- und Emissionsmaxima jeder Verbindung sind nachfolgend gezeigt.
| | Max Extinktion (nm) | Max Emission (nm) |
| DyLight 680 | 677 | 715 |
| DyLight 680B | 680 | 704 |
| 679-Verbindung 1 | 679 | 704 |
| Verbindung der Firma B | 676 | 706 |
-
Die folgenden Eigenschaften von 679-Verbindung 1-NHS, 679-Verbindung 4/4-NHS (V08-15173) und 679-Verbindung 4/4-NHS (V10-04152) wurden mit handelsüblichen Farbstoffen verglichen.
| | DyLight 680B-NHS | 679 Verbindung 1-NHS | V08-15173 NHS | V10-04152 NHS | Firma B Verbindung-NHS | Firma A Verbindung-NHS |
| MW (g/mol) | 1196,16 | 1240,21 | 1728,8 | 1524,75 | ~1150 | 3241 |
| Ex (nm) | 679 | 679 | 684 | 689 | 679 | 681 |
| Em (nm) | 698 | 698 | 706 | 721 | 702 | 698 |
| ε (M–1 cm–1) (theoretisch) | 180.000 | 180.000 | 180.000 | 180.000 | 184.000 | 210.000 |
| PEG (Länge/Nr. der Kette) | 0 | 1/1 | 4/4 | 4/4 | N/A | ? |
| Sulfonat | 5 | 5 | 4 | 2 | 3 | ? |
-
BEISPIEL 7
-
Erfindungsgemäße und handelsübliche Verbindungen, jeweils als NHS-Ester, wurden mit Ziege-Anti-Maus (GAM)-Antikörpern, Ziege-Anti-Kaninchen (GAR)-Antikörpern und Streptavidin (SA) konjugiert. GAM, GAR und SA wurden in einer Konzentration von 10 mg/ml in phosphatgepufferter Kochsalzlösung (PBS) gegen 50 mM Boratpuffer, pH 8,5, dialysiert. Die Verbindungen wurden in Dimethylformamid (DMF) bei 10 mg/ml rekonstituiert und in 2-, 4-, 5-, 7,5- oder 10-fachem molarem Überschuss mit GAM, GAR oder SA zwei Stunden bei Raumtemperatur vereinigt, um die Antikörper oder SA zu markieren.
-
Die markierten Verbindungen, auch als Farbstoffe oder Markierungen bezeichnet, wurden Pierce Dye Removal Resin (PDDR) ausgesetzt, um die unmarkierte (freie) Verbindung zu entfernen; pro mg gereinigten Proteins wurden 100 μl des gepackten Harzes verwendet. Die gereinigten, Antikörpermarkierten Farbstoffe wurden dann 1:50 in PBS verdünnt und auf Extinktion von 700 nm bis 230 nm gescannt, um die Proteinkonzentration sowie das Verhältnis Mol Farbstoff:Mol Protein zu bestimmen. Jedes Konjugat wurde 1:10 in 50% Glycerin verdünnt und in Gegenwart von 10 mM Dithiothreitol (DTT) 5 Min. bei 95°C erwärmt, dann durch Elektrophorese auf Polyacrylamidgelen in Gegenwart von Natriumdodecylsulfat (SDS-PAGE) getrennt. Die Gele wurden dann mit dem Typhoon 9400 Imager gescannt, um das Entfernen der unkonjugierten Verbindung zu überprüfen. Die Markierungseffizienz wurde verglichen, wobei die Ergebnisse, die den Markierungsgrad angeben, nachfolgend gezeigt sind.
| | DyLight 680 | DyLight 6806 | 679-Verbindung 1 | Verbindung der Firma B | Cy5.5 |
| GAM-2X | 0,9 | 1,9 | 2,0 | - | 1,6 |
| GAM-3X | 1,3 | 2,7 | 3,0 | - | 2,2 |
| GAM-4X | 2,0, 1,9 | 3,6, 3,6 | 3,6, 3,7 | 2,8 | 2,6 |
| GAM-6X | 2,3 | 5,0 | 5,1 | 3,9 | - |
| GAM-8X | 2,4 | 5,6 | 5,0 | 4,3 | - |
| GAM-10X | 3,0 | 6,5 | 6,8 | 5,4 | - |
| GAM-12X | 3,0 | 7,4 | 7,2 | 6,2 | - |
| GAR-1X | 0,5 | 0,9 | 1,0 | | 0,7 |
| GAR-2X | 1,0 | 1,5 | 1,6 | | 1,2 |
| GAR-3X | 1,3 | 2,1 | 2,4 | | 1,7 |
| GAR-4X | 1,7, 1,8 | 2,6, 3,1 | 3,1, 3,1 | 2,3 | 2,2 |
| GAR-6X | 2,2 | 4,4 | - | - | - |
| GAR-8X | 2,4 | 5,5 | 5,6 | 4,2 | - |
| GAR-10X | 3,5 | 6,0 | 6,7 | 5,3 | - |
| GAR-12X | 3,4 | 6,6 | 6,7 | 6,2 | - |
| SA-6X | 2,9 | 4,1 | 4,0 | 4,1 | - |
| SA-8X | 3,4 | 4,7 | 5,0 | 4,8 | - |
-
Die Markierungseffizienz von GAM, GAR und SA war für 679-Verbindung 1-NHS im Vergleich zu DyLight 680B-NHS gleich und im Vergleich zu DyLight 680 und der Verbindung der Firma B höher. Die Antikörper wurden, wie oben beschrieben, markiert, gereinigt und mittels SDS-PAGE ausgewertet. Die Antikörper wurden auch mit der Verbindung der Firma A markiert, die in Dimethylsulfoxid (DMSO) rekonstituiert und in 2-, 5-, 7,5-, 10- und 15-fachem molarem Überschuss mit GAM oder GAR fünfundsechzig Minuten bei Raumtemperatur vereinigt wurde, um die Antikörper zu markieren.
-
Erfindungsgemäße und handelsübliche Verbindungen, jeweils als NHS-Ester, wurden mit Ziege-Anti-Ratte (GARat)-Antikörper konjugiert. GARat wurde in einer Konzentration von 10 mg/ml in phosphatgepufferter Kochsalzlösung (PBS) mit 10% v/v mit 0,67 M Boratpuffer gespiket. Die Verbindungen wurden 65 Minuten bei Raumtemperatur in 5- oder 10-fachem molarem Überschuss mit GARat vereinigt, um die Antikörper zu markieren. Die Antikörper wurden, wie oben beschrieben, markiert, gereinigt und mittels SDS-PAGE ausgewertet.
-
Die Markierungseffizienz von GARat war bei 679-Verbindung 1-NHS im Vergleich zu DyLight 680B-NHS, V08-15173-NHS und Verbindung der Firma B-NHS etwas höher.
-
Die Markierung von GAM mit den erfindungsgemäßen und den handelsüblichen Verbindungen in einer weiteren Versuchsreihe ist nachfolgend gezeigt.
| | Verhältnis Mol Farbstoff/Mol Protein @ 2,5X | Verhältnis Mol Farbstoff/Mol Protein @ 5X | Verhältnis Mol Farbstoff/Mol Protein @ 7,5X | Verhältnis Mol Farbstoff/Mol Protein @ 10X | Verhältnis Mol Farbstoff/Mol Protein @ 15X |
| V08-15173 | 2,5 | 4,9 | 7,1 | 8,9 | 12,4 |
| V10-04152 | 2,8 | 5,1 | 7,4 | 10,0 | 13,9 |
| DY679P1 | 1,8 | 4,1 | 6,6 | 8,5 | 12,9 |
| Verbindung der Firma A | 1,1 | 5,3 | 7,4 | 9,4 | 12,6 |
| Verbindung der Firma B | 1,8 | 4,0 | 6,3 | 8,3 | 13,1 |
-
Die Markierungseffizienz von GAM war bei allen Farbstoffen in allen molaren Überschüssen ähnlich.
-
Die Markierung von GAR mit den erfindungsgemäßen und handelsüblichen Verbindungen in einer weiteren Versuchsreihe in 5-, 15- und 25-fachem molarem Überschuss ist nachfolgend gezeigt.
| | Verhältnis Mol Farbstoff/Mol Protein @ 5X | Verhältnis Mol Farbstoff/Mol Protein @ 15X | Verhältnis Mol Farbstoff/Mol Protein @ 25X |
| V08-15173 | 4,6 | 12,7 | 19,6 |
| V10-04152 | 2,2 | 10,1 | 13,9 |
| DY679P1 | 4,8 | 10,6 | 14,4 |
| Verbindung der Firma A | 3,4 | 9,8 | 15,4 |
| Verbindung der Firma B | 4,1 | 15,2* | 46,7* |
-
Bei 5X war die Markierungseffizienz von GAR bei allen Farbstoffen, bis auf V10-04152, gleich. Bei 15X und 25X war die Markierungseffizienz mit Ausnahme der Verbindung der Firma B gleich. *Konjugate der Verbindung der Firma B präzipitierten im Slide-A-Lyzer bei molaren Überschüssen größer 10X, was darauf hindeutet, dass dieses Reinigungsverfahren nicht für Farbstoffe der Firma B geeignet war.
-
BEISPIEL 8
-
Die Leistungsfähigkeit der Farbstoff-GAM-Konjugate, Farbstoff-GAR-Konjugate und Farbstoff-SA-Konjugate wurde in einem Funktionsassay evaluiert. Vertiefungen einer weißen, opaken Platte oder einer schwarzen Platte mit klarem Boden, jeweils mit 96 Vertiefungen, wurden mit den Zielproteinen Maus-IgG-Immunglobulin, Kaninchen-IgG-Immunglobulin oder mit biotinyliertem Rinderserumalbumin (BBSA) beschichtet. Einhundert μl Maus- oder Kaninchen-IgG oder BBSA in einer Konzentration von 10 μg/ml wurden in die entsprechenden Vertiefungen in den Spalten 1 und 2 appliziert. Die Zielproteine wurden von den Vertiefungen in den Spalten 2 bis 11 mit 100 μl PBS im Verhältnis 1:1 in Reihe verdünnt. Einhundert μl der Proben aus den Vertiefungen in Spalte 11 wurden verworfen. Einhundert μl PBS wurden in die Vertiefungen der Spalte 12 gegeben. Die Platten wurden über Nacht bei 4°C inkubiert und dann 2 × 200 μl mit Thermo Scientific SuperBlock®-Blockierpuffer blockiert. Die beschichteten Platten wurden mit 2 × 200 μl PBS-Tween und mit 1 × 200 μl PBS gewaschen. Ausgehend von den berechneten Konzentrationen, wurden die Konjugate 1:250 in PBS verdünnt, zu den entsprechenden Platten gegeben (100 μl/Vertiefung) und dann eine Stunde im Dunkeln inkubiert. Die Platten wurden mit 2 × 200 μl PBS-Tween und mit 1 × 200 μl PBS gewaschen und mit PBS-Puffer (100 μl/Vertiefung) gefüllt, bevor die weißen, opaken Platten auf Tecan Safire bei 679 nmAnregung/702 nmEmission oder die schwarzen Platten mit klarem Boden auf LiCor Odyssey im 700 nm-Kanal gescannt wurden, um die Fluoreszenzintensität zu bestimmen.
-
Wie in den 2–7 gezeigt, wurden RFU und/oder das Signal-Hintergrund-Verhältnis (S/B) der Farbstoffe bei verschiedenen Konzentrationen verglichen, wobei die angegebenen Konjugationsbedingungen zum Einsatz kamen.
-
2 zeigt Tecan Safire-Ergebnisse eines Funktionsassays unter Verwendung von GAM, das entweder mit einem 8-fachen molaren Überschuss (durchgezogene Linien) oder mit einem 10-fachen molaren Überschuss (gestrichelte Linien) der Farbstoffe DyLight 680 (lila ausgefüllte Raute/offenes Quadrat), DyLight 680B (blau ausgefülltes Dreieck/X), 679-Verbindung 1 (rot ausgefüllter Kreis/Sternchen) und einer Verbindung der Firma B (schwarz ausgefülltes Quadrat/+-Zeichen) konjugiert war. DyLight 680B-GAM (8X) zeigte eine höhere Bindungsfluoreszenz als das entsprechende 679-Verbindung 1-GAM-Konjugat (8X). Bei 10-fachem molarem Überschuss zeigte 679-Verbindung 1-GAM ähnliche Eigenschaften wie DyLight 680B-GAM. Sowohl DyLight 680 als auch die Verbindung der Firma B zeigten im Vergleich zu DyLight 680B und den 679-Verbindung 1-Konjugaten eine deutlich niedrigere Intensität. Das Signal/Hintergrund-Verhältnis (S/B) war für DyLight 680B-GAM-Konjugate höher als für 679-Verbindung 1-GAM-Konjugate. Ähnliche Ergebnisse wurden allgemein bei GAR-Konjugaten erhalten.
-
3 zeigt Tecan Safire-Ergebnisse eines Funktionsassays unter Verwendung von SA, konjugiert mit einem 6-fachen molaren Überschuss (durchgezogene Linien) oder einem 8-fachen molaren Überschuss (gestrichelte Linien) der Farbstoffe DyLight 680 (lila ausgefüllte Raute/offenes Quadrat), DyLight 680B (blau ausgefülltes Dreieck/X), 679-Verbindung 1 (rot ausgefüllter Kreis/Sternchen) und Verbindung der Firma B (schwarz ausgefülltes Quadrat/+-Zeichen). 679-Verbindung 1-SA (6X, 8X) zeigte eine etwas niedrigere Bindungsfluoreszenz als das entsprechende DyLight 680B-SA-Konjugat (6X, 8X). Es gab keine Quenching-Neigung bei den Konjugaten mit höherem molarem Überschuss. Das S/B-Verhältnis war bei 679-Verbindung 1-SA-Konjugaten etwas kleiner als bei DyLight 680B-SA-Konjugaten.
-
4 zeigt LiCor Odyssey-Ergebnisse eines Funktionsassays unter Verwendung von GAM, konjugiert mit einem 2-fachen molaren Überschuss (durchgezogene Linien) oder einem 4-fachen molaren Überschuss (gestrichelte Linien) der Farbstoffe DyLight 680 (lila Raute), DyLight 6808 (blaues Dreieck), 679-Verbindung 1 (roter Kreis) und Cy5.5 (schwarzes Sternchen). Die folgende Tabelle zeigt einen Vergleich zwischen S/B und Rohintensitätsdaten.
| S/B | @ 1250 ng Beschichtung | @ 39 ng Beschichtung | @ 0 (Blank) |
| DyLight 680-GAM-2X | 25,3 | 9,8 | 1,0 |
| DyLight 680-GAM-4X | 6,4 | 2,3 | 1,0 |
| DyLight 680B-GAM-2X | 18,2 | 4,6 | 1,0 |
| DyLight 680B-GAM-4X | 31,9 | 8,1 | 1,0 |
| 679-Verbindung 1-GAM-2X | 36,1 | 7,9 | 1,0 |
| 679-Verbindung 1-GAM-4X | 65,2 | 15,9 | 1,0 |
| Cy5.5-GAM-2X | 62,3 | 17,7 | 1,0 |
| Cy5.5-GAM-4X | 19,6 | 6,1 | 1,0 |
| Rohintensität | @ 1250 ng Beschichtung | @ 39 ng Beschichtung | @ 0 (Blank) |
| DyLight 680-GAM-2X | 1941300 | 751514 | 76795 |
| DyLight 680-GAM-4X | 2596363 | 937396 | 403405 |
| DyLight 680B-GAM-2X | 5179777 | 1311798 | 284501 |
| DyLight 680B-GAM-4X | 8614438 | 2190343 | 270357 |
| DY679P1-GAM-2X | 5180336 | 1135001 | 143352 |
| DY679P1-GAM-4X | 7482510 | 1820225 | 114807 |
| Cy5.5-GAM-2X | 3957169 | 1124788 | 63513 |
| Cy5.5-GAM-4X | 4379901 | 1358039 | 223585 |
-
5 zeigt LiCor Odyssey-Ergebnisse eines Funktionsassays unter Verwendung von GAR, konjugiert mit einem 2-fachen molaren Überschuss (durchgezogene Linien) oder einem 4-fachen molaren Überschuss (gestrichelte Linien) der Farbstoffe DyLight 680 (lila Raute), DyLight 6808 (blaues Dreieck), 679-Verbindung 1 (roter Kreis) und Cy5.5 (schwarzes Sternchen). Die folgende Tabelle zeigt einen Vergleich zwischen S/B und Rohintensitätsdaten.
| S/B | @ 1250 ng Beschichtung | @ 39 ng Beschichtung | @ 0 (Blank) |
| DyLight 680-GAR-2X | 66,7 | 19,8 | 1,0 |
| DyLight 680-GAR-4X | 62,2 | 17,4 | 1,0 |
| DyLight 680B-GAR-2X | 210,6 | 47,5 | 1,0 |
| DyLight 680B-GAR-4X | 167,2 | 39,3 | 1,0 |
| DY679P1-GAR-2X | 184,0 | 39,2 | 1,0 |
| DY679P1-GAR-4X | 141,9 | 33,4 | 1,0 |
| Cy5.5-GAR-2X | 57,3 | 16,1 | 1,0 |
| Cy5.5-GAR-4X | 26,7 | 9,0 | 1,0 |
| Rohintensität | @ 1250 ng Beschichtung | @ 39 ng Beschichtung | @ 0 (Blank) |
| DyLight 680-GAR-2X | 1868227 | 554324 | 28015 |
| DyLight 680-GAR-4X | 2140077 | 597726 | 34391 |
| DyLight 680B-GAR-2X | 4178812 | 943008 | 19839 |
| DyLight 680B-GAR-4X | 6285439 | 1476347 | 37592 |
| DY679P1-GAR-2X | 4039443 | 860737 | 21950 |
| DY679P1-GAR-4X | 6527381 | 1537020 | 46001 |
| Cy5.5-GAR-2X | 2408459 | 675886 | 42049 |
| Cy5.5-GAR-4X | 2929556 | 988970 | 109613 |
-
6 zeigt LiCor Odyssey-Ergebnisse eines Funktionsassays unter Verwendung von GAM, konjugiert mit einem 8-fachen molaren Überschuss (durchgezogene Linien) oder einem 10-fachen molaren Überschuss (gestrichelte Linien) der Farbstoffe DyLight 680 (lila Raute), DyLight 6808 (blaues Quadrat), 679-Verbindung 1 (rotes Dreieck) und Verbindung der Firma B (schwarzes X). Die folgende Tabelle zeigt einen Vergleich der S/B-Daten.
| | 2500 ng Maus-IgG/ Vertiefung | 39,1 ng Maus-IgG/ Vertiefung |
| DyLight 680-GAM-8X | 173,6 | 48,9 |
| DyLight 680-GAM-10X | 137,2 | 37,6 |
| DyLight 680B-GAM-8X | 929,3 | 142,4 |
| DyLight 680B-GAM-10X | 914,5 | 165,6 |
| DY679P1-GAM-8X | 675,2 | 110,5 |
| DY679P1-GAM-10X | 871,5 | 183,5 |
| Verbindung der Firma B-GAM-8X | 459,9 | 112,4 |
| Verbindung der Firma B-GAM-10X | 374,0 | 96,1 |
-
679-Verbindung 1-GAM (10X) zeigte eine äquivalente gebundene Fluoreszenz im Vergleich zur entsprechenden DyLight 680B-GAM (10X). Das S/B-Verhältnis war bei 679-Verbindung 1-GAM (8X, 10X) niedriger als bei DyLight 680B-GAM (8X, 10X). Allgemein wurden für die GAR-Konjugate ähnliche Ergebnisse erhalten.
-
7 zeigt LiCor Odyssey-Ergebnisse eines Funktionsassays unter Verwendung von SA, konjugiert mit entweder einem 6-fachen molaren Überschuss (durchgezogene Linien) oder einem 8-fachen molaren Überschuss (gestrichelte Linien) der Farbstoffe DyLight 680 (lila Raute), DyLight 680B (blaues Quadrat), 679-Verbindung 1 (rotes Dreieck) und Verbindung der Firma B (schwarzes X). Die folgende Tabelle vergleicht die S/B-Daten:
| | 250 ng BBSA/ Vertiefung | 3,9 ng BBSA/ Vertiefung |
| DyLight 680-SA-6X | 614,5 | 33,1 |
| DyLight 680-SA-8X | 436,3 | 25,1 |
| DyLight 680B-SA-6X | 2196,7 | 43,8 |
| DyLight 680B-SA-8X | 1969,5 | 75,6 |
| DY679P1-SA-6X | 1742,1 | 58,5 |
| DY679P1-SA-8X | 1406,0 | 54,7 |
| Verbindung der Firma B-SA-6X | 570,2 | 49,7 |
| Verbindung der Firma B-SA-8X | 427,7 | 36,1 |
-
679-Verbindung 1-SA (6X, 8X) zeigte eine geringere gebundene Fluoreszenz und ein kleineres S/B-Verhältnis als das entsprechende DyLight 680B-SA (6X, 8X).
-
Die 679-Verbindung 1 und die Verbindung der Firma wurden mit GAR in hohen molaren Überschüssen konjugiert und in einem Funktionsassay, wie oben beschrieben, evaluiert. 8 zeigt die Ergebnisse, ausgedrückt als RFU eines Funktionsassays unter Verwendung von GAR, das mit 679-Verbindung 1 in 7,5-fachem molarem Überschuss (blaue Raute), 15-fachem molarem Überschuss (rotes Quadrat) oder 22,5-fachem molarem Überschuss (grünes Dreieck), und mit der Verbindung der Firma A in 7,5-fachem molarem Überschuss (lila X), 15-fachem molarem Überschuss (türkises Sternchen) oder 22,5-fachem molarem Überschuss (oranger Kreis) konjugiert war.
-
9 zeigt VarioSkan Flash-Ergebnisse mit Anregung und Emission bei 679 nm/702 nm, ausgedrückt als RFU eines Funktionsassays unter Verwendung von GAM, konjugiert mit einem 5-fachen molaren Überschuss der Verbindung der Firma B (orange Raute), von V08-15173 (blaues Dreieck) und von V10-04152 (roter Kreis). Den Daten zufolge zeigte V0815173-GAM (5X) eine höhere Bindungsfluoreszenz als Verbindung der Firma B-GAM (5X).
-
10 zeigt LiCOR Odyssey-Ergebnisse unter Verwendung des 700 nm-Kanals, ausgedrückt als Rohfluoreszenzintensität eines Funktionsassays unter Verwendung von GAM, konjugiert mit einem 5-fachen molaren Überschuss der 679-Verbindung 1/1 (grünes Dreieck), der Verbindung der Firma A (lila Kreis) und von V08-15173 (blaues Quadrat). 11 zeigt LiCOR Odyssey-Ergebnisse, ausgedrückt als S/B-Verhältnis eines Funktionsassays unter Verwendung von GAM, konjugiert mit 2,5-fachem, 5-fachem, 10-fachem oder 15-fachem molarem Überschuss der 679-Verbindung 1/1, der Verbindung der Firma A und von V08-15173. V08-15173-GAM (5X) zeigte eine ähnliche Bindungsfluoreszenz wie Verbindung der Firma A-GAM (5X). 679-Verbindung 1/1-GAM (5X)-Bindungsfluoreszenz war niedriger als die der anderen beiden Konjugate.
-
12 zeigt LiCOR Odyssey-Ergebnisse unter Verwendung des 700 nm-Kanals, ausgedrückt als Rohfluoreszenzintensität eines Funktionsassays unter Verwendung von GAR, konjugiert mit 5-fachem und 25-fachem molarem Überschuss der 679-Verbindung 1/1 (5X: grüne Raute, durchgezogene Linie; 25X: grüne Raute, gestrichelte Linie), der Verbindung der Firma A (5X: lila Dreieck, durchgezogene Linie; 25X: lila Dreieck, gestrichelte Linie), von V08-15173 (5X: hellblaues Quadrat, durchgezogene Linie; 25X: dunkelblaues Quadrat, gestrichelte Linie) und von V10-04152 (5X: gelber Kreis, durchgezogene Linie; 25X: roter Kreis, gestrichelte Linie).
-
13 zeigt LiCOR Odyssey-Ergebnisse, ausgedrückt als S/B-Verhältnis eines Funktionsassays unter Verwendung von GAR, konjugiert mit 5-fachem, 15-fachem oder 25-fachem molarem Überschuss der 679-Verbindung 1/1, der Verbindung der Firma A, von V08-15173 und von V1004152. Den Rohfluoreszenzintensitätsdaten zufolge gab es für V0815173-GAR in 25-fachem molarem Überschuss kein merkliches Quenching. Die 679-Verbindung 1/1, V10-04152 und die Verbindung der Firma A waren bei 25-fachem Überschuss sättigend. 14 zeigt zusammenfassende Rohfluoreszenzintensitätsdaten und ein merkliches Quenching bei 1000 ng/Vertiefung für einen 25-fachen Überschuss der 679-Verbindung 1/1 (679 1), von V10-04152 und der Verbindung der Firma A, aber kein merkliches Quenching bei einem 25-fachen Überschuss von V08-15173.
-
BEISPIEL 9
-
Die erfindungsgemäßen Verbindungen wurden hinsichtlich ihrer Immunfluoreszenz in zellbasierten Assays unter Anwendung des folgenden Protokolls evaluiert. Eingefrorene A549-Zellplatten, die bei –20°C gelagert worden waren, wurden 30 Min. bei 50°C gehalten. Der Lagerungspuffer (PBS) wurde entfernt, und die Zellen wurden 15 Min. (100 μl/Vertiefung) mit 0,1% Triton-X100 in 1X PBS-Puffer permeabilisiert. Die Platten wurden 30 Min. in 2% BSA in 1X PBS-0,1% Triton-X100 blockiert. Primäre Antikörper, verdünnt in 2% BSA in 1X PBS-0,1% Triton-X100, wurden zu den Platten gegeben (Spalte 1-11; Spalte 12 enthielt nur Blocker) und drei Stunden bei Raumtemperatur inkubiert. Maus-Anti-Lamin A wurde in einer Menge von 1 μg/ml zugegeben, und Kaninchen-Anti-Lamin B1 wurde in einer Menge von 3 μg/ml zugegeben. Nach Inkubation über Nacht wurde die Antikörperlösung aus den Platten entnommen und die Platten wurden mit PBS-0,5% Tween-20 (2x 100 μl/Vertiefung) gewaschen. Sekundäre GAM- und GAR-Antikörper, markiert mit DyLight 680-NHS, DyLight 680B-NHS, 679-Verbindung 1-NHS und Verbindung der Firma B-NHS, wurden auf 4 μg/ml in PBS verdünnt, zugegeben und eine Stunde bei Raumtemperatur inkubiert. Dann wurden die Platten dreimal mit 100 μl/Vertiefung PBS gewaschen, und Hoechst-Stain (Färbemittel), verdünnt bis 0,1 μg/ml in PBS, wurde in jede Vertiefung gegeben (100 μl/Vertiefung). Die Platten wurden auf einem ArrayScan Plate Reader zur Bildgebung und Quantifizierung gescannt.
-
15 zeigt Ergebnisse eines Immunfluoreszenzassays unter Verwendung von Maus-Anti-Lamin A als primärem Antikörper und von DyLight 680-GAM (15A), DyLight 680B-GAM (15B), 679-Verbindung 1-GAM (15C) oder Verbindung der Firma B-GAM (15D) als sekundärem Antikörper, wobei die Verbindung mit GAM (sekundärer Antikörper) in 4-fachem molarem Überschuss (Spalte 1), 6-fachem molarem Überschuss (Spalte 2), 8-fachem molarem Überschuss (Spalte 3), 10-fachem molarem Überschuss (Spalte 4) oder 12-fachem molarem Überschuss (Spalte 5) konjugiert wurde. Die mit GAM konjugierte 679-Verbindung 1 zeigte sehr ähnliche Eigenschaften wie die entsprechenden DyLight 680B-Konjugate.
-
Die Immunfluoreszenz der erfindungsgemäßen Verbindungen und handelsüblicher Farbstoffe wurde in einem zweiten zellbasierten Assay nach folgendem Protokoll evaluiert. Eingefrorene U2OS-Zellplatten, die bei –20°C gelagert worden waren, wurden über Nacht bei 4°C gehalten. Der Lagerungspuffer (PBS) wurde entfernt, und die Zellen wurden 15 Min. (100 μl/Vertiefung) mit 0,1% Triton-X100 in 1X PBS-Puffer permeabilisiert. Die Platten wurden 30 Min. in 2% BSA in 1X PBS-0,1% Triton-X100 blockiert. Primäre Antikörper, verdünnt in 2% BSA in 1X PBS-0,1% Triton-X100, wurden zu den Platten gegeben (Spalte 1-11; Spalte 12 enthielt nur Blocker) und fünf Stunden bei Raumtemperatur inkubiert. Maus-Anti-Lamin A wurde in einer Menge von 2 μg/ml zugegeben, und Kaninchen-Anti-Lamin B1 wurde in einer Menge von 4 μg/ml zugegeben. Nach der Inkubation wurde die Antikörperlösung von den Platten entfernt, und die Platten wurden mit PBS 0,5% Tween-20 (2x 100 μl/Vertiefung) gewaschen. Anschließend wurden sekundäre GAM- und GAR-Antikörper, markiert mit DyLight 680-NHS, DyLight 680B-NHS, 679-Verbindung 1-NHS und Cy5.5-Monoester, bis 4 μg/ml in PBS verdünnt und mit den Zellen eine Stunde bei Raumtemperatur inkubiert. GAM und GAR, konjugiert mit DyLight 680-NHS, DyLight 680B-NHS, 679-Verbindung 1-NHS und der Verbindung der Firma B in 10-fachem molarem Überschuss, wurden bis 4 μg/ml in PBS verdünnt und dann einer Reihenverdünnung im Verhältnis 1:1 in der Platte bis zu den folgenden Konzentrationen unterzogen: 2 μg/ml, 1 μg/ml, 0,5 μg/ml, 0,25 μg/ml, 0,125 μg/ml und/oder 0,0625 μg/ml. Die Platten wurden 3x mit 100 μl/Vertiefung PBS gewaschen, und Hoechst-Stain, verdünnt bis 0,1 μg/ml in PBS, wurde in jede Vertiefung (100 μl/Vertiefung) gegeben. Die Platten wurden auf einem ArrayScan Plate Reader zur Bildgebung und Quantifizierung gescannt.
-
16 zeigt Ergebnisse eines Immunfluoreszenzassays unter Verwendung von Maus-Anti-Lamin A als primärem Antikörper und von DyLight 680-GAM (
16A), DyLight 680B-GAM (
16B), 679-Verbindung 1-GAM (
16C) oder Cy5.5-GAM (
16D) als sekundärem Antikörper, wobei die Verbindung mit GAM (sekundärer Antikörper) in 2-fachem molarem Überschuss (Spalte 1), 3-fachem molarem Überschuss (Spalte 2) oder 4-fachem molarem Überschuss (Spalte 3) konjugiert war. Die Immunfluoreszenzeigenschaften des 679-Verbindung 1-Konjugates entsprachen den Eigenschaften der entsprechenden DyLight 680B-Konjugate. Eine quantitative Analyse der Daten aus
16, ausgedrückt als mittlere Gesamtintensität, bei der es sich um die durchschnittliche Gesamtintensität aller Pixel innerhalb eines definierten Bereiches oder eines definierten Primärobjekts, wie eines Nucleus, handelt, ist nachfolgend dargestellt.
| Mittlere Gesamtintensität |
| | 2X | 3X | 4X |
| DyLight 680 | 91899 | 122829 | 144792 |
| DyLight 680B | 150542 | 228678 | 305700 |
| DY679P1 | 232482 | 263580 | 330865 |
| Cy5.5 | 211945 | 342208 | 451111 |
-
Die Fluoreszenzsignalintensität der DyLight 680B- und 679-Verbindung 1-GAM-Konjugate war, abhängig vom molaren Überschuss, 2–4 Mal höher als bei DyLight 680- oder Cy5.5-GAM-Konjugaten, und die S/B-Verhältnisse der DyLight 680B- & 679-Verbindung 1-GAM-Konjugate bei niedrigen molaren Überschüssen waren miteinander und mit DyLight 680 vergleichbar. Die Gesamtfluoreszenzsignalintensität der DyLight 680B- und 679-Verbindung 1-GAR-Konjugate war etwa zweimal höher als die von DyLight 680. Die S/B-Verhältnisse von DyLight 680B- und 679-Verbindung 1-GAR, markiert mit 2-, 3- oder 4-fachem molarem Überschuss, waren miteinander und mit DyLight 680-Konjugaten vergleichbar.
-
Bei den angegebenen Versuchen wurde die Immunfluoreszenz der erfindungsgemäßen Verbindungen in zellbasierten Assays gemäß folgendem Protokoll evaluiert. Eingefrorene A549-Zellplatten, die bei –20°C gelagert worden waren, wurden 30 Min. bei 50°C gehalten. Der Lagerungspuffer (PBS) wurde entfernt, und die Zellen wurden 15 Min. (100 μl/Vertiefung) mit 0,1% Triton-X100 in 1X PBS-Puffer permeabilisiert.
-
Die Platten wurden 30 Min. in 2% BSA in 1X PBS-0,1% Triton-X100 blockiert. Primäre Antikörper, verdünnt in 2% BSA in 1X PBS-0,1% Triton-X100, wurden zu den Platten gegeben (Spalte 1–11; Spalte 12 enthielt nur Blocker) und drei Stunden bei Raumtemperatur inkubiert. Maus-Anti-Lamin A wurde in einer Menge von 1 μg/ml zugegeben, und Kaninchen-Anti-Lamin B1 wurde in einer Menge von 3 μg/ml zugegeben. Nach Inkubation über Nacht wurde die Antikörperlösung aus den Platten entfernt, und die Platten wurden mit PBS-0,5% Tween-20 (2x 100 μl/Vertiefung) gewaschen. Sekundäre GAM- und GAR-Antikörper, markiert mit DyLight 680-NHS, DyLight 680B-NHS, 679-Verbindung 1-NHS und Verbindung der Firma B-NHS, wurden bis 4 μg/ml in PBS verdünnt, zugegeben und eine Stunde bei Raumtemperatur inkubiert. Dann wurden die Platten dreimal mit 100 μl/Vertiefung PBS gewaschen, und Hoechst-Stain, verdünnt bis 0,1 μg/ml in PBS, wurde in jede Vertiefung (100 μl/Vertiefung) gegeben. Die Platten wurden auf einem ArrayScan Plate Reader zur Bildgebung und Quantifizierung gescannt.
-
Bei den angegebenen Versuchen wurde die Immunfluoreszenz der erfindungsgemäßen Verbindungen und von handelsüblichem Farbstoff in einem zellbasierten Assay gemäß folgendem Protokoll evaluiert. Eingefrorene U2OS-Zellplatten, die bei –80°C gelagert worden waren, wurden 45 Minuten bei 50°C aufgetaut. Der Lagerungspuffer (PBS) wurde entfernt, und die Zellen wurden 15 Minuten mit 0,1% Triton-X100 in 1X PBS-Puffer (100 μl/Vertiefung) permeabilisiert. Dann wurde die Zellplatte 60 Minuten in 2% BSA/PBS-0,1% Triton-X100 blockiert. Primärer Antikörper, entweder Ratte-Anti-Grp94 (5 μg/ml), Maus-Anti-Lamin A (10 μg/ml), oder Kaninchen-Anti-lamin B1 (10 μg/ml), verdünnt in 2% BSA /PBS-0,1% Triton-X100, wurde zu der Platte gegeben und 1 Stunde bei Raumtemperatur inkubiert. Die Kontrollvertiefungen enthielten nur 2% BSA/PBS-0,1% Triton-X100-Blocker. Nach der Inkubation wurde die Antikörperlösung aus der Platte entfernt und die Platte dreimal mit 100 μl/Vertiefung PBS-0,5%Tween-20 und einmal mit 100 μl/Vertiefung PBS gewaschen. Sekundäre GARat-, GAM-, oder GAR-Antikörper, markiert mit verschiedenen molaren Überschussen der erfindungsgemäßen oder der handelsüblichen Verbindung, wurden bis 4 μg/ml in PBS verdünnt und 1 Stunde bei Raumtemperatur inkubiert. Die Platten wurden dreimal mit 100 μl/Vertiefung PEST und einmal mit 100 μl/Vertiefung PBS gewaschen, und Hoechst-Stain (verdünnt bis 0,1 μg/ml in PBS) wurde in jede Vertiefung (100 μl/Vertiefung) gegeben. Die Platten wurden auf einem ArrayScan Plate Reader oder ToxInsight Instrument gescannt.
-
17 zeigt die Detektion von Grp94 in U2OS-Zellen (Spalte 1) mit 679-Verbindung 1-GARat (17A), DyLight 680B-GARat (17B), V08-15173-GARat (17C) und Verbindung der Firma B-GARat (17D), konjugiert mit 5-fachem molarem Überschuss, und entsprechende Kontrollen (Spalte 2).
-
18 zeigt die Detektion von Grp94 in U2OS-Zellen (Spalte 1) mit 679-Verbindung 1-GARat (18A), DyLight 680B-GARat (18B), V08-15173-GARat (18C) und Verbindung der Firma B-GARat (18D), konjugiert mit 10-fachem molarem Überschuss, und entsprechende Kontrollen (Spalte 2).
-
Wie in 17–18 gezeigt, war bei V08-15173-GARat- und Verbindung B Verbindung-GARat-Konjugaten keine unspezifische Bindung zu beobachten, bei DY679P1- und DyLight 6808-GARat-Konjugaten jedoch sehr wohl.
-
Eine quantitative Analyse der Daten aus
17–
18, ausgedrückt als mittlere Gesamtintensität, bei der es sich um die durchschnittliche Gesamtintensität aller Pixel innerhalb eines definierten Bereichs oder eines definierten Primärobjektes, wie einem Nucleus, handelt, ist nachfolgend gezeigt.
| | | | Negative Kontrollen | | |
| | 5X | 10X | 5X | 10X | S/B (5X) | S/B (10X) |
| 679 Verbindung 1-GARat | 81221 | 97162 | 36744 | 70585 | 2,2 | 1,4 |
| DyLight 680B-GARat | 77855 | 91720 | 34773 | 61355 | 2,2 | 1,5 |
| V08-15173-GARat | 76825 | 70881 | 28190 | 26341 | 2,7 | 2,7 |
| Verbindung der Firma B-GARat | 64881 | 56119 | 26762 | 30379 | 2,4 | 1,8 |
-
Das S/B-Verhältnis der V08-15173-GARat-Konjugate (5X, 10X) war geringfügig besser als das der entsprechenden 679-Verbindung 1-GARat-, DyLight 680B-GARat- und Verbindung der Firma B-GARat-Konjugate.
-
Die Immunfluoreszenz von 679-Verbindung 1-GAM, Verbindung der Firma A-GAM und Verbindung der Firma A-R-GAM wurde in einem zellbasierten Assay mittels Detektion von PDI in Zellen mit einem Maus-Anti-PDI-Antikörper evaluiert. 19 zeigt Ergebnisse mit 679-Verbindung 1-GAM in 15-fachem molarem Überschuss (19A), Verbindung der Firma A-GAM in 15-fachem molarem Überschuss (19B), und Verbindung der Firma A R-GAM in 15-fachem molarem Überschuss (19C). Wie aus 19 ersichtlich ist, zeigte 679-Verbindung 1-GAM eine richtige Verfärbung von PDI im ER, während Verbindung der Firma A-GAM und Verbindung der Firma A R-GAM eine unspezifische Verfärbung mit in der gesamten Zelle festzustellender Verfärbung zeigte. Ähnliche Ergebnisse wurden für 679-Verbindung 1-GAM bei 7,5-fachem und 22,5-fachem molarem Überschuss, sowie Verbindung der Firma A-GAM und Verbindung der Firma A R-GAM in 7,5-fachem molarem Überschuss (Daten nicht gezeigt) erhalten.
-
20A–C zeigen die Detektion von Lamin A in U2OS-Zellen (Spalte 1) mit V08-15173-GAM-, V10-04152-GAM-, 679-Verbindung 1/1-GAM-, Verbindung der Firma A-GAM- und Verbindung der Firma B-GAM-Konjugaten (4 μg/ml) in 5-fachem molarem Überschuss (20A), 10-fachem molarem Überschuss (20B) und 15-fachem molarem Überschuss (20C), mit V08-15173-GAM (Reihe A, 20A, 20B, 20C), V10-04152-GAM (Reihe B, 20A, 20B, 20C), 679-Verbindung 1/1-GAM (Reihe C, 20A, 20B und 20C), Verbindung der Firma A-GAM (Reihe D, 20A, 20B, 20C), Verbindung der Firma B-GAM (Reihe E, 20A, 20B, 20C) und entsprechenden negativen Kontrollen (Spalte 2). Es war nur eine äußerst geringe unspezifische Bindung mit V08-15173-GAM und 679-Verbindung 1/1-GAM zu beobachten. Verbindung der Firma A-GAM- und Verbindung der Firma B-GAM-Konjugate zeigten eine hohe unspezifische Bindung ab 5-fachem molarem Überschuss. Bei niedrigem molarem Überschuss zeigte Verbindung der Firma A-GAM eine Verfärbung des Nucleus, die stärker war als bei den anderen Farbstoffen. V10-04152-GAM zeigte eine gute Spezifität, war aber nicht sehr hell. Die Verfärbung des Nucleus mit Verbindung der Firma B-GAM verbesserte sich bei 15-fachem molarem Überschuss deutlich, allerdings bei einer Zunahme der unspezifischen Bindung.
-
Die folgende Tabelle zeigt eine quantitative Analyse der Daten aus
20A–C, ausgedrückt als mittlere Gesamtintensität, bei der es sich um die durchschnittliche Gesamtintensität aller Pixel innerhalb eines definierten Bereichs oder eines definierten Primärobjektes, wie eines Nucleus, handelt und die S/B-Verhältnisse.
| Mittel | V08-15173 | V10-04152 | 679-Verbindung 1/1 | Verbindung der Firma A | Verbindung der Firma B |
| | Negative Kontrolle | | Negative Kontrolle | | Negative Kontrolle | | Negative Kontrolle | | Negative Kontrolle |
| 2,5X | 17366 | 5966 | 11946 | 6085 | 29229 | 5628 | 54496 | 9107 | 7092 | 6329 |
| 5,0X | 32820 | 6643 | 12788 | 7357 | 49279 | 5859 | 72289 | 20303 | 11922 | 8360 |
| 7,5X | 42876 | 7100 | 12513 | 6503 | 28782 | | 152502 | 51104 | 18894 | 13351 |
| 10X | 47756 | 9690 | 21147 | 6266 | 30098 | 6115 | 188505 | 136044 | 25020 | 18330 |
| 15X | 49060 | 10779 | 15942 | 6746 | 48071 | 7277 | 679693 | 665370 | 67705 | 24350 |
| S/B | | | | | |
| | V08-15173 | V10-04152 | 679-Verbindung 1/1P1 | Verbindung der Firma A | Verbindung der Firma B |
| 2,5X | 2,9 | 2,0 | 5,2 | 6,0 | 1,1 |
| 5,0X | 4,9 | 1,7 | 8,4 | 3,6 | 1,4 |
| 7,5X | 6,0 | 1,9 | 4,9 | 3,0 | 1,4 |
| 10X | 4,9 | 3,4 | 4,9 | 1,4 | 1,4 |
| 15X | 4,6 | 2,4 | 6,6 | 1,0 | 2,8 |
-
Lamin A, ein Kernprotein, sollte eine für den Nucleus spezifische Verfärbung zeigen. Jede Lamin A-Verfärbung außerhalb des Nucleus ist eine unspezifische Verfärbung. Zudem werden auch Negativkontrollbedingungen eingesetzt, bei denen ein primärer Antikörper fehlt, um die Antikörper-Verfärbungspezifität zu bestimmen. Die Verbindungen der Firma A und der Firma B zeigten keine unspezifische Bindung. V08-15173 und 679-Verbindung 1/1 zeigten einen minimalen Grad unspezifischer Bindung. Aufgrund der starken unspezifischen Bindung bei höheren molaren Überschüssen zeigten die Verbindungen der Firma A und der Firma B verringerte Signal/Hintergrund (S/B)-Pegel.
-
Die quantitative Analyse eines Wiederholungsversuchs der
20A–C ist nachfolgend gezeigt.
| Mittel | V08-15173 | Verbindung der Firma A | 679-Verbindung 1/1 |
| | Negative Kontrolle | | Negative Kontrolle | | Negative Kontrolle |
| 2,5X | 118440 | 12053 | 198471 | 24758 | 77195 | 8711 |
| 5X | 183078 | 9441 | 351666 | 84270 | 140772 | 8674 |
| 10X | 391473 | 13094 | 638569 | 330337 | 159948 | 20481 |
| 15X | 211270 | 17260 | 560119 | 632936 | 199626 | 16277 |
| S/B | | | |
| | V08-15173 | Verbindung der Firma A | 679-Verbindung 1/1 |
| 2,5X | 9,8 | 8,0 | 8,9 |
| 5X | 19,4 | 4,2 | 16,2 |
| 10X | 29,9 | 1,9 | 7,8 |
| 15X | 12,2 | 0,9 | 12,3 |
-
Die Verbindung der Firma A zeigte eine höhere unspezifische Bindung als V08-15173 und 679-Verbindung 1/1, wobei die unspezifische Bindung bei der 2,5 X-Bedingung für Verbindung der Firma A-GAM auftrat.
-
679-Verbindung 1/1-NHS und V08-15173-NHS zeigten eine im Durchschnitt 20% niedrigere Intensität als Verbindung der Firma A-NHS. Die V10-04152-Intensität war etwa 50% niedriger als die von V08-15173 und etwa 65% niedriger als die der Verbindung der Firma A. Die GAM-Markierungseffizienz war bei allen Farbstoffen in allen molaren Überschüssen gleich. Bei 5-fachem molarem Überschuss war die GAR-Markierungseffizienz aller Farbstoffe mit Ausnahme von V10-04152 gleich. Bei 15- und 25-fachem molarem Überschuss war die GAR-Markierungseffizienz bei allen Verbindungen mit Ausnahme der Verbindung der Firma B gleich. In Immunfluoreszenzstudien zeigten Verbindung der Firma A-, 679-Verbindung 1/1- und Verbindung der Firma B-GAM-Konjugate eine hohe unspezifische Bindung. V08-15173- und V10-04152-GAM-Konjugate zeigten eine geringe unspezifische Bindung. Die Immunfluoreszenzeigenschaften der Konjugate schienen stark von den Eigenschaften des primären Antikörpers abzuhängen.
-
BEISPIEL 10
-
Die erfindungsgemäßen Verbindungen werden für die in vivo-Bildgebung verwendet, um Informationen über die vorwiegend zugänglichen biologischen Gewebe zu erhalten. Die Verbindungen reagieren auf Licht im Nahinfrarotbereich des Spektrums, einem Teil des Spektrums, der einer minimalen Interferenz durch die Extinktion biologischer Materialien unterliegt. Gemäß einer Ausführungsform werden die Verbindungen zur Fluoreszenzbildgebung von Zielen in Tieren verwendet. Beispielsweise können in vivo-Bildgebungsinformationen mit Verfahren wie Röntgen, Magnetresonanzbildgebung, Positronemissionstomographie, Ultraschallbildgebung und -sondierung, und anderen nichtinvasiven Verfahren zur Diagnose und Behandlung von Erkrankungen gewonnen werden. Licht im Nahinfrarotbereich (NIR) mit einer Wellenlänge von etwa 650 nm bis etwa 1000 nm kann mehrere Zentimeter dickes Gewebe durchdringen und somit für die in vivo-Bildgebung verwendet werden. Fluoreszierende Farbstoffe, wie die erfindungsgemäßen Verbindungen, die auf Licht bei diesen längeren Wellenlängen ansprechen, können als Konjugate mit Targeting-Molekülen, wie Antikörpern, verwendet werden, um z. B. an erkranktes Gewebe, wie Tumore, zu binden und sich darin anzusammeln, und können dazu verwendet werden, gesundes von erkranktem Gewebe zu unterscheiden. Bei manchen Verfahren kann die erfindungsgemäße Verbindung an ein Biomolekül, wie ein Protein, ein Peptid oder einen Wirkstoff, gebunden sein, das/der in der gewünschten Gewebeumgebung lokalisiert oder zurückgehalten ist. Fluoreszierende NIR-Farbstoffe zur in vivo-Bildgebung, wie die erfindungsgemäßen Verbindungen, sind Diagnosemittel zum gezielten Targeting von erkranktem Gewebe direkt in Tieren oder Menschen.
-
Für die in-vivo-Bildgebung wird die Verbindung, ein Isomer der Verbindung oder ein Konjugat der Verbindung oder des Isomers mit einem Targetingmittel einem Gewebe (z. B. intravenös) verabreicht, mit vom Kreislaufsystem entfernter überschüssiger Verbindung akkumulieren gelassen, und dann das Gewebe mit Licht einer entsprechenden Wellenlänge bestrahlt. Das fluoreszierende NIR-Licht wird aufgezeichnet und/oder ein Bild wird aus den erhaltenen Daten erzeugt, um die angezielten Zellen oder Gewebe spezifisch zu detektieren und zu visualisieren. Die verabreichte Dosis der Verbindung kann unterschiedlich sein und wäre dem Fachmann bekannt, wobei sie von dem jeweiligen Gewebe, der Anwendung usw. abhängt, solange das Verfahren eine detektierbare Konzentration der Verbindung in dem zu beurteilenden Gewebe erreicht.
-
BEISPIEL 11
-
In vivo-Bildgebung mit einer erfindungsgemäßen Verbindung, konjugiert mit einem Anti-HER2-Antikörper
-
779-Verbindung 1-NHS wird mit einem Kaninchen-Anti-HER2-Antikörper (Genscript USA, Piscataway NJ) konjugiert, indem die Verbindung in Dimethylformamid (DMF) bei 10 mg/ml rekonstituiert und anschließend bei 10-fachem molarem Überschuss mit Kaninchen-Anti-HER2-Antikörper (0,1 mg) eine Stunde bei Raumtemperatur inkubiert wird, um ein 779 Verbindung 1-Anti-HER2-Konjugat zu ergeben. Die Konjugationsreaktion wird dann PDDR unterzogen, um unmarkierte (freie) 779-Verbindung 1 zu entfernen. Zehn Mikrogramm Konjugat werden athymischen Mäusen mit BT474-Tumoren intravenös injiziert. Die Tiere werden im Zeitverlauf 1, 24, 48, 72, 96 und 120 Stunden nach der Injektion auf einem Pearl Imager, LI-COR Biosciences (LI-COR Instruments, Lincoln NE) abgebildet.
-
Bei einer Ganzkörperabbildung ist zu beobachten, dass die Fluoreszenzintensität während der Bildgebung in der ersten Stunde über das gesamte Tier verteilt und nach 72 Stunden deutlich verringert ist. Nach 96 Stunden ist das Signal lokalisiert und spezifisch für den Tumor.
-
679-Verbindung 4/4-NHS wird mit einem Kaninchen-Anti-HER2-Antikörper (Genscript USA, Piscataway NJ) konjugiert, indem die Verbindung in Dimethylformamid (DMF) bei 10 mg/ml rekonstituiert und anschließend bei 10-fachem molarem Überschuss mit Kaninchen-Anti-HER2-Antikörper (0,1 mg) eine Stunde bei Raumtemperatur inkubiert wird, um ein 679-Verbindung 4/4-Anti-HER2-Konjugat zu ergeben. Die Konjugationsreaktion wird dann PDDR unterzogen, um unmarkierte (freie) 679-Verbindung 4/4 zu ergeben. Zehn Mikrogramm Konjugat werden athymischen Mäusen mit BT474-Tumoren intravenös injiziert. Die Tiere werden im Zeitverlauf 1, 24, 48, 72, 96 und 120 Stunden nach der Injektion auf einem Pearl Imager, LI-COR Biosciences (LI-COR Instruments, Lincoln NE) abgebildet.
-
Bei einer Ganzkörperabbildung ist zu beobachten, dass die Fluoreszenzintensität während der Bildgebung in der ersten Stunde über das gesamte Tier verteilt und nach 72 Stunden deutlich verringert ist. Nach 96 Stunden ist das Signal lokalisiert und spezifisch für den Tumor.
-
BEISPIEL 12
-
In vivo-Bildgebung mit monosulfonierter oder disulfonierter erfindungsgemäßer Verbindung
-
Die Verbindung kann weniger hydrophil, d. h. hydrophober, gemacht werden, indem die Anzahl der Sulfonatgruppen verändert wird. Je weniger Sulfonate, desto hydrophober wird die Verbindung. Bei dieser Ausführungsform kann die Verbindung einfacher in einem gewünschten Gewebe oder an einem gewünschten Ort gehalten werden, wenn die entsprechende Anzahl Sulfonate bestimmt wird; z. B. dringt die Verbindung effizienter in Zellen ein, wenn weniger Sulfonate auf dem Molekül vorhanden sind. Die Verbindung kann eine, zwei, drei oder vier Sulfonatgruppen enthalten. Hydrophobe Verbindungen passieren bekanntlich auch effizienter die Zellmembran und sind somit erwünschter, wenn das interessierende Ziel innerhalb der Zelle liegt.
-
Alendronat, eine Verbindung, die an LNCap-Prostatakrebszellen bindet und in diesen zurückgehalten wird, wird mit einer disulfonierten oder monosulfonierten Benzo-779-Verbindung 1 konjugiert, indem eine Lösung, enthaltend 1 mM disulfonierte oder monosulfonierte 779-Verbindung 1-NHS in 1 ml PBS und 0,5 ml Tetrahydrofuran (THF), mit 0,1 mM Alendronat und 0,2 mM Diisopropylethylamin über Nacht bei Raumtemperatur inkubiert wird. Das Konjugat wird mit Umkehrphasen-HPLC mit 0–50% Methanol gegen einen 0,1 M Ammoniumacetatpuffer gereinigt und dann lyophilisiert.
-
LNCap-Zellen werden orthotopisch in Nacktmäusen gezüchtet. 779-Verbindung 1-Alendronat (5 nmol) wird in den Tumor injiziert. Kontrollmäusen wird freie 779-Verbindung 1 injiziert, die einen Carbonsäurerest an Stelle des reaktiven NHS-Esters enthält. Es werden Röntgen- und Nahinfrarot-Fluoreszenzbilder aufgenommen.
-
Bei Bildgebung der gesamten Maus wird mehr 779-Verbindung 1-Alendroneat-Konjugat als unkonjugierte Verbindung im Mäusegewebe gehalten; das Konjugat wird in dem LNCap-Zellen-induzierten Tumor mindestens 18 Stunden zurückgehalten.
-
Alendronat, eine Verbindung, die an LNCap-Prostatakrebszellen bindet und in diesen zurückgehalten wird, wird mit einer disulfonierten oder monosulfonierten 679-Verbindung 4/4 durch Inkubation einer Lösung, enthaltend 1 mM disulfonierte oder monosulfonierte 679-Verbindung 4/4-NHS in 1 ml PBS und 0,5 ml Tetrahydrofuran (THF), mit 0,1 mM Alendronat und 0,2 mM Diisopropylethylamin über Nacht bei Raumtemperatur konjugiert. Das Konjugat wird mit Umkehrphasen-HPLC mit 0–50% Methanol gegen einen 0,1 M Ammoniumacetatpuffer gereinigt und dann lyophilisiert.
-
LNCap-Zellen werden orthotopisch in Nacktmäusen gezüchtet. 679-Verbindung 4/4-Alendronat (5 nmol) wird in den Tumor injiziert. Kontrollmäusen wird freie 679-Verbindung 4/4 injiziert, die einen Carbonsäurerest an Stelle des reaktiven NHS-Esters enthält. Es werden Röntgen- und Nahinfrarot-Fluoreszenzbilder aufgenommen.
-
Bei Bildgebung der gesamten Maus wird mehr 679-Verbindung 4/4-Alendroneat-Konjugat als unkonjugierte Verbindung im Mäusegewebe gehalten; das Konjugat wird in dem LNCap-Zelleninduzierten Tumor mindestens 18 Stunden zurückgehalten.
-
BEISPIEL 13
-
In vivo-Bildgebung mit monosulfonierter oder disulfonierter erfindungsgemäßer Verbindung
-
Ein Wirkstoffabgabe-Nanopartikelsystem, konjugiert mit disulfonierter oder monosulfonierter 779 Verbindung 1, wird wie folgt hergestellt: Eine Lösung, enthaltend 1 mM disulfonierte oder monosulfonierte 779 Verbindung 1-NHS in 1 ml PBS, wird über Nacht bei Raumtemperatur mit 0,1 mM eines Antitumorwirkstoffs, konjugiert mit Transferrin in Form eines Nanopartikels, inkubiert. Das resultierende 779-Verbindung 1-Nanopartikel-Konjugat wird durch Zentrifugation gereinigt und dann lyophilisiert.
-
Das 779-Verbindung 1 (Isomer 1)-Nanopartikel-Konjugat (1 nmol) wird intravenös in eine Maus-Schwanzvene injiziert. Kontrollmäusen wird freier 779-Verbindung 1-Farbstoff injiziert. Es werden Röntgen- und Nahinfrarot-Fluoreszenzbilder des Mäusegehirns aufgenommen.
-
Das 779-Verbindung 1-Nanopartikel-Konjugat lokalisiert sich im Mäusegehirn mehr als etwa 24 Stunden nach der Injektion. Die Tumorgröße verringert sich fortschreitend nach Injektion des 779-Verbindung 1-Nanopartikel-Konjugats, verglichen mit 779-Verbindung 1-Nanopartikel ohne den Antitumorwirkstoff.
-
Ein Wirkstoffabgabe-Nanopartikelsystem, konjugiert mit disulfonierter oder monosulfonierter 679-Verbindung 4/4, wird wie folgt hergestellt: Eine Lösung, enthaltend 1 mM disulfonierte oder monosulfonierte 679-Verbindung 4/4-NHS in 1 ml PBS, wird über Nacht bei Raumtemperatur mit 0,1 mM eines Antitumorwirkstoffs, konjugiert mit Transferrin in Form eines Nanopartikels, inkubiert. Das resultierende 679-Verbindung 4/4-Nanopartikel-Konjugat wird durch Zentrifugation gereinigt und dann lyophilisiert.
-
Das 679-Verbindung 4/4 (Isomer 1)-Nanopartikel-Konjugat (1 nmol) wird intravenös in eine Maus-Schwanzvene injiziert. Kontrollmäusen wird freier 679-Verbindung 4/4 Farbstoff injiziert. Es werden Röntgen- und Nahinfrarot-Fluoreszenzbilder des Mäusegehirns aufgenommen.
-
Das 679-Verbindung 4/4-Nanopartikel-Konjugat lokalisiert sich im Mäusegehirn mehr als etwa 24 Stunden nach der Injektion. Die Tumorgröße verringert sich fortschreitend nach Injektion des 679-Verbindung 4/4-Nanopartikel-Konjugats, verglichen mit 679-Verbindung 4/4-Nanopartikel ohne den Antitumorwirkstoff.
-
BEISPIEL 14
-
Das monosulfonierte Derivat befindet sich an einer beliebigen von acht möglichen Positionen der 579-, 679- oder 779-Verbindung, was die Stereochemie um die Kohlenstoffpositionen an den Ringen sowie die Asymmetrie der beiden Enden jedes Farbstoffs bedingt. Entsprechend können sich die di- und trisubstituierten Sulfonate an mehreren möglichen Positionen der erfindungsgemäßen Verbindungen befinden.
-
BEISPIEL 15
-
Die erfindungsgemäßen Verbindungen werden zur in vivo-Bildgebung, wie in J. Gastrointest Surg (2008) 12: 1938–1950 beschrieben, verwendet. Dabei werden, kurz gesagt, menschliche Bauchspeicheldrüsen-Zelllinien in Medien, die mit Penicillin/Streptomycin ergänzt sind, bei 37°C mit 5% CO2 gehalten. Maus-Anti-CEA-Antikörper und Kontroll-Maus-IgG (in PBS mit 0,20% Natriumazid) werden mit V08-15173 konjugiert. Der Farbstoff wird bei 10 mg/ml in DMF rekonstituiert und dann zu dem Antikörper in 10-fachem molarem Überschuss gegeben. Die Reaktion wird eine Stunde bei Raumtemperatur durchgeführt. Die Proben werden dann gegen 3 X 2 L PBS dialysiert. Die Zelllinien werden in Platten mit 96 Vertiefungen bei 5 × 104 Zellen pro Vertiefung ausplattiert. Nach 48 Stunden Kultivierung in geeigneten Medien werden die Zellen mit 1 μg V08-15173-markiertem Anti-CEA-Antikörper oder V08-15173-markiertem Kontroll-Maus-IgG vier Stunden bei 37°C inkubiert. Dann werden die Zellen dreimal mit PBS gewaschen und anschließend mit einem invertierten Nikon De-485-Mikroskop und einer Spot-Kamera RD abgebildet.
-
Chirurgische Eingriffe und intravitale Bildgebung werden mit den Tieren durchgeführt, die durch intramuskuläre Injektion von 0,02 ml 50% Ketamin, 38% Xylazin und 12 Acepromazinmaleat anästhesiert wurden. Menschliche Bauchspeicheldrüsen- und Kolorektal-Krebszelllinien werden durch Trypsinierung geerntet und zweimal mit serumfreiem Medium gewaschen. Die Zellen (1 × 106 in 100 μl serumfreiem Medium) werden innerhalb von 30 Minuten nach der Ernte über die rechte Flanke subkutan in weibliche nu/nu-Mäuse im Alter von 4–6 Wochen injiziert. Subkutane Tumore werden vor der Verabreichung von konjugiertem Antikörper 7–14 Tage wachsen gelassen, bis sie einen Durchmesser von 1–2 mm erreichen. Bei ASPC-1-Implantaten werden die Zellen durch Trypsinierung geerntet und 3X in serumfreiem Medium gewaschen. Die Zellen werden in serumfreiem Medium resuspendiert. Die Zellen werden in serumfreiem Medium in einer Menge von 5 × 106/ml resuspendiert. Dann wird innerhalb von 30 Minuten nach der Ernte ein Volumen von 200 μl der Zellsuspension direkt in die Peritonealhöhle injiziert.
-
Zur Antikörperabgabe wird den Tieren ein bis zwei Wochen nach subkutaner, orthotopischer oder intraperitonealer Tumorimplantation eine intravenöse (i. v.) Injektion von konjugiertem Anti-CEA- oder konjugiertem Kontroll-IgG-Antikörper, verdünnt in PBS bis zu einem Endvolumen von 100 μl, verabreicht. Alle i. v. Injektionen erfolgen über die Schwanzvene. Für den Dosisreaktionsversuch beträgt die Antikörperdosis 75 μg. Für den in vivo-Zeitverlauf werden die Tiere anästhesiert und 30 Min., 1, 2, 6, 24 Stunden sowie 8 und 15 Tage nach der systemischen Antikörperverabreichung abgebildet.
-
Den vorhergesagten in vivo- und ex vivo-Analyseergebnissen zufolge zeigt die postexperimentale chirurgische Freilegung eine Akkumulierung von Farbstoff in Leber und Blase und einen entzündeten Bereich im subkutanen Gewebe. Eine ex vivo-Analyse der Vitalorgane bestätigt das Vorliegen von Farbstoff vorwiegend in der Leber, wobei Signale zum Teil auch in Milz, Darm und Lungen detektiert wurden.
-
BEISPIEL 16
-
Die erfindungsgemäßen Verbindungen werden zur in vivo-Bildgebung, wie in J. Gastrointest Surg (2008) 12: 1938–1950 beschrieben, verwendet. Dabei werden, kurz gesagt, menschliche Bauchspeicheldrüsen-Zelllinien in Medien, die mit Penicillin/Streptomycin ergänzt sind, bei 37°C mit 5% CO2 gehalten. Maus-Anti-CEA-Antikörper und Kontroll-Maus-IgG (in PBS mit 0,20% Natriumazid) werden mit 779-Verbindung 1 konjugiert. Der Farbstoff wird bei 10 mg/ml in DMF rekonstituiert und dann zu dem Antikörper in 10-fachem molarem Überschuss gegeben. Die Reaktion wird eine Stunde bei Raumtemperatur durchgeführt. Die Proben werden dann gegen 3 X 2 L PBS dialysiert. Die Zelllinien werden in Platten mit 96 Vertiefungen bei 5 × 104 Zellen pro Vertiefung ausplattiert. Nach 48 Stunden Kultivierung in geeigneten Medien werden die Zellen mit 1 μg V08-15173-markiertem Anti-CEA-Antikörper oder V08-15173-markiertem Kontroll-Maus-IgG vier Stunden bei 37°C inkubiert. Dann werden die Zellen dreimal mit PBS gewaschen und anschließend mit einem invertierten Nikon De-485-Mikroskop und einer Spot-Kamera RD abgebildet.
-
Chirurgische Eingriffe und intravitale Bildgebung werden mit den Tieren durchgeführt, die durch intramuskuläre Injektion von 0,02 ml 50% Ketamin, 38% Xylazin und 12 Acepromazinmaleat anästhesiert wurden. Menschliche Bauchspeicheldrüsen- und Kolorektal-Krebszelllinien werden durch Trypsinierung geerntet und zweimal mit serumfreiem Medium gewaschen. Die Zellen (1 × 106 in 100 μl serumfreiem Medium) werden innerhalb von 30 Minuten nach der Ernte über die rechte Flanke subkutan in weibliche nu/nu-Mäuse im Alter von 4–6 Wochen injiziert. Subkutane Tumore werden vor der Verabreichung von konjugiertem Antikörper 7–14 Tage wachsen gelassen, bis sie einen Durchmesser von 1–2 mm erreichen. Bei ASPC-1-Implantaten werden die Zellen durch Trypsinierung geerntet und 3X in serumfreiem Medium gewaschen. Die Zellen werden in serumfreiem Medium resuspendiert. Die Zellen werden in serumfreiem Medium in einer Menge von 5 × 106/ml resuspendiert. Dann wird innerhalb von 30 Minuten nach der Ernte ein Volumen von 200 μl der Zellsuspension direkt in die Peritonealhöhle injiziert.
-
Zur Antikörperabgabe wird den Tieren ein bis zwei Wochen nach subkutaner, orthotopischer oder intraperitonealer Tumorimplantation eine intravenöse (i. v.) Injektion von konjugiertem Anti-CEA- oder konjugiertem Kontroll-IgG-Antikörper, verdünnt in PBS bis zu einem Endvolumen von 100 μl, verabreicht. Alle i. v. Injektionen erfolgen über die Schwanzvene. Für den Dosisreaktionsversuch beträgt die Antikörperdosis 75 μg. Für den in vivo-Zeitverlauf werden die Tiere anästhesiert und 30 Min., 1, 2, 6, 24 Stunden sowie 8 und 15 Tage nach der systemischen Antikörperverabreichung abgebildet.
-
Den vorhergesagten in vivo- und ex vivo-Analyseergebnissen zufolge zeigt die postexperimentale chirurgische Freilegung eine Akkumulierung von Farbstoff in Leber und Blase und einen entzündeten Bereich im subkutanen Gewebe. Eine ex vivo-Analyse der Vitalorgane bestätigt das Vorliegen von Farbstoff vorwiegend in der Leber, wobei Signale zum Teil auch in Milz, Darm und Lungen detektiert wurden.
-
Die in der Beschreibung gezeigten und beschriebenen Ausführungsformen sind lediglich spezifische Ausführungsformen von Erfindern mit dem entsprechenden Fachwissen und sollen die Erfindung in keiner Weise einschränken. Daher sind verschiedene Änderungen, Modifikationen oder Abwandlungen dieser Ausführungsformen möglich, ohne vom Gedanken der Erfindung oder vom Umfang der nachfolgenden Ansprüche abzuweichen. Die zitierten Druckschriften sind hier ausdrücklich in vollem Umfang durch Bezugnahme mitaufgenommen.
-
ZITATE ENTHALTEN IN DER BESCHREIBUNG
-
Diese Liste der vom Anmelder aufgeführten Dokumente wurde automatisiert erzeugt und ist ausschließlich zur besseren Information des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt keinerlei Haftung für etwaige Fehler oder Auslassungen.
-
Zitierte Patentliteratur
-
- US 5846737 [0003]
- US 5627027 [0003, 0004, 0344]
- US 6083485 [0004]
- US 6977305 [0004, 0346]
- US 6974873 [0004, 0346]
- WO 05/044923 [0004]
- US 1524791 [0343]
- US 6048982 [0344]
- US 4981977 [0344]
- US 2006/0199949 [0344]
- US 5268486 [0345]
- US 5486616 [0345]
- US 5569587 [0345]
- US 5569766 [0345]
- JP 03217837 [0345]
- JP 05-313304 [0346, 0347]
- US 2006/0099638 [0346]
- US 2006/0004188 [0346]
- US 2002/0077487 [0346]
- US 2002/0064794 [0346]
- WO 2005/044923 [0347]
- WO 2007/0203343 [0347]
- EP 1792949 [0348]
- US 7745640 [0348]
- US 6939532 [0349]
- US 2009/0305410 [0350]
- US 7172907 [0351]
-
Zitierte Nicht-Patentliteratur
-
- Southwick, Anal. Chem. 67 (1995) 1742–48) [0344]
- Strekowski in: Heterocyclic Polymethine Dyes: Synthesis, Properties and Applications, (2008) Springer-Verlag, Berlin Heidelberg [0351]
- Gragg in: Synthesis of Near-Infrared Heptamethine Cyanine Dyes (2010) [0351]
- Chemistry Theses. Paper 28, Patonay et al. (2004) in: Noncovalent Labeling of Biomolecules with Red and Near-Infrared Dyes. Molcules 9 (2004) 40–49 [0351]
- Wilchek, M. und Miron, T. (1985) (Activation of Sepharose with N,N'-disuccinimidyl carbonate. Applied Biochemistry und Biotechnology 11, 191–193) [0357]
- Hermanson, Bioconjugate Techniques, 2nd Ed., London, Elsevier Inc. 2008 [0361]
- J. Gastrointest Surg (2008) 12: 1938–1950 [0460]
- J. Gastrointest Surg (2008) 12: 1938–1950 [0464]