-
Gebiet der Erfindung
-
Diese
Erfindung betrifft im Allgemeinen ein verbessertes Verfahren von
Diaminopyridinen. Insbesondere stellt die vorliegende Erfindung
ein verbessertes und kostengünstiges Verfahren für
die industrielle Massenproduktion von 2,3-Diaminopyridin, seinen
Derivaten oder eines Salzes desselben mit hoher Reinheit bereit.
-
Hintergrund der Erfindung
-
Diaminopyridin-Verbindungen
sind als Zwischenprodukte für die Herstellung einer Vielzahl
von pharmazeutisch wichtigen Verbindungen, wie 2,3-Diamino-5-methylpyridin
nützlich, welches in der Herstellung von Imidazo[1-2a]-Pyridinverbindungen
verwendet, als ein Arzneimittel für ein Geschwür
verwendet wird. Ferner wird 2,3-Diaminopyridin bei der Herstellung
von Imidazol[4-5b]-Pyridin inotropen Agenzien verwendet. Diese sind
ebenso als Zwischenprodukte für die Synthese von Cephem-antibaktiellen
Substanzen mit einem Imidazo[-4-5b]-Pyridiniummethyl-Substituenten
und ebenso als Ligand in organometallischen Komplexen nützlich.
Daher werden, um die ständig ansteigende Nachfrage nach dieser
Verbindung zu befriedigen, verschiedene Verfahren im Stand der Technik
für die Herstellung von 2,3-Diamonopyridin und seinen Derivaten
berichtet.
-
JP5339236 offenbart ein
Verfahren zum Herstellen von 2,3-Diaminopyridin, welches die Dehalogenierung
und Reduktion von 2-Amino-3-nitro-5-halopyridinen mit Wasserstoffgas
in Alkohol oder Wasser in Gegenwart eines Palladium-Katalysators
einschließt und ferner Mischen mit einer ausgewählten anorganischen
Säure und das Isolieren als Säuresalze.
-
Leese
and Rydon haben in J. Chem. Soc., 1954, 4039, über
die Herstellung von 2,3-Diaminopyridin berichtet, die die katalytische
Reduktion von 2-Amino-3-nitro-5-brompyridin mit Pd-SrCO3 und
die Extraktion mit Ether umfasst.
-
Verschiedene
Dokumente des Standes der Technik offenbaren ein Verfahren zum Herstellen
von 2,3-Diaminopyridinen mittels Hydrierung von 2-Amino-3-nitropyridinen.
JP-2003012647 offenbart
ein Verfahren zum Herstellen von 2,3-Diaminopyridin durch Hydrierung
von 3-Amino-2-nitropyridin in Gegenwart eines Pd-C-Katalysators.
-
EP 159112 offenbart ein Verfahren
zum Herstellen von Diaminopyridinen durch Hydrieren eines Hydrazinnitropyridins
mit einem Raney-Nickelkatalysator. Das Hydrazinnitropyridin wiederum
wird durch Hydrazinieren von 2-Chlor-3-nitropyridinen mit Hydrazin
hergestellt.
-
EP 156495 offenbart das gleichzeitige
Hydrieren und die Hydrogenolyse eines entsprechenden (Benzylamino)-Nitropyridins
in Gegenwart eines Pd-Katalysators und eines Lösungsmittels.
-
Das
deutsche Patent
DE 667219 offenbart ein
Verfahren zum Herstellen von Pyridinderivaten, in dem 2-Chlor-3-amino
(oder alkylamino)-Pyridin mit NH
3 oder einem
primären aliphatischen oder aromatischen Amin in Gegenwart
oder Abwesenheit eines Katalysators, zum Beispiel CuSO
4 und
(oder) einem säurebindenden Mittel zum Erhalt eines entsprechenden
Diaminopyridinderivats erwärmt wird.
-
Schickh
et al. in Ber. Dtsch. Chem. Ges., 1936, 69B, 2593–605,
haben über die Herstellung verschiedener 3-Aminopyridinderivate
berichtet. Die Forschungsarbeit offenbart ein Verfahren zum Herstellen
von 2,3-Diamino- oder 2-Alkylamino-3-aminopyridin durch Behandeln
von 2-Chlor-3-Aminopyridin mit Ammoniak oder einem entsprechenden
Alkylamin in Gegenwart von Kupfersalz. Das Produkt wurde mit Ether
in einer Soxhlet-Vorrichtung extrahiert und mit Benzol rekristallisiert.
2-Chlor-3-aminopyridin wird erhalten, wenn 3-Aminopyridin mit naszierendem
Chlor zusammen mit kleinen Mengen von 2,6-Dichlorpyridin und 2,4,5,6-Tetrachlorpyridin
behandelt wird.
-
Die
PCT-Anmeldung, veröffentlicht als
WO 2004069802 , berichtet über
ein dreistufiges Verfahren zum Herstellen einer 2-Amino-3-substituierten Pyridinverbindung
der Formel (IV). Das Verfahren schließt das Umsetzen einer
3-substituierten-2-Halo-genpyridin-Verbindung der Formel (III)
(R = Elektronendonor-Substituent
mit der Eigenschaft, an den Katalysator zu koordinieren; X = Halogen)
mit Ammoniak in der Gegenwart eines Kupferkatalysators ein, gefolgt
vom Entfernen des Kupfers aus der Reaktionsmischung durch Behandeln
mit einer Sulfidverbindung und das Herstellen des Salzes der Verbindung
IV aus der Kupfer ausschließenden Reaktionsflüssigkeit
und nachfolgendem Isolieren des 2-Amino-3-substituierten Pyridins
(IV) durch Behandeln mit einer Base.
-
JP 2005170848 offenbart
ein weiteres Verfahren für die Herstellung von 2,3-Diaminopyridin-Verbindungen
durch die Umsetzung von 3-Amino-2-haloyridin mit einem Benzylaminderivat
in Gegenwart einer Säure oder eines Kupferkatalysators, um
ein 3-Amino-2-(benzylamino)-Pyridinderivat zu ergeben, gefolgt von
der Hydrierung des 3-Amino-2-(benzylamino)-Pyridinderivats mit Wasserstoff in
Gegenwart eines Palladium-Katalysators.
-
Die
im Stand der Technik offenbarten Verfahren schließen die
Herstellung von unreinen Diaminopyridinderivaten ein, die einige
Schritte zum Extrahieren und Isolieren der gewünschten
Derivate erfordern. Ferner offenbart der Stand der Technik keine Reinigungstechnik,
um ein Produkt mit hoher Reinheit und Ausbeute zu erhalten. Darüber
hinaus schließen die im Stand der Technik erwähnten
Verfahren die Verwendung von gefährlichen und industriell
ungeeigneten Katalysatoren und Lösungsmitteln ein, wodurch
diese für die Massenproduktion unzugänglich werden.
-
Hinsichtlich
der obigen Nachteile in den Verfahren des Standes der Technik und
einer ansteigenden Nachfrage zum Herstellen von 2,3-Diaminopyridinen
besteht Bedarf, ein kommerziell und wirtschaftlich praktikables
Verfahren für die industrielle Massenproduktion von 2,3-Diaminopyridin
oder dessen Derivaten oder eines Salzes desselben mit hoher Reinheit
und Ausbeute zu entwickeln.
-
Daher
stellt die vorliegende Erfindung eine Lösung der vorher
genannten Probleme des Standes der Technik dar, indem ein verbessertes
Verfahren zum Herstellen von Diaminopyridin, dessen Derivaten oder
eines Salzes desselben eingesetzt wird.
-
Zusammenfassung der Erfindung
-
Ein
Hauptgegenstand der vorliegenden Erfindung ist ein Verfahren zum
Herstellen von 2,3-Diaminopyridin, dessen Derivaten oder eines Salzes desselben
bereitzustellen, wobei das Verfahren ermöglicht, hoch reines
2,3-Diaminopyridin, dessen Derivate oder ein Salz desselben in industriellem Maßstab
herzustellen.
-
Ein
weiterer Gegenstand der vorliegenden Erfindung ist ein Verfahren
zum Herstellen von 2,3-Diaminopyridin, dessen Derivaten oder eines Salzes
desselben bereitzustellen, wobei das Verfahren unter Einsetzen einer
minimalen Anzahl an Reaktionsschritten kommerziell anwendbar ist.
-
Ferner
ist Gegenstand der vorliegenden Erfindung ein Verfahren zum Herstellen
von 2,3-Aminopyridin, dessen Derivaten oder eines Salzes desselben
bereitzustellen, wobei das Verfahren einen einstufigen Extraktionsprozess
umfasst, in dem für die Umwelt nicht gefährliche
Lösungsmittel eingesetzt werden.
-
Die
obigen und weitere Gegenstände der vorliegenden Erfindung
werden ferner durch die hierin beschriebenen folgenden Ausführungsformen
erreicht und gestützt. Dennoch ist der Anwendungsbereich
der Erfindung nicht auf die nachfolgend beschriebenen Ausführungsformen
beschränkt.
-
In Übereinstimmung
mit einer Ausführungsform der vorliegenden Erfindung wird
ein verbessertes industrielles Verfahren zum Herstellen von 2,3-Diaminopyridin
der Formel (I), dessen Derivaten oder eines Salzes desselben bereitgestellt,
wobei das Verfahren das Aminieren von 3-Amino-2-halogenpyridin der
Formel (II), dessen Derivaten oder eines Salzes desselben mit wässrigem
Ammoniak in Gegenwart eines Cu-Katalysators und einem Ammoniakdruck von
1–5 kg/cm2 und Erwärmen
der Reaktionsmasse in einem Temperaturbereich von 100–150°C
und bei einem selbst erzeugten Druck von 18–25 kg/cm2, zum Bilden des Roh-2,3-Diaminopyridins
umfasst.
-
In Übereinstimmung
mit einer weiteren Ausführungsform der vorliegenden Erfindung
wird ein verbessertes industrielles Verfahren für die Massenproduktion
zum Herstellen von 2-3-Diaminopyridin der Formel (1), dessen Derivaten
oder eines Salzes desselben bereitgestellt, wobei das Verfahren
das Extrahieren des Roh-2,3-Diaminopyridins aus der Reaktionsmasse
in einem einzelnen Schritt unter Einsetzen eines für die
Umwelt nicht gefährlichen organischen Lösungsmittels,
zum Erhalt von 2,3-Diaminopyridin der Formel (1) mit hoher Reinheit,
umfasst.
-
In Übereinstimmung
mit noch einer weiteren Ausführungsform der vorliegenden
Erfindung wird ein Verfahren zum Herstellen von 2,3-Diaminopyridin der
Formel (I), dessen Derivaten oder eines Salzes desselben bereitgestellt,
wobei das Verfahren das Aminieren von 3-Amino-2-haloyridin der Formel
(II), dessen Derivaten oder eines Salzes desselben mit wässrigem
Ammoniak in Gegenwart eines Katalysators und einem Ammoniakdruck
von 1–5 kg/cm2, Erwärmen
der Reaktionsmasse in einem Temperaturbereich von 100–150°C
für 7–10 Stunden, zum Bilden des Roh-2,3-Diaminopyridins
und das Extrahieren des 2,3-Diaminopyridins aus der Reaktionsmasse
in einem einzelnen Schritt unter Einsetzen eines organischen Lösungsmittels,
zum Erhalt der reinen Form von 2,3-Diaminopyridin der Formel (I),
umfasst.
-
Detaillierte Beschreibung
der Erfindung
-
Während
diese Beschreibung mit den Ansprüchen endet, die insbesondere
hervorheben und deutlich das beanspruchen, was als Erfindung betrachtet
wird, wird erwartet, dass die Erfindung leichter durch das Lesen
der folgenden ausführlichen Beschreibung der Erfindung
und das Studium der eingeschlossenen Beispiele verstanden wird.
-
Die
offenbarte Ausführungsform der vorliegenden Erfindung behandelt
ein Verfahren zum Herstellen von 2,3-Diaminopyridin der Formel (I),
dessen Derivaten oder eines Salzes desselben. Das Verfahren der
vorliegenden Erfindung ist vorteilhaft gegenüber dem Stand
der Technik aufgrund der Verwendung von industriell geeigneten Lösungsmitteln
und kostengünstigen Rohmaterialien. Zusätzlich
beseitigt das Verfahren unerwünschte Verfahrensschritte,
wodurch das Verfahren kommerziell brauchbar und für die
industrielle Massenproduktion von reinem 2,3-Diaminopyridin (I),
dessen Derivaten und einem Salz desselben in kürzerer Zeit
durchführbar wird.
-
Entsprechend
der bevorzugten Ausführungsform der vorliegenden Erfindung
wird ein verbessertes Verfahren für die industrielle Herstellung von
2,3-Diaminopyridin der Formel (I), dessen Derivaten oder eines Salzes
desselben mit hoher Reinheit und Ausbeute bereitgestellt, welches
der Massenproduktion zugänglich ist.
wobei R Wasserstoff oder
eine C
1-C
3 geradkettige oder
verzweigte Alkylgruppe ist.
-
Gemäß dem
Verfahren der vorliegenden Erfindung wird das durch die Formel (I)
wiedergegebene 2,3-Diaminopyridin oder ein Salz desselben durch Aminieren
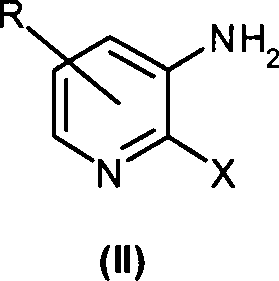
von 3-Amino-2-halopyridin der Formel (II), dessen Derivaten oder
eines Salzes desselben hergestellt,
wobei R Wasserstoff oder
eine C
1-C
3 geradkettige oder
verzweigte Alkylgruppe ist, und wobei X Halogen ist, ausgewählt
aus Chlor oder Brom.
-
Das
Verfahren umfasst das Aminieren von 3-Amino-2-halopyridin der Formel
(II), dessen Derivaten oder eines Salzes desselben mit wässrigem Ammoniak
in Gegenwart eines Kupfer(Cu)-Katalysators und Ammoniakdruck, wobei
der hierin verwendete Ammoniakdruck zwischen 1–5 kg/cm2 liegt, bevorzugt 2–4 kg/cm2, und wobei der in dem Verfahren verwendete
Ammoniak wieder verwertbar ist.
-
Gemäß der
vorliegenden Erfindung ist der in dem Verfahren verwendete Katalysator
ein Kupferkatalysator, ausgewählt aus der Gruppe bestehend
aus Kupfersulfat, Kupferchlorid, Kupfer(II)-Chlorid, Kupfer(II)-Bromid,
bevorzugt Kupfersulfat.
-
Die
Reaktionsmasse wird in einem Temperaturbereich von 100–150°C,
bevorzugt in einem Temperaturbereich von 115–140°C
für 7–10 Stunden bei einem selbst erzeugten Druck
von 18–25 kg/cm2 zum Erhalt des
Roh-2,3-Diaminopyridins erwärmt.
-
Gemäß dem
Verfahren der vorliegenden Erfindung wird die Extraktion des Roh-2,3-Diaminopyridins,
dessen Derivaten oder eines Salzes desselben aus der Reaktionsmasse
in einem einzelnen Schritt durchgeführt, was in der Herstellung
von 2,3-Diaminopyridin, dessen Derivaten oder eines Salzes desselben
mit einer Reinheit von mehr als 99,5% resultiert. Diese Extraktion
wird unter Einsetzen eines für die Umwelt nicht gefährlichen
organischen Lösungsmittels, ausgewählt aus einem
Klasse III-Lösungsmittel, nach den ICH-Richtlinien, durchgeführt,
ist jedoch nicht auf Ethylacetat, Butylacetat, Diisopropylacetat und
Butanol beschränkt und ist bevorzugt Ethylacetat. Das eingesetzte
Lösungsmittel wird durch Phasentrennung abgetrennt und
in dem Verfahren wieder verwertet.
-
Die
vorliegende Erfindung wird unten ferner unter Bezugnahme auf die
folgenden Beispiele dargestellt, ohne dass beabsichtigt ist den
Anwendungsbereich der Erfindung in irgend einer Weise einzuschränken.
-
Beispiel – 1
-
Synthese von 2,3-Diaminopyridin
-
2-Chlor-3-aminopyridin
(23 g); CuSO4·5H2O (9,2
g) und Ammoniaklösung (25%; 230 ml) wurden in einem 0,4
l Autoklaven gegeben. Die Lösung wurde bei 25–30°C
gerührt und ein Ammoniakdruck von 3 kg/cm2 wurde
angelegt. Die resultierende Masse wurde stufenweise auf 130°C
erwärmt und bei dieser Temperatur für 8 Stunden
bei einem Druck von 18–24 kg/cm2 gehalten.
Nach Beendigung der Reaktion wurde die Reaktionsmischung langsam
auf Umgebungstemperatur abgekühlt, während überschüssiges
Ammoniakgas belüftet, gereinigt und wieder verwendet wurde.
Das Produkt wurde dann mit Ethylacetat (190 ml) bei 50–55°C
aus der Reaktionsmasse extrahiert. Die organische Schicht wurde
bei Umgebungstemperatur gesammelt und 60–70% des zugegebenen
Ethylacetats wurde abdestilliert, gefolgt von Abkühlen
der Masse auf ungefähr 5–8°C. Der erhaltene
Kuchen wurde gefiltert und mit Ethalyacetat gewaschen. Nach Trocknen
der Masse unter Vakuum bei 50–60°C für
8 Stunden wurden 11 g 2,3-Diaminopyridin (56% Ausbeute) erhalten;
Schmelzpunkt 112 bis 114°C; die HPLC-Reinheit betrug 99,5%.
Das Ethylacetat wurde zum Wiederverwerten abgesondert. Das Produkt
wurde durch Massenspektroskopie und 1H-NMR
bestätigt.
- ms:m/e 109 (M+); 1H-NMR
(DMSO-D6) δ 7,26 ppm (d, 6H, 1H), δ 6,66 ppm (t,
4H, 1H), δ 6,36 ppm (d, 5H, 1H), δ 5,32 ppm (s,
2H, NH2), δ 4,63 ppm (s, 2H, NH2)
-
Beispiel – 2
-
Synthese von 2,3-Diaminopyridin
-
2-Chlor-3-aminopyridin
(23 g); CuSO4·5H2O (9,2
g) und Ammoniaklösung (25%; 230 ml) wurden in einen 0,4
l Autoklaven gegeben. Die Lösung wurde bei 25–30°C
gerührt und ein Ammoniakdruck von 1,5 kg/cm2 wurde
angelegt. Die resultierende Masse wurde schrittweise auf 130°C
erwärmt und bei dieser Temperatur für 8 Stunden
bei einem Druck von 18–24 kg/cm2 gehalten.
Nach Beendigung der Reaktion wurde die Reaktionsmischung langsam
auf Umgebungstemperatur abgekühlt, während überschüssiges
Ammoniakgas belüftet, gereinigt und wieder verwendet wurde.
Das Produkt wurde dann mit Ethylacetat (190 ml) bei 50–55°C
aus der Reaktionsmasse extrahiert. Die organische Schicht wurde
bei Umgebungstemperatur gesammelt und 60–70% des zugegebenen
Ethylacetats wurden abdestilliert, gefolgt von Abkühlen
der Masse auf ungefähr 5–8°C. Der erhaltene
Kuchen wurde gefiltert und mit Ethylacetat gewaschen. Nach Trocknen
der Masse unter Vakuum bei 50 bis 60°C für 8 Stunden
wurden ~10 g 2,3-Diaminopyridin (52% Ausbeute) erhalten; Schmelzpunkt
112 bis 114°C; die HPLC-Reinheit betrug 99,5%. Das Ethylacetat
wurde zum Wiederverwerten abgesondert.
-
Während
diese Erfindung ausführlich unter Bezugnahme auf bestimmte
bevorzugte Ausführungsformen beschrieben wurde, sollte
verstanden werden, dass die vorliegende Erfindung nicht auf diese
bestimmten Ausführungsformen beschränkt ist, vielmehr
würden dem Fachmann hinsichtlich der vorliegenden Offenbarung,
die die derzeit beste Weise zum Ausführen der Erfindung
beschreibt, viele Modifikationen und Veränderungen gegenwärtig
werden, ohne vom Anwendungsbereich und dem Sinn dieser Erfindung
abzuweichen. Diese Erfindung ist empfänglich für
beträchtliche Veränderungen in ihrer Ausführung
innerhalb des Sinns und des Anwendungsbereiches der beigefügten
Ansprüche.
-
ZITATE ENTHALTEN IN DER BESCHREIBUNG
-
Diese Liste
der vom Anmelder aufgeführten Dokumente wurde automatisiert
erzeugt und ist ausschließlich zur besseren Information
des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen
Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt
keinerlei Haftung für etwaige Fehler oder Auslassungen.
-
Zitierte Patentliteratur
-
- - JP 5339236 [0003]
- - JP 2003012647 [0005]
- - EP 159112 [0006]
- - EP 156495 [0007]
- - DE 667219 [0008]
- - WO 2004069802 [0010]
- - JP 2005170848 [0011]
-
Zitierte Nicht-Patentliteratur
-
- - Leese and
Rydon haben in J. Chem. Soc., 1954, 4039 [0004]
- - Schickh et al. in Ber. Dtsch. Chem. Ges., 1936, 69B, 2593–605 [0009]