CN113646006A - 用于营养不良型大疱性表皮松解症的治疗剂 - Google Patents
用于营养不良型大疱性表皮松解症的治疗剂 Download PDFInfo
- Publication number
- CN113646006A CN113646006A CN202080022396.3A CN202080022396A CN113646006A CN 113646006 A CN113646006 A CN 113646006A CN 202080022396 A CN202080022396 A CN 202080022396A CN 113646006 A CN113646006 A CN 113646006A
- Authority
- CN
- China
- Prior art keywords
- cells
- cell
- composition
- acid sequence
- mesenchymal stem
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 208000010975 Dystrophic epidermolysis bullosa Diseases 0.000 title claims abstract description 43
- 208000004298 epidermolysis bullosa dystrophica Diseases 0.000 title claims abstract description 43
- 239000003814 drug Substances 0.000 title description 5
- 229940124597 therapeutic agent Drugs 0.000 title description 3
- 210000004027 cell Anatomy 0.000 claims abstract description 276
- 239000000203 mixture Substances 0.000 claims abstract description 93
- 210000002901 mesenchymal stem cell Anatomy 0.000 claims abstract description 65
- 108010017377 Collagen Type VII Proteins 0.000 claims abstract description 49
- 102000004510 Collagen Type VII Human genes 0.000 claims abstract description 48
- 108090000623 proteins and genes Proteins 0.000 claims description 55
- 150000007523 nucleic acids Chemical group 0.000 claims description 39
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 33
- 108020005004 Guide RNA Proteins 0.000 claims description 17
- 101150056204 COL7A1 gene Proteins 0.000 claims description 15
- 101100496573 Homo sapiens COL7A1 gene Proteins 0.000 claims description 15
- 210000001185 bone marrow Anatomy 0.000 claims description 14
- 230000000295 complement effect Effects 0.000 claims description 7
- 125000003275 alpha amino acid group Chemical group 0.000 claims 4
- 239000013598 vector Substances 0.000 description 47
- 238000000034 method Methods 0.000 description 44
- 239000013603 viral vector Substances 0.000 description 26
- 150000001413 amino acids Chemical class 0.000 description 21
- 238000010362 genome editing Methods 0.000 description 21
- 102000008186 Collagen Human genes 0.000 description 19
- 108010035532 Collagen Proteins 0.000 description 19
- 229920001436 collagen Polymers 0.000 description 19
- 210000003491 skin Anatomy 0.000 description 18
- 108091033409 CRISPR Proteins 0.000 description 16
- 108010042407 Endonucleases Proteins 0.000 description 14
- 239000007924 injection Substances 0.000 description 14
- 238000002347 injection Methods 0.000 description 14
- 230000035772 mutation Effects 0.000 description 14
- 102100031780 Endonuclease Human genes 0.000 description 12
- 210000002469 basement membrane Anatomy 0.000 description 12
- 238000004806 packaging method and process Methods 0.000 description 11
- 239000013612 plasmid Substances 0.000 description 11
- 210000004207 dermis Anatomy 0.000 description 10
- 238000012239 gene modification Methods 0.000 description 10
- 230000005017 genetic modification Effects 0.000 description 10
- 235000013617 genetically modified food Nutrition 0.000 description 10
- 102100034349 Integrase Human genes 0.000 description 9
- 230000001177 retroviral effect Effects 0.000 description 9
- 108010061833 Integrases Proteins 0.000 description 8
- 206010014989 Epidermolysis bullosa Diseases 0.000 description 7
- 238000003776 cleavage reaction Methods 0.000 description 7
- 210000002615 epidermis Anatomy 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 230000007017 scission Effects 0.000 description 7
- 108020004414 DNA Proteins 0.000 description 6
- 239000002299 complementary DNA Substances 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 210000002510 keratinocyte Anatomy 0.000 description 6
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 108700028369 Alleles Proteins 0.000 description 5
- 238000010453 CRISPR/Cas method Methods 0.000 description 5
- 102100035102 E3 ubiquitin-protein ligase MYCBP2 Human genes 0.000 description 5
- 230000002950 deficient Effects 0.000 description 5
- 238000012744 immunostaining Methods 0.000 description 5
- 108020004707 nucleic acids Proteins 0.000 description 5
- 102000039446 nucleic acids Human genes 0.000 description 5
- 238000012546 transfer Methods 0.000 description 5
- 230000003612 virological effect Effects 0.000 description 5
- 238000010354 CRISPR gene editing Methods 0.000 description 4
- 206010053177 Epidermolysis Diseases 0.000 description 4
- 101000909498 Homo sapiens Collagen alpha-1(VII) chain Proteins 0.000 description 4
- 230000003833 cell viability Effects 0.000 description 4
- 210000002950 fibroblast Anatomy 0.000 description 4
- 238000010172 mouse model Methods 0.000 description 4
- 201000000744 recessive dystrophic epidermolysis bullosa Diseases 0.000 description 4
- 238000001890 transfection Methods 0.000 description 4
- 238000011144 upstream manufacturing Methods 0.000 description 4
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 3
- 238000010356 CRISPR-Cas9 genome editing Methods 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 241000725303 Human immunodeficiency virus Species 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 108091027544 Subgenomic mRNA Proteins 0.000 description 3
- 108091028113 Trans-activating crRNA Proteins 0.000 description 3
- 241000700605 Viruses Species 0.000 description 3
- 125000000539 amino acid group Chemical group 0.000 description 3
- 238000004873 anchoring Methods 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 230000002500 effect on skin Effects 0.000 description 3
- 238000004520 electroporation Methods 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 239000013600 plasmid vector Substances 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 229950010131 puromycin Drugs 0.000 description 3
- 102220032988 rs281865408 Human genes 0.000 description 3
- 210000001626 skin fibroblast Anatomy 0.000 description 3
- 108700001624 vesicular stomatitis virus G Proteins 0.000 description 3
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 241000713756 Caprine arthritis encephalitis virus Species 0.000 description 2
- 102100024335 Collagen alpha-1(VII) chain Human genes 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 241000702421 Dependoparvovirus Species 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- 206010059866 Drug resistance Diseases 0.000 description 2
- 102000004533 Endonucleases Human genes 0.000 description 2
- 101710091045 Envelope protein Proteins 0.000 description 2
- 241000713730 Equine infectious anemia virus Species 0.000 description 2
- 241000713800 Feline immunodeficiency virus Species 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 101000800116 Homo sapiens Thy-1 membrane glycoprotein Proteins 0.000 description 2
- 208000026350 Inborn Genetic disease Diseases 0.000 description 2
- 101710188315 Protein X Proteins 0.000 description 2
- 241000713311 Simian immunodeficiency virus Species 0.000 description 2
- 241000193996 Streptococcus pyogenes Species 0.000 description 2
- 241000194020 Streptococcus thermophilus Species 0.000 description 2
- 101710172711 Structural protein Proteins 0.000 description 2
- 102100033523 Thy-1 membrane glycoprotein Human genes 0.000 description 2
- 241000589892 Treponema denticola Species 0.000 description 2
- 108020000999 Viral RNA Proteins 0.000 description 2
- 241000713325 Visna/maedi virus Species 0.000 description 2
- 101150063416 add gene Proteins 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 210000001789 adipocyte Anatomy 0.000 description 2
- 230000003367 anti-collagen effect Effects 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 210000001612 chondrocyte Anatomy 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 210000000963 osteoblast Anatomy 0.000 description 2
- 210000005259 peripheral blood Anatomy 0.000 description 2
- 239000011886 peripheral blood Substances 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 230000000644 propagated effect Effects 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 210000000130 stem cell Anatomy 0.000 description 2
- 238000010254 subcutaneous injection Methods 0.000 description 2
- 239000007929 subcutaneous injection Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- RNAMYOYQYRYFQY-UHFFFAOYSA-N 2-(4,4-difluoropiperidin-1-yl)-6-methoxy-n-(1-propan-2-ylpiperidin-4-yl)-7-(3-pyrrolidin-1-ylpropoxy)quinazolin-4-amine Chemical compound N1=C(N2CCC(F)(F)CC2)N=C2C=C(OCCCN3CCCC3)C(OC)=CC2=C1NC1CCN(C(C)C)CC1 RNAMYOYQYRYFQY-UHFFFAOYSA-N 0.000 description 1
- 102100022464 5'-nucleotidase Human genes 0.000 description 1
- 206010000349 Acanthosis Diseases 0.000 description 1
- 241000604451 Acidaminococcus Species 0.000 description 1
- 102100032912 CD44 antigen Human genes 0.000 description 1
- 108091079001 CRISPR RNA Proteins 0.000 description 1
- 101100348617 Candida albicans (strain SC5314 / ATCC MYA-2876) NIK1 gene Proteins 0.000 description 1
- 108700004991 Cas12a Proteins 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 238000000116 DAPI staining Methods 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 208000028782 Hereditary disease Diseases 0.000 description 1
- 101000678236 Homo sapiens 5'-nucleotidase Proteins 0.000 description 1
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 1
- 101001046686 Homo sapiens Integrin alpha-M Proteins 0.000 description 1
- 101000935043 Homo sapiens Integrin beta-1 Proteins 0.000 description 1
- 101000692455 Homo sapiens Platelet-derived growth factor receptor beta Proteins 0.000 description 1
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 1
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 1
- 101000835093 Homo sapiens Transferrin receptor protein 1 Proteins 0.000 description 1
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 1
- 241000713340 Human immunodeficiency virus 2 Species 0.000 description 1
- 102100022338 Integrin alpha-M Human genes 0.000 description 1
- 102100025304 Integrin beta-1 Human genes 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 241001112693 Lachnospiraceae Species 0.000 description 1
- 241000689670 Lachnospiraceae bacterium ND2006 Species 0.000 description 1
- 241000713666 Lentivirus Species 0.000 description 1
- 208000024556 Mendelian disease Diseases 0.000 description 1
- 241000588650 Neisseria meningitidis Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 108010077850 Nuclear Localization Signals Proteins 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 102000010292 Peptide Elongation Factor 1 Human genes 0.000 description 1
- 108010077524 Peptide Elongation Factor 1 Proteins 0.000 description 1
- 102100024616 Platelet endothelial cell adhesion molecule Human genes 0.000 description 1
- 108010051742 Platelet-Derived Growth Factor beta Receptor Proteins 0.000 description 1
- 102000018967 Platelet-Derived Growth Factor beta Receptor Human genes 0.000 description 1
- 102100026547 Platelet-derived growth factor receptor beta Human genes 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 1
- 102000018120 Recombinases Human genes 0.000 description 1
- 108010091086 Recombinases Proteins 0.000 description 1
- 101100007329 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS1 gene Proteins 0.000 description 1
- 101100221606 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS7 gene Proteins 0.000 description 1
- 206010040943 Skin Ulcer Diseases 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 238000002105 Southern blotting Methods 0.000 description 1
- 241000191967 Staphylococcus aureus Species 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 238000010459 TALEN Methods 0.000 description 1
- 108010043645 Transcription Activator-Like Effector Nucleases Proteins 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 1
- 102100026144 Transferrin receptor protein 1 Human genes 0.000 description 1
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 1
- 102000016549 Vascular Endothelial Growth Factor Receptor-2 Human genes 0.000 description 1
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 1
- 208000010094 Visna Diseases 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- -1 as well as skin Substances 0.000 description 1
- 210000000270 basal cell Anatomy 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 208000019748 bullous skin disease Diseases 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000002577 cryoprotective agent Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 210000003074 dental pulp Anatomy 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 230000005782 double-strand break Effects 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 210000004700 fetal blood Anatomy 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 210000003692 ilium Anatomy 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 239000003978 infusion fluid Substances 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 1
- 208000008106 junctional epidermolysis bullosa Diseases 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 238000011813 knockout mouse model Methods 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 238000002826 magnetic-activated cell sorting Methods 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 238000001000 micrograph Methods 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000004886 process control Methods 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 238000007390 skin biopsy Methods 0.000 description 1
- 210000004927 skin cell Anatomy 0.000 description 1
- 231100000019 skin ulcer Toxicity 0.000 description 1
- 238000010583 slow cooling Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000037436 splice-site mutation Effects 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 210000001562 sternum Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 210000002303 tibia Anatomy 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/28—Bone marrow; Haematopoietic stem cells; Mesenchymal stem cells of any origin, e.g. adipose-derived stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/39—Connective tissue peptides, e.g. collagen, elastin, laminin, fibronectin, vitronectin, cold insoluble globulin [CIG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
- C07H21/02—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids with ribosyl as saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/78—Connective tissue peptides, e.g. collagen, elastin, laminin, fibronectin, vitronectin, cold insoluble globulin [CIG]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/90—Stable introduction of foreign DNA into chromosome
- C12N15/902—Stable introduction of foreign DNA into chromosome using homologous recombination
- C12N15/907—Stable introduction of foreign DNA into chromosome using homologous recombination in mammalian cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0663—Bone marrow mesenchymal stem cells (BM-MSC)
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/07—Animals genetically altered by homologous recombination
- A01K2217/075—Animals genetically altered by homologous recombination inducing loss of function, i.e. knock out
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/105—Murine
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0306—Animal model for genetic diseases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/20—Type of nucleic acid involving clustered regularly interspaced short palindromic repeats [CRISPRs]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Biotechnology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Cell Biology (AREA)
- Developmental Biology & Embryology (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- Epidemiology (AREA)
- General Engineering & Computer Science (AREA)
- Dermatology (AREA)
- General Chemical & Material Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Hematology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Gastroenterology & Hepatology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Virology (AREA)
- Mycology (AREA)
- Toxicology (AREA)
- Rheumatology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本公开内容涉及用于治疗营养不良型大疱性表皮松解症的组合物,所述组合物包含已被遗传修饰以产生VII型胶原的营养不良型大疱性表皮松解症患者的细胞,其中所述细胞是间充质干细胞。本公开内容还涉及用于治疗营养不良型大疱性表皮松解症的组合物,所述组合物包含产生VII型胶原的细胞,并待施用到水疱内。
Description
技术领域
本申请要求关于日本专利申请号2019-007201的优先权,所述日本专利申请整体引入本文作为参考。
本公开内容涉及用于治疗营养不良型大疱性表皮松解症的组合物。
背景技术
大疱性表皮松解症是这样的疾病,其中负责皮肤组织粘附的粘附性结构分子丧失或消失,然后表皮与真皮剥离,并且当对皮肤施加力时,出现水疱或皮肤溃疡。该疾病包括单纯型大疱性表皮松解症(其中表皮撕裂以形成水疱)、交界型大疱性表皮松解症(其中表皮与基底膜剥离以形成水疱)、以及营养不良型大疱性表皮松解症(其中基底膜与真皮剥离)。
营养不良型大疱性表皮松解症是最常见类型的大疱性表皮松解症,占所有大疱性表皮松解症的约50%。它是由编码VII型胶原的COL7A1基因中的突变引起的遗传性疾病。在皮肤的结构中,在表皮的底部处的表皮基底细胞与称为基底膜的片状结构结合。VII型胶原在真皮中形成称为锚定性原纤维的纤维,并且连接基底膜和真皮。因此,如果VII型胶原基因中存在异常,则基底膜与真皮之间的粘附功能是受损的,导致其中基底膜与真皮之间形成水疱的营养不良型大疱性表皮松解症。在营养不良型大疱性表皮松解症中,重度隐性营养不良型大疱性表皮松解症是非常严重的遗传性大疱性皮肤病,其具有在出生后立即遍及全身的持续烧伤样皮肤症状,并且皮肤棘细胞癌(瘢痕癌)从约30岁开始频繁发生且导致死亡。
目前不存在用于大疱性表皮松解症的有效治疗,并且需要开发从根本上压制发疱的基因疗法。作为这样的基因疗法,公开了治疗技术,其中收集患者的皮肤细胞,进行遗传改造以产生VII型胶原,培养以形成皮肤片层,并且移植给患者(专利文献1)。另外,已提议使缺乏VII型胶原活性的间充质干细胞经受基因组编辑,将因此获得的能够产生VII型胶原的间充质干细胞分化成角质形成细胞或成纤维细胞,培养这些细胞以形成皮肤片层,并且使用皮肤片层用于治疗患者(参见专利文献2)。
引用文献列表
专利文件
专利文件1:WO2017/120147
专利文件2:WO2018/154413。
发明内容
待解决的问题
制造皮肤片层需要先进的工艺控制和培养技术,于是涉及高难度和高成本。需要更易于制造的治疗剂。
问题的解决方案
在一个方面,本公开内容涉及用于治疗营养不良型大疱性表皮松解症的组合物,其包含从营养不良型大疱性表皮松解症患者获得的细胞,其中所述细胞是间充质干细胞,并且被遗传修饰以产生VII型胶原。
在另一个方面,本公开内容涉及用于治疗营养不良型大疱性表皮松解症的组合物,其包含产生VII型胶原的细胞,其中所述组合物待施用到水疱内。
发明效果
本公开内容提供了用于治疗营养不良型大疱性表皮松解症的组合物。
附图说明
图1显示了通过设计的sgRNA(sgAAVS1-#1至#3)对基因组DNA的切割及其切割效率。
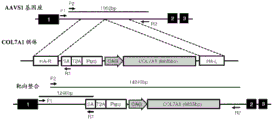
图2是其中将COL7A1基因引入AAVS1区域内的基因组编辑的说明图解。HA-R和HA-L指示具有同源序列的部分,SA指示剪接受体序列,T2A指示编码T2A肽的T2A序列,Puro指示嘌呤霉素抗性基因,并且CAG指示CAG启动子序列。野生型基因组中从F2到R2的长度(顶部)为1952 bp,并且COL7A1基因引入其内的基因组中从F1到R1以及从F2到R2的长度(底部)分别为1246 bp和14249 bp。
图3显示了通过CRISPR-Cas9系统的基因转移效率,以及在间充质干细胞(MSC)中的基因转移后的细胞活力。虚线指示基因组编辑细胞的数目,并且柱指示细胞活力。
图4显示了确认通过基因组编辑引入COL7A1基因的结果。
图5显示了MSC中VII型胶原的表达。符号"(-)"指示没有基因组编辑的对照,并且符号"COL7A1-供体"指示其中通过基因组编辑引入COL7A1基因的遗传修饰的MSC。左侧的照片显示了细胞的免疫染色结果,并且右侧的照片显示了细胞的培养上清液的蛋白质印迹结果。
图6是大疱性表皮松解症模型小鼠的产生的说明图解。右侧的照片显示了形成的水疱。
图7显示了通过皮内或水疱内注射将遗传修饰的MSC注射给其的大疱性表皮松解症模型小鼠的皮肤断层图像。上面的照片显示了VII型胶原的DAPI染色和免疫染色的合并图像,而下面的照片显示了VII型胶原的免疫染色结果。箭头指示VII型胶原的表达。
图8显示了通过皮下注射将遗传修饰的MSC注射给其的大疱性表皮松解症模型小鼠的皮肤断层图像。
图9显示了通过水疱内注射将遗传修饰的MSC注射给其的大疱性表皮松解症模型小鼠的皮肤的电子显微镜图像。箭头指示锚定性原纤维。
具体实施方式
除非另有说明,否则本公开内容中使用的术语具有例如有机化学、医学科学、药物科学、分子生物学和微生物学领域的技术人员一般理解的含义。下文提供了本公开内容中使用的一些术语的定义,并且这些定义取代了本公开内容中的一般理解。
营养不良型大疱性表皮松解症是由编码VII型胶原的COL7A1基因中的突变引起的遗传性疾病,并且已知特点在于不产生VII型胶原或产生由于突变而功能减少的VII型胶原。VII型胶原在真皮中形成称为锚定性原纤维的纤维,并且连接基底膜和真皮。VII型胶原从N末端起含有第一非胶原区域、胶原区域和第二非胶原区域,并且在胶原区域处形成三链,其特点在于甘氨酸-XY的重复序列。两个分子在C末端处彼此结合,且在N末端处与基底膜结合。突变的实例包括其中胶原区域中的甘氨酸被不同氨基酸替换的突变、停止蛋白质翻译的终止密码子突变和剪接位点突变。突变可以在等位基因之一或两者中。营养不良型大疱性表皮松解症包括显性营养不良型大疱性表皮松解症和隐性营养不良型大疱性表皮松解症,并且隐性营养不良型大疱性表皮松解症包括重度泛发性隐性营养不良型大疱性表皮松解症和具有相对轻度症状的其它泛发型。本文中的营养不良型大疱性表皮松解症可以是任何类型的营养不良型大疱性表皮松解症,并且COL7A1基因中的病因突变可以是任何突变。
在本公开内容中,使用产生VII型胶原的细胞。如本文使用的,术语“产生VII型胶原的细胞”意指产生功能性VII型胶原(即,能够形成锚定性原纤维的VII型胶原)的细胞。产生VII型胶原的细胞可以是天然产生VII型胶原的细胞,或已被遗传修饰以产生VII型胶原的细胞。
在本公开内容中,细胞的遗传修饰意指细胞的基因组中基因的遗传修饰和细胞的修饰两者,以从基因组外的核酸构建体(例如载体)表达基因。即,表述“遗传修饰细胞以产生VII型胶原”包括修饰细胞以从基因组中的COL7A1基因表达VII型胶原,并且修饰细胞以从基因组外的核酸构建体中的COL7A1基因表达VII型胶原。另外,“遗传修饰以产生VII型胶原的细胞”包括从基因组中的COL7A1基因表达VII型胶原的细胞,以及从基因组外的核酸构建体中的COL7A1基因表达VII型胶原的细胞。
可以通过引入COL7A1基因、或通过校正基因组中的COL7A1基因中的突变,来进行细胞的遗传修饰。可以通过将COL7A1基因引入细胞的基因组内,或通过将包含COL7A1基因的核酸构建体置于细胞中,使得COL7A1基因从基因组外的核酸构建体表达,来进行COL7A1基因的引入。当将COL7A1基因被引入细胞的基因组内时,COL7A1基因可以在特异性位点处引入,或可以随机引入。在一个实施方案中,将COL7A1基因引入基因组的COL7A1基因座或安全港如AAVS1区域内。
细胞可以是从细胞待施用于其的营养不良型大疱性表皮松解症患者获得的细胞(即,自体细胞),或从除患者外的受试者获得的细胞(即,同种异体细胞)。除患者外的受试者包括健康个体,尤其是HLA匹配的健康个体,或患者的母亲。在一个实施方案中,细胞是从营养不良型大疱性表皮松解症患者获得的细胞。从营养不良型大疱性表皮松解症患者获得的细胞包括不产生VII型胶原的细胞,以及产生由于突变而功能减少的VII型胶原的细胞,并且如本文使用的,“从营养不良型大疱性表皮松解症患者获得的细胞”可以是其中任一种。
细胞可以是任何细胞,只要它在施用于患者时在表皮基底膜附近产生VII型胶原。细胞可以是衍生自皮肤、骨髓或血液(例如外周血)的细胞。在一个实施方案中,细胞是角质形成细胞、皮肤成纤维细胞或间充质干细胞。在一个不同的实施方案中,细胞是从患者或除患者外的受试者获得的细胞诱导的iPS细胞、或者从此类iPS细胞诱导的细胞。因此,细胞可以是从患者或除患者外的受试者获得的细胞,或者可以是从获得的细胞诱导的细胞。当细胞是遗传修饰的细胞,并且也是从患者或除患者外的受试者获得的细胞诱导的细胞时,遗传修饰可以在诱导之前或之后进行。
在本公开内容中,术语“细胞”在包括根据需要而增殖后的细胞的意义上使用。细胞的增殖可以通过培养细胞来进行。例如,“从患者或除患者外的受试者获得的细胞”包括从患者或除患者外的受试者收集然后增殖的细胞,并且“遗传修饰的细胞”包括从通过遗传修饰获得的细胞增殖的细胞。当进行遗传修饰时,细胞可以增殖直到获得遗传修饰所需的量。另外,在遗传修饰后,细胞可以增殖直到获得治疗所需的量。
角质形成细胞和皮肤成纤维细胞可以通过本领域已知的任何方法获得。例如,通过皮肤活检组织的酶促处理和/或机械处理,将表皮和真皮分开,并且使因此分开的表皮和真皮各自进一步经受酶促处理。角质形成细胞可以从表皮样品中获得,并且皮肤成纤维细胞可以从真皮样品中获得。
在一个实施方案中,细胞是间充质干细胞。当施用于患者时,间充质干细胞被视为比角质形成细胞和皮肤成纤维细胞更久地驻留于患者组织中。另外,虽然当遗传修饰的细胞产生迄今为止尚未在患者中产生的蛋白质时,预计炎症反应,但间充质干细胞具有抗炎效应,并且因此比角质形成细胞和皮肤成纤维细胞更有利。
间充质干细胞(本文也称为MSC)对固相(如塑料培养容器)具有粘附性,并且具有自我更新能力和分化成间充质组织(如骨、软骨、脂肪和肌肉)的能力两者。在一个实施方案中,间充质干细胞是能够分化成成骨细胞、软骨细胞和脂肪细胞中的至少一种的细胞。在一个实施方案中,间充质干细胞是能够分化成成骨细胞、软骨细胞和脂肪细胞的细胞。当细胞群体具有上文提到的能力时,它应理解为包括间充质干细胞。间充质干细胞可以从骨髓或其它组织(例如,血液如脐带血和外周血,以及皮肤、脂肪和牙髓)获得。在一个实施方案中,间充质干细胞是骨髓衍生的间充质干细胞(本文也称为BM-MSC)。骨髓衍生的间充质干细胞可以从任何部位获得,所述部位例如股骨、椎骨、胸骨、髂骨和胫骨。
间充质干细胞可以通过本领域已知的任何方法获得。例如,可以提到基于粘附性、细胞表面标记物和密度差异的方法。例如,将从骨髓或含有间充质干细胞的其它组织获得的细胞接种到塑料或玻璃培养容器上,并且收集粘附至培养容器并增殖的细胞。可替代地,也可以使用针对间充质干细胞的表面标记物的抗体,通过细胞分选(例如FACS、MACS)获得间充质干细胞。人间充质干细胞的表面标记物可以是下述中的一种或多种:PDGFRα阳性、PDGFRβ阳性、Lin阴性、CD45阴性、CD44阳性、CD90阳性、CD29阳性、Flk-1阴性、CD105阳性、CD73阳性、CD90阳性、CD71阳性、Stro-1阳性、CD106阳性、CD166阳性、CD31阴性、CD271阳性和CD11b阴性。
iPS细胞可以通过本领域已知的任何方法产生。例如,iPS细胞可以通过将三种类型的转录因子OCT4、SOX2和NANOG引入体细胞内来产生,所述体细胞例如从患者或除患者外的受试者获得的成纤维细胞(Budniatzky和Gepstein,Stem Cells Transl Med. 3(4):448-57,2014;Barrett等人,Stem Cells Trans Med 3 : 1-6 sctm.2014-0121,2014;Focosi等人,Blood Cancer Journal 4: e211,2014)。
如本文使用的,取决于上下文,术语“细胞”可以意指单个细胞或多个细胞。进一步地,细胞可以是由一种细胞类型组成的细胞群体、或包括多种细胞类型的细胞群体。
如本文使用的,术语“COL7A1基因”意指编码VII型胶原的核酸序列,并且用于包括cDNA以及含有一个或多个内含子的序列(例如,基因组序列或小基因)。人COL7A1基因的代表性核酸序列(cDNA)显示于SEQ ID NO: 1中,并且人VII型胶原的代表性氨基酸序列显示于SEQ ID NO: 2中。COL7A1基因的cDNA序列公开于GenBank:NM_000094.3中,而基因组序列公开于GenBank:AC121252.4中。COL7A1基因的序列并不限于任何特异性序列,只要它编码功能型VII型胶原(即,能够形成锚定性原纤维的VII型胶原)。
人COL7A1基因的cDNA序列(8835bp)(SEQ ID NO: 1)
ATGACGCTGCGGCTTCTGGTGGCCGCGCTCTGCGCCGGGATCCTGGCAGAGGCGCCCCGAGTGCGAGCCCAGCACAGGGAGAGAGTGACCTGCACGCGCCTTTACGCCGCTGACATTGTGTTCTTACTGGATGGCTCCTCATCCATTGGCCGCAGCAATTTCCGCGAGGTCCGCAGCTTTCTCGAAGGGCTGGTGCTGCCTTTCTCTGGAGCAGCCAGTGCACAGGGTGTGCGCTTTGCCACAGTGCAGTACAGCGATGATCCACGGACAGAGTTCGGCCTGGATGCACTTGGCTCTGGGGGTGATGTGATCCGCGCCATCCGTGAGCTTAGCTACAAGGGGGGCAACACTCGCACAGGGGCTGCAATTCTCCATGTGGCTGACCATGTCTTCCTGCCCCAGCTGGCCCGACCTGGTGTCCCCAAGGTCTGCATCCTGATCACAGACGGGAAGTCCCAGGACCTGGTGGACACAGCTGCCCAAAGGCTGAAGGGGCAGGGGGTCAAGCTATTTGCTGTGGGGATCAAGAATGCTGACCCTGAGGAGCTGAAGCGAGTTGCCTCACAGCCCACCAGTGACTTCTTCTTCTTCGTCAATGACTTCAGCATCTTGAGGACACTACTGCCCCTCGTTTCCCGGAGAGTGTGCACGACTGCTGGTGGCGTGCCTGTGACCCGACCTCCGGATGACTCGACCTCTGCTCCACGAGACCTGGTGCTGTCTGAGCCAAGCAGCCAATCCTTGAGAGTACAGTGGACAGCGGCCAGTGGCCCTGTGACTGGCTACAAGGTCCAGTACACTCCTCTGACGGGGCTGGGACAGCCACTGCCGAGTGAGCGGCAGGAGGTGAACGTCCCAGCTGGTGAGACCAGTGTGCGGCTGCGGGGTCTCCGGCCACTGACCGAGTACCAAGTGACTGTGATTGCCCTCTACGCCAACAGCATCGGGGAGGCTGTGAGCGGGACAGCTCGGACCACTGCCCTAGAAGGGCCGGAACTGACCATCCAGAATACCACAGCCCACAGCCTCCTGGTGGCCTGGCGGAGTGTGCCAGGTGCCACTGGCTACCGTGTGACATGGCGGGTCCTCAGTGGTGGGCCCACACAGCAGCAGGAGCTGGGCCCTGGGCAGGGTTCAGTGTTGCTGCGTGACTTGGAGCCTGGCACGGACTATGAGGTGACCGTGAGCACCCTATTTGGCCGCAGTGTGGGGCCCGCCACTTCCCTGATGGCTCGCACTGACGCTTCTGTTGAGCAGACCCTGCGCCCGGTCATCCTGGGCCCCACATCCATCCTCCTTTCCTGGAACTTGGTGCCTGAGGCCCGTGGCTACCGGTTGGAATGGCGGCGTGAGACTGGCTTGGAGCCACCGCAGAAGGTGGTACTGCCCTCTGATGTGACCCGCTACCAGTTGGATGGGCTGCAGCCGGGCACTGAGTACCGCCTCACACTCTACACTCTGCTGGAGGGCCACGAGGTGGCCACCCCTGCAACCGTGGTTCCCACTGGACCAGAGCTGCCTGTGAGCCCTGTAACAGACCTGCAAGCCACCGAGCTGCCCGGGCAGCGGGTGCGAGTGTCCTGGAGCCCAGTCCCTGGTGCCACCCAGTACCGCATCATTGTGCGCAGCACCCAGGGGGTTGAGCGGACCCTGGTGCTTCCTGGGAGTCAGACAGCATTCGACTTGGATGACGTTCAGGCTGGGCTTAGCTACACTGTGCGGGTGTCTGCTCGAGTGGGTCCCCGTGAGGGCAGTGCCAGTGTCCTCACTGTCCGCCGGGAGCCGGAAACTCCACTTGCTGTTCCAGGGCTGCGGGTTGTGGTGTCAGATGCAACGCGAGTGAGGGTGGCCTGGGGACCCGTCCCTGGAGCCAGTGGATTTCGGATTAGCTGGAGCACAGGCAGTGGTCCGGAGTCCAGCCAGACACTGCCCCCAGACTCTACTGCCACAGACATCACAGGGCTGCAGCCTGGAACCACCTACCAGGTGGCTGTGTCGGTACTGCGAGGCAGAGAGGAGGGCCCTGCTGCAGTCATCGTGGCTCGAACGGACCCACTGGGCCCAGTGAGGACGGTCCATGTGACTCAGGCCAGCAGCTCATCTGTCACCATTACCTGGACCAGGGTTCCTGGCGCCACAGGATACAGGGTTTCCTGGCACTCAGCCCACGGCCCAGAGAAATCCCAGTTGGTTTCTGGGGAGGCCACGGTGGCTGAGCTGGATGGACTGGAGCCAGATACTGAGTATACGGTGCATGTGAGGGCCCATGTGGCTGGCGTGGATGGGCCCCCTGCCTCTGTGGTTGTGAGGACTGCCCCTGAGCCTGTGGGTCGTGTGTCGAGGCTGCAGATCCTCAATGCTTCCAGCGACGTTCTACGGATCACCTGGGTAGGGGTCACTGGAGCCACAGCTTACAGACTGGCCTGGGGCCGGAGTGAAGGCGGCCCCATGAGGCACCAGATACTCCCAGGAAACACAGACTCTGCAGAGATCCGGGGTCTCGAAGGTGGAGTCAGCTACTCAGTGCGAGTGACTGCACTTGTCGGGGACCGCGAGGGCACACCTGTCTCCATTGTTGTCACTACGCCGCCTGAGGCTCCGCCAGCCCTGGGGACGCTTCACGTGGTGCAGCGCGGGGAGCACTCGCTGAGGCTGCGCTGGGAGCCGGTGCCCAGAGCGCAGGGCTTCCTTCTGCACTGGCAACCTGAGGGTGGCCAGGAACAGTCCCGGGTCCTGGGGCCCGAGCTCAGCAGCTATCACCTGGACGGGCTGGAGCCAGCGACACAGTACCGCGTGAGGCTGAGTGTCCTAGGGCCAGCTGGAGAAGGGCCCTCTGCAGAGGTGACTGCGCGCACTGAGTCACCTCGTGTTCCAAGCATTGAACTACGTGTGGTGGACACCTCGATCGACTCGGTGACTTTGGCCTGGACTCCAGTGTCCAGGGCATCCAGCTACATCCTATCCTGGCGGCCACTCAGAGGCCCTGGCCAGGAAGTGCCTGGGTCCCCGCAGACACTTCCAGGGATCTCAAGCTCCCAGCGGGTGACAGGGCTAGAGCCTGGCGTCTCTTACATCTTCTCCCTGACGCCTGTCCTGGATGGTGTGCGGGGTCCTGAGGCATCTGTCACACAGACGCCAGTGTGCCCCCGTGGCCTGGCGGATGTGGTGTTCCTACCACATGCCACTCAAGACAATGCTCACCGTGCGGAGGCTACGAGGAGGGTCCTGGAGCGTCTGGTGTTGGCACTTGGGCCTCTTGGGCCACAGGCAGTTCAGGTTGGCCTGCTGTCTTACAGTCATCGGCCCTCCCCACTGTTCCCACTGAATGGCTCCCATGACCTTGGCATTATCTTGCAAAGGATCCGTGACATGCCCTACATGGACCCAAGTGGGAACAACCTGGGCACAGCCGTGGTCACAGCTCACAGATACATGTTGGCACCAGATGCTCCTGGGCGCCGCCAGCACGTACCAGGGGTGATGGTTCTGCTAGTGGATGAACCCTTGAGAGGTGACATATTCAGCCCCATCCGTGAGGCCCAGGCTTCTGGGCTTAATGTGGTGATGTTGGGAATGGCTGGAGCGGACCCAGAGCAGCTGCGTCGCTTGGCGCCGGGTATGGACTCTGTCCAGACCTTCTTCGCCGTGGATGATGGGCCAAGCCTGGACCAGGCAGTCAGTGGTCTGGCCACAGCCCTGTGTCAGGCATCCTTCACTACTCAGCCCCGGCCAGAGCCCTGCCCAGTGTATTGTCCAAAGGGCCAGAAGGGGGAACCTGGAGAGATGGGCCTGAGAGGACAAGTTGGGCCTCCTGGCGACCCTGGCCTCCCGGGCAGGACCGGTGCTCCCGGCCCCCAGGGGCCCCCTGGAAGTGCCACTGCCAAGGGCGAGAGGGGCTTCCCTGGAGCAGATGGGCGTCCAGGCAGCCCTGGCCGCGCCGGGAATCCTGGGACCCCTGGAGCCCCTGGCCTAAAGGGCTCTCCAGGGTTGCCTGGCCCTCGTGGGGACCCGGGAGAGCGAGGACCTCGAGGCCCAAAGGGGGAGCCGGGGGCTCCCGGACAAGTCATCGGAGGTGAAGGACCTGGGCTTCCTGGGCGGAAAGGGGACCCTGGACCATCGGGCCCCCCTGGACCTCGTGGACCACTGGGGGACCCAGGACCCCGTGGCCCCCCAGGGCTTCCTGGAACAGCCATGAAGGGTGACAAAGGCGATCGTGGGGAGCGGGGTCCCCCTGGACCAGGTGAAGGTGGCATTGCTCCTGGGGAGCCTGGGCTGCCGGGTCTTCCCGGAAGCCCTGGACCCCAAGGCCCCGTTGGCCCCCCTGGAAAGAAAGGAGAAAAAGGTGACTCTGAGGATGGAGCTCCAGGCCTCCCAGGACAACCTGGGTCTCCGGGTGAGCAGGGCCCACGGGGACCTCCTGGAGCTATTGGCCCCAAAGGTGACCGGGGCTTTCCAGGGCCCCTGGGTGAGGCTGGAGAGAAGGGCGAACGTGGACCCCCAGGCCCAGCGGGATCCCGGGGGCTGCCAGGGGTTGCTGGACGTCCTGGAGCCAAGGGTCCTGAAGGGCCACCAGGACCCACTGGCCGCCAAGGAGAGAAGGGGGAGCCTGGTCGCCCTGGGGACCCTGCAGTGGTGGGACCTGCTGTTGCTGGACCCAAAGGAGAAAAGGGAGATGTGGGGCCCGCTGGGCCCAGAGGAGCTACCGGAGTCCAAGGGGAACGGGGCCCACCCGGCTTGGTTCTTCCTGGAGACCCTGGCCCCAAGGGAGACCCTGGAGACCGGGGTCCCATTGGCCTTACTGGCAGAGCAGGACCCCCAGGTGACTCAGGGCCTCCTGGAGAGAAGGGAGACCCTGGGCGGCCTGGCCCCCCAGGACCTGTTGGCCCCCGAGGACGAGATGGTGAAGTTGGAGAGAAAGGTGACGAGGGTCCTCCGGGTGACCCGGGTTTGCCTGGAAAAGCAGGCGAGCGTGGCCTTCGGGGGGCACCTGGAGTTCGGGGGCCTGTGGGTGAAAAGGGAGACCAGGGAGATCCTGGAGAGGATGGACGAAATGGCAGCCCTGGATCATCTGGACCCAAGGGTGACCGTGGGGAGCCGGGTCCCCCAGGACCCCCGGGACGGCTGGTAGACACAGGACCTGGAGCCAGAGAGAAGGGAGAGCCTGGGGACCGCGGACAAGAGGGTCCTCGAGGGCCCAAGGGTGATCCTGGCCTCCCTGGAGCCCCTGGGGAAAGGGGCATTGAAGGGTTTCGGGGACCCCCAGGCCCACAGGGGGACCCAGGTGTCCGAGGCCCAGCAGGAGAAAAGGGTGACCGGGGTCCCCCTGGGCTGGATGGCCGGAGCGGACTGGATGGGAAACCAGGAGCCGCTGGGCCCTCTGGGCCGAATGGTGCTGCAGGCAAAGCTGGGGACCCAGGGAGAGACGGGCTTCCAGGCCTCCGTGGAGAACAGGGCCTCCCTGGCCCCTCTGGTCCCCCTGGATTACCGGGAAAGCCAGGCGAGGATGGCAAACCTGGCCTGAATGGAAAAAACGGAGAACCTGGGGACCCTGGAGAAGACGGGAGGAAGGGAGAGAAAGGAGATTCAGGCGCCTCTGGGAGAGAAGGTCGTGATGGCCCCAAGGGTGAGCGTGGAGCTCCTGGTATCCTTGGACCCCAGGGGCCTCCAGGCCTCCCAGGGCCAGTGGGCCCTCCTGGCCAGGGTTTTCCTGGTGTCCCAGGAGGCACGGGCCCCAAGGGTGACCGTGGGGAGACTGGATCCAAAGGGGAGCAGGGCCTCCCTGGAGAGCGTGGCCTGCGAGGAGAGCCTGGAAGTGTGCCGAATGTGGATCGGTTGCTGGAAACTGCTGGCATCAAGGCATCTGCCCTGCGGGAGATCGTGGAGACCTGGGATGAGAGCTCTGGTAGCTTCCTGCCTGTGCCCGAACGGCGTCGAGGCCCCAAGGGGGACTCAGGCGAACAGGGCCCCCCAGGCAAGGAGGGCCCCATCGGCTTTCCTGGAGAACGCGGGCTGAAGGGCGACCGTGGAGACCCTGGCCCTCAGGGGCCACCTGGTCTGGCCCTTGGGGAGAGGGGCCCCCCCGGGCCTTCCGGCCTTGCCGGGGAGCCTGGAAAGCCTGGTATTCCCGGGCTCCCAGGCAGGGCTGGGGGTGTGGGAGAGGCAGGAAGGCCAGGAGAGAGGGGAGAACGGGGAGAGAAAGGAGAACGTGGAGAACAGGGCAGAGATGGCCCTCCTGGACTCCCTGGAACCCCTGGGCCCCCCGGACCCCCTGGCCCCAAGGTGTCTGTGGATGAGCCAGGTCCTGGACTCTCTGGAGAACAGGGACCCCCTGGACTCAAGGGTGCTAAGGGGGAGCCGGGCAGCAATGGTGACCAAGGTCCCAAAGGAGACAGGGGTGTGCCAGGCATCAAAGGAGACCGGGGAGAGCCTGGACCGAGGGGTCAGGACGGCAACCCGGGTCTACCAGGAGAGCGTGGTATGGCTGGGCCTGAAGGGAAGCCGGGTCTGCAGGGTCCAAGAGGCCCCCCTGGCCCAGTGGGTGGTCATGGAGACCCTGGACCACCTGGTGCCCCGGGTCTTGCTGGCCCTGCAGGACCCCAAGGACCTTCTGGCCTGAAGGGGGAGCCTGGAGAGACAGGACCTCCAGGACGGGGCCTGACTGGACCTACTGGAGCTGTGGGACTTCCTGGACCCCCCGGCCCTTCAGGCCTTGTGGGTCCACAGGGGTCTCCAGGTTTGCCTGGACAAGTGGGGGAGACAGGGAAGCCGGGAGCCCCAGGTCGAGATGGTGCCAGTGGAAAAGATGGAGACAGAGGGAGCCCTGGTGTGCCAGGGTCACCAGGTCTGCCTGGCCCTGTCGGACCTAAAGGAGAACCTGGCCCCACGGGGGCCCCTGGACAGGCTGTGGTCGGGCTCCCTGGAGCAAAGGGAGAGAAGGGAGCCCCTGGAGGCCTTGCTGGAGACCTGGTGGGTGAGCCGGGAGCCAAAGGTGACCGAGGACTGCCAGGGCCGCGAGGCGAGAAGGGTGAAGCTGGCCGTGCAGGGGAGCCCGGAGACCCTGGGGAAGATGGTCAGAAAGGGGCTCCAGGACCCAAAGGTTTCAAGGGTGACCCAGGAGTCGGGGTCCCGGGCTCCCCTGGGCCTCCTGGCCCTCCAGGTGTGAAGGGAGATCTGGGCCTCCCTGGCCTGCCCGGTGCTCCTGGTGTTGTTGGGTTCCCGGGTCAGACAGGCCCTCGAGGAGAGATGGGTCAGCCAGGCCCTAGTGGAGAGCGGGGTCTGGCAGGCCCCCCAGGGAGAGAAGGAATCCCAGGACCCCTGGGGCCACCTGGACCACCGGGGTCAGTGGGACCACCTGGGGCCTCTGGACTCAAAGGAGACAAGGGAGACCCTGGAGTAGGGCTGCCTGGGCCCCGAGGCGAGCGTGGGGAGCCAGGCATCCGGGGTGAAGATGGCCGCCCCGGCCAGGAGGGACCCCGAGGACTCACGGGGCCCCCTGGCAGCAGGGGAGAGCGTGGGGAGAAGGGTGATGTTGGGAGTGCAGGACTAAAGGGTGACAAGGGAGACTCAGCTGTGATCCTGGGGCCTCCAGGCCCACGGGGTGCCAAGGGGGACATGGGTGAACGAGGGCCTCGGGGCTTGGATGGTGACAAAGGACCTCGGGGAGACAATGGGGACCCTGGTGACAAGGGCAGCAAGGGAGAGCCTGGTGACAAGGGCTCAGCCGGGTTGCCAGGACTGCGTGGACTCCTGGGACCCCAGGGTCAACCTGGTGCAGCAGGGATCCCTGGTGACCCGGGATCCCCAGGAAAGGATGGAGTGCCTGGTATCCGAGGAGAAAAAGGAGATGTTGGCTTCATGGGTCCCCGGGGCCTCAAGGGTGAACGGGGAGTGAAGGGAGCCTGTGGCCTTGATGGAGAGAAGGGAGACAAGGGAGAAGCTGGTCCCCCAGGCCGCCCCGGGCTGGCAGGACACAAAGGAGAGATGGGGGAGCCTGGTGTGCCGGGCCAGTCGGGGGCCCCTGGCAAGGAGGGCCTGATCGGTCCCAAGGGTGACCGAGGCTTTGACGGGCAGCCAGGCCCCAAGGGTGACCAGGGCGAGAAAGGGGAGCGGGGAACCCCAGGAATTGGGGGCTTCCCAGGCCCCAGTGGAAATGATGGCTCTGCTGGTCCCCCAGGGCCACCTGGCAGTGTTGGTCCCAGAGGCCCCGAAGGACTTCAGGGCCAGAAGGGTGAGCGAGGTCCCCCCGGAGAGAGAGTGGTGGGGGCTCCTGGGGTCCCTGGAGCTCCTGGCGAGAGAGGGGAGCAGGGGCGGCCAGGGCCTGCCGGTCCTCGAGGCGAGAAGGGAGAAGCTGCACTGACGGAGGATGACATCCGGGGCTTTGTGCGCCAAGAGATGAGTCAGCACTGTGCCTGCCAGGGCCAGTTCATCGCATCTGGATCACGACCCCTCCCTAGTTATGCTGCAGACACTGCCGGCTCCCAGCTCCATGCTGTGCCTGTGCTCCGCGTCTCTCATGCAGAGGAGGAAGAGCGGGTACCCCCTGAGGATGATGAGTACTCTGAATACTCCGAGTATTCTGTGGAGGAGTACCAGGACCCTGAAGCTCCTTGGGATAGTGATGACCCCTGTTCCCTGCCACTGGATGAGGGCTCCTGCACTGCCTACACCCTGCGCTGGTACCATCGGGCTGTGACAGGCAGCACAGAGGCCTGTCACCCTTTTGTCTATGGTGGCTGTGGAGGGAATGCCAACCGTTTTGGGACCCGTGAGGCCTGCGAGCGCCGCTGCCCACCCCGGGTGGTCCAGAGCCAGGGGACAGGTACTGCCCAGGACTGA
人VII型胶原的氨基酸序列(2944 AA) (SEQ ID NO: 2)
MTLRLLVAALCAGILAEAPRVRAQHRERVTCTRLYAADIVFLLDGSSSIGRSNFREVRSFLEGLVLPFSGAASAQGVRFATVQYSDDPRTEFGLDALGSGGDVIRAIRELSYKGGNTRTGAAILHVADHVFLPQLARPGVPKVCILITDGKSQDLVDTAAQRLKGQGVKLFAVGIKNADPEELKRVASQPTSDFFFFVNDFSILRTLLPLVSRRVCTTAGGVPVTRPPDDSTSAPRDLVLSEPSSQSLRVQWTAASGPVTGYKVQYTPLTGLGQPLPSERQEVNVPAGETSVRLRGLRPLTEYQVTVIALYANSIGEAVSGTARTTALEGPELTIQNTTAHSLLVAWRSVPGATGYRVTWRVLSGGPTQQQELGPGQGSVLLRDLEPGTDYEVTVSTLFGRSVGPATSLMARTDASVEQTLRPVILGPTSILLSWNLVPEARGYRLEWRRETGLEPPQKVVLPSDVTRYQLDGLQPGTEYRLTLYTLLEGHEVATPATVVPTGPELPVSPVTDLQATELPGQRVRVSWSPVPGATQYRIIVRSTQGVERTLVLPGSQTAFDLDDVQAGLSYTVRVSARVGPREGSASVLTVRREPETPLAVPGLRVVVSDATRVRVAWGPVPGASGFRISWSTGSGPESSQTLPPDSTATDITGLQPGTTYQVAVSVLRGREEGPAAVIVARTDPLGPVRTVHVTQASSSSVTITWTRVPGATGYRVSWHSAHGPEKSQLVSGEATVAELDGLEPDTEYTVHVRAHVAGVDGPPASVVVRTAPEPVGRVSRLQILNASSDVLRITWVGVTGATAYRLAWGRSEGGPMRHQILPGNTDSAEIRGLEGGVSYSVRVTALVGDREGTPVSIVVTTPPEAPPALGTLHVVQRGEHSLRLRWEPVPRAQGFLLHWQPEGGQEQSRVLGPELSSYHLDGLEPATQYRVRLSVLGPAGEGPSAEVTARTESPRVPSIELRVVDTSIDSVTLAWTPVSRASSYILSWRPLRGPGQEVPGSPQTLPGISSSQRVTGLEPGVSYIFSLTPVLDGVRGPEASVTQTPVCPRGLADVVFLPHATQDNAHRAEATRRVLERLVLALGPLGPQAVQVGLLSYSHRPSPLFPLNGSHDLGIILQRIRDMPYMDPSGNNLGTAVVTAHRYMLAPDAPGRRQHVPGVMVLLVDEPLRGDIFSPIREAQASGLNVVMLGMAGADPEQLRRLAPGMDSVQTFFAVDDGPSLDQAVSGLATALCQASFTTQPRPEPCPVYCPKGQKGEPGEMGLRGQVGPPGDPGLPGRTGAPGPQGPPGSATAKGERGFPGADGRPGSPGRAGNPGTPGAPGLKGSPGLPGPRGDPGERGPRGPKGEPGAPGQVIGGEGPGLPGRKGDPGPSGPPGPRGPLGDPGPRGPPGLPGTAMKGDKGDRGERGPPGPGEGGIAPGEPGLPGLPGSPGPQGPVGPPGKKGEKGDSEDGAPGLPGQPGSPGEQGPRGPPGAIGPKGDRGFPGPLGEAGEKGERGPPGPAGSRGLPGVAGRPGAKGPEGPPGPTGRQGEKGEPGRPGDPAVVGPAVAGPKGEKGDVGPAGPRGATGVQGERGPPGLVLPGDPGPKGDPGDRGPIGLTGRAGPPGDSGPPGEKGDPGRPGPPGPVGPRGRDGEVGEKGDEGPPGDPGLPGKAGERGLRGAPGVRGPVGEKGDQGDPGEDGRNGSPGSSGPKGDRGEPGPPGPPGRLVDTGPGAREKGEPGDRGQEGPRGPKGDPGLPGAPGERGIEGFRGPPGPQGDPGVRGPAGEKGDRGPPGLDGRSGLDGKPGAAGPSGPNGAAGKAGDPGRDGLPGLRGEQGLPGPSGPPGLPGKPGEDGKPGLNGKNGEPGDPGEDGRKGEKGDSGASGREGRDGPKGERGAPGILGPQGPPGLPGPVGPPGQGFPGVPGGTGPKGDRGETGSKGEQGLPGERGLRGEPGSVPNVDRLLETAGIKASALREIVETWDESSGSFLPVPERRRGPKGDSGEQGPPGKEGPIGFPGERGLKGDRGDPGPQGPPGLALGERGPPGPSGLAGEPGKPGIPGLPGRAGGVGEAGRPGERGERGEKGERGEQGRDGPPGLPGTPGPPGPPGPKVSVDEPGPGLSGEQGPPGLKGAKGEPGSNGDQGPKGDRGVPGIKGDRGEPGPRGQDGNPGLPGERGMAGPEGKPGLQGPRGPPGPVGGHGDPGPPGAPGLAGPAGPQGPSGLKGEPGETGPPGRGLTGPTGAVGLPGPPGPSGLVGPQGSPGLPGQVGETGKPGAPGRDGASGKDGDRGSPGVPGSPGLPGPVGPKGEPGPTGAPGQAVVGLPGAKGEKGAPGGLAGDLVGEPGAKGDRGLPGPRGEKGEAGRAGEPGDPGEDGQKGAPGPKGFKGDPGVGVPGSPGPPGPPGVKGDLGLPGLPGAPGVVGFPGQTGPRGEMGQPGPSGERGLAGPPGREGIPGPLGPPGPPGSVGPPGASGLKGDKGDPGVGLPGPRGERGEPGIRGEDGRPGQEGPRGLTGPPGSRGERGEKGDVGSAGLKGDKGDSAVILGPPGPRGAKGDMGERGPRGLDGDKGPRGDNGDPGDKGSKGEPGDKGSAGLPGLRGLLGPQGQPGAAGIPGDPGSPGKDGVPGIRGEKGDVGFMGPRGLKGERGVKGACGLDGEKGDKGEAGPPGRPGLAGHKGEMGEPGVPGQSGAPGKEGLIGPKGDRGFDGQPGPKGDQGEKGERGTPGIGGFPGPSGNDGSAGPPGPPGSVGPRGPEGLQGQKGERGPPGERVVGAPGVPGAPGERGEQGRPGPAGPRGEKGEAALTEDDIRGFVRQEMSQHCACQGQFIASGSRPLPSYAADTAGSQLHAVPVLRVSHAEEEERVPPEDDEYSEYSEYSVEEYQDPEAPWDSDDPCSLPLDEGSCTAYTLRWYHRAVTGSTEACHPFVYGGCGGNANRFGTREACERRCPPRVVQSQGTGTAQD*
在一个实施方案中,COL7A1基因包含核酸序列或由核酸序列组成,所述核酸序列与SEQ ID NO: 1的核酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多的序列同一性。在一个不同的实施方案中,COL7A1基因包含核酸序列或由核酸序列组成,其中0至30、0至20、0至10、0至5、0至3、0至2或0至1个碱基相对于SEQ ID NO: 1的核酸序列被缺失、取代或添加。在一个进一步的实施方案中,COL7A1基因包含SEQ ID NO: 1的核酸序列或由SEQ ID NO: 1的核酸序列组成。
在一个实施方案中,VII型胶原包含氨基酸序列或由氨基酸序列组成,所述氨基酸序列与SEQ ID NO: 2的氨基酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多的序列同一性。在一个不同的实施方案中,VII型胶原包含氨基酸序列或由氨基酸序列组成,其中0至30、0至20、0至10、0至5、0至3、0至2或0至1个氨基酸残基相对于SEQ ID NO: 2的氨基酸序列被缺失、取代或添加。在一个进一步的实施方案中,VII型胶原包含SEQ ID NO:2的氨基酸序列或由SEQ ID NO: 2的氨基酸序列组成。
在一个实施方案中,COL7A1基因包含核酸序列或由核酸序列组成,所述核酸序列编码与SEQ ID NO: 2的氨基酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多的序列同一性的氨基酸序列。在一个不同的实施方案中,COL7A1基因包含编码氨基酸序列的核酸序列或由编码氨基酸序列的核酸序列组成,所述氨基酸序列中0至30、0至20、0至10、0至5、0至3、0至2或0至1个氨基酸残基相对于SEQ ID NO: 2的氨基酸序列被缺失、取代或添加。
如本文使用的,关于核酸序列或氨基酸序列的术语“序列同一性”意指在待比较的整个序列区域上,最佳比对(比对至最大匹配)的两个序列之间匹配的碱基或氨基酸残基的比例。待比较的序列可以在两个序列的最佳比对中具有添加或缺失(例如,缺口)。可以使用公共数据库(例如,DDBJ(http://www.ddbj.nig.ac.jp))中提供的程序,如FASTA、BLAST或CLUSTAL W来计算序列同一性。可替代地,可以使用商购可得的序列分析软件(例如,VectorNTI®软件、GENETYX®版本12)来获得序列同一性。
细胞可以通过任何方法进行遗传修饰。在一个实施方案中,细胞通过基因组编辑例如CRISPR系统(例如,CRISPR/Cas9、CRISPR/Cpf1)、TALEN或ZFN进行遗传修饰。在一个不同的实施方案中,细胞通过病毒载体例如逆转录病毒载体、慢病毒载体、腺病毒载体或腺相关病毒载体进行遗传修饰。在一个进一步的实施方案中,细胞通过CRISPR/Cas9进行遗传修饰。在一个进一步的实施方案中,细胞通过逆转录病毒载体或慢病毒载体进行遗传修饰。
在基因组编辑中,在基因组中引起切割并且将包含目的序列的供体载体引入细胞内,可以将目的序列插入基因组的切割位点内。待插入基因组内的序列可以是COL7A1基因或待替换COL7A1基因中含有突变的部分的序列(例如COL7A1基因的部分序列)。除目的序列之外,供体载体可以包含控制目的序列表达的调控序列例如启动子或增强子,或其它元件例如用于细胞选择的药物抗性基因,并且还可以在两端处包含与基因组的插入位点的两端同源的序列。作为非同源末端结合或同源重组的结果,可以将供体载体引入所需位点内。作为供体载体,可以使用质粒、腺相关病毒载体、整合酶缺陷型慢病毒载体或任何其它病毒载体。
在CRISPR系统中,核酸内切酶例如Cas9或Cas12(例如Cas12a(也称为Cpf1)、Cas12b、Cas12e)识别称为PAM序列的特异性碱基序列,并且靶DNA的双链通过核酸内切酶的作用进行切割。当核酸内切酶是Cas9时,它切割PAM序列上游约3-4个碱基。核酸内切酶的实例包括化脓性链球菌(S. pyogenes)、金黄色葡萄球菌(S. aureus)、脑膜炎奈瑟球菌(N.meningitidis)、嗜热链球菌(S. thermophilus)或齿垢密螺旋体(T. denticola)的Cas9,以及毛螺菌科细菌ND2006(L. bacterium ND2006)或氨基酸球菌属(Acidaminococcus)物种BV3L6的Cpfl。PAM序列取决于核酸内切酶而变,并且例如化脓性链球菌中Cas9的PAM序列为NGG。gRNA在5'端侧包含PAM序列(靶序列)上游约20个碱基的序列或与其互补的序列,并且发挥将核酸内切酶募集到靶序列的作用。gRNA的除靶序列(或与其互补的序列)外的序列,可以由本领域技术人员根据待使用的核酸内切酶适当地确定。gRNA可以包含crRNA(CRISPR RNA),其包含靶序列或与其互补的序列,并且负责gRNA的序列特异性,以及tracrRNA(反式激活crRNA),其通过形成双链促成与Cas9的复合物形成。crRNA和tracrRNA可以作为分开的分子存在。当核酸内切酶是Cpf1时,单独的crRNA充当gRNA。在本说明书中,在单链上包含充当gRNA所必需的元件的gRNA可以特别地被称为sgRNA。gRNA序列可以通过可用于靶序列选择和gRNA设计的工具来确定,所述工具例如CRISPRdirect (https://crispr.dbcls.jp/)。
可以将包含编码gRNA的核酸序列和编码核酸内切酶的核酸序列的载体引入细胞内并且在细胞中表达,或者可以将已细胞外制备的gRNA和核酸内切酶蛋白引入细胞内。核酸内切酶可以包括核定位信号。编码gRNA的核酸序列和编码核酸内切酶的核酸序列可以存在于不同的载体上。用于将载体、gRNA和核酸内切酶引入细胞内的方法包括但不限于脂质转染、电穿孔、显微注射、磷酸钙法和DEAE-葡聚糖法。
本公开内容提供了可以用于将COL7A1基因引入基因组内的gRNA和包含编码gRNA的核酸序列的载体。在一个实施方案中,gRNA包含SEQ ID NO: 3-5中任一者的序列或与其互补的序列。
在病毒载体的情况下,当使用具有整合酶活性的逆转录病毒载体或慢病毒载体时,可以将COL7A1基因引入细胞的基因组内。可替代地,可以使用整合酶缺陷型逆转录病毒或慢病毒载体。整合酶缺陷型载体缺乏整合酶活性,例如,由于整合酶基因中的突变。当使用整合酶缺陷型载体、或腺病毒载体或腺相关病毒载体时,掺入载体内的序列通常不被引入细胞的基因组内。例如,当COL7A1基因掺入整合酶缺陷型慢病毒载体或腺病毒载体内时,VII型胶原从存在于细胞中(核中)的载体的COL7A1基因表达。
病毒载体包含编码COL7A1基因的序列,并且可以含有控制COL7A1基因表达的调控序列例如启动子或增强子,以及其它元件例如用于细胞选择的药物抗性基因。病毒载体可以通过本领域已知的任何方法来制备。例如,可以通过将病毒载体质粒(其包含在两端处的LTR序列(5' LTR和3' LTR)、包装信号和目的序列)与表达病毒的结构蛋白(如Gag、Pol和Env)的一种或多种质粒载体一起引入包装细胞内、或引入表达此类结构蛋白的包装细胞内,来制备逆转录病毒或慢病毒载体。包装细胞的实例包括但不限于293T细胞、293细胞、HeLa细胞、COS1细胞和COS7细胞。病毒载体可以是假型的,并且可以表达包膜蛋白例如水疱性口炎病毒G蛋白(VSV-G)。通过用如此制备的病毒载体感染靶细胞,可以将目的序列引入靶细胞内。
在一个实施方案中,病毒载体是慢病毒载体。慢病毒载体的实例包括但不限于HIV(人免疫缺陷病毒)(例如HIV-1和HIV-2)、SIV(猴免疫缺陷病毒)、FIV(猫免疫缺陷病毒)、MVV(梅迪-维斯纳病毒(Maedi-Visna virus))、EV1(梅迪-维斯纳样病毒)、EIAV(马传染性贫血病毒)和CAEV(山羊关节炎脑炎病毒)。在一个实施方案中,慢病毒载体是HIV。
作为一个实例,可以如下制备慢病毒载体。首先,将编码病毒基因组的病毒载体质粒,表达Gag、Pol和Rev(以及任选的Tat)的一种或多种质粒载体,以及表达包膜蛋白例如VSV-G的一种或多种质粒载体引入包装细胞内。病毒载体质粒包含在两端处的LTR序列(5'LTR和3' LTR)、包装信号、以及COL7A1基因和控制其表达的启动子(例如CMV启动子、EF1α启动子或hCEF启动子)。5' LTR充当诱导病毒RNA基因组转录的启动子,但可以替换为不同的启动子例如CMV启动子,以增强RNA基因组的表达。在细胞内,病毒RNA基因组从载体质粒转录并包装以形成病毒核心。病毒核心被转运到包装细胞的细胞膜,包封在细胞膜中,并且作为病毒颗粒从包装细胞中释放。释放的病毒颗粒可以从包装细胞的培养上清液中回收。例如,病毒颗粒可以通过常规纯化方法如离心、过滤器过滤和柱纯化中的任一种来回收。慢病毒载体也可以通过使用试剂盒例如Lentiviral High Titer Packaging Mix,Lenti-XTMPackaging Single Shots (Takara Bio Inc.)、以及ViraSafeTM Lentivirus CompleteExpression System (Cell Biolabs Inc.)进行制备。腺相关病毒载体可以通过使用试剂盒例如AAVpro® Helper Free System (Takara Bio Inc.)进行制备。
可以通过DNA印迹或PCR检测目的序列已引入其内的细胞。目的序列只需要被引入至少一个等位基因内。
在本公开内容的组合物的一个实施方案中,间充质干细胞是组合物中最丰富的细胞。在一个进一步的实施方案中,间充质干细胞占组合物中包含的细胞的70%、80%、85%、90%、95%、96%、97%、98%或99%或更多。在一个进一步的实施方案中,本公开内容的组合物基本上不含除间充质干细胞外的细胞。表述“基本上不含除间充质干细胞外的细胞”意指组合物仅包含通过方法获得的细胞,所述方法是本领域技术人员通常理解为用于获得间充质干细胞的方法。
组合物中包含的细胞数目是发挥所需效应所需要的量(本文中也称为有效量),并且由本领域技术人员考虑因素例如患者的年龄、体重和医学状况,细胞类型和用于遗传修饰的方法而适当地确定。细胞的数目并不限于,但可以是例如1个细胞至1 × 107个细胞、1× 10个细胞至1 × 107个细胞、1 × 102个细胞至1 × 107个细胞、1 × 103个细胞至1× 107个细胞、1 × 104个细胞至1 × 107个细胞、1 × 105个细胞至1 × 107个细胞、1 ×105个细胞至5 × 106个细胞、5 × 105个细胞至1 × 106个细胞、或1 × 105个细胞至1 ×106个细胞。除细胞之外,组合物还可以包含药学上可接受的载体和/或添加剂。药学上可接受的载体的实例包括水、培养基、盐水、含有葡萄糖、D-山梨糖醇、D-甘露糖醇等的输液、以及磷酸盐缓冲盐水(PBS)。添加剂的实例包括增溶剂、稳定剂和防腐剂。组合物的剂型并无特别限制,但可以是肠胃外制剂例如注射剂。注射剂的实例包括溶液注射剂、悬浮液注射剂、乳状液注射剂和待使用前制备的注射剂。组合物可以是冷冻的,并且可以含有冷冻保护剂,例如DMSO、甘油、聚乙烯吡咯烷酮、聚乙二醇、葡聚糖或蔗糖。
本公开内容的组合物可以全身或局部施用。在一个实施方案中,将组合物施用于营养不良型大疱性表皮松解症的患者的受影响区域。如本文使用的,受影响的区域意指水疱或在水疱附近的区域。在一个进一步的实施方案中,将组合物在水疱的部位处皮内施用或施用到水疱内。在一个进一步的实施方案中,将组合物施用到水疱内。在本说明书中,施用到水疱内意指施用于水疱的表皮下的空间。与皮内或皮下施用相比,水疱内施用可以减轻患者的痛苦,并且VII型胶原可以在基底膜附近良好地表达。每个部位施用的细胞数目是发挥所需效应所需要的量(有效量),并且由本领域技术人员考虑因素例如患者的年龄、体重和医学状况,细胞类型和用于遗传修饰的方法而适当地确定。细胞的数目并不限于,但可以是例如1个细胞至1 × 107个细胞、1 × 10个细胞至1 × 107个细胞、1 × 102个细胞至1 × 107个细胞、1 × 103个细胞至1 × 107个细胞、1 × 104个细胞至1 × 107个细胞、1× 105个细胞至1 × 107个细胞、1 × 105个细胞至5 × 106个细胞、5 × 105个细胞至1× 106个细胞、或1 × 105个细胞至1 × 106个细胞。在一个实施方案中,每个水疱待施用的细胞数目为1个细胞至1 × 107个细胞、1 × 10个细胞至1 × 107个细胞、1 × 102个细胞至1 × 107个细胞、1 × 103个细胞至1 × 107个细胞、1 × 104个细胞至1 × 107个细胞、1 × 105个细胞至1 × 107个细胞、1 × 105个细胞至5 × 106个细胞、5 × 105个细胞至1 × 106个细胞、或1 × 105个细胞至1 × 106个细胞。当对于圆形近似时具有7至8 mm直径的标准水疱考虑上述量时,可以根据水疱的大小调整每个水疱待施用的量。
下文描述了本发明的示例性实施方案。
[1]一种用于治疗营养不良型大疱性表皮松解症的组合物,其包含从营养不良型大疱性表皮松解症患者获得的细胞,其中所述细胞是间充质干细胞,并且被遗传修饰以产生VII型胶原。
[2]根据项目1的组合物,其中所述细胞通过引入COL7A1基因进行遗传修饰。
[3]根据项目2的组合物,其中将所述COL7A1基因引入细胞的基因组内。
[4]根据项目2或3的组合物,其中所述COL7A1基因包含与SEQ ID NO: 1的核酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的核酸序列,或者编码与SEQ ID NO: 2的氨基酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的氨基酸序列的核酸序列。
[5]根据项目1至4中任一项的组合物,其中所述间充质干细胞是骨髓衍生的间充质干细胞。
[6]根据项目1至5中任一项的组合物,其中所述间充质干细胞是组合物中最丰富的细胞。
[7]根据项目1至6中任一项的组合物,其中所述间充质干细胞占组合物中包含的细胞的70%、80%、85%、90%、95%、96%、97%、98%或99%或更多。
[8]根据项目1至7中任一项的组合物,其中所述组合物基本上不含除间充质干细胞外的细胞。
[9]根据项目1至8中任一项的组合物,其待施用于受影响的区域。
[10]根据项目1至9中任一项的组合物,其待施用到水疱内。
[11]根据项目1至10中任一项的组合物,其中所述细胞通过基因组编辑进行遗传修饰。
[12]根据项目11的组合物,其中所述基因组编辑通过CRISPR/Cas9进行。
[13]根据项目1至10中任一项的组合物,其中所述细胞通过病毒载体进行遗传修饰。
[14]根据项目13的组合物,其中所述病毒载体是逆转录病毒载体或慢病毒载体。
[15]根据项目13或14的组合物,其中所述病毒载体是慢病毒载体。
[16]一种用于治疗营养不良型大疱性表皮松解症的组合物,其包含产生VII型胶原的细胞,其中所述组合物待施用到水疱内。
[17]根据项目16的组合物,其中所述细胞是被遗传修饰以产生VII型胶原的细胞。
[18]根据项目17的组合物,其中所述细胞通过引入COL7A1基因进行遗传修饰。
[19]根据项目18的组合物,其中将所述COL7A1基因引入细胞的基因组内。
[20]根据项目18或19的组合物,其中所述COL7A1基因包含与SEQ ID NO: 1的核酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的核酸序列,或者编码与SEQ ID NO: 2的氨基酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的氨基酸序列的核酸序列。
[21]根据项目17至20中任一项的组合物,其中所述细胞是从营养不良型大疱性表皮松解症患者获得的细胞。
[22]根据项目16至21中任一项的组合物,其中所述细胞是从骨髓获得的细胞。
[23]根据项目16至22中任一项的组合物,其中所述细胞是间充质干细胞。
[24]根据项目23的组合物,其中所述间充质干细胞是骨髓衍生的间充质干细胞。
[25]根据项目23或24的组合物,其中所述间充质干细胞是组合物中最丰富的细胞。
[26]根据项目23至25中任一项的组合物,其中所述间充质干细胞占组合物中包含的细胞的70%、80%、85%、90%、95%、96%、97%、98%或99%或更多。
[27]根据项目23至26中任一项的组合物,其中所述组合物基本上不含除间充质干细胞外的细胞。
[28]根据项目17至27中任一项的组合物,其中所述细胞通过基因组编辑进行遗传修饰。
[29]根据项目28的组合物,其中所述基因组编辑通过CRISPR/Cas9进行。
[30]根据项目17至27中任一项的组合物,其中所述细胞通过病毒载体进行遗传修饰。
[31]根据项目30的组合物,其中所述病毒载体是逆转录病毒载体或慢病毒载体。
[32]根据项目30或31的组合物,其中所述病毒载体是慢病毒载体。
[33]一种生产用于治疗营养不良型大疱性表皮松解症的组合物的方法,其包括
对细胞进行遗传修饰以产生VII型胶原,和,
制备包含遗传修饰的细胞的组合物。
[34]一种治疗营养不良型大疱性表皮松解症的方法,其包括向营养不良型大疱性表皮松解症患者施用包含产生VII型胶原的细胞的组合物。
[35]根据项目34的方法,其中所述细胞被遗传修饰以产生VII型胶原。
[36]根据项目35的方法,其中所述细胞通过引入COL7A1基因进行遗传修饰。
[37]根据项目36的方法,其中将所述COL7A1基因引入细胞的基因组内。
[38]根据项目36或37的组合物,其中所述COL7A1基因包含与SEQ ID NO: 1的核酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的核酸序列,或者编码与SEQ ID NO: 2的氨基酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的氨基酸序列的核酸序列。
[39]根据项目35至38中任一项的方法,其中所述细胞通过基因组编辑进行遗传修饰。
[40]根据项目39的方法,其中所述基因组编辑通过CRISPR/Cas9进行。
[41]根据项目35至38中任一项的方法,其中所述细胞通过病毒载体进行遗传修饰。
[42]根据项目41的方法,其中所述病毒载体是逆转录病毒载体或慢病毒载体。
[43]根据项目41或42的方法,其中所述病毒载体是慢病毒载体。
[44]根据项目35至43中任一项的方法,其进一步包括,在施用于患者之前,对细胞进行遗传修饰以产生VII型胶原。
[45]根据项目33或44的方法,其包括通过引入COL7A1基因对细胞进行遗传修饰。
[46]根据项目45的方法,其包括将COL7A1基因引入细胞的基因组内。
[47]根据项目45或46的方法,其中所述COL7A1基因包含与SEQ ID NO: 1的核酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的核酸序列,或者编码与SEQ ID NO: 2的氨基酸序列具有70%、80%、85%、90%、95%、96%、97%、98%或99%或更多序列同一性的氨基酸序列的核酸序列。
[48]根据项目33和44至47中任一项的方法,其包括通过基因组编辑对细胞进行遗传修饰。
[49]根据项目48的方法,其中所述基因组编辑通过CRISPR/Cas9进行。
[50]根据项目33和44至47中任一项的方法,其包括用病毒载体对细胞进行遗传修饰。
[51]根据项目50的方法,其中所述病毒载体是逆转录病毒载体或慢病毒载体。
[52]根据项目50或51的方法,其中所述病毒载体是慢病毒载体。
[53]根据项目33至52中任一项的方法,其中所述细胞是从营养不良型大疱性表皮松解症患者获得的细胞。
[54]根据项目33和44至53中任一项的方法,其进一步包括,在遗传修饰之前,从营养不良型大疱性表皮松解症患者获得细胞。
[55]根据项目33至54中任一项的方法,其中所述细胞是从骨髓获得的细胞。
[56]根据项目33至55中任一项的方法,其中所述细胞是间充质干细胞。
[57]根据项目56的方法,其中所述间充质干细胞是骨髓衍生的间充质干细胞。
[58]根据项目56或57的方法,其中所述间充质干细胞是组合物中最丰富的细胞。
[59]根据项目56至58中任一项的方法,其中所述间充质干细胞占组合物中包含的细胞的70%、80%、85%、90%、95%、96%、97%、98%或99%或更多。
[60]根据项目56至59中任一项的方法,其中所述组合物基本上不含除间充质干细胞外的细胞。
[61]根据项目34至60中任一项的方法,其包括将所述组合物施用于受感染的区域。
[62]根据项目34至61中任一项的方法,其包括将所述组合物施用到水疱内。
[63]包含从营养不良型大疱性表皮松解症患者获得的细胞的组合物用于制造用于治疗营养不良型大疱性表皮松解症的药物的用途,其中所述细胞包含间充质干细胞,并且所述细胞被遗传修饰以产生VII型胶原。
[64]包含产生VII型胶原的细胞的组合物用于制造用于治疗营养不良型大疱性表皮松解症的药物的用途,其中所述组合物待施用到水疱内。
[65]包含从营养不良型大疱性表皮松解症患者获得的细胞的组合物用于治疗营养不良型大疱性表皮松解症的用途,其中所述细胞包含间充质干细胞,并且所述细胞被遗传修饰以产生VII型胶原。
[66]包含产生VII型胶原的细胞的组合物用于治疗营养不良型大疱性表皮松解症的用途,其中所述组合物待施用到水疱内。
[67]一种gRNA,其包含SEQ ID NO: 3至5中任何一个的序列或与其互补的序列。
[68]一种载体,其包含编码项目67的gRNA的核酸序列。
本发明在下文参考实施例更详细地进行描述,但不限于下文描述的实施方案。
实施例
1. 基因组编辑的设计
制备三种类型的sgRNA,以便在人基因组中的AAVS1(腺相关病毒整合位点1)区域中选择CRISPR-Cas9系统切割效率良好的位点。AAVS1区域是不易受基因转移影响的安全区域(安全港)。由于CRISPR-Cas9系统识别"NGG"的碱基序列并且切割该序列上游的3个碱基,因此选择各自在端部处具有"GG"的区域,并且设计各自含有在"NGG"上游的20个碱基的序列的sgRNA(sgAAVS1-#1至#3)(图1,顶部;表1)。
表1
| sgRNA | 靶序列 | SEQ ID NO. |
| sgAAVS1-#1 | ACCCCACAGTGGGGCCACTA | 3 |
| sgAAVS1-#2 | GTCACCAATCCTGTCCCTAG | 4 |
| sgAAVS1-#3 | GGGGCCACTAGGGACAGGAT | 5 |
将由SEQ ID NO: 3至5中任何一个的序列组成的寡核苷酸与其互补链退火,并且克隆到eSpCas9(1.1)(Addgene质粒# 71814)的Bbs1位点内。通过Lipofectamin 3000(Thermo Fisher Scientific),将该质粒(2.5 μg)引入接种于6孔皿中的HEK293细胞(人胎肾细胞系)内。在转染后48小时,从细胞中提取基因组DNA,并且通过PCR扩增含有靶位点的区域。使PCR扩增的片段经受热处理以成为单链,通过缓慢冷却退火,然后用错配位点特异性核酸内切酶处理。所得到的产物通过电泳进行分级,从条带的密度测量通过基因组切割引入的插入或缺失突变的程度,并且通过下式计算基因组编辑效率(在式中,"a"指示未消化条带的浓度,并且"b"和"c"指示切割条带的浓度)。
sgAAVS1-#1至#3的所有sgRNA都产生了与对照不同的短DNA片段,确认发生了双链断裂(图1,底部)。在下述实验中,使用了具有最高切割效率的sgAAVS1-#3。
2. 将COL7A1基因引入BM-MSC内
为了将COL7A1基因引入AAVS1区域内,设计了在CAG启动子的控制下表达COL7A1基因的质粒(图2)。COL7A1 cDNA得自Flexi ORF序列验证的克隆(Promega,Madison,WI,USA)。将COL7A1 cDNA亚克隆到pENTR1A质粒(ThermoFisher Scientific )内,以制备pENTR1A-COL7A1,并且通过使用LR重组酶(ThermoFisher Scientific )以及pAAVS-P-CAG-DEST(Addgene质粒# 80490)和pENTR1A-COL7A1获得pAAVS-P-CAG-COL7A1。
由于随着质粒的量相对于细胞增加,转移效率增加但细胞活力降低,因此首先检查其中细胞活力和转移效率两者均良好的实验条件。对于人骨髓衍生的间充质干细胞(BM-MSC)[PromoCell(Heidelberg,德国)或Lonza(Basel,瑞士)] (1 × 105 个细胞),通过电穿孔引入pAAVS-P-CAG-COL7A1(0 μg、0.25 μg、0.5 μg或1.0 μg)和表达sgAAVS1-#3的eSpCas9(1.1)(0 μg、0.25 μg、0.5 μg或1.0 μg)。 所有细胞都在转染后24小时收集,并且从相对于细胞总数的台盼蓝染色的阳性细胞(死细胞)数目计算活力。另外,转染48小时后,将BM-MSC在含有0.5 μg/mL嘌呤霉素的培养基(Invivogen,San Diego,CA,USA)中培养约2周用于选择,并且确定分离的集落数目以测量基因组编辑的效率。基于图3中所示的结果,0.25 μg pAAVS-P-CAG-COL7A1和0.5 μg eSpCas9(1.1)用于下述实验中。
对于BM-MSC(1 × 105个细胞),通过电穿孔引入pAAVS-P-CAG-COL7A1(0.25 μg)和表达sgAAVS1-#3的eSpCas9(1.1)(0.5 μg)。转染后48小时,将BM-MSC在含有0.5 μg/mL嘌呤霉素的培养基(Invivogen,San Diego,CA,USA)中培养约2周用于选择。从BM-MSC中提取基因组DNA,并且通过PCR确认基因组编辑和COL7A1基因的引入。
PCR产物通过F1-R1之间的扩增获得,确认已发生了基因组编辑(图4,F1-R1)。另外,在F2-R2之间的PCR产物中检测到野生型(WT)中不存在的长DNA,指示引入了COL7A1基因(图4,F2-R2)。将COL7A1基因引入等位基因之一(图4,单等位基因)或两者(图4,双等位基因)内。
由于胶原是分泌蛋白并且渗出到细胞的外部,因此通过用抗VII型胶原抗体(Sigma Aldrich,St. Louis,MO,USA )的免疫染色和培养上清液的蛋白质印迹,观察到BM-MSC中VII型胶原的表达。如图5中所示,在遗传修饰的MSC中确认了VII型胶原的表达。
3. VII型胶原在大疱性表皮松解症模型小鼠中的表达
检查了接受遗传修饰的MSC的大疱性表皮松解症模型小鼠中VII型胶原的表达。切除显示发疱的新生Col7A1基因敲除小鼠(Col7a1-/-)的全层皮肤,并且移植到免疫缺陷小鼠(NOD-SCID)的背部。移植后一周,上文节段2中描述的遗传修饰的MSC用0.1至1.0 × 106个细胞进行皮下或皮内注射(图6)。对于水疱内注射,紧在移植后,将皮肤表面捏紧且摩擦以形成水疱,并且立即将0.1至1.0 × 106个遗传修饰的MSC细胞注射到表皮下的空间内。每次注射后4周,切除移植的皮肤,并且通过用抗VII型胶原抗体(Sigma Aldrich,St.Louis,MO,USA )的免疫染色,来评估VII型胶原的表达。
如图7中所示,在皮内注射和水疱内注射中在基底膜附近观察到VII型胶原的表达,但在皮内注射中的表达是部分的。在皮下注射中,胶原在与基底膜不同的深层中表达(图8)。这些结果显示了,尤其是通过水疱内注射预计极佳的疗效。
进一步地,以与上文相同的方式,将2.0 × 106个上文节段2中描述的遗传修饰的MSC细胞注射到水疱内。其后4周,切除移植的皮肤并用电子显微镜观察。确认了锚定性原纤维的形成(图9)。
Claims (16)
1.一种用于治疗营养不良型大疱性表皮松解症的组合物,其包含从营养不良型大疱性表皮松解症患者获得的细胞,其中所述细胞是间充质干细胞,并且被遗传修饰以产生VII型胶原。
2.根据权利要求1的组合物,其中所述细胞通过引入COL7A1基因进行遗传修饰。
3. 根据权利要求2的组合物,其中所述COL7A1基因包含与SEQ ID NO: 1的核酸序列具有90%或更多序列同一性的核酸序列,或者编码与SEQ ID NO: 2的氨基酸序列具有90%或更多序列同一性的氨基酸序列的核酸序列。
4.根据权利要求1至3中任一项的组合物,其中所述间充质干细胞是骨髓衍生的间充质干细胞。
5.根据权利要求1至4中任一项的组合物,其中所述间充质干细胞是组合物中最丰富的细胞。
6.根据权利要求1至5中任一项的组合物,其待施用到水疱内。
7.一种用于治疗营养不良型大疱性表皮松解症的组合物,其包含产生VII型胶原的细胞,其中所述组合物待施用到水疱内。
8.根据权利要求7的组合物,其中所述细胞是被遗传修饰以产生VII型胶原的细胞。
9.根据权利要求8的组合物,其中所述细胞通过引入COL7A1基因进行遗传修饰。
10. 根据权利要求9的组合物,其中所述COL7A1基因包含与SEQ ID NO: 1的核酸序列具有90%或更多序列同一性的核酸序列,或者编码与SEQ ID NO: 2的氨基酸序列具有90%或更多序列同一性的氨基酸序列的核酸序列。
11.根据权利要求8至10中任一项的组合物,其中所述细胞是从营养不良型大疱性表皮松解症患者获得的细胞。
12.根据权利要求7至11中任一项的组合物,其中所述细胞是从骨髓获得的细胞。
13.根据权利要求7至12中任一项的组合物,其中所述细胞是间充质干细胞。
14.根据权利要求13的组合物,其中所述间充质干细胞是骨髓衍生的间充质干细胞。
15.根据权利要求13或14的组合物,其中所述间充质干细胞是组合物中最丰富的细胞。
16. 一种gRNA,其包含SEQ ID NO: 3至5中任何一个的序列或与其互补的序列。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019007201 | 2019-01-18 | ||
| JP2019-007201 | 2019-01-18 | ||
| PCT/JP2020/001433 WO2020149395A1 (ja) | 2019-01-18 | 2020-01-17 | 栄養障害型表皮水疱症治療薬 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113646006A true CN113646006A (zh) | 2021-11-12 |
Family
ID=71613343
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202080022396.3A Pending CN113646006A (zh) | 2019-01-18 | 2020-01-17 | 用于营养不良型大疱性表皮松解症的治疗剂 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20220088083A1 (zh) |
| EP (1) | EP3912644A4 (zh) |
| JP (1) | JPWO2020149395A1 (zh) |
| KR (1) | KR20210116531A (zh) |
| CN (1) | CN113646006A (zh) |
| AU (1) | AU2020209687A1 (zh) |
| WO (1) | WO2020149395A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116555349A (zh) * | 2023-01-09 | 2023-08-08 | 中吉智药(南京)生物技术有限公司 | 一种腺相关病毒载体及其构建方法与应用 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022018884A1 (ja) * | 2020-07-22 | 2022-01-27 | 国立大学法人大阪大学 | 栄養障害型表皮水疱症の治療薬 |
| WO2023140349A1 (ja) * | 2022-01-21 | 2023-07-27 | 国立大学法人大阪大学 | 細胞シート |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105683376A (zh) * | 2013-05-15 | 2016-06-15 | 桑格摩生物科学股份有限公司 | 用于治疗遗传病状的方法和组合物 |
| WO2017161180A1 (en) * | 2016-03-18 | 2017-09-21 | Intrexon Corporation | Compositions and methods for treatment of type vii collagen deficiencies |
| WO2018007871A1 (en) * | 2016-07-08 | 2018-01-11 | Crispr Therapeutics Ag | Materials and methods for treatment of transthyretin amyloidosis |
| CN107904208A (zh) * | 2017-12-25 | 2018-04-13 | 云舟生物科技(广州)有限公司 | 细胞表型研究用的细胞克隆及其筛选方法和应用 |
| CN109072255A (zh) * | 2016-04-08 | 2018-12-21 | 克里斯托生物技术股份有限公司 | 用于治疗皮肤的伤口、病症和疾病的组合物和方法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2281050B1 (en) * | 2008-04-14 | 2014-04-02 | Sangamo BioSciences, Inc. | Linear donor constructs for targeted integration |
| RU2650819C2 (ru) * | 2012-05-07 | 2018-04-17 | Сангамо Терапьютикс, Инк. | Способы и композиции для опосредованной нуклеазой направленной интеграции трансгенов |
| US20180104186A1 (en) * | 2013-03-13 | 2018-04-19 | University Of Miami | Methods and compositions for the treatment of epidermolysis bullosa |
| BR112018013576A2 (pt) | 2016-01-04 | 2018-12-11 | Univ Leland Stanford Junior | terapia gênica para epidermólise bolhosa distrófica recessiva usando queratinócitos autólogos geneti-camente corrigidos |
| US10648002B2 (en) * | 2016-11-22 | 2020-05-12 | Regents Of The University Of Minnesota | Method for correcting a genetic sequence |
| US20190365929A1 (en) | 2017-02-22 | 2019-12-05 | Crispr Therapeutics Ag | Materials and methods for treatment of dystrophic epidermolysis bullosa (deb) and other collagen type vii alpha 1 chain (col7a1) gene related conditions or disorders |
| BR112019020294A2 (pt) * | 2017-04-07 | 2020-05-12 | StemRIM Inc. | Medicamento terapêutico para doença fibrótica |
| CA3067963A1 (en) * | 2017-06-19 | 2018-12-27 | National University Corporation Hokkaido University | Treatment agent for epidermolysis bullosa |
| JP2019007201A (ja) | 2017-06-23 | 2019-01-17 | システム計測株式会社 | 免震構造 |
| CN112218882A (zh) * | 2018-04-27 | 2021-01-12 | 西雅图儿童医院(Dba西雅图儿童研究所) | Foxp3在经编辑的cd34+细胞中的表达 |
-
2020
- 2020-01-17 JP JP2020566497A patent/JPWO2020149395A1/ja active Pending
- 2020-01-17 KR KR1020217025601A patent/KR20210116531A/ko unknown
- 2020-01-17 US US17/423,285 patent/US20220088083A1/en active Pending
- 2020-01-17 CN CN202080022396.3A patent/CN113646006A/zh active Pending
- 2020-01-17 WO PCT/JP2020/001433 patent/WO2020149395A1/ja unknown
- 2020-01-17 EP EP20741062.2A patent/EP3912644A4/en active Pending
- 2020-01-17 AU AU2020209687A patent/AU2020209687A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105683376A (zh) * | 2013-05-15 | 2016-06-15 | 桑格摩生物科学股份有限公司 | 用于治疗遗传病状的方法和组合物 |
| WO2017161180A1 (en) * | 2016-03-18 | 2017-09-21 | Intrexon Corporation | Compositions and methods for treatment of type vii collagen deficiencies |
| CN109072255A (zh) * | 2016-04-08 | 2018-12-21 | 克里斯托生物技术股份有限公司 | 用于治疗皮肤的伤口、病症和疾病的组合物和方法 |
| WO2018007871A1 (en) * | 2016-07-08 | 2018-01-11 | Crispr Therapeutics Ag | Materials and methods for treatment of transthyretin amyloidosis |
| CN107904208A (zh) * | 2017-12-25 | 2018-04-13 | 云舟生物科技(广州)有限公司 | 细胞表型研究用的细胞克隆及其筛选方法和应用 |
Non-Patent Citations (2)
| Title |
|---|
| ANASTASIA PETROVA 等: "Lentiviral mediated collagen VII expression in allogeneic MSCs restores anchoring fibrils in a recessive dystrophic epidermolysis bullosa skin graft model", MOLECULAR THERAPY, vol. 26, no. 5, pages 123 - 124, XP055950939 * |
| TOBIAS KÜHL 等: "High Local Concentrations of Intradermal MSCs Restore Skin Integrity and Facilitate Wound Healing in Dystrophic Epidermolysis Bullosa", MOLECULAR THERAPY, vol. 23, no. 8, pages 3 - 5 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116555349A (zh) * | 2023-01-09 | 2023-08-08 | 中吉智药(南京)生物技术有限公司 | 一种腺相关病毒载体及其构建方法与应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220088083A1 (en) | 2022-03-24 |
| AU2020209687A1 (en) | 2021-07-29 |
| EP3912644A4 (en) | 2022-09-28 |
| KR20210116531A (ko) | 2021-09-27 |
| JPWO2020149395A1 (ja) | 2021-11-25 |
| EP3912644A1 (en) | 2021-11-24 |
| WO2020149395A1 (ja) | 2020-07-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7158427B2 (ja) | ヘモグロビン異常症を処置するためのグロビン遺伝子療法 | |
| US20200155606A1 (en) | Crispr/rna-guided nuclease systems and methods | |
| EP3684924B1 (en) | Non-integrating dna vectors for the genetic modification of cells | |
| US20220088083A1 (en) | Composition for use in treating dystrophic epidermolysis bullosa | |
| US20220073951A1 (en) | Systems and methods for the treatment of hemoglobinopathies | |
| US20200291433A1 (en) | Globin gene therapy for treating hemoglobinopathies | |
| JP2023033551A (ja) | ヘモグロビン異常症を治療するためのベクターおよび組成物 | |
| US20240139254A1 (en) | Mesenchymal stem cell having oxidative stress resistance, preparation method therefor, and use thereof | |
| US11261441B2 (en) | Vectors and compositions for treating hemoglobinopathies | |
| WO2019060297A1 (en) | MITOCHONDRIAL REJUVENATION AS A TREATMENT FOR AGE-RELATED AND NEURODEGENERATIVE CONDITIONS | |
| US20210230638A1 (en) | Systems and methods for the treatment of hemoglobinopathies | |
| WO2022018884A1 (ja) | 栄養障害型表皮水疱症の治療薬 | |
| US20200263206A1 (en) | Targeted integration systems and methods for the treatment of hemoglobinopathies | |
| US20240124869A1 (en) | Curing disease by transcription regulatory gene editing | |
| WO2020177618A1 (en) | Recombinant vectors comprising arylsulfatase a and their uses in stem cell therapy for the treatment of metachromatic leukodystrophy | |
| CA3226445A1 (en) | Hepatitis b virus (hbv) knockouts | |
| Papanikolaou et al. | Genetic manipulation of stem cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |