CN113490854A - 微流体设备及试样分析方法 - Google Patents
微流体设备及试样分析方法 Download PDFInfo
- Publication number
- CN113490854A CN113490854A CN202080015365.5A CN202080015365A CN113490854A CN 113490854 A CN113490854 A CN 113490854A CN 202080015365 A CN202080015365 A CN 202080015365A CN 113490854 A CN113490854 A CN 113490854A
- Authority
- CN
- China
- Prior art keywords
- cover member
- microfluidic device
- less
- microwell array
- resin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000012284 sample analysis method Methods 0.000 title claims abstract description 17
- 239000007788 liquid Substances 0.000 claims description 55
- 238000000034 method Methods 0.000 claims description 41
- 238000006243 chemical reaction Methods 0.000 claims description 33
- 238000001514 detection method Methods 0.000 claims description 25
- 230000003746 surface roughness Effects 0.000 claims description 23
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 18
- 230000002209 hydrophobic effect Effects 0.000 claims description 15
- 230000000903 blocking effect Effects 0.000 claims description 14
- 239000011248 coating agent Substances 0.000 claims description 13
- 108090000623 proteins and genes Proteins 0.000 claims description 12
- 238000000576 coating method Methods 0.000 claims description 11
- 102000004169 proteins and genes Human genes 0.000 claims description 11
- 238000010438 heat treatment Methods 0.000 claims description 7
- 241000894006 Bacteria Species 0.000 claims description 4
- 150000002632 lipids Chemical class 0.000 claims description 4
- 229920005989 resin Polymers 0.000 description 58
- 239000011347 resin Substances 0.000 description 58
- 239000010410 layer Substances 0.000 description 55
- 239000000758 substrate Substances 0.000 description 53
- 239000000523 sample Substances 0.000 description 46
- 239000003153 chemical reaction reagent Substances 0.000 description 44
- 238000001179 sorption measurement Methods 0.000 description 30
- 239000000463 material Substances 0.000 description 27
- 230000002093 peripheral effect Effects 0.000 description 26
- 238000005259 measurement Methods 0.000 description 23
- 230000000052 comparative effect Effects 0.000 description 14
- 102000004190 Enzymes Human genes 0.000 description 12
- 108090000790 Enzymes Proteins 0.000 description 12
- 108020004414 DNA Proteins 0.000 description 11
- 229920000089 Cyclic olefin copolymer Polymers 0.000 description 10
- 238000002073 fluorescence micrograph Methods 0.000 description 9
- -1 polydimethylsiloxane Polymers 0.000 description 9
- 239000000203 mixture Substances 0.000 description 8
- 108020004707 nucleic acids Proteins 0.000 description 8
- 102000039446 nucleic acids Human genes 0.000 description 8
- 150000007523 nucleic acids Chemical class 0.000 description 8
- 238000007789 sealing Methods 0.000 description 8
- 239000000872 buffer Substances 0.000 description 7
- 239000012530 fluid Substances 0.000 description 7
- 239000011148 porous material Substances 0.000 description 7
- 239000007853 buffer solution Substances 0.000 description 6
- 238000001746 injection moulding Methods 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000000654 additive Substances 0.000 description 5
- 239000000975 dye Substances 0.000 description 5
- 238000006911 enzymatic reaction Methods 0.000 description 5
- 239000000049 pigment Substances 0.000 description 5
- 239000004094 surface-active agent Substances 0.000 description 5
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 4
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 4
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 4
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 4
- 229920001213 Polysorbate 20 Polymers 0.000 description 4
- 239000004372 Polyvinyl alcohol Substances 0.000 description 4
- 230000000996 additive effect Effects 0.000 description 4
- 230000003321 amplification Effects 0.000 description 4
- 239000011324 bead Substances 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 239000007850 fluorescent dye Substances 0.000 description 4
- 239000005090 green fluorescent protein Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 239000002480 mineral oil Substances 0.000 description 4
- 235000010446 mineral oil Nutrition 0.000 description 4
- 238000003199 nucleic acid amplification method Methods 0.000 description 4
- 238000000206 photolithography Methods 0.000 description 4
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 4
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 4
- 229920002451 polyvinyl alcohol Polymers 0.000 description 4
- 229920000178 Acrylic resin Polymers 0.000 description 3
- 239000004925 Acrylic resin Substances 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 229910003460 diamond Inorganic materials 0.000 description 3
- 239000010432 diamond Substances 0.000 description 3
- 238000007847 digital PCR Methods 0.000 description 3
- 239000004205 dimethyl polysiloxane Substances 0.000 description 3
- 238000000227 grinding Methods 0.000 description 3
- 238000000691 measurement method Methods 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 229920002120 photoresistant polymer Polymers 0.000 description 3
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 3
- 229920002050 silicone resin Polymers 0.000 description 3
- 239000004713 Cyclic olefin copolymer Substances 0.000 description 2
- 102100031780 Endonuclease Human genes 0.000 description 2
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- COHYTHOBJLSHDF-UHFFFAOYSA-N Indigo Chemical compound N1C2=CC=CC=C2C(=O)C1=C1C(=O)C2=CC=CC=C2N1 COHYTHOBJLSHDF-UHFFFAOYSA-N 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- 238000007397 LAMP assay Methods 0.000 description 2
- 238000012408 PCR amplification Methods 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 238000005842 biochemical reaction Methods 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- 238000007872 degassing Methods 0.000 description 2
- 239000000986 disperse dye Substances 0.000 description 2
- 238000005530 etching Methods 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 229920002313 fluoropolymer Polymers 0.000 description 2
- 239000004811 fluoropolymer Substances 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 229910001629 magnesium chloride Inorganic materials 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- 238000005498 polishing Methods 0.000 description 2
- 229920003207 poly(ethylene-2,6-naphthalate) Polymers 0.000 description 2
- 229920006122 polyamide resin Polymers 0.000 description 2
- 229920005668 polycarbonate resin Polymers 0.000 description 2
- 239000004431 polycarbonate resin Substances 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 239000011112 polyethylene naphthalate Substances 0.000 description 2
- 229920013716 polyethylene resin Polymers 0.000 description 2
- 229920000139 polyethylene terephthalate Polymers 0.000 description 2
- 239000005020 polyethylene terephthalate Substances 0.000 description 2
- 229920006324 polyoxymethylene Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 229920002379 silicone rubber Polymers 0.000 description 2
- 239000004945 silicone rubber Substances 0.000 description 2
- 230000003068 static effect Effects 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N 1,1-Diethoxyethane Chemical compound CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- VZXTWGWHSMCWGA-UHFFFAOYSA-N 1,3,5-triazine-2,4-diamine Chemical compound NC1=NC=NC(N)=N1 VZXTWGWHSMCWGA-UHFFFAOYSA-N 0.000 description 1
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical compound C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 description 1
- PIIRYSWVJSPXMW-UHFFFAOYSA-N 1-octyl-4-(4-octylphenoxy)benzene Chemical compound C1=CC(CCCCCCCC)=CC=C1OC1=CC=C(CCCCCCCC)C=C1 PIIRYSWVJSPXMW-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- KXGFMDJXCMQABM-UHFFFAOYSA-N 2-methoxy-6-methylphenol Chemical compound [CH]OC1=CC=CC([CH])=C1O KXGFMDJXCMQABM-UHFFFAOYSA-N 0.000 description 1
- HHBBIOLEJRWIGU-UHFFFAOYSA-N 4-ethoxy-1,1,1,2,2,3,3,4,5,6,6,6-dodecafluoro-5-(trifluoromethyl)hexane Chemical compound CCOC(F)(C(F)(C(F)(F)F)C(F)(F)F)C(F)(F)C(F)(F)C(F)(F)F HHBBIOLEJRWIGU-UHFFFAOYSA-N 0.000 description 1
- JYCQQPHGFMYQCF-UHFFFAOYSA-N 4-tert-Octylphenol monoethoxylate Chemical compound CC(C)(C)CC(C)(C)C1=CC=C(OCCO)C=C1 JYCQQPHGFMYQCF-UHFFFAOYSA-N 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- NVHWGTQHIZULQD-UHFFFAOYSA-N C1(=CC=CC2=CC=CC=C12)O.[Cr] Chemical compound C1(=CC=CC2=CC=CC=C12)O.[Cr] NVHWGTQHIZULQD-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 238000000018 DNA microarray Methods 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 description 1
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 101710180995 Endonuclease 1 Proteins 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 102100026121 Flap endonuclease 1 Human genes 0.000 description 1
- 108090000652 Flap endonucleases Proteins 0.000 description 1
- 206010064571 Gene mutation Diseases 0.000 description 1
- 229920000433 Lyocell Polymers 0.000 description 1
- 239000004640 Melamine resin Substances 0.000 description 1
- 229920000877 Melamine resin Polymers 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- SJEYSFABYSGQBG-UHFFFAOYSA-M Patent blue Chemical compound [Na+].C1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=CC=1)S([O-])(=O)=O)S([O-])(=O)=O)=C1C=CC(=[N+](CC)CC)C=C1 SJEYSFABYSGQBG-UHFFFAOYSA-M 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229930182556 Polyacetal Natural products 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004734 Polyphenylene sulfide Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004820 Pressure-sensitive adhesive Substances 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 206010070834 Sensitisation Diseases 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 229920001807 Urea-formaldehyde Polymers 0.000 description 1
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 1
- AUNAPVYQLLNFOI-UHFFFAOYSA-L [Pb++].[Pb++].[Pb++].[O-]S([O-])(=O)=O.[O-][Cr]([O-])(=O)=O.[O-][Mo]([O-])(=O)=O Chemical compound [Pb++].[Pb++].[Pb++].[O-]S([O-])(=O)=O.[O-][Cr]([O-])(=O)=O.[O-][Mo]([O-])(=O)=O AUNAPVYQLLNFOI-UHFFFAOYSA-L 0.000 description 1
- 239000011354 acetal resin Substances 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 239000000980 acid dye Substances 0.000 description 1
- 229920000122 acrylonitrile butadiene styrene Polymers 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- GZCGUPFRVQAUEE-SLPGGIOYSA-N aldehydo-D-glucose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O GZCGUPFRVQAUEE-SLPGGIOYSA-N 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 238000003491 array Methods 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- IRERQBUNZFJFGC-UHFFFAOYSA-L azure blue Chemical compound [Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Al+3].[Al+3].[Al+3].[Al+3].[Al+3].[Al+3].[S-]S[S-].[O-][Si]([O-])([O-])[O-].[O-][Si]([O-])([O-])[O-].[O-][Si]([O-])([O-])[O-].[O-][Si]([O-])([O-])[O-].[O-][Si]([O-])([O-])[O-].[O-][Si]([O-])([O-])[O-] IRERQBUNZFJFGC-UHFFFAOYSA-L 0.000 description 1
- QFFVPLLCYGOFPU-UHFFFAOYSA-N barium chromate Chemical compound [Ba+2].[O-][Cr]([O-])(=O)=O QFFVPLLCYGOFPU-UHFFFAOYSA-N 0.000 description 1
- 239000000981 basic dye Substances 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000001055 blue pigment Substances 0.000 description 1
- 229910052793 cadmium Inorganic materials 0.000 description 1
- BDOSMKKIYDKNTQ-UHFFFAOYSA-N cadmium atom Chemical compound [Cd] BDOSMKKIYDKNTQ-UHFFFAOYSA-N 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000012461 cellulose resin Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 239000011247 coating layer Substances 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 239000006103 coloring component Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- XCJYREBRNVKWGJ-UHFFFAOYSA-N copper(II) phthalocyanine Chemical compound [Cu+2].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 XCJYREBRNVKWGJ-UHFFFAOYSA-N 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 239000000982 direct dye Substances 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 238000010894 electron beam technology Methods 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000001033 ether group Chemical group 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000001215 fluorescent labelling Methods 0.000 description 1
- NBVXSUQYWXRMNV-UHFFFAOYSA-N fluoromethane Chemical compound FC NBVXSUQYWXRMNV-UHFFFAOYSA-N 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229930182470 glycoside Natural products 0.000 description 1
- 239000001056 green pigment Substances 0.000 description 1
- 125000001165 hydrophobic group Chemical group 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- UCNNJGDEJXIUCC-UHFFFAOYSA-L hydroxy(oxo)iron;iron Chemical compound [Fe].O[Fe]=O.O[Fe]=O UCNNJGDEJXIUCC-UHFFFAOYSA-L 0.000 description 1
- 229920003063 hydroxymethyl cellulose Polymers 0.000 description 1
- 229940031574 hydroxymethyl cellulose Drugs 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000001023 inorganic pigment Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000002032 lab-on-a-chip Methods 0.000 description 1
- MOUPNEIJQCETIW-UHFFFAOYSA-N lead chromate Chemical compound [Pb+2].[O-][Cr]([O-])(=O)=O MOUPNEIJQCETIW-UHFFFAOYSA-N 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 239000000113 methacrylic resin Substances 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000983 mordant dye Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- UPSFMJHZUCSEHU-JYGUBCOQSA-N n-[(2s,3r,4r,5s,6r)-2-[(2r,3s,4r,5r,6s)-5-acetamido-4-hydroxy-2-(hydroxymethyl)-6-(4-methyl-2-oxochromen-7-yl)oxyoxan-3-yl]oxy-4,5-dihydroxy-6-(hydroxymethyl)oxan-3-yl]acetamide Chemical compound CC(=O)N[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@H]1[C@H](O)[C@@H](NC(C)=O)[C@H](OC=2C=C3OC(=O)C=C(C)C3=CC=2)O[C@@H]1CO UPSFMJHZUCSEHU-JYGUBCOQSA-N 0.000 description 1
- 229920003986 novolac Polymers 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 229920002113 octoxynol Polymers 0.000 description 1
- 239000001053 orange pigment Substances 0.000 description 1
- 239000012860 organic pigment Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 229920001568 phenolic resin Polymers 0.000 description 1
- 239000005011 phenolic resin Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical compound N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 1
- 230000010399 physical interaction Effects 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 239000009719 polyimide resin Substances 0.000 description 1
- 239000002952 polymeric resin Substances 0.000 description 1
- 229920005672 polyolefin resin Polymers 0.000 description 1
- 229920000069 polyphenylene sulfide Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920005990 polystyrene resin Polymers 0.000 description 1
- 229920005749 polyurethane resin Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000000985 reactive dye Substances 0.000 description 1
- 239000001054 red pigment Substances 0.000 description 1
- 239000011342 resin composition Substances 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 230000008313 sensitization Effects 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 229920005573 silicon-containing polymer Polymers 0.000 description 1
- VVNRQZDDMYBBJY-UHFFFAOYSA-M sodium 1-[(1-sulfonaphthalen-2-yl)diazenyl]naphthalen-2-olate Chemical compound [Na+].C1=CC=CC2=C(S([O-])(=O)=O)C(N=NC3=C4C=CC=CC4=CC=C3O)=CC=C21 VVNRQZDDMYBBJY-UHFFFAOYSA-M 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 239000000988 sulfur dye Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 229920003002 synthetic resin Polymers 0.000 description 1
- 229920005992 thermoplastic resin Polymers 0.000 description 1
- 229920001187 thermosetting polymer Polymers 0.000 description 1
- JOUDBUYBGJYFFP-FOCLMDBBSA-N thioindigo Chemical compound S\1C2=CC=CC=C2C(=O)C/1=C1/C(=O)C2=CC=CC=C2S1 JOUDBUYBGJYFFP-FOCLMDBBSA-N 0.000 description 1
- SWGJCIMEBVHMTA-UHFFFAOYSA-K trisodium;6-oxido-4-sulfo-5-[(4-sulfonatonaphthalen-1-yl)diazenyl]naphthalene-2-sulfonate Chemical compound [Na+].[Na+].[Na+].C1=CC=C2C(N=NC3=C4C(=CC(=CC4=CC=C3O)S([O-])(=O)=O)S([O-])(=O)=O)=CC=C(S([O-])(=O)=O)C2=C1 SWGJCIMEBVHMTA-UHFFFAOYSA-K 0.000 description 1
- 235000013799 ultramarine blue Nutrition 0.000 description 1
- 239000000984 vat dye Substances 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 238000003466 welding Methods 0.000 description 1
- 239000001052 yellow pigment Substances 0.000 description 1
- NDKWCCLKSWNDBG-UHFFFAOYSA-N zinc;dioxido(dioxo)chromium Chemical compound [Zn+2].[O-][Cr]([O-])(=O)=O NDKWCCLKSWNDBG-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L7/00—Heating or cooling apparatus; Heat insulating devices
- B01L7/52—Heating or cooling apparatus; Heat insulating devices with provision for submitting samples to a predetermined sequence of different temperatures, e.g. for treating nucleic acid samples
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0642—Filling fluids into wells by specific techniques
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0673—Handling of plugs of fluid surrounded by immiscible fluid
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0689—Sealing
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/12—Specific details about manufacturing devices
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0816—Cards, e.g. flat sample carriers usually with flow in two horizontal directions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0848—Specific forms of parts of containers
- B01L2300/0851—Bottom walls
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
- B01L2300/0864—Configuration of multiple channels and/or chambers in a single devices comprising only one inlet and multiple receiving wells, e.g. for separation, splitting
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
- B01L2300/0877—Flow chambers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0893—Geometry, shape and general structure having a very large number of wells, microfabricated wells
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/16—Surface properties and coatings
- B01L2300/161—Control and use of surface tension forces, e.g. hydrophobic, hydrophilic
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/16—Surface properties and coatings
- B01L2300/161—Control and use of surface tension forces, e.g. hydrophobic, hydrophilic
- B01L2300/165—Specific details about hydrophobic, oleophobic surfaces
- B01L2300/166—Suprahydrophobic; Ultraphobic; Lotus-effect
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Analytical Chemistry (AREA)
- Clinical Laboratory Science (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- Dispersion Chemistry (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- Urology & Nephrology (AREA)
- Fluid Mechanics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Optical Measuring Cells (AREA)
- Automatic Analysis And Handling Materials Therefor (AREA)
Abstract
本发明涉及微流体设备(1)以及使用了所述微流体设备(1)的试样分析方法,所述微流体设备(1)具备具有多个微孔的微孔阵列(30)和以离开的状态与所述微孔阵列(30)相向的盖构件(20),在所述微孔阵列(30)与所述盖构件(20)之间具有流路,所述盖构件(20)的微孔阵列(30)侧的表面(20a)的算术平均粗糙度Ra为70nm以下。
Description
技术领域
本发明涉及微流体设备及试样分析方法。
本申请基于2019年3月1日在日本申请的日本特愿2019-037543号主张优先权,在此援引其内容。
背景技术
近年来,探讨了使用半导体电路的制造技术中使用的刻蚀技术或光刻技术、或者微细塑料的成型方法所形成的具有各种形态的微细流路结构的微孔阵列。这些微孔阵列的孔室作为用于在微小体积的流体中使各种生物化学反应或者化学反应进行的化学反应容器来使用。
作为用于制作微流体系统的材料,使用硅及玻璃等硬质的物质、PDMS(聚二甲基硅氧烷)等各种高分子树脂或有机硅橡胶等软质的物质等。例如,专利文献1~3及非专利文献1中记载了将这种微流体系统作为各种微芯片、生物芯片进行使用。
另外,近年来,通过在具有微少量容积的微小空间内进行反应来进行生物体物质的检查的技术受到关注。作为这种技术,例如可举出数字测量技术。作为数字测量技术,例如作为核酸的检测和定量中的新方法之一,可举出数字PCR(Digital PolymeraseReaction,数字聚合酶反应)技术。数字PCR技术是指将试剂与核酸的混合物分割成无数的微小液滴、进行PCR扩增,使得由包含核酸的液滴可检测到荧光等信号,通过计数检测到信号的液滴来进行定量的技术。
作为微小液滴的制作方法,探讨了通过利用封闭液将试剂与核酸的混合物截断来形成微小液滴的方法;通过在形成于基板上的孔中放入试剂与核酸的混合物、接着放入封闭液来形成微小液滴的方法等。
现有技术文献
专利文献
专利文献1:日本专利第6183471号公报
专利文献2:日本特表2014-503831号公报
专利文献3:国际公开第2013-151135号
非专利文献
非专利文献1:KimS.H.,et al.,Large-scale femtoliter droplet array fordigital countingof single biomolecules.,Lab on a Chip,12(23),4986-4991,2012.
发明内容
发明要解决的技术问题
但是,利用微流体设备分析试样时,有时试剂会非特异性地吸附在盖构件上。以往的微流体设备中,在对微细的孔中的荧光信号进行检测时,在并非数字测量的手法中不会成为问题的、由试剂的非特异性吸附所产生的荧光在利用数字测量对含有荧光物质的孔室的数量进行计数时,会变成噪音。
通过在盖构件中使用PDMS等通常说是疏水性的材料,也可以抑制试剂对盖构件的吸附,但能够使用的材料有所限制。
于是,本发明人等发现,即便不使用通常说是疏水性的材料,也可减少试剂对盖构件的非特异性吸附,提高检测效率,从而完成了本发明。本发明的目的在于提供能够减少试剂对盖构件的非特异性吸附、能够提高检测效率的微流体设备。另外,本发明的目的在于提供抑制非特异性吸附所产生的荧光等在对由微孔产生的信号进行检测时变为噪音、能够准确地对信号进行检测的试样分析方法。
用于解决技术问题的手段
为了达成上述目的,本发明包含以下方式。
[1]一种微流体设备,其具备具有多个微孔的微孔阵列和以离开的状态与所述微孔阵列相向的盖构件,在所述微孔阵列与所述盖构件之间具有流路,所述盖构件的微孔阵列侧的表面的算术平均粗糙度Ra为70nm以下。
[2]根据[1]所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面与水的接触角为70度以上。
[3]根据[1]或[2]所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面的表面粗糙度Rz为350nm以下。
[4]根据[1]~[3]中任一项所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面的Ra/Rz为0.10以上且0.23以下。
[5]根据[1]~[4]中任一项所述的微流体设备,其中,对所述盖构件的微孔阵列侧的表面实施有疏水性涂覆。
[6]一种试样分析方法,其为使用了[1]~[5]中任一项所述的微流体设备的试样分析方法,其具备:
将含有试样的水性液体导入到所述流路中;
向所述流路导入封闭液,与存在于所述流路内的所述水性液体进行置换,将所述水性液体封入在所述微孔中;
在所述微孔中引起反应,产生用于检测的信号;以及
对所述信号进行检测。
[7]根据[6]所述的试样分析方法,其中,所述试样为DNA、RNA、蛋白质、脂质、细胞或细菌。
发明效果
本发明可以提供减少了试剂的非特异性吸附的微流体设备。另外,本发明可以提供抑制非特异性吸附所产生的荧光等在对由微孔产生的信号进行检测时成为噪音、能够准确地对信号进行检测的试样分析方法。
附图说明
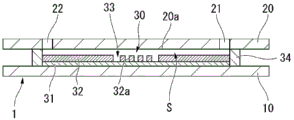
图1为表示本发明一个实施方式的微流体设备的立体图。
图2为图1的b-b线的截面图。
图3为表示本发明一个实施方式的微流体设备的截面图。
图4为表示本发明一个实施方式的微流体设备的使用时状态的图。
图5为表示本发明一个实施方式的微流体设备的使用时状态的图。
图6A为表示使用了本发明一个实施方式的微流体设备的荧光图像的图。
图6B为表示使用了比较例1的微流体设备的荧光图像的图。
图7为表示本发明一个实施方式的微流体设备的盖构件的表面粗糙度的测定数据的图。
图8为表示本发明一个实施方式的微流体设备的盖构件的表面粗糙度的测定数据的图。
图9为表示比较例2的微流体设备的盖构件的表面粗糙度的测定数据的图。
图10为表示比较例3的微流体设备的盖构件的表面粗糙度的测定数据的图。
具体实施方式
参照图1~图5说明本发明的一个实施方式。本说明书中,各附图中的尺寸比有为了说明而有所夸张的部分,并非必须与实际的尺寸一致。
图1为表示本实施方式的微流体设备1的立体图。图2为图1的b-b线的截面图。微流体设备1如图1及图2所示,具备具有多个孔室的微孔阵列30和以离开的状态与所述微孔阵列30相向的盖构件20,在微孔阵列30与盖构件20之间具有流路35。微孔阵列30可以仅具有基板10,也可以除了基板10之外还具有底部层31及壁部层32。周边构件34位于微孔阵列30与盖构件20之间。被微孔阵列30和盖构件20夹持、且被周边构件34包围的区域即为流路35。周边构件34还可以与盖构件20一体地形成。
基板10还可以透过电磁波。这里,作为电磁波,可举出X射线、紫外线、可见光线及红外线等。通过基板10能够透过电磁波,可以从基板10侧观察到由封入在微流体设备1中的试样与试剂的反应所生成的荧光或磷光等。
基板10也可以仅透过规定波长范围的电磁波。例如,当通过在作为可见光区域的350~700nm的波长范围具有峰的荧光的检测来判定微孔内的试样的存在时,将至少能够透过上述波长范围的可见光的基板作为基板10使用即可。
作为形成基板10的材料,例如可举出玻璃及树脂等。作为树脂基板的材料,例如可举出ABS树脂、聚碳酸酯树脂、COC(环烯烃共聚物)、COP(环烯烃聚合物)、丙烯酸树脂、聚氯乙烯、聚苯乙烯树脂、聚乙烯树脂、聚丙烯树脂、聚乙酸乙烯酯、PET(聚对苯二甲酸乙二醇酯)及PEN(聚萘二甲酸乙二醇酯)等。这些树脂还可以包含各种添加剂。作为添加剂的例子,可举出抗氧化剂、赋予疏水性的添加剂、赋予亲水性的添加剂等。树脂基板可以包含上述树脂中的仅一种,也可以混合有多个树脂。
由于在后述的试样分析方法中会利用荧光或磷光,因此作为基板10,使用实质上没有自体荧光的材料。这里,“实质上没有自体荧光”是指基板完全没有用于实验结果检测的波长的自体荧光、或者即便是具有自体荧光也是不会对实验结果的检测造成影响的程度的微弱荧光。例如,若是与检测对象的荧光相比为1/2以下、优选1/10以下左右的自体荧光,则可以说是不会对实验结果的检测造成影响的程度的微弱荧光。
基板10的厚度可以适当决定,为了易于透过在试样分析中发出的荧光或磷光,例如优选为5毫米(mm)以下、更优选为2mm以下、进一步优选为1.6mm以下。另外,为了易于加工,例如优选为0.1mm以上、更优选为0.2mm以上。基板10的厚度的上限及下限可以任意地组合。例如,基板10的厚度优选为0.1mm以上且5mm以下、更优选为0.2mm以上且2mm以下、进一步优选为0.4mm以上且1.6mm以下。
盖构件20(也可仅记为盖20)是形成为板状或者薄片状的构件。盖构件20以离开的状态与微孔阵列30相向。换而言之,盖构件20将多个微孔33覆盖。流路35是被盖构件20、微孔阵列30和周边构件34包围的区域。流路35与多个微孔33的开口连接、位于多个微孔33的上方。
盖构件20具有在厚度方向上贯通的第一孔21及第二孔22。在盖构件20的俯视下,第一孔21及第二孔22按照夹持1个或者多个所述液滴保持部的方式存在。第一孔21及第二孔22在完成的微流体设备1中,与包含微孔阵列30和流路35的内部空间S相连通。第一孔21及第二孔22分别作为向内部空间S供给流体的入口及排出流体的出口发挥功能。
对于形成盖构件20的材料或盖构件20的厚度而言,可以与基板10相同。
盖构件20具有电磁波透过性时,可以对电磁波透过性适当地设定。例如,未从盖构件20侧进行后述的电磁波照射工序时,盖构件20也可以是不能透过电磁波。
所述盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)为70nm以下、优选为60nm以下、更优选为50nm以下、进一步优选为40nm以下、特别优选为35nm以下。进而,所述盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)可以为30nm以下、还可以为25nm以下、还可以为20nm以下、还可以为15nm以下。通过所述盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)为50nm以下时,可以抑制试剂对盖构件20的微孔阵列30侧的表面20a的非特异性吸附。
所述盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)的下限值并无特别限定,例如为5nm。
所述盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)的上限值和下限值可以任意地组合。例如,所述盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)可以为5nm以上且70nm以下、5nm以上且60nm以下、6nm以上且50nm以下、7nm以上且40nm以下、7nm以上且35nm以下、8nm以上且30nm以下、8nm以上且25nm以下、9nm以上且20nm以下、或者10nm以上且15nm以下。
所述算术平均粗糙度(Ra)例如可以根据JIS B 0601-2001所规定的测定方法进行测定。测定范围可以是盖构件的整个面、也可以是代表性区域。本实施方式中的测定范围定义为:是以盖构件20的中心为测定范围中心的直线,且为直线的长度800μm~1.5mm的范围。
使盖构件20的微孔阵列30侧的表面20a的算术平均粗糙度(Ra)为50nm以下的方法并无特别限定,例如可举出对盖构件20实施镜面研磨加工。通过注塑成型制造盖构件20时,还可以举出利用金刚石磨浆等对盖构件20的模具进行镜面加工。
盖构件20的微孔阵列30侧的表面20a与水的接触角可以为70度以上。
此外,由于盖构件20的微孔阵列30侧的表面20a与水的接触角为180度以下,因此盖构件20的微孔阵列30侧的表面与水的接触角例如为70度以上且180度以下。
与水的接触角例如可以根据JIS R 3257-1999所规定的静滴法进行测定。也可以代替JIS R 3257-1999规定的静滴法,利用基于ASTM D5725-1997的方法测定接触角。
所述盖构件20的微孔阵列30侧的表面20a的表面粗糙度(十点平均粗糙度)(Rz)优选为350nm以下、更优选为300nm以下、特别优选为250nm以下。进而,所述盖构件20的微孔阵列30侧的表面20a的表面粗糙度(十点平均粗糙度)(Rz)可以为200nm以下、还可以为150nm以下、还可以为120nm以下、还可以为110nm以下、还可以为100nm以下、还可以为90nm以下。通过所述盖构件20的微孔阵列30侧的表面20a的表面粗糙度(Rz)为350nm以下,可以进一步抑制试剂对盖构件20的微孔阵列30侧的表面20a的非特异性吸附。
所述盖构件20的微孔阵列30侧的表面20a的表面粗糙度(十点平均粗糙度)(Rz)的下限值并无特别限定,例如为50nm。
所述盖构件20的微孔阵列30侧的表面20a的表面粗糙度(十点平均粗糙度)(Rz)的上限值和下限值可以任意地组合。例如,所述盖构件20的微孔阵列30侧的表面20a的表面粗糙度(十点平均粗糙度)(Rz)可以为50nm以上且350nm以下、55nm以上且300nm以下、60nm以上且250nm以下、60nm以上且200nm以下、60nm以上且150nm以下、65nm以上且120nm以下、70nm以上且110nm以下、70nm以上且100nm以下、或者80nm以上且90nm以下。
所述表面粗糙度(Rz)可以根据JIS B 0601-2001所规定的测定方法进行测定。测定范围可以是盖构件的整个面、也可以是代表性区域。本实施方式中的测定范围定义为:是以盖构件20的中心为测定范围中心的直线,且直线的长度800μm~1.5mm的范围。
使盖构件20的微孔阵列30侧的表面20a的表面粗糙度(Rz)为350nm以下的方法并无特别限定,例如可举出对盖构件20实施镜面研磨加工等。利用注塑成型制造盖构件20时,还可以举出利用金刚石磨浆等对盖构件20的模具进行镜面加工。
所述盖构件20的微孔阵列30侧的表面20a的Ra/Rz优选为0.10以上。所述盖构件20的微孔阵列30侧的表面20a的Ra/Rz优选为0.24以下、更优选为0.23以下、更优选为0.225以下。进而,所述盖构件20的微孔阵列30侧的表面20a的Ra/Rz还可以为0.16以下、还可以为0.15以下、还可以为0.14以下、还可以为0.13以下。
所述盖构件20的微孔阵列30侧的表面20a的Ra/Rz的上限值和下限值可以任意组合。例如,所述盖构件20的微孔阵列30侧的表面20a的Ra/Rz可以为0.10以上且0.24以下、0.10以上且0.23以下、0.10以上且0.225以下、0.10以上且0.16以下、0.10以上且0.15以下、0.10以上且0.14以下、或者0.10以上且0.13以下。
所述盖构件20的微孔阵列30侧的表面20a的Ra/Rz为0.10以上且0.24以下时,即便盖构件20的材料是亲水性的,也可以进一步抑制试剂对盖构件20的微孔阵列30侧的表面20a的非特异性吸附。认为其原因在于,不仅可以抑制盖构件20的微孔阵列30侧的表面20a与试剂的电及化学的相互作用的关系,而且由于盖构件20的微孔阵列30侧的表面20a的微小的凹凸较小,还可以抑制物理的相互作用。当Ra/Rz小于0.10时,则意味着在盖构件20的微孔阵列30侧的表面20a上存在部分突出的部分,推测在此部分易于发生试剂的非特异性吸附。当Ra/Rz大于0.24时,则意味着盖构件20的微孔阵列30侧的表面20a整体是粗糙的,推测易于发生试剂的非特异性吸附。
本实施方式的微流体设备通过对所述盖构件20的微孔阵列30侧的表面20a实施疏水性涂覆,可以代替为算术平均粗糙度(Ra)在上述范围内。因此,通过对所述盖构件20的微孔阵列30侧的表面20a实施疏水性涂覆,可以抑制试剂对盖构件20的微孔阵列30侧的表面20a的非特异性吸附。
作为对所述盖构件20的微孔阵列30侧的表面20a进行疏水性涂覆的方法,例如可举出将疏水性涂覆剂涂布在所述盖构件20的微孔阵列30侧的表面20a上并使其干燥的方法等。
作为所述涂覆剂,可举出氟系涂覆剂及含氟聚合物、有机硅树脂等。作为涂覆方法,可举出干式涂覆法及湿式涂覆法等。
在所述盖构件20的微孔阵列30侧的表面20a上涂覆疏水性涂覆剂时的涂覆层的厚度优选为0.01μm以上且3μm以下、更优选为0.05μm以上且1μm以下。
微孔阵列30还可以具有底部层31、壁部层32(也记为隔壁32)和多个微孔33。底部层31设置在基板10上。壁部层32形成在底部层31上。多个微孔33由底部层31和形成于壁部层32的厚度方向上的多个贯通孔32a构成。多个微孔33在壁部层32中形成为阵列状。在基板10与盖构件20之间的内部空间S中,在微孔阵列30与盖构件20之间、换而言之在壁部层32的上表面与盖构件20之间存在空隙。该空隙作为与多个微孔33、以及第一孔21及第二孔22连通的流路发挥功能。
底部层31构成微孔33的底面。因此,在想要对底面赋予亲水性时,只要用亲水性材料形成底部层31即可。底部层31优选按照底部层31能够透过电磁波的方式形成,从而使得不会妨碍从基板10侧对微孔33内的试样进行观察。另外,在想要对底面赋予疏水性时,只要用疏水性材料形成底部层31即可。底部层31优选不会妨碍从基板10侧对微孔33内的试样进行观察。另外,优选底部层31使用实质上没有自体荧光的材料。
此外,微孔33的底面的特性与基板10的特性相同、没有问题时,也可不设置底部层31而在基板10上直接形成壁部层32。因此,此时,由基板10的表面和壁部层32的贯通孔32a构成微孔33。
壁部层32具有在厚度方向上进行观察的状态下设置为阵列状的多个贯通孔32a。各贯通孔32a的内表面构成各微孔33的内壁面。
此外,壁部层32还可以与基板10一体成形。因此,此时,在基板10的表面上构成微孔33。
作为形成壁部层32的材料,可以使用与形成基板10的材料相同的树脂等,但也可以使用在树脂中混合有吸收规定波长的电磁波的有色成分而成的材料。
作为树脂材料,可以考虑微孔33所要求的特性等来使用树脂的构成成分的分子具有亲水性基团的亲水性树脂和树脂的构成成分的分子具有疏水性基团的疏水性树脂中的任一者。
作为亲水性基团,例如可举出羟基、羧基、磺基、磺酰基、氨基、酰胺基、醚基及酯基等。作为亲水性树脂,例如可以从硅氧烷聚合物;环氧树脂;聚乙烯树脂;聚酯树脂;聚氨酯树脂;聚丙烯酰胺树脂;聚乙烯吡咯烷酮树脂;聚丙烯酸共聚物等丙烯酸树脂;阳离子化聚乙烯醇、硅醇化聚乙烯醇、磺化聚乙烯醇等聚乙烯醇树脂;聚乙烯醇缩醛树脂;聚乙烯醇缩丁醛树脂;聚乙烯聚酰胺树脂;聚酰胺聚胺树脂;羟甲基纤维素、甲基纤维素等纤维素衍生物;聚环氧乙烷、聚环氧乙烷-环氧丙烷共聚物等聚氧化烯衍生物;马来酸酐共聚物;乙烯-乙酸乙烯酯共聚物;苯乙烯-丁二烯共聚物;以及上述树脂的组合等中适当选择使用。
作为疏水性树脂的例子,例如可以从酚醛清漆树脂;丙烯酸树脂;甲基丙烯酸树脂;苯乙烯树脂;氯乙烯树脂;偏氯乙烯树脂;聚烯烃树脂;聚酰胺树脂;聚酰亚胺树脂;聚缩醛树脂;聚碳酸酯树脂;聚苯硫醚树脂;聚砜树脂;氟树脂;有机硅树脂;脲醛树脂;三聚氰胺树脂;胍胺树脂;酚醛树脂;纤维素树脂;以及上述树脂的组合等中适当选择根据JISR3257-1999规定的静滴法测得的接触角为70度以上的材料来使用。即,本说明书中的疏水性是指根据JIS R3257-1999规定的静滴法测得的接触角为70度以上。此外,还可以代替JISR3257-1999规定的静滴法,利用基于ASTM D5725-1997的方法来测定接触角。
亲水性树脂及疏水性树脂中的任一者可以是热塑性树脂也可以是热固化性树脂。进而,还可以是通过电子束或UV光等活性能量射线而固化的树脂,也可以是弹性体。
作为树脂材料使用光致抗蚀剂时,可以利用光刻法在壁部层32上精度良好地形成大量的微细的贯通孔32a。
使用光刻法时,对于所用光致抗蚀剂的种类的选择、涂布及曝光(感光)、以及不需要的光致抗蚀剂的除去方法,可以适当选择公知的手段。
不使用抗蚀剂时,例如可以通过注塑成型等形成壁部层32。
作为有色成分,可以示例有机质或者无机质的颜料。具体地说,作为黑色颜料,可举出炭黑、乙炔黑及铁黑等。作为黄色颜料,可举出铬黄、锌黄、黄土、耐晒黄、永固黄及汽油黄。作为橙色颜料,可举出橙色色淀、钼橙及汽油橙。作为红色颜料,可举出氧化铁红、镉红、锑朱、永固红、立索尔红、色淀红、亮猩红及硫靛红。作为蓝色颜料,可举出群青、钴蓝、酞菁蓝、滕氏蓝及靛蓝。作为绿色颜料,可举出铬绿、萘酚铬绿及酞菁绿等。
另外,利用注塑成型等形成壁部层32时,不仅分散在树脂中的颜料、溶解于树脂中的各种染料也可作为有色成分进行使用。染料可根据各种染料法进行示例。具体地说,可举出直接染料、碱性染料、阳离子染料、酸性染料、媒介染料、酸性媒介染料、硫化染料、还原染料、萘酚染料、分散染料及反应染料等。特别是对树脂进行染色时,多选择分散染料。
本说明书中,微孔是指容积为10纳升(nL)以下的孔室。通过使微孔33的容积微小到此程度,可以优选地进行PCR及ICA(Invasive Cleavaged Assay,入侵裂解分析)反应等在微小空间内进行的酶反应。通过数字PCR,例如可以进行基因的突变检测等。
微孔33的容积并无特别限定,优选为10飞升(fL)以上且100皮升(pL)以下、更优选为10fL以上且5pL以下、最优选为10fL以上且2pL以下。当将容积设定在这种范围内,则在后述的试样分析时,适合在1个微孔33中收容仅1个~数个的生物体分子或者载体。
微孔33的形状只要容积在上述范围内则无特别限定。因此,例如可以是圆筒形、由多个面构成的多面体(例如长方体、六角柱、八角柱等)、倒圆锥形及倒角锥形(倒三角锥形、倒四角锥形、倒五角锥形、倒六角锥形及七角以上的倒多角锥形)等。
进而,多个微孔33的形状还可以是将2个以上的上述形状组合而成的形状。例如,可以是多个微孔33的一部分是圆筒形、其余为倒圆锥形。另外,当微孔33为倒圆锥形或者倒角锥形时,圆锥或者角锥的底面成为连通流路35和微孔33的开口部。此时,还可以使用从倒圆锥形或者倒角锥形的顶上切去一部分后而成的形状,使微孔33的底部变得平坦。作为其它例子,还可以是微孔33的底部向开口部突出的曲面形状、也可以是微孔33的底部凹陷的曲面形状。
壁部层32的厚度决定微孔33的深度。微孔为圆筒形时,为了封入包含生物体分子的水性液体(试样),壁部层32的厚度例如可以为10nm以上且100μm以下、优选为100nm以上且50μm以下、更优选为1μm以上且30μm以下、进一步优选为2μm以上且15μm以下、进一步优选为3μm以上且10μm以下的范围内。
微孔33的各部尺寸只要考虑到所收容的水性液体的量、使生物体分子附着的微珠等载体的大小等,按照在1个微孔中收容1个或多个生物体分子的方式适当决定即可。
设置于微孔阵列30中的微孔33的数量或密度可以适当设定。
每1cm2的微孔33的数量例如为1万以上且1000万以下、优选为10万以上且500万以下、进一步优选为10万以上且100万以下。本说明书中,有时将每1cm2的微孔33的数量称作微孔的密度。微孔的密度为该范围内时,将作为试样的水性液体封入在规定数量的孔室中的操作是容易的。另外,当微孔的密度为该范围内时,用于分析实验结果的孔室的观察也是容易的。例如,在对无细胞DNA的突变进行检测时,当相对于野生型DNA、作为检测对象的突变DNA的存在比例为0.01%左右时,例如优选使用100万~200万个左右的微孔。
图1中示出了多个微孔33排成一列而成的一维阵列的例子。但是,如上所述设置多个微孔时,还可以使用将多个微孔二维地排列而成的二维阵列。
在微孔阵列的周围配置有俯视下为框状的周边构件34。微流体设备1的厚度方向上的周边构件34的尺寸大于壁部层32。周边构件34通过支撑盖构件20,在盖构件20与微孔阵列之间确保空隙,维持流路35。即,流路35是被微孔阵列30和盖构件20夹持、且被周边构件34包围的区域。
周边构件34的材质等并无特别限定,例如可举出在由有机硅橡胶或丙烯酸发泡体形成的芯材薄膜的两面层叠有丙烯酸系粘合剂而成的双面胶等。
此外,周边构件34还可以与盖构件20一体成形。此时,周边构件34成为盖构件20的台阶部,通过所述台阶部,在盖构件20与微孔阵列之间确保空隙、维持流路35。
如上构成的微流体设备1例如可以按以下顺序制造。
首先,准备基板10,在基板10的面上形成成为壁部层32的壁部用树脂层。设置底部层31时,在壁部用树脂层的形成前形成底部层31。即便是不设置底部层31时,也可根据需要在基板10的面上设置提高基板10与壁部用树脂层的密合性的锚固层等。
壁部树脂层可以由在树脂材料中混合有色成分而成的材料形成。树脂材料为抗蚀剂时,相对于树脂材料和有色成分的总质量、有色成分的含有率例如可以为0.5质量%(mass%)以上且60mass%以下。就含有率而言,优选为5mass%以上且55mass%以下、进一步优选为20mass%以上且50mass%以下。相对于树脂材料和有色成分的总质量的有色成分的含有率可以考虑抗蚀剂所含的感光成分等的比例、按照能够构筑所希望图案的方式来适当进行设定。另外,当有色成分为颜料时,按照对于待形成的微孔、满足上述规定条件的方式来对颜料的粒径进行设定、准备。还可以和颜料一起、在树脂材料中适当添加分散剂。
当所形成的壁部树脂层由在树脂材料中混合有有色成分的材料形成时,壁部树脂层具有基于壁部树脂层中含有的有色成分的色彩。
接着,在所形成的壁部树脂层上形成贯通孔32a。如上所述,当使用光刻法时,可以简便且精度良好地形成贯通孔32a。利用注塑成型等形成壁部树脂层时,可以以同一工艺进行壁部树脂层的形成和贯通孔的形成。除此以外,还可以通过使用图案掩模的刻蚀等来形成贯通孔32a。
形成贯通孔32a时,壁部树脂层变成壁部层32,微孔阵列30完成。
之后,在微孔阵列30的周围配置周边构件34后、将盖构件20配置在周边构件34上。此时,按照盖构件20的微孔阵列30侧的表面20a的Ra达到50nm以下的方式进行配置。接着,将基板10、周边构件34及盖构件20一体地接合时,微流体设备1完成。流路通过周边构件34形成在盖构件20与基板10之间。接合方法并无特别限定,例如可举出利用粘接剂的接合、使用双面胶的接合、利用激光焊接进行的接合等。
另外,微流体设备1可以将基板10和壁部层32一体成形,还可以将周边构件34和盖构件20一体成形。图3表示将基板10和壁部层32一体成形、将周边构件34和盖构件20一体成形的微流体设备2。微流体设备2可如下制造:将与壁部层32一体成形的基板10配置在与周边构件34一体成形的盖构件20上,将通过周边构件34和盖构件20一体成形所形成的台阶部接合在与壁部层32一体成形的基板10上,从而制造。流路35通过形成于盖构件20上的台阶部而形成于盖构件20与基板10之间。
除将基板10和壁部层32一体成形、将周边构件34和盖构件20一体成形以外的微流体设备2的构成与上述微流体设备1相同。
作为其它方式,还可以是基板10和壁部层32作为分开的要素而具有、将周边构件34和盖构件20一体形成的微流体设备。此时也是,除将周边构件34和盖构件20一体形成以外的微流体设备的构成与上述微流体设备1相同。
接着,参照图4及图5对使用了本实施方式的微流体设备1的本实施方式的试样分析方法进行说明。
本实施方式的试样分析方法是使用了本实施方式的微流体设备1的试样的分析方法,其具备:
将含有试样的水性液体导入至所述流路35中;
向所述流路35导入封闭液,与存在于所述流路35内的所述水性液体置换,将所述水性液体封入在所述微孔33中;
加热所述微流体设备,在所述微孔33中引起反应,产生用于检测的信号;以及
对所述信号进行检测。
这里,水性液体除了试样之外,还可以包含水、缓冲液及检测反应试剂等。另外,水性液体中还可以含有酶。例如,在试样为核酸时,可以使用PCR法、ICA法、LAMP法(注册商标、Loop-Mediated Isothermal Amplification,环介导等温扩增)、TaqMan法(注册商标)或荧光探针法等。例如,在试样为蛋白质时,可以使用ELISA法(注册商标)等。进而,还可以在水性液体中含有表面活性剂等添加物。
作为缓冲液,例如可举出Tris-HCl缓冲液、醋酸缓冲液及磷酸缓冲液等。
作为酶,例如可举出DNA聚合酶、RNA聚合酶、逆转录酶及侧翼核酸内切酶等。
作为表面活性剂,例如可举出Tween 20(也称作聚氧乙烯山梨醇酐单月桂酸酯)、Triton-X100(也称作聚乙二醇单-4-辛基苯基醚(n=约10))、甘油、辛基苯酚乙氧基酯及烷基糖苷等。
本实施方式的微流体设备例如在基因的突变检测等中改变封入的水性液体的温度时,也可以优选地在孔室内保持水性液体。所改变的温度的范围,即温度变化的下限值至上限值的范围例如为0℃~100℃、优选为0℃~80℃、进一步优选为20℃~70℃。封入在孔室中的水性溶液为该范围内时,可以优选地进行PCR或ICA反应等在微小空间内进行的反应。
作为使用本实施方式的微流体设备1进行分析的试样,例如可举出DNA、RNA、miRNA、mRNA、蛋白质、脂质、细胞或细菌等。作为所述试样,例如可以是从血液等生物体中采集的试样。另外,利用试样分析进行检测的检测对象可以是以试样所含DNA为模板而得到的PCR产物等,还可以是人工合成的化合物(例如,模拟作为试样的DNA而得到的人工合成的核酸)等。例如,以作为生物体分子的DNA作为检测对象时,孔室可以具有1分子的DNA进入的形状及大小。
以下,对试样分析方法的详细情况进行说明。作为准备工序,制备含有封入在微孔中的试样的水性液体。含有试样的水性液体是含有检测对象的水为主要溶剂的液体,例如可举出以生物体试样为模板、作为检测试剂包含SYBR Green的PCR反应溶液,包含等位基因探针、ICA寡核苷酸、FEN-1及荧光底物等的ICA反应溶液等。在制备中还可以添加表面活性剂,使试样更容易地进入微孔内。另外,还可以添加特异性识别检测对象的微珠,预先将检测对象捕获。检测对象也可以不直接或间接地与微珠等载体结合、而是浮游在水性液体中。
接着,使用注射器等将所制备的含有试样的水性液体100从第一孔21导入到流路35中(也称作试样供给工序)。所供给的含有试样的水性液体100如图4所示填充到各微孔33内及流路35中。流路35内的气体在试样供给工序之前,预先通过脱气操作而除去。该脱气操作可以通过在流路35内充满缓冲液来进行。作为缓冲液,例如可举出水、包含缓冲液的水、包含表面活性剂的水、以及包含缓冲液及表面活性剂的水等。
接着,进行将含有试样100的水性液体封入在微孔33中的封入工序。封入工序之前,还可以预先对水性液体中含有的试样内的检测对象附加荧光等标记。荧光标记处理可以在试样供给工序之前、例如试样的制备时进行,还可以在试样供给工序后、将荧光标记导入流路35中。
封入工序中,使用注射器等将封闭液110从第一孔21供给至流路35。所供给的封闭液110流过流路内,如图5所示,将存在于流路35内的含有试样的水性液体100挤向第二孔22。进而,封闭液110与填充在流路35内的水性介质100相置换,流路35被封闭液110填充。结果,含有试样的水性液体100仅在各微孔33内以相互间独立的状态配置,试样的封入结束。
本说明书中,封闭液110是指为了使导入至微孔阵列30的各微孔33中的水性液体彼此以相互间不混合的状态隔离而使用的液体,例如可举出油类等。作为油,例如可以使用Sigma公司制的商品名“FC40”或3M公司制的商品名“HFE-7500”、PCR反应等中使用的矿物油等。
封闭液110优选相对于壁部层32的材质的接触角为5度以上且30度以下。封闭液110的接触角为该范围时,封闭液110易挤压水性液体100,水性液体10难以残留在盖构件20的表面。结果,可以优选地将试样封入在各微孔33中。封闭液的接触角例如只要根据基于JIS R3257-1999所规定的静滴法、代替水而使用封闭液进行测定即可。此外,还可以代替JIS R3257-1999所规定的静滴法、利用基于ASTM D5725-1997的方法来测定接触角。
接着,进行下述反应工序:加热所述微流体设备1,在所述微孔33中引起反应,产生用于检测的信号。
作为用于检测的信号的例子,可举出荧光、化学发光、显色、电位变化或者pH变化等,但优选荧光。
在反应工序之前,还可将微流体设备1置于热循环仪,根据需要进行PCR反应或ICA反应等酶反应等。
所述反应例如可以是生物化学反应、更具体地说是酶反应。加热时的温度根据反应适当决定,例如为60℃以上且100℃以下。进行加热时的温度并非是微孔33内的试剂液的实际温度,而是通过热循环仪或者孵育箱等设定的微流体设备的加热温度。另外,进行加热时的温度例如为60℃以上且100℃以下是指温度的最高温度达到60℃以上且100℃以下,并无必要一直保持60℃以上且100℃以下。即,在上述变化的温度范围内,微流体设备1的温度发生变化也是没关系的。作为反应的一例,可举出信号扩增反应。信号扩增反应是在将包含用于信号扩增的酶的试剂液收容在微孔33内的状态下、将微流体设备1在可获得所希望的酶活性的一定温度条件下、例如60℃以上且100℃以下维持规定时间、例如至少10分钟、优选约15分钟的等温反应。
接着,检测通过上述反应由微孔33产生的信号(检测工序)。例如,当信号为荧光时,安装在荧光显微镜中,照射激发光(电磁波)。激发光的波长根据所使用的荧光标记来适当设定。
电磁波的照射可以从微流体设备1的基板10侧进行,也可以从盖构件20侧、即微孔33的上侧进行,还可以从其它任意的方向进行。另外,电磁波照射的结果产生的荧光或者磷光的检测可以从微孔阵列的基板侧进行,也可以从孔室侧进行,还可以从其它任意的方向进行,例如使用荧光显微镜检测荧光或者磷光时,从微流体设备1的基板10侧进行是简单的。
接着,对在构成微孔阵列30的多个微孔33中有几个微孔33发出了荧光或者磷光进行测量。测量可以拍摄微孔阵列30的荧光图像、使用荧光图像来进行。
例如,在微孔阵列30内进行PCR反应,通过检测可观察到PCR扩增的微孔33中的SYBR Green的荧光,可以算出可观察到扩增的微孔33的数量相对于全部微孔33数量的比例。检测对象例如为单核苷酸多态性(SNP:Single Nucleotide Polymorphism)时,通过计数发出荧光的微孔33的数量,可以分析SNP的出现频率等。
在此测量工序中,水性液体有时包含蛋白质或酶作为试样、或者包含作为试剂的酶。这些蛋白质或酶不会被微珠吸附、而是浮游在水性液体中时,蛋白质或酶对盖构件20表面的吸附特别容易发生。蛋白质或酶非特异性吸附在盖构件20上,这些蛋白质或酶发出荧光或磷光时,该荧光或磷光作为噪音被检测到。根据本发明的微流路设备,由于减少了试样或试剂所含的蛋白质或酶对该盖构件20的吸附,因此可以抑制噪音的发生。
本发明的另一方面包含以下方式。
[8]一种微流体设备,其具备具有多个微孔的微孔阵列和以离开的状态与所述微孔阵列相向的盖构件,在所述微孔阵列与所述盖构件之间具有流路,所述盖构件的微孔阵列侧的表面的算术平均粗糙度Ra为5nm以上且50nm以下、十点平均粗糙度(Rz)为50nm以上且250nm以下。
[9]根据[8]所述的微流体设备,其进一步具有位于所述微孔阵列与所述盖构件之间、且将所述流路包围的周边构件。
[10]根据[9]所述的微流体设备,其中,所述周边构件是与所述盖构件一体地形成的台阶部。
[11]根据[8]~[10]中任一项所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面与水的接触角为70度以上。
[12]根据[8]~[11]中任一项所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面的Ra/Rz为0.10以上且0.23以下。
[13]根据[8]~[12]中任一项所述的微流体设备,其特征在于,对所述盖构件的微孔阵列侧的表面实施有疏水性涂覆。
[14]根据[8]~[13]中任一项所述的微流体设备,其中,所述疏水性涂覆是氟系涂覆剂及含氟聚合物、有机硅树脂中的1个。
[15]一种试样分析方法,其为使用了[8]~[14]中任一项所述的微流体设备的试样分析方法,其具备:
将含有试样的水性液体供给到所述流路;
向所述流路中导入封闭液,与存在于所述流路内的所述水性液体置换,将所述水性液体封入在所述微孔中;
在所述微孔中引起反应,产生用于检测的信号;以及
对所述信号进行检测。
[16]根据[15]所述的试样分析方法,其中,所述试样为DNA、RNA、蛋白质、脂质、细胞或细菌。
实施例
接着,示出实施例更为详细地说明本发明,但本发明并不限定于以下的实施例。
(实施例1)
准备通过注塑成型形成的COP制(ZEONOR1010R、日本Zeon公司制)制的矩形基板和COP制的矩形的盖构件的2个树脂制构件。COP制的基板使用在基板整个面上配置有直径为10μm、深度为15μm的圆筒状微小孔、利用注塑成型成形的基板。盖构件上形成有高度为100μm的台阶部、即周边构件和注入口和排出口。注入口和排出口沿着盖构件的长度方向配置在周边构件的内侧。
利用#3000金刚石磨浆对钢制盖构件的模具中的相当于盖构件底面(形成有台阶部的面)的面进行研磨,实施模具的镜面加工。
使用接触角测定器SA-20(协和界面科学公司制)、根据JIS R 3257-1999规定的静滴法来测定所成形的盖构件底面与水的接触角。实施例1的盖构件底面与水的接触角为85度。
另外,使用接触式表面粗糙度测定器(TALYSURF PGI1240、Taylor Hobson公司制)来测定所成形的盖构件的表面粗糙度。本测定中,获取了扫描范围800μm下的相对于开始点(高度为0nm)的高低差。
表1中示出上述盖构件底面的Ra及Rz的测定结果。
表1
按照盖构件的经过镜面加工的面成为基板侧的方式,通过在盖构件的台阶部涂布矿物油而将上述COP制的基板与盖构件粘接,制作微流体设备。
向基板与盖构件之间的流路中送液200μL的下述表2所示组成的缓冲液,在微小孔芯片的各孔室中填充缓冲液。
表2
| 缓冲液组成 | 最终浓度 |
| MgCl<sub>2</sub> | 20mM |
| Tris(pH8.5) | 50mM |
| Tween20 | 0.05% |
接着,向上述流路中送液10μL的具有下述表3所示组成的荧光试剂(Fluorescein、东京化成工业公司制),将缓冲液置换成荧光试剂。进而,送液150μl的氟碳油(FC40、Sigma公司制),将微小孔芯片的各孔室分别地封闭。此外,本实施例中未进行荧光反应,但为了成为与进行荧光反应时相同的状态,在荧光试剂中添加有酶。
表3
| 荧光试剂组成 | 最终浓度 |
| 荧光试剂 | 2μM |
| MgCl<sub>2</sub> | 20mM |
| Tris(pH8.5) | 50mM |
| 侧翼核酸内切酶1 | 0.1mg/ml |
| Tween20 | 0.05% |
将上述微流体设备安装在加热板上,在66℃下加热15分钟后,利用荧光显微镜(BZ-710、KEYENCE公司制)、使用4倍物镜观察微小孔芯片的荧光图像。曝光时间设定为明视野20msec、使用GFP(Green Fluorescent Protein,绿色荧光蛋白)的荧光滤波器为3000msec。
图6A中示出实施例1的微流体设备的液滴形成后的微小孔芯片的荧光观察结果。观察图像的尺寸为580μm×580μm。实施例1的微流体设备中,试剂不会非特异性地吸附在盖构件底面上,准确地对液滴数进行了测量。
(比较例1)
除了不对模具中相当于盖构件底面的面实施镜面加工以外,与实施例1同样地制作微流体设备。将上述盖构件底面的Ra及Rz的测定结果示于表1中。比较例1的盖构件底面与水的接触角为85度。
对于上述制作的微流体设备,与实施例1同样地送液缓冲液和荧光试剂,形成液滴,观察微小孔芯片的荧光图像。
图6B中示出比较例1的微流体设备的液滴形成后的微小孔芯片的荧光观察的结果。图中的箭头部分表示代表性的试剂附着。除箭头部分以外,在整个视野中也可看到大量的试剂附着。
如图6B所示,使用了未镜面加工的盖构件的比较例1的微流体设备中,试剂非特异性吸附在盖构件底面上,所附着的位置导致未能测量准确的液滴数。
由此结果可知,即便是盖构件底面与水的接触角相同,通过Ra为50nm以下,也可减少试剂对盖构件底面的非特异性地吸附。
(实施例2)
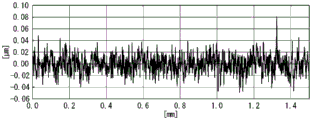
利用与实施例1相同的方法制造COP制的基材。除了延长盖构件的模具中相当于盖构件底面的面的镜面加工的时间以外,利用与实施例1相同的方法制造COP制的盖构件。使用表面粗糙度测定器(SJ-210、Mitutoyo制)对所成形的盖构件的表面粗糙度进行测定。本测定的扫描范围是以盖构件的中心为扫描范围的中心且在垂直于盖构件的长度方向的方向上为1.5mm,获取了相对于开始点(高度为0nm)的高低差。表4中示出实施例2的盖构件底面的Ra及Rz的测定结果。图7是表示实施例2的微流体设备的盖构件的表面粗糙度的测定数据的图。
表4
| Ra(nm) | Rz(nm) | Ra/Rz | 吸附面积(%) | 评价 | |
| 实施例2 | 11 | 87 | 0.126 | 1.8 | 好 |
| 实施例3 | 32 | 237 | 0.135 | 3.6 | 好 |
| 比较例2 | 71 | 378 | 0.187 | 22.3 | 差 |
| 比较例3 | 138 | 837 | 0.164 | 21.0 | 差 |
按照盖构件的经过镜面加工的面成为基板侧的方式,通过在盖构件的台阶部涂布矿物油而将基材与盖构件粘接,制作微流体设备。
在与实施例1相同的条件下将缓冲液、荧光试剂和矿物油送液至微流体设备,在微小孔芯片的各孔室中分别地封闭荧光试剂。此外,本实施例中也是与实施例1同样地未进行荧光反应,但为了成为与进行荧光反应时相同的状态,在荧光试剂中添加有酶。
将上述微流体设备安装在加热板上,在66℃下加热15分钟后,利用荧光显微镜(BZ-710、KEYENCE公司制)、使用4倍物镜观察微小孔芯片的荧光图像。曝光时间设定为明视野20msec、使用GFP(Green Fluorescent Protein,绿色荧光蛋白)的荧光滤波器为3000msec。观察视野为3.6mm×2.7mm的区域。
荧光图像中,当在孔室中存在靶标分子时,以通过酶反应而发光的荧光的强度为基准,将发出基准以上的荧光强度的区域判断为荧光试剂吸附的部分,算出荧光试剂吸附的部分的面积。
将荧光试剂吸附的部分的面积相对于荧光图像整体的面积作为吸附面积的比率(%)求得。吸附面积的比率小于10%时评价为吸附的抑制良好、为10%以上时评价为吸附的抑制差。将其结果示于表4中。
(实施例3)
除了缩短盖构件的模具中相当于盖构件底面的面的镜面加工的时间以外,利用与实施例2相同的方法求得实施例3的试剂的吸附面积的比率。将其结果示于表4中。图8为表示实施例3的微流体设备的盖构件的表面粗糙度的测定数据的图。
(比较例2及比较例3)
除了不进行盖构件的模具中相当于盖构件底面的面的镜面加工以外,利用与实施例2相同的方法求得比较例2及3的试剂的吸附面积的比率。将其结果示于表4中。图9及图10分别表示比较例2及比较例3的微流体设备的盖构件的表面粗糙度的测定数据的图。
在盖构件底面、即盖构件的微孔阵列侧的表面的Ra为70nm以下的实施例2及3中,吸附面积的比率分别为1.8%及3.6%,是良好的值。
另一方面,盖构件的微孔阵列侧的表面的Ra大于70nm的比较例2及3中,吸附面积的比率分别为22.3%及21.0%。比较例2及3中,由于未进行盖构件的模具中相当于盖构件底面的面的镜面加工,因此未能控制盖构件底面的表面粗糙度,在表面粗糙度中产生了不均。
吸附面积的比率小于10%时评价为吸附的抑制良好的理由如下所述。
吸附面积的比率超过10%时,例如当要测定在微流体设备的全部孔室中仅进入1个靶标分子的低浓度样品时,靶标分子以10%以上的概率被封入在与试剂吸附的部分重叠的孔室中。试剂吸附的部分的孔室即便因酶反应而发光,也无法检测到该发光,会被误判成阴性(假阴性)。即便进行2次相同的测定,仍然会以1%以上的概率(100人中有1人以上)变成假阴性。
另一方面,吸附面积的比率小于10%时,例如如实施例2及3那样吸附面积的比率为5%以下时,假阴性变为5%以下的概率,通过进行2次相同的测定,可以将假阴性的概率降低至0.25%以下。
产业上的可利用性
根据本发明,可以提供能够尽量准确地对孔室内的水性液体的荧光或磷光进行检测的微流体设备及试样分析方法。例如,在利用生物体来源的DNA或RNA等的检测进行诊断等情况下,可以将核酸随试剂一起放入到微小的空间内。
符号说明
1 微流体设备
10 基板
20 盖构件
30 微孔阵列
32 壁部层
33 微孔
100 水性液体
110 封闭液
Claims (7)
1.一种微流体设备,其具备具有多个微孔的微孔阵列和以离开的状态与所述微孔阵列相向的盖构件,在所述微孔阵列与所述盖构件之间具有流路,所述盖构件的微孔阵列侧的表面的算术平均粗糙度Ra为70nm以下。
2.根据权利要求1所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面与水的接触角为70度以上。
3.根据权利要求1或2所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面的表面粗糙度Rz为350nm以下。
4.根据权利要求1~3中任一项所述的微流体设备,其中,所述盖构件的微孔阵列侧的表面的Ra/Rz为0.10以上且0.24以下。
5.根据权利要求1~4中任一项所述的微流体设备,其中,对所述盖构件的微孔阵列侧的表面实施有疏水性涂覆。
6.一种试样分析方法,其为使用了权利要求1~5中任一项所述的微流体设备的试样分析方法,其具备:
将含有试样的水性液体供给到所述流路中;
向所述流路导入封闭液,与存在于所述流路内的所述水性液体置换,将所述水性液体封入在所述微孔中;
对所述微流体设备进行加热,在所述微孔中引起反应,产生用于检测的信号;以及
对所述信号进行检测。
7.根据权利要求6所述的试样分析方法,其特征在于,所述试样为DNA、RNA、蛋白质、脂质、细胞或细菌。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019037543 | 2019-03-01 | ||
| JP2019-037543 | 2019-03-01 | ||
| PCT/JP2020/006402 WO2020179442A1 (ja) | 2019-03-01 | 2020-02-19 | マイクロ流体デバイスおよび試料分析方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113490854A true CN113490854A (zh) | 2021-10-08 |
Family
ID=72338444
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202080015365.5A Pending CN113490854A (zh) | 2019-03-01 | 2020-02-19 | 微流体设备及试样分析方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20210394185A1 (zh) |
| EP (1) | EP3933412A4 (zh) |
| JP (2) | JP7464038B2 (zh) |
| CN (1) | CN113490854A (zh) |
| WO (1) | WO2020179442A1 (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022049382A (ja) * | 2020-09-16 | 2022-03-29 | 株式会社エンプラス | 流体取扱装置および流体取扱装置の製造方法 |
| DE212022000320U1 (de) * | 2021-12-09 | 2024-07-19 | Forward Biotech, Inc. | Flüssigkeitsbewertungsvorrichtung |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007244319A (ja) * | 2006-03-17 | 2007-09-27 | Starlite Co Ltd | マイクロ化学デバイス |
| JP2008246348A (ja) * | 2007-03-29 | 2008-10-16 | Fujifilm Corp | マイクロ化学チップ及びその製作方法 |
| CN102762991A (zh) * | 2010-02-10 | 2012-10-31 | 藤森工业株式会社 | 血小板检测用微芯片及使用该微芯片的血小板检测装置 |
| CN102928584A (zh) * | 2003-09-25 | 2013-02-13 | 富山县政府 | 微孔阵列芯片及其制造方法 |
| JP2014224710A (ja) * | 2013-05-15 | 2014-12-04 | 大日本印刷株式会社 | 微細な凹凸表面を持つ免疫アッセイ用担体 |
| JP2017072476A (ja) * | 2015-10-07 | 2017-04-13 | 凸版印刷株式会社 | マイクロウェルアレイ、マイクロ流体デバイス、マイクロウェルアレイのウェル内に水性液体を封入する方法及びマイクロウェルアレイの製造方法 |
| WO2017115863A1 (ja) * | 2015-12-28 | 2017-07-06 | 凸版印刷株式会社 | マイクロ流体デバイスおよび観察方法 |
| CN107109320A (zh) * | 2014-11-04 | 2017-08-29 | 凸版印刷株式会社 | 核酸导入方法、核酸检测方法、生物体成分解析方法、生物体成分定量用阵列器件及生物体成分解析试剂盒 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9952237B2 (en) | 2011-01-28 | 2018-04-24 | Quanterix Corporation | Systems, devices, and methods for ultra-sensitive detection of molecules or particles |
| US9375696B2 (en) | 2012-04-04 | 2016-06-28 | Mitsubishi Rayon Co., Ltd. | Microarray processing apparatus, well plate for microarray processing apparatus, microarray holder, and microarray washing method |
| CN109652295A (zh) | 2014-01-31 | 2019-04-19 | 凸版印刷株式会社 | 生物分子分析试剂盒及生物分子分析方法 |
| JP2019037543A (ja) | 2017-08-25 | 2019-03-14 | 株式会社サンセイアールアンドディ | 遊技機 |
-
2020
- 2020-02-19 WO PCT/JP2020/006402 patent/WO2020179442A1/ja active Application Filing
- 2020-02-19 JP JP2021503528A patent/JP7464038B2/ja active Active
- 2020-02-19 CN CN202080015365.5A patent/CN113490854A/zh active Pending
- 2020-02-19 EP EP20767115.7A patent/EP3933412A4/en active Pending
-
2021
- 2021-09-01 US US17/464,114 patent/US20210394185A1/en active Pending
-
2024
- 2024-03-27 JP JP2024051418A patent/JP2024079799A/ja active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102928584A (zh) * | 2003-09-25 | 2013-02-13 | 富山县政府 | 微孔阵列芯片及其制造方法 |
| JP2007244319A (ja) * | 2006-03-17 | 2007-09-27 | Starlite Co Ltd | マイクロ化学デバイス |
| JP2008246348A (ja) * | 2007-03-29 | 2008-10-16 | Fujifilm Corp | マイクロ化学チップ及びその製作方法 |
| CN102762991A (zh) * | 2010-02-10 | 2012-10-31 | 藤森工业株式会社 | 血小板检测用微芯片及使用该微芯片的血小板检测装置 |
| JP2014224710A (ja) * | 2013-05-15 | 2014-12-04 | 大日本印刷株式会社 | 微細な凹凸表面を持つ免疫アッセイ用担体 |
| CN107109320A (zh) * | 2014-11-04 | 2017-08-29 | 凸版印刷株式会社 | 核酸导入方法、核酸检测方法、生物体成分解析方法、生物体成分定量用阵列器件及生物体成分解析试剂盒 |
| JP2017072476A (ja) * | 2015-10-07 | 2017-04-13 | 凸版印刷株式会社 | マイクロウェルアレイ、マイクロ流体デバイス、マイクロウェルアレイのウェル内に水性液体を封入する方法及びマイクロウェルアレイの製造方法 |
| WO2017115863A1 (ja) * | 2015-12-28 | 2017-07-06 | 凸版印刷株式会社 | マイクロ流体デバイスおよび観察方法 |
Non-Patent Citations (3)
| Title |
|---|
| 张玉虹等: "用按需滴定技术制备聚合物微透镜阵列", 光子学报, no. 11, pages 1639 - 1642 * |
| 杨继生: "表面活性剂原理与应用", vol. 1, 31 December 2012, 东南大学出版社, pages: 55 - 57 * |
| 王磊等: "纯钛表面微弧氧化膜的粗糙度与接触角", 中国组织工程研究与临床康复, no. 42, pages 8291 - 8294 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP7464038B2 (ja) | 2024-04-09 |
| WO2020179442A1 (ja) | 2020-09-10 |
| EP3933412A4 (en) | 2022-04-06 |
| JPWO2020179442A1 (zh) | 2020-09-10 |
| EP3933412A1 (en) | 2022-01-05 |
| JP2024079799A (ja) | 2024-06-11 |
| US20210394185A1 (en) | 2021-12-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11097269B2 (en) | Microfluidic device and sample analysis method | |
| US11662313B2 (en) | Microfluidic devices and observation methods | |
| US10718776B2 (en) | Method for detecting biological substance | |
| US20240033739A1 (en) | Fluidic devices with bead well geometries with spatially separated bead retention and signal detection segments and related methods | |
| JP2024079799A (ja) | マイクロ流体デバイスおよび試料分析方法 | |
| WO2016159068A1 (ja) | マイクロウェルアレイ及びその製造方法、マイクロ流体デバイス、マイクロウェルアレイのウェル内に水性液体を封入する方法及び水性液体の分析方法 | |
| JP2024109978A (ja) | マイクロ流体デバイスおよび試料分析方法 | |
| JP2018531369A6 (ja) | 空間的に分離してビーズを保持するビーズウェル形状及びシグナル検出セグメントを有する流体デバイス並びに関連する方法 | |
| CN110312923A (zh) | 解析设备、解析试剂盒及解析系统 | |
| JP7485004B2 (ja) | 核酸検出方法および検出用試薬 | |
| JP2017072476A (ja) | マイクロウェルアレイ、マイクロ流体デバイス、マイクロウェルアレイのウェル内に水性液体を封入する方法及びマイクロウェルアレイの製造方法 | |
| CN113640512A (zh) | 用于多路测定的解码方法及相关流体设备、试剂盒和固体支持物 | |
| JP2017049151A (ja) | 生体物質検出方法 | |
| JP2017134005A (ja) | アレイデバイス及び生体分子解析用キット | |
| JP2024101996A (ja) | 流体デバイス、検出キット及び標的物質の検出方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |