CN113416841B - 一种从黄铜矿中提取铜的溶剂冶金方法 - Google Patents
一种从黄铜矿中提取铜的溶剂冶金方法 Download PDFInfo
- Publication number
- CN113416841B CN113416841B CN202110697184.1A CN202110697184A CN113416841B CN 113416841 B CN113416841 B CN 113416841B CN 202110697184 A CN202110697184 A CN 202110697184A CN 113416841 B CN113416841 B CN 113416841B
- Authority
- CN
- China
- Prior art keywords
- leaching
- solution
- chalcopyrite
- copper
- solvent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B3/00—Extraction of metal compounds from ores or concentrates by wet processes
- C22B3/04—Extraction of metal compounds from ores or concentrates by wet processes by leaching
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B15/00—Obtaining copper
- C22B15/0063—Hydrometallurgy
- C22B15/0065—Leaching or slurrying
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25C—PROCESSES FOR THE ELECTROLYTIC PRODUCTION, RECOVERY OR REFINING OF METALS; APPARATUS THEREFOR
- C25C1/00—Electrolytic production, recovery or refining of metals by electrolysis of solutions
- C25C1/12—Electrolytic production, recovery or refining of metals by electrolysis of solutions of copper
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P10/00—Technologies related to metal processing
- Y02P10/20—Recycling
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Metallurgy (AREA)
- Organic Chemistry (AREA)
- Materials Engineering (AREA)
- Mechanical Engineering (AREA)
- Manufacturing & Machinery (AREA)
- Electrochemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Life Sciences & Earth Sciences (AREA)
- Environmental & Geological Engineering (AREA)
- General Life Sciences & Earth Sciences (AREA)
- Geochemistry & Mineralogy (AREA)
- Geology (AREA)
- Manufacture And Refinement Of Metals (AREA)
- Electrolytic Production Of Metals (AREA)
Abstract
本发明公开了一种从黄铜矿中提取铜的溶剂冶金方法,包括以下步骤:(a)将黄铜矿干燥后研磨;(b)将研磨好的所述黄铜矿与三氯化铁溶液加入至浸出槽中,在搅拌的条件下浸出;(c)浸出结束后对混合溶液进行过滤,固液分离得到浸出液和含硫浸出渣;(d)将所述浸出液直接电积得到铜板和电积贫液;(e)步骤(d)中将所述电积贫液中的Fe3+/Fe2+分离,得到再生的三氯化铁溶液和含Fe2+溶液;(f)所述再生的三氯化铁溶液回到浸出槽中循环使用。本发明采用上述结构的一种从黄铜矿中提取铜的溶剂冶金方法,整个工艺具有流程操作简单、无净化过程、铜浸出率高、浸出剂再生循环使用、运行成本低、环保无污染等优点。
Description
技术领域
本发明涉及湿法冶金技术领域,特别是涉及一种从黄铜矿中提取铜的溶剂冶金方法。
背景技术
铜可从各种类型的矿石中提取,其中大部分属于硫化矿石,如黄铜矿、斑铜矿、铜辉铜矿和辉铜矿。黄铜矿是最常见的含铜矿物,约占世界铜矿床的70%。目前,黄铜矿生产铜的主要方法是通过高温冶金,高温冶金能耗大且原料中铜含量要求比较高。此外,高温冶金炼铜的过程中会产生SO2造成环境污染问题。
湿法冶金是另一种方法用于从黄铜矿中提取铜,由于运行成本较低,可应用于低品位铜矿湿法浸出黄铜矿中的铜。常用的浸出剂是酸性氯化物介质和酸性硫酸盐介质。在硫酸盐介质中,浸出动力学一般较慢,铜的浸出难以完成,这是由于在硬砂表面形成了钝化层的原因,另一方面需要复杂的净化除杂过程。在酸性氯化物介质中由于盐在氯离子介质中溶解度高,且铜离子可以稳定在浓氯溶液中,因此在氯离子介质中,浸出速度比在硫酸盐介质中快。但酸性氯化物介质的缺点是腐蚀性强,且难以从酸性氯化物介质中电积出优质铜,浸出后也需要复杂的净化除杂过程。
综上所述,高温冶金、湿法冶金浸出都有其局限性,因此开发绿色、可持续的冶金新技术对提高硫化铜矿的浸出效率具有重要意义。
发明内容
本发明的目的是提供一种从黄铜矿中提取铜的溶剂冶金方法,整个工艺具有流程操作简单、无净化过程、铜浸出率高、浸出剂再生循环使用、运行成本低、环保无污染等优点。
为实现上述目的,本发明提供了一种从黄铜矿中提取铜的溶剂冶金方法,包括以下步骤:
(a)将黄铜矿干燥后研磨;
(b)将研磨好的所述黄铜矿与三氯化铁溶液加入至浸出槽中,在搅拌的条件下浸出,所述浸出的反应原理如下:
CuFeS2+3FeCl3→4FeCl2+CuCl+2S;
(c)浸出结束后对混合溶液进行过滤,固液分离得到浸出液和含硫浸出渣;
(d)将所述浸出液直接电积得到铜板和电积贫液;
(e)步骤(d)中将所述电积贫液中的Fe3+/Fe2+分离,得到再生的三氯化铁溶液和含Fe2+溶液;
(f)所述再生的三氯化铁溶液回到浸出槽中循环使用。
优选的,步骤a)中,干燥温度为100℃,干燥时间为24小时,所述黄铜矿研磨至100目以下。
优选的,步骤b)中,所述三氯化铁溶液中三氯化铁浓度为0.1-2.0mol/L,所述三氯化铁溶液中的溶剂为乙醇、丙二醇、甲醇、乙二醇、异丁醇、异十醇中的一种或多种混合物的组成。
优选的,所述黄铜矿质量与三氯化铁溶液体积比为30-150。
优选的,步骤b)中,所述浸出的温度为20-90℃,所述搅拌的速率为50-1000rpm,所述浸出的时间为6-24h。
优选的,步骤c)中,所述固液分离采用的设备为压滤机、沉降离心机、沉降浓密机、浮球澄清器、袋式过滤器或分离柱中的一种或多种。
优选的,步骤d)中,所述电积的阳极板为钛基二氧化铅材质,所述电积的阴极板为不锈钢板,电效在95%以上,所述电积的原理如下:
阳极反应:Fe2+-e=Fe3+
阴极反应:Cu++e=Cu。
优选的,步骤e)中,所述Fe3+/Fe2+分离的方法为通过膜对金属价态的选择性将其分离。
本发明的有益效果为:
(1)所用浸出剂中有机溶剂为绿色溶剂环保无污染,且浸出剂能够实现再生循环使用;
(2)从原料到产品中间不需要净化除杂的过程,工艺流程操作简单、分离效率高、设备投资明显下降、运行成本低、环保无污染;
(3)铜的浸出率高,浸出条件无需高压条件,浸出过程中单质S替代了硫酸的产生避免了酸的排放及后续处理,避免了传统火法冶金炼铜中高能耗和SO2污染环境问题,并且也解决了传统湿法冶金黄铜矿浸出率低、设备耐腐蚀性要求高、设备投资大等缺点。
下面通过附图和实施例,对本发明的技术方案做进一步的详细描述。
附图说明
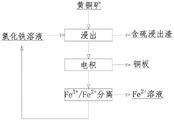
图1是本发明一种从黄铜矿中提取铜的溶剂冶金方法的工艺流程图。
具体实施方式
下面结合实施例,对本发明进一步描述,实施例中所用各种化学品和试剂如无特别说明均为市售购买。
实施例1
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在22℃条件下与2.0L 0.5mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为15.1%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例2
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在60℃条件下与2.0L 0.5mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为45.2%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例3
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.5mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为82.6%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例4
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.5mol/L三氯化铁的乙醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为34.5%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例5
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.5mol/L三氯化铁的丙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为68.7%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例6
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.1mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为18.1%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例7
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.25mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为35.8%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例8
取100g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 1.0mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为96.6%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例9
取60g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.5mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为92.7%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
实施例10
取200g干燥研磨好的黄铜矿(其中铜含量为21.9%,铁含量为19.5)在90℃条件下与2.0L 0.5mol/L三氯化铁的乙二醇溶液混合,其中搅拌速率控制为800rpm,浸出时间为24h。浸出完成后趁热用布氏漏斗过滤得到含单质硫固体渣和含铜、铁浸出溶液,取样检测分析铜的浸出率为31.6%。
滤液再通过在常温条件下电沉积得到金属铜板,其中阳极板为钛基二氧化铅材质,阴极板为不锈钢材质。电积贫液通过膜将Fe3+/Fe2+分离后再生浸出剂返回浸出循环使用。
表1为各实施例浸出变化条件及铜浸出率实验数据。
表1各实施例浸出变化条件及铜浸出率实验数据
由表1的实验数据可得,温度越高黄铜矿中铜的浸出率越高;相同条件下乙二醇做溶剂比乙醇和丙二醇做溶剂对高黄铜矿中铜的浸出效果好;FeCl3浓度越高黄铜矿中铜的浸出率越高;固液比越小(黄铜矿质量/FeCl3溶液体积)黄铜矿中铜的浸出率越高。
最后应说明的是:以上实施例仅用以说明本发明的技术方案而非对其进行限制,尽管参照较佳实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对本发明的技术方案进行修改或者等同替换,而这些修改或者等同替换亦不能使修改后的技术方案脱离本发明技术方案的精神和范围。
Claims (5)
1.一种从黄铜矿中提取铜的溶剂冶金方法,其特征在于,包括以下步骤:
(a)将黄铜矿干燥研磨;
(b)研磨好的黄铜矿与三氯化铁溶液在浸出槽中浸出;所述三氯化铁溶液中三氯化铁浓度为0.1-2.0mol/L,溶剂为乙醇、丙二醇、甲醇、乙二醇、异丁醇、异十醇中的一种或多种混合物的组成;所述黄铜矿质量(mg)与三氯化铁溶液体积(mL)比(G/L)为30-150;
所述浸出温度为20-90℃;搅拌速率为50-1000rpm;浸出时间为6-24h,浸出反应原理如下:
CuFeS2 + 3FeCl3→ 4FeCl2 + CuCl + 2S;
(c)浸出结束后过滤分离得到浸出液和含硫浸出渣;
(d)浸出液直接电积得到铜板和电积贫液;
(e)步骤(d)中电积贫液再经过Fe3+/Fe2+分离得到再生的三氯化铁溶液和含Fe2+溶液;
(f)再生的三氯化铁溶液回浸出循环使用。
2.根据权利要求1所述的一种从黄铜矿中提取铜的溶剂冶金方法,其特征在于:步骤a)中,干燥温度为100℃、干燥时间为24小时;黄铜矿研磨要求为研磨至100目以下。
3.根据权利要求1所述的一种从黄铜矿中提取铜的溶剂冶金方法,其特征在于:步骤c)中,所述过滤分离采用的设备为压滤机、沉降离心机、沉降浓密机、浮球澄清器、袋式过滤器或分离柱中的一种或多种。
4.根据权利要求1所述的一种从黄铜矿中提取铜的溶剂冶金方法,其特征在于:步骤d)中,所述电积阳极板为钛基二氧化铅材质,阴极板为不锈钢板,电效在95%以上,其电积原理如下:
阳极反应:Fe2+-e=Fe3+
阴极反应:Cu++e=Cu。
5.根据权利要求1所述的一种从黄铜矿中提取铜的溶剂冶金方法,其特征在于:步骤e)中,所述Fe3+/Fe2+分离的方法为通过膜对金属价态的选择性将其分离。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110697184.1A CN113416841B (zh) | 2021-06-23 | 2021-06-23 | 一种从黄铜矿中提取铜的溶剂冶金方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110697184.1A CN113416841B (zh) | 2021-06-23 | 2021-06-23 | 一种从黄铜矿中提取铜的溶剂冶金方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN113416841A CN113416841A (zh) | 2021-09-21 |
| CN113416841B true CN113416841B (zh) | 2022-07-12 |
Family
ID=77716236
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110697184.1A Active CN113416841B (zh) | 2021-06-23 | 2021-06-23 | 一种从黄铜矿中提取铜的溶剂冶金方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN113416841B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115772607A (zh) * | 2022-12-12 | 2023-03-10 | 昆明理工大学 | 一种利用超声强化配位剂高效浸出黄铜矿的方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1189541A (zh) * | 1997-01-27 | 1998-08-05 | 东北大学 | 从金铜矿中提取铜铁金银硫的方法 |
| CN100554452C (zh) * | 2008-07-17 | 2009-10-28 | 北京矿冶研究总院 | 一种含铜硫化矿湿法提取铜的方法 |
-
2021
- 2021-06-23 CN CN202110697184.1A patent/CN113416841B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN113416841A (zh) | 2021-09-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7666371B2 (en) | Method for recovering metal values from metal-containing materials using high temperature pressure leaching | |
| JP2008527164A (ja) | 樹脂溶出液流からニッケル及びコバルトを回収する方法 | |
| CN102618719A (zh) | 从硫化锌精矿直接浸出锌及回收镓锗铟的方法 | |
| CN101974685A (zh) | 用矿浆树脂吸附技术从红土矿中提取镍钴工艺 | |
| CN102051478A (zh) | 一种铅冰铜湿法处理工艺 | |
| CN109890988B (zh) | 用于处理矿石的集成湿法冶金和高温冶金方法 | |
| CN102994753A (zh) | 一种从酸浸硫化尾矿的浸出液中分离富集镍的方法 | |
| CA2792401A1 (en) | Method of processing nickel bearing raw material | |
| JP2011021219A (ja) | 含銅鉄物からの銅回収方法 | |
| CN112458280A (zh) | 利用酸性蚀刻液浸出低冰镍提取有价金属的方法 | |
| CN111519026B (zh) | 一种浸出二次包裹金赤铁矿的方法 | |
| CN113088710A (zh) | 一种铜锗置换渣中铜锗分离的方法 | |
| CN113416841B (zh) | 一种从黄铜矿中提取铜的溶剂冶金方法 | |
| CN106222454A (zh) | 一种从含铟烟灰回收铟的方法 | |
| CN102965520B (zh) | 一种从酸浸硫化尾矿的浸出液中分离富集铜的方法 | |
| CN102994778A (zh) | 一种从酸浸硫化尾矿的浸出液中分离富集钴的方法 | |
| EP3739069B1 (en) | Method of extracting metals from polymetallic sulphide ores or concentrates | |
| CN1358871A (zh) | 一种从含铜硫化矿物提取铜的方法 | |
| JP2008208441A (ja) | 塩化物水溶液の溶媒抽出方法 | |
| JP2008115429A (ja) | 湿式銅製錬法における銀の回収方法 | |
| Pandey et al. | Extraction of nickel and copper from the ammoniacal leach solution of sea nodules by LIX 64N | |
| CN107739841A (zh) | 一种从含砷高铜浮渣中分离砷、回收铜的方法 | |
| Flett | Solvent extraction in scrap and waste processing | |
| US3795596A (en) | Method for selectively leaching metal values from ocean floor nodules | |
| CN110484747B (zh) | 一种从粗银中选择性提取钯的工艺 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |