CN106716127B - 用于检测卵巢癌的方法 - Google Patents
用于检测卵巢癌的方法 Download PDFInfo
- Publication number
- CN106716127B CN106716127B CN201580052938.0A CN201580052938A CN106716127B CN 106716127 B CN106716127 B CN 106716127B CN 201580052938 A CN201580052938 A CN 201580052938A CN 106716127 B CN106716127 B CN 106716127B
- Authority
- CN
- China
- Prior art keywords
- small molecule
- concentration
- biomarker
- ovarian cancer
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57449—Specifically defined cancers of ovaries
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4702—Regulators; Modulating activity
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/64—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving ketones
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/92—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving lipids, e.g. cholesterol, lipoproteins, or their receptors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/112—Disease subtyping, staging or classification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/118—Prognosis of disease development
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2405/00—Assays, e.g. immunoassays or enzyme assays, involving lipids
- G01N2405/08—Sphingolipids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2570/00—Omics, e.g. proteomics, glycomics or lipidomics; Methods of analysis focusing on the entire complement of classes of biological molecules or subsets thereof, i.e. focusing on proteomes, glycomes or lipidomes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/70—Mechanisms involved in disease identification
- G01N2800/7023—(Hyper)proliferation
- G01N2800/7028—Cancer
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hospice & Palliative Care (AREA)
- Oncology (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Endocrinology (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Other Investigation Or Analysis Of Materials By Electrical Means (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
本说明书涉及卵巢癌诊断领域。本说明书引入了可以用于检测卵巢癌存在并且提供疾病的预后的新型生物标记物。
Description
技术领域
本说明书涉及卵巢癌的诊断和预后生物标记物(diagnostic and prognosticbiomarker)的领域。特别地,其提供了用于评估受试者是否处于发展卵巢癌的风险或正在遭受卵巢癌的新型体外筛查方法。另外,可以将本生物标记物用于评价存活预后(survivalprognosis)、治疗效力和卵巢癌的肿瘤切除的成功率的方法。通过测量生物标记物在血清或血浆中的浓度可以将本发明的生物标记物用于确定所述生物标记物在肿瘤中的浓度。
背景技术
卵巢癌是低发病率但是存活率不良的异质性疾病(heterogeneous disease)。根据2012年世界卫生组织(WHO)的统计数值,评估世界范围内存在239000个新的卵巢癌病例,代表女性所有癌症的4%。根据该统计数值,在2012年,152000例死亡是由卵巢癌引起的。卵巢癌是女性癌症死亡中第八大常见的原因,以及较大比例的新的卵巢癌发生在人口发展水平高或非常高的国家。发病率在北欧和东欧、北美洲和大洋洲最高,而在非洲和亚洲大部分趋向于相对低。然而,在20世纪90年代和21世纪,例如中国的发病率急剧升高。(世界卫生组织世界癌症报告2014)。最常见的卵巢癌是卵巢恶性肿瘤,其包括五种主要亚型,并且其中高级浆液性恶性肿瘤(serous carcinoma)是最常见的一种(占病例的约70%)。早期诊断对于患者的存活率是关键性的,因为,例如I期患者的5年存活率是约90%,而对于IV期患者,其仅是约20%。然而,卵巢癌的诊断是困难的,以及仅当进行到最后阶段时该疾病趋向于引起患者的症状,并且另外,症状经常与其他疾病的那些类似。因此,新的诊断工具(其可以在早期检测卵巢癌)对于成功治疗卵巢癌患者是重要的。
之前检测卵巢癌的方法依赖于蛋白质生物标记物分析和成像方法。目前用于卵巢癌的主要诊断方法包括骨盆检查、CA-125血液测试和经阴道超声。CA-125和HE4是US FDA批准的用于监测疾病复发或进展,而非筛查的唯一两种生物标记物。由若干蛋白质生物标记物组成的多变量指数测定(multivariate index assay)OVA1自2009年被FDA批准用于骨盆腔肿块的分类(Nguyen et al.,Women's Health,2013,9(2),171-187)。已经报告了CA-125是用于卵巢癌的总存活率的和无进展存活率(progression free survival)的预后因素,而且研究表明存在矛盾的结果。CA-125水平在患有晚期上皮卵巢癌的约90%患者中升高,但是仅在患有I期疾病的50%患者中升高(Gupta&Lis,Journal of Ovarian Cancer,2009,2:13)。因此,黄金标准CA-125对于检测晚期疾病的患者是相对良好的,但是CA-125在其他患者中缺乏灵敏度并且其在存活率预测中的作用存在一定的争议。
与蛋白质相比,尝试将包括代谢物和脂质的小分子用作诊断工具,因为它们直接反映新陈代谢的变化,已知该变化早在肿瘤开始和进展的早期就已经出现。特定路径的基因表达或蛋白水平的小的变化可以导致小分子代谢物和脂质浓度的大的改变,因为可以将它们的水平视为是生物路径的活性的放大输出。尽管有一些尝试寻找用于卵巢癌的小分子生物标记物,但是之前的公开没有提供已经进入临床实践的来自血清的简单的和可靠的小分子卵巢癌生物标记物。WO 2009151967描述了多种用于卵巢癌诊断的新陈代谢生物标记物候选和机器学习分类运算法则。WO2012038525A1描述了多种作为各种卵巢癌的生物标记物的磷脂。WO2013016700描述了使用质谱分析(MS)或核磁共振(NMR)的数据来产生用于上皮卵巢癌的预测模型的分类运算法则的用途。在描述卵巢癌的潜在的生物标记物候选物的其他公开中也应用了NMR技术,如WO2011041892和US2005170441。然而,之前的研究中的限制通常是大量生物标记物的描述,不能使用来自癌症患者的其他信息将其缩小,如血清和肿瘤组织之间的生物标记物水平的相互关系的预知或探究。此外,没有公开的文献表明可以怎样组合单种代谢物或代谢物连同蛋白质标记物的组合的信息来给出卵巢癌患者的更精确的诊断和预后方法。因此,关注的一系列小分子对于更好的卵巢癌诊断将是极度有用的。
定义
3,4-DHBA-3,4-二羟基丁酸
3-HBA-3-羟基丁酸
AUC-曲线下的面积
CA-125-癌症抗原125,恶性肿瘤抗原125,糖抗原125
GC-气相色谱法
GCxGC-二维气相色谱法
HE4-人附睾蛋白质4
LC-液相色谱法
lysoPC-溶血卵磷脂
MS-质谱分析
NMR-核磁共振
PC-卵磷脂
PE-磷脂酰乙醇胺
ROC-接受者操作特征(receiver operating characteristic)
SM-鞘磷脂(sphingomyelin)
TAG-三酰甘油酯
TOF-飞行时间(time-of-flight)
WHO-世界卫生组织
附图说明
图1(a)至图1(i)公开了对照组(没有恶性肿瘤)以及在手术期间具有或不具有完全的肿瘤减少的卵巢癌患者的血清中,目前识别的小分子生物标记物的浓度。总体上,小分子生物标记物示出了渐进的趋势,因为浓度在对照组中最低以及在手术期间的肿瘤切除不完全的患者中最高。该趋势尤其适用于二羟基丁酸和三羟基丁酸。鞘磷脂(SM)则表现出相反的趋势,其中浓度在没有恶性肿瘤的受试者中最高以及在没有完全的肿瘤减少的卵巢癌患者中最低。CA-125和3-羟基丁酸在对照和恶性肿瘤患者之间示出了明显的差异,但是在两种情况下(在具有或不具有肿瘤减少的患者中)没有显著的差异,这间接地暗示这些分子没有表现出与存在于患者中的肿瘤块的量的明显的关联。在表2示中出了,在恶性肿瘤(相对于对照)中以及,在完全的肿瘤减少(相对于不完全的肿瘤减少比较)中的这些分子的每种的t测试值和log2倍数变化。
图2公开了当与对照组相比时卵巢癌患者的血清中的三酰甘油酯(TAG)的变化。在图中,每个圆点代表一种TAG分子,其示出了t测试中组之间的统计上显著的结果,以及x轴表示每种TAG的脂肪酰基侧链中的碳的总数。在卵巢癌患者的血清中,TAG的分布存在明显的变化。除一种脂质之外,与不具有恶性肿瘤的受试者相比,在脂肪酰基侧链中具有53个或更少碳的所有TAG在卵巢癌患者中降低。相反,除两种脂质之外,当与对照组相比时,在脂肪酰基侧链中具有54个或更多碳的所有TAG在卵巢癌患者中升高。
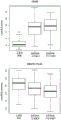
图3(a)至图3(b)公开了当预测具有恶性的卵巢肿瘤的患者时的接受者操作特征(ROC)曲线。交叉验证模型使得将数据组随机分到训练(2/3样品)和验证(1/3样品)组1000次,并在验证组(validation)中测试训练组(training set)中的构造模型。线代表平均值,以及箱图代表所有运行的可变性。表3呈现了曲线(AUC)下的平均面积值和它们的95%置信区间。图和AUC值表明当模型包含CA-125连同3-羟基丁酸和3,4-二羟基丁酸(其中具有或或不具有合并至模型的SM(d18:1/24:0))时,实现了最大的值和最精确的预测。CA-125连同图中所示的三种SM产生的模型稍好于仅合并CA-125的模型。结论是当与仅来自CA-125的信息相比时,将来自小分子生物标记物的信息合并至CA-125浓度,增加了灵敏度和预测的特异性。
图4公开了用于分类I期和II期患者与没有恶性肿瘤的对照受试者的模型的ROC曲线。数据仅包含患I期和II期卵巢癌的7位患者,并且该患者群体的CA-125的AUC值比预期的高。然而,尽管有这些限制,3-羟基丁酸(3-HBA)示出了较高的AUC值(表4示出了所有值),并且尤其是包含来自CA-125连同3-羟基丁酸和3,4-二羟基丁酸(3,4-DHBA)的信息的模型示出了组的几乎完全的分离。该结果给出了证明,即在具有或不具有合并至模型的CA-125的信息的情况下,小分子生物标记物可用于诊断早期卵巢癌患者。
图5(a)至图5(i)公开了每种小分子生物标记物和CA-125的Kaplan-Meier曲线。该图示出了当将患者分为两个组时,对于每种分子的总存活率:具有低于或等于所有样品的中值的浓度的那些和具有高于所有样品的中值的浓度的那些。表2示出了这些结果的p值。显而易见的是对于大部分的小分子生物标记物,血清中的浓度越高表示总存活率越低。然而,对于鞘磷脂(SM),一般而言,血清中的浓度越低表示总存活率越低。CA-125没有示出与患者的总存活率的任何关联,并且因此与CA-125相比,小分子生物标记物是优异的预后标记物。
图6(a)至图6(c)公开了直观化选定的小分子生物标记物的组织和血清浓度之间的相互关系的散布图。表5示出了统计结果,其示出了Spearman和Pearson相互关系分析中的p和R2值。
图7公开了简单的示意图,其示出了人体中的酮体的化学反应。3-羟基丁酸可以在可逆反应中转化为乙酰乙酸,乙酰乙酸在不可逆反应中可以转化为丙酮。本研究的结果示出了卵巢癌患者的血清中的3-羟基丁酸和乙酰乙酸的浓度较高。根据这些反应,丙酮的浓度也升高是合乎逻辑的。
具体实施方式
本发明通过量化定义的分子种类和它们的组合鉴定了小分子卵巢癌生物标记物。重要地,本发明示出了已经处于单种浓度的水平的值。本发明还首次提供了一组可以单独或组合使用的生物标记物,来通过测量在血液或甚至呼吸中的浓度确定它们在卵巢癌肿瘤中的浓度,从而简化测量。
本发明人出乎意料地发现了用于卵巢癌的新型小分子生物标记物。具体地,发现的是每种标记物在来自具有卵巢癌的受试者的样品中表现出浓度的特征升高或降低,并且它们可用于根据本发明的方法和用途。本生物标记物是敏感的和特异性的,并且它们可用于诊断和预后测试。该生物标记物可特别用于早期卵巢癌,如I期或II期卵巢癌。另外,对于卵巢癌诊断,大部分的本发明生物标记物还与患者的存活率有关,并因此它们在预测患者具有恶性卵巢肿瘤中以及在预测这些患者的预后中具有双重作用。本发明因此代表了超过目前用于诊断和/或预测卵巢癌的现有方法的重要优势。
因此,用于卵巢癌的本发明的小分子生物标记物允许更好地诊断或评估发展卵巢癌的风险。进一步地,本标记物在具有卵巢癌的患者中的治疗效力和肿瘤切除的确定中得到应用。
虽然根据本发明可以仅使用单种小分子生物标记物且足以提供可靠的结果,但是优选的是使用若干生物标记物来增加评估的可靠性。进一步地,可以将来自小分子生物标记物的预测或预后信息与用于卵巢癌的蛋白质生物标记物,如CA-125组合用于早期或晚期评估。
根据本发明的第一方面,提供了用于评估受试者是否处于发展卵巢癌的风险或正在遭受卵巢癌的体外筛查的方法,包括
由受试者的样品确定至少一种小分子生物标记物的浓度,其中,当与对照样品比较时,样品的浓度的升高或降低表示受试者遭受卵巢癌或具有增加的发展卵巢癌的风险;
(1)其中,与对照比较,浓度升高的至少一种小分子生物标记物选自由二羟基丁酸和三羟基丁酸组成的组;和/或
(2)其中,与对照比较,浓度降低的至少一种小分子生物标记物选自由鞘磷脂组成的组;和/或
(3)其中,与对照比较,浓度升高的至少一种小分子生物标记物是具有总共包含至少54个碳原子的酰基侧链的长链甘油三酯;和/或
(4)其中,与对照比较,浓度降低的至少一种小分子生物标记物是具有总共包含小于54个碳原子的酰基侧链的甘油三酯;和/或
(5)其中,与对照比较,浓度升高的至少一种小分子生物标记物是己二酸。
在实施方式中,用于评估受试者是否处于发展卵巢癌的风险中或正在遭受卵巢癌的方法进一步包括由样品确定至少一种另外的小分子生物标记物,其中,当与对照样品比较时,生物标记物的浓度的升高表示受试者遭受卵巢癌或具有增加的发展卵巢癌的风险;
(a)其中,与对照比较,浓度升高的至少一种另外的小分子生物标记物选自由羟基酸(醇酸,hydroxyacid)和己二酸组成的组;和/或
(b)其中,与对照比较,浓度升高的至少一种另外的小分子生物标记物选自由羟基丁酸和酮体组成的组。
在实施方式中,用于评估受试者是否处于发展卵巢癌的风险中或正在遭受卵巢癌的方法包括进行第(1)、(2)、(3)、(4)、(5)项中的任一项的确定;或第(1)、(2)、(3)、(4)、(5)项中的任一项以及第(a)或(b)项中的任一项的确定。
在另一实施方式中,确定第(1)、(2)、(a)和(b)项;第(1)、(2)、(3)、(a)和(b)项;或第(1)至(5)、(a)和(b)项。与仅使用一种小分子生物标记物相比,使用多种小分子生物标记物增加了评估的可靠性。
在实施方式中,方法进一步包括确定血液中针对卵巢癌的蛋白质生物标记物,如CA-125或HE4的水平,以及其中,增加的蛋白质生物标记物连同目前鉴定的小分子生物标记物确定(biomarker determination)表明受试者具有增加的发展卵巢癌或遭受卵巢癌的风险。因此,可以将目前识别的生物标记物与CA-125生物标记物组合使用以通过组合至少一种小分子生物标记物和CA-125生物标记物两者的分析来改善确定的可靠性。可以使用本领域已知的任何方法确定CA-125。优选地,由与用于确定小分子生物标记物相同的样品确定CA-125。
在实施方式中,确定卵巢癌蛋白标记物,如CA-125或HE4和3-羟基丁酸,并且其中蛋白质生物标记物和3-羟基丁酸的浓度的升高表示发展卵巢癌或遭受卵巢癌的增加的风险。组合分析增强了CA-125蛋白质生物标记物对于早期和晚期卵巢癌筛查和预后的特异性和灵敏度。CA-125和3-羟基丁酸的组合对于早期卵巢癌是特别有用的。
根据本发明的第二方面,提供了评估受试者是否具有针对卵巢癌的降低的存活预后的方法,包括测量来自受试者的样品中的至少一种小分子生物标记物的水平,其中,
相对于对照样品中对应的小分子生物标记物的水平,至少一种小分子生物标记物的水平的升高表示受试者具有针对卵巢癌的不良的存活预后,并且其中,该至少一种小分子生物标记物选自由二羟基丁酸、三羟基丁酸、羟基酸、己二酸、羟基丁酸和酮体组成的组;和/或
相对于对照样品中对应的小分子生物标记物的水平,至少一种小分子生物标记物的水平的降低表示受试者具有针对卵巢癌的不良的存活预后,并且其中,至少一种小分子生物标记物选自由鞘磷脂组成的组。
当针对癌症患者进行不同类型的治疗和它们的持续时间的评估和判定时,对于遭受卵巢癌的患者来说可靠的预后是重要的。另外,预后影响在治疗之后的后续事项(follow-up)的强度。最后,尽可能精确地评估疾病的预后对于患者和它们的健康来说是重要的。
根据本发明的第三方面,提供了用于评估接受了肿瘤疗法的受试者中的卵巢癌肿瘤切除的成功率的体外方法,包括由受试者的血液样品测量至少一种小分子生物标记物的水平,其中,相对于对照样品中的对应的小分子生物标记物的水平,至少一种小分子生物标记物的水平的升高或降低表示肿瘤切除是成功的,并且
(1)其中,与对照比较,浓度降低的至少一种小分子生物标记物选自由二羟基丁酸和三羟基丁酸组成的组;和/或
(2)其中,与对照比较,浓度升高的至少一种小分子生物标记物选自由鞘磷脂组成的组;和/或
(3)其中,与对照比较,浓度降低的至少一种小分子生物标记物是具有总共包含至少54个碳原子的酰基侧链的长链甘油三酯;和/或
(4)其中,与对照比较,浓度升高的至少一种小分子生物标记物是具有总共包含小于54个碳原子的酰基侧链的甘油三酯;和/或
(5)其中,与对照比较,浓度降低的至少一种小分子生物标记物是己二酸。
在实施方式中,用于评估卵巢癌肿瘤切除的成功率的方法进一步包括由样品确定至少一种另外的小分子生物标记物,其中,当与对照样品相比时,生物标记物的浓度的降低表示肿瘤切除是成功的;
(a)其中,与对照比较,浓度降低的至少一种另外的小分子生物标记物选自由羟基酸和己二酸组成的组;和/或
(b)其中,与对照比较,浓度降低的至少一种另外的小分子生物标记物选自由羟基丁酸和酮体组成的组。
在实施方式中,用于评估卵巢癌肿瘤切除的成功率的方法包括进行第(1)、(2)、(a)和(b)项、或第(1)至(5)、(a)和(b)项的确定。
监测肿瘤切除成功是治疗的一个重要的方面,并且这提供了关于进一步操作或治疗所需要的有价值的信息。因此,基于以上评估的结果,治疗之后可以是进一步的操作或药物疗法。
根据本发明的第四方面,提供了评估受试者中的卵巢癌疗法的效力的体外方法,包括
由受试者的样品确定至少一种小分子生物标记物的浓度,其中,当与对照样品比较时,样品的浓度的升高或降低表示疗法的效力;
(1)其中,将其浓度与对照比较的至少一种小分子生物标记物选自由二羟基丁酸和三羟基丁酸组成的组;和/或
(2)其中,将其浓度与对照比较的至少一种小分子生物标记物选自由鞘磷脂组成的组;和/或
(3)其中,将其浓度与对照比较的至少一种小分子生物标记物是具有总共包含至少54个碳原子的酰基侧链的长链甘油三酯;和/或
(4)其中,将其浓度与对照比较的至少一种小分子生物标记物是具有总共包含小于54个碳原子的酰基侧链的甘油三酯;和/或
(5)其中,将其浓度与对照比较的至少一种小分子生物标记物是己二酸;
(a)其中,将其浓度与对照比较的至少一种另外的小分子生物标记物选自由羟基酸和己二酸组成的组;和/或
(b)其中,与对照比较,浓度降低的至少一种另外的小分子生物标记物选自由羟基丁酸和酮体组成的组;
并且其中,(1)、(3)、(5)、(a)和(b)中的至少一个的升高或(2)或(4)的降低表明治疗无效;和/或
(1)、(3)、(5)、(a)和(b)中的至少一个的降低或(2)或(4)的降低表示治疗有效。
在该方法中,通过以下的目前识别的小分子生物标记物监测疗法的效力。选择的生物标记物反映卵巢癌的进展,并当癌症响应该疗法时,所选择的生物标记物接近针对对照样品确定的浓度。因此,可以基于受试者定制疗法使得仅继续表现出积极应答并因此发现为有效的疗法,以及中止表现出没有应答并因此发现为无效的疗法。
在评价受试者中的卵巢癌疗法的效力的体外方法的实施方式中,小分子生物标记物是3-羟基丁酸,并且另外确定CA-125,其中,3-羟基丁酸或CA-125中任一项的升高表示治疗无效以及3-羟基丁酸或CA-125中任一项的降低表示治疗有效。
在实施方式中,疗法可以包括通常给予具有卵巢癌的受试者的任何治疗,如但不限于化疗、放射疗法、激素疗法、抗血管生成剂疗法、靶定同源重组缺陷的疗法、抗体疗法或其他利用卵巢癌特异性信号路径的定向疗法。治疗可以包括对恶性组织的代谢具有直接影响的治疗。卵巢癌疗法可以包括给予影响脂质代谢的药物试剂。
根据本发明的第五方面,提供了确定受试者的卵巢组织中的代谢物的浓度的体外方法,包括
确定由受试者获得的血液样品中的代谢物的浓度;
比较代谢物的血液浓度与对照样品中的浓度,其中,与对照样品相比,代谢物的水平的升高表示受试者在卵巢组织中具有升高的代谢物浓度;
并且其中,代谢物选自由3-羟基丁酸、2-羟基丁酸、3,4-二羟基丁酸、SM(d18:1/21:0)、SM(d18:1/14:0)、己二酸、4-羟基苯乳酸(hydroxyphenyllactic acid)、2,4-二羟基丁酸、3-羟基异戊酸和2,3-二羟基丁酸组成的组。
在实施方式中,在卵巢组织中确定的该浓度的代谢物选自由2-羟基丁酸和/或3-羟基丁酸组成的组。
通常使用试验来进行生物标记物的确定。可以用多种化学品和高分辨率分析技术进行测定,视情况而定。根据本方法的合适的分析技术包括,但不限于质谱分析(MS)和核磁共振(NMR)。可以将能够溶解单个小分子生物标记物的任何高分辨率技术用于收集关于讨论的生物标记物的信息,如生物样品如血清、血浆、组织、尿液或唾液的生物标记物状况(profile)的浓度。优选地,使用质谱分析收集信息。可以将MS分析与另一种高效分离方法,如气相色谱法(GC)二维气相色谱法(GCxGC)、液相色谱法(LC)、高效液相色谱法(HPLC)或超高效液相色谱法(UPLC)偶联。
来自受试者的样品和对照样品可以是血清样品、血浆样品、唾液样品或尿液样品。血清和血浆样品是优选的。通过本领域熟知的技术可以制备样品。可替换地,来自受试者和对照样品两者的样品也可以是组织样品,例如卵巢组织样品。
根据某些实施方式,本发明的方法提供用于测量血浆样品或血清样品中的小分子生物标记物的水平,而不需要在检测之前分离或浓缩脱落的肿瘤细胞。在实施方式中,样品是非沉积的样品。在另一实施方式中,血浆样品基本不含残留的细胞。在又一实施方式中,用凝结激活剂处理血液样品并通过离心分离血清,可选地随后在分析之前冻融。
在另一实施方式中,在质谱分析之前,用来自样品的溶剂或溶剂混合物提取样品的小分子生物标记物。
合适的溶剂包括有机溶剂,如甲醇、氯仿/甲醇或其他类似的溶剂。
在另一实施方式中,在质谱分析之前衍生小分子生物标记物。在实施方式中,衍生(derivatization)包括用有机溶剂提取,在降低的压力下蒸发溶剂并衍生。
在另一实施方式中,在通过使用除去细胞的过滤器确定小分子生物标记物之前,过滤样品。在实施方式中,将具有30kDa的截留值的过滤器用于除去细胞。在又一实施方式中,使用除去蛋白质的过滤器。在实施方式中,在过滤之后重组样品。
在另一实施方式中,在确定小分子生物标记物之前,稀释样品或重组的样品。在实施方式中,在确定小分子生物标记物之前,将样品以至少1:2稀释。
在另一实施方式中,将防腐剂或内部质量标准添加到样品中。
本发明的小分子卵巢癌生物标记物使得能够容易、可靠和早期地预测卵巢癌。这将有助于,例如早期干涉、较少的症状发展和患病以及降低的发病率。本生物标记物还使得能够容易监测卵巢癌的进展,因为在不需要收集组织样品的情况下可以在血清样品上进行分析。
在某些实施方式中,卵巢癌是早期卵巢癌。
作为小分子卵巢癌生物标记物的羟基酸优选包含选自由4-羟基苯乳酸和3-羟基异戊酸组成的组中的至少一种化合物。
作为小分子卵巢癌生物标记物的二羟基丁酸优选包含选自由2,4-二羟基丁酸、3,4-二羟基丁酸和2,3-二羟基丁酸组成的组中的至少一种化合物。
作为小分子卵巢癌生物标记物的三羟基丁酸优选包含选自由2,3,4-三羟基丁酸组成的组中的至少一种化合物。
作为小分子卵巢癌生物标记物的鞘磷脂优先选自鞘磷脂,其具有d18:1类鞘氨醇碱、可选地具有含有14-24个碳原子和0-1个双键的酰胺连接的脂肪酸。更加优选地,鞘磷脂选自由SM(d18:1/14:0)、SM(d18:1/20:1)、SM(d18:1/21:0)、SM(d18:1/22:0)、SM(d18:1/22:1)、SM(d18:1/23:0)、SM(d18:1/24:0)组成的组。
作为小分子卵巢癌生物标记物的羟基丁酸和酮体优选地包含选自由2-羟基丁酸、3-羟基丁酸、丙酮和乙酰乙酸组成的组中的化合物。
作为小分子卵巢癌生物标记物的长链甘油三酯包含具有至少54个碳原子的总酰基链长度的化合物。
作为小分子卵巢癌生物标记物的短链甘油三酯包含具有不多于53个碳原子的总酰基链长度的化合物。
对照可以是由单个健康个体或具有良性肿瘤或其他引起与卵巢癌类似的症状的医学病症的受试者或发展恶性组织之前的相同的受试者确定的浓度。对照还可以是这样的样品,其代表来自健康的个体的普遍群体的样品的组合。可替换地,对照可以是涉及之前确定的、计算的或推断的样品中的生物标记物的一组数据,或可能还有待于确定、计算或推断,或也可以从文献中获得。
当由血清样品作为用于卵巢癌的生物标记物分析3-羟基丁酸、2-羟基丁酸、3,4-二羟基丁酸、2,4-二羟基丁酸、2,3-二羟基丁酸、SM(d18:1/21:0)、SM(d18:1/14:0)、己二酸、4-羟基苯乳酸和3-羟基异戊酸时,发明人出乎意料地发现它们的浓度遵循在癌症组织中确定的浓度。因此,通过确定它们在血清中的浓度可以确定这些化合物在卵巢组织中的浓度。通过使用来自血清的样品能够确定肿瘤内生物标记物的浓度具有直接由血液样品监测肿瘤内的代谢的优势。这可以在不成像或手术的情况下监测肿瘤的大小和在身体中的转移。另外,小分子代谢物可以用作治疗疗效的标记物,以及多种治疗选择如何影响肿瘤细胞的代谢。
根据第六方面,提供了用于评估受试者是否处于发展卵巢癌的风险或正在遭受卵巢癌的体外筛查的方法,包括确定呼吸中的挥发性有机化合物(VOC)的浓度,其中,当与对照样品比较时,呼吸中的VOC的浓度的升高表示受试者遭受卵巢癌或具有增加的发展卵巢癌的风险。
可以例如通过质谱法、传感器阵列(sensor assay)和电子鼻、激光吸收光谱或离子迁移率光谱法检测挥发性有机化合物,如丙酮,以及,例如已经报告了健康的个人应当在它们的呼吸中具有低于0.9ppm的丙酮水平。本发明人在体液中识别了卵巢癌的小分子生物标记物,其可以挥发或在化学反应中转化为挥发性化合物,并且因此由于它们趋向于,例如从血液移到肺的呼气中还可以从呼吸中被检测到。因此,根据本发明的任何易挥发的生物标记物如丙酮,具有在受试者的呼吸中测量的水平高于在对照中测量的水平时,表示发展卵巢癌的风险增加。
在示例性的实施方式中,与对照比较,浓度升高的至少一种小分子生物标记物选自由2,4-二羟基丁酸、3,4-二羟基丁酸、2,3-二羟基丁酸、2,3,4-三羟基丁酸、4-羟基苯乳酸、3-羟基异戊酸、己二酸、2-羟基丁酸、3-羟基丁酸、乙酰乙酸和丙酮组成的组。
在示例性的实施方式中,与对照比较,浓度降低的至少一种小分子生物标记物选自由SM(d18:1/14:0)、SM(d18:1/20:1)、SM(d18:1/21:0)、SM(d18:1/22:0)、SM(d18:1/22:1)、SM(d 18:1/23:0)和SM(d18:1/24:0)组成的组。
在示例性的实施方式中,以上方法包括确定选自由以上在第(1)-(5)、(a)和(b)项中列出的生物标记物组成的组中的1、2、3、4、5、6、7、8、9、10或更多种小分子生物标记物。
在示例性的实施方式中,通过使用质谱分析、核磁共振波谱法、荧光光谱法或双偏振干涉、免疫测定、酶测定、比色测定、荧光测定、快速测试、呼吸测试和/或通过能够特异结合生物标记物的结合部分(binding moiety)确定生物标记物浓度。
在另一方面,提供了药物在用于治疗需要其的受试者的卵巢癌或其一种或多种并发症中的用途,该方法包括使用用于卵巢癌治疗的有效的药物,其中,使用根据本发明的第四方面的用于评价治疗效力的以上方法来评价通过药物的治疗效力。
在示例性的实施方式中,以引起肿瘤中的至少一种小分子卵巢癌生物标记物的浓度从初始水平变化至对照样品的浓度的剂量给予药物,并且其中,使用根据以上方法的方法确定至少一种小分子卵巢癌生物标记物的浓度。
实施例
提供了以下实施例以举例说明本发明的各个方面。它们不旨在限制本发明,本发明通过所附权利要求限定。
实施例1材料和方法
描述研究群组和样品
在2000年09月至2011年02年之间在Charite医科大学(柏林,德国)从手术前的初级卵巢癌患者以及从没有卵巢癌的患者收集血清样品。伦理委员会批准了该样品用于研究的用途。在手术之前或在随后的治疗、样品收集以及临床和手术数据的文档编制期间,得到患者告知同意书。将验证的文档编制系统用于记录手术数据。没有卵巢癌的研究群体由具有引起与卵巢癌类似的症状的良性肿瘤、子宫内膜异位、子宫肌瘤(uterus)、子宫附件炎和其他病症的患者组来组成。使用包含凝结激活剂(Vacutainer,BD,Medical-Pharmaceutical System,Franklin Lakes,NJ)的血清管在Tumor Bank Ovarian Cancer项目(http://toc-network.de)内收集血液。在室温下使收集的血液凝结30分钟至2小时,以及在1200g下通过离心分离血清15分钟。等分血清并将其存储在-80℃。
在手术时收集肿瘤组织样品并在切除15分钟内立即将其冷冻在液氮中,然后存储在-80℃。所有组织样品都经历组织病理学说评估以验证组织亚类型和高组织质量(tissuequality),并且仅将呈现适当的肿瘤面积的试样包括在代谢和脂质分析中。
GCxGC-TOF方法
通过用Retsch均化器(3分钟,20Hz)均匀化3-4mg组织来制备肿瘤样品。将样品均匀化到0.9%NaCl中,并调节体积以得到0.05mg/μl的浓度。将400μl甲醇和5μl标准混合物(缬氨酸-d8,37.6mg/l)、十七烷酸(186.5mg/l)、琥珀酸-d4(62.9mg/l)添加到70μl匀浆液中。对于血清样品,将400μl甲醇和10μl标准混合物(缬氨酸-d8,37.6mg/l)、十七烷酸(186.5mg/l)、琥珀酸-d4(62.9mg/l)、谷氨酸-d5(103.5mg/l)添加到30μl样品中。涡旋样品2分钟。在室温下30分钟之后,在10000rpm下离心样品5分钟。将200μl的上清液移至GC小瓶中并在氮气下蒸发至干燥。用25μl(MOX)(45℃,60分钟)和25μl(MSTFA)(45℃,60分钟)和50μl己烷与保留化合物(retention index compound)衍生化样品,并将注射标准物(4,4'-二溴八氟联苯)添加到样品中。
对于分析,使用配备有低温调节器的Leco Pegasus 4D GCxGC-TOFMS仪器(LecoCorp.,St.Joseph,Ml)。该仪器的GC部分是Agilent 6890气相色谱仪(AgilentTechnologies,Palo Alto,CA),其配备有分离/不分离(split/splitless)注射器。第一尺寸色谱柱是具有0.18mm的内径和0.18μm的固定相膜厚度的10-m Rxi-5MS毛细管柱,以及第二尺寸色谱柱是具有100μm的内径和0.1μm的膜厚度的1.5m BPX-50毛细管柱。将甲基去活的保留缺口(methyl deactivated retention gap)(1.5m x 0.53mm i.d.)用于第一柱的前面。将高纯度氦用作恒定压力模式(40psig)下的载气。在第二尺寸中使用4-s分离时间(separation time)。用100光谱/秒在45-700amu下测量MS光谱。在240℃下将不分离注射(1.0μl)用于注射。温度程序如下:第一尺寸柱式加热炉线性变化开始于50℃,保持2分钟,之后将温度以7℃/min的速率程序升温至240℃,以及进一步以25℃/min至300℃,然后保持在该温度下3分钟。将第二尺寸柱温保持比对应的第一尺寸柱高15℃。程序升温速率和保持时间对于两个柱相同。
将ChromaTOF供应商软件(LECO)用于内部样品数据处理,以及自行研制的Guineu(Castillo et al.,2011,Anal Chem)用于样品的排列、归一化和峰匹配。首先基于在运行的所有样品的总分布中检测到的峰数过滤峰。通过校正内标C17:0进行未校正的代谢物的归一化。手动检查每个血清样品中的27种代谢物以及每个肿瘤组织样品中的29种代谢物用于正确的积分和识别。针对NIST05质谱资料库搜索来自GC*GC-TOFMS分析的其他质谱。
LC-MS方法
通过用Retsch均化器(3分钟,20Hz)均匀化2-3mg组织来制备肿瘤样品。将样品均匀化到0.9%NaCl中,并调节体积以得到约0.05mg/μl的浓度。在添加内标与0.5-1μg/样品的浓度水平的Cer(d18:1/17:0)、PC(17:0/0:0)、PC(17:0/17:0)、PE(17:0/17:0)和TG(17:0/17:0/17:0)的混合物之后,用氯仿:甲醇(2:1;250μl)提取样品。涡旋样品2分钟,在RT下培育30分钟并在7800g下离心3分钟。在UPLC-MS分析之前,将0.5μg/样品浓度水平的包含PC(16:1-D3/0:0)、PC(16:1/16:1-D6)和TG(16:0/16:0/16:0-13C3)的标记的脂质标准混合物添加到分离的脂质提取物(100μl)中。
将10μl血清样品用于分析,以及通过添加内标与0.2μg/样品的浓度水平的DG(17:0/17:0/0:0)、CE(19:0)、Cer(d18:1/17:0)、MG(17:0/0:0/0:0)、PA(17:0/17:0)、PC(17:0/0:0)、PC(17:0/17:0)、PE(17:0/17:0)、PG(17:0/17:0)和TG(17:0/17:0/17:0)的混合物,用氯仿:甲醇(2:1,100μl)提取来制备样品。涡旋样品2分钟,在RT下培育30分钟并在7800g下离心3分钟。在UPLC-MS分析之前,将0.5μg/样品浓度水平的包含PC(16:1-D3/0:0)、PC(16:1/16:1-D6)和TG(16:0/16:0/16:0-13C3)的标记的脂质标准混合物添加到分离的脂质提取物(60μl)中。
来自肿瘤和血清样品的脂质提取物在与Acquity Ultra Performance LCTM(UPLCTM)组合的Waters Q-Tof Premier质谱仪上分析。柱是Acquity UPLCTM BEH C18 2.1×100mm,颗粒1.7μm。溶剂体系包含:A)水(1%1M NH4Ac,0.1%HCOOH)和B)乙腈/异丙醇(1:1,1%1M NH4Ac,0.1%HCOOH)。梯度起始于65%A/35%B,在2分钟内达到80%,在7分钟内达到100%B,并保持接下来的7分钟。在以下运行之前,存在5分钟的再平衡步骤。流动速率是0.400ml/min以及注射量是1.0μl。将利血平(reserpine)用作锁定喷射的参考化合物。使用ESI以积极模式进行脂质剖析,并在m/z 300-1200的质量范围下用0.2秒的扫描持续时间采集数据。
使用MZmine 2软件(http://mzmine.sourceforge.net/)处理数据,以及该处理包括峰的排列、峰积分、归一化和峰识别。脂质识别是基于内部的频谱资料库。使用内标(其代表存在于样品中的脂质的类别)归一化数据:通过将每种识别的脂质的强度除以其对应的标准的强度,以及将其与标准的浓度相乘归一化每种识别的脂质的强度。用PC(17:0/0:0)归一化除胆甾醇酯之外的所有单酰基脂质,如单酰基甘油磷脂,用PC(17:0/17:0)归一化除氨乙醇磷脂之外的所有二酰基脂质,用Cer(d18:1/17:0)归一化所有神经酰胺,用PE(17:0/17:0)归一化所有二酰基氨乙醇磷脂,用TG(17:0/17:0/17:0)归一化三酰甘油酯,以及用血清中的ChoE(19:0)和组织样品中的TG(17:0/17:0/17:0)归一化胆甾醇酯。用以下归一化其他(未识别的)分子物质:PC(17:0/0:0),停留时间<300s;PC(17:0/17:0),停留时间在300s和410s之间;以及TG(17:0/17:0/17:0),停留时间更长。用样品的重量归一化肿瘤样品。
统计学分析
针对没有恶性病(对照组)的100个受试者以及158个卵巢癌患者血清样品得到来自GCxGC-TOF方法的数据。另外,针对具有匹配的血清样品的112个卵巢癌患者得到来自肿瘤组织分析的数据。针对没有恶性病的100个受试者以及158个卵巢癌患者血清样品得到来自LC-MS方法的结果。另外,针对具有匹配的血清样品的134个卵巢癌患者得到来自肿瘤组织分析的数据。可获得145个卵巢癌患者和73个没有恶性病的受试者的CA-125数据。
使用3.1.0版本的R进行所有的统计学分析。为了比较两组,在log2转换数据之后,计算未配对的t测试和倍数变化。在数据中存在零值的情况下,用对应于所有样品中的对应的分子的最小值的一半的值输入数据。通过Kaplan-Meier图与中位分隔(median split)和时序测试(logrank test)探究小分子与存活率的关联。另外,在将肿瘤减少信息合并和没有合并到模型的情况下,针对每个小分子进行Cox比例风险回归(Cox比例危险回归,Coxproportional hazard regression)测试。用于来自具有小分子的卵巢癌诊断的预测模型是二进制逻辑回归模型。为了交叉验证,将数据集1000次随机分到训练组(包含2/3样品)中,并在验证组(包含1/3样品)中测试构造的模型。对于I-II期肿瘤的分析,没有进行交叉验证。
使用RANSAC排列方法匹配来自LC-MS和GCxGC-TOF-MS数据的肿瘤组织和血清样品的小分子生物标记物,该RANSAC排列方法已经在MZmine 2(Pluskal et al.,2010,BMCBioinformatics)以及在自行研发(in-house develop)的Guineu软件(Castillo et al.,201 1,Anal Chem)中进行。
实施例2结果
关于选定的生物标记物分子的信息
GCxGC-TOF-MS数据包含497个代谢物峰以及LC-MS数据包含635个脂质峰。在本专利申请中,对于大部分关心的选定的代谢物,示出了实例结果并将其列于表1中。基于统计学分析的结果、化合物的化学结构和生物重要性选择分子。
有时,GCxGC-TOF-MS数据可以包含具有相同识别标志的若干峰。这可能是因为分析原因或者,例如立体异构结构。在GCxGC-TOF-MS分析包含参考标准化合物的情况下,始终将对应于标准化合物的峰选定为最后的结果。2,3-二羟基丁酸和2,3,4-三羟基丁酸参考化合物没有包含在分析中。对于这些分子,将示出了恶性对良性比较以及存活率分析两者中的统计上显著的结果的峰选定为实例。
表1.示出了实例结果的分子的质谱细节。对于由LC-MS方法获得的分子,示出了停留时间(s)和m/z值。对于由GCxGC-TOF-MS方法获得的分子,示出了保留指数(RTI)和质谱。
小分子生物标记物的浓度在患卵巢癌的患者中以及尤其在肿瘤减少不完全的患者中变化。
表2总结了对于选定的小分子生物标记物和作为比较的在卵巢癌诊断中广泛使用的蛋白质生物标记物CA-125的结果。
由表2和图1(a)至图1(i)显然的是,当与具有良性肿瘤和其他非恶性病症的对照受试者相比时,所有小分子生物标记物在它们在卵巢癌患者血清样品中的水平上示出统计学高度显著的差异。除了鞘磷脂示出相反的趋势,所有选定的小分子生物标记物在患恶性卵巢肿瘤的患者中升高。尤其是3,4-二羟基丁酸和3-羟基丁酸分别示出了1e-27和1e-21数量级的低的p值,表示高度显著的结果。
同样,三酰甘油酯(TAG)示出了它们在卵巢癌患者的血清中的水平的变化。这些脂质呈现了这样的趋势,其中当与对照组相比时,在卵巢癌患者中,在它们的脂肪酰基侧链中具有53或更少碳的那些TAG降低以及具有54或更多碳的那些升高。
为了探究小分子生物标记物是否与患者中的肿瘤块的量有关,将卵巢癌患者分成两组,即在手术期间肿瘤减少完全或不完全的那些。该信息没有直接提供肿瘤的大小,但是在手术期间肿瘤减少的完全性与存在于身体中的肿瘤块相关是合乎逻辑的。如表2所示,典型的卵巢癌标记物CA-125没有示出肿瘤减少完全或不完全的患者之间的统计学上的显著的差异。相反,尤其是属于二羟基丁酸和三羟基丁酸以及鞘磷脂类的小分子示出了统计学上显著的结果。值得注意的,对于二羟基丁酸和三羟基丁酸观察到渐进的变化使得在患良性病症的患者中观察到最低的水平,以及在恶性肿瘤和肿瘤减少不完全的患者中观察到最高的水平(图2)。对于鞘磷脂类的化合物观察到正相反的现象。
总之,所有小分子生物标记物以及CA-125蛋白质标记物在卵巢癌患者的血清中示出改变的水平,但是仅选择的小分子生物标记物与肿瘤减少有关,并因此与患者的肿瘤块直接有关。因此,小分子生物标记物比CA-125更好地反映肿瘤的大小。
表2.恶性肿瘤、肿瘤减少和患者的总存活率的统计学分析结果。log2 fc=log2倍数变化,TR=肿瘤减少。以粗体突出显示了P值<0.05。
用于恶性肿瘤的预测模型
构造逻辑回归模型以探究小分子生物标记物的浓度是否可以用于预测哪位患者正在遭受恶性肿瘤。为此,在每种情况下,将数据随机分配1000次到训练组(2/3样品)中并在验证组(剩余的1/3样品)中测试训练组中构成的模型。基于所有1000个模型绘出ROC曲线,并在图3(a)至图3(b)中示出了对于四种不同情况的实例。表3示出了小分子生物标记物和CA-125的不同组合的结果。
如表3所示,选择了1000次的随机的3种脂质或代谢物示出相当低的AUC值(意味着小于0.70)和大的置信区间,表示仅特定的小分子生物标记物能够预测患者患有恶性卵巢肿瘤。三种鞘磷脂示出了平均AUC值0.78,以及3,4-二羟基丁酸连同3-羟基丁酸示出了高平均AUC值0.91。CA-125还示出了平均AUC值0.95,但是当将鞘磷脂或丁酸中的任一种连同CA-125合并至模型时,预测更加准确。尤其是将3,4-二羟基丁酸和3-羟基丁酸合并到模型中使AUC值升高至0.98,即接近于将组完全分开。
表3.具有小分子和CA-125蛋白质标记物的不同组合的实施例逻辑回归模型的平均AUC值和95%置信区间。
CA-125蛋白质标记物在诊断晚期卵巢癌上是良好的,但是早期卵巢癌的检测更具挑战。因此,将需要用于早期卵巢癌的新的生物标记物。本研究的群体包括仅少数患者患早期(I或II)卵巢癌(n=7)。不过,在从对照组分类这些病例中,构造了逻辑回归模型。变量包括在这些实例模型中以及它们的AUC值呈现在表4中并在图4中直观化。在该研究群体中,CA-125出乎意料地示出了高AUC值0.91。出乎意料地,例如仅3-羟基丁酸示出了较好的AUC值0.93。此外,当将一种或多种小分子生物标记物连同CA-125合并到模型中时,AUC值升高。最终,与CA-125合并的3-羟基丁酸示出AUC值0.994,以及当另外地将3,4-二羟基丁酸添加到模型中时,AUC值达到1.0。
表4.小分子和CA-125蛋白质标记物的不同组合的逻辑回归模型的AUC值。
| CA-125 | 3,4-DHBA | 3-HBA | SM(d18:1/24:0) | SM(d18:1/22:1) | SM(d18:1/23:0) | AUC |
| x | x | x | x | 1.00 | ||
| x | x | x | 1.00 | |||
| x | x | 0.99 | ||||
| x | x | x | x | 0.95 | ||
| x | x | 0.95 | ||||
| x | x | x | 0.94 | |||
| x | x | 0.93 | ||||
| x | 0.93 | |||||
| x | 0.91 | |||||
| x | x | x | 0.64 |
总之,小分子生物标记物在,尤其早期卵巢癌的诊断中胜过CA-125,还在整个研究群体中示出了良好的预测值。尤其组合一种或若干种生物标记物连同CA-125,与仅CA-125相比,可以得到具有对于卵巢癌诊断的更高的灵敏度和特异性的模型。
小分子水平与患者的总存活率有关
接下来,探究小分子生物标记物是否与患恶性肿瘤的患者的总存活率有关。为了探究这个,针对每种探究的小分子和CA-125蛋白质标记物,将患者分为两组,具有高于或低于所有样品的中值的分子浓度的那些。然后,构造Kaplan-Meier图(图5(a)至图5(i)),并将时序测试用于计算组之间的总存活率的差异的p值。在该研究群体中,CA-125标记物没有示出关于患者的存活率的统计上显著的结果(表2)。然而,所有小分子(除SM(d18:1/14:0)以及羟基丁酸和酮体之外)示出了统计上显著的结果。由图5(a)至图5(i)和表2明显的是,二羟基丁酸和三羟基丁酸、羟基酸和己二酸的浓度升高与更差的总存活率有关。相反,卵巢癌患者的血清中的鞘磷脂的浓度越低预示患者的总存活率越差。
直观的是在手术期间的肿瘤减少的成功与患者的总存活率有关。随着发现多种小分子与肿瘤减少有关(从而间接与肿瘤负担有关),探究了小分子生物标记物是否可以由肿瘤减少的成功性独立预测存活率。为此,在具有或不具有合并至模型的肿瘤减少信息的情况下,针对每种小分子和CA-125构造cox比例风险回归模型。值得注意的,在Kaplan-Meier分析中示出了统计学上显著的结果的几乎所有的小分子生物标记物还在cox回归模型中示出了统计上显著的结果,即使将肿瘤减少合并到模型中。这意味着小分子是患者的总存活率的强预报因子,并且可以独立于肿瘤减少信息预测存活率。
总之,小分子生物标记物与患者的总存活率有关,并与CA-125相反,示出了预后值。
血清中的小分子生物标记物的浓度与肿瘤浓度相关
由之前的结果明显的是,卵巢癌的存在引起患者的血清中的小生物标记物的浓度的变化。为了探究在相同患者的肿瘤中是否也可以观察到相同现象,将相同的方法论应用于肿瘤组织样品,以及用Pearson和Spearman相互关系分析来评价血清和肿瘤组织之间的代谢物的相互关系。表5示出了那些小分子生物标记物的结果,其在Pearson或Spearman相关分析中示出了统计上显著的结果(p<0.05)和R2值>0.2。如表5所示,之前的章节中提到的多种小分子生物标记物示出了显著的相关性。对于羟基丁酸3,4-二羟基丁酸和鞘磷脂观察到最大的相互关系,以及结果示于图6(a)至图6(c)中。
表5.当测量血清和组织样品中的浓度之间的相互关系时,小分子生物标记物的Pearson和Spearman p值和R2值。
结果的生物重要性
在之前章节中呈现的结果中观察到的值得注意的现象是用于卵巢癌诊断和预后的最有希望的小生物标记物仅属于几个化合物类别。脂肪酸氧化产生酮体、3-羟基丁酸酯、乙酰乙酸和丙酮。这三种中,酮体、3-羟基丁酸酯和乙酰乙酸包含在数据组中,以及这些中的两者在卵巢癌患者的血清中增加。另外,示出了类似的结构的化合物、即2-羟基丁酸、3,4-二羟基丁酸、2,3-二羟基丁酸、2,3,4-三羟基丁酸和3-羟基异戊酸(也称为β-羟基β-甲基丁酸)都在卵巢癌患者的血清中升高,并且这些中的大部分还示出了强预后值。此外,3-羟基丁酸和2-羟基丁酸在它们在血清和肿瘤的水平上示出了强相关性。最后,通过Ω氧化可以在人体生理学中产生己二酸(其还示出了诊断和预后值),Ω氧化是另一种脂肪酸氧化路线。因此,合理的是脂肪酸氧化和酮体的生产增加是卵巢癌代谢的关键特征,这可以解释目前的结果。可能的血清脂质的吸收增加可以改变血清及其脂蛋白组成,并因此也可能通过卵巢癌细胞的改变的脂质代谢来解释鞘磷脂的水平降低以及它们与患者的预后的关联。在本研究中唯一没有示出与羟基丁酸或脂质代谢的明显关联的小生物标记物是4-羟基苯乳酸,这可能指向肿瘤中的氨基酸分解代谢。
重要的是认识到β-羟基丁酸和乙酰乙酸两者在卵巢癌患者中升高,以及如图7所示,β-羟基丁酸酯可以转化为乙酰乙酸,乙酰乙酸可以转化为丙酮。丙酮是易挥发的分子,可以在呼吸中检测到它。因此,基于目前的发现,可以将卵巢癌患者的血清或呼吸中的丙酮用作卵巢癌的诊断生物标记物是合乎逻辑的。
Claims (23)
1.小分子生物标记物在制备用于评估受试者是否处于发展卵巢癌的风险或者正在遭受卵巢癌的试剂、组合物或试剂盒中的用途,其中,所述评估包括:
由来自所述受试者的样品确定至少一种小分子生物标记物的浓度,其中,当与对照样品比较时,所述至少一种小分子生物标记物的浓度的升高表示所述受试者遭受卵巢癌,或者具有发展卵巢癌的增加的风险;
其中,与所述对照样品比较,浓度升高的所述至少一种小分子生物标记物是二羟基丁酸和/或三羟基丁酸。
2.根据权利要求1所述的用途,进一步包括由所述来自所述受试者的样品确定至少一种另外的小分子生物标记物的浓度,其中,当与对照样品比较时,所述生物标记物的浓度的升高或降低表示所述受试者遭受卵巢癌,或者具有发展卵巢癌的增加的风险;
其中,与所述对照样品比较,浓度升高的所述至少一种另外的小分子生物标记物是羟基酸、羟基丁酸、酮体、具有总共包含至少54个碳原子的酰基侧链的长链甘油三酯和/或己二酸,和/或
其中,与所述对照样品比较,浓度降低的所述至少一种另外的小分子生物标记物是鞘磷脂和/或具有总共包含小于54个碳原子的酰基侧链的甘油三酯。
3.根据权利要求2所述的用途,其中,确定二羟基丁酸、三羟基丁酸、鞘磷脂、羟基酸、己二酸、羟基丁酸或酮体的浓度。
4.根据权利要求1所述的用途,进一步包括确定血液中的CA-125和/或HE4的水平,其中,当权利要求1所述的用途表明发展或遭受卵巢癌的风险增加时,升高的CA-125和/或HE4水平表示所述受试者具有发展或遭受卵巢癌的增加的风险。
5.根据权利要求2所述的用途,其中,所述小分子生物标记物是3-羟基丁酸,以及所述用途用于评估早期或晚期卵巢癌。
6.小分子生物标记物在制备用于评估受试者对于卵巢癌是否具有降低的存活预后的试剂、组合物或试剂盒中的用途,其中,所述评估包括测量来自所述受试者的样品中的至少一种小分子生物标记物的水平,其中,
相对于对照样品中的对应的小分子生物标记物的水平,所述至少一种小分子生物标记物的水平的升高表示所述受试者对于卵巢癌具有不良的存活预后,并且其中,所述至少一种小分子生物标记物选是二羟基丁酸和/或三羟基丁酸。
7.根据权利要求6所述的用途,进一步包括由所述来自所述受试者的样品确定至少一种另外的小分子生物标记物,其中,相对于对照样品中的相应小分子生物标记物的水平,所述至少一种另外的生物标记物的水平的升高或降低表示所述受试者对于卵巢癌具有差的存活预后;
其中,与所述对照样品比较,水平升高的所述至少一种另外的小分子生物标记物是羟基酸、己二酸、羟基丁酸和/或酮体,和/或
其中,与所述对照样品比较,水平降低的所述至少一种另外的小分子生物标记物是鞘磷脂。
8.小分子生物标记物在制备用于评估受试者中的卵巢癌肿瘤切除的成功率的试剂、组合物或试剂盒中的用途,其中,所述评估包括测量来自所述受试者的样品中的至少一种小分子生物标记物的水平,其中,相对于对照样品中的对应的小分子生物标记物的水平,所述至少一种小分子生物标记物的水平的降低表示肿瘤切除是成功的,
其中,与所述对照样品比较,浓度降低的所述至少一种小分子生物标记物是二羟基丁酸和/或三羟基丁酸。
9.根据权利要求8所述的用途,进一步包括由所述来自所述受试者的样品确定至少一种另外的小分子生物标记物的浓度,其中,当与对照样品比较时,所述生物标记物的浓度的升高或降低表示所述肿瘤切除是成功的;
其中,与所述对照样品比较,浓度降低的所述至少一种另外的小分子生物标记物是羟基酸、羟基丁酸、酮体、具有总共包含至少54个碳原子的酰基侧链的长链甘油三酯和/或己二酸,和/或
其中,与所述对照样品比较,浓度升高的所述至少一种另外的小分子生物标记物是鞘磷脂和/或具有总共包含小于54个碳原子的酰基侧链的甘油三酯。
10.根据权利要求9所述的用途,其中,确定二羟基丁酸、三羟基丁酸、鞘磷脂、羟基酸、己二酸、羟基丁酸或酮体的浓度。
11.小分子生物标记物在制备用于评估受试者中的卵巢癌疗法的效力的试剂、组合物或试剂盒中的用途,其中,所述评估包括
由来自所述受试者的样品确定至少一种小分子生物标记物的浓度,其中,当与对照样品比较时,所述至少一种小分子生物标记物的浓度的降低表示所述疗法的效力;
其中,与所述对照样品比较,浓度降低的所述至少一种小分子生物标记物是二羟基丁酸和/或三羟基丁酸。
12.根据权利要求11所述的用途,进一步包括由所述来自所述受试者的样品确定至少一种另外的小分子生物标记物的浓度,其中,当与对照样品比较时,所述生物标记物的浓度的升高或降低表示所述疗法的效力;
其中,与所述对照样品比较,浓度升高的所述至少一种另外的小分子生物标记物是鞘磷脂和/或具有总共包含小于54个碳原子的酰基侧链的甘油三酯;和/或
其中,与所述对照样品比较,浓度降低的所述至少一种另外的小分子生物标记物是具有总共包含至少54个碳原子的酰基侧链的长链甘油三酯、己二酸、羟基酸、羟基丁酸和/或酮体。
13.根据权利要求12所述的用途,其中,所述小分子生物标记物是3-羟基丁酸,并且另外确定CA-125和/或HE4,其中,3-羟基丁酸、CA-125和/或HE4中的任一种的升高表示治疗无效,以及3-羟基丁酸、CA-125和/或HE4中的任一种的降低表示治疗有效。
14.根据权利要求11所述的用途,其中,所述卵巢癌疗法包括给予影响脂质代谢的药物试剂。
15.小分子生物标记物在制备用于确定受试者的卵巢组织中的代谢物的浓度的试剂、组合物或试剂盒中的用途,其中,所述确定包括
确定由所述受试者获得的血液样品中的所述代谢物的浓度;
比较所述代谢物的血液浓度与对照样品中的浓度,其中,与所述对照样品相比,所述代谢物的水平的升高表示所述受试者在卵巢组织中具有升高的所述代谢物的浓度;
并且其中,所述代谢物是:3,4-二羟基丁酸、2,4-二羟基丁酸和/或2,3-二羟基丁酸。
16.根据权利要求15所述的用途,进一步包括由来自所述受试者的样品确定至少一种另外的代谢物的浓度,其中,所述至少一种另外的代谢物是3-羟基丁酸、2-羟基丁酸、SM(d18:1/21:0)、SM(d18:1/14:0)、己二酸、4-羟基苯乳酸和/或3-羟基异戊酸。
17.根据权利要求16所述的用途,其中,在所述卵巢组织中确定浓度的所述代谢物选自由2-羟基丁酸和3-羟基丁酸组成的组。
18.根据权利要求1-17中任一项所述的用途,其中,所述用途包括确定2、3、4、5、6、7、8、9或10种小分子生物标记物的浓度。
19.根据权利要求1-17中任一项所述的用途,其中,通过使用质谱分析、核磁共振波谱法、荧光光谱法、双偏振干涉、免疫测定、酶测定、比色测定、荧光测定、快速测试、呼吸测试或利用能够特异地结合所述生物标记物的结合部分确定所述生物标记物浓度。
20.根据权利要求1-17中任一项所述的用途,其中,所述至少一种小分子生物标记物是:2,4-二羟基丁酸、3,4-二羟基丁酸、2,3-二羟基丁酸和/或2,3,4-三羟基丁酸,该至少一种小分子生物标记物的浓度是与所述对照样品比较的。
21.根据权利要求2、3、4、7、9、10和12中任一项所述的用途,其中,所述至少一种小分子生物标记物是SM(d18:1/14:0)、SM(d18:1/20:1)、SM(d18:1/21:0)、SM(d18:1/22:0)、SM(d18:1/22:1)、SM(d18:1/23:0)和/或SM(d18:1/24:0),该至少一种小分子生物标记物的浓度是与所述对照样品比较的。
22.根据权利要求1、6、8、11和16中任一项所述的用途,其中,所述卵巢癌是早期卵巢癌。
23.小分子生物标记物在制备用于评价用于卵巢癌治疗的药物的有效性的试剂、组合物或试剂盒中的用途,所述有效性是根据权利要求11中所公开的评估来评价的。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FI20145855 | 2014-10-02 | ||
| FI20145855 | 2014-10-02 | ||
| PCT/FI2015/050654 WO2016051020A1 (en) | 2014-10-02 | 2015-10-02 | Methods for detecting ovarian cancer |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN106716127A CN106716127A (zh) | 2017-05-24 |
| CN106716127B true CN106716127B (zh) | 2020-12-08 |
Family
ID=55629471
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201580052938.0A Active CN106716127B (zh) | 2014-10-02 | 2015-10-02 | 用于检测卵巢癌的方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US10534001B2 (zh) |
| EP (1) | EP3201623B1 (zh) |
| JP (1) | JP6892820B2 (zh) |
| KR (1) | KR20170061704A (zh) |
| CN (1) | CN106716127B (zh) |
| AU (1) | AU2015326756A1 (zh) |
| BR (1) | BR112017006593A2 (zh) |
| CA (1) | CA2959832A1 (zh) |
| SG (1) | SG11201701875YA (zh) |
| WO (1) | WO2016051020A1 (zh) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3351938A1 (en) * | 2017-01-18 | 2018-07-25 | BIOCRATES Life Sciences AG | New biomarkers for assessing ovarian cancer |
| WO2019008009A1 (en) | 2017-07-05 | 2019-01-10 | Zora Biosciences Oy | METHODS OF DETECTING OVARIAN CANCER |
| CN107656006A (zh) * | 2017-09-08 | 2018-02-02 | 上海市东方医院 | 用于检测血清或者血浆中α‑羟基丁酸浓度的试剂盒和方法 |
| CN108152430A (zh) * | 2017-12-21 | 2018-06-12 | 上海中科新生命生物科技有限公司 | 基于prm检测的卵巢癌标志物检测试剂盒及检测方法 |
| CN111430030A (zh) * | 2020-04-17 | 2020-07-17 | 武汉大学 | 生物标志物在卵巢癌评估中的应用方法及系统 |
| CN114544848B (zh) * | 2020-11-25 | 2023-04-28 | 中国科学院大连化学物理研究所 | 一种用于诊断卵巢上皮癌的血清脂质标志物组合物及试剂盒和其与应用 |
| EP4246146A1 (en) * | 2022-03-14 | 2023-09-20 | Fundació Institut Mar d'Investigacions Mèdiques (IMIM) | Method for diagnosing cancer |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5994141A (en) * | 1996-05-30 | 1999-11-30 | The Cleveland Clinic Foundation | Method of detecting gynecological carcinomas |
| WO2009052186A1 (en) * | 2007-10-15 | 2009-04-23 | Georgia Tech Research Corporation | Metabolomics-based identification of disease-causing agents |
| WO2009096903A1 (en) * | 2008-01-28 | 2009-08-06 | National University Of Singapore | Lipid tumour profile |
| WO2012168561A1 (en) * | 2011-06-10 | 2012-12-13 | Teknologian Tutkimuskeskus Vtt | Method of diagnosing on increased risk of alzheimer's disease |
| WO2013016700A1 (en) * | 2011-07-27 | 2013-01-31 | The Research Foundation Of State University Of New York | Methods for generating predictive models for epithelial ovarian cancer and methods for identifying eoc |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050054942A1 (en) * | 2002-01-22 | 2005-03-10 | Melker Richard J. | System and method for therapeutic drug monitoring |
| US20030180953A1 (en) * | 2000-12-29 | 2003-09-25 | Elitra Pharmaceuticals, Inc. | Gene disruption methodologies for drug target discovery |
| WO2003015436A1 (de) * | 2001-08-10 | 2003-02-20 | Siemens Aktiengesellschaft | Verfahren zum schnellen und lokalen fehlerbeheben beim ausfall einzelner physikalischer verbindungen in gebündelten kommunikationsverbindungen und kommunikationssystem-vorrichtung zum durchführen des verfahrens |
| US20040180387A1 (en) * | 2003-03-13 | 2004-09-16 | Fujirebio Diagnostics, Inc. | Detection of urinary mesothelin-/megakaryocyte potentiating factor-related peptides for assessment of ovarian cancer |
| US20050170441A1 (en) | 2003-09-12 | 2005-08-04 | Health Research, Inc. | Early detection of cancer of specific type using 1HNMR metabonomics |
| US8039668B2 (en) * | 2008-10-17 | 2011-10-18 | Burnham Institute For Medical Research | Naphthalene-based inhibitors of anti-apoptotic proteins |
| EP2279417B1 (en) | 2008-05-28 | 2016-07-20 | Georgia Tech Research Corporation | Metabolic biomarkers for ovarian cancer and methods of use thereof |
| JP4744618B2 (ja) * | 2009-04-13 | 2011-08-10 | シャープ株式会社 | ガス成分検出装置 |
| EP2513653A1 (en) * | 2009-10-09 | 2012-10-24 | Carolyn Slupsky | Methods for diagnosis, treatment and monitoring of patient health using metabolomics |
| US20110114511A1 (en) * | 2009-11-17 | 2011-05-19 | Sjong Angele | Apparatus for detecting volatile organic compounds and related methods |
| GB201016139D0 (en) | 2010-09-24 | 2010-11-10 | Univ Leuven Kath | Cancer phosholipidome |
-
2015
- 2015-10-02 WO PCT/FI2015/050654 patent/WO2016051020A1/en active Application Filing
- 2015-10-02 JP JP2017516994A patent/JP6892820B2/ja active Active
- 2015-10-02 BR BR112017006593A patent/BR112017006593A2/pt not_active Application Discontinuation
- 2015-10-02 KR KR1020177011691A patent/KR20170061704A/ko unknown
- 2015-10-02 US US15/513,755 patent/US10534001B2/en active Active
- 2015-10-02 CN CN201580052938.0A patent/CN106716127B/zh active Active
- 2015-10-02 CA CA2959832A patent/CA2959832A1/en not_active Abandoned
- 2015-10-02 SG SG11201701875YA patent/SG11201701875YA/en unknown
- 2015-10-02 EP EP15846140.0A patent/EP3201623B1/en active Active
- 2015-10-02 AU AU2015326756A patent/AU2015326756A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5994141A (en) * | 1996-05-30 | 1999-11-30 | The Cleveland Clinic Foundation | Method of detecting gynecological carcinomas |
| WO2009052186A1 (en) * | 2007-10-15 | 2009-04-23 | Georgia Tech Research Corporation | Metabolomics-based identification of disease-causing agents |
| WO2009096903A1 (en) * | 2008-01-28 | 2009-08-06 | National University Of Singapore | Lipid tumour profile |
| WO2012168561A1 (en) * | 2011-06-10 | 2012-12-13 | Teknologian Tutkimuskeskus Vtt | Method of diagnosing on increased risk of alzheimer's disease |
| WO2013016700A1 (en) * | 2011-07-27 | 2013-01-31 | The Research Foundation Of State University Of New York | Methods for generating predictive models for epithelial ovarian cancer and methods for identifying eoc |
Non-Patent Citations (2)
| Title |
|---|
| Cancer biomarkers and mass spectrometry-based;Karol Jelonek et al.;《Clinicl lipidology》;20130201;第145页第1列第24-30行 * |
| Dtection of epithelial ovarian cancer using 1H-NMR-based metabonomics;Kunle Odunsi et al;《international journal of cancer,》;20040101;正文第5页第3段,附图1 * |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20170061704A (ko) | 2017-06-05 |
| EP3201623B1 (en) | 2020-07-22 |
| US10534001B2 (en) | 2020-01-14 |
| WO2016051020A1 (en) | 2016-04-07 |
| SG11201701875YA (en) | 2017-04-27 |
| US20170285036A1 (en) | 2017-10-05 |
| EP3201623A1 (en) | 2017-08-09 |
| CA2959832A1 (en) | 2016-04-07 |
| CN106716127A (zh) | 2017-05-24 |
| JP2017535756A (ja) | 2017-11-30 |
| JP6892820B2 (ja) | 2021-06-23 |
| AU2015326756A1 (en) | 2017-05-11 |
| BR112017006593A2 (pt) | 2017-12-19 |
| EP3201623A4 (en) | 2018-07-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN106716127B (zh) | 用于检测卵巢癌的方法 | |
| US10006925B2 (en) | Methods and systems for metabolite and/or lipid-based detection of colorectal cancer and/or adenomatous polyps | |
| EP3546940B1 (en) | Biomarkers related to kidney function and methods using the same | |
| JP6021187B2 (ja) | 自閉症の代謝バイオマーカー | |
| US11598779B2 (en) | Detection of cancer biomarkers using nanoparticles | |
| JP2018066765A (ja) | 対象において膵臓がんを診断する手段及び方法 | |
| Chan et al. | Metabonomic profiling of bladder cancer | |
| JP7288283B2 (ja) | 小児がん検査用尿中代謝物マーカー | |
| CA2775033C (en) | Method for the diagnosis of non-alcoholic steatohepatitis based on a metabolomic profile | |
| WO2017213246A1 (ja) | 尿中代謝物による疾病診断法 | |
| US20180275144A1 (en) | Diagnostic tools for alzheimer's disease | |
| Liang et al. | Serum metabolomics uncovering specific metabolite signatures of intra-and extrahepatic cholangiocarcinoma | |
| Nizioł et al. | Nuclear magnetic resonance and surface-assisted laser desorption/ionization mass spectrometry-based metabolome profiling of urine samples from kidney cancer patients | |
| Li et al. | Serum untargeted metabolomics reveal metabolic alteration of non‐small cell lung cancer and refine disease detection | |
| Ossoliński et al. | Targeted and untargeted urinary metabolic profiling of bladder cancer | |
| Krishnan et al. | Circulating metabolite biomarkers: A game changer in the human prostate cancer diagnosis | |
| Chen et al. | Targeting amine-and phenol-containing metabolites in urine by dansylation isotope labeling and liquid chromatography mass spectrometry for evaluation of bladder cancer biomarkers | |
| JP7226732B2 (ja) | 尿中腫瘍マーカーによるがん検出方法、キット及び装置 | |
| JP2013246080A (ja) | 大腸がん検査方法 | |
| CN110749732B (zh) | 诊断多发性骨髓瘤的血液代谢物标志物及应用 | |
| JP2010266386A (ja) | 患者由来の代謝物を使用したがんの検査方法 | |
| Jirásko et al. | Pola nski | |
| Recber et al. | Optimization and normalization strategies for long term untargeted HILIC-LC-qTOF-MS based metabolomics analysis: Early diagnosis of breast cancer | |
| WO2023233945A1 (ja) | 胆道がん検査方法 | |
| US20130090550A1 (en) | Methods of identifying patients with ovarian epithelial neoplasms based on high-resolution mass spectrometry |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |