CN1036703C - 吸收残余气体的方法 - Google Patents
吸收残余气体的方法 Download PDFInfo
- Publication number
- CN1036703C CN1036703C CN92109723.9A CN92109723A CN1036703C CN 1036703 C CN1036703 C CN 1036703C CN 92109723 A CN92109723 A CN 92109723A CN 1036703 C CN1036703 C CN 1036703C
- Authority
- CN
- China
- Prior art keywords
- alloy
- gas
- barium
- getter
- small
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 229910045601 alloy Inorganic materials 0.000 title claims abstract description 67
- 239000000956 alloy Substances 0.000 title claims abstract description 67
- 229910052788 barium Inorganic materials 0.000 title claims abstract description 37
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 title claims abstract description 37
- 238000000034 method Methods 0.000 title claims abstract description 36
- 239000007789 gas Substances 0.000 title description 52
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 title description 51
- 229910001873 dinitrogen Inorganic materials 0.000 title 1
- 238000001179 sorption measurement Methods 0.000 title 1
- 229910052751 metal Inorganic materials 0.000 claims abstract description 11
- 239000002245 particle Substances 0.000 claims abstract description 10
- 239000002184 metal Substances 0.000 claims abstract description 9
- 230000000737 periodic effect Effects 0.000 claims abstract description 9
- 239000011575 calcium Substances 0.000 claims description 13
- 229910052749 magnesium Inorganic materials 0.000 claims description 10
- 239000011777 magnesium Substances 0.000 claims description 10
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 claims description 8
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 claims description 7
- 229910052791 calcium Inorganic materials 0.000 claims description 7
- 229910000838 Al alloy Inorganic materials 0.000 claims description 6
- 239000004411 aluminium Substances 0.000 claims description 4
- 229910052782 aluminium Inorganic materials 0.000 claims description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 claims description 4
- 229910052712 strontium Inorganic materials 0.000 claims description 3
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 claims description 3
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 claims description 2
- 229910052796 boron Inorganic materials 0.000 claims description 2
- 238000009413 insulation Methods 0.000 claims description 2
- 229910052760 oxygen Inorganic materials 0.000 claims description 2
- 238000005275 alloying Methods 0.000 claims 2
- 239000008188 pellet Substances 0.000 claims 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 26
- 229910052757 nitrogen Inorganic materials 0.000 description 25
- 238000010521 absorption reaction Methods 0.000 description 15
- 238000012360 testing method Methods 0.000 description 14
- 229910052786 argon Inorganic materials 0.000 description 13
- 238000013461 design Methods 0.000 description 11
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 11
- 238000010438 heat treatment Methods 0.000 description 10
- 239000000463 material Substances 0.000 description 10
- 238000005247 gettering Methods 0.000 description 9
- 230000006698 induction Effects 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 235000001465 calcium Nutrition 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 239000011521 glass Substances 0.000 description 7
- 229910052742 iron Inorganic materials 0.000 description 7
- 230000003434 inspiratory effect Effects 0.000 description 6
- 229920003023 plastic Polymers 0.000 description 6
- 239000004033 plastic Substances 0.000 description 6
- 238000009795 derivation Methods 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 229910000733 Li alloy Inorganic materials 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 235000010210 aluminium Nutrition 0.000 description 4
- 239000001989 lithium alloy Substances 0.000 description 4
- 239000004570 mortar (masonry) Substances 0.000 description 4
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 3
- COHCXWLRUISKOO-UHFFFAOYSA-N [AlH3].[Ba] Chemical compound [AlH3].[Ba] COHCXWLRUISKOO-UHFFFAOYSA-N 0.000 description 3
- 239000002250 absorbent Substances 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- 238000002161 passivation Methods 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 238000005086 pumping Methods 0.000 description 3
- 238000001275 scanning Auger electron spectroscopy Methods 0.000 description 3
- 229910015999 BaAl Inorganic materials 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 2
- QFAXEJRYQFPRJW-UHFFFAOYSA-N [Li].[Ca].[Ba] Chemical compound [Li].[Ca].[Ba] QFAXEJRYQFPRJW-UHFFFAOYSA-N 0.000 description 2
- 230000002745 absorbent Effects 0.000 description 2
- YSZKOFNTXPLTCU-UHFFFAOYSA-N barium lithium Chemical compound [Li].[Ba] YSZKOFNTXPLTCU-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 239000000155 melt Substances 0.000 description 2
- 238000004088 simulation Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 229910000600 Ba alloy Inorganic materials 0.000 description 1
- 229910016015 BaAl4 Inorganic materials 0.000 description 1
- 229910000952 Be alloy Inorganic materials 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 229910003023 Mg-Al Inorganic materials 0.000 description 1
- 229910003310 Ni-Al Inorganic materials 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 229910007727 Zr V Inorganic materials 0.000 description 1
- 229910007837 Zr—V—Ni Inorganic materials 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- -1 barium-lithium-aluminium Chemical compound 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- OMFXVFTZEKFJBZ-HJTSIMOOSA-N corticosterone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@H](CC4)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OMFXVFTZEKFJBZ-HJTSIMOOSA-N 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 230000016507 interphase Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000012495 reaction gas Substances 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000002344 surface layer Substances 0.000 description 1
- 229910052716 thallium Inorganic materials 0.000 description 1
- BKVIYDNLLOSFOA-UHFFFAOYSA-N thallium Chemical compound [Tl] BKVIYDNLLOSFOA-UHFFFAOYSA-N 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J7/00—Details not provided for in the preceding groups and common to two or more basic types of discharge tubes or lamps
- H01J7/14—Means for obtaining or maintaining the desired pressure within the vessel
- H01J7/18—Means for absorbing or adsorbing gas, e.g. by gettering
- H01J7/183—Composition or manufacture of getters
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22C—ALLOYS
- C22C24/00—Alloys based on an alkali or an alkaline earth metal
Landscapes
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Mechanical Engineering (AREA)
- Metallurgy (AREA)
- Organic Chemistry (AREA)
- Gas Separation By Absorption (AREA)
- Solid-Sorbent Or Filter-Aiding Compositions (AREA)
Abstract
本发明方法用非挥发的钡吸气剂吸收容器中不需要的气体,包括下列步骤:在真空或惰性气氛下把Ba1-xAxLi4--yBy合金细碎到颗粒尺寸小于5毫米,然后把细碎的合金放在容器中,在把细碎的合金暴露在低于150℃的容器中的残余气体中时,它吸收气体。其中金属A是元素周期表中IIα族除钡外的元素,而金属B是元素周期表中IIIα族元素中的一种,而x值最好为0≤x≤0.5,而y值最好为0≤y≤3.5。
Description
本发明涉及吸收残余气体的方法,特别是涉及用非挥发的钡吸气剂吸收残余气体的方法。
钡吸气剂在现有技术中是公知的。钡以高纯度或低纯度元素的形式放在金属容器内保护它避免与空气作用。然而,当需要用时,把钡吸气剂放在一真空装置内,在局部抽真空并把容器密封后,钡会挥发。在挥发后,钡以薄膜形式沉积在真空装置上,在装置的工作寿命范围内吸收残余气体或不需要的气体。
当这些吸气剂装置放出钡,它们也放出大量不需要的气体,在贮存或在运输时必须吸收掉。这是因为吸气剂材料是易与气体反应的元素形式的钡。
为了减小钡的活性把它与一种或多种金属合金化。这些合金可以是Ba-Mg、Ba-Sr-Mg、Ba-Mg-Al等合金。其实例可参考在1939年在Leipzig由M.Littmann和E.Winter’scheVerlagshandlung出版的书“Getterstoff and Ihre Anwen-dang in the Hochvakuumtechik”其中一个最成功的合金是BaAl4,钡的重量百分比为40至60。这种合金很惰性;当用各种惰性的钡合金时,在其能吸收气体前必须挥发。只要把BaAl4合金加热就可分离及释放出钡。但是,现在广泛地应用把BaAl4合金与近似等量的镍相混合。这两种粉末状材料在加热时发生放热反应生成Ni-Al固体残余物和挥发的钡。但是在放热反应开始前,这些吸气剂材料必须加热到约800℃,然后当发生放热反应突然释放出热量时,它们达到1000℃或高于1000℃。
在日本专利特开昭42-4123公开了钡-铝合金(约50%钡)与最好约为15%(重量)的锡粉混合来制造吸气剂。在排气过程中,所述的吸气剂用高频感应加热到600℃保持1分钟。由于所述加热得到的反应结果,可以制出BaSn2,或者由于钡-铝合金中铝一锡反应而释放出钡。无论在那种情况下,在室温下是稳定的钡-铝合金和锡的混合吸气剂材料激活后在室温下吸收气体。然而在该方法中包含要加热到几百度的高温的加热过程。另外还发生不受控制的化学反应。
另一族吸气剂装置基于元素铬或钛。这种吸气剂有粉末的Zr84%-Al16%,Zr2Fe和Zr2Ni等。这些吸气剂是非挥发的吸气剂,因为它们不要求使它们的组分元素挥发便可以吸收气体。但是它们要求加热到高温以使它们可吸收气体。因为它们复盖着氧化物及氮化物的表面层,使它们钝化,变成惰性的。在真空下加热,这些钝化层扩散到基体材料中,表面变纯并活化。加热过热通常是在高温下进行的,例如900℃保温10-30秒钟。该温度可降低,但时间要求更长。例如在500℃下要保温几小时。
最近,基于Zr-V的非挥发吸气剂已经使用。如Zr-V-Fe和Zr-V-Ni已广泛地被接受为“冷温”激活的非挥发的吸气剂。“冷温激活”意味着在不高的温度下在比较短的时间内它们的吸气能力有很大部分起作用。可以认为这是由于在比较低温度下钝化的材料表面层扩散到基体材料中很容易。不管在比较低为400-500℃温度下它们能激活的原因是什么,但是在很多情况下,这一温度仍然是不希望的高的温度。所有这些吸气材料已与其它吸气或不吸气的材料混合使用,试图降低它们的激活温度。
在很多情况下,要求从不能加热到高温的容器中除去不需要的气体。譬如,容器是由有机塑料制成或含有有机塑料成分。加热时有机塑料会熔化。即使它们不熔化,也会达到开始分解或者至少会放出大量的如烃类和其它有机气体的温度。如果它们被吸气剂材料吸收,会引起吸气剂过早的失效,因为它们只有有限的吸气能量或能力,只能吸收一定量的气体。迅速地吸收大量气体,使得对以后在装置使用的寿命中它们的吸气能力大为降低。换言之,会出现太高的气体压力使该装置不能按要求进行工作。装置的工作温度低到约150℃。在该温度或更低温度下,氧和水蒸汽的渗透,特别是氮都成问题。
已经有人建议用锂有机树脂从不纯的气体流中吸收气体杂质,但是它们适宜用来纯化氮气,而不是吸收氮气,可参考US-A-4603148和US-A-4604270。
虽然已经建议把非挥发的吸气剂以预激活的形式引入到装置中,但是它已经经过加热到约600℃,经过很多制造步骤,如磨细到一定颗粒尺寸,与其它材料混合,压实或形成小球。
因此本发明的目的是提供一种能克服现有技术方法的一个或多个缺点的吸收容器中残余气体的方法。它不需要在高于150℃温度下激活吸气剂,它不必使容器加热到150℃以上,它不要求把吸气剂与其它材料混合就可使用,它可以用到由有机塑料的容器中,并且它还以用到由有机塑料制的或含有机塑料的容器中吸收氮气。
为实现本发明的目的,本发明提供了一种用非挥发的钡吸气剂吸收容器中残余气体的方法,包括下面的步骤:
1)在真空或惰性气氛下把Ba1-xAxLi4-yBy细碎成颗粒制得细碎的合金;
2)把细碎的合金放在容器中;
3)在温度低于150℃下把细碎的合金暴露在残余气体中,
其中A是元素周期表中除钡外的其它IIa族元素中的一种,
而B是元素周期表中IIIa族元素和镁中的一种金属,
x值为0≤x≤0.8,和
y值为0≤y≤3.5。
通过下面结合附图对本发明进行详细说明,对本发明的上述目的和其它优点可了解得更清楚,附图中:
图1示意地示出为实施本发明方法而使用的测量合金的吸气性能的装置的示意图;
图2是在25℃对本发明的BaLi4合金的吸收N2的试验的结果。
图3是在25℃本发明的BaLi4合金的吸收各种气体的试验结果;
图4是本发明的BaLi4合金在几个温度范围吸收氮气的试验结果;
图5是本发明的BaLi4合金在25℃下吸收氮气的试验结果;
图6是从图2至图5所示曲线导出的吸气速度与吸气量的函数关系;
图7-9是本发明的Ba0.75Ca0.25Li4合金在25℃下吸收氮气的试验结果;
图10是图7至图9所示曲线导出的吸气速度与吸收氮气量的函数关系;
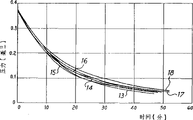
图11-15是本发明的Ba0.5Ca0.5Li4合金在25℃下吸收氮气的试验结果;
图16是图11至图15所示曲线导出的吸气速度与吸收氮气量的函数关系;
图17-18是本发明的BaLi3Al合金在25℃下吸收氮气的试验结果;
图19是图17至18所示曲线导出的吸气速度与吸收氮气量的函数关系;
图20是用得到图6,10,16和19的曲线的不同方法得到的BaLi4和一传统的非挥发吸气剂在几个温度吸收氮气的速度。
本发明的方法提供用非挥发的钡吸气剂吸收容器中的残余气体。该方法包括在真空或惰性气体下把Ba1-xAxLi4-yBy细碎成最好为小于5mm的颗粒,然后把细碎的合金放在容器中。把细碎的合金暴露在低于150℃的容器残余气体中。该合金中A是从元素周期表中IIa族元素中的一种金属(不包括钡)。而元素B是从元素周期表IIIa族元素和镁中的一种。
本发明的合金不必激活,由于它们已经可以在室温下吸收气体,并且在吸收气体前它们不必要挥发而产生激活金属(如钡)的膜。然而它们仍可以加热到低于150℃而活化。如可以加热到50°至150°至少保温10分钟,然后降到50℃以下。该合金可以表达为一般分子式为Ba1-xAxLi4-yBy,其中A是从元素周期表中IIa族元素中的一种金属(不包括钡),(元素族的编号根据美国化学协会采用的编号)。因此A可以是钙、镁、锶,但最好是钙,因为钙的活性比钡的活性只差一点。镁和锶则更差一点,这是因为它们的活化度低,x的值可以低到零,也就是不含IIa族金属元素(除钡以外)。另外,x也可以高到0.8。高于0.8,则合金会失去在室温下以足够高的吸收速度与残余气体反应的能力。
金属元素B是从元素周期表IIIa族元素及镁中选出的元素。所有在元素周期表IIIa族中元素都可用例如硼,但最好用铝,它比较容易得到,有较高的熔点并且极便宜,而镓在环境温度下是液态的。铟的熔点比较低,且比铝贵。而铊的毒性较高。另外,在所指的分子式中0≤y≤3.5。
这些化合物可以容易地处理或细碎成特殊的形式而没有任何困难。例如,它们可在真空或惰性气氛下细碎到直径小于5mm的颗粒尺寸,最好小于1mm,然后转移到含有要除去的不希望有的气体的容器中。这只要把细碎的合金放入容器中,并且在室温下把细碎的合金暴露在残余气体中。
细碎的合金可直接转移到容器中,但是最好用中间容器先把合金贮存在真空或惰性气氛下直到要使用它时。
很惊人地,它们立即开始吸收大量不需要的气体。甚至更惊人地发现,它们与不经激活或在不高于150℃下激活的现有的非挥发吸气装置相比,有更高的吸氮速度和更大的吸收量。
参照下面的实例对本发明可以更好地了解,在实例中如无特别注明,所有分量及百分比均指重量而言。设计这些实例用来指导本专业的技术人员如何实施本发明,并列出已知的实施本发明的最好模式。实例1:
本实例并不代表本发明,但是它示出了适合用来实施本发明方法的用于测量合金吸气性的一个装置。图1是以示意图形式示出了测量本发明使用的合金Ba1-xAxLi4-yBy的吸气性的装置100。真空泵系统102通过第一阀104与容积计量装置106相连。而与容积计量装置106连着一组第二阀110,110′,110″,它们用来从一组分别含有N2、人工空气及CO的试验气体罐112、112′、112″输入试验气体,还连着一测压计114。容积计量装置106还通过第三阀116连着含有进行试验的样品120的试验室118。
在操作时,阀110、110′、110″和116是闭合的,而阀104是打开的,真空泵系统102把系统抽真空到10-6毫巴。对所有试验容积计量装置106的容积都为0.71升。含在约为0.1-0.3升容积(取决于试样)的玻璃球管试验室118中的细末合金试样120,在氩气气氛下通过阀116(关闭的)加到装置100中。阀116打开,再把系统抽到10-6毫巴,而试样在约100℃下保持20分钟,这是模拟吸气剂进行的处理程序。阀104和116再闭合,试验气体通过打开的阀110(110′,110″)从气体罐112(112′、112″)通入容积计量装置106,通一短的时间。压力由压力计114监控,掌握在打开阀116把一定量的试验气体引到试样120后,使压力为0.4-1.0毫巴。实例2
本实例设计来示出如何来制造在本发明方法中用的合金。
在一铁坩埚中放入从Degussa公司得到的155.88克商业纯的钡(纯度大于98%)和11.3克的锂。该坩埚放在感应炉中,并在400毫巴压力的氩气气氛下用中频感应加热直到混合物完全熔解并均匀化形成一熔体。然后仍在氩的保护气氛下把熔体浇入冷的铜模中并冷到室温。
该合金相应于金属互化物BaLi4。实例3
本实例设计来示出在本发明方法中合金的使用。
按上述实例2制备的钡-锂合金放在处于略大于1大气压的氩的保护气氛下的一个手套箱中。该合金用研钵和研杵磨碎到颗粒尺寸小于1毫米,并取2.7克试样密封在容积为0.17升的玻璃容器中。在玻璃容器中的试样通过试验室118连到实例1的试验装置上。接着进行实例1的步骤,把第一份气体(在该情况下为氮气)通过阀110从气体罐112引到试样。用压力计114测出容器中的压力与时间的关系。该曲线列于图2中曲线1。吸气是如此迅速以至于压降几乎是瞬时发生。再引入第二份氮气,压力计114测得的在容器中的压力列到图2中的曲线2。
再换用人工空气,也就是80%体积的N2和20%体积的O2从气体罐112′通过阀110′通入,在容器中的压力列在图3的曲线3。再重复,得到曲线4。再换用CO气体,从气体罐112″通过阀110″通入,在容器中的气体吸收如此迅速以至于压力降几乎瞬时完成这时容器中压力如曲线5所示。再通入人工空气,得到曲线6。
然后将样品冷却到0℃,在引入N2气试样时记录下曲线7。
然后用酒精+冰水将样品冷却到-8℃至-6℃,引入氮,记录下曲线8。
在25℃再引入一份氮气试样,并记录下曲线9。
另外3份氮气引入,记录下曲线10-12。
在这些试验中样品吸收的气体的总剂量为:N2=2818毫巴·厘米3;O2=421毫巴·厘米3;CO=216毫巴·厘米3。
图6示出图2-5的曲线导出的用微分表示的吸气速度与吸收的气体量的函数关系。实例4
本实例设计来示出如何制造在本发明方法中使用的另一种用钙代替部分钡的合金。
在铁坩埚中放入114.08克钡(由SAES吸气剂公司制造的HP型)和30.75克锂和1.10克颗粒状钙(由Carlo Erba公司供应的,纯度大于99.5%)。
坩埚放入感应炉中,在400毫巴的氩气气氛下用中频感应加热到混合物完全熔化和均匀化而形成熔体。然后仍在氩气的保护气氛下把熔体浇入冷铁模中和冷却到室温。在熔化后合金的重量为138克。
合金相应于成分为Ba0.75Ca0.25Li4。实例5
本实例设计用来示出按本发明实例4制造的合金的用法。
按实例4制备的钡-钙-锂合金放入压力略大于1大气压的氩气保护气氛的手套箱中。用研钵和研杵把合金磨到颗粒尺寸小于1毫米,再把2.0克的试样密封达容积为0.32升的玻璃容器中。如实例3一样在25℃下测量对N2的吸收性能,其结果示于图7-9中的曲线1-14。图10示出由图7-9的曲线导出的用微分表示的吸氮速度与吸氮量的函数关系。实例6
本发明设计来示出如何制造在本发明方法中用的另一咱用钙代替更多的钡的合金。
在铁坩埚中放入25.3克钡(SAES吸气剂公司制造的HP型)和从Carlo Erba公司购得的颗粒状钙(纯度大于99.5%)和10.23克锂,坩埚放入感应炉中在400毫巴的氩气气氛下用中频感应加热到混合物全部熔化及均匀化形成熔体,然后仍在氩气保护气氛下把熔体浇入冷铁模中并冷却到室温。在熔化后合金的重量为39.6克。
合金相应于成分为Ba0.5Ca0.5Li4。实例7
本实例设计用来示出使用本发明方法如实例6制造的合金。
把按上面实例7制备的钡-钙-锂合金放在压力略大于1大气压的氩气保护气氛的手套箱中。用研钵和研杵把合金磨到颗粒尺寸小于1毫米,把2.47克试样密封在容积为0.15升的玻璃容器中。如实例3那样测定在25℃下对氮气的吸收性能,其结果列于图11-15的曲线1-28中。图16示出由图11-15中曲线导出的吸气速度与吸气量的函数关系。实例8
本实例设计来示出如何制造在本发明方法中使用的另一种合金。
在铁坩埚中放入59.14克的钡(SAES吸气剂公司制造的HP型)和8.97克锂及11.61克SAVA铝珠(纯度大于98.5%)。
坩埚放在感应炉中,在400毫巴的氩气气氛下用中频感应加热到混合物完全熔化和均匀化得到熔体。然后仍在氩气保护气氛下把熔体浇入冷铁模中和冷却到室温。熔化后的合金重量为78.3克。
合金相应于成分为BaLi3AL。实例9
本实例设计来示出使用按本发明方法如实例8制造的合金。
按照上面实例8制备的钡-锂-铝合金放在压力略大于1大气压的氩气保护气氛的手套箱中。用研钵和研杵把合金磨到颗粒尺寸小于1毫米,把2.4克的试棒密封在容积为0.32升的玻璃容器中。如实例3一样测定25℃下对N2为吸收性能,其结果列于图17-18的曲线1-7。图19示出由图17-18的曲线导出的用微分表示的吸气速度与吸气量的函数关系。实例10
本实例设计来示出现有技术合金的吸收N2的性能。重量为100毫克的低温激活的非挥发的70%Zr-24.6%V-5.4%Fe(公称重量成分),在真空下(最好低于10-3毫巴)在450℃下保持10分钟进行激活,然后在25℃下,在压力为约10-5毫巴的条件下,在用来测定吸气速率、吸气能力、和在分子流区域中非挥发吸气剂的气体含量的,ASTM F798-82标准方法中所述的装置中吸收N2。对当量的2克吸气剂,测得吸气速率(或称吸收速度)与吸气量的关系作图得到图20中的曲线A。
再在吸气温度为350℃重复试验,对当量的2克吸气剂的吸收N2曲线作出图20中的曲线B。实例11
本实例设计来示出按照本发明的合金的吸氮气性能。如上述实例2制备的钡-锂合金,把2克颗粒尺寸小于1毫米的上述合金放在实例10所用的同样的ASTM装置中。在100℃下保持15-20分钟(该条件模拟吸气剂可能处理的方法)然后冷到25℃,它的吸收氮气曲线示于图20的曲线C。在吸气剂吸收了一份气体后,停止气流。再继续得到曲线C′,接着得到曲线C″和C。实例12
除了吸气剂在130℃下保持3小时,然后在100℃下保持16小时进行激活,并且吸气剂保持在80℃进行吸氮外,其它都重复实例11。现次得到的吸气速率和吸气量的关系示于图20的曲线D。讨论:
比较图20的曲线C与A,以及曲线D与B,可以看出在本发明方法中作用的合金比传统的吸气剂合金在已吸收更大量氮气时,还有更高的吸气速率(吸气速度)。另外,在更低得多的温度下激活也得到这些性能。
另外,图6、10、16和19示出了本发明合金对大量的N2和其它吸收气体有显著的吸气能力。
虽然参照用来对本专业技术人员进行如何最好地实施本发明的指导的一些最佳实施例对本发明进行了详细的说明,可以明白在不背离本发明所附权利要求的精神和范围情况下可作其它改型。
例如,可以明白少量锂可以用碱金属系列的其它元素和值得注意的钠和钾来替代,不会对吸气性能有本质上的恶化。另外,虽然借助于化学计算的化合物BaLi4来举例说明本发明,但在通式Ba1-xAxLi4-yBy范围内可以允许一定程度偏离化学计算值,例如为BaLi4±1Li。
Claims (11)
1.一种用非挥发的钡吸气剂吸收容器中包括N2,O2,H2O,CO和CO2的残余气体的方法,包括下面的步骤:
1)在真空或惰性气氛下把Ba1-xAxLi4-yBy合金细碎成颗粒制得细碎的合金;
2)把细碎的合金放在容器中;
3)在温度低于150℃下把细碎的合金暴露在残余气体中,
其中A是元素周期表中除钡外的其它IIa族元素中的一种,而B是元素周期表中IIIa族元素和镁中的一种金属,
x值为0≤x≤0.8,和
y值为0≤y≤3.5。
2.按照权利要求1的方法,其特征在于所述的第3)步骤中包括把细碎的合金暴露在残余气体中,在50℃至150℃保温至少10分钟,然后把温度降到低于50℃。
3.按照权利要求1的方法,其特征在于所述的合金中A是镁、钙和锶中的一种金属。
4.按照权利要求1的方法,其特征在于所述的合金中B是硼、铝和镁中的一种金属。
5.按照权利要求1的方法,其特征在于x值落在0≤x≤0.5范围内。
6.按照权利要求1的方法,其特征在于所述的非挥发的钡吸气剂是BaLi4合金。
7.按照权利要求1的方法,其特征在于所述的非挥发的钡吸气剂是Ba0.75Ca0.25Li4合金。
8.按照权利要求1的方法,其特征在于所述的非挥发的钡吸气剂是Ba0.5Ca0.5Li4合金。
9.按照权利要求1的方法,其特征在于所述的非挥发的钡吸气剂是BaLi3Al合金。
10.按照权利要求1的方法,其特征在于所述的细碎的合金颗粒尺寸小于5毫米。
11.按照权利要求10的方法,其特征在于所述的细碎的合金颗粒尺寸小于1毫米。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ITMI911038A IT1246786B (it) | 1991-04-16 | 1991-04-16 | Processo per l'assorbimento di gas residui, in particolare azoto, mediante una lega getter a base di bario non evaporato. |
| JP4119832A JP2627703B2 (ja) | 1991-04-16 | 1992-04-15 | 非蒸発型バリウムゲッタ合金による残留気体、特に窒素気体の収着方法 |
| DE69205050T DE69205050T2 (de) | 1991-04-16 | 1992-04-16 | Verfahren zur Sorption von Restgasen, insbesondere von Stickstoff mittels eines nichtverdampfbaren Bariumgetters. |
| EP92830186A EP0509971B1 (en) | 1991-04-16 | 1992-04-16 | A process for the sorption of residual gas and especially nitrogen gas by means of a non-evaporated barium getter |
| CN92109723.9A CN1036703C (zh) | 1991-04-16 | 1992-08-24 | 吸收残余气体的方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ITMI911038A IT1246786B (it) | 1991-04-16 | 1991-04-16 | Processo per l'assorbimento di gas residui, in particolare azoto, mediante una lega getter a base di bario non evaporato. |
| CN92109723.9A CN1036703C (zh) | 1991-04-16 | 1992-08-24 | 吸收残余气体的方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1083413A CN1083413A (zh) | 1994-03-09 |
| CN1036703C true CN1036703C (zh) | 1997-12-17 |
Family
ID=36790877
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN92109723.9A Expired - Fee Related CN1036703C (zh) | 1991-04-16 | 1992-08-24 | 吸收残余气体的方法 |
Country Status (5)
| Country | Link |
|---|---|
| EP (1) | EP0509971B1 (zh) |
| JP (1) | JP2627703B2 (zh) |
| CN (1) | CN1036703C (zh) |
| DE (1) | DE69205050T2 (zh) |
| IT (1) | IT1246786B (zh) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITMI20012273A1 (it) * | 2001-10-29 | 2003-04-29 | Getters Spa | Leghe e dispositivi getter per l'evaporazione del calcio |
| WO2006075680A1 (ja) * | 2005-01-14 | 2006-07-20 | Matsushita Electric Industrial Co., Ltd. | 気体吸着性物質、気体吸着合金および気体吸着材 |
| JP4889947B2 (ja) * | 2005-01-14 | 2012-03-07 | パナソニック株式会社 | 気体吸着合金 |
| JP5061289B2 (ja) * | 2005-03-25 | 2012-10-31 | パナソニック株式会社 | 気体吸着性物質および気体吸着材 |
| ITMI20051500A1 (it) * | 2005-07-29 | 2007-01-30 | Getters Spa | Sistemi getter comprendenti una fase attiva inserita in un materiale poroso distribuito in un mezzo disperdente permeabile |
| EP1791151A1 (en) * | 2005-11-29 | 2007-05-30 | Nanoshell Materials Research & Development GmbH | Metallic gas sorbents on the basis of lithium alloys |
| CN101890328A (zh) * | 2010-08-06 | 2010-11-24 | 朱雷 | 一种非蒸散型吸气剂及其应用 |
| WO2012111267A1 (ja) | 2011-02-14 | 2012-08-23 | パナソニック株式会社 | 気体吸着デバイス及びそれを備えた真空断熱材 |
| CN102258975A (zh) * | 2011-05-03 | 2011-11-30 | 济南桑乐真空管有限公司 | 一种全玻璃太阳能真空集热管高效蒸散型合金吸气剂 |
| DE102012110083B4 (de) | 2012-10-23 | 2014-12-11 | Gabriele Uslenghi | Verfahren zur Herstellung von Vakuumisolierglas |
| US10421059B2 (en) | 2014-10-24 | 2019-09-24 | Samsung Electronics Co., Ltd. | Gas-adsorbing material and vacuum insulation material including the same |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB387724A (en) * | 1931-07-04 | 1933-02-06 | Osborg Hans | Improvements in scavengers or improvers for use in the treatment of molten metals and alloys |
| US2706554A (en) * | 1952-05-12 | 1955-04-19 | King Lab Inc | Getter assembly |
| US3193508A (en) * | 1962-07-13 | 1965-07-06 | Union Carbide Corp | Silicon-containing barium-aluminum getter material |
| IT1206459B (it) * | 1984-07-05 | 1989-04-27 | Getters Spa | Dispositivo getter atto a ridurre il metano nei gas residui in un tubo a vuoto. |
| US4717500A (en) * | 1985-11-27 | 1988-01-05 | Union Carbide Corporation | Getter device for frit sealed picture tubes |
-
1991
- 1991-04-16 IT ITMI911038A patent/IT1246786B/it active IP Right Grant
-
1992
- 1992-04-15 JP JP4119832A patent/JP2627703B2/ja not_active Expired - Fee Related
- 1992-04-16 EP EP92830186A patent/EP0509971B1/en not_active Expired - Lifetime
- 1992-04-16 DE DE69205050T patent/DE69205050T2/de not_active Expired - Fee Related
- 1992-08-24 CN CN92109723.9A patent/CN1036703C/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CN1083413A (zh) | 1994-03-09 |
| JPH05131134A (ja) | 1993-05-28 |
| ITMI911038A1 (it) | 1992-10-16 |
| EP0509971A1 (en) | 1992-10-21 |
| IT1246786B (it) | 1994-11-26 |
| EP0509971B1 (en) | 1995-09-27 |
| DE69205050T2 (de) | 1996-03-07 |
| ITMI911038A0 (it) | 1991-04-16 |
| DE69205050D1 (de) | 1995-11-02 |
| JP2627703B2 (ja) | 1997-07-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1036703C (zh) | 吸收残余气体的方法 | |
| US5312606A (en) | Process for the sorption of residual gas by means of a non-evaporated barium getter alloy | |
| CN1123036C (zh) | 用于吸气材料激活的低温触发的材料组合物以及含有这种材料组合物的吸气装置 | |
| US4079523A (en) | Iron-titanium-mischmetal alloys for hydrogen storage | |
| US4300946A (en) | Granulating and activating metal to form metal hydride | |
| CN101068942A (zh) | 用于氢气吸附的非蒸散型吸气剂合金 | |
| US4907948A (en) | Non-evaporable ternary gettering alloy, particularly for the sorption of water and water vapor in nuclear reactor fuel elements | |
| US4161402A (en) | Nickel-mischmetal-calcium alloys for hydrogen storage | |
| US5312607A (en) | Process for the sorption of residual gas by means by a non-evaporated barium getter alloy | |
| KR910004831B1 (ko) | 삼불화질소 기체의 정제방법 | |
| EP1600232B1 (en) | New gas sorbents on the basis of intermetallic compounds and a method for producing the same | |
| US20060225817A1 (en) | Gas sorbents on the basis of intermetallic compounds and a method for producing the same | |
| WO2009053969A2 (en) | Safe gas sorbents with high sorption capacity on the basis of lithium alloys | |
| CN115074578B (zh) | 一种Y-Mg-Ni基储氢合金及其制备方法 | |
| RU2082249C1 (ru) | Способ сорбции остаточного газа, в частности газообразного азота посредством неиспаренного бариевого газопоглотительного сплава | |
| CN1053476C (zh) | 多元非蒸散型低温激活锆基吸气剂合金及其制法 | |
| US4201739A (en) | Manufacture of metal halide particles | |
| CN112779432A (zh) | 一种用于铝镁系合金真空熔炼的熔体净化剂及其制备方法 | |
| CN1213158C (zh) | 用碳酸锂制备锂的方法 | |
| CN100344779C (zh) | 含镧镁合金复合净化熔剂及其生产方法 | |
| US7083825B2 (en) | Composition used in producing calcium-rich getter thin film | |
| CA1098887A (en) | Nickel-mischmetal-calcium alloys for hydrogen storage | |
| CN100344778C (zh) | 含铈镁合金复合净化熔剂及其生产方法 | |
| Wolkoff et al. | The melt refining of irradiated uranium: application to EBR-II fast reactor fuel. IX. Sorption and retention of sodium and cesium vapor on stationary beds at elevated temperature | |
| JP2848947B2 (ja) | 三弗化窒素ガスの精製方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C15 | Extension of patent right duration from 15 to 20 years for appl. with date before 31.12.1992 and still valid on 11.12.2001 (patent law change 1993) | ||
| OR01 | Other related matters | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 19971217 Termination date: 20100824 |