CN103232541A - 针对活化蛋白c的单克隆抗体 - Google Patents
针对活化蛋白c的单克隆抗体 Download PDFInfo
- Publication number
- CN103232541A CN103232541A CN2013101082220A CN201310108222A CN103232541A CN 103232541 A CN103232541 A CN 103232541A CN 2013101082220 A CN2013101082220 A CN 2013101082220A CN 201310108222 A CN201310108222 A CN 201310108222A CN 103232541 A CN103232541 A CN 103232541A
- Authority
- CN
- China
- Prior art keywords
- antibody
- apc
- activated protein
- protein
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/36—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against blood coagulation factors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Hematology (AREA)
- Epidemiology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Diabetes (AREA)
- Dermatology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
Abstract
本发明提供了选择性结合并抑制活化蛋白C而不结合或抑制未活化蛋白C的单克隆抗体。其它抗体既抑制活化蛋白C又活化未活化蛋白C。本发明描述了使用这些抗体的治疗方法以及筛选和检测这些抗体的方法。
Description
本申请是中国专利申请200880121024.5的分案申请,后者是2008年10月24日提交的PCT申请PCT/US2008/081110的中国国家阶段申请。
本发明要求2007年10月26日提交的美国临时申请序列号No.60/983,092的优先权,其全部内容在此通过引用并入本文。
1.技术领域
本发明一般性地涉及抗体领域。更具体地,本发明描述了选择性针对活化蛋白C(activated protein,APC)的单克隆抗体和抗体片段的鉴定和用途。
2.背景技术
血液凝固是由多种血液成分或因子的复杂相互作用组成的过程,其最终导致纤维蛋白凝集。一般地,参与凝血“级联”的血液成分是酶前体或酶原-无酶活性的蛋白质,其通过活化剂的作用转变为活性形式。血液凝固的调节很大程度上由活化蛋白C(APC)实现的促凝血因子(pro-coagulation factor)Va和VIIIa的蛋白水解失活通过酶作用完成(Esmon,1989)。
蛋白C是APC的前体,其为有力的天然抗凝血剂。蛋白C由与凝血调节蛋白(TM)复合的凝血酶所活化。内皮细胞蛋白C受体(EPCR)增强了所述活化。TM和EPCR可被炎性介质(例如肿瘤坏死因子)所下调,由Esmon(1999)综述。也已发现在一些形式的败血症休克特别是脑膜炎球菌血症中TM和EPCR减少。因为EPCR和TM在内皮上表达,所以不可能在不除去血管的情况下直接确定它们的功能的好坏。
APC通过蛋白水解性切割和下调促凝血因子(pro-coagulant factor)起到抗凝血剂作用。APC还具有作为抗凋亡剂、抗炎症分子和细胞保护剂的重要功能。可通过除去APC来治疗关键因子丧失(例如在血友病中缺乏因子VIII)导致止血失调的出血疾病,或者在外伤过程导致暂时性止血损伤的外伤患者中。但是,这样的治疗除了除去抗凝血活性之外,还可导致除去APC有益功能的不希望的有害后果。因此,希望有一种选择性靶向APC的抗凝血活性而同时保留所述分子的其它功能完好无损的治疗剂。
发明内容
已经开发并在本文中描述了治疗出血疾病的方法,其涉及使用识别活化蛋白C但是不识别未活化蛋白C的单克隆抗体。在这点上,本发明还提供了选择性结合和/或阻断活化蛋白C中蛋白水解活性位点的单克隆抗体。在某些实施方案中,这些抗体可抑制活化蛋白C的抗凝血活性,但是可不影响未活化蛋白C的任何活性。在某些实施方案中,这些抗体还可保留活化蛋白C的细胞保护作用。因此,本发明的方法还包括利用这些单克隆抗体进行治疗,其中希望选择性抑制活化蛋白C的抗凝血活性。
因此,本发明的某些一般方面涉及单克隆抗体,其中所述抗体结合并抑制活化蛋白C,但是不结合或抑制未活化蛋白C。例如,本发明的某些实施方案涉及单克隆抗体,其中所述抗体结合并抑制活化蛋白C的抗凝血活性,但是不结合或抑制未活化蛋白C的活化。在某些实施方案中,本发明的单克隆抗体是HAPC1573。结合并抑制活化蛋白C及其抗凝血活性的本发明抗体可以在体内和/或体外起作用。
本发明涉及其他单克隆抗体,例如抑制活化或未活化蛋白C与内皮细胞蛋白C受体(EPCR)或磷脂结合并抑制未活化蛋白C活化的抗体。在某些方面,此类抗体结合小鼠未活化蛋白C的Gla结构域。可以在体外或体内情形下利用这些抗体。
本发明的抗体可以例如是鼠抗体,本发明的抗体可以例如是人源化抗体。本发明的抗体可以包含在药物组合物中,其中所述药物组合物还包含可药用载体。本发明的抗体还可用于其中抗体与细胞在体外或体内接触的方法中。
本发明还涉及在对象中抑制活化蛋白C的抗凝血活性的方法,其包括向所述对象(例如哺乳动物,如人)施用有效量的本发明抗体。在涉及施用本发明抗体的本发明方法或任何其它方法中,在某些实施方案中,活化蛋白C的细胞保护作用可以不降低,或者可保持在正常水平内。
本发明还涉及在对象中抑制活化蛋白C的酰胺裂解活性的方法,其包括向所述对象施用有效量的本发明抗体。
本发明还涉及治疗需要凝血的对象的方法,其包括向所述对象施用有效量的本发明抗体。这些对象可患有例如血友病或出血。
本文还涉及治疗患有败血症的对象的方法,其包括施用有效量的本发明抗体。这些方法还可利用施用活化蛋白C。
本发明还涉及治疗患有血友病的对象的方法,其包括向所述对象施用有效量的本发明抗体。
本发明的抗体还可用于例如在对象中调节止血或者在对象中调节血栓形成的方法,其包括施用有效量的本发明抗体。这些方法还可利用施用活化蛋白C。
本发明的某些方法涉及抑制未活化蛋白C的活化的方法,其包括向对象施用有效量的本发明单克隆抗体。这些方法中所用的抗体还可抑制活化或未活化蛋白C与内皮细胞蛋白C受体(EPCR)或磷脂的结合。
根据本发明的对象可以是例如哺乳动物,如小鼠、大鼠、兔、狗、马或人。
除非另作说明,否则本文所述的任何抗体均可以是抗体片段。例如,所述抗体可以进一步限定为Fab′、Fab、F(ab′)2、单结构域抗体、Fv’或scFv,其都是众所周知的抗体片段类型。除非另作说明,否则本发明的抗体也包括这些片段。
如下文所述,术语“抗体”用于表示具有抗原结合区域的任何抗体样分子,包括抗体片段例如Fab′、Fab、F(ab′)2、单结构域抗体(DAB)、Fv、scFv(单链Fv)等。制备和使用多种基于抗体的构建物和片段的方法在本领域中是众所周知的。制备和表征抗体的手段也是本领域中众所周知的(参见例如Antibodies:A Laboratory Manual,Cold Spring HarborLaboratory,1988;在此通过引用并入本文)。
本发明的另一个方面涉及包含替代性互补决定区(或CDR)以及构架区(或FR)的可变区。CDR是所述可变区内通常赋予抗原特异性的序列。
本发明还涵盖包含足以赋予抗原结合之可变区序列的抗体部分。抗体部分包括但不限于Fab、Fab′、F(ab′)2、Fv、SFv、scFv(单链Fv),无论是由蛋白水解切割完整抗体(例如木瓜蛋白酶或胃蛋白酶切割)产生还是由重组方法产生,其中操纵完整重链和轻链的cDNA来产生重链和轻链的片段,它们分别产生或者作为同一多肽的部分而产生。
本发明范围内的mAb还包括对应于人抗体、动物抗体和其组合的序列。本文所用的术语“嵌合抗体”包括具有与另一分子(例如来自人抗体的恒定结构域)融合的来自动物抗体(例如大鼠或小鼠抗体)之可变区的抗体。一种嵌合抗体类型“人源化抗体”具有发生了改变的可变区(通过诱变或CDR接枝)以(尽可能地)匹配人可变区的已知序列。CDR接枝包括将来自具有所需特异性之抗体的CDR接枝到人抗体的FR上,由此用人序列替换大量的非人序列。因此,人源化抗体更接近地匹配(在氨基酸序列上)已知人抗体序列。通过将小鼠单克隆抗体人源化,降低了人抗小鼠抗体(或HAMA)应答的严重程度。本发明还包括全人抗体,其尽可能多地避免了HAMA应答。下文更详细地描述人源化抗体的产生。
本文所用的“可药用载体”任何和所有的溶剂、分散介质、包衣剂、表面活性剂、抗氧化剂、防腐剂(例如抗细菌剂、抗真菌剂)、等渗剂、吸收延迟剂、盐、防腐剂、药物、药物稳定剂、凝胶、粘合剂、赋形剂、崩解剂、润滑剂、甜味剂、调味剂、染料等材料及其组合,其对于本领域技术人员来说是公知的(参见例如Remington′s Pharmaceutical Sciences,18th Ed.Mack Printing Company,1990,1289-1329页)。任何常规载体除非与活性成分不相容,否则均考虑将其用于治疗或药物组合物中。
在用于细胞时,术语“接触”在本文中用于描述本发明化合物被递送到靶细胞或者处于与靶细胞直接相邻的位置。
如说明书和/或权利要求书中所用的术语“有效”(例如“有效量”)意为足够实现所期望的、预计的或者计划的结果。
术语“基本上”及其变化形式定义为在很大程度上但是并不一定完全地,如本领域普通技术人员所理解的,在一个非限制性实施方案中,基本上表示10%、5%、1%或0.5%以内的范围。
术语“抑制”、“减少”或“防止”或这些术语的任何变化形式,在用于权利要求和/或说明书时包括任何可测量的减少或者完全抑制,以实现所需结果。例如,可以是相比于正常而言活性减少或降低5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%或更多或其中引出的任何范围。
在本申请全文中,术语“约”用于表示包括用于测定数值的装置或方法的固有误差变化,或者研究对象之间存在的变化的值。例如,“约”可以是在10%、优选5%、更优选1%、最优选0.5%内。
在权利要求和/或说明书中与术语“包括”或“包含”联用时,单数形式可能意为“一个/种”,但是也与“一个或多个”、“至少一个”以及“一个或多于一个”的含义一致。
除非明确指明可选方案是唯一的或者可选方案是互斥的,否则在权利要求中术语“或”的使用意为“和/或”,尽管本公开内容支持表示唯一可选以及“和/或”的定义。
本说明书中和权利要求书中所用的表述“包括”(以及任何形式的包括)、“具有”(以及任何形式的具有)、“包含”(以及任何形式的包含)或“含有”(以及任何形式的含有)是包含性质的或者开放式的,不排除其它未陈述的要素或方法步骤。
本发明涉及说明书中所述任何实施方案可针对本发明的任何化合物、方法或组合物而实施,反之亦然。
通过下述详细说明,本发明的其它目的、特征和优点将变得显而易见。但是,应当理解的是,尽管指出了本发明的优选实施方案,但详细说明和具体实施例仅以举例说明的方式给出,因为从本详细说明出发在本发明精神和范围内的多种变化和修改对于本领域技术人员来说是显而易见的。
附图说明
下列附图构成本说明书的一部分,其用于进一步说明本发明的某些方面。参考这些附图的一个或多个并结合本文给出的具体实施方案的详细说明可更好地理解本发明。
图1APC ELISA标准曲线。
图2HAP1573增强APC在内皮上的结合。
图3HAPC1573促进APC内化进EA细胞。
图4HAPC1573改变APC对发色底物的酰胺裂解活性。
图5在血浆凝血测定中HAPC1573阻断APC抗凝血活性。
图6HAPC1573增强APC对组蛋白的切割。
图7A-B HAPC1573对APC针对组蛋白之细胞保护作用的影响。
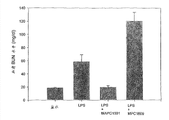
图8A-C MPC1609和MAPC1591抑制APC抗凝血活性。(图8A)在无或有125nM MPC1609或MAPC1591存在的情况下将bEnd3细胞与100nM FL-APC一起在冰上孵育15分钟,进行流式细胞术。(图8B)在无或有100nM MPC1609或MAPC1591存在的情况下将bEnd3细胞与100nM蛋白C和5nM凝血酶一起在37摄氏度下孵育15分钟,通过PCa发色底物测定APC活性。(图8C)使用200ng/ml在有或无5μg/ml MPC1609或MAPC1591存在的情况下测定单级血浆凝固时间。一式两份进行蛋白C活化和凝血测定,所有误差均在5%以内。
图9MPC1609而不是MAPC1591使小鼠恶化成在亚致死剂量的LPS下死亡。将10mg/kgLPS以及10mg/kg MPC1609或MAPC1591静脉内注射给BL6小鼠,标明了存活率。
图10A-D用LPS和MPC1609或MAPC1591攻击的小鼠的体温、血清IL-6、BUN和肌酐水平。将盐水、10mg/kg LPS或者10mg/kg LPS与10mg/kg MPC1609或MAPC1591静脉内注射给BL6小鼠(每组4只小鼠)。攻击小鼠3小时或18小时后测定(图10A)小鼠体温,(图10B)血清IL-6,(图10C-D)血清BUN和肌酐水平。
图11A-C、MAPC1591增强APC对组蛋白的切割。(图11A)将Opti-MEM中的100微克/毫升牛胸腺组蛋白H3(左图)或H4(右图)在含或不含100nM APC以及存在或不存在200nM MAPC1591的情况下在37摄氏度下孵育1小时。然后将样品进行SDS-PAGE和考马斯蓝染色。(图11B)在有或没有APC(100nM)和MAPC1591(200nM)的情况下将EA.hy926细胞与牛胸腺组蛋白(50微克/毫升)一起在37摄氏度下培养1小时。通过PI(FL3)阳性染色的流式细胞术测定细胞死亡。(图11C)将盐水、10mg/kg LPS或者10mg/kg LPS与10mg/kg MAPC1591或MPC1609静脉内注射给BL6小鼠。攻击后18小时取血浆样品,对其进行SDS-PAGE并使用山羊抗组蛋白H3抗体进行蛋白质印迹。
具体实施方式
本发明涉及发现这样的单克隆抗体,其选择性结合活化蛋白C但不结合未活化蛋白C并且特异性抑制活化蛋白C的抗凝血活性。下文更详细地描述本发明的这些及其它方面。
A.抗体结构
抗体包含具有共同结构特征的糖蛋白大家族。抗体由四条多肽构成,其形成类似于字母Y的三维结构。通常,抗体由两条不同的多肽构成,即重链和轻链。抗体分子由一个或多个Y单元构成,每个Y包含两条重链和两条轻链。
抗体分子通常由三个功能结构域组成:Fc、Fab和抗原结合位点。Fc结构域位于Y的底部。Y的臂包含Fab结构域。抗原结合位点位于Y的每个臂的末端。Y的臂支点处的区域是绞链区。
有五种不同类型的重链多肽,其命名为α、δ、ε、γ和μ。有两种不同类型的轻链多肽,其命名为κ和λ。抗体通常含有仅仅一种类型的重链以及仅仅一种类型的轻链,尽管任何轻链都可与任何重链结合。
每个重链多肽的羧基端称为恒定(Fc)区。每个重链和轻链多肽的氨基端称为可变(V)区。在链的可变区内有高变区,其被称为互补性决定区(CDR)。一个重链和一个轻链的可变区联合形成抗原结合位点。每个重链和每个轻链包含三个CDR。抗原结合位点的6个CDR确定了形成实际抗原结合部位的氨基酸残基。CDR的可变性导致了抗原识别的多样性。
B.本发明单克隆抗体的制备
本发明涉及能够与另一分子“特异性结合”的分子的生产和用途。如本文使用的,如果结合依赖于分子各自的结构,则称分子能够“特异性结合”另一个分子。抗体结合免疫原的已知能力是“特异性结合”的一个实例。这种相互作用与非特异性结合不同,所述非特异性结合涉及化合物种类,与其化学结构无关(例如蛋白质与硝酸纤维素的结合,等)。最优选地,本发明的抗体会显示“高特异性结合”,使得它们不能或基本上不能结合密切相关的异源分子。事实上,本发明的优选单克隆抗体显示结合活化蛋白C的能力,但是基本上不能结合未活化蛋白C。在另一些实施方案中,所述单克隆抗体通过结合和阻断APC的蛋白水解活性位点而仅特异性抑制APC的抗凝血活性。
因此,在一个实施方案中,这些分子包括例如通过mAb的蛋白水解切割产生的片段(例如(F(ab′)、F(ab′)2),或者例如可通过重组手段产生的单链免疫球蛋白。这些抗体衍生物是单价的。在一个实施方案中,这些片段可彼此组合,或者与其它抗体片段或受体配体组合,形成“嵌合”结合分子。重要地,此类嵌合分子可含有能够结合同一分子中不同表位的取代基,或者它们可能够结合活化蛋白C表位以及“未活化蛋白C”表位。
单克隆抗体可容易地通过众所周知的方法来制备,例如美国专利4,196,265中举例说明的那些,其在此通过引用并入本文。通常,方法涉及首先用所选的抗原(例如本发明的多肽或多核苷酸)以足以提供免疫应答的方式免疫合适的动物。啮齿类动物例如小鼠和大鼠是优选的动物。然后,将来自免疫动物的脾细胞与永生化骨髓瘤细胞融合。当所述免疫动物是小鼠时,优选的骨髓瘤细胞是小鼠NS-1骨髓瘤细胞。
将所述融合的脾/骨髓瘤细胞培养在选择性培养基中,以选择来自母细胞的融合脾/骨髓瘤细胞。将融合细胞与未融合的母细胞混合物分离开,例如,通过添加阻断组织培养基中核苷酸从头合成的物质。示例性以及优选的物质是氨基蝶呤、甲氨蝶呤和偶氮丝氨酸。氨基蝶呤和甲氨蝶呤阻断嘌呤和嘧啶的从头合成,而偶氮丝氨酸仅阻断嘌呤合成。当使用氨基蝶呤或甲氨蝶呤时,培养基中补充次有黄嘌呤和胸苷作为核苷酸来源。当使用偶氮丝氨酸时,培养基中补充有次黄嘌呤。
该培养提供了用于选择特定杂交瘤的杂交瘤群体。通常,杂交瘤的选择通过单克隆稀释在微量滴定板中培养细胞来进行,然后检测各个克隆上清与抗原多肽的反应性。然后,无限扩增所选克隆,以提供单克隆抗体。
例如,为产生单克隆抗体,将包含多肽的约1-200μg抗原腹膜内注射给小鼠。通过注射与佐剂例如完全弗氏佐剂(含有杀死的结核分枝杆菌(Mycobacterium tuberculosis)的免疫应答非特异性刺激物)组合的抗原来刺激B淋巴细胞生长。在第一次注射后的某个时间(例如至少两周),通过注射第二剂与弗氏不完全佐剂混合的抗原对小鼠进行加强。
第二次注射后数周,对小鼠进行尾部取血,通过针对放射性标记抗原的免疫沉淀测定血清效价。优选地,重复进行加强和测定效价的过程直至获得合适的效价。取出具有最高效价的小鼠脾,用注射器将脾匀浆获得脾淋巴细胞。通常,来自免疫小鼠的脾含有约5×107至2×108个淋巴细胞。
被称为骨髓瘤细胞的突变淋巴细胞获得自实验动物,其中这些细胞已经通过多种众所周知的方法诱导生长。骨髓瘤细胞缺乏核苷酸生物合成的补救途径。由于骨髓瘤细胞是肿瘤细胞,所以它们可在组织培养物中无限增殖,因此称为永生化。已经建立了多种来自小鼠和大鼠的骨髓瘤细胞培养细胞系,例如鼠NS-1骨髓瘤细胞。
在适于促进融合的条件下,将骨髓瘤细胞与来自注射抗原/多肽的小鼠或大鼠脾的产生抗体之正常细胞相组合。融合条件包括例如存在聚乙二醇。所得融合细胞是杂交瘤细胞。类似于骨髓瘤细胞,杂交瘤细胞在培养物中无限生长。
通过在选择培养基例如HAT培养基(次黄嘌呤、氨基蝶呤、胸苷)中培养,将杂交瘤细胞与非融合的骨髓瘤细胞分离开。未融合的骨髓瘤细胞缺乏从补救途径合成核苷酸所必需的酶,因为它们在氨基蝶呤、甲氨蝶呤或偶氮丝氨酸存在下被杀死。未融合淋巴细胞在组织培养物中也不会继续生长。因此,只有成功融合的细胞(杂交瘤细胞)可以在选择培养基中生长。
每个存活的杂交瘤细胞产生一种抗体。然后,对这些细胞筛选对抗原/多肽具有免疫反应性之特异性抗体的产生。有限稀释杂交瘤分离出单细胞杂交瘤。多次连续稀释杂交瘤,在使稀释物生长之后,检测上清中单克隆抗体的存在。然后大量培养产生抗体的克隆,以产生适宜量的抗体。
Liaw等人(2003)(在此通过引用并入本文)描述了某些抗人活化蛋白C和人未活化蛋白C的小鼠单克隆抗体的制备。
当所述抗体或其片段用于治疗目的时,将其“人源化”以减弱任何免疫反应可能是理想的。这些人源化抗体可以在体外或体内情形下进行研究。例如可以通过用相应非免疫原性部分替代抗体的免疫原性部分来产生人源化抗体(即嵌合抗体)。Robinson等人,PCT申请PCT/U.S.86/02269;Akira等人,EP申请184,187;Taniguchi,EP申请171,496;Morrison等人,EP申请173,494;Neuberger等人,PCT申请WO86/01533;Cabilly等人,EP申请125,023;Better等人(1988);Liu等人(1987);Liu等人(1987);Sun等人(1987);Nishimura等人(1987);Wood等人(1985);Shaw等人(1988);所有这些在此通过引用并入本文。“人源化”嵌合抗体的一般性综述由Morrison(1985)以及Oi等人(1986)提供;其在此通过引用并入本文。
或者,合适的“人源化”抗体可通过CDR或CEA替换来产生。Jones等人(1986);Verhoeyan等人(1988);Beidler等人(1988);所有这些在此通过引用并入本文。
D.药物组合物
本发明的药物组合物包含溶解或分散于可药用载体中的有效量的一种或多种抗体、治疗剂或添加物质。本发明的水性组合物包含溶解或分散于可药用载体或水介质中的有效量抗体。短语“可药用”表示在适当地施用给动物或人时不产生不利、过敏或其它不良反应的分子实体和组合物。
本文使用的“可药用载体”包括任何和所有的溶剂、分散介质、包衣剂、表面活性剂、抗氧化剂、防腐剂(例如抗细菌剂、抗真菌剂)、等渗剂、吸收延迟剂、盐、防腐剂、药物、药物稳定剂、凝胶、粘合剂、赋形剂、崩解剂、润滑剂、甜味剂、调味剂、染料等材料及其组合,其对于本领域技术人员来说是公知的(参见例如Remington′s Pharmaceutical Sciences,18th Ed.Mack Printing Company,1990,1289-1329页,其在此通过引用并入本文)。这些介质和试剂用于药物活性物质的用途是本领域中众所周知的。任何常规介质或试剂除非与所述活性成分不相容,否则均考虑用于所述治疗组合物中。还可将补充性活性成分加入所述组合物中。对于人施用而言,制剂应满足FDA生物学标准所要求的无菌、无热源、一般安全性和纯度标准。
适当时,所述生物材料应充分透析以除去不希望的小分子量分子和/或冻干用以更容易地配制到所期望载体中。然后,所述活性化合物一般配制成用于胃肠外施用,例如配制成用于通过静脉内、肌内、皮下、鼻内、病变内或者甚至腹膜内进行注射。通常,这些组合物可制备为可注射形式,液体溶液或混悬液;也可制备成适用于在注射之前添加液体以制备溶液或混悬液的固体形式;还可将所述制剂乳化。
适于注射使用的药物形式包括无菌水溶液或分散体;包含芝麻油、花生油或丙二醇水溶液的制剂;以及用于即时制备无菌注射溶液或分散体的无菌粉末。在所有情况下,所述形式必须是无菌的,并且必须是易于注射程度的流体。其在制备和储存条件下必须是稳定的,必须防止微生物(例如细菌和真菌)污染。
所述活性化合物作为游离碱或可药用盐的溶液可在适当地混有表面活性剂例如羟丙基纤维素的水中制备。也可在甘油、液体聚乙二醇及其混合物和油中制备分散体。在普通的储存和使用条件下,这些制剂含有防止微生物生长的防腐剂。
本发明的抗体可制备成游离碱、中性或盐形式的组合物。可药用盐包括酸加成盐(与蛋白质的游离氨基形成),以及与无机酸(例如盐酸或磷酸)或者有机酸(例如醋酸、草酸、酒石酸、扁桃酸)等形成的酸加成盐。与游离羧基形成的盐也可来自无机碱(例如氢氧化钠、氢氧化钾、氢氧化铵、氢氧化钙或氢氧化铁)以及有机碱(例如异丙胺、三甲胺、组氨酸、普鲁卡因)等等。
所述载体还可以是溶剂或分散介质,其含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)以及其合适的混合物,以及植物油。可以例如通过使用包衣(例如卵磷脂)、通过保持所需粒度(在分散体的情况下)以及通过使用表面活性剂来保持合适的流动性。可通过多种抗细菌剂和抗真菌剂(例如对羟基苯甲酸酯类、氯丁醇、苯酚、抗坏血酸、硫柳汞等)防止微生物作用。在许多情况下,包含等渗剂(例如糖或氯化钠)是优选的。所述可注射组合物的延长吸收可通过在所述组合物中包含延迟吸收的试剂(例如单硬脂酸铝和明胶)来实现。
必要时,可通过将所需量的活性化合物与多种上述其它成分掺入合适的溶剂中,随后过滤除菌来制备无菌注射溶液。通常,通过将多种无菌活性成分掺入无菌载体中来制备分散体,所述载体含有基本分散介质和上文列举的其它所需的成分。在用于制备无菌注射溶液的无菌粉末的情形下,优选的制备方法是真空干燥和冻干技术,它们从之前经过滤除菌的溶液产生所述活性成分加任何额外所需成分的粉末。还涉及用于直接注射的更浓缩或高浓缩溶液的制剂,其中设想使用DMSO作为溶剂,导致非常快速的穿透,将高浓度活性剂递送到小的区域。
配制之后,将溶液以与剂型(dosage formulation)相容的形式和治疗有效的量施用。所述制剂容易地以多种剂型施用,例如上文所述的注射液类型,还可使用药物释放胶囊等。
例如,对于水溶液的胃肠外施用,如果必要,所述溶液应该适当地缓冲,首先用足够的盐水或葡萄糖使得液体稀释剂等渗。这些特定的水溶液尤其适合于静脉内、肌内、皮下、鼻内和腹膜内施用。就此而论,在本公开内容的指导下,可利用的无菌水性介质对本领域技术人员来说是公知的。例如,一剂可溶于1毫升等渗NaCl溶液中,添加到1000ml皮下灌注流体或者注射到输注的预定部位(参见例如,″Remington′s PharmaceuticalSciences″第15版,1035-1038页和1570-1580页)。根据所治疗对象的情况,剂量必然会发生一些变化。在任何情况下,负责施用的人会确定对于单个对象的合适剂量。
除了配制用于胃肠外施用(例如静脉内或肌内注射)的化合物之外,其它可药用形式包括例如片剂或用于经口施用的其它固体;脂质体制剂;延时释放胶囊;以及任何其它目前使用的形式,包括霜剂。
在某些实施方案中,涉及使用脂质体和/或纳米颗粒,以配制和施用所述抗体和/或其类似物。脂质体的形成和用途通常是本领域技术人员公知的,也如下文所述。
纳米胶囊通常能以稳定且可再生的形式包封化合物。为了避免由于胞内聚合物超负荷造成的副作用,应当利用能够体内降解的聚合物来设计这些超细颗粒(约0.1微米大小)。设想将满足这些要求的可生物降解聚烷基-氰基丙烯酸酯纳米颗粒用于本发明,这些颗粒可容易地制造。
脂质体由分散于水介质中并自发形成多层同心双层囊泡(也称为多层囊泡(multilamellar vesicles,MLV))的磷脂形成。MLV一般具有25纳米至4微米的直径。对MLV超声导致形成直径在200-500埃范围内的小单层囊泡(SUV),其在核心中含有水溶液。
下列信息也可用于产生脂质体制剂。当分散于水中时,磷脂可形成除了脂质体之外的多种结构,这取决于脂质与水的摩尔比。在低比值时,脂质体是优选结构。脂质体的物理性质取决于pH、离子强度和二价阳离子的存在。脂质体可显示出对离子和极性物质的低透过性,但是在高温下发生显著改变了其透过性的相变。所述相变包括从致密堆积的有序结构(称为凝胶状态)变为疏松堆积的低有序结构(称为流体状态)。这在特征性相变温度下发生,导致对离子、糖和药物的透过性增加。
脂质体通过四种不同机制与细胞相互作用:被网状内皮系统的吞噬细胞(例如巨噬细胞和中性粒细胞)胞吞;通过非特异性弱疏水作用或静电力或者通过与细胞表面组分的特异性相互作用而吸附于细胞表面;通过将脂质体的脂质双层插入质膜而与浆细胞膜融合,同时将脂质体内含物释放进细胞质;以及将脂质体脂质转变为细胞膜或亚细胞膜(反之亦然),而没有任何与脂质体内含物的结合。尽管可以有超过一种的机制同时作用,改变脂质体制剂可改变起作用的作用机制。
所述治疗剂可包含不同类型的载体,这取决于是以固体、液体还是气雾剂形式施用,以及对于比如注射的施用途径而言是否需要无菌。本发明可以下列方式施用:静脉内、真皮内、动脉内、腹膜内、病变内、颅内、关节内、前列腺内、胸膜内、气管内、鼻内、玻璃体内、阴道内、直肠内、表面(topically)、肿瘤内、肌内、腹膜内、皮下、结膜下、囊泡内、粘膜、心包内、脐带内、眼内、经口、表面、局部、吸入(例如气雾剂吸入)、注射、输注、连续输注、局部输注直接浸没靶细胞、通过导管、通过灌洗、在霜剂中,在脂质组合物(例如脂质体)中,或者通过其它方法或任何上述的组合,如本领域普通技术人员公知的(参见例如Remington′sPharmaceutical Sciences,第18版Mack Printing Company,1990,在此通过引用并入本文)。
施用给动物患者的本发明组合物的实际剂量可根据物理和生理因素例如体重、病症严重程度、待治疗疾病的类型、之前或同时的治疗性介入、患者的特发病以及施用途径来确定。在任何情况下,由对施用负责的医生为单个对象确定组合物中活性成分的浓度和合适的剂量。
在某些实施方案中,药物组合物可包含例如至少约0.1%的活性化合物。在其它一些实施方案中,活性化合物可为单位重量的约2%至约75%,或者例如约25%至约60%,以及可由其中得出的任何范围。在另一些非限制性实例中,每次施用的剂量还可为约1微克/千克体重、约5微克/千克体重、约10微克/千克体重、约50微克/千克体重、约100微克/千克体重、约200微克/千克体重、约350微克/千克体重、约500微克/千克体重、约1毫克/千克体重、约5毫克/千克体重、约10毫克/千克体重、约50毫克/千克体重、约100毫克/千克体重、约200毫克/千克体重、约350毫克/千克体重、约500毫克/千克体重、约1000毫克/千克体重以及可由其中得出的任何范围。在从本文所列数字衍生范围的非限制性实例中,基于上文所述的数字,可施用约5毫克/千克体重至约100毫克/千克体重、约5微克/千克体重至约500毫克/千克体重等等。
在任何情况下,所述组合物可包含多种抗氧化剂,以延迟一种或多种成分的氧化。
在所述组合物是液体形式的实施方案中,载体可以是溶剂或分散介质,其包括但不限于水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)、脂质(例如甘油三酯、植物油、脂质体)及其组合。可通过下列方式维持合适的流动性,例如,使用包衣剂例如卵磷脂;通过分散在载体例如液体多元醇或脂质来维持所需粒径;使用表面活性剂例如羟丙基纤维素;或其组合。在许多情况下,优选的是包含等渗剂例如糖、氯化钠或其组合。
在另一些实施方案中,可在本发明中使用的滴眼剂、洗鼻液(nasalsolution)或喷雾剂、气雾剂或吸入剂。这些组合物一般设计成与靶组织类型相容。在非限制性实例中,洗鼻液通常是设计成以滴剂或喷雾剂施用到鼻道的水溶液。制备鼻溶液使得它们在许多方面类似于鼻分泌物,从而维持正常的纤毛作用。因此,在一些优选实施方案中,水性洗鼻液通常是等渗的或稍加缓冲,以维持约5.5至约6.5的pH。另外,如果需要,可将类似于眼科制剂所用的抗微生物防腐剂、药物或合适的药物稳定剂包含在所述制剂中。例如,多种可商购鼻制剂是公知的,包括药物例如抗生素或抗组胺剂。
在某些实施方案中,将抗体制备成用于通过经口摄入的此类途径来施用。在这些实施方案中,所述固体组合物可包括例如溶液、混悬剂、乳剂、片剂、丸剂、胶囊(例如硬壳或软壳明胶胶囊)、持续释放制剂、口含组合物、锭剂、酏剂、混悬剂、糖浆、薄片剂(wafer)或者其组合。经口组合物可直接掺入到膳食食物中。用于经口施用的优选载体包括惰性稀释剂、可吸收食用载体或其组合。在本发明的另一些方面,所述经口组合物可制备成糖浆或酏剂。糖浆或酏剂可包含例如至少一种活性剂、甜味剂、防腐剂、调味剂、染料、防腐剂或其组合。
在某些优选实施方案中,经口组合物可包含一种或多种粘合剂、赋形剂、崩解剂、润滑剂、调味剂和其组合。在某些实施方案中,组合物可包含下列的一种或多种:粘合剂例如黄蓍胶、阿拉伯胶、玉米淀粉、明胶或其组合;赋形剂例如磷酸氢钙、甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、纤维素、碳酸镁或其组合;崩解剂例如玉米淀粉、马铃薯淀粉、藻酸或其组合;润滑剂例如硬脂酸镁;甜味剂例如蔗糖、乳糖、糖精或其组合;调味剂例如薄荷、冬青油、樱桃调味品、橙调味品等等;或上述的组合。当剂量单位形式是胶囊时,其可含有除上述材料类型之外的载体,例如液体载体。多种其它材料可作为包衣存在,或者以其它方式修饰剂量单位的物理外形。例如,片剂、丸剂或胶囊可用虫胶、糖或两者包衣。
适于其它施用方式的另外制剂包括栓剂。栓剂是多种重量和形状的固体剂型,通常用于插入直肠、阴道或尿道用药。在插入后,栓剂软化、融化或溶于腔内流体中。通常,对于栓剂来说,传统载体可包括例如聚烷撑二醇、甘油三酯或其组合。在某些实施方案中,栓剂可由包含例如约0.5%至约10%、优选约1%至约2%的活性成分的混合物形成。
所述组合物在制备和储存条件下必须是稳定的,必须防止微生物(例如细菌和真菌)的污染作用。应当理解的是,内毒素污染最低限度应维持在安全水平,例如低于0.5ng/mg蛋白质。
在一些特定实施方案中,通过在组合物中使用延迟吸收的物质例如单硬脂酸铝、明胶或其组合,可带来注射组合物的延长吸收。
E.药盒
本文所述的任何组合物均可包含在药盒中。因此,所述药盒包含在合适的容器装置中的本发明抗体和/或其它物质。本发明人设想了可包含在药盒中的其它组分。本发明的治疗性药盒包含在合适的容器装置中在可药用制剂中的抗体可药用制剂。所述药盒可具有单个容器装置和/或其可具有针对各个化合物的不同容器装置。
当所述药盒的组分在一种和/或多种液体溶液中提供时,所述液体溶液是水溶液,无菌水溶液是特别优选的。所述抗体还可配制成可注射组合物,在这种情况下,所述容器装置本身可以是注射器、移液管和/或其它类似装置,从其中将所述试剂施加到身体的患病区域、注射到动物中和/或甚至施加到所述药盒的其它成分中和/或与其混合。
但是,所述药盒的组分可以干燥粉末的形式提供。当以干燥粉末形式提供试剂和/或组分时,所述粉末可以通过添加合适溶剂而重构。设想所述溶剂还可在另一个容器装置中提供。
所述容器装置一般包括西林瓶、试管、烧瓶、瓶、注射器和/或其它容器装置中的至少一个,所述抗体/抗体制剂被置于其中,优选合适地分配在其中。所述药盒还可包含第二容器装置,用于容纳无菌可药用缓冲液和/或其它稀释剂。
本发明的药盒还通常包含用于紧密固定地容纳西林瓶以进行销售的装置,例如注塑和/或吹塑的塑料容器,所述西林瓶被放置于其中。
不论容器的数目和/或类型如何,本发明的药盒还可包含工具和/或与其包装在一起,所述工具用于协助将所述最终抗体注射/施用和/或放置于动物体内。此工具可以是注射器、移液管、钳子和/或任何此类医学上批准的递送工具。
F.实施例
包含下列实施例以展示本发明的优选实施方案。本领域技术人员应当理解的是,下文实施例公开的方法代表本发明人发现在本发明的实施中工作良好的方法,因此可被认为构成其实施的优选形式。但是,本领域技术人员应当理解的是,在本公开内容的教导下,在公开的具体实施方案中可进行许多改变,并仍获得类似或相似的结果,而不脱离本发明的精神和范围。
实施例1-筛选、鉴定和使用本发明人MAb的方法
材料。如之前所述制备人蛋白C、牛凝血酶(Esmon等人,1993;在此通过引用以整体并入本文)。重组APC(Xigris)来自Eli Lilly。Spectroxyme PCa来自American Diagnostica。1-棕榈酰基-2-油酰基-磷脂酰胆碱(PC)、1-棕榈酰基-2-油酰基磷脂酰丝氨酸(PS)和1-棕榈酰基-2-油酰基-磷脂酰乙醇胺(PE)来自Avanti Polar Lipids,Inc.。人内皮细胞来源的EA.hy926细胞被维持在补充了10%胎牛血清、L-谷氨酰胺和HAT(次黄嘌呤、氨基蝶呤、胸苷)的DMEM(Dulbecco′s modified Eagle′s medium)中。用来自Molecular Probes的荧光素-EX蛋白标记试剂盒根据制造商说明制备荧光素标记的APC(FL-APC)。在这些实施例中,没有用“活化的”修饰的“蛋白C”指未活化蛋白C。
小鼠抗人蛋白C和APC单克隆抗体的产生。通过标准技术开发抗人蛋白C或APC的小鼠单克隆抗体(mAb)(Rezaie and Esmon,1992)。
筛选蛋白C或APC的特异性mAb。通过FACS筛选mAb阻断FL-APC与EA.hy926细胞结合的能力而获得了人蛋白C mAb1574和1580(HPC1575和HPC1580)。简要地,将EA.hy926细胞与50nM FL-蛋白C和100nM多种抗蛋白C的单克隆抗体在含有0.5%BSA、3mM CaCl2和0.6mM MgCl2的HBSS(Hanks′平衡盐溶液)缓冲液中一起在冰上孵育30分钟,对其进行FACS分析。通过ELISA测定筛选mAb与APC结合而不与蛋白C结合的能力而获得了人APC mAb1573(HAPC1573)。简言之,用15mM Na2CO3、35mM NaHCO3、pH9.6的缓冲液中的5微克/毫升不同的mAb在4摄氏度下包被96孔MaxiSorp板(NUNC)过夜。用含有1mM CaCl2的TTBS(含有0.05%吐温-20的TBS)(TTBS钙缓冲液)清洗所述板,用在TBS(20mM Tris-HCl,150mM NaCl,pH7.5)中0.1%明胶封闭1小时,用TTBS钙缓冲液再次清洗,与TTBS钙缓冲液中的100ng/ml蛋白C或APC一起孵育1小时。用TTBS钙缓冲液清洗之后,将所述板与2微克/毫升生物素化的HPC1580一起孵育1小时,再次用TTBS钙缓冲液清洗,用TTBS钙缓冲液中1微克/毫升链霉亲和素碱性磷酸酶缀合物一起孵育另外1小时。用TTBS钙缓冲液最后一次清洗并添加对硝基苯磷酸盐液体底物(Sigma)后,在Vmax微板读数仪上读取405nm处的终点吸光度。
针对血浆中APC的ELISA测定。所述测定从前述用于筛选针对APC的mAb的ELISA测定改变而来。简言之,用5微克/毫升HAPC1573包被所述板,用含有1X酪蛋白(Vector Lab)的TBS封闭,再次用TTBS钙缓冲液清洗。将重组APC以0-8ng/ml掺入到含有10mM苯甲脒、1mMEDAT和0.25X酪蛋白缓冲液(稀释缓冲液)或1∶4稀释的人血浆的TTBS中,将所述板中的样品孵育1小时。用TTBS钙缓冲液清洗后,将板与含10mM苯甲脒、5mM CaCl2和0.25X酪蛋白缓冲液的TTBS中1微克/毫升生物素化的HPC1575一起孵育1小时。用TTBS钙缓冲液清洗后,将所述板与含10mM苯甲脒、5mM CaCl2和0.25X酪蛋白缓冲液的TTBS中0.5微克/毫升的链霉亲和素-HRP一起再孵育1小时,用TTBS钙缓冲液再次清洗,用Ultra-TMB底物(Pierce)显色。在添加0.5M H2SO4停止HRP酶促反应后读取OD450。
mAb对内皮细胞上FL-APC结合的影响。在存在或不存在多种浓度HAPC1573或HPC1575的情况下,将EA.hy926细胞与含0.5%BSA、3mMCaCl2和0.6mM MgCl2的HBSS缓冲液中的50nM FL-APC在冰上一起孵育30分钟,对其进行FACS分析。
在血浆凝固测定中mAb对APC抗凝血活性的影响。使用ST4凝血仪器(Diagnostica Stago)在改良的因子Xa单级凝固测定中确定mAb对血浆中APC抗凝血活性的影响。在标准测定中,向人正常血库血浆添加调节量的X-CP(来自鲁塞尔蝰蛇毒的因子X-活化酶),以在含0.1%BSA的TBS中磷脂囊泡(最终10微克/毫升40%PE、20%PS和40%PC w/v)和CaCl2(6.25mM)混合物中得到30s的凝固时间。通过添加CaCl2起始凝固。在添加CaCl2之前,添加APC(最终200ng/ml)或HAPC1573(最终20微克/毫升)。
mAb对于APC对发色底物的酰胺裂解活性的影响。通过添加50mMHEPES、100mM NaCl、pH7.5缓冲液中的50微升0-2mM系列稀释的Spectrozyme PCa来测定在存在或不存在66.7nM HPC1555或HAPC1573的情况下HBSS缓冲液(含有0.1%牛血清白蛋白、3mMCaCl2、0.6mMMgCl2的HBSS)中50微升10nM APC的酰胺裂解活性。
组蛋白细胞毒性测定。在存在或不存在Opti-MEM培养基(Invitrogen)中100nM APC和200nM HAPC1573的情况下,将EA.hy926细胞与牛胸腺组蛋白H3或H4(Roche)在37摄氏度下一起孵育1小时,然后在添加10微克/毫升碘化丙啶(PI)后在室温下孵育5分钟。清洗细胞,用EDTA/PBS使其脱壁,进行针对PI阳性染色的流式细胞术。
实施例2-筛选、鉴定和使用本发明的人MAb的结果
HAPC1573增强内皮上的APC结合。为了检测HAPC1575对内皮上APC的结合是否具有任何影响,本发明人将EA.hy926细胞与FL-APC在存在或不存在HAPC1573或HPC1575的情况下一起孵育,通过流式细胞术测定细胞上FL-APC的结合。流式细胞术的频率分布图显示HAPC1573增强了内皮上的FL-APC结合,而HPC1575抑制所述细胞上FL-APC的结合(图2)。HAPC1573促进内皮上的APC内化,FL-APC可通过APC的Gla结构域与细胞上的EPCR的相互作用内化到EA.hy926细胞中,EPCR阻断性Ab(JRK1494)或Gla结构域阻断性Ab(HPC1575)可阻断此内化(图3)。HAPC1573可促进FL-APC内化进细胞,EPCR阻断性Ab可完全阻断此作用(图3)。
HAPC1573改变APC针对发色底物的酰胺裂解活性。因为HAPC1573识别ELISA板和内皮细胞上的APC,本发明人研究了HAPC1573是否可影响APC针对发色底物的酰胺裂解活性。合成肽底物通常是小分子,约几百道尔顿的分子量,针对血浆中丝氨酸蛋白酶的多数抗体对这些小底物的酶活性没什么影响。但是,HAPC1573显著改变了APC对其发色底物Spectrozyme PCa的动力学参数(图4)。在HAPC1573存在时,APC对Spectrozyme PCa的km为15nM,而在Ab不存在或者HPC1555存在时则为270nM。在HAPC1573存在时,APC对SpectrozymePCa的kcat为18,而在Ab不存在或者HPC1555存在时则为67。在HAPC1573存在时APC对小肽底物的重大改变表明,该mAb识别APC中接近活性位点的表位,Ab与抗原的相互作用显著增加了APC对小肽底物的亲和力,而降低了产物从APC催化部位离开的速率。
HAPC1573阻断血浆中APC抗凝血活性。图5显示,在因子Xa起始单级血浆凝固测定中HAPC1573几乎完全消除了APC的延时作用,表明HAPC1573与APC的相互作用阻止APC切割因子Va。
HAPC1573对APC切割细胞外组蛋白的影响。最近,本发明人发现APC可切割细胞外组蛋白,并保护内皮免受组蛋白的细胞毒性(稿件正在准备中)。因为HAPC1573改变了APC对发色底物的酰胺裂解活性并阻断血浆中APC的抗凝血活性,本发明人研究了此mAb是否可影响APC切割细胞外组蛋白H3和H4以及影响APC为内皮提供针对组蛋白H3和H4细胞毒性的细胞保护作用。
出乎意料地,HAPC1573不抑制而实际上提高APC对组蛋白H3和H4的切割(图6)。一致地,HAPC1573不抑制而是略微增强APC在内皮上抗组蛋白H3和H4的细胞保护活性(图7A-B)。
实施例3-筛选、鉴定和使用本发明的人MAb的讨论
蛋白C由与内皮上凝血调节蛋白复合的凝血酶所活化。与体内活性凝血酶的数秒短促寿命不同,人APC在其产生后在循环中具有约20分钟的半衰期(Berg等人,2003)。因此,可以测定血浆中的APC水平,从而研究在多种病理生理条件下的调控。
目前可用于测定APC的方法基于酶捕获测定,其使用捕获APC的抗体,然后用发色底物测定APC活性。因为这些测定中所用的所有抗体都不仅识别APC而且还识别其酶原(蛋白C),又由于在正常循环中蛋白C浓度是APC的约1000倍,所以使用这些方法测定APC不是临床相关的。在诊断和治疗中,用于APC测定的快速且有力的方法是令人期望的。上文的结果显示,一种mAb(即HAPC1573)识别APC而不识别蛋白C,证明开发出了用于体内测定血浆中APC水平的方便的ELISA方法。通常,用此方法测定含有1ng/ml APC的血浆样品需要不到4小时的时间,而使用酶捕获测定则需要19个小时或者甚至数周(Gruber and Griffen,1992;Liaw等人,2003)。
最近的研究显示,APC的抗凝血活性对于其细胞保护功能不是必要的,但是APC对PAR1的切割活性可能对其抗凋亡作用来说是必不可少的(Mosnier等人,2004)。但是,已经不仅在表达EPCR的内皮细胞中而且在其细胞表面上不表达EPCR的其它细胞(例如神经元和角化细胞)中显示出APC的细胞保护作用(Guo等人,2004;Berg等人,2003),表明可能存在PAR1介导的APC信号转导之外的机制。HAPC1573改变了APC对发色肽底物的切割活性,在血浆凝固测定中也阻断了APC抗凝血活性,表明此mAb识别APC活性位点附近的表位,并在抗体-抗原结合后改变其催化活性。
另一方面,HAPC1573不抑制而且实际上增强APC对细胞外组蛋白的切割,并且增强APC在内皮上针对组蛋白的细胞保护活性,表明APC切割活化因子V和VIII的抗凝血活性对其通过切割细胞外组蛋白的细胞保护活性而言不是必需的。与抗凝血活性无关的对细胞外组蛋白的切割可能是APC调节炎症和细胞保护的分子机制之一。
HAPC1573可例如用于治疗A型血友病患者。APC切割因子VIIIa和因子Va,因此负性调节血液凝固。在A型血友病患者中,因子VIII水平低,在这些患者中APC造成的因子Va失活可能是调节止血和血栓形成的主要途径。最近的临床报告证明对APC切割有抗性的因子V Laiden突变体对A型血友病患者的出血症状是有益的(van′t Zant等人,1997)。mAb例如HAPC1573阻断体内APC对因子Va的抗凝血活性可能是A型血友病治疗的一种替代途径,尤其是对于具有高水平因子VIII抑制剂而使得因子VIII替代治疗不会非常有效的患者。
HAPC1573的另一种可能的临床应用是治疗稳态被破坏、可能大出血以及推迟外科手术以恢复稳态的外伤患者。使用HAPC1573治疗可选择性恢复前凝血状态,而不消除活化蛋白C的细胞保护或抗炎活性。
HAPC1573的另一种可能的临床应用是其与APC相组合用于败血病的治疗。APC目前是唯一被FDA批准用于严重败血病的药物。其在患者中的出血副作用是由于APC的抗凝血活性造成的。HAPC1573阻断APC的抗凝血活性,而维持甚至增强APC的细胞保护作用。考虑到其出血副作用,此mAb-APC复合物可能是比单独的APC更好的治疗剂。
实施例4-筛选和使用本发明小鼠单克隆抗体的方法
材料和方法按照标准方法在本实验室产生重组小鼠蛋白C、APC、大鼠mAb MPC1609和MAPC1591。用来自Molecular Probes的荧光素-EX蛋白标记试剂盒根据制造商的说明制备荧光素标记的APC(FL-APC)。
动物研究。根据俄克拉荷马州医学研究基金的动物管理和使用委员会批准的动物方案,将6至12周龄雄性BL6小鼠用于本研究。
细胞培养。将bEnd3细胞(小鼠脑来源的内皮细胞系)在补充了10%胎牛血清、L-谷氨酰胺的DMEM(Dulbecco′s modified Eagle′s medium)中培养。将EA.hy926细胞(人内皮细胞系)在补充了10%胎牛血清、L-谷氨酰胺和HAT(次黄嘌呤、氨基蝶呤、胸苷)的DMEM中培养。
内皮上的FL-APC结合和蛋白C活化。在存在或不存在125nMMPC1609或MAPC1591的情况下,将bEnd3细胞与含0.5%BSA、3mMCaCl2和0.6mM MgCl2的HBSS缓冲液中的100nM FL-APC在冰上一起孵育15分钟,对其进行FACS分析。
mAb对内皮细胞上蛋白C活化的影响。用HBSS缓冲液(含有0.1%牛血清白蛋白、3mM CaCl2、0.6mM MgCl2)将24孔板中的bEnd3细胞清洗一次,与含0.1μM蛋白C和0.1μM MPC1609或MAPC1591的HBSS缓冲液一起预孵育5分钟。通过添加总体积0.2ml的5nM牛凝血酶起始活化反应。在37摄氏度下15分钟后,通过向反应中添加50微升牛抗凝血酶III(1.67mg/ml)停止反应。将50微升上清转移到96孔微板中,使用在100mM NaCl、50mM HEPES-NaOH、pH7.5缓冲液中的50微升0.4mMSpectrozyme PCa底物的405nm的Vmax确定蛋白C的活化速率。
APC抗凝血活性测定。使用ST4凝血仪器(Diagnostica Stago)在改良因子Xa单级凝固测定中测定mAb对血浆中APC抗凝血活性的影响。在该测定中,向血浆(50%小鼠血浆和50%人正常血库血浆)中添加调节量的X-CP(来自鲁塞尔蝰蛇毒的因子X-活化酶),以在含0.1%BSA的磷脂囊泡(最终10微克/毫升40%磷脂酰乙醇胺、20%磷脂酰丝氨酸和40%磷脂酰胆碱,w/v)和CaCl2(6.35mM,在20Mm Tris-HCl、150mM NaCl缓冲液(pH7.5)中)混合物中得到30s的凝血时间。通过添加CaCl2起始凝血。在添加CaCl2之前,添加APC(最终200ng/ml)和MPC1609(最终5微克/毫升)或MAPC1591(最终5微克/毫升)。
组蛋白细胞毒性测定。在存在或不存在Opti-MEM培养基(Invitrogen)中100nM APC和200nM MAPC1591的情况下,将EA.hy926细胞与50微克/毫升牛胸腺组蛋白(Sigma)在37摄氏度下一起孵育1小时,然后在添加10微克/毫升碘化丙啶(PI)后在室温下孵育5分钟。清洗细胞,用PBS中0.526mM EDTA使其脱壁,进行针对PI阳性染色的流式细胞术。
IL-6、BUN和肌酐测定。在Vitros250化学分析仪(Ortho-ClinicalDiagnostics)上分析小鼠血清的BUN和肌酐。通过Quantikine Colorimetric夹心法ELISA(R&D Systems)测定血清IL-6。
实施例5-筛选和使用本发明小鼠单克隆抗体的结果
MPC1609抗蛋白C和APC,并且可抑制蛋白C和APC在内皮上的结合(图8A,数据未显示)。MAPC1591抗APC,但是不抗蛋白C,并且可增强APC在内皮上的结合(图8A,数据未显示)。MPC1609存在时,内皮上蛋白C的活化显著降低(图8B)。MAPC1591还在一定程度上减少了蛋白C的活化,可能由于其增强了APC在所述细胞上的结合(图8B)。在血浆凝固测定中,MPC1609和MAPC1591都可完全抑制APC抗凝血活性(图8C)。基于这些体外研究,本发明人得出以下结论:MPC1609通过掩蔽蛋白C或APC中负责蛋白C或APC在内皮或磷脂上的结合的Gla结构域来抑制蛋白C和APC在内皮或磷脂上的结合。MAPC1591通过与APC活性位点周围表位的相互作用识别APC,但是不识别蛋白C,此相互作用很可能通过阻止APC切割因子Va来抑制APC抗凝血活性。
为了研究APC在LPS诱导的败血症休克中保护作用的分子机制,本发明人将亚致死剂量的LPS与MPC1609或MAPC1591注射到小鼠中,发现注射LPS和MPC1609的小鼠在48小时内全部死亡,而注射LPS和MAPC1591的小鼠全部存活(图9)。输注后18小时,注射LPS和MPC1609的小鼠显示严重的败血症休克症状,包括低体温,外周血中高中性粒细胞、低淋巴细胞和低血小板计数(图10A,数据未显示)。血清IL-6水平在这些小鼠中非常高(图10B),但是在这些小鼠和注射LPS加MAPC1591的小鼠之间没有观察到心脏、肺、肝、脾、胸腺和外周血中IL-6mRNA水平的显著性差异(数据未显示),表明IL-6的从头合成可能不是败血症休克小鼠中持续高IL-6水平的主要原因。注射LPS和MPC1609的小鼠中血清BUN和肌酐水平比其它小鼠的高(图10C-D),表明这些小鼠中发生的急性肾衰竭,可能是由于IL-6清除缓慢造成的。令人感兴趣地是,注射LPS和MAPC1591的小鼠中BUN和肌酐水平甚至比仅注射LPS的小鼠中的水平还低(图10C),表明在LPS攻击时MAPC1591和APC的复合物对肾的体内保护可能比APC更有效。
细胞外组蛋白可见于活化的嗜中性粒细胞和巨噬细胞以及凋亡的细胞上(Brinkmann等人,2004;Radic等人,2004),它们对哺乳动物细胞有细胞毒性(Abakushin等人,1999;Currie等人,1997;Kleine等人,1997)。APC可切割组蛋白H3和组蛋白H4,MAPC1591不抑制而是事实上增强APC对这些组蛋白的切割(图10A)。APC可减少组蛋白对内皮的细胞毒性,MAPC1591可增强此APC细胞保护活性(图11B)。在注射LPS和MPC1609后的败血病小鼠血清中检测到细胞外组蛋白,而未在注射LPS或LPS和MAPC1591的小鼠中检测到(图11C),表明蛋白C活化不足、循环中细胞外组蛋白的存在与小鼠在败血症休克中的致死性之间的体内相关性。综合这些体外数据与体内结果,本发明人可通过MAPC1591将APC的细胞保护活性与其抗凝血活性区分开来,不依赖于抗凝血活性的APC对细胞毒性组蛋白的切割提供了APC防止小鼠发生LPS诱导败血症休克的新的分子机制。
实施例6-筛选和使用本发明小鼠单克隆抗体的讨论
蛋白C通路在凝血和炎症的调节中起到重要的作用(Esmon,2006)。已经证明人APC显著降低严重败血病中的死亡率,并且已被批准用作针对严重败血病治疗的第一种药物(Bernard等人,2001)。但是,对败血症中APC保护作用的分子机制仍然知之甚少。诱变研究表明,APC的抗凝血活性显然对APC对内皮细胞的抗凋亡作用是非必需的(Mosnier等人,2004),APC信号转导的抗炎和抗凋亡作用在内皮细胞中是由蛋白酶活化的受体-1(PAR-1)介导的(Reiwald等人,2002)。但是,在LPS攻击时,PAR-1缺陷型小鼠具有与野生型对照小鼠类似的表型,表明PAR-1可能不是体内APC调节炎症和细胞保护的主要因素(Pawlinski等人,2004;Camerer2006)。考虑到APC在体内调节病理生理功能的核心作用,本发明人制备了两种抗小鼠蛋白C和小鼠APC的mAb,并在LPS诱导的小鼠败血症休克中使用这两种mAb研究知之甚少的APC保护作用机制。
在本公开内容的教导下,不需过度实验即可制备和实施本文公开和要求权利保护的所有组合物和/或方法。尽管以优选实施方案的形式对本发明的组合物和方法进行了描述,但是对于本领域技术人员而言显而易见的是,在不背离本发明构思、精神和范围的情况下,可对本文所述的组合物和/或方法以及在所述方法的步骤或步骤顺序进行改变。更具体地说,显然可用化学和生理上相关的某些物质来取代本文所述的物质,而实现相同或相似的结果。所有这些对于本领域技术人员来说显而易见的类似取代和修改认为落在如所附权利要求定义的本发明的精神、范围和构思之内。
示例性实施方案
1.单克隆抗体,其中所述抗体结合活化的蛋白C并抑制抗凝血活性,但是不结合未活化的蛋白C或者抑制其活化。
2.根据1的单克隆抗体,其中所述与活化蛋白C的结合发生在活化蛋白C的活性位点,并且不抑制活化蛋白C的细胞保护作用。
3.根据1的单克隆抗体,其进一步限定为HAPC1573。
4.根据1的单克隆抗体,其中所述对活化或未活化蛋白C的抑制是在体内。
5.根据1的单克隆抗体,其中所述对活化或未活化蛋白C的抑制是在体外。
6.根据1的单克隆抗体,其中所述抗体是鼠抗体。
7.根据1的单克隆抗体,其中所述抗体是人抗体。
8.根据1的单克隆抗体,其中所述抗体是人源化抗体。
9.根据1的单克隆抗体,其中所述抗体是抗体片段。
10.根据9的单克隆抗体,其中所述抗体片段进一步限定为Fab′、Fab、F(ab′)2、单结构域抗体、Fv或scFv。
11.单克隆抗体,其中所述抗体抑制活化或未活化蛋白C与内皮细胞蛋白C受体(EPCR)或磷脂的结合,并抑制未活化蛋白C的活化。
12.根据11的单克隆抗体,其中所述抗体与小鼠未活化蛋白C的Gla结构域结合。
13.根据11的单克隆抗体,其中所述对活化或未活化蛋白C的抑制是在体内。
14.根据11的单克隆抗体,其中所述对活化或未活化蛋白C的抑制是在体外。
15.根据11的单克隆抗体,其中所述抗体是鼠抗体。
16.根据11的抗体,其中所述抗体是人抗体。
17.根据11的抗体,其中所述抗体是人源化抗体。
18.根据11的抗体,其中所述抗体是抗体片段。
19.根据18的抗体,其中所述抗体片段进一步限定为Fab′、Fab、F(ab′)2、单结构域抗体、Fv或scFv。
20.包含1的抗体以及可药用载体的药物组合物。
21.包含11的抗体以及可药用载体的药物组合物。
22.抑制对象中活化蛋白C的抗凝血活性的方法,其包括向所述对象施用有效量的1的单克隆抗体。
23.根据22的方法,其中所述单克隆抗体不降低活化蛋白C的细胞保护作用。
24.抑制对象中活化蛋白C的酰胺裂解活性的方法,其包括向所述对象施用有效量的1的抗体。
25.治疗需要凝血的对象的方法,其包括向所述对象施用有效量的1的抗体。
26.治疗需要凝血的对象的方法,其包括向所述对象施用有效量的11的抗体。
27.治疗患败血症的对象的方法,其包括施用有效量的1的抗体。
28.根据27的方法,其还包括施用活化蛋白C。
29.治疗患败血症的对象的方法,其包括施用有效量的11的抗体。
30.根据29的方法,其还包括施用活化蛋白C。
31.治疗患血友病的对象的方法,其包括施用有效量的1的抗体。
32.治疗患血友病的对象的方法,其包括施用有效量的11的抗体。
33.调整对象中止血的方法,其包括施用有效量的1的抗体。
34.根据33的方法,其中所述对象是外伤患者。
35.调整对象中止血的方法,其包括施用有效量的11的抗体。
36.根据35的方法,其中所述对象是外伤患者。
37.调整对象中血栓形成的方法,其包括施用有效量的1的抗体。
38.调整对象中血栓形成的方法,其包括施用有效量的11的抗体。
39.抑制未活化蛋白C的活化的方法,其包括向对象施用有效量的11的单克隆抗体。
参考文献
本申请全文中提及的参考文献,包括下列参考文献,以提供作为举例的程序性或其它补充本文所述内容之细节的程度,在此通过引用特别地并入本文:
U.S.Patent4,196,265
Abakushin et al.,Biochemistry(Mosc.),64:693-698,1999.
Antibodies:A Laboratory Manual,Cold Spring Harbor Laboratory,Cold SpringHarbor Press,Cold Spring Harbor,New York,1988.
Beidler et al.,J.Immunol.,141:4053-4060,1988.
Berg et al.,Proc.Natl.Acad.Sci.USA,100:4423-4428,2003.
Bernard et al.,New England J.Medicine,344:699-709,2001.
Better et al.,Science,240:1041-1043,1988.
Brinkmann,Science,203:1532-1535,2004.
Camerer,Blood,107:3912-3921,2006.
Currie et al.,Biochim.Biophys.Acta,1355:248-258,1997.
EP Appln.125,023
EP Appln.171,496
EP Appln.173,494
EP Appln.184,187
Esmon,In:Natural anticoagulants and their pathways,Handbook of Exper.Pharm.,132:447-476,Born et al.(Eds.),Springer-Verlag,NY,1999.
Esmon,J.Biol.Chem.,264;4743-4746,1989.
Esmon,Proteolytic Enzymes in Coagulation,Fibrinolysis,and ComplementActivation,Part A,222:359-385,1993.
Esmon,Semin.Thromb.Hemost.,32Suppl1:49-60,2006.
Gruber and Griffin,Blood,79:2340-2348,1992.
Guo et al.,Neuron.,41:563-572,2004.
Jones et al.,Nature,321:552-525,1986.
Kleine et al.,Am.J.Physiol273:C1925-C1936,1997.
Liaw et al.,J.Thrombosis and Haemostasis,1:662-670,2003.
Liu et al.,J.Immunol.,139:3521-3526,1987.
Liu et al.,Proc.Natl.Acad.Sci.USA,84:3439-3443,1987.
Morrison,Science,229:1202-1207,1985.
Mosnier et al.,Blood,104:1740-1744,2004.
Nishimura et al.,Canc.Res.,47:999-1005,1987.
Oi et al.,BioTechniques,4:214,1986.
Pawlinski et al.,Blood,103:1342-1347,2004.
PCT Appln.PCT/U.S.86/02269
PCT Appln.WO86/01533
Radic et al.,J.Immunol.,172:6692-6700,2004.
Remington′s Pharmaceutical Sciences,18th Ed.,Mack Printing Company,1289-1329,1990.
Remington′s Pharmaceutical Sciences,15th Ed.,1035-1038and1570-1580,1990.
Rezaie and Esmon,J.Biol.Chem.,267:26104-26109,1992.
Riewald et al.,Science,296:1880-1882,2002.
Shaw et al.,J.Natl.Cancer Inst.,80:1553-1559,1988.
Sun et al.,Proc.Natl.Acad.Sci.USA,84:214-218,1987.
van’t Zant et al.,Blood,90(8):3067-3072,1997.
Verhoeyan et al.,Science,239:1534,1988.
Wood et al.,Nature,314:446-449,1985.
Claims (18)
1.单克隆抗体,其中所述抗体抑制活化或未活化蛋白C与内皮细胞蛋白C受体(EPCR)或磷脂的结合,并抑制未活化蛋白C的活化。
2.根据权利要求1的单克隆抗体,其中所述抗体与小鼠未活化蛋白C的Gla结构域结合。
3.根据权利要求1的单克隆抗体,其中所述对活化或未活化蛋白C的抑制是在体内。
4.根据权利要求1的单克隆抗体,其中所述对活化或未活化蛋白C的抑制是在体外。
5.根据权利要求1的单克隆抗体,其中所述抗体是鼠抗体。
6.根据权利要求1的抗体,其中所述抗体是人抗体。
7.根据权利要求1的抗体,其中所述抗体是人源化抗体。
8.根据权利要求1的抗体,其中所述抗体是抗体片段。
9.根据权利要求8的抗体,其中所述抗体片段进一步限定为Fab'、Fab、F(ab')2、单结构域抗体、Fv或scFv。
10.包含权利要求1的抗体以及可药用载体的药物组合物。
11.有效量的权利要求1的抗体在制备用于治疗需要凝血的对象的药物中的用途。
12.有效量的权利要求1的抗体在制备用于治疗患败血症的对象的药物中的用途。
13.根据权利要求12的用途,其还包括施用活化蛋白C。
14.有效量的权利要求1的抗体在制备用于治疗患血友病的对象的药物中的用途。
15.有效量的权利要求1的抗体在制备用于调整对象中止血的药物中的用途。
16.根据权利要求15的用途,其中所述对象是外伤患者。
17.有效量的权利要求1的抗体在制备用于调整对象中血栓形成的药物中的用途。
18.有效量的权利要求1的单克隆抗体在制备用于抑制未活化蛋白C的活化的药物中的用途。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US98309207P | 2007-10-26 | 2007-10-26 | |
| US60/983,092 | 2007-10-26 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2008801210245A Division CN101918453A (zh) | 2007-10-26 | 2008-10-24 | 针对活化蛋白c的单克隆抗体 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103232541A true CN103232541A (zh) | 2013-08-07 |
Family
ID=40289112
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2008801210245A Pending CN101918453A (zh) | 2007-10-26 | 2008-10-24 | 针对活化蛋白c的单克隆抗体 |
| CN201510462991.XA Pending CN105153308A (zh) | 2007-10-26 | 2008-10-24 | 针对活化蛋白c的单克隆抗体 |
| CN2013101082220A Pending CN103232541A (zh) | 2007-10-26 | 2008-10-24 | 针对活化蛋白c的单克隆抗体 |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2008801210245A Pending CN101918453A (zh) | 2007-10-26 | 2008-10-24 | 针对活化蛋白c的单克隆抗体 |
| CN201510462991.XA Pending CN105153308A (zh) | 2007-10-26 | 2008-10-24 | 针对活化蛋白c的单克隆抗体 |
Country Status (13)
| Country | Link |
|---|---|
| US (3) | US8153766B2 (zh) |
| EP (1) | EP2205638B1 (zh) |
| JP (3) | JP2011500843A (zh) |
| KR (2) | KR101856210B1 (zh) |
| CN (3) | CN101918453A (zh) |
| AU (1) | AU2008316661B2 (zh) |
| BR (1) | BRPI0818865A2 (zh) |
| CA (1) | CA2703738C (zh) |
| IL (2) | IL205284A (zh) |
| MX (1) | MX2010004615A (zh) |
| RU (2) | RU2539729C2 (zh) |
| WO (1) | WO2009055669A2 (zh) |
| ZA (1) | ZA201105704B (zh) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112014022855A2 (pt) * | 2012-03-16 | 2017-07-18 | Regeneron Pharma | animal não humano geneticamente modificado, mamífero geneticamente modificado, e, método para fabricar um animal não humano |
| US20150307625A1 (en) * | 2012-11-29 | 2015-10-29 | Bayer Healthcare Llc | MONOCLONAL ANTIBODIES AGAINST ACTIVATED PROTEIN C (aPC) |
| CN104936618A (zh) * | 2012-11-29 | 2015-09-23 | 拜尔健康护理有限责任公司 | 针对活化蛋白c的人源化单克隆抗体及其用途 |
| WO2015041310A1 (ja) | 2013-09-20 | 2015-03-26 | 中外製薬株式会社 | 抗プロテインc抗体による出血性疾患の治療 |
| GB201322091D0 (en) | 2013-12-13 | 2014-01-29 | Cambridge Entpr Ltd | Modified serpins for the treatment of bleeding disorders |
| WO2015179435A1 (en) * | 2014-05-19 | 2015-11-26 | Bayer Healthcare Llc | Optimized humanized monoclonal antibodies against activated protein c and uses thereof |
| US11077187B2 (en) | 2015-11-17 | 2021-08-03 | Oklahoma Medical Research Foundation | Epitope of optimized humanized monoclonal antibodies against activated protein C and uses thereof |
| IL271194B2 (en) | 2017-06-20 | 2024-10-01 | Teneobio Inc | Anti-BCMA antibodies containing only heavy chains |
| TW201906868A (zh) * | 2017-07-07 | 2019-02-16 | 日商第一三共股份有限公司 | 抗蛋白c抗體 |
| US11327082B2 (en) * | 2017-09-13 | 2022-05-10 | B.R.A.H.M.S Gmbh | Proadrenomedullin as a marker for abnormal platelet levels |
| WO2020051277A1 (en) * | 2018-09-06 | 2020-03-12 | Board Of Regents, The University Of Texas System | Treatment and prevention of hemophilic arthropathy with an antibody against endothelial cell protein c receptor (epcr) |
| CN109897108B (zh) * | 2019-03-11 | 2021-04-02 | 上海恒赛生物科技有限公司 | 抗人内皮蛋白c受体的羊驼单域抗体及应用 |
| CN115611986A (zh) * | 2021-07-13 | 2023-01-17 | 上海莱士血液制品股份有限公司 | 针对人活化蛋白c的单克隆抗体及其制备和应用 |
| CN118370814A (zh) * | 2023-01-20 | 2024-07-23 | 上海莱士血液制品股份有限公司 | 一种抗aPC单克隆抗体的制剂及其应用 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7247453B1 (en) * | 1988-12-30 | 2007-07-24 | Oklahoma Medical Research Foundation | Calcium binding recombinant antibody against protein C |
| US5202253A (en) * | 1988-12-30 | 1993-04-13 | Oklahoma Medical Research Foundation | Monoclonal antibody specific for protein C and antibody purification method |
| US5279956A (en) * | 1991-06-24 | 1994-01-18 | The Scripps Research Institute | Activated protein C polypeptides and anti-peptide antibodies, diagnostic methods and systems for inhibiting activated protein C |
| US5695993A (en) | 1994-08-12 | 1997-12-09 | Oklahoma Medical Research Foundation | Cloning and regulation of an endothelial cell protein C/activated protein C receptor |
| US6953568B1 (en) | 1998-08-25 | 2005-10-11 | Oklahoma Medical Research Foundation | Targeting of molecules to large vessel endothelium using EPCR |
| WO2002029015A1 (en) * | 2000-10-02 | 2002-04-11 | Oklahoma Medical Research Foundation | Assay for rapid detection of human activated protein c and highly specific monoclonal antibody therefor |
| US7423128B2 (en) | 2004-11-03 | 2008-09-09 | Amgen Fremont Inc. | Anti-properdin antibodies, and methods for making and using same |
-
2008
- 2008-10-24 KR KR1020107011548A patent/KR101856210B1/ko active IP Right Grant
- 2008-10-24 BR BRPI0818865 patent/BRPI0818865A2/pt active Search and Examination
- 2008-10-24 RU RU2010121148/10A patent/RU2539729C2/ru active
- 2008-10-24 CN CN2008801210245A patent/CN101918453A/zh active Pending
- 2008-10-24 WO PCT/US2008/081110 patent/WO2009055669A2/en active Application Filing
- 2008-10-24 CN CN201510462991.XA patent/CN105153308A/zh active Pending
- 2008-10-24 CN CN2013101082220A patent/CN103232541A/zh active Pending
- 2008-10-24 AU AU2008316661A patent/AU2008316661B2/en active Active
- 2008-10-24 US US12/257,706 patent/US8153766B2/en active Active
- 2008-10-24 EP EP08841295.2A patent/EP2205638B1/en active Active
- 2008-10-24 KR KR1020157020430A patent/KR20150092358A/ko not_active Application Discontinuation
- 2008-10-24 CA CA2703738A patent/CA2703738C/en active Active
- 2008-10-24 MX MX2010004615A patent/MX2010004615A/es active IP Right Grant
- 2008-10-24 JP JP2010531275A patent/JP2011500843A/ja not_active Withdrawn
-
2010
- 2010-04-22 IL IL205284A patent/IL205284A/en active IP Right Grant
-
2011
- 2011-08-03 ZA ZA2011/05704A patent/ZA201105704B/en unknown
- 2011-11-29 US US13/306,301 patent/US9127072B2/en active Active
-
2012
- 2012-06-24 IL IL220622A patent/IL220622A0/en unknown
- 2012-10-26 JP JP2012236531A patent/JP2013049694A/ja active Pending
- 2012-11-27 RU RU2012150953/10A patent/RU2012150953A/ru not_active Application Discontinuation
-
2014
- 2014-07-02 JP JP2014136566A patent/JP6117741B2/ja active Active
-
2015
- 2015-06-09 US US14/734,055 patent/US20150344588A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| IL205284A0 (en) | 2010-12-30 |
| CN101918453A (zh) | 2010-12-15 |
| MX2010004615A (es) | 2010-07-06 |
| US9127072B2 (en) | 2015-09-08 |
| BRPI0818865A2 (pt) | 2015-05-05 |
| JP6117741B2 (ja) | 2017-04-19 |
| AU2008316661A1 (en) | 2009-04-30 |
| US20120164150A1 (en) | 2012-06-28 |
| IL205284A (en) | 2014-06-30 |
| KR20100116166A (ko) | 2010-10-29 |
| AU2008316661B2 (en) | 2013-05-23 |
| RU2539729C2 (ru) | 2015-01-27 |
| RU2010121148A (ru) | 2011-12-10 |
| KR101856210B1 (ko) | 2018-05-09 |
| EP2205638B1 (en) | 2017-03-01 |
| CN105153308A (zh) | 2015-12-16 |
| US20090110683A1 (en) | 2009-04-30 |
| JP2011500843A (ja) | 2011-01-06 |
| JP2014237651A (ja) | 2014-12-18 |
| KR20150092358A (ko) | 2015-08-12 |
| EP2205638A2 (en) | 2010-07-14 |
| US20150344588A1 (en) | 2015-12-03 |
| WO2009055669A2 (en) | 2009-04-30 |
| IL220622A0 (en) | 2012-08-30 |
| CA2703738A1 (en) | 2009-04-30 |
| RU2012150953A (ru) | 2014-06-10 |
| ZA201105704B (en) | 2014-05-28 |
| JP2013049694A (ja) | 2013-03-14 |
| US8153766B2 (en) | 2012-04-10 |
| WO2009055669A3 (en) | 2009-09-03 |
| CA2703738C (en) | 2018-02-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103232541A (zh) | 针对活化蛋白c的单克隆抗体 | |
| US20240092938A1 (en) | Compositions for inhibiting masp-2 dependent complement activation | |
| CA2635588C (en) | Metalloproteinase binding proteins | |
| TWI818919B (zh) | 用於治療和/ 或預防與造血幹細胞移植有關的移植物抗宿主病和/ 或瀰漫性肺泡出血和/ 或靜脈閉塞性病的方法 | |
| CN104936618A (zh) | 针对活化蛋白c的人源化单克隆抗体及其用途 | |
| JP2023503611A (ja) | 造血幹細胞移植に関連する特発性肺炎症候群(ips)および/または毛細血管漏出症候群(cls)および/または生着症候群(es)および/または体液過剰(fo)を治療および/または予防するための方法 | |
| AU2016203760B2 (en) | Monoclonal antibodies against activated and unactivated protein c | |
| AU2015200348B2 (en) | Monoclonal antibodies against activated and unactivated protein c | |
| AU2013202464B2 (en) | Monoclonal antibodies against activated and unactivated protein c | |
| TW201609809A (zh) | 活化蛋白c之最佳化人化單株抗體及其用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 1187631 Country of ref document: HK |
|
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20130807 |
|
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: WD Ref document number: 1187631 Country of ref document: HK |