CN100460503C - 一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变株的疫苗及应用 - Google Patents
一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变株的疫苗及应用 Download PDFInfo
- Publication number
- CN100460503C CN100460503C CNB2007100513892A CN200710051389A CN100460503C CN 100460503 C CN100460503 C CN 100460503C CN B2007100513892 A CNB2007100513892 A CN B2007100513892A CN 200710051389 A CN200710051389 A CN 200710051389A CN 100460503 C CN100460503 C CN 100460503C
- Authority
- CN
- China
- Prior art keywords
- gene deletion
- vaccine
- gene
- actinobacillus pleuropneumoniae
- dual
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000012224 gene deletion Methods 0.000 title claims abstract description 88
- 229960005486 vaccine Drugs 0.000 title claims abstract description 70
- 239000003550 marker Substances 0.000 title claims abstract description 19
- 241000122975 Actinobacillus pleuropneumoniae serovar 1 Species 0.000 title claims abstract 5
- 241000606748 Actinobacillus pleuropneumoniae Species 0.000 claims abstract description 56
- 238000002360 preparation method Methods 0.000 claims abstract description 25
- 208000015181 infectious disease Diseases 0.000 claims abstract description 8
- 206010035664 Pneumonia Diseases 0.000 claims abstract description 5
- 241000204031 Mycoplasma Species 0.000 claims abstract description 4
- 201000006509 pleuropneumonia Diseases 0.000 claims abstract description 4
- 238000004321 preservation Methods 0.000 claims abstract description 4
- 230000002458 infectious effect Effects 0.000 claims abstract 2
- 230000001580 bacterial effect Effects 0.000 claims description 48
- 241000894006 Bacteria Species 0.000 abstract description 60
- 108700012359 toxins Proteins 0.000 abstract description 30
- 108090000623 proteins and genes Proteins 0.000 abstract description 29
- 101100148257 Actinobacillus pleuropneumoniae apxIC gene Proteins 0.000 abstract description 27
- 101150015540 apxIIC gene Proteins 0.000 abstract description 23
- 230000001018 virulence Effects 0.000 abstract description 15
- 241001465754 Metazoa Species 0.000 abstract description 10
- 230000001681 protective effect Effects 0.000 abstract description 8
- 241000282887 Suidae Species 0.000 abstract description 7
- 239000012190 activator Substances 0.000 abstract description 4
- 238000010276 construction Methods 0.000 abstract description 2
- 238000010353 genetic engineering Methods 0.000 abstract description 2
- 230000002163 immunogen Effects 0.000 abstract description 2
- 230000028993 immune response Effects 0.000 abstract 1
- 210000002966 serum Anatomy 0.000 description 51
- 241000699666 Mus <mouse, genus> Species 0.000 description 34
- 238000002965 ELISA Methods 0.000 description 27
- 238000000034 method Methods 0.000 description 26
- 229940031551 inactivated vaccine Drugs 0.000 description 24
- 239000003053 toxin Substances 0.000 description 23
- 231100000765 toxin Toxicity 0.000 description 23
- 239000013612 plasmid Substances 0.000 description 22
- 241000282898 Sus scrofa Species 0.000 description 19
- 230000036039 immunity Effects 0.000 description 17
- 230000035931 haemagglutination Effects 0.000 description 16
- 239000000047 product Substances 0.000 description 14
- 238000012360 testing method Methods 0.000 description 14
- 101000657454 Actinobacillus pleuropneumoniae RTX-I toxin determinant A from serotypes 1/9 Proteins 0.000 description 13
- 208000012353 Contagious Pleuropneumonia Diseases 0.000 description 13
- 238000001514 detection method Methods 0.000 description 12
- 231100000614 poison Toxicity 0.000 description 11
- 239000002574 poison Substances 0.000 description 11
- 238000012216 screening Methods 0.000 description 10
- 238000011144 upstream manufacturing Methods 0.000 description 10
- 230000008034 disappearance Effects 0.000 description 9
- 238000002347 injection Methods 0.000 description 9
- 239000007924 injection Substances 0.000 description 9
- 229930027945 nicotinamide-adenine dinucleotide Natural products 0.000 description 9
- 108090000790 Enzymes Proteins 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 8
- 230000008859 change Effects 0.000 description 8
- 238000002474 experimental method Methods 0.000 description 8
- BAWFJGJZGIEFAR-NNYOXOHSSA-N NAD zwitterion Chemical compound NC(=O)C1=CC=C[N+]([C@H]2[C@@H]([C@H](O)[C@@H](COP([O-])(=O)OP(O)(=O)OC[C@@H]3[C@H]([C@@H](O)[C@@H](O3)N3C4=NC=NC(N)=C4N=C3)O)O2)O)=C1 BAWFJGJZGIEFAR-NNYOXOHSSA-N 0.000 description 7
- 238000012408 PCR amplification Methods 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 238000011156 evaluation Methods 0.000 description 7
- 230000006872 improvement Effects 0.000 description 7
- 238000011081 inoculation Methods 0.000 description 7
- 229950006238 nadide Drugs 0.000 description 7
- BOPGDPNILDQYTO-NNYOXOHSSA-N nicotinamide-adenine dinucleotide Chemical compound C1=CCC(C(=O)N)=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C3=NC=NC(N)=C3N=C2)O)O1 BOPGDPNILDQYTO-NNYOXOHSSA-N 0.000 description 7
- 239000000304 virulence factor Substances 0.000 description 7
- 230000007923 virulence factor Effects 0.000 description 7
- 239000002158 endotoxin Substances 0.000 description 6
- 230000002068 genetic effect Effects 0.000 description 6
- 229920006008 lipopolysaccharide Polymers 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 206010018910 Haemolysis Diseases 0.000 description 5
- 101710084578 Short neurotoxin 1 Proteins 0.000 description 5
- 101710182532 Toxin a Proteins 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 238000010241 blood sampling Methods 0.000 description 5
- 244000309466 calf Species 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 230000008588 hemolysis Effects 0.000 description 5
- 230000002949 hemolytic effect Effects 0.000 description 5
- 239000005720 sucrose Substances 0.000 description 5
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 4
- 101000654311 Androctonus australis Alpha-mammal toxin AaH2 Proteins 0.000 description 4
- 101000583076 Anemonia sulcata Delta-actitoxin-Avd1c Proteins 0.000 description 4
- 108010010803 Gelatin Proteins 0.000 description 4
- 101000761697 Hemachatus haemachatus Short neurotoxin 1 Proteins 0.000 description 4
- 101000588937 Heteractis magnifica Delta-stichotoxin-Rpa1a Proteins 0.000 description 4
- 241000699670 Mus sp. Species 0.000 description 4
- 101000800755 Naja oxiana Alpha-elapitoxin-Nno2a Proteins 0.000 description 4
- 101000640206 Tityus serrulatus Alpha-mammal toxin Ts2 Proteins 0.000 description 4
- 230000003187 abdominal effect Effects 0.000 description 4
- WIIZWVCIJKGZOK-RKDXNWHRSA-N chloramphenicol Chemical compound ClC(Cl)C(=O)N[C@H](CO)[C@H](O)C1=CC=C([N+]([O-])=O)C=C1 WIIZWVCIJKGZOK-RKDXNWHRSA-N 0.000 description 4
- 230000004087 circulation Effects 0.000 description 4
- 230000002950 deficient Effects 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 239000008273 gelatin Substances 0.000 description 4
- 229920000159 gelatin Polymers 0.000 description 4
- 235000019322 gelatine Nutrition 0.000 description 4
- 235000011852 gelatine desserts Nutrition 0.000 description 4
- 230000003053 immunization Effects 0.000 description 4
- 230000005847 immunogenicity Effects 0.000 description 4
- 230000000968 intestinal effect Effects 0.000 description 4
- 210000004072 lung Anatomy 0.000 description 4
- 235000015097 nutrients Nutrition 0.000 description 4
- 229940049547 paraxin Drugs 0.000 description 4
- 230000001717 pathogenic effect Effects 0.000 description 4
- 238000012797 qualification Methods 0.000 description 4
- 108091008146 restriction endonucleases Proteins 0.000 description 4
- 230000028327 secretion Effects 0.000 description 4
- 238000001262 western blot Methods 0.000 description 4
- 241000606750 Actinobacillus Species 0.000 description 3
- 101710116435 Outer membrane protein Proteins 0.000 description 3
- 229930006000 Sucrose Natural products 0.000 description 3
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 3
- 230000003321 amplification Effects 0.000 description 3
- 101150047086 arm gene Proteins 0.000 description 3
- 230000003013 cytotoxicity Effects 0.000 description 3
- 231100000135 cytotoxicity Toxicity 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 238000004108 freeze drying Methods 0.000 description 3
- 238000002649 immunization Methods 0.000 description 3
- 230000003902 lesion Effects 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 238000003199 nucleic acid amplification method Methods 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 230000001954 sterilising effect Effects 0.000 description 3
- 238000004659 sterilization and disinfection Methods 0.000 description 3
- 229940031626 subunit vaccine Drugs 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 210000003462 vein Anatomy 0.000 description 3
- 101100148256 Actinobacillus pleuropneumoniae apxIB gene Proteins 0.000 description 2
- 101100148258 Actinobacillus pleuropneumoniae apxID gene Proteins 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- 101150076489 B gene Proteins 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 101150111062 C gene Proteins 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 101150097493 D gene Proteins 0.000 description 2
- 208000000059 Dyspnea Diseases 0.000 description 2
- 206010013975 Dyspnoeas Diseases 0.000 description 2
- 208000032843 Hemorrhage Diseases 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 102000003960 Ligases Human genes 0.000 description 2
- 108090000364 Ligases Proteins 0.000 description 2
- 101710194807 Protective antigen Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 230000010933 acylation Effects 0.000 description 2
- 238000005917 acylation reaction Methods 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- 239000000427 antigen Substances 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 230000036528 appetite Effects 0.000 description 2
- 235000019789 appetite Nutrition 0.000 description 2
- 101150056862 apxIC gene Proteins 0.000 description 2
- 238000003149 assay kit Methods 0.000 description 2
- 230000002238 attenuated effect Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 230000015271 coagulation Effects 0.000 description 2
- 238000005345 coagulation Methods 0.000 description 2
- 238000013016 damping Methods 0.000 description 2
- 230000000994 depressogenic effect Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 244000144992 flock Species 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 238000013467 fragmentation Methods 0.000 description 2
- 238000006062 fragmentation reaction Methods 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 206010025482 malaise Diseases 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 230000001323 posttranslational effect Effects 0.000 description 2
- 230000002685 pulmonary effect Effects 0.000 description 2
- 230000000630 rising effect Effects 0.000 description 2
- 230000000405 serological effect Effects 0.000 description 2
- DAJSVUQLFFJUSX-UHFFFAOYSA-M sodium;dodecane-1-sulfonate Chemical compound [Na+].CCCCCCCCCCCCS([O-])(=O)=O DAJSVUQLFFJUSX-UHFFFAOYSA-M 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 238000002255 vaccination Methods 0.000 description 2
- 108700026220 vif Genes Proteins 0.000 description 2
- FRXSZNDVFUDTIR-UHFFFAOYSA-N 6-methoxy-1,2,3,4-tetrahydroquinoline Chemical compound N1CCCC2=CC(OC)=CC=C21 FRXSZNDVFUDTIR-UHFFFAOYSA-N 0.000 description 1
- 101100520070 Arabidopsis thaliana PII-2 gene Proteins 0.000 description 1
- 241000193830 Bacillus <bacterium> Species 0.000 description 1
- 108010067770 Endopeptidase K Proteins 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 241000726221 Gemma Species 0.000 description 1
- 108010006464 Hemolysin Proteins Proteins 0.000 description 1
- 102000008133 Iron-Binding Proteins Human genes 0.000 description 1
- 108010035210 Iron-Binding Proteins Proteins 0.000 description 1
- 101710175243 Major antigen Proteins 0.000 description 1
- 108010064696 N,O-diacetylmuramidase Proteins 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010034107 Pasteurella infections Diseases 0.000 description 1
- 241000606752 Pasteurellaceae Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 208000037581 Persistent Infection Diseases 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 208000018569 Respiratory Tract disease Diseases 0.000 description 1
- 206010041349 Somnolence Diseases 0.000 description 1
- 101710172711 Structural protein Proteins 0.000 description 1
- 102000002070 Transferrins Human genes 0.000 description 1
- 108010015865 Transferrins Proteins 0.000 description 1
- 108010046334 Urease Proteins 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000000246 agarose gel electrophoresis Methods 0.000 description 1
- BIVUUOPIAYRCAP-UHFFFAOYSA-N aminoazanium;chloride Chemical compound Cl.NN BIVUUOPIAYRCAP-UHFFFAOYSA-N 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 101150031224 app gene Proteins 0.000 description 1
- 101150051095 apxIA gene Proteins 0.000 description 1
- HFACYLZERDEVSX-UHFFFAOYSA-N benzidine Chemical compound C1=CC(N)=CC=C1C1=CC=C(N)C=C1 HFACYLZERDEVSX-UHFFFAOYSA-N 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 239000006161 blood agar Substances 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 230000009849 deactivation Effects 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 239000013613 expression plasmid Substances 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000003228 hemolysin Substances 0.000 description 1
- 108010037896 heparin-binding hemagglutinin Proteins 0.000 description 1
- 244000144980 herd Species 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 150000002505 iron Chemical class 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- PHTQWCKDNZKARW-UHFFFAOYSA-N isoamylol Chemical compound CC(C)CCO PHTQWCKDNZKARW-UHFFFAOYSA-N 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 238000002703 mutagenesis Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 230000000869 mutational effect Effects 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 238000012856 packing Methods 0.000 description 1
- 201000005115 pasteurellosis Diseases 0.000 description 1
- 230000036285 pathological change Effects 0.000 description 1
- 231100000915 pathological change Toxicity 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000008521 reorganization Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000029058 respiratory gaseous exchange Effects 0.000 description 1
- 230000036387 respiratory rate Effects 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
本发明属于动物细菌基因工程技术领域,具体涉及一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的构建、疫苗制备及应用。本发明得到一株不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株Actinobacillus pleuropneumoniaeAPP-1-mut01(保藏号为CCTCC NO;M207005)。该菌株缺失了猪胸膜肺炎放线杆菌血清1型两个主要毒力基因激活因子apxIC和apxIIC,产生没有毒力的毒素蛋白ApxIA和ApxIIA,但这两个毒素蛋白仍然具有免疫原性。本发明还公开了利用该双基因缺失菌株制备猪传染性胸膜肺炎双基因缺失疫苗及其应用。本发明制备的双基因缺失疫苗可以刺激猪产生抵抗猪胸膜肺炎放线杆菌同源和异源血清型野毒株的保护性免疫反应,有效防止猪胸膜肺炎放线杆菌的感染。
Description
技术领域
本发明属于动物细菌基因工程技术领域,具体涉及一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的构建、疫苗制备及应用
背景技术
猪传染性胸膜肺炎(porcine contagious pleuropneumonia,PCP)是由胸膜肺炎放线杆菌(Actinobacillus pleuropneumoniae,APP)引起的一种猪传染性呼吸道疾病,给世界养猪业造成了严重的经济损失。自我国发现PCP流行以来,广大兽医工作者对其病原学、流行病学、诊断及防制等方面都进行了一系列研究,取得了一定的成就。但目前该病在我国发病率仍逐年增长,有的猪场阳性率已达到70%以上,已经成为集约化猪场的主要传染病之一,严重危及到我国的养猪业。
胸膜肺炎放线杆菌,属于巴氏杆菌科(Pasteurellaceae)、放线杆菌属(Actinobacillus),是一种革兰氏阴性小球杆菌,有荚膜和菌毛,不形成芽孢,能产生毒素,最近研究发现该菌还有鞭毛。根据APP生长对烟酰胺腺嘌呤二核苷酸(Nicotinamide Adenine Dinucleotide,NAD,又称V因子)的依赖性,把APP分为生物I型和生物II型两个生物型。生物□型菌株的生长依赖NAD,而生物I型菌株的生长不依赖NAD,但需要其它特定嘌呤或嘌呤前产物以辅助生长(NielsenR,Andresen L O,Plambeck T,Nielsen J P,Krarup L T,Jorsal S E.Serological characterizationof Actinobacillus pleuropneumoniae biotype 2 strains isolated from pigs in two Danish herds.Vet Microbiol,1997,54(1):35-46)。
胸膜肺炎放线杆菌主要抗原是荚膜多糖、脂多糖、外膜蛋白、溶血素、粘附素等抗原(王春来等,2001)。根据细菌荚膜(capsule,CP)和脂多糖(lipopolysaccharide,LPS)抗原的不同,人们最初将APP生物I型分离菌株鉴定为15个血清型。各地方流行的血清型有所差异,不同血清型之间的交叉保护不强。我国主要流行血清1、2、3和7型,所有血清型均具有强弱不同的溶血活性与细胞毒性。同时,APP的是一种多毒力因子病原,其毒力因子很多。现已发现与APP的致病性有关的毒力因子包括荚膜多糖(CP)、脂多糖(LPS)、外膜蛋白(OMP)、转铁结合蛋白(TBP)、溶血外毒素(Apx)、蛋白酶、渗透因子、黏附因子、菌毛、尿素酶以及细菌对转铁蛋白携带铁的利用能力等。
目前在APP中已发现4种不同的Apx具有溶血活性或细胞毒性,即ApxI、ApxII、ApxIII和ApxIV(Schaller A,Kuhn R,Kuhnert P,Nicolet J,Anderson T J,MacInnes J I,SegerR P A M,Frey J.Characterization of apxIVA,a new RTX determinant of Actinobacilluspleuropneumoniae.Microbiology,1999,8(Pt8):2105-2116)。如果要产生和分泌具有生物活性的Apx毒素,需要相邻的按一定顺序排列的四个基因CABD组成的操纵子调控,其中A基因编码毒素结构蛋白,C基因编码毒素激活蛋白,负责对毒素进行酰基化激活,B基因和D基因的翻译后蛋白产物形成跨膜通道,负责毒素由细胞内到细胞外的分泌。ApxI、ApxIII操纵子有完整的CABD基因,而ApxII操纵子只有C基因和A基因,其产物由ApxI的BD基因产物负责分泌到细胞外。
大量试验已证实,这些毒力因子大部分都是APP重要的保护性抗原。其中APP产生的溶血外毒素(Apx)被认为既是APP最重要的一个毒力因子(Tascon R I,Vazquez Boland J A,Gutierrez Martin C B,Rodriguez Barbosa I,Rodriguez Ferri EF.The RTX haemolysins ApxI andApx II are major virulence factors of the swine pathogen Actinobacillus pleuropneumoniae:evidence from mutational analysis.Mol Microbiol,1994,14(2):207-216;Frey J,Beck M,van denBosch J F,Segers R P,Nicolet J.Development of an efficient PCR method for toxin typing ofActinobacillus pleuropneumoniae strains.Mol Cell Probes,1995,9(4):277-282)。研究发现,不分泌或缺失了Apx的APP菌株对猪和小鼠均不致病,但缺失突变菌株在补充Apx的结构基因和分泌基因后又可恢复原来的毒力(Tascon R I,Vazquez Boland J A,Gutierrez Martin C B,Rodriguez Barbosa I,Rodriguez Ferri EF.The RTX haemolysins ApxI and ApxII are majorvirulence factors of the swine pathogen Actinobacillus pleuropneumoniae:evidence frommutational analysis.Mol Microbiol,1994,14(2):207-216;Reimer D,Frey J,Jansen R,Veit H P,Inzana T J.Molecular investigation of the role of ApxI and Apx II in the virulence ofActinobacillus pleuropneumoniae serotype 5.Microb Pathog,1995,18(3):197-209),而且Apx气管灌注可以直接引起APP的临床症状和肺部病变(Kamp E M,Stockhofe-Zurwieden N,vanLeengoed L A,Smits M A.Endobronchial inoculation with Apx toxins of Actinobacilluspleuropneumoniae leads to pleuropneumonia in pigs.Infect Immun,1997,65(10):4350-4354)。同时,无毒性的溶血外毒素(Apx)也是一种很重要的免疫保护性抗原。Prideaux等(1998)(Prideaux C T,Pierce L,Krywult J,Hodgson A L.Protection of mice against challenge withhomologous and heterologous serovars of Actinobacillus pleuropneumoniae after live vaccination.Curr Microbiol,1998,37(5):324-332利用插入失活的方法把含有apxIA基因的一个表达质粒插入到已经分离到的一株天然缺失结构毒素ApxIIA和翻译后激活蛋白ApxIIC但仍保留分泌必须基因apxIB和apxID的APP血清7型APP突变菌株,构建了表达无活性ApxI蛋白的弱毒菌株,免疫小鼠后证实在小鼠模型是致弱的且能诱导小鼠产生Apx特异性抗体,不仅能抵抗APP血清型7型的攻击,而且能对异源血清1型也产生了较好的保护力。与该突变菌株相比,不表达ApxI的亲本菌株对异血清1型没有保护力。这进一步证实了毒素在交叉保护中所起的重要作用,也为毒素弱毒菌株的构建提供了一个新的思路。然而,这种弱毒活疫苗疫苗的应用,由于含有保护性抗原的质粒在体内复制过程中容易丢失而受到限制。随后Prideaux等(1999)(Prideaux C T,Lenghaus C,Krywult J,Hodgson A L.Vaccination and protection of pigsagainst pleuropneumonia with a vaccine strain of Actinobacillus pleuropneumoniae produced bysite-specific mutagenesis of the Apx II operon.Infect Immun,1999,67〔4):1962-1966通过使用位点特异性突变构建了apxIIC基因插入失活的基因工程突变菌株,但结构毒素ApxIIA和两个分泌必须基因apxIB、apxID仍然存在,这样细菌可以持续而安全地表达无活性的ApxIIA毒素。突变菌株经鼻腔内接种动物,不仅表现出毒力降低,而且能诱导动物产生针对不同血清型APP攻击的交叉保护,展示了APP基因缺失疫苗良好的应用前景。这也是首次报道APP弱毒菌株接种动物能够提供抗APP异源血清型很好的交叉保护。
目前商品化的全菌灭活疫苗和亚单位疫苗能够减轻同源血清型菌感染猪引起的临床症状并降低死亡率,但不能降低发病率、慢性感染和阻止肺部病变,对异源血清型菌的感染也不能提供完全的交叉保护。可以说,目前采用灭活苗和亚单位疫苗免疫不是最好的选择,迫切需要更安全、高效、廉价的新型疫苗来预防和控制该传染病的发生与流行。
与灭活疫苗和亚单位疫苗不同,自然感染或试验感染能够诱导抗任何异源血清型的保护。这样,弱毒活疫苗也许是解决当前商品化疫苗不足的一种可行方法。构建胸膜肺炎放线杆菌突变菌株的传统方法存在很多缺陷。如利用化学或转座子介导的突变方法存在随机性,只适合于表型发生明显变化突变子的筛选,而不导致明显表型变化的突变菌株就不能够通过这些方法获得;而通过同源重组导致靶基因突变方法获得的突变菌株最后含有抗性标记,由于不符合生物安全性要求不能作为疫苗株用于疫苗生产。
发明内容
本发明的目的在于克服现有技术存在的缺陷,获得一种免疫原性更好和安全性更强的猪胸膜肺炎放线杆菌双基因缺失疫苗;
本发明的第二个目的是利用胸膜肺炎放线杆菌双基因缺失突变菌株制备猪传染性胸膜肺炎双基因缺失疫苗;
本发明的第三个目的是胸膜肺炎放线杆菌双基因缺失突变菌株在制备猪传染性胸膜肺炎双基因缺失疫苗中的应用。
本发明通过以下技术方案实现:
一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株-猪胸膜肺炎放线杆菌(分类命名:Actinobacillus pleuropneumoniae)APP-1-mut01,于2007年1月19日保藏在中国典型培养物保藏中心(CCTCC),保藏编号:CCTCC NO:M207005。
所述的不含抗性标记猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株缺失胸膜肺炎放线杆菌血清1型两个主要毒力基因激活因子apxIC和apxIIC,缺失后产生没有毒力的毒素蛋白ApxI和ApxII,但毒素蛋白仍具有很好免疫原性。
本发明的不含抗性标记猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株,其基因工程菌株衍生于本申请人申请日前已经公开报道的自行分离鉴定的猪胸膜肺炎放线杆菌(参见:王贵平等,猪胸膜肺炎放线杆菌快速PCR检测方法的建立,中国兽医学报,2004,24(2),129-131)。所述的重组猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株其主要毒力基因apxIC缺失了500bp,apxIIC缺失了480bp,导致毒力大大降低,该细菌不再具有细胞毒性和溶血活性,因而具有很高的安全性。而且由于突变菌株仍然能表达无毒性的ApxIA和ApxIIA蛋白,因此具有很好的免疫保护力。
本发明的基本构建方法是:利用基因工程技术使猪胸膜肺炎放线杆菌血清1型(简称APP-1,下同)两个主要毒力因子的激活因子apxIC和apxIIC完全缺失后,因为要产生和分泌具有生物活性的Apx毒素,需要相邻的按一定顺序排列的四个基因CABD组成的操纵子调控,其中A基因编码毒素结构蛋白,C基因编码毒素激活蛋白,负责对毒素进行酰基化激活,B基因和D基因的翻译后蛋白产物形成跨膜通道,负责毒素由细胞内到细胞外的分泌。ApxI、有完整的CABD基因,而ApxII操纵子只有C基因和A基因,其产物由ApxI的BD基因产物负责分泌到细胞外。因此,当毒力基因的激活因子apxIC和apxIIC完全缺失后就不会产生具有毒性的毒素蛋白,由于A基因是结构蛋白,与免疫保护性相关,表达的ApxIA和ApxIIA蛋白的生物学特性没有改变。通过大量的生物学实验数据证明本发明制备的双基因缺失菌株可用于制备猪传染性胸膜肺炎双基因缺失疫苗。
本发明的主要优点是:
1、本发明所用血清型菌株是目前我国流行并严重导致猪发病的优势血清型,毒力最强,同时免疫保护性也最好。因此,用该亲本菌构建的双基因缺失突变菌株制成疫苗对猪免疫具有很强的针对性,具有广阔的市场应用前景。
2、猪胸膜肺炎放线杆菌血清1型两个主要毒力基因的激活因子apxIC和apxIIC完全缺失后基因缺失突变菌株毒力大大降低,但免疫原性未发生改变,可以保护同源和异源血清型菌攻击。
3、本发明猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株不含抗性标记,完全符合疫苗生物安全性要求。
附图说明
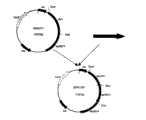
图1:是本发明中用于构建不含抗性标记猪胸膜肺炎放线杆菌血清1双基因缺失突变菌株的物理图谱。
图2:是本发明制备的转移质粒pEMΔIC的鉴定结果。
图中M:DNA marker(DL15000)1:pEMΔIC/XbaI I+SmaI2:pEMΔIC/XbaI
图3:是本发明制备的转移质粒pEMΔIIC的鉴定结果。
图中M:DNA marker(DL15000)1:pEMΔIIC/XbaI I+SmaI2:pEMΔIIC/XbaI
图4:是本发明制备的pEMΔIC转移质粒构建的流程图。
图5:是本发明的pEMΔIIC转移质粒构建的流程图。
图6:是本发明中不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的PCR检测电泳图谱。
图A:apxIC—双交换PCR鉴定图,图中M:DL2000DNA分子量对照;77号为筛选的缺失株;(+)质粒阳性对照;(-)H2O阴性对照;
图B:apxIIC—双交换PCR鉴定图,M:DL2000 DNA分子量对照;7号为筛选的双基因缺失株
图7:是本发明中的不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的Western-blotting分析结果。
图A是用Western-blotting方法检测ApxII
图中1:亲本株;2:突变菌株
图B是用Western-blotting方法 检测ApxI
图中1:亲本株;2:突变菌株
图8:是本发明中的不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的溶血实验结果。
图中A区:表示亲本菌株;B区表示apxIC—单基因缺失株;C区表示/apxIC、apxIIC双基因缺失株
图9:是本发明中的不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的生长特性实验结果。
图10:是本发明中的不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变菌株的遗传稳定性实验结果。
具体实施方式
以下结合说明书附图对本发明作进一步的说明。
实施例1
1、引物设计(用于基因克隆和分子检测)
根据已报道的APP-1株序列(参照GenBank登录号为X68595的基因序列)设计四对引物分别扩增毒素apxI激活基因apxIC上游臂和下游臂,扩增片段大小分别为800bp和1700bp,上游臂两端分别设计EcoRI和HindIII酶切位点,下游臂两端分别设计HindIII和XhoI酶切位点;apxII的激活基因apxIIC的上游臂和下游臂,扩增片段大小分别为1600bp和1800bp,上游臂两端分别设计PstI和EcoRI酶切位点,下游臂两端分别设计KpnI和XhoI酶切位点。上述引物均由上海生物工程公司合成。引物序列如下:
pI-1:5’-AGCGAATTCTTAAATTGCCTTTTACT-3’(EcoRI)
pI-2:5’-GCTAAGCTTTGATTACTCTCAATCGC-3’(HindIII)上臂800bp
pI-3:5’-GTACTCGAGCTAAGGAGACAACATG-3’(HindIII)
pI-4:5’-ACACTCGAGGTTTGCTTACGCTCACG-3(XhoI)下臂1700bp
pII-1:5’GCCTGCAGATTAAACAGCACCCTAC-3’(PstI)
pII-2:5’-GTGAATTCGTAGCATCATCCCTCCC-3’(EcoRI)上臂1600bp
pII-3:5’-TCCTCGAGGGCAATTAGAATCTATC-3’(EcoRI)
pII-4:5’-GCGGTACCTTCACCTGGAGTTAGT-3’(KpnI)下臂1800bp
2.猪胸膜肺炎放线杆菌毒素apxI激活基因apxIC上游臂和下游臂、apxII的激活基因apxIIC的上游臂和下游臂的克隆
将改良的TSA(即胰蛋白大豆琼脂培养基,购自美国GIBCO公司,以该培养基为基本成分,附加按体积比为1%的烟酰胺腺嘌呤二核苷酸和10%的小牛血清)融化,冷却至50℃,加适量烟酰胺腺嘌呤二核苷酸(Nicotinamide Adenine Dinucleotide,NAD,又称V因子,购自中国上海化学试剂公司),倒于平板中,待冷却凝固后,置37℃温箱2~3h至水汽烘干。将冻干的APP血清1型和7型菌接至烘干平板中过夜培养。第二天挑取单菌落接种于改良TSB(即胰蛋白大豆琼脂培养基,购自美国GIBCO公司,以该培养基为基本成分,附加按体积比为1%的烟酰胺腺嘌呤二核苷酸和10%的小牛血清)培养基中,37℃200r/min培养7-10h提取细菌的基因组。
取1mL改良TSB培养基于EP管中,室温8000r/min离心5min,弃上清,沉淀悬浮于1mL TE溶液中。加入6μL50mg/mL的溶菌酶,37℃作用2h后加2mol/L NaCl 50μL,10%十二烷基磺酸钠(SDS)110μL,20mg/mL的蛋白酶K3μL,50℃作用3h或37℃过夜。均分到两个EP管,加等体积的酚∶氯仿∶异戊醇(100∶99∶1)抽提两次,用0.6V的异丙醇沉淀0.5h以上,离心后再用75%的乙醇洗涤,凉干后,溶于500μL ddH2O中作PCR模板。
扩增反应在50μL的体系中进行,反应体系如下:模板DNA(1:100质粒DNA)2μL,10×PCR缓冲液5μL,25mmol/L MgCl22.5μL,10μmol/L P1 0.5μL,10μmol/L P2 0.5μL,1mmol/L dNTPs 2μL,TaqE 1μL,ddH2O 33.4μL。
扩增条件为:95℃变性5min后进入循环,循环参数为94℃ 1min,57℃ 1min,72℃40sec。35个循环后,72℃延伸10min。扩增的PCR产物经0.8%的琼脂糖凝胶电泳分析,扩增四个片段大小分别为800bp、1700bp、1600bp和1800bp,与预期大小相当。将得到的目的基因克隆到pMD-18载体(购自大连宝生物工程有限公司),送大连宝生物工程有限公司进行外源基因序列的测定,参见图1所示。
3.pEM△IC转移质粒的构建
用EcoRI和HindIII酶切大小为800bp的apxIC上游臂PCR扩增产物,用HindIII和XhoI酶切大小为1700bp的apxIC下游臂PCR扩增产物,同时用EcoRI和XhoI酶切载体pEMOC2。回收apxIC上游臂基因、apxIC下游臂基因和载体pEMOC2,然后用T4DNA ligase连接,16℃水浴过夜,转化DH5α感受态细菌,37℃培养,挑菌,然后将连接产物转化DH5α大肠杆菌,小量制备质粒、酶切鉴定,从而获得转移质粒pEMΔIC。其物理图谱见图1。鉴定结果证实构建的转移质粒pEM△IC正确的(见图2),转移质粒pEMΔIC构建流程如图3所示。
4.pEM△IIC转移质粒的构建
用PstI和EcoRI酶切大小为1600bp的apxIIC上游臂PCR扩增产物,用KpnI和XhoI酶切大小为1800bp的apxIIC下游臂PCR扩增产物,同时用PstI和XhoI酶切载体pEMOC2。回收上下游同源臂基因和载体pEMOC2,然后用T4DNA ligase连接,16℃水浴过夜,转化DH5α感受态细菌,37℃培养,挑菌,然后将连接产物转化DH5α大肠杆菌,小量制备质粒、酶切鉴定,从而获得转移质粒pEMΔIIC。其物理图谱见图1。鉴定结果证实构建的转移质粒pEMΔIIC正确的(见图4〕,转移质粒pEMΔIIC构建流程如图5所示。
5.apxIC单基因缺失突变菌株SJ01/apxIC-的构建
将构建的转移质粒pEMΔIC转化进入大肠杆菌Ecoli β2155(德国汉若威大学Gerald-F.Gerlach professor赠送)中,然后将携带有转移质粒pEMΔIC的大肠杆菌(Ecoliβ2155)与亲本菌APP血清1型(APP-1)进行转接,在氯霉素抗性平板(将25ug/mL的氯霉素加入进温度为50-60℃灭菌的TSA培养基中)上筛选阳性菌落,将阳性单菌落在不含氯霉素抗性TSB培养基上培养增殖得到抗性菌落后,再在5%蔗糖平板上筛选耐蔗糖菌落,将经过筛选得到单基因缺失突变株菌命名为SJ01/apxIC-。
提取单基因缺失突变菌株SJ01/apxIC-基因组DNA,用PCR扩增apxIC基因,以确定是否能扩增出大小为500bp apxIC特异性DNA片段。如果不能扩增出所述的DNA片段,则表明结果与预期相符,即可初步鉴定筛选的单基因缺失突变菌株是正确的,如图6A所示。
6.apxIC、apxIIC双基因缺失突变菌株SJ01/apxIC—/apxIIC—的构建
将构建的重组质粒pEMΔIIC转化至大肠杆菌Ecoli β2155,同时将以上构建的毒素apxIC单基因缺失突变菌株作为亲本菌,将携带有重组质粒pEMΔIIC大肠杆菌Ecoli β2155与亲本菌进行转接,在氯霉素抗性平板(将25ug/mL的氯霉素加入进温度为50-60℃灭菌的TSA培养基中)上筛选阳性菌落,将阳性单菌落在不含氯霉素抗性TSB(含NAD和血清)培养增殖抗性菌落后,在5%蔗糖平板上筛选耐蔗糖菌落,命名为SJ01/apxIC—/apxIIC—。
提取双基因缺失突变菌株SJ01/apxIC—/apxIIC—基因组DNA,用PCR扩增apxIIC基因,看是否能扩增出大小为480 bp apxIIC特异性DNA片段。如果不能扩增出所述的DNA片段,表明结果与预期相符,可初步鉴定筛选的突变菌株是正确的,如图6B所示。
7.apxIC、apxIIC双基因缺失突变菌株(SJ01/apxIC—/apxIIC—)的生物学特性及其鉴定(1)双基因缺失突变菌株(实验编号为:SJ01/apxIC—/apxIIC—)免疫学活性分析
以突变菌株培养后的上清液和离心后的溶菌液为样品进行SDS-PAGE(聚丙稀酰胺凝胶电泳),按此方法进行蛋白表达和聚丙烯酰氨凝胶电泳(SDS-PAGE)凝胶转移至硝酸纤维素膜,用0.5%牛血清白蛋白(BSA)封闭30分钟后加入一抗1小时,兔抗猪IgG-HRP,37℃1h经TBS洗后3,3’二氨基联苯二胺盐酸盐(购自Sigma公司)显色。结果如图7所示:猪传染性胸膜肺炎放线杆菌血清1型双基因apxIC、apxIIC失活后仍能分泌大小约110KDa具有良好免疫原性的毒素蛋白ApxIA、ApxIIA。
(2)双基因缺失突变菌株溶血活性分析
挑取双基因缺失突变菌株和亲本菌APP-1和APP-7型,分别接种于含有绵羊血的血琼脂平皿(按照常规方法),37℃培养过夜,观察它们的溶血情况。结果如图8。图8显示基因缺失突变菌株完全失去了溶血。
(3)双基因缺失突变菌株生长特性分析
分别挑取亲本菌(实验编号:SJ01)、单基因缺失突变菌株(实验编号:SJ01/apxIC—)和双基因缺失突变菌株(实验编号:SJ01/apxIC—/apxIIC—)单菌落,接种入TSB培养基中培养,每间隔1小时取样,以分光光度计OD600读取其值,通过每一个相同时间段OD600值大小来比较它们的生长快慢。结果如图9所示:apxIC和apxIIC基因的缺失对APP的生长没有影响。
(4)双基因缺失突变菌株的遗传稳定性
将本发明制备的双基因缺失突变菌株在改良的TSA培养基连续传代10次,用PCR鉴定,看每一代的突变菌株是否都能扩增出0.5kb的apxIC和0.48kb的apxIIC基因特异性片段。若不能,表明本发明的突变菌株是能够稳定遗传的。具体PCR操作方法:提取双基因缺失突变株基因组DNA,以其为模板进行PCR扩增。扩增反应在25μL的体系中进行,反应体系如下:模板基因组DNA(1:100质粒DNA)1μL,10×PCR缓冲液2.5μL,25mmol/L MgCl2 1.25μL,10μmol/L P1 0.25μL,10μmol/L P2 0.25μL,1mmol/L dNTPs 1μL,TaqE0.5μL,ddH2O16μL。扩增条件为:95℃变性5min后进入循环,循环参数为94℃1min,53℃1min,72℃30sec。32个循环后,72℃延伸7min。结果如图10所示:本发明制备的双基因缺失突变菌株能够稳定遗传。
8、猪传染性胸膜肺炎双基因缺失疫苗(实验编号:SJ01/apxIC—/apxIIC—)的制备
将获得的猪胸膜肺炎放线杆菌双基因缺失突变菌株(实验编号:SJ01/apxIC—/apxIIC一)进行鉴定,每代接种于改良的TSA培养基上,该培养基以TSA培养基为基本成分,附加按体积比为1%的烟酰胺腺嘌呤二核苷酸和10%的小牛血清,利用胸膜肺炎放线杆菌的apxIC、apxIIC基因进行PCR检测鉴定重组细菌的遗传稳定性,经20次传代后发现仍然不能扩增出大小分别为(500bp)apxIC和(480bp)apxIIC基因,遗传性稳定。通过Western-blotting检测ApxIA和ApxIIA毒素蛋白可以在突变菌株中能够稳定的表达,并具有良好的生物学活性。该猪胸膜肺炎放线杆菌双基因缺失突变菌株在改良的TSA(附加按体积比为1%的烟酰胺腺嘌呤二核苷酸和10%的小牛血清)固体培养基上培养,挑取单菌落于改良的TBS(以TBS培养基为基本培养基,附加按体积比为1%的烟酰胺腺嘌呤二核苷酸和10%的小牛血清)固体培养基上培养,直到活细菌浓度达到2×108CFU/mL,按细菌液:明胶保护剂(体积/体积)为7:1的比例加入明胶保护剂(该明胶保护剂配制方法是:每100ml去离子水中加蔗糖40g,明胶8g,充分融化后,置121℃下灭菌30min后保存备用),于灭菌冻干瓶中按2.0mL/瓶分装,置-50℃冷冻干燥机中冻干,冻干36-40h后压盖,复苏后确定没有杂菌污染,置-20℃保存备用,作为研制基因缺失疫苗的疫苗菌株。
9、猪传染性胸膜肺炎双基因缺失疫苗(SJ01/apxIC—/apxIIC—)的安全性评价
为测定构建的基因缺失疫苗菌株(SJ01/apxIC—/apxIIC—)对Bab/C小鼠的安全性,将60只Bab/C小鼠平均分为6组。其中3组每只小鼠注射0.5mL双基因缺失疫苗菌株(SJ01/apxIC—/apxIIC—),活菌浓度从低到高依次为2×108CFU,1×109CFU,2×109CFU;另3组每只小鼠注射0.5mL APP血清1型亲本株,浓度依次为2×107CFU,1×108CFU,2×108CFU,通过小鼠死亡率,评价双基因缺失疫苗菌株(SJ01/apxIC—/apxIIC—)与亲本株(SJ01)相比毒力是否减弱以及对小鼠是否安全。
结果见表1:用亲本株3个浓度注射小鼠后,最低浓度(2×107CFU)只有一只小鼠死亡,最高浓度(2×108CFU)使小鼠全部死亡;而本发明的双基因缺失疫苗菌株(SJ01/apxIC-/apxIIC-)注射的小鼠,最低浓度(2×108CFU)到最高浓度(2×109CFU)没有小鼠死亡,表明本发明的双基因缺失突变菌株(SJ01/apxIC—/apxIIC—)与亲本株相比,毒力明显降低且对小鼠是安全的。
表1 本发明的双基因缺失疫苗菌株与亲本株毒力比较试验
将本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)按每头猪注射2mL(含2×108CFU活菌数)接种6周龄的仔猪,部分接种仔猪出现轻度的--过性的发热、体温升高反应,两天后恢复正常,在此期间注射本发明制备的基因缺失疫苗的仔猪的精神食欲正常,未见异常变化,可以检测到胸膜肺炎放线杆菌间接血凝菌体抗体和毒素抗体。亲本菌株SJ01接种的仔猪(即对照1),第二天全部呈现发热、体温升高、呼吸困难等反应,持续一周,并有一头死亡,剖检发现具有典型的猪传染性胸膜肺炎病理变化;而对照组2既没有体温升高,也没有异常临床表现。按每头猪注射2mL(含2×108CFU活菌数)接种本发明的SJ01/apxIC—/apxIIC—双基因缺失疫苗和未接种的妊娠母猪,窝产仔数基本相当,均没有出现死胎、木乃伊胎等,证实本发明制备的基因缺失疫苗对妊娠母猪也是安全的。
8.猪传染性胸膜肺炎双基因缺失疫苗(SJ01/apxIC—/apxIIC—)在小鼠体内的免疫效力检测
1)小鼠的免疫程序:
选择体重为18g左右的Balb/c小鼠作为免疫效力评价,根据试验要求分为3组,分别为本发明制备的双基因缺失疫苗免疫组(SJ01/apxIC—/apxIIC—)、单基因缺失疫苗组(apxIIC一)、三价灭活疫苗免疫组和非免疫空白对照组,每组10只,免疫途径为腹腔注射0.5mL(含2×108CFU活菌量)细菌液或TSB培养基(购自美国GIBCO公司),分别于免疫前0天、首免后14天和28天检测APP间接血凝抗体(HIA,操作方法参照中国农业科学院兰州兽医研究所APP间接血凝抗体检测试剂盒说明书)以及毒素ApxI抗体水平(方法参照刘建杰等,猪胸膜肺炎放线杆菌毒素I基因的克隆、表达及其ELISA检测方法的建立,中国农业科学,37(1):148-151,2004)、ApxII抗体水平(方法参照梁望旺等,猪胸膜肺炎放线杆菌毒素II蛋白的表达、纯化及其间接ELISA检测方法的建立与应用,中国兽医学报,25(2):145-147,2005)。
2)免疫小鼠体液免疫抗体水平检测
小鼠免疫前采血,第二、三次采血分别在首免后14、28天进行,经尾静脉负压采血,分离血清,检测APP全菌抗体和特异性抗APP的ApxI抗体(方法参照刘建杰等,猪胸膜肺炎放线杆菌毒素I基因的克隆、表达及其ELISA检测方法的建立,中国农业科学,37(1):148-151,2004)、ApxII ELISA抗体(方法参照梁望旺等,猪胸膜肺炎放线杆菌毒素II蛋白的表达、纯化及其间接ELISA检测方法的建立与应用,中国兽医学报,25(2):145-147,2005)。结果见表2。从表2中可以看出,首免后第2周本发明制备的基因缺失疫苗组和灭活疫苗免疫组全部转阳,首免后2周,本发明制备的双基因缺失疫苗诱导产生的间接血凝抗体效价在1:8~1:32之间,ApxIA ELISA和ApxIIA ELISA抗体水平在1:160~1:320。而灭活疫苗组诱导产生的间接血凝抗体效价在1:4~1:16之间,ApxIAELISA和ApxIIA ELISA抗体水平小于1:40。而同步进行的TSB对照均为阴性。二免后2周(即首免后4周),本发明制备的双基因缺失疫苗和灭活疫苗免疫组产生的无论是间接血凝还是ELISA抗体均有一定程度的上升。本发明制备的双基因缺失疫苗二种检测方法所产生的抗体效价高于灭活疫苗组,其间接血凝抗体效价在1:64~1:256之间,而ApxIA ELISA和ApxIIA ELISA抗体水平在1:640~1:2560之间,TSB对照组抗体检测仍为阴性。上述结果表明本发明制备的双基因缺失疫苗免疫小鼠后能诱导机体产生特异性的抗APP的体液免疫应答。
表2本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫小鼠血清抗体检测(HIA和ELISA法)
3)胸膜肺炎放线杆菌攻击双基因缺失疫苗免疫Balb/C小白鼠的保护性试验:
将20克左右胸膜肺炎放线杆菌阴性Bab/C小鼠48只,平均分为三个大组(或6个小组),即本发明制备的基因缺失疫苗(SJ01/apxIC—/apxIIC—)、灭活疫苗对照组、TSB对照组。基因缺失疫苗组以0.5mL(活菌含量2×108CFU)培养液通过腹腔注射Bab/C小鼠。灭活疫苗对照组每只小鼠通过腹腔注射0.5mL灭活疫苗;TSB对照组只腹腔注射0.5mL TSB培养基。
免疫后第4周,TSB对照组、灭活疫苗对照组和基因缺失疫苗组分别用2LD50APP血清7型菌(活菌含量1×108CFU)和2LD50APP血清1型(活菌含量2×108CFU)对免疫小鼠进行攻毒。结果,APP血清7型和1型菌攻击的TSB对照组12h内小鼠全部死亡,死亡小鼠肺部有出血,从心血和肺脏能分离攻毒用APP。灭活疫苗对照组APP血清7型攻击的8只小鼠死亡2只,而APP血清1型攻击的8只小鼠死亡1只,死亡小鼠解剖可见肺部出血。本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)用APP血清1型菌攻毒的8只小鼠没有死亡,小鼠攻毒开始24h内呈现精神沉郁、不食、扎堆,之后逐步恢复正常,观察到第三天和攻毒前没有差别。而用APP血清7型菌攻毒的8只小鼠,死亡1只,其余小鼠攻毒后24h精神沉郁、不食、扎堆,之后逐步恢复正常。结果说明了以亲本菌株SJ01血清1型研制的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫鼠可以完全保护同源血清1型菌攻击,而对异源血清7型菌攻击只有7/8(87.5%)保护,但仍然优于传统的灭活疫苗。攻毒后保护率情况见表3所示。
表3 本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)对APP攻击Balb/C小白鼠的保护性
9.猪传染性胸膜肺炎双基因缺失疫苗(SJ01/apxIC—/apxIIC—)在仔猪体内的免疫效力检测
1)猪的免疫程序:
选择猪传染性胸膜肺炎阴性、40-50日龄的断奶仔猪24头,试验分3组,第一组为TSB对照组,编号1~8,第二组为灭活疫苗对照组,编号9~16,第三组为双基因缺失疫苗组(SJ01/apxIC—/apxIIC—),编号17~24。
TSB对照组每头猪注射1mL TSB培养基,灭活疫苗对照组每只猪颈部肌肉注射灭活疫苗2mL,而本发明的双基因缺失疫苗免疫组(SJ01/apxIC—/apxIIC—)通过气管和肌肉注射培养液1mL(活菌含量1×109CFU),免疫2次,间隔2周。在一免后2周和二免后2周各采血一次,分别用间接血凝试验(参照中国农业科学院兰州首义研究所,APP间接血凝抗体检测试剂盒说明书)和毒素ApxI抗体水平〔方法参照刘建杰等,猪胸膜肺炎放线杆菌毒素I基因的克隆、表达及其ELISA检测方法的建立,中国农业科学,37(1):148-151,2004)、ApxII抗体水平(参照梁望旺等,猪胸膜肺炎放线杆菌毒素II蛋白的表达、纯化及其间接ELISA检测方法的建立与应用,中国兽医学报,25(2):145-147,2005)
试验分组、免疫途径和免疫剂量详细情况见表4。
表4 猪胸膜肺炎放线杆菌双基因缺失疫苗免疫仔猪试验动物分组设计
2)免疫仔猪间接血凝抗体水平检测
首免后第2和第4周(二免后第2周)前腔静脉采血,分离血清,检测APP间接血凝抗体(操作方法按兰州兽医研究所的间接血凝检测方法对菌体的血凝抗体进行测定),以血清效价大于或等于1∶16判为阳性。结果见表5,从表中可以看出,首免后2周,本发明制备的基因缺失疫苗能够诱导免疫仔猪产生一定水平的APP间接血凝抗体;首免后4周,本发明制备的基因缺失疫苗免疫组APP间接血凝抗体水平有上升。无论是首免后2周还是首免后4周,本发明制备的双基因缺失疫苗SJ01/apxIC—/apxIIC—诱导的APP间接血凝抗体高于灭活疫苗,这表明毒素激活基因的缺失并不影响双基因缺失疫苗的免疫原性。
表5 本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫仔猪APP间接血凝抗体检测结果
3)APP特异性毒素ApxIA、ApxIIA ELISA抗体
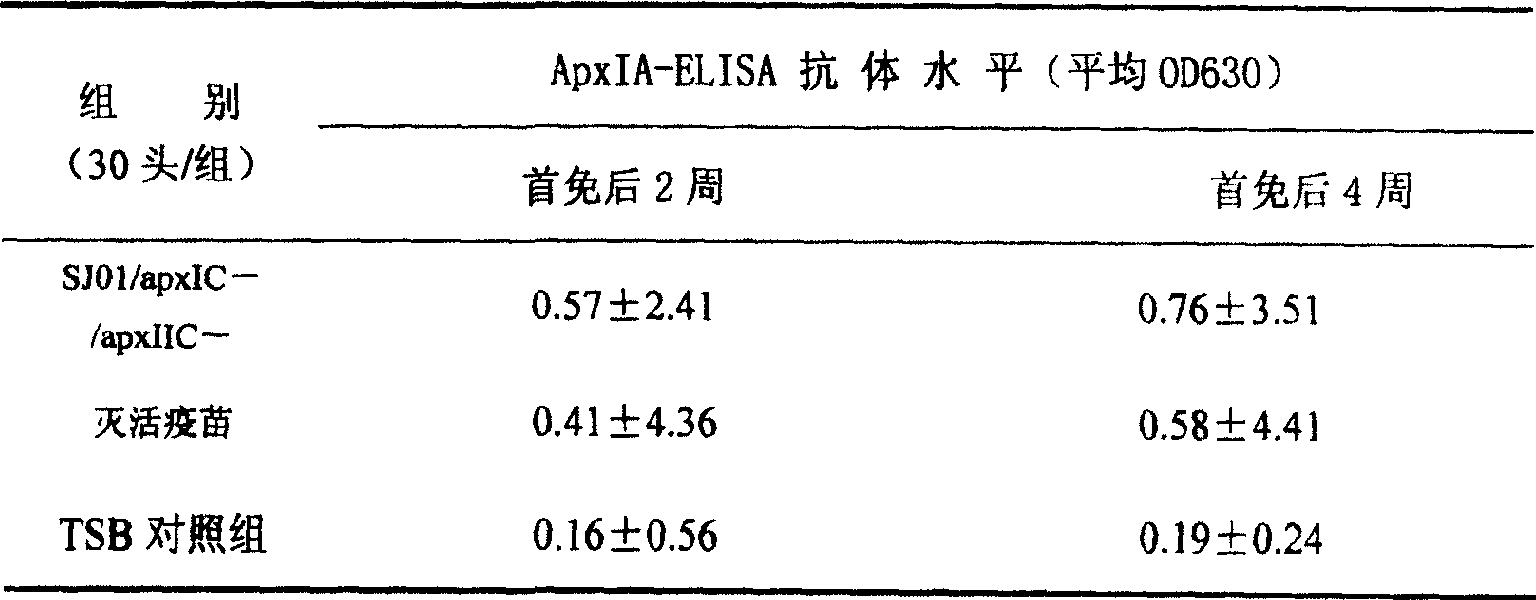
分别在第一次2周和第二次免疫后2周前腔静脉采血,分离血清,采用间接ELISA检测分别检测ApxIA ELISA抗体(方法参照刘建杰等,猪胸膜肺炎放线杆菌毒素I基因的克隆、表达及其ELISA检测方法的建立,中国农业科学,37(1):148-151,2004)和ApxIIA ELISA抗体(方法参照梁望旺等,猪胸膜肺炎放线杆菌毒素II蛋白的表达、纯化及其间接ELISA检测方法的建立与应用,中国兽医学报,25(2):145-147,2005),结果见表7:TSB对照组ApxIA抗体无论一免或二免都维持在阴性水平,平均OD630值分别为0.16和0.19,与免疫前OD630平均0.18相比没有差别;灭活疫苗对照组免疫前平均值OD630为0.21,免疫后第一次平均值为0.41,而第二次平均值为0.58;而双基因缺失疫苗免疫断奶仔猪,首免后2周ELISA抗体OD630平均值为0.57,二免后2周ELISA抗体明显上升,OD630平均值为0.76,ApxIA抗体水平总体情况见表6所示。
表6 本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫仔猪APP ApxIA-ELISA抗体检测结果
同样,TSB对照组ApxIIA抗体无论一免或二免都维持在阴性水平,平均OD630值分别为0.19和0.20,与免疫前OD630平均0.18相比没有差别;灭活疫苗对照组免疫前平均值OD630为0.20,免疫后第一次平均值为0.37,而第二次平均值为0.48;而双基因缺失疫苗免疫断奶仔猪,首免后2周ELISA抗体OD630平均值为0.59,二免后2周ELISA抗体明显上升,OD630平均值为0.74,ApxII抗体水平总体情况见表表7。
表7本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫仔猪APP ApxIIA-ELISA抗体检测结果
4)免疫仔猪攻毒保护率试验
二免后2周TSB对照组1~4号、灭活疫苗对照组9~12号、本发明的双基因缺失疫苗组17~20号猪通过气管用2.0mL(活菌含量1×109CFU)APP血清1型菌(菌株号S4074,标准菌株,由澳大利亚动物保健研究所Dr.Pat Blackall赠送)培养液攻毒;而对照组5~8号、灭活疫苗对照组13~16号、本发明的双基因缺失疫苗试验组21~24号猪用2.0mL(活菌含量2×109CFU)APP血清7型菌(菌株号WH83,标准菌株,由澳大利亚动物保健研究所Dr.PatBlackall赠送)培养液气管攻毒。连续观察1周,观察临床症状并最后计算攻毒保护率情况。结果说明以SJ01血清1型研制的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫断奶仔猪可以完全保护同源血清1型攻击,而对异源血清7型攻击只有75%保护,但仍然优于传统的灭活疫苗。攻毒后保护率情况见表8
表8 本发明制备的双基因缺失疫苗(SJ01/apxIC—/apxIIC—)免疫仔猪后攻毒保护结果
a,b肺炎和胸膜炎的病变程度:—,无;+,轻微;++,中等程度;+++,严重
c呼吸频率:每15秒的呼吸次数
d呼吸困难:0,正常;1,轻微;2,中等程度;3,严重
e嗜睡程度:0,正常;1,轻微;2,中等程度;3,严重
f食欲情况(36h内):0,吃食;1,不吃食。
g细菌分离:+,从肺部能分离;—,不能分离。
本发明实施例的试验结果显示,本发明的猪传染性胸膜肺炎双基因缺失疫苗(SJ01/apxIC—/apxIIC—)能激发机体产生高效价APP的间接血凝抗体,以及产生针对猪猪胸膜肺炎放线杆菌SJ01血清1型毒素ApxIA、ApxIIA特异性ELISA抗体并好于APP三价灭活疫苗免疫组产生的抗体,攻毒保护率也高于灭活疫苗。
Claims (3)
1.一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型的双基因缺失突变菌株,其特征在于该菌株是猪胸膜肺炎放线杆菌Actinobacillus pleuropneumoniae APP-1-mut01,其保藏号为CCTCC NO:M207005。
3.包含权利要求1所述的一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型的双基因缺失突变菌株的疫苗。
3.权利要求1所述的猪胸膜肺炎放线杆菌APP-1-mut01在制备猪传染性胸膜肺炎双基因缺失疫苗中的应用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CNB2007100513892A CN100460503C (zh) | 2007-01-26 | 2007-01-26 | 一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变株的疫苗及应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CNB2007100513892A CN100460503C (zh) | 2007-01-26 | 2007-01-26 | 一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变株的疫苗及应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN101037664A CN101037664A (zh) | 2007-09-19 |
| CN100460503C true CN100460503C (zh) | 2009-02-11 |
Family
ID=38888838
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB2007100513892A Expired - Fee Related CN100460503C (zh) | 2007-01-26 | 2007-01-26 | 一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变株的疫苗及应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN100460503C (zh) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102796679B (zh) * | 2012-01-16 | 2014-09-24 | 四川农业大学 | 血清5型猪胸膜肺炎放线杆菌Apx I C/Apx II C双基因缺失疫苗候选株 |
| CN113350495B (zh) * | 2021-03-05 | 2022-09-13 | 中国农业科学院哈尔滨兽医研究所(中国动物卫生与流行病学中心哈尔滨分中心) | 猪链球菌病-副猪嗜血杆菌病-猪传染性胸膜肺炎三联亚单位疫苗及其制备方法 |
| CN113416666A (zh) * | 2021-04-27 | 2021-09-21 | 华中农业大学 | 猪胸膜肺炎放线杆菌血清10型突变菌株、ApxIA蛋白及应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1713921A (zh) * | 2002-11-20 | 2005-12-28 | 西班牙海博乐生物大药厂 | 抗猪胸膜肺炎的减毒活疫苗 |
-
2007
- 2007-01-26 CN CNB2007100513892A patent/CN100460503C/zh not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1713921A (zh) * | 2002-11-20 | 2005-12-28 | 西班牙海博乐生物大药厂 | 抗猪胸膜肺炎的减毒活疫苗 |
Non-Patent Citations (2)
| Title |
|---|
| 猪传染性胸膜肺炎放线杆菌apxⅡ/Ampr突变株的构建. 贝为成等.畜牧兽医学报,第35卷第2期. 2004 |
| 猪传染性胸膜肺炎放线杆菌apxⅡ/Ampr突变株的构建. 贝为成等.畜牧兽医学报,第35卷第2期. 2004 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN101037664A (zh) | 2007-09-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ramjeet et al. | Actinobacillus pleuropneumoniae vaccines: from bacterins to new insights into vaccination strategies | |
| CN101633909B (zh) | 预防猪感染猪繁殖与呼吸综合征的减毒活疫苗 | |
| CN101265457B (zh) | 区分疫苗免疫和野毒感染动物的猪胸膜肺炎放线杆菌血清7型双基因缺失突变株的疫苗及应用 | |
| CN105039233B (zh) | 一种牛种布鲁氏菌分子标记疫苗株及其应用 | |
| Li et al. | Surface Display of porcine circovirus type 2 antigen protein cap on the spores of bacillus subtilis 168: An effective mucosal vaccine candidate | |
| CN104894009B (zh) | 一株猪肺炎支原体菌种及其应用 | |
| US20150037370A1 (en) | Diatom-based vaccines | |
| CN101603024B (zh) | 猪支原体肺炎与猪传染性胸膜肺炎放线杆菌血清1型基因工程株疫苗及应用 | |
| CN105112349B (zh) | 一种羊种布鲁氏菌分子标记疫苗株及其应用 | |
| CN100460503C (zh) | 一种不含抗性标记的猪胸膜肺炎放线杆菌血清1型双基因缺失突变株的疫苗及应用 | |
| CN106929451A (zh) | 一株猪链球菌及其应用 | |
| Bullifent et al. | Antibody responses to Yersinia pestis F1-antigen expressed in Salmonella typhimurium aroA from in vivo-inducible promoters | |
| CN106701650B (zh) | 一株鸭疫里默氏杆菌基因缺失弱毒株及其构建方法与应用 | |
| CN103421731A (zh) | 一种副猪嗜血杆菌减毒沙门氏菌苗 | |
| CN102732473B (zh) | 表达猪肺炎支原体p46蛋白的重组猪霍乱沙门氏菌及制备方法与应用 | |
| CN108018230A (zh) | 一种血清7型副猪嗜血杆菌天然弱毒菌株及其应用 | |
| CN114854654B (zh) | 一种肠炎沙门氏菌活疫苗 | |
| CN102676419B (zh) | 一种伤寒沙门氏菌基因缺失菌株及由其制备的疫苗和应用 | |
| CN103834669B (zh) | 一种无乳链球菌的口服疫苗及其制备方法 | |
| CN108251382A (zh) | 一种猪伪狂犬病病毒致弱方法、及其致弱的病毒株、疫苗组合物和应用 | |
| CN109609468A (zh) | 一种六基因缺失的猪伪狂犬病毒、猪伪狂犬病疫苗以及制备方法 | |
| CN108410784B (zh) | 猪链球菌△CPS/SsnA-mSly(P353L)-SC19工程菌及在疫苗中应用 | |
| CN103484397B (zh) | 一种hhdA基因缺失的无抗性标记的副猪嗜血杆菌工程菌株及其构建方法 | |
| CN101962625A (zh) | 一种不含抗性标记的猪霍乱沙门氏菌基因缺失突变菌株及其疫苗 | |
| CN102676421B (zh) | 一种支气管败血波氏杆菌基因缺失菌株及由其制备的疫苗和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20090211 Termination date: 20190126 |