BR112016008928B1 - Dispositivo de imersão, seu uso e estojo para utilização em um dispositivo - Google Patents
Dispositivo de imersão, seu uso e estojo para utilização em um dispositivo Download PDFInfo
- Publication number
- BR112016008928B1 BR112016008928B1 BR112016008928-6A BR112016008928A BR112016008928B1 BR 112016008928 B1 BR112016008928 B1 BR 112016008928B1 BR 112016008928 A BR112016008928 A BR 112016008928A BR 112016008928 B1 BR112016008928 B1 BR 112016008928B1
- Authority
- BR
- Brazil
- Prior art keywords
- sge
- immersion
- nitric oxide
- treatment
- medium
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61H—PHYSICAL THERAPY APPARATUS, e.g. DEVICES FOR LOCATING OR STIMULATING REFLEX POINTS IN THE BODY; ARTIFICIAL RESPIRATION; MASSAGE; BATHING DEVICES FOR SPECIAL THERAPEUTIC OR HYGIENIC PURPOSES OR SPECIFIC PARTS OF THE BODY
- A61H33/00—Bathing devices for special therapeutic or hygienic purposes
- A61H33/14—Devices for gas baths with ozone, hydrogen, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61H—PHYSICAL THERAPY APPARATUS, e.g. DEVICES FOR LOCATING OR STIMULATING REFLEX POINTS IN THE BODY; ARTIFICIAL RESPIRATION; MASSAGE; BATHING DEVICES FOR SPECIAL THERAPEUTIC OR HYGIENIC PURPOSES OR SPECIFIC PARTS OF THE BODY
- A61H35/00—Baths for specific parts of the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61H—PHYSICAL THERAPY APPARATUS, e.g. DEVICES FOR LOCATING OR STIMULATING REFLEX POINTS IN THE BODY; ARTIFICIAL RESPIRATION; MASSAGE; BATHING DEVICES FOR SPECIAL THERAPEUTIC OR HYGIENIC PURPOSES OR SPECIFIC PARTS OF THE BODY
- A61H35/00—Baths for specific parts of the body
- A61H35/006—Baths for specific parts of the body for the feet
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0002—Galenical forms characterised by the drug release technique; Application systems commanded by energy
- A61K9/0009—Galenical forms characterised by the drug release technique; Application systems commanded by energy involving or responsive to electricity, magnetism or acoustic waves; Galenical aspects of sonophoresis, iontophoresis, electroporation or electroosmosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M35/00—Devices for applying media, e.g. remedies, on the human body
- A61M35/30—Gas therapy for therapeutic treatment of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61H—PHYSICAL THERAPY APPARATUS, e.g. DEVICES FOR LOCATING OR STIMULATING REFLEX POINTS IN THE BODY; ARTIFICIAL RESPIRATION; MASSAGE; BATHING DEVICES FOR SPECIAL THERAPEUTIC OR HYGIENIC PURPOSES OR SPECIFIC PARTS OF THE BODY
- A61H33/00—Bathing devices for special therapeutic or hygienic purposes
- A61H33/04—Appliances for sand, mud, wax or foam baths; Appliances for metal baths, e.g. using metal salt solutions
- A61H2033/048—Baths using solutions, e.g. salts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61H—PHYSICAL THERAPY APPARATUS, e.g. DEVICES FOR LOCATING OR STIMULATING REFLEX POINTS IN THE BODY; ARTIFICIAL RESPIRATION; MASSAGE; BATHING DEVICES FOR SPECIAL THERAPEUTIC OR HYGIENIC PURPOSES OR SPECIFIC PARTS OF THE BODY
- A61H2230/00—Measuring physical parameters of the user
- A61H2230/25—Blood flowrate, e.g. by Doppler effect
- A61H2230/255—Blood flowrate, e.g. by Doppler effect used as a control parameter for the apparatus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61H—PHYSICAL THERAPY APPARATUS, e.g. DEVICES FOR LOCATING OR STIMULATING REFLEX POINTS IN THE BODY; ARTIFICIAL RESPIRATION; MASSAGE; BATHING DEVICES FOR SPECIAL THERAPEUTIC OR HYGIENIC PURPOSES OR SPECIFIC PARTS OF THE BODY
- A61H2230/00—Measuring physical parameters of the user
- A61H2230/50—Temperature
- A61H2230/505—Temperature used as a control parameter for the apparatus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/02—Gases
- A61M2202/0266—Nitrogen (N)
- A61M2202/0275—Nitric oxide [NO]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/12—General characteristics of the apparatus with interchangeable cassettes forming partially or totally the fluid circuit
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/36—General characteristics of the apparatus related to heating or cooling
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2210/00—Anatomical parts of the body
- A61M2210/08—Limbs
Landscapes
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Pain & Pain Management (AREA)
- Physical Education & Sports Medicine (AREA)
- Rehabilitation Therapy (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Diabetes (AREA)
- Dermatology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Anesthesiology (AREA)
- Communicable Diseases (AREA)
- Obesity (AREA)
- Cardiology (AREA)
- Oncology (AREA)
- Emergency Medicine (AREA)
- Transplantation (AREA)
- Tropical Medicine & Parasitology (AREA)
- Endocrinology (AREA)
- Rheumatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Devices For Medical Bathing And Washing (AREA)
Abstract
dispositivo para imersão. a presente invenção diz respeito a um dispositivo para imersão que compreende uma unidade geradora de óxido nítrico e uma unidade de volume proporcionada para a imersão de objetos. a invenção também diz respeito à utilização do referido dispositivo para o tratamento de doenças, em particular, de feridas crônicas e diabetes, e também para deficiências no fluxo sanguíneo associadas a distúrbios nos vasos sanguíneos.
Description
[001] A presente invenção diz respeito a um dispositivo para imersão que compreende uma unidade geradora de óxido nítrico e uma unidade de volume proporcionada para a imersão de objetos e à utilização do referido dispositivo para o tratamento de doenças, em particular, de feridas crônicas e diabetes, e também para deficiências no fluxo sanguíneo associadas a distúrbios nos vasos sanguíneos.
[002] O tratamento de distúrbios circulatórios e das feridas crônicas resultantes é ainda inadequado na prática clínica. Estas queixas constituem não só um grave problema médico, mas também um problema económico. Estima-se que cerco de 2,4 milhões de diabéticos na Alemanha sofram de distúrbios circulatórios e/ou de uma cicatrização de feridas deficiente. A qualidade de vida dos pacientes é limitada e sofrem de uma dor evitável. Estima-se que os custos de tratamento sejam de 3 mil milhões de euros por ano. Com o envelhecimento da população cada vez mais pessoas irão sofrer de tais problemas de cicatrização lenta de feridas. Assim, prevê-se que estes números dupliquem até ao ano 2025.
[003] O tratamento corrente é baseado principalmente em um suporte farmacológico de perfusão de tecidos moderadamente eficaz, bem como no suporte por sistemas de revestimento para feridas crônicas insuficiente.
[004] Um princípio fisiológico importante da pele humana é a produção enzimática de óxido nítrico com o auxílio de enzimas da família das NO- sintases, que pode ser sintetizado por todos os tipos de células [1]. O substrato das NO-sintases é o aminoácido L-arginina. Hoje em dia, é possível distinguir entre duas isoformas de NO-sintases expressas constitutivamente e indutíveis. As NO-sintases expressas constitutivamente incluem a óxido nítrico-sintase predominantente localizada nos neurónios (nNOS) e a NO-sintase predominantemente localizada no endotélio (eNOS), que, no entanto, também é expressa em fibroblastos dérmicos e em túbulos musculares da pele, ao passo que a isoforma intudível, iNOS, é induzida apelas pela ação de estímulos pró-inflamatórios e, ao contrário das isoformas constitutivas, ao longo de períodos de tempo mais alargados (dias) e pode produzir concentrações locais elevadas de NO.
[005] Os seguintes termos monóxido de azoto, óxido nítrico, radical de óxido nítrico, NO e NO^ são utilizados como termos sinónimos para a mesma molécula.
[006] Além disso, o NO também pode ser libertado não enzimaticamente a partir de nitrito ou de tióis nitrosos. A geração não enzimática de NO tem lugar sob condições de acídicas e redutoras. Neste caso, v.g., o NO é libertado a partir de nitrito. Esta reação é significativa em termos fisiológicos em ambiente acídicos do estômago e da pele. Também se sabe que luz UVA em nitrito pode libertar uma substância com as propriedades fisiológicas de NO [2]. De fato, foi demonstrado que o NO pode ser gerado por decomposição de nitrito induzida por energia proveniente de luz [3; 4].
[007] O NO controla, como parte dos processos inflamatórios da pele, a interação entre os diferentes sistemas de células, inter alia, a proliferação, a diferenciação de células, e, assim, v.g., também a cicatrização de feridas [5]. Nos processos de cicatrização de feridas da pele foram identificados vários genes dominantes regulados por NO [6; 7] e, em consequência, mostraram que a cicatrização de feridas em murganhos deficientes em é um processo significativamente retardado [8]. Outros genes, que estão sob o controlo transcipcional de NO, têm um efeito protetor em genes protetores contra o stresse, tais como proteínas de choque térmico, chaperona e de homoxigenase-1. Uma outra parte de genes regulados por NO é a contra- regulação da resposta inflamatória ou reparação de danos locais (esta inclui, em particular, muitos membros da família as metaloproteinases de matriz (MMP)). O NO pode influenciar a expressão de genes de MMP, mas também dos seus inibidores fisiológicos, inibidores de tecido de proteinases de matriz (TIMP), e também modular a sua atividade por nitrosação e, assim, contrariar uma degradação aumentada de colágeno pelas MMP [9]. Além disso, o NO também afeta a expressão e a atividade de fatores de crescimento, tais como VEGF [37. 38]. Assim, v.g., a angiogénese, para além da síntese de colágeno, componente importante da cicatrização de feridas, pode ser estimulada por doadores de NO [39], em que o NO é capaz de induzir a síntese de fatores VEGF angiogénicos em queratinócitos e macrófagos [5; 40].
[008] Além do mais, foi demonstrado em experiências com doadores de No exógenos que o NO proporciona um aumento significativo da síntese de colágeno em fibroblastos [10; 11]. Um indutor fisiológico importante da síntese de colágeno é o fator-β de crescimento transformante (TGF-β), ao passo que interleucina-1 (IL-1), IL-6, TNF-α e espécies reativas de oxigénio (ROS) poem reduzir significativamente a síntese de colágeno ou mesmo inibi-la [12; 13]. Devido à sua aptidão para reagir com outros radicais e eliminá-los, o NO também pode ter um efeito protetor [14]. Assim, o NO é capaz de proteger contra danos no ADN induzidos por radicais hidroxilo e contra morte celular induzida por H2O2 e apresenta uma capacidade superior para terminar a peroxidação de lípidos induzida por radicais em comparação com a vitamina E [15; 16].
[009] Além disso, foram já descritas outras propriedades protetoras de NO. Assim, o NO, através da proteção contra danos induzidos por hipoxia, efeitos de desdobramento de hepatócitos e neuroprotetores e inativação de caspases efectoras, pode proteger contra apoptose [17]. Além disso, o NO, mesmo em concentrações reduzidas, pode modular componentes importantes da proteção antioxidante, v.g., tais como o metabolismo de glutationa (GSH), através do aumento da expressão de duas enzimas chave envolvidas na indução da síntese de GSH, a Y—glutamil—cisteina—sintetase e a Y-glutamil- transpeptidase [18].
[010] Após a sua formação, o NO difunde-se rapidamente tanto na parede celular como no lúmen dos vasos e está envolvido, v.g., na regulação da adesão de plaquetas e agregação de plaquetas, enrolamentos vasculares, bem como na transmigração de granulócitos e monócitos, e também da permeabilidade endotelial [20]. O NO relaxa também na parede vascular do músculo liso através da ativação de uma guanilato ciclase solúvel, uma enzima chave na regulação da pressão sanguínea. Assim o NO endotelial formado tem uma importância essencial para a manutenção da função vascular e da estrutura vascular, e, assim, afeta significativamente os parâmetros hemodinâmicos, em particular, a pressão sanguínea, mas também estados isquémicos de tecidos [21; 22].
[011] Uma redução na síntese de NO em um modelo animal retardou a neovascularização e a cicatrização de feridas, bem como prejudicou fortemente a re-epitelialização de feridas devido a uma diminuição na taxa de proliferação de queratinócitos. Como transmissor de vasorrelaxamento, o NO pode aumentar o caudal sanguíneo na área da ferida, dando assim origem a um aumento no fornecimento de oxigénio e nutrientes e uma infiltração celular aumentada do tecido [5].
[012] O tratamento tópico de feridas com doadores de NO durante a fase inicial de cicatrização de feridas cutâneas proporciona um fecho de feridas e uma re-epitelialização significativamente acelerados em ratos, bem como uma cicatrização de feridas melhorada em murganhos com antecedentes diabéticos [24]. A exposição tópica diária de feridas a ar-plasma que contém NO melhorou significativamente a cicatrização de feridas, bem como de feridas sépticas e assépticas em um modelo de rato [25]. Apesar das diversas referências a propósito da influência positiva de NO sobre a cicatrização de feridas, apenas um estudo piloto com um paciente masculino com 55 anos de idade foi documento em humanos até à data, no qual o tratamento com NO gasoso proporcionou uma cicatrização completa de uma úlcera venosa no pé resistente a terapia, com vários anos de idade [26]. O NO administrado exogenamente pode atenuar a isquemia/lesões por reperfusão reduzindo as espécies reativas a oxigénio e melhorar significativamente a microcirculação do tecido da pele. Estas propriedades desempenham um papel importante na revitalização de áreas periféricas isentas de abas como parte de revestimentos de tecidos moles [26].
[013] Presentemente, as terapias com NO domiciliares são principalmente dirigidas à cascata de sinalização dependente de cGMP induzida por NO. As abordagens terapêuticas que influenciam diretamente a disponibilidade de NO no corpo são limitadas à utilização de nitritos e nitratos orgânicos [27]. Até à data, o NO gasoso é apenas utilizado por inalação em áreas clínicas no tratamento de diversos distúrbios pulmonares agudos, que tem apresentado, em estudos experimentais, ter também um efeito sistémico através de NOS inalado [28]. O coeficiente de difusão de No a 37°C é 1,4 vezes superior ao de oxigénio e de monóxido de carbono, tendo sido calculada uma via de difusão para a molécula de NO de 500 μm nos tecidos [29].
[014] Ghaffari et al. descreveram efeitos antibacterianos significativos e, assim, a relevância do tratamento com NO gasoso exógeno de feridas infectadas, de queimaduras e de feriadas que não cicatrizam [31; 32], em que as concentrações em NO utilizadas in vitro não apresentaram efeitos tóxicos em fibroblastos, queratinócitos ou células endoteliais humanas [33].
[015] Em resumo, foi aqui demonstrado que o óxido nítrico (NO) é uma molécula bioativa fisiologicamente importante. Através do seu efeito de alargamento de vasos sanguíneos, o qual também ocorre muito rapidamente, o NO possui uma grande importância para o fornecimento de sangue aos órgãos. Além disso, o NO em outros processos fisiológicos desempenha um papel como um neurotransmissor importante. Assim, o NO, enquanto eliminador, protege antes de lesões induzidas por hipoxia e modula componentes importantes da proteção antioxidante. De um modo significativo, o NO controla, em processos inflamatórios da pele, a interação entre diferentes sistemas de células, por exemplo, a proliferação e a diferenciação de células da pele, promovendo assim a cicatrização de feridas.
[016] De igual modo, foi demonstrado em modelos animais, que uma diminuição na taxa de síntese de NO é acompanhada por uma neovascularização e cicatrização de feridas retardadas.
[017] Com base nestas conclusões sobre NO, existem já abordagens para a utilização de NO gasoso para a terapia de distúrbios circulatórios e feridas crônicas. Anteriormente, não tem sido utilizado gás que contém NO a partir de cilindros de gás (gás industrial) para fins terapêuticos, uma vez que o seu armazenamento e manuseamento em hospitais ou instalações de tratamento são complexos devido às medidas de segurança necessárias. Tal é particularmente verdadeiro para um dispositivo móvel. Além disso, a qualidade do gás armazenado para aplicações médicas deverá satisfazer requisitos restritos, fato este que aumenta ainda o peso sobre a produção e sobre o armazenamento. Mesmo uma pequena contaminação do gás pode dar origem à formação de produtos secundários indesejáveis e possivelmente tóxicos. Em consequência, as autoridades de saúde e farmacêuticas europeias têm requisitos elevados sobre a pureza do óxido nítrico que se pretenda utilizar. Para além da utilização de gases NO “técnicos” para utilização médica, existem métodos para a produção química no plasma de óxido nítrico. Estes processos requerem a jusante processos de purificação, por vezes muito complexos, sendo difícil fixar uma concentração óptima de NO para cada fim terapêutico.
[018] Assim sendo, existe ainda necessidade de novos métodos para o tratamento de distúrbios circulatórios e de feridas crônicas.
[019] O objeto da invenção é, assim, proporcionar uma nova abordagem terapêutica para o tratamento de distúrbios circulatórios e de feridas crônicas, o qual apresenta pelo menos uma melhoria em relação às desvantagens apresentadas antes.
[020] Descrição abreviada da invenção
[021] De acordo com a invenção, este objeto é alcançado pelo fato de ser proporcionado um dispositivo de imersão, o qual compreende: a. uma unidade geradora (SGE) de óxido nítrico (NO) para clivagem de NO a partir de precursores de óxido nítrico (NOD), os quais se encontram dissolvidos em um meio solvente como meio de transporte, por meio de clivagem por estímulo físico-químico e b. uma unidade de volume (VE) para a imersão de objetos e, em particular, de seções do tronco, partes do corpo ou corpos completos, que está associada à SGE, e pode acomodar um meio de imersão, tal como um meio de transporte, que é enriquecido com o NO produzido na SGE.
[022] A invenção diz respeito a um aparelho de imersão que apresenta diversas vantagens importantes sobre abordagens terapêuticas conhecidas a partir da técnica anterior.
[023] A separação da unidade geradora de NO da unidade de volume, na qual os objetos podem ser imersos, está associada a uma segurança aumentada. Assim, os precursores de óxido nítricos possivelmente prejudicais ou nocivos podem ser seletivamente mantidos na SGE, sem entrarem em contato com os objetos imersos e apenas o NO é transmitido através da ligação entre a SGE e a VE.
[024] No método vantajoso de geração de NO fotoquímica da presente invenção, o qual funciona, de preferência, por radiação UV, a fonte de UV é assim fácil de blindar e de proteger o utilizador contra a exposição a raios UV nocivos.
[025] Além disso, esta separação também permite que o teor e a pureza de NO no meio de transporte presente no VE seja controlado e regulado, e, em casos extremos, a ligação entre estas duas unidades pode ser completamente interrompida (por exemplo, através de uma válvula de segurança).
[026] Tipicamente, o curto período de vida de NO complica a sua utilização terapêutica. Como dispositivo de acordo com a invenção, é possível manter níveis de NO constantes através de uma pós-síntese contínua de NO, apenas do seu curto período de vida.
[027] Esta capacidade de regular e controlar gera uma vantagem terapêutica decisiva, já que permite uma adequação do tratamento a cada paciente.
[028] A concepção modular também permite a utilização de recipientes de recarga de NOD (v.g., sob a foram de cartuchos), que podem proporcionar uma produção de NO reprodutível e segura.
[029] Através de um simples ajuste da unidade de volume no que diz respeito ao tamanho, forma e material, é possível efetuar diversas aplicações de imersão dependentes de NO diferentes, através da ação sobre itens, tais como ferramentas e instrumentos até ao tratamento terapêutico de organismos humanos e animais, por imersão de qualquer parte do corpo ou do corpo completo.
[030] Visto que a unidade geradora de NO faz parte de um dispositivo de imersão de acordo com a invenção, é possível omitir uma alimentação externa de NO, tal como acontece normalmente com os cilindros de gás.
[031] Tal permite a utilização de um sistema móvel que permite uma aplicação no exterior de instalações médicas ou de clínicas, acompanhada de um tratamento mais eficaz em termos de custos e uma superior aceitação por parte do paciente.
[032] O dispositivo de imersão de acordo com a invenção é um dispositivo de construção simples com componentes convencionais de modo que seja não só barato de produzir, mas também fácil de utilizar com uma taxa de erro reduzida.
[033] Em resumo, a invenção diz respeito a um dispositivo de imersão, uma forma de terapia com base em NO, na qual é possível produzir misturas que contém NO baratas, confiáveis, seguras e individualizadas para o paciente.
[034] Descrição minuciosa da invenção
[035] De acordo com um segundo aspecto, a invenção proporciona um dispositivo de imersão que compreende:
[036] uma unidade geradora de óxido nítrico (NO) (SGE) a partir de meio de radiação UV com uma fonte de radiação UV e uma câmara volumétrica para a imersão de objetos, em particular, seções do tronco, porções de membros ou corpos completos, em que a câmara volumétrica pode conter, como meio de transporte, uma solução de meio, em que o NO é gerado por clivagem de precursores de óxido nítrico (NOD) através radiação UV a partir de uma fonte de radiação UV e o meio de solução é enriquecido com o NO, como meio de imersão.
[037] De acordo com um terceiro aspecto, a invenção proporciona um dispositivo de imersão que contém as seguintes unidades e, em particular, é constituído pelas seguintes unidades: a. uma unidade geradora de óxido nítrico (NO) (SGE) com uma fonte de radiação UV e uma câmara volumétrica para receber um meio de transporte que contém NOD, em que a SGE é concebida de um modo tal que, através de radiação UV, o meio de transporte pode ser enriquecido com NO, b. e uma unidade de volume VE para imersão de objetos, em que o VE pode suportar o meio de transporte enriquecido com NO transferido a partir da SGE.
[038] De acordo com uma variante, a unidade de volume do dispositivo de imersão da invenção é um recipiente aberto no topo. Deste modo, é possível carregar facilmente a unidade de volume com o meio de imersão, como meio de transporte, e com o objeto que se pretende imergir a partir da parte superior na unidade de volume e, assim, imergi-lo no meio de imersão.
[039] De acordo com uma variante preferida, a SGE do dispositivo de imersão pode ser selada de um modo estanque. Desta forma, não existe uma libertação relevante de NO a partir da unidade geradora de NO para o meio ambiente, sendo este seletivamente transferido para o meio de transporte, estando assim completamente disponível para aplicações de imersão (terapêuticas). Esta configuração proporciona uma grande vantagem para a sua utilização terapêutica, visto que o utilizador não é exposto desnecessariamente a NO.
[040] De acordo com uma variante da invenção, o meio de dissolução da SGE é idêntico ao meio de imersão na VE. Deste modo, o meio de solução enriquecido com NO é transferido para a VE e, de um modo preferido, é feito regressar novamente para a SGE, de forma que exista um circuito fechado para este meio. Deste modo, o meio de imersão “utilizado” do circuito é “regenerado” e novamente enriquecido em NO na SGE.
[041] De acordo com uma variante alternativa da invenção, o meio de dissolução da SGE não é o mesmo do meio de imersão da VE. Visto que estes dois compartimentos estão ligados entre si, neste caso é necessário um separador que seja permeável a NO (v.g., uma membrana ou diafragma). Deste modo, é possível adaptar de um modo óptimo a composição destes meios à utilização pretendida, isto é, o meio de dissolução para a produção de NO na SGE e o meio de imersão para a imersão de corpos na VE. Assim, é possível utilizar precursores geradores de óxido nítrico, que seriam irritantes ou mesmo prejudiciais para a pele como parte da solução de imersão para o corpo. Por outro lado, o meio de imersão pode ser preparado com substâncias ou misturas de substâncias que, de outro modo, seriam degradadas por irradicação com UV ou que poderiam interferir ou mesmo evitar a produção de NO na SGE.
[042] De acordo com uma variante, no dispositivo de imersão, a câmara volumétrica da SGE, em comunicação com a unidade de volume (VE), contém um meio de transporte que pode ser dirigido por meio de um dispositivo de circulação ou de uma bomba através da câmara volumétrica da SGE e novamente descarregado na VE.
[043] De acordo com uma variante da invenção, a câmara volumétrica da SGE e a unidade de volume estão ligadas através de um ou mais aberturas na parede comum ou através de uma ou mais condutas, isto é, o meio de transporte pode passar através das aberturas ou condutas da SGE para a VE e depois transportado de volta para a SGE.
[044] De acordo com a invenção, uma conduta pode ser qualquer sistema com o propósito de transportar o meio de transporte líquido, viscoso ou sob a forma de um gel, da invenção. Como exemplos de condutas correspondentes refere-se tubos, tubagens ou canais que são integrados de um modo expediente com o dispositivo de bombeamento.
[045] De preferência, a câmara volumétrica da SGE e a unidade de volume estão associadas através de duas aberturas em uma parede comum ou através de duas condutas.
[046] Adequadamente a câmara volumétrica da SGE e a unidade de volume formam um circuito fechado para o meio de transporte, de modo que o meio de transporte “gasto” na VE possa ser re-enriquecido após novo transporte para a SGE com NO e a concentração desejada em NO seja preparada para um novo transporte para a VE. Este sistema fechado é fácil de garantir por meio de um transporte através de dois orifícios ou de duas condutas.
[047] De acordo com a invenção, tanto o meio de solução como o meio de imersão deverão ser considerados como um meio de transporte.
[048] De acordo com uma variante, o meio de transporte é um meio de suporte orgânico ou inorgânico, líquido, viscoso ou de tipo gel.
[049] De acordo com uma variante preferida, este meio de transporte é uma solução aquosa e, mais preferencialmente, uma solução aquosa tampão.
[050] O meio de dissolução de SGE é caracterizado pelo fato do meio de transporte gasoso, líquido ou gel compreender um ou mais precursores de NO (NOD): catalisadores, detergentes, substâncias tampão, cromóforos, substâncias que estabilizam os NOD, tais como sulfóxido de dimetilo ou etanol, substâncias que aumentam o período de semi-vida de NO, tais como descritas, por exemplo, no documento US 2003/0039697, estabilizadores de NOD, antioxidantes, corantes, indicadores de pH, materiais auxiliares, fragrâncias, substâncias farmacologicamente ativas.
[051] De acordo com uma variante particularmente preferida, o meio de transporte, o meio de solução e/ou o meio de imersão, contém um sistema que degrada ou neutraliza repetidamente óxidos de azoto oxidados, aniões do radical oxigénio, radicais hidroxilo ou “elétrons aquosos”.
[052] De acordo com uma variante específica, este sistema que degrada ou neutraliza repetidamente óxidos de azoto oxidados, aniões do radical oxigénio, radicais hidroxilo ou “elétrons aquosos”, é selecionado entre o conjunto constituído por ácido ascórbico, ascorbato, vitamina E, derivados de vitamina E, tióis, agentes de eliminação e enzimas que degradam espécies de oxigénio ou espécies de azoto.
[053] Em uma solução tamponada como meio de dissolução, o pH está adequadamente compreendido entre 3,0 e 10, de preferência, entre 5,5 e 7,4 e, mais preferencialmente, entre 6,0 e 7,0.
[054] De preferência, o meio de dissolução é uma solução de sal isotónica e, de mais preferencialmente, um soluto salino tamponado isotónico.
[055] De um modo particularmente preferido, o meio de solução aquoso possui a seguinte composição: • sais tampão para ajustar o pH da solução de 6,0 até 7,4 • NOD 50-250 mM • antioxidantes 50-250 mM.
[056] De um modo específico, o meio de solução possui a seguinte composição: • soluto salino tamponado com fosfato (PBS) a pH 6,0 a 7,4 • NOD 100 mM • antioxidantes 150 mM.
[057] De preferência, o PBS na solução possui a seguinte composição: • NaCl 8 g/L • KCl 0,2 g/L • Na2HPO4 1,424 g/L • KH2PO4 0,2 g/L.
[058] De acordo com uma variante alternativa, é utilizada uma solução de sal tamponada com acetato que possui a seguinte composição: • NaCl 8 g/L • KCl 0,2 g/L • mistura de ácido acético e acetato de sódio com uma concentração final de 50-250 mM.
[059] As variantes anteriores também compreendem aplicações em casos especiais, em que o meio de solução é idêntico ao meio de imersão.
[060] Dê preferência, o meio de imersão contém uma ou mais das seguintes substâncias: catalisadores, detergentes, substâncias tampão, cromóforos, substâncias que estabilizam os NOD, tais como sulfóxido de dimetilo ou etanol, substâncias que aumentam o período de semi-vida de NO, tais como descritas, por exemplo, no documento US 2003/0039697, estabilizadores de NOD, antioxidantes, corantes, indicadores de pH, materiais auxiliares, fragrâncias, substâncias farmacologicamente ativas.
[061] Como substâncias que aumentam o período de semi-vida de NO refere-se, por exemplo, as descritas no pedido de patente de invenção norte- americana n° 2003/0039697, cuja descrição se considera aqui totalmente incorporada por referência.
[062] Um especialista na matéria irá escolher as substâncias ou misturas adequadas com base e propósitos específicos e com base nos seus conhecimentos gerais. Neste caso, deverá ter-se em consideração, que no caso de utilização no dispositivo de imersão, as substâncias e misturas deverão ser fisiologicamente toleráveis e/ou dermatologicamente aceitáveis.
[063] De preferência, o meio de imersão está presente sob a forma de uma solução aquosa tamponada.
[064] Em uma solução tamponada como meio de imersão, o pH está adequadamente compreendido entre 3,0 e 10, de preferência, entre 5,5 e 7,4 e, mais preferencialmente, entre 6,0 e 7,0.
[065] Dê preferência, o meio de imersão é uma solução de sal isotónica e, de mais preferencialmente, um soluto salino tamponado isotónico.
[066] De um modo particularmente preferido, o meio de imersão aquoso possui a seguinte composição: • sais tampão para ajustar o pH da solução de 5,0 até 8,0 • NOD 50-250 mM • antioxidantes 50-250 mM.
[067] De um modo particularmente preferido, o meio de imersão aquoso possui a seguinte composição: • sais tampão para ajustar o pH da solução de 6,0 até 7,4 • NOD 50-250 mM • antioxidantes 50-250 mM.
[068] De um modo específico, o meio de imersão possui a seguinte composição: • soluto salino tamponado com fosfato (PBS) a pH 6,0 a 7,4 • NOD 100 mM • antioxidantes 150 mM.
[069] De preferência, o PBS na solução possui a seguinte composição: • NaCl 8 g/L • KCl 0,2 g/L • Na2HPO4 1,424 g/L • KH2PO4 0,2 g/L.
[070] De acordo com uma variante alternativa, é utilizada uma solução de sal tamponada com acetato que possui a seguinte composição: • NaCl 8 g/L • KCl 0,2 g/L • mistura de ácido acético e acetato de sódio com uma concentração final de 50-250 mM.
[071] De acordo com uma variante da invenção, o meio de imersão compreende uma ou mais substâncias farmacologicamente ativas. Estas podem suportar o efeito farmacológico de NO ou atuar de um modo independente de NO de um modo terapeuticamente relevante para a correspondente doença.
[072] De acordo com uma variante da invenção, o meio de imersão compreende uma ou mais das seguintes substâncias farmacologicamente ativas: agentes anti-inflamatórios, tais como fármacos anti-inflamatórios não esteroidais (NSAID) ou corticoesteróides, imunossupressores, antibióticos, anticoagulantes, agentes antitrombóticos, agentes antivirais, agentes antifúngicos, anestésicos locais e analgésicos.
[073] Estas outras substâncias farmacologicamente ativas podem não só fazer parte do meio de imersão em termos de um tratamento em combinação, mas também ser utilizadas antes ou após o processo de imersão.
[074] De acordo com uma variante da invenção, é proporcionado um banho efervescente pelo dispositivo de imersão. Tal pode ser produzido por insuflação de um gás ou por reação química na qual um agente formador de gás, tal como um sal carbonato, é induzido por acidificação da solução para libertar gás CO2.
[075] De acordo com uma outra variante da invenção, é proporcionado um dispositivo de imersão com um dispositivo que reduz a libertação de NO para o meio ambiente ou a previne completamente. Tal pode ser uma separação mecânica, uma cobertura para a unidade de volume, por exemplo, sob a forma de uma tampa ou cobertura, a qual apresenta uma abertura para a parte do corpo imersa. Em alternativa, poderá ser um dispositivo de sucção, que suga o NO libertado a partir do meio de imersão e degrada ou filtra o meio de imersão ou de dissolução que fornece o NO.
[076] De acordo com uma variante preferida, a SGE é um sistema substancialmente fechado, isto é, fechado hermética e completamente para o meio ambiente, que está apenas ligada à unidade de volume. Tal permite garantir que o NO produzido na SGE (de preferência, seletivamente) é transportado para o VE e não libertado para o meio ambiente.
[077] De acordo com outra variante, a SGE é acoplada a um sensor de NO, de modo que com base no valor medido de NO, seja possível ajustar flexivelmente a nível de geração de NO.
[078] Este sensor de NO, que possui um dispositivo de medição para a quantificação de NO, pode ser montado na SGE, na estrutura ou no exterior do dispositivo de imersão. De acordo com uma variante particular, o controlador associado ao sensor de NO garante que quando se excede um valor crítico de NO a SGE cessa a geração de NO por completo.
[079] De acordo com uma variante da invenção, a SGE é conduzida de um modo que, no meio de imersão, o teor em NO seja mantido constante ao longo do período de tratamento.
[080] De acordo com uma variante alternativa da invenção, a SGE é controlada de um modo tal que o teor em NO aumenta ao longo do período de tempo de tratamento, ou diminui.
[081] De acordo com outra variante da invenção, é utilizado o dispositivo de imersão para o tratamento de objetos, dispositivos ou instrumentos. Devido ao efeito de NO nesses bens, estes podem ser limpos ou desinfectados, a carga microbiana pode ser reduzida ou uma biopelícula pode ser reduzida ou removida.
[082] De acordo com uma variante preferida, o dispositivo de imersão é utilizado, neste caso, para a limpeza ou desinfecção de instrumentos médicos ou cirúrgicos.
[083] De acordo com uma variante da invenção, o NO é gerado por meios plasma-químicos. Para além da utilização de gases NO “técnicos” para utilização medicinal, existem métodos para a produção plasma-químicos de óxido nítrico. A partir dos documentos WO 95/07610 A, US 5 396 882 A e DE 198 23 748 A são conhecidos processos para a produção de NO através de meios plasma-químicos, nos quais é gerado NO sob a influência de uma descarga fluorescente, uma descarga com faísca ou uma descarga em arco, em um gás de processo que contém azoto (N2) e oxigénio (O2). A descarga de gás do tipo descrito apresenta, quando efetuada a uma temperatura baixa (conforme observada na descarga fluorescente), uma eficácia reduzida de produção de NO na mistura de gás. Além disso, sob estas condições, é preferencialmente gerado o radical NO2 (NO2^) indesejável para inalação. Para se remover o radical NO2 do gás de inalação, é necessária a utilização de uma técnica de absorção muito cara. Em particular, a desvantagem de um absorvedor reside no fato do material do absorvedor ter de ser frequentemente substituído ou reciclado. A descarga com faíscas ou com arco rica em energia em comparação com a descarga fluorescente produz um aquecimento do gás comparativamente mais forte, sendo assim alcançada uma produção de NO eficaz. No entanto, em particular, a elevada carga térmica através de faíscas sobre os eléctrodos no ponto inicial dá origem a uma desvantajosa erosão forte do eléctrodo, isto é, uma degradação progressiva do material do eléctrodo. Devido a esta erosão do eléctrodo, o processo é bastante intensivo em termos de manutenção, uma vez que os eléctrodos são bastante susceptíveis a desgaste. Por outro lado, deverá ser prevenido que o gás em material de eléctrodo erodido e finamente divido chegue ao paciente. Tal requer um processo de purificação complicado do gás.
[084] O NO também pode ser gerado por clivagem eletrolítica e termolítica de derivados de NO adequadamente lábeis (precursores de NO).
[085] Assim, por exemplo, é possível submeter a clivagem (fotólise) uma solução que contém nitrito (v.g., nitrito de sódio), contendo o ião nitrito (NO2-) por meio de radiação eletromagnética (v.g., radiação UVA com comprimentos de onda de 320 a 440 nm) (fotólise), através da qual é gerado o NO. Sob condições redutoras ou sob um gás inerte (v.g., azoto), é possível efetuar o decaimento de nitrito induzido por radiação eletromagnética através de diferentes canais, parcialmente paralelos e, no entanto, com pesos diferentes sob o ponto de vista termodinâmico. É possível assumir que, no canal 1 (reações 1 a 5), a radiação UVA (com um óptimo a 354-366 nm) clive o nitrito no radical óxido nítrico (NO-) e no anião do radical oxigénio (O--) (equação 1). Este último produto dá início, nas seguintes soluções aquosas, à formação do radical hidroxilo reativo (OH-) (equação 2). O radical hidroxilo reage com nitrito dando origem à formação de radicais dióxido de azoto (NO2-) (equação 3). Tal pode continuar a reagir com óxido nítrico para dar origem a trióxido de diazoto (N2O3) (equação 4). NO2- + hv - NO- + O-- (1) O-- + H2O ’ OH- + OH- (2) NO2- + OH’ ^ NO2’ + OH- (3) NO2’ + NO2’ ^ N2O3 (4) N2O3 + H2O ^ 2NO2- + 2H+ (5).
[086] No canal 2 (equações 6-10), os radicais hidroxilo parecem desempenhar um papel sob estas condições, mas são formados um elétron “aquoso” (e-aq) e um radical dióxido de azoto (equação 6). No caso de nitrito em excesso, o elétron é transferido para este e o anião nitrito resultante (equação 7) é dissolvido em água para se obter um radical NO reduzido (equação 8). As reações seguintes, nas equações (9) e (10) correspondem às das equações (4) e (5). A ponderação entre o canal 1 e o canal 2 corresponde a uma proporção de cerca de 40:60. NO2- + hv ^ NO2’ + e-aq (6) e-aq + NO2- ^ NO2- (7) NO2- + H2O ^ NO’ + 2OH- (8) NO’ + NO2’ ^ N2O3 (9) N2O3 + H2O ^ 2NO2- + 2H+ (10).
[087] Conforme é evidente a partir das reações 1 a 10, a decomposição fotolítica de nitrito é acompanhada por uma produção paralela de espécies químicas reativas e citotóxicas. A partir das reações nas equações (4) e (9), também é possível observar que os radicais NO2 (NO2’) formados na equação (1), podem reagir novamente com NO.
[088] Foi reconhecido (EP1903003A1) que através da utilização de pelo menos um sistema, no qual ocorra a degradação ou neutralização de radicais NO2 ou de espécies de oxigénio durante a geração de ácido nítrico, a formação destes intermediários reativos durante o decaimento de nitrito induzido por luz (NO2-, O’-, OH’, e-aq) é inibida ou eliminada, ao passo que a geração de óxido nítrico não é reduzida. Assim, o rendimento em NO livre disponível e a pureza do gás são aumentados.
[089] O aumento na libertação de NO, bem como o elevado grau de pureza são baseados na eliminação associada à reação de intermediários reativos, por exemplo, de acordo com as seguintes reações (11) a (17). N2O3 + RS- ^ NO2- + RSNO (11) RSNO + hv ^ NO* + RS* (12) NO/ + RS- ^ NO2- + RS* (13) NO* + RS ^ RSNO (14) BA + OH ^ BA-OH (15) VitC + NO2* ^ NO2- + VitC*- (16) Trol + NO2* ^ NO2- + Trol*- (17).
[090] (Abreviaturas: RS-, tiol; RSNO, S-nitroso-tiol, RS*, radical tioílo; BA, ácido benzoico; VitC, vitamina C, ascorbato, ácido ascórbico; VitC*, o radical de VitC; Trol, Trolox; Trol*, o radical de Trolox).
[091] Este método (EP1903003A1) tornado possível pela presença destes ou de outros sistemas funcionalmente equivalentes durante a formação de óxido nítrico, proporcionam um elevado rendimento em óxido nítrico, enquanto, em simultâneo, a formação de óxidos de azoto oxidados (múltiplos) indesejáveis, em particular, NO2*, bem como dos radicais hidroxilo e elétrons aquosos reativos, é eficazmente prevenida ou estas substâncias são eliminadas após a sua formação ou apenas podem ser geradas em quantidades tão pequenas que permanecem em solução e não conseguem passar para a fase gasosa. Assim, estas substâncias não podem causar, v.g., lesões patológicas relevantes, como resultado da inalação dos gases de inalação.
[092] Nos sistemas, que reduzem ou neutralizam espécies de óxido de azoto reativas (v.g., radicais de azoto) ou espécies de oxigénio reativas, são utilizadas, de preferência, substâncias (antioxidantes) que degradam ou neutralizam espécies de oxigénio e espécies de oxigénio reativas (ROS ou RNS). São também preferidos o ácido ascórbico, ascorbato, vitamina E e seus derivados, tióis, outros oxidantes, os agentes de eliminação de radicais livres ou enzimas que degradam ROS e RNS.
[093] São conhecidos pelos especialistas na matéria diversos antioxidantes, os quais deverão ser selecionados de acordo com o meio de transporte respectivo e com o mecanismo para a geração de NO.
[094] Para um meio de transporte lipofílico, tal como um proporcionado por um solvente orgânico, coo antioxidantes é possível referir, por exemplo, tocoferóis, tocotrienóis, tocomonoenóis, butil-hidroxianisole (BHA) e butil- hidroxitolueno (BHT).
[095] Para uma solução de transporte hidrofílica, neste caso, de preferência, soluções aquosas, são particularmente adequados compostos que contêm enxofre, tais como glutationa, cisteína ou ácido tioláctico, ou ácidos orgânicos, tais como ácido ascórbico, ácido alfa-lipóico, ácido hidroxicinâmico, tais como ácido p-coumárico, ácido felúrico, ácido sinapínico ou ácido cafeico, ou ácidos hidroxibenzóicos, tais como ácido gálico, ácido protocatecuico, ácido siríngico e ácido vanílico.
[096] Como outros antioxidantes preferidos refere-se compostos polifenólicos, tais como antocianinas, flavonoides e fitoesterogénios.
[097] Além do mais, concluiu-se que a ligação ou eliminação destes intermediários reativos do decaimento de nitrito induzido por luz (NO2; O2", OH e-aq) também pode ter lugar em um intervalo neutro de pH, em que é possível alcançar a libertação máxima de NO nitrito com uma pureza máxima.
[098] Sob condições acídicas (pH < 7,0) em soluções aquosoas, o decaimento de nitrito “espontâneo” é favorecido. Assim sendo, nas equações 18-20 o anião nitrito (NO2-) está em equilíbrio, em soluções aquosas, com o seu conjugado ácido, o ácido nitroso (HNO2). Por sua vez, o HNO2 está em equilíbrio com trióxido de diazoto (N2O3), que se quebra espontaneamente para se obter NO^ e NO2\ NO2- + H+ θ HNO2 (18) 2 HNO2 θ N2O3 + H20 (19) N2O3 θ NO^ + NO/ (20).
[099] De acordo com uma variante do procedimento descrito (EP1903003A1), a geração de óxido nítrico induzida por UVA é efetuada, de preferência, em um intervalo de pH compreendido entre 0 e 12, em particular, entre 1 e 10, mais particularmente, entre 1,5 e 6, ainda mais particularmente, entre 2 e 6 e, especialmente, entre 2,5 e 4.
[100] O teor em NO no meio de dissolução e/ou meio de imersão está compreendido entre 10 μM e 5 mM, de preferência, entre 50 μM e 2 mM e, mais preferencialmente, entre 100 μM e 200 μM.
[101] Dependendo da concentração utilizada de nitrito ou de antioxidante, bem como da quantidade utilizada de estímulo de descompensação física, que dá origem à desintegração de nitrito, é possível alcançar uma concentração elevada em monóxido de azoto pelo método supramencionado (EP1903003A1).
[102] Em uma solução, a quantidade de monóxido de azoto gerada é controlada pela concentração utilização de agentes libertadores de óxido nítrico e pela indução física e/ou química, que é responsável pela libertação de óxido nítrico a partir dos agentes.
[103] Aqui, a expressão “indução física e/ou química” designa, para além da intensidade de radiação eletromagnética e da duração de exposição que é exposta à solução de reação, também os parâmetros de reação que influenciam a formação de óxido nítrico per se e a concentração de óxido nítrico. De um modo geral, estes incluem o pH da solução de reação, o estado redox da solução de reação, a temperatura da solução de reação, a área exposta à irradiação, o tempo de ação de intensidade de indução sobre os agentes libertadores de óxido nítrico, a remoção da fonte de radiação eletromagnética da solução de reação, o espectro da fonte de radiação eletromagnética, as propriedades de absorção, transmissão e reflexão da solução de reação a concentração de substâncias catalisadoras ou promotoras biológicas ou químicas que também podem ser exteriores às condições físico- químicas “típicas” de uma libertação óptima de NO, tais como substâncias geradoras de NO por catálise ou aceitadores adequados. Em particular, pretende-se designar cromóforos e outras substâncias que com o auxílio, v.g., de radiação eletromagnética para além do intervalo do espectro de UVA podem permitir a libertação de NO a partir dos correspondentes agentes formadores de NO.
[104] Assim, por exemplo, é possível manter a intensidade de indução constante através da utilização de concentrações variáveis de substâncias libertadoras de óxido nítrico de forma a libertar quantidades variáveis de óxido nítrico.
[105] Além disso, para uma concentração constante de substâncias libertadoras de óxido nítrico é possível modificar a libertação de óxido nítrico variando os parâmetros fixados para as respectivas intensidades de indução. Assim, mantendo constante a intensidade de indução, é possível libertar quantidades elevadas de NO e vice-versa através da utilização de concentrações elevadas de substâncias libertadoras de NO. Para uma concentração constante de substância libertadora de NO, a geração de NO pode ser alterada variando os parâmetros das respectivas intensidades de indução. Assim, os parâmetros de ajustamento podem ser utilizados em alternativa ou simultaneamente para a regulação da produção de NO. Em particular, através da regulação simultânea da produção de NO por meio de diversos parâmetros de ajustamento, o método pode ser optimizado vantajosamente em termos de produção de NO e da produção de produtos secundários indesejados.
[106] A substância utilizável para a libertação de óxido nítrico e utilizável no processo de acordo com a invenção não está, em princípio, sujeita a qualquer restrição, desde que esta seja capaz de libertar óxido nítrico sob a influência de radiação eletromagnética. É possível utilizar, por exemplo, substâncias do conjunto constituído por (a) substâncias puras ou misturas que geram óxido nítrico sob a influência de radiação eletromagnética; (b) misturas de substâncias que, para além das substâncias ou misturas referidas na alínea (a), contêm substâncias auxiliares selecionadas entre o conjunto constituído por fotoaceitadores, fotoamplificadores, metais de transição, em particular iões de cobre, enzimas ou catalisadores, que geram óxido nítrico espontaneamente ou através de influência física ou química e (c) substâncias ou misturas selecionadas entre aquelas que são obtidas após uma reação química prévia com o auxílio das substâncias referidas na alínea (a) e, facultativamente, as substâncias auxiliares que geram óxido nítrico sob a influência de radiação eletromagnética, espontaneamente ou sob influência física ou química.
[107] Além disso, as substâncias descritas na alínea (a) podem ainda proporcionar a libertação através de variações de temperatura e/ou alterações na humidade e/ou alterações no pH das suas soluções e/ou alterações no estado redox das suas soluções de óxido nítrico.
[108] De acordo com uma variante preferida da invenção, os precursores de óxido nítrico (NOD) são selecionados entre o conjunto constituído por nitratos orgânicos, nitratos inorgânicos, nitritos, enxofre, compostos nitrosos de azoto ou de oxigénio, compostos NO-metal e substâncias quelantes de NO.
[109] Os precursores de óxido nítrico são conhecidos na especialidade e familiares dos especialistas na matéria. Como exemplos de NOD refere-se diolatos de diazénio (v.g., patentes de invenção norte-americanas nos. 7 105 502; 7 122 529; 6 673 338), trans [RuCl( [15]anoN4)NO]+2, ligando de nitrosilo, 6-nitrobenzo [a]pirol, S-nitroso-glutationa, S-nitroso-tiol, derivados de nitroanilina (ver documento US 2013/0224083), 2-metil-2-nitrosopropano, derivados de imidazoílo, hidroxilnitrosamina, hidroxilamina e hidroxiureia.
[110] De acordo com uma variante da invenção, o meio de imersão e/ou o meio de dissolução pode ser utilizado por meio de um recipiente de recarga. Neste caso, o meio formulado acabado é introduzido por meio do encaixe para recipientes no dispositivo de imersão, garantindo-se assim pelo fabricante uma formulação pré-definida que é a formulação terapêutica óptima.
[111] De acordo com outra variante, os ingredientes do meio de imersão e/ou do meio de dissolução são adicionados ao meio em uma forma pré- fracionada preferida (designada por embalagem). Visto que a geração de NO de acordo com a invenção é possível com água corrente, o utilizador é capaz de misturar a tal água corrente os ingredientes, os quais incluem, por exemplo, agentes de tamponamento, sais, NOD e antioxidantes, de modo a obter um meio de dissolução ou de imersão preparado no momento.
[112] Na forma pré-fracionada, os ingredientes encontram-se, de preferência, na forma sólida. Assim, podem ser apresentados sob a forma de pó, poeira, grânulo, comprimido, comprimido revestido, drageia, cápsula de gelatina mole, cápsula de gelatina dura, oblongo, pílula, comprimido ou pílula efervescente, em que a unidade embalada contém uma quantidade suficiente para um tratamento.
[113] De acordo com uma variante preferida, os ingredientes encontram- se sob a forma de um comprimido efervescente. Nesta forma, são dissolvidos rapidamente e também enriquecem o meio com um gás inerte adequado (v.g., CO2). Esta forma de dosagem também é utilizada no campo de aplicações para banho de utilizadores bem conhecidas, com uma enorme aceitação.
[114] Em alternativa, os ingredientes podem encontrar-se sob á forma de um líquido ou semi-sólido. As formas semi-sólidas incluem, por exemplo, suspensões, emulsões, pastas, cremes, unguentos, geles ou loções. O pré- fraccionamento como unidade embalada pode ser garantido, por exemplo, pela embalagem em frascos, garrafas, saquetas ou tubos.
[115] De acordo com outra variante preferida, a unidade de embalagem é concebida de um modo tal que a sua forma permita a aplicação correta no dispositivo de imersão. Assim, de um modo preferido, a forma é configurada como um cartucho, que é fixável apenas em uma orientação no dispositivo de imersão. Além disso, tal cartucho pode ser configurado com um mecanismo de bloqueamento, que no dispositivo de imersão liberta os ingredientes do modo desejado apenas após a fixação correta. De um modo conveniente, o dispositivo de imersão neste caso é equipado com um sensor que detecta uma orientação ou fixação incorreta do cartucho, indicando tal informação ao utilizador.
[116] De acordo com outro aspecto, a invenção proporciona um estojo que compreende uma unidade embalada para um tratamento, em que a referida unidade embalada contém um NOD sob a forma de um pó, líquido ou gel, agentes de tamponamento, antixodantes e, facultativamente, solventes.
[117] A libertação pode ser efetuada a partir de soluções aquosas de nitrito ou de S-nitrosotióis. Neste caso, por razões práticas, é preferida a utilização de uma solução aquosa de nitrito de sódio ou de S-nitrosotióis como fonte de NO. A solução aquosa pode ter uma concentração em precursores de NO compreendida, de preferência, entre 0,001 e 10000 mM, em particular, entre 0,2 e 6000 mM, mais preferencialmente, entre 0,3 e 5000 mM, ainda mais preferencialmente, entre 0,4 e 2000 mM e, muito mais preferencialmente, entre 0,5 e 1500 mM.
[118] De acordo com outra variante, a solução aquosa, como meio de imersão e/ou de dissolução, possui uma concentração em precursores de NO compreendida entre 1 μM e 5000 mM, de preferência, entre 100 μM e 2000 mM, mais preferencialmente, entre 500 μM e 500 mM e, ainda mais preferencialmente, entre 1 mM e 150 mM.
[119] O tipo de radiação utilizável para substratos geradores de NO é conhecido pelos especialistas na matéria. É possível utilizar qualquer radiação eletromagnética que seja capaz de decompor derivados de NO fotolabéis para formar monóxido de azoto. Por exemplo, na presente invenção, está incluída a produção de óxido nítrico por meio de clivagem fotolítica utilizando uma radiação de UVA com comprimentos de onda, por exemplo, de 320-440 nm. No entanto também é possível utilizar uma radiação eletromagnética de outro qualquer comprimento de onda, por si só ou com o auxílio de métodos químicos, físicos, ou biológicos, que induza diretamente ou que induza, facilite ou catalise a clivagem de precursores de NO (derivados de NO) geradores de NO.
[120] A produção de óxido nítrico também pode ter lugar em soluções que estejam saturadas com gases inertes. Em tais soluções saturadas com gases inertes (azoto (N2), hélio (H2), árgon, etc.) o NO aí dissolvido apresente um período de vida muito mais longo e pode permanecer em solução mesmo em concentrações mais elevadas. De um modo geral, é assumido que a solubilidade máxima de NO em soluções aquosas é de cerca de 2 mM. Neste contexto, o termo soluções aquosas, deverá ser entendido como designando um meio de cultura ou meio de infusão, tampões, soro, sangue, geles e quaisquer outras substâncias capazes de absorver gases.
[121] O óxido nítrico produzido por fotólise de precursores de NO fotolábeis pode ser utilizado, por exemplo, para fins de inalação. Como áreas de aplicação mais específicas refere-se o estímulo do metabolismo de tecidos por aplicação externa, a modificação estrutural de superfícies orgânicas e inorgânicas, a esterilização ou a criação de citotoxicidade. O óxido nítrico gerado por fotólise também pode ser utilizado para a fumigação de feridas, em particular, para a cicatrização de feridas de feridas crônicas não cicatrizantes possivelmente infectadas com bactérias. O óxido nítrico, quando produzido em lípidos saturados, também pode ser utilizado para tratar hipertensão sistémica. Por último, o óxido nítrico também pode ser gerado em veículos nitrosados com óxido nítrico que libertam o NO espontaneamente. O óxido nítrico também pode ser utilizado para a produção de diferentes substâncias de ligação a NO (v.g., doadores de NO).
[122] A qualidade do gás armazenado ou introduzido em soluções para aplicações médicas tem de satisfazer requisitos bastante restritos. Uma ligeira contaminação do gás dá origem à formação de produtos secundários indesejáveis e possivelmente tóxicos. A formação destes produtos secundários em botijas de gás que contêm óxido nítrico durante armazenamentos prolongados, bem como na produção à escala do plasma de óxido nítrico, e a remoção destes radicais constitui um problema técnico importante e uma desvantagem financeira. As vantagens do processo fotolítico para a preparação de soluções que contêm óxido nítrico são a simplicidade do método de produção de gás que contém NO, do grau particularmente elevado de pureza da mistura gasosa de NO, de ser muito económico e não apresentar custos de armazenamento, do manuseamento particularmente simples da produção de NO e do controlo de pureza, da proporção incomparavelmente favorável de custos de produção do gás NO produzido.
[123] Dispositivo da invenção
[124] O NO para utilização externa pode ser aplicado sob a forma de gás ou plasma que contém NO, bem como sob a forma de um dador de NO de decaimento espontâneo ou induzido. A presente invenção diz respeito a um dispositivo de imersão médico que é capaz, em um meio de dissolução, v.g., tal como uma solução de imersão, clivar precursores de óxido nítrico dissolvidos através de estímulos físico-químicos e o óxido nítrico assim produzido enriquecer o meio de solução, v.g., a solução de imersão, de modo que o dispositivo e a solução de imersão possam ser utilizadas para suportar terapias médicas em animais e em humanos, bem como o enriquecimento de diferentes meios com NO.
[125] De acordo com uma variante da invenção, o dispositivo de imersão é utilizado para o tratamento de doenças. Neste caso, de um modo expediente, seções do tronco, seções do corpo ou a totalidade do corpo são imersos no meio de imersão que contém NO.
[126] A invenção diz respeito a um dispositivo de imersão que pode ser utilizado não só para o tratamento de doenças crônicas ou agudas, mas também para a possível prevenção de tais doenças. Salvo quando indicado de outro modo, o termo “terapia” ou “tratamento” designa todas as medidas para mitigar, curar ou prevenir doenças relevantes.
[127] Neste caso, os estímulos físicos referidos para a clivagem de precursores de NO podem ser o pH, eletricidade, calor ou radiação eletromagnética, isto é, estímulos que são capazes de clivar os precursores de NO pH-lábeis, electro-lábeis, termo-lábeis ou foto-lábeis adequados, de um modo dependente do pH, electroliticamente, por electrólise ou fotólise, para libertar NO.
[128] Devido ao comportamento limitado em solução de NO, é possível gerar concentrações fisiologicamente relevantes de No nas correspondentes soluções, embora inferiores aquelas que podem causar problemas de saúde para os humanos. Além disso, é possível alcançar um tratamento com NO muito mais preciso por contato directo da superfície do corpo humano com as soluções que contêm NO, tais como, v.g., com misturas gasosas que contêm NO ou doadores de NO que se decompõem espontaneamente. Além do mais, a possibilidade do dispositivo ser utilizado de um modo dependente da carga com o precursor de NO adequado por diferentes utilizadores finais, desde amadores até profissionais, constitui uma vantagem essencial do dispositivo da invenção em relação a outras técnicas com base em NO.
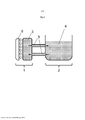
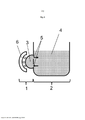
[129] O dispositivo da invenção é constituído por um recipiente para receber um volume (doravante designado por VE = unidade de volume) do meio de dissolução ou meio de imersão, por exemplo, solução de banho, e uma outra unidade técnica (doravante referida como SGE = unidade geradora de óxido nítrico) que gera óxido nítrico no meio de dissolução, enriquecendo assim o meio de dissolução de VE com NO.
[130] No entanto, existe ainda a possibilidade da SGE não gerar diretamente o NO para o meio de dissolução de VE, mas para uma solução diferente, a qual é então misturada com o meio de dissolução de VE na diluição desejada. Como alternativa, uma mistura gasosa que contém NO gerada da SGE, ou uma mistura de gás que contém NO fornecida a partir de uma botija de gás, pode ser introduzida no meio de dissolução de VE e assim enriquecer com NO o meio de dissolução de VE, tal como uma solução de imersão.
[131] Em tal solução de imersão enriquecida com NO, para fins terapêuticos, é possível imergir um local do corpo. Estes podem ser partes do corpo no tronco ou extremidades de humanos ou de animais. Dependendo da aplicação desejada, a VE pode ter um volume de 0,001 litros a 1000 litros e mais, é possível tratar pequenas porções do tronco e extremidades e imergir a totalidade do corpo; um tal tratamento pode demorar desde alguns segundos até várias horas.
[132] De acordo com uma variante preferida da invenção, o corpo, ou a parte do corpo, que se pretende tratar é imerso no meio de imersão durante 5 a 30 minutos, de preferência, de 7,5 minutos a 20 minutos e, mais preferencialmente, de 10 minutos a 15 minutos.
[133] De preferência, tal banho é utilizado diversas vezes ao dia e, mais preferencialmente, 2 a 3 vezes ao dia.
[134] Para se controlar a duração do tratamento, o dispositivo de imersão pode incluir, de preferência, uma unidade de tempo, a qual desliga a geração de NO de acordo com um tempo permanentemente prescrito ou programável flexível.
[135] Além do mais, o meio de imersão pode conter um corante que sofra uma alteração na cor decorrido um determinado período de tempo, de forma que o utilizador seja informado do final do período de tratamento.
[136] Além do mais, o dispositivo de imersão também pode incluir um dispositivo para a medição do fluxo sanguíneo, que permite um controlo particularmente bom do sucesso da terapia com base na duração do tratamento e/ou na intensidade de tratamento. São do conhecimento dos especialistas na matéria vários dispositivos para a medição do fluxo sanguíneo. Como exemplos é possível referir tacómetros vasculares ou o microsensor descrito no documento WO 97/46853. Este sensor compreende uma inserção permeável a um indicador, que é montada em uma abertura de um recipiente indicador, que é formada por um recipiente, em que a inserção forma uma porção de parede permeável do recipiente.
[137] Como parâmetro de substituição para a circulação sanguínea é possível utilizar outros parâmetros de medição vasculares, tais como a vermelhidão da pele ou a temperatura da pele, para os quais são conhecidos métodos e dispositivos de medição correspondentes a partir da técnica anterior.
[138] A SGE gera o óxido nítrico para o enriquecimento, v.g., de soluções de imersão, por clivagem induzida por pH, eletrolítica, termólise ou qualquer outra clivagem induzida fisicamente, mas preferencialmente por clivagem fotolítica de precursores de óxido nítrico. Neste caso, a SGE pode ser um componente integrante do dispositivo completo ou um componente firmemente ligado à VE. Em alternativa, a SGE também pode ser uma unidade independente, externa, não ligada à VE.
[139] Uma característica essencial da SGE reside no fato dela própria ter o seu próprio volume, o qual está ligado ao volume da VE, e no fato do volume da SGE poder ser transportado com todo o seu conteúdo possível ao estímulo físico adequado para gerar NO a partir de precursores químicos de NO. No entanto, em alternativa, a SGE também pode ser utilizada para gerar misturas gasosas que contêm NO introduzidas a partir do exterior para a produção de soluções enriquecidas em NO, v.g., soluções de imersão.
[140] A seguir, a título de exemplo, irá ser descrita uma variante particular do dispositivo da invenção de radiação eletromagnética como estímulo físico relevante para a clivagem de precursores químicos de NO.
[141] A radiação eletromagnética pode ser emitida a partir de uma fonte de luz, a qual pode ser montada no exterior e/ou no interior da unidade SG. É importante que o fluxo de luz do conteúdo da SGE em conjunto com as substâncias libertadoras de óxido nítrico, para o propósito de um decaimento do material induzido ou libertação de óxido nítrico, esteja no máximo. Assim, a fonte de radiação eletromagnética pode ser revestida com os fluorocrómos incandescentes ou com uma lâmpada de descarga de gás adequados (descarga sob pressão reduzida ou pressão elevada), um díodo emissor de luz (LED), um díodo emissor de luz orgânico (OLED), LASER ou qualquer fonte de radiação eletromagnética utilizável que seja capaz de gerar NO a partir de precursores químicos ou substratos correspondentes.
[142] Para um óptimo processamento dos precursores de NO fotolábeis dissolvidos na solução de imersão, a fonte de luz pode irradiar o volume de SGE com radiação eletromagnética com comprimentos de onda compreendidos entre 100 e 2000 nm, ou com radiação eletromagnética que emita em um outro qualquer comprimento de onda, por si só ou com o auxílio de métodos químicos, físicos ou biológicos, de modo a induzir a clivagem de precursores de óxido nítrico e, assim, libertar o óxido nítrico.
[143] Dê preferência, caso a SGE seja construída a partir de um material que não afete as propriedades para uma libertação óptima de óxido nítrico, então é possível gerar ou optimizar a energia necessária de uma fonte de radiação eletromagnética, ou, devido às suas características, criar ou optimizar as propriedades de luz necessárias para a libertação de óxido nítrico induzida por luz, ou, no caso da geração de NO dependente de pH, promover ou optimizar o decaimento de nitrido induzido por pH.
[144] De acordo com a invenção, a câmara volumétrica da SGE contém um meio de transporte com precursores de óxido nítrico (NOD) e também um dispositivo para a geração de NO a partir de pelo menos um NOD.
[145] Tal pode ser um dispositivo para a adição de ácido à câmara volumétrica, na qual é então gerado NO induzido por pH.
[146] De acordo com uma variante preferida, a SGE é proporcionada com uma fonte de radiação UV, que gera NO através de decaimento fotolítico através de radiação UV diretamente no meio de transporte. Tal possui a vantagem do meio de transporte poder estar em um compartimento fechado e, adicionalmente, a geração de NO poder proceder de um modo controlado e reprodutível.
[147] Dê preferência, o meio de transporte na SGE é iluminado em um recipiente plano pela fonte de radiação para gerar NO.
[148] Assim, para a clivagem fotolítica é adequado um recipiente com uma espessura de camada de 1-20 mm, de preferência, entre 2,5 e 10 mm e, mais preferencialmente, entre 5 e 7,8 mm. Concluiu-se que utilizando uma espessura de camada adequadamente dimensionada, através de uma utilização óptima da radiação UV, é possível obter um elevado rendimento em NO.
[149] Assim sendo, o material do recipiente para radiação UV é permeável. Com base nos conhecimentos sobre a transmitância de UV, um especialista na matéria será capaz de escolher os materiais adequados para o recipiente que contém o meio de transporte. Quando se utiliza uma radiação no intervalo de UVA (315 a 380 nm) é possível utilizar o vidro sodocálcico mais convencional, para uma radiação de energia superior até 290 é possível utilizar vidros de boro-silicato e para uma radiação UV inferior a 290 nm é adequado um vidro de quartzo.
[150] Além disso, como material para o recipiente, também é possível utilizar plásticos transparentes a UV, tais como polimetilpenteno (PMP), metacrilato de polimetilo modificado (PMMA), polivinil-butiral modificado (Trosivol UV+®).
[151] De um modo preferido, o recipiente é formado de modo que possua uma distância definida constante da sua superfície voltada para a fonte de radiação. Em uma fonte de radiação tubular, o recipiente é moldado em conformidade com um cilindro oco, no centro do qual o tubo é posicionado. Neste caso, o meio de transporte é vantajosamente alimentado em uma extremidade do cilindro, flui ao longo do comprimento do cilindro passando pela fonte de radiação UV, onde é enriquecido de um modo crescente com NO, e é removido na outra extremidade do cilindro para ser fornecido à VE.
[152] Em alternativa, o recipiente também pode ser um tubo que é formado sob a forma de uma espiral com um diâmetro interno definido, em que a fonte de UV tubular é montada no centro da espiral. Esta montagem permite um aumento gradual da concentração em NO, em que o rendimento em NO pode ser aqui controlado, com uma intensidade de radiação constante, pelo caudal.
[153] De acordo com uma variante alternativa, quando é utilizada uma fonte de radiação do tipo folha (por exemplo, um painel LED), o recipiente é montado com uma forma de caixa tipo folha. De preferência, neste caso, existem entradas e saída diametricamente opostas para o meio de transporte e podem conter internamente partições, que podem controlar o fluxo do meio de transporte de um modo adequado.
[154] De acordo com outra variante, o recipiente do lado oposto à fonte de radiação possui um revestimento refletor de UV. Assim, a eficácia da radiação pode ser ainda aumentada por meio da luz UV refletida, que pode passar novamente através do meio de transporte, sendo assim possível gerar NO fotoliticamente. São do conhecimento dos especialistas na matéria as correspondentes camada refletoras de UV, tais como camadas de alumínio ou dielétricas. De acordo com uma variante alternativa, o revestimento refletor de UV não está ligado ao próprio recipiente, mas em separado, v.g., a uma parede interna da SGE.
[155] De acordo com uma variante, a geração fotolítica de NO é efetuada antes do tratamento, sendo necessário um período máximo de 30 minutos, de preferência, entre 10 e 15 minutos, mais preferencialmente, inferior a 10 minutos, para se atingir a concentração em NO terapeuticamente necessária.
[156] Para o propósito de enriquecer com NO a solução de banho contida na VE, as soluções de banho da VE podem ser passadas através do volume da SGE, sendo aí expostas radiação eletromagnética emitida a partir da fonte de luz na SGE e novamente introduzidas no volume principal de VE do dispositivo. Tal tem lugar entre a VE e a SGE, sendo o movimento do volume efetuado através de uma unidade de bombeamento, em que o dispositivo de circulação pode ser um componente de SGE ou de VE ou pode atuar totalmente como um componente externo ao dispositivo.
[157] Os dispositivos de bombeamento ou de circulação são do conhecimento dos especialistas na matéria a partir da técnica anterior e estes podem selecionar o dispositivo correto com base nos parâmetros relevantes, tais como a viscosidade do meio de transporte, a potência de bomba necessária, o volume de VE e de SGE.
[158] Como dispositivos de bombeamento que é possível considerar refere-se, por exemplo: bombas peristálticas, bombas de diafragma, bombas de pistão, bombas acopladas magneticamente e bombas propulsoras.
[159] O dispositivo de imersão é adequadamente fornecido com um dispositivo para o controlo de temperatura. Este permite o aquecimento e/ou arrefecimento por meio da fixação de uma temperatura selecionada. A temperatura é um dos parâmetros que determinam o rendimento em NO e a solubilidade do NO gerado. Além disso, a temperatura do banho pode ser ajustada para um valor de temperatura de banho óptimo para utilização terapêutica. Tal pode ser uma temperatura agradável para o utilizador de 23°C- 28°C ou uma temperatura compreendida entre 5°C e 15°C, que faz aumentar a circulação na pele.
[160] O especialista na matéria conhece dispositivos para o controlo de temperatura a partir da técnica anterior e pode escolher o dispositivo correto com base em parâmetros relevantes, tais como o volume de líquido e o aquecimento e arrefecimento.
[161] De acordo com uma variante preferida, é necessário um dispositivo de controlo de temperatura em combinação com uma fonte de radiação (UV), uma vez que tal proporciona um aquecimento do meio de transporte qualquer sobreaquecimento do meio deverá neste caso ser corrigido por meio de arrefecimento intenso ou prolongado para que a radiação seja ativa.
[162] De acordo com outra variante, a fonte de radiação eletromagnética atua não só como parte da geração de NO, mas também como fonte de aquecimento para um dispositivo de temperatura.
[163] Como parte central do dispositivo da invenção, a SGE é um sistema aberto ou um sistema estanquemente selado. A SGE é caracterizada pelo fato de estar mecanicamente fixada ao dispositivo completo ou estar fracamente ligada a este e ser facilmente substituível, de modo que seja apenas utilizada no dispositivo global antes da utilização do mesmo.
[164] Uma outra característica da SGE do dispositivo de acordo com a invenção reside no fato de ser possível utilizar na SGE um recipiente de enchimento intercambiável ou substituível (v.g., recipiente de permuta, inserções, cartuchos, almofadas, etc.; doravante referidos como FB = distribuidores), de preferência, é possível utilizar substâncias potencialmente armazenadoras de NO e substâncias potencialmente libertadoras de NO (v.g., nitratos orgânicos ou inorgânicos, nitritos, compostos S-, N- ou O-nitrosos, agentes quelantes de NO), quimicamente estáveis ou estabilizados, por si sós ou em várias combinações, que podem libertar NO em uma forma pura ou dissolvido em vários solventes, através de uma reação, catalisada ou não catalisada, iniciada de um modo físico e/ou químico e/ou enzimático na SGE, com ou sem uma bomba de circulação, direta ou indiretamente no volume da solução de banho de VE.
[165] De preferência, diz respeito a um recipiente de enchimento substituível que pode ser inserido na SGE e/ou na VE sob a forma de um cartucho. De um modo adequado, este cartucho contém uma composição que compreende NOD sob a forma de um pó, líquido ou gel, substâncias tampão, antioxidantes e, facultativamente, um solvente.
[166] A vantagem da utilização de tais FB substituíveis ou interpermutáveis reside no fato de através do enchimento de um FB com os agentes reativos em várias combinações e concentrações, ser possível geral padrões de libertação de NO, em diferentes comprimentos e concentrações na SGE, característicos, utilizáveis e específicos para tratamento, em soluções de banho. Assim, é possível alcançar um padrão de libertação ou concentração deliberado de NO escolhendo um FB especificamente carregado e inserido na SGE, o que permite adaptar as soluções de banho às capacidades técnicas e responsáveis do utilizador final para uma optimização da aplicação. No que diz respeito ao enchimento de FB, são selecionadas quantidades de precursores de NO (v.g., como nitrito ou S-nitrosotióis) que, após dissolução da substância na solução de banho, proporcionem concentrações finais compreendidas entre 0,001 e 10000 mm, em particular, entre 0,01 e 6000 mM, mais preferencialmente, entre 0,1 e 5000 mM, ainda mais preferencialmente, entre 0,4 e 2000 mM e, muito mais preferencialmente, entre 0,5 e 1500 mM.
[167] De preferência, a produção de NO na SGE do dispositivo de acordo com a invenção é controlada por meio da manipulação de vários parâmetros de ajustamento. Aqui, como parâmetros de ajustamento são considerados a concentração utilizada, os agentes libertadores de NO, a intensidade da radiação eletromagnética e as propriedades de outras variáveis de indução físicas e/ou químicas, que sejam responsáveis pela libertação de NO a partir dos agentes. Além do mais, como variáveis potenciais de indução de libertação de NO a partir de substâncias geradoras de NO, individualmente ou em várias combinações, é possível variar e utilizar os seguintes parâmetros: - o valor de pH, - o estado redox (presença de substâncias redutoras ou oxidantes), - a temperatura, - fluxo de corrente e/ou voltagem, - pressão envolvente, - intensidade da radiação eletromagnética e duração de exposição que a solução de banho é exposta na SGE, - área exposta a radiação, - tempo de exposição a indução dos agentes libertadores de NO, caudal da solução de banho através da SGE, - remoção da fonte de radiação eletromagnética da solução de reação, - espectro da fonte de radiação eletromagnética, - características de absorção, transmissão e reflexão da solução de banho, - ou concentração de catalisadores ou mediadores químicos ou biológicos, condições físico-químicas exteriores “típicas” para uma libertação óptima de NO a partir de substâncias geradoras de NO por catálise ou aceitadores correspondentes (por exemplo, por meio de cromóforos e outras substâncias, com o auxílio, v.g., de radiação eletromagnética fora do intervalo do espectro UVA, que poderá está disponível a partir de agentes formadores de NO correspondentes para facilitar a libertação de NO).
[168] No que diz respeito ao último ponto referido, faz-se observar que, em particular na presença de metais de transição, tais como, Cu2+, as soluções aquosas de nitrito são capazes de absorver luz a comprimentos de onda substancialmente mais longos do que soluções puras de nitrito, e, assim, o ião nitrito pode ser clivado libertando NO a comprimentos de onda de 400-450 nm e mesmo a outros comprimentos de onda > 450 nm. Além disso, também é verdade que devido a uma ligação relativamente fraca entre NO e o resto da molécula, os compostos químicos nitrosados em S e N também podem ser clivados fotoliticamente por radiação eletromagnética > 400 nm e libertar NO.
[169] No entanto, o dispositivo de acordo com a invenção pode ser construído, em alternativa, de um modo tal que a SGE com as características referidas seja dispensada, sendo os meios físico-químicos necessários para a geração de NO, v.g., a fonte de luz com as propriedades mencionadas, uma parte integral da VE, em que as soluções de banho que contêm NO são geradas diretamente na VE, não sendo assim necessário um volume irradiado na SGE. Por exemplo, o decaimento fotolítico proporcionado pela fonte de radiação pode assim ser exterior à VE e/ou pode ser montado na VE, de modo que o fluxo de radiação de VE em conjunto com as substâncias de libertação de óxido nítrico com o propósito de um de decaimento de material induzido ou libertação de óxido nítrico esteja em um valor máximo ou óptimo para a aplicação desejada. O ajuste de VE com derivados de NO fotolábeis, quer diretamente por sua adição à solução de banho quer a partir da sua libertação a partir de FB associado à VE.
[170] Além disso, as emissões associadas à fonte de radiação de VE, de preferência, radiação eletromagnética com comprimentos de onda de 100 a 2000 nm, ou radiação eletromagnética com outros comprimentos de onda, pode induzir, por si só ou com o auxílio de métodos químicos, físicos ou biológicos, a clivagem de precursores de óxido nítrico, induzindo assim a libertação de óxido nítrico.
[171] Este é constituído por um material que não afete as propriedades para uma libertação óptima de óxido nítrico, então é possível gerar ou optimizar a energia necessária de uma fonte de radiação eletromagnética, ou, devido às suas características, criar ou optimizar as propriedades de luz necessárias para a libertação de óxido nítrico induzida por luz, ou, no caso da geração de NO dependente de pH, promover ou optimizar o decaimento de nitrido induzido por pH. Através do enchimento da VE com um recipiente de enchimento substituível ou intercambiável (FB), que pode ser carregado com agentes em várias combinações e concentrações, a VE pode gerar um padrão de libertação de NO em soluções de imersão com características diferentes em termos de comprimento e concentração e uma utilização e tratamentos específicos. Assim, o padrão de não libertação nas soluções de imersão permitem escolher um FB substituível ou permutável carregado especificamente, sendo possível a sua inserção na VE, para uma optimização e adaptação por responsabilidade técnica e competência do utilizador final.
[172] Por razões práticas, na embalagem, como fonte de nitrito, é preferida uma solução aquosa com concentrações compreendidas, de preferência, entre 0,001 e 10000 mM, em particular, entre 0,01 e 6000 mM, mais particularmente, entre 0,1 e 5000 mM, em particular, entre 0,4 e 2000 mM e, ainda mais particularmente, entre 0,5 e 1500 mM.
[173] De acordo com uma variante alternativa, a fonte de nitrito na solução aquosa de VE possui uma concentração compreendida, de preferência, entre 100 μM e 5000 mM, mais preferencialmente, entre 500 μM e 100 mM e, ainda mais preferencialmente, entre 1 mM e 10 mM.
[174] Também por razões práticas, na VE, também é possível utilizar, de preferência, uma solução aquosa com várias substâncias ou misturas de substâncias da família de compostos nitrosos (R-NO), com concentrações compreendidas, de preferência, entre 0,001 e 10000 mM, em particular, entre 0,01 e 6000 mM, mais preferencialmente, entre 0,1 e 5000 mM, ainda mais preferencialmente, entre 0,4 e 2000 mM e, muito mais preferencialmente, entre 0,5 e 1500 mM.
[175] De acordo com uma variante alternativa, as substâncias ou misturas de substâncias da família química dos compostos nitrosos (R-NO) na solução aquosa de VE possuem, de preferência, uma concentração compreendida entre 100 μM e 5000 mM, mais preferencialmente, entre 500 μM e 2000 mM e, ainda mais preferencialmente, entre 10 mM e 500 mM.
[176] Para o propósito da produção de NO induzida fotoliticamente, na VE, dependendo da concentração desejada ou necessária de gás NO dissolvido na solução de imersão e dependendo da duração desejada ou necessária do respectivo teor em NO da solução de imersão, as substâncias sólidas geradoras de NO podem ser utilizadas em uma quantidade específica ou em soluções com sais nitrito, ou as substâncias geradores de NO supramencionadas podem ser utilizadas nas concentrações desejadas ou pretendidas.
[177] De preferência, a produção de NO na VE pode ser controlada por manipulação de parâmetros de ajustamento técnicos, químicos e físicos. Como parâmetros de ajustamento, é possível referir a concentração utilizada, os agentes libertadores de NO, a intensidade da radiação eletromagnética e as características de outras variáveis de indução físicas e/ou químicas, que são responsáveis pela libertação de NO a partir de agentes. Os parâmetros podem variar e ser utilizados individualmente ou em combinação com forças de indução da libertação de NO a partir de substâncias potencialmente geradoras de NO, v.g., o pH da solução de imersão, o estado redox da solução de imersão (presença de substâncias redutoras ou oxidantes), a temperatura da solução de imersão, a intensidade da radiação eletromagmética e o tempo de exposição que é exposta a solução de imersão na VE, a área exposta de radiação, o tempo de atuação de forças de indução sobre os agentes libertadores de NO, o caudal da solução de imersão na VE, a remoção da fonte de radiação eletromagnética da solução de imersão, o espectro da fonte de radiação eletromagnética, as características de absorção, transmissão, reflexão da solução de imersão, a concentração em substâncias catalisadoras ou promotoras biológicas ou químicas que também podem permitir para além das condições físico-químicas “típicas” a libertação óptima de NO através de catalisadores ou de aceitadores correspondentes (v.g., com o auxílio de cromóforos e outras substâncias, v.g., também com o auxílio de radiação eletromagnética fora do espectro de UVA, em uma posição que possa permitir a libertação de NO a partir de agentes formadores de NO correspondentes).
[178] No que diz respeito às variáveis de controlo referidas antes, as substâncias libertadoras de óxido nítrico podem ser produzidas com quantidades variáveis de azoto e dissolvidas na solução de imersão do dispositivo da invenção, em que a força de indução é mantida constante através da utilização de concentrações variáveis. Por outro lado, mantendo constante a concentração de substâncias libertadoras de óxido nítrico, é possível alterar a libertação de óxido nítrico na solução de imersão variando os parâmetros de ajustamento da força de indução.
[179] Sabe-se que o NO pode ser dissolvido em soluções aquosas até uma concentração de cerca de 2 mM, antes de conseguir escapar da solução para o ar envolvente. Para aumentar a concentração da solução e/ou o período de vida de NO nas soluções aquosas de imersão e para aumentar a solubilidade de NO na solução de imersão, as soluções de imersão são saturadas, antes ou durante a utilização, com gases inertes, v.g., azoto (N2), hélio (He) ou árgon (Ar). Para este fim, o dispositivo da invenção pode ainda incluir um aparelho integrado ou externo através do qual a solução de imersão é conduzida e, se necessário, é misturada, enriquecida e/ou saturada com um gás inerte.
[180] Assim sendo, de acordo com uma variante da invenção, o meio de transporte irá ser enriquecido com gases inertes e, de preferência, com azoto, hélio ou árgon.
[181] De acordo com uma variante preferida, a concentração de NO no meio de transporte é determinada pela solubilidade máxima de NO. Tal significa que o NO está presente totalmente como NO dissolvido e não como NO libertado, v.g., ocorre como bolhas de gás NO. Para além da contaminação desnecessária do ambiente pela libertação de gás NO, também foi demonstrado que o NO gasoso é fracamente dissolvido novamente no meio de transporte.
[182] Em um meio aquoso, a solubilidade máxima de NO está compreendida, dependendo da temperatura, do valor de pH e de outros componentes, entre 0,2 mM e 5 mM.
[183] Neste ponto, faz-se notar que, como meio de transporte para a dissolução de NO do dispositivo de acordo com a invenção, não é forçosamente necessário utilizar uma solução aquosa, sendo possível utilizar outro qualquer meio de transporte orgânico ou inorgânico, líquido, viscoso e gelatinoso, que seja capaz de guardar o NO transportá-lo para dissolução e libertá-lo.
[184] As soluções de imersão que contêm NO geradas utilizando o dispositivo da invenção aqui descrito, devido ao papel fisiológico de NO para estimular o metabolismo de tecidos, são utilizadas por administração tópica na área de dermatologia para o tratamento de feridas cirúrgicas ou acidentais, feridas crônicas infectadas com bactérias e/ou de lenta cicatrização e para o tratamento de distúrbios dermatológicos do conjunto de doenças inflamatórias, imunologicamente controladas ou doenças autoimunes. Como exemplos de aplicações possíveis refere-se: • estímulo do metabolismo de tecidos por utilização externa em humanos e animais; • tratamentos de pés e feridas diabéticos; • tratamento de dor neuropática em diabetes e noutras doenças; • tratamento de varizes; • tratamento de isquemia superficial ou profunda local ou doenças trombopáticas de tecidos; • inflamação aguda e crónica da pele; • alergias de pele; • infecções parasíticas da pele; • dermatite atópica, em particular, neurodermatite; • dermatomitose; • pemphigus vulgaris e/ou outas infecções locais e sistémicas e/ou situações inflamatórias agudas e crônicas, • feridas, tais como úlcera neuropática diabética crónica; • Ulcus cruris; • úlceras por pressão; • feridas infectadas com cicatrização secundária; • feridas de cicatrização primária não inflamadas, tais como, em particular, fendas ablativas ou escoriações; • transplantes (pelo), • tratamento de dor diabética das extremidades inferiores (pés ou pernas) e • tratamento de tecidos com fraca perfusão.
[185] De acordo com um outro aspecto, a invenção proporciona um método para o tratamento de um paciente, o qual compreende os passos que consistem em: a. gerar um meio de transporte enriquecido em NO através do dispositivo de imersão da invenção e b. submergir seções do tronco, extremidades do corpo ou o corpo completo do paciente no meio de transporte do dispositivo de imersão.
[186] De acordo com uma variante preferida, o tratamento com este processo é selecionado entre o conjunto constituído por: • estímulo do metabolismo de tecidos por utilização externa em humanos e animais; • tratamento de feridas cirúrgicas ou acidentais; • tratamento de feridas crônicas não cicatrizantes ou de fraca cicatrização; • tratamento de feridas infectadas com bactérias e/ou fungos; • tratamento de doenças dermatológicas sob a forma de um conjunto de doenças inflamatórias, controladas imunologicamente ou autoimunes; • tratamentos de pés e feridas diabéticos; • tratamento de dor neuropática; • tratamento de varizes; • tratamento de isquemia superficial ou profunda local ou doenças trombopáticas de tecidos; • tratamento de inflamação aguda e crónica da pele; • tratamento de alergias de pele; • tratamento de infecções parasíticas da pele; • tratamento de dermatite atópica, em particular, neurodermatite, dermatomitose e pemphigus vulgaris; • tratamento de feridas, tais como úlcera neuropática diabética crónica, Ulcus cruris, úlceras por pressão; • tratamento de áreas grandes do corpo para o tratamento de doenças sistémicas, tais como pressão sanguínea elevada (hipertensão) e distúrbios hemodinâmicos associados; • tratamento de pacientes com transplantes (pele); • tratamento de dor diabética das extremidades inferiores (pés ou pernas) e • tratamento de tecidos com fraca perfusão.
[187] De acordo com uma variante preferida, o método é aplicado para o tratamento de feridas crônicas dos membros inferiores de pacientes diabéticos.
[188] Adequadamente, o método da invenção é caracterizado pelo fato do tratamento por imersão do corpo completo, de uma porção do corpo ou de uma porção de um membro, ter uma duração de alguns segundos a várias horas.
[189] De preferência, de acordo com o método, o tratamento é efetuado por imersão do corpo completo, de uma porção do corpo ou de uma extremidade do corpo, no meio de transporte, durante 5 a 30 minutos, de preferência, 7,5 a 20 minutos e, mais preferencialmente, 10 a 15 minutos.
[190] De acordo com uma variante particularmente preferida, o dispositivo da invenção é utilizado para o tratamento por imersão de feridas crônicas dos membros inferiores e, em particular, de diabéticos. Neste caso, o risco de ocorrência de feridas crônicas, bem como do número de amputações médicas, é reduzido por meio de tratamento em um sentido profiláctico. A redução de dor neuropática na perna e produção de um ambiente de cicatrização de feridas melhorado está associado a uma melhoria notória na qualidade de vida do paciente. Além do mais, através da redução dos cuidados com a ferida, é esperado uma redução significativa nos custos de tratamento.
[191] De acordo com uma variante da invenção, o dispositivo de imersão é utilizado para o tratamento de feridas com fraca cicatrização. Os distúrbios de fluxo sanguíneo arterial deficiente e/ou refluxo venoso são causas significativas no desenvolvimento e cronicidade de feridas dos membros inferiores. Uma vasodilatação arterial induzida por NO, melhora a circulação sanguínea dos tecidos afetados e, através do efeito anti-trombogênico de NO, o retorno venoso de sangue é significativamente melhorado e facilitado. A melhoria dependente de NO de ambos os parâmetros hemodinâmicos proporciona o aspecto decisivo de terapia relevante de um efeito local e sistémico que reduz significativamente o risco de desenvolvimento de escaras ou acelera significativamente a sua cura. Os meios do dispositivo de imersão através do meio de transporte (meio de imersão) que fornecem NO ao longo do corpo, às extremidades do corpo ou a partes do corpo que se pretende tratar, podem assim ser utilizados com sucesso para o tratamento de feridas com cicatrização fraca.
[192] De acordo com uma variante particular, o dispositivo de imersão da invenção pode ser utilizado para o tratamento de dor diabética nas extremidades inferiores tais como os pés e/ou pernas. A dor diabética constitui um evento muito comum no curso da diabetes. A dor no pé/perna diabética é o resultado de níveis elevados de glicose no sangue prolongados, que constitui a causa principal para danos nervosos e vasculares observados na diabetes. Uma vasodilatação arterial induzida por NO, melhora circulação sanguínea dos tecidos afetados e ajuda a transmissão de dor no sentido de uma influência anestésica. Assim sendo, é possível utilizar com sucesso o NO fornecido pelo meio de transporte (meio de imersão) a partir do exterior do pé e/ou perna para o tratamento de dor diabética no pé/perna.
[193] De acordo com uma variante específica da invenção, o dispositivo de imersão da invenção pode ser utilizado para o tratamento de pacientes com transplantes (pele) e, neste caso em particular, para o tratamento de tecidos com fraca perfusão. Ambas as variáveis hemodinâmicas referidas antes, a circulação arterial e o retorno venoso, constituem parâmetros essenciais para o sucesso terapêutico de tecidos transportados cirurgicamente. Tal como referido pelas técnicas de cirurgia plástica, os tecidos transportados operados são removidos da pele e/ou de um tecido (dispensáveis) de um local do mesmo indivíduo e são transportados para a nova localização desejada. Normalmente, são utilizados tecidos puros de pele, no entanto, são transplantados quaisquer tecidos, com ou sem pele, tanto com pedículo (isto é, com os seus vasos sanguíneos fornecedores e nervos associados) como livres (isto é, com ligação de vasos sanguíneos no fornecimento de sangue ao novo ambiente). Aceitação funcional do tecido transplantado é exclusivamente dependente do fornecimento de sangue arterial e de uma saída regulada de sangue venoso. Uma vasodilatação arterial induzida por NO, melhora a circulação sanguínea e, assim, o necessário fornecimento para cirurgia de tecidos, e, através do efeito anti-trombogênico de NO, o fluxo de saída ou retorno de sangue venoso é encorajado ou facilitado. Assim sendo, os suplementos de NO utilizados externamente podem ser seguros e promover o sucesso de uma cirurgia de transplante de tecidos com base na opção de tratamento.
[194] Além disso, pode ser possível o tratamento de partes do corpo maiores e doenças sistémicas, tais como distúrbios dirigidos a uma pressão sanguínea elevada (hipertensão) e distúrbios hemodinâmicos associados.
[195] Além do mais, o dispositivo da invenção também pode ser utilizado para produzir líquidos saturados em NO que podem ser utilizados sistemicamente, v.g., para o tratamento de pressão sanguínea elevada, para fazer veículos nitrosados que libertam espontaneamente NO e, v.g., podem ser utilizados topicamente no contexto de terapias dermatológicas, para a produção de várias substâncias de ligação a NO (v.g., como doadores de NO).
[196] Assim, para o dispositivo da invenção como veículo, meio de ligação ou meio de transporte para o NO também podem servir líquidos, geles ou sólidos. Com o gás NO, é concebível a utilização de líquidos saturados, tais como tampões, soluções, meios, soro ou sangue, como meio de transporte, e aplicá-los, v.g., em terapia, sendo introduzidos local ou sistemicamente na corrente sanguínea ou como meio visco saturado em NO, tal como geles atópicos, para utilização no tratamento de feridas.
[197] Para propósitos de tratamento, as áreas ou objetos a tratar são imersas na solução de banho durante um período de tratamento adequado, o qual poderá durar entre alguns segundos e várias horas. Com o objetivo de uma melhor mistura da solução de banho, o dispositivo da invenção pode ter um dispositivo de circulação, o qual pode ser integrado no dispositivo global ou ligado externamente. De preferência, o processo de imersão é efetuado em um recipiente aberto no topo, em que a abertura no topo pode, em alternativa, ser selada por um vedante ou uma tampa, sendo, no entanto, possível a inserção de um objeto através do vedante.
[198] Para reduzir, evitar ou prevenir uma contaminação potencial do ar envolvente com NO ou com os seus produtos de reação oxidativa, a presente variante de VE aberta no topo proporciona um dispositivo que gera, sobre a solução de banho, um fluxo de ar ligeiro permanente com sucção permanente, e o qual se faz passar através de um filtro de carvão ativado, ou através de qualquer outro dispositivo que seja capaz de neutralizar ou eliminar as correspondentes espécies gasosas reativas. Segundo esta ideia, uma variante de VE vedada no topo é equipada com um dispositivo que suga permanentemente o volume de gás por cima da solução de banho e o faz passar para o exterior através de um filtro de carvão ativado ou através de outro dispositivo. Assim, é garantida uma inativação permanente de espécies de óxido de azoto reativas. O espaço proporcionado para o filtro de carvão ativado, ou um correspondente dispositivo de diferente tipo técnico, pode ser uma unidade substituível e renovável da VE. Para garantir uma utilização segura do dispositivo de acordo com a invenção, este possui um programa de seleção específico da aplicação e controlado eletronicamente, incluindo o fecho por segurança da unidade, através de sensores de NO, NO2, temperatura e segurança correspondentes e de um controlo remoto, bem como conectividade a dispositivos de controlo externo e dispositivos de documentação. Para uma gestão segura, também inclui uma detecção específica para a aplicação e específica para o utilizador e controlada eletronicamente de dispositivos de enchimento intercambiável ou substituível carregado (FB), circulação e filtração.
[199] De acordo com um aspecto particular, a invenção proporciona as seguintes variantes.
[200] Variante 1: um dispositivo para a imersão de objetos, caracterizado pelo fato de no dispositivo ser possível enriquecer com óxido nítrico (NO) um meio adequado para a imersão de objetos (meio de imersão) através de clivagem química, induzida por um estímulo físico, de precursores de óxido nítrico (doravante referidos como NOD = derivados de NO) e utilizado para fins médicos e industriais.
[201] Variante 2: um dispositivo de acordo com a variante 1, caracterizado pelo fato do dispositivo ter uma unidade de volume (VE) receptora do meio de imersão que está associada a uma unidade geradora (SGE) de óxido nítrico (NO), que serve para enriquecer com NO o meio de imersão da VE.
[202] Variante 3: dispositivo de acordo com a variante 1 e 2, caracterizado pelo fato da SGE poder manter qualquer conteúdo, o qual comunica com o volume da VE, em que o conteúdo de VE, o qual é, de preferência, uma solução aquosa, mas também pode ser qualquer meio de transporte orgânico ou inorgânico, líquido viscoso ou de tipo gel ou sólido, que seja capaz de dissolver precursores de NO ou se ligar a NO e armazenar e mesmo libertar, é dirigido por meio de um dispositivo de circulação ou bomba através da câmara volumétrica da SGE e novamente descarregada na câmara volumétrica de VE.
[203] Variante 4: dispositivo de acordo com as variantes 1 a 3, caracterizado pelo fato de o conteúdo volumétrico da SGE poder ser exposto a um estímulo eletrolítico e/ou termolítico e/ou eletromagnético e/ou qualquer outros estímulo físico ou químico, mas, de preferência, a luz emitida a partir de uma fonte de radiação eletromagnética, em que a fonte de radiação pode ser revestida com fluorocrómos incandescentes adequados ou com uma lâmpada de descarga de gás adequada (descarga de pressão reduzida ou de pressão elevada), um díodo emissor de luz (LED), um díodo emissor de luz orgânico (OLED), um laser ou qualquer outra fonte de radiação eletromagnética que seja capaz de, na ausência de catálise de precursores ou substratos químicos relevantes, por si só ou com o auxílio de processos químicos ou físicos ou como parte de uma reação catalisada, v.g., por iões e metais de transição, tais como iões de Cu2+, promover a divisão de NOD, induzindo assim a libertação de NO.
[204] Variante 5: um dispositivo de acordo com as variantes 1 a 4, caracterizado pelo fato de os NOD (por exemplo, nitratos orgânicos e inorgânicos, nitritos, compostos nitrosos de enxofre, azoto ou oxigénio, compostos NO-metal, agentes quelantes de NO, etc.), necessários para a produção de NO por clivagem, serem fornecidos em um meio de volume da VE através de um dispositivo de circulação ou bomba da SGE ou, em alternativa, ser utilizado na SGE um cartucho ou recipiente de enchimento removível ou substituível (doravante designado = AFB recipiente de enchimento substituível) que contém NOD e outras substâncias em qualquer concentração e combinação que possa libertar NO na SGE, que em uma forma gasosa ou em uma forma dissolvida possa ser introduzido no volume da VE que contém o meio de imersão, sendo possível geral padrões de libertação de NO, em diferentes comprimentos e concentrações na SGE, característicos, utilizáveis e específicos para tratamento, no meio de imersão.
[205] Variante 6: dispositivo de acordo com as variantes 1 a 5, caracterizado pelo fato de o meio de transporte pode ser saturado com o NO dissolvido através de uma parte do dispositivo adicional antes da utilização ou durante a utilização, com gases inertes não reativos com NO, tais coo azoto (N2), hélio (He), árgon (Ar), para assim aumentar a solubilidade do meio de solução para o NO formado e aumentar o período de vida do NO dissolvido no meio de dissolução.
[206] Variante 7: um dispositivo de acordo com as variantes 1 a 6, caracterizado pelo fato de o aparelho ter uma gestão de segurança autónoma, controlada eletronicamente, em que 1) envolve um programa de seleção específico da aplicação controlada eletronicamente e uma opção de desligar de segurança, 2) a produção de NO é, de preferência, baseada na manipulação de parâmetros de ajustamento técnicos, químicos e físicos relevantes de percepção sensorial da temperatura, pressão, concentração de NO, concentração de dióxido de azoto (NO2), e outros e outros parâmetros de segurança relevantes, 3.) a aplicação e utilizador e detecção controlada eletronicamente e utilização da aceitação de AFB com enchimento específico intercambiável e, possivelmente, um dispositivo de circulação ou bomba, e 3) inclui uma detecção controlada eletronicamente e utilização de aceitação de um dispositivo integrado e substituível no dispositivo de filtragem para a eliminação de gases potencialmente prejudiciais para a saúde.
[207] Variante 8: um dispositivo de acordo com as variantes 1 a 7, caracterizado pelo fato de o dispositivo ter a possibilidade de controlo remoto e conectividade a dispositivos de controlo externo e documentação ou aplicações de controlo.
[208] Variante 9: um aparelho de acordo com as variantes 1 a 8, caracterizado pelo fato de poder ser utilizado para estimular o metabolismo de tecidos por utilização externa em humanos e animais, na área de dermatologia e cirurgia para o tratamento de feridas cirúrgicas e acidentais, de feridas crônicas sem cicatrização ou com fraca cicatrização e/ou infectadas com bactérias e/ou fungos, poder ser utilizado para o tratamento de condições dermatológicas do conjunto de doenças inflamatórias, controladas imunologicamente ou autoimunes, tal como para o tratamento de feridas diabéticas nos pés e pernas, dor neuropática em diabetes e outras doenças, varizes, isquemia superficial e profunda local e doenças trombopáticas de tecidos, inflamação aguda e crónica da pele, alergias da pele, infecções de pele parasíticas, dermatite atópica, em particular, neurodermite, dermatomiosite, pemphigus vulgaris e/ou outras infecções locais e sistémicas e/ou condições inflamatórias agudas e crônicas, transplantes (pele), defeitos em feridas, tais coo úlceras neuropáticas diabéticas crônicas, úlceras da perna, úlceras por pressão, feridas infectadas de cicatrização secundária, feridas de cicatrização primária não inflamadas, em particular fendas ablativas ou escoriações, mas também para o tratamento de áreas maiores do corpo, para o tratamento de doenças sistémicas, tais como pressão sanguínea elevada (hipertensão) e doenças hemodinâmicas associadas, em que um tratamento pode ter a duração de alguns segundos a várias horas.
[209] EXEMPLOS
[210] 1. Produção de NO através do dispositivo da invenção
[211] Unidade geradora de óxido nítrico que contém água corrente, sais tampão (NaCl 8 g/L + KCl 0,2 g/L + Na2HPO4 1,424 g/L + KH2PO4 0,.2 g/L, pH = 7,0), NaNO2 1,45 mM e Na-ascorbato 10 mM.
[212] Formou-se uma solução por irradiação UV da solução que continha nitrito, cerca de 150 μM de NO. A partir desta solução, analisou-se a estabilidade dos NO gerados e a aparência dos produtos de oxidação. Além disso, testou-se o efeito quando utilizada como banho para pés no que diz respeito à circulação e a eritema.
[213] 1.1 Teste de estabilidade
[214] Em primeiro lugar, submeteu-se esta solução a um teste de estabilidade, isto é, determinou-se o teor como alterações em NO ao longo de um período de 20 minutos. A cada 2 minutos, retirou-se com uma pipeta uma alíquota de 10 mL da solução de banho para um gás hélio (100 mL/min) passando através do pistão (capacidade de 175 mL), já carregado com 40 mL de uma solução de PBS (pH 7,4). Durante a totalidade do procedimento, o material evasivo do frasco da mistura de gás hélio foram levadas diretamente para um analisador de NO (detector de quimiluminescência - CLD 822 Sr Eco Physics, Duernten, Suíça) e foi detectada e registada a quantidade de NO presente na mistura gasosa em p.p.m. (partes por milhão) (ver também, Oplander et al, 2010 Nitric oxide-Bio Ch 23: 275-283). Os resultados da medição são apresentados na figura 1A. Concluiu-se que o teor em NO ao longo do período de 20 minutos foi praticamente constante, embora não estatisticamente significativo por cerca de 10%.
[215] 1.2 Geração de produtos de oxidação
[216] Com base na solução descrita antes, detectou-se em paralelo com a detecção de NO referida antes e durante a mesma medição, a quantidade de radicais de dióxido de azoto, enquanto produto de oxidação principal de NO. Este ocorreu apenas decorrido 10 minutos em concentrações muito reduzidas de NO2 na ordem de 1,5 p.p.m., que aumentaram apenas ligeiramente até ao valor máximo de 20 minutos. Os valores medidos NO2 não foram significativamente superiores à linha de referência (ver figura 1 B).
[217] 1.3 Utilização como banho para os pés
[218] Na solução descrita antes (27°C) que contém uma quantidade constante de NO, pés de voluntários foram imersos, e foram mantidos neste banho para pés durante 10 minutos. Durante o banho para pés, a solução foi agitada suavemente através de um ligeiro movimento do pé submerso. Analisou-se o pé durante estes 10 minutos de intervalo de exposição e durante os 15 minutos subsequentes para fluxo sanguíneo na pele, em uma profundidade de tecidos de 1-2 mm e 6-8 mm. Além disso, o pé foi examinado quando a eritemas.
[219] 1.3.1. Fluxo sanguíneo dérmico
[220] Para ambas as profundidades, observou-se um aumento significativo no fluxo sanguíneo aio longo da exposição durante 10 minutos ao banho de pés com NO (ver figura 2A e 2B) e depois um regresso para os níveis de controlo ao longo de um período de 10 a 15 minutos. O aumento na circulação sanguínea, podem pode ser observado à vista desarmada pela formação de um eritema temporário (ver FIG. 3).
[221] FIGURAS
[222] A invenção será agora explicada por referência às figuras, as quais não são limitativas do âmbito da invenção.
[223] Figura 1A: resultado de uma medição de estabilidade de uma solução aquosa tamponada que contém NO do exemplo 1 ao longo de um período de 20 minutos. É apresentada a proporção em percentagem (%) com base no ter o original em NO.
[224] Fig. 1B: é apresentado o resultado de uma análise do produto de oxidação NO2- em uma solução aquosa tamponada que contém NO do exemplo 1 ao longo de um período de 20 minutos, o teor em NO2- é apresentado em partes por milhão (p.p.m.).
[225] Fig. 2: determinação da circulação sanguínea durante uma exposição de 10 minutos por imersão de um pé em um banho para pés que contém NO e um subsequente período de 15 minutos (ver exemplo 1). É apresentada a proporção relativa de fluxo sanguíneo em uma unidade arbitrária (unidade arbitrária; AU), tanto para uma profundidade de tecido de 1 a 2 mm (A) como para uma profundidade de tecido de 6 a 8 mm (B). Neste caso, foi medida a distância em uma solução tamponada que contém NO (quadrados brancos) ou como controlo em uma solução tampão adequada (diamantes pretos) e foi registado não invasivamente o fluxo sanguíneo utilizando uma sonda e o sistema de detecção espectroscópico 02C-Doppler (LEA Medizintechnik GmbH, Giessen, Alemanha) nos pontos de tempo indicados.
[226] Fig. 3: detecção do fluxo sanguíneo aumentado após 10 minutos de exposição de um pé a um banho de pés que contém NO por meio de eritema (temporário). Na foto é claramente visível que o pé está bastante vermelho na área submersa devido a um fluxo sanguíneo aumentado.
[227] Fig. 4: representação esquemática de um dispositivo de imersão em uma seção transversal com a unidade geradora de óxido nítrico (SGE) (1) e a unidade de volume (VE) (2), que estão ligadas entre si por meio de duas condutas de ligação (5). O recipiente aberto no topo contém um meio de imersão (4) para a imersão dos objetos. A SGE compreende uma câmara volumétrica com um meio de transporte (3) que é irradiado por uma fonte de radiação (6).
[228] Fig. 5: representação esquemática de um dispositivo de imersão em uma seção transversal com a unidade geradora de óxido nítrico (SGE) (1) e a unidade de volume (VE) (2), a SGE está ligada diretamente à VE e a ligação entre estes compartimentos (5) é feita por dois orifícios. O recipiente aberto no topo contém um meio de imersão (4) para a imersão dos objetos. A SGE compreende uma câmara volumétrica com um meio de transporte (3) que é irradiado por uma fonte de radiação (6) (6).
[229] Fig. 6: representação esquemática de um dispositivo de imersão em uma seção transversal conforme observado a partir de cima com a unidade geradora de óxido nítrico (SGE) (1) e a unidade de volume (VE) (2), a SGE e a VE estão dispostas em um recipiente circular e a SGE como um segmento exterior de VE é separada. A ligação de SGE com VE é efetuada por dois orifícios (5). A VE, como região interior do recipiente circular, está carregada com o meio de imersão (4) para a imersão de objetos. O meio de transporte presente na câmara volumétrica (3) é irradiado por uma fonte de radiação UV externa curva (6).
[230] LITERATURA [1] K.D. Kroncke, K. Fehsei, and V. Kolb-Bachofen, Inducible nitric oxide synthase in human diseases. Clin Exp Immunol 113 (1998) 147-56. [2] K. Matsunaga, and R.F. Furchgott, Responses of rabbit aorta to nitric oxide and Superoxide generated by ultraviolet Irradiation of solutions containing inorganic nitrite. J Pharmacol Exp Ther 259 (1991 ) 1140-6. [3] M. Fischer, and P. Warneck, Photodecomposition of nitrite and undissociated nitrous acid in aqueous Solution. J.Phys.Chem. 100 (1996) 18749-18756. [4] H. Strehlow, and I. Wagner, Flash photolysis in aqueous nitrite Solutions. Z. Phys. Chem. NF 132 (1982) 151-160. [5] S. Frank, H. Kampfer, C. Wetzler, and J. Pfeilschifter, Nitric oxide drives skin repair: novel functions of an established mediator. Kidney Int 61 (2002) 882-8. [6] S. Frank, B. Stallmeyer, H. Kampfer, N. Kolb, and J. Pfeilschifter, Nitric oxide triggers enhanced induction of vascular endothelial growth fator expression in cultured keratinocytes (HaCaT) and during cutaneous wound repair. Faseb J 13 (1999) 2002-14. [7] S. Frank, H. Kampfer, M. Podda, R. Kaufmann, and J. Pfeilschifter, Identification of copper/zinc Superoxide dismutase as a nitric oxide- regulated gene in human (HaCaT) keratinocytes: implications for keratinocyte proliferation. Biochem J 346 Pt 3 (2000) 719-28. [8] K. Yamasaki, H.D. Edington, C. McCIosky, E. Tzeng, A. Lizonova, I. Kovesdi, D.L. Steed, and T.R. Billiar, Reversal of impaired wound repair in iNOS-deficient mice by topical adenoviral-mediated iNOS gene transfer. J Clin Invest 101 (1998) 967-71 . [9] J. Pfeilschifter, W. Eberhardt, and A. Huwiler, Nitric oxide and mechanisms of redox signalling: matrix and matrix-metabolizing enzymes as prime nitric oxide targets. Eur J Pharmacol 429 (2001 ) 279-86. [10] Y. Ishii, T. Ogura, M. Tatemichi, H. Fujisawa, F. Otsuka, and H. Esumi, Induction of matrix metalloproteinase gene transcription by nitric oxide and mechanisms of MMP-1 gene induction in human melanoma cell lines. Int J Cancer 103 (2003) 161-8. [11] M.B. Witte, F.J. Thornton, D.T. Efron, and A. Barbul, Enhancement of fibroblast collagen synthesis by nitric oxide. Nitric Oxide 4 (2000) 572-82. [12] F. Verrecchia, and A. Mauviel, TGF-beta and TNF-alpha: antagonistic cytokines Controlling type I collagen gene expression. Cell Signal 16 (2004) 873-80. [13] D.A. Siwik, and W.S. Colucci, Regulation of matrix metalloproteinases by cytokines and reactive oxygen/nitrogen species in the myocardium. Heart Fail Rev 9 (2004) 43-51 . [14] V.M. Darley-Usmar, R.P. Patel, V.B. O'Donnell, and B.A. Freeman, Antioxidant actions of nitric oxide. in: L.J. Ignarro, (Ed.), Nitric Oxide: Biology and Pathobiology, Academic Press, San Diego, 2000, pp. 265-276. [15] S.P. Goss, B. Kalyanaraman, and N. Hogg, Antioxidant effects of nitric oxide and nitric oxide donor Compounds on low-density lipoprotein oxidation. Methods Enzymol 301 (1999) 444-53. [16] D.A. Wink, J.A. Cook, R. Pacelli, J. Liebmann, M.C. Krishna, and J.B. Mitchell, Nitric oxide (NO) protects against cellular damage by reactive oxygen species. Toxicol Lett 82-83 (1995) 221-6. [17] B. Brüne, A. von Knethen, and K.B. Sandau, Nitric oxide (NO): an effector of apoptosis. Cell Death Differ 6 (1999) 969-75. [18] D. Moellering, J. McAndrew, R.P. Patel, T. Cornwell, T. Lincoln, X. Cao, J.L. Messina, H J. Forman, H. Jo, and V.M. Darley-Usmar, Nitric oxide-dependent induction of glutathione synthesis through increased expression of gamma-glutamylcysteine synthetase. Arch Biochem Biophys 358 (1998) 74-82. [19] U. Forstermann, M. Nakane, W.R. Tracey, and J.S. Pollock, Isoforms of nitric oxide synthase: functions in the cardiovascular system. Eur Heart J 14 Suppl I (1993) 10-5. [20] P. He, M. Zeng, and F.E. Curry, Effect of nitric oxide synthase Inhibitors on basal microvessel permeability and endothelial cell [Ca2+]i. Am J Physiol 273 (1997) H747-55. [21] M. Toborek, and S. Kaiser, Endothelial cell functions. Relationship to atherogenesis. Basic Res Cardiol 94 (1999) 295-314. [22] M. Keim, and B. Strauer, Endotheliale Dysfunktion; Therapeutische und prognostische Relevanz. Internist. 40 (1999) 1300-1307. [23] T.P. Amadeu, A.B. Seabra, M.G. de Oliveira, and A.M. Costa, S- nitrosoglutathione- containing hydrogel accelerates rat cutaneous wound repair. J Eur Acad Dermatol Venereol 21 (2007) 629-37. [24] R. Weller, and M.J. Finnen, The effects of topical treatment with acidified nitrite on wound healing in normal and diabetic mice. Nitric Oxide 15 (2006) 395-9. [25] A.B. Shekhter, V.A. Serezhenkov, T.G. Rudenko, A.V. Pekshev, and A.F. Vanin, Beneficial effect of gaseous nitric oxide on the healing of skin wounds. Nitric Oxide 12 (2005) 210-9. [26] W.S. McDonald, T.P. Lo, Jr., M. Thurmond, C. Jones, R. Cohen, A. Miller, and D. Beasley, Role of nitric oxide in skin flap delay. Plast Reconstr Surg 1 13 (2004) 927-31. [27] C. Beige, P.B. Massion, M. Pelat, and J.L. Balligand, Nitric oxide and the heart: update on new paradigms. Ann N Y Acad Sei 1047 (2005) 17382. [28] B. Gaston, Summary: systemic effects of inhaled nitric oxide. Proc Am Thorac Soc 3 (2006) 170-2. [29] T.M. Dawson, and S.H. Snyder, Gases as biological messengers: nitric oxide and carbon monoxide in the brain. J Neurosci 14 (1994) 5147-59. [30] C.C. Miller, M.K. Miller, A. Ghaffari, and B. Kunimoto, Treatment of chronic nonhealing leg ulceration with gaseous nitric oxide: a case study. J Cutan Med Surg 8 (2004) 233-8. [31] ] A. Ghaffari, D.H . Neil, A. Ardakani, J. Road, A. Ghahary, and C.C. Miller, A direct nitric oxide gas delivery system for bacterial and mammalian cell cultures. Nitric Oxide 12 (2005) 129-40. [32] A. Ghaffari, C.C. Miller, B. McMullin, and A. Ghahary, Potential application of gaseous nitric oxide as a topical antimicrobial agent. Nitric Oxide 14 (2006) 21-9. [33] A. Ghaffari, R. Jalili, M. Ghaffari, C. Miller, and A. Ghahary, Efficacy of gaseous nitric oxide in the treatment of skin and soft tissue infections. Wound Repair Regen 15 (2007) 368-77. [34] Z.S. Galis, and J.J. Khatri, Matrix metalloproteinases in vascular remodeling and atherogenesis: the good, the bad, and the ugly. Circ Res 90 (2002) 251-62. [35] S.C. Tyagi, and M.R. Hayden, Role of nitric oxide in matrix remodeling in diabetes and heart failure. Heart Fail Rev 8 (2003) 23-8. [36] J. Pfeilschifter, W. Eberhardt, and K.F. Beck, Regulation of gene expression by nitric oxide. Pflugers Arch 442 (2001 ) 479-86. [37] R. Zamora, Y. Vodovotz, K.S. Aulak, P.K. Kim, J.M. Kane, 3rd, L. Alarcon, DJ. Stuehr, and T.R. Billiar, A DNA microarray study of nitric oxideinduced genes in mouse hepatocytes: implications for hepatic heme oxygenase-1 expression in ischemia/reperfusion. Nitric Oxide 7 (2002) 165-86. [38] J. Hemish, N. Nakaya, V. Mittal, and G. Enikolopov, Nitric oxide ativates diverse signaling pathways to regulate gene expression. J Biol Chem 278 (2003) 42321-9. [39] M. Ziehe, L. Morbidelli, E. Masini, S. Amerini, HJ. Granger, CA. Maggi, P. Geppetti, and F. Ledda, Nitric oxide mediates angiogenesis in vivo and endothelial cell growth and migration in vitro promoted by substance P. J Clin Invest 94 (1994) 2036-44. [40] SJ. Leibovich, PJ. Polverini, T.W. Fong, L.A. Harlow, and A.E. Koch, Production of angiogenic activity by human monocytes requires an L- arginine/nitric oxide-synthase- dependent effector mechanism. Proc Natl Acad Sei USA 91 (1994) 4190-4. [41] N.S. Bryan, B.O. Fernandez, S.M. Bauer, M.F. Garcia-Saura, A.B. Milsom, T. Rassaf, R.E. Maloney, A. Bharti, J. Rodriguez, and M. Feelisch, Nitrite is a signaling molecule and regulator of gene expression in mammalian tissues. Nature Chemical Biology 1 (2005) 290- 297.
Claims (5)
1. Dispositivo de imersão que compreende a. uma unidade geradora (SGE) (1) de óxido nítrico (NO) com uma fonte de radiação UV (6) e uma câmara volumétrica (3) para receber uma solução aquosa que contém NOD, em que a SGE é concebida de um modo tal que por meio de radiação UV a solução aquosa pode ser enriquecida com NO e b. uma unidade de volume VE (2) para a imersão de objetos, em que a VE pode receber a solução aquosa enriquecida com NO transferida da SGE (1), em que a unidade de volume (2) é um recipiente aberto no topo e a SGE (1) é selada estanquemente, caracterizado por a transferência da solução aquosa ser efetuada por duas aberturas (5) de ligação entre SGE e VE em uma parede comum ou através de duas condutas e solução aquosa poder ser descarregada na unidade de volume (2) através da câmara volumétrica (3) da SGE (1) por meio de um dispositivo de circulação ou bomba, de modo que a câmara volumétrica (3) da SGE (1) e a unidade de volume (2) formem um circuito fechado para a solução aquosa e o dispositivo de imersão ser proporcionado com um dispositivo de controlo de temperatura que permite o ajuste de uma temperatura selecionada por aquecimento ou arrefecimento e a fonte de radiação UV (6) ser selecionada entre o conjunto constituído por uma superfície revestida com os fluorocrómos incandescentes adequados ou com uma lâmpada de descarga de gás adequada (descarga de pressão reduzida ou de pressão elevada), um díodo emissor de luz (LED), um díodo emissor de luz orgânico (OLED) e um laser.
2. Dispositivo de imersão de acordo com a reivindicação 1, caracterizado por a câmara volumétrica (3) da SGE (1) e/ou na unidade de volume (VE) (2) ser possível utilizar recipiente de enchimento substituível que contém uma composição, em pó, gel ou líquido que compreende NOD, uma substância tampão, um antioxidante e, facultativamente, um solvente.
3. Dispositivo de imersão de acordo com a reivindicação 1 ou 2, caracterizado por o recipiente de enchimento substituível ser um cartucho.
4. Dispositivo de imersão de acordo com qualquer uma das reivindicações 1 a 3, caracterizado por ser para utilização no tratamento de doenças, através da imersão de seções do tronco, porções dos membros ou corpos completos como objetos, no meio veículo.
5. Dispositivo de imersão de acordo com a reivindicação 4, caracterizado por o SGE (1) ser controlada de um modo tal que o teor em NO aumenta ou diminui ao longo do período de tratamento.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102013017524.0 | 2013-10-24 | ||
| DE102013017524 | 2013-10-24 | ||
| PCT/EP2014/072844 WO2015059273A1 (de) | 2013-10-24 | 2014-10-24 | Eintauchvorrichtung |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BR112016008928A2 BR112016008928A2 (pt) | 2017-08-01 |
| BR112016008928B1 true BR112016008928B1 (pt) | 2022-04-19 |
Family
ID=51870992
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR112016008928-6A BR112016008928B1 (pt) | 2013-10-24 | 2014-10-24 | Dispositivo de imersão, seu uso e estojo para utilização em um dispositivo |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US10022527B2 (pt) |
| EP (1) | EP3060189B1 (pt) |
| JP (1) | JP6505686B2 (pt) |
| CN (1) | CN105848624B (pt) |
| AU (1) | AU2014338918B2 (pt) |
| BR (1) | BR112016008928B1 (pt) |
| CA (1) | CA2945724C (pt) |
| MX (1) | MX371039B (pt) |
| WO (1) | WO2015059273A1 (pt) |
| ZA (1) | ZA201603353B (pt) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2528921A (en) * | 2014-08-05 | 2016-02-10 | Linde Ag | Plasma treatment of an infected nail or infected skin |
| DE102016014942A1 (de) * | 2016-12-14 | 2018-06-14 | Lohmann & Rauscher Gmbh | Vorrichtung zur human- und tiermedizinischen Behandlung und Applikationseinrichtung dafür |
| WO2020069368A1 (en) * | 2018-09-27 | 2020-04-02 | The Regents Of The University Of Michigan | Gas delivery devices |
| AT17416U1 (de) | 2020-05-14 | 2022-03-15 | Rp Technik Gmbh | Beleuchtungsmittel, insbesondere zur Reduktion von Keimen, mit vorzugsweise wenigstens zwei Lichtquellen, sowie Verfahren zur Nutzung des Beleuchtungsmittels als mobiles Desinfektionsgerät |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5098415A (en) * | 1990-10-09 | 1992-03-24 | Jack Levin | Device and method for using an aqueous solution containing ozone to treat foot diseases |
| US5396882A (en) | 1992-03-11 | 1995-03-14 | The General Hospital Corporation | Generation of nitric oxide from air for medical uses |
| ATE153311T1 (de) | 1993-09-13 | 1997-06-15 | Aga Ab | Verfahren und vorrichtung zum erzeugen von stickstoffoxyde |
| JPH08126678A (ja) * | 1994-11-01 | 1996-05-21 | Hitachi Home Tec Ltd | 脚温浴器 |
| JPH08252192A (ja) * | 1995-03-15 | 1996-10-01 | Toyo Tanso Kk | 風呂給湯装置 |
| DK174312B1 (da) | 1996-06-06 | 2002-12-02 | Ole Pedersen | Fremgangsmåde til måling af strømningshastighed og diffusivitet, mikrosensor til brug ved fremgangsmåden samt anvendelse af sådan mikrosensor |
| DE19823748C2 (de) | 1998-05-27 | 2000-05-18 | Siemens Ag | Verfahren und Vorrichtung zur plasmachemischen Erzeugung von Stickstoffmonoxid |
| US7122018B2 (en) * | 2000-12-26 | 2006-10-17 | Sensormedics Corporation | Device and method for treatment of wounds with nitric oxide |
| AU2001242836B2 (en) * | 2001-03-20 | 2004-04-08 | Ahn, Shin-Young | Foot massage apparatus |
| US6810288B2 (en) * | 2001-07-06 | 2004-10-26 | Ceramatec, Inc. | Device and method for wound healing and infection control |
| US7122529B2 (en) | 2001-07-12 | 2006-10-17 | The Johns Hopkins University | Compounds that release nitric oxide at controlled rates upon photolysis |
| US6673338B1 (en) | 2001-09-10 | 2004-01-06 | The United States Of America As Represented By The Department Of Health And Human Services | Nitric oxide-releasing imidate and thioimidate diazeniumdiolates, compositions, uses thereof and method of making same |
| US20030039697A1 (en) | 2002-09-12 | 2003-02-27 | Yi-Ju Zhao | Matrices containing nitric oxide donors and reducing agents and their use |
| US8017074B2 (en) * | 2004-01-07 | 2011-09-13 | Noxilizer, Inc. | Sterilization system and device |
| US8663179B2 (en) * | 2004-03-22 | 2014-03-04 | Cure Care, Inc. | Wound treatment system and method of use |
| US8708982B2 (en) * | 2005-05-04 | 2014-04-29 | Edward D. Lin | Wound protection and therapy system |
| WO2007084533A2 (en) * | 2006-01-17 | 2007-07-26 | The University Of Akron | Debridement method using topical nitric oxide donor devices and compositions |
| EP3023389B1 (de) | 2006-07-05 | 2020-03-18 | BSN medical GmbH | Vorrichtung zur photolytischen erzeugung von stickstoffmonoxid |
| WO2008012845A1 (en) | 2006-07-26 | 2008-01-31 | Stmicroelectronics S.R.L. | Use of nitroaniline derivatives for the production of nitric oxide |
| US20120065576A1 (en) * | 2007-08-14 | 2012-03-15 | Stryker Corporation | Drug delivery system |
| US8877508B2 (en) * | 2007-10-30 | 2014-11-04 | The Invention Science Fund I, Llc | Devices and systems that deliver nitric oxide |
| JP5071857B2 (ja) * | 2008-03-11 | 2012-11-14 | 学校法人東京理科大学 | 光触媒並びに硝酸イオンおよび亜硝酸イオン還元方法 |
| CN101569781A (zh) * | 2008-04-30 | 2009-11-04 | 姚广权 | 一种治疗创口的装置 |
| JP4543186B1 (ja) * | 2009-03-13 | 2010-09-15 | 国立大学法人茨城大学 | 二酸化窒素光分解コンバータおよび二酸化窒素光分解コンバータを備えた窒素酸化物濃度測定装置 |
| CN102753132B (zh) * | 2009-11-24 | 2014-06-18 | 川上进盟 | 人治愈能力提高装置及人治愈能力提高装置的工作方法 |
| JPWO2012086635A1 (ja) * | 2010-12-20 | 2014-05-22 | 中村 正一 | 心筋梗塞を予防、改善又は治療するための炭酸ガスミスト圧浴方法及び炭酸ガスミスト圧浴装置 |
-
2014
- 2014-10-24 CA CA2945724A patent/CA2945724C/en active Active
- 2014-10-24 BR BR112016008928-6A patent/BR112016008928B1/pt active IP Right Grant
- 2014-10-24 AU AU2014338918A patent/AU2014338918B2/en active Active
- 2014-10-24 JP JP2016526077A patent/JP6505686B2/ja active Active
- 2014-10-24 EP EP14795974.6A patent/EP3060189B1/de active Active
- 2014-10-24 CN CN201480070296.2A patent/CN105848624B/zh active Active
- 2014-10-24 US US15/030,865 patent/US10022527B2/en active Active
- 2014-10-24 WO PCT/EP2014/072844 patent/WO2015059273A1/de active Application Filing
- 2014-10-24 MX MX2016005064A patent/MX371039B/es active IP Right Grant
-
2016
- 2016-05-17 ZA ZA2016/03353A patent/ZA201603353B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017505148A (ja) | 2017-02-16 |
| AU2014338918A1 (en) | 2016-06-09 |
| BR112016008928A2 (pt) | 2017-08-01 |
| WO2015059273A1 (de) | 2015-04-30 |
| MX371039B (es) | 2020-01-13 |
| EP3060189A1 (de) | 2016-08-31 |
| JP6505686B2 (ja) | 2019-04-24 |
| CN105848624B (zh) | 2018-04-10 |
| US10022527B2 (en) | 2018-07-17 |
| EP3060189B1 (de) | 2018-05-09 |
| CA2945724C (en) | 2022-12-06 |
| ZA201603353B (en) | 2018-08-29 |
| CA2945724A1 (en) | 2015-04-30 |
| AU2014338918B2 (en) | 2019-09-12 |
| US20160296738A1 (en) | 2016-10-13 |
| MX2016005064A (es) | 2016-09-13 |
| CN105848624A (zh) | 2016-08-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2206202T5 (es) | Uso de xenón para preparar una preparación farmacéutica para tratar neurointoxicaciones | |
| AU2016256577B2 (en) | Medical bathing device | |
| BR112016008928B1 (pt) | Dispositivo de imersão, seu uso e estojo para utilização em um dispositivo | |
| JP2008532605A (ja) | 皮膚用包帯に関する改良 | |
| US20170361078A1 (en) | Onychomycosis treatment system and method | |
| Chakravarthy et al. | Cold spark discharge plasma treatment of inflammatory bowel disease in an animal model of ulcerative colitis | |
| BR112017022126B1 (pt) | Aparelho de acumulação, aparelho de produção de solução e seu uso e aparelho de banho de óxido nítrico (no) e método para acumular | |
| JP2017035510A (ja) | 一酸化窒素の生成方法及び装置 | |
| Jani et al. | Ozone therapy: the alternative medicine of future | |
| Sato et al. | Efficacy and safety of a therapeutic apparatus using hydrogen peroxide photolysis to treat dental and periodontal infectious diseases | |
| Arjunan et al. | A nitric oxide producing pin-to-hole spark discharge plasma enhances endothelial cell proliferation and migration | |
| Opländer et al. | A new method for sustained generation of ultra-pure nitric oxide-containing gas mixtures via controlled UVA-photolysis of nitrite solutions | |
| Verma et al. | A review of patents on therapeutic potential and delivery of hydroge n sulfide | |
| US20170354616A1 (en) | Onychomycosis treatment system and method | |
| Sun et al. | Local delivery of gaseous signaling molecules for orthopedic disease therapy | |
| BR112017023057B1 (pt) | Processo para preparação de no e processo cosmético | |
| KR20080061095A (ko) | 복합 미용기 | |
| Gianfaldoni et al. | Vitiligo repigmentation: what’s new | |
| KR20220104141A (ko) | 약물 수용 장치 및 관련 조성물 | |
| Arjunan | Plasma produced reactive oxygen and nitrogen species in angiogenesis | |
| RU2430757C1 (ru) | Способ подавления патогенных и условно-патогенных микроорганизмов | |
| AR048138A1 (es) | Formulacion farmaceutica de liberacion controlada | |
| CN109846872B (zh) | 一种用于防治创伤后应激综合征的药物和功能性食品 | |
| JP4819444B2 (ja) | 遺体の維持保存処理方法 | |
| RU2349326C1 (ru) | Способ лечения длительно незаживающих ран в эксперименте |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25C | Requirement related to requested transfer of rights |
Owner name: BSN MEDICAL GMBH (DE) |
|
| B25A | Requested transfer of rights approved |
Owner name: BSN MEDICAL HOLDING GMBH (DE) |
|
| B25D | Requested change of name of applicant approved |
Owner name: BSN MEDICAL GMBH (DE) |
|
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 24/10/2014, OBSERVADAS AS CONDICOES LEGAIS. |