WO2023276785A1 - 歯周病の体外診断方法、及び、Pg菌検出方法 - Google Patents
歯周病の体外診断方法、及び、Pg菌検出方法 Download PDFInfo
- Publication number
- WO2023276785A1 WO2023276785A1 PCT/JP2022/024727 JP2022024727W WO2023276785A1 WO 2023276785 A1 WO2023276785 A1 WO 2023276785A1 JP 2022024727 W JP2022024727 W JP 2022024727W WO 2023276785 A1 WO2023276785 A1 WO 2023276785A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- periodontal disease
- electrode
- information
- electrochemical measurement
- current
- Prior art date
Links
- 208000028169 periodontal disease Diseases 0.000 title claims abstract description 49
- 238000000034 method Methods 0.000 title claims abstract description 44
- 238000000338 in vitro Methods 0.000 title claims abstract description 32
- 238000003745 diagnosis Methods 0.000 title claims abstract description 7
- 241000894006 Bacteria Species 0.000 title claims description 51
- 238000001514 detection method Methods 0.000 title claims description 18
- 238000002848 electrochemical method Methods 0.000 claims abstract description 46
- 150000001413 amino acids Chemical class 0.000 claims abstract description 34
- 210000000214 mouth Anatomy 0.000 claims abstract description 16
- 235000001014 amino acid Nutrition 0.000 claims description 33
- 238000002405 diagnostic procedure Methods 0.000 claims description 27
- 238000005259 measurement Methods 0.000 claims description 25
- 230000002394 glycogenic effect Effects 0.000 claims description 23
- AUNGANRZJHBGPY-SCRDCRAPSA-N Riboflavin Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-SCRDCRAPSA-N 0.000 claims description 18
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 claims description 18
- 235000014304 histidine Nutrition 0.000 claims description 18
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 claims description 14
- 235000003704 aspartic acid Nutrition 0.000 claims description 14
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 claims description 14
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims description 12
- 235000013922 glutamic acid Nutrition 0.000 claims description 12
- 239000004220 glutamic acid Substances 0.000 claims description 12
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 10
- AUNGANRZJHBGPY-UHFFFAOYSA-N D-Lyxoflavin Natural products OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-UHFFFAOYSA-N 0.000 claims description 9
- FVTCRASFADXXNN-SCRDCRAPSA-N flavin mononucleotide Chemical compound OP(=O)(O)OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O FVTCRASFADXXNN-SCRDCRAPSA-N 0.000 claims description 9
- 239000011768 flavin mononucleotide Substances 0.000 claims description 9
- 229940013640 flavin mononucleotide Drugs 0.000 claims description 9
- FVTCRASFADXXNN-UHFFFAOYSA-N flavin mononucleotide Natural products OP(=O)(O)OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O FVTCRASFADXXNN-UHFFFAOYSA-N 0.000 claims description 9
- 239000002151 riboflavin Substances 0.000 claims description 9
- 235000019192 riboflavin Nutrition 0.000 claims description 9
- 229960002477 riboflavin Drugs 0.000 claims description 9
- 235000019231 riboflavin-5'-phosphate Nutrition 0.000 claims description 9
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 claims description 8
- CSFWPUWCSPOLJW-UHFFFAOYSA-N lawsone Chemical group C1=CC=C2C(=O)C(O)=CC(=O)C2=C1 CSFWPUWCSPOLJW-UHFFFAOYSA-N 0.000 claims description 8
- WVCHIGAIXREVNS-UHFFFAOYSA-N 2-hydroxy-1,4-naphthoquinone Chemical compound C1=CC=C2C(O)=CC(=O)C(=O)C2=C1 WVCHIGAIXREVNS-UHFFFAOYSA-N 0.000 claims description 6
- 239000004475 Arginine Substances 0.000 claims description 6
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 claims description 6
- 241000605862 Porphyromonas gingivalis Species 0.000 claims description 6
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 claims description 6
- 235000009697 arginine Nutrition 0.000 claims description 6
- GTKRFUAGOKINCA-UHFFFAOYSA-M chlorosilver;silver Chemical compound [Ag].[Ag]Cl GTKRFUAGOKINCA-UHFFFAOYSA-M 0.000 claims description 5
- 230000002250 progressing effect Effects 0.000 claims description 5
- 230000003087 glucogenic effect Effects 0.000 abstract 1
- 229940024606 amino acid Drugs 0.000 description 30
- 239000000523 sample Substances 0.000 description 19
- 230000000694 effects Effects 0.000 description 13
- 230000001580 bacterial effect Effects 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 7
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 7
- 229910021607 Silver chloride Inorganic materials 0.000 description 6
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 5
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 239000003792 electrolyte Substances 0.000 description 4
- 239000008103 glucose Substances 0.000 description 4
- 230000003239 periodontal effect Effects 0.000 description 4
- 238000011282 treatment Methods 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 3
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 3
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 238000011158 quantitative evaluation Methods 0.000 description 3
- 210000003296 saliva Anatomy 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 241000190885 Capnocytophaga ochracea Species 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 241000194019 Streptococcus mutans Species 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 244000052616 bacterial pathogen Species 0.000 description 2
- 239000011651 chromium Substances 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 239000010948 rhodium Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 102000005927 Cysteine Proteases Human genes 0.000 description 1
- 108010005843 Cysteine Proteases Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- 241000186660 Lactobacillus Species 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- 208000005888 Periodontal Pocket Diseases 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 241000589892 Treponema denticola Species 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 238000004082 amperometric method Methods 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000012496 blank sample Substances 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 238000000970 chrono-amperometry Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000002484 cyclic voltammetry Methods 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 229910003460 diamond Inorganic materials 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 229910021389 graphene Inorganic materials 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 229940039696 lactobacillus Drugs 0.000 description 1
- 238000004502 linear sweep voltammetry Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- RJIWZDNTCBHXAL-UHFFFAOYSA-N nitroxoline Chemical compound C1=CN=C2C(O)=CC=C([N+]([O-])=O)C2=C1 RJIWZDNTCBHXAL-UHFFFAOYSA-N 0.000 description 1
- 229910000510 noble metal Inorganic materials 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000027756 respiratory electron transport chain Effects 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 229910052707 ruthenium Inorganic materials 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 230000001810 trypsinlike Effects 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 238000004832 voltammetry Methods 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/001—Enzyme electrodes
- C12Q1/004—Enzyme electrodes mediator-assisted
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/34—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving hydrolase
- C12Q1/37—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving hydrolase involving peptidase or proteinase
Definitions
- the present invention relates to an in vitro diagnostic method for periodontal disease and a method for detecting Pg bacteria.
- Periodontal disease is a general term for diseases in the periodontal tissue, which is the tissue that supports the teeth, and is considered a multifactorial disease caused by various factors. Among these many factors, one of the major ones is the infection of periodontal pathogenic bacteria in periodontal pockets. Due to such bacterial infection, the periodontal tissue is destroyed, and eventually the teeth are lost.
- Treponema denticola (hereinafter also referred to as “Td bacteria”) are highly likely to be causative bacteria of periodontal disease. They are also considered to be related to diseases, and investigations are underway for in vitro diagnostic methods for detecting the activity of these bacteria in the oral cavity of subjects.
- Patent Literature 1 describes "a periodontal disease detection method characterized by using a cysteine protease produced by Lactobacillus gingipalis as a periodontal disease marker for detecting periodontal disease.”
- the periodontal disease detection method described in Patent Document 1 measures enzyme activity, and the activity varies greatly depending on the reaction temperature, and the measurement operation is complicated. There was room.
- a specimen derived from the oral cavity of a subject is brought into contact with an electrode, electrochemically measured in the presence of a sugar source amino acid and an electron mediator under an anaerobic environment, and as a result of the electrochemical measurement, current generation is detected. If so, providing information for determining that periodontal disease is progressing in the oral cavity of the subject.
- the glycogenic amino acid contains at least one selected from the group consisting of arginine, histidine, aspartic acid, and glutamic acid.
- the electronic mediator contains at least one selected from the group consisting of flavin mononucleotide, riboflavin, and 2-hydroxy-1,4-napthoquinone, [ 1] or the method for in vitro diagnosis of periodontal disease according to [2].
- the information for the determination is at least one selected from the group consisting of the time from the start of the electrochemical measurement to the detection of the current generation, and the maximum value of the current density of the generated current.
- the information for the determination is at least one selected from the group consisting of the time from the start of the electrochemical measurement to the detection of the current generation, and the maximum value of the current density of the generated current.
- the Pg bacterium detection method according to any one of [10] to [12], including the measurement result of species.
- the in-vitro diagnostic method of the present invention includes contacting a specimen derived from the oral cavity of a subject with an electrode, performing electrochemical measurement in the presence of a saccharogenic amino acid and an electron mediator under an anaerobic environment, and obtaining the results of the electrochemical measurement. and providing information for determining that periodontal disease is progressing in the subject's oral cavity if current generation is detected. According to this method, information for judging the progress of periodontal disease can be obtained by a simple operation of electrochemically measuring a specimen in the presence of a glycogenic amino acid and an electronic mediator.
- the glycogenic amino acid contains at least one selected from the group consisting of arginine, histidine, aspartic acid, and glutamic acid
- the resulting generated current tends to be larger. Since the measurement can be performed with higher sensitivity than this, more accurate information can be obtained as a result.
- the electronic mediator contains at least one selected from the group consisting of flavin mononucleotide (FMN), riboflavin (RF), and 2-hydroxy-1,4-naphthoquinone (hereinafter also referred to as "HNQ")
- FMN flavin mononucleotide
- RF riboflavin
- HNQ 2-hydroxy-1,4-naphthoquinone
- the above tendency is particularly pronounced when the electronic mediator includes HNQ.
- the inventors have experimentally determined that when the electron mediator comprises HNQ, surprisingly, the time until current production is detected is also shorter. That is, it is possible to shorten the time until information is provided.
- the method of electrochemical measurement is to control the potential of an electrode and measure the current flowing through said electrode as a function of time, the current generation is more detectable, resulting in more accurate information. easy to get
- the information for determination is at least one measurement result selected from the group consisting of the time from the start of the electrochemical measurement until the current generation is detected, and the maximum value of the current density of the generated current.
- the progress of periodontal disease can be determined in chronological order by comparing the obtained information.
- the information for the determination includes comparison information between a predetermined reference value and the measurement result, for example, if the reference value set for each subject is used, the progress of periodontal disease can be evaluated. easier to judge. In addition, if a reference value determined for each attribute of the subject, such as age and gender, is used, even if it is a single measurement, the comparison target becomes clear, so the progress of periodontal disease from the obtained information Easier to judge the degree.
- the method for detecting Pg bacteria of the present invention comprises contacting a specimen with an electrode, performing electrochemical measurement in the presence of a saccharogenic amino acid and HNQ in an anaerobic environment, and detecting current generation as a result of the electrochemical measurement. If so, providing information for determining that the specimen contains Pg bacteria.
- HNQ is used as an electron mediator
- Pg bacteria can be specifically detected with a simple operation even when the sample contains contaminants and/or other bacteria. Since Pg bacteria, which are periodontopathogenic bacteria, can be detected without performing operations such as culturing, it can be easily applied to determination of dental treatment policy.
- the electrochemical measurement method is a method of controlling the potential of the electrode and measuring the current flowing through the electrode as a function of time, it is easier to detect the current generation by Pg bacteria, and as a result, it is easier to detect. Easy to get accurate information.
- the information for the determination is at least one selected from the group consisting of the time from the start of the electrochemical measurement to the detection of the current generation, and the maximum value of the current density of the generated current. Including measurement results is preferable in that quantitative evaluation is easier. For example, it is possible to compare the number of Pg bacteria between specimens.
- the information for judgment includes comparison information between a predetermined reference value and measurement results, for example, creating a reference value based on a blank sample will enable more accurate measurement.
- FIG. 1 is a flow chart of an in-vitro diagnostic method according to an embodiment of the present invention
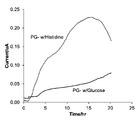
- 4 is a chronoamperogram showing the effect of histidine on the generated current.
- 4 is a chronoamperogram showing the effect of aspartic acid on the generated current.
- 4 is a chronoamperogram showing the effect of glutamic acid on generated current.
- FIG. 10 is a diagram showing current production specific to Pg bacteria when aspartic acid is used as a saccharogenic amino acid. It is an experimental result of examining the influence of HNQ on current generation. It is an experimental result of examining the influence of FMN on current generation. It is the experimental result which investigated the influence on current generation of RF.
- FIG. 1 is a flow chart of an in-vitro diagnostic method according to an embodiment of the present invention.
- a sample derived from the oral cavity of a subject is brought into contact with an electrode, and electrochemical measurement is performed in the presence of a glycogenic amino acid and an electron mediator under an anaerobic environment (step S11).
- the specimen is not particularly limited as long as it is derived from the oral cavity of the subject, but preferably contains saliva, plaque, blood, pus, mixtures thereof, and the like. Especially, when the specimen contains saliva, it is more non-invasive and easier to collect, which is preferable.
- the specimen may contain water, electrolytes, and the like as components other than those described above.
- the electrolyte is not particularly limited, but known electrolytes can be used. However, it is preferable that the electrolyte does not contain organic substances other than the saccharogenic amino acids described later.
- Electrochemical measurements are performed in the presence of glycogenic amino acids. Electrochemical measurement in the presence of a glycogenic amino acid typically includes a form in which the glycogenic amino acid is added to the sample. Examples of glycogenic amino acids include alanine, glycine, serine, threonine, cysteine, tryptophan, isoleucine, methionine, valine, aspartic acid, arginine, glutamic acid, histidine, proline, tyrosine, and phenylalanine, among others.
- At least one selected from the group consisting of arginine, histidine, aspartic acid, and glutamic acid is preferable, and at least one selected from the group consisting of arginine and histidine from the viewpoint that the generated current (density) tends to be larger 1 type is more preferable.
- histidine Compared to aspartic acid and glutamic acid, histidine has higher water solubility and is preferable in that even when added to a specimen, it tends to be more uniform. If the water solubility is high, there is no need to add an acid or the like to the sample, which is preferable in that the background current in the measurement tends to be small. In addition, the present inventors have experimentally confirmed that when the glycogenic amino acid is histidine, the generated current derived from the Pg bacterium tends to increase (see Examples).
- acid e.g., hydrochloric acid
- the content of the glycogenic amino acid in the sample is not particularly limited, but is generally preferably 0.1 to 1000 mM.
- Electrochemical measurements are also performed in the presence of an electronic mediator. Periodontopathogenic bacteria generate electric current in an anaerobic environment, and some have the function of transferring the electric current to an extracellular electron acceptor (e.g., anode electrode), but electrochemical measurements are performed in the presence of an electron mediator. This is more preferable because electron transfer can be performed more smoothly. Electrochemical measurement in the presence of an electron mediator typically includes a form in which an electron mediator is added to a specimen, as in the case of the sugargenic amino acid described above.
- the electronic mediator that can be used is not particularly limited, and known electronic mediators can be used.
- the electron mediator is preferably water-soluble, and is selected from the group consisting of flavin mononucleotide, riboflavin, and 2-hydroxy-1,4-naphthoquinone (2-hydroxy-1,4-napthoquinone, HNQ). When at least one is included, a larger generated current (density) can be obtained.
- the glycogenic amino acid and the electron mediator may not be added to the specimen.
- the glycogenic amino acid may be immobilized on the electrode surface.
- a method of controlling the potential of the electrode and measuring the current as a function of time is preferable.
- Such methods include, for example, the amperometry method, the cyclic voltammetry method, the linear sweep voltammetry method, and the rectangular wave voltammetry method.
- the material of the electrodes is not particularly limited, and known electrodes for electrochemical measurements can be used.
- Materials for the electrodes include, for example, ITO (indium tin oxide), noble metals (gold (Au), silver (Ag), platinum (Pt), palladium (Pd), rhodium (Rh), iridium (Ir), ruthenium (Ru ), etc.), copper (Cu), aluminum (Al), tungsten (W), molybdenum (Mo), chromium (Cr), titanium (Ti), nickel (Ni), and the like.
- Carbon materials such as carbon and graphite (graphene) may also be used.
- a boron-doped diamond electrode is also preferable in that it has a wide potential window.
- a general electrochemical measuring device can be used for the electrochemical measurement.
- a three-electrode electrochemical measurement device in which a working electrode, a counter electrode, and a reference electrode are housed in a cell can be used.
- the temperature at which the electrochemical measurement is performed is not particularly limited, it can be performed at the same temperature as the sampling site of the sample, or the temperature can be controlled. In that case, the temperature of the specimen is preferably 10 to 40°C.
- the measurement may be performed in a general anaerobic glove box (anaerobic chamber), preferably under anoxic conditions.
- the potential of the electrode (working electrode) exceeds 0 V (vs. Ag/AgCl), and the potential window Control within a range less than the upper limit is preferred. Further, from the viewpoint of easily obtaining a larger generated current or easily generating a current in a shorter time, it is preferable to set the potential of the electrode to 0 to +0.6 V (vs. Ag/AgCl).
- step S12 If current generation is detected by this electrochemical measurement (step S12: Yes), the presence of periodontopathogenic bacteria in the sample is suggested. In this case, information for determining that periodontal disease is progressing in the oral cavity of the subject is provided (step S13).
- step S12 if current generation is not detected by this electrochemical measurement (step S12: No), the diagnosis ends and no information is provided for determining that periodontal disease is progressing.
- the above information is based on the measurement results, and its form is not particularly limited, but it consists of the time from the start of electrochemical measurement to the detection of current generation, and the maximum current density of the generated current.
- Information containing at least one measurement result selected from the group (hereinafter also referred to as “specific information”) is more preferable because it is likely to be information that contributes to quantitative evaluation of the progress of periodontal disease.
- the above-mentioned specific information is a numerical value related to the content of periodontopathogenic bacteria in the specimen, and for example, by comparing it with the value of a healthy subject or comparing it with the past value of the same subject, The information is likely to be useful for judging the degree of periodontal disease occurring in the oral cavity of the subject and the chronological progression of the disease.
- Modification A modification of the in-vitro diagnostic method according to the above-described embodiment compares the obtained measurement result with a reference value when current generation is detected, and provides information including the comparison information as periodontal disease in the oral cavity of the subject. It is an in vitro diagnostic method that provides information for judging progress.
- Examples of the reference value in the extracorporeal diagnostic method include the result of measurement by the same method using a healthy subject's sample, the past test result of the same subject, and the like.
- the comparative information includes, for example, the difference between the specific information measured by the same method using a healthy subject's sample and the specific information of the sample.
- the time from the start of electrochemical measurement to the detection of current generation in the case of measuring by the same method using a healthy subject's specimen, and the same as above for the specimen obtained from the subject The difference from the time measured by the method of . If the time measured for the sample is earlier and the difference is larger, it can be used as information for determining that the sample contains more periodontopathogenic bacteria.
- the above comparison information is an example, and information other than the above may be used.
- the specimen is brought into contact with an electrode, and in the presence of a glycogenic amino acid and 2-hydroxy-1,4-napthoquinone, Including performing electrochemical measurement in an anaerobic environment, and providing information for determining that the specimen contains Porphyromonas gingivalis when current generation is detected as a result of the electrochemical measurement. .
- the specimens in this detection method are not limited to those derived from the oral cavity of the subject, but may be specimens cultured for testing and research, environmental specimens (water and dust), and the like. If the specimen is not liquid, it can be used after extraction and purification using water or the like.
- Figure 2 is a chronoamperogram showing the effect of histidine on the generated current.
- PG-w/Histidine means that the sample contains histidine which is a glycogenic amino acid
- PG-w/Glucose means that the sample does not contain histidine and contains glucose instead. This is the result.
- current production was detected immediately after adding the Pg bacterial solution.
- current generation was detected, but at a smaller magnitude and with a longer time to current generation.
- Fig. 3 is a chronoamperogram showing the effect of aspartic acid on the generated current.
- FIG. 4 is a chronoamperogram showing the effect of glutamic acid on the generated current. In both cases, current production was detected immediately after adding the Pg bacterial solution.
- Figure 5 shows the above results. From FIG. 5, it was found that in the sample containing aspartic acid, Pg-specific current production could be detected.
- FIG. 6 shows experimental results when using HNQ, FIG. 7 using FMN, and FIG. 8 using RF.
- FIGS. 6 to 8 when any of the electron mediators was used, a larger current was rapidly obtained after addition of the bacterial solution (compare with FIG. 2).
- HNQ when HNQ was used, a larger current was obtained than when FMN and RF were used, and this tendency was particularly noticeable at concentrations exceeding 10 ⁇ M.
- saliva can be used as a specimen, and information for determining the progression of periodontal disease can be obtained in a simple manner.
- the information provided by the in-vitro diagnostic method of the present invention can be used not only for dentists to determine treatment strategies, but also for oral health management by patients themselves at home or in remote locations.
- the Pg bacterium detection method of the present invention it is possible to detect Pg bacterium-specific current generation by using a combination of saccharogenic amino acids and HNQ. This method is useful not only in formulating a dental treatment policy but also in the field of experimental research.
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Pathology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- General Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Description
[2] 上記糖源性アミノ酸がアルギニン、ヒスチジン、アスパラギン酸、及び、グルタミン酸からなる群より選択される少なくとも1種を含む、[1]に記載の歯周病の体外診断方法。
[3] 上記電子メディエータが、フラビンモノヌクレオチド、リボフラビン、及び、2-ヒドロキシ-1,4-ナフトキノン(2-hydroxy-1,4-napthoquinone)からなる群より選択される少なくとも1種を含む、[1]又は[2]に記載の歯周病の体外診断方法。
[4] 上記電子メディエータが、2-ヒドロキシ-1,4-ナフトキノンである、[1]~[3]のいずれかに記載の歯周病の体外診断方法。
[5] 上記電気化学測定の方法が、上記電極の電位を制御して、上記電極を流れる電流を時間の関数として測定する方法である、[1]~[4]のいずれかに記載の歯周病の体外診断方法。
[6] 上記電位が、銀-塩化銀電極に対して0Vを超えて、電位窓の上限値未満の範囲内である、[5]に記載の歯周病の体外診断方法。
[7] 上記判断するための情報が、上記電気化学測定の開始から上記電流生成が検出されるまでの時間、及び、生成される電流の電流密度の最大値からなる群より選択される少なくとも1種の測定結果を含む、[1]~[6]のいずれかに記載の歯周病の体外診断方法。
[8] 上記判断するための情報が、予め定められた基準値と、上記測定結果との比較情報を含む、[7]に記載の歯周病の体外診断方法。
[9] 上記歯周病の原因菌が、ポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)を含む、[1]~[8]のいずれかに記載の歯周病の体外診断方法。
[10] 検体を電極と接触させ、糖源性アミノ酸と2-ヒドロキシ-1,4-ナフトキノン(2-hydroxy-1,4-napthoquinone)との存在下、嫌気環境下で電気化学測定することと、上記電気化学測定の結果、電流生成が検出された場合、上記検体に、ポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)が含まれると判断するための情報を提供することと、を含むPg菌検出方法。
[11] 上記電気化学測定の方法が、上記電極の電位を制御して、上記電極を流れる電流を時間の関数として測定する方法である、[10]に記載のPg菌検出方法。
[12] 上記電位が、銀-塩化銀電極に対して0Vを超えて、電位窓の上限値未満の範囲内である、[11]に記載のPg菌検出方法。
[13] 上記判断するための情報が、上記電気化学測定の開始から上記電流生成が検出されるまでの時間、及び、生成される電流の電流密度の最大値からなる群より選択される少なくとも1種の測定結果を含む、[10]~[12]のいずれかに記載のPg菌検出方法。
[14] 上記判断するための情報が、予め定められた基準値と、上記測定結果との比較情報を含む、[13]に記載のPg菌検出方法。
上記方法によれば、電子メディエータとしてHNQを用いるため、検体に夾雑物質、及び/又は、他の細菌が含まれる場合にも、簡単な操作でPg菌を特異的に検出できる。培養等の操作を行わなくても、歯周病原性細菌であるPg菌を検出できるため、歯科治療方針の決定等に容易に応用できる。
以下に記載する構成要件の説明は、本発明の代表的な実施形態に基づいてなされることがあるが、本発明はそのような実施形態に制限されるものではない。
なお、本明細書において、「~」を用いて表される数値範囲は、「~」の前後に記載される数値を下限値及び上限値として含む範囲を意味する。
図1は本発明の実施形態に係る体外診断方法のフローチャートである。
まず、被験者の口腔に由来する検体を電極と接触させ、糖源性アミノ酸と電子メディエータとの存在下、嫌気環境下で電気化学測定する(ステップS11)。
電解質としては、特に制限されないが、公知の電解質を用いることができる。但し、電解質には、後述する糖源性アミノ酸以外の有機物が含まれないことが好ましい。
糖源性アミノ酸としては、例えば、アラニン、グリシン、セリン、トレオニン、システイン、トリプトファン、イソロイシン、メチオニン、バリン、アスパラギン酸、アルギニン、グルタミン酸、ヒスチジン、プロリン、チロシン、及び、フェニルアラニン等が挙られ、なかでも、生成電流(密度)がより大きくなりやすい観点では、アルギニン、ヒスチジン、アスパラギン酸、及び、グルタミン酸からなる群より選択される少なくとも1種が好ましく、アルギニン、及び、ヒスチジンからなる群より選択される少なくとも1種がより好ましい。
また、糖源性アミノ酸がヒスチジンである場合、Pg菌に由来する生成電流がより大きくなりやすいことを本発明者らは実験的に確かめている(実施例参照)。
検体中における糖源性アミノ酸の含有量としては特に制限されないが、一般に、0.1~1000mMが好ましい。
電子メディエータの存在下で電気化学測定を行う、とは、上記糖源性アミノ酸の場合と同様に、典型的には、検体に電子メディエータを添加する形態が挙げられる。
電気化学測定を行う温度は特に制限されないが、検体の採取場所と同程度の温度で行うこともできるし、温度を制御して行ってもよい。その場合、検体の温度は、10~40℃が好ましい。
測定は、一般的な嫌気グローブボックス(嫌気チャンバー)内で、好ましくは無酸素状態で測定を行えばよい。
上記実施形態に係る体外診断方法の変形例は、電流生成が検出される場合、得られた測定結果を基準値と比較して、その比較情報を含む情報を被験者の口腔内において歯周病が進行していると判断するための情報として提供する、体外診断方法である。
比較情報とは、健常者の検体を用いて同一の方法により測定した特定情報と、検体の特定情報との差等が挙げられる。
本発明の実施形態に係るPg菌検出方法は、検体を電極と接触させ、糖源性アミノ酸と2-ヒドロキシ-1,4-ナフトキノン(2-hydroxy-1,4-napthoquinone)との存在下、嫌気環境下で電気化学測定することと、電気化学測定の結果、電流生成が検出された場合、検体に、ポルフィロモナス・ジンジバリスが含まれると判断するための情報を提供することと、を含む。
(実験1:参考例)
Pg菌を用いて、糖源性アミノ酸が電流生成に与える影響を確認した。3電極電気化学セル(作用電極:ITO、対電極:白金、参照電極:Ag/AgCl)を用いて、検体をトータル5mLとして測定した。温度は37℃とした。
検体としては、イーストエクストラクトを除いたDM液体培地に、10mMのヒスチジン、又は、グルコースを添加したものに、更にPg菌液(OD600:0.1)を添加したものを用いた。測定は100%の窒素を充填したCOY嫌気チャンバー内で、クロノアンペロメトリー法により行った。
次に、ヒスチジンに代えて糖源性アミノ酸としてアスパラギン酸、及び、グルタミン酸を用いて試験を行った。なおアスパラギン酸とグルタミン酸は、いずれも水への溶解性が低いため、0.5MのHClに溶解させた。従ってDM液体培地のpHが~5.2となった。
(実験3:参考例)
Pg菌液(OD600:0.1)に代えて、Pg菌液(OD600:0.5)、Streptococcus mutans菌液(OD600:0.5)、及び、Capnocytophaga ochracea(OD600:0.5)を用いたことを除いては、実験1と同様にして、生成電流を調べた。
(実験4:実施例)
3電極電気化学セル(作用電極:ITO、対電極:白金、参照電極:Ag/AgCl)に代えて、96ウェルプレートの底面に3電極が印刷された電気化学測定プレートを用いて、電子メディエータによる電流生成への影響を調べた。
使用した電子メディエータは、HNQ、FMN、及び、RFで、それぞれ濃度を10μM、50μM、100μMとした。また、菌液としては、Pg菌液(OD600:0.5)を用い、それ以外の条件は実験1と同様にした。
なかでも、HNQを用いた場合、FMN、及び、RFを用いた場合よりもより大きな電流が得られ、特に、10μMを超える濃度ではその傾向が顕著であった。
Claims (14)
- 被験者の口腔に由来する検体を電極と接触させ、糖源性アミノ酸と電子メディエータとの存在下、嫌気環境下で電気化学測定することと、
前記電気化学測定の結果、電流生成が検出された場合、前記被験者の口腔内において歯周病が進行していると判断するための情報を提供することと、を含む、歯周病の体外診断方法。 - 前記糖源性アミノ酸がアルギニン、ヒスチジン、アスパラギン酸、及び、グルタミン酸からなる群より選択される少なくとも1種を含む、請求項1に記載の歯周病の体外診断方法。
- 前記電子メディエータが、フラビンモノヌクレオチド、リボフラビン、及び、2-ヒドロキシ-1,4-ナフトキノン(2-hydroxy-1,4-napthoquinone)からなる群より選択される少なくとも1種を含む、請求項1又は2に記載の歯周病の体外診断方法。
- 前記電子メディエータが、2-ヒドロキシ-1,4-ナフトキノンである、請求項1~3のいずれか1項に記載の歯周病の体外診断方法。
- 前記電気化学測定の方法が、前記電極の電位を制御して、前記電極を流れる電流を時間の関数として測定する方法である、請求項1~4のいずれか1項に記載の歯周病の体外診断方法。
- 前記電位が、銀-塩化銀電極に対して0Vを超えて、電位窓の上限値未満の範囲内である、請求項5に記載の歯周病の体外診断方法。
- 前記判断するための情報が、前記電気化学測定の開始から前記電流生成が検出されるまでの時間、及び、生成される電流の電流密度の最大値からなる群より選択される少なくとも1種の測定結果を含む、請求項1~6のいずれか1項に記載の歯周病の体外診断方法。
- 前記判断するための情報が、予め定められた基準値と、前記測定結果との比較情報を含む、請求項7に記載の歯周病の体外診断方法。
- 前記歯周病の原因菌が、ポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)を含む、請求項1~8のいずれか1項に記載の歯周病の体外診断方法。
- 検体を電極と接触させ、糖源性アミノ酸と2-ヒドロキシ-1,4-ナフトキノン(2-hydroxy-1,4-napthoquinone)との存在下、嫌気環境下で電気化学測定することと、
前記電気化学測定の結果、電流生成が検出された場合、前記検体に、ポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)が含まれると判断するための情報を提供することと、を含むPg菌検出方法。 - 前記電気化学測定の方法が、前記電極の電位を制御して、前記電極を流れる電流を時間の関数として測定する方法である、請求項10に記載のPg菌検出方法。
- 前記電位が、銀-塩化銀電極に対して0Vを超えて、電位窓の上限値未満の範囲内である、請求項11に記載のPg菌検出方法。
- 前記判断するための情報が、前記電気化学測定の開始から前記電流生成が検出されるまでの時間、及び、生成される電流の電流密度の最大値からなる群より選択される少なくとも1種の測定結果を含む、請求項10~12のいずれか1項に記載のPg菌検出方法。
- 前記判断するための情報が、予め定められた基準値と、前記測定結果との比較情報を含む、請求項13に記載のPg菌検出方法。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023531840A JPWO2023276785A1 (ja) | 2021-06-29 | 2022-06-21 | |
| EP22832933.0A EP4365585A1 (en) | 2021-06-29 | 2022-06-21 | In vitro diagnosis method for periodontal diseases, and pg bacterium detection method |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021-107163 | 2021-06-29 | ||
| JP2021107163 | 2021-06-29 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2023276785A1 true WO2023276785A1 (ja) | 2023-01-05 |
Family
ID=84691742
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2022/024727 WO2023276785A1 (ja) | 2021-06-29 | 2022-06-21 | 歯周病の体外診断方法、及び、Pg菌検出方法 |
Country Status (3)
| Country | Link |
|---|---|
| EP (1) | EP4365585A1 (ja) |
| JP (1) | JPWO2023276785A1 (ja) |
| WO (1) | WO2023276785A1 (ja) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004106541A1 (ja) | 2003-05-30 | 2004-12-09 | Kyushu Tlo Company, Limited | 歯周病マーカー |
| JP2005069836A (ja) * | 2003-08-22 | 2005-03-17 | Daikin Ind Ltd | 電極、タンパク測定装置及び酵素活性の測定方法 |
| JP2007084534A (ja) * | 2005-08-26 | 2007-04-05 | Osaka Univ | 口腔用組成物 |
| JP2018142541A (ja) * | 2017-02-28 | 2018-09-13 | 公立大学法人大阪府立大学 | 電気化学デバイスおよびその製造方法 |
| WO2020204075A1 (ja) * | 2019-04-02 | 2020-10-08 | 国立研究開発法人物質・材料研究機構 | 薬剤感受性測定方法、及び、薬剤感受性測定装置 |
| WO2020235403A1 (ja) * | 2019-05-20 | 2020-11-26 | 国立研究開発法人物質・材料研究機構 | 検出装置、及び、データ収集方法 |
| JP2021082394A (ja) * | 2019-11-14 | 2021-05-27 | Phcホールディングス株式会社 | 酵素電極およびバイオセンサ並びにバイオ燃料電池 |
-
2022
- 2022-06-21 WO PCT/JP2022/024727 patent/WO2023276785A1/ja active Application Filing
- 2022-06-21 EP EP22832933.0A patent/EP4365585A1/en active Pending
- 2022-06-21 JP JP2023531840A patent/JPWO2023276785A1/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004106541A1 (ja) | 2003-05-30 | 2004-12-09 | Kyushu Tlo Company, Limited | 歯周病マーカー |
| JP2005069836A (ja) * | 2003-08-22 | 2005-03-17 | Daikin Ind Ltd | 電極、タンパク測定装置及び酵素活性の測定方法 |
| JP2007084534A (ja) * | 2005-08-26 | 2007-04-05 | Osaka Univ | 口腔用組成物 |
| JP2018142541A (ja) * | 2017-02-28 | 2018-09-13 | 公立大学法人大阪府立大学 | 電気化学デバイスおよびその製造方法 |
| WO2020204075A1 (ja) * | 2019-04-02 | 2020-10-08 | 国立研究開発法人物質・材料研究機構 | 薬剤感受性測定方法、及び、薬剤感受性測定装置 |
| WO2020235403A1 (ja) * | 2019-05-20 | 2020-11-26 | 国立研究開発法人物質・材料研究機構 | 検出装置、及び、データ収集方法 |
| JP2021082394A (ja) * | 2019-11-14 | 2021-05-27 | Phcホールディングス株式会社 | 酵素電極およびバイオセンサ並びにバイオ燃料電池 |
Non-Patent Citations (3)
| Title |
|---|
| NAGATA, SHINICHIRO; OHSHIMA, TAKESHI; OHTSUKA, KEIICHI; SATO, SHINOBU; NAGAYOSHI, MASATO; KITAMURA, CHIAKI; NISHIHARA, TATSUJI; TA: "Electrochemical Detection of Periodontal Disease Using Protease Assay", PEPTIDE SCIENCE, PROTEIN RESEARCH FOUNDATION, MINOO,, JP, 1 March 2012 (2012-03-01), JP , pages 407 - 408, XP009542112, ISSN: 1344-7661 * |
| PARK SEONHWA, PARK KIRYEON, NA HEE SAM, CHUNG JIN, YANG HAESIK: "Washing- and Separation-Free Electrochemical Detection of Porphyromonas gingivalis in Saliva for Initial Diagnosis of Periodontitis", ANALYTICAL CHEMISTRY, AMERICAN CHEMICAL SOCIETY, US, vol. 93, no. 13, 6 April 2021 (2021-04-06), US , pages 5644 - 5650, XP093017847, ISSN: 0003-2700, DOI: 10.1021/acs.analchem.1c00572 * |
| SATO SHINOBU, SHINICHIRO NAGATA, JUNPEI SHIMAMOTO, TOSHINORI OKINAGA, WATARU ARIYOSHI, MICHIHIKO USUI, KEISUKE NAKASHIMA, TASTUJI : "An Electrochemical Protease Assay Using Ferrocenylpeptide for Screening of Periodontal Disease", BUNSEKI KAGAKU, vol. 70, no. 3, 5 March 2021 (2021-03-05), pages 199 - 206, XP093017849, DOI: 10.2116/bunsekikagaku.70.199 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2023276785A1 (ja) | 2023-01-05 |
| EP4365585A1 (en) | 2024-05-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Krishnaveni et al. | Electron transfer studies of a conventional redox probe in human sweat and saliva bio-mimicking conditions | |
| Kianipour et al. | Room temperature ionic liquid/multiwalled carbon nanotube/chitosan-modified glassy carbon electrode as a sensor for simultaneous determination of ascorbic acid, uric acid, acetaminophen, and mefenamic acid | |
| Jafari et al. | Non-invasive quantification of malondialdehyde biomarker in human exhaled breath condensate using self-assembled organic-inorganic nanohybrid: a new platform for early diagnosis of lung disease | |
| Levent et al. | Application of a pencil graphite electrode for voltammetric simultaneous determination of ascorbic acid, norepinephrine, and uric acid in real samples | |
| Wang et al. | A strategy to differentiate dopamine and levodopa based on their cyclization reaction regulated by pH | |
| WO2020225357A1 (en) | Method and device for detecting nicotine in sweat | |
| JP5088148B2 (ja) | 代謝物濃度を測定する方法及びこれに用いられる電気化学センサ | |
| JP2013208259A (ja) | ダイヤモンド微小電極を用いた還元型グルタチオンの測定装置 | |
| WO2023276785A1 (ja) | 歯周病の体外診断方法、及び、Pg菌検出方法 | |
| Nithianandam et al. | Flexible, Miniaturized Sensing Probes Inspired by Biofuel Cells for Monitoring Synaptically Released Glutamate in the Mouse Brain | |
| TW201102649A (en) | Metabolites for oral health and uses thereof | |
| JPH08511625A (ja) | ガス濃度の測定 | |
| Savitri et al. | The Dependence of Boron Concentration in Diamond Electrode for Ciprofloxacin Electrochemical Sensor Application | |
| Mitsumori et al. | A new approach to noninvasive measurement of blood glucose using saliva analyzing system | |
| Kumar et al. | Electrochemical behavior of melatonin and its sensing in pharmaceutical formulations and in human urine | |
| EP0630204B1 (en) | Measuring sulfides within a periodontal pocket | |
| KR100541266B1 (ko) | 경피 글루코스 측정용 전극의 조성 | |
| Sutow et al. | Corrosion potential variation of aged dental amalgam restorations over time | |
| JP5360907B2 (ja) | 有機化合物検出用電極及びそれを使用した有機化合物濃度の電気化学検出装置 | |
| Sannino et al. | Preliminary impedance spectroscopy study for carious lesions detection | |
| KR20030047971A (ko) | 피부 관통형 글루코스 바이오센서 | |
| JPH095321A (ja) | 生化学物質測定装置及びそれに適用する唾液収集方法 | |
| Justice et al. | In vivo voltammetry | |
| KR102455729B1 (ko) | 퓨린 대사체 검출 물질 및 이를 이용한 바이오센서 | |
| Cherebin | Electrochemical Tape-And-Paper-Based PH Sensors Suitable for Oral PH Measurements |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 22832933 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2023531840 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 18569549 Country of ref document: US |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2022832933 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2022832933 Country of ref document: EP Effective date: 20240129 |