이하, 첨부된 도면을 참조하여, 발명의 내용을 특정한 구현예와 예시들을 통해 더욱 상세하게 설명한다. 상기 첨부된 도면은 발명의 일부 구현예를 포함하지만, 모든 구현예를 포함하고 있지는 않다는 점에 유의해야 한다. 본 명세서에 의해 개시되는 발명의 내용은 다양하게 구현될 수 있으며, 여기에 설명되는 특정 구현예로 제한되지 않는다. 본 명세서에 개시된 발명이 속한 기술분야에 있어 통상의 기술자라면, 본 명세서에 개시된 발명의 내용에 대한 많은 변형 및 다른 구현예들을 떠올릴 수 있을 것이다. 따라서, 본 명세서에서 개시된 발명의 내용은 여기에 기재된 특정 구현예로 제한되지 않으며, 이에 대한 변형 및 다른 구현예들도 청구범위 내에 포함되는 것으로 이해되어야 한다.
용어 정의
본 명세서에서 사용하는 주요 용어에 대한 정의는 아래와 같다.
UBR (Ubiquitin protein ligase E3 component n-recognin)
본 명세서에서 사용되는 용어 UBR은 Ubiquitin protein ligase E3 component n-recognin의 약자를 의미한다. 상기 UBR은 단백질의 N-말단 잔기를 인식하는 N-레코그닌이며, 포유류 내에 UBR 1 내지 7의 적어도 7가지 종류가 존재한다고 알려져 있다. 상기 UBR은 N-레코그닌으로, 생체 내 단백질 분해 경로인 N-말단 법칙 경로에 연관되어 있다. 구체적으로, 상기 UBR은 단백질의 N-말단 분해 신호(N-degron)를 인식하며, 기질 단백질이 유비퀴틴 프로테아좀 경로를 통해 분해되는 과정에 연관되어 있다.
UBR 박스 도메인(UBR box domain)
본 명세서에서 사용되는 용어 UBR 박스 도메인은 UBR 단백질 내에 존재하는 도메인으로 징크 핑거 모티프이다. 상기 UBR 단백질은 UBR 1 내지 7 단백질을 포함한다. 상기 UBR 박스 도메인은 기질(substrate) 단백질이 결합하는 도메인으로 알려져 있다. 본 명세서에 개시되는 UBR 박스 도메인 리간드로의 화합물은 상기 UBR 박스 도메인에 결합하여 UBR 박스 도메인 기질의 결합을 억제할 수 있다. 더 나아가, 본 명세서에서 개시되는 UBR 박스 도메인 리간드로의 화합물은 세포 내 단백질 분해 경로에 영향을 줄 수 있다.
RING 도메인(RING domain)
본 명세서에서 사용되는 용어 RING 도메인은 UBR 1, 2 및 3 단백질 내에 존재한다고 알려져 있다. 상기 RING 도메인은 RING 유비퀴틴화 도메인이라는 용어로도 사용될 수 있다. 상기 RING 도메인은 단백질 내에 존재하는 도메인으로 징크 핑거 모티프이다. 상기 RING 도메인은 E2에 있는 유비퀴틴이 기질 단백질로 이동되는 과정에 중요한 역할을 하는 도메인으로, RING 도메인은 상기 유비퀴틴이 기질 단백질로 이동되는 과정이 한 단계(one-step)로 일어나게 하는 역할을 한다.
HECT 도메인(HECT domain)
본 명세서에서 사용되는 용어 HECT 도메인은 UBR 5 단백질 내에 존재한다고 알려져 있다. 상기 HECT 도메인은 HECT 유비퀴틴화 도메인이라는 용어로도 사용될 수 있다. 상기 HECT 도메인은 E2에 있는 유비퀴틴이 기질 단백질로 이동되는 과정에 중요한 역할을 하는 도메인이다. E2에 있는 유비퀴틴은 HECT 도메인에 전달되고, 그 후 기질 단백질로 이동되게 된다. 즉, HECT 도메인은 상기 유비퀴틴이 기질 단백질로 이동되는 과정이 두 단계(two step)로 일어나게 하는 역할을 한다.
징크 핑거 모티프(zinc finger motif)
본 명세서에서 사용되는 용어 징크 핑거 모티프는 단백질의 구조를 안정시키기 위해 하나 이상의 아연(Zinc) 이온이 존재하는 단백질 구조 모티프를 의미한다. 본 명세서의 UBR 박스 도메인 및 RING 도메인은 징크 핑거 모티프이다.
리간드(ligand)
본 명세서에서 사용되는 용어 리간드는 단백질에 특이적으로 결합하는 물질을 의미한다. 상기 단백질은 효소 또는 수용체를 포함하며, 상기 단백질이 효소인 경우 리간드는 효소에 결합하는 기질 등을 의미할 수 있고, 상기 단백질이 수용체인 경우 리간드는 수용체에 결합하는 호르몬 등을 의미할 수 있다.
본 명세서에서 제공하는 UBR 박스 도메인 리간드로의 화합물은 UBR 박스 도메인에 결합하는 화합물을 의미한다. 일 실시예로, 상기 화합물은 UBR 단백질 내의 UBR 박스 도메인에 결합하는 화합물을 의미한다. 구체적인 일 실시예로, 상기 화합물은 UBR1 내지 7 중 하나 이상의 단백질 내에 존재하는 UBR 박스 도메인에 결합하는 화합물을 의미한다. 다만, 이에 제한되지 않는다.
본 명세서에서 제공하는 UBR 박스 도메인 리간드로의 화합물은 UBR 박스 도메인의 기질과 경쟁적으로 작용할 수 있다. 즉, 상기 화합물은 UBR 박스 도메인의 기질이 결합하는 것을 억제할 수 있다. 또한, 상기 화합물은 상기 기질의 결합을 억제하여 기질의 분해를 저해할 수 있다.
아미노알킬(aminoalkyl)
본 명세서에서 사용되는 용어 아미노알킬은 아미노기로 치환된 알킬 모이어티를 의미한다. 상기 아미노알킬기는 -CH(NH2)CH3 및 -CH2(NH2)를 포함한다.
시클로알킬(cycloalkyl) 및 헤테로시클로알킬(heterocycloalkyl)
본 명세서에서 사용되는 용어 시클로알킬은 하나 이상의 포화 고리 구조를 함유하는 카보시클릭기를 의미하며 바이시클릭을 포함한다. 시클로알킬은 예시로 시클로프로필(cyclopropyl), 시클로부틸(cyclobutyl), 시클로펜틸(cyclopentyl), 시클로헥실(cyclohexyl), 시클로헵틸(cycloheptyl) 및 시클로옥틸(cyclooctyl)를 포함한다.
헤테로시클로알킬은 상기 시클로알킬에서 고리-탄소 원자 외에 P, N, O 및 S로부터 선택된 1개 이상의 헤테로 원자를 포함하는 고리 구조를 의미한다.
헤테로시클릴(heterocyclyl)
본 명세서에서 사용되는 용어 헤테로시클릴은 2 내지 14개의 고리 탄소 원자의 불포화, 포화 또는 부분 불포화 모노시클릴, 바이시클릭, 또는 트리시클릭기를 지칭하고, 고리-탄소 원자 외에 P, N, O 및 S로부터 선택된 1개 이상의 헤테로 원자를 포함한다. 상기 헤테로시클릴은 헤테로시클로알킬을 포함한다. 다양한 실시 양태에서 헤테로시클릭기는 탄소 또는 헤테로 원자를 통해 또 다른 모이어티에 부착되고, 탄소 또는 헤테로 원자 상에서 임의로 치환된다. 헤테로시클릴의 예는 아제티디닐(azetidinyl), 벤조이미다졸릴(benzoimidazolyl), 벤조푸라닐(benzofuranyl), 벤조푸라자닐(benzofurazanyl), 벤조피라졸릴(benzopyrazolyl), 벤조트리아졸릴(benzotriazolyl), 벤조티오페닐(benzothiophenyl), 벤족사졸릴(benzoxazolyl), 카르바졸릴(carbazolyl), 카볼리닐(carbolinyl), 신놀리닐(cinnolinyl), 푸라닐(furanyl), 이미다졸릴(imidazolyl), 인돌리닐(indolinyl), 이소인돌리닐(isoindolinyl), 인돌릴(indolyl), 인돌라지닐(indolazinyl), 인다졸릴(indazolyl), 이소벤조푸라닐(isobenzofuranyl), 이소인돌릴(isoindolyl), 이소퀴놀릴(isoquinolyl), 이소티아졸릴(isothiazolyl), 이속사졸릴(isoxazolyl), 나프트피리디닐(naphthpyridinyl), 옥사디아졸릴(oxadiazolyl), 옥사졸릴(oxazolyl), 옥사졸린(oxazoline), 이속사졸린(isooxazoline), 옥세타닐(oxetanyl), 피라닐(pyranyl), 피라지닐(pyrazinyl), 피라졸릴(pyrazolyl), 피리다지닐(pyridazinyl), 피리도피리디닐(pyridopyridinyl), 피리다지닐(pyridazinyl), 피리딜(pyridyl), 피리미딜(pyrimidyl), 피롤릴(pyrrolyl), 퀴나졸리닐(quinazolinyl), 퀴놀릴(quinolyl), 퀴녹살리닐(quinoxalinyl), 테트라히드로피라닐(tetrahydropyranyl), 테트라히드로티오피라닐(tetrahydrothiopyranyl), 테트라히드로이소퀴놀리닐(tetrahydroisoquinolinyl), 테트라졸릴(tetrazolyl), 테트라졸로피리딜(tetrazolopyridyl), 티아디아졸릴(thiadiazolyl), 티아졸릴(thiazolyl), 티에닐(thienyl), 트리아졸릴(triazolyl), 아제티디닐(azetidinyl), 1,4-디옥사닐(1,4-dioxanyl), 헥사히드로아제피닐(hexahydroazepinyl), 피페라지닐(piperazinyl), 피페리디닐(piperidinyl), 피리딘-2-오닐(pyridin-2-only), 피롤리디닐(pyrrolidinyl), 피롤로피리디닐(pyrrolopyridinyl), 모르폴리닐(morpholinyl), 티오모르폴리닐(thiomorpholinyl), 디하이드로벤조이미다졸릴(dihydrobenzoimidazolyl), 디하이드로벤조푸라닐(dihydrobenzofuranyl), 디하이드로벤조티오페닐(dihydrobenzothiophenyl), 디하이드로벤족사졸릴(dihydrobenzoxazolyl), 디하이드로푸라닐(dihydrofuranyl), 디하이드로이미다졸릴(dihydroimidazolyl), 디하이드로인돌릴(dihydroindolyl), 디하이드로이소옥사졸릴(dihydroisooxazolyl), 디하이드로이소티아졸릴(dihydroisothiazolyl), 디하이드로옥사디아졸릴(dihydrooxadiazolyl), 디하이드로옥사졸릴(dihydrooxazolyl), 디하이드로피라지닐(dihydropyrazinyl), 디하이드로피라졸릴(dihydropyrazolyl), 디하이드로피리디닐(dihydropyridinyl), 디하이드로피리미디닐(dihydropyrimidinyl), 디하이드피롤릴(dihydropyrrolyl), 디하이드로퀴놀리닐(dihydroquinolinyl), 디하이드로테트라졸릴(dihydrotetrazolyl), 디하이드로티아디아졸릴(dihydrothiadiazolyl), 디하이드로티아졸릴(dihydrothiazolyl), 디하이드로티에닐(dihydrothienyl), 디하이드로트리아졸릴(dihydrotriazolyl), 디하이드로아제티디닐(dihydroazetidinyl), 메틸렌디옥시벤조일(methylenedioxybenzoyl), 테트라히드로푸라닐(tetrahydrofuranyl) 및 테트라히드로티에닐(tetrahydrothienyl) 등을 포함한다.
달리 정의되지 않는 한, 본 명세서에서 사용되는 모든 기술적 및 과학적 용어는 본 발명이 속하는 기술분야의 당업자에 의해 통상적으로 이해되는 것과 동일한 의미를 가진다. 본 명세서에서 언급된 모든 간행물, 특허 및 기타 다른 참고문헌은 전체가 참고로 포함된다.
이하, 발명의 구체적인 내용을 개시한다.
Ⅰ. UBR 박스 도메인
1.개요
본 명세서에서 제공하는 UBR 박스 도메인 리간드로의 화합물은 UBR 박스 도메인에 결합한다. 상기 UBR 박스 도메인은 N-말단 잔기 서열 또는 N-말단 분해 신호가 결합하는 도메인으로 알려져 있다. 상기 도메인은 N-말단 경로 법칙에 의해 단백질이 분해되는 과정에 연관되어 있다. 따라서, 상기 화합물은 N-말단 법칙 경로를 통한 단백질 분해 과정에 영향을 미칠 수 있다.
2.N-말단 법칙 경로(N-end rule pathway)
세포들은 단백질 분해를 통해 단백질의 양을 조절한다. 이 때, 단백질의 분해 과정은 단백질의 분해 신호인 데그론(degron)을 인식하는 과정을 통해 진행된다고 알려져 있다. 구체적으로, 단백질의 N-말단 잔기서열에 의존적으로 단백질 분해가 조절되고, N-말단에 존재하는 단백질 분해 신호들을 통틀어 N-데그론(N-degron)이라고 한다. 상기 N-데그론은 N-말단에 양전하를 갖는 잔기(예, 아르기닌, 라이신, 히스티딘) 또는 크기가 큰 소수성 잔기(페닐알라닌, 류신, 트립토판, 이소류신, 티로신)를 가지는 것을 포함한다. 이와 같이 단백질의 반감기는 그 단백질의 N-말단에 존재하는 아미노산 잔기가 무엇인가에 의해 결정된다는 연관성을 기초로 N-말단 법칙(N-end rule)이라는 용어가 사용되었다.
3.UBR 박스 도메인
상기 N-말단 법칙 경로에서 N-데그론은 N-레코그닌에 의해 인식되는데, N-레코그닌으로 UBR(Ubiquitin protein ligase E3 component n-recognin)이 발견되었다. 상기 UBR은 UBR 박스 도메인을 통해 N-말단 잔기 서열 또는 N-말단 분해 신호를 인식한다고 알려져 있다. 즉, UBR이 UBR 박스 도메인을 통해 단백질 분해 신호를 인식하고, 이를 통해 단백질의 분해 과정이 진행된다.
상기 UBR에 의한 단백질 분해 과정은 아래의 내용을 포함할 수 있다. UBR 박스 도메인이 N-말단 분해 신호를 가진 기질을 인식하고, 상기 기질에 유비퀴틴이 결합되고, 유비퀴틴이 결합된 기질은 프로테아좀에 의해 분해될 수 있다. 즉, N-말단 분해 신호를 가진 기질이 유비퀴틴 프로테아좀 시스템(Ubiquitin proteasome system, UPS)에 의해 분해될 수 있다.
Ⅱ. UBR 박스 도메인 리간드
1.개요
1)본 명세서의 화합물은 UBR 박스 도메인의 구조 및 N-말단 경로 기질과의 결합 특성을 반영한다
본 명세서에서 개시하는 UBR 박스 도메인 리간드로의 화합물은 UBR 박스 도메인의 구조 및 UBR 박스 도메인과 N-말단 경로 기질과의 결합 형태를 고려하여 설계되었다.
UBR 박스 도메인에 존재하는 다양한 아미노산들은 N-말단 경로 기질의 아미노산과 이온 상호작용(ionic interaction), 수소 결합(hydrogen bond), 소수성 작용(hydrophobic interaction) 등으로 상호작용하며 결합한다. 이러한 결합 모드를 분석하여 본 명세서에서는 UBR 박스 도메인과 적합한 결합 모드를 형성할 수 있는 저분자 화합물이 합성되어 제공된다. 나아가, 본 명세서에서는 이하 화학식 1 내지 55에 의한 화합물이 제공된다.
2)본 명세서의 화합물은 UBR 박스 도메인에 잘 결합하도록 하는 코어 구조를 가진다
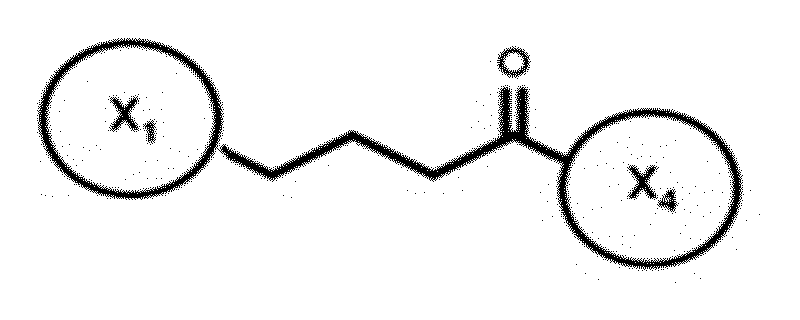
본 명세서에서는, 상기에서 기재한 바와 같이 UBR 박스 도메인과 N-말단 경로 기질의 아미노산과의 결합 모드가 분석되어, 화합물의 코어 구조가 도출되었다. 본 명세서에서 제공되는 화합물은 화합물의 코어 구조를 바탕으로 도출된 아래의 [화학식 1]의 구조를 가질 수 있다. [화학식 1]은 아래와 같다:
[화학식1]
본 명세서에서는 상기 [화학식 1]을 바탕으로 다양한 화합물이 설계되어 제공된다. 이 때, X1, X2, X3, B1, A1, B1, X4에 대한 후보들은 UBR 박스 도메인과의 결합 모드를 고려하여 도출되었다. 상기 [화학식 1]을 바탕으로 한 다양한 화합물들에 대한 보다 자세한 설명은 아래에 기재되어 있다.
2.화학식 1
[화학식 1]
1)X2 , B1 , X3 및 A1
①X2
상기 화학식 1에서 X2는 본 명세서에 개시되는 화합물 내에 꺾임 구조를 유발하는 구조일 수 있다. 상기 꺾임 구조는 본 명세서에 개시되는 화합물의 X1이 UBR 박스 도메인과 상호작용(charge-charge interaction) 혹은 수소결합 혹은 소수성 작용을 원활하게 유지하며 결합력을 높이는데 도움을 줄 수 있다. 이에 따라, 일 실시예로, 상기 X2는 꺾임 구조를 유발할 수 있는 다양한 구조들 중의 하나일 수 있다. 구체적인 일 실시예로, 상기 X2는 SO2 또는 CRaRb 일 수 있다. 이 때, 상기 Ra 및 Rb는 각각 독립적으로 H 또는 CH2로부터 선택될 수 있다. 나아가, 상기 X2는 CH2, CH(CH3) 또는 C(CH3)2 일 수 있다. 다른 구체적인 일 실시예로, 상기 X2는 SO2일 수 있다.
② B1, X3 및 A1
상기 화학식 1에서 A1은 일 실시예로, CH2 또는 NH일 수 있다.
상기 화학식 1에서 B1은 일 실시예로, CH2 또는 NH일 수 있다.
상기 화학식 1에서 X3는 일 실시예로, CH2 또는 NH일 수 있다.
이때, 일 실시예로, 상기 화학식 1에서 B1이 CH2인 경우, X3는 CH2가 아닐 수 있다.
다만, 이에 제한되지 않는다.
③ X2, B1, X3 및 A1의 예시
상기 화학식 1은 일 실시예로, 아래로부터 선택된 구조를 가질 수 있다:
[화학식 1-1] [화학식 1-2]
[화학식 1-3] [화학식 1-4]
[화학식 1-5] [화학식 1-6]
[화학식 1-7] [화학식 1-8]
[화학식 1-9] [화학식 1-10]
[화학식 1-11] [화학식 1-12]
[화학식 1-13] [화학식 1-14]
[화학식 1-15] [화학식 1-16]
[화학식 1-17] [화학식 1-18]
[화학식 1-19] [화학식 1-20]
[화학식 1-21] [화학식 1-22]
[화학식 1-23] [화학식 1-24]
[화학식 1-25] [화학식 1-26]
[화학식 1-27] [화학식 1-28]
[화학식 1-29] [화학식 1-30]
[화학식 1-31] [화학식 1-32]
[화학식 1-33] [화학식 1-34]
[화학식 1-35] [화학식 1-36]
[화학식 1-37] [화학식 1-38]
[화학식 1-39] [화학식 1-40]
[화학식 1-41] [화학식 1-42]
[화학식 1-43] [화학식 1-44]
[화학식 1-45]
구체적인 일 실시예로, 상기 화학식 1에서,
-X2-B1-X3 은 -SO2-NH-NH, -SO2-NH-CH2, -SO2-CH2-NH 및 -CH2-NH-NH으로 구성된 군에서 선택되고,
A1은 CH2 또는 NH이고,
I는 0 또는 1의 정수이다.
상기 화학식 1은 구체적인 일 실시예로, 아래로부터 선택된 구조를 가질 수 있다:
[화학식 1-1]
[화학식 1-2]
[화학식 1-3]
[화학식 1-4]
2)X1
UBR1과 UBR2의 UBR 박스와 N-데그론(degron)의 복합체 구조 분석과 화학식 1의 코어 구조를 가진 화합물과 분자 도킹 연구(molecular docking study)를 수행한 결과, 상기 화학식 1에서 X1은 N-데그론의 첫 번째 잔기(N1)의 사이드 체인(side chain)에 해당되며 X1은 음전하 지역(negative charged-surrounded region)에 결합할 것으로 예상된다. 이에 따라, 일 실시예로, 상기 화학식 1에서 X1은 전하를 가지거나 수소결합을 형성하는 모이어티(moiety)를 포함하는 고리 구조를 가질 수 있다. 구체적인 일 실시예로, 상기 X1은 전하를 가지거나 수소결합을 형성하는 모이어티를 포함하는 플래너(Planar) 구조를 가지는 고리 구조일 수 있다. 추가적으로, 상기 화합물이 다른 물질과 결합되어 사용되는 경우, 상기 화학식 1에서 X1은 링커와 결합할 수 있는 구조를 포함할 수 있다.
일 실시예로, 상기 X1은 임의적으로 하나 이상의 R2로 치환되거나 비치환된 페닐, 시클로알킬 또는 헤테로시클릴일 수 있다. 구체적인 일 실시예로, 상기 X1은 임의적으로 하나 이상의 R2로 치환되거나 비치환된 페닐, 시클로헥실, 시클로펜틸, 푸라닐, 티아졸릴, 1H-피라졸릴, 피롤리디닐, 피페리디닐, 피페라지닐, 모르폴리닐, 인돌리닐, 1H-인돌리닐, 1H-인돌릴, 1H-인다졸릴, 이소인돌리닐, 인돌린-2-오닐, 2,3-디히드로-1H-인데닐 및 1H-피롤로피리디닐로부터 선택될 수 있다. 이때, 각각의 R2는 독립적으로 알킬, 알콕시, 아미노, 아미노알킬, -NO2, =O, -NHC2H4OH, -C(=NH)NH2, -C(=O)NH2, -C(=O)NHCH3, -C(=O)OH, 페닐 또는 헤테로시클로알킬로부터 선택될 수 있다. 일 실시예로, 각각의 R2는 독립적으로 메틸, 에틸, 아미노, 아미노알킬, 아미노(히드록시알킬), 메톡시, 에톡시, -C(=NH)NH2, -C(=O)NH2, -C(=O)OH, 페닐, 피롤리디닐, 피페라지닐, 피페리디닐 및 모르폴리닐로부터 선택될 수 있다. 구체적인 일 실시예로, R2는 아미노일 수 있다.
더 구체적인 일 실시예로, 상기 X1은 아래의 구조로부터 선택될 수 있다:
보다 더 구체적인 일 실시예로, 상기 X1은 아래의 구조로부터 선택될 수 있다:
3)X4
상기 화학식 1에서 X4는 N-데그론의 두 번째 잔기(N2)의 사이드 체인(side chain)에 해당되며 UBR 박스와 결합 시 결합 공간을 채우는 역할을 할 수 있도록 고리 혹은 사슬 구조를 가질 수 있다. 이때, 일 실시예로 상기 고리 혹은 사슬 구조는 전하를 가지거나 수소 결합을 형성하는 모이어티가 도입되어 결합력을 높일 수 있다. 추가적으로, X4는 본 명세서의 화합물이 추후 다른 물질과 결합하여 이용되는 경우, 링커와 결합하는 역할을 수행할 수 있는 구조를 포함할 수 있다.
일 실시예로, 상기 X4는 임의적으로 하나 이상의 R3로 치환되거나 비치환된 페닐, 시클로알킬 또는 헤테로시클릴일 수 있다. 구체적인 일 실시예로, 상기 X4은 임의적으로 하나 이상의 R3로 치환되거나 비치환된 페닐, 시클로헥실, 시클로펜틸, 푸라닐, 티아졸릴, 1H-피라졸릴, 피롤리디닐, 피페리디닐, 피페라지닐, 모르폴리닐, 인돌리닐, 1H-인돌리닐, 1H-인돌릴, 1H-인다졸릴, 이소인돌리닐, 인돌린-2-오닐, 2,3-디히드로-1H-인데닐 및 1H-피롤로피리디닐로부터 선택될 수 있다. 이때, 각각의 R3는 독립적으로 알킬, 알콕시, 아미노, 할로, 히드록실, 알킬아미노, 디알킬아미노, -NO2, -CONR'R'', -CO2R', -NHCOR', 페닐 또는 헤테로시클로알킬로부터 선택될 수 있다. 일 실시예로, 각각의 R3는 독립적으로 히드록실, 플루오로, 클로로, 브로모, 아미노, 메틸, 에틸, 이소프로필, 메톡시, 에톡시, 이소프로필옥시, 알킬아미노, 디알킬아미노, -NO2, -C(=O)NH2, -CO2R', -NHCOR', -CONR'R'' 및 페닐로부터 선택될 수 있다. 구체적인 일 실시예로, R3는 히드록실일 수 있다. 이때, 각각의 R' 및 R''는 독립적으로 -H 또는 알킬일 수 있다.
더 구체적인 일 실시예로, 상기 X4는 아래로부터 선택될 수 있다:
보다 더 구체적인 일 실시예로, 상기 X4는 아래로부터 선택될 수 있다:
본 명세서에서 개시되는 화합물은 입체 이성질체 또는 이의 염의 형태로 존재할 수 있으며, 이와 같은 화합물의 이성질체 또는 염의 형태가 본 명세서의 범위에 포함된다.
Ⅲ. UBR 박스 도메인 리간드로의 화합물의 구체적인 예시
1.화합물의 구체적인 예시
아래의 내용은 본 명세서에서 개시되는 화합물의 구체적인 실시예들을 나타낸다. 아래의 구체적인 실시예들은 본 명세서에서 개시하는 화합물의 용이한 이해를 위한 예시적인 구조들이며, 아래의 실시예들로 본 명세서에서 개시하는 화합물의 범위가 제한되지 않는다.
구체적인 일 실시예로, 본 명세서에서 개시하는 화합물은 [화학식 1-1]의 구조를 가질 수 있다:
[화학식 1-1]
이때, 상기 화합물에서 A1은 CH2 또는 NH이고, I는 0 또는 1의 정수이다.
상기 X1 및 X4는 목차 Ⅱ. UBR 박스 도메인 리간드의 2) X1 및 3)X4에 기재된 내용과 동일하게 적용된다.
보다 더 구체적인 일 실시예로, [화학식 1-1]에 대한 구체적인 예시 화합물은 아래로부터 선택될 수 있다.
화학식 [1-1]에 대한 구체적인 예시 화합물
| 화합물번호 |
화합물 |
| 1 |
N'-(4-히드록시벤조일)-4-메틸벤젠설포노히드라지드 |
| 2 |
4-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 3 |
4-아미노-N'-(4-히드록시벤조일)-3-모르폴리노벤젠설포노히드라지드 |
| 4 |
N'-(4-히드록시벤조일)-2-옥소인돌린-5-설포노히드라지드 |
| 5 |
N'-(4-히드록시벤조일)인돌린-5-설포노히드라지드 |
| 6 |
N'-([1,1'-바이페닐]-4-카르보닐)-4-아미노벤젠설포노히드라지드 |
| 7 |
N'-([1,1'-바이페닐]-3-카르보닐)-4-아미노벤젠설포노히드라지드 |
| 8 |
3-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 9 |
4-(1-아미노에틸)-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 10 |
3,5-디아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 11 |
N'-(4-히드록시벤조일)-4-((2-히드록시에틸)아미노)벤젠설포노히드라지드 |
| 13 |
N'-(4-히드록시벤조일)-4-메톡시벤젠설포노히드라지드 |
| 14 |
4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤지미드아미드 |
| 15 |
4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤즈아미드 |
| 17 |
6-아미노-N'-(4-히드록시벤조일)-[1,1'-바이페닐]-3-설포노히드라지드 |
| 18 |
4-(2-((4-아미노페닐)설포닐)히드라진-1-카르보닐)벤즈아미드 |
| 20 |
4-아미노-N'-(1H-인돌-3-카르보닐)벤젠설포노히드라지드 |
| 21 |
4-아미노-N'-(4-히드록시벤조일)-3-(피롤리딘-1-일)벤젠술포노히드라지드 |
| 22 |
N'-(4-히드록시벤조일)-4-니트로-3-(피롤리딘-1-일)벤젠설포노히드라지드 |
| 23 |
4-아미노-N'-(4-히드록시벤조일)-3-(피페리딘-1-일)벤젠설포노히드라지드 |
| 24 |
N'-(4-히드록시벤조일)-1H-피라졸-4-설포노히드라지드 |
| 25 |
N'-(4-히드록시벤조일)인돌린-4-설포노히드라지드 |
| 26 |
N'-(4-히드록시벤조일)-1H-인돌-4-설포노히드라지드 |
| 27 |
2-((4-아미노페닐)설포닐)-N-페닐히드라진-1-카르복사미드 |
| 28 |
4-아미노-N'-(1H-인돌-4-카르보닐)-3-모르폴리노벤젠설포노히드라지드 |
| 29 |
4-아미노-N'-(인돌린-4-카르보닐)벤젠설포노히드라지드 |
| 30 |
4-아미노-N'-(4-히드록시벤조일)-3-(페파라진-1-일)벤젠설포노히드라지드 |
| 31 |
4-아미노-N'-(2,3-디히드로-1H-인덴-2-카르보닐)벤젠설포노히드라지드 |
| 32 |
4-아미노-N'-(이소인돌린-2-카르보닐)벤젠설포노히드라지드 |
| 33 |
N'-(4-히드록시벤조일)-1H-인돌-2-설포노히드라지드 |
| 34 |
4-아미노-N'-(2-페닐아세틸)벤젠설포노히드라지드 |
| 35 |
N'-(4-히드록시벤조일)-1H-인다졸-3-설포노히드라지드 |
| 36 |
4-아미노-N'-(인돌린-6-카르보닐)벤젠설포노히드라지드 |
| 37 |
4-아미노-N'-(인돌린-3-카르보닐)벤젠설포노히드라지드 |
| 38 |
N'-(4-히드록시벤조일)피페리딘-4-설포노히드라지드 |
| 39 |
4-아미노-N'-(인돌린-6-카르보닐)-3-모르폴리노벤젠설포노히드라지드 |
| 40 |
4-아미노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드 |
| 41 |
4-아미노-3-모르폴리노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드 |
| 42 |
N'-(4-히드록시벤조일)-2-메틸티아졸-4-설포노히드라지드 |
| 43 |
(1S,4S)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드 |
| 44 |
(1R,4R)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드 |
| 45 |
4-((2-(4-히드록시벤조일)히드라지닐)설포닐)-5-메틸퓨란-2-카르복실산 |
| 46 |
N'-(4-히드록시벤조일)피롤리딘-3-설포노히드라지드 |
| 47 |
N'-(4-히드록시벤조일)-1H-피롤로[2,3-b]피리딘-2-설포노히드라지드 |
| 52 |
2-((4-아미노페닐)설포닐)-N-(3-히드록시페닐)히드라진 -1-카르복사미드 |
| 53 |
2-((4-아미노-3-모르폴리노페닐)설포닐)-N-페닐히드라진-1-카르복사미드 |
다른 구체적인 일 실시예로, 본 명세서에서 개시하는 화합물은 [화학식 1-2]의 구조를 가질 수 있다:[화학식 1-2]
이때, 상기 화합물에서 상기 X1 및 X4는 목차 Ⅱ. UBR 박스 도메인 리간드의 2) X1 및 3)X4에 기재된 내용과 동일하게 적용된다.
[화학식 1-2]에 대한 구체적인 예시 화합물은 아래로부터 선택될 수 있다.
화학식 [1-2]에 대한 구체적인 예시 화합물
| 화합물번호 |
화합물 |
| 19 |
N'-(4-아미노벤질)-4-히드록시벤조히드라지드 |
| 48 |
4-히드록시-N'-(4-메톡시벤질)벤조히드라지드 |
| 49 |
N'-(4-아미노벤질)-2,3-디히드로-1H-인덴-2-카르보히드라지드 |
다른 구체적인 일 실시예로, 본 명세서에서 개시하는 화합물은 [화학식 1-3]의 구조를 가질 수 있다:[화학식 1-3]
이때, 상기 화합물에서 상기 X1 및 X4는 목차 Ⅱ. UBR 박스 도메인 리간드의 2) X1 및 3)X4에 기재된 내용과 동일하게 적용된다.
[화학식 1-3]에 대한 구체적인 예시 화합물은 아래로부터 선택될 수 있다.
화학식 [1-3]에 대한 구체적인 예시 화합물
| 화합물번호 |
화합물 |
| 12 |
4-아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드 |
| 50 |
4-아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)-3-모르폴리노벤젠설폰아미드 |
| 51 |
3,5-디아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드 |
다른 구체적인 일 실시예로, 본 명세서에서 개시하는 화합물은 [화학식 1-4]의 구조를 가질 수 있다:
[화학식 1-4]
[화학식 1-4]에 대한 구체적인 예시 화합물은 아래로부터 선택될 수 있다.
화학식 [1-4]에 대한 구체적인 예시 화합물
| 화합물번호 |
화합물 |
| 16 |
N-(((4-아미노페닐)설포닐)메틸)-4-히드록시벤즈아미드 |
| 54 |
4-히드록시-N-(((4-메톡시페닐)설포닐)메틸)벤즈아미드 |
| 55 |
N-(((4-아미노페닐)설포닐)메틸)-[1,1'-바이페닐]-4-카르복사미드 |
이때, 상기 화합물은 이의 가능한 이성질체 중 하나의 형태 또는 이의 혼합물의형태가 고려될 수 있다. 예를 들어, 거울상 이성질체(enantiomer) 및 부분 입체 이성질체(diastereomer)를 포함하는 모든 입체 이성질체(stereoisomer) 또는 이의 혼합물(예, 라세미 혼합물)이 고려될 수 있다.
2.상기 화합물의 염
본 명세서에서 개시되는 화합물은 이의 염의 형태가 고려될 수 있다. 이때, 염은 제약상 허용되는 염을 포함한다. 본 명세서에서 개시되는 염은 산 부가염(acid addition salt) 또는 염기 부가염(basic addition salt)을 포함한다. 상기 염을 형성하는 예시적인 산은 염산, 황산, 인산, 글리콜산, 락트산, 피루브산, 시트르산, 숙신산, 글루타르산 등을 포함하고, 염을 형성하는 예시적인 염기는 리튬, 나트륨, 칼륨, 칼슘, 마그네슘, 메틸아민, 트리메틸 아민 등을 포함한다. 다만, 이에 제한되지 않고 당업자에 의해 쉽게 선택될 수 있다.
Ⅳ. 화합물의 용도
1.UBR 박스 도메인 기질 결합 억제
UBR 박스 도메인 기질 결합 억제용 조성물(A composition for inhibition of UBR box domain substrate binding)
본 명세서에 개시되는 화합물은 UBR 박스 도메인 기질의 결합 억제를 위한 조성물 제조에 사용될 수 있다. 일 실시예로, 본 명세서에 개시되는 상기 화합물을 포함하는 조성물은 UBR 박스 도메인에 결합하여 UBR 박스 도메인 기질의 결합을 억제하는데 사용될 수 있다. 또 다른 실시예로, 상기 화합물을 포함하는 조성물은 UBR 박스 도메인에 결합되어 분해되는 기질이 분해되는 것을 방지하기 위한 용도로 사용될 수 있다. 구체적인 일 실시예로, 상기 화합물을 포함하는 조성물은 기질이 UBR 박스 도메인에 결합되어 유비퀴틴-프로테아좀 경로에 의해 분해되는 것을 방지하기 위한 용도로 사용될 수 있다.
구체적인 일 실시예로, 본 명세서에 개시되는 화합물을 포함하는 조성물은 UBR 박스 도메인에 결합하는 N-말단 잔기를 가지는 기질의 결합을 억제하는 용도로 사용될 수 있다. 구체적인 일 실시예로, 아르기닌(Arg), 라이신(Lys), 히스티딘(His), 트립토판(Trp), 페닐알라닌(Phe), 티로신(Tyr), 류신(Leu), 및 이소류신(Ile) 등의 N-말단 잔기를 가지는 기질의 결합을 억제하는 용도로 사용될 수 있다. 다만 이에 제한되지 않으며, 당업계에 UBR 박스 도메인의 기질로 공지되어 있는 물질의 결합을 억제하는 용도로 사용될 수 있다.
실시예를 참고하면, 본 명세서에서 개시하는 화합물은 UBR에 결합함을 통해 기질의 분해를 억제하는 것을 확인할 수 있다(도 1 내지 19 참고).
2.UBR 관련 질환의 치료
본 명세서의 화합물 또는 이의 염은 UBR 박스 도메인에 결합하는 특성을 가진다. 즉, UBR 박스 도메인에 결합하는 리간드로서 기능하는 화합물이다. 따라서, 이러한 화합물을 이용하여, 체내에서 UBR 박스 도메인에 결합됨을 통해 분해되는 단백질의 분해를 억제할 수 있고, 이러한 메커니즘을 이용하여 UBR 관련 질환을 치료할 수 있다.
1)약학적 조성물
본 명세서에 개시되는 화합물은 이를 필요로 하는 대상을 치료하기 위한 약학적 조성물 제조에 이용될 수 있다.
이때, 상기 치료는 특정한 의학적 상태의 증상이 개선되거나, 질병의 진행이 지연되는 효과를 가지는 것을 포함한다. 이때, 상기 대상은 인간, 비인간 동물을 포함한다. 이때, 상기 약학적 조성물은 상기 화합물과 함께 제약상 허용되는 담체, 부형제 및/또는 첨가제를 포함할 수 있다. 상기 제약상 허용되는 담체, 부형제 및 또는 첨가제는 물, 식염수, 글리콜, 글리세롤, 동물성 및 식물성 지방, 오일, 전분 등을 포함하지만, 이에 제한되지 않고 당업계에 공지되어 있는 제약상 허용되는 담체, 부형제 및/또는 첨가제를 모두 포함한다.
2)치료 방법
본 명세서에서는 본 명세서에 개시되는 화합물 또는 이의 제약상 허용되는 염을 이를 필요로 하는 대상에게 투여하는 것을 포함하는 치료방법을 제공한다. 이 때, 상기 화합물 또는 이의 제약상 허용되는 염의 투여는 투여 받지 않은 대상에 비해 특정한 의학적 상태의 증상이 개선되거나, 질병의 진행이 지연되는 효과를 가질 수 있다. 이때, 상기 대상은 인간, 비인간 동물을 포함한다.
-UBR 관련 질환
일 실시예로, 본 명세서에서는 상기 화합물 또는 이의 제약상 허용되는 염을 UBR 관련 질환을 가지는 대상에게 투여하는 것을 포함하는 치료 방법을 제공한다. 즉, 본 명세서에서 개시하는 화합물 또는 이의 제약상 허용되는 염은 UBR 관련 질환을 치료하는데 사용될 수 있다. 구체적인 일 실시예로, 상기 화합물 또는 이의 제약상 허용되는 염은 UBR 박스 도메인에 결합됨을 통해 분해되는 단백질의 분해를 억제함으로써 치료될 수 있는 특정 질환을 치료하는데 사용될 수 있다.
상기 특정 질환은 근육 위축증으로 발병되는 근육 손실증(Becker, Congennital, Duchenne, Distal, Emery-Dreifuss, Facioscapulohumeral, Limb-girdle, myotonic, ocuophargyngeal)(muscular dystrophy), 근육감소증(sarcopenia)이나 암 악액질(cancer cachexia)을 포함한 근육 손실이나 분해로 매개되는 질병(muscle wasting disease)들과 더불어 과다한 단백질 분해로 발병되는 지방육종(liposarcoma), 낭포성섬유증(cystic fibrosis), 요한슨-블리자드 질병(Johanson-Blizzard syndrome), 폐쇄성 요로질환(urethral obstruction sequence), 자가면역 췌장염(autoimmune pancreatitis) 또는 어셔 질병(Usher syndrome)과 같은 UBR box와 UBR 단백질에 관련된 질환으로 공지된 질환들을 포함한다.
일 실시예로, 상기 화합물 또는 이의 제약상 허용되는 염은 UBR에 의해 매개되는 근육 손실을 치료하는데 사용될 수 있다. 예를 들어, 암, 패혈증, 갑상선 기능 항진증 등과 같은 질병 상태에서 수반되는 급격한 근육량의 손실은 근육 내 단백질의 분해가 증가하는 것과 관련이 있고, 이는 유비퀴틴 프로테아좀 시스템의 활성화와 연관되어 있다고 알려져 있다. 이 때, 특별히 N-말단 법칙 경로가 활성화됨을 통해 유비퀴틴 결합이 증가되고 결과적으로 근육 손실이 일어난다고 알려져있다[ALFRED L. GOLDBERG et al. 1998, 1999]. 이에 따라, 본 명세서에 개시되는 화합물 또는 이의 제약상 허용되는 염은 UBR 박스 도메인에 결합함을 통해 근육 손실 경로가 활성화되는 것을 방지하여 상기 질환을 치료하는데 사용될 수 있다. 다만, 이에 제한되지 않고, 상기 특정 질환은 당업계에서 UBR에 관련된 질환으로 공지된 질환들을 모두 포함한다.
Ⅴ. 실시예
실시예 1. 화합물 합성
화합물 목록
|
번호
|
화합물 명칭
|
| 1 |
N'-(4-히드록시벤조일)-4-메틸벤젠설포노히드라지드 |
| 2 |
4-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 3 |
4-아미노-N'-(4-히드록시벤조일)-3-모르폴리노벤젠설포노히드라지드 |
| 4 |
N'-(4-히드록시벤조일)-2-옥소인돌린-5-설포노히드라지드 |
| 5 |
N'-(4-히드록시벤조일)인돌린-5-설포노히드라지드 |
| 6 |
N'-([1,1'-바이페닐]-4-카르보닐)-4-아미노벤젠설포노히드라지드 |
| 7 |
N'-([1,1'-바이페닐]-3-카르보닐)-4-아미노벤젠설포노히드라지드 |
| 8 |
3-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 9 |
4-(1-아미노에틸)-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 10 |
3,5-디아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드 |
| 11 |
N'-(4-히드록시벤조일)-4-((2-히드록시에틸)아미노)벤젠설포노히드라지드 |
| 12 |
4-아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드 |
| 13 |
N'-(4-히드록시벤조일)-4-메톡시벤젠설포노히드라지드 |
| 14 |
4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤지미드아미드 |
| 15 |
4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤즈아미드 |
| 16 |
N-(((4-아미노페닐)설포닐)메틸)-4-히드록시벤즈아미드 |
| 17 |
6-아미노-N'-(4-히드록시벤조일)-[1,1'-바이페닐]-3-설포노히드라지드 |
| 18 |
4-(2-((4-아미노페닐)설포닐)히드라진-1-카르보닐)벤즈아미드 |
| 19 |
N'-(4-아미노벤질)-4-히드록시벤조히드라지드 |
| 20 |
4-아미노-N'-(1H-인돌-3-카르보닐)벤젠설포노히드라지드 |
| 21 |
4-아미노-N'-(4-히드록시벤조일)-3-(피롤리딘-1-일)벤젠술포노히드라지드 |
| 22 |
N'-(4-히드록시벤조일)-4-니트로-3-(피롤리딘-1-일)벤젠설포노히드라지드 |
| 23 |
4-아미노-N'-(4-히드록시벤조일)-3-(피페리딘-1-일)벤젠설포노히드라지드 |
| 24 |
N'-(4-히드록시벤조일)-1H-피라졸-4-설포노히드라지드 |
| 25 |
N'-(4-히드록시벤조일)인돌린-4-설포노히드라지드 |
| 26 |
N'-(4-히드록시벤조일)-1H-인돌-4-설포노히드라지드 |
| 27 |
2-((4-아미노페닐)설포닐)-N-페닐히드라진-1-카르복사미드 |
| 28 |
4-아미노-N'-(1H-인돌-4-카르보닐)-3-모르폴리노벤젠설포노히드라지드 |
| 29 |
4-아미노-N'-(인돌린-4-카르보닐)벤젠설포노히드라지드 |
| 30 |
4-아미노-N'-(4-히드록시벤조일)-3-(페파라진-1-일)벤젠설포노히드라지드 |
| 31 |
4-아미노-N'-(2,3-디히드로-1H-인덴-2-카르보닐)벤젠설포노히드라지드 |
| 32 |
4-아미노-N'-(이소인돌린-2-카르보닐)벤젠설포노히드라지드 |
| 33 |
N'-(4-히드록시벤조일)-1H-인돌-2-설포노히드라지드 |
| 34 |
4-아미노-N'-(2-페닐아세틸)벤젠설포노히드라지드 |
| 35 |
N'-(4-히드록시벤조일)-1H-인다졸-3-설포노히드라지드 |
| 36 |
4-아미노-N'-(인돌린-6-카르보닐)벤젠설포노히드라지드 |
| 37 |
4-아미노-N'-(인돌린-3-카르보닐)벤젠설포노히드라지드 |
| 38 |
N'-(4-히드록시벤조일)피페리딘-4-설포노히드라지드 |
| 39 |
4-아미노-N'-(인돌린-6-카르보닐)-3-모르폴리노벤젠설포노히드라지드 |
| 40 |
4-아미노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드 |
| 41 |
4-아미노-3-모르폴리노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드 |
| 42 |
N'-(4-히드록시벤조일)-2-메틸티아졸-4-설포노히드라지드 |
| 43 |
(1S,4S)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드 |
| 44 |
(1R,4R)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드 |
| 45 |
4-((2-(4-히드록시벤조일)히드라지닐)설포닐)-5-메틸퓨란-2-카르복실산 |
| 46 |
N'-(4-히드록시벤조일)피롤리딘-3-설포노히드라지드 |
| 47 |
N'-(4-히드록시벤조일)-1H-피롤로[2,3-b]피리딘-2-설포노히드라지드 |
| 48 |
4-히드록시-N'-(4-메톡시벤질)벤조히드라지드 |
| 49 |
N'-(4-아미노벤질)-2,3-디히드로-1H-인덴-2-카르보히드라지드 |
| 50 |
4-아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)-3-모르폴리노벤젠설폰아미드 |
| 51 |
3,5-디아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드 |
| 52 |
2-((4-아미노페닐)설포닐)-N-(3-히드록시페닐)히드라진 -1-카르복사미드 |
| 53 |
2-((4-아미노-3-모르폴리노페닐)설포닐)-N-페닐히드라진-1-카르복사미드 |
| 54 |
4-히드록시-N-(((4-메톡시페닐)설포닐)메틸)벤즈아미드 |
| 55 |
N-(((4-아미노페닐)설포닐)메틸)-[1,1'-바이페닐]-4-카르복사미드 |
1H NMR 스펙트럼은 Bruker Avance III 400 MHz 및 Bruker Fourier 300 MHz에서 기록되었으며 TMS는 내부 표준으로 사용되었다.LCMS는 Agilent 1260HPLC 및 6120MSD에서 사중극자 질량 분석기(quadrupole Mass Spectrometer)에서 측정되었다. (ES (+) 또는 (-) 이온화모드에서 작동하는 컬럼: C18 (50 Х 4.6 mm, 5 μm); T = 30oC; 유속 = 1.5 mL/min; 감지된 파장: 220 nm, 254 nm)
실험예 1-1. 화합물1 (
N
'-(4-히드록시벤조일)-4-메틸벤젠설포노히드라지드)의 제조
단계 1) A2의 합성
A1 (메틸 4-히드록시벤조에이트, 2.00 g, 13 mmol, 1.0 eq) 및 히드라진 모노하이드레이트(20 mL)의 혼합물이 100oC에서 16 시간 동안 교반되었다. 용매가 감압 하에서 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~1/1)으로 정제되어 A2 (4-히드록시벤조히드라지드, 2.0 g, yield 60%)가 백색 고체로 얻어졌다.
1H NMR (DMSO-d 6, 400 MHz): δ 9.49 (s, 1H), 7.67-7.69 (m, 2H), 6.76-6.79 (m, 2H), 4.38 (br s, 2H).
단계 2) 화합물1의 합성
피리딘 (5 mL) 내 A2 (4-히드록시벤조히드라지드, 0.3 g, 1.97 mmol, 1.0 eq) 및 4-메틸벤젠설포닐 클로라이드(0.3 g, 1.57 mmol, 0.8 eq)의 혼합물이 80oC에서 16시간 동안 교반되었다. 이어서 혼합물에 pH=3이 될 때까지 1N HCl이 첨가되고 EA로 추출되었다 (20 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물(400 mg)이 얻어졌다. 약 130 mg의 조생성물이 prep-HPLC로 정제되었다. 수집된 분획이 농축되어 대부분의 CH3CN이 제거되었다. 잔류 분획이 동결 건조되어 화합물1 (N'-(4-히드록시벤조일)-4-메틸벤젠설포노히드라지드, 50 mg, 24.8 % yield)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.38 (s, 1H), 10.09 (s, 1H), 9.76 (s, 1H), 7.69 (d, J = 8.4 Hz, 1H), 7.56 (d, J = 8.8 Hz, 1H), 7.32 (d, J = 8.0 Hz, 1H), 6.76 (d, J = 8.8 Hz, 1H), 2.35 (s, 3H).
LCMS; Mass Calcd.:306.3; MS Found: 306.9.
실험예 1-2. 화합물2 (4-아미노-
N
'-(4-히드록시벤조일) 벤젠설포노히드라지드)의 제조
단계 1) A3의 합성
피리딘(5 mL) 내 A2 (4-히드록시벤조히드라지드, 0.3 g, 1.97 mmol, 1.0 eq) 및 4-니트로벤젠 -1-설포닐 클로라이드(0.35 g, 1.57 mmol, 0.8 eq)의 혼합물이 80oC에서 16 시간 동안 교반되었다. 이어서 혼합물이 pH=3이 될 때까지 1N HCl이 첨가되고 EA로 추출되었다(20 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물 A3 (N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 370 mg)이 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:337.1; MS Found: 337.6 [MS], 359.6[MS+22].
단계 2) 화합물2의 합성
EtOH (10 mL) 내 A3 (N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 150 mg, 0.45 mmol, 1.0 eq) 및 5% Pd/C (200 mg, 50% in water)의 혼합물이 10oC에서 4시간 동안 H2 벌룬(balloon)과 함께 교반되었다. 이어서 혼합물이 여과되고 여과액이 농축되어 조생성물이 얻어졌고, prep-HPLC로 정제되었다. 수집된 분획이 농축되어 대부분의 CH3CN이 제거되었다. 잔류 분획이 동결-건조되어 화합물2 (4-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드), 50 mg, yield 36.6%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.31 (s, 1H), 10.06 (s, 1H), 9.13 (s, 1H), 7.56 (d, J = 8.8 Hz, 2H), 7.41 (d, J = 8.8 Hz, 2H), 6.76 (d, J = 8.08 Hz, 2H), 6.50 (d, J = 8.8 Hz, 2H), 5.95 (s, 2H).
LCMS; Mass Calcd.:307.3; MS Found: 307.9.
실험예 1-3. 화합물3 (4-아미노-
N
'-(4-히드록시벤조일)-3-모르폴리노벤젠설포노히드라지드)의 제조
단계 1) A4의 합성
피리딘 (5 mL) 내 A2 (4-히드록시벤조히드라지드, 500 mg, 3.29 mmol, 1.0 eq)의 혼합물에 피리딘 (3 mL) 내 3-플루오로-4-니트로벤젠-1-설포닐 클로라이드(790 mg, 3.29 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 25oC에서 3시간 동안 교반되었다. 상기 용액이 물에 부어졌다(30 mL). 혼합물이 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~30/1)으로 정제되어 A4 (3-플루오로-N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 500 mg, 42.8%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.55 (s, 1H), 10.49 (s, 1H), 10.14 (s, 1H), 8.32 (t, J = 8.0 Hz, 1H), 7.98 (d, J = 10.4 Hz, 1H), 7.85 (d, J = 8.8 Hz, 1H), 7.60 (d, J = 8.8 Hz, 2H), 6.78 (d, J = 8.4 Hz, 2H).
단계 2) A5의 합성
DMF (10 mL) 내 A4 (3-플루오로-N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 500 mg, 1.41 mmol, 1.0 eq) 및 모르폴린 (184 mg, 2.11 mmol, 1.5 eq)의 혼합물에 K2CO3 (486 mg, 3.52 mmol, 2.5 eq)가 25oC에서 첨가되었다. 이어서 혼합물이 25oC에서 16시간 동안 교반되었다. 상기 용액이 물에 부어졌다 (30 mL). 혼합물이 EA로 추출되었다(30 mL x 3). 합한 유기층이 물(50 mL x 3) 및 염수로 세척되었고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~30/1)으로 정제되어 A5 (N'-(4-히드록시벤조일)-3-모르폴리노 -4-니트로벤젠설포노히드라지드, 180 mg, 30.3%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.51 (s, 1H), 10.24 (s, 1H), 10.14 (s, 1H), 7.96 (d, J = 8.4 Hz, 1H), 7.60-7.62 (m, 3H), 7.52 (d, J = 8.4 Hz, 1H), 6.79 (d, J = 8.4 Hz, 2H), 3.64 (t, J = 4.8 Hz, 4H), 2.90-2.94 (m, 4H).
단계 3) 화합물3의 합성
EtOH (10 mL) 내 A5 (N'-(4-히드록시벤조일)-3-모르폴리노-4-니트로벤젠설포노히드라지드, 180 mg, 0.427 mmol, 1.0 eq)의 혼합물에 Pd/C (200 mg)이 25oC에서 첨가되었다. 이어서 혼합물이 25oC에서 4시간 동안 H2 벌룬(balloon) 하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되고 prep-HPLC로 정제되어 화합물3 (4-아미노-N'-(4-히드록시벤조일)-3-모르폴리노벤젠설포노히드라지드, 40 mg, 23.9%)이 백색 고체로 얻어졌다. (TLC: N/A)
1HNMR (DMSO-d 6, 400 MHz): δ 10.35 (d, J = 3.6 Hz, 1H), 10.06 (s, 1H), 9.20 (d, J = 4.0 Hz, 1H), 7.58 (d, J = 8.4 Hz, 2H), 7.23-7.28 (m, 2H), 6.76 (d, J = 8.8 Hz, 2H), 6.66 (d, J = 8.4 Hz, 1H), 5.63 (s, 2H), 3.69 (t, J = 4.4 Hz, 4H), 2.62 (t, J = 4.4 Hz, 4H).
LCMS; Mass Calcd.:392.4; MS Found: 393.
실험예 1-4. 화합물4 (
N
'-(4-히드록시벤조일)-2-옥소인돌린-5-설포노히드라지드)의 제조
단계 1) A7의 합성
클로로설폰산 (0.88 g, 7.52 mmol, 1.0 eq) 및 A6 (인돌린-2-온, 1.0 g, 7.52 mmol, 1.0 eq)의 혼합물이 25oC에서 1.5시간 동안 교반되었고 이어서 68oC에서 1 시간 동안 교반되었다. 혼합물이 냉각되고 조심스럽게 물에 부어졌다. 형성된 침전물이 여과에 의해 수집되고, 물로 세척되고 진공 하에서 건조되어 A7 (2-옥소인돌린-5-설포닐 클로라이드, 0.7 g, crude)이 분홍색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ10.47 (br s, 1H), 7.44-7.46 (m, 2H), 6.75 (d, J = 8.8 Hz, 1H), 3.47 (s, 2H).
단계 2) 화합물4의 합성
피리딘 (10 mL) 내 A2 (4-히드록시벤조히드라지드, 0.20 g, 1.32 mmol, 1.0 eq) 및 A7 (2-옥소인돌린-5-설포닐 클로라이드, 0.30 g, 1.32 mmol, 1.0 eq)의 혼합물이 30oC에서 5시간 동안 교반되었다. 혼합물이 물에 부어졌다. 형성된 침전물이 여과에 의해 수집되고, 물로 세척되고 진공 하에 건조되었다. 고체가 DCM에서 30oC에서 30분 동안 교반되었다. 혼합물이 여과되었고 필터케이크가 건조되어 화합물4 (N'-(4-히드록시벤조일)-2-옥소인돌린-5-설포노히드라지드 50 mg, 11%)가 분홍색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.79 (br s, 1H), 10.35 (br s, 1H), 10.11 (br s, 1H), 9.62 (br s, 1H), 7.63-7.66 (m, 2H), 7.57 (d, J = 8.4 Hz, 2H), 6.88 (d, J = 8.4 Hz, 1H), 6.77 (d, J = 8.4 Hz, 2H), 3.51 (s, 2H).
LCMS; Mass Calcd.: 347.3; MS Found: 347.8.
실험예 1-5. 화합물5 (
N'
-(4-히드록시벤조일)인돌린-5-설포노히드라지드)의 제조
단계 1) A8의 합성
피리딘 (10 mL) 내 A2 (4-히드록시벤조히드라지드, 293 mg, 1.93 mmol, 1.0 eq) 및 1-아세틸인돌린-5-설포닐클로라이드(500 mg, 1.93 mmol, 1.0 eq)의 혼합물이 30oC에서 5시간 동안 교반되었다. 완료 후, 반응 혼합물이 H2O로 희석되고(20 mL) EA로 추출되었다(20 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A8 (1-아세틸-N'-(4-히드록시벤조일)인돌린-5-설포노히드라지드, 500 mg, crude)이 노란색 고체로 얻어졌다.
단계 2) 화합물5의 합성
THF (10 mL) 내 A8 (1-아세틸-N'-(4-히드록시벤조일)인돌린-5-설포노히드라지드, 200 mg, 0.53 mmol, 1.0 eq) 및 2N HCl (6 mL)의 혼합물이 50oC에서 5시간 동안 교반되었다. 완료 후, 반응 혼합물이 H2O로 희석되었고(20 mL) EA로 추출되었다(20 mL x 3). 합한 유기층이 염수로 세척되었고, Na2SO4로 건조되고 농축되었다. 조생성물이 prep-HPLC로 정제되고 동결건조되어 화합물5 (N'-(4-히드록시벤조일)인돌린-5-설포노히드라지드, 50 mg, 28.2%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.30 (br s, 1H), 10.05 (br s, 1H), 9.14 (br s, 1H), 7.58 (d, J = 8.4 Hz, 2H), 7.33-7.36 (m, 2H), 6.77 (d, J = 8.4 Hz, 2H), 6.37-6.40(m, 2H), 3.51 (t, J = 8.4 Hz, 2H), 2.90 (t, J = 8.4 Hz, 2H).
LCMS; Mass Calcd.: 333.3; MS Found: 333.8.
실험예 1-6. 화합물6 (
N
'-([1,1'-바이페닐]-4-카르보닐)-4-아미노벤젠설포노히드라지드)의 제조
단계 1) A10의 합성
디옥산 내 브로모벤젠(400 mg, 2.5mmol)의 용액에 메틸 4-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)벤조에이트(A9, 801 mg, 3.0 mmol), K3PO4 (541 mg, 7.5 mmol) 및 Pd(dppf) Cl2 -CH2Cl2 (208 mg, 0.25 mmol)이 실온에서 첨가되었다. 혼합물이 100oC에서 12시간 동안 교반되었다. 반응이 완료된 후, 반응 혼합물이 냉각되었다. 반응 혼합물이 셀라이트를 통해 여과된 후 에틸 아세테이트로 추출되었다. 유기층이 무수 MgSO4로 건조되고 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피로 정제되어(Hex/EA = 3/1) A10(메틸 [1,1'-바이페닐]-4-카르복실레이트, 160 mg, yield: 45%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm): 8.05-8.03 (m, 2H), 7.84-7.83 (m, 2H), 7.76-7.74 (m, 2H), 7.52-7.50 (m, 2H), 7.50-7.42 (m, 1H), 3.87 (s, 3H); LCMS Calcd m/z for C14H12O2 [M+H] + 213.25 Found 213.
단계 2) A11의 합성
히드라진 모노하이드레이트(8 mL) 내 A10(메틸 [1,1'-바이페닐]-4-카르복실레이트, 160 mg, 0.70 mmol)의 용액이 100 oC에서 16 시간 동안 교반되었다. 반응이 완료된 후, 반응 혼합물이 냉각되고 이어서 감압 하에 농축되고 이어서 플래쉬 컬럼 크로마토그래피로 정제되어 (DCM/MeOH = 15/1) 조생성물, A11 ([1,1'-바이페닐]-4-카르보히드라지드, 152 mg, theoretical yield: 100%)이 백색 고체로 얻어졌다. LCMS Calcd m/z for C13H12N2O [M+H] + 213.25 Found 213.
단계 3) A12의 합성
피리딘 (5 mL) 내 A11 ([1,1'-바이페닐]-4-카르보히드라지드, 152 mg, 0.70 mmol)의 용액에 4-니트로설포닐 클로라이드(143 mg, 0.60 mmol)가 첨가되었다. 혼합물이 12시간 동안 환류되었다. 반응이 완료된 후, 생성된 혼합물이 냉각되고 증발되어 피리딘을 제거하고 플래쉬 컬럼 크로마토그래피로 정제되어 (DCM/MeOH = 15/1) 조생성물, A12(N'-([1,1'-바이페닐]-4-카르보닐)-4-니트로벤젠설포노히드라지드, 60 mg, yield: 21%)가 노란색 고체로 얻어졌다. LCMS Calcd m/z for C19H15N3O5S [M+H] + 398.41 Found 398.
단계 4) 화합물6의 합성
THF:MeOH = 3:1 (12 mL) 내 A12(N'-([1,1'-바이페닐]-4-카르보닐)-4-니트로벤젠설포노히드라지드, 60 mg, 0.15 mmol)의 용액에 Zn (99 mg, 1.5 mmol) 및 NH4Cl (81 mg, 1.5 mmol)이 첨가되었다. 혼합물이 실온에서 12시간 동안 교반되었다. 반응이 완료된 후 에틸 아세테이트가 첨가되었다. 혼합물이 셀라이트를 통해 여과되었다. 여과액이 감압 하에 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피로 정제되어(DCM/MeOH = 15/1) 화합물6(N'-([1,1'-바이페닐]-4-카르보닐)-4-아미노벤젠설포노히드라지드, 10 mg, yield: 20%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm): δ 10.64 (br s, 1H), 9.32 (br s, 1H), 7.79-7.77 (m, 2H), 7.74-7.70 (m, 4H), 7.49 (t, 2H), 7.45-7.39 (m, 3H), 6.51 (d, J = 6.0 Hz, 2H), 5.96 (s, 1H), 6.52(d, J = 5.0 Hz, 2H); LCMS Calcd m/z for C19H17N3O3S [M+H] + 368.42 Found 368.
실험예 1-7. 화합물7 (
N
'-([1,1'-바이페닐]-3-카르보닐)-4-아미노벤젠설포노히드라지드)의 제조
단계 1) A14의 합성
디옥산 내 브로모벤젠 (400 mg, 2.5mmol)의 용액에 메틸 3-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)벤조에이트(A13, 801 mg, 3.0 mmol), K3PO4 (541 mg, 7.5 mmol) 및 Pd(dppf) Cl2 -CH2Cl2 (208 mg, 0.25 mmol)이 실온에서 첨가되었다. 혼합물이 100oC에서 12시간 동안 교반되었다. 반응이 완료된 후, 반응 혼합물이 냉각되었다. 혼합물이 셀라이트를 통해 여과된 후 에틸 아세테이트로 추출되었다. 유기층이 무수 MgSO4로 건조되고 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피로 정제되어(Hex/EA = 3/1) A14 (메틸 [1,1'-바이페닐]-3-카르복실레이트, 160 mg, yield: 49%)가 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm) : 8.18 (t, J = 1.8 Hz, 1H), 7.97-7.95 (m, 2H), 7.71-7.70 (m, 2H), 7.63 (t, J = 7.7 Hz, 1H), 7.52-7.49 (m, 2H), 7.43-7.41 (m, 1H), 3.89 (s, 3H); LCMS Calcd m/z for C14H12O2 [M+H] + 213.25 Found 213.
단계 2) A15의 합성
히드라진 모노하이드레이트 (8 mL) 내 A14 (메틸 [1,1'-바이페닐]-3-카르복실레이트, 160 mg, 7.5 mmol)의 용액이 100oC에서 16시간동안 교반되었다. 반응이 완료된 후, 반응 혼합물이 냉각되고 이어 감압 하에서 농축되고 이어서 플래쉬 컬럼 크로마토그래피로 정제되어(DCM/MeOH = 15/1) 조생성물 A15 ([1,1'-바이페닐]-3-카르보히드라지드, 200 mg, yield: 100%)가 노란색 고체로 얻어졌다.
LCMS Calcd m/z for C13H12N2O [M+H] + 213.25 Found 213.
단계 3) A16의 합성
피리딘 (7 mL) 내 A15 ([1,1'-바이페닐]-3-카르보히드라지드, 200 mg, 0.90 mmol)의 용액에 4-니트로설포닐 클로라이드(2.5 mL)이 첨가되었다. 혼합물을 12시간 동안 환류시켰다. 반응이 완료된 후, 생성된 혼합물이 냉각되고 증발되어 피리딘을 제거한 다음 플래쉬 컬럼 크로마토그래피로 정제되어(DCM/MeOH = 15/1) 조생성물, A16 (N'-([1,1'-바이페닐]-3-카르보닐)-4-니트로벤젠설포노히드라지드, 102 mg, yield: 53%)이 상아색 고체로 얻어졌다.
LCMS Calcd m/z for C19H15N3O5S [M+H] + 398.41 Found 398.
단계 4)
화합물7의 합성
THF:MeOH = 3:1 (10 mL) 내 A16 (N'-([1,1'-바이페닐]-3-카르보닐)-4-니트로벤젠설포노히드라지드, 102 mg, 0.25 mmol)의 용액에 Zn (168 mg, 2.5 mmol) 및 NH4Cl (137 mg, 2.5 mmol)이 첨가되었다. 혼합물이 실온에서 12시간 동안 교반되었다. 반응이 완료된 후 에틸 아세테이트가 첨가되었다. 혼합물이 셀라이트를 통해 여과되었다. 여과액이 감압 하에 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피로 정제되어(DCM/MeOH = 15/1) 화합물7 (N'-([1,1'-바이페닐]-3-카르보닐)-4-아미노벤젠설포노히드라지드, 14 m g, yield: 14%, purity: 96.8%)가 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm) : δ 10.71 (br s, 1H), 9.37 (br s, 1H), 7.97 (s, 1H), 7.83 (d, J = 6.0 Hz, 1H), 7.72 (d, J = 6.0 Hz, 2H), 7.65 (d, J = 6.0 Hz, 1H), 7.54-7.49 (m, 3H), 7.45 (d, J = 6.0 Hz, 2H), 7.42 (t, 1H), 6.52(d, J = 6.0 Hz, 2H), 5.97 (s, 2H); ESI-MS Calcd m/z for C19H17N3O3S [M+H] + 368.42 Found 368.
실험예 1-8. 화합물8 (3-아미노-
N
'-(4-히드록시벤조일)벤젠설포노히드라지드)의 제조
단계 1)
A17의 합성
피리딘 (8 mL) 내 A2 (200 mg, 0.90 mmol)의 용액에 3-니트로설포닐 클로라이드(168 mg, 1.08 mmol)가 첨가되었다. 혼합물이 12시간 동안 환류되었다. 반응이 완료된 후, 생성된 혼합물이 냉각되고 증발되어 피리딘이 제거된 다음 플래쉬 컬럼 크로마토그래피로 정제되어 (DCM/MeOH = 15/1) 조생성물, A17(N'-(4-히드록시벤조일)-3-니트로벤젠설포노히드라지드, 129 mg, yield: 43%)이 상아색 고체로 얻어졌다. LCMS Calcd m/z for C13H11N3O6S [M+H] + 338.31 Found 338.
단계 2) 화합물8의 합성
THF:MeOH = 3:1 (10 mL) 내 A17(N'-(4-히드록시벤조일)-3-니트로벤젠설포노히드라지드, 129 mg, 0.38 mmol)의 용액에 Zn (250 mg, 3.8 mmol) 및 NH4Cl (204 mg, 3.8 mmol)이 첨가되었다. 혼합물이 실온에서 12시간 동안 교반되었다. 반응이 완료된 후 이어서 에틸 아세테이트가 첨가되었다. 혼합물이 셀라이트를 통해 여과되었다. 여과액이 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피로 정제되어 (DCM/MeOH = 15/1) 화합물8(3-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 25 mg, yield: 21%, purity: 98.0%)이 백색 고체로 얻어졌다. 1H NMR (DMSO-d6, 600 MHz) δ (ppm) : δ 10.36 (br s, 1H), 10.06 (br s, 1H), 9.53 (br s, 1H), 7.59 (d, J = 12 Hz, 2H), 7.11-7.08 (t, J = 9.0 Hz, 1H), 7.02 (s, 1H) 6.90 (d, J = 6.0 Hz, 1H), 6.77 (d, J = 6.0 Hz, 1H), 6.71 (d, J = 12 Hz, 1H), 5.49 (s, 2H); LCMS Calcd m/z for C13H13N3O4S [M+H] + 308.32 Found 308.
실험예 1-9. 화합물9 (4-(1-아미노에틸)-
N
'-(4-히드록시벤조일)벤젠설포노히드라지드)의 제조
단계 1) A18의 합성
피리딘 (5 mL) 내 A2 (4-히드록시벤조히드라지드, 500 mg, 3.29 mmol, 1.0 eq) 및 4-아세틸벤젠-1-설포닐 클로라이드(717 mg, 3.29 mmol, 1.0 eq)의 혼합물이 25oC에서 3시간 동안 교반되었다. 혼합물이 냉각되고 조심스럽게 물에 부어졌다. 혼합물이 EA로 추출되었다(50 mL x 2). 합한 유기층이 염수로 세척되었고, 무수 Na2SO4로 건조되고 농축되어 A18 (4-아세틸-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 0.5 g, crude)이 갈색 고체로 얻어졌다.
LCMS Calcd m/z for C15H14N2O5S [M+H] + 335.3 Found 335.
단계 2) 화합물9의 합성
MeOH (5 mL) 내 A18 (4-아세틸-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 200 mg, 0.60 mmol, 1.0 eq), NH4OAc (461 mg, 5.98 mmol, 10 eq) 및 나트륨 시아노보로히드라이드(188 mg, 2.99 mmol, 5 eq)의 혼합물이 60oC에서 16시간 동안 교반되었다. 혼합물이 농축되고 prep-HPLC로 정제되고 동결 건조되어 화합물9 (4-(1-아미노에틸)-N'-(4-히드록시벤조일)벤젠설포노히드라지드,55 mg, 24%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.37 (br s, 2H), 8.28 (s, 1H), 7.80 (d, J = 8.0 Hz, 2H), 7.57 (dd, J = 11.2, 8.8 Hz, 2H), 6.77 (d, J = 8.4 Hz, 2H), 4.22 (q, J = 6.8 Hz, 1H), 1.33 (d, J = 6.4 Hz, 3H).
LCMS; Mass Calcd.: 335.3(C15H17N3O4S); MS Found: 336.
실험예 1-10. 화합물10 (3,5-디아미노-
N
'-(4-히드록시벤조일)벤젠설포노히드라지드)의 제조
단계 1) A20의 합성
농축 HCl (10 mL) 내 3,5-디니트로아닐린 (A19, 500 mg, 2.73 mmol, 1.0 eq)의 혼합물에 H2O(2 mL) 내 NaNO2 (226 mg, 3.28 mmol, 1.2 eq)를 0oC에서 첨가하였다. 혼합물이 0oC에서 0.5시간 동안 교반되었다. H2O (10 mL) 내 CuCl (27 mg, 0.27 mmol, 0.1 eq)의 혼합물에 SOCl2 (1.30 g, 10.9 mmol, 4.0 eq)가 0oC에서 첨가되었다. 이어서 디아조 염 용액이 0oC에서 적가되었다. 혼합물이 0oC에서 3 시간동안 교반되고 이어서 물에 부어졌다. 형성된 침전물이 여과에 의해 수집되고 진공하에 건조되어 A20 (3,5-디니트로벤젠설포닐 클로라이드, 0.5 g, crude)이 노란색 고체로 얻어졌다.
단계 2) A21의 합성
피리딘 (5 mL) 내 A20 (3,5-디니트로벤젠설포닐 클로라이드, 175 mg, 0.66 mmol, 1.0 eq) 및 A2 (4-히드록시벤조히드라지드, 100 mg, 0.66 mmol, 1.0 eq)의 혼합물이 60oC에서 16시간 동안 교반되었다. 혼합물이 냉각되고 조심스럽게 물에 부어졌다. 혼합물이 EA로 추출되었다(50 mL x 2). 합한 유기층이 염수로 세척되고, 무수 Na2SO4로 건조되고 농축되어 A21 (N'-(4-히드록시벤조일)-3,5-디니트로벤젠설포노히드라지드, 0.1 g, crude)이 분홍색 고체로 얻어졌다.
단계 3) 화합물10(3,5-디아미노-
N
'-(4-히드록시벤조일)벤젠설포노히드라지드)의 합성
EtOH (5 mL) 내 A21 (N'-(4-히드록시벤조일)-3,5-디니트로벤젠설포노히드라지드,0.1 g, 0.26 mmol, 1.0 eq) 및 10% Pd/C (0.1 g)의 혼합물이 실온에서 3시간 동안 H2 벌룬(balloon)하에서 교반되었다. 반응 혼합물이 여과되고, 필터 케이크가 EA로 세척되었다(50 mL x 2). 합한 여과액이 농축되어 조생성물이 얻어지고, MeOH (5 mL) 내에서 10 분 동안 교반되었다. 혼합물이 여과되고 필터 케이크가 진공에서 건조되어 화합물10(3,5-디아미노 -N'-(4-히드록시벤조일)벤젠설포노히드라지드, 27 mg, 32%)가 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.20 (br s, 1H), 10.04 (br s, 1H), 9.19 (br s, 1H), 7.63 (d, J = 8.8 Hz, 2H), 7.78 (d, J = 8.4 Hz, 2H), 6.26 (d, J = 1.6 Hz, 2H), 5.94 (s, 1H), 5.10 (s, 4H).
LCMS; Mass Calcd.: 322.3(C13H14N4O4S); MS Found: 323 [MS+1].
실험예 1-11. 화합물11 (
N
'-(4-히드록시벤조일)-4-((2-히드록시에틸)아미노)벤젠설포노히드라지드)의 제조
AcOH/H2O=1:1 (4 mL) 내 화합물2 (4-아미노-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 500 mg, 1.63 mmol, 1.0 eq) 및 옥시란 (72 mg, 1.63 mmol, 1.0 eq)의 혼합물이 25 oC에서 4시간 동안 교반되었다. 이어서 혼합물이 pH=8이 될 때까지 NaHCO3가 첨가되고 EA로 추출되었다(50 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, prep-TLC로 정제되어 화합물11 (N'-(4-히드록시벤조일)-4-((2-히드록시에틸)아미노)벤젠설포노히드라지드, 50 mg, yield 8.8%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 7.56 (d, J = 8.4 Hz, 2H), 7.46 (d, J = 8.8 Hz, 2H), 6.73 (d, J = 8.4 Hz, 2H), 6.56 (d, J = 8.8 Hz, 2H), 6.45 (t, J = 5.2 Hz, 1H), 3.53 (t, J = 6.0 Hz, 2H), 3.12 (q, J = 6.0 Hz, 2H).
LCMS; Mass Calcd.:351.3; MS Found: 351.8 [MS+1].
실험예 1-12. 화합물12 (4-아미노-
N
-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드)의 제조
단계 1) A23의 합성
EtOH (40 mL) 내 A22 (1-(4-(벤질옥시)페닐)에탄-1-온, 4.0 g, 17.7 mmol, 1.0 eq)의 혼합물에 Br2 (2.83 g, 17.7 mmol, 1.0 eq)가 5oC에서 첨가되었다. 혼합물이 30oC에서 30분 동안 교반되었다. 혼합물이 PE로 부어지고 30분 동안 교반되었다. 혼합물이 여과되고, 필터 케이크가 건조되어 A23(1-(4-(벤질옥시)페닐)-2-브로모에탄-1-온, 2.5 g, 46.3%)이 백색 고체로 얻어졌다.
단계 2) A24의 합성
DCM (20 mL) 내 A23 (1-(4-(벤질옥시)페닐)-2-브로모에탄-1-온, 2.0 g, 6.55 mmol, 1.0 eq) 및 HMTA (1.38 g, 9.83 mmol, 1.5 eq)의 혼합물이 10oC에서 2시간 동안 교반되었다. 이어서 혼합물이 여과되고 필터 케이크가 EtOH (15 mL) 및 농축 HCl (5 mL)에 용해되었다. 혼합물이 85oC에서 2시간 동안 교반되었다. 혼합물이 여과되고 필터 케이크가 건조되어 A24 (2-아미노-1-(4-(벤질옥시)페닐)에탄-1-온 히드로클로라이드, 2.0 g, crude)가 백색 고체로 얻어졌다.
1HNMR (CD3OD, 400 MHz): δ 8.03 (d, J = 8.8 Hz, 2H), 7.47 (d, J = 7.2 Hz, 2H), 7.34-7.42 (m, 3H), 7.17 (d, J = 8.8 Hz, 2H), 5.23 (s, 2H), 4.55 (s, 2H).
단계 3) A25의 합성
DCM (20 mL) 내 A24 (2-아미노-1-(4-(벤질옥시)페닐)에탄-1-온 히드로클로라이드, 2.00 g, 7.20 mmol, 1.0 eq), 4-니트로벤젠-1-설포닐 클로라이드(1.60 g, 7.20 mmol, 1.0 eq) 및 TEA (2.19 g, 21.6 mmol, 3.0 eq)의 혼합물이 20oC에서 1시간 동안 교반되었다. 혼합물이 물에 부어지고 DCM으로 추출되었다. 유기층이 물 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, PE에서 30분 동안 교반되었다. 혼합물이 여과되고 필터 케이크로 A25 (N-(2-(4-(벤질옥시)페닐)-2-옥소에틸)-4-니트로벤젠설폰아미드, 1.0 g, 35.8% for 2 steps)가 백색 고체로 얻어졌다.
1HNMR (CD3Cl, 400 MHz): δ 8.36 (d, J = 8.8 Hz, 2H), 8.10 (d, J = 8.4 Hz, 2H), 7.84 (d, J = 8.8 Hz, 2H), 7.37-7.43 (m, 5H), 7.03 (d, J = 8.4 Hz, 2H), 5.86 (t, J = 4.0 Hz, 1H), 5.16 (s, 2H), 4.49 (d, J = 4.0 Hz, 2H).
단계 4) 화합물12의 합성
EtOH (10 mL) 내 A25 (N-(2-(4-(벤질옥시)페닐)-2-옥소에틸)-4-니트로벤젠설폰아미드, 200 mg, 0.47 mmol, 1.0 eq) 및 Pd/C (150 mg, 50% in water)의 혼합물이 25oC에서 4 시간 동안 H2 벌룬(balloon) 하에서 교반되었다. 이어서 혼합물이 여과되고 그리고 혼합물이 농축되고 prep-HPLC 로 정제되고 동결 건조되어 화합물12 (4-아미노-N-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드, 69 mg, yield 48.0%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.43 (s, 1H), 7.79 (d, J = 8.4 Hz, 2H), 7.46 (d, J = 8.4 Hz, 2H), 7.32 (t, J = 5.6 Hz, 1H), 6.83 (d, J = 8.4 Hz, 1H), 6.58 (d, J = 8.8 Hz, 2H), 5.91 (s, 2H), 4.19 (d, J = 5.6 Hz, 2H).
LCMS; Mass Calcd.:306.3; MS Found: 307 [MS+1].
실험예 1-13. 화합물13 (
N
'-(4-히드록시벤조일)-4-메톡시벤젠설포노히드라지드)의 제조
DMF (6 mL) 내 A2 (4-히드록시벤조히드라지드, 100 mg, 0.66 mmol)의 용액에 트리에틸아민(0.11 mL, 0.76 mmol) 및 4-메톡시벤젠설포닐 클로라이드(124 mg, 0.60 mmol)가 첨가되었다. 혼합물이 실온에서 12 시간동안 유지되었다. 반응이 완료된 후, 반응 혼합물이 증발되고 에틸 아세테이트로 추출되었다. 유기층이 염수로 세척되고, 무수 MgSO4로 건조되고 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피(DCM/MeOH = 5/1)로 정제되어 화합물13 (N'-(4-히드록시벤조일)-4-메톡시벤젠설포노히드라지드, 25 mg, yield: 12%, purity: 96.9%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm): δ 10.37 (br s, 1H), 10.07 (br s, 1H), 9.64 (br s, 1H), 7.73 (d, J = 12 Hz, 2H), 7.57 (d, J = 6.0 Hz, 2H), 7.03 (d, J = 6.0 Hz, 2H), 6.76 (d, J = 6.0 Hz, 2H), 3.80 (s, 3H); LCMS Calcd m/z for C14H14N2O5S [M+H] + 323.3 Found 323.
실험예 1-14. 화합물14 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤지미드아미드의 제조
단계 1) A26의 합성
피리딘 (10 mL) 내 A2 (4-히드록시벤조히드라지드, 1.00 g, 6.57 mmol, 1.0 eq)의 혼합물에 피리딘 (3 mL) 내 4-시아노벤젠-1-설포닐 클로라이드(1.33 g, 6.57 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 25oC에서 3시간 동안 교반되었다. 상기 용액이 물에 부어졌다(50 mL). 혼합물이 EA로 추출되었다(50 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(PE/EA=1/1)으로 정제되어 A26 (4-시아노-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 1.40 g, 67.1%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.49 (s, 1H), 10.27 (s, 1H), 10.14 (s, 1H), 8.02-8.04 (m, 2H), 7.97-7.99 (m, 2H), 7.57 (d, J = 8.4 Hz, 2H), 7.78 (d, J = 8.8 Hz, 2H).
단계 2) 화합물14의 합성
HCl/EtOH (5 mL, 6 mol/L) 내 A26 (4-시아노-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 200 mg, 0.63 mmol, 1.0 eq)의 혼합물이 25oC에서 3시간 동안 교반되었다. 상기 용액이 농축되고 MeOH에 첨가되었다. 혼합물이 다시 농축되었다. 잔류물이 MeOH (10 mL)에 첨가되고 이어서 NH4OAc (485 mg, 6.30 mmol, 10 eq)에 첨가되었다. 혼합물이 25oC에서 16시간 동안 교반되었다. 혼합물이 농축되고 prep-HPLC로 정제되고 동결 건조되어 화합물14 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤지미드아미드, 26 mg, 10.8%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 8.43 (s, 1H), 8.00 (d, J = 8.0 Hz, 2H), 7.92 (d, J = 8.4 Hz, 2H), 7.59 (d, J = 8.8 Hz, 2H), 6.77 (d, J = 8.8 Hz, 2H).
LCMS; Mass Calcd.:334; MS Found: 334.8 [MS+1].
실험예 1-15. 화합물15 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤즈아미드)의 제조
DMSO 내 A26 (4-시아노-N'-(4-히드록시벤조일)벤젠설포노히드라지드, 210 mg, 0.66 mmol)의 냉각된(0 oC) 용액에 과산화수소, 35% w/w aq. Soln., (0.42 mL, 4.8 mmol) 및 탄산 칼륨(30 mg, 0.20 mmol)이 첨가되었다. 반응이 실온으로 가온되고 12시간 동안 교반되었다. 반응이 완료된 후, 반응 혼합물이 증발되고 에틸 아세테이트로 추출되었다. 유기층이 염수로 세척되고, 무수 MgSO4로 건조되고 감압하에 농축되었다. 잔류물이 컬럼 크로마토그래피(DCM/MeOH = 5/1)로 정제되어 화합물15 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)벤즈아미드, 20 mg, yield: 10%, purity: 96.5%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm) : δ 10.44 (br s, 1H), 10.10 (br s, 1H), 10.03 (br s, 1H), 8.15 (br s, 1H), 7.96 (d, J = 6.0 Hz, 2H), 7.87 (d, J = 10 Hz, 2H), 7.59 (br s, 1H), 7.57 (d, J = 6.0 Hz, 2H), 6.76 (d, J = 6.0 Hz, 2H); LCMS Calcd m/z for C14H13N3O5S [M+H] + 336.33 Found 336.
실험예 1-16. 화합물16 (
N
-(((4-아미노페닐)설포닐)메틸)-4-히드록시벤즈아미드)의 제조
단계 1) A28의 합성
DMF (40 mL) 내 A27 (4-히드록시벤즈아미드, 4.0 g, 29.2 mmol, 1.0 eq)의 혼합물에 K2CO3 (6.05 g, 43.8 mmol, 1.5 eq) 및 BnBr (4.99 g, 29.2 mmol, 1.0 eq)이 첨가되었다. 혼합물이 60oC에서 16시간 동안 교반되었다. 혼합물이 물에 부어지고 EA로 추출되었다. 유기층이 물 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 A28 (4-(벤질옥시)벤즈아미드, 6.0 g, 90.5%)이 백색 고체로 얻어졌다.
단계 2) A29의 합성
THF/H2O (40 mL, v/v=1/1) 내 A28 (4-(벤질옥시)벤즈아미드, 4.0 g, 17.6 mmol, 1.0 eq), K2CO3 (0.24 g, 1.76 mmol, 0.1 eq) 및 HCOH (1.43 g, 17.6 mmol,, 37% in water, 1.0 eq)의 혼합물이 65oC에서 16시간 동안 교반되었다. 이어서 혼합물이 농축되고 여과되었다. 필터 케이크가 건조되어 A29 (4-(벤질옥시)-N-(히드록시메틸)벤즈아미드, 4.0 g, crude)가 백색 고체로 얻어졌다.
단계 3) A30의 합성
TFA (20 mL) 내 A29 (4-(벤질옥시)-N-(히드록시메틸)벤즈아미드, 4.00 g, 15.6 mmol, 1.0 eq) 및 4-니트로벤젠티올(2.41 g, 15.6 mmol, 1.0 eq)의 혼합물이 20oC에서 1시간 동안 교반되었다. 혼합물이 농축되고 물에 첨가되고 aq. NaHCO3로 pH=8로 조정되었다. 혼합물이 EA로 추출되었다. 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A30 (4-(벤질옥시)-N-(((4-니트로페닐)티오)메틸)벤즈아미드, 2.0 g, 32.6% for 2 steps)이 백색 고체로 얻어졌다.
단계 4) A31의 합성
DCM (20 mL) 내 A30 (4-(벤질옥시)-N-(((4-니트로페닐)티오)메틸)벤즈아미드, 500 mg, 1.27 mmol, 1.0 eq) 및 m-CPBA (656 g, 3.80 mmol, 3.0 eq)의 혼합물이 20oC에서 16시간 동안 교반되었다. 혼합물이 aq. Na2O3S2 로 부어지고 추출되었다. 유기층이 aq. NaHCO3 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 A31 (4-(벤질옥시)-N-(((4-니트로페닐)설포닐)메틸)벤즈아미드, 300 mg, crude)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 9.39 (t, J = 6.4 Hz, 1H), 8.42 (d, J = 8.8 Hz, 2H), 8.14 (d, J = 8.8 Hz, 2H), 7.73 (d, J = 8.8 Hz, 2H), 7.34-7.46 (m, 5H), 7.08 (d, J = 8.8 Hz, 2H), 5.17 (s, 2H), 5.00 (d, J = 6.4 Hz, 2H).
단계 5) 화합물16의 합성
EtOH (10 mL) 내 A31 (4-(벤질옥시)-N-(((4-니트로페닐)설포닐)메틸)벤즈아미드, 300 mg, 0.47 mmol, 1.0 eq) 및 Pd/C (150 mg, 50% in water)의 혼합물이 25 oC에서 2시간 동안 H2 벌룬(balloon)하에서 교반되었다. 이어서 혼합물이 여과되고 혼합물이 농축되고 prep-HPLC로 정제되고 동결 건조되어 화합물16 (N-(((4-아미노페닐)설포닐)메틸)-4-히드록시벤즈아미드, 35 mg, yield 9.0% for 2 steps)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.15 (br s, 1H), 9.06 (t, J = 6.4 Hz, 1H), 7.65 (d, J = 8.8 Hz, 2H), 7.40 (d, J = 8.8 Hz, 2H), 6.79 (d, J = 8.8 Hz, 2H), 6.58 (d, J = 8.8 Hz, 2H), 6.12 (s, 2H), 4.65 (d, J = 6.4 Hz, 2H).
LCMS ; Mass Calcd.:306; MS Found: 307 [MS+1].
실험예 1-17. 화합물17 (6-아미노-
N
'-(4-히드록시벤조일)-[1,1'-바이페닐]-3-설포노히드라지드)의 제조
단계 1) A33의 합성
톨루엔 (10 mL) 내 A32 (3-브로모-4-니트로아닐린, 1 g, 4.61 mmol, 1.0 eq), 페닐보론산(0.56 g, 4.61 mmol, 1.0 eq), Pd(dppf)Cl2 (337 mg, 0.09 mmol, 0.1 eq) 및 AcOK (1.14 g, 13.8 mmol, 3.0 eq)의 혼합물이 16 시간 동안 90oC에서 N2하에서 교반되었다. 혼합물이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 2). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되었다. 조생성물이 플래쉬 컬럼(PE/EA = 30/1~10/1)으로 정제되어 A33 (6-니트로-[1,1'-바이페닐]-3-아민, 1 g, crude)이 노란색 고체로 얻어졌다.
단계 2) A34의 합성
AcOH (10 mL) 및 농축 HCl (5 mL) 내 A33 (6-니트로-[1,1'-바이페닐]-3-아민, 500 mg, 2.33 mmol, 1.0 eq)의 혼합물에 H2O (2 mL) 내 NaNO2 (193 mg, 2.8 mmol, 1.2 eq)가 0oC에서 적가되었다. 혼합물이 0oC에서 0.5시간 동안 교반되었다. H2O (10 mL) 내 CuCl (31.3 mg, 0.23 mmol, 0.1 eq)의 혼합물에 SOCl2 (1.39 g, 11.6 mmol, 5.0 eq)가 0oC에서 첨가되었다. 이어서 디아조 염 용액이 0oC에서 적가되었다. 혼합물이 0oC에서 3시간 동안 교반되고 이어서 물로 부어졌다. 형성된 침전물이 여과에 의해 수집되고 진공 하에 건조시켜 A34 (6-니트로-[1,1'-바이페닐]-3-설포닐 클로라이드, 400 mg, 57.6%)가 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 7.98 (d, J = 8.4 Hz, 1H), 7.78-7.80 (m, 1H), 7.64 (d, J = 1.2 Hz, 1H), 7.44-7.50 (m, 3H), 7.32-7.34 (m, 2H).
단계 3) A35의 합성
피리딘 (5 mL) 내 A34 (6-니트로-[1,1'-바이페닐]-3-설포닐 클로라이드, 200 mg, 0.67 mmol, 1.0 eq) 및 4-히드록시벤조히드라지드(122 mg, 0.81 mmol, 1.2 eq)의 혼합물이 30oC에서 0.5시간 동안 교반되었다. 혼합물이 조심스럽게 물에 부어졌다. 혼합물이 EA로 추출되었다(50 mL x 2). 합한 유기층이 염수로 세척되고, 무수 Na2SO4로 건조되고 농축되어 A35 (N'-(4-히드록시벤조일)-6-니트로-[1,1'-바이페닐]-3-설포노히드라지드, 200 mg, crude)가 갈색 고체로 얻어졌다.
단계 4) 화합물17의 합성
EtOH (10 mL) 내 A35 (N'-(4-히드록시벤조일)-6-니트로-[1,1'-바이페닐]-3-설포노히드라지드, 200 mg, 0.48 mmol, 1.0 eq) 및 10% Pd/C (200 mg)의 혼합물이 30oC에서 3시간 동안 H2 벌룬(balloon)하에서 교반되었다. 반응 혼합물이 여과되고 필터 케이크가 EA로 세척되었다(50 mL x 2). 합한 여과물을 농축하여 조생성물이 얻어졌고, prep-HPLC로 정제되고 동결 건조되어 화합물17 (6-아미노-N'-(4-히드록시벤조일)-[1,1'-바이페닐]-3-설포노히드라지드, 45 mg, 17.5% for 2 steps)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.39 (s, 1H), 10.09 (s, 1H), 9.32 (s, 1H), 7.61 (d, J = 8.8 Hz, 2H), 7.32-7.59 (m, 5H), 7.23 (d, J = 6.4 Hz, 2H), 6.73-6.79 (m, 3H), 5.64 (s, 2H).
LCMS; Mass Calcd.: 383; MS Found: 384 [MS+1].
실험예 1-18. 화합물18 (4-(2-((4-아미노페닐)설포닐)히드라진-1-카르보닐)벤즈아미드)의 제조
단계 1) A37의 합성
DCM 내 메틸 4-(클로로카르보닐)벤조에이트(A36, 1.5 g, 7.5 mmol)의 냉각된 (0oC) 용액에 암모니아 용액(25~30%) (1.8 mL, 15 mmol)이 첨가되었다. 반응이 실온으로 가온되고 4시간 동안 교반되었다. 반응이 완료된 후, 반응 혼합물이 증발된 다음 물이 첨가되었다. 형성된 침전물이 여과에 의해 수집되었다. 필터 케이크는 물로 세척되고 건조되어 A37 (메틸 4-카르바모일벤조에이트, 1.0 g, 74%)이 백색 고체로 얻어졌다. LCMS Calcd m/z for C9H9NO3 [M+H] + 152.17 Found 152.
단계 2) A38의 합성
MeOH (10 mL) 내 A37 (메틸 4-카르바모일벤조에이트, 1 g, 6.6 mmol) 및 히드라진 모노하이드레이트(10 mL)의 용액이 80oC에서 16시간 동안 교반되었다. 용매가 감압 하에서 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH = 10/1)으로 정제되어 A38 (4-(히드라진카르보닐)벤즈아미드, 600 mg, yield: 60%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm) : δ 9.87 (s, 1H), 8.06 (s, 1H), 7.92-7.91 (m, 2H), 7.87-7.86 (m, 2H), 7.48 (s, 1H), 4.55 (brs, 2H).
단계 3) A39의 합성
DMF (7 mL) 내 A38 (4-(히드라진카르보닐)벤즈아미드, 600 mg, 3.3 mmol)의 용액에 TEA(0.55 mL, 3.9 mmol) 및 4-메톡시벤젠설포닐 클로라이드(676 mg, 3.0 mmol)가 첨가되었다. 혼합물이 12시간 동안 실온에서 유지되었다. 반응이 완료된 후, 반응 혼합물이 증발되고 에틸 아세테이트로 추출되었다. 유기층이 염수로 세척되고, 무수 MgSO4로 건조되고 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피(DCM/MeOH = 10/1)로 정제되어 A39(4-(2-((4-니트로페닐)설포닐)히드라진-1-카르보닐)벤즈아미드, 366 mg, yield: 30%)가 백색 고체로 얻어졌다. LCMS Calcd m/z for C14H12N4O6 S [M+H] + 365.33 Found 365.
단계 4) 화합물18의 합성
THF:MeOH = 3:1 (10 mL) 내 A39 (4-(2-((4-니트로페닐)설포닐)히드라진-1-카르보닐)벤즈아미드, 366 mg, 1.0 mmol)의 용액에 Zn (657 mg, 10 mmol) 및 NH4Cl (537 mg, 10 mmol)이 60oC에서 5시간 동안 첨가되었다. 반응이 완료된 후, 반응 혼합물이 냉각되고 이어서 에틸 아세테이트가 첨가되었다. 혼합물이 셀라이트를 통해 여과되었다. 여과물이 감압 하에 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피(DCM/MeOH = 15/1)로 정제되어 화합물18 (4-(2-((4-아미노페닐)설포닐)히드라진-1-카르보닐)벤즈아미드, 10 mg, 4.51 mmol, yield: 3%, purity: 97.0%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm) : δ 10.68 (br s, 1H), 9.38 (br s, 1H), 8.06 (s, 1H), 7.90 (d, J = 6.0 Hz, 2H), 7.73 (d, J = 6.0 Hz, 2H), 7.05 (s, 1H), 7.44 (d, J = 6.0 Hz, 2H), 6.51 (d, J = 6.0 Hz, 2H), 5.97 (s, 2H); LCMS Calcd m/z for C14H14N4O4 S [M+H] + 335.35 Found 335.
실험예 1-19. 화합물19 (
N
'-(4-아미노벤질)-4-히드록시벤조히드라지드)의 제조
단계 1) A40의 합성
DMF (10 mL) 내 A2(500 mg, 3.2 mmol)의 용액에 트리에틸아민(0.46 mL, 3.2 mmol) 및 1-(브로모메틸)-4-니트로벤젠(545 mg, 2.5 mmol)이 첨가되었다. 혼합물이 실온에서 12시간 동안 유지되었다. 반응이 완료된 후, 반응 혼합물이 증발되고 에틸 아세테이트로 추출되었다. 유기층이 염수로 세척되고, 무수 MgSO4로 건조되고 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피(DCM/MeOH = 5/1)로 정제되어 A40 (4-히드록시-N'-(4-니트로벤질)벤조히드라지드, 410 mg, yield: 44%)이 노란색 고체로 얻어졌다. LCMS Calcd m/z for C14H13N3O4 [M+H] + 288.28 Found 288.
단계 2) 화합물19의 합성
THF:MeOH = 3:1 (12 mL) 내 A40 (4-히드록시-N'-(4-니트로벤질)벤조히드라지드, 410 mg, 1.4 mmol)의 용액에 Zn (933 mg, 14 mmol) 및 NH4Cl (764 mg, 14 mmol)이 첨가되었다. 혼합물이 실온에서 12시간 동안 교반되었다. 반응이 완료된 후 이어서 에틸 아세테이트가 첨가되었다. 혼합물이 셀라이트를 통해 여과되었다. 여과액이 감압 하에서 농축되었다. 잔류물이 플래쉬 컬럼 크로마토그래피(DCM/MeOH = 15/1)로 정제되어 화합물19 (N'-(4-아미노벤질)-4-히드록시벤조히드라지드, 6 mg, yield: 16%, purity: 95.0%)이 백색 고체로 얻어졌다.
1H NMR (DMSO-d6, 600 MHz) δ (ppm): δ 10.03 (br s, 1H), 9.80 (br s, 1H), 7.67 (d, J = 6.0 Hz, 2H), 7.00 (d, J = 6.0 Hz, 2H), 6.77 (d, J = 6.0 Hz, 2H), 6.51 (d, J = 6.0 Hz, 2H), 4.97 (bs, 3H), 3.72 (bs, 2H); LCMS Calcd m/z for C14H15N3O2 [M+H] + 258.29 Found 258.
실험예 1-20. 화합물20 (4-아미노-
N
'-(1
H
-인돌-3-카르보닐)벤젠설포노히드라지드)의 합성
단계 1) A42의 합성
피리딘(5 mL) 내 A41 (1H-인돌-3-카르보히드라지드, 500 mg, 2.85 mmol, 1.0 eq)의 혼합물에 피리딘(5 mL) 내 4-니트로벤젠-1-설포닐 클로라이드(632 mg, 2.85 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~30/1)으로 정제하여 A42 (N'-(1H-인돌-3-카르보닐)-4-니트로벤젠설포노히드라지드, 0.9 g, yield 87.5%)가 노란색 고체로 얻어졌다. (TLC: DCM/MeOH =20/1, Rf=0.5)
단계 2) 화합물20의 합성
MeOH (10 mL) 내 A42 (N'-(1H-인돌-3-카르보닐)-4-니트로벤젠설포노히드라지드, 300 mg, 0.83 mmol, 1.0 eq)의 혼합물에 Pd/C (100 mg)가 첨가되었다. 이어서 혼합물이 10oC에서 2시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 prep-HPLC로 정제되고 동결 건조되어 화합물20 (4-아미노-N'-(1H-인돌-3-카르보닐)벤젠설포노히드라지드, 30 mg, yield 10.9%)이 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 11.62 (d, J = 2.8 Hz, 1H), 9.98 (s, 1H), 9.11 (d, J = 3.2 Hz, 1H), 8.00 (d, J = 2.8 Hz, 1H), 7.90 (d, J = 7.6 Hz, 1H), 7.40-7.46 (m, 3H), 7.05-7.16 (m, 2H), 6.51 (d, J = 8.8 Hz, 2H), 5.89 (br s, 2H).
LCMS ; Mass Calcd.:330; MS Found: 331.1 [MS+1].
실험예 1-21 및 실험예 1-22. 화합물21 (4-아미노-N'-(4-히드록시벤조일)-3-(피롤리딘-1-일)벤젠설포노히드라지드) 및 화합물22 (
N
'-(4-히드록시벤조일)-4-니트로-3-(피롤리딘-1-yl)벤젠설포노히드라지드)의 제조
단계 1) 화합물22의 합성
DMF (10 mL) 내 A4 (3-플루오로-N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 400 mg, 1.13 mmol, 1.0 eq) 및 K2CO3 (389 mg, 2.81 mmol, 2.5 eq)의 혼합물에 피롤리딘(96 mg, 1.35 mmol, 1.2 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 25oC에서 16시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어졌고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~30/1)으로 정제되어 화합물22 (N'-(4-히드록시벤조일)-4-니트로-3-(피롤리딘-1-일)벤젠설포노히드라지드, 176 mg, yield 38.5%)이 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.48 (s, 1H), 10.14 (s, 2H), 7.86 (d, J = 8.8 Hz, 1H), 7.61 (d, J = 8.8 Hz, 2H), 7.37 (d, J = 1.6 Hz, 1H), 7.11-7.13 (m, 1H), 6.78 (d, J = 8.8 Hz, 2H), 3.64 (t, J = 6.0 Hz, 4H), 1.86 (t, J = 6.0 Hz, 4H).
단계 2) 화합물21의 합성
MeOH (5 mL) 내 화합물22 (N'-(4-히드록시벤조일)-4-니트로-3-(피롤리딘-1-일)벤젠설포노히드라지드, 100 mg, 0.54 mmol, 1.0 eq)의 혼합물에 Pd/C (30 mg)이 첨가되었다. 이어서 혼합물이 10oC에서 16시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되어 조생성물이 얻어졌고, MeOH (5 mL) 및 DMSO (0.5 mL) 내에서 5 분 동안 교반되었다. 혼합물이 여과되고 필터 케이크가 MeOH로 세척되고 건조되어 화합물21 (4-아미노-N'-(4-히드록시벤조일)-3-(피롤리딘-1-일)벤젠설포노히드라지드, 30 mg, yield 32.4%)이 회백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.34 (s, 1H), 10.06 (s, 1H), 9.13 (s, 1H), 7.54 (d, J = 8.4 Hz, 2H), 7.17 (t, J = 1.6 Hz, 2H), 6.76 (d, J = 8.8 Hz, 2H), 6.61 (d, J = 8.4 Hz, 1H), 5.47 (s, 2H), 2.80 (s, 4H), 1.77 (s, 4H).
LCMS ; Mass Calcd.:330; MS Found: 331.1 [MS+1].
실험예 1-23. 화합물23 (4-아미노-
N
'-(4-히드록시벤조일)-3-(피페리딘-1-일)벤젠설포노히드라지드)의 합성
단계 1) A43의 합성
DMF (10 mL) 내 A4 (3-플루오로-N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 400 mg, 1.13 mmol, 1.0 eq) 및 K2CO3 (389 mg, 2.81 mmol, 2.5 eq)의 혼합물에 피페리딘 (115 mg, 1.35 mmol, 1.2 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 25oC에서 16시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~30/1)으로 정제되어 A43 (N'-(4-히드록시벤조일)-4-니트로-3-(피페리딘-1-일)벤젠설포노히드라지드, 240 mg, yield 50.7%)이 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.53 (s, 1H), 10.21 (s, 1H), 10.15 (s, 1H), 7.91 (d, J = 8.4 Hz, 1H), 7.62 (d, J = 8.8 Hz, 2H), 7.56 (d, J = 1.6 Hz, 1H), 7.40-7.43 (m, 1H), 6.79 (d, J = 8.8 Hz, 2H), 2.88 (t, J = 5.2 Hz, 4H), 1.50-1.51 (m, 6H).
단계 2) 화합물23의 합성
MeOH (5 mL) 내 A43 (N'-(4-히드록시벤조일)-4-니트로-3-(피페리딘-1-일)벤젠설포노히드라지드, 100 mg, 0.24 mmol, 1.0 eq)의 혼합물에 Pd/C (30 mg)이 첨가되었다. 이어서 혼합물이 10oC에서 16시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 prep-HPLC로 정제되고 동결 건조되어 화합물23 (4-아미노-N'-(4-히드록시벤조일)-3-(피페리딘-1-일)벤젠설포노히드라지드, 25 mg, yield 26.9%)가 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ10.37 (d, J = 4.0 Hz, 1H), 10.07 (s, 1H), 9.17 (d, J = 4.0 Hz, 1H), 7.58 (d, J = 8.8 Hz, 2H), 7.2-7.25 (m, 2H), 6.77 (d, J = 7.2 Hz, 2H), 6.64 (d, J = 8.4 Hz, 1H), 5.51 (s, 2H), 2.55 (s, 4H), 1.55-1.60 (m, 4H), 1.45 (s, 2H).
LCMS ; Mass Calcd.:390; MS Found: 390.8 [MS+1].
실험예 1-24. 화합물24 (
N
'-(4-히드록시벤조일)-1
H
-피라졸-4-설포노히드라지드)의 합성
단계 1) A44의 합성
클로로설폰산 (5 mL) 내 1H-피라졸(1 g, 14.7mmol, 1.0 eq)의 용액이 100oC에서 밤새 교반되었다. 상기 용액이 물(30 mL)에 부어졌고 EA로 추출되었다(30 mL * 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A44 (1H-피라졸-4-설포닐 클로라이드, 340 mg, yield 14%)가 회백색 고체로 얻어졌다.
1HNMR (CDCl3, 400 MHz): 8.22 (s, 2H), 7.92 (s, 1H).
단계 2) 화합물24의 합성
피리딘 (20 mL) 내 A44 (1H-피라졸-4-설포닐 클로라이드, 100 mg, 0.6 mmol, 1.0 eq) 및 A2 (4-히드록시벤조히드라지드, 109 mg, 0.72 mmol, 1.2 eq)의 혼합물이 80oC에서 밤새 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL * 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌다. 잔류물이 prep-HPLC로 정제되어 화합물24 (N'-(4-히드록시벤조일)-1H-피라졸-4-설포노히드라지드, 60 mg)이 회백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): 13.4 (s, 1H), 10.39 (s, 1H), 10.1 (s, 1H), 9.5 (s, 1H), 8.47-7.63 (m, 2H), 7.62 (d, 2H), 6.78 (d, 2H).
실험예 1-25 및 실험예 1-26. 화합물25 (
N
'-(4-히드록시벤조일)인돌린-4-설포노히드라지드) 및 화합물26 (
N
'-(4-히드록시벤조일)-1
H
-인돌-4-설포노히드라지드)의 제조
단계 1) A46의 합성
THF (10 mL) 및 Et2O (10 mL) 내 A45 (4-브로모-1H-인돌, 1.0 g, 5.10 mmol, 1.0 eq)의 용액에 NaH (204 mg, 5.10 mmol, 60% in mineral oil, 1.0 eq)가 0oC에서 첨가되었다. 15분 동안의 교반 후, 혼합물이 -78oC로 냉각되고, t-BuLi (7.9 mL, 10.2 mmol, 1.3 M in THF, 2.0 eq)이 천천히 첨가되었다. 30분 후, SO2 (gas, 1 L)가 -78oC에서 천천히 첨가되었다. 혼합물이 실온으로 가온되고 밤새 교반되었다. Et2O (15 mL) 내 아세트산(307 mg, 5.10 mmol, 1.0 eq)의 혼합물이 0oC에서 첨가되었다. 혼합물이 30분 동안 0oC에서 교반되고 이어서 여과되었다. 필터 케이크가 Et2O로 빠르게 세척되었다. 고체가 Et2O (15 mL)에 현탁되고, 0oC로 냉각되고 NCS (682 g, 5.10 mmol, 1.0 eq)를 조심스럽게 첨가하였다. 생성된 현탁액이 30 분 동안 빠르게 교반 된 다음, 여과되었다. 필터 케이크를 Et2O로 세척하였다. 합한 여과액이 농축되어 A46 (1H-인돌-4-설포닐 클로라이드, 420 mg, crude)이 갈색 고체로 얻어졌다.
단계 2) 화합물26의 합성
피리딘(30 mL) 내 A46 (1H-인돌-4-설포닐 클로라이드, 420 mg, 1.95 mmol, 1.0 eq) 및 4-히드록시벤조히드라지드(A2, 297 mg, 1.95 mmol, 1.0 eq)의 혼합물이 25oC에서 30분 동안 교반되었다. 상기 용액이 물(30 mL)에 부어졌다. 형성된 고체는 여과에 의해 수집되었고 필터케이크는 물에 의해 세척되었다. 조생성물이 prep-HPLC로 정제되고 동결 건조되어 화합물26 (N'-(4-히드록시벤조일)-1H-인돌-4-설포노히드라지드, 200 mg, yield 31.0%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 11.48 (s, 1H), 10.30 (s, 1H), 10.04 (s, 1H), 9.52 (s, 1H), 7.65 (d, J = 8.0 Hz, 1H), 7.49-7.52 (m, 4H), 7.16 (t, J = 8.0 Hz, 1H), 6.85 (t, J = 2.0 Hz, 1H), 6.73 (dd, J = 6.8, 2.0 Hz, 2H).
LCMS ; Mass Calcd.:331.3; MS Found: 331.9 [MS+1].
단계 3) 화합물25의 합성
TFA (5 mL) 및 DCM (5 mL) 내 화합물26 (N'-(4-히드록시벤조일)-1H-인돌-4-설포노히드라지드, 150 mg, 0.48 mmol, 1.0 eq)의 혼합물에 NaBH3CN (89 mg, 1.43 mmol, 3.0 eq)이 0oC에서 첨가되었다. 혼합물이 10oC에서 30분 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 DCM으로 추출하였다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, prep-HPLC로 정제되고 동결 건조되어 화합물25 (N'-(4-히드록시벤조일)인돌린-4-설포노히드라지드, 30 mg, yield 20.0%)이 회색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.35 (d, J = 2.8 Hz, 1H), 10.09 (s, 1H), 9.62 (d, J = 2.8 Hz, 1H), 7.57 (d, J = 8.8 Hz, 2H), 6.97-6.99 (m, 1H), 6.93 (d, J = 6.8 Hz, 1H), 6.76 (d, J = 8.8 Hz, 2H), 6.67 (d, J = 7.2 Hz, 1H), 3.39-3.44 (m, 2H), 3.27-3.32 (m, 2H).
LCMS ; Mass Calcd.:333; MS Found: 333.8 [MS+1].
실험예 1-27. 화합물27 (2-((4-아미노페닐)설포닐)-
N
-페닐히드라진-1-카르복사미드)의 제조
단계 1) A47의 합성
피리딘 (25 mL) 내 4-니트로벤젠설포닐 클로라이드(3 g, 13.5 mmol, 1.0 eq)의 혼합물에 피리딘 (5 mL) 내 tert-부틸 히드라진카르복실레이트(1.8 g, 13.6 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 물(100 mL)에 부어지고 용액이 1시간 동안 교반되었다. 형성된 고체는 여과에 의해 수집되었고 건조되어 A47 (tert-부틸2-((4-니트로페닐)설포닐)히드라진-1-카르복실레이트, 3.0 g, yield 69.7%)이 노란색 고체로 얻어졌다.
1HNMR (CDCl3, 400 MHz): δ 8.35 (d, J = 8.4 Hz, 2H), 8.13 (dd, J = 7.2, 2.0 Hz, 2H), 6.79 (s, 1H), 6.68 (s, 1H), 1.25 (s, 9H).
단계 2) A48의 합성
MeOH (30 mL) 내 A47 (tert-부틸 2-((4-니트로페닐)설포닐)히드라진-1-카르복실레이트, 3 g, 9.45 mmol, 1.0 eq)의 혼합물에 MeOH/HCl (30 mL, 6 mol/L)이 첨가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 농축되어 A48 (4-니트로벤젠설포노히드라지드 히드로클로라이드, 2.0 g, yield 83.4%)이 노란색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 8.45-8.48 (m, 2H), 8.15 (d, J = 8.8 Hz, 2H).
단계 3) A49의 합성
THF (20 mL) 내 A48 (4-니트로벤젠설포노히드라지드 하이드로클로라이드, 500 mg, 1.97 mmol, 1.0 eq)의 혼합물에 DIEA (764 mg, 5.91 mmol, 3.0 eq) 및 이소시아나토벤젠 (235 mg, 1.97 mmol, 1.0 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 물(80 mL)에 부어졌다. 형성된 고체가 여과되고 필터 케이크가 EA (20 mL)에서 30 분 동안 교반되었다. 이어서 혼합물이 다시 여과되고 필터케이크가 건조되어 A49 (2-((4-니트로페닐)설포닐)-N-페닐히드라진-1-카르복사미드, 340 mg, yield 51.3%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 10.09 (s, 1H), 8.69 (s, 1H), 8.53 (s, 1H), 8.40-8.43 (m, 2H), 8.09 (dd, J = 7.2, 2.0 Hz, 2H), 7.34 (t, J = 8.0 Hz, 2H), 7.21 (t, J = 8.0 Hz, 1H), 6.94 (t, J = 7.2 Hz, 1H).
단계 4) 화합물27의 합성
MeOH (30 mL) 내 A49 (2-((4-니트로페닐)설포닐)-N-페닐히드라진-1-카르복사미드, 340 mg, 1.01 mmol, 1.0 eq) 및 Pd/C (200 mg)의 혼합물이 10oC에서 15시간 동안 H2 벌룬(balloon) 하에서 교반되었다. 상기 용액이 여과되고 여과액은 농축되어 조 생성물이 얻어졌고, MeOH (5 mL)에서 30분 동안 교반되었다. 혼합물이 여과되고 필터 케이크는 진공에서 건조되어 화합물27 (2-((4-아미노페닐)설포닐)-N-페닐히드라진-1-카르복사미드, 50 mg, yield 16.2%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 9.12 (s, 1H), 8.41 (s, 1H), 8.15 (s, 1H), 7.47 (d, J = 8.8 Hz, 2H), 7.38 (d, J = 8.0 Hz, 2H), 7.22 (t, J = 8.0 Hz, 2H), 6.94 (t, J = 7.2 Hz, 1H), 6.60 (d, J = 8.8 Hz, 2H), 6.04 (s, 2H).
LCMS ; Mass Calcd.:306; MS Found: 306.9.
실험예 1-28. 화합물28 (4-아미노-
N
'-(1
H
-인돌-4-카르보닐)-3-모르폴리노벤젠설포노히드라지드)의 제조
단계 1) A51의 합성
N2H4 H2O (10 mL) 내 A50 (메틸 1H-인돌-4-카르복실레이트, 1.00 g, 5.71 mmol, 1.0 eq)의 혼합물이 100oC에서 한시간 동안 교반되었다. 상기 용액이 물로 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 Na2SO4로 건조되고 농축되어 A51 (1H-인돌-4-카르보히드라지드, 500 mg, crude)이 노란색 고체로 얻어졌다.
단계 2) A52의 합성
피리딘 (2 mL) 내 A51 (1H-인돌-4-카르보히드라지드, 100 mg, 0.57 mmol, 1.0 eq)의 혼합물에 피리딘(2 mL) 내 3-플루오로-4-니트로벤젠-1-설포닐 클로라이드(175 mg, 0.57 mmol, 1.0 eq)이 적가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어졌고 EA로 추출되었다(30 mL x 3). 합한 유기층이 1N HCl (30 mL x 2) 및 염수로 세척되었고, Na2SO4로 건조되고 농축되어 A52 (3-플루오로-N'-(1H-인돌-4-카르보닐)-4-니트로벤젠설포노히드라지드, 200 mg, crude)가 노란색 고체로 얻어졌다.
단계 3) A53의 합성
DMF (5 mL) 내 A52 (3-플루오로-N'-(1H-인돌-4-카르보닐)-4-니트로벤젠설포노히드라지드, 200 mg, 0.52 mmol, 1.0 eq) 및 K2CO3 (183 mg, 1.30 mmol, 2.5 eq)의 혼합물에 모르폴린(54 mg, 0.62 mmol, 1.2 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 25oC에서 16시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A53(N'-(1H-인돌-4-카르보닐)-3-모르폴리노-4-니트로벤젠설포노히드라지드, 100 mg, crude)이 노란색 고체로 얻어졌다.
단계 4) 화합물28의 합성
EtOH (5 mL) 내 A53 (N'-(1H-인돌-4-카르보닐)-3-모르폴리노-4-니트로벤젠설포노히드라지드, 100 mg, 0.22 mmol, 1.0 eq)의 혼합물에 Fe (61.6 mg, 1.10 mmol, 5.0 eq) 및 sat. aq. NH4Cl (3 mL)이 첨가되었다. 이어서 혼합물이 85oC에서 3 시간 동안 교반되었다. 상기 용액이 여과되고 여과액이 prep-HPLC로 정제되고 동결 건조되어 화합물28(4-아미노-N'-(1H-인돌-4-카르보닐)-3-모르폴리노벤젠설포노히드라지드, 20 mg, yield 21.5%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ11.30 (s, 1H), 10.34 (s, 1H), 9.35 (d, J = 4.0 Hz, 1H), 7.54 (d, J = 8.4 Hz, 1H), 7.43 (t, J = 2.4 Hz, 1H), 7.30-7.35 (m, 3H), 7.11 (t, J = 7.6 Hz, 1H), 6.65-6.67 (m, 2H), 5.60 (br s, 2H), 3.64 (t, J = 4.0 Hz, 4H), 2.60 (t, J = 4.0 Hz, 4H).
LCMS ; Mass Calcd.:415; MS Found: 415.9 [MS+1].
실험예 1-29. 화합물29 (4-아미노-
N
'-(인돌린-4-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A54의 합성
피리딘(5 mL) 내 A51 (1H-인돌-4-카르보히드라지드, 400 mg, 2.29 mmol, 1.0 eq)의 혼합물에 피리딘(5 mL) 내 4-니트로벤젠-1-설포닐 클로라이드(505 mg, 2.29 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A54 (N'-(1H-인돌-4-카르보닐)-4-니트로벤젠설포노히드라지드, 300 mg, crude)가 노란색 고체로 얻어졌다.
단계 2) A55의 합성
DCM (5 mL) 내 A54 (N'-(1H-인돌-4-카르보닐)-4-니트로벤젠설포노히드라지드, 300 mg, 0.83 mmol, 1.0 eq)의 혼합물에 TFA(1.5 mL) 및 NaBH3CN(157 mg, 2.49 mmol, 3.0 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 10oC에서 45분 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 sat. aq. NaHCO3으로 pH = 7로 조정되었다. 혼합물이 여과되고 필터 케이크가 MTBE로 세척되고 진공에서 건조되어 A55 (N'-(인돌린-4-카르보닐)-4-니트로벤젠설포노히드라지드, 150 mg, crude)가 노란색 고체로 얻어졌다.
단계 3) 화합물29의 합성
MeOH (5 mL) 내 A55 (N'-(인돌린-4-카르보닐)-4-니트로벤젠설포노히드라지드, 150 mg, 0.41 mmol, 1.0 eq) 및 Pd/C (100 mg)의 혼합물이 10oC에서 2시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되어 조생성물이 얻어졌고, MeOH (10 mL) 내에서 30분 동안 교반되었다. 혼합물이 여과되고 필터 케이크가 진공에서 건조되어 화합물29 (4-아미노-N'-(인돌린-4-카르보닐)벤젠설포노히드라지드, 40 mg, yield 29.1%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ10.28 (d, J = 3.6 Hz, 1H), 9.28 (d, J = 3.6 Hz, 1H), 7.46 (d, J = 8.4 Hz, 2H), 7.03 (t, J = 8.0 Hz, 1H), 6.83 (d, J = 7.2 Hz, 1H), 6.75 (d, J = 7.2 Hz, 1H), 6.53 (d, J = 8.8 Hz, 2H), 3.42 (t, J = 8.4 Hz, 2H), 2.96 (t, J = 8.4 Hz, 2H).
LCMS ; Mass Calcd.:332; MS Found: 332.8 [MS+1].
실험예 1-30. 화합물30 (4-아미노-N'-(4-히드록시벤조일)-3-(피페라진-1-일)벤젠설포노히드라지드)의 제조
단계 1) A56의 합성
DMF (5 mL) 내 A4 (3-플루오로-N'-(4-히드록시벤조일)-4-니트로벤젠설포노히드라지드, 500 mg, 1.41 mmol, 1.0 eq) 및 K2CO3 (290 mg, 2.10 mmol, 1.5 eq)의 혼합물에 tert-부틸 피페라진-1-카르복실레이트(315 mg, 1.69 mmol, 1.2 eq)가 10oC에서 첨가되었다. 이어서 혼합물이 10oC에서 16시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬 컬럼(DCM/MeOH=50/1~30/1)으로 정제되어 A56 (tert-부틸 4-(5-((2-(4-히드록시벤조일)히드라지닐)설포닐)-2-니트로페닐)피페라진-1-카르복실레이트, 310 mg, crude)이 노란색 고체로 얻어졌다.
단계 2) A57의 합성
EtOH(3 mL) 내 A56 (tert-부틸 4-(5-((2-(4-히드록시벤조일)히드라지닐)설포닐)-2-니트로페닐)피페라진-1-카르복실레이트, 250 mg, 0.48 mmol, 1.0 eq)의 혼합물에 sat. aq. NH4Cl (3 mL) 및 Fe (135 mg, 2.41 mmol, 5.0 eq)이 첨가되었다. 이어서 혼합물이 85oC에서 1시간 동안 교반되었다. 상기 용액이 여과되고 여과액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4으로 건조되고 농축되어 A57 (tert-부틸 4-(2-아미노-5-((2-(4-히드록시벤조일)히드라지닐)설포닐)페닐)피페라진-1-카르복실레이트, 210 mg, crude)이 노란색 고체로 얻어졌다.
단계 3) 화합물30의 합성
DCM (5 mL) 내 A57 (tert-부틸 4-(2-아미노-5-((2-(4-히드록시벤조일)히드라지닐)설포닐)페닐)피페라진-1-카르복실레이트, 270 mg, 0.55 mmol, 1.0 eq)의 혼합물에 TFA (0.5 mL)가 10oC에서 첨가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 농축되어 조생성물이 얻어졌고, prep-HPLC로 정제되고 동결 건조되어 조생성물이 얻어졌다. 조생성물이 MeOH(2.5 mL) 및 CH3CN(2.5 mL) 내에서 5분 동안 교반되었다. 혼합물이 여과되고 필터케이크가 MeOH로 세척되고 건조되어 화합물30(4-아미노-N'-(4-히드록시벤조일)-3-(피페라진-1-일)벤젠설포노히드라지드, 20 mg, yield 9.30%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d 6, 400 MHz): δ 7.57 (d, J = 8.0 Hz, 2H), 7.21-7.25 (m, 2H), 6.76 (d, J = 8.0 Hz, 2H), 6.64 (d, J = 8.4 Hz, 1H), 5.54 (s, 2H), 2.78 (s, 4H), 2.54 (s, 4H).
LCMS ; Mass Calcd.:391; MS Found: 392.1 [MS+1].
실험예 1-31. 화합물31 (4-아미노-
N
'-(2,3-디히드로-1
H
-인덴-2-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A59의 합성
MeOH (50 mL) 내 A58 (2,3-디히드로-1H-인덴-2-카르복실산, 5.0 g, 30.8 mmol, 1.0 eq)의 혼합물에 H2SO4 (5 mL)가 적가되었다. 이어서 혼합물이 70oC에서 12시간 동안 교반되었다. 상기 용액이 물(60 mL)에 부어지고 EA로 추출되었다(60 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A59 (메틸 2,3-디히드로-1H-인덴-2-카르복실레이트, 5.3 g, yield 97.5%)가 노란색 오일로 얻어졌다.
단계 2) A60의 합성
MeOH (30 mL) 내 A59 (메틸 2,3-디히드로-1H-인덴-2-카르복실레이트, 3.0 g, 17.1 mmol, 1.0 eq)의 혼합물에 N2H4.H2O (8.56 g, 171 mmol, 10 eq)가 적가되었다. 이어서 혼합물이 80oC에서 12시간 동안 교반되었다. 상기 용액이 농축되어 A60 (2,3-디히드로-1H-인덴-2-카르보히드라지드, 2.0 g, yield 87.5%)이 노란색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 9.13 (s, 1H), 7.18-7.20 (m, 2H), 7.11-7.13 (m, 2H), 4.25 (br s, 2H), 3.01-3.11 (m, 5H).
단계 3) A61의 합성
피리딘 (20 mL) 내 A60 (2,3-디히드로-1H-인덴-2-카르보히드라지드, 2 g, 11.4 mmol, 1.0 eq)의 혼합물에 4-니트로벤젠-1-설포닐 클로라이드(2.52 g, 11.4 mmol, 1.0 eq)가 부분적으로 첨가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 물(100 mL)에 부어지고 EA로 추출되었다(100 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A61 (N'-(2,3-디히드로-1H-인덴-2-카르보닐)-4-니트로벤젠설포노히드라지드, 1.4 g, yield 34.1%)이 노란색 고체로 얻어졌다. (TLC: DCM/MeOH =10/1, Rf=0.5)
단계 4) 화합물31의 합성
MeOH (10 mL) 내 A61 (N'-(2,3-디히드로-1H-인덴-2-카르보닐)-4-니트로벤젠설포노히드라지드, 200 mg, 0.83 mmol, 1.0 eq)의 혼합물에 Pd/C (100 mg)가 첨가되었다. 이어서 혼합물이 10oC에서 12시간 동안 H2 벌룬(balloon)하에서 농축되었다. 상기 용액이 여과되고 여과액이 prep-HPLC로 정제되고 동결 건조되어 화합물31 (4-아미노-N'-(2,3-디히드로-1H-인덴-2-카르보닐)벤젠설포노히드라지드, 80 mg, yield 43.6%)이 백색 고체로 얻어졌다.
1HNMR (CD3OD, 400 MHz): δ 7.55 (dd, J = 6.8, 2.0 Hz, 2H), 7.07-7.12 (m, 4H), 6.65 (dd, J = 6.8, 2.0 Hz, 2H), 2.92-3.03 (m, 5H).
LCMS ; Mass Calcd.:331; MS Found: 331.8 [MS+1].
실험예 1-32. 화합물32 (4-아미노-N'-(이소인돌린-2-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A63의 합성
디클로로메탄(10 mL) 내 A62(이소인돌린, 1.00 g, 8.4 mmol, 1.0 eq)의 혼합물에 트리에틸아민(2 mL) 및 4-니트로페닐 클로로포르메이트(1.68 g, 8.4 mmol)가 첨가되었다. 혼합물은 실온에서 16 시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 디클로로메탄으로 추출되었다(30 mL x 3). 합한 유기층이 Na2SO4로 건조되고 농축되었다. 생성물이 테트라히드로퓨란(10 mL) 및 N2H4 H2O(2 mL)에 첨가되었다. 혼합물은 60oC에서 16시간 동안 교반되었다. 상기 용액이 물(50 mL)에 부어지고 에틸아세테이트로 추출되었다(30 mL x 3). 합한 유기층이 황산나트륨(Na2SO4 )으로 건조되고 농축되어 A63 (이소인돌린-2-카르보히드라지드, 600 mg, crude)이 노란색 고체로 얻어졌다. (TLC: DCM/MeOH =10/1, Rf=0.6)
LCMS ; Mass Calcd.:177.2; MS Found: 178.2 [MS+1].
단계 2) A64의 합성
피리딘(10 mL) 내 A63 (이소인돌린-2-카르보히드라지드, 600 mg, 3.39 mmol, 1.0 eq)의 혼합물에 피리딘 (5 mL) 내 4-니트로벤젠 -1-설포닐 클로라이드(750 mg, 3.39 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물(50 mL)에 부어지고 EA로 추출되었다(50 mL x 3). 합한 유기층이 1N HCl (50 mL x 2) 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 A64(N'-(이소인돌린-2-카르보닐)-4-니트로벤젠설포노히드라지드, 200 mg, crude)가 노란색 고체로 얻어졌다. (TLC: DCM/MeOH =20/1, Rf=0.5)
LCMS ; Mass Calcd.:362.3; MS Found: 363.1 [MS+1].
단계 3) 화합물32 (4-아미노-N'-(이소인돌린-2-카르보닐)벤젠설포노히드라지드)의 합성
에탄올 (10 mL) 내 A64 (200 mg, 0.55 mmol, 1.0 eq)의 혼합물에 Fe (154 mg, 2.75 mmol, 5.0 eq) 및 sat. aq. NH4Cl (6mL)이 첨가되었다. 이어서 혼합물이 85oC에서 3시간 동안 교반되었다. 상기 용액이 여과되고, 여과액이 농축되어 조 생성물이 얻어졌다. 조생성물이 prep-HPLC로 정제되고 동결 건조되어 화합물32 (4-아미노-N'-(이소인돌린-2-카르보닐)벤젠설포노히드라지드, 20 mg, yield 11.0%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 8.64 (s, 1H), 8.53 (s, 1H), 7.41-7.44 (m, 2H), 7.29-7.31 (m, 4H), 6.51-6.54 (m, 2H), 5.93 (s, 2H), 4.51 (s, 4H).
LCMS; Mass Calcd.:332; MS Found: 333 [MS+1].
실험예 1-33. 화합물33 (N'-(4-히드록시벤조일)-1H-인돌-2-설포노히드라지드)의 제조
단계 1) A66의 합성
테트라히드로퓨란(20 mL) 내 A65 (tert-부틸 1H-인돌-1-카르복실레이트, 2.00 g, 9.2 mmol, 1.0 eq)의 교반된 용액에 n-BuLi (4.0 mL, 2.5M in hexanes, 10.0 mmol, 1.1 eq)을 -70oC에서 적가하였다. 1 시간 후, SO2 (gas, 1 L)가 -70oC에서 천천히 첨가되었다. 반응 혼합물은 2시간에 걸쳐 10°C로 가온되었다. 용매가 감압하에 제거되었다. 잔류물이 디클로로메탄에 용해되었다(DCM, 20 mL). N-클로로숙신이미드 (NCS, 1.84g, 13.8 mmol, 1.5 eq)가 첨가되었다. 혼합물이 실온에서 10시간 동안 교반되었다. 혼합물이 물(2 X 20 mL) 및 염수(2 x 20 mL)로 세척되었다. 유기층이 건조되고 농축되었다. 잔류물이 컬럼크로마토그래피로 정제되어 (PE/EA=30/1-5/1) A66(tert-부틸 2-(클로로설포닐)-1H-인돌-1-카르복실레이트, 1.0 g, yield 34.4%)이 갈색 오일로 얻어졌다.
1HNMR (CDCl3, 400 MHz): δ 8.23-8.25 (m, 1H), 7.72 (d, J = 8.0 Hz, 1H), 7.69 (s, 1H), 7.56-7.60 (m, 1H), 7.35-7.39 (m, 1H), 1.75(s, 9H).
단계 2) A67의 합성
피리딘(10 mL) 내 4-히드록시벤조히드라지드(481 mg, 3.17 mmol, 1.0 eq)의 교반된 용액에 피리딘(5 mL) 내 A66 (tert-부틸 2-(클로로설포닐)-1H-인돌-1-카르복실레이트, 1.0 g, 3.17 mmol, 1.0 eq)의 용액이 0oC에서 적가되었다. 혼합물이 실온에서 5시간 동안 교반되었다. 혼합물이 여과되었다. 여과액이 농축되고 컬럼크로마토그래피로 정제되어 A67 (tert-부틸 2-((2-(4-히드록시벤조일)히드라지닐)설포닐)-1H-인돌-1-카르복실레이트, 500 mg, yield 36.5%)이 백색 고체로 얻어졌다.
단계 3) 화합물33의 합성
메탄올 (MeOH, 5 mL) 내 A67 (500 mg, 1.16 mmol, 1.0 eq)의 교반된 용액에 4N HCl(g)/MeOH (2 mL)이 0oC에서 첨가되었다. 혼합물이 실온에서 4시간 동안 교반되었다. 혼합물이 농축되고, prep-HPLC로 정제되고 동결 건조되어 화합물33 (N'-(4-히드록시벤조일)-1H-인돌-2-설포노히드라지드, 50 mg, yield 13%)이 회백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 11.94 (s, 1H), 10.42 (d, J = 1.6 Hz, 1H), 10.09 (s, 1H), 9.86 (d, J = 2.8 Hz, 1H), 7.61-7.64 (m, 3H), 7.45-7.47 (m, 1H), 7.24-7.28 (m, 1H), 7.07-7.11 (m, 1H), 6.99 (d, J = 1.2 Hz, 1H), 6.77 (d, J = 8.8 Hz, 2H).
LCMS ; Mass Calcd.:341; MS Found: 342 [MS+1].
실험예 1-34. 화합물34 (4-아미노-N'-(2-페닐아세틸)벤젠설포노히드라지드)의 제조
단계 1) A69의 합성
피리딘 (5 mL) 내 A68 (2-페닐아세토히드라지드, 500 mg, 3.33 mmol, 1.0 eq)의 혼합물에 피리딘 (5 mL) 내 4-니트로벤젠-1-설포닐 클로라이드(738 mg, 3.33 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 에틸아세테이트로 추출되었다(EA, 30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, DCM (30 mL) 내에서 30분 동안 교반되었다. 혼합물이 여과되고 필터케이크가 건조되어 A69 (4-니트로-N'-(2-페닐아세틸)벤젠설포노히드라지드, 1 g, yield 89.6%)가 노란색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 10.50 (s, 1H), 10.37 (s, 1H), 8.22 (d, J = 8.8 Hz, 2H), 7.92 (d, J = 8.8 Hz, 2H), 7.21-7.29 (m, 3H), 7.10-7.12 (m, 2H), 3.30 (s, 2H).
단계 1) 화합물34의 합성
MeOH (10 mL) 내 A69 (200 mg, 0.60 mmol, 1.0 eq)의 혼합물에 Pd/C (50 mg)이 첨가되었다. 이어서 혼합물이 10oC에서 2시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되었다. 조생성물이 MeOH (10 mL)로부터 3회 결정화되어 화합물34 (4-아미노-N'-(2-페닐아세틸)벤젠설포노히드라지드, 20 mg, yield 10.9%)이 회색 고체로 얻어졌다.(TLC: DCM/MeOH =10/1, Rf=0.3)
1HNMR (DMSO-d6, 400 MHz): δ 9.87 (s, 1H), 8.77 (s, 1H), 7.40 (d, J = 6.8 Hz, 2H), 7.18-7.29 (m, 3H), 7.13 (d, J = 6.8 Hz, 2H), 5.74 (s, 2H), 3.37 (s, 2H).
LCMS ; Mass Calcd.:305; MS Found: 306.1 [MS+1].
실험예 1-35. 화합물35 (N'-(4-히드록시벤조일)-1H-인다졸-3-설포노히드라지드)의 제조
단계 1) A70의 합성
아세트산 (16 mL), con. 염산 (1.6 mL) 및 포름산 (1.6 mL) 내 1H-인다졸-3-아민 (1.00 g, 7.5 mmol, 1.0 eq)의 교반된 용액에 NaNO2 (0.62 g, 9.0 mmol, 1.2 eq)가 0oC에서 첨가되었다. 혼합물이 1시간 동안 교반되었다. SO2 (gas, 1 L) 및 CuCl2 (0.38 g, 2.3 mmol, 0.3 eq)가 0oC에서 천천히 첨가되었다. 반응 혼합물이 10°C로 가온되었다. 혼합물이 감압하에서 농축되었다. 잔류물이 컬럼크로마토그래피로 정제되어(PE/EA=30:1-1:1) A70 (1H-인다졸-3-설포닐 클로라이드, 0.5 g, yield 30.8%)이 갈색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 14.13 (s, 2H), 7.94-7.92 (m, 1H), 7.46-7.38 (m, 2H), 7.14 (s, 1H).
단계 2) 화합물35 (N'-(4-히드록시벤조일)-1H-인다졸-3-설포노히드라지드)의 합성
피리딘 (5 mL) 내 4-히드록시벤조히드라지드(225 mg, 1.48 mmol, 0.8 eq)의 교반된 용액에 피리딘 (5 mL) 내 A70 (1H-인다졸-3-설포닐 클로라이드, 0.40 g, 1.85 mmol, 1.0 eq)의 용액이 0oC에서 적가되었다. 혼합물이 실온에서 5시간 동안 교반되었다. 혼합물이 농축되었다. 잔류물이 prep-HPLC로 정제되고 동결 건조되어 화합물35 (N'-(4-히드록시벤조일)-1H-인다졸-3-설포노히드라지드, 60 mg, yield 9.77%)가 백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 13.90 (s, 1H), 10.43 (s, 1H), 10.05-9.99 (m, 2H), 7.92 (d, J = 8.0 Hz, 1H), 7.62 (d, J = 8.4 Hz, 1H), 7.49 (d, J = 8.0 Hz, 2H), 7.42 (t, J = 7.0 Hz, 1H), 7.22 (t, J = 7.0 Hz, 1H), 6.72 (d, J = 8.0 Hz, 2H).
LCMS; Mass Calcd.:332; MS Found: 333 [MS+1].
실험예 1-36. 화합물36 (4-아미노-N'-(인돌린-6-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A72의 합성
A71 (methyl 1H-indole-6-carboxylate, 500 mg, 2.86 mmol, 1.0 eq) 및 히드라진 모노하이드레이트 (10 mL)의 혼합물이 100oC에서 3시간 동안 교반되었다. 이어서 혼합물이 0oC로 냉각되고 여과되었다. 필터케이크가 얼음물로 세척되고 진공에서 건조되어 A72 (1H-인돌-6-카르보히드라지드, 300 mg, yield 60.0%)가 백색 고체로 얻어졌다.
LCMS; Mass Calcd.:175.18; MS Found: 176.0 [MS+1].
단계 2) A73의 합성
피리딘 (5 mL) 내 A72 (300 mg, 1.71 mmol, 1.0 eq)의 혼합물에 4-니트로벤젠설포닐 클로라이드(380 mg, 1.71 mmol, 1.0 eq)가 0oC에서 첨가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 1N HCl (30 mL x 2) 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 플래쉬컬럼 (DCM/MeOH=50/1~30/1)으로 정제되어 A73 (N'-(1H-인돌-6-카르보닐)-4-니트로벤젠설포노히드라지드, 500 mg, yield 81.0%)이 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:360.34; MS Found: 361.1 [MS+1].
단계 3) A74의 합성
DCM (15 mL) 및 TFA (5 mL) 내 A73 (400 mg, 1.11 mmol, 1.0 eq)의 혼합물에 NaBH3CN (209 mg, 3.33 mmol, 3.0 eq)이 0oC에서 첨가되었다. 이어서 혼합물이 15oC에서 1시간동안 교반되었다. 상기 용액이 얼음 물(30 mL)에 부어졌고 sat. aq. NaHCO3으로 pH=7~8로 조정되었다. 상기 용액이 여과되었고, 필터케이크가 PE로 세척되고 건조되어 A74 (N'-(인돌린-6-카르보닐)-4-니트로벤젠설포노히드라지드, 200 mg crude)가 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:362.36; MS Found: 363.1 [MS+1].
단계 3) 화합물36의 합성
H2O (10 mL) 및 EtOH (20 mL) 내 A74 (200 mg, 0.55 mmol, 1.0 eq), NH4Cl (146 mg, 2.75 mmol, 5.0 eq), Fe (154 mg, 2.75 mmol, 5.0 eq)의 혼합물이 85oC에서 2시간 동안 교반되었다. 혼합물이 여과되고 여과액이 EA로 추출되었다(20 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되었다. 조생성물이 메탄올로 재결정화되고, 고체가 동결 건조되어 화합물36 (4-아미노-N'-(인돌린-6-카르보닐)벤젠설포노히드라지드, 60 mg, 32.7%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 10.32 (s, 1H), 9.14 (s, 1H), 7.40 (d, J = 8.4 Hz, 2H), 7.02 (d, J = 7.6 Hz, 1H), 6.87 (d, J = 7.2 Hz, 1H), 6.75 (s, 1H), 6.49 (d, J = 8.4 Hz, 2H), 5.95 (s, 2H), 5.67 (s, 1H), 3.41 (t, J = 8.2 Hz, 2H), 2.91 (t, J = 8.6 Hz, 2H).
LCMS; Mass Calcd.:332; MS Found: 333 [M+1].
실험예 1-37. 화합물37 (4-아미노-N'-(인돌린-3-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A76의 합성
DCM (10 mL) 내 A75 (메틸 1H-인돌-3-카르복실레이트, 1.00 g, 5.71 mmol, 1.0 eq) 및 트리에틸아민(TEA, 1.16 g, 11.4 mmol, 2.0 eq)의 혼합물에 Boc2O (1.37 g, 6.28 mmol, 1.1 eq)가 20oC에서 적가되었다. 이어서 혼합물이 20oC에서 12시간 동안 교반되었다. 상기 용액이 물(60 mL)에 부어지고 DCM으로 추출되었다(60 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A76 (1-(tert-부틸) 3-메틸 1H-인돌-1,3-디카르복실레이트, 1.20 g, crude)이 노란색 고체로 얻어졌다.
단계 2) A77의 합성
에틸아세테이트(EA, 30 mL) 내 A76 (1.20 g, 4.36 mmol, 1.0 eq)의 혼합물에 Pd/C (0.65 g)이 첨가되고 탈기되었다. 이어서 혼합물이 60oC에서 12시간 동안 H2(50 psi) 하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되어 조생성물이 얻어졌다. 조생성물이 실리카겔로 정제되어 (PE/EA=30:1~15:1) A77 (1-(tert-부틸) 3-메틸 인돌린-1,3-디카르복실레이트, 0.80 g, yield 66.2%)이 백색 고체로 얻어졌다.
단계 3) A78의 합성
MeOH (20 mL) 내 A77 (800 mg, 2.89 mmol, 1.0 eq)의 혼합물에 N2H4.H2O (1.6 mL)가 첨가되었다. 이어서 혼합물이 80oC에서 4시간 동안 교반되었다. 반응 혼합물이 농축되어 A78 (tert-부틸 3-(히드라진카르보닐)인돌린-1-카르복실레이트700 mg, yield 87.5%)이 백색 고체로 얻어졌다.
단계 3) A79의 합성
피리딘 (5 mL) 내 A78 (tert-부틸 3-(히드라진카르보닐)인돌린-1-카르복실레이트, 300 mg, 1.08 mmol, 1.0 eq)의 혼합물에 4-니트로벤젠-1-설포닐 클로라이드 (0.24 g, 1.08 mmol, 1.0 eq)가 부분적으로 첨가되었다. 이어서 혼합물이 10oC에서 4시간동안 교반되었다. 상기 용액이 물(100 mL)에 부어지고 EA로 추출되었다 (100 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A79 (tert-부틸 3-(2-((4-니트로페닐)설포닐)히드라진-1-카르보닐)인돌린-1-카르복실레이트, 200 mg, yield 39.7%)가 노란색 고체로 얻어졌다.
단계 4) A80의 합성
EA (10 mL) 내 A79 (200 mg, 0.43 mmol, 1.0 eq)의 혼합물에 Pd/C (50 mg)가 첨가되었다. 이어서 혼합물이 10oC에서 12시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되어 A80 (tert-부틸 3-(2-((4-아미노페닐)설포닐)히드라진-1-카르보닐)인돌린-1-카르복실레이트, 200 mg, yield:100%)이 노란색 고체로 얻어졌다.
단계 5) 화합물37(4-아미노-N'-(인돌린-3-카르보닐)벤젠설포노히드라지드)의 합성
DCM (5 mL) 내 A80 (200 mg, 0.463 mmol, 1.0 eq)의 혼합물에 트리플루오로아세트산(TFA, 1 mL)이 첨가되었다. 이어서 혼합물이 10oC에서 2시간 동안 교반되었다. 상기 용액이 농축되고, 잔류물에 H2O (5 mL)이 첨가되고 aq. K2CO3으로 pH=9-10으로 조정되었다. 용액이 EA로 추출되었다(20mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌다. 조생성물이 Prep-HPLC로 정제되고 동결 건조되어 화합물37 (4-아미노-N'-(인돌린-3-카르보닐)벤젠설포노히드라지드, 30.0 mg, yield 19.6%)가 회백색 고체로 얻어졌다.
1HNMR (DMSO_d6, 400 MHz): δ 7.45 (d, J = 8.4 Hz, 2H), 6.91-6.95 (m, 2H), 6.48-6.59 (m, 4H), 5.72 (s, 2H), 5.23 (s, 1H), 3.93 (br s, 1H), 3.49 (d, J = 9.2 Hz, 2H).
LCMS; MS Found: 333.1 [MS+1].
실험예 1-38. 화합물38 (N'-(4-히드록시벤조일)피페리딘-4-설포노히드라지드)의 제조
단계 1) A82의 합성
피리딘 (2 mL) 내 4-히드록시벤조히드라지드(A2, 268 mg, 1.77 mmol, 1.0 eq)의 혼합물에 피리딘 (1 mL) 내 A81 (tert-부틸 4-(클로로설포닐)피페리딘-1-카르복실레이트, 500 mg, 1.77 mmol, 1.0 eq)의 용액이 0oC에서 적가되었다. 혼합물이 실온에서 5시간 동안 교반되었다. 상기 용액이 여과되었다. 여과액이 농축되고 컬럼 크로마토그래피로 정제되어 (DCM/MeOH=100:1-10:1) A82 (tert-부틸 4-((2-(4-히드록시벤조일)히드라지닐)설포닐)피페리딘-1-카르복실레이트, 300 mg, yield 42%)가 노란색 고체로 얻어졌다.
1HNMR (CDCl3, 400 MHz): δ 8.47 (br s, 1H), 7.70 (d, J = 8.8 Hz, 2H), 7.30 (br s, 1H), 6.87 (d, J = 8.4 Hz, 2H), 3.15-3.18 (m, 1H), 2.67-2.71 (m, 2H), 2.25 (d, J = 10.8 Hz, 2H), 1.72-1.78 (m, 2H), 1.61-1.63 (m, 2H), 1.45 (s, 9H).
단계 2) 화합물38 (N'-(4-히드록시벤조일)피페리딘-4-설포노히드라지드)의 합성
DCM (5 mL) 내 A82 (300 mg, 0.75 mmol, 1.0 eq)의 혼합물에 TFA (1.5 mL)가 0oC에서 첨가되었다. 혼합물이 실온에서 4시간 동안 교반되었다. 상기 용액이 농축되고 prep-HPLC로 정제되고 동결 건조되어 화합물38 (N'-(4-히드록시벤조일)피페리딘-4-설포노히드라지드, 50 mg, yield 22%)가 노란색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 10.40 (br s, 1H), 8.34 (s, 1H), 7.75 (d, J = 8.4 Hz, 2H), 6.83 (d, J = 8.8 Hz, 2H), 3.17-3.24 (m, 3H), 2.69 (t, J = 12.0 Hz, 2H), 2.28 (d, J = 12.0 Hz, 2H), 1.64-1.74 (m, 2H).
LCMS; Mass Calcd.:299; MS Found: 300 [Ms+1].
실험예 1-39. 화합물39 (4-아미노-N'-(인돌린-6-카르보닐)-3-모르폴리노벤젠설포노히드라지드)의 제조
단계 1) A83의 합성
피리딘 (5 mL) 내 A72 (1H-인돌-6-카르보히드라지드, 500 mg, 2.86 mmol, 1.0 eq)의 혼합물에 피리딘 (2 mL) 내 3-플루오로-4-니트로벤젠-1-설포닐 클로라이드 (686 mg, 2.86 mmol, 1.0 eq)가 0oC에서 적가되었다. 이어서 혼합물이 10oC에서 3 시간 동안 교반되었다. 상기 용액이 농축되어 조생성물이 얻어지고, 컬럼으로 정제되어(DCM:MeOH=50:1---20:1) A83 (3-플루오로-N'-(1H-인돌-6-카르보닐)-4-니트로벤젠설포노히드라지드, 700 mg, yield:64.8%)이 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:378.3; MS Found: 379.1 [Ms+1].
단계 2) A84의 합성
DMF (7 mL) 내 A83 (700 mg, 1.85 mmol, 1.0 eq) 및 K2CO3 (640 mg, 4.64 mmol, 2.5 eq)의 혼합물에 모르폴린(193 mg, 2.22 mmol, 1.2 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 25oC에서 16시간 동안 교반되었다. 상기 용액이 물 (30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A84 (N'-(1H-인돌-6-카르보닐)-3-모르폴리노-4-니트로벤젠설포노히드라지드, 600 mg, yield:72.8%)가 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:445.4; MS Found: 446.1 [Ms+1].
단계 3) A85의 합성
DCM (5 mL) 내 A84 (600 mg, 1.35 mmol, 1.0 eq)의 혼합물에 TFA (1 mL) 및 NaBH3CN (251 mg, 4.04 mmol, 3.0 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 25oC에서 4시간 동안 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA 로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 A85 (N'-(인돌린-6-카르보닐)-3-모르폴리노-4-니트로벤젠설포노히드라지드, 450 mg, crude)가 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:447.4; MS Found: 448.2 [Ms+1].
단계 4) 화합물39 (4-아미노-N'-(인돌린-6-카르보닐)-3-모르폴리노벤젠설포노히드라지드)의 합성
EtOH (5 mL) 내 A85 (450 mg, 1.01 mmol, 1.0 eq)의 혼합물에 Fe (282 mg, 5.05 mmol, 5.0 eq) 및 sat. aq. NH4Cl (1 mL)이 첨가되었다. 이어서 혼합물이 85oC에서 3시간 동안 교반되었다. 상기 용액이 농축되고, 이어서 DMSO (5 mL)가 첨가되고 여과되었다. 여과액이 prep-HPLC로 정제되고 동결 건조되어 화합물39 (4-아미노-N'-(인돌린-6-카르보닐)-3-모르폴리노벤젠설포노히드라지드, 30 mg, yield 7.0%)이 회백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ10.36 (d, J = 4.4 Hz, 1H), 9.21 (d, J = 4.4 Hz, 1H), 7.23-7.27 (m, 2H), 7.03 (d, J = 7.6 Hz, 1H), 6.89 (d, J = 7.6 Hz, 1H), 6.67 (s, 1H), 6.65 (d, J = 8.4 Hz, 1H), 5.63 (br s, 2H), 3.69 (t, J = 4.2 Hz, 4H), 3.42 (t, J = 8.6 Hz, 2H), 2.91 (t, J = 8.6 Hz, 2H),2.63 (t, J = 4.2 Hz, 4H).
LCMS; Mass Calcd.:417.1; MS Found: 418.1 [MS+1].
실험예 1-40. 화합물40 (4-아미노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A87의 합성
피리딘 (10 mL) 내 A86 (tert-부틸 4-(히드라진카르보닐)피페라진-1-카르복실레이트, 1.00 g, 4.09 mmol, 1.0 eq)의 혼합물에 피리딘 (5 mL) 내 4-니트로벤젠-1-설포닐 클로라이드(906 mg, 4.09 mmol, 1.0 eq)가 10oC에서 적가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물(50 mL)에 부어지고 EA로 추출되었다(50 mL x 3). 합한 유기층이 1N HCl (50 mL x 2) 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌다. 조생성물이 EA로 세척되고(5 mL), 여과되고 진공에서 고체를 건조시켜 A87 (tert-부틸 4-(2-((4-니트로페닐)설포닐)히드라진-1-카르보닐)피페라진-1-카르복실레이트, 800 mg, yield 45.5%)이 노란색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 9.74 (s, 1H), 9.08 (s, 1H), 8.38 (d, J = 8.0 Hz, 2H), 8.03 (d, J = 8.4 Hz, 2H), 3.17 (br s, 8H), 1.40 (s, 9H).
단계 2) A88의 합성
THF (10 mL) 내 A87 (400 mg, 0.93 mmol, 1.0 eq)의 혼합물에 Pd/C (40 mg)가 첨가되었다. 이어서 혼합물이 10oC에서 16시간 동안 H2 벌룬(balloon)하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되어 A88 (tert-부틸 4-(2-((4-아미노페닐)설포닐)히드라진-1-카르보닐)피페라진-1-카르복실레이트, 350 mg, yield 94%)이 노란색 고체로 얻어졌다.
단계 3) 화합물40 (4-아미노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드)의 합성
DCM (5 mL) 내 A88 (150 mg, 0.37 mmol, 1.0 eq)의 혼합물에 TFA (1 mL)가 첨가되었다. 이어서 혼합물이 25oC에서 3시간 동안 교반되었다. 상기 용액이 농축되어 조생성물이 얻어졌다. 조생성물에 MeOH (5 mL)가 첨가되고, K2CO3 (62 mg, 0.45 mmol)가 첨가되고 실온에서 1시간 동안 교반되었다. 용액이 여과되고 prep-HPLC으로 정제되고 동결 건조되어 화합물40 (4-아미노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드, 50 mg, yield 38.7%)이 백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 8.80 (d, J = 2.8 Hz, 1H), 8.28-8.32 (m, 3H), 7.38 (d, J = 8.8 Hz, 2H), 6.56 (d, J = 8.8 Hz, 2H), 5.98 (s, 2H), 3.22 (s, 4H), 2.69 (s, 4H).
LCMS; Mass Calcd.:299; MS Found: 300 [MS+1].
실험예 1-41. 화합물41 (4-아미노-3-모르폴리노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드)의 제조
단계 1) A89의 합성
피리딘 (10 mL) 내 A86 (1.50 g, 6.14 mmol, 1.0 eq)의 혼합물에 피리딘 (5 mL) 내 3-플루오로-4-니트로벤젠-1-설포닐 클로라이드(1.46 g, 6.14 mmol, 1.0 eq)가 적가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물 (30 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 1N HCl (30 mL x 2) 및 염수로 세척되고, Na2SO4로 건조되고 농축되어 A89 (tert-부틸 4-(2-((3-플루오로-4-니트로페닐)설포닐)히드라진-1-카르보닐)피페라진-1-카르복실레이트, 1.5 g, crude)가 노란색 고체로 얻어졌다.
단계 2) A90의 합성
DMF (15 mL) 내 A89 (1.50 g, 3.35 mmol, 1.0 eq) 및 K2CO3 (1.16 g, 8.37 mmol, 2.5 eq)의 혼합물에 모르폴린(350 mg, 4.02 mmol, 1.2 eq)이 10oC에서 첨가되었다. 이어서 혼합물이 25oC에서 16시간 동안 교반되었다. 상기 용액이 물(50 mL)에 부어지고 EA로 추출되었다(30 mL x 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, 컬럼으로 정제되어 (DCM/MeOH =50/1―10/1) A90 (tert-부틸 4-(2-((3-모르폴리노-4-니트로페닐)설포닐)히드라진-1-카르보닐)피페라진-1-카르복실레이트, 700 mg, yield:40.6%)이 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:514.55; MS Found: 516.2[MS+2].
단계 3) A91의 합성
THF (10 mL) 내 A90 (700 mg, 1.36 mmol, 1.0 eq)의 혼합물에 Pd/C (200 mg)가 첨가되었다. 이어서 혼합물이 실온에서 15 분 동안 H2(50 psi)하에서 교반되었다. 상기 용액이 여과되고 여과액이 농축되어 A91 (tert-부틸 4-(2-((4-아미노 -3-모르폴리노페닐)설포닐)히드라진-1-카르보닐)피페라진-1-카르복실레이트, 300 mg, crude)이 노란색 고체로 얻어졌다.
단계 4) 화합물41 (4-아미노-3-모르폴리노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드)의 합성
DCM (10 mL) 내 A91 (200 mg, 0.41 mmol, 1.0 eq)의 혼합물에 TFA (2 mL)가 첨가되었다. 이어서 혼합물이 실온에서 3시간 동안 교반되었다. 혼합물이 농축되고 prep-HPLC로 정제되고 동결 건조되어 화합물41 (4-아미노-3-모르폴리노-N'-(피페라진-1-카르보닐)벤젠설포노히드라지드, 20.0 mg, yield 12.6%)이 분홍색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): δ 8.92 (d, J = 5.2 Hz, 1H), 8.69-8.75 (m, 2H), 7.23 (d, J = 5.6 Hz, 2H), 6.70 (t, J = 8.6Hz, 1H), 5.68 (s, 2H), 3.78 (s, 4H), 3.39 (s,4H), 2.98 (s, 4H), 2.76 (s, 4H).
LCMS; Mass Calcd.:384; MS Found: 384.9 [MS+1].
실험예 1-42. 화합물42 (N'-(4-히드록시벤조일)-2-메틸티아졸-4-설포노히드라지드)의 제조
단계 1) A92의 합성
2,2,2-트리클로로아세트알데히드(20 g, 0.13 mmol), 아세트아미드(7 g, 0.118 mmol), 및 농축된 황산 (1.2 g)의 교반된 혼합물이 100oC에서 1시간 동안 가열되었다. 반응 혼합물이 냉각하여 결정화되었다. 혼합물을 탈이온수로 분쇄하고, 여과하고, 다량의 물로 세척하고, 에탄올로 재결정하여 A92 (N-(2,2,2-트리클로로-1-히드록시에틸)아세트아미드, 15 g)가 백색 고체로 얻어졌다.
1HNMR (DMSO_d6, 400 MHz): 8.72 (d, 1H), 7.64 (d, 1H), 5.74-5.70 (m, 1H), 1.92 (s, 3H).
단계 2) A93의 합성
아연 가루(5 g, 78 mmol)가 빙초산 (50 mL) 내 A92 (8 g, 39 mmol)의 교반된 현탁액에 3시간에 걸쳐 천천히 첨가되었다. 아연 첨가 동안 반응 혼합물의 온도는 40oC이하로 유지되었다. 반응 혼합물은 실온에서 24시간 동안 교반되었다. 이어서 침전된 아연 염을 여과하고 빙초산으로 세척하였다. 아세트산이 감압 하에 제거되었다. 고체 잔류물을 탈이온수로 분쇄하고 재결정하여 A93 (N-(2,2-디클로로비닐)아세트아미드, 3 g)이 백색 고체로 얻어졌다.
1HNMR (DMSO_d6, 400 MHz): 9.87 (d, 1H), 7.21 (d, 1H), 2.03 (s, 3H).
단계 3) A94의 합성
벤질티올 (4 g, 32 mmol) 및 트리에틸아민 (3.29 g, 32.6 mmol)이 2-프로판올 (25 mL) 내 A93 (2 g, 13 mmol)의 교반된 용액에 첨가되었다. 반응 혼합물이 실온에서 48시간 동안 교반되었다. 이어서 용매가 감압 하에서 제거되고 잔류물이 물로 분쇄되어 결정질 고체가 생성되었다. 조생성물이 2-프로판올 또는 에탄올로부터 재결정화하여 정제되어 A94 (N-(1-(benzylthio)-2,2-dichloroethyl)acetamide, 2.5 g)가 백색 고체로 얻어졌다.
1HNMR (DMSO_d6, 400 MHz): 8.72(d, 1H), 7.23-7.25 (m, 5H), 6.42 (d, 1H), 5.40 (dd, 1H), 3.87 (q, 2H), 1.93 (S, 3H).
단계 4) A95의 합성
Lawesson 시약 (7.6 g, 18.8 mmol)이 톨루엔(30 mL) 내 A94 (5 mmol)의 교반된 용액에 첨가되었다. 반응 혼합물이 8시간 동안 환류되고, 용매가 감압 하에 제거되었다. 잔류물이 10% 수성 NaOH로 분쇄되고, pH 9로 조정되었다. 미가공 생성물이 여과되고, 건조되고, 2-프로판올로부터 재결정화되었다. 액체 생성물이 디클로로메탄으로 추출되어 A95 (4-(벤질티오)-2-메틸티아졸, crude, 2.5 g)가 노란색 오일로 얻어졌다.
1HNMR (DMSO_d6, 400 MHz): 7.44 (s, 1H), 7.30-7.20 (m, 5H), 4.04 (s, 2H), 2.59 (S, 3H).
단계 5) A96의 합성
아세트산(10 ml) 내 A95 (crude,1 g)의 용액에 NCS (3 g) 및 물(2 mL)이 0oC에서 첨가되었다. 반응 혼합물이 실온에서 밤새 교반되었다. 반응 혼합물이 pH =8로 조정한 10% 수성 NaHCO3로 분쇄되고, DCM으로 추출되었다 (30 mL * 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌다. 잔류물이 실리카 겔 통과를 통해 정제되어 A96 (2-메틸티아졸-4-설포닐 클로라이드, 100 mg)이 노란색 고체로 얻어졌다.
1HNMR (CDCl3, 400 MHz): 8.33 (s, 1H), 2.86 (S, 3H).
단계 6) 화합물42 (N'-(4-히드록시벤조일)-2-메틸티아졸-4-설포노히드라지드)의 합성
피리딘 (20 mL) 내 A96 (100 mg, 0.5 mmol) 및 A2 (4-히드록시벤조히드라지드, 80 mg, 0.5 mmol)의 혼합물이 80oC에서 밤새 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL * 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌다. 잔류물이 prep-HPLC로 정제되어 화합물42 (N'-(4-히드록시벤조일)-2-메틸티아졸-4-설포노히드라지드, 30 mg)가 회백색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): 10.53 (s, 1H), 10.27 (s, 1H), 10.13 (s, 1H), 8.02 (s, 1H), 7.63 (d, 2H), 6.80 (d, 2H), 2.70 (s, 3H).
LCMS; Mass Calcd.:313.3; MS Found: 314.0 [MS+1].
실험예 1-43. 화합물43 ((1S,4S)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드)의 제조
단계 1) A98의 합성
피리딘 (100mL) 내 A97 (tert-부틸 ((1r,4r)-4-히드록시시클로헥실)카바메이트, 27 g, 126 mmol, 1.0eq)의 혼합물에 4-메틸벤젠설포닐 클로라이드(28.6 g, 151mmol, 1.2eq)가 부분적으로 첨가되었고, 혼합물이 실온에서 밤새 교반되었다. 피리딘이 진공에서 제거되고, 잔류물이 실리카겔 컬럼 크로마토그래피로 정제되어 A98 ((1r,4r)-4-((tert-부톡시카르보닐)아미노)시클로헥실 4-메틸벤젠설포네이트, 40 g, 86.4%)이 백색 고체로 얻어졌다.
단계 2) A99의 합성
DMF (100mL) 내 A98 (10.0 g, 27.1 mmol, 1.0eq)의 용액이 티오아세테이트 칼륨(9.3 g, 81.3 mmol, 3.0eq)으로 처리되고 반응 혼합물이 60oC에서 질소 하에서 4시간 동안 교반되었다. 반응 혼합물이 염수(200mL)로 퀜치되고 EtOAc로 추출되었다(100 mL*2). 합한 유기물이 건조되고 감압 하에 농축되고, 조생성물이 실리카겔 컬럼 크로마토 그래피로 정제되어 A99 (S-((1s,4s)-4-((tert-부톡시카르보닐)아미노)시클로헥실)에탄티오에이트, 3.0 g, 40.5%)가 백색 고체로 얻어졌다.
단계 3) A100의 합성
DCM (30 mL) 및 물 (30 mL) 내 A99 (2.50 g, 9.16 mmol, 1.0 eq)의 용액에 0oC에서 30분 동안 염소 가스가 버블링 되었다. 두 층이 분리되고, DCM 층이 aq. 티오 황산나트륨 및 염수로 세척되고, 황산나트륨으로 건조되고, 여과되고 농축되어 조(crude) A100 (tert-부틸 ((1s,4s)-4-(클로로설포닐)시클로헥실)카바메이트)이 갈색 고체로 얻어졌다.
단계 4) A101의 합성
피리딘 (10 mL) 내 4-히드록시벤조히드라지드(A2, 2.76 g, 18.2 mmol, 2.0eq)의 용액에 DCM (5 mL) 내 A100 (crude)의 용액이 적가되고, 혼합물이 실온에서 2 시간동안 교반되었다. 용매가 진공에서 제고되고 조생성물이 실리카겔 컬럼 크로마토그래피로 정제되어 A101 (tert-부틸 ((1s,4s)-4-((2-(4-히드록시벤조일)히드라지닐)설포닐)시클로헥실)카바메이트, 0.2 g, 5.3% for 2 steps)이 백색 고체로 얻어졌다.
단계 5) 화합물43 ((1s,4s)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드)의 합성
A101 (200 mg, 4.2 mmol, 1.0 eq)이 TFA (1 mL) 및 DCM (5 mL)의 혼합물에 용해되고, 2시간 동안 교반되었다. 혼합물이 진공에서 농축되고 MeOH에 용해되고, NH3/MeOH가 pH=9로 첨가되고, 용매가 진공에서 농축되고, 잔류물이 MeOH에 용해되고, prep-HPLC로 정제되고 동결 건조하여 화합물43 ((1s,4s)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드, 20 mg, 13.2%)이 노란색 고체로 얻어졌다.
1HNMR (CD3OD, 400 MHz): δ 7.749 (d, J=8.8Hz, 2H), 6.862 (d, J=8.4Hz, 2H), 3.286-3.331 (m, 2H), 2.315-2.350 (m, 2H), 1.995-2.153 (m, 4H), 1.855-1.918 (m, 2H).
LCMS; MS Calcd.:313.11; MS Found: 313.9 ([M+1]+).
실험예 1-44. 화합물44 ((1R,4R)-4-아미노-N'-(4-히드록시벤조일)시클로헥산-1-설포노히드라지드)의 제조
A97 대신 tert-부틸 ((1s,4s)-4-히드록시시클로헥실)카바메이트를 출발 물질로 사용하여 실험예 1-45와 동일한 방법으로 화합물44를 백색 고체로(26.7 % yield) 합성하였다.
1HNMR (CD3OD, 400 MHz): δ 7.750 (d, J=8.8Hz, 2H), 6.868 (d, J=8.4Ha, 2H), 3.042-3.174 (m, 2H), 2.567 (d, J=12.4Hz, 2H), 2.180 (d, J=12.4Hz, 2H), 1.680-1.784 (m, 2H), 1.410-1.514 (m, 2H).
LCMS; MS Calcd.:313.11; MS Found: 313.9 ([M+1]+).
실험예 1-45. 화합물45 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)-5-메틸퓨란-2-카르복실산)의 제조
단계 1) A102의 합성
5-메틸퓨란-2-카르복실 산(10 g, 80 mmol), 클로로설폰산 (30 mL)의 교반된 혼합물이 얼음물로 퀜칭되기 전에 50oC에서 3시간 동안 교반되었다. 수성층이 DCM으로 추출되었고, 합한 유기 추출물이 염수로 세척되었고, 무수 황산나트륨으로 건조되고, 진공에서 농축되어 화합물 A102 (14 g)가 노란색 고체로 얻어졌다.
1HNMR (DMSO_d6, 400 MHz): 13.95 (s, 1H), 6.97 (s, 1H), 2.50 (s, 3H).
단계 2) 화합물45 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)-5-메틸퓨란-2-카르복실 산)의 합성
피리딘 (50 mL) 내 화합물 A102 (5 g, 22.3 mmol) 및 화합물 A2 (3.4 g, 22.3 mmol)의 혼합물이 60oC에서 밤새 교반되었다. 상기 용액이 물(30 mL)에 부어지고 EA로 추출되었다(30 mL * 3). 합한 유기층이 염수로 세척되고, Na2SO4로 건조되고 농축되어 조 생성물이 얻어졌다. 잔류물이 prep-HPLC로 정제되어 화합물45 (4-((2-(4-히드록시벤조일)히드라지닐)설포닐)-5-메틸퓨란-2-카르복실 산, 1.3 g)가 노란색 고체로 얻어졌다.
1HNMR (DMSO-d6, 400 MHz): 13.5 (brs, 1H), 10.47 (s, 1H), 10.14 (s, 1H), 10.03 (s, 1H), 7.63 (d, 2H), 7.18 (s, 1H), 6.79 (s, 2H), 3.17 (s, 3H)
실험예 1-46. 화합물46 (N'-(4-히드록시벤조일)피롤리딘-3-설포노히드라지드)의 제조
단계 1) A104의 합성
DCM (50 mL) 내 A103 (5.00 g, 26.7 mmol, 1.0 eq) 및 TEA (5.40 g, 53.4 mmol, 2.0 eq)의 교반된 용액에 메탄 설포닐 클로라이드(4.59 g, 40.1 mmol, 1.5 eq)가 0 oC에서 적가되었다. 혼합물이 실온에서 2시간 동안 교반되었다. 혼합물이 H2O (100 mL)로 퀜치되었고 DCM으로 추출되었다(100 mLx2). 합한 유기층이 염수로 세척되었고(100 mL), 건조되고, 농축되었다. 잔류물이 컬럼 크로마토그래피로 정제되어 (PE/EA=100:1-10:1) A104 (5.0 g, yield 70.6%)가 노란색 오일로 얻어졌다. (PE/EA = 10:1, Rf = 0.6)
단계 2) A105의 합성
DMF (50 mL) 내 A104 (5.00 g, 18.9 mmol, 1.0 eq) 및 티오아세테이트 칼륨 (4.30 g, 37.7 mmol, 2.0 eq)의 혼합물이 70oC에서 16시간 동안 교반되었다. 혼합물이 H2O (200 mL)로 처리되고 EA로 추출되었다(200 mLx2). 합한 유기층이 H2O (100 mLx3), 염수 (100 mL)로 세척되고, 건조되고, 농축되었다. 잔류물이 컬럼 크로마토그래피로 정제되어 (PE/EA=50:1-5:1) A105 (2.0 g, yield 43.4%) 가 갈색 고체로 얻어졌다.
단계 3) A106의 합성
아세트산 (AcOH 30 mL) 및 H2O (30 mL) 내 A105 (2.00 g, 8.16 mmol, 1.0 eq)의 교반된 용액에 N-클로로숙신이미드(5.45 g, 40.8 mmol, 5.0 eq)가 첨가되었다. 혼합물이 실온에서 16시간 동안 교반되었다. 혼합물이 농축되고 컬럼크로마토그래피로 정제되어 (PE/EA=50:1-1:1) A106 (1.0 g, yield 45.6%)이 노란색 오일로 얻어졌다. (PE/EA = 3:1, Rf = 0.5)
1HNMR (CDCl3, 400 MHz): δ 4.28-4.31 (m, 1H), 4.00-4.02 (m, 1H), 3.85-3.95 (m, 1H), 3.66-3.75 (m, 1H), 3.52-3.58 (m, 1H), 2.63 (br s, 1H), 2.44-2.54 (m, 1H), 1.49 (s, 9H).
단계 4) A107의 합성
피리디늄 (30 mL) 내 4-히드록시벤조히드라지드 (0.56 g, 3.71 mmol, 1.0 eq)의 교반된 용액에 피리디늄 (10 mL) 내 A106 (1.00 g, 3.71 mmol, 1.0 eq)의 용액이 0oC에서 적가되었다. 혼합물이 실온에서 6시간 동안 교반되었다. 혼합물이 농축되고 컬럼 크로마토그래피로 정제되어 (DCM/MeOH=100:1-10:1) A107 (0.50 g, yield 34.9%)이 노란색 오일로 얻어졌다. (DCM/MeOH = 10:1, Rf = 0.4)
단계 5) 화합물46 (N'-(4-히드록시벤조일)피롤리딘-3-설포노히드라지드)의 합성
DCM (10 mL) 내 A107 (500 mg, 1.30 mmol, 1.0 eq)의 혼합물에 TFA (4 mL)가 0oC에서 첨가되었다. 혼합물이 실온에서 4시간 동안 교반되었다. 상기 용액이 농축되고 prep-HPLC로 정제되고 동결 건조되어 화합물46 (N'-(4-히드록시벤조일)피롤리딘-3-설포노히드라지드, 30 mg, yield 7.0%)이 옅은 노란색 고체로 얻어졌다. (TLC: N/A)
1HNMR (DMSO-d6, 400 MHz): δ 10.47 (br s, 2H), 8.25 (s, 1H), 7.75 (d, J = 8.4 Hz, 2H), 6.83 (d, J = 8.8 Hz, 2H), 3.67-3.72 (m, 1H), 3.19-3.21 (m, 2H), 2.89-2.91 (m, 1H), 2.83-2.85 (m, 1H), 2.07-2.10 (m, 2H).
실험예 1-47. 화합물47 (N'-(4-히드록시벤조일)-1H-피롤로 [2,3-b]피리딘-2-설포노히드라지드)의 제조
단계 1) A109의 합성
THF (60 mL) 내 1H-피롤로[2,3-b]피리딘 (A108, 6.00 g, 50.8 mmol, 1.0 eq)의 혼합물에 NaH (2.44 g (60% w/w), 60.9 mmol, 1.2 eq)가 0oC에서 첨가되고 1 시간 동안 0oC에서 교반되었다. 이어서 용액에 THF (20 mL) 내 TsCl (9.65 g, 50.8 mmol, 1.0 eq)가 적가되었다. 용액이 16시간 동안 교반되었다. 상기 용액이 물(200 mL)에 부어지고 EA로 추출되었다(100 mL x 3). 합한 유기층이 Na2SO4로 건조되고 농축되어 조생성물이 얻어졌고, PE (30 mL)로 한시간 동안 세척되고, 여과되고 고체가 수집되었다. 고체가 진공에서 건조되어 A109(11.0 g, yield 79.5%)가 백색 고체로 얻어졌다. (TLC: N/A)
*LCMS; Mass Calcd.:272.32; MS Found: 273.1 [MS+1].
단계 2) A110의 합성
THF (20 mL) 내 A109 (2.00 g, 7.35 mmol, 1.0 eq)의 혼합물에 n-BuLi (3.24 mL, 8.08 mmol, 1.1 eq)이 -76oC에서 적가되었다. 혼합물이 -76oC에서 1시간 동안 교반되었다. 이어서 혼합물이 -76oC 내지 10oC에서 1시간 동안 SO2 벌룬(balloon)하에서 교반되었고 용액이 농축되었다. DCM (30 mL) 내 잔류물에 NCS (1.58 g, 11.7 mmol, 1.6 eq)가 20oC에서 첨가되었고, 이어서 혼합물이 20oC에서 한시간 동안 교반되었다. 상기 용액이 물(50 mL)에 부어지고 DCM으로 추출되었다(50 mL x 3). 합한 유기층이 Na2SO4로 건조되고 농축되어 A110 (1.30 g, yield 47.8%)이 노란색 고체로 얻어졌다.
LCMS; Mass Calcd.:370.82; MS Found: 371.0 [MS+1].
단계 3) A111의 합성
피리딘 (10 mL) 내 A110 (1.30 g, 3.51 mmol, 1.0 eq)의 혼합물에 피리딘 (5 mL) 내 4-히드록시벤조히드라지드(A2, 587 mg, 3.86 mmol, 1.1 eq)가 10oC에서 적가되었다. 이어서 혼합물이 10oC에서 3시간 동안 교반되었다. 상기 용액이 물 (50 mL)에 부어지고 EA로 추출되었다(50 mL x 3). 합한 유기층이 1N HCl (50 mL x 2) 및 염수(50 mL)로 세척되고, Na2SO4로 건조되고 농축되어 조생성물이 얻어졌다. 조생성물이 EA (5 mL)로 세척되고, 여과되고 진공에서 고체로 건조되어 A111 (600 mg, yield 35.3%)이 노란색 고체로 얻어졌다. (TLC: N/A)
LCMS; Mass Calcd.:486.51; MS Found: 487.1 [MS+1].
단계 4) 화합물47 (N'-(4-히드록시벤조일)-1H-피롤로[2,3-b]피리딘-2-설포노히드라지드)의 합성
MeOH (6 mL) 내 A111 (350 mg, 0.71 mmol, 1.0 eq)의 혼합물에 con. HCl (2 mL)이 첨가되었다. 이어서 혼합물이 60oC에서 3시간 동안 교반되었다. 상기 용액이 농축되고, 조생성물이 prep-HPLC로 정제되고 동결 건조되어 화합물47 (N'-(4-히드록시벤조일)-1H-피롤로[2,3-b]피리딘-2-설포노히드라지드, 20 mg, yield 8.36%)가 백색 고체로 얻어졌다. (TLC: N/A)
1HNMR (DMSO-d6, 400 MHz): δ 12.61 (s, 1H), 10.45 (s, 1H), 10.11 (br s, 1H), 9.90 (d, J=2 Hz, 1H), 8.40-8.42 (m, 1H), 8.08-8.10 (m, 1H), 7.62 (d, J=8.8 Hz, 2H), 7.16-7.19 (m, 1H), 7.13 (s, 1H), 6.77 (d, J=8.8 Hz, 2H).
LCMS; Mass Calcd.:332; MS Found: 333 [MS+1].
실험예 1-48. 화합물48 (4-히드록시-
N
'-(4-메톡시벤질)벤조히드라지드 )의 제조
실험예 1-19와 동일한 제조 방법으로, 1-(브로모메틸)-4-니트로벤젠 대신 1-(브로모메틸)-4-메톡시벤젠을 사용하여 화합물48이 얻어진다.
실험예 1-49. 화합물49 (
N
'-(4-아미노벤질)-2,3-디히드로-1
H
-인덴-2-카르보히드라지드)의 제조
A2 대신 A60 (2,3-디히드로-1H-인덴-2-카르보히드라지드)를 출발물질로 사용하여 실험예 1-19와 동일한 제조 방법으로 화합물49가 얻어진다.
실험예 1-50. 화합물50 (4-아미노-
N
-(2-(4-히드록시페닐)-2-옥소에틸)-3-모르폴리노벤젠설폰아미드)의 제조
실험예 1-12의 단계 3에서 4-니트로벤젠-1-설포닐 클로라이드 대신 3-플루오로-4-니트로벤젠설포닐 클로라이드를 사용하여 실험예 1-12와 유사한 제조 방법으로 화합물50이 얻어진다.
실험예 1-51. 화합물51 (3,5-디아미노-
N
-(2-(4-히드록시페닐)-2-옥소에틸)벤젠설폰아미드)의 제조
실험예 1-12의 단계 3에서 4-니트로벤젠-1-설포닐 클로라이드 대신 3,5-디니트로벤젠설포닐 클로라이드(A20)를 사용하여 실험예 1-12와 유사한 제조 방법으로 화합물51이 얻어진다.
실험예 1-52. 화합물52 (2-((4-아미노페닐)설포닐)-
N
-(3-히드록시페닐)히드라진-1-카르복사미드)의 제조
실험예 1-27의 단계 3에서 이소시아나토벤젠 대신 3-이소시아나토페놀을 사용하여 실험예 1-27와 동일한 제조 방법으로 화합물52가 얻어진다.
실험예 1-53. 화합물53 (2-((4-아미노-3-모르폴리노페닐)설포닐)-
N
-페닐히드라진-1-카르복사미드)의 제조
출발물질을 4-니트로벤젠설포닐클로라이드 대신 3-플루오로-4-니트로벤젠설포닐 클로라이드를 사용하여 실험예 1-27와 유사한 제조 방법으로 화합물53이 얻어진다.
실험예 1-54. 화합물54 (4-히드록시-
N
-(((4-메톡시페닐)설포닐)메틸)벤즈아미드)의 제조
실험예 1-16와 동일한 제조 방법으로, 합성단계 3에서 4-니트로벤젠티올 대신 4-메톡시벤젠티올을 사용하여 화합물54가 얻어진다.
실험예 1-55. 화합물55 (
N
-(((4-아미노페닐)설포닐)메틸)-[1,1'-바이페닐]-4-카르복사미드)의 제조
실험예 1-16의 중간체인 A28 대신 [1,1`-바이페닐]-4-카복스아미드를 출발물질로 사용하여 실험예 1-16와 유사한 제조 방법으로 화합물55가 얻어진다.
실시예 2. Binding assay 실험
실시예 2-1 머슬 액틴(muscle actin)이 Arg/N-데그론(degron) 경로 기질인지 여부 확인
랫드 근육 유래 세포인 L6 세포주를 5% 이산화탄소가 유지되는 배양기내에서 10% FBS와 1% 스트렙토마이신/페니실린을 함유한 DMEM 배지를 사용하여 배양 후 12웰 플레이트에 각각의 세포를 분주하였다. 세포가 플레이트의 표면에 완전히 부착되도록 24시간이 추가적인 배양을 하였다. MG132가 UBR1 결합을 증가시키는지 확인하기 위하여 24시간 동안 MG132(10 uM)을 단독으로 처리한 후 세포를 취합하였다. 취합된 세포로부터 단백질을 추출하기 위해 각 샘플에 50 uL의 용해버퍼(20 mM Tris, pH 7.4, 150 mM NaCl, 1% triton-X-100, 2mM NaF, 2 mM EDTA, 2 mM b-glycerophosphate, 5 mM sodium orthovanadate, 1 mM PMSF, leupeptin, aprotenin)을 주입하고 세포를 용해시켰다. 측정된 총 단백질의 농도를 기반으로 각 샘플에 샘플버퍼를 추가하여 100°C에서 5분간 반응시켰다. 반응을 마친 샘플로부터 5 uL을 취하여 아크릴아마이드 젤의 각 웰에 분주한 후 면역블로팅법을 실시하였고, 실험의 결과는 [도 1]에 나타내었다. 면역블로팅법은 3회 이상의 독립적인 실험으로부터 대표적인 것을 도식 화하였다.
도 1을 참고하면, 대조군(control)보다 MG132에 의해 ACTA1, ACTC1, ACTG2의 레벨이 더 증가함을 확인할 수 있었다. 또한, UBR 단백질을 넉다운(knock down)하였을 때 ACTA1, ACTG2 레벨이 증가함을 확인하였다. 즉, 머슬 액틴이 Arg/N-데그론(degron) 경로 기질인 것을 확인할 수 있었다.
실시예 2-2 시험관 내 전사 번역 방법을 통한 R-nsP4 분해 억제 확인
화합물들의 R-nsP4 발현을 확인하기 위해 TnT® Quick Coupled Transcription/Translation System kit를 사용하였다. Transcend Biotin-Lysyl-tRNA, Methionine, Bestatin, TnT quick Master mix와 DHFR-Ub-R-nsP4 Plasmid를 사용해 Pre-mix를 만든 후 화합물(1 uM)과 섞어주었다. 각 샘플을 30°C에서 40분간 반응시킨 후 5X SDS loading dye를 넣어주었다. 95°C에서 2분간 반응시킨 후 5 uL을 취하여 아크릴아마이드 젤의 각 웰에 분주한 후 면역블로팅법을 실시하였고, 실험의 결과는 [도 2]에 나타내었다. 시험관 내 전사 번역 방법은 3회 이상의 독립적인 실험으로부터 대표적인 것을 도식화하였다.
도 2를 참고하면, 대조군(Control)에 비해 화합물2, 화합물3, 화합물7, 화합물12, 화합물14, 화합물16에 의해 R-nsP4의 레벨이 더 증가함을 확인할 수 있다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1에 결합함을 통해 R-nsP4 레벨이 증가함을 확인할 수 있었다.
실시예 2-3 트렌스펙션을 통한 세포 내 RGS4 분해 억제 평가
랫드 근육 유래 세포인 L6 세포주를 5% 이산화탄소가 유지되는 배양기내에서 10% FBS와 1% 스트렙토마이신/페니실린을 함유한 DMEM 배지를 사용하여 배양하였다. 본 화합물들 중 선택된 대표 화합물의 처리에 따른 UBR1 결합력을 측정하기 위하여, 6웰 플레이트에 각각의 세포를 분주하였다. 세포가 플레이트의 표면에 완전히 부착되도록 24시간이 추가적인 배양을 하였다. 트렌스펙션을 하기 위해 Opti-MEM, Lipofectamin, RGS4 plasmid를 반응시켜준다. 반응이 끝난 후 세포에 처리하여 DNA가 세포 내에 발현되도록 처리한다. 24시간 후 화합물이 UBR1 결합을 증가시키는지 확인하기 위하여 24시간 동안 화합물(5 uM)을 단독으로 처리한 후 세포를 취합하였다. 취합된 세포로부터 단백질을 추출하기 위해 각 샘플에 50 uL의 용해버퍼(20 mM Tris, pH 7.4, 150 mM NaCl, 1% triton-X-100, 2mM NaF, 2 mM EDTA, 2 mM b-glycerophosphate, 5 mM sodium orthovanadate, 1 mM PMSF, leupeptin, aprotenin)을 주입하고 세포를 용해시켰다. 측정된 총 단백질의 농도를 기반으로 각 샘플에 샘플버퍼를 추가하여 100°C에서 5분간 반응시켰다. 반응을 마친 샘플로부터 5 uL을 취하여 아크릴아마이드 젤의 각 웰에 분주한 후 면역블로팅법을 실시하였고, 실험의 결과는 [도 3]에 나타내었다. 면역블로팅법은 3회 이상의 독립적인 실험으로부터 대표적인 것을 도식 화하였다.
도 3을 참고하면, 대조군(Control)에 비해 화합물2, 화합물3에 의해 RGS4의 레벨이 더 증가함을 확인할 수 있었다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1에 결합함을 통해 RGS4의 레벨이 더 증가함을 확인할 수 있었다.
실시예 2-4 면역블로팅법을 통한 근육 세포 액틴 분해 억제 평가
화합물들이 근육 세포내 액틴 분해를 평가하기 위해 랫드 근육 유래 세포인 L6 세포주를 5% 이산화탄소가 유지되는 배양기내에서 10% FBS와 1% 스트렙토마이신/페니실린을 함유한 DMEM 배지를 사용하여 배양하였다. 본 화합물들 중 선택된 대표 화합물의 처리에 따른 UBR1 결합력을 측정하기 위하여, 12웰 플레이트에 각각의 세포를 분주하였다. 세포가 플레이트의 표면에 완전히 부착되도록 24시간이 추가적인 배양을 하였다. 화합물이 UBR1 결합을 증가시키는지 확인하기 위하여 24시간 동안 화합물(5 uM)을 단독으로 처리한 후 세포를 취합하였다. 취합된 세포로부터 단백질을 추출하기 위해 각 샘플에 50 uL의 용해버퍼(20 mM Tris, pH 7.4, 150 mM NaCl, 1% triton-X-100, 2mM NaF, 2 mM EDTA, 2 mM b-glycerophosphate, 5 mM sodium orthovanadate, 1 mM PMSF, leupeptin, aprotenin)을 주입하고 세포를 용해시켰다. 측정된 총 단백질의 농도를 기반으로 각 샘플에 샘플버퍼를 추가하여 100°C에서 5분간 반응시켰다. 반응을 마친 샘플로부터 5 uL을 취하여 아크릴아마이드 젤의 각 웰에 분주한 후 면역블로팅법을 실시하였고, 실험의 결과는 [도 4], [도 5], [도 6], [도 7], [도 8] 및 [도 9]에 나타내었다. 면역블로팅법은 3회 이상의 독립적인 실험으로부터 대표적인 것을 도식 화하였다.
도 4,5를 참고하면, 대조군(Control)에 비해 화합물1, 화합물2, 화합물3, 화합물4, 화합물5, 화합물6, 화합물7, 화합물16, 화합물35, 화합물36, 화합물37, 화합물38, 화합물39, 화합물43, 화합물44, 화합물45, 화합물46, 화합물47에 의해 ACTA1의 레벨이 더 증가함을 확인할 수 있다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1에 결합함을 통해 근육 내 단백질인 ACTA1 분해 억제함을 확인할 수 있었다.
도 6,7를 참고하면, 대조군(Control)에 비해 화합물8, 화합물9, 화합물18, 화합물19, 화합물20, 화합물21, 화합물22, 화합물23, 화합물24, 화합물25, 화합물26, 화합물27, 화합물28, 화합물32, 화합물33, 화합물34에 의해 ACTA2의 레벨이 더 증가함을 확인할 수 있다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1에 결합함을 통해 근육 내 단백질인 ACTA2 분해 억제함을 확인할 수 있었다.
도 8을 참고하면, 대조군(Control)에 비해 화합물41, 화합물42에 의해 ACTC1의 레벨이 더 증가함을 확인할 수 있다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1에 결합함을 통해 근육 내 단백질인 ACTC1 분해 억제함을 확인할 수 있었다.
도 9를 참고하면, 대조군(Control)에 비해 화합물12, 화합물13, 화합물14, 화합물15, 화합물17, 화합물29, 화합물30, 화합물31에 의해 ACTG2의 레벨이 더 증가함을 확인할 수 있었다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1에 결합함을 통해 근육 내 단백질인 ACTG2 분해 억제함을 확인할 수 있었다.
실시예 2-5 면역침전분석법을 통한 UBR 박스 도메인 결합력 평가
화합물들의 UBR 박스 도메인을 통한 UBR1, UBR2, UBR3와 UBR5에 대한 결합력을 평가하기 위해 랫드 근육 유래 세포인 L6 세포주를 5% 이산화탄소가 유지되는 배양기내에서 10% FBS와 1% 스트렙토마이신/페니실린을 함유한 DMEM 배지를 사용하여 배양하였다. 본 화합물들 중 선택된 대표 화합물의 처리에 따른 UBR1 결합력을 측정하기 위하여, 100pi dish에 각각의 세포를 분주하였다. 세포가 플레이트의 표면에 완전히 부착되도록 24시간이 추가적인 배양을 하였다. 화합물이 UBR1 결합을 증가시키는지 확인하기 위하여 24시간 동안 화합물(5 uM)이나 프로테아좀 억제제인 MG132 (10 uM), 또는 positive control (5 uM)을 단독으로 처리한 후 세포를 취합하였다. 취합된 세포로부터 단백질을 추출하기 위해 각 샘플에 50 uL의 용해버퍼(20 mM Tris, pH 7.4, 150 mM NaCl, 1% triton-X-100, 2mM NaF, 2 mM EDTA, 2 mM b-glycerophosphate, 5 mM sodium orthovanadate, 1 mM PMSF, leupeptin, aprotenin)을 주입하고 세포를 용해시켰다. 측정된 총 단백질의 농도를 기반으로 각 샘플에 UBR1 항체를 16시간 반응시킨 후, Protein A/G bead를 3시간 반응시켰다. 반응을 마친 샘플에 샘플버퍼를 추가하여 100°C에서 5분간 반응시켰다. 반응을 마친 샘플로부터 20 uL을 취하여 아크릴아마이드 젤의 각 웰에 분주한 후 면역블로팅법을 실시하였고, 실험의 결과는 [도 10], [도 11]에 나타내었다. 면역블로팅법은 3회 이상의 독립적인 실험으로부터 대표적인 것을 도식 화하였다.
도 10,11을 참고하면 DMSO 대조군(DMSO control)과 음성 대조군(negative control)로 사용한 프로테아좀 억제제인 MG132을 처리하였을 때 UBR1과 기질인 ACTA1의 결합력이 유지되는 반면에, 화합물을 처리하였을때 양성 대조군(positive control)과 비슷하게 ACTA1, UBR2와 ACTA1, UBR3와 ACTA1, UBR5와 ACTA1의 결합력이 감소함으로써 화합물인 화합물2가 실제 UBR 단백질들의 UBR 박스 도메인에 결합함을 확인할 수 있다. 즉, 본 발명에 따른 화합물을 처리한 경우 UBR1, UBR2, UBR3나 UBR5에 결합함을 통해 근육 내 단백질인 ACTG2 분해 억제함을 확인할 수 있었다.
실시예 2-6 MST를 통한 UBR 박스 도메인 결합력 평가
1)UBR1 단백질 준비
Human UBR1 (UniProt ID: Q8IWV7)의 UBR 박스에 해당하는 Gln97-Pro168부분을 modified expression vector에 클로닝한 후 E.coli에서 발현하였다. 친화 크로마토그래피를 사용 후 protease로 tag을 제거한 후 N-말단에 Gly-His-Met이 추가되었다. 이온 크로마토그래피를 수행한 후, 10 mM NaCl, 20 mM Tris-HCl, 2 mM beta-mercaptoethanol, pH 7.5의 버퍼 조성에서 겔 여과 크로마토그래피를 사용하여 최종 UBR1의 UBR 박스 단백질을 정제하였다.
2)UBR1 UBR 박스 단백질 레이블링
The Monolith protein labeling Kit RED-NHS 2nd generation (Cat# MO-L011)의 dye는 primary amines (lysine residues)과 공유결합을 형성하는 NHS-ester group을 가지고 있다. 이 dye는 RED detector를 가진 Monolith-series 장비에 최적화 되어있다. 이 kit를 이용하여 정제된 UBR1 UBR 박스 단백질은 제시된 프로토콜을 따라 단밸질을 표지했다.
3)MST를 이용하여 UBR1과 ligand 결합여부 측정
열 영동(thermophoresis)은 온도 구배에 의해 입자가 이동하는 현상을 말한다. 높은 온도 영역에 있는 입자는 낮은 온도 영역에 있는 입자보다 더 큰 운동에너지를 가지고 주변 입자들과 더 큰 에너지로 더 자주 충동하게 된다. 그 결과 입자들은 높은 온도 영역에서 낮은 온도 영역으로 이동하게 된다.
단백질의 열 영동은 단백질-ligand 복합체의 열 영동과는 전형적으로 다르다. 리간드가 결합함으로써 크기, 전하 그리고 용매화 에너지(solvation energy)가 변하기 때문이다. 심지어 리간드 결합이 단백질의 크기, 전하를 중요하게 변하지 않게 하더라도, MST는 리간드 결합에 의한 단백질 분자의 용매화 엔트로피(solvation entropy) 변화를 감지할 수 있다. 따라서 UBR1 UBR 박스 단백질과 리간드 화합물과의 결합여부를 MST를 이용하여 측정하였고 제시된 리간드는 UBR1 UBR 박스와 결합함을 확인하였다(도 12 내지 19 참고).